JPWO2004046110A1 - メラニン凝集ホルモン受容体拮抗剤 - Google Patents
メラニン凝集ホルモン受容体拮抗剤 Download PDFInfo
- Publication number
- JPWO2004046110A1 JPWO2004046110A1 JP2004553173A JP2004553173A JPWO2004046110A1 JP WO2004046110 A1 JPWO2004046110 A1 JP WO2004046110A1 JP 2004553173 A JP2004553173 A JP 2004553173A JP 2004553173 A JP2004553173 A JP 2004553173A JP WO2004046110 A1 JPWO2004046110 A1 JP WO2004046110A1
- Authority
- JP
- Japan
- Prior art keywords
- lower alkyl
- piperidin
- optionally substituted
- phenyl
- fluorophenyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/445—Non condensed piperidines, e.g. piperocaine
- A61K31/4523—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems
- A61K31/454—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems containing a five-membered ring with nitrogen as a ring hetero atom, e.g. pimozide, domperidone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/439—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom the ring forming part of a bridged ring system, e.g. quinuclidine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4427—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems
- A61K31/4436—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems containing a heterocyclic ring having sulfur as a ring hetero atom
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/445—Non condensed piperidines, e.g. piperocaine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/445—Non condensed piperidines, e.g. piperocaine
- A61K31/4468—Non condensed piperidines, e.g. piperocaine having a nitrogen directly attached in position 4, e.g. clebopride, fentanyl
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/445—Non condensed piperidines, e.g. piperocaine
- A61K31/4523—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/445—Non condensed piperidines, e.g. piperocaine
- A61K31/4523—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems
- A61K31/4525—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems containing a five-membered ring with oxygen as a ring hetero atom
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/445—Non condensed piperidines, e.g. piperocaine
- A61K31/4523—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems
- A61K31/453—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems containing a six-membered ring with oxygen as a ring hetero atom
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/445—Non condensed piperidines, e.g. piperocaine
- A61K31/4523—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems
- A61K31/4545—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems containing a six-membered ring with nitrogen as a ring hetero atom, e.g. pipamperone, anabasine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/46—8-Azabicyclo [3.2.1] octane; Derivatives thereof, e.g. atropine, cocaine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/4709—Non-condensed quinolines and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/496—Non-condensed piperazines containing further heterocyclic rings, e.g. rifampin, thiothixene or sparfloxacin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/5375—1,4-Oxazines, e.g. morpholine
- A61K31/5377—1,4-Oxazines, e.g. morpholine not condensed and containing further heterocyclic rings, e.g. timolol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/04—Anorexiants; Antiobesity agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D211/00—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings
- C07D211/04—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D211/06—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members
- C07D211/08—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members with hydrocarbon or substituted hydrocarbon radicals directly attached to ring carbon atoms
- C07D211/18—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members with hydrocarbon or substituted hydrocarbon radicals directly attached to ring carbon atoms with substituted hydrocarbon radicals attached to ring carbon atoms
- C07D211/34—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members with hydrocarbon or substituted hydrocarbon radicals directly attached to ring carbon atoms with substituted hydrocarbon radicals attached to ring carbon atoms with hydrocarbon radicals, substituted by carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Medicinal Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Child & Adolescent Psychology (AREA)
- Emergency Medicine (AREA)
- Diabetes (AREA)
- Hematology (AREA)
- Obesity (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Hydrogenated Pyridines (AREA)
- Plural Heterocyclic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
Abstract
本発明は、医薬、特に主要骨格として含窒素ヘテロ環を有する誘導体又はその製薬学的に許容される塩を有効成分とするメラニン凝集ホルモン受容体拮抗剤、更に好ましくは抗肥満薬並びに該医薬として有用な新規含窒素飽和ヘテロ環、その製薬学的に許容される塩、又はその医薬組成物に関する。
Description
本発明は、医薬、特に含窒素ヘテロ環化合物を有効成分とするメラニン凝集ホルモン受容体拮抗剤、更に好ましくは抗肥満薬並びに該医薬として有用な新規含窒素飽和ヘテロ環、その製薬学的に許容される塩、又はその医薬組成物に関する。
肥満は、一つに脂肪組織重量の増加した状態と定義され、エネルギー摂取と消費のバランスの破綻により生じる。過食、運動不足といった現代の生活習慣は、エネルギー収支を正に導き、世界各国における肥満人口の急激な増加に関与している(例えば、非特許文献1参照)。近年、肥満は単なる体型の問題にとどまらず、糖尿病、及び高脂血症を含む生活習慣病のリスクファクターであることが明らかとなってきた(例えば、非特許文献1参照)。
メラニン凝集ホルモン(Melanin−Concentrating−Hormone、以下MCH)は、鮭の下垂体より初めて単離された環状ペプチドホルモンである(例えば、非特許文献2参照)。その後、ラット、ヒトなどでもそのホモログが単離された(例えば、非特許文献3及び4参照)。
一方SLC−1と称する遺伝子が得られたが、該遺伝子がMCH受容体であることが明らかとなった(例えば、非特許文献5参照)。SLC−1はヒト及びラットの海馬、偏桃核、視床、中脳、橋、及び視床下部を含む脳の多くの領域に発現している(例えば、非特許文献6及び7参照)。視床下部においては摂食及びエネルギーバランス制御に関与する弓状核、腹内側核、背内側核、及び孤束核に分布が見られ、MCHはエネルギーホメオスタシス制御を媒介する可能性が示唆されている(例えば、非特許文献8参照)。実際、SLC−1阻害薬がMCH誘発摂食及び嗜好食の摂取を抑制し、高脂肪食による体重増加を抑制した(例えば、非特許文献9及び10参照)。
従って、メラニン凝集ホルモン受容体拮抗剤は抗肥満薬として有用であると考えられる。メラニン凝集ホルモン受容体拮抗剤としては、単環式芳香環を主要骨格とする化合物(特許文献1)、縮合多環式芳香環を主要骨格とする化合物(特許文献2)、2個の芳香環を有するメタンを主要骨格とする化合物(特許文献3)、含窒素非芳香族複素環と縮合したベンゼン環を主要骨格とする化合物(特許文献4)、4−フェニルメチルピペリジン誘導体(特許文献5)、2個のカルボニル及びジヒドロピリミジン環を有する化合物(特許文献6)、フェニルアミノカルボニルを有する芳香環化合物(特許文献7)、N−ヘテロアリール−N’−ヘテロアリールウレア誘導体(特許文献8)、置換されていてもよいアミノフェニルを有するピペリジン誘導体(特許文献10)、非環式炭化水素既置換フェニル基を有するピペリジン誘導体(特許文献11)、キノリン誘導体(特許文献12及び13)が報告されている。しかしながら、当該拮抗剤として、含窒素飽和ヘテロ環を主要骨格とする化合物は知られていない。
また本発明化合物と構造類似の化合物としては以下の通りである。
尿失禁や後天性免疫不全症候群(AIDS)の治療に有用なピペリジルカルバメート誘導体(特許文献12及び14)が、また、神経細胞保護に有用な置換されていてもよいアミノフェニルを有するピペリジン誘導体(特許文献11)が開示されているが、MCH(又はSLC−1)阻害活性については開示も示唆もない。
かかる状況下、更なる有用なメラニン凝集ホルモン受容体拮抗剤を提供することが課題である。
非特許文献1 Kopelman P.G.(2000)Nature 404、635−643
非特許文献2 Kawauchi、H.et al.(1983)Nature 305、321−323
非特許文献3 Nahon、J.L.et al.(1989)Endocrinology 125、2056−2065
非特許文献4 Presse、F.et al.(1990)Mol.Endocrinol.4、632−637
非特許文献5 Saito、Y.et al.(1999)Nature 400、265−269
非特許文献6 Kolakowski L.F.et al.(1996)FEBS Lett.398、253−258
非特許文献7 Lembo P.M.C.et al.(1999)Nature Cell Biol.1、267−271
非特許文献8 Hervieu G.J.et al.(2000)Eur.J.Neurosci.12、1194−1216
非特許文献9 Takekawa S.et al.(2002)Eur.J.Phramacol.438、129−135
非特許文献10 Borowski B.et al.(2002)Nature Med.8、825−830
特許文献1 国際公開第01/21577号パンフレット
特許文献2 国際公開第01/82975号パンフレット
特許文献3 国際公開第01/21169号パンフレット
特許文献4 国際公開第01/87834号パンフレット
特許文献5 国際公開第02/051809号パンフレット
特許文献6 国際公開第02/06245号パンフレット
特許文献7 国際公開第02/10146号パンフレット
特許文献8 国際公開第02/057233号パンフレット
特許文献9 国際公開第95/06635号パンフレット
特許文献10 特開2001−226269号
特許文献11 欧州公開特許1045693号
特許文献12 欧州公開特許1052992
特許文献13 国際公開第03/35624号パンフレット
特許文献14 国際公開第03/45920号パンフレット
メラニン凝集ホルモン(Melanin−Concentrating−Hormone、以下MCH)は、鮭の下垂体より初めて単離された環状ペプチドホルモンである(例えば、非特許文献2参照)。その後、ラット、ヒトなどでもそのホモログが単離された(例えば、非特許文献3及び4参照)。
一方SLC−1と称する遺伝子が得られたが、該遺伝子がMCH受容体であることが明らかとなった(例えば、非特許文献5参照)。SLC−1はヒト及びラットの海馬、偏桃核、視床、中脳、橋、及び視床下部を含む脳の多くの領域に発現している(例えば、非特許文献6及び7参照)。視床下部においては摂食及びエネルギーバランス制御に関与する弓状核、腹内側核、背内側核、及び孤束核に分布が見られ、MCHはエネルギーホメオスタシス制御を媒介する可能性が示唆されている(例えば、非特許文献8参照)。実際、SLC−1阻害薬がMCH誘発摂食及び嗜好食の摂取を抑制し、高脂肪食による体重増加を抑制した(例えば、非特許文献9及び10参照)。
従って、メラニン凝集ホルモン受容体拮抗剤は抗肥満薬として有用であると考えられる。メラニン凝集ホルモン受容体拮抗剤としては、単環式芳香環を主要骨格とする化合物(特許文献1)、縮合多環式芳香環を主要骨格とする化合物(特許文献2)、2個の芳香環を有するメタンを主要骨格とする化合物(特許文献3)、含窒素非芳香族複素環と縮合したベンゼン環を主要骨格とする化合物(特許文献4)、4−フェニルメチルピペリジン誘導体(特許文献5)、2個のカルボニル及びジヒドロピリミジン環を有する化合物(特許文献6)、フェニルアミノカルボニルを有する芳香環化合物(特許文献7)、N−ヘテロアリール−N’−ヘテロアリールウレア誘導体(特許文献8)、置換されていてもよいアミノフェニルを有するピペリジン誘導体(特許文献10)、非環式炭化水素既置換フェニル基を有するピペリジン誘導体(特許文献11)、キノリン誘導体(特許文献12及び13)が報告されている。しかしながら、当該拮抗剤として、含窒素飽和ヘテロ環を主要骨格とする化合物は知られていない。
また本発明化合物と構造類似の化合物としては以下の通りである。
尿失禁や後天性免疫不全症候群(AIDS)の治療に有用なピペリジルカルバメート誘導体(特許文献12及び14)が、また、神経細胞保護に有用な置換されていてもよいアミノフェニルを有するピペリジン誘導体(特許文献11)が開示されているが、MCH(又はSLC−1)阻害活性については開示も示唆もない。
かかる状況下、更なる有用なメラニン凝集ホルモン受容体拮抗剤を提供することが課題である。
非特許文献1 Kopelman P.G.(2000)Nature 404、635−643
非特許文献2 Kawauchi、H.et al.(1983)Nature 305、321−323
非特許文献3 Nahon、J.L.et al.(1989)Endocrinology 125、2056−2065
非特許文献4 Presse、F.et al.(1990)Mol.Endocrinol.4、632−637
非特許文献5 Saito、Y.et al.(1999)Nature 400、265−269
非特許文献6 Kolakowski L.F.et al.(1996)FEBS Lett.398、253−258
非特許文献7 Lembo P.M.C.et al.(1999)Nature Cell Biol.1、267−271
非特許文献8 Hervieu G.J.et al.(2000)Eur.J.Neurosci.12、1194−1216
非特許文献9 Takekawa S.et al.(2002)Eur.J.Phramacol.438、129−135
非特許文献10 Borowski B.et al.(2002)Nature Med.8、825−830
特許文献1 国際公開第01/21577号パンフレット
特許文献2 国際公開第01/82975号パンフレット
特許文献3 国際公開第01/21169号パンフレット
特許文献4 国際公開第01/87834号パンフレット
特許文献5 国際公開第02/051809号パンフレット
特許文献6 国際公開第02/06245号パンフレット
特許文献7 国際公開第02/10146号パンフレット
特許文献8 国際公開第02/057233号パンフレット
特許文献9 国際公開第95/06635号パンフレット
特許文献10 特開2001−226269号
特許文献11 欧州公開特許1045693号
特許文献12 欧州公開特許1052992
特許文献13 国際公開第03/35624号パンフレット
特許文献14 国際公開第03/45920号パンフレット
本発明者等は、メラニン凝集ホルモン受容体拮抗剤及び当該作用を有する化合物につき鋭意検討した結果、従来の当該拮抗剤の化学構造とは異なり主要骨格として含窒素飽和ヘテロ環を有する誘導体、特に下記一般式(I)中L1としてアミド結合、スルホンアミド結合、ウレアを有する当該ヘテロ環、好ましくは単環式の含窒素飽和ヘテロ環、特に好ましくはピペリジン又はピペラジンを主要骨格とする誘導体及び製薬学的に許容される塩が優れたメラニン凝集ホルモン受容体拮抗作用を有することを見出し、本発明を完成した。
即ち本発明は、以下の通りである。
1.下記一般式(I)
(R1及びR2:同一又は異なってH;又は置換されていてもよい炭化水素基又は置換されていてもよいヘテロ環基、
ALK1及びALK2:同一又は異なって、置換されていてもよい2価の炭化水素基
L1:連結原子数1から6個のリンカー
L2:単結合;又は連結原子数1から6個のリンカー
Het1:置換されていてもよい飽和含窒素ヘテロ環基
m及びn:同一又は異なって0又は1)で示されるヘテロ環誘導体又はその製薬学的に許容される塩を有効成分とするメラニン凝集ホルモン受容体拮抗剤。
好ましいメラニン凝集ホルモン受容体拮抗剤は以下の通りである。
2.Het1が置換されていてもよい単環式飽和含窒素ヘテロ環基である前記1項に記載のメラニン凝集ホルモン受容体拮抗剤。
3.Het1が置換されていてもよいピペリジン環である前記1乃至2の何れかに記載のメラニン凝集ホルモン受容体拮抗剤。
4.ALK2が置換されていてもよい低級アルケニレンである前記1乃至3の何れかに記載のメラニン凝集ホルモン受容体拮抗剤。
5.L1が窒素原子(N)を有するリンカーである前記1乃至4の何れかに記載のメラニン凝集ホルモン受容体拮抗剤。
6.R2が置換されていてもよい炭化水素環基である前記1乃至5の何れかに記載のメラニン凝集ホルモン受容体拮抗剤。
7.R2が置換されていてもよいフェニルである前記1乃至6の何れかに記載のメラニン凝集ホルモン受容体拮抗剤。
8.抗肥満薬である前記1から7の何れかに記載のメラニン凝集ホルモン受容体拮抗剤。
9.下記一般式(II)
(一般式中の記号は以下の意味を示す。
Q:CH;又はN、
R1a,R1b,R1c,R1d,及びR1e:同一又は異なって、
H;
CN;
ハロゲン;
HO、ハロゲン、低級アルキル−NH−若しくは低級アルキル−O−アルキル−NH−で置換されていてもよい低級アルキル;
HO;
ハロゲン若しくはアリールで置換されていてもよい低級アルキル−O−;
置換されていてもよいアリール;
低級アルキル−CO−NH−で置換されていてもよいアリール−O−;
H2N;
H2N、低級アルキル−NH−若しくは(低級アルキル)2N−で置換されていてもよい低級アルキル−NH−;
低級アルキル−CO−NH−;
[H2N、低級アルキル−NH−若しくは(低級アルキル)2N−で置換されていてもよい低級アルキル]2N−;
HO−OC−;
低級アルキル−O−CO−;
H2NCO;
低級アルキル−NHCO−;
(低級アルキル)2NCO−;
低級アルキル若しくは低級アルキル−O−CO−で置換されていてもよいヘテロ環−CO−;
Cy1:炭化水素環;又はヘテロ環、
R2a、R2b及びR2c:同一又は異なって、
H;
CN;
ハロゲン;
NO2;
HO;
置換されていてもよいアリール;
CN、ハロゲン若しくはヘテロ環で置換されていてもよい低級アルキル;
H2N;
H2N、低級アルキル−NH−若しくは(低級アルキル)2N−で置換されていてもよい低級アルキル−NH−;
[H2N、低級アルキル−NH−若しくは(低級アルキル)2N−で置換されていてもよい低級アルキル]2N−;
(低級アルキル−O−CO−)(H2N、低級アルキル−NH−若しくは(低級アルキル)2N−で置換されていてもよい低級アルキル)N−;
低級アルキル−CO−NH−;
HO−CO−;
低級アルキル−O−CO−;
H2NCO;
低級アルキル−NH−、若しくは(低級アルキル)2N−で置換されていてもよい低級アルキル−NHCO−;
(低級アルキル)2NCO−;
低級アルキル若しくは低級アルキル−O−CO−で置換されていてもよいヘテロ環−CO−;
HS;
低級アルキル−S−;
CN、ハロゲン、HO、NH2、低級アルキル−NH−、若しくは(低級アルキル)2Nで置換されていてもよい低級アルキル−O−;
低級アルキルで置換されていてもよいヘテロ環;
(R13a、R13b及びR13c:同一又は異なってH;低級アルキル;HO−CO;低級アルキル−O−;低級アルキル−CO−;若しくは低級アルキル−O−CO−、
Cy3:炭化水素環、
Alk3:低級アルキレン、
n1:0;又は1);
更にR2a及びR2bが一緒になって低級アルキレンジオキシ若しくはヘテロ環を形成していてもよい。
R4及びR5:同一又は異なって、
H;
HO;
H2N;
低級アルキル−CO−NH−;
ハロゲン、H2N、低級アルキル−NH−,若しくは(低級アルキル)2N−若しくはアリールで置換されていてもよい低級アルキル;又は
L1a:−NR11−CO−NR12−;−NR11SO2−;−SO2NR11−;−CONR11−;−NR11CO−;又は−CO−
R11及びR12:同一又は異なって、
H;
−CO2R13、−NR14R15、−CONR14R15若しくはアリールで置換されていてもよい低級アルキル;
シクロアルキル;
又はハロゲン若しくは低級アルキル−NH−CO−で置換されていてもよいアリール、
R13、R14及びR15:同一又は異なってH;又は低級アルキル
Alk1a:低級アルキレン
m1:0;又は1
m2:0;1;又は2
m3:0;又は1
m4:0;又は1
R6及びR7:同一又は異なって、
H;
HO;
低級アルキル;又は
置換されていてもよいヘテロ環;
更にR6及びR7は一緒になって低級アルキレンを形成する。
R8a及びR8b:同一又は異なって、H;低級アルキル;又はR8a及びR8bが一緒になってオキソ、
R9a、R9b、R10a及びR10:同一又は異なってH;低級アルキル;又はアリール、
Cy2:炭化水素環;又はヘテロ環
−−−−:R9bとCy2が一緒になって縮合環、R9a、R10a及び隣接する炭素原子と一体となって飽和炭素環、又はR9a,及びR10aが一体となって結合を形成する。
但し、R1a,R1b,R1c,R1d,及びR1eの何れかがH2N若しくはCH3CONHの場合、m1又はm2の何れか一方は1で且つm3がOであり;
R6及びR7の何れかがHOの場合、m1又はm2の何れか一方は1で且つm3がOであり;
L1aが−CONR11−で且つR4及びR5の何れか一方がシクロアルキルの場合、他方は(1)H、(2)H2N、(3)低級アルキル−CO−NH−、(4)ハロゲン、H2N、低級アルキル−NH−,若しくは(低級アルキル)2N−若しくは
L1aが−CONR11−の場合、m1が0で且つCy1が炭化水素環で且つR11が(1)H、(2)−CO2R13、−NR14R15、−CONR14R15若しくは一個のアリールで置換されていてもよい低級アルキル、(3)シクロアルキル、又は(4)ハロゲン若しくは低級アルキル−NH−CO−で置換されていてもよいアリールであり、
L1aが−CONR11−で、m1が0で、Cy1が炭化水素環で且つR1a、R1b、R1c、R1d及びR1e何れかが低級アルキル−O−の場合、R2a、R2b及びR2cの何れかがH以外の基であり、
L1aが−NR11CO−でCy1がヘテロ環の場合、m2が1若しくは2で且つR4及びR5の何れか一方はH以外の基であり;
L1aが−NR11CO−で、m1が0で且つCy1炭化水素環での場合、m2が1又は2で且つR9aがHである。)含窒素飽和ヘテロ環誘導体又はその製薬学的に許容される塩。
好ましい含窒素飽和ヘテロ環誘導体は、以下の通りである。
10.m4が、1である請求の範囲9に記載の含窒素飽和ヘテロ環誘導体又はその製薬学的に許容される塩。
11.m2が0である前記10項に記載の含窒素飽和ヘテロ環誘導体又はその製薬学的に許容される塩。
12.Cy1がアリールである前記9から11項の何れかに記載の含窒素飽和ヘテロ環誘導体又はその製薬学的に許容される塩。
13.Cy1がフェニルである前記9から12項の何れかに記載の含窒素飽和ヘテロ環誘導体又はその製薬学的に許容される塩。
15.Cy2がアリールである前記9から14項の何れかに記載の含窒素飽和ヘテロ環誘導体又はその製薬学的に許容される塩。
16.Cy2がフェニルである前記9から15項の何れかに記載の含窒素飽和ヘテロ環誘導体又はその製薬学的に許容される塩。
17.下記一般式(IIa)、一般式(IIb)、一般式(IIc)及び一般式(IId)から選ばれる含窒素飽和ヘテロ環誘導体である前記9から16項の何れかに記載の含窒素飽和ヘテロ環誘導体又はその製薬学的に許容される塩。
18.N−[ビス(4−フルオロフェニル)メチル]−2−{1−[(2E)−3−(4−シアノフェニル)プロパ−2−エン−1−イル]ピペリジン−4−イル}−N−メチルアセトアミド、2,2−ビス(4−フルオロフェニル)−N−(1−{(2E)−3−[4−(3−ピロリジン−1−イルプロポキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、2,2−ビス(4−フルオロフェニル)−N−メチル−N−(1−{(2E)−3−[4−(3−ピロリジン−1−イルプロポキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、N−{1−[(2E)−3−(4−シアノフェニル)プロパ−2−エン−1−イル]ピペリジン−4−イル}−2,2−ビス(4−フルオロフェニル)−N−メチルアセトアミド、N−{1−[(2E)−3−(4−シアノフェニル)プロパ−2−エン−1−イル]ピペリジン−4−イル}−2,2−ビス(4−フルオロフェニル)アセトアミド、N−[ビス(4−フルオロフェニル)メチル]−2−{1−[(2E)−3−(4−シアノフェニル)プロパ−2−エン−1−イル]ピペリジン−4−イル}アセトアミド、N−(4−フルオロベンジル)−2−(1−{(2E)−3−[4−(ピペリジン−4−イルオキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、N−[ビス(4−フルオロフェニル)メチル]−N−メチル−2−[1−((2E)−3−{4−[(3R)−ピロリジン−3−イルオキシ]フェニル}プロパ−2−エン−1−イル)ピペリジン−4−イル]アセトアミド、N−[ビス(4−フルオロフェニル)メチル]−N−メチル−2−(1−{(2E)−3−[4−(ピペリジン−3−イルメトキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、N−(4−フルオロベンジル)−N−イソプロピル−2−(1−{(2E)−3−[4−(ピペリジン−4−イルオキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、2−[ビス(4−フルオロフェニル)アミノ]−N−(1−{(2E)−3−[4−(ピペリジン−4−イルオキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、2,2−ビス(4−フルオロフェニル)−N−メチル−N−(1−{(2E)−3−[4−(ピペリジン−4−イルオキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、2,2−ビス(4−フルオロフェニル)−N−(1−{(2E)−3−[4−(ピペリジン−4−イルオキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)プロパンアミド、2−[3,5−ビス(トリフルオロメチル)フェニル]−N−(1−{(2E)−3−[4−(ピペリジン−4−イルオキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、N−[ビス(4−フルオロフェニル)メチル]−N−メチル−2−(1−{(2E)−3−[4−(ピペリジン−4−イルオキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、N−[ビス(4−フルオロフェニル)メチル]−2−(1−{(2E)−3−[4−(3−ピロリジン−1−イルプロポキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、2,2−ビス(4−フルオロフェニル)−N−(1−{(2E)−3−[4−(ピペリジン−4−イルオキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、2,2−ビス(4−フルオロフェニル)−N−(1−{(2E)−3−[2−フルオロ−4−(ピペリジン−4−イルオキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、2−(1−{(2E)−3−[4−(3−アゼチジン−1−イルプロポキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)−N−[ビス(4−フルオロフェニル)メチル]−N−メチルアセトアミド、N−[ビス(4−フルオロフェニル)メチル]−N−メチル−2−(1−{(2E)−3−[4−(3−ピロリジン−1−イルプロポキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、N−[ビス(4−フルオロフェニル)メチル]−2−(1−{(2E)−3−[4−(3−ピペリジン−1−イルプロポキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、N−[ビス(4−フルオロフェニル)メチル]−N−メチル−2−{1−[(2E)−3−(4−{[(3S)−1−メチルピロリジン−3−イル]オキシ}フェニル)プロパ−2−エン−1−イル]ピペリジン−4−イル}アセトアミド、及び2,2−ビス(4−フルオロフェニル)−N−メチル−N−{1−[(2E)−3−(4−{[(3R)−1−メチルピロリジン−3−イル]オキシ}フェニル)プロパ−2−エン−1−イル]ピペリジン−4−イル}アセトアミドの群から選ばれる化合物である請求の範囲9に記載の含窒素飽和ヘテロ環誘導体又はその製薬学的に許容される塩。
19.前記9項に記載の一般式(II)で示される含窒素飽和ヘテロ環誘導体又はその製薬学的に許容される塩を有効成分とする医薬組成物。
20.前記1項に記載の一般式(I)で示されるヘテロ環化合物若しくは前記9項に記載の一般式(II)で示される含窒素飽和ヘテロ環誘導体又はそれらの製薬学的に許容される塩の有効量を患者に投与することからなるメラニン凝集ホルモン受容体に関与する疾患の治療方法。
21.メラニン凝集ホルモン受容体に関与する疾患が肥満である前記20項に記載の治療方法。
22.前記1項に記載の一般式(I)で示されるヘテロ環化合物若しくは前記9項に記載の一般式(II)で示される含窒素飽和ヘテロ環誘導体又はそれらの製薬学的に許容される塩を有効成分とするメラニン凝集ホルモン受容体拮抗剤の製造のための使用。
即ち本発明は、以下の通りである。
1.下記一般式(I)
(R1及びR2:同一又は異なってH;又は置換されていてもよい炭化水素基又は置換されていてもよいヘテロ環基、
ALK1及びALK2:同一又は異なって、置換されていてもよい2価の炭化水素基
L1:連結原子数1から6個のリンカー
L2:単結合;又は連結原子数1から6個のリンカー
Het1:置換されていてもよい飽和含窒素ヘテロ環基
m及びn:同一又は異なって0又は1)で示されるヘテロ環誘導体又はその製薬学的に許容される塩を有効成分とするメラニン凝集ホルモン受容体拮抗剤。
好ましいメラニン凝集ホルモン受容体拮抗剤は以下の通りである。
2.Het1が置換されていてもよい単環式飽和含窒素ヘテロ環基である前記1項に記載のメラニン凝集ホルモン受容体拮抗剤。
3.Het1が置換されていてもよいピペリジン環である前記1乃至2の何れかに記載のメラニン凝集ホルモン受容体拮抗剤。
4.ALK2が置換されていてもよい低級アルケニレンである前記1乃至3の何れかに記載のメラニン凝集ホルモン受容体拮抗剤。
5.L1が窒素原子(N)を有するリンカーである前記1乃至4の何れかに記載のメラニン凝集ホルモン受容体拮抗剤。
6.R2が置換されていてもよい炭化水素環基である前記1乃至5の何れかに記載のメラニン凝集ホルモン受容体拮抗剤。
7.R2が置換されていてもよいフェニルである前記1乃至6の何れかに記載のメラニン凝集ホルモン受容体拮抗剤。
8.抗肥満薬である前記1から7の何れかに記載のメラニン凝集ホルモン受容体拮抗剤。
9.下記一般式(II)
(一般式中の記号は以下の意味を示す。
Q:CH;又はN、
R1a,R1b,R1c,R1d,及びR1e:同一又は異なって、
H;
CN;
ハロゲン;
HO、ハロゲン、低級アルキル−NH−若しくは低級アルキル−O−アルキル−NH−で置換されていてもよい低級アルキル;
HO;
ハロゲン若しくはアリールで置換されていてもよい低級アルキル−O−;
置換されていてもよいアリール;
低級アルキル−CO−NH−で置換されていてもよいアリール−O−;
H2N;
H2N、低級アルキル−NH−若しくは(低級アルキル)2N−で置換されていてもよい低級アルキル−NH−;
低級アルキル−CO−NH−;
[H2N、低級アルキル−NH−若しくは(低級アルキル)2N−で置換されていてもよい低級アルキル]2N−;
HO−OC−;
低級アルキル−O−CO−;
H2NCO;
低級アルキル−NHCO−;
(低級アルキル)2NCO−;
低級アルキル若しくは低級アルキル−O−CO−で置換されていてもよいヘテロ環−CO−;
Cy1:炭化水素環;又はヘテロ環、
R2a、R2b及びR2c:同一又は異なって、
H;
CN;
ハロゲン;
NO2;
HO;
置換されていてもよいアリール;
CN、ハロゲン若しくはヘテロ環で置換されていてもよい低級アルキル;
H2N;
H2N、低級アルキル−NH−若しくは(低級アルキル)2N−で置換されていてもよい低級アルキル−NH−;
[H2N、低級アルキル−NH−若しくは(低級アルキル)2N−で置換されていてもよい低級アルキル]2N−;
(低級アルキル−O−CO−)(H2N、低級アルキル−NH−若しくは(低級アルキル)2N−で置換されていてもよい低級アルキル)N−;
低級アルキル−CO−NH−;
HO−CO−;
低級アルキル−O−CO−;
H2NCO;
低級アルキル−NH−、若しくは(低級アルキル)2N−で置換されていてもよい低級アルキル−NHCO−;
(低級アルキル)2NCO−;
低級アルキル若しくは低級アルキル−O−CO−で置換されていてもよいヘテロ環−CO−;
HS;
低級アルキル−S−;
CN、ハロゲン、HO、NH2、低級アルキル−NH−、若しくは(低級アルキル)2Nで置換されていてもよい低級アルキル−O−;
低級アルキルで置換されていてもよいヘテロ環;
(R13a、R13b及びR13c:同一又は異なってH;低級アルキル;HO−CO;低級アルキル−O−;低級アルキル−CO−;若しくは低級アルキル−O−CO−、
Cy3:炭化水素環、
Alk3:低級アルキレン、
n1:0;又は1);
更にR2a及びR2bが一緒になって低級アルキレンジオキシ若しくはヘテロ環を形成していてもよい。
R4及びR5:同一又は異なって、
H;
HO;
H2N;
低級アルキル−CO−NH−;
ハロゲン、H2N、低級アルキル−NH−,若しくは(低級アルキル)2N−若しくはアリールで置換されていてもよい低級アルキル;又は
L1a:−NR11−CO−NR12−;−NR11SO2−;−SO2NR11−;−CONR11−;−NR11CO−;又は−CO−
R11及びR12:同一又は異なって、
H;
−CO2R13、−NR14R15、−CONR14R15若しくはアリールで置換されていてもよい低級アルキル;
シクロアルキル;
又はハロゲン若しくは低級アルキル−NH−CO−で置換されていてもよいアリール、
R13、R14及びR15:同一又は異なってH;又は低級アルキル
Alk1a:低級アルキレン
m1:0;又は1
m2:0;1;又は2
m3:0;又は1
m4:0;又は1
R6及びR7:同一又は異なって、
H;
HO;
低級アルキル;又は
置換されていてもよいヘテロ環;
更にR6及びR7は一緒になって低級アルキレンを形成する。
R8a及びR8b:同一又は異なって、H;低級アルキル;又はR8a及びR8bが一緒になってオキソ、
R9a、R9b、R10a及びR10:同一又は異なってH;低級アルキル;又はアリール、
Cy2:炭化水素環;又はヘテロ環
−−−−:R9bとCy2が一緒になって縮合環、R9a、R10a及び隣接する炭素原子と一体となって飽和炭素環、又はR9a,及びR10aが一体となって結合を形成する。
但し、R1a,R1b,R1c,R1d,及びR1eの何れかがH2N若しくはCH3CONHの場合、m1又はm2の何れか一方は1で且つm3がOであり;
R6及びR7の何れかがHOの場合、m1又はm2の何れか一方は1で且つm3がOであり;
L1aが−CONR11−で且つR4及びR5の何れか一方がシクロアルキルの場合、他方は(1)H、(2)H2N、(3)低級アルキル−CO−NH−、(4)ハロゲン、H2N、低級アルキル−NH−,若しくは(低級アルキル)2N−若しくは
L1aが−CONR11−の場合、m1が0で且つCy1が炭化水素環で且つR11が(1)H、(2)−CO2R13、−NR14R15、−CONR14R15若しくは一個のアリールで置換されていてもよい低級アルキル、(3)シクロアルキル、又は(4)ハロゲン若しくは低級アルキル−NH−CO−で置換されていてもよいアリールであり、
L1aが−CONR11−で、m1が0で、Cy1が炭化水素環で且つR1a、R1b、R1c、R1d及びR1e何れかが低級アルキル−O−の場合、R2a、R2b及びR2cの何れかがH以外の基であり、
L1aが−NR11CO−でCy1がヘテロ環の場合、m2が1若しくは2で且つR4及びR5の何れか一方はH以外の基であり;
L1aが−NR11CO−で、m1が0で且つCy1炭化水素環での場合、m2が1又は2で且つR9aがHである。)含窒素飽和ヘテロ環誘導体又はその製薬学的に許容される塩。
好ましい含窒素飽和ヘテロ環誘導体は、以下の通りである。
10.m4が、1である請求の範囲9に記載の含窒素飽和ヘテロ環誘導体又はその製薬学的に許容される塩。
11.m2が0である前記10項に記載の含窒素飽和ヘテロ環誘導体又はその製薬学的に許容される塩。
12.Cy1がアリールである前記9から11項の何れかに記載の含窒素飽和ヘテロ環誘導体又はその製薬学的に許容される塩。
13.Cy1がフェニルである前記9から12項の何れかに記載の含窒素飽和ヘテロ環誘導体又はその製薬学的に許容される塩。
15.Cy2がアリールである前記9から14項の何れかに記載の含窒素飽和ヘテロ環誘導体又はその製薬学的に許容される塩。
16.Cy2がフェニルである前記9から15項の何れかに記載の含窒素飽和ヘテロ環誘導体又はその製薬学的に許容される塩。
17.下記一般式(IIa)、一般式(IIb)、一般式(IIc)及び一般式(IId)から選ばれる含窒素飽和ヘテロ環誘導体である前記9から16項の何れかに記載の含窒素飽和ヘテロ環誘導体又はその製薬学的に許容される塩。
18.N−[ビス(4−フルオロフェニル)メチル]−2−{1−[(2E)−3−(4−シアノフェニル)プロパ−2−エン−1−イル]ピペリジン−4−イル}−N−メチルアセトアミド、2,2−ビス(4−フルオロフェニル)−N−(1−{(2E)−3−[4−(3−ピロリジン−1−イルプロポキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、2,2−ビス(4−フルオロフェニル)−N−メチル−N−(1−{(2E)−3−[4−(3−ピロリジン−1−イルプロポキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、N−{1−[(2E)−3−(4−シアノフェニル)プロパ−2−エン−1−イル]ピペリジン−4−イル}−2,2−ビス(4−フルオロフェニル)−N−メチルアセトアミド、N−{1−[(2E)−3−(4−シアノフェニル)プロパ−2−エン−1−イル]ピペリジン−4−イル}−2,2−ビス(4−フルオロフェニル)アセトアミド、N−[ビス(4−フルオロフェニル)メチル]−2−{1−[(2E)−3−(4−シアノフェニル)プロパ−2−エン−1−イル]ピペリジン−4−イル}アセトアミド、N−(4−フルオロベンジル)−2−(1−{(2E)−3−[4−(ピペリジン−4−イルオキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、N−[ビス(4−フルオロフェニル)メチル]−N−メチル−2−[1−((2E)−3−{4−[(3R)−ピロリジン−3−イルオキシ]フェニル}プロパ−2−エン−1−イル)ピペリジン−4−イル]アセトアミド、N−[ビス(4−フルオロフェニル)メチル]−N−メチル−2−(1−{(2E)−3−[4−(ピペリジン−3−イルメトキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、N−(4−フルオロベンジル)−N−イソプロピル−2−(1−{(2E)−3−[4−(ピペリジン−4−イルオキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、2−[ビス(4−フルオロフェニル)アミノ]−N−(1−{(2E)−3−[4−(ピペリジン−4−イルオキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、2,2−ビス(4−フルオロフェニル)−N−メチル−N−(1−{(2E)−3−[4−(ピペリジン−4−イルオキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、2,2−ビス(4−フルオロフェニル)−N−(1−{(2E)−3−[4−(ピペリジン−4−イルオキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)プロパンアミド、2−[3,5−ビス(トリフルオロメチル)フェニル]−N−(1−{(2E)−3−[4−(ピペリジン−4−イルオキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、N−[ビス(4−フルオロフェニル)メチル]−N−メチル−2−(1−{(2E)−3−[4−(ピペリジン−4−イルオキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、N−[ビス(4−フルオロフェニル)メチル]−2−(1−{(2E)−3−[4−(3−ピロリジン−1−イルプロポキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、2,2−ビス(4−フルオロフェニル)−N−(1−{(2E)−3−[4−(ピペリジン−4−イルオキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、2,2−ビス(4−フルオロフェニル)−N−(1−{(2E)−3−[2−フルオロ−4−(ピペリジン−4−イルオキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、2−(1−{(2E)−3−[4−(3−アゼチジン−1−イルプロポキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)−N−[ビス(4−フルオロフェニル)メチル]−N−メチルアセトアミド、N−[ビス(4−フルオロフェニル)メチル]−N−メチル−2−(1−{(2E)−3−[4−(3−ピロリジン−1−イルプロポキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、N−[ビス(4−フルオロフェニル)メチル]−2−(1−{(2E)−3−[4−(3−ピペリジン−1−イルプロポキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、N−[ビス(4−フルオロフェニル)メチル]−N−メチル−2−{1−[(2E)−3−(4−{[(3S)−1−メチルピロリジン−3−イル]オキシ}フェニル)プロパ−2−エン−1−イル]ピペリジン−4−イル}アセトアミド、及び2,2−ビス(4−フルオロフェニル)−N−メチル−N−{1−[(2E)−3−(4−{[(3R)−1−メチルピロリジン−3−イル]オキシ}フェニル)プロパ−2−エン−1−イル]ピペリジン−4−イル}アセトアミドの群から選ばれる化合物である請求の範囲9に記載の含窒素飽和ヘテロ環誘導体又はその製薬学的に許容される塩。
19.前記9項に記載の一般式(II)で示される含窒素飽和ヘテロ環誘導体又はその製薬学的に許容される塩を有効成分とする医薬組成物。
20.前記1項に記載の一般式(I)で示されるヘテロ環化合物若しくは前記9項に記載の一般式(II)で示される含窒素飽和ヘテロ環誘導体又はそれらの製薬学的に許容される塩の有効量を患者に投与することからなるメラニン凝集ホルモン受容体に関与する疾患の治療方法。
21.メラニン凝集ホルモン受容体に関与する疾患が肥満である前記20項に記載の治療方法。
22.前記1項に記載の一般式(I)で示されるヘテロ環化合物若しくは前記9項に記載の一般式(II)で示される含窒素飽和ヘテロ環誘導体又はそれらの製薬学的に許容される塩を有効成分とするメラニン凝集ホルモン受容体拮抗剤の製造のための使用。
第1図は実施例50の化合物を皮下投与した場合の絶食誘発摂食に対する作用を示す。
第2図は実施例130の化合物を経口投与した場合の絶食誘発摂食に対する作用を示す。
第3図は実施例130の化合物を皮下投与した場合の絶食誘発摂食に対する作用を示す。
第2図は実施例130の化合物を経口投与した場合の絶食誘発摂食に対する作用を示す。
第3図は実施例130の化合物を皮下投与した場合の絶食誘発摂食に対する作用を示す。
更に本発明を詳述する。
「炭化水素基」とはC1−15の炭素及び水素からなる基であり、直鎖若しくは分岐状、単環式若しくは縮合多環式、及び/又は飽和若しくは不飽和の何れの形態でもよく、好ましくはアルキル、アルケニル、アルキニル、シクロアルキル、シクロアルキル−アルキル、シクロアルケニル、アリール、アルキル−アリール、アリール−アリール、アリール−アルキル又はアルキル−アリール−アルキルを意味する。
「アルキル」とは直鎖又は分岐状飽和炭化水素基を意味し、好ましくはC1−10アルキルであり、更に好ましくはC1−6アルキルである。具体的にはメチル、エチル、プロピル、イソプロピル、ブチル、ペンチル、ヘキシル、又はデシル等である。「アルケニル」とは直鎖又は分岐状で且つ少なくとも1以上の二重結合を有する炭化水素基を意味し、好ましくはC2−10アルケニルであり、具体的にはビニル、プロペニル、アリル、イソプロペニル、又はヘキセニル等である。「アルキニル」とは直鎖又は分岐状で且つ少なくとも1以上の三重結合を有する炭化水素基を意味し、好ましくはC2−10アルキニルであり、具体的にはエチニル、プロピニル、ブチニル等である。「シクロアルキル」とは、架橋を有していてもよい単環式飽和炭化水素環を意味し、好ましくは「架橋を有していてもよいC3−8シクロアルキル」であり、具体的にはシクロプロピル、シクロペンチル、シクロヘキシル、ビシクロ[2.2.1]ヘプチル又はビシクロ[2.2.2]オクチル等である。「シクロアルケニル」とは、架橋を有していてもよい単環式脂肪族の不飽和炭化水素環を意味し、好ましくは「架橋を有していてもよいC3−8シクロアルケニル」であり、具体的にはシクロペンテニル、シクロヘキセニル、ビシクロ[2.2.1]ヘプチニル又はビシクロ[2.2.2]オクテニル等である。「アリール」とは芳香性の不飽和炭化水素環を意味し、好ましくはC6−14アリールであり、具体的には、フェニル、ナフチル、1,2,3,4−テトラヒドロナフチル、インデニル、アントリル又はフルオレニル等である。
「炭化水素環基」とは上記シクロアルキル、シクロアルケニル又はアリールである。
「ヘテロ環基」とはN、S及びOから選択されるヘテロ原子を1乃至4個含有する4乃至16員の、単環式、2環式若しくは3環式の飽和若しくは不飽和環である。当該ヘテロ環基は架橋を有していても良い。不飽和環には芳香性の環(ヘテロアリール)や非芳香性の環を含む。単環式としては、アゼチジニル、ピロリジニル、ピラゾリジニル、ジオキサニル、ピペラジニル、ピペリジニル、モルホリニル、トリチアニル、ジオキソラニル、フリル、チエニル、ピロリル、イミダゾリル、ピラゾリル、チアゾリル、オキサゾリル、ピリジル、ピラジニル、ピリミジル、トリアゾリル、チアジアゾリル、ピリダジニル、トリアジニル、テトラヒドロピラニル若しくはオキサジアゾリルが、二環式としては、インドリニル、3、4−メチレンジオキシフェニル、3、4−エチレンジオキシフェニル、ベンゾフラニル、ベンゾチエニル、ベンゾチアジアゾリル、ベンゾチアゾリル、ベンゾイミダゾリル、インドリル、2,3−ジヒドロインドリル、キノリル、イソキノリル、1、2、3、4−テトラヒドロキノリル、1、2、3、4−テトラヒドロイソキノリル若しくはキノキサリニル等が、又は3環式としては、カルバゾリル、アクリジニル若しくはフェノチアジニル等が挙げられる。架橋ヘテロ環基としては、キヌクリジニル、8−アザビシクロ[3.2.1]オクチル若しくは7−アザビシクロ[2.2.1]ヘプチル等が挙げられる。
「2価の炭化水素基」とは上記炭化水素基の任意の水素原子が1個除かれた2価基を意味する。好ましくはC1−10アルキレン、C1−10アルケニレン又はC1−10アルキニレンが挙げられる。更に好ましくはC1−6アルケニレンである。
「連結原子数1から6個のリンカー」とは、置換されていてもよく、連結原子としてC、N、S、及びOの群から選択された原子が連なっている間隔を意味する。好ましくは−O−、−S−、−CO−、−SO−、−SO2−、−NR104−、−CONR104−、−NR104CO−、−NR104SO2−、−SO2NR104−、−O−CO−、−NR105CONR104−、−NR105SO2NR104−、−CSNR104−、−NR104CS−、−COO−、及び−CH2CONR104−である。
R104及びR105は同一又は異なって(1)H;(2)アリール、HO−OC−、アルキル−O−CO−、R101R102N、H2NCO−、アルキル−NHCO−、若しくは(アルキル)2NCO−で置換されていてもよいアルキル;又は(3)アシル(4)アルキルで置換されていてもよいヘテロ環である。
R104及びR1、又はR104及びR105が隣接する窒素原子と一体になって置換されていてもよいヘテロ環を形成することができる。
より好ましくは、−NR104CONR105−、−SO2NR104−、−NR104SO2−、−CONR104−、−NR104CO−及び−CO−であり、更に好ましくは−NR11CONR12−、−SO2NR11−、−NR11SO2−、−CONR11−、及び−NR11CO−である。
R11及びR12は一又は異なって、H;−CO2R13、−NR14R15、−CONR14R15若しくはアリールで置換されていてもよい低級アルキル;シクロアルキル;又はハロゲン若しくは低級アルキル−NH−CO−で置換されていてもよいアリールである。
「飽和含窒素ヘテロ環」とは少なくとも1個の窒素原子を有する飽和の上記ヘテロ環基であり、好ましくは、架橋を有していてもよい4乃至16員含窒素単環式飽和ヘテロ環である。より好ましくはアゼチジニル、ピロリジニル、ピペリジニル、ピペラジニル、キヌクリジニル、8−アザビシクロ[3.2.1]オクチル又は7−アザビシクロ[2.2.1]ヘプチル等が挙げられる。
「アシル」とはHCO−、C1−15炭化水素基−CO−、ヘテロ環基−CO−、ヘテロ環基−アルキル−CO−、ヘテロ環基−アルケニル−CO−、ヘテロ環基−アルキニル−CO−、C1−15炭化水素基−CS−、ヘテロ環基−CS−、ヘテロ環基−アルキル−CS−、ヘテロ環基−アルケニル−CS−、又はヘテロ環基−アルキニル−CS−が挙げられる。好ましくはC1−15炭化水素基−CO−、及びヘテロ環基−CO−であり、具体的にはHCO−、アセチル、プロピオニル、ベンゾイル、ニコチノイル、テノイル、ピロリジニルカルボニル又はピペリジニルカルボニル等である。
「置換されていてもよい炭化水素基」、「置換されていてもよいヘテロ環」、「置換されていてもよいアリール」及び「置換されていてもよい炭化水素2価基」における置換基としては、具体的には下記a群の置換基が挙げられる。
a群:(1)ハロゲン;(2)CN;(3)OH;(4)COOH;(5)NO2;(6)アルキル、ハロゲン、アルキル又はアシルで置換されていてもよいヘテロ環基、(7)R101R102N(R101及びR102:同一又は異なって(i)H、(ii)NH2、アルキル−NH−若しくは(アルキル)2N−で置換されていてもよいアルキル、(iii)アシル、(iv)アルキル−O−CO−、又は(v)C6−14アリール);
(8)R103−O−(R103:(i)C6−14アリール、ヘテロ環基、CN若しくはR101R102Nで置換されていてもよいアルキル、(ii)アルキル、アシル又はアルキル−O−CO−で置換されていてもよいヘテロ環、又は(iii)アリール);
(9)R103−S−;
(10)アルキル−O−CO−
(11)アルキルで置換されていてもよいアシル;(12)R101R102NCO−;(13)ハロゲンで置換されていてもよいアルキル;(14)アルキルで置換されていてもよいヘテロ環−CO−;
(15)アリール又は(16)アリールで置換されていてもよいC1−10アルケニル、
「低級」とは、特に断らない限り炭素数1から6個の直鎖又は分岐状の炭素鎖を意味する。
以下同様。
本発明有効成分又は本発明化合物には、二重結合を有するため幾何異性体や互変異性体が存在する。本発明にはこれらの異性体の分離したもの、あるいは混合物をも包含される。
また、置換基の種類によっては本発明化合物は不斉炭素原子を有する場合があり、不斉炭素原子に基づく異性体が存在しうる。本発明にはこれら光学異性体の混合物や単離されたものを包含する。また、本発明には、本発明化合物を放射性同位元素でラベル化した化合物も包含する。
更に、本発明有効成分又は本発明化合物は、酸付加塩又は置換基の種類によっては塩基との塩を形成する場合もあり、かかる塩が製薬学的に許容され得る塩である限りにおいて本発明に包含される。具体的には、塩酸、臭化水素酸、ヨウ化水素酸、硫酸、硝酸及びリン酸等の無機酸や、ギ酸、酢酸、プロピオン酸、シュウ酸、マロン酸、コハク酸、フマル酸、マレイン酸、乳酸、リンゴ酸、酒石酸、クエン酸、メタンスルホン酸、エタンスルホン酸、p−トルエンスルホン酸、アスパラギン酸及びグルタミン酸等の有機酸との酸付加塩、ナトリウム、カリウム、マグネシウム、カルシウム及びアルミニウム等の無機塩基、メチルアミン、エチルアミン、エタノールアミン、リシン及びオルニチン等の有機塩基との塩やアンモニウム塩等が挙げられる。本発明は本発明有効成分、本発明化合物及びその製薬学的に許容され得る塩の各種の水和物や溶媒和物をも包含する。更に当該結晶多形を有する物質も包含する。
また、本発明有効成分又は本発明化合物には、生体内で代謝され変換される化合物、いわゆるプロドラッグも全て包含される。本発明のプロドラッグを形成する基としては、Prog.Med.、5、2157−2161(1985)や「医薬品の開発」第7巻(廣川書店、1990年)分子設計163−198に記載の基等が挙げられる。
(製造法)
本発明化合物及びその製薬学的に許容される塩は,その基本骨格あるいは置換基の種類に基づく特徴を利用し,種々の公知の合成法を適用して製造することができる。
その際,官能基の種類によっては,当該官能基を原料乃至中間体の段階で適当な保護基(容易に当該官能基に転化可能な基)に置き換えておくことが製造技術上効果的な場合がある。このような官能基としては例えばアミノ基,水酸基又はカルボキシル基等であり,それらの保護基としては例えばグリーン(Greene)及びウッツ(Wuts)著,「Protective Groups in Organic Synthesis(第2版)」に記載の保護基を挙げることができ,これらを反応条件に応じて適宜選択して用いればよい。
このような方法では,当該保護基を導入して反応を行った後,必要に応じて保護基を除去することにより,所望の化合物を得ることができる。また,本発明有効成分が公知化合物である場合は市販若しくは種々の公知文献に基づき容易に入手可能である。
以下,本発明化合物又はその中間体の代表的な製造法を説明する。
(以下の文章中の記号は,次の通りである。
DMF:N,N−ジメチルホルムアミド;DMSO:ジメチルスルホキシド;THF:トラヒドロフラン;TFA:トリフルオロ酢酸;Tol:トルエン;EtOAc:酢酸エチル;DCE:1,2−ジクロロエタン;TEA:トリエチルアミン;Compound:化合物)
以下に本発明化合物の代表的な製造法について説明するが,これらの製造法に限定されるものではない。
また,本発明化合物中に同様な置換基が当該製造法の反応式中以外の位置に存在していれば置換基修飾反応により,容易に本発明に包含される化合物が製造される。当該置換基修飾反応は,反応点のみ説明する。
第1製造法
本反応はアルキル化反応である。1級アミン,2級アミン,アルコール,チオール,1級アミド,及び2級アミド等とその反応対応量の脱離基を有する化合物とを,反応に不活性な溶媒中,等量または一方を過剰量用いて,冷却下乃至加熱下攪拌しながら行われる。塩基(例えば炭酸カリウム,炭酸ナトリウム及び炭酸セシウム等の無機塩基,又はTEA及びジイソプロピルエチルアミン等の有機塩基,カリウムtert−ブトキシド及びナトリウムtert−ブトキシド等の金属アルコキシド,又は水素化ナトリウム及び水素化リチウム等),添加剤(ヨウ化テトラ−n−ブチルアンモニウム,ヨウ化カリウム又はヨウ化ナトリウム等)の存在下に反応させるのが,反応を円滑に進行させる上で有利な場合がある。
上述の反応に不活性な溶媒としては,例えばジクロロメタン,DCE,クロロホルム,ベンゼン,Tol,キシレン,エーテル,THF,ジオキサン,EtOAc,エタノール,メタノール,2−プロパノール,アセトニトリル,DMF,N,N−ジメチルアセトアミド,N−メチルピロリドン,ジメチルイミダゾリジノン,DMSO,アセトン,メチルエチルケトン又は水等や,これらの均一系及び不均一系混合溶媒が挙げられるが,種々の反応条件に応じて適宜選択される。
代表的な例として,本発明化合物(3)は,アミン(1)並びに脱離基を有する化合物(2)を上述のアルキル化反応に共することにより得られる。
また,化合物(6a)は水酸基を有する化合物(4a)と化合物(5)を,化合物(6b)はチオール基を有する化合物(4b)と化合物(5),並びに化合物(9)はアミン(7)と化合物(8)を反応に共することにより得られる。
以下、反応中心部のみ記載する。
(式中の記号は以下の意味を示す。
X1:ハロゲン;メタンスルホニルオキシ;又はp−トルエンスルホニルキシ等の脱離基、
R102a:H2N、アルキル−NH−若しくは(アルキル)2N−で置換されていてもよいアルキル、
R103a:ハロゲン若しくはアリールで置換されていてもよい低級アルキル;又は低級アルキル−CO−NH−で置換されていてもよいアリール、
以下同様。)
第2製造法
本反応は,還元的アミノ化反応である。
1級又は2級アミンとアルデヒド又はケトンとを還元的アミノ化の常法に従って反応させることにより行うことができる。例えば,日本化学会編「実験化学講座(丸善)」(第4版,20巻,1992年,300)等に記載の方法が挙げられる。
具体的には1級又は2級アミンとその反応対応量のアルデヒド又はケトンとを第1製造法に記載の反応に不活性な溶媒中冷却下乃至加熱下攪拌することでイミン化合物を得,該化合物に前記の反応に不活性な溶媒中水素化シアノホウ素ナトリウム,又は水素化トリアセトキシホウ素ナトリウム,水素化ホウ素ナトリウム及びギ酸等の還元剤を加え冷却下乃至加熱下攪拌することで得られる。酸(例えばチタニウムテトライソプロポキシド等のルイス酸,酢酸又はp−トルエンスルホン酸等)の存在下に反応させるのが,反応を円滑に進行させる上で有利な場合がある。上述の還元については水素雰囲気下或いはギ酸アンモニウム等の水素供与剤存在下,パラジウム(Pd),又は白金(Pt)等の金属触媒を用いて前記の反応に不活性な溶媒中接触還元することによっても行われる。
還元剤の添加時期は1級又は2級アミンとアルデヒド又はケトンの混合直後に入れても,時間をおいて入れても良い。
代表的な例として,本発明化合物(3a),(12)又は(15)はアミン[(1),(7)又は(13)]とその反応対応量のアルデヒド若しくはケトン[(10),(11)又は(14)]とを反応に共することにより得られる。
以下、反応中心部のみ記載する。
(上記式中の記号は以下の意味を示す。
ALK3:前記ALK2より炭素数1少ない置換されていてもよい2価の炭化水素基、
R102b及びR102c:同一又は異なってH;又はNH2,アルキル−NH−若しくは(アルキル)2N−で置換されていてもよいアルキル、
R13c1及びR13c2:同一又は異なってH;又はアルキル、
以下同様。)
第3製造法
本反応は,アミド化反応である。1級又は2級アミンとその反応対応量のカルボン酸若しくはその反応性誘導体とを反応させることにより行うことができる。例えば,M.Bodanszky著「Peptide Chemistry」(1988年,p55−73),泉屋信夫ら「ペプチド合成の基礎と実験」(1985年,p89−142)等に記載の方法が挙げられる。
具体的には,本反応は,通常使用される縮合試薬(ジシクロヘキシルカルボジイミド,1−エチル−3−(3−ジメチルアミノプロピル)カルボジイミド又は1,1’−カルボニルジイミダゾール(CDl)等)を用いる方法や,クロロギ酸エチルやクロロギ酸イソブチルを用いる混合酸無水物法,或いはエトキシアセチレンやtert−ブチルエチニルジメチルアミン等のアルキニルアミンを用いた対称酸無水物法により行うのが好ましい。
カルボン酸をチオニルクロリド,オキサリルクロリド又はオキシ塩化リン等のハロゲン化試剤により酸ハロゲン化物の如く反応性誘導体とした後,1級又は2級アミンと反応させることも可能である。反応は第1製造法に記載の反応不活性な溶媒中,必要により塩基(例えばTEA,ジイソプロピルエチルアミン及びピリジン等の有機塩基,又は炭酸カリウム及び炭酸水素ナトリウム等の無機塩基)の存在下,冷却下乃至加熱下攪拌しながら行われる。
代表的な例として,本発明化合物(18),(21),(23),(26)又は(28)はカルボン酸若しくはその反応性誘導体[(16),(20),(22),(24)又は(27)]とアミン[(17),(19),(1),(25)又は(7)]とを反応に共することにより得られる。
以下、反応中心部のみ記載する。
(上記式中の記号は以下の意味を示す。
X2:OH;又はハロゲン,1−ヒドロキシベンゾトリアゾール−1−イルオキシ,メトキシ,フェノキシ及びアジド基等の脱離基,或いは混合酸無水物や対称酸無水物の脱離部位、R102d−CO−:前記アシル、
以下同様。)
第4製造法
本製造法は,イソシアナートと1級又は2級アミンとを反応させることによりウレア化合物を製造する方法である。
本反応はイソシアナートと1級又は2級アミンとを第1製造法に記載の反応不活性な溶媒中,等量または一方を過剰量用いて,冷却下乃至加熱下攪拌しながら行われる。イソシアナートは,対応する酸アジドのCurtius転位等により合成できる(J.March著,ADVANCED ORGANIC CHEMISTRY(John WILEY & SONS(1992))。当該酸アジドは,カルボン酸の反応性誘導体とアジ化ナトリウム等のアジ化物塩との反応,又はカルボン酸とジフェニルリン酸アジド(DPPA)との反応により製造できる。
代表的な例として,本発明化合物(30)はイソシアナート(29)とアミン(19)とを反応に共することにより得られる。
また化合物(30a)は,前出の化合物(16)より前記と同様にして得られるイソシアナート(31)を,化合物(17)と反応させることによって製造できる。
更に化合物(30b)は,化合物(17a)と化合物(19)とを,Comprehensive Organic Functional Group Transformation,6:499,1995記載の方法により,ホスゲン,ジホスゲン,トリホスゲン,CDl,クロロギ酸4−ニトロフェニル及びクロロギ酸フェニル等のホスゲン等価体で処理しても製造できる。反応は前記の反応に不活性な溶媒中,等量から過剰量の塩基(例えばTEA及びジイソプロピルエチルアミン等の有機塩基,又は炭酸水素ナトリウム等の無機塩基)存在下,化合物(17a)又は化合物(19)の一方をホスゲン等価体で処理し,次いでもう一方の化合物を反応させることにより製造できる。クロロギ酸4−ニトロフェニル又はクロロギ酸フェニルを使用する場合,中間体であるフェニルカルバマート体を一旦単離して反応を行っても良い。
第5製造法
本製造法は,一般式(1)で表されるアミン,一般式(32)で表されるWittig試薬又はHorner−Emmons試薬及び一般式(33)で表されるアルデヒド又はケトンを反応させることにより本発明化合物(34)を製造する方法である。
本反応は,等量から過剰量の塩基(例えばTEA及びジイソプロピルエチルアミン等の有機塩基又は炭酸カリウム,炭酸ナトリウム及び炭酸セシウム等の無機塩基)存在下,化合物(1),化合物(32)及び化合物(33)を前記の不活性な溶媒中,等量またはいずれかを過剰量用いて,冷却下乃至加熱下撹拌しながら行われる。添加剤(ヨウ化テトラ−n−ブチルアンモニウム又はヨウ化カリウム等)の存在下に反応させるのが,反応を円滑に進行させる上で有利な場合がある。
先に化合物(1)と化合物(32)とを反応させ,一旦中間体を単離した後,化合物(33)との反応を行っても良い。
また,先に化合物(32)と化合物(33)とを反応させ,一旦中間体を単離した後,化合物(1)との反応を行っても良い。
(上記式中の記号は以下の意味を示す。
ALK4:置換されていてもよい2価の炭化水素基,
X3:ホスホニウム塩及び亜リン酸ジエステル等のWittig試薬;又はHorner−Emmons試薬に用いられる基、以下同様。)
第6製造法
本製造法は,一般式(35)で表される脱離基を有する化合物から本発明化合物(36)を製造する方法である。
本反応は化合物(35)を,等量から過剰量のクロロ化試剤(例えば五塩化リン及びオキシ塩化リン等の無機酸ハロゲン化物,又は塩化水素酸,塩素,塩化ナトリウム及び塩化カルシウム等)の存在下,第1製造法に記載の反応不活性な溶媒中,冷却下乃至加熱下撹拌しながら行われる。
以下、反応中心部のみ記載する。
(上記式中の記号は以下の意味を示す。
X4:Br,I,メタンスルホニルオキシ及びp−トルエンスルホニルオキシ等の脱離基、
ALK5:前記アルキレン、以下同様。)
(原料化合物の製造法)
本発明化合物を製造するための原料化合物は既知化合物を所望により,前記製造法記載の反応,あるいは,当業者にとって自明の反応(J.March著,ADVANCED ORGANIC CHEMISTRY(John WILEY & SONS(1992))(例えば,アシル化,アルキル化,ウレア化,酸化,還元(好ましくはCOMPREHENSIVE ORGANIC SYNTHESIS 8 REDUCTION(Pergamon Press)(1991)),ハロゲン化反応等)に付すことにより製造できる。
以下に原料化合物の代表的な製造法について説明するが,これらの製造法に限定されるものではない。
第7製造法
原料化合物(39),(41),(43),(46),(49),(52),(17),(58),(61),(65),(69),(72),又は(74)は,それぞれ対応するアミンから,前記第1製造法のアルキル化反応又は第2製造法の還元的アミノ化反応,あるいは第5製造法の縮合反応及びアルキル化反応と同様の方法により合成できる。
以下、反応中心部のみ記載する。
(上記式中の記号は以下の意味を示す。
P1,及びP2:保護基、
R104a,及びR104b:同一又は異なってH;又はNH2,アルキル−NH−若しくは(アルキル)2N−で置換されていてもよいアルキル、
R104a並びにR104bは接する炭素原子と一緒になって炭化水素環基を形成することができる。R1f及びR2dは2価の炭化水素基、R103b:アリールで置換されていてもよいアリール、
以下同様。)
第8製造法
原料化合物(77),(80),(82),(85),(88),又は(90)は,前記第3製造法のアミド化反応又は第4製造法のウレア化反応と同様の方法により合成できる。
又は
(上記式中の記号は以下の意味を示す。
R101a及びR102a:アルキル、
R1A:R1より炭素数の1少ない置換されていてもよい炭化水素基、
以下同様。)
第9製造法
(上記式中の記号は以下の意味を示す。
X4:シアノ基,エステル基等の還元反応によりアルデヒドへ変換できる基、
以下同様。)
原料化合物(92)は,化合物(91)の還元反応により合成できる。
本反応は化合物(91)を,還元剤(例えば水素化リチウムアルミニウム又は水素化ジイソブチルアルミニウム等)の存在下,第1製造法に記載の反応不活性な溶媒中,冷却下乃至加熱下攪拌しながら行うことが好ましい。
第10製造法
原料化合物(92),(33)又は(96)は,化合物(93),(94)又は(95)の酸化反応により合成できる。
本反応は化合物(93),(94)又は(95)を,酸化剤(例えば三酸化クロム,過マンガン酸カリウム又は二酸化マンガン等)の存在下,第1製造法に記載の反応不活性な溶媒中,冷却下乃至加熱下攪拌しながら行われる。
以下,反応中心部のみ記載する。
第11製造法
(上記式中の記号は以下の意味を示す。
X5:Br及びCl等のハロゲン、
以下同様。)
原料化合物(99)は,化合物(98)のホルミル化反応により合成できる。
本反応は化合物(98)を,ホルミル化剤(例えばDMF又はN−メチル−N−フェニルホルムアミド等)の存在下,第1製造法に記載の反応不活性な溶媒中,冷却下乃至加熱下撹拌しながら行うことが好ましい。
化合物(98)は対応するハロゲン化合物(97)のリチオ化反応により合成できる。
本反応はリチオ化剤(例えばn−ブチルリチウム又はリチウム等)の存在下,前記の反応に不活性な溶媒中,冷却下乃至加熱下攪拌しながら行われる。
第12製造法
(上記式中の記号は以下の意味を示す。
R1B,及びR1C:同一又は異なってH,置換されていてもよい炭化水素基又は置換されていてもよいヘテロ環基、以下同様。)
原料化合物(102)は,化合物(101)の還元反応により合成できる。
本反応は化合物(101)を,還元剤(例えば水素化リチウムアルミニウム又はジボラン等)の存在下,あるいは触媒(パラジウム炭素又は酸化白金等)を用いた接触水素添加条件下,第1製造法に記載の反応に不活性な溶媒中,冷却下乃至加熱下攪拌しながら行うことが好ましい。また,化合物(101)を,金属(亜鉛,鉄又はスズ等)の存在下,酸性条件(酢酸,ギ酸又は塩酸等)で,冷却下乃至加熱下攪拌しながら行うこともできる。
化合物(101)は対応するカルボニル化合物(100)のオキシム化反応により合成できる。
本反応は化合物(100)とヒドロキシルアミンとを,前記の反応に不活性な溶媒中,等量または一方を過剰量用いて,冷却下乃至加熱下攪拌しながら行われる。ヒドロキシルアミンの代わりにO−アルキルヒドロキシルアミン(例えばO−メチルヒドロキシルアミン又はO−ベンジルヒドロキシルアミン等)を用いてもよく,得られたオキシムエーテル化合物から上述の還元反応と同様の方法により,化合物(102)を合成できる。
第13製造法
原料化合物(102)は、化合物(104)の還元反応により合成できる。
本反応は化合物(104)を、還元剤(例えば水素化リチウムアルミニウム、水素化ホウ素亜鉛等)の存在下、あるいは触媒(パラジウム炭素、酸化白金等)を用いた接触水素添加条件下、前記の反応に不活性な溶媒中、冷却下乃至加熱下攪拌しながら行われる。また、化合物(104)とトリフェニルホスフィンとを、水の存在下、前記の反応に不活性な溶媒中、冷却下乃至加熱下攪拌しながら行うこともできる。
化合物(104)は対応する脱離基を有する化合物(103)のアジド化反応により合成できる。
本反応は化合物(103)を、アジド化剤(アゾ化ナトリウム、アゾ化リチウム等)の存在下、前記の反応に不活性な溶媒中、冷却下乃至加熱下攪拌しながら行われる。
第14製造法
(上記式中の記号は以下の意味を示す。
X6:シアノ基及びニトロ基等の電子吸引基、
以下同様。)
原料化合物(108),(109)及び(110)は,化合物(105)から,前記第6製造法のアリールが電子吸引基で置換されている場合の反応と同様の方法により合成できる。
第15製造法
原料化合物(112)は,一般式(111)で表されるWittig試薬又はHorner−Emmons試薬と一般式(33)で表されるアルデヒド又はケトンとを反応させることにより合成できる。
本反応は,等量から過剰量の塩基(例えば炭酸カリウム,炭酸ナトリウム及び炭酸セシウム等の無機塩基,又はTEA及びジイソプロピルエチルアミン等の有機塩基,カリウムtert−ブトキシド及びナトリウムtert−ブトキシド等の金属アルコキシド,又は水素化ナトリウム等)存在下,化合物(111)と化合物(33)とを第1製造法に記載の不活性な溶媒中,等量またはいずれかを過剰量用いて,冷却下乃至加熱下攪拌しながら行われる。
(上記式中の記号は以下の意味を示す。
X7:ハロゲン,メタンスルホニルオキシ及びp−トルエンスルホニルオキシ等の脱離基;保護基で保護されていてもよいOH;及び保護基で保護されていてもよいCO2H等、
以下同様。)
第16製造法
原料化合物(114)又は(118)は,一般式(113)又は(117)で表されるエステル化合物を公知の還元反応に付すことにより合成できる。
本反応は,等量から過剰量の還元剤(例えば水素化リチウムアルミニウム,水素化ジイソブチルアルミニウム及び水素化ホウ素ナトリウム等)存在下,エステル化合物(113)又は(117)を第1製造法に記載の不活性な溶媒中,冷却下乃至加熱下攪拌しながら行われる。
エステル化合物(113)から公知の脱保護反応により合成したカルボン酸(115)を,等量から過剰量の還元剤(例えば水素化リチウムアルミニウム,水素化ジイソブチルアルミニウム及びジボラン等)存在下,第1製造法に記載の不活性な溶媒中,冷却下乃至加熱下攪拌しながら行ってもよい。
また,カルボン酸(115)をCDl,クロロギ酸エステル及びオキサリルクロリド等で反応性誘導体へと変換した後,等量から過剰量の還元剤(例えば水素化リチウムアルミニウム及び水素化ホウ素ナトリウム等)存在下,誘導体第1製造法に記載の不活性な溶媒中,冷却下乃至加熱下攪拌しながら行ってもよい。
原料化合物(116)は,カルボン酸(65)を前記の還元反応に付し,次いで脱保護を行うことにより合成できる。
又は
(上記式中の記号は以下の意味を示す。
Alk7:置換されていてもよい2価の炭化水素基、
以下同様。)
第17製造法
原料化合物(2),(121)又は(103)のうち脱離基X1がハロゲンである化合物は,化合物(119),(120)又は(122)のハロゲン化反応により合成できる。
本反応は,化合物(119),(120)又は(122)とハロゲン化剤(例えばチオニルクロリド,チオニルブロミド,三塩化リン,五塩化リン及びオキシ塩化リン等の無機酸ハロゲン化物,又は塩化水素酸及び臭化水素酸等のハロゲン化水素酸等)とを,第1製造法に記載の反応不活性な溶媒中,冷却下乃至加熱下撹拌しながら行われる。溶媒の非存在下に反応させるのが,反応を円滑に進行させる上で有利な場合がある。
原料化合物(2),(121)又は(103)のうち脱離基X1がメタンスルホニルオキシなどのC1−10アルキルスルホニルオキシ又はp−トルエンスルホニルオキシ等の置換されていても良いC6−10アリールスルホニルオキシである化合物は,化合物(119),(120)又は(122)のスルホニル化反応により合成できる。
本反応は,化合物(119),(120)又は(122)と対応するスルホニルハライドとを,塩基(例えばTEA,ジイソプロピルエチルアミン,N−メチルモルホリン及びピリジン等の有機塩基,又は炭酸カリウム,炭酸ナトリウム,炭酸セシウム及び炭酸水素ナトリウム等の無機塩基)存在下,第1製造法に記載の不活性な溶媒中,冷却下乃至加熱下攪拌しながら行われる。
又は
(上記式中の記号は以下の意味を示す。
R103c:アルキル、以下同様。)
第18製造法
原料化合物(124)は,カルバマート体(123)を還元反応に付すことにより合成できる。
本反応は化合物(123)を,等量から過剰量の還元剤(例えば水素化リチウムアルミニウム等)存在下,第1製造法に記載の不活性な溶媒中,冷却下乃至加熱下攪拌しながら行われる。
カルバマート体(123)は,グリーン(Greene)及びウッツ(Wuts)著,「Protective Groups in Organic Synthesis(第2版)」に記載のアミノ基をカルバマート化により保護する方法を用いることで合成できる。
(上記式中の記号は以下の意味を示す。
R401:メチル基;エチル基;tert−ブチル基;及びベンゾル基等、以下同様。)
第19製造法
原料化合物(128)は,化合物(125)とケトン化合物(126)との付加反応を行った後、脱保護を行うことで合成できる。
化合物(125)と(126)との付加反応は,化合物(125)を第1製造法に記載の不活性な溶媒中,冷却下乃至加熱下,等量から過剰量の塩基(例えばn−ブチルリチウム,水素化ナトリウム及び水酸化カリウム等)で処理し,次いで等量から過剰量のカルボニル化合物(126)を加え,冷却下乃至加熱下攪拌しながら行われる。
メタンスルホンアミド体(125)は,グリーン(Greene)及びウッツ(Wuts)著,「Protective Groups in Organic Synthesis(第2版)」に記載のアミノ基をスルホンアミド化により保護する方法を用いることで合成できる。
第20製造法
原料化合物(130)は,アミド化合物(129)の還元反応により合成できる。
本反応は,等量から過剰量の還元剤(例えば水素化リチウムアルミニウム及びジボラン等)存在下,アミド化合物(129)を第1製造法に記載の不活性な溶媒中,冷却下乃至加熱下攪拌しながら行われる。
第21製造法
原料化合物(132)は,ニトリル化合物(131)の還元反応により合成できる。
本反応は,等量から過剰量の還元剤(例えば水素化リチウムアルミニウム,水素化アルミニウム及び水素化トリメトキシアルミニウムリチウム等)存在下,ニトリル化合物(131)を第1製造法に記載の不活性な溶媒中,冷却下乃至加熱下攪拌しながら行われる。また,水素雰囲気下及びアンモニア存在下,第1製造法に記載の不活性な溶媒中,冷却下乃至加熱下及び常圧乃至加圧下,ラネーニッケル等の金属触媒を用いて接触還元することによっても行われる。
第22製造法
原料化合物(134)は,一般式(33)で表されるカルボニル化合物をKnoevenagel反応に付すことにより合成できる。
本反応は,化合物(33)と等量から過剰量のマロン酸(133)とを,塩基(例えばアンモニア及びピペリジン等)存在下,第1製造法に記載の不活性な溶媒中,冷却下乃至加熱下攪拌しながら行われる。
第23製造法
原料化合物(136)は,一般式(135)で表されるアルコールを光延反応に付すことにより合成できる。
本反応は,化合物(135)と(106)とを,等量から過剰量のトリフェニルホスフィン及びアゾジカルボン酸ジエチル存在下,第1製造法に記載の不活性な溶媒中,冷却下乃至加熱下攪拌しながら行われる。
以下、反応中心部のみ記載する。
第24製造法
原料化合物(140)は,一般式(137)で表されるアミンの選択的保護及び脱保護により合成できる。
例えば,化合物(137)と等量のベンズアルデヒドとを,第1製造法に記載の不活性な溶媒中,冷却下乃至加熱下攪拌することにより,1級アミンをベンジリデンで保護した後,等量のジ−tert−ブチルジカルボナートで処理し,2級アミンをカルバマートとして保護する。次いで,ベンジリデンアミンの加水分解により脱保護を行うことで,2級アミンが選択的に保護された化合物(140)を合成できる。
(上記式中の記号は以下の意味を示す。
P1a=N−:イミン誘導体として保護されたアミノ基、以下同様。)
このようにして製造された本発明化合物又は原料化合物は遊離のまま,あるいはその塩として単離される。当該化合物の塩は遊離の塩基である本発明化合物に通常の造塩反応を付すことにより製造できる。
また本発明化合物又はその塩は,その水和物,その溶媒和物,あるいは結晶多形の物質として単離精製される。単離精製は,抽出,濃縮,留去,結晶化,濾過,再結晶及び各種クロマトグラフィー等の通常の化学操作を適用して行われる。
各種の異性体は,適当な原料化合物を選択することにより,あるいは異性体間の物質的性質の差を利用して分離することができる。例えば,光学異性体は,適当な原料を選択することにより,あるいはラセミ化合物のラセミ分割法(例えば,一般的な光学活性な酸とのジアステレオマー塩に導き光学分割する方法等)により立体化学的に純粋な異性体を得ることができる。
以下,実施例に基づき本発明を更に詳細に説明する。本発明化合物は下記実施例に記載の化合物に限定されるものではない。また原料化合物の製法を参考例に示す。なお,参考例化合物及び実施例化合物の構造式と物理化学的性状を以下表4から40に示す。表中の記号は以下の意味を有する。
Rf.:参考例番号;Ex.:実施例番号;Structure:構造式;Salt:付加塩;Data:物理化学的性状(FA:質量分析値FAB−MS(M+1);EI:質量分析値EI−MS(M+);N:NMR(DMSO−d6,TMS内部標準)の特徴的ピークδppm);NO.:化合物番号;Me:メチル;Et:エチル;Pr:プロピル;iPr:イソプロピル;Bn:ベンジル;Ac:アセチル;Boc:tert−ブトキシカルボニル;Py:ピリジン;Az:アゼチジン;Pyrroli:ピロリジン;Pipe:ピペリジン;Pipera:ピペラジン;Mo:モルホリン;Th:チオフェン;IM:イミダゾール;Bu:ブチル;Ph:フェニル;2−FPh:2−フルオロフェニル;3−FPh:3−フルオロフェニル;4−FPh:4−フルオロフェニル;2,4−diFPh:2,4−ジフルオロフェニル;2−MeOPh:2−メトキシフェニル;3−MeOPh:3−メトキシフェニル;4−MeOPh:4−メトキシフェニル;2−CNPh:2−シアノフェニル;3−CNPh:3−シアノフェニル;4−CNPh:4−シアノフェニル;3−H2NCOPh:3−(アミノカルボニル)フェニル;4−H2NCOPh:4−(アミノカルボニル)フェニル;4−MeNHCOPh:4−[(メチルアミノ)カルボニル]フェニル;4−AcNHPh:4−(アセチルアミノ)フェニル;3−HOPh:3−ヒドロキシフェニル;4−HOPh:4−ヒドロキシフェニル;3−CHOPh:3−ホルミルフェニル;4−CHOPh:4−ホルミルフェニル;2,4−diCF3Ph:2,4−ジ(トリフルオロメチル)フェニル;2,4−diiPrPh:2,4−ジイソプロピルフェニル;4−(1−Boc−Pipe−4−yloxy)Ph:4−[1−(tert−ブトキシカルボニル)ピペリジン−4−イルオキシ]フェニル;3−(1−Me−Pipe−4−yloxy)Ph:3−(1−メチルピペリジン−4−イルオキシ)フェニル;4−(1−Me−Pipe−4−yloxy)Ph:4−(1−メチルピペリジン−4−イルオキシ)フェニル;3−(1−Me−Pipe−3−yloxy)Ph:3−(1−メチルピペリジン−3−イルオキシ)フェニル;4−(1−Me−Pipe−3−yloxy)Ph:4−(1−メチルピペリジン−3−イルオキシ)フェニル;4−(1−Me−Pyrroli−3−yloxy)Ph:4−(1−メチルピロリジン−3−イルオキシ)フェニル;4−CN−3−(Pipe−4−yloxy)Ph:4−シアノ−3−(ピペリジン−4−イルオキシ)フェニル;cPr:シクロプロピル;cHex:シクロヘキシル;cOct:シクロオクチル;fum:フマル酸塩;HCl:塩酸塩;free:フリー体
参考例1
ピペリジン−4−イル酢酸エチル塩酸塩6.63gをアセトニトリル60mlに懸濁し,炭酸カリウム13.24gを加えて室温で1時間攪拌した後,シンナミルブロミド7.55gを加えて室温で30時間攪拌した。反応液をEtOAcで希釈し飽和炭酸水素ナトリウム水溶液で洗浄した後,有機層を無水硫酸ナトリウムで乾燥した。減圧下に溶媒を留去して得られた残渣をシリカゲルカラムクロマトグラフィー(クロロホルム:メタノール=97:3)で精製し,無色油状の{1−[(2E)−3−フェニルプロパ−2−エン−1−イル]ピペリジン−4−イル}酢酸エチル7.20gを得た。
参考例1と同様の方法により,参考例2から6,43から46,実施例119から131及び実施例143から148の化合物を得た。
参考例7
{1−[(2E)−3−フェニルプロパ−2−エン−1−イル]ピペリジン−4−イル}酢酸エチル6.28gをエタノール100mlに溶解し,1M水酸化ナトリウム水溶液50mlを加え,室温で23時間攪拌した。反応液を1M塩酸水溶液で中和した後,減圧下に溶媒を留去し,得られた残渣にクロロホルム:メタノール=7:3混合液150mlを加え,室温で30分間攪拌した。析出した塩化ナトリウムを濾去した後,減圧下に溶媒を留去して得られた残渣をアセトンで洗浄し,無色固体の{1−[(2E)−3−フェニルプロパ−2−エン−1−イル]ピペリジン−4−イル}酢酸4.22gを得た。
参考例7と同様の方法により,参考例8から10,47,48,61から64及び実施例149から152の化合物を得た。
参考例11
[1−(tert−ブトキシカルボニル)ピペリジン−4−イル]酢酸26.91gをDMF350mlに溶解し,N−エチル−N’−3−ジメチルアミノプロピルカルボジイミド塩酸塩21.19g及び1−ヒドロキシベンゾトリアゾール14.94gを加えて氷冷下30分間攪拌した後,ベンズヒドリルアミン19.06ml及びTEA15.4mlを加え,室温で4時間攪拌した。反応液をEtOAcで希釈し,10%クエン酸水溶液,飽和炭酸水素ナトリウム水溶液及び飽和食塩水で洗浄した。有機層を無水硫酸ナトリウムで乾燥し,減圧下に溶媒を留去した後,残渣をEtOAcより再結晶し,無色固体の4−[2−(ベンズヒドリルアミノ)−2−オキソエチル]ピペリジン−1−カルボン酸tert−ブチル37.70gを得た。
参考例11と同様の方法により,参考例12,13,59,60,65から70,実施例132から142及び実施例153から174の化合物を得た。
参考例14
[1−(tert−ブトキシカルボニル)ピペリジン−4−イル]酢酸1.28g,TEA0.74ml及びTHF12mlの混液に,氷−メタノール浴冷却下クロロギ酸イソブチル0.68mlを加え30分間攪拌した後に,(±)−[(3−フルオロフェニル)(フェニル)メチル]アミン0.97g及びTHF4mlの混液を滴下し,室温まで徐々に昇温して計5時間攪拌した。反応液にEtOAc80mlを加え,10%クエン酸水溶液40ml,水40ml,飽和炭酸水素ナトリウム水溶液40ml,水40ml,飽和食塩水40mlで順次洗浄後,有機層を無水硫酸ナトリウムで乾燥し減圧下に溶媒を留去した。残渣をシリカゲルカラムクロマトグラフィー(EtOAc:ヘキサン=1:5→1:3)で精製し,無晶状粉末の(±)−4−(2−{[(3−フルオロフェニル)(フェニル)メチル]アミノ}−2−オキソエチル)ピペリジン−1−カルボン酸tert−ブチル2.12gを得た。
参考例14と同様の方法により,参考例15及び実施例175の化合物を得た。
参考例16
4−(アミノメチル)ピペリジン−1−カルボン酸tert−ブチル0.32g,TEA0.28ml及びTHF6mlの混液に,氷冷下ジフェニルアセチルクロリド0.46gを加え氷冷下1時間,室温で3時間攪拌した。反応液にEtOAc50mlを加え,飽和炭酸水素ナトリウム水溶液25ml,水25ml,飽和食塩水25mlで順次洗浄後,有機層を無水硫酸ナトリウムで乾燥し溶媒を減圧留去した。残渣をシリカゲルカラムクロマトグラフィー(EtOAc:ヘキサン=1:3→1:2)で精製し,無晶状粉末の4−{[(ジフェニルアセチル)アミノ]メチル}ピペリジン−1−カルボン酸tert−ブチル0.37gを得た。
参考例16と同様の方法により,実施例176及び177の化合物を得た。
参考例17
1−(tert−ブトキシカルボニル)−4−メチルピペリジン−4−カルボン酸365mg,TEA0.25ml及びTol5mlの混液に,ジフェニルリン酸アジド0.39mlを加え室温で4時間,80℃で3時間攪拌した。反応液を放冷し,(ジフェニルメチル)アミン0.31mlを室温で加え,室温で3時間攪拌した。反応液にEtOAc50mlを加え,10%クエン酸水溶液25ml,水25ml,飽和炭酸水素ナトリウム水溶液25ml,水25ml,飽和食塩水25mlで順次洗浄後,有機層を無水硫酸ナトリウムで乾燥し溶媒を減圧留去した。残渣をシリカゲルカラムクロマトグラフィー(EtOAc:ヘキサン=1:2→1:1)で精製し,無晶状粉末の4−({[(ジフェニルメチル)アミノ]カルボニル}アミノ)−4−メチルピペリジン−1−カルボン酸tert−ブチル0.61gを得た。
以下,参考例17と同様の方法により実施例178の化合物を得た。
参考例18
4−[2−(ベンズヒドリルアミノ)−2−オキソエチル]ピペリジン−1−カルボン酸tert−ブチル37.70gをEtOAc140mlに溶解し,氷冷下,4M塩酸−EtOAc420mlを加え,室温で2時間攪拌した。析出した固体を濾取した後,EtOAcで洗浄し,無色固体のN−ベンズヒドリル−2−ピペリジン−4−イルアセトアミド塩酸塩31.83gを得た。
参考例18と同様の方法により,参考例19,20,57,58,71から77,及び実施例179から223の化合物を得た。
参考例21
4−ヒドロキシピペリジン−1−カルボン酸tert−ブチル20.13gをDMF200mlに溶解し,tert−ブトキシカリウム11.22gを加え,室温で4時間攪拌した。減圧下に溶媒を留去した後,残渣をDMF300mlに溶解し,4−フルオロベンゾニトリル12.11gを加え,60℃で24時間撹拌した。減圧下に溶媒を留去した後,残渣をEtOAcで希釈し,水及び飽和食塩水で洗浄した。有機層を無水硫酸ナトリウムで乾燥した後,減圧下に溶媒を留去し,薄茶色油状の4−(4−シアノフェノキシ)ピペリジン−1−カルボン酸tert−ブチル27.00gを得た。
参考例21と同様の方法により,参考例22から30及び82から86の化合物を得た。
参考例31
4−(4−シアノフェノキシ)ピペリジン−1−カルボン酸tert−ブチル26.99gをTol130mlに溶解した後,−78℃で攪拌下,反応液の温度が−60℃を超えないように水素化ジイソブチルアルミニウム(1.0mol/l Tol溶液)を滴下した。−78℃で3時間攪拌した後,同温度で飽和塩化アンモニウム水溶液80mlを滴下し,ゆっくりと室温まで昇温した。反応液をジエチルエーテル500mlで希釈し,無水硫酸マグネシウムを加え,室温で16時間攪拌した。不溶物を濾去した後,減圧下に溶媒を留去し,薄茶色油状の4−(4−ホルミルフェノキシ)ピペリジン−1−カルボン酸tert−ブチル13.14gを得た。
参考例31と同様の方法により,参考例32から39及び87から90の化合物を得た。
参考例40
4−ブロモ−3−メチルベンゾニトリル5.87gをTHF140ml及びヘキサン40mlの混合溶媒に溶解し,−100℃で撹拌下n−ブチルリチウム(1.59Mヘキサン溶液)18.8mlを滴下した。5分後,DMF12mlを加え−40℃に昇温した。さらに2時間後,反応液に塩化アンモニウム水溶液を加え,室温まで昇温した。EtOAcで希釈し飽和炭酸水素ナトリウム水溶液で洗浄した後,有機層を無水硫酸ナトリウムで乾燥した。減圧下に溶媒を留去して得られた残渣をシリカゲルカラムクロマトグラフィー(EtOAc:ヘキサン=1:2)で精製し,無色個体の4−ホルミル−3−メチルベンゾニトリル3.70gを得た。
参考例40と同様の方法により,参考例41の化合物を得た。
参考例42
ピペリジン−4−イル酢酸エチル塩酸塩8.93gを2−プロパノール400mlに溶解し,臭化(2−クロロエチル)トリフェニルホスホニウム17.45g,炭酸カリウム29.71g,よう化テトラ−n−ブチルアンモニウム3.18g及び4−(4−ホルミルフェノキシ)ピペリジン−1−カルボン酸tert−ブチル13.13gを加え,加熱還流下,24時間攪拌した後,室温まで冷却した。減圧下に溶媒を留去した後,得られた残渣をEtOAcで希釈し,水及び飽和食塩水で洗浄した。有機層を無水硫酸ナトリウムで乾燥した後,減圧下に溶媒を留去して得られた残渣をシリカゲルカラムクロマトグラフィー(クロロホルム:メタノール:濃アンモニア水=98:2:0.2)で精製し,薄茶色油状の4−(4−{(1E)−3−[4−(2−エトキシ−2−オキソエチル)ピペリジン−1−イル]プロパ−1−エン−1−イル}フェノキシ)ピペリジン−1−カルボン酸tert−ブチル10.33gを得た。
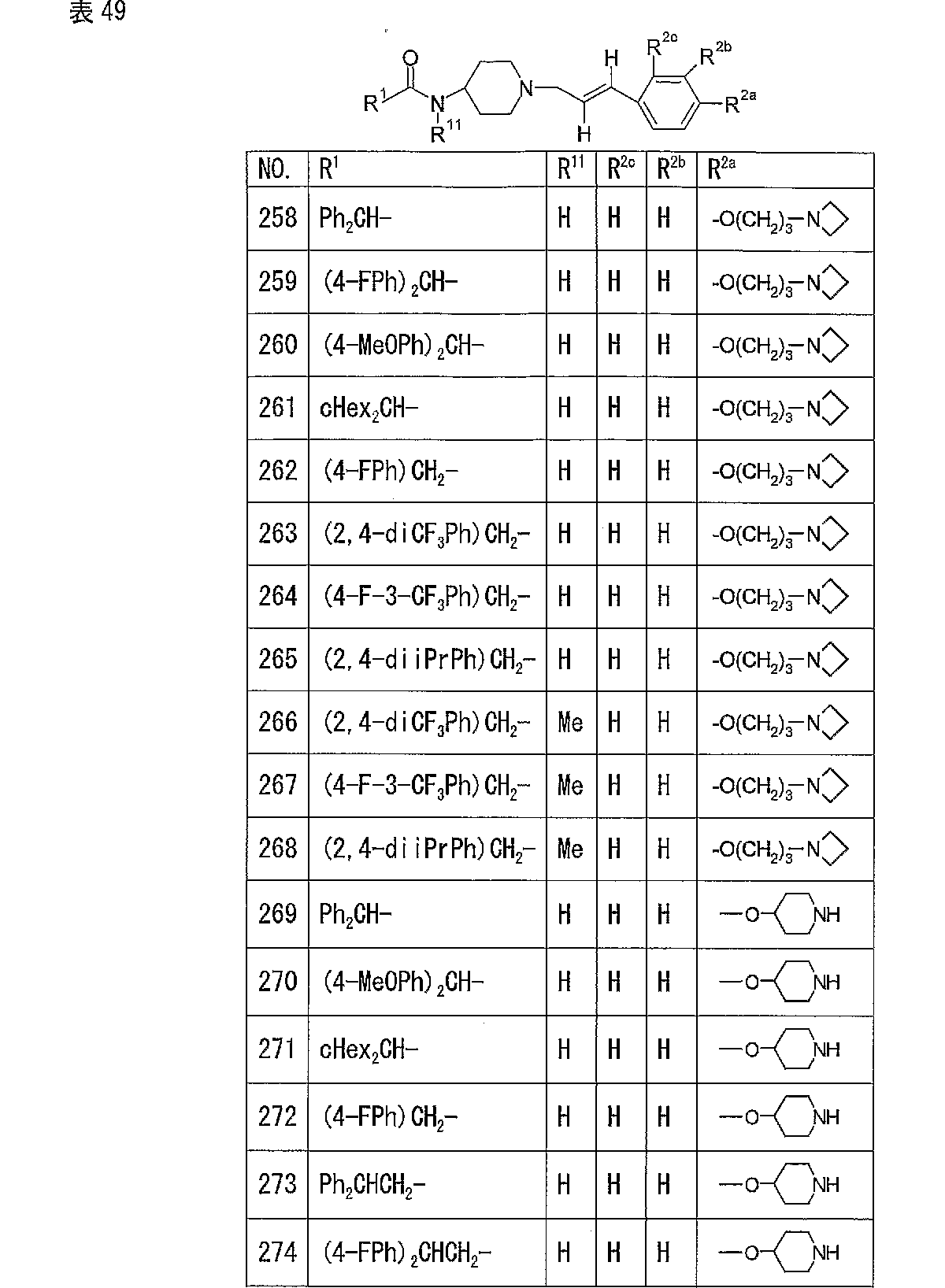
参考例42と同様の方法により,参考例91,及び実施例224から322の化合物を得た。
参考例49
N−(4−ベンゾイルフェニル)アセトアミド1.29gをピリジン15mlに溶解し,塩酸ヒドロキシルアミン0.41gを加え,80℃で4時間攪拌した。反応液を室温まで冷却した後,減圧下に溶媒を留去し,残渣にEtOAcを加え,飽和食塩水で洗浄した。有機層を無水硫酸ナトリウムで乾燥した後,減圧下に溶媒を留去して得られた残渣をシリカゲルカラムクロマトグラフィー(EtOAc:ヘキサン=50:50)で精製し,オキシム化合物1.29gを得た。このオキシム化合物0.99gを酢酸25mlに溶解し,亜鉛(粉末)1.02gを加え,室温で96時間攪拌した。不溶物を濾去した後,減圧下に溶媒を留去し,残渣にEtOAcを加え,飽和炭酸水素ナトリウム水溶液及び飽和食塩水で洗浄した。有機層を無水硫酸ナトリウムで乾燥した後,減圧下に溶媒を留去して得られた残渣をシリカゲルカラムクロマトグラフィー(クロロホルム:メタノール:濃アンモニア水=95:5:0.5)で精製し,薄茶色固体の(±)−N−{4−[アミノ(フェニル)メチル]フェニル}アセトアミド0.52gを得た。
参考例49と同様の方法により,参考例50の化合物を合成した。
参考例51
(±)−フェニル(3−チエニル)メタノール1.95gをチオニルクロリド20mlに溶解し,50℃で1.5時間攪拌した。反応液を室温まで冷却した後,減圧下に溶媒を留去し,残渣にDMF25ml及びアジ化ナトリウム1.65gを加え,80℃で14時間攪拌した。反応液を室温まで冷却した後水で希釈し,ジエチルエーテルで抽出した。有機層を飽和食塩水で洗浄し,無水硫酸ナトリウムで乾燥した後,減圧下に溶媒を留去して,アジド化合物1.71gを得た。このアジド化合物1.71gをTHF20mlに溶解し,氷冷下,水素化リチウムアルミニウム0.45gを加え,2時間攪拌した。残存している水素化リチウムアルミニウムを1M水酸化ナトリウム水溶液で処理した後,不溶物を濾去した。濾液をEtOAcで希釈した後,氷冷下,4M塩酸−EtOAc10mlを加え,同温度で30分間攪拌した。減圧下に溶媒を留去して得られた残渣をメタノール−EtOAc混合液で洗浄し,無色固体の(±)−1−フェニル−1−(3−チエニル)メチルアミン塩酸塩1.26gを得た。
参考例51と同様の方法により,参考例52及び53の化合物を合成した。
参考例54
(±)−4−[ヒドロキシ(フェニル)メチル]ベンゾニトリル3.29gをチオニルクロリド35mlに溶解し,50℃で2時間攪拌した。反応液を室温まで冷却した後,滅圧下に溶媒を留去し,残渣にDMF40ml及びアジ化ナトリウム2.56gを加え,80℃で16時間攪拌した。反応液を室温まで冷却した後,残渣に水を加え,ジエチルエーテルで抽出した。有機層を飽和食塩水で洗浄し,無水硫酸ナトリウムで乾燥した。滅圧下に溶媒を留去して得られた残渣をシリカゲルカラムクロマトグラフィー(ヘキサン:EtOAc=95:5)で精製し,アジド化合物1.19gを得た。このアジド化合物1.19gをTHF15mlに溶解し,トリフェニルホスフィン2.00gを加え,50℃で30分間攪拌した後,水0.14gを加え,50℃で2時間攪拌した。反応液を室温まで冷却した後,減圧下に溶媒を留去し,残渣にジエチルエーテル50mlを加え,室温で30分間攪拌した。不溶物を濾去した後,減圧下に溶媒を留去して得られた残渣をEtOAc20mlに溶解した。氷冷下,4M塩酸−EtOAc5mlを加え,20分間攪拌した後,析出した固体を濾取し,無色固体の(±)−4−[アミノ(フェニル)メチル]ベンゾニトリル塩酸塩0.27gを得た。
参考例55
(±)−[3−(ベンジルオキシ)フェニル](フェニル)メチルアミン1.98gをTFA20mlに溶解し,ペンタメチルベンゼン296mgを加え,室温で14時間攪拌した。減圧下に溶媒を留去した後,残渣をEtOAcで希釈し,飽和炭酸水素ナトリウム水溶液及び飽和食塩水で洗浄した。有機層を無水硫酸ナトリウムで乾燥した後,無水硫酸ナトリウムを濾去した濾液に4M塩酸−EtOAc10mlを加え,室温で20分間攪拌した。減圧下に溶媒を留去して得られた残渣をEtOAcで洗浄し,無色固体の(±)−3−[アミノ(フェニル)メチル]フェノール塩酸塩1.35gを得た。
参考例55と同様の方法により,参考例56の化合物を合成した。
参考例78
1−(tert−ブトキシカルボニル)ピペリジン−4−カルボン酸及び1,1−ビス(4−フルオロフェニル)メタンアミンを用い,参考例11及び参考例18と同様の方法を続けて行うことにより,参考例78の化合物を得た。
参考例78と同様の方法により,参考例79から81の化合物を合成した。
参考例92
4−{4−[(1E)−3−エトキシ−3−オキソプロパ−1−エン−1−イル]フェノキシ}ピペリジン−1−カルボン酸tert−ブチル8.2g,THF44mlの溶液に,−78℃撹拌下水素化ジイソブチルアルミニウム1.0MTol溶液51mlを内温が−60℃を越えない範囲で徐々に滴下後,2時間攪拌した。反応液に飽和塩化アンモニウム水溶液を加え室温に昇温し,EtOAcを加え,5%硫酸水素カリウム溶液で順次洗浄後,有機層を無水硫酸ナトリウムで乾燥し減圧下に溶媒を留去し,淡黄色粉末の4−{4−[(1E)−3−ヒドロキシプロパ−1−エン−1−イル]フェノキシ}ピペリジン−1−カルボン酸tert−ブチル7.2gを得た。
参考例92と同様の方法により,参考例93から95の化合物を合成した。
参考例96
4−{4−[(1E)−3−ヒドロキシプロパ−1−エン−1−イル]フェノキシ}ピペリジン−1−カルボン酸tert−ブチル2.00g,ジクロロメタン50ml溶液に,室温撹拌下酸化マンガン(IV)5.00gを加え一晩攪拌した。セライトを用いて濾過し減圧下に溶媒を留去し,淡黄色粉末の4−{4−[(1E)−3−オキソプロパ−1−エン−1−イル]フェノキシ}ピペリジン−1−カルボン酸tert−ブチル2.00gを得た。
参考例96と同様の方法により,参考例97から100の化合物を合成した。
参考例101
参考例83の化合物を用い,参考例92及び参考例96と同様の方法を続けて行うことにより参考例101の化合物を得た。
参考例102
水素化ナトリウム1.4g,THF50mlの懸濁液に,氷冷下ジエチルホスホノ酢酸エチル6.3mlを加え30分間攪拌した後に,[4−(4−ホルミルフェノキシ)ピペリジン−1−カルボン酸tert−ブチル8.1g,THF30ml溶液を滴下し,室温まで徐々に昇温して一晩攪拌した。反応液に飽和塩化アンモニウム水溶液を加え,EtOAcを用いて抽出後,有機層を無水硫酸ナトリウムで乾燥し減圧下に溶媒を留去した。残渣をシリカゲルカラムクロマトグラフィー(EtOAc:ヘキサン=1:6→1:4)で精製し,無色油状の4−{4−[(1E)−3−エトキシ−3−オキソプロパ−1−エン−1−イル]フェノキシ}ピペリジン−1−カルボン酸tert−ブチル8.23gを得た。
参考例102と同様の方法により,参考例103から104の化合物を合成した。
参考例105
4−フルオロサリチル酸468mg,DMF10mlの溶液に,室温撹拌下炭酸カリウム1.25g,臭化ベンジル0.82mlを順次加え2時間30分撹拌した。反応液に水を加え,EtOAcを用いて抽出後,有機層を無水硫酸ナトリウムで乾燥し減圧下に溶媒を留去し,淡黄色油状の残留物を得た。得られた残留物はそのまま次反応に用いた。
残留物のメタノール9ml,THF9ml混液に,室温撹拌下1M水酸化ナトリウム水溶液9mlを加え一晩撹拌した。反応液を1M塩酸水溶液にて酸性とし,析出した結晶をろ取し,無色結晶の2−(ベンジルオキシ)−4−フルオロ安息香酸698mgを得た。
参考例106
2−(ベンジルオキシ)−4−フルオロ安息香酸698mg,DMF7mlの溶液に,室温撹拌下1−ヒドロキシベンゾトリアゾール576mg,1−エチル3−(3−ジメチルアミノプロピル)カルボジイミド塩酸塩1.1gを順次加え30分間攪拌した後に,炭酸アンモニウム700mgを加え,4時間攪拌した。反応液に飽和炭酸水素ナトリウム水溶液を適量加え,析出した結晶をろ取し,無色結晶の2−(ベンジルオキシ)−4−フルオロベンズアミド640mgを得た。
参考例107
2−(ベンジルオキシ)−4−フルオロベンズアミド640mg,THF20mlの溶液に,室温撹拌下水素化リチウムアルミニウム200mgを徐々に加えた後に,1時間加熱還流した。室温まで冷却後,硫酸ナトリウム十水和物を適量加え,2時間攪拌した。セライトを用いて濾過し減圧下に溶媒を留去し,淡黄色油状の[2−(ベンジルオキシ)−4−フルオロベンジル]アミン600mgを得た。
参考例108
2−フルオロベンゾニトリル6.1g,DMF40mlの溶液に,室温下炭酸カリウム17g,4−ヒドロキシアセトアニリド6.2gを順次加えた後に,100℃にて4時間撹拌した。室温まで冷却後,反応液に水を適量加え,析出した結晶をろ取し,無色結晶のN−[4−(2−シアノフェノキシ)フェニル]アセトアミド10gを得た。
参考例109
4−(2−ブロモエチル)安息香酸2.29g,クロロホルム20ml,TEA3.1mlの混液に,ピロリジン0.85gを加え,室温で6時間攪拌した。減圧下で溶媒を留去した後,残渣にメタノール30mlを加え,これに硫酸1.5mlを滴下し,5.5時間加熱還流した。反応液を室温まで冷却し,飽和炭酸ナトリウム水溶液で中和し,減圧下で溶媒を留去した後,EtOAc40mlで抽出し、有機層を飽和食塩水20mlで洗浄した。減圧下で溶媒を留去した後,残渣をシリカゲルカラムクロマトグラフィー(クロロホルム→クロロホルム:メタノール=10:1)で精製し,淡黄色固体の4−(2−ピロリジン−1−イルエチル)安息香酸メチル1.43gを得た。
参考例110
水素化リチウムアルミニウム0.33g,THF10mlの混液に,氷冷下4−(2−ピロリジン−1−イルエチル)安息香酸メチル1.42gTHF10mlの混液を滴下し,室温で2.5時間撹拌した。氷冷下反応液に水0.33ml,15%水酸化ナトリウム水溶液0.33ml,水0.99mlを順次滴下し,室温で1時間攪拌した。不溶物をセライト濾過した後,減圧下で溶媒を留去した。残渣にクロロホルム10ml,酸化マンガン(IV)1.0gを加え加熱還流した。2時間後反応溶液を薄層クロマトグラフィーでチェックし,原料が残っていたため酸化マンガン(IV)1.0gを加え加熱還流した。この操作を原料が消失するまで繰り返し計6時間加熱還流した。反応終了後,不溶物をセライト濾過し,減圧下で溶媒を留去した。残渣をシリカゲルカラムクロマトグラフィー(クロロホルム→クロロホルム:メタノール=10:1)で精製し,茶色油状の4−(2−ピロリジン−1−イルエチル)ベンズアルデヒド0.69gを得た。
参考例111
3−(ピペリジン−4−イル)プロピオン酸エチル塩酸塩443mg,4−[(1E)−3−クロロプロパ−1−エン−1−イル]ベンゾニトリル428mg、炭酸カリウム690mg,ヨウ化ナリウウム298mgのDMF10ml混合溶液を60℃にて30分間加熱攪拌した。反応液に水を加えEtOAcで抽出し、水、飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し溶媒を減圧留去した。残渣をシリカゲルカラムクロマトグラフィー(クロロホルム:メタノール:濃アンモニア水=50:1:0.1)で精製し、油状物の3−{1−[(2E)−3−(4−シアノフェニル)プロパ−2−エン−1−イル]ピペリジン−4−イル}プロピオン酸エチル172mgを得た。
参考例111と同様の方法により,参考例112,113,及び実施例354の化合物を合成した。
参考例114
N−(4−フルオロフェニル)グリシンエチル394mg,35%ホルムアルデヒド水溶液3ml,ギ酸3mlの混合溶液を1時間加熱還流した。反応溶液に飽和炭酸水素ナトリウム水溶液を加えてEtOAcで抽出し、飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥した。溶媒を減圧留去することにより油状のN−(4−フルオロフェニル)−N−メチルグリシンエチル397mgを得た。
参考例115
ビス(4−フルオロフェニル)アミン615mgとブロモ酢酸エチルエステル1mlを160℃で6時間加熱攪拌した。反応混合物をシリカゲルカラムクロマトグラフィー(ヘキサン:EtOAc=5:1)で精製することにより油状のN,N−ビス(4−フルオロフェニル)グリシンエチル790mgを得た。
参考例116
N,N−ビス(4−フルオロフェニル)グリシン342mg,1−トリフルオロアセチルピペリジン−4−アミン塩酸塩350mg,1−エチル3−(3−ジメチルアミノプロピル)カルボジイミド塩酸塩346mg,1−ヒドロキシベンゾトリアゾール203mg,TEA0.209mlのDMF5ml混合溶液を室温下3時間攪拌した。反応溶液に水を加えてEtOAcで抽出し、1M塩酸、飽和炭酸水素ナトリウム水溶液、水、飽和食塩水の順で洗浄した。無水硫酸ナトリウムで乾燥し、溶媒を減圧留去後、残渣をメタノール10mlに溶解し、1M水酸化ナトリウム水溶液5mlを加えて室温下3時間攪拌した。メタノールを減圧留去後、EtOAcで抽出し、水、飽和食塩水で洗浄した。無水硫酸ナトリウムで乾燥し、溶媒を減圧留去することによりアモルファスの2−[ビス(4−フルオロフェニル)アミノ]−N−(ピペリジン−4−イル)アセトアミド417mgを得た。
参考例117
2−(ピペラジン−1−イル)酢酸エチルエステル310mg,4−{4−[(1E)−3−オキソプロパ−1−エン−1−イル]フェノキシ}ピペリジン−1−カルボン酸tert−ブチル497mg,酢酸0.45mlのDCE10ml混合溶液を室温下15分間攪拌し、さらに水素化トリアセトキシホウ素ナトリウム636mgを加えて2時間撹拌した。反応溶液に飽和炭酸水素ナトリウム水溶液を加えてクロロホルムで抽出し、無水硫酸ナトリウムで乾燥した。溶媒を減圧留去後、残渣をシリカゲルカラムクロマトグラフィー(クロロホルム:メタノール:濃アンモニア水=50:1:0.1)で精製することにより油状物の4−(4−[(1E)−3−[4−(2−エトキシ−2−オキソエチル)ピペラジン−1−イル]プロパ−1−エン−1−イル]フェノキシ)ピペリジン−1−カルボン酸tert−ブチル718mgを得た。
参考例117と同様の方法により,参考例118から119の化合物を合成した。
参考例120
[ビス(4−フルオロフェニル)メチル]アミン768mg,TEA1.25mlのDCE15ml混合溶液に氷冷下、メタンスルホニルクロリド0.278mlを加えて氷冷から室温下で3時間攪拌した。反応溶液に水を加えてクロロホルムで抽出し、無水硫酸ナトリウムで乾燥後、溶媒を減圧留去した。残渣をTHF20mlに溶解し、アルゴン雰囲気下、−78℃に冷却し、n−ブチルリチウム(1.56Mヘキサン溶液)4.7mlを加えて同温で1時間攪拌した。反応溶液にN−ベンジル−4−ピペリドン795mgを加えてさらに1時間攪拌した。反応溶液を0℃まで昇温し、飽和塩化アンモニウム水溶液を加えた後、THFを減圧留去した。水層をクロロホルムで抽出し、無水硫酸ナトリウムで乾燥後、溶媒を減圧留去して残渣をシリカケルカラムクロマトグラフィー(クロロホルム:メタノール:濃アンモニア水=20:1:0.1)で精製することにより白色固体の1−(1−ベンジル−4−ヒドロキシピペリジン−4−イル)−N−[ビス(4−フルオロフェニル)メチル]メタンスルホナミド504mgを得た。
参考例121
1−(1−ベンジル−4−ヒドロキシピペリジン−4−イル)−N−[ビス(4−フルオロフェニル)メチル]メタンスルホンアミド450mgのエタノール10ml溶液に10%パラジウム炭素100mgを加えて水素雰囲気下、常圧、室温で4日間攪拌した。不溶物をろ過して除去し、溶媒を減圧留去後、残渣をシリカゲルカラムクロマトグラフィー(クロロホルム:メタノール:濃アンモニア水=5:1:0.1)で精製することにより無色アモルファスの1−(4−ヒドロキシピペリジン−4−イル)−N−[ビス(4−フルオロフェニル)メチル]メタンスルホンアミド127mgを得た。
参考例122
4−{2−[(4−フルオロフェニル)アミノ]−2−オキソエチル}ピペリジン−1−カルボン酸tert−ブチル672mgのDMF10ml溶液に室温下、60%油性水素化ナトリウム120mgを加えて30分間攪拌した。反応溶液に4−ブロモメチル安息香酸メチル687mgを加えてさらに3時間攪拌した。反応溶液に水を加えてEtOAcで抽出し、水、飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥した。溶媒を減圧留去後、残渣をシリカゲルカラムクロマトグラフィー(クロロホルム:EtOAc=4:1)で精製することにより油状物の4−{2−[N−(4−フルオロフェニル)−N−(4−メトキシカルボニルベンジル)アミノ]−2−オキソエチル}ピペリジン−1−カルボン酸tert−ブチル940mgを得た。
参考例123
[1−(tert−ブトキシカルボニル)ピペリジン−4−イル]酢酸及び4−アミノ安息香酸エチルを用い,参考例11及び参考例122と同様の方法を続けて行うことにより,参考例123の化合物を得た。
参考例124
4−{2−[N−(4−フルオロフェニル)−N−(4−ヒドロキシメチルベンジル)アミノ]−2−オキソエチル}ピペリジン−1−カルボン酸t−ブチル570mgのDCE10ml溶液に室温下、TFA5mlを加えて一晩攪拌した。反応溶液に飽和炭酸水素ナトリウム水溶液を加えて中和した後、クロロホルムで抽出し、無水硫酸ナトリウムで乾燥後、溶媒を減圧留去することにより無色アモルファスのN−[4−(ヒドロキシメチル)ベンジル]−N−(4−フルオロフェニル)−2−(ピペリジン−4−イル)アセトアミド450mgを得た。
参考例125
2−フルオロ−4−メトキシベンズアルデヒド5g,マロン酸6.7gのピリジン70ml溶液にピペリジンを5,6滴加えて6時間加熱還流した。溶媒を減圧留去し、残渣を希アンモニア水に溶解した後、EtOAcで洗浄した。水層を1M塩酸で中和して析出物をろ取し、水で洗浄後、減圧乾燥することにより白色結晶の(2E)−3−(2−フルオロ−4−メトキシフェニル)アクリル酸2.1gを得た。
参考例126
(2E)−3−(2−フルオロ−4−メトキシフェニル)アクリル酸2.1gのジクロロメタン40ml溶液にアルゴン雰囲気下、−78℃で1M三臭化ホウ素ジクロロメタン溶液40mlを加えて室温下一晩攪拌した。反応溶液を氷水に注ぎ、析出物をろ取し、水、ジクロロメタンで洗浄後、減圧乾燥することにより無色結晶の(2E)−3−(2−フルオロ−4−ヒドロキシフェニル)アクリル酸1.8gを得た。
参考例127
(2E)−3−(2−フルオロ−4−ヒドロキシフェニル)アクリル酸1.8gのエタノール100ml溶液にチオニルクロリド10mlを滴下して加え、2時間加熱還流した。溶媒を減圧留去後、残渣をEtOAcに溶解し、水、飽和食塩水で洗浄した。無水硫酸ナトリウムで乾燥後、溶媒を減圧留去することにより無色結晶の(2E)−3−(2−フルオロ−4−ヒドロキシフェニル)アクリル酸エチル2.0gを得た。
参考例128
(2E)−3−(2−フルオロ−4−ヒドロキシフェニル)アクリル酸エチル1.05gのTHF50ml溶液に氷冷下、4−ヒドロキシピペリジン−1−カルボン酸tert−ブチル2.01g,トリフェニルフォスフィン2.62g,アゾジカルボン酸ジエチル1.57mlを加えて室温下4時間攪拌した。溶媒を減圧留去し、残渣をEtOAcに溶解して水、飽和食塩水で洗浄後、溶媒を減圧留去した。残渣をシリカゲルカラムクロマトグラフィー(ヘキサン:EtOAc=3:1で精製することにより無色油状物の4−{3−フルオロ−4−[(1E)−3−エトキシ−3−オキソプロパ−1−エン−1−イル]フェノキシ}ピペリジン−1−カルボン酸tert−ブチル2.0gを得た。
参考例129
4−{[{[1−(tert−ブトキシカルボニル)ピペリジン−4−イル]アセチル}(4−フルオロフェニル)アミノ]メチル}安息香酸600mgのTHF10ml溶液に1,1’−カルボニルジイミダゾール415mgを加えて室温下3時間攪拌した。反応溶液に水素化ホウ素ナトリウム486mg,水数滴を加えてさらに2時間撹拌した。反応溶液に氷冷下、1M塩酸を加えて30分間攪拌した後、EtOAcで抽出し、1M水酸化ナトリウム水溶液、水、飽和食塩水で洗浄した。無水硫酸ナトリウムで乾燥して溶媒を減圧留去することにより無色アモルファスの4−(2−{(4−フルオロフェニル)[4−(ヒドロキシメチル)ベンジル]アミノ}−2−オキソエチル)ピペリジン−1−カルボン酸tert−ブチル570mgを得た。
参考例130
シクロプロピルアミン2.28gをTHF20mlに溶解し,氷冷下,4−フルオロベンジルブロミド1.89gを加え,室温で3時間攪拌した。減圧下に溶媒を留去した後,残渣をEtOAc50mlに溶解し,飽和炭酸水素ナトリウム水溶液50ml及び飽和食塩水50mlで洗浄した。有機層を無水硫酸ナトリウムで乾燥した後,減圧下に溶媒を留去した。残渣をEtOAc10mlに溶解し,氷冷下,4M塩酸−EtOAc10mlを加え,同温度で30分間攪拌した。減圧下に溶媒を留去して得られた残渣をEtOAcで洗浄し,無色固体のN−(4−フルオロフェニル)シクロプロパンアミン塩酸塩1.35gを得た。
参考例131
1,1−ジシクロヘキシルメタンアミン2.36gをTHF25mlに溶解し,ジ−tert−ブチルジカルボナート2.90gを加え,室温で72時間攪拌した。減圧下に溶媒を留去した後,残渣をEtOAc100mlに溶解し,10%クエン酸水溶液100ml,飽和炭酸水素ナトリウム水溶液100ml,飽和食塩水100mlで順次洗浄した。有機層を無水硫酸ナトリウムで乾燥した後,減圧下に溶媒を留去し,無色油状のtert−ブチル(ジシクロヘキシルメチル)カルバマート3.02gを得た。
参考例132
tert−ブチル(ジシクロヘキシルメチル)カルバマート2.90gをTHF30mlに溶解し,氷冷下,水素化リチウムアルミニウム1.12gを少量ずつ加えた後,加熱還流下,15時間攪拌した。氷冷下,残存している水素化リチウムアルミニウムを1M水酸化ナトリウム水溶液で処理し,セライト濾過により不溶物を除去した後,減圧下に溶媒を留去し,無色油状の(ジシクロヘキシルメチル)メチルアミン1.58gを得た。
参考例133
メチルアミン(40%メタノール溶液)20mlに1−(クロロメチル)−2,4−ジフルオロベンゼン2.07gを加え,40℃で17時間攪拌した。減圧下に溶媒を留去した後,残渣をEtOAc100mlに溶解し,飽和炭酸水素ナトリウム水溶液100ml及び飽和食塩水100mlで洗浄した。有機層を無水硫酸ナトリウムで乾燥した後,減圧下に溶媒を留去した。残渣をEtOAc10mlに溶解し,氷冷下,4M塩酸−EtOAc5mlを加え,同温度で30分間攪拌した。減圧下に溶媒を留去して得られた残渣をEtOAcで洗浄し,無色固体のN−(2,4−ジフルオロベンジル)−N−メチルアミン塩酸塩0.35gを得た。
参考例133と同様の方法により,参考例134から135及び実施例355の化合物を合成した。
参考例137
チオニルクロリド20mlにビス(2−フルオロフェニル)メタノール2.02gを少量ずつ加え,50℃で1.5時間攪拌した。減圧下に溶媒を留去し,薄茶色油状の1−[クロロ(2−フルオロフェニル)メチル]−2−フルオロベンゼン2.18gを得た。
参考例137と同様の方法により,参考例136の化合物を合成した。
参考例139
1−[クロロ(2−フルオロフェニル)メチル]−2−フルオロベンゼン1.08gをDMF10mlに溶解し,アジ化ナトリウム0.74gを加え,80℃で24時間攪拌した。反応液を室温まで冷却した後,水50mlを加え,ジエチルエール50mlで抽出した。無水硫酸ナトリウムで乾燥した後,減圧下に溶媒を留去し,薄茶色油状の1−[アジド(2−フルオロフェニル)メチル]−2−フルオロベンゼン0.99gを得た。
参考例139と同様の方法により,参考例138の化合物を合成した。
参考例140
1−[アジド(2−フルオロフェニル)メチル]−2−フルオロベンゼン0.97gをTHF10mlに溶解し,氷冷下,水素化リチウムアルミニウム0.23gを少量ずつ加え,徐々に室温まで温度を上げながら2時間攪拌した。氷冷下,残存している水素化リチウムアルミニウムを1M水酸化ナトリウム水溶液で処理し,セライト濾過により不溶物を除去した後,減圧下に溶媒を留去した。残渣をEtOAc10mlに溶解し,氷冷下,4M塩酸−EtOAc4mlを加え,同温度で15分間攪拌した。減圧下に溶媒を留去して得られた残渣をEtOAc−ヘキサン混合液で洗浄し,無色固体の1,1−ビス(2−フルオロフェニル)メタンアミン塩酸塩0.83gを得た。
参考例140と同様の方法により,参考例141の化合物を合成した。
参考例142
1−{(2E)−3−[4−(ピペリジン−4−イルオキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−アミン1.61gをベンゼン20mlに溶解し,ベンズアルデヒド0.54gを加え,加熱還流下,生成する水を共沸により除去しながら,5時間撹拌した。反応液を室温まで冷却した後,ジ−tert−ブチルジカルボナート1.11gを加え,室温で16時間攪拌した。次いで,1M硫酸水素カリウム水溶液6.6mlを加えて室温で2時間攪拌した後,濃アンモニア水0.88gを加え,室温で1時間攪拌した。クロロホルム30mlで3回抽出した後,有機層を無水硫酸ナトリウムで乾燥し,減圧下に溶媒を留去した。残渣をシリカゲルカラムクロマトグラフィー(クロロホルム:メタノール:濃アンモニア水=90:10:1)で精製し,無色固体の4−{4−[(1E)−3−(4−アミノピペリジン−1−イル)プロパ−1−エン−1−イル]フェノキシ}ピペリジン−1−カルボン酸tert−ブチル1.57gを得た。
「炭化水素基」とはC1−15の炭素及び水素からなる基であり、直鎖若しくは分岐状、単環式若しくは縮合多環式、及び/又は飽和若しくは不飽和の何れの形態でもよく、好ましくはアルキル、アルケニル、アルキニル、シクロアルキル、シクロアルキル−アルキル、シクロアルケニル、アリール、アルキル−アリール、アリール−アリール、アリール−アルキル又はアルキル−アリール−アルキルを意味する。
「アルキル」とは直鎖又は分岐状飽和炭化水素基を意味し、好ましくはC1−10アルキルであり、更に好ましくはC1−6アルキルである。具体的にはメチル、エチル、プロピル、イソプロピル、ブチル、ペンチル、ヘキシル、又はデシル等である。「アルケニル」とは直鎖又は分岐状で且つ少なくとも1以上の二重結合を有する炭化水素基を意味し、好ましくはC2−10アルケニルであり、具体的にはビニル、プロペニル、アリル、イソプロペニル、又はヘキセニル等である。「アルキニル」とは直鎖又は分岐状で且つ少なくとも1以上の三重結合を有する炭化水素基を意味し、好ましくはC2−10アルキニルであり、具体的にはエチニル、プロピニル、ブチニル等である。「シクロアルキル」とは、架橋を有していてもよい単環式飽和炭化水素環を意味し、好ましくは「架橋を有していてもよいC3−8シクロアルキル」であり、具体的にはシクロプロピル、シクロペンチル、シクロヘキシル、ビシクロ[2.2.1]ヘプチル又はビシクロ[2.2.2]オクチル等である。「シクロアルケニル」とは、架橋を有していてもよい単環式脂肪族の不飽和炭化水素環を意味し、好ましくは「架橋を有していてもよいC3−8シクロアルケニル」であり、具体的にはシクロペンテニル、シクロヘキセニル、ビシクロ[2.2.1]ヘプチニル又はビシクロ[2.2.2]オクテニル等である。「アリール」とは芳香性の不飽和炭化水素環を意味し、好ましくはC6−14アリールであり、具体的には、フェニル、ナフチル、1,2,3,4−テトラヒドロナフチル、インデニル、アントリル又はフルオレニル等である。
「炭化水素環基」とは上記シクロアルキル、シクロアルケニル又はアリールである。
「ヘテロ環基」とはN、S及びOから選択されるヘテロ原子を1乃至4個含有する4乃至16員の、単環式、2環式若しくは3環式の飽和若しくは不飽和環である。当該ヘテロ環基は架橋を有していても良い。不飽和環には芳香性の環(ヘテロアリール)や非芳香性の環を含む。単環式としては、アゼチジニル、ピロリジニル、ピラゾリジニル、ジオキサニル、ピペラジニル、ピペリジニル、モルホリニル、トリチアニル、ジオキソラニル、フリル、チエニル、ピロリル、イミダゾリル、ピラゾリル、チアゾリル、オキサゾリル、ピリジル、ピラジニル、ピリミジル、トリアゾリル、チアジアゾリル、ピリダジニル、トリアジニル、テトラヒドロピラニル若しくはオキサジアゾリルが、二環式としては、インドリニル、3、4−メチレンジオキシフェニル、3、4−エチレンジオキシフェニル、ベンゾフラニル、ベンゾチエニル、ベンゾチアジアゾリル、ベンゾチアゾリル、ベンゾイミダゾリル、インドリル、2,3−ジヒドロインドリル、キノリル、イソキノリル、1、2、3、4−テトラヒドロキノリル、1、2、3、4−テトラヒドロイソキノリル若しくはキノキサリニル等が、又は3環式としては、カルバゾリル、アクリジニル若しくはフェノチアジニル等が挙げられる。架橋ヘテロ環基としては、キヌクリジニル、8−アザビシクロ[3.2.1]オクチル若しくは7−アザビシクロ[2.2.1]ヘプチル等が挙げられる。
「2価の炭化水素基」とは上記炭化水素基の任意の水素原子が1個除かれた2価基を意味する。好ましくはC1−10アルキレン、C1−10アルケニレン又はC1−10アルキニレンが挙げられる。更に好ましくはC1−6アルケニレンである。
「連結原子数1から6個のリンカー」とは、置換されていてもよく、連結原子としてC、N、S、及びOの群から選択された原子が連なっている間隔を意味する。好ましくは−O−、−S−、−CO−、−SO−、−SO2−、−NR104−、−CONR104−、−NR104CO−、−NR104SO2−、−SO2NR104−、−O−CO−、−NR105CONR104−、−NR105SO2NR104−、−CSNR104−、−NR104CS−、−COO−、及び−CH2CONR104−である。
R104及びR105は同一又は異なって(1)H;(2)アリール、HO−OC−、アルキル−O−CO−、R101R102N、H2NCO−、アルキル−NHCO−、若しくは(アルキル)2NCO−で置換されていてもよいアルキル;又は(3)アシル(4)アルキルで置換されていてもよいヘテロ環である。
R104及びR1、又はR104及びR105が隣接する窒素原子と一体になって置換されていてもよいヘテロ環を形成することができる。
より好ましくは、−NR104CONR105−、−SO2NR104−、−NR104SO2−、−CONR104−、−NR104CO−及び−CO−であり、更に好ましくは−NR11CONR12−、−SO2NR11−、−NR11SO2−、−CONR11−、及び−NR11CO−である。
R11及びR12は一又は異なって、H;−CO2R13、−NR14R15、−CONR14R15若しくはアリールで置換されていてもよい低級アルキル;シクロアルキル;又はハロゲン若しくは低級アルキル−NH−CO−で置換されていてもよいアリールである。
「飽和含窒素ヘテロ環」とは少なくとも1個の窒素原子を有する飽和の上記ヘテロ環基であり、好ましくは、架橋を有していてもよい4乃至16員含窒素単環式飽和ヘテロ環である。より好ましくはアゼチジニル、ピロリジニル、ピペリジニル、ピペラジニル、キヌクリジニル、8−アザビシクロ[3.2.1]オクチル又は7−アザビシクロ[2.2.1]ヘプチル等が挙げられる。
「アシル」とはHCO−、C1−15炭化水素基−CO−、ヘテロ環基−CO−、ヘテロ環基−アルキル−CO−、ヘテロ環基−アルケニル−CO−、ヘテロ環基−アルキニル−CO−、C1−15炭化水素基−CS−、ヘテロ環基−CS−、ヘテロ環基−アルキル−CS−、ヘテロ環基−アルケニル−CS−、又はヘテロ環基−アルキニル−CS−が挙げられる。好ましくはC1−15炭化水素基−CO−、及びヘテロ環基−CO−であり、具体的にはHCO−、アセチル、プロピオニル、ベンゾイル、ニコチノイル、テノイル、ピロリジニルカルボニル又はピペリジニルカルボニル等である。
「置換されていてもよい炭化水素基」、「置換されていてもよいヘテロ環」、「置換されていてもよいアリール」及び「置換されていてもよい炭化水素2価基」における置換基としては、具体的には下記a群の置換基が挙げられる。
a群:(1)ハロゲン;(2)CN;(3)OH;(4)COOH;(5)NO2;(6)アルキル、ハロゲン、アルキル又はアシルで置換されていてもよいヘテロ環基、(7)R101R102N(R101及びR102:同一又は異なって(i)H、(ii)NH2、アルキル−NH−若しくは(アルキル)2N−で置換されていてもよいアルキル、(iii)アシル、(iv)アルキル−O−CO−、又は(v)C6−14アリール);
(8)R103−O−(R103:(i)C6−14アリール、ヘテロ環基、CN若しくはR101R102Nで置換されていてもよいアルキル、(ii)アルキル、アシル又はアルキル−O−CO−で置換されていてもよいヘテロ環、又は(iii)アリール);
(9)R103−S−;
(10)アルキル−O−CO−
(11)アルキルで置換されていてもよいアシル;(12)R101R102NCO−;(13)ハロゲンで置換されていてもよいアルキル;(14)アルキルで置換されていてもよいヘテロ環−CO−;
(15)アリール又は(16)アリールで置換されていてもよいC1−10アルケニル、
「低級」とは、特に断らない限り炭素数1から6個の直鎖又は分岐状の炭素鎖を意味する。
以下同様。
本発明有効成分又は本発明化合物には、二重結合を有するため幾何異性体や互変異性体が存在する。本発明にはこれらの異性体の分離したもの、あるいは混合物をも包含される。
また、置換基の種類によっては本発明化合物は不斉炭素原子を有する場合があり、不斉炭素原子に基づく異性体が存在しうる。本発明にはこれら光学異性体の混合物や単離されたものを包含する。また、本発明には、本発明化合物を放射性同位元素でラベル化した化合物も包含する。
更に、本発明有効成分又は本発明化合物は、酸付加塩又は置換基の種類によっては塩基との塩を形成する場合もあり、かかる塩が製薬学的に許容され得る塩である限りにおいて本発明に包含される。具体的には、塩酸、臭化水素酸、ヨウ化水素酸、硫酸、硝酸及びリン酸等の無機酸や、ギ酸、酢酸、プロピオン酸、シュウ酸、マロン酸、コハク酸、フマル酸、マレイン酸、乳酸、リンゴ酸、酒石酸、クエン酸、メタンスルホン酸、エタンスルホン酸、p−トルエンスルホン酸、アスパラギン酸及びグルタミン酸等の有機酸との酸付加塩、ナトリウム、カリウム、マグネシウム、カルシウム及びアルミニウム等の無機塩基、メチルアミン、エチルアミン、エタノールアミン、リシン及びオルニチン等の有機塩基との塩やアンモニウム塩等が挙げられる。本発明は本発明有効成分、本発明化合物及びその製薬学的に許容され得る塩の各種の水和物や溶媒和物をも包含する。更に当該結晶多形を有する物質も包含する。
また、本発明有効成分又は本発明化合物には、生体内で代謝され変換される化合物、いわゆるプロドラッグも全て包含される。本発明のプロドラッグを形成する基としては、Prog.Med.、5、2157−2161(1985)や「医薬品の開発」第7巻(廣川書店、1990年)分子設計163−198に記載の基等が挙げられる。
(製造法)
本発明化合物及びその製薬学的に許容される塩は,その基本骨格あるいは置換基の種類に基づく特徴を利用し,種々の公知の合成法を適用して製造することができる。
その際,官能基の種類によっては,当該官能基を原料乃至中間体の段階で適当な保護基(容易に当該官能基に転化可能な基)に置き換えておくことが製造技術上効果的な場合がある。このような官能基としては例えばアミノ基,水酸基又はカルボキシル基等であり,それらの保護基としては例えばグリーン(Greene)及びウッツ(Wuts)著,「Protective Groups in Organic Synthesis(第2版)」に記載の保護基を挙げることができ,これらを反応条件に応じて適宜選択して用いればよい。
このような方法では,当該保護基を導入して反応を行った後,必要に応じて保護基を除去することにより,所望の化合物を得ることができる。また,本発明有効成分が公知化合物である場合は市販若しくは種々の公知文献に基づき容易に入手可能である。
以下,本発明化合物又はその中間体の代表的な製造法を説明する。
(以下の文章中の記号は,次の通りである。
DMF:N,N−ジメチルホルムアミド;DMSO:ジメチルスルホキシド;THF:トラヒドロフラン;TFA:トリフルオロ酢酸;Tol:トルエン;EtOAc:酢酸エチル;DCE:1,2−ジクロロエタン;TEA:トリエチルアミン;Compound:化合物)
以下に本発明化合物の代表的な製造法について説明するが,これらの製造法に限定されるものではない。
また,本発明化合物中に同様な置換基が当該製造法の反応式中以外の位置に存在していれば置換基修飾反応により,容易に本発明に包含される化合物が製造される。当該置換基修飾反応は,反応点のみ説明する。
第1製造法
本反応はアルキル化反応である。1級アミン,2級アミン,アルコール,チオール,1級アミド,及び2級アミド等とその反応対応量の脱離基を有する化合物とを,反応に不活性な溶媒中,等量または一方を過剰量用いて,冷却下乃至加熱下攪拌しながら行われる。塩基(例えば炭酸カリウム,炭酸ナトリウム及び炭酸セシウム等の無機塩基,又はTEA及びジイソプロピルエチルアミン等の有機塩基,カリウムtert−ブトキシド及びナトリウムtert−ブトキシド等の金属アルコキシド,又は水素化ナトリウム及び水素化リチウム等),添加剤(ヨウ化テトラ−n−ブチルアンモニウム,ヨウ化カリウム又はヨウ化ナトリウム等)の存在下に反応させるのが,反応を円滑に進行させる上で有利な場合がある。
上述の反応に不活性な溶媒としては,例えばジクロロメタン,DCE,クロロホルム,ベンゼン,Tol,キシレン,エーテル,THF,ジオキサン,EtOAc,エタノール,メタノール,2−プロパノール,アセトニトリル,DMF,N,N−ジメチルアセトアミド,N−メチルピロリドン,ジメチルイミダゾリジノン,DMSO,アセトン,メチルエチルケトン又は水等や,これらの均一系及び不均一系混合溶媒が挙げられるが,種々の反応条件に応じて適宜選択される。
代表的な例として,本発明化合物(3)は,アミン(1)並びに脱離基を有する化合物(2)を上述のアルキル化反応に共することにより得られる。
また,化合物(6a)は水酸基を有する化合物(4a)と化合物(5)を,化合物(6b)はチオール基を有する化合物(4b)と化合物(5),並びに化合物(9)はアミン(7)と化合物(8)を反応に共することにより得られる。
以下、反応中心部のみ記載する。
(式中の記号は以下の意味を示す。
X1:ハロゲン;メタンスルホニルオキシ;又はp−トルエンスルホニルキシ等の脱離基、
R102a:H2N、アルキル−NH−若しくは(アルキル)2N−で置換されていてもよいアルキル、
R103a:ハロゲン若しくはアリールで置換されていてもよい低級アルキル;又は低級アルキル−CO−NH−で置換されていてもよいアリール、
以下同様。)
第2製造法
本反応は,還元的アミノ化反応である。
1級又は2級アミンとアルデヒド又はケトンとを還元的アミノ化の常法に従って反応させることにより行うことができる。例えば,日本化学会編「実験化学講座(丸善)」(第4版,20巻,1992年,300)等に記載の方法が挙げられる。
具体的には1級又は2級アミンとその反応対応量のアルデヒド又はケトンとを第1製造法に記載の反応に不活性な溶媒中冷却下乃至加熱下攪拌することでイミン化合物を得,該化合物に前記の反応に不活性な溶媒中水素化シアノホウ素ナトリウム,又は水素化トリアセトキシホウ素ナトリウム,水素化ホウ素ナトリウム及びギ酸等の還元剤を加え冷却下乃至加熱下攪拌することで得られる。酸(例えばチタニウムテトライソプロポキシド等のルイス酸,酢酸又はp−トルエンスルホン酸等)の存在下に反応させるのが,反応を円滑に進行させる上で有利な場合がある。上述の還元については水素雰囲気下或いはギ酸アンモニウム等の水素供与剤存在下,パラジウム(Pd),又は白金(Pt)等の金属触媒を用いて前記の反応に不活性な溶媒中接触還元することによっても行われる。
還元剤の添加時期は1級又は2級アミンとアルデヒド又はケトンの混合直後に入れても,時間をおいて入れても良い。
代表的な例として,本発明化合物(3a),(12)又は(15)はアミン[(1),(7)又は(13)]とその反応対応量のアルデヒド若しくはケトン[(10),(11)又は(14)]とを反応に共することにより得られる。
以下、反応中心部のみ記載する。
(上記式中の記号は以下の意味を示す。
ALK3:前記ALK2より炭素数1少ない置換されていてもよい2価の炭化水素基、
R102b及びR102c:同一又は異なってH;又はNH2,アルキル−NH−若しくは(アルキル)2N−で置換されていてもよいアルキル、
R13c1及びR13c2:同一又は異なってH;又はアルキル、
以下同様。)
第3製造法
本反応は,アミド化反応である。1級又は2級アミンとその反応対応量のカルボン酸若しくはその反応性誘導体とを反応させることにより行うことができる。例えば,M.Bodanszky著「Peptide Chemistry」(1988年,p55−73),泉屋信夫ら「ペプチド合成の基礎と実験」(1985年,p89−142)等に記載の方法が挙げられる。
具体的には,本反応は,通常使用される縮合試薬(ジシクロヘキシルカルボジイミド,1−エチル−3−(3−ジメチルアミノプロピル)カルボジイミド又は1,1’−カルボニルジイミダゾール(CDl)等)を用いる方法や,クロロギ酸エチルやクロロギ酸イソブチルを用いる混合酸無水物法,或いはエトキシアセチレンやtert−ブチルエチニルジメチルアミン等のアルキニルアミンを用いた対称酸無水物法により行うのが好ましい。
カルボン酸をチオニルクロリド,オキサリルクロリド又はオキシ塩化リン等のハロゲン化試剤により酸ハロゲン化物の如く反応性誘導体とした後,1級又は2級アミンと反応させることも可能である。反応は第1製造法に記載の反応不活性な溶媒中,必要により塩基(例えばTEA,ジイソプロピルエチルアミン及びピリジン等の有機塩基,又は炭酸カリウム及び炭酸水素ナトリウム等の無機塩基)の存在下,冷却下乃至加熱下攪拌しながら行われる。
代表的な例として,本発明化合物(18),(21),(23),(26)又は(28)はカルボン酸若しくはその反応性誘導体[(16),(20),(22),(24)又は(27)]とアミン[(17),(19),(1),(25)又は(7)]とを反応に共することにより得られる。
以下、反応中心部のみ記載する。
(上記式中の記号は以下の意味を示す。
X2:OH;又はハロゲン,1−ヒドロキシベンゾトリアゾール−1−イルオキシ,メトキシ,フェノキシ及びアジド基等の脱離基,或いは混合酸無水物や対称酸無水物の脱離部位、R102d−CO−:前記アシル、
以下同様。)
第4製造法
本製造法は,イソシアナートと1級又は2級アミンとを反応させることによりウレア化合物を製造する方法である。
本反応はイソシアナートと1級又は2級アミンとを第1製造法に記載の反応不活性な溶媒中,等量または一方を過剰量用いて,冷却下乃至加熱下攪拌しながら行われる。イソシアナートは,対応する酸アジドのCurtius転位等により合成できる(J.March著,ADVANCED ORGANIC CHEMISTRY(John WILEY & SONS(1992))。当該酸アジドは,カルボン酸の反応性誘導体とアジ化ナトリウム等のアジ化物塩との反応,又はカルボン酸とジフェニルリン酸アジド(DPPA)との反応により製造できる。
代表的な例として,本発明化合物(30)はイソシアナート(29)とアミン(19)とを反応に共することにより得られる。
また化合物(30a)は,前出の化合物(16)より前記と同様にして得られるイソシアナート(31)を,化合物(17)と反応させることによって製造できる。
更に化合物(30b)は,化合物(17a)と化合物(19)とを,Comprehensive Organic Functional Group Transformation,6:499,1995記載の方法により,ホスゲン,ジホスゲン,トリホスゲン,CDl,クロロギ酸4−ニトロフェニル及びクロロギ酸フェニル等のホスゲン等価体で処理しても製造できる。反応は前記の反応に不活性な溶媒中,等量から過剰量の塩基(例えばTEA及びジイソプロピルエチルアミン等の有機塩基,又は炭酸水素ナトリウム等の無機塩基)存在下,化合物(17a)又は化合物(19)の一方をホスゲン等価体で処理し,次いでもう一方の化合物を反応させることにより製造できる。クロロギ酸4−ニトロフェニル又はクロロギ酸フェニルを使用する場合,中間体であるフェニルカルバマート体を一旦単離して反応を行っても良い。
第5製造法
本製造法は,一般式(1)で表されるアミン,一般式(32)で表されるWittig試薬又はHorner−Emmons試薬及び一般式(33)で表されるアルデヒド又はケトンを反応させることにより本発明化合物(34)を製造する方法である。
本反応は,等量から過剰量の塩基(例えばTEA及びジイソプロピルエチルアミン等の有機塩基又は炭酸カリウム,炭酸ナトリウム及び炭酸セシウム等の無機塩基)存在下,化合物(1),化合物(32)及び化合物(33)を前記の不活性な溶媒中,等量またはいずれかを過剰量用いて,冷却下乃至加熱下撹拌しながら行われる。添加剤(ヨウ化テトラ−n−ブチルアンモニウム又はヨウ化カリウム等)の存在下に反応させるのが,反応を円滑に進行させる上で有利な場合がある。
先に化合物(1)と化合物(32)とを反応させ,一旦中間体を単離した後,化合物(33)との反応を行っても良い。
また,先に化合物(32)と化合物(33)とを反応させ,一旦中間体を単離した後,化合物(1)との反応を行っても良い。
(上記式中の記号は以下の意味を示す。
ALK4:置換されていてもよい2価の炭化水素基,
X3:ホスホニウム塩及び亜リン酸ジエステル等のWittig試薬;又はHorner−Emmons試薬に用いられる基、以下同様。)
第6製造法
本製造法は,一般式(35)で表される脱離基を有する化合物から本発明化合物(36)を製造する方法である。
本反応は化合物(35)を,等量から過剰量のクロロ化試剤(例えば五塩化リン及びオキシ塩化リン等の無機酸ハロゲン化物,又は塩化水素酸,塩素,塩化ナトリウム及び塩化カルシウム等)の存在下,第1製造法に記載の反応不活性な溶媒中,冷却下乃至加熱下撹拌しながら行われる。
以下、反応中心部のみ記載する。
(上記式中の記号は以下の意味を示す。
X4:Br,I,メタンスルホニルオキシ及びp−トルエンスルホニルオキシ等の脱離基、
ALK5:前記アルキレン、以下同様。)
(原料化合物の製造法)
本発明化合物を製造するための原料化合物は既知化合物を所望により,前記製造法記載の反応,あるいは,当業者にとって自明の反応(J.March著,ADVANCED ORGANIC CHEMISTRY(John WILEY & SONS(1992))(例えば,アシル化,アルキル化,ウレア化,酸化,還元(好ましくはCOMPREHENSIVE ORGANIC SYNTHESIS 8 REDUCTION(Pergamon Press)(1991)),ハロゲン化反応等)に付すことにより製造できる。
以下に原料化合物の代表的な製造法について説明するが,これらの製造法に限定されるものではない。
第7製造法
原料化合物(39),(41),(43),(46),(49),(52),(17),(58),(61),(65),(69),(72),又は(74)は,それぞれ対応するアミンから,前記第1製造法のアルキル化反応又は第2製造法の還元的アミノ化反応,あるいは第5製造法の縮合反応及びアルキル化反応と同様の方法により合成できる。
以下、反応中心部のみ記載する。
(上記式中の記号は以下の意味を示す。
P1,及びP2:保護基、
R104a,及びR104b:同一又は異なってH;又はNH2,アルキル−NH−若しくは(アルキル)2N−で置換されていてもよいアルキル、
R104a並びにR104bは接する炭素原子と一緒になって炭化水素環基を形成することができる。R1f及びR2dは2価の炭化水素基、R103b:アリールで置換されていてもよいアリール、
以下同様。)
第8製造法
原料化合物(77),(80),(82),(85),(88),又は(90)は,前記第3製造法のアミド化反応又は第4製造法のウレア化反応と同様の方法により合成できる。
又は
(上記式中の記号は以下の意味を示す。
R101a及びR102a:アルキル、
R1A:R1より炭素数の1少ない置換されていてもよい炭化水素基、
以下同様。)
第9製造法
(上記式中の記号は以下の意味を示す。
X4:シアノ基,エステル基等の還元反応によりアルデヒドへ変換できる基、
以下同様。)
原料化合物(92)は,化合物(91)の還元反応により合成できる。
本反応は化合物(91)を,還元剤(例えば水素化リチウムアルミニウム又は水素化ジイソブチルアルミニウム等)の存在下,第1製造法に記載の反応不活性な溶媒中,冷却下乃至加熱下攪拌しながら行うことが好ましい。
第10製造法
原料化合物(92),(33)又は(96)は,化合物(93),(94)又は(95)の酸化反応により合成できる。
本反応は化合物(93),(94)又は(95)を,酸化剤(例えば三酸化クロム,過マンガン酸カリウム又は二酸化マンガン等)の存在下,第1製造法に記載の反応不活性な溶媒中,冷却下乃至加熱下攪拌しながら行われる。
以下,反応中心部のみ記載する。
第11製造法
(上記式中の記号は以下の意味を示す。
X5:Br及びCl等のハロゲン、
以下同様。)
原料化合物(99)は,化合物(98)のホルミル化反応により合成できる。
本反応は化合物(98)を,ホルミル化剤(例えばDMF又はN−メチル−N−フェニルホルムアミド等)の存在下,第1製造法に記載の反応不活性な溶媒中,冷却下乃至加熱下撹拌しながら行うことが好ましい。
化合物(98)は対応するハロゲン化合物(97)のリチオ化反応により合成できる。
本反応はリチオ化剤(例えばn−ブチルリチウム又はリチウム等)の存在下,前記の反応に不活性な溶媒中,冷却下乃至加熱下攪拌しながら行われる。
第12製造法
(上記式中の記号は以下の意味を示す。
R1B,及びR1C:同一又は異なってH,置換されていてもよい炭化水素基又は置換されていてもよいヘテロ環基、以下同様。)
原料化合物(102)は,化合物(101)の還元反応により合成できる。
本反応は化合物(101)を,還元剤(例えば水素化リチウムアルミニウム又はジボラン等)の存在下,あるいは触媒(パラジウム炭素又は酸化白金等)を用いた接触水素添加条件下,第1製造法に記載の反応に不活性な溶媒中,冷却下乃至加熱下攪拌しながら行うことが好ましい。また,化合物(101)を,金属(亜鉛,鉄又はスズ等)の存在下,酸性条件(酢酸,ギ酸又は塩酸等)で,冷却下乃至加熱下攪拌しながら行うこともできる。
化合物(101)は対応するカルボニル化合物(100)のオキシム化反応により合成できる。
本反応は化合物(100)とヒドロキシルアミンとを,前記の反応に不活性な溶媒中,等量または一方を過剰量用いて,冷却下乃至加熱下攪拌しながら行われる。ヒドロキシルアミンの代わりにO−アルキルヒドロキシルアミン(例えばO−メチルヒドロキシルアミン又はO−ベンジルヒドロキシルアミン等)を用いてもよく,得られたオキシムエーテル化合物から上述の還元反応と同様の方法により,化合物(102)を合成できる。
第13製造法
原料化合物(102)は、化合物(104)の還元反応により合成できる。
本反応は化合物(104)を、還元剤(例えば水素化リチウムアルミニウム、水素化ホウ素亜鉛等)の存在下、あるいは触媒(パラジウム炭素、酸化白金等)を用いた接触水素添加条件下、前記の反応に不活性な溶媒中、冷却下乃至加熱下攪拌しながら行われる。また、化合物(104)とトリフェニルホスフィンとを、水の存在下、前記の反応に不活性な溶媒中、冷却下乃至加熱下攪拌しながら行うこともできる。
化合物(104)は対応する脱離基を有する化合物(103)のアジド化反応により合成できる。
本反応は化合物(103)を、アジド化剤(アゾ化ナトリウム、アゾ化リチウム等)の存在下、前記の反応に不活性な溶媒中、冷却下乃至加熱下攪拌しながら行われる。
第14製造法
(上記式中の記号は以下の意味を示す。
X6:シアノ基及びニトロ基等の電子吸引基、
以下同様。)
原料化合物(108),(109)及び(110)は,化合物(105)から,前記第6製造法のアリールが電子吸引基で置換されている場合の反応と同様の方法により合成できる。
第15製造法
原料化合物(112)は,一般式(111)で表されるWittig試薬又はHorner−Emmons試薬と一般式(33)で表されるアルデヒド又はケトンとを反応させることにより合成できる。
本反応は,等量から過剰量の塩基(例えば炭酸カリウム,炭酸ナトリウム及び炭酸セシウム等の無機塩基,又はTEA及びジイソプロピルエチルアミン等の有機塩基,カリウムtert−ブトキシド及びナトリウムtert−ブトキシド等の金属アルコキシド,又は水素化ナトリウム等)存在下,化合物(111)と化合物(33)とを第1製造法に記載の不活性な溶媒中,等量またはいずれかを過剰量用いて,冷却下乃至加熱下攪拌しながら行われる。
(上記式中の記号は以下の意味を示す。
X7:ハロゲン,メタンスルホニルオキシ及びp−トルエンスルホニルオキシ等の脱離基;保護基で保護されていてもよいOH;及び保護基で保護されていてもよいCO2H等、
以下同様。)
第16製造法
原料化合物(114)又は(118)は,一般式(113)又は(117)で表されるエステル化合物を公知の還元反応に付すことにより合成できる。
本反応は,等量から過剰量の還元剤(例えば水素化リチウムアルミニウム,水素化ジイソブチルアルミニウム及び水素化ホウ素ナトリウム等)存在下,エステル化合物(113)又は(117)を第1製造法に記載の不活性な溶媒中,冷却下乃至加熱下攪拌しながら行われる。
エステル化合物(113)から公知の脱保護反応により合成したカルボン酸(115)を,等量から過剰量の還元剤(例えば水素化リチウムアルミニウム,水素化ジイソブチルアルミニウム及びジボラン等)存在下,第1製造法に記載の不活性な溶媒中,冷却下乃至加熱下攪拌しながら行ってもよい。
また,カルボン酸(115)をCDl,クロロギ酸エステル及びオキサリルクロリド等で反応性誘導体へと変換した後,等量から過剰量の還元剤(例えば水素化リチウムアルミニウム及び水素化ホウ素ナトリウム等)存在下,誘導体第1製造法に記載の不活性な溶媒中,冷却下乃至加熱下攪拌しながら行ってもよい。
原料化合物(116)は,カルボン酸(65)を前記の還元反応に付し,次いで脱保護を行うことにより合成できる。
又は
(上記式中の記号は以下の意味を示す。
Alk7:置換されていてもよい2価の炭化水素基、
以下同様。)
第17製造法
原料化合物(2),(121)又は(103)のうち脱離基X1がハロゲンである化合物は,化合物(119),(120)又は(122)のハロゲン化反応により合成できる。
本反応は,化合物(119),(120)又は(122)とハロゲン化剤(例えばチオニルクロリド,チオニルブロミド,三塩化リン,五塩化リン及びオキシ塩化リン等の無機酸ハロゲン化物,又は塩化水素酸及び臭化水素酸等のハロゲン化水素酸等)とを,第1製造法に記載の反応不活性な溶媒中,冷却下乃至加熱下撹拌しながら行われる。溶媒の非存在下に反応させるのが,反応を円滑に進行させる上で有利な場合がある。
原料化合物(2),(121)又は(103)のうち脱離基X1がメタンスルホニルオキシなどのC1−10アルキルスルホニルオキシ又はp−トルエンスルホニルオキシ等の置換されていても良いC6−10アリールスルホニルオキシである化合物は,化合物(119),(120)又は(122)のスルホニル化反応により合成できる。
本反応は,化合物(119),(120)又は(122)と対応するスルホニルハライドとを,塩基(例えばTEA,ジイソプロピルエチルアミン,N−メチルモルホリン及びピリジン等の有機塩基,又は炭酸カリウム,炭酸ナトリウム,炭酸セシウム及び炭酸水素ナトリウム等の無機塩基)存在下,第1製造法に記載の不活性な溶媒中,冷却下乃至加熱下攪拌しながら行われる。
又は
(上記式中の記号は以下の意味を示す。
R103c:アルキル、以下同様。)
第18製造法
原料化合物(124)は,カルバマート体(123)を還元反応に付すことにより合成できる。
本反応は化合物(123)を,等量から過剰量の還元剤(例えば水素化リチウムアルミニウム等)存在下,第1製造法に記載の不活性な溶媒中,冷却下乃至加熱下攪拌しながら行われる。
カルバマート体(123)は,グリーン(Greene)及びウッツ(Wuts)著,「Protective Groups in Organic Synthesis(第2版)」に記載のアミノ基をカルバマート化により保護する方法を用いることで合成できる。
(上記式中の記号は以下の意味を示す。
R401:メチル基;エチル基;tert−ブチル基;及びベンゾル基等、以下同様。)
第19製造法
原料化合物(128)は,化合物(125)とケトン化合物(126)との付加反応を行った後、脱保護を行うことで合成できる。
化合物(125)と(126)との付加反応は,化合物(125)を第1製造法に記載の不活性な溶媒中,冷却下乃至加熱下,等量から過剰量の塩基(例えばn−ブチルリチウム,水素化ナトリウム及び水酸化カリウム等)で処理し,次いで等量から過剰量のカルボニル化合物(126)を加え,冷却下乃至加熱下攪拌しながら行われる。
メタンスルホンアミド体(125)は,グリーン(Greene)及びウッツ(Wuts)著,「Protective Groups in Organic Synthesis(第2版)」に記載のアミノ基をスルホンアミド化により保護する方法を用いることで合成できる。
第20製造法
原料化合物(130)は,アミド化合物(129)の還元反応により合成できる。
本反応は,等量から過剰量の還元剤(例えば水素化リチウムアルミニウム及びジボラン等)存在下,アミド化合物(129)を第1製造法に記載の不活性な溶媒中,冷却下乃至加熱下攪拌しながら行われる。
第21製造法
原料化合物(132)は,ニトリル化合物(131)の還元反応により合成できる。
本反応は,等量から過剰量の還元剤(例えば水素化リチウムアルミニウム,水素化アルミニウム及び水素化トリメトキシアルミニウムリチウム等)存在下,ニトリル化合物(131)を第1製造法に記載の不活性な溶媒中,冷却下乃至加熱下攪拌しながら行われる。また,水素雰囲気下及びアンモニア存在下,第1製造法に記載の不活性な溶媒中,冷却下乃至加熱下及び常圧乃至加圧下,ラネーニッケル等の金属触媒を用いて接触還元することによっても行われる。
第22製造法
原料化合物(134)は,一般式(33)で表されるカルボニル化合物をKnoevenagel反応に付すことにより合成できる。
本反応は,化合物(33)と等量から過剰量のマロン酸(133)とを,塩基(例えばアンモニア及びピペリジン等)存在下,第1製造法に記載の不活性な溶媒中,冷却下乃至加熱下攪拌しながら行われる。
第23製造法
原料化合物(136)は,一般式(135)で表されるアルコールを光延反応に付すことにより合成できる。
本反応は,化合物(135)と(106)とを,等量から過剰量のトリフェニルホスフィン及びアゾジカルボン酸ジエチル存在下,第1製造法に記載の不活性な溶媒中,冷却下乃至加熱下攪拌しながら行われる。
以下、反応中心部のみ記載する。
第24製造法
原料化合物(140)は,一般式(137)で表されるアミンの選択的保護及び脱保護により合成できる。
例えば,化合物(137)と等量のベンズアルデヒドとを,第1製造法に記載の不活性な溶媒中,冷却下乃至加熱下攪拌することにより,1級アミンをベンジリデンで保護した後,等量のジ−tert−ブチルジカルボナートで処理し,2級アミンをカルバマートとして保護する。次いで,ベンジリデンアミンの加水分解により脱保護を行うことで,2級アミンが選択的に保護された化合物(140)を合成できる。
(上記式中の記号は以下の意味を示す。
P1a=N−:イミン誘導体として保護されたアミノ基、以下同様。)
このようにして製造された本発明化合物又は原料化合物は遊離のまま,あるいはその塩として単離される。当該化合物の塩は遊離の塩基である本発明化合物に通常の造塩反応を付すことにより製造できる。
また本発明化合物又はその塩は,その水和物,その溶媒和物,あるいは結晶多形の物質として単離精製される。単離精製は,抽出,濃縮,留去,結晶化,濾過,再結晶及び各種クロマトグラフィー等の通常の化学操作を適用して行われる。
各種の異性体は,適当な原料化合物を選択することにより,あるいは異性体間の物質的性質の差を利用して分離することができる。例えば,光学異性体は,適当な原料を選択することにより,あるいはラセミ化合物のラセミ分割法(例えば,一般的な光学活性な酸とのジアステレオマー塩に導き光学分割する方法等)により立体化学的に純粋な異性体を得ることができる。
以下,実施例に基づき本発明を更に詳細に説明する。本発明化合物は下記実施例に記載の化合物に限定されるものではない。また原料化合物の製法を参考例に示す。なお,参考例化合物及び実施例化合物の構造式と物理化学的性状を以下表4から40に示す。表中の記号は以下の意味を有する。
Rf.:参考例番号;Ex.:実施例番号;Structure:構造式;Salt:付加塩;Data:物理化学的性状(FA:質量分析値FAB−MS(M+1);EI:質量分析値EI−MS(M+);N:NMR(DMSO−d6,TMS内部標準)の特徴的ピークδppm);NO.:化合物番号;Me:メチル;Et:エチル;Pr:プロピル;iPr:イソプロピル;Bn:ベンジル;Ac:アセチル;Boc:tert−ブトキシカルボニル;Py:ピリジン;Az:アゼチジン;Pyrroli:ピロリジン;Pipe:ピペリジン;Pipera:ピペラジン;Mo:モルホリン;Th:チオフェン;IM:イミダゾール;Bu:ブチル;Ph:フェニル;2−FPh:2−フルオロフェニル;3−FPh:3−フルオロフェニル;4−FPh:4−フルオロフェニル;2,4−diFPh:2,4−ジフルオロフェニル;2−MeOPh:2−メトキシフェニル;3−MeOPh:3−メトキシフェニル;4−MeOPh:4−メトキシフェニル;2−CNPh:2−シアノフェニル;3−CNPh:3−シアノフェニル;4−CNPh:4−シアノフェニル;3−H2NCOPh:3−(アミノカルボニル)フェニル;4−H2NCOPh:4−(アミノカルボニル)フェニル;4−MeNHCOPh:4−[(メチルアミノ)カルボニル]フェニル;4−AcNHPh:4−(アセチルアミノ)フェニル;3−HOPh:3−ヒドロキシフェニル;4−HOPh:4−ヒドロキシフェニル;3−CHOPh:3−ホルミルフェニル;4−CHOPh:4−ホルミルフェニル;2,4−diCF3Ph:2,4−ジ(トリフルオロメチル)フェニル;2,4−diiPrPh:2,4−ジイソプロピルフェニル;4−(1−Boc−Pipe−4−yloxy)Ph:4−[1−(tert−ブトキシカルボニル)ピペリジン−4−イルオキシ]フェニル;3−(1−Me−Pipe−4−yloxy)Ph:3−(1−メチルピペリジン−4−イルオキシ)フェニル;4−(1−Me−Pipe−4−yloxy)Ph:4−(1−メチルピペリジン−4−イルオキシ)フェニル;3−(1−Me−Pipe−3−yloxy)Ph:3−(1−メチルピペリジン−3−イルオキシ)フェニル;4−(1−Me−Pipe−3−yloxy)Ph:4−(1−メチルピペリジン−3−イルオキシ)フェニル;4−(1−Me−Pyrroli−3−yloxy)Ph:4−(1−メチルピロリジン−3−イルオキシ)フェニル;4−CN−3−(Pipe−4−yloxy)Ph:4−シアノ−3−(ピペリジン−4−イルオキシ)フェニル;cPr:シクロプロピル;cHex:シクロヘキシル;cOct:シクロオクチル;fum:フマル酸塩;HCl:塩酸塩;free:フリー体
参考例1
ピペリジン−4−イル酢酸エチル塩酸塩6.63gをアセトニトリル60mlに懸濁し,炭酸カリウム13.24gを加えて室温で1時間攪拌した後,シンナミルブロミド7.55gを加えて室温で30時間攪拌した。反応液をEtOAcで希釈し飽和炭酸水素ナトリウム水溶液で洗浄した後,有機層を無水硫酸ナトリウムで乾燥した。減圧下に溶媒を留去して得られた残渣をシリカゲルカラムクロマトグラフィー(クロロホルム:メタノール=97:3)で精製し,無色油状の{1−[(2E)−3−フェニルプロパ−2−エン−1−イル]ピペリジン−4−イル}酢酸エチル7.20gを得た。
参考例1と同様の方法により,参考例2から6,43から46,実施例119から131及び実施例143から148の化合物を得た。
参考例7
{1−[(2E)−3−フェニルプロパ−2−エン−1−イル]ピペリジン−4−イル}酢酸エチル6.28gをエタノール100mlに溶解し,1M水酸化ナトリウム水溶液50mlを加え,室温で23時間攪拌した。反応液を1M塩酸水溶液で中和した後,減圧下に溶媒を留去し,得られた残渣にクロロホルム:メタノール=7:3混合液150mlを加え,室温で30分間攪拌した。析出した塩化ナトリウムを濾去した後,減圧下に溶媒を留去して得られた残渣をアセトンで洗浄し,無色固体の{1−[(2E)−3−フェニルプロパ−2−エン−1−イル]ピペリジン−4−イル}酢酸4.22gを得た。
参考例7と同様の方法により,参考例8から10,47,48,61から64及び実施例149から152の化合物を得た。
参考例11
[1−(tert−ブトキシカルボニル)ピペリジン−4−イル]酢酸26.91gをDMF350mlに溶解し,N−エチル−N’−3−ジメチルアミノプロピルカルボジイミド塩酸塩21.19g及び1−ヒドロキシベンゾトリアゾール14.94gを加えて氷冷下30分間攪拌した後,ベンズヒドリルアミン19.06ml及びTEA15.4mlを加え,室温で4時間攪拌した。反応液をEtOAcで希釈し,10%クエン酸水溶液,飽和炭酸水素ナトリウム水溶液及び飽和食塩水で洗浄した。有機層を無水硫酸ナトリウムで乾燥し,減圧下に溶媒を留去した後,残渣をEtOAcより再結晶し,無色固体の4−[2−(ベンズヒドリルアミノ)−2−オキソエチル]ピペリジン−1−カルボン酸tert−ブチル37.70gを得た。
参考例11と同様の方法により,参考例12,13,59,60,65から70,実施例132から142及び実施例153から174の化合物を得た。
参考例14
[1−(tert−ブトキシカルボニル)ピペリジン−4−イル]酢酸1.28g,TEA0.74ml及びTHF12mlの混液に,氷−メタノール浴冷却下クロロギ酸イソブチル0.68mlを加え30分間攪拌した後に,(±)−[(3−フルオロフェニル)(フェニル)メチル]アミン0.97g及びTHF4mlの混液を滴下し,室温まで徐々に昇温して計5時間攪拌した。反応液にEtOAc80mlを加え,10%クエン酸水溶液40ml,水40ml,飽和炭酸水素ナトリウム水溶液40ml,水40ml,飽和食塩水40mlで順次洗浄後,有機層を無水硫酸ナトリウムで乾燥し減圧下に溶媒を留去した。残渣をシリカゲルカラムクロマトグラフィー(EtOAc:ヘキサン=1:5→1:3)で精製し,無晶状粉末の(±)−4−(2−{[(3−フルオロフェニル)(フェニル)メチル]アミノ}−2−オキソエチル)ピペリジン−1−カルボン酸tert−ブチル2.12gを得た。
参考例14と同様の方法により,参考例15及び実施例175の化合物を得た。
参考例16
4−(アミノメチル)ピペリジン−1−カルボン酸tert−ブチル0.32g,TEA0.28ml及びTHF6mlの混液に,氷冷下ジフェニルアセチルクロリド0.46gを加え氷冷下1時間,室温で3時間攪拌した。反応液にEtOAc50mlを加え,飽和炭酸水素ナトリウム水溶液25ml,水25ml,飽和食塩水25mlで順次洗浄後,有機層を無水硫酸ナトリウムで乾燥し溶媒を減圧留去した。残渣をシリカゲルカラムクロマトグラフィー(EtOAc:ヘキサン=1:3→1:2)で精製し,無晶状粉末の4−{[(ジフェニルアセチル)アミノ]メチル}ピペリジン−1−カルボン酸tert−ブチル0.37gを得た。
参考例16と同様の方法により,実施例176及び177の化合物を得た。
参考例17
1−(tert−ブトキシカルボニル)−4−メチルピペリジン−4−カルボン酸365mg,TEA0.25ml及びTol5mlの混液に,ジフェニルリン酸アジド0.39mlを加え室温で4時間,80℃で3時間攪拌した。反応液を放冷し,(ジフェニルメチル)アミン0.31mlを室温で加え,室温で3時間攪拌した。反応液にEtOAc50mlを加え,10%クエン酸水溶液25ml,水25ml,飽和炭酸水素ナトリウム水溶液25ml,水25ml,飽和食塩水25mlで順次洗浄後,有機層を無水硫酸ナトリウムで乾燥し溶媒を減圧留去した。残渣をシリカゲルカラムクロマトグラフィー(EtOAc:ヘキサン=1:2→1:1)で精製し,無晶状粉末の4−({[(ジフェニルメチル)アミノ]カルボニル}アミノ)−4−メチルピペリジン−1−カルボン酸tert−ブチル0.61gを得た。
以下,参考例17と同様の方法により実施例178の化合物を得た。
参考例18
4−[2−(ベンズヒドリルアミノ)−2−オキソエチル]ピペリジン−1−カルボン酸tert−ブチル37.70gをEtOAc140mlに溶解し,氷冷下,4M塩酸−EtOAc420mlを加え,室温で2時間攪拌した。析出した固体を濾取した後,EtOAcで洗浄し,無色固体のN−ベンズヒドリル−2−ピペリジン−4−イルアセトアミド塩酸塩31.83gを得た。
参考例18と同様の方法により,参考例19,20,57,58,71から77,及び実施例179から223の化合物を得た。
参考例21
4−ヒドロキシピペリジン−1−カルボン酸tert−ブチル20.13gをDMF200mlに溶解し,tert−ブトキシカリウム11.22gを加え,室温で4時間攪拌した。減圧下に溶媒を留去した後,残渣をDMF300mlに溶解し,4−フルオロベンゾニトリル12.11gを加え,60℃で24時間撹拌した。減圧下に溶媒を留去した後,残渣をEtOAcで希釈し,水及び飽和食塩水で洗浄した。有機層を無水硫酸ナトリウムで乾燥した後,減圧下に溶媒を留去し,薄茶色油状の4−(4−シアノフェノキシ)ピペリジン−1−カルボン酸tert−ブチル27.00gを得た。
参考例21と同様の方法により,参考例22から30及び82から86の化合物を得た。
参考例31
4−(4−シアノフェノキシ)ピペリジン−1−カルボン酸tert−ブチル26.99gをTol130mlに溶解した後,−78℃で攪拌下,反応液の温度が−60℃を超えないように水素化ジイソブチルアルミニウム(1.0mol/l Tol溶液)を滴下した。−78℃で3時間攪拌した後,同温度で飽和塩化アンモニウム水溶液80mlを滴下し,ゆっくりと室温まで昇温した。反応液をジエチルエーテル500mlで希釈し,無水硫酸マグネシウムを加え,室温で16時間攪拌した。不溶物を濾去した後,減圧下に溶媒を留去し,薄茶色油状の4−(4−ホルミルフェノキシ)ピペリジン−1−カルボン酸tert−ブチル13.14gを得た。
参考例31と同様の方法により,参考例32から39及び87から90の化合物を得た。
参考例40
4−ブロモ−3−メチルベンゾニトリル5.87gをTHF140ml及びヘキサン40mlの混合溶媒に溶解し,−100℃で撹拌下n−ブチルリチウム(1.59Mヘキサン溶液)18.8mlを滴下した。5分後,DMF12mlを加え−40℃に昇温した。さらに2時間後,反応液に塩化アンモニウム水溶液を加え,室温まで昇温した。EtOAcで希釈し飽和炭酸水素ナトリウム水溶液で洗浄した後,有機層を無水硫酸ナトリウムで乾燥した。減圧下に溶媒を留去して得られた残渣をシリカゲルカラムクロマトグラフィー(EtOAc:ヘキサン=1:2)で精製し,無色個体の4−ホルミル−3−メチルベンゾニトリル3.70gを得た。
参考例40と同様の方法により,参考例41の化合物を得た。
参考例42
ピペリジン−4−イル酢酸エチル塩酸塩8.93gを2−プロパノール400mlに溶解し,臭化(2−クロロエチル)トリフェニルホスホニウム17.45g,炭酸カリウム29.71g,よう化テトラ−n−ブチルアンモニウム3.18g及び4−(4−ホルミルフェノキシ)ピペリジン−1−カルボン酸tert−ブチル13.13gを加え,加熱還流下,24時間攪拌した後,室温まで冷却した。減圧下に溶媒を留去した後,得られた残渣をEtOAcで希釈し,水及び飽和食塩水で洗浄した。有機層を無水硫酸ナトリウムで乾燥した後,減圧下に溶媒を留去して得られた残渣をシリカゲルカラムクロマトグラフィー(クロロホルム:メタノール:濃アンモニア水=98:2:0.2)で精製し,薄茶色油状の4−(4−{(1E)−3−[4−(2−エトキシ−2−オキソエチル)ピペリジン−1−イル]プロパ−1−エン−1−イル}フェノキシ)ピペリジン−1−カルボン酸tert−ブチル10.33gを得た。
参考例42と同様の方法により,参考例91,及び実施例224から322の化合物を得た。
参考例49
N−(4−ベンゾイルフェニル)アセトアミド1.29gをピリジン15mlに溶解し,塩酸ヒドロキシルアミン0.41gを加え,80℃で4時間攪拌した。反応液を室温まで冷却した後,減圧下に溶媒を留去し,残渣にEtOAcを加え,飽和食塩水で洗浄した。有機層を無水硫酸ナトリウムで乾燥した後,減圧下に溶媒を留去して得られた残渣をシリカゲルカラムクロマトグラフィー(EtOAc:ヘキサン=50:50)で精製し,オキシム化合物1.29gを得た。このオキシム化合物0.99gを酢酸25mlに溶解し,亜鉛(粉末)1.02gを加え,室温で96時間攪拌した。不溶物を濾去した後,減圧下に溶媒を留去し,残渣にEtOAcを加え,飽和炭酸水素ナトリウム水溶液及び飽和食塩水で洗浄した。有機層を無水硫酸ナトリウムで乾燥した後,減圧下に溶媒を留去して得られた残渣をシリカゲルカラムクロマトグラフィー(クロロホルム:メタノール:濃アンモニア水=95:5:0.5)で精製し,薄茶色固体の(±)−N−{4−[アミノ(フェニル)メチル]フェニル}アセトアミド0.52gを得た。
参考例49と同様の方法により,参考例50の化合物を合成した。
参考例51
(±)−フェニル(3−チエニル)メタノール1.95gをチオニルクロリド20mlに溶解し,50℃で1.5時間攪拌した。反応液を室温まで冷却した後,減圧下に溶媒を留去し,残渣にDMF25ml及びアジ化ナトリウム1.65gを加え,80℃で14時間攪拌した。反応液を室温まで冷却した後水で希釈し,ジエチルエーテルで抽出した。有機層を飽和食塩水で洗浄し,無水硫酸ナトリウムで乾燥した後,減圧下に溶媒を留去して,アジド化合物1.71gを得た。このアジド化合物1.71gをTHF20mlに溶解し,氷冷下,水素化リチウムアルミニウム0.45gを加え,2時間攪拌した。残存している水素化リチウムアルミニウムを1M水酸化ナトリウム水溶液で処理した後,不溶物を濾去した。濾液をEtOAcで希釈した後,氷冷下,4M塩酸−EtOAc10mlを加え,同温度で30分間攪拌した。減圧下に溶媒を留去して得られた残渣をメタノール−EtOAc混合液で洗浄し,無色固体の(±)−1−フェニル−1−(3−チエニル)メチルアミン塩酸塩1.26gを得た。
参考例51と同様の方法により,参考例52及び53の化合物を合成した。
参考例54
(±)−4−[ヒドロキシ(フェニル)メチル]ベンゾニトリル3.29gをチオニルクロリド35mlに溶解し,50℃で2時間攪拌した。反応液を室温まで冷却した後,滅圧下に溶媒を留去し,残渣にDMF40ml及びアジ化ナトリウム2.56gを加え,80℃で16時間攪拌した。反応液を室温まで冷却した後,残渣に水を加え,ジエチルエーテルで抽出した。有機層を飽和食塩水で洗浄し,無水硫酸ナトリウムで乾燥した。滅圧下に溶媒を留去して得られた残渣をシリカゲルカラムクロマトグラフィー(ヘキサン:EtOAc=95:5)で精製し,アジド化合物1.19gを得た。このアジド化合物1.19gをTHF15mlに溶解し,トリフェニルホスフィン2.00gを加え,50℃で30分間攪拌した後,水0.14gを加え,50℃で2時間攪拌した。反応液を室温まで冷却した後,減圧下に溶媒を留去し,残渣にジエチルエーテル50mlを加え,室温で30分間攪拌した。不溶物を濾去した後,減圧下に溶媒を留去して得られた残渣をEtOAc20mlに溶解した。氷冷下,4M塩酸−EtOAc5mlを加え,20分間攪拌した後,析出した固体を濾取し,無色固体の(±)−4−[アミノ(フェニル)メチル]ベンゾニトリル塩酸塩0.27gを得た。
参考例55
(±)−[3−(ベンジルオキシ)フェニル](フェニル)メチルアミン1.98gをTFA20mlに溶解し,ペンタメチルベンゼン296mgを加え,室温で14時間攪拌した。減圧下に溶媒を留去した後,残渣をEtOAcで希釈し,飽和炭酸水素ナトリウム水溶液及び飽和食塩水で洗浄した。有機層を無水硫酸ナトリウムで乾燥した後,無水硫酸ナトリウムを濾去した濾液に4M塩酸−EtOAc10mlを加え,室温で20分間攪拌した。減圧下に溶媒を留去して得られた残渣をEtOAcで洗浄し,無色固体の(±)−3−[アミノ(フェニル)メチル]フェノール塩酸塩1.35gを得た。
参考例55と同様の方法により,参考例56の化合物を合成した。
参考例78
1−(tert−ブトキシカルボニル)ピペリジン−4−カルボン酸及び1,1−ビス(4−フルオロフェニル)メタンアミンを用い,参考例11及び参考例18と同様の方法を続けて行うことにより,参考例78の化合物を得た。
参考例78と同様の方法により,参考例79から81の化合物を合成した。
参考例92
4−{4−[(1E)−3−エトキシ−3−オキソプロパ−1−エン−1−イル]フェノキシ}ピペリジン−1−カルボン酸tert−ブチル8.2g,THF44mlの溶液に,−78℃撹拌下水素化ジイソブチルアルミニウム1.0MTol溶液51mlを内温が−60℃を越えない範囲で徐々に滴下後,2時間攪拌した。反応液に飽和塩化アンモニウム水溶液を加え室温に昇温し,EtOAcを加え,5%硫酸水素カリウム溶液で順次洗浄後,有機層を無水硫酸ナトリウムで乾燥し減圧下に溶媒を留去し,淡黄色粉末の4−{4−[(1E)−3−ヒドロキシプロパ−1−エン−1−イル]フェノキシ}ピペリジン−1−カルボン酸tert−ブチル7.2gを得た。
参考例92と同様の方法により,参考例93から95の化合物を合成した。
参考例96
4−{4−[(1E)−3−ヒドロキシプロパ−1−エン−1−イル]フェノキシ}ピペリジン−1−カルボン酸tert−ブチル2.00g,ジクロロメタン50ml溶液に,室温撹拌下酸化マンガン(IV)5.00gを加え一晩攪拌した。セライトを用いて濾過し減圧下に溶媒を留去し,淡黄色粉末の4−{4−[(1E)−3−オキソプロパ−1−エン−1−イル]フェノキシ}ピペリジン−1−カルボン酸tert−ブチル2.00gを得た。
参考例96と同様の方法により,参考例97から100の化合物を合成した。
参考例101
参考例83の化合物を用い,参考例92及び参考例96と同様の方法を続けて行うことにより参考例101の化合物を得た。
参考例102
水素化ナトリウム1.4g,THF50mlの懸濁液に,氷冷下ジエチルホスホノ酢酸エチル6.3mlを加え30分間攪拌した後に,[4−(4−ホルミルフェノキシ)ピペリジン−1−カルボン酸tert−ブチル8.1g,THF30ml溶液を滴下し,室温まで徐々に昇温して一晩攪拌した。反応液に飽和塩化アンモニウム水溶液を加え,EtOAcを用いて抽出後,有機層を無水硫酸ナトリウムで乾燥し減圧下に溶媒を留去した。残渣をシリカゲルカラムクロマトグラフィー(EtOAc:ヘキサン=1:6→1:4)で精製し,無色油状の4−{4−[(1E)−3−エトキシ−3−オキソプロパ−1−エン−1−イル]フェノキシ}ピペリジン−1−カルボン酸tert−ブチル8.23gを得た。
参考例102と同様の方法により,参考例103から104の化合物を合成した。
参考例105
4−フルオロサリチル酸468mg,DMF10mlの溶液に,室温撹拌下炭酸カリウム1.25g,臭化ベンジル0.82mlを順次加え2時間30分撹拌した。反応液に水を加え,EtOAcを用いて抽出後,有機層を無水硫酸ナトリウムで乾燥し減圧下に溶媒を留去し,淡黄色油状の残留物を得た。得られた残留物はそのまま次反応に用いた。
残留物のメタノール9ml,THF9ml混液に,室温撹拌下1M水酸化ナトリウム水溶液9mlを加え一晩撹拌した。反応液を1M塩酸水溶液にて酸性とし,析出した結晶をろ取し,無色結晶の2−(ベンジルオキシ)−4−フルオロ安息香酸698mgを得た。
参考例106
2−(ベンジルオキシ)−4−フルオロ安息香酸698mg,DMF7mlの溶液に,室温撹拌下1−ヒドロキシベンゾトリアゾール576mg,1−エチル3−(3−ジメチルアミノプロピル)カルボジイミド塩酸塩1.1gを順次加え30分間攪拌した後に,炭酸アンモニウム700mgを加え,4時間攪拌した。反応液に飽和炭酸水素ナトリウム水溶液を適量加え,析出した結晶をろ取し,無色結晶の2−(ベンジルオキシ)−4−フルオロベンズアミド640mgを得た。
参考例107
2−(ベンジルオキシ)−4−フルオロベンズアミド640mg,THF20mlの溶液に,室温撹拌下水素化リチウムアルミニウム200mgを徐々に加えた後に,1時間加熱還流した。室温まで冷却後,硫酸ナトリウム十水和物を適量加え,2時間攪拌した。セライトを用いて濾過し減圧下に溶媒を留去し,淡黄色油状の[2−(ベンジルオキシ)−4−フルオロベンジル]アミン600mgを得た。
参考例108
2−フルオロベンゾニトリル6.1g,DMF40mlの溶液に,室温下炭酸カリウム17g,4−ヒドロキシアセトアニリド6.2gを順次加えた後に,100℃にて4時間撹拌した。室温まで冷却後,反応液に水を適量加え,析出した結晶をろ取し,無色結晶のN−[4−(2−シアノフェノキシ)フェニル]アセトアミド10gを得た。
参考例109
4−(2−ブロモエチル)安息香酸2.29g,クロロホルム20ml,TEA3.1mlの混液に,ピロリジン0.85gを加え,室温で6時間攪拌した。減圧下で溶媒を留去した後,残渣にメタノール30mlを加え,これに硫酸1.5mlを滴下し,5.5時間加熱還流した。反応液を室温まで冷却し,飽和炭酸ナトリウム水溶液で中和し,減圧下で溶媒を留去した後,EtOAc40mlで抽出し、有機層を飽和食塩水20mlで洗浄した。減圧下で溶媒を留去した後,残渣をシリカゲルカラムクロマトグラフィー(クロロホルム→クロロホルム:メタノール=10:1)で精製し,淡黄色固体の4−(2−ピロリジン−1−イルエチル)安息香酸メチル1.43gを得た。
参考例110
水素化リチウムアルミニウム0.33g,THF10mlの混液に,氷冷下4−(2−ピロリジン−1−イルエチル)安息香酸メチル1.42gTHF10mlの混液を滴下し,室温で2.5時間撹拌した。氷冷下反応液に水0.33ml,15%水酸化ナトリウム水溶液0.33ml,水0.99mlを順次滴下し,室温で1時間攪拌した。不溶物をセライト濾過した後,減圧下で溶媒を留去した。残渣にクロロホルム10ml,酸化マンガン(IV)1.0gを加え加熱還流した。2時間後反応溶液を薄層クロマトグラフィーでチェックし,原料が残っていたため酸化マンガン(IV)1.0gを加え加熱還流した。この操作を原料が消失するまで繰り返し計6時間加熱還流した。反応終了後,不溶物をセライト濾過し,減圧下で溶媒を留去した。残渣をシリカゲルカラムクロマトグラフィー(クロロホルム→クロロホルム:メタノール=10:1)で精製し,茶色油状の4−(2−ピロリジン−1−イルエチル)ベンズアルデヒド0.69gを得た。
参考例111
3−(ピペリジン−4−イル)プロピオン酸エチル塩酸塩443mg,4−[(1E)−3−クロロプロパ−1−エン−1−イル]ベンゾニトリル428mg、炭酸カリウム690mg,ヨウ化ナリウウム298mgのDMF10ml混合溶液を60℃にて30分間加熱攪拌した。反応液に水を加えEtOAcで抽出し、水、飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し溶媒を減圧留去した。残渣をシリカゲルカラムクロマトグラフィー(クロロホルム:メタノール:濃アンモニア水=50:1:0.1)で精製し、油状物の3−{1−[(2E)−3−(4−シアノフェニル)プロパ−2−エン−1−イル]ピペリジン−4−イル}プロピオン酸エチル172mgを得た。
参考例111と同様の方法により,参考例112,113,及び実施例354の化合物を合成した。
参考例114
N−(4−フルオロフェニル)グリシンエチル394mg,35%ホルムアルデヒド水溶液3ml,ギ酸3mlの混合溶液を1時間加熱還流した。反応溶液に飽和炭酸水素ナトリウム水溶液を加えてEtOAcで抽出し、飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥した。溶媒を減圧留去することにより油状のN−(4−フルオロフェニル)−N−メチルグリシンエチル397mgを得た。
参考例115
ビス(4−フルオロフェニル)アミン615mgとブロモ酢酸エチルエステル1mlを160℃で6時間加熱攪拌した。反応混合物をシリカゲルカラムクロマトグラフィー(ヘキサン:EtOAc=5:1)で精製することにより油状のN,N−ビス(4−フルオロフェニル)グリシンエチル790mgを得た。
参考例116
N,N−ビス(4−フルオロフェニル)グリシン342mg,1−トリフルオロアセチルピペリジン−4−アミン塩酸塩350mg,1−エチル3−(3−ジメチルアミノプロピル)カルボジイミド塩酸塩346mg,1−ヒドロキシベンゾトリアゾール203mg,TEA0.209mlのDMF5ml混合溶液を室温下3時間攪拌した。反応溶液に水を加えてEtOAcで抽出し、1M塩酸、飽和炭酸水素ナトリウム水溶液、水、飽和食塩水の順で洗浄した。無水硫酸ナトリウムで乾燥し、溶媒を減圧留去後、残渣をメタノール10mlに溶解し、1M水酸化ナトリウム水溶液5mlを加えて室温下3時間攪拌した。メタノールを減圧留去後、EtOAcで抽出し、水、飽和食塩水で洗浄した。無水硫酸ナトリウムで乾燥し、溶媒を減圧留去することによりアモルファスの2−[ビス(4−フルオロフェニル)アミノ]−N−(ピペリジン−4−イル)アセトアミド417mgを得た。
参考例117
2−(ピペラジン−1−イル)酢酸エチルエステル310mg,4−{4−[(1E)−3−オキソプロパ−1−エン−1−イル]フェノキシ}ピペリジン−1−カルボン酸tert−ブチル497mg,酢酸0.45mlのDCE10ml混合溶液を室温下15分間攪拌し、さらに水素化トリアセトキシホウ素ナトリウム636mgを加えて2時間撹拌した。反応溶液に飽和炭酸水素ナトリウム水溶液を加えてクロロホルムで抽出し、無水硫酸ナトリウムで乾燥した。溶媒を減圧留去後、残渣をシリカゲルカラムクロマトグラフィー(クロロホルム:メタノール:濃アンモニア水=50:1:0.1)で精製することにより油状物の4−(4−[(1E)−3−[4−(2−エトキシ−2−オキソエチル)ピペラジン−1−イル]プロパ−1−エン−1−イル]フェノキシ)ピペリジン−1−カルボン酸tert−ブチル718mgを得た。
参考例117と同様の方法により,参考例118から119の化合物を合成した。
参考例120
[ビス(4−フルオロフェニル)メチル]アミン768mg,TEA1.25mlのDCE15ml混合溶液に氷冷下、メタンスルホニルクロリド0.278mlを加えて氷冷から室温下で3時間攪拌した。反応溶液に水を加えてクロロホルムで抽出し、無水硫酸ナトリウムで乾燥後、溶媒を減圧留去した。残渣をTHF20mlに溶解し、アルゴン雰囲気下、−78℃に冷却し、n−ブチルリチウム(1.56Mヘキサン溶液)4.7mlを加えて同温で1時間攪拌した。反応溶液にN−ベンジル−4−ピペリドン795mgを加えてさらに1時間攪拌した。反応溶液を0℃まで昇温し、飽和塩化アンモニウム水溶液を加えた後、THFを減圧留去した。水層をクロロホルムで抽出し、無水硫酸ナトリウムで乾燥後、溶媒を減圧留去して残渣をシリカケルカラムクロマトグラフィー(クロロホルム:メタノール:濃アンモニア水=20:1:0.1)で精製することにより白色固体の1−(1−ベンジル−4−ヒドロキシピペリジン−4−イル)−N−[ビス(4−フルオロフェニル)メチル]メタンスルホナミド504mgを得た。
参考例121
1−(1−ベンジル−4−ヒドロキシピペリジン−4−イル)−N−[ビス(4−フルオロフェニル)メチル]メタンスルホンアミド450mgのエタノール10ml溶液に10%パラジウム炭素100mgを加えて水素雰囲気下、常圧、室温で4日間攪拌した。不溶物をろ過して除去し、溶媒を減圧留去後、残渣をシリカゲルカラムクロマトグラフィー(クロロホルム:メタノール:濃アンモニア水=5:1:0.1)で精製することにより無色アモルファスの1−(4−ヒドロキシピペリジン−4−イル)−N−[ビス(4−フルオロフェニル)メチル]メタンスルホンアミド127mgを得た。
参考例122
4−{2−[(4−フルオロフェニル)アミノ]−2−オキソエチル}ピペリジン−1−カルボン酸tert−ブチル672mgのDMF10ml溶液に室温下、60%油性水素化ナトリウム120mgを加えて30分間攪拌した。反応溶液に4−ブロモメチル安息香酸メチル687mgを加えてさらに3時間攪拌した。反応溶液に水を加えてEtOAcで抽出し、水、飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥した。溶媒を減圧留去後、残渣をシリカゲルカラムクロマトグラフィー(クロロホルム:EtOAc=4:1)で精製することにより油状物の4−{2−[N−(4−フルオロフェニル)−N−(4−メトキシカルボニルベンジル)アミノ]−2−オキソエチル}ピペリジン−1−カルボン酸tert−ブチル940mgを得た。
参考例123
[1−(tert−ブトキシカルボニル)ピペリジン−4−イル]酢酸及び4−アミノ安息香酸エチルを用い,参考例11及び参考例122と同様の方法を続けて行うことにより,参考例123の化合物を得た。
参考例124
4−{2−[N−(4−フルオロフェニル)−N−(4−ヒドロキシメチルベンジル)アミノ]−2−オキソエチル}ピペリジン−1−カルボン酸t−ブチル570mgのDCE10ml溶液に室温下、TFA5mlを加えて一晩攪拌した。反応溶液に飽和炭酸水素ナトリウム水溶液を加えて中和した後、クロロホルムで抽出し、無水硫酸ナトリウムで乾燥後、溶媒を減圧留去することにより無色アモルファスのN−[4−(ヒドロキシメチル)ベンジル]−N−(4−フルオロフェニル)−2−(ピペリジン−4−イル)アセトアミド450mgを得た。
参考例125
2−フルオロ−4−メトキシベンズアルデヒド5g,マロン酸6.7gのピリジン70ml溶液にピペリジンを5,6滴加えて6時間加熱還流した。溶媒を減圧留去し、残渣を希アンモニア水に溶解した後、EtOAcで洗浄した。水層を1M塩酸で中和して析出物をろ取し、水で洗浄後、減圧乾燥することにより白色結晶の(2E)−3−(2−フルオロ−4−メトキシフェニル)アクリル酸2.1gを得た。
参考例126
(2E)−3−(2−フルオロ−4−メトキシフェニル)アクリル酸2.1gのジクロロメタン40ml溶液にアルゴン雰囲気下、−78℃で1M三臭化ホウ素ジクロロメタン溶液40mlを加えて室温下一晩攪拌した。反応溶液を氷水に注ぎ、析出物をろ取し、水、ジクロロメタンで洗浄後、減圧乾燥することにより無色結晶の(2E)−3−(2−フルオロ−4−ヒドロキシフェニル)アクリル酸1.8gを得た。
参考例127
(2E)−3−(2−フルオロ−4−ヒドロキシフェニル)アクリル酸1.8gのエタノール100ml溶液にチオニルクロリド10mlを滴下して加え、2時間加熱還流した。溶媒を減圧留去後、残渣をEtOAcに溶解し、水、飽和食塩水で洗浄した。無水硫酸ナトリウムで乾燥後、溶媒を減圧留去することにより無色結晶の(2E)−3−(2−フルオロ−4−ヒドロキシフェニル)アクリル酸エチル2.0gを得た。
参考例128
(2E)−3−(2−フルオロ−4−ヒドロキシフェニル)アクリル酸エチル1.05gのTHF50ml溶液に氷冷下、4−ヒドロキシピペリジン−1−カルボン酸tert−ブチル2.01g,トリフェニルフォスフィン2.62g,アゾジカルボン酸ジエチル1.57mlを加えて室温下4時間攪拌した。溶媒を減圧留去し、残渣をEtOAcに溶解して水、飽和食塩水で洗浄後、溶媒を減圧留去した。残渣をシリカゲルカラムクロマトグラフィー(ヘキサン:EtOAc=3:1で精製することにより無色油状物の4−{3−フルオロ−4−[(1E)−3−エトキシ−3−オキソプロパ−1−エン−1−イル]フェノキシ}ピペリジン−1−カルボン酸tert−ブチル2.0gを得た。
参考例129
4−{[{[1−(tert−ブトキシカルボニル)ピペリジン−4−イル]アセチル}(4−フルオロフェニル)アミノ]メチル}安息香酸600mgのTHF10ml溶液に1,1’−カルボニルジイミダゾール415mgを加えて室温下3時間攪拌した。反応溶液に水素化ホウ素ナトリウム486mg,水数滴を加えてさらに2時間撹拌した。反応溶液に氷冷下、1M塩酸を加えて30分間攪拌した後、EtOAcで抽出し、1M水酸化ナトリウム水溶液、水、飽和食塩水で洗浄した。無水硫酸ナトリウムで乾燥して溶媒を減圧留去することにより無色アモルファスの4−(2−{(4−フルオロフェニル)[4−(ヒドロキシメチル)ベンジル]アミノ}−2−オキソエチル)ピペリジン−1−カルボン酸tert−ブチル570mgを得た。
参考例130
シクロプロピルアミン2.28gをTHF20mlに溶解し,氷冷下,4−フルオロベンジルブロミド1.89gを加え,室温で3時間攪拌した。減圧下に溶媒を留去した後,残渣をEtOAc50mlに溶解し,飽和炭酸水素ナトリウム水溶液50ml及び飽和食塩水50mlで洗浄した。有機層を無水硫酸ナトリウムで乾燥した後,減圧下に溶媒を留去した。残渣をEtOAc10mlに溶解し,氷冷下,4M塩酸−EtOAc10mlを加え,同温度で30分間攪拌した。減圧下に溶媒を留去して得られた残渣をEtOAcで洗浄し,無色固体のN−(4−フルオロフェニル)シクロプロパンアミン塩酸塩1.35gを得た。
参考例131
1,1−ジシクロヘキシルメタンアミン2.36gをTHF25mlに溶解し,ジ−tert−ブチルジカルボナート2.90gを加え,室温で72時間攪拌した。減圧下に溶媒を留去した後,残渣をEtOAc100mlに溶解し,10%クエン酸水溶液100ml,飽和炭酸水素ナトリウム水溶液100ml,飽和食塩水100mlで順次洗浄した。有機層を無水硫酸ナトリウムで乾燥した後,減圧下に溶媒を留去し,無色油状のtert−ブチル(ジシクロヘキシルメチル)カルバマート3.02gを得た。
参考例132
tert−ブチル(ジシクロヘキシルメチル)カルバマート2.90gをTHF30mlに溶解し,氷冷下,水素化リチウムアルミニウム1.12gを少量ずつ加えた後,加熱還流下,15時間攪拌した。氷冷下,残存している水素化リチウムアルミニウムを1M水酸化ナトリウム水溶液で処理し,セライト濾過により不溶物を除去した後,減圧下に溶媒を留去し,無色油状の(ジシクロヘキシルメチル)メチルアミン1.58gを得た。
参考例133
メチルアミン(40%メタノール溶液)20mlに1−(クロロメチル)−2,4−ジフルオロベンゼン2.07gを加え,40℃で17時間攪拌した。減圧下に溶媒を留去した後,残渣をEtOAc100mlに溶解し,飽和炭酸水素ナトリウム水溶液100ml及び飽和食塩水100mlで洗浄した。有機層を無水硫酸ナトリウムで乾燥した後,減圧下に溶媒を留去した。残渣をEtOAc10mlに溶解し,氷冷下,4M塩酸−EtOAc5mlを加え,同温度で30分間攪拌した。減圧下に溶媒を留去して得られた残渣をEtOAcで洗浄し,無色固体のN−(2,4−ジフルオロベンジル)−N−メチルアミン塩酸塩0.35gを得た。
参考例133と同様の方法により,参考例134から135及び実施例355の化合物を合成した。
参考例137
チオニルクロリド20mlにビス(2−フルオロフェニル)メタノール2.02gを少量ずつ加え,50℃で1.5時間攪拌した。減圧下に溶媒を留去し,薄茶色油状の1−[クロロ(2−フルオロフェニル)メチル]−2−フルオロベンゼン2.18gを得た。
参考例137と同様の方法により,参考例136の化合物を合成した。
参考例139
1−[クロロ(2−フルオロフェニル)メチル]−2−フルオロベンゼン1.08gをDMF10mlに溶解し,アジ化ナトリウム0.74gを加え,80℃で24時間攪拌した。反応液を室温まで冷却した後,水50mlを加え,ジエチルエール50mlで抽出した。無水硫酸ナトリウムで乾燥した後,減圧下に溶媒を留去し,薄茶色油状の1−[アジド(2−フルオロフェニル)メチル]−2−フルオロベンゼン0.99gを得た。
参考例139と同様の方法により,参考例138の化合物を合成した。
参考例140
1−[アジド(2−フルオロフェニル)メチル]−2−フルオロベンゼン0.97gをTHF10mlに溶解し,氷冷下,水素化リチウムアルミニウム0.23gを少量ずつ加え,徐々に室温まで温度を上げながら2時間攪拌した。氷冷下,残存している水素化リチウムアルミニウムを1M水酸化ナトリウム水溶液で処理し,セライト濾過により不溶物を除去した後,減圧下に溶媒を留去した。残渣をEtOAc10mlに溶解し,氷冷下,4M塩酸−EtOAc4mlを加え,同温度で15分間攪拌した。減圧下に溶媒を留去して得られた残渣をEtOAc−ヘキサン混合液で洗浄し,無色固体の1,1−ビス(2−フルオロフェニル)メタンアミン塩酸塩0.83gを得た。
参考例140と同様の方法により,参考例141の化合物を合成した。
参考例142
1−{(2E)−3−[4−(ピペリジン−4−イルオキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−アミン1.61gをベンゼン20mlに溶解し,ベンズアルデヒド0.54gを加え,加熱還流下,生成する水を共沸により除去しながら,5時間撹拌した。反応液を室温まで冷却した後,ジ−tert−ブチルジカルボナート1.11gを加え,室温で16時間攪拌した。次いで,1M硫酸水素カリウム水溶液6.6mlを加えて室温で2時間攪拌した後,濃アンモニア水0.88gを加え,室温で1時間攪拌した。クロロホルム30mlで3回抽出した後,有機層を無水硫酸ナトリウムで乾燥し,減圧下に溶媒を留去した。残渣をシリカゲルカラムクロマトグラフィー(クロロホルム:メタノール:濃アンモニア水=90:10:1)で精製し,無色固体の4−{4−[(1E)−3−(4−アミノピペリジン−1−イル)プロパ−1−エン−1−イル]フェノキシ}ピペリジン−1−カルボン酸tert−ブチル1.57gを得た。
参考例11と同様の方法により得られたN−シクロオクチル−2−{1−[(2E)−3−フェニルプロパ−2−エン−1−イル]ピペリジン−4−イル}アセトアミド0.062gをエタノール1mlに溶解し,氷冷下,4M塩酸−EtOAc1mlを加え,同温度で15分間攪拌した。減圧下に溶媒を留去した後,残渣をエタノール−EtOAc混合液より再結晶し,無色固体のN−シクロオクチル−2−{1−[(2E)−3−フェニルプロパ−2−エン−1−イル]ピペリジン−4−イル}アセトアミド塩酸塩0.062gを得た。
実施例1と同様の方法により実施例2の化合物を得た。
実施例1と同様の方法により実施例2の化合物を得た。
参考例3の化合物を用い,参考例7及び実施例1と同様の方法を続けて行うことにより実施例3の化合物を得た。
参考例11と同様の方法により得られた2−{1−[(2E)−3−(4−シアノフェニル)プロパ−2−エン−1−イル]ピペリジン−4−イル}−N−シクロオクチルアセトアミド0.186gをエタノール10mlに溶解し,フマル酸0.055gを加え,室温で1時間攪拌した。減圧下に溶媒を留去した後,残渣をエタノール−EtOAc混合液より再結晶し,無色固体の2−{1−[(2E)−3−(4−シアノフェニル)プロパ−2−エン−1−イル]ピペリジン−4−イル}−N−シクロオクチルアセトアミドフマル酸塩0.139gを得た。
実施例4と同様の方法により,実施例5から49の化合物を得た。
実施例4と同様の方法により,実施例5から49の化合物を得た。
{1−[(2E)−3−フェニルプロパ−2−エン−1−イル]ピペリジン−4−イル}酢酸0.39g,1,1−ジフェニルメタンアミン0.31ml及びDMF5mlの混液に,氷冷下ジフェニルリン酸アジド0.39ml及びTEA0.25mlを加え氷冷下3時間,室温で一夜撹拌した。反応液にEtOAc50mlを加え,10%クエン酸水溶液25ml,水25ml,飽和炭酸水素ナトリウム水溶液25ml,水25ml,飽和食塩水25mlで順次洗浄後,有機層を無水硫酸ナトリウムで乾燥し溶媒を減圧留去した。残留物をシリカゲルカラムクロマトグラフィー(クロロホルム:メタノール:濃アンモニア水=100:1:0.1→50:1:0.1→30:1:0.1)で精製し,N−(ジフェニルメチル)−2−{1−[(2E)−3−フェニルプロパ−2−エン−1−イル]ピペリジン−4−イル}アセトアミドをクリーム色固体として475mg得た。得られた化合物を実施例4と同様の造塩工程によりフマル酸塩とし,白色固体のN−(ジフェニルメチル)−2−{1−[(2E)−3−フェニルプロパ−2−エン−1−イル]ピペリジン−4−イル}アセトアミドフマル酸塩を530mg得た。
実施例50と同様の方法により,実施例51から62の化合物を得た。
実施例50と同様の方法により,実施例51から62の化合物を得た。
参考例14の化合物を用い,参考例18及び実施例50と同様の方法を続けて行うことにより,(±)−N−[(3−フルオロフェニル)(フェニル)メチル]−2−[1−(2−ナフトイル)ピペリジン−4−イル]アセトアミドを得た。
参考例14の化合物を用い,参考例18及び参考例1と同様の方法を続けて行うことにより得られた化合物を実施例4と同様の造塩工程によりフマル酸塩とし(±)−N−[(3−フルオロフェニル)(フェニル)メチル]−2−{1−[(2E)−3−フェニルプロパ−2−エン−1−イル]ピペリジン−4−イル}アセトアミドフマル酸塩を得た。
以下,実施例64と同様の方法により実施例65から69の化合物を得た。
以下,実施例64と同様の方法により実施例65から69の化合物を得た。
N−ベンズヒドリル−2−ピペリジン−4−イルアセトアミド塩酸塩0.34gをDCE5mlに溶解し,TEA0.20gを加えて室温で30分間攪拌した後,6−メトキシ−2−ナフトアルデヒド0.18g及び酢酸0.24gを加え,室温で1時間攪拌した。この反応液に水素化トリアセトキシホウ素ナトリウム0.63gを加え,室温で66時間撹拌した後,減圧下に溶媒を留去した。得られた残渣をEtOAcに溶解し,飽和炭酸水素ナトリウム水溶液及び飽和食塩水で洗浄した。有機層を無水硫酸ナトリウムで乾燥し,減圧下に溶媒を留去した後,残渣をエタノールより再結晶した。得られた化合物0.234gを実施例4と同様の造塩工程によりフマル酸塩とし,無色固体のN−ベンズヒドリル−2−[1−[(6−メトキシ−2−ナフチル)メチル]ピペリジン−4−イル}アセトアミドフマル酸塩0.186gを得た。
以下,実施例73と同様の方法により,実施例74から95の化合物を得た。
以下,実施例73と同様の方法により,実施例74から95の化合物を得た。
2−[1−(2−ナフチルメチル)ピペリジン−4−イル]−N−フェニルアセトアミド0.18g及びDMF2mlの混液に,氷冷下60%油性水素化ナトリウム20mgを加え氷冷下10分間攪拌した後に,臭化ベンジル0.07mlを加え室温で5時間攪拌した。反応液にEtOAc40mlを加え,水25mlで2回,飽和食塩水25mlで順次洗浄し,有機層を無水硫酸ナトリウムで乾燥した。減圧下に溶媒を留去した後,残渣をシリカゲルカラムクロマトグラフィー(クロロホルム→クロロホルム:メタノール:濃アンモニア水=100:1:0.1)で精製した。得られた化合物を実施例1と同様の造塩工程により塩酸塩とし,白色固体のN−ベンジル−2−[1−(2−ナフチルメチル)ピペリジン−4−イル]−N−フェニルアセトアミド塩酸塩190mgを得た。
以下,実施例101と同様の方法により実施例102の化合物を得た。
以下,実施例101と同様の方法により実施例102の化合物を得た。
1−[(2E)−3−フェニルプロパ−2−エン−1−イル]ピペリジン−4−アミン0.2g,TEA0.28ml及びTHF3mlの混液にフェニルベンズヒドリルカルバマート0.33gを加え室温で3日間,50℃で5時間撹拌した後,フェニルベンズヒドリルカルバマート0.1gをさらに加えて50℃で一夜攪拌した。反応液にEtOAc60mlを加え,水30ml,飽和炭酸水素ナトリウム水溶液30ml,水30ml,飽和食塩水30mlで順次洗浄後,有機層を無水硫酸ナトリウムで乾燥し減圧下に溶媒を留去した。残渣をシリカゲルカラムクロマトグラフィー(クロロホルム:メタノール:濃アンモニア水=100:1:0.1→50:1:0.1)で精製後,ジエチルエーテル−ヘキサン(2:1)で洗浄し,無色結晶のN−(ジフェニルメチル)−N’−{1−[(2E)−3−フェニルプロパ−2−エン−1−イル]ピペリジン−4−イル}ウレア0.29gを得た。
(±)−3−{フェニル[({1−[(2E)−3−フェニルプロパ−2−エン−1−イル]ピペリジン−4−イル}アセチル)アミノ]メチル}安息香酸0.30gをTHF5mlに溶解し,1,1’カルボニルジイミダゾール0.11gを加え,50℃で2時間攪拌した。反応液を室温まで冷却した後,濃アンモニア水10mlを加え,室温で2時間攪拌した。反応液をEtOAcで希釈した後,水及び飽和食塩水で洗浄し,無水硫酸ナトリウムで乾燥した。減圧下に溶媒を留去した後,残渣をEtOAcヘキサン混合液で洗浄した。得られた化合物を実施例4と同様の造塩工程によりフマル酸塩とし,無色固体の(±)−3−{フェニル[({1−[(2E)−3−フェニルプロパ−2−エン−1−イル]ピペリジン−4−イル}アセチル)アミノ]メチル}ベンズアミドフマル酸塩0.083gを得た。
実施例104と同様の方法により実施例105から113の化合物を得た。
実施例104と同様の方法により実施例105から113の化合物を得た。
3−[(1E)−3−(4−{2−[(ジフェニルメチル)アミノ]−2−オキソエチル}ピペリジン−1−イル)プロパ−1−エン−1−イル]安息香酸メチル204mgを濃アンモニア水:THF:2−プロパノール=2:1:1の混液20mlに溶解し,封管中,95℃で24時間攪拌した。反応液を室温まで冷却した後,減圧下に溶媒を留去して得られた残渣をシリカゲルカラムクロマトグラフィー(クロロホルム:メタノール=40:1→30:1)で精製した。得られた化合物を実施例4と同様の造塩工程によりフマル酸塩とし,無色固体の3−[(1E)−3−(4−{2−[(ジフェニルメチル)アミノ]−2−オキソエチル}ピペリジン−1−イル)プロパ−1−エン−1−イル]ベンズアミドフマル酸塩46mgを得た。
実施例114と同様の方法により実施例115の化合物を得た。
実施例114と同様の方法により実施例115の化合物を得た。
参考例19及び41の化合物を用い,参考例42及び参考例18と同様の方法を続けて行うことにより得られた化合物を実施例1と同様の造塩工程により塩酸塩としN−[ビス(4−フルオロフェニル)メチル]−2−(1−{(2E)−3−[4−シアノ−3−(ピペリジン−4−イルオキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド2塩酸塩を得た。
2−(1−[(2E)−3−[3−(ベンジルオキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)−N−(ジフェニルメチル)アセトアミド212mgをTFA5mlに溶解し,ペンタメチルベンゼン296mgを加え,室温で5時間攪拌した。減圧下に溶媒を留去した後,残渣をEtOAcで希釈し,飽和炭酸水素ナトリウム水溶液及び飽和食塩水で洗浄した。有機層を無水硫酸ナトリウムで乾燥した後,減圧下に溶媒を留去して得られた残渣をシリカゲルカラムクロマトグラフィー(クロロホルム:メタノール=40:1)で精製した。得られた化合物を実施例4と同様の造塩工程によりフマル酸塩とし,無色固体のN−(ジフェニルメチル)−2−[1−[(2E)−3−(3−ヒドロキシフェニル)プロパ−2−エン−1−イル]ピペリジン−4−イル}アセトアミドフマル酸塩88mgを得た。
実施例117と同様の方法により実施例118の化合物を得た。
実施例117と同様の方法により実施例118の化合物を得た。
参考例111の化合物を用い、参考例7及び参考例11と同様の方法を続けて行うことにより、N−[ビス(4−フルオロフェニル)メチル]−3−{1−[(2E)−3−(4−シアノフェニル)プロパ−2−エン−1−イル]ピペリジン−4−イル}プロパンアミド塩酸塩を得た。
実施例323と同様の方法により実施例324及び325の化合物を得た。
実施例323と同様の方法により実施例324及び325の化合物を得た。
参考例107及び参考例48の化合物を用い、参考例11及び参考例18と同様の方法を続けて行うことにより、N−[2−(ベンジルオキシ)−4−フルオロベンジル]−2−(1−{(2E)−3−[4−(ピペリジン−4−イルオキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド2塩酸塩を得た。
参考例96及び参考例74の化合物を用い、実施例73及び参考例18と同様の方法を続けて行うことにより、2,2−ビス(4−フルオロフェニル)−N−(1−{(2E)−3−[4−(ピペリジン−4−イルオキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド2塩酸塩を得た。
実施例327と同様の方法により実施例328から332の化合物を得た。
実施例327と同様の方法により実施例328から332の化合物を得た。
4−{4−[(1E)−3−ヒドロキシプロパ−1−エン−1−イル]フェノキシ}ピペリジン−1−カルボン酸tert−ブチル666mg,TEA0.56ml及びジクロロメタン10mlの混液に,氷冷下メタンスルホニルクロリド0.19mlを加え1時間攪拌した。反応液に飽和炭酸水素ナトリウム水溶液を加え室温に昇温し,EtOAcを用いて抽出後,有機層を無水硫酸ナトリウムで乾燥し減圧下に溶媒を留去し,淡黄色油状の残留物を得た。得られた残留物はそのまま次反応に用いた。
残留物のDMF10ml溶液に,室温撹拌下炭酸カリウム344mg,N−(4−フルオロベンジル)−N−メチル−2−ピペリジン−4−イルアセトアミド220mgを順次加え2時間撹拌した。反応液に水を加え,EtOAcを用いて抽出後,有機層を無水硫酸ナトリウムで乾燥し減圧下に溶媒を留去した。残渣をシリカゲルカラムクロマトグラフィー(メタノール:クロロホルム=1:99→5:95)で精製し,無色結晶の4−{4−[(1E)−3−(4−{2−[(4−フルオロベンジル)(メチル)アミノ]−2−オキソエチル}ピペリジン−1−イル)プロパ−1−エン−1−イル]フェノキシ}ピペリジン−1−カルボン酸tert−ブチル224mgを得た。
残留物のDMF10ml溶液に,室温撹拌下炭酸カリウム344mg,N−(4−フルオロベンジル)−N−メチル−2−ピペリジン−4−イルアセトアミド220mgを順次加え2時間撹拌した。反応液に水を加え,EtOAcを用いて抽出後,有機層を無水硫酸ナトリウムで乾燥し減圧下に溶媒を留去した。残渣をシリカゲルカラムクロマトグラフィー(メタノール:クロロホルム=1:99→5:95)で精製し,無色結晶の4−{4−[(1E)−3−(4−{2−[(4−フルオロベンジル)(メチル)アミノ]−2−オキソエチル}ピペリジン−1−イル)プロパ−1−エン−1−イル]フェノキシ}ピペリジン−1−カルボン酸tert−ブチル224mgを得た。
3−クロロ−4−ホルミルベンゾニトリルを用い、参考例102、参考例7、参考例129及び実施例333を続けて行うことにより、N−[ビス(4−フルオロフェニル)メチル]−2−{1−[(2E)−3−(2−クロロ−4−シアノフェニル)プロパ−2−エン−1−イル]ピペリジン−4−イル}アセトアミド塩酸塩を得た。
N−(4−フルオロベンジル)−2−ピペリジン−4−イルアセトアミド塩酸塩430mg,メタノール3ml溶液に,酢酸ナトリウム123mgを加え30分間攪拌した。溶媒を留去し得られた残留物,DCE5mlの溶液に,室温撹拌下(2E)−3−[4−(3−ピロリジン−1−イルプロポキシ)フェニル]アクリルアルデヒド310mg,チタニウムテトライソプロポキシド0.3mlを順次加え10分間攪拌した後に,水素化トリアセトキシホウ素ナトリウム424mgを加え,2時間攪拌した。反応液に1M水酸化ナトリウム水溶液を加え,EtOAcを用いて抽出後,有機層を無水硫酸ナトリウムで乾燥し減圧下に溶媒を留去した。残渣をシリカゲルカラムクロマトグラフィー(濃アンモニア水:メタノール:クロロホルム=0.5:5:95)で精製後,4M塩酸−EtOAc溶液にて処理し、無色固体のN−(4−フルオロベンジル)−2−(1−{(2E)−3−[4−(3−ピロリジン−1−イルプロポキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド2塩酸塩488mgを得た。
実施例335と同様の方法により実施例336の化合物を得た。
実施例335と同様の方法により実施例336の化合物を得た。
参考例64の化合物を用い、参考例11、参考例18及び実施例335と同様の方法を続けて行うことにより、4−[({1−[(2E)−3−(4−シアノフェニル)プロパ−2−エン−1−イル]ピペリジン−4−イル}アセチル)(4−フルオロベンジル)アミノ]−N−メチルベンズアミド塩酸塩を得た。
N−[ビス(4−フルオロフェニル)メチル]−2−(1−{(2E)−3−[4−(3−ヒドロキシプロポキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド320mg,ジクロロメタン8.0ml,TEA0.125mlの混液に,氷冷下メタンスルホニルクロリド0.086mlを滴下し0℃で1時間攪拌した。反応液に水10mlを加え,クロロホルム:2−プロパノール=3:1で抽出し,減圧下で溶媒を留去した。残渣をシリカゲルカラムクロマトグラフィー(クロロホルム→クロロホルム:メタノール=50:1→10:1)で精製し,無色油状の3−(4−{(1E)−3−[4−(2−{[ビス(4−フルオロフェニル)メチル]アミノ}−2−オキソエチル)ピペリジン−1−イル]プロパ−1−エン−1−イル}フェノキシ)プロピルメタンスルホナート218mgを得た。
アゼチジン塩酸塩332mg,DMF5.0mlの混液に,氷冷下水素化リチウム28mgを加え,室温で45分間攪拌した。これに氷冷下3−(4−{(1E)−3−[4−(2−{[ビス(4−フルオロフェニル)メチル]アミノ}−2−オキソエチル)ピペリジン−1−イル]プロパ−1−エン−1−イル}フェノキシ)プロピルメタンスルホナート218mg,DMF5mlの混液を加え,室温で2日間攪拌した。反応終了後,減圧下で溶媒を留去し,残渣にクロロホルム:メタノール=3:1溶液5mlを加え,水5mlで洗浄した。減圧下で溶媒を留去し,残渣をシリカゲルカラムクロマトグラフィー(クロロホルム→クロロホルム:メタノール=10:1→6:1)で精製し,淡黄色アモルファスの2−(1−{(2E)−3−[4−(3−アゼチジン−1−イルプロポキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)−N−[ビス(4−フルオロフェニル)メチル]アセトアミド71mgを得た。
2−(1−{(2E)−3−[4−(3−アゼチジン−1−イルプロポキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)−N−[ビス(4−フルオロフェニル)メチル]アセトアミド68mg,エタノール7mlの混液にフマル酸27mgを加え,50℃で1時間攪拌した後,減圧下で溶媒を留去した。残渣にEtOAc10mlを加え,室温で2時間攪拌し,不溶物を濾取した後,減圧下で乾燥し,淡黄色アモルファスの2−(1−{(2E)−3−[4−(3−アゼチジン−1−イルプロポキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)−N−[ビス(4−フルオロフェニル)メチル]アセトアミドフマル酸塩90mgを得た。
実施例338と同様の方法により実施例339の化合物を得た。
アゼチジン塩酸塩332mg,DMF5.0mlの混液に,氷冷下水素化リチウム28mgを加え,室温で45分間攪拌した。これに氷冷下3−(4−{(1E)−3−[4−(2−{[ビス(4−フルオロフェニル)メチル]アミノ}−2−オキソエチル)ピペリジン−1−イル]プロパ−1−エン−1−イル}フェノキシ)プロピルメタンスルホナート218mg,DMF5mlの混液を加え,室温で2日間攪拌した。反応終了後,減圧下で溶媒を留去し,残渣にクロロホルム:メタノール=3:1溶液5mlを加え,水5mlで洗浄した。減圧下で溶媒を留去し,残渣をシリカゲルカラムクロマトグラフィー(クロロホルム→クロロホルム:メタノール=10:1→6:1)で精製し,淡黄色アモルファスの2−(1−{(2E)−3−[4−(3−アゼチジン−1−イルプロポキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)−N−[ビス(4−フルオロフェニル)メチル]アセトアミド71mgを得た。
2−(1−{(2E)−3−[4−(3−アゼチジン−1−イルプロポキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)−N−[ビス(4−フルオロフェニル)メチル]アセトアミド68mg,エタノール7mlの混液にフマル酸27mgを加え,50℃で1時間攪拌した後,減圧下で溶媒を留去した。残渣にEtOAc10mlを加え,室温で2時間攪拌し,不溶物を濾取した後,減圧下で乾燥し,淡黄色アモルファスの2−(1−{(2E)−3−[4−(3−アゼチジン−1−イルプロポキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)−N−[ビス(4−フルオロフェニル)メチル]アセトアミドフマル酸塩90mgを得た。
実施例338と同様の方法により実施例339の化合物を得た。
N−[ビス(4−フルオロフェニル)メチル]−2−(1−{(2E)−3−[4−(3−ヒドロキシプロポキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド230mg,THF5.0ml,TEA0.078mlの混液に,氷冷下メタンスルホニルクロリド0.04mlを滴下し0℃で1時間攪拌した。不溶物を濾過した後,減圧下で溶媒を留去し,黄色アモルファスの3−(4−{(1E)−3−[4−(2−{[ビス(4−フルオロフェニル)メチル]アミノ}−2−オキソエチル)ピペリジン−1−イル]プロパ−1−エン−1−イル}フェノキシ)プロピルメタンスルホナート263mgを得た。これにクロロホルム5mlを加え,氷冷下ピペリジン0.36gを滴下し,室温で41時間攪拌した。反応液に水10mlを加え,EtOAc10mlで抽出した後,減圧下で溶媒を留去した。残渣をシリカゲルカラムクロマトグラフィー(クロロホルム→クロロホルム:メタノール=40:1→20:1)で精製し,淡黄色アモルファスのN−[ビス(4−フルオロフェニル)メチル]−2−(1−{(2E)−3−[4−(3−ピペリジン−1−イルプロポキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド194mgを得た。
N−[ビス(4−フルオロフェニル)メチル]−2−(1−{(2E)−3−[4−(3−ピペリジン−1−イルプロポキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド191mg,エタノール10mlの混液に,フマル酸36mgを加え,50℃で1時間攪拌した後,減圧下で溶媒を留去した。残渣にEtOAc5.0ml,ヘキサン5mlを加え,室温で2時間攪拌し,不溶物を濾取した後,減圧下で乾燥し,白色固体のN−[ビス(4−フルオロフェニル)メチル]−2−(1−{(2E)−3−[4−(3−ピペリジン−1−イルプロポキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミドフマル酸塩197mgを得た。
実施例340と同様の方法により実施例341から342の化合物を得た。
N−[ビス(4−フルオロフェニル)メチル]−2−(1−{(2E)−3−[4−(3−ピペリジン−1−イルプロポキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド191mg,エタノール10mlの混液に,フマル酸36mgを加え,50℃で1時間攪拌した後,減圧下で溶媒を留去した。残渣にEtOAc5.0ml,ヘキサン5mlを加え,室温で2時間攪拌し,不溶物を濾取した後,減圧下で乾燥し,白色固体のN−[ビス(4−フルオロフェニル)メチル]−2−(1−{(2E)−3−[4−(3−ピペリジン−1−イルプロポキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミドフマル酸塩197mgを得た。
実施例340と同様の方法により実施例341から342の化合物を得た。
N−[ビス(4−フルオロフェニル)メチル]−N−メチル−2−[1−((2E)−3−[4−{(3S)−ピロリジン−3−イルオキシ}フェニル}プロパ−2−エン−1−イル)ピペリジン−4−イル]アセトアミド152mg,THF5mlの混液に,ホルムアルデヒド水溶液0.033mlを加え,室温で1時間攪拌した後,酢酸0.023ml,水素化トリアセトキシホウ素ナトリウム86mgを加え,室温で23時間攪拌した。反応溶液にクロロホルム:メタノール=4:1溶液10mlを加え,飽和炭酸水素ナトリウム溶液10mlで洗浄し,減圧下で溶媒を留去した後,残渣をシリカゲルカラムクロマトグラフィー(クロロホルム:メタノール=5:1)で精製し,淡黄色アモルファスのN−[ビス(4−フルオロフェニル)メチル]−N−メチル−2−[1−((2E)−3−{4−{[(3S)−1−メチルピロリジン−3−イル]オキシ}フェニル}プロパ−2−エン−1−イル)ピペリジン−4−イル]アセトアミド95mgを得た。
N−[ビス(4−フルオロフェニル)メチル]−N−メチル−2−[1−((2E)−3−{4−{[(3S)−1−メチルピロリジン−3−イル]オキシ}フェニル}プロパ−2−エン−1−イル)ピペリジン−4−イル]アセトアミド95mg,エタノール10mlの混液にフマル酸38mgを加え,50℃で1時間攪拌した後,減圧下で溶媒を留去した。残渣にジエチルエーテル10ml,エタノール少量を加え,室温で2時間攪拌し,不溶物を濾取した後,減圧下で乾燥し,淡黄色アモルファスのN−[ビス(4−フルオロフェニル)メチル]−N−メチル−2−[1−((2E)−3−{4−{[(3S)−1−メチルピロリジン−3−イル]オキシ}フェニル}プロパ−2−エン−1−イル)ピペリジン−4−イル]アセトアミド2フマル酸塩109mgを得た。
実施例343と同様の方法により実施例96から100及び実施例344から349の化合物を得た。
N−[ビス(4−フルオロフェニル)メチル]−N−メチル−2−[1−((2E)−3−{4−{[(3S)−1−メチルピロリジン−3−イル]オキシ}フェニル}プロパ−2−エン−1−イル)ピペリジン−4−イル]アセトアミド95mg,エタノール10mlの混液にフマル酸38mgを加え,50℃で1時間攪拌した後,減圧下で溶媒を留去した。残渣にジエチルエーテル10ml,エタノール少量を加え,室温で2時間攪拌し,不溶物を濾取した後,減圧下で乾燥し,淡黄色アモルファスのN−[ビス(4−フルオロフェニル)メチル]−N−メチル−2−[1−((2E)−3−{4−{[(3S)−1−メチルピロリジン−3−イル]オキシ}フェニル}プロパ−2−エン−1−イル)ピペリジン−4−イル]アセトアミド2フマル酸塩109mgを得た。
実施例343と同様の方法により実施例96から100及び実施例344から349の化合物を得た。
N−[4−(2−シアノフェノキシ)フェニル]アセトアミド10g,濃アンモニア水10ml,エタノール100mlの混液に,ラネーニッケル触媒を加え,3.4気圧の水素気流下一晩撹拌した。セライトを用いて濾過し減圧下に溶媒を留去し,淡黄色油状のN−[4−(2−アミノメチル)フェノキシ]フェニル}アセトアミド7.8gを得た。
N−[4−(2−アミノメチル)フェノキシ]フェニル}アセトアミド7.8g,DMF5mlの溶液に,室温撹拌下1−ヒドロキシベンゾトリアゾール107mg,1−エチル3−(3−ジメチルアミノプロピル)カルボジイミド塩酸塩203mgを順次加え30分間攪拌した後に,{1−[(2E)−3−(4−シアノフェニル)プロパ−2−エン−1−イル]ピペリジン−4−イル}酢酸267mgを加え,3時間攪拌した。反応液に水を加え,EtOAcを用いて抽出後,有機層を無水硫酸ナトリウムで乾燥し減圧下に溶媒を留去した。残渣をシリカゲルカラムクロマトグラフィー(濃アンモニア水:メタノール:クロロホルム=0.5:5:95)で精製後,4M塩酸EtOAc溶液にて処理し、無色固体のN−{2−[4−(アセチルアミノ)フェノキシ]ベンジル}−2−{1−[(2E)−3−(4−シアノフェニル)プロパ−2−エン−1−イル]ピペリジン−4−イル}アセトアミド塩酸塩95mgを得た。
N−[4−(2−アミノメチル)フェノキシ]フェニル}アセトアミド7.8g,DMF5mlの溶液に,室温撹拌下1−ヒドロキシベンゾトリアゾール107mg,1−エチル3−(3−ジメチルアミノプロピル)カルボジイミド塩酸塩203mgを順次加え30分間攪拌した後に,{1−[(2E)−3−(4−シアノフェニル)プロパ−2−エン−1−イル]ピペリジン−4−イル}酢酸267mgを加え,3時間攪拌した。反応液に水を加え,EtOAcを用いて抽出後,有機層を無水硫酸ナトリウムで乾燥し減圧下に溶媒を留去した。残渣をシリカゲルカラムクロマトグラフィー(濃アンモニア水:メタノール:クロロホルム=0.5:5:95)で精製後,4M塩酸EtOAc溶液にて処理し、無色固体のN−{2−[4−(アセチルアミノ)フェノキシ]ベンジル}−2−{1−[(2E)−3−(4−シアノフェニル)プロパ−2−エン−1−イル]ピペリジン−4−イル}アセトアミド塩酸塩95mgを得た。
N−{1−[(2E)−3−(4−シアノフェニル)プロパ−2−エン−1−イル]ピペリジン−4−イル}−2−[(4−フルオロフェニル)アミノ]アセトアミド2塩酸塩125mg,TEA0.278mlのクロロホルム5ml混合溶液に氷冷下、ピバロイルクロリド121mgを加えて室温で3時間攪拌した。反応溶液に水を加えてクロロホルムで抽出し、無水硫酸ナトリウムで乾燥後、溶媒を減圧留去した。残渣をシリカゲルカラムクロマトグラフィー(クロロホルム:メタノール:濃アンモニア水=50:1:0.1)で精製し、さらにこれを実施例1と同様の造塩工程により塩酸塩とすることにより無色結晶のN−[2−({1−[(2E)−3−(4−シアノフェニル)プロパ−2−エン−1−イル]ピペリジン−4−イル}アミノ)−2−オキソエチル]−N−(4−フルオロフェニル)−2,2−ジメチルプロパンアミド塩酸塩114mgを得た。
2,2−ジフェニルグリシン227mg,4−[(1E)−3−(4−アミノピペリジン−1−イル)プロパ−1−エン−1−イル]ベンゾニトリル2塩酸塩314mg,TEA0.278ml,N−エチル−N’−3−ジメチルアミノプロピルカルボジイミド塩酸塩384mg,1−ヒドロキシベンゾトリアゾール202mgのDMF10ml混合溶液を室温で一晩攪拌した。反応溶液に水を加えてEtOAcで抽出し、飽和炭酸水素ナトリウム水溶液、水、飽和食塩水で洗浄した。無水硫酸ナトリウムで乾燥後、溶媒を減圧留去し、残渣をピリジン20mlに溶解した。これに室温下、無水酢酸5mlを加えて同温でさらに一晩攪拌した。反応溶液に水を加えてEtOAc、ジエチルエーテルの混合溶媒で抽出し、水、飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥して溶媒を減圧留去した。残渣をシリカゲルカラムクロマトグラフィー(クロロホルム:メタノール:濃アンモニア水=50:1:0.1)で精製後、常法によりフマル酸塩とすることにより無色結晶の2−(アセチルアミノ)−N−{1−[(2E)−3−(4−シアノフェニル)プロパ−2−エン−1−イル]ピペリジン−4−イル}−2,2−ジフェニルアセトアミドフマル酸塩87mgを得た。
4−ブロモ−2,2−ジフェニルブタン酸319mgをチオニルクロリド5mlに溶解し、60℃で1時間加熱攪拌した。溶媒を減圧留去し、残渣をTHF3mlに溶解したものを、4−[(1E)−3−(4−アミノピペリジン−1−イル)プロパ−1−エン−1−イル]ベンゾニトリル2塩酸塩173mg,N,N−ジイソプロピルエチルアミン0.348mlのピリジン5ml溶液に加えて室温で5時間攪拌した。溶媒を減圧留去後、残渣をEtOAcに溶解し、水、飽和食塩水で洗浄した。無水硫酸ナトリウムで乾燥後、溶媒を減圧留去し、残渣をシリカゲルカラムクロマトグラフィー(クロロホルム:メタノール:濃アンモニア水=50:1:0.1)で精製することにより無色アモルファス235mgを得た。これを4M塩酸EtOAc溶液に溶解し、室温下攪拌後、さらに常法により精製、造塩することにより淡黄色結晶の4−クロロ−N−{1−[(2E)−3−(4−シアノフェニル)プロパ−2−エン−1−イル]ピペリジン−4−イル}−2,2−ジフェニルブタンアミド塩酸塩を得た。
また、上述した合成法に準じ、下表41から56の化合物を得ることができる。
以下、薬理試験につき詳述する。
また、上述した合成法に準じ、下表41から56の化合物を得ることができる。
以下、薬理試験につき詳述する。
ヒトSLC−1遺伝子の単離と発現ベクターへのクローニング及びSLC−1安定発現細胞の作製
ヒトSLC−1をコードする全長cDNA(配列番号1)は、PCRにより取得した。SLC−1をコードする遺伝子の増幅には、ヒト脳由来のMarathon Ready cDNA(Clontech社)を鋳型に、フォワードプライマーとして5’−ggaaagcttgccgccatggacctggaagcctcgc−3’(配列番号3)、リバースプライマーとして5’−ggactcgagtcaggtgcctttgctttctg−3’(配列番号4)を用いた。PCRはPfuTurbo DNA Polymerase(Stratagene社)を用い、95℃(30秒)/60℃(30秒)/74℃(1分)のサイクルを35回繰り返した。pcDNA3.1/Zeo(+)(Invitrogen社)のHindIII/XhoIサイトに、5’−agctgccgccatgaagacgatcatcgccctgagctacatcttctgcctggtattcgccgactacaaggacgatgatgacaaggggaagcttgtac−3’(配列番号5)と5’−tcgagtacaagcttccccttgtcatcatcgtccttgtagtcggcgaataccaggcagaagatgtagctcagggcgatgatcgtcttcatggcggc−3’(配列番号6)をアニーリングしたDNA断片をライゲーションしpcDNA3.1sf/Zeo(+)を構築した。PCRで増幅した約1.1kbpのDNA断片はpcDNA3.1sf/Zeo(+)を用いてクローニングし、SLC−1発現ベクターを構築した。塩基配列の確認はジデオキシターミネーター法によりABI377 DNA Sequencer(Applied Biosystems社)を用いて行った。
TypeI Collagenをコートした10cm培養シャーレ(旭テクノグラス社)に293細胞を1x106細胞で播種して24時間培養後、0.8μgのpcDNA3.1/Hygro(+)(Invitrogen社)及び7.2μgのpSRE−Luc(Clontech社)をFuGENE6(Boeringer Mannheim社)を用いて遺伝子導入した。遺伝子導入40時間後に新たに10cm培養シャーレに播種しなおし、100μg/mlのhygromycin(Boehringer Mannheim社)で選択し、生き残ってコロニーを形成した細胞を回収し、SRE−lucierase遺伝子安定導入細胞を得た。更にこの細胞に同様にSLC−1発現ベクターをFuGENE6(Boeringer Mannheim社)を用いて遺伝子導入し、40μg/mlのzeocin(Invitrogen社)で選択し、ヒトSLC−1安定発現細胞を得た。
ヒトSLC−1をコードする全長cDNA(配列番号1)は、PCRにより取得した。SLC−1をコードする遺伝子の増幅には、ヒト脳由来のMarathon Ready cDNA(Clontech社)を鋳型に、フォワードプライマーとして5’−ggaaagcttgccgccatggacctggaagcctcgc−3’(配列番号3)、リバースプライマーとして5’−ggactcgagtcaggtgcctttgctttctg−3’(配列番号4)を用いた。PCRはPfuTurbo DNA Polymerase(Stratagene社)を用い、95℃(30秒)/60℃(30秒)/74℃(1分)のサイクルを35回繰り返した。pcDNA3.1/Zeo(+)(Invitrogen社)のHindIII/XhoIサイトに、5’−agctgccgccatgaagacgatcatcgccctgagctacatcttctgcctggtattcgccgactacaaggacgatgatgacaaggggaagcttgtac−3’(配列番号5)と5’−tcgagtacaagcttccccttgtcatcatcgtccttgtagtcggcgaataccaggcagaagatgtagctcagggcgatgatcgtcttcatggcggc−3’(配列番号6)をアニーリングしたDNA断片をライゲーションしpcDNA3.1sf/Zeo(+)を構築した。PCRで増幅した約1.1kbpのDNA断片はpcDNA3.1sf/Zeo(+)を用いてクローニングし、SLC−1発現ベクターを構築した。塩基配列の確認はジデオキシターミネーター法によりABI377 DNA Sequencer(Applied Biosystems社)を用いて行った。
TypeI Collagenをコートした10cm培養シャーレ(旭テクノグラス社)に293細胞を1x106細胞で播種して24時間培養後、0.8μgのpcDNA3.1/Hygro(+)(Invitrogen社)及び7.2μgのpSRE−Luc(Clontech社)をFuGENE6(Boeringer Mannheim社)を用いて遺伝子導入した。遺伝子導入40時間後に新たに10cm培養シャーレに播種しなおし、100μg/mlのhygromycin(Boehringer Mannheim社)で選択し、生き残ってコロニーを形成した細胞を回収し、SRE−lucierase遺伝子安定導入細胞を得た。更にこの細胞に同様にSLC−1発現ベクターをFuGENE6(Boeringer Mannheim社)を用いて遺伝子導入し、40μg/mlのzeocin(Invitrogen社)で選択し、ヒトSLC−1安定発現細胞を得た。
[Phe13、[125I]Tyr19]−MCHのSLC−1結合実験を用いた被験物の結合阻害活性の測定
実施例356で作製したヒトSLC−1安定発現細胞を回収し洗浄後、0.32M sucroseに懸濁してDounce homogenizerにてホモジェナイズした。1、300xgで10分間遠心して脱核を行い、その上清を再度12、000xgで15分間遠心して沈殿画分を得た。これを、0.0075%のTriton−X100を含む50mM Tris.HCl(pH7.4)に懸濁し、4℃で30分間ゆっくり攪拌を行った後、12、000xgで15分間遠心し、得られた沈殿を5mM Tris.HCl(pH7.4)で一回、50mM Tris.HCl(pH7.4)、10mM MgCl2、2mM EGTA、10KIU/ml aprotinin、1μg/ml pepstatinAで二回洗浄し、再度同じ緩衝液に懸濁してこれを膜画分とした。被験物の結合阻害活性は以下の通り実施した。蛋白質15μgを含む膜画分50μlに50mM Tris.HCl(pH7.4)、10mM MgCl2、2mM EGTA、50μg/ml bacitracin、0.1% BSA溶液に溶解した被験物25μlを添加し、更に0.5nMの[Phe13、[125I]Tyr19]−MCHを25μl添加して結合反応を行った。室温で1時間反応させた後、グラスフィルター(GF/B)を用いて吸引ろ過し、さらに洗浄液(燐酸緩衝液pH7.4、0.01% Triton−X100)で3回洗浄した。グラスフィルターにマイクロシンチレーターを25μl添加し、回収された放射活性をトップカウント(Packard社)にて測定した。また、同時に前述の試験において被験物を添加しない群、非標識のリガンドを過剰に加えた群の放射活性も測定した。MCH結合阻害率(%)=(被験物を添加したときの放射活性−過剰の非標識リガンドを加えたときの放射活性)/(被験物を添加しないときの放射活性−過剰の非標識リガンドを加えたときの放射活性)x100として、阻害率から被験物のIC50値を算出した。その結果、実施例50の化合物は430nMのIC50値を示した。
実施例356で作製したヒトSLC−1安定発現細胞を回収し洗浄後、0.32M sucroseに懸濁してDounce homogenizerにてホモジェナイズした。1、300xgで10分間遠心して脱核を行い、その上清を再度12、000xgで15分間遠心して沈殿画分を得た。これを、0.0075%のTriton−X100を含む50mM Tris.HCl(pH7.4)に懸濁し、4℃で30分間ゆっくり攪拌を行った後、12、000xgで15分間遠心し、得られた沈殿を5mM Tris.HCl(pH7.4)で一回、50mM Tris.HCl(pH7.4)、10mM MgCl2、2mM EGTA、10KIU/ml aprotinin、1μg/ml pepstatinAで二回洗浄し、再度同じ緩衝液に懸濁してこれを膜画分とした。被験物の結合阻害活性は以下の通り実施した。蛋白質15μgを含む膜画分50μlに50mM Tris.HCl(pH7.4)、10mM MgCl2、2mM EGTA、50μg/ml bacitracin、0.1% BSA溶液に溶解した被験物25μlを添加し、更に0.5nMの[Phe13、[125I]Tyr19]−MCHを25μl添加して結合反応を行った。室温で1時間反応させた後、グラスフィルター(GF/B)を用いて吸引ろ過し、さらに洗浄液(燐酸緩衝液pH7.4、0.01% Triton−X100)で3回洗浄した。グラスフィルターにマイクロシンチレーターを25μl添加し、回収された放射活性をトップカウント(Packard社)にて測定した。また、同時に前述の試験において被験物を添加しない群、非標識のリガンドを過剰に加えた群の放射活性も測定した。MCH結合阻害率(%)=(被験物を添加したときの放射活性−過剰の非標識リガンドを加えたときの放射活性)/(被験物を添加しないときの放射活性−過剰の非標識リガンドを加えたときの放射活性)x100として、阻害率から被験物のIC50値を算出した。その結果、実施例50の化合物は430nMのIC50値を示した。
ルシフェラーゼレポーターアッセイを用いた被験物のSLC−1アンタゴニスト活性の測定
実施例356で作製したヒトSLC−1安定発現細胞を96ウェルプレートに1ウェルあたり6x103個播種して37℃で24時間培養した。被検物を添加し、37℃で10分間培養後、MCHを最終濃度40nMになるように添加した。このとき、被検物未添加群、及びMCH未刺激群を作り、被検物のSLC−1活性化阻害率の算出に用いた。37℃で4時間反応後、培地を廃棄し、細胞溶解液(12.5mM Tris HCl(pH7.8)、1mM DTT、5% glycerol、0.5% Triton−X100)を含んだルシフェリン基質液(3.8mM Tricine、0.3mM MgCO3、0.5mM MgSO4、20μM EDTA、24mM DTT、0.015% CoenzymeA、40μM ATP、0.01%ルシフェリン)を1ウェルあたり150μl加えて溶解、反応させた。続いて、ルシフェラーゼの活性をルミノメーター(ML3000;ダイナテックラボラトリーズ社)を用いて測定した。SLC−1活性化阻害率(%)=(被験物存在下MCH刺激したときのルシフェラーゼ活性−MCH未刺激時のルシフェラーゼ活性)/(被験物非存在下MCH刺激したときのルシフェラーゼ活性−MCH未刺激時のルシフェラーゼ活性)x100として、阻害率から被験物のIC50値を算出した。その結果を代表的な実施例化合物につき下表に示した。これらの化合物はメラニン凝集ホルモン受容体阻害作用を有した。
実施例356で作製したヒトSLC−1安定発現細胞を96ウェルプレートに1ウェルあたり6x103個播種して37℃で24時間培養した。被検物を添加し、37℃で10分間培養後、MCHを最終濃度40nMになるように添加した。このとき、被検物未添加群、及びMCH未刺激群を作り、被検物のSLC−1活性化阻害率の算出に用いた。37℃で4時間反応後、培地を廃棄し、細胞溶解液(12.5mM Tris HCl(pH7.8)、1mM DTT、5% glycerol、0.5% Triton−X100)を含んだルシフェリン基質液(3.8mM Tricine、0.3mM MgCO3、0.5mM MgSO4、20μM EDTA、24mM DTT、0.015% CoenzymeA、40μM ATP、0.01%ルシフェリン)を1ウェルあたり150μl加えて溶解、反応させた。続いて、ルシフェラーゼの活性をルミノメーター(ML3000;ダイナテックラボラトリーズ社)を用いて測定した。SLC−1活性化阻害率(%)=(被験物存在下MCH刺激したときのルシフェラーゼ活性−MCH未刺激時のルシフェラーゼ活性)/(被験物非存在下MCH刺激したときのルシフェラーゼ活性−MCH未刺激時のルシフェラーゼ活性)x100として、阻害率から被験物のIC50値を算出した。その結果を代表的な実施例化合物につき下表に示した。これらの化合物はメラニン凝集ホルモン受容体阻害作用を有した。
マウスSLC−1遺伝子の単離と発現ベクターへのクローニング及びSLC−1安定発現細胞の作製
マウスSLC−1をコードする全長cDNA(配列番号9)は、PCRにより取得した。SLC−1をコードする遺伝子の増幅には、マウス脳由来のcDNAを鋳型に、フォワードプライマーとして5’−ggaaagcttgccgccatggatytgcaagcctcgttgc−3’(配列番号7)、リバースプライマーとして5’−ggactcgagtcaggtgcctttgctttctgtc−3’(配列番号8)を用いた。PCRはPfuTurbo DNA Polymerase(Stratagene社)を用い、94℃(30秒)/60℃(30秒)/74℃(1分)のサイクルを35回繰り返した。その結果、1062塩基のオープンリーディングルーム(配列番号:8)を有するDNA断片が増幅された。この断片をpcDNA3.1/Zeo(+)(Invitrogen社)のHindIII/XhoIサイトに挿入し、マウスSLC−1発現ベクターを構築した。
TypeI Collagenをコートした10cm培養シャーレ(旭テクノグラス社)に293細胞を1x106細胞で播種して24時間培養後、0.8μgのpcDNA3.1/Hygro(+)(Invitrogen社)及び7.2μgのpSRE−Luc(Clontech社)をFuGENE6(Boeringer Mannheim社)を用いて遺伝子導入した。遺伝子導入40時間後に新たに10cm培養シャーレに播種しなおし、100μg/mlのhygromycin(Boehringer Mannheim社)で選択し、生き残ってコロニーを形成した細胞を回収し、SRE−lucierase遺伝子安定導入細胞を得た。更にこの細胞に同様にマウスSLC−1発現ベクターをFuGENE6(Boeringer Mannheim社)を用いて遺伝子導入し、40μg/mlのzeocin(Invitrogen社)で選択し、本発明のマウスSLC−1安定発現細胞を得た。
マウスSLC−1をコードする全長cDNA(配列番号9)は、PCRにより取得した。SLC−1をコードする遺伝子の増幅には、マウス脳由来のcDNAを鋳型に、フォワードプライマーとして5’−ggaaagcttgccgccatggatytgcaagcctcgttgc−3’(配列番号7)、リバースプライマーとして5’−ggactcgagtcaggtgcctttgctttctgtc−3’(配列番号8)を用いた。PCRはPfuTurbo DNA Polymerase(Stratagene社)を用い、94℃(30秒)/60℃(30秒)/74℃(1分)のサイクルを35回繰り返した。その結果、1062塩基のオープンリーディングルーム(配列番号:8)を有するDNA断片が増幅された。この断片をpcDNA3.1/Zeo(+)(Invitrogen社)のHindIII/XhoIサイトに挿入し、マウスSLC−1発現ベクターを構築した。
TypeI Collagenをコートした10cm培養シャーレ(旭テクノグラス社)に293細胞を1x106細胞で播種して24時間培養後、0.8μgのpcDNA3.1/Hygro(+)(Invitrogen社)及び7.2μgのpSRE−Luc(Clontech社)をFuGENE6(Boeringer Mannheim社)を用いて遺伝子導入した。遺伝子導入40時間後に新たに10cm培養シャーレに播種しなおし、100μg/mlのhygromycin(Boehringer Mannheim社)で選択し、生き残ってコロニーを形成した細胞を回収し、SRE−lucierase遺伝子安定導入細胞を得た。更にこの細胞に同様にマウスSLC−1発現ベクターをFuGENE6(Boeringer Mannheim社)を用いて遺伝子導入し、40μg/mlのzeocin(Invitrogen社)で選択し、本発明のマウスSLC−1安定発現細胞を得た。
被験物のMCH結合実験を用いたマウスSLC−1結合阻害活性の測定
実施例359で作製したマウスSLC−1安定発現細胞を回収し洗浄後、0.32M sucroseに懸濁してDounce homogenizerにてホモジェナイズした。1、300×gで10分間遠心して脱核を行い、その上清を再度12、000×gで15分間遠心して沈殿画分を得た。これを、0.0075%のTriton−X100を含む50mM Tris.HCl(pH7.4)に懸濁し、4℃で30分間ゆっくり攪拌を行った後、12、000×gで15分間遠心し、得られた沈殿を5mM Tris.HCl(pH7.4)で一回、膜溶解バッファー(50mM Tris.HCl(pH7.4)、10mM MgCl2、2mM EGTA、10KIU/ml aprotinin、1μg/ml pepstatinA)で二回洗浄し、再度膜溶解バッファーに懸濁してこれを膜画分とした。被験物のSLC−1結合阻害活性は以下の通り実施した。蛋白貿30μgを含む膜画分50μlに50mM Tris.HCl(pH7.4)、10mM MgCl2、2mM EGTA、50μg/ml bacitracin、0.1% BSA溶液に溶解した被験物25μlを添加し、更に0.5nMの[Phe13、[125I]Tyr19]−MCHを25μl添加して結合反応を行った。室温で1時間反応させた後、グラスフィルター(GF/B)を用いて吸引ろ過し、さらに洗浄液(phospate−based saline、0.01% Triton−X100)で3回洗浄した。グラスフィルターにマイクロシンチレーターを25μl添加し、回収された放射活性をトップカウント(Packard社)にて測定した。また、同時に前述の試験において被験物を添加しない群、非標識のリガンドを過剰に加えた群の放射活性も測定した。MCH結合阻害率(%)=(被験物とMCHを添加したときの放射活性−非標識のリガンドを加えたときの放射活性)/(被験物を添加しないときの放射活性−非標識のリガンドを加えたときの放射活性)×100として、阻害率から被験物のIC50値を算出した。その結果、実施例50の化合物は300nMのIC50値を示した。
実施例359で作製したマウスSLC−1安定発現細胞を回収し洗浄後、0.32M sucroseに懸濁してDounce homogenizerにてホモジェナイズした。1、300×gで10分間遠心して脱核を行い、その上清を再度12、000×gで15分間遠心して沈殿画分を得た。これを、0.0075%のTriton−X100を含む50mM Tris.HCl(pH7.4)に懸濁し、4℃で30分間ゆっくり攪拌を行った後、12、000×gで15分間遠心し、得られた沈殿を5mM Tris.HCl(pH7.4)で一回、膜溶解バッファー(50mM Tris.HCl(pH7.4)、10mM MgCl2、2mM EGTA、10KIU/ml aprotinin、1μg/ml pepstatinA)で二回洗浄し、再度膜溶解バッファーに懸濁してこれを膜画分とした。被験物のSLC−1結合阻害活性は以下の通り実施した。蛋白貿30μgを含む膜画分50μlに50mM Tris.HCl(pH7.4)、10mM MgCl2、2mM EGTA、50μg/ml bacitracin、0.1% BSA溶液に溶解した被験物25μlを添加し、更に0.5nMの[Phe13、[125I]Tyr19]−MCHを25μl添加して結合反応を行った。室温で1時間反応させた後、グラスフィルター(GF/B)を用いて吸引ろ過し、さらに洗浄液(phospate−based saline、0.01% Triton−X100)で3回洗浄した。グラスフィルターにマイクロシンチレーターを25μl添加し、回収された放射活性をトップカウント(Packard社)にて測定した。また、同時に前述の試験において被験物を添加しない群、非標識のリガンドを過剰に加えた群の放射活性も測定した。MCH結合阻害率(%)=(被験物とMCHを添加したときの放射活性−非標識のリガンドを加えたときの放射活性)/(被験物を添加しないときの放射活性−非標識のリガンドを加えたときの放射活性)×100として、阻害率から被験物のIC50値を算出した。その結果、実施例50の化合物は300nMのIC50値を示した。
被験物のルシフェラーゼレポーターアッセイを用いたマウスSLC−1アンタゴニスト活性の測定
実施例359で作製したマウスSLC−1安定発現細胞を96ウェルプレートに1ウェルあたり9×103個播種して37℃で24時間培養した。被検物を添加し、37℃で10分間培養後、MCHを最終濃度50nMになるように添加した。このとき、被検物未添加、及びMCH未刺激群を作り、被検物のSLC−1活性化阻害率の算出に用いた。37℃で4時間反応後、培地を廃棄し、細胞溶解液(12.5mM Tris HCl(pH7.8)、1mM DTT、5% glycerol、0.5% Triton−X100)を含んだルシフェリン基質液(3.8mM Tricine、0.3mM MgCO3、0.5mM MgSO4、20μM EDTA、24mM DTT、0.015% CoenzymeA、40μM ATP、0.01%ルシフェリン)を1ウェルあたり150μl加えて溶解、反応させた。続いて、ルシフェラーゼの活性をルミノメーター(ML3000;ダイナテックラボラトリーズ社)を用いて測定した。SLC−1活性化阻害率(%)=(被験物とMCHを添加したときのルシフェラーゼ活性−何も添加していないときのルシフェラーゼ活性)/(MCHのみを添加したときのルシフェラーゼ活性−何も添加していないときのルシフェラーゼ活性)×100として、阻害率から被験物のIC50値を算出した。その結果を代表的な実施例化合物につき下表に示した。これらの化合物はメラニン凝集ホルモン受容体阻害作用を有した。
実施例359で作製したマウスSLC−1安定発現細胞を96ウェルプレートに1ウェルあたり9×103個播種して37℃で24時間培養した。被検物を添加し、37℃で10分間培養後、MCHを最終濃度50nMになるように添加した。このとき、被検物未添加、及びMCH未刺激群を作り、被検物のSLC−1活性化阻害率の算出に用いた。37℃で4時間反応後、培地を廃棄し、細胞溶解液(12.5mM Tris HCl(pH7.8)、1mM DTT、5% glycerol、0.5% Triton−X100)を含んだルシフェリン基質液(3.8mM Tricine、0.3mM MgCO3、0.5mM MgSO4、20μM EDTA、24mM DTT、0.015% CoenzymeA、40μM ATP、0.01%ルシフェリン)を1ウェルあたり150μl加えて溶解、反応させた。続いて、ルシフェラーゼの活性をルミノメーター(ML3000;ダイナテックラボラトリーズ社)を用いて測定した。SLC−1活性化阻害率(%)=(被験物とMCHを添加したときのルシフェラーゼ活性−何も添加していないときのルシフェラーゼ活性)/(MCHのみを添加したときのルシフェラーゼ活性−何も添加していないときのルシフェラーゼ活性)×100として、阻害率から被験物のIC50値を算出した。その結果を代表的な実施例化合物につき下表に示した。これらの化合物はメラニン凝集ホルモン受容体阻害作用を有した。
絶食誘発摂食に対する作用
動物
雄性ddyマウス(7−9週令,日本SLC株式会社)を使用した。動物は標準飼育条件下(明期7:30−20:30,室温23±2℃,湿度55±10%)で飼育し,給餌および飲水は自由に行わせた。全ての実験は明期に実施した。
絶食誘発摂食実験
入荷1週間後に個別飼育ケージに移し,1週間慣化した後に実験を実施した。16時間絶食したマウスに化合物もしくはvehicleを皮下もしくは経口投与し,投与1時間後に餌を与え,給餌から1時間後までの摂食量を測定した。
化合物溶液調整
化合物は4−12% DMSO(関東化学株式会社)および4−12%クレモホール(ナカライテスク株式会社)を含む生理食塩水もしくは蒸留水に溶解、もしくは0.5%メチルセルロース(純正化学株式会社)を含む蒸留水に懸濁した。
データ解析
結果は平均値±S.E.M.で表示した。統計ツールにはSAS(ver.6.11)を使用し,vehicle群との比較はDunnett’s testで行った。
結果を第1図から第3図に示す。対象群(Vehicle)、実施例50(3,10,30mg/kg)若しくは実施例130(1,3,10,mg/kg)の化合物を給餌1時間前に皮下投与した。又実施例130の化合物を給餌1時間前に経口投与(3,10,30mg/kg)した。給餌から1時間後までの摂食量(Food Intake)を測定した。その結果、対象群に比し、これらの化合物は有意に摂食抑制作用を示した。
動物
雄性ddyマウス(7−9週令,日本SLC株式会社)を使用した。動物は標準飼育条件下(明期7:30−20:30,室温23±2℃,湿度55±10%)で飼育し,給餌および飲水は自由に行わせた。全ての実験は明期に実施した。
絶食誘発摂食実験
入荷1週間後に個別飼育ケージに移し,1週間慣化した後に実験を実施した。16時間絶食したマウスに化合物もしくはvehicleを皮下もしくは経口投与し,投与1時間後に餌を与え,給餌から1時間後までの摂食量を測定した。
化合物溶液調整
化合物は4−12% DMSO(関東化学株式会社)および4−12%クレモホール(ナカライテスク株式会社)を含む生理食塩水もしくは蒸留水に溶解、もしくは0.5%メチルセルロース(純正化学株式会社)を含む蒸留水に懸濁した。
データ解析
結果は平均値±S.E.M.で表示した。統計ツールにはSAS(ver.6.11)を使用し,vehicle群との比較はDunnett’s testで行った。
結果を第1図から第3図に示す。対象群(Vehicle)、実施例50(3,10,30mg/kg)若しくは実施例130(1,3,10,mg/kg)の化合物を給餌1時間前に皮下投与した。又実施例130の化合物を給餌1時間前に経口投与(3,10,30mg/kg)した。給餌から1時間後までの摂食量(Food Intake)を測定した。その結果、対象群に比し、これらの化合物は有意に摂食抑制作用を示した。
上述の薬理試験結果からも明らかなように本発明化合物のうち代表的な化合物はメラニン凝集ホルモン受容体拮抗作用を有し、また摂食抑制作用を有することから本発明化合物は、抗肥満薬及び肥満に起因する生活習慣病の予防・治療薬として有用である。本発明有効成分並びに本発明化合物又はその製薬学的に許容され得る塩は単独でも医薬として供しうるが通常1種又は2種以上を、当分野において通常用いられている薬剤用担体又は賦形剤等を用いて通常使用されている方法によって調製することができる。投与は錠剤、丸剤、カプセル剤、顆粒剤、散剤及び液剤等による経口投与(舌下投与を含む)、又は関節内、静脈内、筋肉内等の注射剤、坐剤、点眼剤、眼軟膏、経皮用液剤、軟膏剤、経皮用貼付剤、経粘膜液剤、経粘膜貼付剤及び吸入剤等による非経口投与のいずれの形態であってもよい。
本発明による経口投与のための固体組成物としては、錠剤、散剤又は顆粒剤等が用いられる。このような固体組成物においては、1種又は2種以上の有効成分を、少なくとも1種の不活性な希釈剤、例えば乳糖、マンニトール、ブドウ糖、ヒドロキシプロピルセルロース、微結晶セルロース、デンプン、ポリビニルピロリドン又はメタケイ酸アルミン酸マグネシウム等と混合される。組成物は、常法に従って、不活性な希釈剤以外の添加剤、例えばステアリン酸マグネシウムのような滑沢剤や繊維素グリコール酸カルシウムのような崩壊剤、ラクトースのような安定化剤又はグルタミン酸並びにアスパラギン酸のような溶解補助剤を含有していてもよい。
錠剤又は丸剤は必要によりショ糖、ゼラチン、ヒドロキシプロピルセルロース及びヒドロキシプロピルメチルセルロースフタレート等の糖衣又は胃溶性若しくは腸溶性物質のフィルムで被膜してもよい。
経口投与のための液体組成物は、薬剤的に許容される乳濁剤、溶液剤、懸濁剤、シロップ剤及びエリキシル剤等を含み、一般的に用いられる不活性な希釈剤、例えば精製水、エタノールを含む。当該液体組成物は不活性な希釈剤以外に可溶化剤、湿潤剤、懸濁剤のような補助剤、甘味剤、風味剤、芳香剤又は防腐剤を含有していてもよい。
経口投与のための注射剤は、無菌の水性又は非水性の溶液剤、懸濁剤あるいは乳濁剤を含有する。水性の溶液剤又は懸濁剤としては、例えば注射用蒸留水及び生理食塩液が含まれる。非水溶性の溶液剤又は懸濁剤としては、例えばプロピレングリコール、ポリエチレングリコール、オリーブ油のような植物油、エタノールのようなアルコール類又はポリソルベート80(商品名)等がある。このような組成物は、さらに等張化剤、防腐剤、湿潤剤、乳化剤、分散剤、安定化剤(例えば、ラクトース)又は溶解補助剤(例えば、グルタミン酸、アスパラギン酸)のような補助剤を含んでもよい。これらは例えばバクテリア保留フィルターを通す濾過、殺菌剤の配合又は照射によって無菌化される。また、これらは無菌の固体組成物を製造し、使用前に無菌水又は無菌の注射用溶媒に溶解又は懸濁して使用することもできる。
通常経口投与の場合、1日の投与量は、体重当たり約0.001〜100mg/kg、好ましくは0.1〜10mg/kgが適当であり、これを1回であるいは数回好ましくは2乃至4回に分けて投与する。静脈内投与される場合は、1日の投与量は、体重当たり約0.0001〜100mg/kgが適当で、1日1回乃至複数回に分けて投与する。関節内投与の場合は、1日の投与量は、体重当たり約0.0001〜10mg/kgが適当で、1日1回乃至複数回に分けて投与する。また、経粘膜剤としては、体重当たり約0.001〜100mg/kgを1日1回乃至複数回に分けて投与する。投与量は症状、年令及び性別等を考慮して個々の場合に応じて適宜決定される。
本発明による経口投与のための固体組成物としては、錠剤、散剤又は顆粒剤等が用いられる。このような固体組成物においては、1種又は2種以上の有効成分を、少なくとも1種の不活性な希釈剤、例えば乳糖、マンニトール、ブドウ糖、ヒドロキシプロピルセルロース、微結晶セルロース、デンプン、ポリビニルピロリドン又はメタケイ酸アルミン酸マグネシウム等と混合される。組成物は、常法に従って、不活性な希釈剤以外の添加剤、例えばステアリン酸マグネシウムのような滑沢剤や繊維素グリコール酸カルシウムのような崩壊剤、ラクトースのような安定化剤又はグルタミン酸並びにアスパラギン酸のような溶解補助剤を含有していてもよい。
錠剤又は丸剤は必要によりショ糖、ゼラチン、ヒドロキシプロピルセルロース及びヒドロキシプロピルメチルセルロースフタレート等の糖衣又は胃溶性若しくは腸溶性物質のフィルムで被膜してもよい。
経口投与のための液体組成物は、薬剤的に許容される乳濁剤、溶液剤、懸濁剤、シロップ剤及びエリキシル剤等を含み、一般的に用いられる不活性な希釈剤、例えば精製水、エタノールを含む。当該液体組成物は不活性な希釈剤以外に可溶化剤、湿潤剤、懸濁剤のような補助剤、甘味剤、風味剤、芳香剤又は防腐剤を含有していてもよい。
経口投与のための注射剤は、無菌の水性又は非水性の溶液剤、懸濁剤あるいは乳濁剤を含有する。水性の溶液剤又は懸濁剤としては、例えば注射用蒸留水及び生理食塩液が含まれる。非水溶性の溶液剤又は懸濁剤としては、例えばプロピレングリコール、ポリエチレングリコール、オリーブ油のような植物油、エタノールのようなアルコール類又はポリソルベート80(商品名)等がある。このような組成物は、さらに等張化剤、防腐剤、湿潤剤、乳化剤、分散剤、安定化剤(例えば、ラクトース)又は溶解補助剤(例えば、グルタミン酸、アスパラギン酸)のような補助剤を含んでもよい。これらは例えばバクテリア保留フィルターを通す濾過、殺菌剤の配合又は照射によって無菌化される。また、これらは無菌の固体組成物を製造し、使用前に無菌水又は無菌の注射用溶媒に溶解又は懸濁して使用することもできる。
通常経口投与の場合、1日の投与量は、体重当たり約0.001〜100mg/kg、好ましくは0.1〜10mg/kgが適当であり、これを1回であるいは数回好ましくは2乃至4回に分けて投与する。静脈内投与される場合は、1日の投与量は、体重当たり約0.0001〜100mg/kgが適当で、1日1回乃至複数回に分けて投与する。関節内投与の場合は、1日の投与量は、体重当たり約0.0001〜10mg/kgが適当で、1日1回乃至複数回に分けて投与する。また、経粘膜剤としては、体重当たり約0.001〜100mg/kgを1日1回乃至複数回に分けて投与する。投与量は症状、年令及び性別等を考慮して個々の場合に応じて適宜決定される。
Claims (18)
- Het1が置換されていてもよい単環式飽和含窒素ヘテロ環基である請求の範囲1に記載のメラニン凝集ホルモン受容体拮抗剤。
- Het1が置換されていてもよいピペリジン環である請求の範囲1乃至2の何れかに記載のメラニン凝集ホルモン受容体拮抗剤。
- Alk2が置換されていてもよい低級アルケニレンである請求の範囲1乃至3の何れかに記載のメラニン凝集ホルモン受容体拮抗剤。
- L1が窒素原子(N)を有するリンカーである請求の範囲1乃至4の何れかに記載のメラニン凝集ホルモン受容体拮抗剤。
- Rbが置換されていてもよい炭化水素環基である請求の範囲1乃至6の何れかに記載のメラニン凝集ホルモン受容体拮抗剤。
- R2が置換されていてもよいフェニルである請求の範囲1乃至5の何れかに記載のメラニン凝集ホルモン受容体拮抗剤。
- 抗肥満薬である請求の範囲1から7の何れかに記載のメラニン凝集ホルモン受容体拮抗剤。
- 下記一般式式
(一般式中の記号は以下の意味を示す。
Q:CH;又はN、
R1a,R1b,R1c,R1d,及びR1e:同一又は異なって、
H;
CN;
ハロゲン;
HO、ハロゲン、低級アルキル−NH−若しくは低級アルキル−O−アルキル−NH−で置換されていてもよい低級アルキル;
HO;
ハロゲン若しくはアリールで置換されていてもよい低級アルキル−O−;
置換されていてもよいアリール;
低級アルキル−CO−NH−で置換されていてもよいアリール−O−;
H2N;
H2N、低級アルキル−NH−若しくは(低級アルキル)2N−で置換されていてもよい低級アルキル−NH−;
低級アルキル−CO−NH−;
[H2N、低級アルキル−NH−若しくは(低級アルキル)2N−で置換されていてもよい低級アルキル]2N−;
HO−OC−;
低級アルキル−O−CO−;
H2NCO;
低級アルキル−NHCO−;
(低級アルキル)2NCO−;
低級アルキル若しくは低級アルキル−O−CO−で置換されていてもよいヘテロ環−CO−;
Cy1:炭化水素環;又はヘテロ環、
R2a、R2b及びR2c:同一又は異なって、
H;
CN;
ハロゲン;
NO2;
HO;
置換されていてもよいアリール;
CN、ハロゲン若しくはヘテロ環で置換されていてもよい低級アルキル;
H2N;
H2N、低級アルキル−NH−若しくは(低級アルキル)2N−で置換されていてもよい低級アルキル−NH−;
[H2N、低級アルキル−NH−若しくは(低級アルキル)2N−で置換されていてもよい低級アルキル]2N−;
(低級アルキル−O−CO−)(H2N、低級アルキル−NH−若しくは(低級アルキル)2N−で置換されていてもよい低級アルキル)N−;
低級アルキル−CO−NH−;
HO−CO−;
低級アルキル−O−CO−;
H2NCO;
低級アルキル−NH−、若しくは(低級アルキル)2N−で置換されていてもよい低級アルキル−NHCO−;
(低級アルキル)2NCO−;
低級アルキル若しくは低級アルキル−O−CO−で置換されていてもよいヘテロ環−CO−;
HS;
低級アルキル−S−;
CN、ハロゲン、HO、NH2、低級アルキル−NH−、若しくは(低級アルキル)2Nで置換されていてもよい低級アルキル−O−;
低級アルキルで置換されていてもよいヘテロ環;
(R13a、R13b及びR13c:同一又は異なってH;低級アルキル;HO−CO;低級アルキル−O−;低級アルキル−CO−;若しくは低級アルキル−O−CO−、
Cy3:炭化水素環、
Alk3:低級アルキレン、
n1:0;又は1);
更にR2a及びR2bが一緒になって低級アルキレンジオキシ若しくはヘテロ環を形成していてもよい。
R4及びR5:同一又は異なって、
H;
HO;
H2N;
低級アルキル−CO−NH−;
ハロゲン、H2N、低級アルキル−NH−,若しくは(低級アルキル)2N−若しくはアリールで置換されていてもよい低級アルキル;又は
L1a:−NR11−CO−NR12−;−NR11SO2−;−SO2NR11−;−CONR11−;−NR11CO−;又は−CO−
R11及びR12:同一又は異なって、
H;
−CO2R13、−NR14R15、−CONR14R15若しくはアリールで置換されていてもよい低級アルキル;
シクロアルキル;
又はハロゲン若しくは低級アルキル−NH−CO−で置換されていてもよいアリール、
R13、R14及びR15:同一又は異なってH;又は低級アルキル
Alk1a:低級アルキレン
m1:0;又は1
m2:0;1;又は2
m3:0;又は1
m4:0;又は1
R6及びR7:同一又は異なって、
H;
HO;
低級アルキル;又は
置換されていてもよいヘテロ環;
更にR6及びR7は一緒になって低級アルキレンを形成する。
R8a及びR8b:同一又は異なって、H;低級アルキル;又はR8a及びR8bが一緒になってオキソ、
R9a、R9b、R10a及びR10:同一又は異なってH;低級アルキル;又はアリール、
Cy2:炭化水素環;又はヘテロ環
−−−−:R9bとCy2が一緒になって縮合環、R9a、R10a及び隣接する炭素原子と一体となって飽和炭素環、又はR9a及びR10aが一体となって結合を形成する。
但し、R1a,R1b,R1c,R1d,及びR1eの何れかがH2N若しくはCH3CONHの場合、m1又はm2の何れか一方は1で且つm3がOであり;
R6及びR7の何れかがHOの場合、m1又はm2の何れか一方は1で且つm3がOであり;
L1aが−CONR11−で且つR4及びR5の何れか一方がシクロアルキルの場合、他方は(1)H、(2)H2N、(3)低級アルキル−CO−NH−、(4)ハロゲン、H2N、低級アルキル−NH−,若しくは(低級アルキル)2N−若しくは
L1aが−CONR11−の場合、m1が0で且つCy1が炭化水素環で且つR11が(1)H、(2)−CO2R13、−NR14R15、−CONR14R15若しくは一個のアリールで置換されていてもよい低級アルキル、(3)シクロアルキル、又は(4)ハロゲン若しくは低級アルキル−NH−CO−で置換されていてもよいアリールであり、
L1aが−CONR11−で、m1が0で、Cy1が炭化水素環で且つR1a、R1b、R1c、R1d及びR1e何れかが低級アルキル−O−の場合、R2a、R2b及びR2cの何れかがH以外の基であり、
L1aが−NR11CO−でCy1がヘテロ環の場合、m2が1若しくは2で且つR4及びR5の何れか一方はH以外の基であり;
L1aが−NR11CO−で、m1が0で且つCy1が炭化水素環での場合、m2が1又は2で且つR9aがHである。)含窒素飽和ヘテロ環誘導体又はその製薬学的に許容される塩。
好ましい含窒素飽和ヘテロ環誘導体は、以下の通りである。 - m4が、1である請求の範囲9に記載の含窒素飽和ヘテロ環誘導体又はその製薬学的に許容される塩。
- m2が0である前記10項に記載の含窒素飽和ヘテロ環誘導体又はその製薬学的に許容される塩。
- Cy1がアリールである前記9から11項の何れかに記載の含窒素飽和ヘテロ環誘導体又はその製薬学的に許容される塩。
- Cy1がフェニルである前記9から12項の何れかに記載の含窒素飽和ヘテロ環誘導体又はその製薬学的に許容される塩。
- Cy2がアリールである前記9から14項の何れかに記載の含窒素飽和ヘテロ環誘導体又はその製薬学的に許容される塩。
- Cy2がフェニルである前記9から15項の何れかに記載の含窒素飽和ヘテロ環誘導体又はその製薬学的に許容される塩。
- N−[ビス(4−フルオロフェニル)メチル]−2−{1−[(2E)−3−(4−シアノフェニル)プロパ−2−エン−1−イル]ピペリジン−4−イル}−N−メチルアセトアミド、2,2−ビス(4−フルオロフェニル)−N−(1−{(2E)−3−[4−(3−ピロリジン−1−イルプロポキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、2,2−ビス(4−フルオロフェニル)−N−メチル−N−(1−{(2E)−3−[4−(3−ピロリジン−1−イルプロポキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、N−{1−[(2E)−3−(4−シアノフェニル)プロパ−2−エン−1−イル]ピペリジン−4−イル}−2,2−ビス(4−フルオロフェニル)−N−メチルアセトアミド、N−{1−[(2E)−3−(4−シアノフェニル)プロパ−2−エン−1−イル]ピペリジン−4−イル}−2,2−ビス(4−フルオロフェニル)アセトアミド、N−[ビス(4−フルオロフェニル)メチル]−2−{1−[(2E)−3−(4−シアノフェニル)プロパ−2−エン−1−イル]ピペリジン−4−イル}アセトアミド、N−(4−フルオロベンジル)−2−(1−{(2E)−3−[4−(ピペリジン−4−イルオキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、N−[ビス(4−フルオロフェニル)メチル]−N−メチル−2−[1−((2E)−3−{4−[(3R)−ピロリジン−3−イルオキシ]フェニル}プロパ−2−エン−1−イル)ピペリジン−4−イル]アセトアミド、N−[ビス(4−フルオロフェニル)メチル]−N−メチル−2−(1−{(2E)−3−[4−(ピペリジン−3−イルメトキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、N−(4−フルオロベンジル)−N−イソプロピル−2−(1−{(2E)−3−[4−(ピペリジン−4−イルオキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、2−[ビス(4−フルオロフェニル)アミノ]−N−(1−{(2E)−3−[4−(ピペリジン−4−イルオキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、2,2−ビス(4−フルオロフェニル)−N−メチル−N−(1−{(2E)−3−[4−(ピペリジン−4−イルオキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、2,2−ビス(4−フルオロフェニル)−N−(1−{(2E)−3−[4−(ピペリジン−4−イルオキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)プロパンアミド、2−[3,5−ビス(トリフルオロメチル)フェニル]−N−(1−{(2E)−3−[4−(ピペリジン−4−イルオキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、N−[ビス(4−フルオロフェニル)メチル]−N−メチル−2−(1−{(2E)−3−[4−(ピペリジン−4−イルオキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、N−[ビス(4−フルオロフェニル)メチル]−2−(1−{(2E)−3−[4−(3−ピロリジン−1−イルプロポキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、2,2−ビス(4−フルオロフェニル)−N−(1−{(2E)−3−[4−(ピペリジン−4−イルオキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、2,2−ビス(4−フルオロフェニル)−N−(1−{(2E)−3−[2−フルオロ−4−(ピペリジン−4−イルオキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、2−(1−{(2E)−3−[4−(3−アゼチジン−1−イルプロポキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)−N−[ビス(4−フルオロフェニル)メチル]−N−メチルアセトアミド、N−[ビス(4−フルオロフェニル)メチル]−N−メチル−2−(1−{(2E)−3−[4−(3−ピロリジン−1−イルプロポキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、N−[ビス(4−フルオロフェニル)メチル]−2−(1−{(2E)−3−[4−(3−ピペリジン−1−イルプロポキシ)フェニル]プロパ−2−エン−1−イル}ピペリジン−4−イル)アセトアミド、N−[ビス(4−フルオロフェニル)メチル]−N−メチル−2−{1−[(2E)−3−(4−{[(3S)−1−メチルピロリジン−3−イル]オキシ}フェニル)プロパ−2−エン−1−イル]ピペリジン−4−イル}アセトアミド、及び2,2−ビス(4−フルオロフェニル)−N−メチル−N−{1−[(2E)−3−(4−{[(3R)−1−メチルピロリジン−3−イル]オキシ}フェニル)プロパ−2−エン−1−イル]ピペリジン−4−イル}アセトアミドの群から選ばれる化合物である請求の範囲9に記載の含窒素飽和ヘテロ環誘導体又はその製薬学的に許容される塩。
- 請求の範囲9に記載の一般式(II)で示される含窒素飽和ヘテロ環誘導体又はその製薬学的に許容される塩を有効成分とする医薬組成物。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2002332950 | 2002-11-15 | ||
| JP2002332950 | 2002-11-15 | ||
| PCT/JP2003/014534 WO2004046110A1 (ja) | 2002-11-15 | 2003-11-14 | メラニン凝集ホルモン受容体拮抗剤 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JPWO2004046110A1 true JPWO2004046110A1 (ja) | 2006-03-16 |
Family
ID=32321679
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2004553173A Withdrawn JPWO2004046110A1 (ja) | 2002-11-15 | 2003-11-14 | メラニン凝集ホルモン受容体拮抗剤 |
Country Status (3)
| Country | Link |
|---|---|
| JP (1) | JPWO2004046110A1 (ja) |
| AU (1) | AU2003284402A1 (ja) |
| WO (1) | WO2004046110A1 (ja) |
Families Citing this family (46)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR101078505B1 (ko) | 2003-03-14 | 2011-10-31 | 오노 야꾸힝 고교 가부시키가이샤 | 질소 함유 복소환 유도체 및 이들을 유효 성분으로 하는약제 |
| MY141862A (en) | 2003-07-22 | 2010-07-16 | Arena Pharm Inc | Diaryl and arylheteroaryl urea derivatives as modulators of the 5-ht2a serotonin receptor useful for the prophylaxis and treatment of disorders related thereto |
| US7378420B2 (en) * | 2004-08-30 | 2008-05-27 | Neuromed Pharmaceuticals Ltd. | Urea derivatives as calcium channel blockers |
| PE20090123A1 (es) | 2004-09-13 | 2009-03-10 | Ono Pharmaceutical Co | Un derivado heterociclico conteniendo nitrogeno y un farmaco conteniendo el mismo como el ingrediente activo |
| MX2008011414A (es) | 2006-03-10 | 2008-09-22 | Ono Pharmaceutical Co | Derivado heterociclico nitrogenado y agente farmaceutico que comprende el derivado como ingrediente activo. |
| US9108948B2 (en) | 2006-06-23 | 2015-08-18 | Abbvie Inc. | Cyclopropyl amine derivatives |
| RU2449989C2 (ru) | 2006-06-23 | 2012-05-10 | Эбботт Лэборетриз | Производные циклопропиламина в качестве модуляторов h3-гистаминового рецептора |
| TWI415845B (zh) | 2006-10-03 | 2013-11-21 | Arena Pharm Inc | 用於治療與5-ht2a血清素受體相關聯病症之作為5-ht2a血清素受體之調節劑的吡唑衍生物 |
| CA2666084A1 (en) * | 2006-10-06 | 2008-04-17 | Taisho Pharmaceutical Co., Ltd. | 1-naphthyl alkylpiperidine derivative |
| JP5393677B2 (ja) | 2007-08-15 | 2014-01-22 | アリーナ ファーマシューティカルズ, インコーポレイテッド | 5−HT2Aセロトニン受容体に関連した障害の治療のための5−HT2Aセロトニン受容体のモジュレーターとしてのイミダゾ[1,2−a]ピリジン誘導体 |
| WO2009024823A2 (en) | 2007-08-22 | 2009-02-26 | Astrazeneca Ab | Oxadiazole derivatives as dgat inhibitors |
| WO2009123714A2 (en) | 2008-04-02 | 2009-10-08 | Arena Pharmaceuticals, Inc. | Processes for the preparation of pyrazole derivatives useful as modulators of the 5-ht2a serotonin receptor |
| US8377968B2 (en) * | 2008-06-02 | 2013-02-19 | Zalicus Pharmaceuticals, Ltd. | N-piperidinyl acetamide derivatives as calcium channel blockers |
| EP2364142B1 (en) | 2008-10-28 | 2018-01-17 | Arena Pharmaceuticals, Inc. | Compositions of a 5-ht2a serotonin receptor modulator useful for the treatment of disorders related thereto |
| WO2010062321A1 (en) | 2008-10-28 | 2010-06-03 | Arena Pharmaceuticals, Inc. | Processes useful for the preparation of 1-[3-(4-bromo-2-methyl-2h-pyrazol-3-yl)-4-methoxy-phenyl]-3-(2,4-difluoro-phenyl)-urea and crystalline forms related thereto |
| WO2010080864A1 (en) | 2009-01-12 | 2010-07-15 | Array Biopharma Inc. | Piperidine-containing compounds and use thereof |
| TW201039825A (en) | 2009-02-20 | 2010-11-16 | Astrazeneca Ab | Cyclopropyl amide derivatives 983 |
| US9186353B2 (en) | 2009-04-27 | 2015-11-17 | Abbvie Inc. | Treatment of osteoarthritis pain |
| US8673920B2 (en) | 2009-05-06 | 2014-03-18 | Merck Sharp & Dohme Corp. | Inhibitors of the renal outer medullary potassium channel |
| RU2012139082A (ru) | 2010-02-18 | 2014-03-27 | Астразенека Аб | Способы получения производных циклопропиламида и связанных с ними промежуточных соединений |
| WO2012037258A1 (en) | 2010-09-16 | 2012-03-22 | Abbott Laboratories | Processes for preparing 1,2-substituted cyclopropyl derivatives |
| WO2012058116A1 (en) | 2010-10-27 | 2012-05-03 | Merck Sharp & Dohme Corp. | Inhibitors of the renal outer medullary potassium channel |
| WO2012058134A1 (en) | 2010-10-29 | 2012-05-03 | Merck Sharp & Dohme Corp. | Inhibitors of the renal outer medullary potassium channel |
| WO2012113103A1 (en) | 2011-02-25 | 2012-08-30 | Helsinn Healthcare S.A. | Asymmetric ureas and medical uses thereof |
| CA2838643A1 (en) * | 2011-06-07 | 2012-12-13 | Japan Science And Technology Agency | Inhibition of fatty acid and cholesterol uptake by carbon monoxide (co) |
| JP2014521751A (ja) | 2011-08-19 | 2014-08-28 | メルク・シャープ・アンド・ドーム・コーポレーション | 腎髄質外層カリウムチャンネルの阻害薬 |
| US9527830B2 (en) | 2011-09-16 | 2016-12-27 | Merck Sharp & Dohme Corp. | Inhibitors of the renal outer medullary potassium channel |
| WO2013062900A1 (en) | 2011-10-25 | 2013-05-02 | Merck Sharp & Dohme Corp. | Inhibitors of the renal outer medullary potassium channel |
| US8999990B2 (en) | 2011-10-25 | 2015-04-07 | Merck Sharp & Dohme Corp. | Inhibitors of the renal outer medullary potassium channel |
| WO2013066718A2 (en) | 2011-10-31 | 2013-05-10 | Merck Sharp & Dohme Corp. | Inhibitors of the renal outer medullary potassium channel |
| US9108947B2 (en) | 2011-10-31 | 2015-08-18 | Merck Sharp & Dohme Corp. | Inhibitors of the Renal Outer Medullary Potassium channel |
| US9139585B2 (en) | 2011-10-31 | 2015-09-22 | Merck Sharp & Dohme Corp. | Inhibitors of the Renal Outer Medullary Potassium channel |
| EP2790511B1 (en) | 2011-12-16 | 2016-09-14 | Merck Sharp & Dohme Corp. | Inhibitors of the renal outer medullary potassium channel |
| AR092031A1 (es) | 2012-07-26 | 2015-03-18 | Merck Sharp & Dohme | Inhibidores del canal de potasio medular externo renal |
| WO2014085210A1 (en) | 2012-11-29 | 2014-06-05 | Merck Sharp & Dohme Corp. | Inhibitors of the renal outer medullary potassium channel |
| EP2934533B1 (en) | 2012-12-19 | 2017-11-15 | Merck Sharp & Dohme Corp. | Inhibitors of the renal outer medullary potassium channel |
| WO2014126944A2 (en) | 2013-02-18 | 2014-08-21 | Merck Sharp & Dohme Corp. | Inhibitors of the renal outer medullary potassium channel |
| EP2961403A4 (en) | 2013-03-01 | 2016-11-30 | Zalicus Pharmaceuticals Ltd | HETEROCYCLIC INHIBITORS OF SODIUM CHANNEL |
| US9765074B2 (en) | 2013-03-15 | 2017-09-19 | Merck Sharp & Dohme Corp. | Inhibitors of the renal outer medullary potassium channel |
| EP3027625B1 (en) | 2013-07-31 | 2018-05-30 | Merck Sharp & Dohme Corp. | Spiro-fused derivatives of piperidine useful for the treatment of inter alia hypertension and acute or chronic heart failure |
| WO2016127358A1 (en) | 2015-02-12 | 2016-08-18 | Merck Sharp & Dohme Corp. | Inhibitors of renal outer medullary potassium channel |
| CA2989343A1 (en) | 2015-06-12 | 2016-12-15 | Yandong Wen | Diaryl and arylheteroaryl urea derivatives useful for the prophylaxis and treatment of rem sleep behavior disorder |
| RU2018103338A (ru) | 2015-07-15 | 2019-08-15 | Аксовант Сайенсиз Гмбх | Производные диарил- и арилгетероарилмочевины для профилактики и лечения галлюцинаций, ассоциированных с нейродегенеративным заболеванием |
| KR102640774B1 (ko) | 2016-03-22 | 2024-02-26 | 헬신 헬쓰케어 에스.에이. | 벤젠술포닐-비대칭 우레아 및 그의 의학적 용도 |
| US9650338B1 (en) | 2016-07-29 | 2017-05-16 | VDM Biochemicals, Inc. | Opioid antagonist compounds and methods of making and using |
| BR112022000429A2 (pt) | 2019-07-11 | 2022-03-29 | Praxis Prec Medicines Inc | Formulações de moduladores do canal de cálcio tipo t e métodos de uso dos mesmos |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB1473262A (en) * | 1974-11-20 | 1977-05-11 | Delalande Sa | Derivatives of n-3,4,5-trimethoxy cinnamoyl-piperazine their process of preparation and their therapeutic application |
| GB1575310A (en) * | 1976-11-16 | 1980-09-17 | Anphar Sa | Piperidine derivatives |
| FR2522325B1 (fr) * | 1982-02-26 | 1985-08-09 | Delalande Sa | Nouveaux derives aryliques de la piperazine, de l'homopiperazine et de n,n'-dialkyl diamino-1,2 ethane, leur procede de preparation et leur application en therapeutique |
| CA2386474A1 (en) * | 1999-09-20 | 2001-03-29 | Takeda Chemical Industries, Ltd. | Melanin concentrating hormone antagonist |
| AU7315800A (en) * | 1999-09-20 | 2001-04-24 | Takeda Chemical Industries Ltd. | Mch antagonists |
| JP2001172257A (ja) * | 1999-10-05 | 2001-06-26 | Fujisawa Pharmaceut Co Ltd | 有機スルホンアミド化合物 |
| FR2804429B1 (fr) * | 2000-01-31 | 2003-05-09 | Adir | Nouveaux derives de 4-sulfonamides piperidine, leur procede de preparation et les compositions pharmaceutiques qui les contiennent |
| DE60234116D1 (de) * | 2001-11-26 | 2009-12-03 | Schering Corp | Piperidin mch antagonisten und ihre verwendung in der behandlung von obesität und störungen des zentralnervensystems |
-
2003
- 2003-11-14 JP JP2004553173A patent/JPWO2004046110A1/ja not_active Withdrawn
- 2003-11-14 WO PCT/JP2003/014534 patent/WO2004046110A1/ja not_active Ceased
- 2003-11-14 AU AU2003284402A patent/AU2003284402A1/en not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| AU2003284402A1 (en) | 2004-06-15 |
| WO2004046110A1 (ja) | 2004-06-03 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JPWO2004046110A1 (ja) | メラニン凝集ホルモン受容体拮抗剤 | |
| US7951821B2 (en) | N-[phenyl(piperidin-2-yl)methyl]benzamide derivatives, preparation thereof, and use thereof in therapy | |
| TWI450893B (zh) | Inhibition of prostaglandin D synthase in the piper Compounds | |
| US8153658B2 (en) | Piperidine derivative or salt thereof | |
| DK1882684T3 (en) | PYRROLIDE INGREDIENTS OR SALTS THEREOF | |
| TW200940507A (en) | Pyridyl non-aromatic nitrogenated heterocyclic-1-carboxylate ester derivative | |
| CZ20023777A3 (cs) | Farmaceuticky aktivní piperidinové deriváty, zvláště jako modulátory receptoru chemokinu | |
| JP5232143B2 (ja) | モチリン受容体アンタゴニストとしてのベンジルピペラジン誘導体 | |
| TW201039814A (en) | Diacylethylenediamine compounds | |
| MX2011003500A (es) | Derivado de 7-piperidinoalquil-3,4-dihidroquinolona. | |
| JPWO2004011430A1 (ja) | ナトリウムチャネル阻害剤 | |
| US7834008B2 (en) | Cyclopropyl derivatives as NK3 receptor antagonists | |
| CA2824536A1 (en) | Protease activated receptor 2 (par2) antagonists | |
| US20130317041A1 (en) | Compounds | |
| CN100516040C (zh) | 具有2,6-二取代苯乙烯基的含氮杂环衍生物 | |
| US20100179118A1 (en) | Cyclic aminoalkylcarboxamide derivative | |
| US20060252797A1 (en) | Receptor regulator | |
| EA022043B1 (ru) | Сульфоновые соединения в качестве лигандов 5-htрецептора | |
| WO2001025199A1 (en) | Urea compounds, process for producing the same and use thereof | |
| EP1351935A1 (en) | Aryl piperidine derivatives as inducers of ldl-receptor expression | |
| WO2002055497A1 (en) | Aryl piperidine derivatives as inducers of ldl-receptor expression | |
| US6294537B1 (en) | Compounds which are specific antagonists of the human NK3 receptor and their use as medicinal products and diagnostic tools | |
| JP2005325031A (ja) | 1−シンナミルピペリジン誘導体 | |
| JPWO2001025199A1 (ja) | ウレア化合物、その製造法および用途 | |
| WO2006025471A1 (ja) | ピペリジン誘導体又はその製薬学的に許容される塩 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A300 | Withdrawal of application because of no request for examination |
Free format text: JAPANESE INTERMEDIATE CODE: A300 Effective date: 20070206 |