JP7676769B2 - Ophthalmic composition - Google Patents
Ophthalmic composition Download PDFInfo
- Publication number
- JP7676769B2 JP7676769B2 JP2020214997A JP2020214997A JP7676769B2 JP 7676769 B2 JP7676769 B2 JP 7676769B2 JP 2020214997 A JP2020214997 A JP 2020214997A JP 2020214997 A JP2020214997 A JP 2020214997A JP 7676769 B2 JP7676769 B2 JP 7676769B2
- Authority
- JP
- Japan
- Prior art keywords
- component
- content
- ophthalmic composition
- polyoxyethylene
- vitamin
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Landscapes
- Medicinal Preparation (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Description
本発明は、ベルベリン又はその塩を含有する眼科用組成物に関するものである。 The present invention relates to an ophthalmic composition containing berberine or a salt thereof.
ベルベリン又はその塩は、抗炎症作用や細菌に対する高い抗菌性を持つことが知られている。一方、ビタミンAは上皮細胞の増殖・分化に必須な物質として知られており、ムチン産生を促進する作用、角膜創傷を治癒する作用が報告されている(特許文献1:特許第5673531号公報)。また、ビタミンEは、抗酸化成分等として有用な成分である。以上のことから、ベルベリン又はその塩と、ビタミンA又はビタミンEとを併用する眼科用組成物が望まれていた。 Berberine or its salts are known to have anti-inflammatory effects and high antibacterial properties against bacteria. On the other hand, vitamin A is known to be an essential substance for the proliferation and differentiation of epithelial cells, and has been reported to promote mucin production and heal corneal wounds (Patent Document 1: Japanese Patent No. 5673531). Vitamin E is also a useful component as an antioxidant component. For these reasons, there has been a demand for an ophthalmic composition that uses berberine or its salts in combination with vitamin A or vitamin E.
(A)ベルベリン又はその塩と、(B)(B1)ビタミンA及び(B2)ビタミンEから選ばれる1種以上と、(D)ノニオン界面活性剤とを併用した場合、凍結融解を繰り返すと、眼科用組成物の透過率が悪化するという課題が生じた。以下、凍結融解を繰り返すと、眼科用組成物の透過率が悪化することを、「凍結融解を繰り返すことによる透過率悪化」と記載する場合がある。 When (A) berberine or a salt thereof, (B) one or more selected from (B1) vitamin A and (B2) vitamin E, and (D) a nonionic surfactant are used in combination, a problem occurs in that the transmittance of the ophthalmic composition deteriorates when the composition is subjected to repeated freezing and thawing. Hereinafter, the deterioration of the transmittance of the ophthalmic composition when the composition is subjected to repeated freezing and thawing may be referred to as "deterioration of transmittance due to repeated freezing and thawing."
本発明は上記事情に鑑みなされたもので、上記(A)、(B)及び(D)成分を含有する眼科用組成物において、凍結融解を繰り返すことによる眼科用組成物の透過率悪化が抑制された、ベルベリン又はその塩を含有する眼科用組成物を提供することを目的とする。 The present invention has been made in consideration of the above circumstances, and aims to provide an ophthalmic composition containing berberine or a salt thereof, which contains the above components (A), (B) and (D) and in which deterioration of the transmittance of the ophthalmic composition caused by repeated freezing and thawing is suppressed.
本発明者らは、上記目的を達成するため鋭意検討した結果、上記(A)、(B)及び(D)成分を含有する眼科用組成物に、(C)フェニレフリン又はその塩を配合することで、上記課題を解決できることを知見し、本発明をなすに至ったものである。 As a result of intensive research into achieving the above object, the inventors discovered that the above problem could be solved by adding (C) phenylephrine or a salt thereof to an ophthalmic composition containing the above components (A), (B), and (D), and thus came up with the present invention.
従って、本発明は下記眼科用組成物を提供する。
1.(A)ベルベリン又はその塩、
(B)(B1)ビタミンA及び(B2)ビタミンEから選ばれる1種以上、
(C)フェニレフリン又はその塩、及び
(D)ノニオン界面活性剤
を含有する眼科用組成物。
2.下記式で表される含有質量比が、2.4≦((C)+(D))/((A)+(B))≦23である1記載の眼科用組成物。
3.(A)成分の含有量が、0.01~0.025w/v%、
(B1)成分の含有量が、0.02~0.04w/v%、
(B2)成分の含有量が、0.02~0.05w/v%、
(C)成分の含有量が、0.1~0.6w/v%、及び
(D)成分の含有量が、0.14~0.56w/v%
である1又は2記載の眼科用組成物。
4.さらに、(E)コンドロイチン硫酸及びその塩、グリチルリチン酸及びその塩、ならびにプロピレングリコールから選ばれる1種以上を含有する1~3のいずれかに記載の眼科用組成物。
5.下記式で表される含有質量比が、2.0≦((D)+(E))/((A)+(B))≦20である4記載の眼科用組成物。
6.(E)成分の含有量が、0.05w/v%以上である4又は5記載の眼科用組成物。
Accordingly, the present invention provides the following ophthalmic compositions.
1. (A) berberine or a salt thereof,
(B) one or more selected from (B1) vitamin A and (B2) vitamin E;
An ophthalmic composition comprising (C) phenylephrine or a salt thereof, and (D) a nonionic surfactant.
2. The ophthalmic composition according to 1, wherein the content mass ratio represented by the following formula satisfies 2.4≦((C)+(D))/((A)+(B))≦23.
3. The content of the component (A) is 0.01 to 0.025 w/v%,
The content of the component (B1) is 0.02 to 0.04 w/v%,
The content of the component (B2) is 0.02 to 0.05 w/v%,
The content of the component (C) is 0.1 to 0.6 w/v%, and the content of the component (D) is 0.14 to 0.56 w/v%.
3. The ophthalmic composition according to 1 or 2,
4. The ophthalmic composition according to any one of 1 to 3, further comprising (E) one or more members selected from chondroitin sulfate and its salts, glycyrrhizinic acid and its salts, and propylene glycol.
5. The ophthalmic composition according to 4, wherein the content mass ratio represented by the following formula satisfies 2.0≦((D)+(E))/((A)+(B))≦20.
6. The ophthalmic composition according to 4 or 5, wherein the content of component (E) is 0.05 w/v % or more.
本発明によれば、凍結融解を繰り返すことによる眼科用組成物の透過率悪化が抑制された、ベルベリン又はその塩を含有する眼科用組成物を提供することができる。 According to the present invention, it is possible to provide an ophthalmic composition containing berberine or a salt thereof, in which deterioration of the transmittance of the ophthalmic composition caused by repeated freezing and thawing is suppressed.
以下、本発明について詳細に説明する。
[(A)成分]
本発明の(A)成分はベルベリン又はその塩であり、1種単独で又は2種以上を適宜組み合わせて用いることができる。ベルベリン又はその塩としては、例えば、ベルベリン硫化物やベルベリン塩化物等の硫酸塩、塩酸塩等が挙げられる。また、水和物等であってもよい。例えば、日本薬局方:ベルベリン塩化物水和物、アルプス工業(株)製等を用いることができる。
The present invention will be described in detail below.
[Component (A)]
The component (A) of the present invention is berberine or a salt thereof, which may be used alone or in combination of two or more. Examples of berberine or a salt thereof include sulfates such as berberine sulfide and berberine chloride, and hydrochlorides. It may also be a hydrate. For example, Japanese Pharmacopoeia: berberine chloride hydrate, manufactured by Alps Industries Co., Ltd., may be used.
(A)成分の含有量は、眼科用組成物中0.005w/v%(質量/体積%、g/100mL)以上が好ましく、凍結融解における析出及び凍結融解を繰り返すことによる透過率悪化を抑制する点から、0.1w/v%以下が好ましく、0.01~0.025w/v%がより好ましい。 The content of component (A) in the ophthalmic composition is preferably 0.005 w/v% (mass/volume%, g/100 mL) or more, and from the viewpoint of suppressing precipitation during freezing and thawing and deterioration of transmittance due to repeated freezing and thawing, it is preferably 0.1 w/v% or less, and more preferably 0.01 to 0.025 w/v%.
[(B)成分]
本発明の(B)成分は、(B1)ビタミンA及び(B2)ビタミンEから選ばれる1種以上であり、2種以上を適宜組み合わせて用いることができる。
[(B) Component]
The component (B) of the present invention is at least one selected from (B1) vitamin A and (B2) vitamin E, and two or more of them can be used in appropriate combination.
(B-1)ビタミンA
ビタミンAは、角膜・結膜や皮膚粘膜の角化症、角膜上皮障害等の予防や治療に有効な成分であり、涙液油層安定化効果も有する。特に、コンタクトレンズ使用者は角膜上皮障害を受けやすいため、ビタミンAは有用である。ビタミンAとしては、ビタミンAそれ自体の他に、ビタミンA油等のビタミンA含有混合物、ビタミンA脂肪酸エステル等のビタミンA誘導体が挙げられ、1種単独で又は2種以上を適宜組み合わせて用いることができる。具体的には、レチノールパルミチン酸エステル、レチノール酢酸エステル、レチノール、レチノイン酸、レチノイド等が挙げられる。中でも、レチノールパルミチン酸エステル、レチノール酢酸エステル、レチノイン酸が好ましい。レチノールパルミチン酸エステルは、通常100~180万国際単位/g(以下、I.U./gと略記する場合がある。ものが市販されており、具体的には、DSM社製レチノールパルミチン酸エステル[174万I.U./g)]、シグマアルドリッチ社製パルミチン酸レチノール等が挙げられる。
(B-1) Vitamin A
Vitamin A is an effective ingredient for preventing and treating keratosis of the cornea, conjunctiva, skin and mucous membrane, corneal epithelial disorder, etc., and also has the effect of stabilizing the tear lipid layer. In particular, vitamin A is useful for contact lens users, who are prone to corneal epithelial disorder. Examples of vitamin A include vitamin A itself, vitamin A-containing mixtures such as vitamin A oil, and vitamin A derivatives such as vitamin A fatty acid esters, and can be used alone or in appropriate combination of two or more. Specific examples include retinol palmitate, retinol acetate, retinol, retinoic acid, retinoid, etc. Among them, retinol palmitate, retinol acetate, and retinoic acid are preferred. Retinol palmitate is commercially available in amounts of usually 1 to 1.8 million international units/g (hereinafter, may be abbreviated as I.U./g). Specific examples include retinol palmitate (1.74 million I.U./g) manufactured by DSM and retinol palmitate manufactured by Sigma-Aldrich.
(B-2)ビタミンE
ビタミンEとしては、酢酸トコフェロール(酢酸d-α-トコフェロール、酢酸dl-α-トコフェロール)が挙げられ、1種単独で又は2種以上を適宜組み合わせて用いることができる。中でも、酢酸d-α-トコフェロールが好ましい。具体的には、理研ビタミン(株)製酢酸d-α-トコフェロール、理研Eアセテートα等が挙げられる。
(B-2) Vitamin E
Examples of vitamin E include tocopherol acetate (d-α-tocopherol acetate, dl-α-tocopherol acetate), which may be used alone or in appropriate combination of two or more. Among these, d-α-tocopherol acetate is preferred. Specific examples include d-α-tocopherol acetate and Riken E Acetate α, both manufactured by Riken Vitamin Co., Ltd.
(B)成分全体の含有量は、眼科用組成物中0.01w/v%以上が好ましく、凍結融解を繰り返すことによる透過率悪化を抑制する点から、0.09w/v%以下が好ましい。(B1)成分の含有量は、0.005~0.08w/v%が好ましく、0.02~0.04w/v%がより好ましい。(B2)成分の含有量は0.005~0.08w/v%が好ましく、0.02~0.05w/v%がより好ましい。174万I.U./gを用いた場合は、8,700~139,200国際単位/100mLが好ましく、348,000~87,000国際単位/100mLがより好ましい。 The total content of the (B) components in the ophthalmic composition is preferably 0.01 w/v% or more, and from the viewpoint of suppressing deterioration of transmittance due to repeated freezing and thawing, it is preferably 0.09 w/v% or less. The content of the (B1) component is preferably 0.005 to 0.08 w/v%, more preferably 0.02 to 0.04 w/v%. The content of the (B2) component is preferably 0.005 to 0.08 w/v%, more preferably 0.02 to 0.05 w/v%. When 1.74 million I.U./g is used, it is preferably 8,700 to 139,200 international units/100 mL, more preferably 348,000 to 87,000 international units/100 mL.
[(C)成分]
(C)成分は、フェニレフリン及びその塩から選ばれる1種以上であり、1種単独で又は2種以上を適宜組み合わせて用いることができる。例えば、フェニレフリン塩としては、フェニレフリン塩酸塩、フェニレフリン酢酸塩等の医薬的に許容される塩が挙げられる。フェニレフリン塩酸塩としては、例えば、岩城製薬(株)製の日本薬局方 フェニレフリン塩酸塩等が挙げられる。
[(C) Component]
The component (C) is one or more selected from phenylephrine and its salts, and can be used alone or in combination of two or more. For example, the phenylephrine salt can be phenylephrine hydrochloride, phenylephrine acetate, or other pharmacopoeia salts. For example, the phenylephrine hydrochloride can be phenylephrine hydrochloride, as listed in the Japanese Pharmacopoeia, manufactured by Iwaki Pharmaceutical Co., Ltd.
(C)成分の含有量は、凍結融解における析出及び凍結融解を繰り返すことによる透過率悪化を抑制する点から、眼科用組成物中0.08~0.8w/v%が好ましく、0.1~0.6w/v%がより好ましい。 The content of component (C) in the ophthalmic composition is preferably 0.08 to 0.8 w/v%, and more preferably 0.1 to 0.6 w/v%, in order to suppress precipitation during freezing and thawing and deterioration of transmittance due to repeated freezing and thawing.
[(D)成分]
本発明の(D)成分は非イオン性界面活性剤であり、1種単独で又は2種以上を適宜組み合わせて用いることができる。ビタミンA保存安定性の観点から、2種以上を適宜組み合わせて用いることが好ましい。具体的には、ポリオキシエチレンヒマシ油、ポリオキシエチレン硬化ヒマシ油、ポリオキシエチレンソルビタン脂肪酸エステル(POEソルビタン脂肪酸エステル)、ポリオキシエチレンポリオキシプロピレングリコール(POEPOPグリコール)、ポリエチレングリコール脂肪酸エステル等が挙げられる。
[(D) Component]
The component (D) of the present invention is a nonionic surfactant, and may be used alone or in combination of two or more. From the viewpoint of vitamin A storage stability, it is preferable to use two or more in combination. Specific examples include polyoxyethylene castor oil, polyoxyethylene hydrogenated castor oil, polyoxyethylene sorbitan fatty acid ester (POE sorbitan fatty acid ester), polyoxyethylene polyoxypropylene glycol (POEPOP glycol), polyethylene glycol fatty acid ester, etc.
ポリオキシエチレンヒマシ油(POEヒマシ油)は、ヒマシ油に酸化エチレン(EO)を付加重合することによって得られる化合物であり、酸化エチレンの平均付加モル数が異なるいくつかの種類が知られている。ポリオキシエチレンヒマシ油における酸化エチレンの平均付加モル数については、特に限定はないが、3~60モルが例示される。具体的にはポリオキシエチレンヒマシ油3(EO平均付加モル数3)、ポリオキシエチレンヒマシ油10(EO平均付加モル数10)、ポリオキシエチレンヒマシ油20(EO平均付加モル数20)、ポリオキシエチレンヒマシ油35(EO平均付加モル数35)、ポリオキシエチレンヒマシ油40(EO平均付加モル数40)、ポリオキシエチレンヒマシ油50(EO平均付加モル数50)、ポリオキシエチレンヒマシ油60(EO平均付加モル数60)等が挙げられる。中でも、ポリオキシエチレンヒマシ油35が好ましい。 Polyoxyethylene castor oil (POE castor oil) is a compound obtained by addition polymerization of ethylene oxide (EO) to castor oil, and several types with different average added moles of ethylene oxide are known. The average added moles of ethylene oxide in polyoxyethylene castor oil is not particularly limited, but examples include 3 to 60 moles. Specific examples include polyoxyethylene castor oil 3 (average added moles of EO: 3), polyoxyethylene castor oil 10 (average added moles of EO: 10), polyoxyethylene castor oil 20 (average added moles of EO: 20), polyoxyethylene castor oil 35 (average added moles of EO: 35), polyoxyethylene castor oil 40 (average added moles of EO: 40), polyoxyethylene castor oil 50 (average added moles of EO: 50), and polyoxyethylene castor oil 60 (average added moles of EO: 60). Among these, polyoxyethylene castor oil 35 is preferred.
ポリオキシエチレン硬化ヒマシ油(POE硬化ヒマシ油)は、水添したヒマシ油に酸化エチレンを付加重合することによって得られる化合物であり、酸化エチレンの平均付加モル数が異なるいくつかの種類が知られている。ポリオキシエチレン硬化ヒマシ油における酸化エチレンの平均付加モル数については、特に限定はないが、5~100モルが例示される。具体的にはポリオキシエチレン硬化ヒマシ油5(EO平均付加モル数5)、ポリオキシエチレン硬化ヒマシ油10(EO平均付加モル数10)、ポリオキシエチレン硬化ヒマシ油20(EO平均付加モル数20)、ポリオキシエチレン硬化ヒマシ油30(EO平均付加モル数30)、ポリオキシエチレン硬化ヒマシ油40(EO平均付加モル数40)、ポリオキシエチレン硬化ヒマシ油50(EO平均付加モル数50)、ポリオキシエチレン硬化ヒマシ油60(EO平均付加モル数60)、ポリオキシエチレン硬化ヒマシ油80(EO平均付加モル数80)、ポリオキシエチレン硬化ヒマシ油100(EO平均付加モル数100)等が挙げられる。中でも、ポリオキシエチレン硬化ヒマシ油40、ポリオキシエチレン硬化ヒマシ油60が好ましい。 Polyoxyethylene hydrogenated castor oil (POE hydrogenated castor oil) is a compound obtained by addition polymerization of ethylene oxide to hydrogenated castor oil, and several types with different average added moles of ethylene oxide are known. There are no particular limitations on the average added moles of ethylene oxide in polyoxyethylene hydrogenated castor oil, but examples include 5 to 100 moles. Specifically, polyoxyethylene hydrogenated castor oil 5 (average number of moles of EO added: 5), polyoxyethylene hydrogenated castor oil 10 (average number of moles of EO added: 10), polyoxyethylene hydrogenated castor oil 20 (average number of moles of EO added: 20), polyoxyethylene hydrogenated castor oil 30 (average number of moles of EO added: 30), polyoxyethylene hydrogenated castor oil 40 (average number of moles of EO added: 40), polyoxyethylene hydrogenated castor oil 50 (average number of moles of EO added: 50), polyoxyethylene hydrogenated castor oil 60 (average number of moles of EO added: 60), polyoxyethylene hydrogenated castor oil 80 (average number of moles of EO added: 80), polyoxyethylene hydrogenated castor oil 100 (average number of moles of EO added: 100), etc. are mentioned. Among them, polyoxyethylene hydrogenated castor oil 40 and polyoxyethylene hydrogenated castor oil 60 are preferable.
ポリオキシエチレンソルビタン脂肪酸エステル(POEソルビタン脂肪酸エステル)としては、モノラウリン酸ポリオキシエチレン(20)ソルビタン(ポリソルベート20)、モノパルミチン酸ポリオキシエチレン(20)ソルビタン(ポリソルベート40)、モノステアリン酸ポリオキシエチレン(20)ソルビタン(ポリソルベート60)、トリステアリン酸ポリオキシエチレン(20)ソルビタン(ポリソルベート65)、モノオレイン酸ポリオキシエチレン(20)ソルビタン(ポリソルベート80)が挙げられる。中でも、モノオレイン酸ポリオキシエチレン(20)ソルビタン(ポリソルベート80)が好ましい。 Examples of polyoxyethylene sorbitan fatty acid esters (POE sorbitan fatty acid esters) include polyoxyethylene (20) sorbitan monolaurate (polysorbate 20), polyoxyethylene (20) sorbitan monopalmitate (polysorbate 40), polyoxyethylene (20) sorbitan monostearate (polysorbate 60), polyoxyethylene (20) sorbitan tristearate (polysorbate 65), and polyoxyethylene (20) sorbitan monooleate (polysorbate 80). Of these, polyoxyethylene (20) sorbitan monooleate (polysorbate 80) is preferred.
ポリオキシエチレンポリオキシプロピレングリコール(POEPOPグリコール)は特に限定されるものではなく、医薬品添加物規格(薬添規)に記載されたものを用いることができる。エチレンオキシドの平均重合度は4~200が好ましく、20~200がより好ましく、プロピレンオキシドの平均重合度は5~100が好ましく、20~70がより好ましく、ブロック共重合体でもランダム重合体でもよい。具体的には、ポリオキシエチレン(200)ポリオキシプロピレン(70)グリコール:Lutrol F127(BASF社製)、ユニルーブ70DP-950B(日本油脂(株)製)等、ポリオキシエチレン(120)ポリオキシプロピレン(40)グリコール:プルロニックF-87(BASF社製)、ポリオキシエチレン(160)ポリオキシプロピレン(30)グリコール:プルロニックF-68(BASF社製)、プロノン#188P(日本油脂(株)製)等、ポリオキシエチレン(42)ポリオキシプロピレン(67)グリコール:プルロニックP123(BASF社製)、ポリオキシエチレン(54)ポリオキシプロピレン(39)グリコール:プルロニックP85(BASF社製)、プロノン#235P(日本油脂(株)製)等、ポリオキシエチレン(20)ポリオキシプロピレン(20)グリコール:プルロニックL-44、テトロニック(BASF社製)等が挙げられる。中でも、ポリオキシエチレン(200)ポリオキシプロピレン(70)グリコールが好ましい。 Polyoxyethylene polyoxypropylene glycol (POEPOP glycol) is not particularly limited, and those listed in the Pharmaceutical Additives Standards (Pharmaceutical Additives Regulations) can be used. The average degree of polymerization of ethylene oxide is preferably 4 to 200, more preferably 20 to 200, and the average degree of polymerization of propylene oxide is preferably 5 to 100, more preferably 20 to 70, and may be either a block copolymer or a random polymer. Specifically, polyoxyethylene (200) polyoxypropylene (70) glycol: Lutrol F127 (manufactured by BASF), Unilube 70DP-950B (manufactured by NOF Corporation), polyoxyethylene (120) polyoxypropylene (40) glycol: Pluronic F-87 (manufactured by BASF), polyoxyethylene (160) polyoxypropylene (30) glycol: Pluronic F-68 (manufactured by BASF), Pronon #188P (manufactured by NOF Corporation), polyoxyethylene (42) polyoxypropylene (67) glycol: Pluronic P123 (manufactured by BASF), polyoxyethylene (54) polyoxypropylene (39) glycol: Pluronic P85 (manufactured by BASF), Pronon #235P (manufactured by NOF Corporation), polyoxyethylene (20) polyoxypropylene (20) glycol: Pluronic L-44, Tetronic (manufactured by BASF), and the like. Of these, polyoxyethylene (200) polyoxypropylene (70) glycol is preferred.
ポリエチレングリコール脂肪酸エステルとしては、ステアリン酸ポリエチレングリコール-25、ステアリン酸ポリエチレングリコール-40等が挙げられ、中でもステアリン酸ポリエチレングリコール-40が好ましい。 Examples of polyethylene glycol fatty acid esters include polyethylene glycol-25 stearate and polyethylene glycol-40 stearate, with polyethylene glycol-40 stearate being preferred.
中でも、ポリオキシエチレン硬化ヒマシ油が好ましく、ポリオキシエチレン硬化ヒマシ油とポリオキシエチレンソルビタン脂肪酸エステルとの組み合わせが好ましい。 Among these, polyoxyethylene hydrogenated castor oil is preferred, and a combination of polyoxyethylene hydrogenated castor oil and polyoxyethylene sorbitan fatty acid ester is preferred.
(D)成分の含有量は、凍結融解を繰り返すことによる透過率悪化を抑制する点から、眼科用組成物中0.02~2w/v%が好ましく、0.07~0.9w/v%がより好ましく、0.14~0.56w/v%がさらに好ましい。 The content of component (D) in the ophthalmic composition is preferably 0.02 to 2 w/v%, more preferably 0.07 to 0.9 w/v%, and even more preferably 0.14 to 0.56 w/v%, in order to prevent deterioration of transmittance due to repeated freezing and thawing.
ポリオキシエチレン硬化ヒマシ油を配合する場合、眼科用組成物中0.01~1.0w/v%が好ましく、0.05~0.8w/v%がより好ましく、0.1~0.5w/v%がさらに好ましい。ポリオキシエチレンソルビタン脂肪酸エステルの場合、0.01~1.0w/v%が好ましく、0.02~0.1w/v%がより好ましく、0.04~0.06w/v%がさらに好ましい。 When polyoxyethylene hydrogenated castor oil is used, it is preferably contained in the ophthalmic composition at 0.01 to 1.0 w/v%, more preferably 0.05 to 0.8 w/v%, and even more preferably 0.1 to 0.5 w/v%. When polyoxyethylene sorbitan fatty acid ester is used, it is preferably contained in the ophthalmic composition at 0.01 to 1.0 w/v%, more preferably 0.02 to 0.1 w/v%, and even more preferably 0.04 to 0.06 w/v%.
[(E)成分]
本発明の眼科用組成物には、凍結融解における析出を抑制する点から、(E)コンドロイチン硫酸及びその塩、グリチルリチン酸及びその塩、ならびにプロピレングリコールから選ばれる1種以上を配合することが好ましい。(E)成分は1種単独で又は2種以上組み合わせて用いることができる。コンドロイチン硫酸及びその塩としては、例えば、マルハニチロ社(株)製のコンドロイチン硫酸エステルナトリウム:局外規コンドロイチン硫酸ナトリウム、生化学工業(株)製のコンドロイチン硫酸ナトリウム、日本バイオコン(株)製のコンドロイチン硫酸ナトリウム等が挙げられる。グリチルリチン酸塩としては、グリチルリチン酸二カリウム、グリチルリチン酸二ナトリウム、グリチルリチン酸三ナトリウム、グリチルリチン酸三カリウム、グリチルリチン酸モノアンモニウムが挙げられる。
[(E) component]
In order to suppress precipitation during freezing and thawing, the ophthalmic composition of the present invention preferably contains (E) one or more selected from chondroitin sulfate and its salts, glycyrrhizic acid and its salts, and propylene glycol. The (E) component can be used alone or in combination of two or more. Examples of chondroitin sulfate and its salts include sodium chondroitin sulfate ester (external standard sodium chondroitin sulfate) manufactured by Maruha Nichiro Co., Ltd., sodium chondroitin sulfate manufactured by Seikagaku Corporation, and sodium chondroitin sulfate manufactured by Nippon Biocon Co., Ltd. Examples of glycyrrhizinate salts include dipotassium glycyrrhizinate, disodium glycyrrhizinate, trisodium glycyrrhizinate, tripotassium glycyrrhizinate, and monoammonium glycyrrhizinate.
(E)成分を配合する場合、凍結融解における析出を抑制する点から、眼科用組成物中0.05w/v%以上が好ましく、凍結融解を繰り返すことによる透過率悪化を抑制する点から、1.25w/v%以下が好ましく、0.1~1.25w/v%がより好ましい。 When component (E) is included, the content in the ophthalmic composition is preferably 0.05 w/v% or more in order to suppress precipitation during freezing and thawing, and is preferably 1.25 w/v% or less in order to suppress deterioration of transmittance due to repeated freezing and thawing, and more preferably 0.1 to 1.25 w/v%.
下記式で表される含有質量比は、凍結融解を繰り返すことによる透過率悪化を抑制する点から、2.4≦((C)+(D))/((A)+(B))≦23が好ましく、2.5~10がより好ましく、2.6~8.0がさらに好ましい。 The mass content ratio represented by the formula below is preferably 2.4≦((C)+(D))/((A)+(B))≦23, more preferably 2.5 to 10, and even more preferably 2.6 to 8.0, in order to prevent deterioration of transmittance due to repeated freezing and thawing.
下記式で表される含有質量比は、2.0≦((D)+(E))/((A)+(B))≦20が好ましく、2.5~18がより好ましい。凍結融解における析出を抑制する点から、2.0以上が好ましく、凍結融解を繰り返すことによる透過率悪化を抑制する点から、20以下が好ましい。 The content mass ratio represented by the formula below is preferably 2.0≦((D)+(E))/((A)+(B))≦20, and more preferably 2.5 to 18. From the viewpoint of suppressing precipitation during freezing and thawing, a content mass ratio of 2.0 or more is preferable, and from the viewpoint of suppressing deterioration of transmittance due to repeated freezing and thawing, a content mass ratio of 20 or less is preferable.
[その他の成分]
本発明の組成物には、本発明の効果を損なわない範囲で、眼科用組成物に配合されるその他の成分を適量配合することができる。その他の成分としては下記のものが例示され、1種単独で又は2種以上を適宜組み合わせて用いることができる。
[Other ingredients]
The composition of the present invention may contain other components that are to be incorporated into ophthalmic compositions in appropriate amounts, provided that the effects of the present invention are not impaired. Examples of other components include the following, which may be used alone or in appropriate combination of two or more.
糖類としては、例えば、グルコース、シクロデキストリン、キシリトール、ソルビトール、マンニトール等が挙げられる。なお、これらは、d体、l体又はdl体のいずれでもよい。糖類を配合する場合の含有量は、組成物中0.001~5.0w/v%が好ましく、0.001~1w/v%がより好ましく、0.001~0.1w/v%がさらに好ましい。 Examples of sugars include glucose, cyclodextrin, xylitol, sorbitol, mannitol, etc. These may be in the d-, l-, or dl-form. When sugars are added, their content in the composition is preferably 0.001 to 5.0 w/v%, more preferably 0.001 to 1 w/v%, and even more preferably 0.001 to 0.1 w/v%.
緩衝剤としては、例えば、ホウ酸又はその塩(ホウ砂等)、トロメタモール、クエン酸又はその塩(クエン酸ナトリウム等)、リン酸又はその塩(リン酸水素ナトリウム、リン酸二水素ナトリウム等)、酒石酸又はその塩(酒石酸ナトリウム等)、グルコン酸又はその塩(グルコン酸ナトリウム等)、酢酸又はその塩(酢酸ナトリウム等)、炭酸又はその塩(炭酸水素ナトリウム等)、各種アミノ酸類(イプシロン-アミノカプロン酸、アスパラギン酸カリウム、アミノエチルスルホン酸、グルタミン酸、グルタミン酸ナトリウム)等が挙げられる。中でも、ホウ酸、ホウ砂、トロメタモールが好ましい。緩衝剤を配合する場合の含有量は、組成物中0.001~5.0w/v%が好ましく、0.001~2w/v%がより好ましく、0.001~1w/v%がさらに好ましい。 Examples of buffering agents include boric acid or its salts (e.g., borax), trometamol, citric acid or its salts (e.g., sodium citrate), phosphoric acid or its salts (e.g., sodium hydrogen phosphate, sodium dihydrogen phosphate), tartaric acid or its salts (e.g., sodium tartrate), gluconic acid or its salts (e.g., sodium gluconate), acetic acid or its salts (e.g., sodium acetate), carbonic acid or its salts (e.g., sodium hydrogen carbonate), and various amino acids (epsilon-aminocaproic acid, potassium aspartate, aminoethylsulfonic acid, glutamic acid, sodium glutamate). Among these, boric acid, borax, and trometamol are preferred. When a buffering agent is added, the content in the composition is preferably 0.001 to 5.0 w/v%, more preferably 0.001 to 2 w/v%, and even more preferably 0.001 to 1 w/v%.
pH調整剤としては、例えば、無機酸又は無機アルカリ剤が挙げられる。具体的には、無機酸としては(希)塩酸が挙げられる。無機アルカリ剤としては、水酸化ナトリウム、水酸化カリウム、炭酸ナトリウム、炭酸水素ナトリウム等が挙げられる。組成物のpHは、涙液油層不安定化が引き起こす諸症状をより改善する点から、3.5~8.0が好ましく、5.5~8.0がより好ましい。なお、pHの測定は、25℃でpHメータ(HM-25R、東亜ディーケーケー(株))を用いて行う。 Examples of pH adjusters include inorganic acids and inorganic alkali agents. Specifically, an example of an inorganic acid is (dilute) hydrochloric acid. Examples of inorganic alkali agents include sodium hydroxide, potassium hydroxide, sodium carbonate, and sodium bicarbonate. The pH of the composition is preferably 3.5 to 8.0, and more preferably 5.5 to 8.0, from the viewpoint of further improving the various symptoms caused by destabilization of the tear lipid layer. The pH is measured at 25°C using a pH meter (HM-25R, DKK Toa Corporation).
等張化剤としては、例えば、塩化ナトリウム、塩化カリウム、塩化カルシウム、炭酸水素ナトリウム、炭酸ナトリウム、乾燥炭酸ナトリウム、硫酸マグネシウム、リン酸水素ナトリウム、リン酸二水素ナトリウム、リン酸二水素カリウム等が挙げられる。涙液油層不安定化が引き起こす諸症状をより改善する点から、塩化ナトリウム又は塩化カリウムを配合し、等張化されていることが好ましい。組成物の対生理食塩水浸透圧比は、0.60~2.00が好ましく、0.60~1.55がより好ましく、0.83~1.20が最も好ましい。なお、浸透圧の測定は、25℃で自動浸透圧計(A2O、アドバンスドインストルメンツ社)を用いて行う。 Examples of isotonicity agents include sodium chloride, potassium chloride, calcium chloride, sodium bicarbonate, sodium carbonate, dry sodium carbonate, magnesium sulfate, sodium hydrogen phosphate, sodium dihydrogen phosphate, potassium dihydrogen phosphate, etc. In order to further improve the symptoms caused by destabilization of the tear lipid layer, it is preferable to incorporate sodium chloride or potassium chloride to make the composition isotonic. The osmotic pressure ratio of the composition to physiological saline is preferably 0.60 to 2.00, more preferably 0.60 to 1.55, and most preferably 0.83 to 1.20. The osmotic pressure is measured at 25°C using an automatic osmometer (A2O, Advanced Instruments).
安定化剤としては、例えば、エデト酸ナトリウム、エデト酸ナトリウム水和物、シクロデキストリン、亜硫酸塩、ジブチルヒドロキシトルエン等が挙げられる。VA安定性の観点からエデト酸ナトリウム、エデト酸ナトリウム水和物、亜硫酸塩、ジブチルヒドロキシトルエンを配合することが好ましい。安定化剤を配合する場合の含有量は、組成物中0.001~5.0w/v%が好ましく、0.001~1w/v%がより好ましく、0.001~0.1w/v%がさらに好ましい。 Examples of stabilizers include sodium edetate, sodium edetate hydrate, cyclodextrin, sulfite, dibutylhydroxytoluene, etc. From the viewpoint of VA stability, it is preferable to incorporate sodium edetate, sodium edetate hydrate, sulfite, and dibutylhydroxytoluene. When a stabilizer is incorporated, the content in the composition is preferably 0.001 to 5.0 w/v%, more preferably 0.001 to 1 w/v%, and even more preferably 0.001 to 0.1 w/v%.
清涼化剤としては、例えば、メントール、カンフル、ボルネオール、ゲラニオール、シネオール、リナロール等が挙げられる。d体、l体又はdl体のいずれでもよい。清涼化剤を配合する場合の含有量は、組成物中0.0001~0.2w/v%が好ましい。 Examples of cooling agents include menthol, camphor, borneol, geraniol, cineol, linalool, etc. Any of the d-, l- or dl-isomers may be used. When a cooling agent is added, the content is preferably 0.0001 to 0.2 w/v% in the composition.
多価アルコールとしては、例えば、グリセリン、ブチレングリコール、ポリエチレングリコール等が挙げられる。中でも、グリセリン、ブチレングリコール、ポリエチレングリコールが好ましい。多価アルコールを配合する場合の含有量は、眼科用組成物中0.001~5.0w/v%が好ましく、0.001~1w/v%がより好ましく、0.001~0.1w/v%がさらに好ましい。 Examples of polyhydric alcohols include glycerin, butylene glycol, and polyethylene glycol. Among these, glycerin, butylene glycol, and polyethylene glycol are preferred. When polyhydric alcohols are included, their content in the ophthalmic composition is preferably 0.001 to 5.0 w/v%, more preferably 0.001 to 1 w/v%, and even more preferably 0.001 to 0.1 w/v%.
粘稠剤としては、例えば、ポリビニルピロリドン、ヒドロキシエチルセルロース、ヒドロキシプロピルメチルセルロース、メチルセルロース、ポリビニルアルコール、ヒアルロン酸ナトリウム、ポリアクリル酸、カルボキシビニルポリマー等が挙げられる。粘稠剤を配合する場合、その含有量は組成物中0.001~5.0w/v%が好ましく、0.001~1w/v%がより好ましく、0.001~0.1w/v%がさらに好ましい。 Examples of thickening agents include polyvinylpyrrolidone, hydroxyethyl cellulose, hydroxypropyl methylcellulose, methyl cellulose, polyvinyl alcohol, sodium hyaluronate, polyacrylic acid, carboxyvinyl polymer, etc. When a thickening agent is added, its content in the composition is preferably 0.001 to 5.0 w/v%, more preferably 0.001 to 1 w/v%, and even more preferably 0.001 to 0.1 w/v%.
防腐剤としては、塩化ベンザルコニウム、塩化ベンゼトニウム、ソルビン酸、チメロサール、フェニルエチルアルコール、アルキルアミノエチルグリシン、クロルヘキシジン、グルコン酸、パラオシキ安息香酸メチル、パラオキシ安息香酸エチル等が挙げられる。これらは、組成物中0.005w/v%以下が好ましく、0.001w/v%以下がより好ましく、0.0001w/v%以下がさらに好ましく、配合しなくてもよい。かわき目やドライアイ症状を有する場合、またその予防のためには、防腐剤を配合しないことが好ましい。 Preservatives include benzalkonium chloride, benzethonium chloride, sorbic acid, thimerosal, phenylethyl alcohol, alkylaminoethylglycine, chlorhexidine, gluconic acid, methyl parahydroxybenzoate, and ethyl parahydroxybenzoate. These are preferably present in an amount of 0.005 w/v% or less in the composition, more preferably 0.001 w/v% or less, and even more preferably 0.0001 w/v% or less, and may not be included at all. If you have dry eyes or dry eye symptoms, or if you want to prevent dry eyes, it is preferable not to include a preservative.
油性成分としては、流動パラフィン、ヒマシ油、大豆油、オリーブ油、ゴマ油、コーン油、ヤシ油、アーモンド油、中鎖脂肪酸トリグリセリド、白色ワセリン、ミックストコフェロール、流動パラフィン、ワックスエステル、ステロールエステル等が挙げられる。油成分を配合する場合その含有量は、組成物中0.001~1.0w/v%が好ましく、0.001~0.5w/v%がより好ましく、0.001~0.25w/v%がさらに好ましい。 Examples of oily components include liquid paraffin, castor oil, soybean oil, olive oil, sesame oil, corn oil, coconut oil, almond oil, medium-chain fatty acid triglycerides, white petrolatum, mixed tocopherols, liquid paraffin, wax esters, sterol esters, etc. When an oil component is added, its content in the composition is preferably 0.001 to 1.0 w/v%, more preferably 0.001 to 0.5 w/v%, and even more preferably 0.001 to 0.25 w/v%.
薬物(薬学的有効成分)としては、例えば、充血除去成分(例えば、エピネフリン、塩酸エピネフリン、エフェドリン塩酸塩、ナファゾリン塩酸塩、ナファゾリン硝酸塩、dl-メチルエフェドリン塩酸塩等)、消炎・収斂剤(例えば、イプシロン-アミノカプロン酸、アラントイン、アズレンスルホン酸ナトリウム、硫酸亜鉛、乳酸亜鉛、リゾチーム塩酸塩等)、抗ヒスタミン剤等、水溶性ビタミン類(フラビンアデニンジヌクレオチドナトリウム、シアノコバラミン、ピリドキシン塩酸塩、パンテノール、パントテン酸カルシウム、パントテン酸ナトリウム等)、アミノ酸類(例えば、L-アスパラギン酸カリウム、L-アスパラギン酸マグネシウム、L-アスパラギン酸カリウム・マグネシウム(等量混合物)、アミノエチルスルホン酸等)、サルファ剤等が挙げられる。薬物を配合する場合、薬物の含有量は、各薬物の有効な適性量を選択することができるが、組成物中0.001~5w/v%が好ましく、0.001~1w/v%がより好ましく、0.001~0.1w/v%がさらに好ましい。 Examples of drugs (pharmacologically active ingredients) include congestion relief ingredients (e.g., epinephrine, epinephrine hydrochloride, ephedrine hydrochloride, naphazoline hydrochloride, naphazoline nitrate, dl-methylephedrine hydrochloride, etc.), anti-inflammatory/astringent agents (e.g., epsilon-aminocaproic acid, allantoin, sodium azulene sulfonate, zinc sulfate, zinc lactate, lysozyme hydrochloride, etc.), antihistamines, water-soluble vitamins (sodium flavin adenine dinucleotide, cyanocobalamin, pyridoxine hydrochloride, panthenol, calcium pantothenate, sodium pantothenate, etc.), amino acids (e.g., potassium L-aspartate, magnesium L-aspartate, potassium and magnesium L-aspartate (mixture of equal parts), aminoethylsulfonic acid, etc.), and sulfa drugs. When drugs are included, the content of each drug can be selected based on the effective amount of the drug, but it is preferably 0.001 to 5 w/v% in the composition, more preferably 0.001 to 1 w/v%, and even more preferably 0.001 to 0.1 w/v%.
水としては、精製水、滅菌水等を用いることができ、水の含有量は、組成物の残部とすることができる。具体的には、組成物中90~99.9w/v%が好ましく、93~98w/v%がより好ましい。 Purified water, sterilized water, etc. can be used as the water, and the content of water can be the remainder of the composition. Specifically, the content of water in the composition is preferably 90 to 99.9 w/v %, and more preferably 93 to 98 w/v %.
[眼科用組成物]
本発明の眼科用組成物の透過率は90~100%が好ましい。本発明の透過率は、分光光度計(例えば、UV-1800、(株)島津製作所)を用いて測定した波長600nmの透過率をいう。
[Ophthalmic composition]
The transmittance of the ophthalmic composition of the present invention is preferably 90 to 100%. The transmittance in the present invention refers to the transmittance at a wavelength of 600 nm measured using a spectrophotometer (e.g., UV-1800, Shimadzu Corporation).
本発明の眼科用組成物は目への適応を容易にする点から液体が好ましく、25℃における粘度は、20mPa・s以下が好ましく、10mPa・s以下がより好ましく、5mPa・s以下がさらに好ましい。なお、粘度の測定方法はコーンプレート型粘度計(DV2T、英弘精機(株))を用いて行う。 The ophthalmic composition of the present invention is preferably a liquid in order to facilitate application to the eye, and the viscosity at 25°C is preferably 20 mPa·s or less, more preferably 10 mPa·s or less, and even more preferably 5 mPa·s or less. The viscosity is measured using a cone-plate viscometer (DV2T, Eiko Seiki Co., Ltd.).
本発明の眼科用組成物は、そのまま液剤としてもよく、ゲル剤等に調製してもよい。使用形態としては、具体的には点眼剤(例えば、一般用点眼剤、コンタクトレンズ用点眼剤等)、洗眼剤(一般用洗眼剤、コンタクトレンズをはずした後に使用する洗眼剤等)、コンタクトレンズ装着液、コンタクト取り出し液等が挙げられる。中でも、コンタクトレンズ用点眼剤、コンタクトレンズをはずした後に使用する洗眼剤、コンタクトレンズ装着液、コンタクト取り出し液等のコンタクトレンズ用眼科用組成物として好適である。ソフトコンタクトレンズとしては、ハードコンタクトレンズ、O2ハードコンタクトレンズ、ソフトコンタクトレンズ、シリコーンハイドロゲルコンタクトレンズ等特に限定されない。 The ophthalmic composition of the present invention may be prepared as a liquid formulation or as a gel formulation. Specific examples of the form of use include eye drops (e.g., general eye drops, eye drops for contact lenses, etc.), eyewash (general eyewash, eyewash used after removing contact lenses, etc.), contact lens wetting solution, contact lens removal solution, etc. Among these, the ophthalmic composition is suitable as a contact lens ophthalmic composition such as contact lens eye drops, eyewash used after removing contact lenses, contact lens wetting solution, contact lens removal solution, etc. Soft contact lenses are not particularly limited to hard contact lenses, O2 hard contact lenses, soft contact lenses, silicone hydrogel contact lenses, etc.
本発明の眼科用組成物は、点眼剤又はコンタクトレンズ用点眼剤として使用する場合、1回につき10~100μLを1~3滴、1日につき1~6回点眼することが好ましく、1回につき10~50μLを1~3滴、1日につき1~6回がより好ましい。1回につき10~30μLを1~3滴1日につき1~6回がさらに好ましい。洗眼剤として使用する場合、1回につき3~6mL、1日につき3~6回洗眼することが好ましい。 When the ophthalmic composition of the present invention is used as eye drops or eye drops for contact lenses, it is preferable to instill 10-100 μL at 1-3 drops per time, 1-6 times per day, more preferably 10-50 μL at 1-3 drops per time, 1-6 times per day. It is even more preferable to instill 10-30 μL at 1-3 drops per time, 1-6 times per day. When used as an eyewash, it is preferable to wash the eyes with 3-6 mL at a time, 3-6 times per day.
また、本発明は、凍結融解を繰り返すことによる、眼科用組成物の透過率悪化を抑制する下記方法を提供する。
(A)ベルベリン又はその塩、
(B)(B1)ビタミンA及び(B2)ビタミンEから選ばれる1種以上、
(D)ノニオン界面活性剤
を含有する眼科用組成物に、(C)フェニレフリン又はその塩を配合する、凍結融解を繰り返すことによる、上記眼科用組成物の透過率悪化を抑制する方法。この方法において、好適な成分及び含有量等は上記と同じである。
The present invention also provides the following method for suppressing deterioration in the transmittance of an ophthalmic composition caused by repeated freezing and thawing.
(A) berberine or a salt thereof,
(B) one or more selected from (B1) vitamin A and (B2) vitamin E;
A method for suppressing deterioration of the transmittance of an ophthalmic composition caused by repeated freezing and thawing, comprising blending (C) phenylephrine or a salt thereof with an ophthalmic composition containing (D) a nonionic surfactant. In this method, the preferred components and contents thereof are the same as those described above.
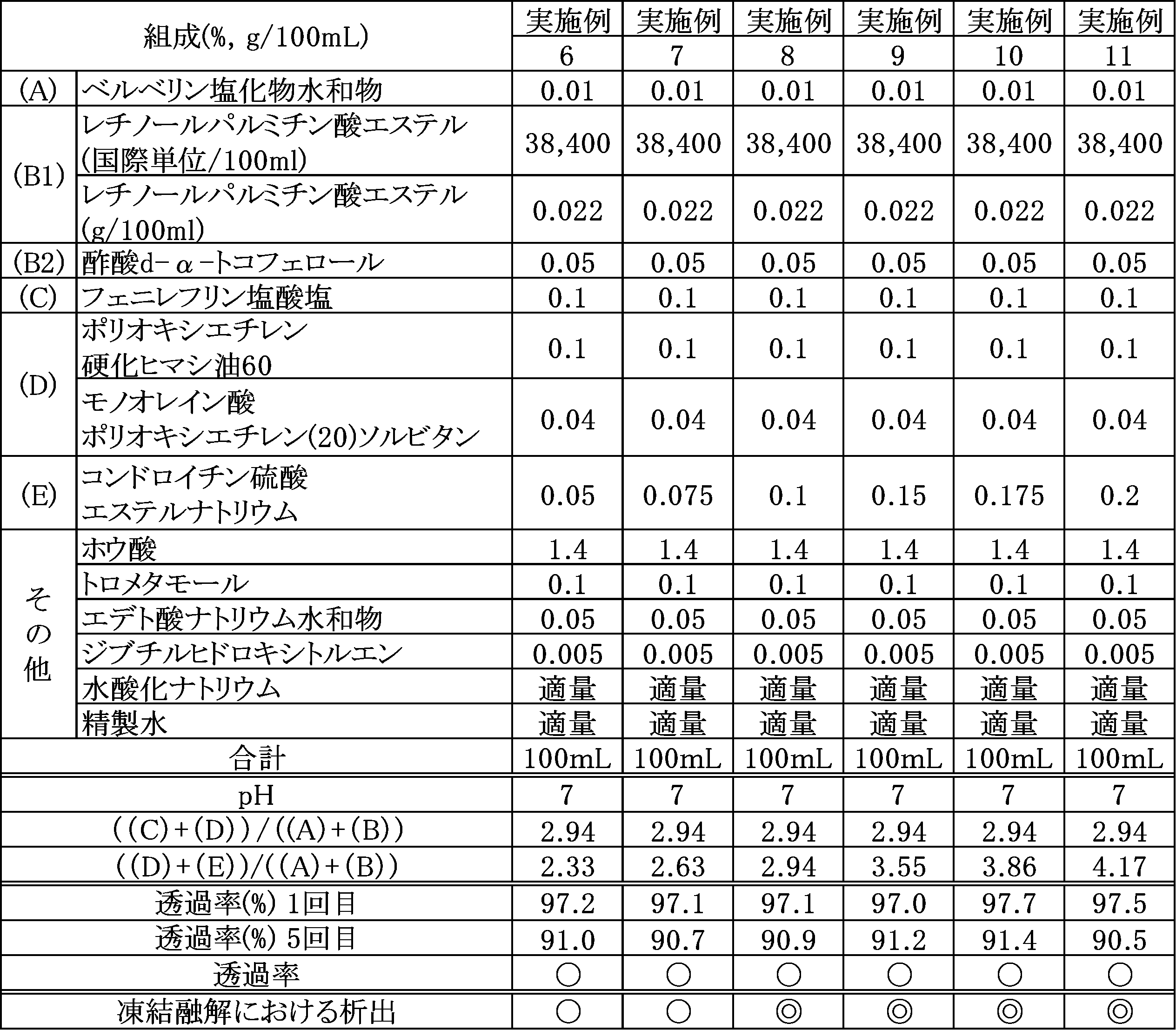
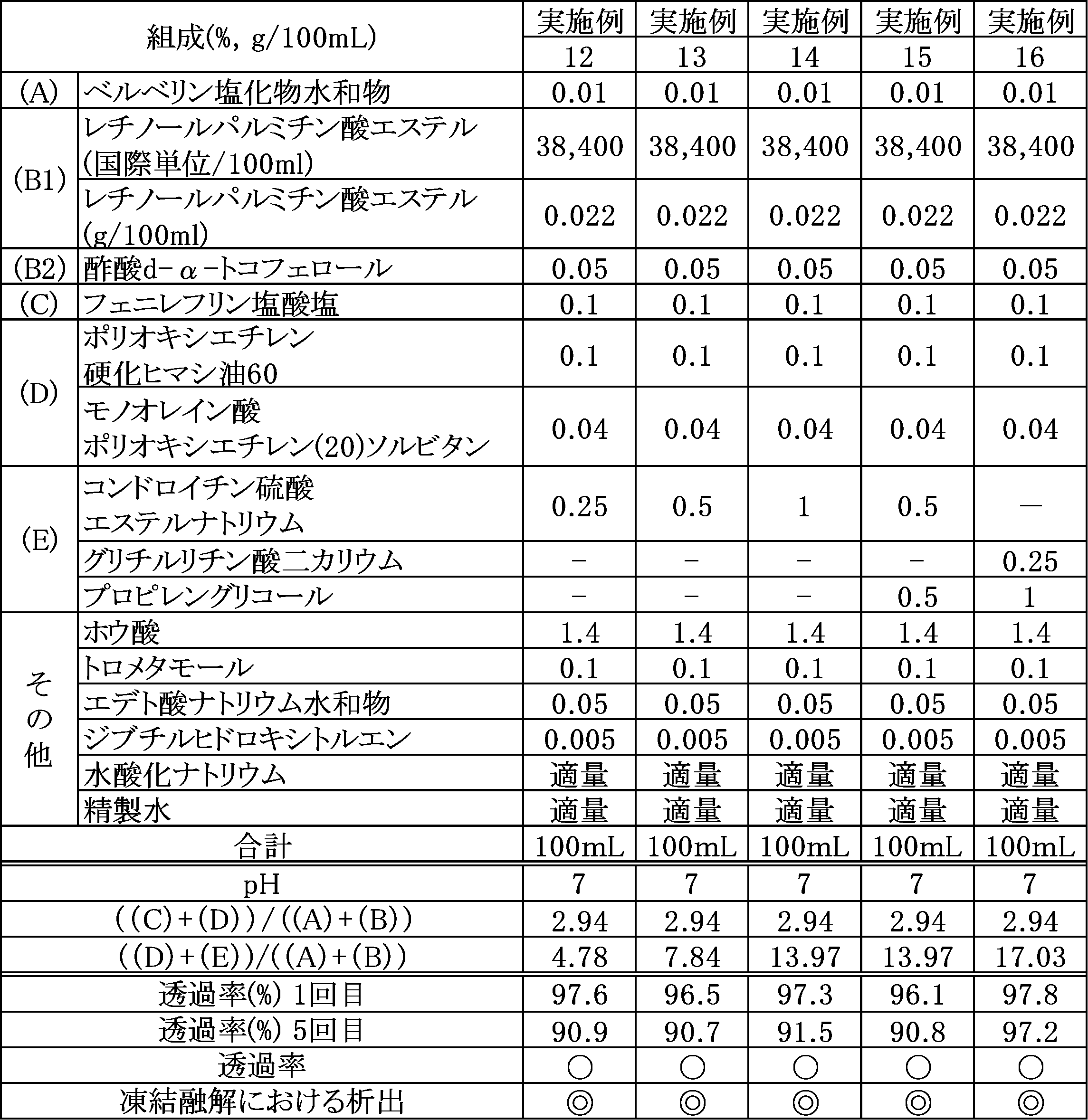
以下、実施例及び比較例を示し、本発明を具体的に説明するが、本発明は下記の実施例に制限されるものではない。組成の「%」はw/v%(g/100mL)、組成の「%」はw/v%、比率は質量比(w/v%比と同じ値)を示す。なお、実施例1~7は参考例である。 The present invention will be specifically described below with reference to examples and comparative examples, but the present invention is not limited to the following examples. The "%" of the composition indicates w/v% (g/100 mL), the "%" of the composition indicates w/v%, and the ratio indicates the mass ratio (the same value as the w/v% ratio). Examples 1 to 7 are reference examples.
[実施例、比較例]
下記表に示す各水性成分を1,000mLの水に溶解し、90℃、15分間加温混合して水性成分水溶液を得た。別途、(B)成分及び(D)成分の混合溶液を作製し、90℃、15分間加熱混合した。次に、(B)成分及び(D)成分の混合溶液を上記水性成分水溶液に所定量加え、さらに90℃、15分間加熱混合した。同時に、(A)成分及び(C)成分の混合溶液を作製し40℃、10分間加温混合した。(A)成分及び(C)成分の混合溶液を上記水性成分水溶液に所定量加え混合した。その後、室温まで冷却し、1,000mLになるように水を加え、眼科用組成物を得た。なお、表中は100mL中の量で示す。得られた眼科用組成物について、下記評価を行った。結果を表中に併記する。
[Examples and Comparative Examples]
Each aqueous component shown in the table below was dissolved in 1,000 mL of water and mixed at 90° C. for 15 minutes to obtain an aqueous component solution. Separately, a mixed solution of components (B) and (D) was prepared and mixed at 90° C. for 15 minutes. Next, a predetermined amount of the mixed solution of components (B) and (D) was added to the aqueous component solution, and further mixed at 90° C. for 15 minutes. At the same time, a mixed solution of components (A) and (C) was prepared and mixed at 40° C. for 10 minutes. A predetermined amount of the mixed solution of components (A) and (C) was added to the aqueous component solution and mixed. Then, the mixture was cooled to room temperature, and water was added to make the total volume 1,000 mL to obtain an ophthalmic composition. The amount in 100 mL is shown in the table. The obtained ophthalmic composition was evaluated as follows. The results are also shown in the table.
[透過率(%)]
製造直後の眼科用組成物13mLをポリエチレンテレフタレート製点眼剤容器(15mL)に充填し試験サンプルとした。凍結(-20℃)・融解(25℃)の操作を5回繰り返し、以下を評価した。
[透過率(%)]
凍結後、融解させ、3日間室温暗所にて静置した後、紫外可視近赤外分光光度計(UV-1800、(株)島津製作所)を用いて、各試験サンプルの透過率(波長:600nm)を測定した。5回目の凍結融解において、90%以上の透過率の試験サンプルを「〇」(合格)とし、90%未満の場合「×」(不合格)とした。
[Transmittance (%)]
Immediately after production, 13 mL of the ophthalmic composition was filled into a polyethylene terephthalate eye drop container (15 mL) to prepare a test sample. The freezing (-20°C)/thawing (25°C) operation was repeated five times, and the following evaluations were performed.
[Transmittance (%)]
After freezing and thawing, the samples were allowed to stand in a dark place at room temperature for 3 days, and then the transmittance (wavelength: 600 nm) of each test sample was measured using an ultraviolet-visible-near infrared spectrophotometer (UV-1800, Shimadzu Corporation). Test samples with a transmittance of 90% or more after the fifth freeze-thaw were rated as "◯" (pass), and samples with a transmittance of less than 90% were rated as "×" (fail).
[凍結融解における析出(沈殿の有無)]
1~5回の凍結融解を繰り返し、全ての凍結融解後において沈殿物の有無を目視にて確認した。1~5回のいずれかの凍結融解後にて、顕著な沈殿が認められた場合は「×」、軽微な沈殿が認められた場合は「〇」、沈殿が全く認められなかった場合は「◎」と判断した。なお、析出物を分析したところ、(A)成分のベルベリンを含むことを確認した。
[Precipitation during freezing and thawing (presence or absence of precipitation)]
The samples were repeatedly frozen and thawed 1 to 5 times, and the presence or absence of precipitate was visually confirmed after each freeze-thaw. After any of the freeze-thaw cycles, the samples were judged as "X" if significant precipitate was observed, "O" if slight precipitate was observed, and "◎" if no precipitate was observed. Analysis of the precipitate confirmed that it contained berberine, the component (A).
上記例で使用した原料を下記に示す。なお、特に明記がない限り、表中の各成分の量は純分換算量である。
ベルベリン塩化物水和物(日局 ベルベリン塩化物水和物、アルプス薬品工業社製)
レチノールパルミチン酸エステル(レチノールパルミチン酸エステル[174万I.U./g)]、DSM社製)
酢酸d-α-トコフェロール(理研Eアセテートα、理研ビタミン社製)
フェニレフリン塩酸塩:日本薬局方 フェニレフリン塩酸塩、岩城製薬社製
ポリオキシエチレン硬化ヒマシ油60(HCO60、日本サーファクタント工業社製)
モノオレイン酸ポリオキシエチレン(20)ソルビタン(レオドールTW-O120V、花王社製)
コンドロイチン硫酸エステルナトリウム(局外規 コンドロイチン硫酸ナトリウム、マルハニチロ社製)
プロピレングリコール(日本薬局方 プロピレングリコール、ADEKA社製)
グリチルリチン酸二カリウム(局外規 グリチルリチン酸二カリウム、丸善製薬社製)
The raw materials used in the above examples are shown below. Unless otherwise specified, the amounts of each component in the table are calculated as pure amounts.
Berberine chloride hydrate (JP Berberine chloride hydrate, manufactured by Alps Pharmaceutical Co., Ltd.)
Retinol palmitate (retinol palmitate [1.74 million IU/g], manufactured by DSM)
d-α-tocopherol acetate (Riken E Acetate α, manufactured by Riken Vitamin Co., Ltd.)
Phenylephrine hydrochloride: Japanese Pharmacopoeia Phenylephrine Hydrochloride, manufactured by Iwaki Pharmaceutical Co., Ltd. Polyoxyethylene hydrogenated castor oil 60 (HCO60, manufactured by Nippon Surfactant Kogyo Co., Ltd.)
Polyoxyethylene (20) sorbitan monooleate (Rheodol TW-O120V, manufactured by Kao Corporation)
Sodium chondroitin sulfate (non-regulated sodium chondroitin sulfate, manufactured by Maruha Nichiro Co., Ltd.)
Propylene glycol (Japanese Pharmacopoeia Propylene Glycol, manufactured by ADEKA Corporation)
Dipotassium glycyrrhizinate (non-regulated dipotassium glycyrrhizinate, manufactured by Maruzen Pharmaceuticals)
Claims (6)
(B)(B1)ビタミンA及び(B2)ビタミンEから選ばれる1種以上、
(C)フェニレフリン又はその塩、
(D)ノニオン界面活性剤、及び
(E)コンドロイチン硫酸及びその塩、グリチルリチン酸及びその塩、ならびにプロピレングリコールから選ばれる1種以上
を含有し、
(A)成分の含有量が、0.01~0.025w/v%、
(B)成分の含有量が、0.01~0.09w/v%、
(C)成分の含有量が、0.1~0.6w/v%、
(D)成分の含有量が、0.14~0.56w/v%、及び
(E)成分の含有量が、0.1~1.25w/v%
である眼科用組成物。 (A) berberine or a salt thereof,
(B) one or more selected from (B1) vitamin A and (B2) vitamin E;
(C) phenylephrine or a salt thereof,
(D) a nonionic surfactant , and
(E) one or more selected from chondroitin sulfate and its salts, glycyrrhizinic acid and its salts, and propylene glycol
Contains
The content of the component (A) is 0.01 to 0.025 w/v%,
The content of the component (B) is 0.01 to 0.09 w/v%,
The content of the component (C) is 0.1 to 0.6 w/v%,
The content of the component (D) is 0.14 to 0.56 w/v%, and
The content of the component (E) is 0.1 to 1.25 w/v%
13. An ophthalmic composition comprising :
(B1)成分の含有量が、0.02~0.04w/v%、The content of the component (B1) is 0.02 to 0.04 w/v%,
(B2)成分の含有量が、0.02~0.05w/v%、The content of the component (B2) is 0.02 to 0.05 w/v%,
である請求項1又は2記載の眼科用組成物。3. The ophthalmic composition according to claim 1 or 2,
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2020214997A JP7676769B2 (en) | 2020-12-24 | 2020-12-24 | Ophthalmic composition |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2020214997A JP7676769B2 (en) | 2020-12-24 | 2020-12-24 | Ophthalmic composition |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2022100796A JP2022100796A (en) | 2022-07-06 |
| JP7676769B2 true JP7676769B2 (en) | 2025-05-15 |
Family
ID=82271187
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020214997A Active JP7676769B2 (en) | 2020-12-24 | 2020-12-24 | Ophthalmic composition |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP7676769B2 (en) |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2005247798A (en) | 2004-03-08 | 2005-09-15 | Zeria Pharmaceut Co Ltd | Eye drops |
| JP2005272461A (en) | 2004-02-27 | 2005-10-06 | Taisho Pharmaceut Co Ltd | Eye drops |
| JP2012144509A (en) | 2011-01-12 | 2012-08-02 | Saga Seiyaku Kk | Ophthalmic solution compounded with many ingredients |
| JP2018118964A (en) | 2017-01-20 | 2018-08-02 | ロート製薬株式会社 | Ophthalmic composition |
| JP2020015683A (en) | 2018-07-25 | 2020-01-30 | ライオン株式会社 | Ophthalmic composition and method for suppressing precipitation |
| JP2020105086A (en) | 2018-12-26 | 2020-07-09 | ライオン株式会社 | Ophthalmic composition |
-
2020
- 2020-12-24 JP JP2020214997A patent/JP7676769B2/en active Active
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2005272461A (en) | 2004-02-27 | 2005-10-06 | Taisho Pharmaceut Co Ltd | Eye drops |
| JP2005247798A (en) | 2004-03-08 | 2005-09-15 | Zeria Pharmaceut Co Ltd | Eye drops |
| JP2012144509A (en) | 2011-01-12 | 2012-08-02 | Saga Seiyaku Kk | Ophthalmic solution compounded with many ingredients |
| JP2018118964A (en) | 2017-01-20 | 2018-08-02 | ロート製薬株式会社 | Ophthalmic composition |
| JP2020015683A (en) | 2018-07-25 | 2020-01-30 | ライオン株式会社 | Ophthalmic composition and method for suppressing precipitation |
| JP2020105086A (en) | 2018-12-26 | 2020-07-09 | ライオン株式会社 | Ophthalmic composition |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2022100796A (en) | 2022-07-06 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5549669B2 (en) | Ophthalmic composition, dry eye treatment and method for stabilizing vitamin A | |
| US9119827B2 (en) | Ophthalmic composition | |
| JP3142842B1 (en) | Ophthalmic composition and method for suppressing adsorption to soft contact lens | |
| JP5729109B2 (en) | Ophthalmic composition for soft contact lenses | |
| JP2009173638A (en) | Ophthalmic composition and method for stabilizing vitamin A | |
| JP6260230B2 (en) | Ophthalmic composition | |
| JP5800072B2 (en) | Ophthalmic composition and method for suppressing cloudiness / precipitation | |
| CN102481268B (en) | Ophthalmic composition and method for prevention of cloudiness/precipitation | |
| JP2013181020A (en) | Ophthalmic composition | |
| JP7310113B2 (en) | Ophthalmic composition, method for producing the same, and method for suppressing adsorption | |
| JP7238773B2 (en) | OPHTHALMIC COMPOSITION FOR SOFT CONTACT LENS AND METHOD FOR PREVENTING VITAMIN A SEPARATION | |
| JP7014078B2 (en) | Ophthalmic composition and precipitation suppression method | |
| JP4844706B2 (en) | Ophthalmic composition | |
| JP2011246383A (en) | Ophthalmologic formulation for alleviation of tired eyes of contact lens wearer | |
| JP7676769B2 (en) | Ophthalmic composition | |
| JP2011207874A (en) | Ophthalmic composition for soft contact lens | |
| WO2021246172A1 (en) | Ophthalmic composition, photostabilization method and method for suppressing discoloration | |
| JP7379913B2 (en) | Ophthalmic compositions and products for soft contact lenses | |
| JP7459508B2 (en) | Mucin degeneration inhibitor and ophthalmic composition | |
| JP2024064436A (en) | Ophthalmic Composition | |
| JP2025073773A (en) | Ophthalmic composition | |
| JP2024065059A (en) | Ophthalmic Composition | |
| JP2024107483A (en) | Ophthalmic Composition | |
| JP2021104969A (en) | Friction reducer and ophthalmic composition | |
| TW201100071A (en) | Ophthalmic composition and vitamin A stabilization method |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20231205 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20241029 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20241030 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20241224 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20250401 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20250414 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7676769 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |