JP7235772B2 - 選択的Treg刺激因子RUR20kD-IL-2及び関連組成物 - Google Patents
選択的Treg刺激因子RUR20kD-IL-2及び関連組成物 Download PDFInfo
- Publication number
- JP7235772B2 JP7235772B2 JP2020564540A JP2020564540A JP7235772B2 JP 7235772 B2 JP7235772 B2 JP 7235772B2 JP 2020564540 A JP2020564540 A JP 2020564540A JP 2020564540 A JP2020564540 A JP 2020564540A JP 7235772 B2 JP7235772 B2 JP 7235772B2
- Authority
- JP
- Japan
- Prior art keywords
- composition
- pegylated
- rur
- cells
- conjugate
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/56—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule
- A61K47/59—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyureas or polyurethanes
- A61K47/60—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyureas or polyurethanes the organic macromolecular compound being a polyoxyalkylene oligomer, polymer or dendrimer, e.g. PEG, PPG, PEO or polyglycerol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/19—Cytokines; Lymphokines; Interferons
- A61K38/20—Interleukins [IL]
- A61K38/2013—IL-2
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/02—Inorganic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/10—Alcohols; Phenols; Salts thereof, e.g. glycerol; Polyethylene glycols [PEG]; Poloxamers; PEG/POE alkyl ethers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/12—Carboxylic acids; Salts or anhydrides thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/26—Carbohydrates, e.g. sugar alcohols, amino sugars, nucleic acids, mono-, di- or oligo-saccharides; Derivatives thereof, e.g. polysorbates, sorbitan fatty acid esters or glycyrrhizin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
- A61K9/0021—Intradermal administration, e.g. through microneedle arrays, needleless injectors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/08—Antiallergic agents
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Epidemiology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Immunology (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Dermatology (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Zoology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Gastroenterology & Hepatology (AREA)
- Inorganic Chemistry (AREA)
- Biochemistry (AREA)
- Molecular Biology (AREA)
- Pulmonology (AREA)
- Transplantation (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicinal Preparation (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Description
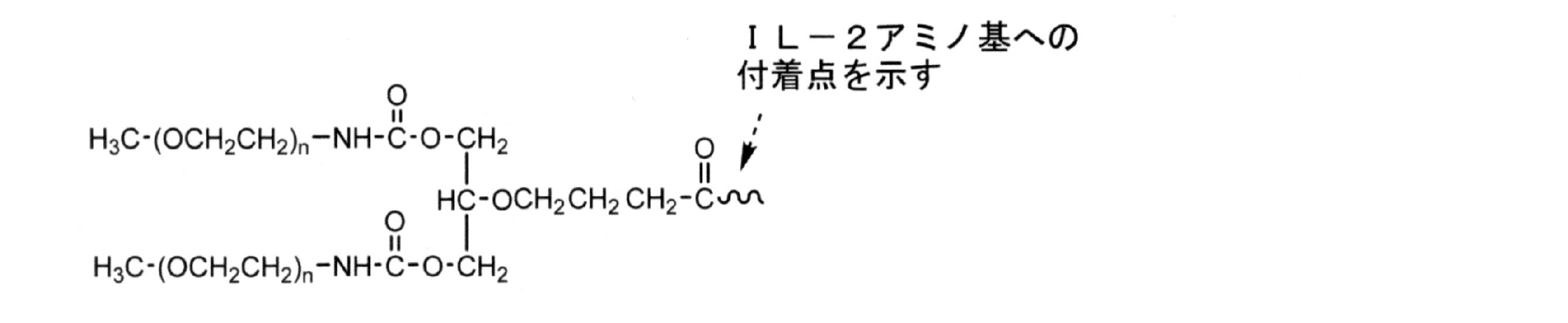
nは各出現で独立して約3~約4000の整数である)
を有するPEG化IL-2を含む組成物を提供する。
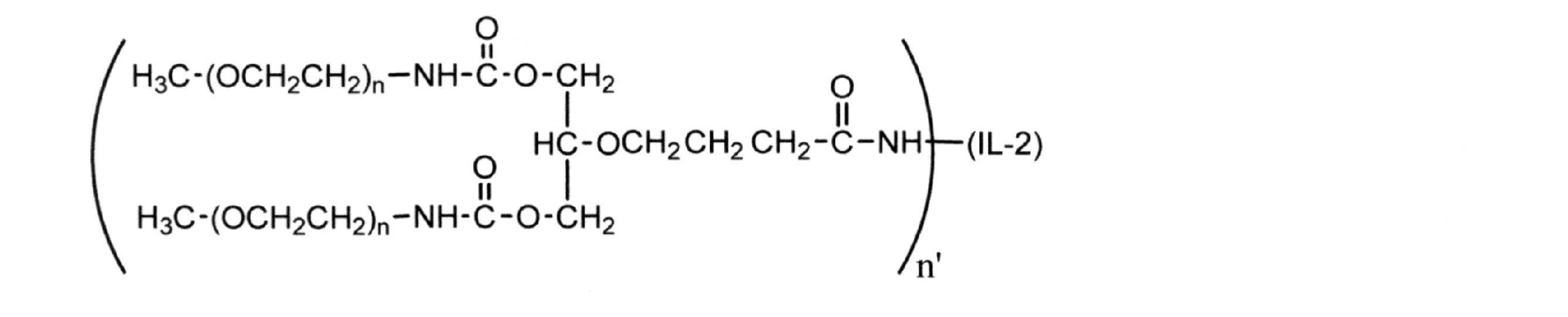
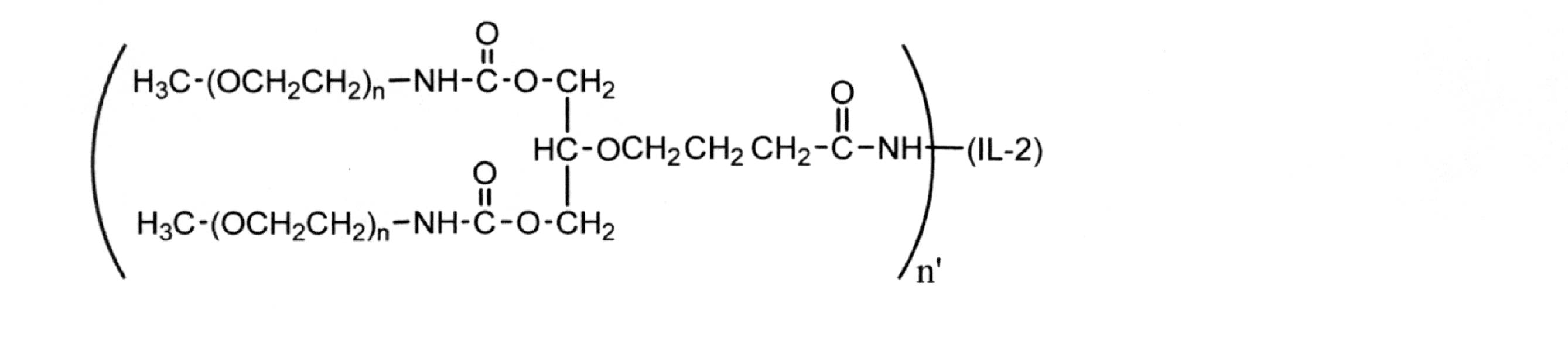
本明細書で提供される組成物は、nが2に等しいコンジュゲート、例えば、上に示す1,3-ビス(メトキシポリ(エチレングリコール)10kDカルバモイル)-2-プロパノキシ)-4-ブタノイル構造をそれぞれ有する2つの分岐ポリエチレングリコールポリマーが組成物中の実質的に全てのジ-PEG化IL-2コンジュゲートについて同じ相対位置に付着しているジ-PEG化コンジュゲートを含み得る。或いは、ジ-PEG化コンジュゲートは、ジ-PEG化コンジュゲートの混合物、例えば、分岐ポリエチレングリコール部分の付着がIL-2上の2つの部位で起こり、特定の付着部位が組成物に含まれる全てのジ-PEG化IL-2コンジュゲートについて同じではない、ジ-PEG化コンジュゲートの混合物を含み得る。したがって、かかるジ-PEG化組成物は、PEG化の程度、特に付着した分岐PEG部分の数(例えば、2-mer)に関しては均一であるが、IL-2分子上のPEG付着の位置に関しては不均一であり、この場合、PEG付着の位置異性体となる。
n’は1、4、5、又は5より大きい整数から選択される。
1、4、5、又は5より大きい整数から選択されるn’を有する。
1、4、5、又は5より大きい整数から選択されるn’を有する。
未修飾のIL-2とは対照的に、本明細書に記載のRUR20kD-IL-2の実施形態及び関連組成物を含む選択的Treg刺激因子組成物は、自己反応性免疫に関連する根底にある病理に対処し、並びに有益なT細胞機能をもたらす特定の機構を標的として、未修飾のIL-2の投与に比べて大幅な改善を提供する。既存の自己免疫疾患療法の欠陥に対処するため、本組成物は、投与時に持続的な曝露を提供し、独特の薬理学的プロファイルを有する。本発明の組成物は、in vivoで内因性Tregを選択的に拡大及び活性化し、従来のT細胞及び/又はナチュラルキラー細胞の拡大を制限して、それにより自己免疫疾患の治療のための優れたアプローチを提供する。
構造:
nは各出現で独立して約3~約4000の整数である)を有するPEG化IL-2を含む組成物を提供する。治療法で使用するための当該組成物の特定の実施形態では、IL-2はアルデスロイキンである。治療法で使用するための当該組成物の特定の実施形態では、各分岐ポリエチレングリコール部分の名目上の平均分子量は、約20000ダルトンである。治療法で使用するための当該組成物の更なる特定の実施形態では、組成物のPEG化IL-2コンジュゲートは、リジン31に付着したPEG部分を有する。治療法で使用するための当該組成物の特定の実施形態では、治療法は自己免疫疾患に使用するためのものである。
本開示の特定の特徴を説明及び主張する際に、以下の用語は、別段の指定がない限り、以下に記載される定義に従って使用される。
「Tcon」又は「従来のT細胞」という用語は、aβT細胞受容体(TCR)、並びに共受容体CD4又はCD8を発現し、Tヘルパー細胞機能及び細胞傷害性T細胞エフェクター機能等の確立された適応免疫エフェクター機能を実行するTリンパ球を指す。例えば、TconはCD4+CD25-ナイーブな従来のT細胞を指す場合がある。「エフェクターT細胞(Teff)」は、当業者に知られているように、ヘルパーT細胞、細胞傷害性T細胞等のCD4+及びCD8+細胞エフェクター表現型を指す。「ナチュラルキラー細胞」、「K細胞」、又は「キラー細胞」としても知られる「NK細胞」は、リンパ球(白血球)の一種であり、自然免疫系の構成要素である。NK細胞は、腫瘍やウイルスに感染した細胞の宿主拒絶反応において主要な役割を果たす。
調製及び実施例は、限定ではなく例示として記載されており、当業者によって様々な修正を加えることができることを理解されたい。RUR20kD-IL-2の実施形態及び関連組成物を含む、選択的Treg刺激因子組成物を調製する方法は、本明細書に記載され、及び/又は当業者に知られている。試薬及び開始物質は、容易に入手可能であるか、又は当業者によって容易に合成され得る。これらの方法の工程に適した条件はよく知られており、緩衝液及び試薬の適切な置換は当業者の範囲内である。更に、当業者は、幾つかの状況では、組成物が製造される工程及び順序が変更されてもよく、これは当業者によって十分に理解されることを理解するであろう。同様に、調製物は、必要に応じて又は所望に応じて、様々な周知の手法によって単離及び/又は精製され得ることが理解されるであろう。
IL-2部分は、非組換え法及び/又は組換え法から誘導することができ、本開示は、この点に関して限定されない。IL-2部分は、ヒト由来、動物由来、及び植物由来であり得る。例えば、生物学的システムからIL-2を単離すること、或いは培養培地からIL-2を得ることが可能である。例えば、米国特許第4,401,756号及びPaulyら(1984)J.Immunol Methods 75(1):73-84に記載されている手順を参照されたい。
RUR20kD-IL-2の例示的な選択的Treg刺激因子組成物は、一般に、約9の高pHのビシン溶液中で、精製IL-2をモル過剰(IL-2に関してモル当量の過剰)のPEG試薬、mPEG2(20kD)-ブタン酸、N-ヒドロキシスクシンイミドエステル(又は他の適切に活性化されたエステル)(1,3-ビス(メトキシポリ(エチレングリコール)MW10000カルバモイル)-2-プロパノキシ)-4-スクシンイミジルブタノエートと反応させることによって調製される。反応物を、一般に穏やかな条件下、例えば、約20℃~約65℃、又は約20℃~約40℃、又は周囲温度若しくは室温で約30分~約5時間、又は約30分~4時間、又は約30分~2時間、又は約30分~1時間混合する。反応は、酢酸等の適切な酸の添加による低pHへの酸性化によってクエンチされる。
本明細書で提供される更に1つ以上の実施形態は、RUR20kD-IL-2の実施形態及び関連組成物を含む選択的Treg刺激因子組成物であり、本明細書に記載のIL-2コンジュゲート組成物、及び薬学的に許容可能な賦形剤を含む。
本明細書で提供されるRUR20kD-IL-2の実施形態及び関連組成物を含む選択的Treg刺激因子組成物の投薬量は、幾つかの要因に応じて変化するが、組成物が単位用量容器(例えば、バイアル)に保管される場合、治療上有効な用量であることが最適である。更に、製剤は注射器に収容することができる。治療有効用量は、自己免疫症状及び/又は免疫抑制の緩和、及び/又は寛容の誘導等の本明細書に記載の臨床的に望ましいエンドポイントをもたらす量を決定するために、本明細書に提供されるRUR20kD-IL-2実施形態及び関連組成物を含む選択的Treg刺激因子組成物の漸増量の反復投与によって実験的に決定され得る。
本明細書で提供される組成物は、治療有効用量で被験体に投与された場合、CD4+細胞及びCD8+細胞等のエフェクターT細胞に対するFoxP3+細胞及びCD25+細胞等の制御性T細胞の比率を増加させるのに有用である。例えば、本明細書で提供されるRUR20kD-IL-2及び関連組成物を含む選択的Treg刺激因子組成物の投与は、ベースラインと比較され、例えば本明細書に記載されるようなin-vivoマウスモデルにおいて評価される場合、制御性T細胞の少なくとも2倍の増加をもたらすのに効果的であり得る。この方法はまた、幾つかの実施形態では、ベースラインと比較され、例えば本明細書に記載されるようなin-vivoマウスモデルにおいて評価される場合、制御性T細胞の少なくとも4倍の増加をもたらすのに有効であり得る。場合によっては、制御性T細胞数の増加は、投与後少なくとも3日間、又は更には投与後少なくとも5日間、ベースラインレベルを超えて持続する。
アルデスロイキン(デス-アラニル-1、セリン-125ヒトインターロイキン-2、図2を参照されたい)と同一のアミノ酸配列を有する組換えヒトIL-2をクローン化し、発現させ、使用して、ここではRUR20kD-IL-2と称される例示的な選択的Treg刺激因子組成物を調製する。この配列は、天然の成熟ヒトIL-2配列からアミノ酸#1(アラニン)を除外しており、アミノ酸#125にシステインからセリンへのアミノ酸変異がある。配列の第1のアミノ酸は、細菌を直接発現させるためのメチオニンである(シグナルペプチドはコードされていない)。発現すると、N末端メチオニンは宿主メチオニンアミノペプチダーゼによって除去される。単一のジスルフィド結合が、アミノ酸58位と105位とのシステイン間に形成される。このタンパク質は大腸菌に由来するため、グリコシル化されていない。一部の記載において、複合化されたIL-2組成物は、幾つかの点で(1,3-ビス(メトキシポリ(エチレングリコール)カルバモイル)-2-プロパノキシ)-4-ブタンアミド)インターロイキン-2)として記載する場合があり、この命名法はPEG化パターン又は混合物を完全に説明するものではないことに留意されたい。
RUR20kD-IL-2及び関連組成物の調製
mPEG2-ru-20K NHSのストック溶液(100mg/ml)を2mM HCl中に調製する。IL-2の典型的なPEG化反応を次のように行う:IL-2(アルデスロイキン)ストック溶液(1.3mg/ml)115mLを250mLのプラスチックボトルに移し、0.5Mビシン(N,N-ビス(2-ヒドロキシエチル)グリシン)15mL、pH9.2及び水0.5mLをIL-2の溶液に加える。PEG化を、19.5mLのmPEG2-ru-20K NHSストック溶液をIL-2含有溶液に滴下することで開始する。得られた反応混合物は、1mg/mlのIL-2、50mM ビシン、及び10モル当量のmPEG2-ru-20K NHS(タンパク質に関して)を含み、pHは8.7である。穏やかに攪拌しながら、反応を周囲温度で40分間進行させる。酢酸2.2mLを加えて反応物のpHを4.1に下げることにより、反応を停止する。
RUR20kD-IL-2及び関連組成物の代替の調製
所望のRUR20kD-IL-2及び関連組成物の調製は、rhIL-2タンパク質プロセス中間体の発酵及び精製、rhIL-2とPEG試薬開始物質mPEG2-ru-20K NHSとの複合化、特定の程度のPEG化を有するIL-2コンジュゲート画分の精製、並びに本明細書に記載の実施形態による所望の分布のRUR20kD-IL-2組成物を生成するためのPEG化rhIL-2コンジュゲートの最終の製剤化からなる。
逆相高速液体クロマトグラフィーによるRUR20kD-IL-2組成物の純度及び特性評価
ダイオードアレイ検出器(215nmのUV)を備えたAgilent 1200シリーズ機器を用いて、逆相高速液体クロマトグラフィー(RP-HPLC)を使用し、RUR20kD-IL-2組成のサンプルのクロマトグラフィー純度及び同一性を評定する。使用するカラムは、ACE 3 Phenyl-300カラム(Mac-Mod Analytical Inc.)(又は他の適切なカラム)で、溶離液の流量は0.6mL/分である。RP-HPLCは、2つの移動相:(1)移動相A、0.1%ギ酸水溶液、及び(2)移動相B、0.1%ギ酸のアセトニトリル溶液の混合物を含む勾配を使用し行われる。線形勾配は、60%移動相A/40%移動相Bから40%移動相A/60%移動相B、20%移動相A/80%移動相B、60%移動相A/40%移動相Bの範囲であった。希釈剤/配合バッファーの成分は、10mM酢酸ナトリウム、200mM塩化ナトリウム、2%スクロース、pH5.0である。
サイズ排除高速液体クロマトグラフィーによるRUR20kD-IL-2組成物の純度及び特性評価
ダイオードアレイ検出器(280nmのUV)及びYarraSEC-2000カラム(Phenomenex)を備えたAgilent1200シリーズ機器を用いて、0.225mL/分の溶離液流量で、サイズ排除高速液体クロマトグラフィー(SEC-HPLC)を使用し、RUR20kD-IL-2組成物の純度を決定し、特性評価をすることもできる。移動相は、アセトニトリルを含む80:20の体積比の0.2M酢酸アンモニウム(pH5.5)である。希釈剤/製剤バッファーは、10mM酢酸ナトリウム、200mM塩化ナトリウム、2%スクロースを含み、pHは5.0であった。
SDS-Page
SDS-PAGEを、RUR20kD-IL-2組成物の同一性の確認に利用する。RUR20kD-IL-2組成物のサンプル、分子量マーカー、及び適切なRUR20kD-IL-2組成物の標準物質を、NuPAGE Bis-Trisゲルにロードし、ゲル内を泳動させる。電気泳動後、GelCodeTM Blue Safe Protein Stainを使用してゲルを染色する。ゲル泳動のバンドパターンを標準物質と比較し、サンプルに新たなバンドがないことを確認すると、サンプルの同一性が確認される。最も強い2つのバンドは、トリ-PEG化画分とジ-PEG化画分に対応する。レーンの一番上のバンドはより高PEG化された変種に対応し、最も低いバンドはモノ-PEG化変種に対応する。
表面プラズモン共鳴(SPR)を使用したIL-2Rαβに対する親和性、及びヒトIL-2Rαβα複合体を発現するU-2 OS細胞における効力。
RUR20kD-IL-2組成物のPEG化部位占有率
2つのロットに由来するRUR20kD-IL-2組成物のPEG化部位占有率を、ペプチドマッピングによるRUR20kD-IL-2組成物とrhIL-2との直接比較によって特性評価する。RUR20kD-IL-2消化物において、リジン含有ペプチドはPEG化され得て、標準rhIL-2消化物中の同じペプチドと比較して、より少ない存在量を有する対応する天然のリジン含有ペプチドによって反映され得る。したがって、PEG化部位の占有率は、分析されたRUR20kD-IL-2消化物中の天然ペプチドの存在量の減少に基づいて計算することができる。更に、代用物質のペプチドマッピングを、部位占有率の追加確認に使用できる。
RUR20kD-IL-2組成の代用物として使用される物質は、単分散4kD PEGのrhIL-2のリジンへの複合化による結合生じる生成物である。RUR20kD-IL-2組成物のPEG化プロファイルを模倣するため、代用物を同じ複合化リンカーを使用して調製し、複合化反応を、RUR20kD-IL-2組成物を調製するために使用したのと同じ反応条件下で実施した。LC MS/MSベースのGluCマッピング及び代用物のトリプシンマッピングは、PEG化されたリジンを識別し、RUR20kD-IL-2を裏付ける情報を提供する。
RUR20kD-IL-2組成物におけるPEG化部位占有率:GMPロット及びDEMOロット
RUR20kD-IL-2組成物の液相安定性
RUR20kD-IL-2組成物(2%(重量/体積)スクロースを含む10mM酢酸ナトリウム、200mM塩化ナトリウム、pH5中の約1mg/mlのrhIL-2当量)1.0mg/mlの溶液の安定性を、室温(周囲実験室条件)、5℃(冷蔵)及び-20℃の3つの異なる保管条件下で、前述のようにRP-HPLCによって1、3、5及び7日間の時点で評価する。
in vitro法は、IL-2受容体複合体の代表である受容体の活性化後の生物学的活性を特性評価するための細胞ベースのアッセイを含む、RUR20kD-IL-2組成物の生物学的効力の更なる測定及び生物学的特性評価に使用され得る。
CTLL-2細胞増殖アッセイ
細胞増殖アッセイでは、サンプル及び標準を約26時間インキュベートした後、CTLL-2細胞を使用してin vitroで細胞増殖を測定し、ここでは細胞増殖は、発光アデノシン三リン酸ベースのアッセイ(CellTiter-Glo(登録商標)、ウィスコンシン州のPromega)で測定される。例えば、この細胞ベースの増殖アッセイでは、rhIL-2タンパク質に対して用量依存的な増殖応答を示すCTLL-2細胞株を使用する。rhIL-2はアッセイ対照として使用され、この方法ではRUR20kD-IL-2組成とは異なる濃度範囲で調製される。このアッセイを96ウェルプレートフォーマットで行う。CTLL-2細胞を飢餓培地でrhIL-2の飢餓状態にし、37℃及び5%CO2インキュベーター内で20±3時間一晩インキュベートする。飢餓状態の細胞を96ウェルプレートにプレーティングし、RUR20kD-IL-2組成物の希釈系列を細胞に供給し、37℃及び5%CO2インキュベーターで更に25±3時間インキュベートする。RUR20kD-IL-2組成により誘導される各ウェルの細胞増殖を、PromegaのCellTiterGlo(登録商標)検出キットを使用して測定する。CellTiterGlo(登録商標)は、各ウェルに存在するATPの量に比例する発光シグナルを生成し、これは、存在する生細胞に正比例する。発光シグナルをSpectramaxM5プレートリーダーで読み取る。RUR20kD-IL-2組成物の標準物質及び各サンプルの用量反応曲線を、発光シグナル(y軸)を濃度(x軸)に対してプロットすることによって生成する。プロットを、4パラメータのロジスティック非線形回帰モデルに適合させる。Parallel Line Analysis(PLA)ソフトウェアを使用して、回帰の有意性である勾配の差(平行度)に対する同等性試験を評定し、同じプレート内の標準物質に対するサンプルの効力比を計算する。
リン酸-STAT5の活性化
受容体結合後のリン酸化STAT5アッセイでは、下流の細胞シグナル伝達がリン酸化を介してシグナル伝達性転写因子5(STAT5)を活性化し、遺伝子発現を促進して細胞増殖を誘導する。リン酸-STAT5の活性化は、IL-2依存性マウスTリンパ球細胞株であるCTLL-2細胞において、サンプル及び標準の約10分間の処理に応答して、リン酸-STAT5/全STAT5マルチプレックスアッセイ(メリーランド州のMeso Scale Discovery)を使用して測定される。
in vivo研究:マウスにおける単回用量PK/PD研究
RUR20kD-IL-2組成物によるTregの選択的刺激を、マウスで実証することができる。C57BL/6マウス(n=4/群)に、0.03、0.1及び0.3mg/kgの用量のRUR20kD-IL-2組成物の単回皮下投与を行う。投与後、投与後1~7日目及び10日目に血液及び脾臓のサンプルを収集する。より具体的には、各時点で、血液及び脾臓のサンプルを収集し、サンプルをプールし、フローサイトメトリーによるリンパ球細胞集団に対する薬物作用の薬力学的分析について評定し(例えば、実施例5を参照されたい)、ビヒクル対照と比較した倍率変化として表す。細胞数の変化に加えて、機能マーカー及び活性マーカーを定量する。最後に、血漿薬物濃度も評定する。
in vitro Treg抑制アッセイ
この研究の目的は、制御性T細胞の阻害機能を評定することである。皮下投与後1日~7日及び10日に、ナイーブ及びRUR20kD-IL-2組成物で治療したC57BL/6マウスからTregを磁気的に分離する。Treg及びTconを1:2~1:512の範囲の比率で3日間共培養する。アッセイの最後の16時間に3H-チミジンの取り込みによって細胞増殖を評価し、プレート対照と比較した増殖細胞の割合を計算する。
マウスKLH DTH有効性モデルにおけるRUR20kD-IL-2組成物の評価
T細胞抗原による炎症を抑制するRUR20kD-IL-2組成物の投与によるTreg誘導の能力を評定するため、Balb/cマウス(n=6~10/群)を遅延型過敏症(DTH)のモデルで利用する。完全フロイントアジュバント(CFA)及び不完全フロイントアジュバントをそれぞれ1:1:1の比率で含むエマルションに、100μgのキーホールリンピットヘモシアニン(KLH)を含む100μlの皮下注射を用いて、マウスを背部の皮下で感作する。5日後、チャレンジの前にベースラインの耳介厚を測定し、左耳に10μgのKLHを皮内投与し、右耳は未治療のままにする。耳介厚の測定値を、全ての群でKLHチャレンジの24時間、48時間、72時間及び96時間後にキャリパーで測定する。RUR20kD-IL-2組成物を、感作時の0日目に、3日ごとに0.003mg/kg~0.3mg/kgの範囲の皮下用量で投与する。シクロスポリン(10mg/kg、単回用量)からなる陽性対照を0日目に投与した。
カニクイザルにおける単回用量研究
この研究では、雌1匹と雄1匹のカニクイザルに、25μg/kgのRUR20kD-IL-2組成物を皮下投与する。Treg細胞数と活性化状態のフローサイトメトリーによる評定のため、治療前(-6及び-1日目)と治療後の複数の間隔で各動物から一連の血液サンプルを採取する。
T細胞パネル:CD45/CD3/CD4/CD8/ICOS
T/B/NKパネル:CD45/CD3/CD16/CD20
pSTAT5パネル:CD3/CD4/CD8/CD25/CD127/pSTAT5
Tregパネル1:CD3/CD4/CD8/CD25/FoxP3/Ki67
Tregパネル2:CD3/CD4/CD8/CD25/FoxP3/Helios
コンピュータ化されたシステムを研究の実施に使用することができ、例えば、フローサイトメトリーデータの取得にはBD FACSCanto II/FACSDiva LEGENDPlexデータ分析ソフトウェアを使用でき、フローサイトメトリーデータ分析にはDe Novo FCS Expressソフトウェアを使用できる。
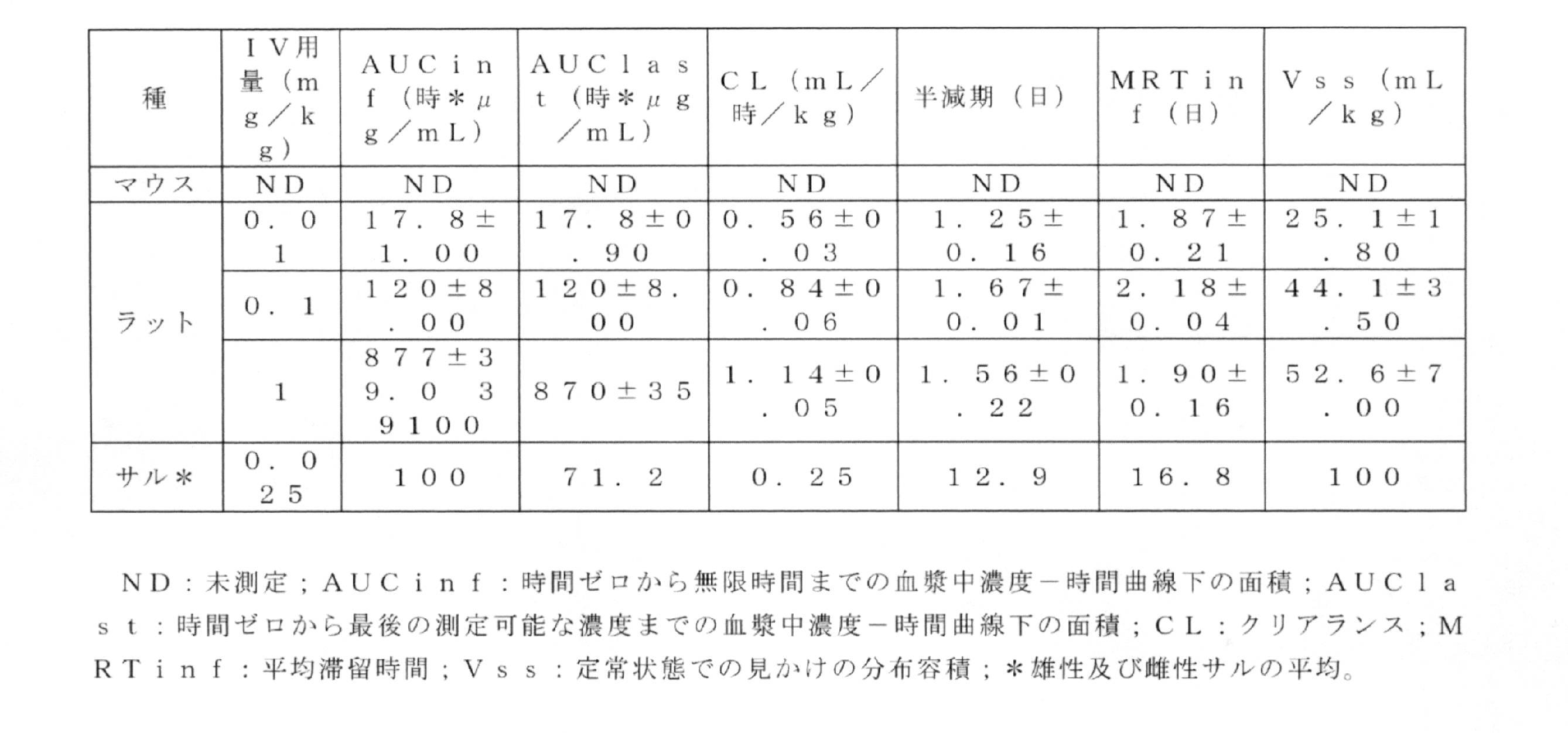
マウス、ラット及びサルにおける単回用量の薬物動態及び毒物動態
マウス、ラット、及びサルにおけるRUR20kD-IL-2組成物の単回用量の薬物動態/毒物動態の結果を要約する。投与計画の詳細を表10に示す。
マウスでの比較研究
C57BL/6マウスに、0.03、0.1及び0.3mg/kgのRUR20kD-IL-2組成物の単回皮下用量を投与するか、又は0.03mg/kg(qddx5)、0.1mg/kg(qdx5)及び1mg/kg(qdx5)の投与量の未修飾IL-2(アルデスロイキン)を投与する、実施例2に記載の研究と本質的に同様の研究を実施する。投与後、血液及び脾臓のサンプルを収集し、フローサイトメトリーによるリンパ球細胞集団に対する薬力学的分析のために分析して、ビヒクル対照と比較した倍率変化として表す。結果を図10A及び図10Bに示す(RUR20kD-IL-2組成物は「RUR-IL-2」と表示され、アルデスロイキンは「IL-2」と表示される)。
全身性エリテマトーデス(SLE)のマウスモデルにおけるRUR20kD-IL-2組成物の有効性の調査
この研究は、この疾患の最も一般的に研究されているマウスモデルであるMRL/MpJ-Faslprマウスモデル(Perry D.,ら,J Biomed Biotechnol 2011:271694)を使用して、SLEの発症と進行及びそれに関連する特徴に対するRUR20kD-IL-2組成物の有効性を決定するために実施される。MRL/MpJ-Faslprマウスモデルは、リンパ節腫大、IgGレベルの上昇、抗核抗体産生、タンパク尿、及び糸球体の炎症による腎不全等、ヒトSLEの病態を反映する自己免疫疾患を発症する。実施例1に記載のRUR20kD-IL-2組成物のストック溶液を、注射用滅菌水(SWFI)、USPで調製;pH5.0±0.1)に調製したビヒクル(透明な液体;10mM酢酸ナトリウム/200mM塩化ナトリウム/2%(重量/体積)スクロース)中に供給される試験品(1.58mg/mL)として使用する。投与日に、適切な量の試験品を取り出し、ビヒクルで希釈して、所望の投与濃度(0.03mg/kg用量及び0.3mg/kg用量)に到達させる。投薬量は5mL/kgであった。この研究に使用した動物は、MRL/MpJ-Faslprマウス及びMRL/MpJナイーブの雌性マウスで、6週齢~8週齢である。動物を無作為化に治療群に割り当てる。治療群を、以下の表13に記載する。45匹のMRL/MpJ-Faslprマウスを、実験開始前の体重及び尿中のタンパク質含有量のレベルに基づいて、3群(群2~4でそれぞれ15匹)に無作為化する。群2~4の動物には、表6に記載されているように、ビヒクル又は試験品を皮下投与する。群1-MRL/MpJマウスは陰性対照としてとしてビヒクルを受ける。
抗原依存性、T細胞性、遅延型過敏症(DTH)モデルにおけるRUR20kD-IL-2組成の研究
この研究は、RUR20kD-IL-2組成物によるin vivo Treg刺激及び増殖が、高度のアナフィラキシーが確立される食物アレルギーモデルにおいて、抗原依存的にT細胞性遅延型過敏症(DTH)応答を下方制御する方法をモデル化している。
健康なボランティアにおけるRUR20kD-IL-2組成物の単回漸増皮下投与の安全性、忍容性、薬物動態及び薬力学を評価するための第I相、二重盲検、無作為化プラセボ対照研究
健康なボランティアにおけるRUR20kD-IL-2組成物(RUR20kD-IL-2)の単回漸増低皮下用量の安全性、忍容性、薬物動態及び薬力学を評価するために、二重盲検、無作為化、プラセボ対照研究を行う。この研究は7つのコホートに分けられ、被験者は0.3、1.0、3.0、6.0、9.0、13.5又は20.0μg/kgのRUR20kD-IL-2を受けた。12人の被験者を各用量コホートに無作為化され、そのうち9人はRUR20kD-IL-2の単回皮下投与を受け、3人はプラセボを受けた。RUR20kD-IL-2を、0.9%塩化ナトリウム滅菌液で希釈した皮下注射用の滅菌液として配合する。医薬品を使い捨てガラスバイアルで供給し、2℃~8℃で保管する。医薬品の各バイアルには、0.75±0.1mgのrhIL-2(RUR20kD-IL-2に基づく)が含まれていた。RUR20kD-IL-2を、10mM酢酸ナトリウム、150mM塩化ナトリウム、2%(重量/体積)スクロース、pH5.0中におよそ1.0mg/mlタンパク質の濃度で配合する。プラセボは市販の0.9%塩化ナトリウム溶液である。0.3μg/kgの開始用量は、最小予測生物学的影響レベル(MABEL)アプローチを使用して選択され、非臨床毒性研究からの最も感受性の高い種における無毒性量(NOAEL)によって支持される。RUR20kD-IL-2の薬物動態及び安全性の評価を可能にするため、開始用量を0.3μg/kgに設定する。1人はRUR20kD-IL-2を受け、もう1人はプラセボを受けた2人の被験者に二重盲検法で投薬し、研究開始前の少なくとも7日間、起こりうる副作用を監視する。
全身性エリテマトーデス患者における皮下RUR20kD-IL-2の安全性、忍容性、薬物動態及び薬力学を評価するための第I相、二重盲検、無作為化プラセボ対照漸増複数回用量研究
最小から中等度の全身性エリテマトーデス(SLE)の患者の4つの用量コホートにおけるRUR20kD-IL-2の漸増複数回用量の安全性、忍容性、PK及び免疫学的効果を評価するための二重盲検、無作為化、プラセボ対照研究を行う。SLE疾患活動性への影響も評価する。疾患活動性が最小から中程度の12人のSLE患者を、4つの用量コホートのそれぞれに無作為化し、そのうち9人はRUR-IL-2-20kDの1.0mg/ml水溶液の皮下用量を複数回受け、3人はプラセボを受けた。RUR20kD-IL-2薬物及びプラセボを、本明細書に記載されているように、例えば実施例1-Aのとおりに調製する。活動性の臨床SLE疾患活動は選択基準として必要とされない。コホート1では、3.0μg/kgの開始用量を2週間間隔で3回投与する(1、15及び29日目)。この開始用量は、上記の研究で以前に決定されたRUR20kD-IL-2の単一皮下用量の好ましい安全性及びPDプロファイルに基づいている。コホート2、3及び4のその後の用量レベルは、それぞれ、前の用量コホートの最大2倍であった。コホート1~3の患者は、2週間間隔で合計4週間にわたって3回の治験薬の投与を受けた。研究の過程で評価される用量は、3.0μg/kg~24μg/kgの範囲である。コホート4の患者は、1、15、29、43、57、71及び85日目に投与されるRUR20kD-IL-2による12週間の治療を受ける。このコホートは、RUR20kD-IL-2治療の長期にわたる投与の安全性、並びにPK及びPDプロファイルに関するデータを提供する。RUR20kD-IL-2又はプラセボの最終投与を受けた後、安全性、PK、PD及び予備的有効性を評価するために患者を更に50日間追跡する。各コホートの12人の被験者のうち8人を、安全性の問題の可能性について、安全性審査委員会によって最終患者の3回目の投薬の2週間後に評価する。更に、安全性審査委員会によって2回、すなわち(1)最初の8人の被験者が3回目の投与を受けてから2週間後、及び(2)全ての被験者が全ての投与量の治験薬を投与されてから2週間後にコホート4の全ての患者を評価する
安全性の所見に加えて、Treg、CD4+-T細胞、CD8+-T細胞、NK細胞応答、サイトカインレベル、利用可能なPKデータ等の免疫学的変化を使用して、用量レベルを決定する。この研究の主要目的は、SLE患者に複数回漸増皮下用量として投与されたRUR20kD-IL-2の安全性及び忍容性を評価することであり、この研究の副次目的は、(1)SLE患者における複数回の皮下投与後のRUR20kD-IL-2のPKプロファイルを特性評価すること、(2)SLE患者におけるTreg及びTregサブセットの数及び機能、CD4+-T細胞、CD8+-T細胞、NK細胞、並びにサイトカインレベルを含む、PDバイオマーカーの変化の時間経過及び程度に関するRUR20kD-IL-2の効果を評定すること、(3)二本鎖DNAに対する抗体の存在及びレベル、並びにSLE患者の補体C3及びC4のレベルに対するRUR20kD-IL-2の効果を評定すること、並びに(4)SLE患者の疾患活動性に対するRUR20kD-IL-2の効果を評定することである。漸増複数回用量研究からの予備的なPKデータを表す結果を、以下の表15の単回皮下研究からのデータと比較する。
[1]構造:
nは各出現で独立して約3~約4000の整数である)
を有するPEG化IL-2コンジュゲートを含む組成物。
[2]IL-2がアルデスロイキンである、上記[1]に記載の組成物。
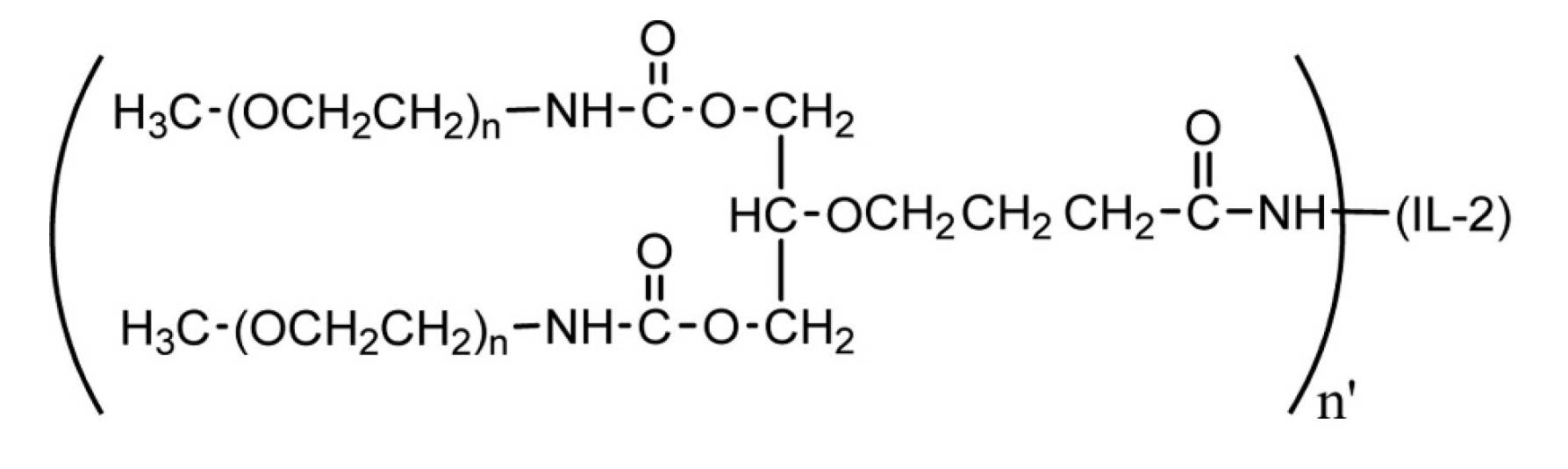
[3]前記組成物が、あわせて考慮した場合に、
式
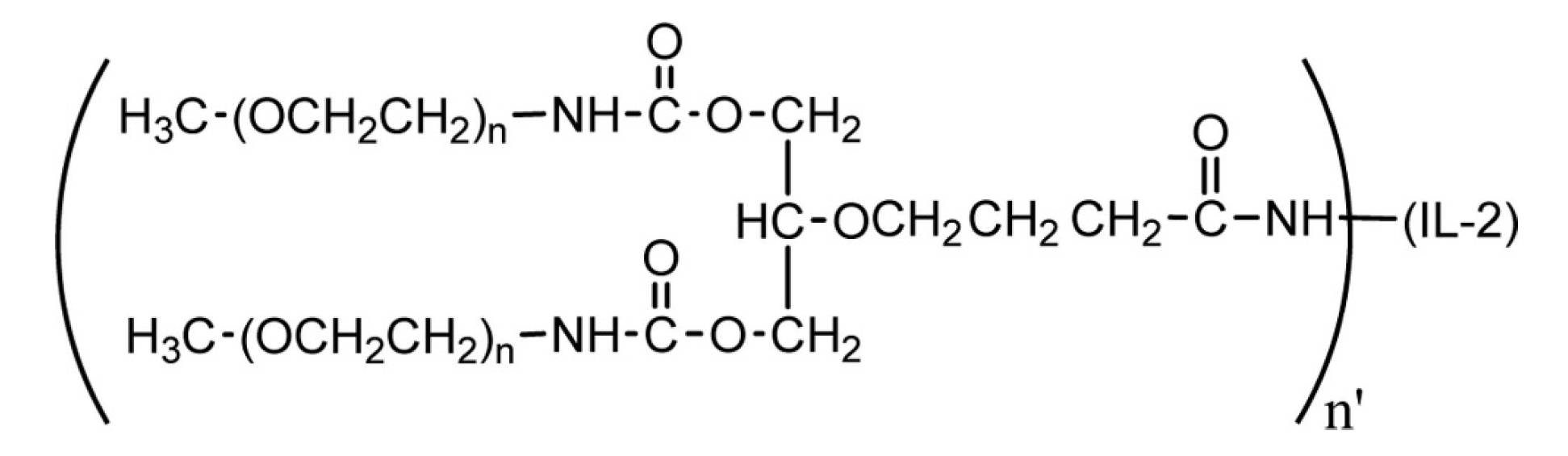
[4]前記組成物が、あわせて考慮した場合に、
式
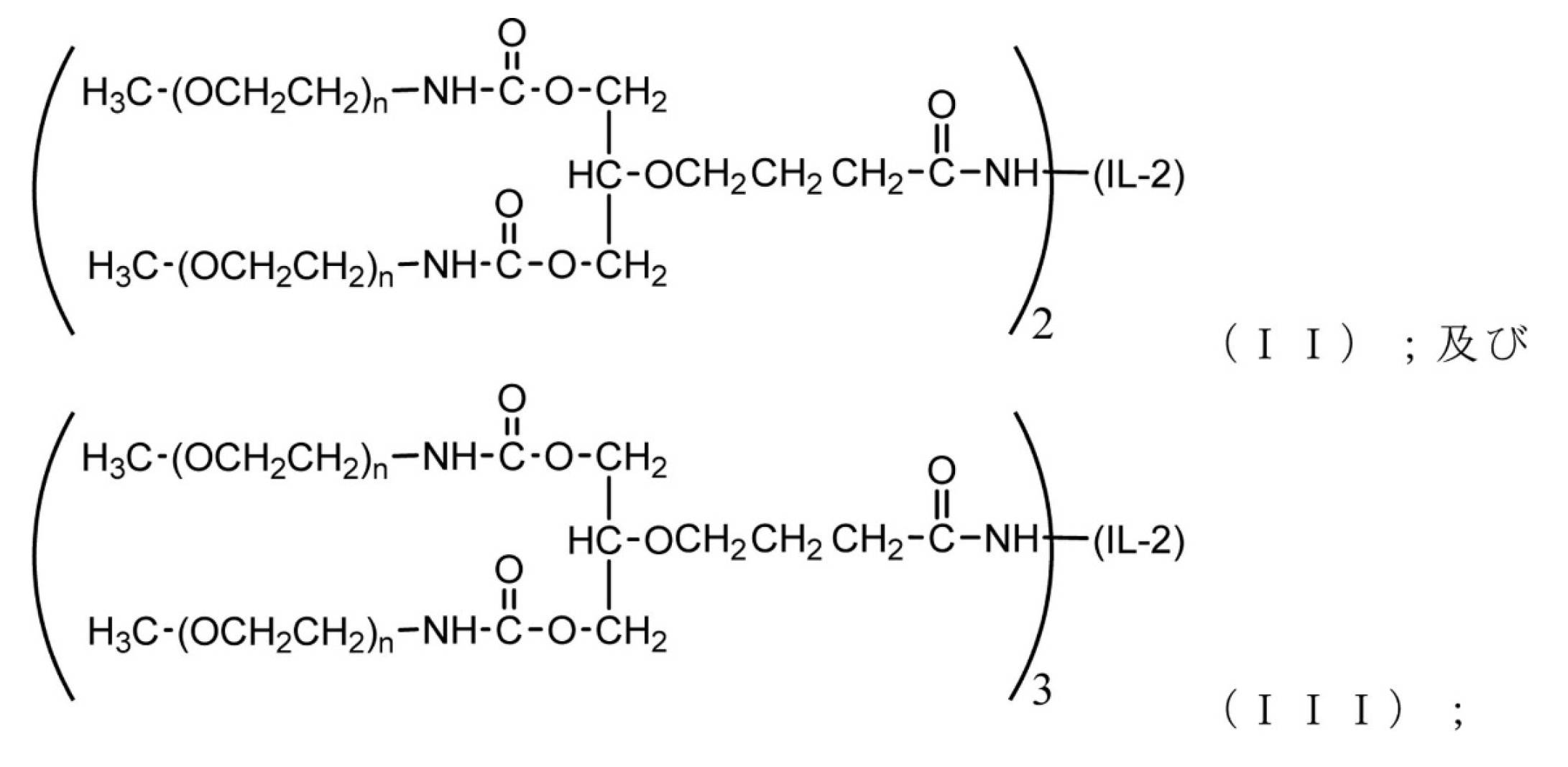
[5]前記組成物が、あわせて考慮した場合に、式
[6]1に等しいn’を有するPEG化IL-2コンジュゲートを約10モル%以下で含む、上記[3]~[5]に記載のいずれか一項に記載の組成物。
[7]1に等しいn’を有するPEG化IL-2コンジュゲートを約7モル%以下で含む、上記[3]~[5]に記載のいずれか一項に記載の組成物。
[8]1に等しいn’を有するPEG化IL-2コンジュゲートを約5モル%以下で含む、上記[3]~[5]に記載のいずれか一項に記載の組成物。
[9]4に等しいn’を有するPEG化IL-2コンジュゲートを約10モル%以下で含む、上記[3]~[8]に記載のいずれか一項に記載の組成物。
[10]4に等しいn’を有するPEG化IL-2コンジュゲートを約7モル%以下で含む、上記[3]~[8]に記載のいずれか一項に記載の組成物。
[11]4に等しいn’を有するPEG化IL-2コンジュゲートを約5モル%以下で含む、上記[3]~[8]に記載のいずれか一項に記載の組成物。
[12]前記組成物が、ほぼ等モル量の
[13]組前記組成物が、式
[14]アルデスロイキンあたりの分岐ポリエチレングリコール部分、
[15]アルデスロイキンあたりの分岐ポリエチレングリコール部分の平均数が約2.5である、上記[13]に記載の組成物。
[16]nの値が5~2000の範囲である、上記[1]~[15]に記載のいずれか一項に記載の組成物。
[17]nの値が10~1000の範囲である、上記[1]~[15]に記載のいずれか一項に記載の組成物。
[18]nの値が10~750の範囲である、上記[1]~[15]に記載のいずれか一項に記載の組成物。
[19]nの値が10~500の範囲である、上記[1]~[15]に記載のいずれか一項に記載の組成物。
[20]nの値が20~250の範囲である、上記[1]~[15]に記載のいずれか一項に記載の組成物。
[21]nの平均値が約226である、上記[1]~[15]に記載のいずれか一項に記載の組成物。
[22]各分岐ポリエチレングリコール部分の名目上の平均分子量が、約250ダルトン~約90000ダルトンの範囲にある、上記[1]~[15]に記載のいずれか一項に記載の組成物。
[23]各分岐ポリエチレングリコール部分の名目上の平均分子量が、約1000ダルトン~約60000ダルトンの範囲にある、上記[1]~[15]に記載のいずれか一項に記載の組成物。
[24]各分岐ポリエチレングリコール部分の名目上の平均分子量が、約5000ダルトン~約60000ダルトンの範囲にある、上記[1]~[15]に記載のいずれか一項に記載の組成物。
[25]各分岐ポリエチレングリコール部分の名目上の平均分子量が、約10000ダルトン~約55000ダルトンの範囲にある、上記[1]~[15]に記載のいずれか一項に記載の組成物。
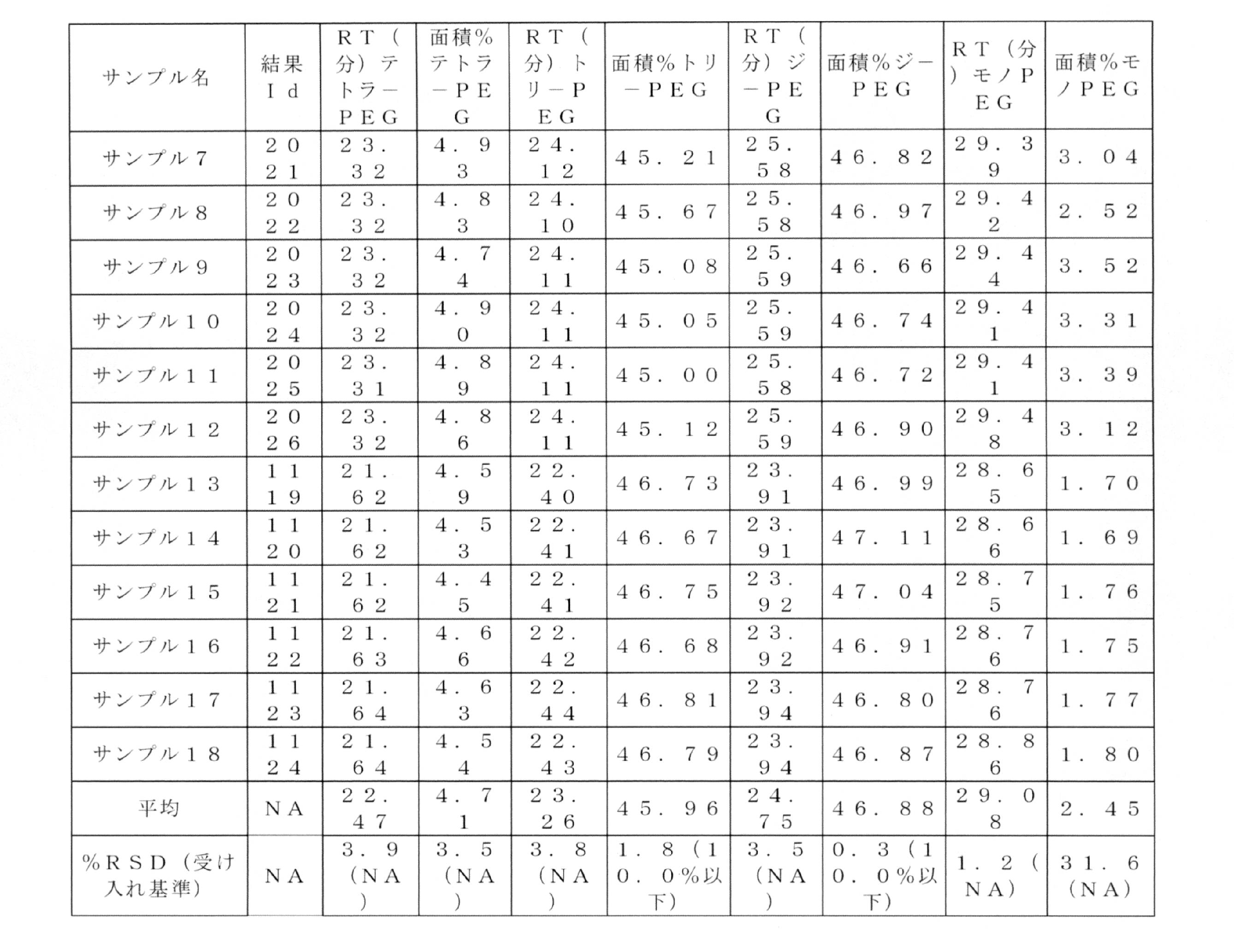
[26]モルベースで、約5モル%以下のモノ-PEG化IL-2コンジュゲート、及び約28モル%~約60モル%のジ-PEG化IL-2コンジュゲート、及び約24モル%~約65モル%のトリ-PEG化IL-2コンジュゲート、及び約12モル%以下のより高PEG化されたIL-2コンジュゲートを含み、各分岐ポリエチレングリコール部分の名目上の平均分子量が約20000ダルトンである、上記[1]又は[2]に記載の組成物。
[27]80%以上の組み合わされたジ-及びトリ-PEG化IL-2コンジュゲートを更に含む、上記[26]に記載の組成物。
[28]モルベースで、約2.5~約4.5モル%のモノ-PEG化IL-2コンジュゲート、及び約35~約50モル%のジ-PEG化IL-2コンジュゲート、及び約38~約46モル%のトリ-PEG化IL-2コンジュゲート、及び約3~約10モル%のより高PEG化されたIL-2コンジュゲートを含み、各分岐ポリエチレングリコール部分の名目上の平均分子量が約20000ダルトンである、上記[1]又は[2]に記載の組成物。
[29]あわせた合計が約80~約95モル%のジ-PEG化及びトリ-PEG化IL-2コンジュゲートを更に含む、上記[28]に記載の組成物。
[30]モルベースで、約2.8~約3.8モル%のモノ-PEG化IL-2コンジュゲート、及び約44~約48モル%のジ-PEG化IL-2コンジュゲート、及び約41~約44モル%のトリ-PEG化IL-2コンジュゲート、及び約7~約9モル%のより高PEG化されたIL-2コンジュゲートを含み、各分岐ポリエチレングリコール部分の名目上の平均分子量が約20000ダルトンである、上記[1]又は[2]に記載の組成物。
[31]あわせた合計が約87~約90モル%のジ-PEG化及びトリ-PEG化IL-2コンジュゲートを更に含む、上記[30]に記載の組成物。
[32]モルベースで、約2.8~約3.8モル%のモノ-PEG化IL-2コンジュゲート、及び約44~約48モル%のジ-PEG化IL-2コンジュゲート、及び約41~約44モル%のトリ-PEG化IL-2コンジュゲート、及び約7~約9モル%のより高PEG化されたIL-2コンジュゲートを含み、前記組成物がリジンK7又はK8又はK31又はK75の1つに付着したPEG部分を有するモノ-PEG化IL-2コンジュゲートの混合物を含み、各分岐ポリエチレングリコール部分の名目上の平均分子量が約20000ダルトンである、上記[1]又は[2]に記載の組成物。
[33]あわせた合計が約87~約90モル%のジ-PEG化及びトリ-PEG化IL-2コンジュゲートを更に含む、上記[32]に記載の組成物。
[34]モルベースで、約2.8~約3.8モル%のモノ-PEG化IL-2コンジュゲート、及び約44~約48モル%のジ-PEG化IL-2コンジュゲート、及び約41~約44モル%のトリ-PEG化IL-2コンジュゲート、及び約7~約9モル%のより高PEG化されたIL-2コンジュゲートを含み、前記組成物がリジンK7に付着したPEG部分を有するモノ-PEG化IL-2コンジュゲートを含み、各分岐ポリエチレングリコール部分の名目上の平均分子量が約20000ダルトンである、上記[1]又は[2]に記載の組成物。
[35]あわせた合計が約87~約90モル%のジ-PEG化及びトリ-PEG化IL-2コンジュゲートを更に含む、上記[34]に記載の組成物。
[36]薬学的に許容可能な賦形剤を更に含む、上記[1]~[35]に記載のいずれか一項に記載の組成物。
[37]非経口投与に適した形態の、上記[1]~[35]に記載のいずれか一項に記載の組成物。
[38]皮下投与に適した形態の、上記[1]~[35]に記載のいずれか一項に記載の組成物。
[39]水性希釈剤を含む、上記[36]に記載の組成物。
[40]約5のpHを有する、上記[39]に記載の組成物。
[41]酢酸ナトリウム、塩化ナトリウム及びスクロースを更に含む、上記[39]又は上記[40]に記載の組成物。
[42]1.5mg/mlタンパク質当量、10mM酢酸ナトリウム、110mM塩化ナトリウム、2%スクロース(重量/体積)、pH5.0を含む上記[37]記載の組成物。
[43]上記[1]~[42]に記載のいずれか一項に記載の組成物の治療有効量を被験体に投与することにより、被験体における制御性T細胞対エフェクターT細胞の比率を増加させる方法。
[44]制御性T細胞がFoxp3+細胞及びCD25+細胞から選択される、上記[43]に記載の方法。
[45]エフェクターT細胞がCD4+細胞及びCD8+細胞から選択される、上記[44]に記載の方法。
[46]ベースラインと比較した場合、制御性T細胞の倍増が、in-vivoマウスモデルで評価した場合、少なくとも約2の値に達する、上記[43]~[45]に記載のいずれか一項に記載の方法。
[47]ベースラインと比較した場合、制御性T細胞の倍増が、in-vivoマウスモデルで評価した場合、少なくとも約4の値に達する、上記[43]~[45]に記載のいずれか一項に記載の方法。
[48]制御性T細胞数の増加が、投与後少なくとも3日間、ベースラインレベルを超えて持続する、上記[43]~[47]に記載のいずれか一項に記載の方法。
[49]制御性T細胞数の増加が、投与後少なくとも5日間、ベースラインレベルを超えて持続する、上記[43]に記載の方法。
[50]上記[1]~[42いずれか一項]に記載の組成物の治療有効量を被験体に投与することを含む、自己免疫疾患を有する被験体を治療する方法。
[51]前記投与が皮下注射によるものである、上記[50]に記載の方法。
[52]前記投与が2週間に1回又は4週間に1回行われる、上記[50]~[51]に記載のいずれか一項に記載の方法。
[53]前記投与が、2週間に1回、3μg/kg~24μg/kgの用量を含む、上記[50]~[52]に記載のいずれか一項に記載の方法。
[54]治療法に使用するための、上記[1]~[42]に記載のいずれか一項に記載の組成物。
[55]自己免疫疾患の治療に使用するための、上記[1]~[42]に記載のいずれか一項に記載の組成物。
[56]自己免疫疾患を治療するための薬剤を製造するための、上記[1]~[42]に記載のいずれか一項に記載の組成物の使用。
Claims (39)
- IL-2がアルデスロイキンである、請求項1に記載の組成物。
- 4に等しいn’を有するPEG化IL-2コンジュゲートを約10モルパーセント以下で含む、請求項1~3のいずれか一項に記載の組成物。
- 4に等しいn’を有するPEG化IL-2コンジュゲートを約7モルパーセント以下で含む、請求項1~3のいずれか一項に記載の組成物。
- 4に等しいn’を有するPEG化IL-2コンジュゲートを約5モルパーセント以下で含む、請求項1~3のいずれか一項に記載の組成物。
- アルデスロイキンあたりの分岐ポリエチレングリコール部分の平均数が約2.5である、請求項2に記載の組成物。
- nの平均値が約226である、請求項1または2に記載の組成物。
- あわせた合計が約80~約95モルパーセントのジ-PEG化及びトリ-PEG化IL-2コンジュゲートを更に含む、請求項1~9のいずれか一項に記載の組成物。
- モルベースで、約2.8~約3.8モルパーセントのモノ-PEG化IL-2コンジュゲート、及び約44~約48モルパーセントのジ-PEG化IL-2コンジュゲート、及び約41~約44モルパーセントのトリ-PEG化IL-2コンジュゲート、及び約7~約9モルパーセントのより高PEG化されたIL-2コンジュゲートを含み、各分岐ポリエチレングリコール部分の名目上の平均分子量が約20000ダルトンである、請求項1~9のいずれか一項に記載の組成物。
- あわせた合計が約87~約90モルパーセントのジ-PEG化及びトリ-PEG化IL-2コンジュゲートを更に含む、請求項11に記載の組成物。
- モルベースで、約2.8~約3.8モルパーセントのモノ-PEG化IL-2コンジュゲート、及び約44~約48モルパーセントのジ-PEG化IL-2コンジュゲート、及び約41~約44モルパーセントのトリ-PEG化IL-2コンジュゲート、及び約7~約9モルパーセントのより高PEG化されたIL-2コンジュゲートを含み、前記組成物がリジンK7又はK8又はK31又はK75の1つに付着したPEG部分を有するモノ-PEG化IL-2コンジュゲートの混合物を含み、各分岐ポリエチレングリコール部分の名目上の平均分子量が約20000ダルトンである、請求項1~10のいずれか一項に記載の組成物。
- あわせた合計が約87~約90モルパーセントのジ-PEG化及びトリ-PEG化IL-2コンジュゲートを更に含む、請求項13に記載の組成物。
- モルベースで、約2.8~約3.8モルパーセントのモノ-PEG化IL-2コンジュゲート、及び約44~約48モルパーセントのジ-PEG化IL-2コンジュゲート、及び約41~約44モルパーセントのトリ-PEG化IL-2コンジュゲート、及び約7~約9モルパーセントのより高PEG化されたIL-2コンジュゲートを含み、前記組成物がリジンK7に付着したPEG部分を有するモノ-PEG化IL-2コンジュゲートを含み、各分岐ポリエチレングリコール部分の名目上の平均分子量が約20000ダルトンである、請求項1~10のいずれか一項に記載の組成物。
- あわせた合計が約87~約90モルパーセントのジ-PEG化及びトリ-PEG化IL-2コンジュゲートを更に含む、請求項15に記載の組成物。
- 薬学的に許容可能な賦形剤を更に含む、請求項1~16のいずれか一項に記載の組成物。
- 非経口投与に適した形態の、請求項1~17のいずれか一項に記載の組成物。
- 皮下投与に適した形態の、請求項1~17のいずれか一項に記載の組成物。
- 水性希釈剤を含む、請求項17に記載の組成物。
- 約5のpHを有する、請求項20に記載の組成物。
- 酢酸ナトリウム、塩化ナトリウム及びスクロースを更に含む、請求項21に記載の組成物。
- 1.5mg/mlタンパク質当量、10mM酢酸ナトリウム、110mM塩化ナトリウム、2%スクロース(重量/体積)、pH5.0を含む請求項17に記載の組成物。
- 治療法に使用するための、請求項1~23のいずれか1項に記載の組成物。
- 制御性T細胞対エフェクターT細胞の比率を増加させる方法に使用するための、請求項1~23のいずれか一項に記載の組成物。
- 制御性T細胞がFoxp3+細胞及びCD25+細胞から選択される、請求項25に記載の組成物。
- エフェクターT細胞がCD4+細胞及びCD8+細胞から選択される、請求項25に記載の組成物。
- ベースラインと比較した場合、制御性T細胞の倍増が、in-vivoマウスモデルで評価した場合、少なくとも約2の値に達する、請求項25に記載の組成物。
- ベースラインと比較した場合、制御性T細胞の倍増が、in-vivoマウスモデルで評価した場合、少なくとも約4の値に達する、請求項25に記載の組成物。
- 制御性T細胞数の増加が、投与後少なくとも3日間、ベースラインレベルを超えて持続する、請求項25に記載の組成物。
- 制御性T細胞数の増加が、投与後少なくとも5日間、ベースラインレベルを超えて持続する、請求項25に記載の組成物。
- 自己免疫疾患の治療に使用するための、請求項1~31のいずれか一項に記載の組成物。
- 皮下注射により投与される、請求項32に記載の組成物。
- 2週間に1回又は4週間に1回投与される、請求項32または33に記載の組成物。
- 2週間に1回、3μg/kg~24μg/kgの用量で投与される、請求項32または33に記載の組成物。
- 前記自己免疫疾患が、全身性エリテマトーデスである、請求項32~35のいずれか一項に記載の組成物。
- 前記自己免疫疾患が、アトピー性皮膚炎である、請求項32~35のいずれか一項に記載の組成物。
- 前記自己免疫疾患が、潰瘍性大腸炎またはクローン病である、請求項32~35のいずれか1項に記載の組成物。
- アレルギー疾患に使用するための、請求項1または2に記載の組成物。
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2022206250A JP7801991B2 (ja) | 2018-05-21 | 2022-12-23 | 選択的Treg刺激因子RUR20kD-IL-2及び関連組成物 |
| JP2024092962A JP2024116272A (ja) | 2018-05-21 | 2024-06-07 | 選択的Treg刺激因子RUR20kD-IL-2及び関連組成物 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201862674244P | 2018-05-21 | 2018-05-21 | |
| US62/674,244 | 2018-05-21 | ||
| PCT/US2019/033100 WO2019226538A1 (en) | 2018-05-21 | 2019-05-20 | SELECTIVE TREG STIMULATOR RUR20kD-IL-2 AND RELATED COMPOSITIONS |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022206250A Division JP7801991B2 (ja) | 2018-05-21 | 2022-12-23 | 選択的Treg刺激因子RUR20kD-IL-2及び関連組成物 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2021523922A JP2021523922A (ja) | 2021-09-09 |
| JP7235772B2 true JP7235772B2 (ja) | 2023-03-08 |
Family
ID=67002369
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020564540A Active JP7235772B2 (ja) | 2018-05-21 | 2019-05-20 | 選択的Treg刺激因子RUR20kD-IL-2及び関連組成物 |
| JP2022206250A Active JP7801991B2 (ja) | 2018-05-21 | 2022-12-23 | 選択的Treg刺激因子RUR20kD-IL-2及び関連組成物 |
| JP2024092962A Pending JP2024116272A (ja) | 2018-05-21 | 2024-06-07 | 選択的Treg刺激因子RUR20kD-IL-2及び関連組成物 |
Family Applications After (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022206250A Active JP7801991B2 (ja) | 2018-05-21 | 2022-12-23 | 選択的Treg刺激因子RUR20kD-IL-2及び関連組成物 |
| JP2024092962A Pending JP2024116272A (ja) | 2018-05-21 | 2024-06-07 | 選択的Treg刺激因子RUR20kD-IL-2及び関連組成物 |
Country Status (21)
| Country | Link |
|---|---|
| US (1) | US20210205413A1 (ja) |
| EP (1) | EP3796940A1 (ja) |
| JP (3) | JP7235772B2 (ja) |
| KR (2) | KR102706554B1 (ja) |
| CN (2) | CN112399859B (ja) |
| AU (3) | AU2019274409B2 (ja) |
| BR (1) | BR112020021564A2 (ja) |
| CA (1) | CA3100204A1 (ja) |
| CL (1) | CL2020003008A1 (ja) |
| CO (1) | CO2020014510A2 (ja) |
| CR (1) | CR20200546A (ja) |
| DO (1) | DOP2020000212A (ja) |
| EA (1) | EA202092489A1 (ja) |
| EC (1) | ECSP20074392A (ja) |
| IL (2) | IL312646A (ja) |
| JO (1) | JOP20200290A1 (ja) |
| MX (1) | MX2024012807A (ja) |
| PE (1) | PE20211307A1 (ja) |
| PH (1) | PH12020551976A1 (ja) |
| SG (1) | SG11202011242SA (ja) |
| WO (1) | WO2019226538A1 (ja) |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20220140514A (ko) | 2020-01-10 | 2022-10-18 | 브라이트 피크 테라퓨틱스 아게 | 변형된 il-2 폴리펩타이드 및 그의 용도 |
| CN113121670B (zh) * | 2020-01-15 | 2022-11-22 | 天津键凯科技有限公司 | 二取代peg化白细胞介素2及其制备方法、应用 |
| US20230102464A1 (en) * | 2020-01-15 | 2023-03-30 | Jenkem Technology Co., Ltd. (Tianjin) | Method for preparing pegylated biomolecule with controllable binding sites |
| JP2021143142A (ja) * | 2020-03-11 | 2021-09-24 | 花王株式会社 | 制御性t細胞誘導剤 |
| US20230272001A1 (en) * | 2020-05-22 | 2023-08-31 | Merck Sharp & Dohme Llc | Novel processes for preparing conjugates of the il-2 protein |
| TW202228784A (zh) | 2020-09-23 | 2022-08-01 | 奧地利商艾柏力維亞生技有限公司 | 用以於一患者中螯合非預期的抗peg抗體的化合物 |
| WO2022109477A1 (en) * | 2020-11-23 | 2022-05-27 | University Of Florida Research Foundation, Incorporated | Use of insulin-like growth factors with gamma-chain cytokines to induce homeostatic proliferation of lymphocytes |
| MX2024007345A (es) | 2021-12-14 | 2024-09-30 | Nektar Therapeutics | Pautas posologicas para el estimulador de treg selectivo rur20kd-il-2 y composiciones relacionadas. |
| CN116212040B (zh) * | 2023-02-14 | 2025-11-28 | 河北菲尼斯生物技术有限公司 | 一种作为Treg靶向调节剂的PEG修饰IL-2的组合物及其制备方法和用途 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2014506116A (ja) | 2010-11-12 | 2014-03-13 | ウェルズ ファーゴ バンク ナショナル アソシエイション | Il−2部分とポリマーとのコンジュゲート |
| JP2014510725A (ja) | 2011-03-11 | 2014-05-01 | アシスタンス ピュブリク−オピトー ドゥ パリ | 自己免疫関連障害または炎症性障害の治療のための低用量il−2の使用 |
| WO2017156720A1 (zh) | 2016-03-16 | 2017-09-21 | 谢彦晖 | 糖皮质激素联合聚乙二醇修饰的白介素2治疗呼吸道疾病 |
Family Cites Families (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4401756A (en) | 1981-04-14 | 1983-08-30 | Immunex Corporation | Process for preparing human interleukin 2 |
| US4569790A (en) | 1984-03-28 | 1986-02-11 | Cetus Corporation | Process for recovering microbially produced interleukin-2 and purified recombinant interleukin-2 compositions |
| US5116943A (en) | 1985-01-18 | 1992-05-26 | Cetus Corporation | Oxidation-resistant muteins of Il-2 and other protein |
| US5206344A (en) | 1985-06-26 | 1993-04-27 | Cetus Oncology Corporation | Interleukin-2 muteins and polymer conjugation thereof |
| US5153310A (en) | 1989-02-28 | 1992-10-06 | Du Pont Merck Pharmaceutical Company | Il-2 analogs containing n-linked glycosylation sites |
| US5635597A (en) | 1994-05-27 | 1997-06-03 | Affymax Technologies, N.V. | Peptides that bind IL-2 receptors |
| US6168785B1 (en) | 1998-07-16 | 2001-01-02 | Institut Pasteur | Biological applications of new peptides of IL-2 and derivatives and use as therapeutic agents |
| FR2826365B1 (fr) | 2001-06-20 | 2003-09-26 | Oreal | Compositions cosmetiques photoprotectrices contenant des derives amides, sulfonamides ou carbamates aromatiques d'acrylonitrile et nouveaux derives amides, sulfonamides ou carbamates d'acrylonitrile |
| HUE043911T2 (hu) | 2003-05-23 | 2019-09-30 | Nektar Therapeutics | Két PEG láncot tartalmazó PEG származékok |
| US7569215B2 (en) | 2003-07-18 | 2009-08-04 | Massachusetts Institute Of Technology | Mutant interleukin-2 (IL-2) polypeptides |
| US20110166319A1 (en) * | 2005-02-11 | 2011-07-07 | Immunogen, Inc. | Process for preparing purified drug conjugates |
| US7567215B1 (en) | 2007-10-23 | 2009-07-28 | The United States Of America As Represented By The Secretary Of The Navy | Portable and inflatable antenna device |
-
2019
- 2019-05-20 CN CN201980034052.1A patent/CN112399859B/zh active Active
- 2019-05-20 AU AU2019274409A patent/AU2019274409B2/en active Active
- 2019-05-20 CN CN202411607743.5A patent/CN120131983A/zh active Pending
- 2019-05-20 KR KR1020207033346A patent/KR102706554B1/ko active Active
- 2019-05-20 EA EA202092489A patent/EA202092489A1/ru unknown
- 2019-05-20 JO JOP/2020/0290A patent/JOP20200290A1/ar unknown
- 2019-05-20 EP EP19732788.5A patent/EP3796940A1/en active Pending
- 2019-05-20 PE PE2020001854A patent/PE20211307A1/es unknown
- 2019-05-20 WO PCT/US2019/033100 patent/WO2019226538A1/en not_active Ceased
- 2019-05-20 JP JP2020564540A patent/JP7235772B2/ja active Active
- 2019-05-20 CA CA3100204A patent/CA3100204A1/en active Pending
- 2019-05-20 IL IL312646A patent/IL312646A/en unknown
- 2019-05-20 BR BR112020021564-3A patent/BR112020021564A2/pt unknown
- 2019-05-20 IL IL278528A patent/IL278528B2/en unknown
- 2019-05-20 CR CR20200546A patent/CR20200546A/es unknown
- 2019-05-20 SG SG11202011242SA patent/SG11202011242SA/en unknown
- 2019-05-20 US US17/056,050 patent/US20210205413A1/en active Pending
- 2019-05-20 KR KR1020247030258A patent/KR20240137713A/ko active Pending
-
2020
- 2020-11-18 PH PH12020551976A patent/PH12020551976A1/en unknown
- 2020-11-19 MX MX2024012807A patent/MX2024012807A/es unknown
- 2020-11-19 DO DO2020000212A patent/DOP2020000212A/es unknown
- 2020-11-19 CL CL2020003008A patent/CL2020003008A1/es unknown
- 2020-11-20 EC ECSENADI202074392A patent/ECSP20074392A/es unknown
- 2020-11-23 CO CONC2020/0014510A patent/CO2020014510A2/es unknown
-
2022
- 2022-10-06 AU AU2022246440A patent/AU2022246440B2/en active Active
- 2022-12-23 JP JP2022206250A patent/JP7801991B2/ja active Active
-
2024
- 2024-06-07 JP JP2024092962A patent/JP2024116272A/ja active Pending
-
2025
- 2025-02-11 AU AU2025200920A patent/AU2025200920A1/en active Pending
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2014506116A (ja) | 2010-11-12 | 2014-03-13 | ウェルズ ファーゴ バンク ナショナル アソシエイション | Il−2部分とポリマーとのコンジュゲート |
| JP2014510725A (ja) | 2011-03-11 | 2014-05-01 | アシスタンス ピュブリク−オピトー ドゥ パリ | 自己免疫関連障害または炎症性障害の治療のための低用量il−2の使用 |
| WO2017156720A1 (zh) | 2016-03-16 | 2017-09-21 | 谢彦晖 | 糖皮质激素联合聚乙二醇修饰的白介素2治疗呼吸道疾病 |
Non-Patent Citations (1)
| Title |
|---|
| Int. Immunopharmacol. (Feb 2018) vol.56, p.269-276 |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7235772B2 (ja) | 選択的Treg刺激因子RUR20kD-IL-2及び関連組成物 | |
| JP7772733B2 (ja) | 長時間作用型インターロイキン-15受容体作動薬並びに関連する免疫治療組成物及び方法 | |
| JP2017511322A (ja) | Il−15部分とポリマーとのコンジュゲート | |
| CN105209054A (zh) | 使用白细胞介素-10治疗疾病和病症的方法 | |
| WO2022020637A1 (en) | Il-7 receptor agonist composition and related methods and uses | |
| WO2025254932A1 (en) | Selective treg stimulator and methods of uses thereof | |
| EA043667B1 (ru) | Длительно действующие агонисты рецептора интерлейкина-15, связанные с ними композиции и способы их получения и применения |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210115 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20210115 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20211214 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20220302 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20220511 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220613 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20220614 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20221004 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20221223 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20230221 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20230224 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7235772 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| RD02 | Notification of acceptance of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: R3D02 |