JP7145608B2 - 有機エレクトロルミネッセンス素子用化合物、液状組成物、インク組成物、薄膜、及び有機エレクトロルミネッセンス素子 - Google Patents
有機エレクトロルミネッセンス素子用化合物、液状組成物、インク組成物、薄膜、及び有機エレクトロルミネッセンス素子 Download PDFInfo
- Publication number
- JP7145608B2 JP7145608B2 JP2017244291A JP2017244291A JP7145608B2 JP 7145608 B2 JP7145608 B2 JP 7145608B2 JP 2017244291 A JP2017244291 A JP 2017244291A JP 2017244291 A JP2017244291 A JP 2017244291A JP 7145608 B2 JP7145608 B2 JP 7145608B2
- Authority
- JP
- Japan
- Prior art keywords
- group
- substituted
- unsubstituted
- compound
- organic electroluminescence
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/14—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/56—Ring systems containing three or more rings
- C07D209/80—[b, c]- or [b, d]-condensed
- C07D209/82—Carbazoles; Hydrogenated carbazoles
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D251/00—Heterocyclic compounds containing 1,3,5-triazine rings
- C07D251/02—Heterocyclic compounds containing 1,3,5-triazine rings not condensed with other rings
- C07D251/12—Heterocyclic compounds containing 1,3,5-triazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members
- C07D251/14—Heterocyclic compounds containing 1,3,5-triazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members with hydrogen or carbon atoms directly attached to at least one ring carbon atom
- C07D251/24—Heterocyclic compounds containing 1,3,5-triazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members with hydrogen or carbon atoms directly attached to at least one ring carbon atom to three ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D307/00—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom
- C07D307/77—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D307/91—Dibenzofurans; Hydrogenated dibenzofurans
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/06—Luminescent, e.g. electroluminescent, chemiluminescent materials containing organic luminescent materials
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6574—Polycyclic condensed heteroaromatic hydrocarbons comprising only oxygen in the heteroaromatic polycondensed ring system, e.g. cumarine dyes
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6576—Polycyclic condensed heteroaromatic hydrocarbons comprising only sulfur in the heteroaromatic polycondensed ring system, e.g. benzothiophene
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1088—Heterocyclic compounds characterised by ligands containing oxygen as the only heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1092—Heterocyclic compounds characterised by ligands containing sulfur as the only heteroatom
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Optics & Photonics (AREA)
- Electroluminescent Light Sources (AREA)
- Plural Heterocyclic Compounds (AREA)
- Inks, Pencil-Leads, Or Crayons (AREA)
Description
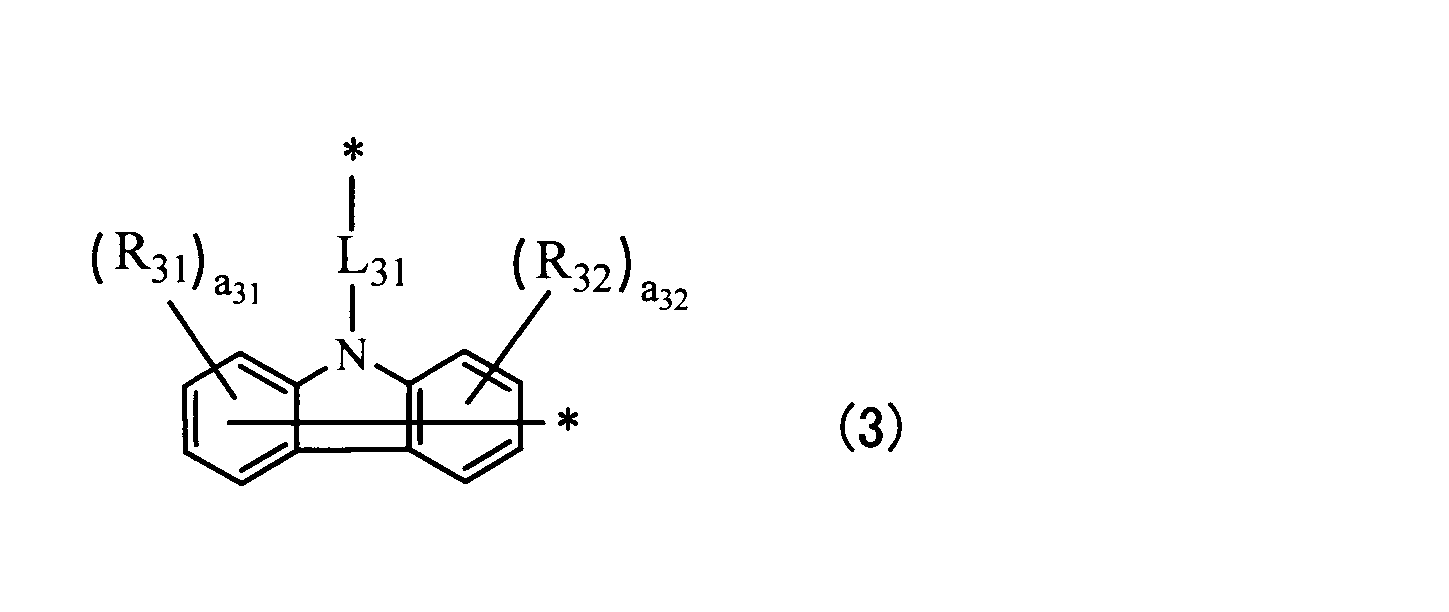
Aは、式(2)
Xは、酸素原子、又は硫黄原子であり、
Azは、置換若しくは無置換の環形成原子数5~60の含窒素芳香族複素環基であり、
Czは、置換若しくは無置換のカルバゾール、置換若しくは無置換のアザカルバゾール、置換若しくは無置換のベンゾカルバゾール、置換若しくは無置換のヒドロカルバゾール、置換若しくは無置換のアクリジン、置換若しくは無置換のインドール、置換若しくは無置換のキサンテン、置換若しくは無置換のフェノキサジン、又は置換若しくは無置換のジフェニルアミンから誘導された基であり、複数の置換基を有する場合、隣接する置換基が結合して新たな環を形成してもよく、
L11及びL12は、それぞれ独立に、単結合、置換若しくは無置換の環形成炭素数6~60の芳香族炭化水素基、又は、置換若しくは無置換の環形成原子数5~60の芳香族複素環基であり、
R1は、水素原子、重水素原子、ハロゲン原子、置換若しくは無置換の環形成炭素数6~60の芳香族炭化水素基、又は、置換若しくは無置換の環形成原子数5~60の芳香族複素環基であり、
R2~R7は、それぞれ独立に、水素原子、重水素原子、ハロゲン原子、置換若しくは無置換の環形成炭素数6~60の芳香族炭化水素基、又は、置換若しくは無置換の環形成原子数5~60の芳香族複素環基であり、隣接する基と結合して新たな環を形成してもよく、
mは1~4の整数であり、
pは1~4の整数であり、pが2以上の場合、L12は、p個のCzのいずれに結合してもよい]で表される化合物であり、
Lは、複数のAのいずれに結合してもよい連結基、又は単結合を表し、
nは1~4の整数であり、nが1の場合には、式(1)と式(2)とは同一の化合物を表す。
Xは、酸素原子、又は硫黄原子であり、
Azは、置換若しくは無置換の環形成原子数5~60の含窒素芳香族複素環基であり、
Czは、置換若しくは無置換のカルバゾール、置換若しくは無置換のアザカルバゾール、置換若しくは無置換のベンゾカルバゾール、置換若しくは無置換のヒドロカルバゾール、置換若しくは無置換のアクリジン、置換若しくは無置換のインドール、置換若しくは無置換のキサンテン、置換若しくは無置換のフェノキサジン、又は置換若しくは無置換のジフェニルアミンから誘導された基であり、複数の置換基を有する場合、隣接する置換基が結合して新たな環を形成してもよく、
L11及びL12は、それぞれ独立に、単結合、置換若しくは無置換の環形成炭素数6~60の芳香族炭化水素基、又は、置換若しくは無置換の環形成原子数5~60の芳香族複素環基であり、
R1は、水素原子、重水素原子、ハロゲン原子、置換若しくは無置換の環形成炭素数6~60の芳香族炭化水素基、又は、置換若しくは無置換の環形成原子数5~60の芳香族複素環基であり、
R2~R7は、それぞれ独立に、水素原子、重水素原子、ハロゲン原子、置換若しくは無置換の環形成炭素数6~60の芳香族炭化水素基、又は、置換若しくは無置換の環形成原子数5~60の芳香族複素環基であり、隣接する基と結合して新たな環を形成してもよく、
mは1~4の整数であり、
pは1~4の整数であり、pが2以上の場合、L12は、p個のCzのいずれに結合してもよい。
Lは、複数のAのいずれに結合してもよい連結基、又は単結合を表し、
nは1~4の整数であり、nが1の場合には、上式(1)と上式(2)とは同一の化合物を表す。そして、上式(1)で表される化合物に含まれる芳香環の数は、9~60である。
(合成例1)
米国特許出願公開第2016/0111657号明細書に準拠して、本形態による化合物有機エレクトロルミネッセンス素子用化合物であるHost-1を以下の通りに合成した。
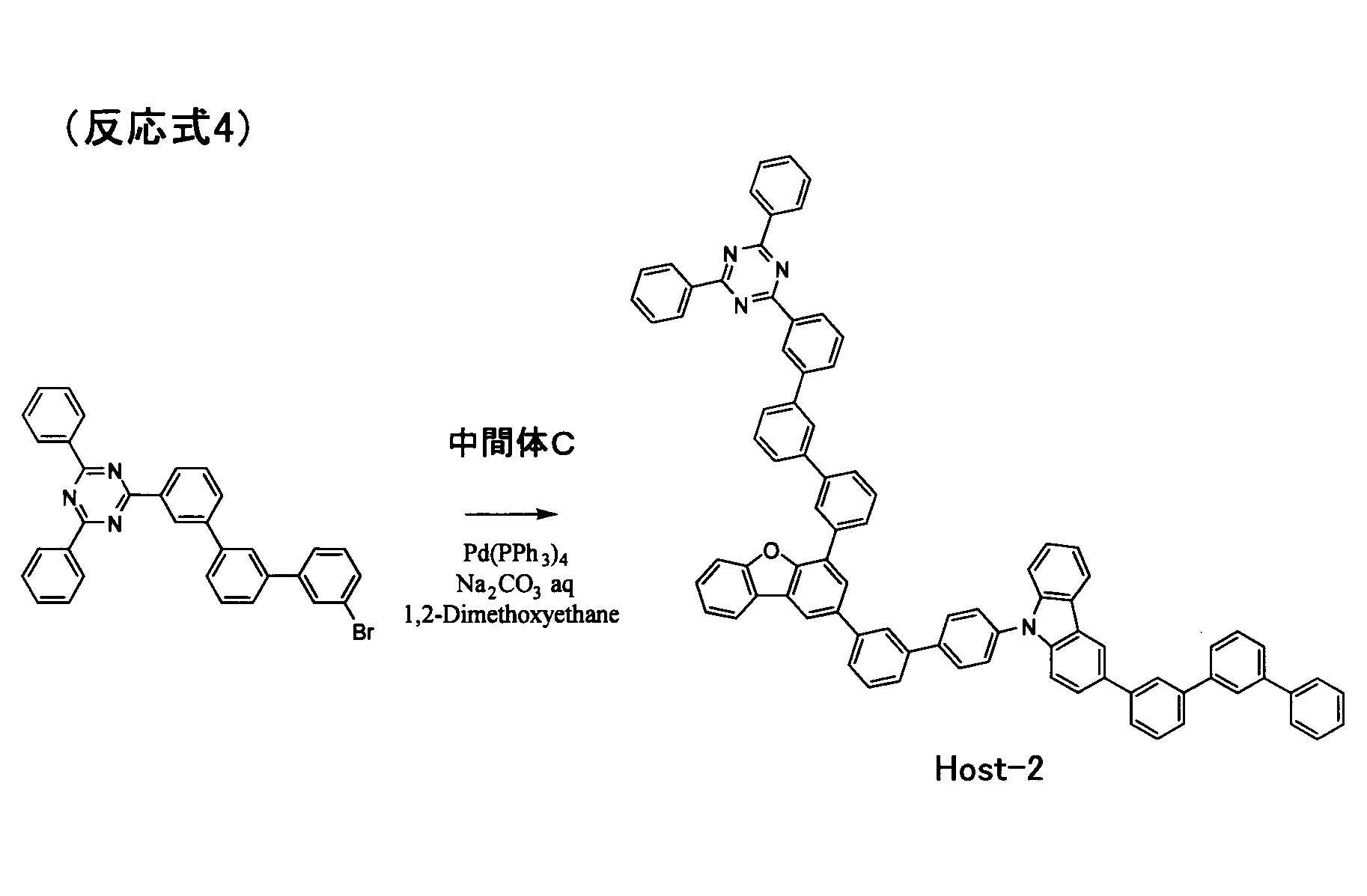
合成例1と同様にして、Host-2を合成した。但し、合成例2においては、反応式3に代えて、下記反応式4に従って合成を行った。
(実施例1)
第1電極(陽極)としてストライプ(stripe)状の酸化インジウムスズ(ITO)が膜厚150nmにて成膜されたガラス基板上に、PEDOT-PSS(poly(3,4-ethylene dioxythiophene)/poly(4-styrene sulfonate)(Sigma-Aldrich社製)を乾燥膜厚が15nmになるようにスピンコート法にて塗布し、正孔注入層を形成した。
Host化合物を、表1のように変更した以外は実施例1と同様にして、有機エレクトロルミネッセンス素子を作製、素子特性を評価した。
発光層用塗布液を調整する際に、ホスト材料として、host-a及びhost-bを用いたこと以外は実施例1と同様にして、有機エレクトロルミネッセンス素子を作製した。なお、host-aとhost-bとの質量比は5:5とした。
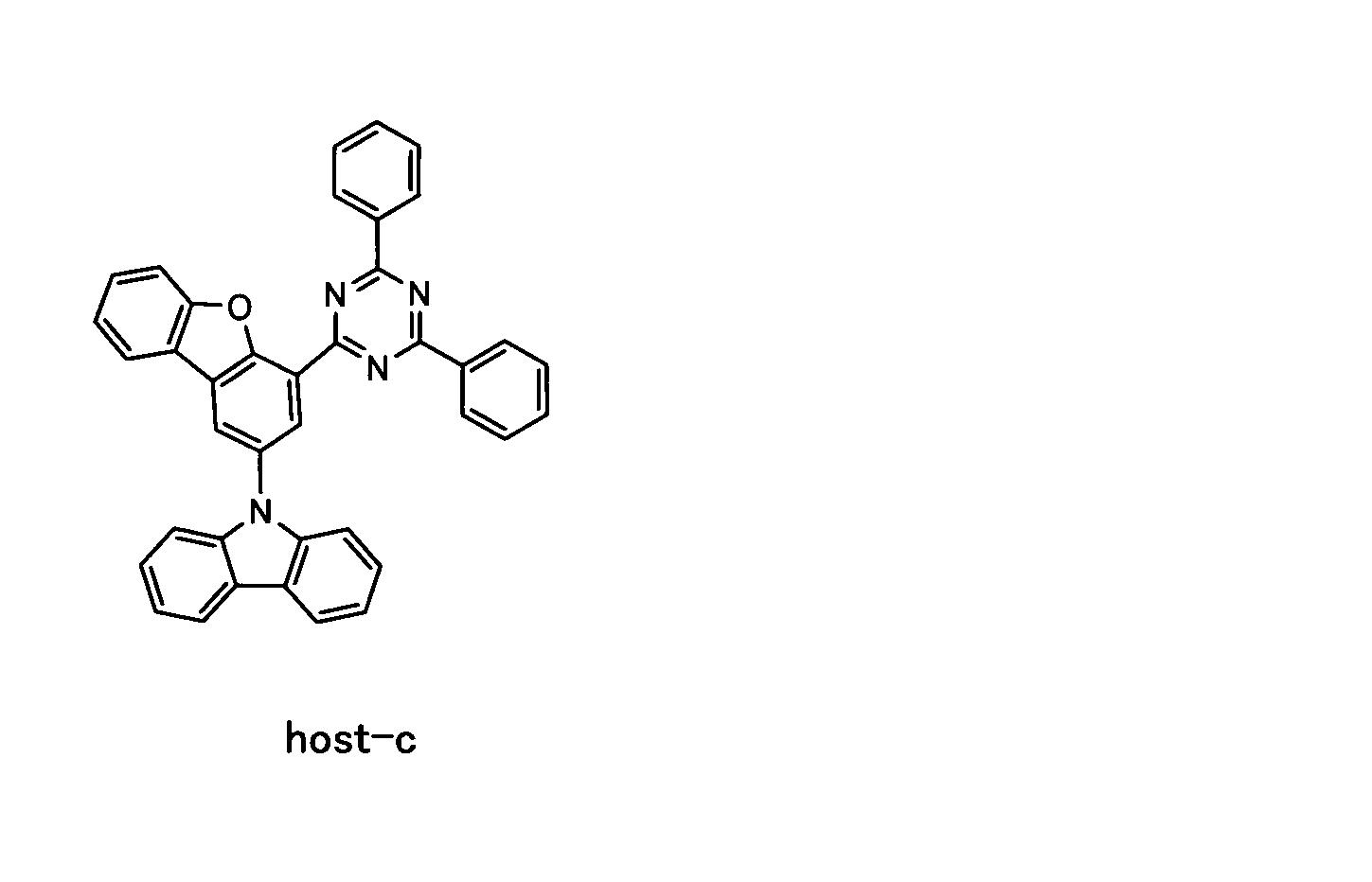
発光層用塗布液を調製する際にhost-cを用いたこと以外は実施例1と同様にして、有機エレクトロルミネッセンス素子の作製を試みた。しかし、host-cが、安息香酸メチルに溶解せず、素子作製ができなかった。
有機エレクトロルミネッセンス素子の発光効率、及び発光寿命を、以下の方法にて評価した。なお、本実施例では、発光効率は電流効率(cd/A)で評価した。
110 基板
120 第1電極
130 正孔注入層
140 正孔輸送層
150 発光層
160 電子輸送層
170 電子注入層
180 第2電極
Claims (7)
- 分子量が850~3000である、請求項1に記載の有機エレクトロルミネッセンス素子用化合物。
- ホスト材料又は電荷輸送材料として用いられる、請求項1又は2に記載の有機エレクトロルミネッセンス素子用化合物。
- 請求項1~3のいずれか一項に記載の有機エレクトロルミネッセンス素子用化合物と、溶媒とを含有する、液状組成物。
- 請求項1~3のいずれか一項に記載の有機エレクトロルミネッセンス素子用化合物を含有する、インク組成物。
- 請求項1~3のいずれか一項に記載の有機エレクトロルミネッセンス素子用化合物を含有する、薄膜。
- 第1電極と、
前記第1電極に対向して設けられた第2電極と、
前記第1電極と前記第2電極との間に設けられた有機層と
を備え、
前記有機層は、請求項1~3のいずれか一項に記載された有機エレクトロルミネッセンス素子用化合物を含有する、有機エレクトロルミネッセンス素子。
Priority Applications (6)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2017244291A JP7145608B2 (ja) | 2017-12-20 | 2017-12-20 | 有機エレクトロルミネッセンス素子用化合物、液状組成物、インク組成物、薄膜、及び有機エレクトロルミネッセンス素子 |
| KR1020180076110A KR102592697B1 (ko) | 2017-12-20 | 2018-06-29 | 축합환 화합물, 이를 포함하는 조성물 및 이를 포함하는 유기 발광 소자 |
| EP18206972.4A EP3502108A1 (en) | 2017-12-20 | 2018-11-19 | Condensed cyclic compound, composition including the condensed cyclic compound, and organic light-emitting device including the composition |
| CN201811478220.XA CN109942558A (zh) | 2017-12-20 | 2018-12-05 | 稠环化合物、以及包括其的组合物和有机发光器件 |
| US16/217,194 US11700767B2 (en) | 2017-12-20 | 2018-12-12 | Condensed cyclic compound, composition including the condensed cyclic compound, and organic light-emitting device including the composition |
| US18/320,576 US20230292607A1 (en) | 2017-12-20 | 2023-05-19 | Condensed cyclic compound, composition including the condensed cyclic compound, and organic light-emitting device including the composition |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2017244291A JP7145608B2 (ja) | 2017-12-20 | 2017-12-20 | 有機エレクトロルミネッセンス素子用化合物、液状組成物、インク組成物、薄膜、及び有機エレクトロルミネッセンス素子 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2019108315A JP2019108315A (ja) | 2019-07-04 |
| JP7145608B2 true JP7145608B2 (ja) | 2022-10-03 |
Family
ID=67066250
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2017244291A Active JP7145608B2 (ja) | 2017-12-20 | 2017-12-20 | 有機エレクトロルミネッセンス素子用化合物、液状組成物、インク組成物、薄膜、及び有機エレクトロルミネッセンス素子 |
Country Status (2)
| Country | Link |
|---|---|
| JP (1) | JP7145608B2 (ja) |
| KR (1) | KR102592697B1 (ja) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2020060286A1 (ko) * | 2018-09-21 | 2020-03-26 | 주식회사 엘지화학 | 신규한 헤테로 고리 화합물 및 이를 이용한 유기 발광 소자 |
| WO2023181507A1 (ja) * | 2022-03-25 | 2023-09-28 | 三菱ケミカル株式会社 | 有機電界発光素子の発光層用材料、発光層形成用組成物、有機電界発光素子、及び有機電界発光素子の製造方法 |
Citations (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2012028548A (ja) | 2010-07-23 | 2012-02-09 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子用材料、および有機エレクトロルミネッセンス素子、これを用いた表示装置、照明装置 |
| JP2013069905A (ja) | 2011-09-22 | 2013-04-18 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子、表示装置、照明装置および有機エレクトロルミネッセンス材料 |
| JP2013110262A (ja) | 2011-11-21 | 2013-06-06 | Konica Minolta Holdings Inc | 有機el素子ならびに有機elモジュールおよびその製造方法 |
| WO2013180020A1 (ja) | 2012-05-31 | 2013-12-05 | コニカミノルタ株式会社 | 透明電極、電子デバイス及び有機エレクトロルミネッセンス素子 |
| JP2014116454A (ja) | 2012-12-10 | 2014-06-26 | Konica Minolta Inc | 有機エレクトロルミネッセンス素子材料及び有機エレクトロルミネッセンス素子 |
| WO2014163083A1 (ja) | 2013-04-05 | 2014-10-09 | コニカミノルタ株式会社 | 発光層形成用塗布液、有機エレクトロルミネッセンス素子とその製造方法及び照明・表示装置 |
| WO2016175068A1 (ja) | 2015-04-27 | 2016-11-03 | コニカミノルタ株式会社 | 有機エレクトロルミネッセンス素子用材料、有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| WO2017018795A2 (ko) | 2015-07-27 | 2017-02-02 | 희성소재(주) | 헤테로고리 화합물 및 이를 이용한 유기 발광 소자 |
| WO2017078494A1 (ko) | 2015-11-06 | 2017-05-11 | 희성소재(주) | 헤테로고리 화합물 및 이를 이용한 유기 발광 소자 |
| WO2017099490A1 (ko) | 2015-12-08 | 2017-06-15 | 희성소재(주) | 헤테로고리 화합물 및 이를 이용한 유기 발광 소자 |
| WO2017099471A1 (ko) | 2015-12-08 | 2017-06-15 | 주식회사 엘지화학 | 헤테로고리 화합물 및 이를 포함하는 유기 발광 소자 |
| CN107226811A (zh) | 2017-06-07 | 2017-10-03 | 江苏三月光电科技有限公司 | 一种以二联二苯并五元杂环为骨架的有机化合物及其在oled上的应用 |
| WO2017196081A1 (en) | 2016-05-11 | 2017-11-16 | Sk Chemicals Co., Ltd. | Compound for organic electroluminescent device and organic electroluminescent device comprising the same |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR102283293B1 (ko) * | 2014-12-26 | 2021-07-28 | 솔루스첨단소재 주식회사 | 유기 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| JP5831654B1 (ja) * | 2015-02-13 | 2015-12-09 | コニカミノルタ株式会社 | 芳香族複素環誘導体、それを用いた有機エレクトロルミネッセンス素子、照明装置及び表示装置 |
| KR101805686B1 (ko) * | 2015-07-27 | 2017-12-07 | 희성소재(주) | 헤테로고리 화합물 및 이를 이용한 유기 발광 소자 |
| KR101991428B1 (ko) * | 2015-11-17 | 2019-06-20 | 주식회사 엘지화학 | 헤테로고리 화합물 및 이를 포함하는 유기 전자 소자 |
| KR20170127353A (ko) * | 2016-05-11 | 2017-11-21 | 에스케이케미칼주식회사 | 유기전계발광소자용 화합물 및 그를 포함하는 유기전계발광소자 |
-
2017
- 2017-12-20 JP JP2017244291A patent/JP7145608B2/ja active Active
-
2018
- 2018-06-29 KR KR1020180076110A patent/KR102592697B1/ko active Active
Patent Citations (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2012028548A (ja) | 2010-07-23 | 2012-02-09 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子用材料、および有機エレクトロルミネッセンス素子、これを用いた表示装置、照明装置 |
| JP2013069905A (ja) | 2011-09-22 | 2013-04-18 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子、表示装置、照明装置および有機エレクトロルミネッセンス材料 |
| JP2013110262A (ja) | 2011-11-21 | 2013-06-06 | Konica Minolta Holdings Inc | 有機el素子ならびに有機elモジュールおよびその製造方法 |
| WO2013180020A1 (ja) | 2012-05-31 | 2013-12-05 | コニカミノルタ株式会社 | 透明電極、電子デバイス及び有機エレクトロルミネッセンス素子 |
| JP2014116454A (ja) | 2012-12-10 | 2014-06-26 | Konica Minolta Inc | 有機エレクトロルミネッセンス素子材料及び有機エレクトロルミネッセンス素子 |
| WO2014163083A1 (ja) | 2013-04-05 | 2014-10-09 | コニカミノルタ株式会社 | 発光層形成用塗布液、有機エレクトロルミネッセンス素子とその製造方法及び照明・表示装置 |
| WO2016175068A1 (ja) | 2015-04-27 | 2016-11-03 | コニカミノルタ株式会社 | 有機エレクトロルミネッセンス素子用材料、有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| WO2017018795A2 (ko) | 2015-07-27 | 2017-02-02 | 희성소재(주) | 헤테로고리 화합물 및 이를 이용한 유기 발광 소자 |
| WO2017078494A1 (ko) | 2015-11-06 | 2017-05-11 | 희성소재(주) | 헤테로고리 화합물 및 이를 이용한 유기 발광 소자 |
| WO2017099490A1 (ko) | 2015-12-08 | 2017-06-15 | 희성소재(주) | 헤테로고리 화합물 및 이를 이용한 유기 발광 소자 |
| WO2017099471A1 (ko) | 2015-12-08 | 2017-06-15 | 주식회사 엘지화학 | 헤테로고리 화합물 및 이를 포함하는 유기 발광 소자 |
| WO2017196081A1 (en) | 2016-05-11 | 2017-11-16 | Sk Chemicals Co., Ltd. | Compound for organic electroluminescent device and organic electroluminescent device comprising the same |
| CN107226811A (zh) | 2017-06-07 | 2017-10-03 | 江苏三月光电科技有限公司 | 一种以二联二苯并五元杂环为骨架的有机化合物及其在oled上的应用 |
Non-Patent Citations (1)
| Title |
|---|
| Gilman, H. et al.,Dibenzofuran. II. Metalation,Journal of the American Chemical Society,1934年,(1934), 56, 1415-16 |
Also Published As
| Publication number | Publication date |
|---|---|
| KR102592697B1 (ko) | 2023-10-23 |
| KR20190074931A (ko) | 2019-06-28 |
| JP2019108315A (ja) | 2019-07-04 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN109075261B (zh) | 有机发光器件 | |
| KR101881082B1 (ko) | 카보레인 화합물, 이를 포함한 유기 전계 발광 소자 및 상기 유기 전계 발광 소자를 포함하는 평판 표시 장치 | |
| KR101565724B1 (ko) | 트리페닐렌기를 포함하는 벤조 융합 티오펜 또는 벤조 융합 푸란 화합물 | |
| CN112585145B (zh) | 多环化合物和包含其的有机发光器件 | |
| US9290498B2 (en) | Organic electroluminescent device having an electron- and/or exciton-blocking layer comprising an indolocarbazole compound | |
| KR102181234B1 (ko) | 화합물 및 이를 포함한 유기 발광 소자 | |
| US10336772B2 (en) | Bicarbazole compound, material for organic light-emitting device including bicarbazole compound, and organic light-emitting device including bicarbazole compound | |
| KR102792548B1 (ko) | 비카바졸 화합물, 이를 포함하는 유기 발광 소자용 재료 및 이를 포함하는 유기 발광 소자 | |
| KR101885696B1 (ko) | 헤테로고리 화합물, 이를 포함한 유기 전계 발광 소자 및 상기 유기 전계 발광 소자를 포함하는 평판 표시 장치 | |
| JP6940275B2 (ja) | 化合物、有機エレクトロルミネッセンス素子材料、有機エレクトロルミネッセンス素子製造用組成物および有機エレクトロルミネッセンス素子 | |
| KR102125619B1 (ko) | 신규 화합물 및 이를 포함하는 유기 발광 소자 | |
| KR102203102B1 (ko) | 화합물 및 이를 포함한 유기 발광 소자 | |
| TWI580759B (zh) | 新型稠環化合物及包含其之有機發光裝置 | |
| TW201410662A (zh) | 雜環化合物、包含其之有機發光裝置以及包含有機發光裝置的有機發光顯示設備 | |
| JP7512556B2 (ja) | 新規な化合物およびこれを利用した有機発光素子 | |
| KR20150025529A (ko) | 축합환 화합물을 포함하는 유기 전계 발광 소자 | |
| KR20160082209A (ko) | 화합물 및 이를 포함하는 유기 발광 소자 | |
| CN106045863A (zh) | 化合物及包含该化合物的有机发光装置 | |
| CN111225905A (zh) | 杂环化合物及包含其的有机发光器件 | |
| JP7186037B2 (ja) | 含窒素化合物及びそれを含む有機電界発光素子 | |
| KR102504296B1 (ko) | 유기 전계 발광 소자용 재료 및 이를 포함하는 유기 전계 발광 소자 | |
| CN106518748A (zh) | 化合物、包括其的有机发光装置及平板显示器装置 | |
| JP7145608B2 (ja) | 有機エレクトロルミネッセンス素子用化合物、液状組成物、インク組成物、薄膜、及び有機エレクトロルミネッセンス素子 | |
| KR20150105534A (ko) | 화합물 및 이를 포함한 유기 발광 소자 | |
| KR20120092910A (ko) | 인돌로티오펜 유도체 및 이를 포함하는 유기전계발광소자 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20201218 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20211022 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20211102 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220126 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20220607 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220714 |
|
| C60 | Trial request (containing other claim documents, opposition documents) |
Free format text: JAPANESE INTERMEDIATE CODE: C60 Effective date: 20220714 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20220726 |
|
| C21 | Notice of transfer of a case for reconsideration by examiners before appeal proceedings |
Free format text: JAPANESE INTERMEDIATE CODE: C21 Effective date: 20220802 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20220823 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20220920 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7145608 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |