JP7057281B2 - 眼疾患のための遺伝子療法 - Google Patents
眼疾患のための遺伝子療法 Download PDFInfo
- Publication number
- JP7057281B2 JP7057281B2 JP2018531202A JP2018531202A JP7057281B2 JP 7057281 B2 JP7057281 B2 JP 7057281B2 JP 2018531202 A JP2018531202 A JP 2018531202A JP 2018531202 A JP2018531202 A JP 2018531202A JP 7057281 B2 JP7057281 B2 JP 7057281B2
- Authority
- JP
- Japan
- Prior art keywords
- aav
- promoter
- seq
- sequence
- expression
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
- A61K48/005—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy characterised by an aspect of the 'active' part of the composition delivered, i.e. the nucleic acid delivered
- A61K48/0058—Nucleic acids adapted for tissue specific expression, e.g. having tissue specific promoters as part of a contruct
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0048—Eye, e.g. artificial tears
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/46—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates
- C07K14/47—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates from mammals
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/79—Vectors or expression systems specially adapted for eukaryotic hosts
- C12N15/85—Vectors or expression systems specially adapted for eukaryotic hosts for animal cells
- C12N15/86—Viral vectors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2750/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssDNA viruses
- C12N2750/00011—Details
- C12N2750/14011—Parvoviridae
- C12N2750/14111—Dependovirus, e.g. adenoassociated viruses
- C12N2750/14141—Use of virus, viral particle or viral elements as a vector
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2750/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssDNA viruses
- C12N2750/00011—Details
- C12N2750/14011—Parvoviridae
- C12N2750/14111—Dependovirus, e.g. adenoassociated viruses
- C12N2750/14141—Use of virus, viral particle or viral elements as a vector
- C12N2750/14143—Use of virus, viral particle or viral elements as a vector viral genome or elements thereof as genetic vector
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2799/00—Uses of viruses
- C12N2799/02—Uses of viruses as vector
- C12N2799/021—Uses of viruses as vector for the expression of a heterologous nucleic acid
- C12N2799/022—Uses of viruses as vector for the expression of a heterologous nucleic acid where the vector is derived from an adenovirus
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2799/00—Uses of viruses
- C12N2799/02—Uses of viruses as vector
- C12N2799/04—Uses of viruses as vector in vivo
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2800/00—Nucleic acids vectors
- C12N2800/10—Plasmid DNA
- C12N2800/106—Plasmid DNA for vertebrates
- C12N2800/107—Plasmid DNA for vertebrates for mammalian
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2800/00—Nucleic acids vectors
- C12N2800/22—Vectors comprising a coding region that has been codon optimised for expression in a respective host
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2840/00—Vectors comprising a special translation-regulating system
- C12N2840/002—Vectors comprising a special translation-regulating system controllable or inducible
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2840/00—Vectors comprising a special translation-regulating system
- C12N2840/007—Vectors comprising a special translation-regulating system cell or tissue specific
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Genetics & Genomics (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Molecular Biology (AREA)
- Zoology (AREA)
- Biotechnology (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Biochemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biomedical Technology (AREA)
- Epidemiology (AREA)
- Biophysics (AREA)
- General Engineering & Computer Science (AREA)
- Wood Science & Technology (AREA)
- Ophthalmology & Optometry (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Gastroenterology & Hepatology (AREA)
- Toxicology (AREA)
- Plant Pathology (AREA)
- Virology (AREA)
- Physics & Mathematics (AREA)
- Microbiology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Cell Biology (AREA)
- Immunology (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
Description
出願人は、電子形態で添付して申請される配列表材料を、本明細書の一部を構成するものとして援用する。このファイルは“16-7660PCT_Seq_Listing_ST25.txt”と標識される。
コロイデレミア(CHM)は、X-連鎖遺伝性網膜疾患であり、光受容体、網膜色素上皮(RPE)及び脈絡毛細管板の変性を特徴とする。症状は夜間視覚の悪さ(夜盲症)及び周辺視覚の進行的な喪失の病訴を以て生後10歳未満又は20歳未満に現れる。疾患の進行とともに視野は狭まる。これは、早い場合には30歳代に、中心視覚(視力)の喪失及び失明を以て最高点に達する。140種類を超えるCHM遺伝子中の突然変異がコロイデレミアを引き起こすことが見出された。突然変異は異常に小さい、非機能性及び/又は不安定なRabエスコートタンパク質-1(REP-1)タンパク質の産生、タンパク質の機能における低下又はREP-1タンパク質産生の喪失を生ずる場合がある。正常なREP-1の欠如は、細胞内トラフィッキングを助けるRabタンパク質の能力を崩壊させる。細胞内におけるタンパク質及び細胞小器官の移動不全は細胞の機能を衰えさせ、かつ早死にをもたらす。
コロイデレミア(CHM)はX-連鎖網膜変性であり、それは生後10歳未満又は20歳未満に夜盲症及び周辺視覚の喪失を引き起こして発症する。疾患は中年期を通じて進行し、その頃にほとんどの被験者は失明する。CHMは遺伝子増強療法(gene augmentation therapy)のための好ましい標的であり、それは疾患が網膜細胞の健康に必要なタンパク質、CHM遺伝子によりコードされるRabエスコートタンパク質1(REP1)の機能の喪失の故だからである。ヒトの遺伝子療法研究において確立された実績を有する組換えアデノ関連ウイルス(rAAV)中にCHMcDNAをパッケージングする場合がある。さらに、Rab27のようなRabタンパク質をプレニル化し、REP-1欠損細胞中のプレニル化の欠如の故のRab27局在化及びトラフィッキングにおける欠陥を修正するREP1の能力を含むその活性を実証(document)するための高感度かつ定量的なアッセイがある。
A配列はヒトにおける発現のためにコドン最適化される。
を含む。
本明細書に説明される方法及び組成物は、眼疾患、主にコロイデレミアのような失明疾患の処置のために哺乳類被験者にREP-1をコードする最適化CHMを送達するための組成物及び方法を含む。さらに、本明細書に説明される方法及び組成物は、眼疾患、主に色覚異常のような失明疾患の処置のために哺乳類被験者に最適化CNGA3又はCNGB3を送達するための組成物及び方法を含む。1つの態様において、そのような組成物はREP-1、CNGA3又はCNGB3コード配列のコドン最適化を含む。これらの特徴は産物の有効性を向上させ、より低用量の試薬(reagent)が用いられるので安全性を向上させると思われる。この導入遺伝子カセットの最適化は、内在性配列を用いて産生され得るレベルと比較して実験的タンパク質の産生のレベルを理論的に最大にする場合があると思われる。しかしながら、それぞれ配列番号3、配列番号13及び配列番号19に示されるような天然のREP1、CNGA3及びCNGB3コード配列を含む組成物も本明細書に含まれる。REP-1、CNGA3又はCNGB3のいずれかに関して態様が説
明される場合、類似の態様が他に引用されることが意図されていることが理解されるべきである。
含まれる。1つの態様において、被験者は色覚異常を有する。他の態様において、被験者はコロイデレミア又はX-連鎖遺伝性網膜変性を有する。そのよう眼疾患の臨床的徴候は、周辺視覚の低下、中心(読書(reading))視覚の低下、夜間視覚の低下、色覚の喪失、視力の低下、光受容体機能の低下、色素変化(pigmentary changes)及び究極的に失明を含むがこれらに限られない。
るなら自然の環境)から取り出されていることを意味する。例えば生きている動物中に存在する天然のポリヌクレオチド又はポリペプチドは単離されていないが、自然界で共存する材料の一部又は全部から分離された同じポリヌクレオチド又はポリペプチドは、その後自然界に再導入されるとしても単離されている。そのようなポリヌクレオチドはベクターの一部となり得、及び/又は、そのようなポリヌクレオチド又はポリペプチドは組成物の一部となり得るが、それでもまだそのようなベクター又は組成物はその自然環境の一部でない点で単離されている。
Press,Cold Spring Harbor,NY(2012)を参照されたい。
うなプラスミド中へのクローニングのための制限部位を含む。配列番号23のヌクレオチド13から2448はCNGB3のためのORFを与える。一部の態様において、導入遺伝子は配列番号20の配列をコードするコドン最適化CNGB3である。一部の態様において、導入遺伝子は配列番号19に示される配列によりコードされる。一部の態様において、導入遺伝子は配列番号21に示される配列によりコードされる。一部の態様において、導入遺伝子は本明細書に説明されるプラスミドのようなプラスミド中へのクローニングのために改変された末端を含む。配列番号21は、あるサイレント突然変異が天然のコード配列に導入されている新規なcDNA配列である。本明細書に説明される天然の配列へのさらなる改変は本発明が意図するものである。
用いて組換えAAVゲノムを作製する。
AV6、AAV7、AAV8、AAV9、AAV8bp、AAV7M8及びAAVAnc80か、既知の又は言及されたAAVsのいずれかの変異体か、未発見のAAVsあるいはそれらの変異体又は混合物を含むがこれらに限られないいずれのAAVかの中からも容易に選ばれる場合がある。例えば引用により本明細書に取り込まれる国際公開第2005/033321号パンフレットを参照されたい。別の態様において、AAVキャプシドは優先的に双極細胞を標的とするAAV8bpキャプシドである。引用により本明細書に取り込まれる国際公開第2014/024282号パンフレットを参照されたい。別の態様において、AAVキャプシドは外側網膜(outer retina)への優先的送達を示したAAV7m8キャプシドである。引用により本明細書に取り込まれるDalkaraら、In Vivo-Directed Evolution of a New Adeno-Associated Virus for Therapeutic Outer Retinal Gene Delivery from the Vitreous,Sci Transl Med 5,189ra76(2013)を参照されたい。1つの態様において、AAVキャプシドはAAV8キャプシドである。別の態様において、AAVキャプシドはAAV9キャプシドである。別の態様において、AAVキャプシドはAAV5キャプシドである。別の態様において、AAVキャプシドはAAV2キャプシドである。
プシド、組換えAAVキャプシド又は「ヒト化(humanized)」AAVキャプシドの場合があるが、これに限られない。1ある種のAAVのキャプシドが別種のキャプシドタンパク質で置き換えられている偽型ベクターは本発明において有用である。1つの態様において、AAV2/5及びAAV2/8は代表的な偽型ベクターである。
%又は少なくとも90%のパーセント同一性を有する場合がある。1つの態様において、コドン最適化REP-1は、天然の配列と少なくとも51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98又は99%のパーセント同一性を有する。1つの態様において、天然の核酸配列番号3と並べられると、コドン最適化REP-1(配列番号1)はわずか74%のパーセント配列同一性を有することが明らかになった(図2を参照されたい)。
、遺伝的要素はプラスミドである。
;欧州特許第1310571号明細書を参照されたい。国際公開第2003/042397号パンフレット(AAV7及び他のサルAAV)、米国特許第7790449号明細書及び米国特許第7282199号明細書(AAV8)、国際公開第2005/033321号パンフレット及び米国特許第7,906,111号明細書(AAV9)ならびに国際公開第2006/110689号パンフレット及び国際公開第2003/042397号パンフレット(rh.10)も参照されたい。これらの文書はAAVの作製のために選ばれることがある他のAAVも説明しており、それらの記載事項は引用することにより本明細書の内容となる。いくつかの態様において、ウイルスベクター中で用いるためのAAV
capを、上記で挙げたAAV キャプシド又はそのコード核酸の1つの突然変異誘発により(すなわち挿入、欠失又は置換により)作製する場合がある。いくつかの態様において、AAVキャプシドは、前記で挙げたAAVキャプシドたんぱく質の2つ又は3つ又は4つ又はそれより多くからのドメインを含むキメラである。いくつかの態様において、AAVキャプシドは2又は3種のAAVsあるいは組換えAAVsからのVp1、Vp2及びVp3モノマーのモザイクである。いくつかの態様において、rAAV組成物は前記で挙げたCapsの1つより多くを含む。
approach,Gene Therapy 21,96-105(January
2014)に説明されており、引用により本明細書に取り込まれる。
vector:Vector development,production and clinical spplicatioons,”Adv.Biochem.Engin/Biotechnol.99:119-145;Buningら、2008,“Recent developments in adeno-associated virus vector technology,”J.Gene Med.10:717-733及び下記で引用される参照文献を参照されたく、それらのそれぞれの記載事項全体は引用により本明細書に取り込まれる。
gene encoding human rhodopsin,PNAS,81:4851-5(August 1984)を参照されたい。別の態様において、プロモーターはヒトロドプシンプロモーターの一部又はフラグメントである。別の態様において、プロモーターはヒトロドプシンプロモーターの変異体である。
が本明細書に取り込まれるShuら、IOVS,May 2102)。本発明において有用な他のプロモーターには杆体オプシンプロモーター、赤-緑オプシンプロモーター、青オプシンプロモーター、cGMP-β-ホスホジエステラーゼプロモーター(Qguetaら、IOVS,Invest Ophthalmol Vis Sci.2000 Dec;41(13):4059-63)、マウスオプシンプロモーター(上記で引用したBeltran et al 2010)、ロドプシンプロモーター(Mussolinoら、Gene Ther,July 2011,18(7):637-45);錐体トランスジューシンのアルファ-サブユニット(Morrisseyら、BMC Dev,Biol,Jan 2011,11:3);ベータホスホジエステラーゼ(PDE)プロモーター;網膜色素変性症(RP1)プロモーター(Nicordら、J.Gene Med,Dec 2007,9(12):1015-23);NXNL2/NXNL1プロモーター(Lambardら、PloS One,Oct.2010,5(10):el3025)、RPE65プロモーター;網膜変性スロー(retinal degeneration slow)/ペリフェリン2(Rds/perph2)プロモーター(Caiら、Exp Eye Res.2010 Ayg;91(2):186-94);及びVMD2プロモーター(Kachiら、Human Gene Therapy,2009(20:31-9))が含まれるが、これに限られない。これらの文書のそれぞれは引用によりその全体が本明細書に取り込まれる。別の態様において、プロモーターはヒトEF1αプロモーター、ロドプシンプロモーター、ロドプシンキナーゼ、光受容体間結合タンパク質(IRBP)、錐体オプシンプロモーター(赤-緑、青)、赤-緑錐体遺伝子座調節領域を含む錐体オプシン上流配列、錐体形質導入及び転写因子プロモーター(神経網膜ロイシンジッパー(neural retina leucine zipper)(Nrl)及び光受容体特異的核受容体Nr2e3、bZIP)から選ばれる。
又はヘテロダイマーリプレッサースイッチを含む既知のプロモーターから選ばれる場合がある。引用によりその全体が本明細書に取り込まれるSochorら、An Autogenously Regulated Expression System for Gene Therapeutic Ocular Applications.Scientific Reports.2015 Nov 24;5:17105及びDaber R,Lewis M.,A novel molecular switch.J
Mol Biol 2009 Aug 28;391(4):661-70,Epub
2009 Jun 21を参照されたい。
agents)、製薬学的薬剤(pharmaceutical agents)、安定剤、緩衝剤、担体、添加剤、希釈剤などの使用を含む。注入のために、担体は典型的に液体であろう。代表的な生理学的に許容され得る担体には発熱物質を含まない滅菌水及び発熱物質を含まない滅菌リン酸塩緩衝食塩水が含まれる。多様なそのような既知の担体が引用により本明細書に取り込まれる米国特許公開第7,629,322号明細書に提供されている。1つの態様において、担体は等張塩化ナトリウム溶液である。別の態様におい
て、担体は平衡塩溶液である。1つの態様において、担体はtweenを含む。ウイルスを長期間保存するべき場合、それをグリセロール又はTween20の存在下で凍結する場合がある。
×1012、3×1012、4×1012、5×1012、6×1012、7×1012、8×1012又は9×1012個のGCを含むように調製される。別の態様において、組成物は、すべての整数又は分数量を範囲内に含んで用量当たりに少なくとも1×1013、2×1013、3×1013、4×1013、5×1013、6×1013、7×1013、8×1013又は9×1013個のGCを含むように調製される。別の態様において、組成物は、すべての整数又は分数量を範囲内に含んで用量当たりに少なくとも1×1014、2×1014、3×1014、4×1014、5×1014、6×1014、7×1014、8×1014又は9×1014個のGCを含むように調製される。別の態様において、組成物は、すべての整数又は分数量を範囲内に含んで用量当たりに少なくとも1×1015、2×1015、3×1015、4×1015、5×1015、6×1015、7×1015、8×1015又は9×1015個のGCを含むように調製される。1つの態様において、ヒトへの適用のために用量は、すべての整数又は分数量を範囲内に含んで用量当たりに1×1010~約1×1012個のGCの範囲である場合がある。すべての用量は、例えば引用により本明細書に取り込まれるM.Lockら、Hum
Gene Methods.2014 Apr.25(2):115-24.Doi:10.1089/hgtb.2013.131に説明されているoqPCR又はデジタルドロップレットPCR(ddPCR)による測定を含むいずれかの既知の方法によって測定される場合がある。
れている被験者の種、それらの身体的状態又は健康ならびに用量に応じて網膜電図記録法(ERG)、視野測定法、共焦点走査型レーザー眼底検査法(confocal scanning laser ophthalmoscopy)(cSLO)及び光干渉断層撮影(OCT)による網膜の層のトポグラフィー的マッピング(topographical mapping)及びその層の厚さの測定、補償光学(AO)を介する錐体密度のトポグラフィー的マッピング、眼の機能性検査(functional eye exam)などを含む場合がある。画像化及び機能性研究の観点から、本発明のいくつかの態様において、罹患した眼の種々の領域を標的とするために、同じ眼において1回以上の注入が行われる。各注入の容積及びウイルス力価は本明細書でさらに説明される通りに個別に決定され、同じ又は反対側の眼において行われる他の注入と同じか又は異なる場合がある。別の態様において、眼全体を処置するために1回の比較的大きい容積の注入が行われる。1つの態様において、rAAV組成物の容積及び濃度は、損なわれた眼細胞の領域のみに影響を及ぼすように選ばれる。別の態様において、rAAV組成物の容積及び/又は濃度は、損なわれていない光受容体を含む眼のもっと大きい部分に達するために、もっと多量である。
である。これら及び他の有効性試験は、引用により本明細書に取り込まれる米国特許第8,147,823号明細書;同時係属国際特許出願公開国際公開第2014/011210号パンフレット又は国際公開第2014/124282号パンフレットに説明されている。
である。「からなる」(“consist”)、「からなる」(“consisting”)という用語及びその変形は包含的にではなく排他的に解釈されるべきである。明細書中の種々の態様は「含む」(“comprising”)の語法(language)を用いて提示されるが、他の状況下で、関連する態様は「からなる」(“consisting of”)又は「本質的にからなる」(“consisting essentially of”)の語法を用いて解釈されるべきことも意図されており、そのように説明される。
コロイデレミアは関連するマウスモデルを欠いており、かつイヌモデルはなく、従って疾患のヒト網膜細胞モデルにおいて形質導入及び発現を調べる。生存する被験者から網膜細胞を得るのは不可能なので、人工多能性幹細胞からRPEを作製する。引用によりその全体が本明細書に取り込まれるBuchholzら、Rapid and Efficient Directed Differentiation of Human Pluripotent Stem Cell Into Retinal Pigmented Epithelium,Stem Cells Translational Medicine,2013;2:384-393により説明されているプロトコルを用い、多能性幹細胞をRPEに方向付ける。引用によりその全体が本明細書に取り込まれるCeresoら、Proof of concept for AAV2/5-mediated gene therapy in iPSC-derived retinal
pigment epithelium of a choroideremia patient,Molecular Therapy-Methods & Clinical Development(2014)1,14011も参照されたい。RPEの作製のための他の方法は当該技術分野において既知である。
Dkk1、10ng/ml IGF1及び10mM ニコチンアミドを基本培地に加える。2日から4日に、10ng/ml Noggin、10ng/ml Dkk1、10ng/ml IGF1、5ng/ml bFGF及び10mM ニコチンアミドを基本培地に加える。4日から6日に、10ng/ml Dkk1、10ng/ml IGF1及び100ng/ml Activin A(R&D Systems)を基本培地に加える。6日から14日に、100ng/ml Activin A、10μM SU5402(EMD Millipore,Darmstadt,Germany)及び1mM VIPを基本培地に加える。基本培地のみ(DMEM/F12、B27、N2及びNEAA)中で対照標準実験を行う。
要するに、HEK293細胞の一過性トランスフェクションにより、REP-1コドン最適化配列が導入されたAAV2/8CMV.CBA-REP-1ウイルスベクターを作製し、ポリエチレングリコールを用いていずれかの(either)上澄み液からウイルス粒子を沈殿させる。例えば引用により本明細書に取り込まれるGuoら、Rapid and simplified purification of recombinant adeno-associated virus,J.Virol Methods.2012 Aug;183(2):139-146を参照されたい。ベクターを二重CsCl遠心により精製し、透析し、ドットブロットアッセイにより滴定する。
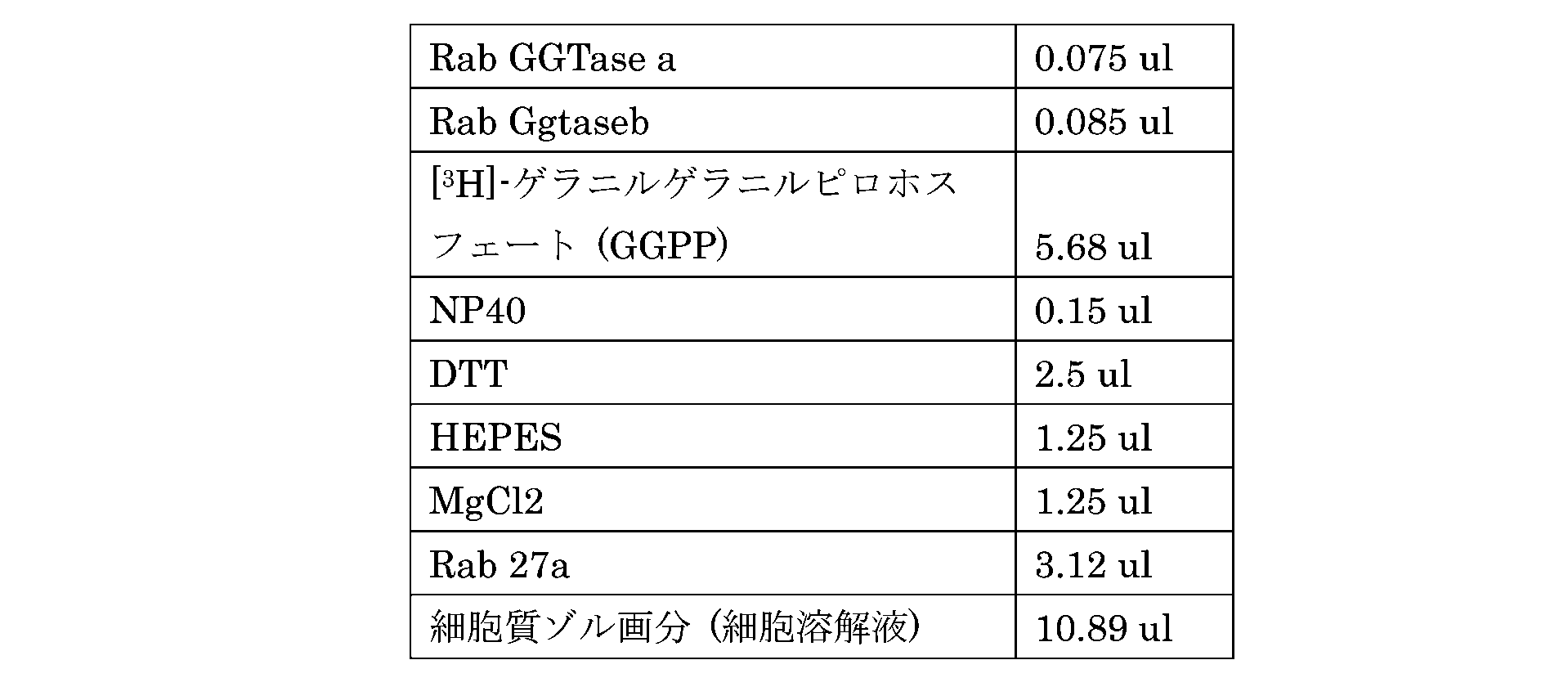
上記で引用したVasireddyら、PloS One.2013 May 7;8(5):e61396に説明されている通りに、プレニル基ドナーとして[3H]-ゲラニルゲラニルピロホスフェート(GGPP)(Perkin Elmer.Boston,MA,USA)を用い、組換えRabゲラニルゲラニルトランスフェラーゼ及びRAB27の存在下で試験管内プレニル化アッセイを行う。RAB27タンパク質中への放射性標識プレニル基の導入をシンチレーションカウンターにより測定する。一貫性のために、対照標準値を100に正規化(normalized)し、基本値として用いる。すべての実験を3回繰り返して行い、実験グループと対照標準グループの間のプレニル化の統計的な比較を両側非対スチューデントのテスト(two-tailed unpaired
studwnt’s test)を用いて評価する。
時間に及ぶ75,000-100 000gにおける細胞溶解液の遠心により、細胞質ゾル画分を集める。
この研究の目的は、コドン最適化CHM遺伝子(配列番号1)をコードする一系列の次世代AAV2及びAAV8ベクターを用いる遺伝子送達後の84-31及びCOS-7細胞株におけるAAV媒介CHM発現の能力を評価することであった。
gene)が続く。追加のプラスミドはスタッファーを欠いているが、カナマイシン選択遺伝子を含む。高-コピー数ベクターはpUCプラスミドのそれに類似である(バクテリア細胞当たりに約300個のコピー)。低コピー数プラスミド(バクテリア細胞当たりに約10個のコピー)はp15Aを起源とする。正しい開始コドンからの翻訳を増強するために、すべての次世代コンストラクトは開始コドン、ATGの上流にコザック共通配列を含む。作製されたプラスミドを、プロモーター+エンハンサー伸長(extention)配列又はコドン最適化CHM配列のいずれかを特異的に標的とすることができるプライマーを用いて配列検証する。5つのコンストラクトすべてのプラスミドマップ及び配列を図6-10に示す。リン酸カルシウムを用いる標準的な三重トランスフェクションを用いて下記に挙げるAAVベクターを作製した(ベクターの定性(qualification)に関して表2を参照されたい)。AAV2及びAAV8血清型のベクターの両方を作製し、結果が血清型-非依存性であることを確かめた。
AAV形質導入された細胞を未処理の対照標準細胞と共に、十分なPBS洗浄の後に回収した。次いでプロテアーゼ阻害剤を有するRIPA緩衝液を用いて、細胞を氷上で溶解した。13,000rpmにおける10分間の遠心により細胞溶解液を透明にした。2.タンパク質の定量及び調製。ThermoFisher Micro BCATM Protein Assay Kitを用い、製造者の指示に従って細胞溶解液のタンパク質定量を行った。562nmにおけるOD読み取り値を得ることにより、タンパク質濃度を決定した。CHMの試験管内発現を評価するために、4-12% Bis-Trisゲル上に40-60μgの測定されたタンパク質を負荷した。3.既知のプロトコルに従ってSDS-PAGE及びブロッティングSDS-PAGEならびにウェスタンブロット分析を行った。要するに、タンパク質ゲルをニトロセルロース膜上に転移させ、ミルク中でブロッキングし、一次抗体と一緒にインキュベーションした。抗ヒトREP-1 2F1抗体(2F1,1:1000希釈)及び以下:抗GAPDH抗体(1:1000希釈)、抗アクチン抗体(1:1000希釈)又は抗チューブリン抗体(1:5000希釈)の1つを各ブロットのための一次抗体として用いた。ブロットの洗浄後、1:5000の濃度におけるHRP共役抗マウスIgG抗体及び/又は抗ウサギIgG抗体を二次抗体として用いた。製造者の指示に従ってECL試薬を用いる化学発光により、ブロットを発光させた。対照標準:1.負荷対照標準:以下:抗アクチン抗体、抗チューブリン抗体又は抗GAPDH抗体の1つを、ゲルの各ウェル中のタンパク質の等しい負荷を示すために負荷対照標準として用いた。抗チューブリン抗体は~51kDaのタンパク質を検出し、抗アクチン抗体は~42kDaのタンパク質を検出し、抗GAPDH抗体は~39kDaのタンパク質を検出する。抗チューブリン抗体又は抗アクチン抗体又は抗GAPDH抗体のいずれかをそれらの利用可能性に応じて用いて最初のブロットを調べた(probed)。最初の実験の後、一貫性のために、抗GAPDH抗体を負荷対照標準として用いた。2.陽性対照標準:AAV2.V2a形質導入されたCOS-7細胞においてhREP-1タンパク質の産生が確定した後、後のウェスタンブロット実験における陽性対照標準としてAAV2.V2a-Cos-7細胞溶解液を用いた。3.陰性対照標準:陰性対照標準として未処理の細胞を用いた。種々の細胞株におけるREP-1タンパク質産生のウェスタンブロット結果の分析を表.5にまとめる。
産生をもたらした。
この研究の目的は、84-31細胞株に基づく研究モデルにおけるREP-1タンパク質のレベルを測定することにより、CHM-含有導入遺伝子カセットの種々のバージョンを含むAAVベクター(血清型2及び8)の形質導入効率を説明する(delineate)ことであった。
1.パイロット実験において、AAV2.hCHM.バージョン1、バージョン2a及びバージョン2bを用いてCOS-7及び84-31細胞を形質導入した。ウェスタンブロットを行い、2つの細胞株における形質導入効率レベルを比較した。
3.4.1 細胞培養
5%CO2が供給される環境中で37℃において、10%胎仔ウシ血清及び1%ペニシリン/ストレプトマイシンを有するダルベッコ変法イーグル培地ダルベッコ変法イーグル培地(DMEM)-高グルコース中で84-31細胞及びCOS-7の両方を培養した。
形質導入の前日(18-24時間前)、84-31及びCOS-7細胞を6-ウェル細胞培養皿のウェル当たり2mlの細胞培地中に3×105(3E5)の密度で播種した。播種された細胞を5%CO2が供給される環境において37℃でインキュベーションした。
84-31細胞及びCOS-7のウェルを、下記に説明されるAAVベクターに3×105のMOIにおいて感染させた(パイロット実験に関して表6、第2組の実験に関して表7を参照されたい)。陰性(形質導入されない)対照標準にはウイルスを加えなかった。要するに、6ウェル細胞培養皿中の各ウェルにおいて最初に組織培地を除去し、ウェル当たり2mlの新しい培地で置き換えた。次いであらかじめ決定された量のAAVベクター(形質導入のために用いられるベクター容積に関し、表2を参照されたい)を(原液から)測定し、各ウェルに直接加えた。5%CO2を用いて37℃において、細胞をAAVウイルスと一緒に回収まで36-48時間インキュベーションした。回収前に、異常の検査のために細胞を顕微鏡下で観察した。実施例4に説明した通りにウェスタンブロット分
析を行った。
この実験において、ベクターなしで(未処理対照標準)、AAV2.hCHM.バージョン1、AAV2.hCHM.バージョン2a又はAav2.hCHM.バージョン2bを用いて84-31及びCOS-7細胞を形質導入した。抗ヒトREP-1抗体を用いるウェスタンブロット分析は、すべてのAAV2(V1、V2a、V2b)形質導入試料において、かつ両方の細胞株においてREP-1タンパク質レベルが~75-80kDaにおいて検出可能であることを示した(データは示されない)。84-31細胞株においてわずかに優れたタンパク質発現が見られた(表8)。抗REP1抗体は、未処理の細胞において無視し得る量のREP-1タンパク質を検出した。GAPDH抗体を用いるブロットの標識は、未処理の細胞を含むすべての細胞溶解液中で~39kDaにおけるバンドを検出した。
DNA不純物の量へのラムダスタッファー配列の効果を評価するために、上記の表2に示される8つのAAVベクターのすべてについて1回のqPCR(定量的ポリメラーゼ連鎖反応)実験を行った。アッセイ標準の作製に線状化AAVプラスミド標準を用いた。正しくパッケージングされたAAVゲノムの定量のためにCMV/CBAプロモーター領域又は逆パッケージングのためにカナマイシン耐性(KanR)コード領域のいずれかの上にプライマー-プローブセットを設計した。標準及びベクター試料を、CMV/CBAプライマー-プローブセットを用いる1つ及びKanRセットを用いる他の2つのセットにおいて実験した。各標準曲線のそれぞれからベクター試料値(mL当たりのウイルスゲノムコピー)を決定した。CMV/CBA含有配列に対して各ベクターロット中のKanR-含有不純物の相対的な量を比較することにより、スタッファー配列の効果を評価した。試薬:
導入遺伝子-含有ウイルスベクター力価:
参照標準:CMV-CBAプロモーター
プライマー:CMV-F:CCC ACT TGG CAG TAC ATC AA
CMV-R:GCC AAG TAF GAA AGT CCC ATA A
FAM-プローブ:/56-FAM/CA TAA TGC C/ZEN/A GGC GGG CCA TTT AC/3IABkFQ/
不純物-含有ウイルスベクター力価:
参照標準:カナマイシン耐性遺伝子
プライマー:
KAN-F:GAT GGT CGG AAG TGG CAT AA
KAN-R:TGC GCC AGA GTT GTT TCT
FAM-プローブ:/56-FAM/CC GTC AGC C/ZEN/A GTT TAG TCT GAC CA/3IABkFQ/
希釈試薬:希釈剤 Q(ヌクレアーゼ非含有水中の0.001%PF-68):無菌水を用いて1%PF-68溶液を1000-倍に希釈。希釈剤 S:希釈剤 Q+2ng/μLサケ精子DNA(Agilent technologies Cat#201190)。
ABI TaqMan TM Universal Master Mix(Applied Biosystems 4304437/4326708)
Quiagen PCR Product Purification Kit(Quiagen 28104)
・ABI QuantStudio 6 Flex System
以下:Dnase緩衝液(10X) 5μL、ヌクレアーゼ非含有H2O 30μL、Dnase I(Invitrogen,18068-015) 5μLを混合することにより、Dnase消化(digest)溶液を調製した。
XhoIを用いてプラスミドp1008(スタッファーなしの低コピー導入遺伝子プラスミド)を消化し、Quiagen PCR精製キットを用いて精製することにより、参照標準DNA(線状化)を調製した。精製された材料をアガロースゲル上で分析して身元を確認し、Nanodropにより定量した。以下の等式(equivalence):1bp=1.096×10-21gを用いてDNAコピー数を原液濃度から決定した。qPCR標準を以下の表に従って調製した:
抽出されたDNA試料を1回のqPCR実験において同じ条件の実験を3回繰り返して(3つのウェル)分析した。実験は参照DNA標準をウェル当たり103~108個のコピーの範囲で含み、同じ条件を実験を3回繰り返した。陰性対照標準としてテンプレートなしの対照標準(no-template-control、NTC)を含んだ。CMV/CBA及びKanRプライマー/プローブセットの両方を用いて各AAVベクター調製物を分析した。同様に、各セットの定量のために、標準もCMV/CBA及びKanRプライマー/プローブセットの両方を用いて分析した。
1サイクル;95℃ 15秒 40サイクル;60℃ 1分 40サイクル
実験性能。ウェル当たり103~108個のDNAコピーにおいて標準を調製し、実験した。この実験のためにアッセイ感度は重要な因子ではないので、アッセイの下限を1000個のコピーに設定した。標準コピー数及び標準のCT(閾サイクル(threshold cycle))値を用いて実験に関する標準曲線を作成した。ABIソフトウェアを用いて標準の線形回帰を行った(データは示されない)。標準曲線適合は、0.998かそれより大きい相関係数(R2値)を有し、信頼性のある適合モデルを示した。標準曲線の傾きは-3.5であった。傾きを用いて増幅反応の効率を算出し、-3.2~-3.6の値は90%~110%の増幅効率を示した。両方の標準反応は92.6~93.8%の高率で行われた(run)。三重のウェルの精度は2~10%の範囲であり、複製産物の間の優れた一致を示した。テンプレートなしの対照標準(NTC)は、アッセイの下限より低い定量不可能な増幅を生じた。
試料値決定:試料値(AAVゲノム及び逆-パッケージングコピー数)を、CT値を用いて各適合標準曲線(CMV/CBA又はKanR)から内挿した。内挿されたDNAコピー数を初期希釈及び/又は消化希釈に関して修正した。試料中の二本鎖DNA標準及び一本鎖DNAの間の差を説明するために補正係数2を追加で適用した。
この研究の目的は、コドン最適化REP-1-コード遺伝子を保有する一系列の次世代AAV2及びAAV8ベクターを用いる遺伝子送達の後の人工多能性細胞株(iPSC)におけるAAV媒介CHM発現の能力を評価することであった。
1.12ウェル細胞培養プレート上で培養されたiPS細胞をAAV2.hCHMバージョン1、バージョン2a;バージョン2b;バージョン3a;バージョン3b(AAV2.V1;V2a;V2b;V3a;V3b)に1×105又は3×105のいずれかのMOIにおいて感染させる。24時間の形質導入の後、1mlのiPS細胞培地を細胞に加えた。36-48時間の形質導入の後、細胞を回収し、溶解し、SDS-PAGE及び続くウェスタンブロット分析のために処理した。すべてのバージョンのコンストラクトを用いて形質導入された細胞においてREP-1タンパク質の産生を評価し、未処理の対照標準と比較した。
3.4.1 細胞培養
CHM被験者からのiPS細胞の培養。要するに、5%CO2及び5%O2が供給される環境中で37℃において、iPS細胞培地中のマウス胚線維芽細胞(MEFs、支持細胞)上でiPS細胞を培養した。
細胞を播種する前日、12-ウェル皿に、参照文献NCP.003(NCP.003:Culturing of iPS cells from CHM patient and controls)に説明されているMatrigelをコーティングした。それぞれAAV2又はAAV8ウイルスベクターを用いてiPS細胞を形質導入する前に、MEFs上で培養されている細胞をMEFsなしのMatrigel上に播種した(支持細胞なしの培養)。12-ウェル細胞培養皿の各ウェル中の1mlのiPS細胞培地に4.5×105(4.5+E5)~6×105個の密度で細胞を播種した。播種された細胞を5%CO2,5%O2が供給される環境中で37℃においてインキュベーションした。
iPS細胞をウイルスベクターに感染させるために、細胞を約50-60%コンフルエントまで生育させた。(これは支持細胞なしの条件で2-4日かかり得る)。50-60%コンフルエントに達したら、12-ウェル中の1つのウェルを分離し、細胞カウントを行ってウェル当たりの細胞数の合計を決定した。次いでiPS細胞のウェルを下記に挙げるAAVベクターに、あらかじめ決定されたMOI(表18及び19を参照されたい)で感染させた。形質導入の前に、古いiPS細胞培地をプレートから除去し、各ウェルに新しい1mlのiPS細胞培地を加えた。原液からあらかじめ決定された容積のウイルスを直接各ウェルに加えた。感染した細胞数の合計、MOI及び感染のために用いられたウイルスの容積についての情報に関し、表18及び表19を参照されたい。次いで5%CO2,5%O2が供給される環境中で37℃において、細胞を18-48時間インキュベーションした。18-24時間の形質導入の後、異常又は細胞死に関して顕微鏡下で細胞を観察した。このタイムポイントで、感染及び非感染細胞を含む各ウェルにさらに1mlの新しいiPS細胞培地を加え、5%CO2,5%O2が供給される環境中で37℃においてさらに追加の18-24時間インキュベーションした。回収の前に、細胞死又は異常な外観を評価するために細胞を顕微鏡下で観察した。
5.1 JB588 iPS細胞株におけるAAV2-hCHM V1、V2a、V2b、V3a、V3bの発現:モノクローナルヒトREP-1特異的抗体は、形質導入されたJB 588 iPS細胞において1つの~75-80kDa単一hREP-1タンパク質を検出した(データは示されない)。未処理対照標準の場合、バンドは観察されず、疾患の存在を確認した(データは示されない)。3×105のMOIにおけるREP-1タンパク質バンドの強度はすべてのベクターにおいて1×105のMOIと比較してより強いことが観察された。iPS細胞へのhCHM遺伝子の組換えAAV2.hCHMウイルス媒介送達は、REP-1タンパク質の用量-依存性産生を生じた。GAPDH抗体を用いるブロットの探査は、すべての細胞溶解液において等しい濃度のバンドを示した。GAPDHは~39kDaにおけるタンパク質を検出した。REP-1及びGAPDH抗体の両方は予測される分子量の特異的なバンドのみを検出した。ブロットにおいて非特異的なバンドは観察されなかった。
H抗体の両方は予測されるサイズ分子量における特異的なタンパク質バンドのみを検出した。ブロットにおいて検出可能な非特異的タンパク質バンドは観察されなかった。
本報告において提示される予備的な結果は以下の観察を明らかにした:ウェスタンブロット分析は3つの被験者-由来iPSCs(JB588、JB500、JB527)のそれぞれにおけるCHM(REP-1タンパク質の欠如)の存在を確認した。試験管内発現研究は、AAV2.hCHM.バージョン2a、2b、3a、3b及びAAV2.hCHMバージョン1(現在の臨床試験候補)へのCHM被験者からのiPS細胞の感染が、すべての調べられたMOIsにおいてREP-1タンパク質の産生を誘導することを示した。AAV8.hCHM.バージョン2a及びAAV8.hCHMバージョン1への1×106のMOIにおけるiPS細胞の感染は、3つのCHM iPS細胞株のすべてにおいてREP1タンパク質の産生をもたらした。REP1産生のレベルは、AAV8.hCHM.V1に感染したiPSCsよりAAV8.hCHM.V2aに感染したものにおいてより高かった。
複数の網膜疾患のための遺伝子療法は、適切な標的細胞の有効な形質導入に依存しており、コロイデレミアの場合、適切な標的細胞は網膜色素上皮(RPE)及び光受容体細胞である。この研究報告は、天然CHM配列に基づくコンストラクト(バージョン1)及びAAV8主鎖中にパッケージングされた4つの次世代導入遺伝子カセットにより誘導される野生型マウスにおける生体内発現の比較に焦点を当てる。ここで我々は光受容体細胞への遺伝子転移を向上させる目的のためにAAV8血清型を評価した。
プラスミド及びベクターは実施例4において説明された通りであった。マウス(動物):REP-1タンパク質の産生により評価されるCHMの生体内発現を調べるために、野生型CD1マウスを用いた。CD1マウス株は非近交系スイスマウス株であり、そのコロニーを我々は学内で維持する。研究の詳細はCAROT研究プロトコルPCPR02.01の下に説明されている。
3.3.1 動物飼育:~20-30グラムの体重の雄及び雌の両方のマウス(~3-4月令)に説明される試験物質を注入した。動物をペンシルバニア大学のジョンモルガン大学実験室動物資源(the University of Pennsylvania’s John Morgan University Laboratory Animal Resources)(ULAR)施設に、ペンシルバニア大学のULAR規制に従って収容した。マウスを12-時間明/12-時間暗サイクルで保持した。食物及び水は随意に与えられた。すべての動物は耳の標識番号で同定された。
リン酸塩-緩衝食塩水を用いて試験物質を標的濃度に希釈する。合計で60μlのマスターミックスを調製した。
試験物質の網膜下注入の前に、注入ログを以下の情報と一緒に保持した:
・ゲージ番号/マウス番号
・研究の同定
・株
・生年月日
・注入日
・研究者/注入者の名前
・注入される眼(左又は右)
・注入される材料(ベクター/血清型)
・用量及び容積
・投与経路(ROA)
動物屠殺(Animal Sacrifice):a.動物に試験物質を注入した後、すべての動物を注入後関連異常に関して48時間観察した。B.注入から21-35日後、眼底検査法を用いて動物を眼の異常に関して観察した。C.注入から90-12-日後、動物を屠殺し、SDS-PAGE及びその後のウェスタンブロット分析による外来性REP-1タンパク質の産生の評価のために、眼組織を回収した。
要するに:1.組織細胞溶解液の調製
a.2種類の用量の次世代AAV8.CHM及びAAV8.V1が注入された動物の眼組織を、非注入対照標準動物組織と共に、動物を屠殺することにより注入から21-35日後に集めた。B.次いでプロテアーゼ阻害剤を有するRIPA緩衝液を用いて組織を氷上で溶解した。
c.13,000rpmにおける10分間の遠心により組織細胞溶解液を清澄化した。
a.ThermoFisher Micro BCATM Protein Assay Kitを用い、製造者の指示に従って細胞溶解液のタンパク質定量を行った。B.562nmにおけるOD読み取り値を得ることにより、タンパク質濃度を決定した。C.CHMの生体内発現を評価するために、4-12% Bis-Trisゲル上に20-40μgの測定されたタンパク質を負荷した。
タンパク質ゲルをニトロセルロース膜上に転移させ、ミルク中でブロッキングし、一次抗体と一緒にインキュベーションした。抗ヒトREP-1 2F1抗体(2F1,1:1000希釈)及び/又は抗GAPDH抗体(1:1000希釈)を一次抗体として用いた。ブロットの洗浄後、1:5000の濃度におけるHRP結合抗マウスIgG抗体及び/又は抗ウサギIgG抗体を二次抗体として用いた。製造者の指示に従ってECL試薬を用いる化学発光により、ブロットを発光させた。
a)負荷対照標準:ゲルの各ウェル中のタンパク質の等しい負荷を示すために、抗GA
PDH抗体を負荷対照標準として用いた。抗GAPDH抗体は~39kDaのタンパク質を検出する。B)陽性対照標準:AAV2.V2aが形質導入されたCOS-7細胞溶解液を陽性対照標準として用いた。C)陰性対照標準:注入されない動物の眼組織を陰性対照標準として用いた。
Image Jソフトウェアを用いる分析によるウェスタンブロット分析の定量。要するに、この報告に提示される濃度測定的評価を対応する試料のGAPDHタンパク質の内在性発現のレベルに最初に正規化する。次いで発現レベルを非注入対照標準の平均REP-1発現レベルに再び正規化する。
1.表22及び23において、第2列はREP-1タンパク質の生の値を示し、第3列はGAPDHタンパク質の生の値を示す。
2.各試料のGAPDH値を最初にAAV8.V1の動物-1のGAPDH値に正規化し、それを表22において第4列に示す。
3.各試料の値をAAV8.V1の動物-2のGAPDH値にも正規化し、それを表22において第5列に示す。
4.次いでREP-1の値(第2列)を動物1に正規化されたGAPDH(第4列)又は前に動物2に正規化されたGAPDH(第5列)のいずれかに正規化する。これらをそれぞれ第6列及び第7列に示す。
5.正規化されたREP-1の値を次いで相対値(fold change)に転換する。
6.それぞれのREP-1の値をAAV8.V1が注入されたグループの動物1又は動物2のいずれかにおけるREP-1の発現に正規化し、相対値として表す(第8及び9列)。
7.第10列はREP-1タンパク質発現における平均相対値を示す。
天然CHM AAV8.V1対コドン最適化CHMベクター:AAV8.V2a、V2b、V3a及びV3bを用いるCHM発現の比較:野生型CD1マウスに2種類の用量の各AAV8ベクター:眼当たり5×109個のベクターゲノムの高用量及び眼当たり5×108個のベクターゲノムの低用量を注入した。以下の結果は、高用量及び低用量のAAV8.V1、AAV8.V2a及びAAV8.V3aを用いる注入の後のREP1タンパク質のレベルを説明している。
たタンパク質マーカーを用いる。ImageJソフトウェアを用いるブロットの濃度測定的評価(発現レベルの定量)は、次世代AAV8.高及び低用量コンストラクト(V2a又はV3a)の1つが注入された動物においてREP-1の産生が増加することを示した。(値に関して表22を参照されたい。)
5×108個の用量で次世代AAV8.V2a、V3a及びAAV8.バージョン1が注入された動物の眼組織のヒト抗REP-1抗体、ウェスタンブロット分析は、注入されたマウスの組織において~75-80kDa hREP-1タンパク質バンドを検出した。両方の注入されない対照標準マウスの眼組織細胞溶解液において、REP-1の弱い(最小)バンドが観察された。バージョン1を用いて形質導入された細胞溶解液と比較して、次世代ベクターを用いて形質導入された組織細胞溶解液において強度が増したバンドが観察された。抗GAPDH抗体は、すべての組織溶解液において、~39kDaにおける等しい強度のタンパク質バンドを検出した。このデータは、AAV8を介する次世代V2
a CHMの送達がAAV8.V3a又はAAV8.V1の注入後に産生されるレベルと比較して確固としたレベルのREP-1タンパク質を生ずることを示す。
進行中の本研究及びqPCR力価分析によるAAVベクター作製へのラムダスタッファーの効果の評価を同時に行った。我々は研究プロトコルPCPR.02に説明される生体内発現研究のためのすべての動物注入を行い、すべての試料を回収した。(上記の)ラムダスタッファー要素についてのqPCR研究が完結した後、我々はAAV8.2b及びAAV8.3bのようなスタッファーのないAAVベクターの発現を調べるだけのためにウェスタンブロット実験を行い、さらなる分析(バージョン1との比較のような)からそれらを除外することを決定した。
我々はAAV8.3bが注入されたCD1マウス(グループ当たり2匹のマウス)の眼組織について、抗REP-1抗体を用いるウェスタンブロット分析を行い、それは低用量で注入された1つの眼において及び高用量のAAV8.3bを注入された両眼において~75-80kDaのタンパク質の存在を明らかにした。未注入マウスの眼組織に、REP-1発現は検出されなかった(図12B)。産生されるREP-1のレベルはAAV8.3bが注入された動物において用量依存性であった。高用量のAAV8.3b(5×109個のベクターゲノム)を用いる注入は、低用量が注入された眼(5×108個のベクターゲノム)と比較してより多量のREP-1を誘導した。抗GAPDH抗体は、すべての注入された及び注入されない動物の眼組織細胞溶解液において~39kDaのタンパク質を検出した。
1)次世代ベクターAAV8.バージョン2a、2b、3a及び3bは眼組織を有効に形質導入することができる。2)導入遺伝子(コドン最適化CHM)の発現は、次世代ベクターのすべてに関して検出可能であった。3)導入遺伝子(コドン最適化CHM)の発現は、用量依存性である。4)AAV8.バージョン2a及びAAV8.バージョン2bは、CD-1マウスの眼組織においてAAV8.バージョン1と比較して増加したREP-1タンパク質の産生を誘導した。5)同じ用量を注入された眼の間で導入遺伝子タンパク質の産生の正確なレベルに変動があり、外科手術的送達法におけるばらつきを反映している。しかしながら、レベルの差は低(5×108個)及び高(5×109個)用量の間で大きい。6)AAV8.CHM.V2a及びAAV8.V3aは、マウスにおいて網膜下に高用量(5×109個のベクターゲノム)のベクターを生体内投与した後、AAV8.V1よりずっと高いレベルのREP-1タンパク質産生を生ずる。
Claims (28)
- 配列番号1のcDNA配列を含む、発現カセット。
- AAVキャプシドと、AAV逆位末端反復(ITR)配列を含む核酸配列と、ヒトRabエスコートタンパク質-1(REP-1)をコードする配列番号1の核酸配列と、宿主細胞における前記REP-1の発現を方向付ける発現調節配列とを含む、アデノ随伴ウイルス(AAV)ベクター。
- 前記発現調節配列はプロモーターを含む、請求項2に記載のAAVベクター。
- 前記プロモーターはロドプシンプロモーターである、請求項3に記載のAAVベクター。
- 前記プロモーターはロドプシンキナーゼプロモーターである、請求項3に記載のAAVベクター。
- 前記プロモーターは眼細胞特異的プロモーターである、請求項3に記載のAAVベクター。
- 前記プロモーターは、ヒトEF1αプロモーター、代謝型グルタミン酸受容体6(mGluR6)プロモーター、ロドプシンプロモーター、錐体オプシンプロモーター及び転写因子プロモーターから選ばれる、請求項3に記載のAAVベクター。
- 前記プロモーターは、誘導可能なプロモーター、構成的プロモーター又は組織特異的プロモーターである、請求項3に記載のAAVベクター。
- 前記プロモーターは、ラパマイシンまたはラパログ(rapalog)プロモーター、エクジソンプロモーター、エストロゲン-反応性プロモーター及びテトラサイクリン-反応性プロモーターから選ばれる誘導可能なプロモーターであるか、又はヘテロダイマーリプレッサースイッチである、請求項8に記載のAAVベクター。
- イントロン、コザック配列、ポリA及び転写後調節要素の1つ以上をさらに含む、請求項4~9のいずれかに記載のAAVベクター。
- 前記AAVキャプシドは、AAV2、AAV5、AAV8、AAV9、AAV8bpまたはAAV7m8キャプシドである、請求項4~10のいずれかに記載のAAVベクター。
- 前記ITR配列は前記AAVキャプシドを供給するものと異なるAAVに由来する、請求項5~11のいずれかに記載のAAVベクター。
- 前記ITR配列はAAV2に由来する、請求項5~12のいずれかに記載のAAVベクター。
- AAV8キャプシド及び組換えAAV(rAAV)ゲノムを含み、ここで該rAAVゲノムは、REP-1をコードする配列番号1の核酸配列と、逆位末端反復配列と、宿主細胞における前記REP-1の発現を方向付ける発現調節配列とを含む、アデノ随伴ウイルス(AAV)ベクター。
- 製薬学的に許容され得る担体及び少なくとも1つの請求項2~14のいずれか1つに記載のAAVベクターを含む、製薬学的組成物。
- AAVベクターを作製するためのプラスミドであって、該プラスミドは配列番号1の核酸配列、配列番号25、配列番号26、配列番号27又は配列番号28を含む、プラスミド。
- 配列番号25のヌクレオチド1~4233、配列番号26のヌクレオチド1~4233、配列番号27のヌクレオチド1~4233又は配列番号28のヌクレオチド1~4233を含むベクターゲノムを含む、AAVベクター。
- 5’ITR、CMVエンハンサー、ニワトリベータ-アクチンプロモーター、CBAエキソン1及びイントロン、コザック配列、配列番号1の核酸配列、bGHポリA1ならびに3’ITRを含むベクターゲノムを含む、AAVベクター。
- 請求項2~14、17又は18のいずれかのAAVベクターを含む、コロイデレミアの処置方法における使用のための組成物。
- 前記組成物を網膜下に投与する、請求項19に記載の組成物。
- 前記組成物を硝子体内、静脈内又は脈絡膜に投与する、請求項19に記載の組成物。
- 前記組成物は哺乳類に投与される、請求項19に記載の組成物。
- 前記組成物はヒトに投与される、請求項22に記載の組成物。
- 前記組成物を別の治療との組み合わせにおいて投与する、請求項19~23のいずれかに記載の組成物。
- 前記組成物を約109個~約1013個のベクターゲノム(VG)の用量で投与する、請求項19~24のいずれかに記載の組成物。
- 前記組成物を約100μL~約500μLの容積で投与する、請求項19~25のいずれかに記載の組成物。
- 前記組成物を2回以上投与する、請求項19~26のいずれかに記載の組成物。
- コロイデレミアの処置のための薬剤の製造における、請求項2~14、17又は18のいずれかのAAVベクターの使用。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2022063749A JP2022088656A (ja) | 2015-12-14 | 2022-04-07 | 眼疾患のための遺伝子療法 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201562266789P | 2015-12-14 | 2015-12-14 | |
| US62/266,789 | 2015-12-14 | ||
| PCT/US2016/066402 WO2017106202A2 (en) | 2015-12-14 | 2016-12-13 | Gene therapy for ocular disorders |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022063749A Division JP2022088656A (ja) | 2015-12-14 | 2022-04-07 | 眼疾患のための遺伝子療法 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2019502378A JP2019502378A (ja) | 2019-01-31 |
| JP2019502378A5 JP2019502378A5 (ja) | 2020-01-30 |
| JP7057281B2 true JP7057281B2 (ja) | 2022-04-19 |
Family
ID=58455636
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018531202A Active JP7057281B2 (ja) | 2015-12-14 | 2016-12-13 | 眼疾患のための遺伝子療法 |
| JP2022063749A Pending JP2022088656A (ja) | 2015-12-14 | 2022-04-07 | 眼疾患のための遺伝子療法 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022063749A Pending JP2022088656A (ja) | 2015-12-14 | 2022-04-07 | 眼疾患のための遺伝子療法 |
Country Status (12)
| Country | Link |
|---|---|
| US (2) | US11090392B2 (ja) |
| EP (2) | EP3795180B1 (ja) |
| JP (2) | JP7057281B2 (ja) |
| KR (1) | KR20180099719A (ja) |
| CN (1) | CN109069668B (ja) |
| AU (1) | AU2016370487C1 (ja) |
| BR (1) | BR112018011838A2 (ja) |
| CA (1) | CA3008264A1 (ja) |
| ES (1) | ES2826384T3 (ja) |
| MX (2) | MX2018007230A (ja) |
| RU (1) | RU2762747C2 (ja) |
| WO (1) | WO2017106202A2 (ja) |
Families Citing this family (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP7057281B2 (ja) * | 2015-12-14 | 2022-04-19 | ザ・トラステイーズ・オブ・ザ・ユニバーシテイ・オブ・ペンシルベニア | 眼疾患のための遺伝子療法 |
| SG11201808314QA (en) * | 2016-04-08 | 2018-10-30 | Krystal Biotech Inc | Compositions and methods for the treatment of wounds, disorders, and diseases of the skin |
| CN109952114A (zh) * | 2016-07-26 | 2019-06-28 | 康奈尔大学 | 用于治疗醛脱氢酶缺乏的基因疗法 |
| EP3638316A4 (en) | 2017-06-14 | 2021-03-24 | The Trustees Of The University Of Pennsylvania | GENE THERAPY FOR EYE DISEASES |
| JP7602999B2 (ja) | 2018-04-27 | 2024-12-19 | クリスタル バイオテック インコーポレイテッド | 審美的用途のための美容用タンパク質をコードする組換え核酸 |
| KR20210124277A (ko) | 2019-02-08 | 2021-10-14 | 크리스탈 바이오테크, 인크. | Cftr 폴리펩타이드를 전달하기 위한 조성물 및 방법 |
| EP3934699A4 (en) | 2019-03-04 | 2022-12-21 | The Trustees of The University of Pennsylvania | NEUROPROTECTIVE GENE THERAPY TARGETING THE AKT PATHWAY |
| CN110889859A (zh) * | 2019-11-11 | 2020-03-17 | 珠海上工医信科技有限公司 | 一种用于眼底图像血管分割的u型网络 |
| EP4150051A4 (en) * | 2020-04-27 | 2025-05-21 | The Trustees of The University of Pennsylvania | COMPOSITIONS FOR THE TREATMENT OF CDKL5 DEFICIENCY DISORDER (CDD) |
| CN116806158A (zh) * | 2020-09-02 | 2023-09-26 | 4D分子治疗有限公司 | 密码子优化的rep1基因及其用途 |
| EP4284335A1 (en) | 2021-02-01 | 2023-12-06 | RegenxBio Inc. | Gene therapy for neuronal ceroid lipofuscinoses |
| TW202302856A (zh) | 2021-02-26 | 2023-01-16 | 美商邏輯生物療法公司 | 重組aav載體之製造及使用 |
| CA3213789A1 (en) | 2021-04-02 | 2022-10-06 | Krystal Biotech, Inc. | Viral vectors for cancer therapy |
| WO2023014892A1 (en) * | 2021-08-04 | 2023-02-09 | Alpine Biotherapeutics Corporation | Sustainable ocular cell-mediated intraocular delivery of cellular therapeutics for treatment of ocular diseases or disorders |
Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2005500008A (ja) | 2001-01-19 | 2005-01-06 | インサイト・ゲノミックス・インコーポレイテッド | 受容体および膜結合タンパク質 |
| WO2010005533A2 (en) | 2008-06-30 | 2010-01-14 | The Johns Hopkins University | Compositions and methods for the treatment of ocular oxidative stress and retinitis pigmentosa |
| US20110305772A1 (en) | 2009-02-26 | 2011-12-15 | The Johns Hopkins University | Compositions and methods for ex vivo hepatic nucleic acid delivery |
| WO2013086515A1 (en) | 2011-12-09 | 2013-06-13 | The Johns Hopkins University | Compositions and methods for the prevention or treatment of diabetic complications |
| JP2014512171A (ja) | 2011-02-22 | 2014-05-22 | アイシス イノベーション リミテッド | コロイデレミアの遺伝子治療に使用するためのaavベクター |
| WO2014170480A1 (en) | 2013-04-18 | 2014-10-23 | Fondazione Telethon | Effective delivery of large genes by dual aav vectors |
| WO2014186160A1 (en) | 2013-05-16 | 2014-11-20 | Applied Genetic Technologies Corporation | Promoters, expression cassettes, vectors, kits, and methods for the threatment of achromatopsia and other diseases |
Family Cites Families (39)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5139941A (en) | 1985-10-31 | 1992-08-18 | University Of Florida Research Foundation, Inc. | AAV transduction vectors |
| US5436146A (en) | 1989-09-07 | 1995-07-25 | The Trustees Of Princeton University | Helper-free stocks of recombinant adeno-associated virus vectors |
| US6268213B1 (en) | 1992-06-03 | 2001-07-31 | Richard Jude Samulski | Adeno-associated virus vector and cis-acting regulatory and promoter elements capable of expressing at least one gene and method of using same for gene therapy |
| US5478745A (en) | 1992-12-04 | 1995-12-26 | University Of Pittsburgh | Recombinant viral vector system |
| US5869305A (en) | 1992-12-04 | 1999-02-09 | The University Of Pittsburgh | Recombinant viral vector system |
| US6204059B1 (en) | 1994-06-30 | 2001-03-20 | University Of Pittsburgh | AAV capsid vehicles for molecular transfer |
| US6093570A (en) | 1995-06-07 | 2000-07-25 | The University Of North Carolina At Chapel Hill | Helper virus-free AAV production |
| US5741683A (en) | 1995-06-07 | 1998-04-21 | The Research Foundation Of State University Of New York | In vitro packaging of adeno-associated virus DNA |
| WO1998046728A1 (en) | 1997-04-14 | 1998-10-22 | Cell Genesys, Inc. | Methods for increasing the efficiency of recombinant aav product |
| WO1999061643A1 (en) | 1998-05-27 | 1999-12-02 | University Of Florida | Method of preparing recombinant adeno-associated virus compositions by using an iodixananol gradient |
| DE69941905D1 (de) | 1998-11-10 | 2010-02-25 | Univ North Carolina | Virusvektoren und verfahren für ihre herstellung und verabreichung. |
| ES2308989T3 (es) | 1999-08-09 | 2008-12-16 | Targeted Genetics Corporation | Aumento de la expresion de una secuencia nucleotidica heterologa a partir de vectores viricos recombinantes que contienen una secuencia que forman pares de bases intracatenarios. |
| ES2327609T3 (es) | 2000-06-01 | 2009-11-02 | University Of North Carolina At Chapel Hill | Procedimientos y compuestos para controlar la liberacion de vectores de parvovirus reconbinantes. |
| EP1381276A4 (en) | 2001-04-13 | 2005-02-02 | Univ Pennsylvania | METHOD FOR TREATMENT OR DEVELOPMENT SLUDGE DEGRADATION |
| JP4677187B2 (ja) | 2001-11-13 | 2011-04-27 | ザ・トラステイーズ・オブ・ザ・ユニバーシテイ・オブ・ペンシルベニア | 新規なアデノ随伴ウイルス(aav)7配列、それを含むベクターおよびそれらの使用 |
| WO2003052051A2 (en) | 2001-12-17 | 2003-06-26 | The Trustees Of The University Of Pennsylvania | Adeno-associated virus (aav) serotype 8 sequences |
| US20070015238A1 (en) | 2002-06-05 | 2007-01-18 | Snyder Richard O | Production of pseudotyped recombinant AAV virions |
| EP1486567A1 (en) | 2003-06-11 | 2004-12-15 | Deutsches Krebsforschungszentrum Stiftung des öffentlichen Rechts | Improved adeno-associated virus (AAV) vector for gene therapy |
| NZ545628A (en) | 2003-09-30 | 2009-04-30 | Univ Pennsylvania | Adeno-associated virus (AAV) clades, sequences, vectors containing same, and uses therefor |
| EP2359866B1 (en) | 2005-04-07 | 2013-07-17 | The Trustees of The University of Pennsylvania | Modified AAV rh48 capsids, compositions containing same and uses thereof |
| EP1777906A1 (en) | 2005-06-09 | 2007-04-25 | Matsushita Electric Industrial Co., Ltd. | Amplitude error compensating apparatus and orthogonality error compensating apparatus |
| WO2007120542A2 (en) | 2006-03-30 | 2007-10-25 | The Board Of Trustees Of The Leland Stanford Junior University | Aav capsid library and aav capsid proteins |
| RU2444977C2 (ru) | 2009-08-03 | 2012-03-20 | Федеральное государственное учреждение "МОСКОВСКИЙ НАУЧНО-ИССЛЕДОВАТЕЛЬСКИЙ ИНСТИТУТ ГЛАЗНЫХ БОЛЕЗНЕЙ ИМЕНИ ГЕЛЬМГОЛЬЦА ФЕДЕРАЛЬНОГО АГЕНТСТВА ПО ВЫСОКОТЕХНОЛОГИЧНОЙ МЕДИЦИНСКОЙ ПОМОЩИ" | Способ диагностики ахроматопсии |
| WO2011034947A2 (en) * | 2009-09-15 | 2011-03-24 | University Of Washington | Reagents and methods for modulating cone photoreceptor activity |
| SG10201502270TA (en) | 2010-03-29 | 2015-05-28 | Univ Pennsylvania | Pharmacologically induced transgene ablation system |
| US9315825B2 (en) | 2010-03-29 | 2016-04-19 | The Trustees Of The University Of Pennsylvania | Pharmacologically induced transgene ablation system |
| CA2823890C (en) * | 2011-01-07 | 2020-10-06 | Applied Genetic Technologies Corporation | Promoters, expression cassettes, vectors, kits, and methods for the treatment of achromatopsia and other diseases |
| WO2012158757A1 (en) | 2011-05-16 | 2012-11-22 | The Trustees Of The University Of Pennsylvania | Proviral plasmids for production of recombinant adeno-associated virus |
| FR2977562B1 (fr) | 2011-07-06 | 2016-12-23 | Gaztransport Et Technigaz | Cuve etanche et thermiquement isolante integree dans une structure porteuse |
| WO2013063601A1 (en) | 2011-10-28 | 2013-05-02 | University Of Florida Research Foundation, Inc. | Chimeric promoter for cone photoreceptor targeted gene therapy |
| HK1206779A1 (en) | 2012-04-02 | 2016-01-15 | Modernatx, Inc. | Modified polynucleotides for the production of nuclear proteins |
| US9770491B2 (en) | 2012-07-11 | 2017-09-26 | The Trustees Of The University Of Pennsylvania | AAV-mediated gene therapy for RPGR X-linked retinal degeneration |
| EP2883981A4 (en) | 2012-08-08 | 2016-05-11 | Nihon Parkerizing | METAL SURFACE TREATMENT LIQUID, SURFACE TREATMENT METHOD FOR A METAL BASE, AND METAL BASE OBTAINED BY THE SURFACE TREATMENT PROCESS FOR METAL BASIS |
| WO2014124282A1 (en) | 2013-02-08 | 2014-08-14 | The Trustees Of The University Of Pennsylvania | Enhanced aav-mediated gene transfer for retinal therapies |
| GB201322798D0 (en) | 2013-12-20 | 2014-02-05 | Oxford Biomedica Ltd | Production system |
| CN106414474B (zh) | 2014-03-17 | 2021-01-15 | 阿德夫拉姆生物技术股份有限公司 | 用于视锥细胞中增强的基因表达的组合物和方法 |
| AU2015247777B2 (en) * | 2014-04-15 | 2019-03-21 | Beacon Therapeutics Limited | Codon optimized nucleic acid encoding a retinitis pigmentosa GTPase regulator (RPGR) |
| US20160206704A1 (en) * | 2015-01-16 | 2016-07-21 | Isis Innovation Limited | Method |
| JP7057281B2 (ja) * | 2015-12-14 | 2022-04-19 | ザ・トラステイーズ・オブ・ザ・ユニバーシテイ・オブ・ペンシルベニア | 眼疾患のための遺伝子療法 |
-
2016
- 2016-12-13 JP JP2018531202A patent/JP7057281B2/ja active Active
- 2016-12-13 CA CA3008264A patent/CA3008264A1/en active Pending
- 2016-12-13 BR BR112018011838-9A patent/BR112018011838A2/pt active Search and Examination
- 2016-12-13 MX MX2018007230A patent/MX2018007230A/es unknown
- 2016-12-13 CN CN201680081801.2A patent/CN109069668B/zh active Active
- 2016-12-13 EP EP20183330.8A patent/EP3795180B1/en active Active
- 2016-12-13 KR KR1020187019811A patent/KR20180099719A/ko not_active Ceased
- 2016-12-13 WO PCT/US2016/066402 patent/WO2017106202A2/en not_active Ceased
- 2016-12-13 ES ES16852859T patent/ES2826384T3/es active Active
- 2016-12-13 US US16/061,530 patent/US11090392B2/en active Active
- 2016-12-13 AU AU2016370487A patent/AU2016370487C1/en active Active
- 2016-12-13 RU RU2018125468A patent/RU2762747C2/ru active
- 2016-12-13 EP EP16852859.4A patent/EP3389724B1/en active Active
-
2018
- 2018-06-13 MX MX2022010959A patent/MX2022010959A/es unknown
-
2021
- 2021-07-07 US US17/369,525 patent/US12403204B2/en active Active
-
2022
- 2022-04-07 JP JP2022063749A patent/JP2022088656A/ja active Pending
Patent Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2005500008A (ja) | 2001-01-19 | 2005-01-06 | インサイト・ゲノミックス・インコーポレイテッド | 受容体および膜結合タンパク質 |
| WO2010005533A2 (en) | 2008-06-30 | 2010-01-14 | The Johns Hopkins University | Compositions and methods for the treatment of ocular oxidative stress and retinitis pigmentosa |
| US20110305772A1 (en) | 2009-02-26 | 2011-12-15 | The Johns Hopkins University | Compositions and methods for ex vivo hepatic nucleic acid delivery |
| JP2014512171A (ja) | 2011-02-22 | 2014-05-22 | アイシス イノベーション リミテッド | コロイデレミアの遺伝子治療に使用するためのaavベクター |
| WO2013086515A1 (en) | 2011-12-09 | 2013-06-13 | The Johns Hopkins University | Compositions and methods for the prevention or treatment of diabetic complications |
| WO2014170480A1 (en) | 2013-04-18 | 2014-10-23 | Fondazione Telethon | Effective delivery of large genes by dual aav vectors |
| WO2014186160A1 (en) | 2013-05-16 | 2014-11-20 | Applied Genetic Technologies Corporation | Promoters, expression cassettes, vectors, kits, and methods for the threatment of achromatopsia and other diseases |
Non-Patent Citations (1)
| Title |
|---|
| Human Molecular Genetics,2011年,Vol. 20, No. 4,p.681-693 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP3795180B1 (en) | 2025-11-05 |
| JP2022088656A (ja) | 2022-06-14 |
| US12403204B2 (en) | 2025-09-02 |
| US20210330816A1 (en) | 2021-10-28 |
| CN109069668A (zh) | 2018-12-21 |
| KR20180099719A (ko) | 2018-09-05 |
| ES2826384T3 (es) | 2021-05-18 |
| HK1258518A1 (zh) | 2019-11-15 |
| AU2016370487C1 (en) | 2022-03-03 |
| JP2019502378A (ja) | 2019-01-31 |
| RU2018125468A3 (ja) | 2020-10-22 |
| WO2017106202A3 (en) | 2017-08-31 |
| AU2016370487B2 (en) | 2021-08-05 |
| US20200061209A1 (en) | 2020-02-27 |
| CA3008264A1 (en) | 2017-06-22 |
| EP3389724B1 (en) | 2020-07-01 |
| RU2762747C2 (ru) | 2021-12-22 |
| RU2018125468A (ru) | 2020-01-16 |
| WO2017106202A2 (en) | 2017-06-22 |
| MX2022010959A (es) | 2022-10-07 |
| MX2018007230A (es) | 2018-11-09 |
| BR112018011838A2 (pt) | 2018-12-04 |
| US11090392B2 (en) | 2021-08-17 |
| CN109069668B (zh) | 2023-04-18 |
| AU2016370487A1 (en) | 2018-07-05 |
| EP3795180A1 (en) | 2021-03-24 |
| EP3389724A2 (en) | 2018-10-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7057281B2 (ja) | 眼疾患のための遺伝子療法 | |
| JP7766393B2 (ja) | 眼疾患のための遺伝子療法 | |
| JP7101656B2 (ja) | Rdh12が関与する疾患及び疾病を治療する方法及び組成物 | |
| JP7287611B2 (ja) | 改良型アデノ随伴ウイルスベクター | |
| JP2022524140A (ja) | 遺伝子置換による希少な眼疾患のための改善された治療方法 | |
| JP7637060B2 (ja) | Akt経路を標的とする神経保護遺伝子療法 | |
| US20240307559A1 (en) | Kcnv2 gene therapy | |
| HK40049894A (en) | Gene therapy for ocular disorders | |
| CN117980489A (zh) | Retgc基因疗法 | |
| WO2025247393A1 (zh) | 用于治疗Prom1相关视网膜疾病的新型治疗药物 | |
| HK40066183A (zh) | 靶向akt通路的神经保护性基因疗法 | |
| HK40066183B (zh) | 靶向akt通路的神经保护性基因疗法 | |
| HK40013460A (en) | Methods and compositions for treatment of disorders and diseases involving rdh12 | |
| HK40013460B (zh) | 用於治疗涉及rdh12的病症和疾病的方法和组合物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A524 | Written submission of copy of amendment under article 19 pct |
Free format text: JAPANESE INTERMEDIATE CODE: A524 Effective date: 20191209 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20191209 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20201202 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210302 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20210623 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20210913 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20211119 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20220309 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20220407 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7057281 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |