JP6817608B2 - A method for obtaining an index for testing the onset or risk of developing bone marrow tumor in humans, a method for obtaining an index for predicting the presence or future occurrence of a somatic mutation of the DDX41 gene in humans, and for these tests or predictions. kit - Google Patents
A method for obtaining an index for testing the onset or risk of developing bone marrow tumor in humans, a method for obtaining an index for predicting the presence or future occurrence of a somatic mutation of the DDX41 gene in humans, and for these tests or predictions. kit Download PDFInfo
- Publication number
- JP6817608B2 JP6817608B2 JP2015239547A JP2015239547A JP6817608B2 JP 6817608 B2 JP6817608 B2 JP 6817608B2 JP 2015239547 A JP2015239547 A JP 2015239547A JP 2015239547 A JP2015239547 A JP 2015239547A JP 6817608 B2 JP6817608 B2 JP 6817608B2
- Authority
- JP
- Japan
- Prior art keywords
- mutation
- ddx41
- gene
- amino acid
- seq
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Landscapes
- Investigating Or Analysing Biological Materials (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
Description
本発明は、ヒトにおける骨髄異形成症候群(MDS)、急性骨髄性白血病(AML)等の骨髄腫瘍の発症又は発症リスクを検査する方法、検査のための指標の取得方法、ヒトにおけるDDX41遺伝子の体細胞変異の存在又は将来的な発生を予測する方法、予測のための指標の取得方法並びに、これらの方法のためのキットに関する。 The present invention relates to a method for examining the onset or risk of developing bone marrow tumors such as myelodysplastic syndrome (MDS) and acute myeloid leukemia (AML) in humans, a method for obtaining an index for the examination, and the body of the DDX41 gene in humans. The present invention relates to a method for predicting the existence or future development of a cell mutation, a method for obtaining an index for prediction, and a kit for these methods.
骨髄異形成症候群(MDS)および急性骨髄性白血病(AML)はいずれも骨髄腫瘍に分類される疾患でMDS発症後AMLへ移行すると考えられている。両疾患は中高年齢で発症するため、発症と関連する遺伝子変異はこれまで後天性の遺伝子変異(体細胞変異)であると考えられていた。しかし、発明者らはコーカサス人種のMDS・AML患者と健常者を対象に遺伝子解析を行い、MDS・AML患者の中にDDX41遺伝子の胚細胞変異を有する症例が認められること、当該変異が遺伝するとほぼ全例でMDS又はAMLが発症することを初めて報告している(非特許文献1)。 Myelodysplastic syndrome (MDS) and acute myeloid leukemia (AML) are both classified as bone marrow tumors and are thought to transition to AML after the onset of MDS. Since both diseases develop at middle and old age, the gene mutation associated with the onset has been previously considered to be an acquired gene mutation (somatic mutation). However, the inventors conducted genetic analysis on MDS / AML patients of Caucasian race and healthy subjects, and found that some MDS / AML patients had a embryonic cell mutation of the DDX41 gene, and the mutation was inherited. Then, it is reported for the first time that MDS or AML develops in almost all cases (Non-Patent Document 1).
上記の通りMDS/AMLは、従来、発症と関連する遺伝子変異はこれまで後天性の遺伝子変異(体細胞変異)であると考えらており、胚細胞変異を調べることでMDS/AMLの発症又は発症リスクを検査することは従来不可能と考えられてきた。 As mentioned above, in MDS / AML, it has been considered that the gene mutation associated with the onset is an acquired gene mutation (somatic mutation), and by examining the embryonic cell mutation, the onset of MDS / AML or It has traditionally been considered impossible to test for the risk of developing the disease.
非特許文献1ではコーカサス人種でのMDS/AML患者に特異的な胚細胞変異が認められることが報告されているが、東アジア人種等の黄色人種では変異部位が同一であるとは限らない。また、コーカサス人種ではMDS/AMLの家族性症例が知られているのに対して、黄色人種ではMDS/AMLは孤発性症例のみが知られており家族性症例は従来知られていなかったため、黄色人種でのMDS/AMLは、コーカサス人種でのMDS/AMLとは異質なものと考えられていた。しかも、家族性疾患とは異なり、孤発性疾患では、疾患と相関する胚細胞変異を特定することは困難である。従って、非特許文献1に開示の知見を、黄色人種での胚細胞変異を調べMDS/AMLの発症又は発症リスクを検査することに応用することは不可能であった。
そこで本発明は、ヒト、特に東アジア人種等の黄色人種、におけるMDS、AML等の骨髄腫瘍の発症又は発症リスクを検査するための手段を提供することを目的とする。本発明はまた、MDS、AML等の骨髄腫瘍の治療のために有用な指標を取得するための手段を提供することを目的とする。 Therefore, an object of the present invention is to provide a means for examining the onset or risk of developing bone marrow tumors such as MDS and AML in humans, especially yellow races such as East Asian races. It is also an object of the present invention to provide a means for obtaining useful indicators for the treatment of bone marrow tumors such as MDS and AML.
本発明は以下の課題を解決するための手段として以下の発明を提供する。
(1) ヒトにおける骨髄腫瘍の発症又は発症リスクを検査するための指標の取得方法であって、
野生型DDX41遺伝子によりコードされるポリペプチドの配列番号2に示すアミノ酸配列において第500位、第259位、第363位、第364位、第3位、第7位、第35位、第187位及び第256位からなる群から選択される1以上のアミノ酸での変異を生じる、DDX41遺伝子の1以上の胚細胞変異を検出することを特徴とする方法。
(2) 前記アミノ酸での変異が、配列番号2に示すアミノ酸配列における、
第500位のアラニンのフレームシフト変異、
第259位のチロシンのシステインへの置換、
第363位のセリン及び第364位のチロシンの、1つのチロシンへの置換、又は、第363位のセリンの欠失、
第3位のグルタミン酸のリジンへの置換、
第7位のグルタミン酸のナンセンス変異、
第35位のプロリンのアルギニンへの置換、
第187位のリジンのアルギニンへの置換、及び
第256位のグルタミン酸のリジンへの置換
からなる群から選択される1以上の変異である、(1)に記載の方法。
(3) DDX41遺伝子の変異が、配列番号1に示す野生型DDX41のcDNA塩基配列における位置として、
第1496位のシトシンの重複、
第776位のアデニンのグアニンへの置換、
第1088位から第1090位のシトシン-シトシン-チミンの欠失又は第1087位から第1089位のチミン-シトシン-シトシンの欠失、
第7位のグアニンのアデニンへの置換、
第19位のグアニンのチミンへの置換、
第104位のシトシンのグアニンへの置換、
第560位のアデニンのグアニンへの置換、及び
第766位のグアニンのアデニンへの置換、
からなる群から選択される1以上の変異である、(1)又は(2)に記載の方法。
(4) 前記アミノ酸での変異が、配列番号2に示すアミノ酸配列における、
第500位のアラニンのフレームシフト変異、及び
第259位のチロシンのシステインへの置換、
のうち1以上の変異である、(2)に記載の方法。
(5) DDX41遺伝子の変異が、配列番号1に示す野生型DDX41のcDNA塩基配列における位置として、
第1496位のシトシンの重複、及び
第776位のアデニンのグアニンへの置換、
のうち1以上の変異である、(3)に記載の方法。
(6) 骨髄腫瘍が、骨髄異形成症候群(MDS)及び/又は急性骨髄性白血病(AML)である、(1)〜(5)のいずれかに記載の方法。
(7) 検査するMDS及び/又はAMLの発症又は発症リスクが、進行型MDS及び/又はAMLの発症又は発症リスクである、(6)に記載の方法。
(8) CUX1遺伝子の変異を検出することを更に含む、(1)〜(7)のいずれかに記載の方法。
(9) ヒトにおけるDDX41遺伝子の体細胞変異の存在又は将来的な発生を予測するための指標の取得方法であって、
野生型DDX41遺伝子によりコードされるポリペプチドの配列番号2に示すアミノ酸配列において第500位、第259位、第363位、第364位、第3位、第7位、第35位、第187位及び第256位からなる群から選択される1以上のアミノ酸での変異を生じる、DDX41遺伝子の1以上の胚細胞変異を検出することを特徴とする方法。
(10) 前記DDX41遺伝子の体細胞変異が、
野生型DDX41遺伝子によりコードされる配列番号2に示すアミノ酸配列における、第525位のアルギニンの変異を生じるDDX41遺伝子の体細胞変異である、(9)に記載の方法。
(11) ヒトにおける骨髄腫瘍の発症又は発症リスクを検査する方法、並びに、ヒトにおけるDDX41遺伝子の体細胞変異の存在又は将来的な発生を予測する方法のうち少なくとも1つの方法に用いるキットであって、
DDX41遺伝子のうち、変異した場合に、野生型DDX41遺伝子によりコードされるポリペプチドの配列番号2に示すアミノ酸配列において第500位、第259位、第363位、第364位、第3位、第7位、第35位、第187位及び第256位からなる群から選択される1以上のアミノ酸での変異を生じる塩基を1以上含む部位を増幅できるように設計されたプライマーセット、
DDX41遺伝子のうち、変異した場合に、野生型DDX41遺伝子によりコードされるポリペプチドの配列番号2に示すアミノ酸配列において第500位、第259位、第363位、第364位、第3位、第7位、第35位、第187位及び第256位からなる群から選択される1以上のアミノ酸での変異を生じる塩基を1以上含む部位と結合できるように設計されたプローブ、及び
DDX41遺伝子による翻訳産物であるポリペプチドのうち、配列番号2に示す野生型のアミノ酸配列において第500位、第259位、第363位、第364位、第3位、第7位、第35位、第187位及び第256位からなる群から選択される1以上のアミノ酸に対応するアミノ酸を含む部位を認識する抗体
からなる群から選択される1種以上を含有するキット。
(12) CUX1遺伝子の変異を検出するための試薬を更に含む、(11)に記載のキット。
The present invention provides the following invention as a means for solving the following problems.
(1) A method for obtaining an index for examining the onset or risk of developing bone marrow tumor in humans.
At position 500, position 259, position 363,
(2) The mutation in the amino acid is in the amino acid sequence shown in SEQ ID NO: 2.
Frameshift mutation in the 500th place alanine,
Substitution of tyrosine at position 259 with cysteine,
Substitution of serine at position 363 and tyrosine at
Substitution of glutamic acid at position 3 with lysine,
Nonsense mutation in glutamic acid at position 7,
Substitution of 35th place proline with arginine,
The method according to (1), wherein the mutation is one or more selected from the group consisting of the substitution of lysine at position 187 with arginine and the substitution of glutamic acid at position 256 with lysine.
(3) A mutation in the DDX41 gene is used as the position in the cDNA base sequence of wild-type DDX41 shown in SEQ ID NO: 1.
Overlapping cytosine in 1496,
Substitution of adenine at position 776 with guanine,
Cytosine-cytosine-thymine deletion at positions 1088 to 1090 or thymine-cytosine-cytosine deletion at positions 1087 to 1089,
Substitution of 7th place guanine with adenine,
Substitution of guanine at position 19 with thymine,
Substitution of cytosine at position 104 with guanine,
Substitution of adenine at position 560 with guanine, and substitution of guanine at position 766 with guanine,
The method according to (1) or (2), which is one or more mutations selected from the group consisting of.
(4) The mutation in the amino acid is in the amino acid sequence shown in SEQ ID NO: 2.
Frameshift mutation in alanine at position 500, and substitution of tyrosine at position 259 with cysteine,
The method according to (2), which is one or more of the mutations.
(5) A mutation in the DDX41 gene is used as the position in the cDNA base sequence of wild-type DDX41 shown in SEQ ID NO: 1.
Overlapping cytosine at position 1496 and replacement of adenine at position 776 with guanine,
The method according to (3), which is one or more of the mutations.
(6) The method according to any one of (1) to (5), wherein the bone marrow tumor is myelodysplastic syndrome (MDS) and / or acute myeloid leukemia (AML).
(7) The method according to (6), wherein the onset or risk of developing MDS and / or AML to be examined is the onset or risk of developing advanced MDS and / or AML.
(8) The method according to any one of (1) to (7), further comprising detecting a mutation in the CUX1 gene.
(9) A method for obtaining an index for predicting the existence or future development of a somatic mutation in the DDX41 gene in humans.
At position 500, position 259, position 363,
(10) A somatic mutation in the DDX41 gene
The method according to (9), which is a somatic mutation of the DDX41 gene that causes a mutation of arginine at position 525 in the amino acid sequence shown in SEQ ID NO: 2 encoded by the wild-type DDX41 gene.
(11) A kit used for at least one of a method for examining the onset or risk of developing bone marrow tumor in humans and a method for predicting the presence or future occurrence of a somatic mutation of the DDX41 gene in humans. ,
Of the DDX41 genes, when mutated, the amino acid sequence shown in SEQ ID NO: 2 of the polypeptide encoded by the wild-type DDX41 gene is position 500, position 259, position 363,
Of the DDX41 genes, when mutated, the amino acid sequence shown in SEQ ID NO: 2 of the polypeptide encoded by the wild-type DDX41 gene is position 500, position 259, position 363,
Among the polypeptides translated by the DDX41 gene, the wild-type amino acid sequence shown in SEQ ID NO: 2 is located at
(12) The kit according to (11), further comprising a reagent for detecting a mutation in the CUX1 gene.
本発明によれば、ヒト、特に東アジア人種等の黄色人種、におけるMDS、AML等の骨髄腫瘍の発症又は発症リスクを検査するための指標の取得が可能となる。各変異は胚細胞変異であり、一般に、MDS、AML等の骨髄腫瘍は高齢時に発症するため子孫に遺伝するリスクが高いが、本発明によれば、骨髄腫瘍を発症前の段階から早期発見することができ、予防に繋げることが可能となる。 According to the present invention, it is possible to obtain an index for examining the onset or risk of developing bone marrow tumors such as MDS and AML in humans, particularly yellow races such as East Asian races. Each mutation is an embryonic cell mutation, and in general, bone marrow tumors such as MDS and AML develop at an early age and therefore have a high risk of being inherited to offspring. However, according to the present invention, bone marrow tumors are detected early from the presymptomatic stage. It is possible to lead to prevention.
本発明の他の態様によれば、ヒト、特に東アジア人種等の黄色人種、におけるDDX41遺伝子の体細胞変異の存在又は将来的な発生を予測するための指標の取得が可能になる。DDX41遺伝子の体細胞変異のうち一部はDDX41遺伝子がコードするポリペプチドのアミノ酸配列に変異を起こすが、このようなアミノ酸配列の変異は、骨髄腫瘍を対象とした新薬開発のターゲットとして有効である。 According to another aspect of the present invention, it is possible to obtain an index for predicting the existence or future development of a somatic mutation of the DDX41 gene in humans, particularly yellow races such as East Asian races. Some of the somatic mutations in the DDX41 gene cause mutations in the amino acid sequence of the polypeptide encoded by the DDX41 gene, and such mutations in the amino acid sequence are effective targets for new drug development in bone marrow tumors. ..
以下、本発明を詳細に説明する。
<遺伝子>
本発明において「遺伝子」とは、ゲノムDNA、mRNA、cDNA等のポリヌクレオチドを含み、天然に存在するものだけでなく人為的に調製されたものであってもよい。また「DDX41遺伝子」や「CUX1遺伝子」といったとき、これらの遺伝子の遺伝情報を保持するポリヌクレオチドを指し、アミノ酸配列をコードするセンス鎖には限らず、その相補鎖(鋳型鎖)であるアンチセンス鎖であってもよく、全体である必要はなく一部の断片であってもよい。また前記ポリヌクレオチドは、DNAの二本鎖であってもよいし、DNAやRNAの一本鎖であってもよい。
Hereinafter, the present invention will be described in detail.
<Gene>
In the present invention, the "gene" includes polynucleotides such as genomic DNA, mRNA, and cDNA, and may be artificially prepared as well as naturally occurring ones. The terms "DDX41 gene" and "CUX1 gene" refer to polynucleotides that retain the genetic information of these genes, and are not limited to the sense strand that encodes the amino acid sequence, but antisense, which is the complementary strand (template strand) thereof. It may be a chain, not necessarily the whole, but a partial fragment. Further, the polynucleotide may be a double strand of DNA or a single strand of DNA or RNA.
DDX41 (DEAD (Asp-Glu-Ala-Asp) ボックスポリペプチド41, DEAD (Asp-Glu-Ala-Asp) box polypeptide 41) 遺伝子はヒト第5染色体上に存在し、その代表的なcDNA塩基配列(GenBank Accession No. NM_016222のCDS)は配列番号1に示す通りであり、配列番号1に示す塩基配列がコードするポリペプチドのアミノ酸配列は配列番号2に示す通りである。本発明では、DDX41遺伝子に含まれる塩基の位置を示すために、配列番号1に示すcDNA塩基配列における塩基の位置を用いるが、該位置は、DDX41遺伝子が配列番号1に示すcDNA塩基配列以外の形態の遺伝子、例えばゲノムDNA、mRNA(他のアイソフォームのmRNAでもよい)、cDNA(他のアイソフォームのcDNAでもよい)等の各ポリヌクレオチドである場合には、各形態の遺伝子における、配列番号1に示すcDNA塩基配列の位置に対応する位置の塩基を意味する。例えば「配列番号1に示す野生型DDX41のcDNA塩基配列における位置として、第1496位のシトシンの重複」と表現した場合は、ゲノムDNA、mRNA(他のアイソフォームのmRNAでもよい)、cDNA(他のアイソフォームのcDNAでもよい)等の各ポリヌクレオチド中での、配列番号1に示すcDNA塩基配列の第1496位のシトシンに対応する位置において、cDNA上でのシトシンに対応する塩基(ゲノムDNAセンス鎖、cDNAセンス鎖及びmRNAではシトシンであり、ゲノムDNAアンチセンス鎖及びcDNAアンチセンス鎖ではグアニン)が2つ重複して存在する変異を包含する。
The DDX41 (DEAD (Asp-Glu-Ala-Asp) box polypeptide 41, DEAD (Asp-Glu-Ala-Asp) box polypeptide 41) gene is located on
CUX1 (カット-ライクホメオボックス1,cut-like homeobox 1) 遺伝子はヒト第7染色体上に存在し、その代表的なcDNA塩基配列(GenBank Accession No. NM_001202543のCDS)は配列番号3に示す通りであり、配列番号3に示す塩基配列がコードするポリペプチドのアミノ酸配列は配列番号4に示す通りである。CUX1遺伝子についても、DDX41遺伝子と同様に、CUX1遺伝子に含まれる塩基の位置を示すために、配列番号3に示すcDNA塩基配列における塩基の位置を用いる。 The CUX1 (cut-like homeobox 1) gene is located on human chromosome 7, and its typical cDNA base sequence (GenBank Accession No. NM_001202543 CDS) is as shown in SEQ ID NO: 3. Yes, the amino acid sequence of the polypeptide encoded by the nucleotide sequence shown in SEQ ID NO: 3 is as shown in SEQ ID NO: 4. As for the CUX1 gene, as in the DDX41 gene, the base position in the cDNA base sequence shown in SEQ ID NO: 3 is used to indicate the position of the base contained in the CUX1 gene.
<ヒトにおける骨髄腫瘍の発症又は発症リスクを検査する指標の取得方法>
本発明において「ヒトにおける骨髄腫瘍の発症又は発症リスクを検査する指標の取得方法」とは、「ヒトにおける骨髄腫瘍の発症又は発症リスクを判定するためのデータ(又は指標)を取得する方法」、「ヒトにおける骨髄腫瘍の発症又は発症リスクの検査を補助(又は支援)する方法」と表現することもできる。
<Method of obtaining an index for testing the onset or risk of developing bone marrow tumor in humans>
In the present invention, the "method for obtaining an index for examining the onset or risk of developing bone marrow tumor in humans" is "a method for obtaining data (or index) for determining the onset or risk of developing bone marrow tumor in humans", It can also be expressed as "a method of assisting (or supporting) the examination of the onset or risk of developing bone marrow tumor in humans".
本発明の方法の対象となるヒトは、特に限定されるものではなく、骨髄腫瘍が既に発症しているヒトであってもよいし、本方法の実施時点では発症していないヒトであってもよい。ヒトの人種としては、好ましくは黄色人種であり、より好ましくは東アジア人種である。東アジア人種とは、日本、朝鮮半島、中国を含む、アジア大陸の東部及びその周辺の出身の先祖を持つ人々を指す。 The human being who is the target of the method of the present invention is not particularly limited, and may be a human who has already developed a bone marrow tumor or a human who has not developed a bone marrow tumor at the time of carrying out the method. Good. The human race is preferably the yellow race, more preferably the East Asian race. East Asians refer to people with ancestors from the eastern part of the Asian continent and its surroundings, including Japan, the Korean Peninsula, and China.
本発明の方法は検査対象のヒトから分離した試料を用いて行うことができる。
本発明の方法は、野生型DDX41遺伝子によりコードされるポリペプチドの配列番号2に示すアミノ酸配列において第500位、第259位、第363位、第364位、第3位、第7位、第35位、第187位及び第256位からなる群から選択される1以上のアミノ酸での変異を生じる、DDX41遺伝子の1以上の胚細胞変異を検出することを特徴とする。これらの変異は、DDX41遺伝子によりコードされるポリペプチドの機能を変化又は喪失させる変異である可能性がある。
The method of the present invention can be carried out using a sample separated from the human to be inspected.
The method of the present invention is located at
検出された変異が体細胞変異ではなく胚細胞変異であることは、例えば、被験体の正常組織から取得した試料において変異の存在を確認することにより判断することができ、より好ましくは正常組織から取得した試料と、骨髄腫瘍の腫瘍組織又は腫瘍組織と疑われる組織から取得した試料との両方おいて変異の存在を確認することにより判断することができる。正常組織から取得した試料のみを用いる場合は、複数回の測定を行い、及び/又は、正常組織の複数個所から取得された試料を用いて測定を行い、変異を確認することにより該変異が胚細胞変異であると判断することが好ましい。 It can be determined that the detected mutation is not a somatic mutation but an embryonic cell mutation, for example, by confirming the presence of the mutation in a sample obtained from the normal tissue of the subject, and more preferably from the normal tissue. It can be determined by confirming the presence of mutations in both the obtained sample and the sample obtained from the tumor tissue of the bone marrow tumor or the tissue suspected to be the tumor tissue. When using only samples obtained from normal tissue, multiple measurements are performed, and / or measurements are performed using samples obtained from multiple locations in normal tissue, and the mutation is confirmed by confirming the mutation. It is preferable to judge that it is a cell mutation.
本発明の方法では、配列番号2の第500位、第259位、第363位、第364位、第3位、第7位、第35位、第187位及び第256位からなる群のうち、少なくとも1以上のアミノ酸での変異を生じる、DDX41遺伝子の少なくとも1つの胚細胞変異を検出すればよいが、前記群は、より好ましくは第500位、第259位、第363位、第364位及び第35位からなり、更に好ましくは第500位及び第259位からなり、最も好ましくは第500位からなる。本発明者らはこれらの胚細胞変異を有するヒトが、MDS、AML等の骨髄腫瘍を発症するリスクが特に高いことを見出した。
In the method of the present invention, among the group consisting of the 500th position, the 259th position, the 363rd position, the 364th position, the 3rd position, the 7th position, the 35th position, the 187th position and the 256th position of SEQ ID NO: 2. , At least one embryonic cell mutation of the DDX41 gene that results in a mutation at at least one amino acid may be detected, but the group is more preferably at
本発明では、ポリペプチドにおけるアミノ酸又は遺伝子における塩基の各変異を、所定の1又は2の表現により特定するが、同一変異を更に別の表現でも特定することができる場合があり、それらは全て同一の変異として扱う。 In the present invention, each mutation of an amino acid or a base in a gene in a polypeptide is specified by a predetermined expression of 1 or 2, but the same mutation may be specified by yet another expression, and they are all the same. Treat as a mutation in.
本発明の方法では、ヒト被験体が、前記のDDX41遺伝子の胚細胞変異の1つ以上をDDX41遺伝子の対立遺伝子座の少なくとも一方に有していれば、該ヒト被験体が骨髄腫瘍を発症している、又は現時点で発症していなくても将来的に発症のリスクがあると判定することができる。なお、実施例に示す本発明者らの調査の範囲では、DDX41胚細胞変異陽性患者はいずれも、上記のDDX41胚細胞変異のうち1つのみを有しており、且つ、該変異は対立遺伝子座の一方のみに認められている。 In the method of the invention, if a human subject has one or more of the embryonic mutations in the DDX41 gene at at least one of the allelic loci of the DDX41 gene, the human subject will develop a bone marrow tumor. It can be determined that there is a risk of developing the disease in the future even if the disease does not occur at this time. In addition, within the scope of the investigation by the present inventors shown in Examples, all DDX41 embryo cell mutation-positive patients have only one of the above DDX41 embryo cell mutations, and the mutation is an allele. Only one of the loci is allowed.
野生型DDX41遺伝子によりコードされるポリペプチドの配列番号2に示すアミノ酸配列での上記各アミノ酸の変異とは、ミスセンス変異(他アミノ酸への変異)、ナンセンス変異(遺伝子中での終止コドンへの変異)、フレームシフト変異(遺伝子中での塩基の挿入及び/又は欠失により、遺伝子中での塩基の変異位置に対応するアミノ酸及び/又はそれより下流のアミノ酸配列が変化する変異)、インフレーム欠失変異等を包含する。配列番号2の前記各位置でのこれらのアミノ酸変異は、配列番号2での各位置のアミノ酸だけでなく、それよりも下流のアミノ酸配列の変異を伴い得る。 The mutations of each of the above amino acids in the amino acid sequence shown in SEQ ID NO: 2 of the polypeptide encoded by the wild-type DDX41 gene are missense mutation (mutation to another amino acid) and nonsense mutation (mutation to termination codon in the gene). ), Frame shift mutation (a mutation in which the amino acid corresponding to the mutation position of the base in the gene and / or the amino acid sequence downstream of it changes due to the insertion and / or deletion of the base in the gene), in-frame missing Includes loss mutation and the like. These amino acid mutations at each of the above positions of SEQ ID NO: 2 may involve mutations in the amino acid sequence at each position in SEQ ID NO: 2 as well as the amino acid sequence downstream thereof.
各アミノ酸での変異は上記のいずれであってもよいが、典型的には、前記アミノ酸での変異が、配列番号2に示すアミノ酸配列における、
第500位のアラニンのフレームシフト変異、
第259位のチロシンのシステインへの置換、
第363位のセリン及び第364位のチロシンの、1つのチロシンへの置換、又は第363位のセリンの欠失、
第3位のグルタミン酸のリジンへの置換、
第7位のグルタミン酸のナンセンス変異、
第35位のプロリンのアルギニンへの置換、
第187位のリジンのアルギニンへの置換、及び
第256位のグルタミン酸のリジンへの置換
からなる群から選択される1以上の変異であり、
より好ましくは、
配列番号2に示すアミノ酸配列における、
第500位のアラニンのフレームシフト変異、
第259位のチロシンのシステインへの置換、
第363位のセリン及び第364位のチロシンの、1つのチロシンへの置換、又は第363位のセリンの欠失、及び
第35位のプロリンのアルギニンへの置換
のうち1以上の変異であり、
特に好ましくは
配列番号2に示すアミノ酸配列における、
第500位のアラニンのフレームシフト変異、及び
第259位のチロシンのシステインへの置換、
のうち1以上の変異である。
The mutation at each amino acid may be any of the above, but typically the mutation at the amino acid is in the amino acid sequence shown in SEQ ID NO: 2.
Frameshift mutation in the 500th place alanine,
Substitution of tyrosine at position 259 with cysteine,
Substitution of serine at position 363 and tyrosine at
Substitution of glutamic acid at position 3 with lysine,
Nonsense mutation in glutamic acid at position 7,
Substitution of 35th place proline with arginine,
One or more mutations selected from the group consisting of the substitution of lysine at position 187 with arginine and the substitution of glutamic acid at position 256 with lysine.
More preferably
In the amino acid sequence shown in SEQ ID NO: 2,
Frameshift mutation in the 500th place alanine,
Substitution of tyrosine at position 259 with cysteine,
One or more mutations in the substitution of serine at position 363 and tyrosine at
Particularly preferably, in the amino acid sequence shown in SEQ ID NO: 2.
Frameshift mutation in alanine at position 500, and substitution of tyrosine at position 259 with cysteine,
One or more of these mutations.
配列番号2での第500位のアラニンのフレームシフト変異は、DDX41遺伝子において、配列番号1に示す野生型DDX41のcDNA塩基配列における位置として、第1496位のシトシンの重複により生じるものであることが好ましいがこれには限定されない。ここで「第1496位のシトシンの重複」は、配列番号1に示す野生型DDX41のcDNA塩基配列における位置として第1496位の1塩基のシトシンが2塩基のシトシン−シトシンに置換されたと表現することができる変異であり、「第1495位と第1496位との間へのシトシンの挿入」、「第1495位のシトシンの重複」等の各種表現で表すことができる。 The frameshift mutation of alanine at position 500 in SEQ ID NO: 2 may result from duplication of cytosine at position 1496 as a position in the cDNA sequence of wild-type DDX41 shown in SEQ ID NO: 1 in the DDX41 gene. Preferred but not limited to this. Here, "overlapping cytosine at position 1496" is expressed as the position in the cDNA base sequence of wild-type DDX41 shown in SEQ ID NO: 1 in which 1-base cytosine at position 1496 is replaced with 2-base cytosine-cytosine. It is a mutation that can be expressed by various expressions such as "insertion of cytosine between positions 1495 and 1496" and "overlap of cytosine at position 1495".
配列番号2での第259位のチロシンのシステインへの置換は、DDX41遺伝子において、配列番号1に示す野生型DDX41のcDNA塩基配列における位置として、第776位のアデニンのグアニンへの置換により生じるものであることが好ましいがこれには限定されない。 The substitution of tyrosine at position 259 with cysteine in SEQ ID NO: 2 is caused by the substitution of adenine at position 776 with guanine as the position in the cDNA base sequence of wild-type DDX41 shown in SEQ ID NO: 1 in the DDX41 gene. However, the present invention is not limited to this.
配列番号2での第363位のセリン及び第364位のチロシンの、1つのチロシンへの置換(又は第363位のセリンの欠失)は、DDX41遺伝子において、配列番号1に示す野生型DDX41のcDNA塩基配列における位置として、第1088位から第1090位のシトシン-シトシン-チミンの欠失(又は第1087位から第1089位のチミン-シトシン-シトシンの欠失)により生じるものであることが好ましいがこれには限定されない。
Substitution of thymine at position 363 and thymine at
配列番号2での第3位のグルタミン酸のリジンへの置換は、DDX41遺伝子において、配列番号1に示す野生型DDX41のcDNA塩基配列における位置として、第7位のグアニンのアデニンへの置換により生じるものであることが好ましいがこれには限定されない。 The substitution of glutamic acid at position 3 with lysine in SEQ ID NO: 2 is caused by the substitution of guanine at position 7 with adenine as the position in the cDNA base sequence of wild-type DDX41 shown in SEQ ID NO: 1 in the DDX41 gene. However, the present invention is not limited to this.
配列番号2での第7位のグルタミン酸のナンセンス変異は、DDX41遺伝子において、配列番号1に示す野生型DDX41のcDNA塩基配列における位置として、第19位のグアニンのチミンへの置換により生じるものであることが好ましいがこれには限定されない。 The nonsense mutation of glutamic acid at position 7 in SEQ ID NO: 2 is caused by the replacement of guanine at position 19 with thymine as a position in the cDNA base sequence of wild-type DDX41 shown in SEQ ID NO: 1 in the DDX41 gene. It is preferable, but not limited to this.
配列番号2での第35位のプロリンのアルギニンへの置換は、DDX41遺伝子において、配列番号1に示す野生型DDX41のcDNA塩基配列における位置として、第104位のシトシンのグアニンへの置換により生じるものであることが好ましいがこれには限定されない。 The substitution of proline at position 35 with arginine in SEQ ID NO: 2 is caused by the substitution of cytosine at position 104 with guanine as the position in the cDNA base sequence of wild-type DDX41 shown in SEQ ID NO: 1 in the DDX41 gene. However, the present invention is not limited to this.
配列番号2での第187位のリジンのアルギニンへの置換は、DDX41遺伝子において、配列番号1に示す野生型DDX41のcDNA塩基配列における位置として、第560位のアデニンのグアニンへの置換により生じるものであることが好ましいがこれには限定されない。 The substitution of lysine at position 187 with arginine in SEQ ID NO: 2 results from the substitution of adenine at position 560 with guanine as the position in the cDNA base sequence of wild-type DDX41 shown in SEQ ID NO: 1 in the DDX41 gene. However, the present invention is not limited to this.
配列番号2での第256位のグルタミン酸のリジンへの置換は、DDX41遺伝子において、配列番号1に示す野生型DDX41のcDNA塩基配列における位置として、第766位のグアニンのアデニンへの置換により生じるものであることが好ましいがこれには限定されない。 The substitution of glutamic acid at position 256 with lysine in SEQ ID NO: 2 is caused by the substitution of guanine at position 766 with adenine as the position in the cDNA base sequence of wild-type DDX41 shown in SEQ ID NO: 1 in the DDX41 gene. However, the present invention is not limited to this.
本発明では、被験体から分離された試料において上記胚細胞変異の1つ以上が検出された場合に、該被験体は骨髄腫瘍を発症している、又は現時点で発症していなくても将来的に発症のリスクがあると判定するための指標とすることができる。本発明において「骨髄腫瘍」とは、骨髄系細胞を由来とする腫瘍性疾患を指し、骨髄異形成症候群(MDS)、急性骨髄性白血病(AML)、MDS/MPN(骨髄異形成骨髄増殖性腫瘍)、MPN(骨髄増殖性腫瘍)等の疾患を包含する総称である。本発明の方法は「骨髄腫瘍」がMDS及び/又はAMLである場合に特に有効である。本発明者らは図4に示すように、MDS及び/又はAML症例のなかでも特に骨髄芽球が骨髄で5%を超える進行型MDSの症例及びAMLの症例において特に高頻度に上記胚細胞変異を見出した。このことから、本発明の方法により上記胚細胞変異が検出された被験体は進行型MDS又はAMLが発症している、又は現時点で発症していなくても将来的に発症のリスクがあると判定するための指標を取得することができる。 In the present invention, when one or more of the above embryonic cell mutations is detected in a sample isolated from a subject, the subject has developed a bone marrow tumor, or even if it has not developed at this time, in the future. It can be used as an index for determining that there is a risk of developing the disease. In the present invention, "myeloproliferative neoplasm" refers to a neoplastic disease derived from myeloid cells, such as myelodysplastic syndrome (MDS), acute myeloid leukemia (AML), and MDS / MPN (myeloproliferative neoplasm). ), MPN (myeloproliferative neoplasm) and other diseases. The method of the present invention is particularly effective when the "bone marrow tumor" is MDS and / or AML. As shown in FIG. 4, the present inventors have particularly frequently performed the above-mentioned embryonic cell mutations in cases of advanced MDS in which myeloblasts exceed 5% in the bone marrow and cases of AML among MDS and / or AML cases. I found. From this, it is determined that the subject in which the embryonic cell mutation is detected by the method of the present invention has advanced MDS or AML, or is at risk of developing it in the future even if it does not develop at present. You can get the index to do.
本発明の方法において、各変異の有無を検出する手段は特に限定されず任意の手段を採用することができる。各変異の検出は、DDX41遺伝子において各アミノ酸での変異を生じる塩基での変異の有無を検出することにより行ってもよいし、DDX41遺伝子がコードするポリペプチドにおいて各アミノ酸の変異の有無を検出することにより行ってもよい。なお本発明では、配列番号2で前記1つ以上のアミノ酸での変異を生じるDDX41遺伝子の塩基の変異が存在するとは、変異DDX41遺伝子の転写・翻訳産物として、所定のアミノ酸が変異した変異体ポリペプチドが実際に被験体内で存在する必要はなく、変異DDX41遺伝子が転写され翻訳されたと仮定した時に所定のアミノ酸が変異した変異体ポリペプチドを生じさせるDDX41遺伝子の塩基の変異が被験体内に存在すればよい (他の遺伝子での変異についても同様である)。DDX41遺伝子での変異の検出方法としては、プライマーセットを用いて核酸増幅し増幅産物をシークエンシングする方法、変異部位に特異的にハイブリダイズするプローブを用いる方法、リアルタイムPCRやDNAチップを用いる方法等が挙げられる。DDX41遺伝子がコードするポリペプチドにおいて各アミノ酸の変異の有無を検出する方法としては免疫染色法やタンパクアレイ法が挙げられる。 In the method of the present invention, the means for detecting the presence or absence of each mutation is not particularly limited, and any means can be adopted. Each mutation may be detected by detecting the presence or absence of a mutation in a base that causes a mutation in each amino acid in the DDX41 gene, or the presence or absence of a mutation in each amino acid in a polypeptide encoded by the DDX41 gene. It may be done by. In the present invention, the presence of a mutation in the base of the DDX41 gene that causes a mutation in one or more amino acids in SEQ ID NO: 2 means that a mutant poly in which a predetermined amino acid is mutated as a transcription / translation product of the mutated DDX41 gene. The peptide does not have to actually be present in the subject, but a mutation in the base of the DDX41 gene that gives rise to a mutant polypeptide in which a given amino acid is mutated, assuming that the mutant DDX41 gene is transcribed and translated. (The same applies to mutations in other genes). Methods for detecting mutations in the DDX41 gene include a method of nucleic acid amplification using a primer set and sequencing of the amplification product, a method of using a probe that specifically hybridizes to the mutation site, a method of using real-time PCR and a DNA chip, etc. Can be mentioned. Methods for detecting the presence or absence of mutations in each amino acid in the polypeptide encoded by the DDX41 gene include immunostaining and protein array methods.
以下では、ヒト生体から分離された試料に含有されるゲノムDNA、mRNA(又はmRNAから調製されたcDNA)、ポリペプチドを用いて変異を検出する実施形態について個別に説明する。 Hereinafter, embodiments of detecting mutations using genomic DNA, mRNA (or cDNA prepared from mRNA), and polypeptide contained in a sample isolated from a human living body will be individually described.
(1) ゲノムDNAでの変異を検出する実施形態
ヒトから分離された試料に含有されるゲノムDNAを用いて変異を検出する場合、ヒトから分離された試料からゲノムDNAを抽出する。抽出方法は特に限定されず公知の方法を使用することができる。
(1) Embodiment of detecting mutation in genomic DNA When a mutation is detected using the genomic DNA contained in a sample isolated from human, the genomic DNA is extracted from the sample isolated from human. The extraction method is not particularly limited, and a known method can be used.
ヒトから分離された試料は、特に限定されるものではなく、ゲノムDNAを抽出可能なものであればよい。具体的には、例えば、血液、骨髄液、毛髪、爪、口腔粘膜、皮膚、尿、便、他の臓器を過去に別の目的で採取した場合の病理標本(例えばヘリコバクターピロリ菌検出目的の胃粘膜生検等)等を挙げることができる。また、ヒトから分離した細胞を培養し、増殖したものからゲノムDNAを抽出してもよい。 The sample isolated from humans is not particularly limited as long as it can extract genomic DNA. Specifically, for example, a pathological specimen (for example, a stomach for detecting Helicobacter pylori) when blood, bone marrow fluid, hair, nails, oral mucosa, skin, urine, stool, and other organs are collected for another purpose in the past. Mucosal biopsy, etc.) and the like. Alternatively, cells isolated from humans may be cultured and genomic DNA may be extracted from the proliferated cells.
また、抽出したゲノムDNAは、例えば、PCR(Polymerase Chain Reaction)法、LAMP(Loop-Mediated Isothermal Amplification)法、NASBA(Nucleic acid sequence based amplification)法、TMA(Transcription-mediated amplification)法、SDA(Strand Displacement Amplification)法、ICAN(Isothermal and Chimeric primer-initiated Amplification of Nucleic acids)法などの通常行われる遺伝子増幅法により増幅して用いてもよい。このとき分析すべきDDX41遺伝子の少なくとも1つの変異を含む領域を増幅すればよい。 In addition, the extracted genomic DNA is, for example, PCR (Polymerase Chain Reaction) method, LAMP (Loop-Mediated Isothermal Amplification) method, NASBA (Nucleic acid sequence based amplification) method, TMA (Transcription-mediated amplification) method, SDA (Strand). It may be amplified by a commonly used gene amplification method such as Displacement Amplification) method or ICAN (Isothermal and Chimeric primer-initiated Amplification of Nucleic acids) method. At this time, the region containing at least one mutation of the DDX41 gene to be analyzed may be amplified.
本発明で分析する変異はDDX41遺伝子のエクソン領域に含まれる変異であるため、ゲノムDNAからエクソン領域のみを切り出したものを検出対象試料としてもよい。 Since the mutation analyzed in the present invention is a mutation contained in the exon region of the DDX41 gene, a sample obtained by cutting out only the exon region from genomic DNA may be used as a detection target sample.
調製されたゲノムDNAを含有する試料を用いて、DDX41遺伝子での変異の有無を検出する方法は、特に限定されるものではないが、例えば、ゲノムDNA又は増幅産物をシークエンシングする方法、特異的オリゴヌクレオチドプローブ法、オリゴヌクレオチドライゲーションアッセイ(Oligonucleotide Ligation Assay)法、PCR-SSCP法、PCR-CFLP法、PCR-PHFA法、インベーダー法、RCA(Rolling Circle Amplification)法、プライマーオリゴベースエクステンション(Primer Oligo Base Extension)法等を挙げることができる。 The method for detecting the presence or absence of mutation in the DDX41 gene using a sample containing the prepared genomic DNA is not particularly limited, but for example, a method for sequencing genomic DNA or an amplification product, specific. Oligonucleotide probe method, Oligonucleotide Ligation Assay method, PCR-SSCP method, PCR-CFLP method, PCR-PHFA method, Invader method, RCA (Rolling Circle Amplification) method, Primer Oligo Base Extension) method, etc. can be mentioned.
なお、変異の検出において使用するプライマーセット、プローブ等の各核酸材料はDNAシンセサイザーなどにより作製することができる。 Each nucleic acid material such as a primer set and a probe used for detecting a mutation can be prepared by a DNA synthesizer or the like.
また、ゲノムDNA又は増幅産物を適当な制限酵素で消化し、切断された断片のサイズの違いをサザンブロッティングなどで検出することによっても、遺伝子における変異の有無を検出することができる。 The presence or absence of mutation in the gene can also be detected by digesting the genomic DNA or the amplification product with an appropriate restriction enzyme and detecting the difference in the size of the cleaved fragments by Southern blotting or the like.
このように、被験体(ヒト生体)から分離された試料に含有されるゲノムDNAを用いて、ヒトにおけるMDS、AML等の骨髄腫瘍の発症又は発症リスクを検査するための指標を得ることができる。該指標は、具体的には、所定の変異が見出された場合に、該被験体はMDS、AML等の骨髄腫瘍が発症している、又は現時点で発症していなくても将来的に発症のリスクがあると判定するための指標である。 In this way, the genomic DNA contained in the sample isolated from the subject (human body) can be used to obtain an index for examining the onset or risk of developing bone marrow tumors such as MDS and AML in humans. .. Specifically, when a predetermined mutation is found, the index indicates that the subject has developed a bone marrow tumor such as MDS or AML, or will develop in the future even if it has not developed at present. It is an index for judging that there is a risk of.
(2) mRNA又はcDNAでの変異を検出する実施形態
被験体(ヒト生体)から分離された試料に含有されるmRNAを用いて変異を検出する場合、通常はまず、ヒト生体から分離された試料からmRNAを抽出する。抽出方法は特に限定されず公知の方法を使用することができる。
(2) Embodiment of detecting mutation in mRNA or cDNA When detecting mutation using mRNA contained in a sample isolated from a subject (human body), usually, first, a sample isolated from a human body is usually first detected. Extract the mRNA from. The extraction method is not particularly limited, and a known method can be used.
上記被験体から分離された試料は、特に限定されるものではなく、mRNAを抽出可能であり、DDX41遺伝子を発現している、または発現している可能性があるものであればよい。 The sample isolated from the subject is not particularly limited as long as it can extract mRNA and expresses or may express the DDX41 gene.
次に、抽出したmRNAから逆転写反応によってcDNAを調製する。さらに、得られたcDNAは必要に応じてゲノムDNAに関して上述したような遺伝子増幅法により増幅してもよい。 Next, cDNA is prepared from the extracted mRNA by reverse transcription reaction. Further, the obtained cDNA may be amplified by the gene amplification method as described above for genomic DNA, if necessary.
調製されたcDNAを含有する試料を用いて、DDX41遺伝子における変異の有無を検出する方法は、特に限定されるものではないが、例えば、上記ゲノムDNAを用いて遺伝子の変異を検出する場合と同様の方法を用いて、DDX41遺伝子の変異の有無を検出することができる。 The method for detecting the presence or absence of a mutation in the DDX41 gene using a sample containing the prepared cDNA is not particularly limited, but is the same as, for example, in the case of detecting a gene mutation using the above genomic DNA. The presence or absence of mutation in the DDX41 gene can be detected using the above method.
このように、被験体(ヒト生体)から分離された試料に含有されるmRNA又はcDNAを用いて、ヒトにおけるMDS、AML等の骨髄腫瘍の発症又は発症リスクを検査するための指標を得ることができる。該指標は、具体的には、所定の変異が見出された場合に、該被験体はMDS、AML等の骨髄腫瘍が発症している、又は現時点で発症していなくても将来的に発症のリスクがあると判定するための指標である。 In this way, using mRNA or cDNA contained in a sample isolated from a subject (human body), it is possible to obtain an index for examining the onset or risk of developing bone marrow tumors such as MDS and AML in humans. it can. Specifically, when a predetermined mutation is found, the index indicates that the subject has developed a bone marrow tumor such as MDS or AML, or will develop in the future even if it has not developed at present. It is an index for judging that there is a risk of.
(3) ポリペプチドでの変異を検出する実施形態
被験体(ヒト生体)から分離された試料に含有されるポリペプチド(タンパク質)を用いて変異を検出する実施形態では、まず、被験体から分離された試料からポリペプチドを抽出する。抽出方法は特に限定されず公知の方法を使用することができる。
(3) Embodiment of detecting mutation in polypeptide In embodiment of detecting mutation using a polypeptide (protein) contained in a sample separated from a subject (human body), first, separation from the subject is performed. The polypeptide is extracted from the sample. The extraction method is not particularly limited, and a known method can be used.
ヒト生体から分離された試料は、特に限定されるものではなく、ポリペプチドを抽出可能であり、DDX41遺伝子の翻訳産物(すなわちDDX41タンパク質)を発現している、または発現している可能性があるものであればよい。 The sample isolated from the human body is not particularly limited, and a polypeptide can be extracted, and a translation product of the DDX41 gene (that is, the DDX41 protein) is expressed or may be expressed. Anything is fine.
調製されたポリペプチドを含有する試料を用いて、DDX41遺伝子における変異の有無を検出する方法は、特に限定されるものではないが、例えば、DDX41遺伝子の翻訳産物であるポリペプチドについて、上記で挙げたような所定のアミノ酸変異を有するポリペプチドのみ又は所定のアミノ酸変異を有さないポリペプチドのみを特異的に認識する抗体を作製し、該抗体を用いたELISA法やウエスタンブロット法により変異を検出することができる。 The method for detecting the presence or absence of a mutation in the DDX41 gene using a sample containing the prepared polypeptide is not particularly limited, and for example, the polypeptide which is a translation product of the DDX41 gene is mentioned above. An antibody that specifically recognizes only a polypeptide having a predetermined amino acid mutation or only a polypeptide not having a predetermined amino acid mutation is prepared, and the mutation is detected by the ELISA method or Western blotting using the antibody. can do.
また、前記ポリペプチドを含有する試料から、DDX41遺伝子の翻訳産物(ポリペプチド)を単離し、直接または必要に応じ、酵素等で切断し、プロテインシークエンサーや、質量分析装置を利用して変異を検出することができる。 In addition, a translation product (polypeptide) of the DDX41 gene is isolated from the sample containing the polypeptide, cleaved directly or with an enzyme or the like as necessary, and mutations are detected using a protein sequencer or a mass spectrometer. can do.
さらに、前記ポリペプチドを含有する試料から、DDX41遺伝子の翻訳産物(ポリペプチド)を単離し、該ポリペプチドの等電点に基づいて、変異を検出することもできる。 Furthermore, a translation product (polypeptide) of the DDX41 gene can be isolated from a sample containing the polypeptide, and mutations can be detected based on the isoelectric point of the polypeptide.
このように、被験体(ヒト生体)から分離された試料に含有されるポリペプチドを用いて、ヒトにおけるMDS、AML等の骨髄腫瘍の発症又は発症リスクを検査するための指標を得ることができる。該指標は、具体的には、所定の変異が見出された場合に、該被験体はMDS、AML等の骨髄腫瘍が発症している、又は現時点で発症していなくても将来的に発症のリスクがあると判定するための指標である。 In this way, the polypeptide contained in the sample isolated from the subject (human body) can be used to obtain an index for examining the onset or risk of developing bone marrow tumors such as MDS and AML in humans. .. Specifically, when a predetermined mutation is found, the index indicates that the subject has developed a bone marrow tumor such as MDS or AML, or will develop in the future even if it has not developed at present. It is an index for judging that there is a risk of.
以下、本発明の方法についての説明に戻る。
本発明の方法は、より好ましくは、DDX41遺伝子の胚細胞変異に加えて、CUX1遺伝子の体細胞変異を検出することを更に含む。CUX1遺伝子の体細胞変異は、MDS/AMLを始めとする骨髄腫瘍において、腫瘍抑制遺伝子として、予後不良な病型において機能消失型の変異あるいはハプロ欠失を来たすことを以前に我々は報告している。そこで、被験体においてDDX41遺伝子の胚細胞変異が認められた症例において更にCUX1遺伝子の変異を検出し、CUX1遺伝子の変異が検出された場合には、該被験体での骨髄腫瘍の不良な予後を予測することができる。CUX1遺伝子の変異の位置は特に限定されないが、例えば配列番号4のアミノ酸配列での第142位、第439位、第796位、第815位及び第890位からなる群から選択される1以上のアミノ酸での変異を生じる、CUX1遺伝子の1以上の変異である。CUX1遺伝子の変異の検出は、上述のDDX41遺伝子での変異の検出方法と同様の方法で検出可能である。この場合に検出するCUX1遺伝子の変異は通常は体細胞変異である。CUX1遺伝子の変異が体細胞変異であることは、骨髄腫瘍の腫瘍組織又は腫瘍組織と疑われる組織から取得した試料において変異の存在を確認することにより判断することができ、より好ましくは、骨髄腫瘍の腫瘍組織又は腫瘍組織と疑われる組織から取得した試料において変異の存在を確認することができ、且つ、正常組織から取得した試料において変異の存在を確認することが出来ない場合に該変異が体細胞変異であると判断することができる。本発明のこの実施形態は、骨髄腫瘍を発症していることが予め確認されている被験体に対して特に有用である。
Hereinafter, the description of the method of the present invention will be returned.
The method of the present invention more preferably further comprises detecting a somatic mutation in the CUX1 gene in addition to the embryonic mutation in the DDX41 gene. We have previously reported that somatic mutations in the CUX1 gene cause loss-of-function mutations or haplo deletions in bone marrow tumors such as MDS / AML as tumor suppressor genes in poor prognosis types. There is. Therefore, in the case where the embryonic cell mutation of the DDX41 gene was found in the subject, the mutation of the CUX1 gene was further detected, and if the mutation of the CUX1 gene was detected, the poor prognosis of the bone marrow tumor in the subject was determined. Can be predicted. The position of the mutation in the CUX1 gene is not particularly limited, but for example, one or more selected from the group consisting of positions 142, 439, 796, 815 and 890 in the amino acid sequence of SEQ ID NO: 4. One or more mutations in the CUX1 gene that result in mutations in amino acids. The CUX1 gene mutation can be detected by the same method as the above-mentioned method for detecting the mutation in the DDX41 gene. The mutation in the CUX1 gene detected in this case is usually a somatic mutation. A mutation in the CUX1 gene can be determined to be a somatic mutation by confirming the presence of the mutation in a sample obtained from a tumor tissue of a bone marrow tumor or a tissue suspected to be a tumor tissue, and more preferably, a bone marrow tumor. If the presence of a mutation can be confirmed in a sample obtained from a tumor tissue or a tissue suspected to be a tumor tissue, and the presence of a mutation cannot be confirmed in a sample obtained from a normal tissue, the mutation is a somatic mutation. It can be determined that it is a cell mutation. This embodiment of the present invention is particularly useful for subjects who have been previously identified as developing bone marrow tumors.
<ヒトにおけるDDX41遺伝子の体細胞変異の存在又は将来的な発生を予測するための指標の取得方法>
本発明の他の実施形態は、被験体において、野生型DDX41遺伝子によりコードされるポリペプチドの配列番号2に示すアミノ酸配列において第500位、第259位、第363位、第364位、第3位、第7位、第35位、第187位及び第256位からなる群から選択される1以上のアミノ酸での変異を生じる、DDX41遺伝子の1以上の胚細胞変異を検出し、該変異が検出された場合に、当該被験体においてDDX41遺伝子の体細胞変異が存在する又は将来的に発生する可能性があると予測するための指標を取得する方法に関する。
<Method of obtaining an index for predicting the existence or future development of somatic mutations in the DDX41 gene in humans>
Another embodiment of the invention is in a subject at
この時、存在又は将来的な発生を予測する「DDX41遺伝子の体細胞変異」としては、野生型DDX41遺伝子によりコードされる配列番号2に示すアミノ酸配列における、第525位、第227位、第232位、第191位、第183位、第530位、第592位、第321位、第35位、第499位、第370位、第219位及び第377位からなる群から選択される1以上のアミノ酸での変異、より好ましくは第525位、第227位及び第232位からなる群から選択される1以上のアミノ酸での変異、を生じるDDX41遺伝子の体細胞変異が特に好ましい。実施例に示す本発明者らの調査では、上記のDDX41胚細胞変異のうち1つを対立遺伝子座の一方に有する、骨髄腫瘍を罹患した被験体では、高い確率で、対立遺伝子座の他方に上記のDDX41遺伝子の体細胞変異の1つを有することが明らかとなった。配列番号2に示すアミノ酸配列における第525位のアルギニンの変異としてはヒスチジンへの置換が挙げられるがこれには限定されない。配列番号2に示すアミノ酸配列における第227位のスレオニンの変異としてはメチオニン又はアラニンへの置換が挙げられるがこれには限定されない。配列番号2に示すアミノ酸配列における第232位のスレオニンの変異としてはアラニンへの置換が挙げられるがこれには限定されない。存在又は将来的な発生を予測する「DDX41遺伝子の体細胞変異」としては、第525位のアルギニンのヒスチジンへの置換を生じるDDX41遺伝子の体細胞変異が特に好ましい。このようなDDX41タンパク質のアミノ酸の変異は、MDS、AML等の骨髄腫瘍を対象とした医薬のターゲットとして有効であることから、本発明の方法により、DDX41遺伝子の体細胞変異の存在又は将来的な存在を予測することで、該被験体に対する有効な治療又は予防のための医薬の選択が支援される。 At this time, the "somatic mutations in the DDX41 gene" that predict the existence or future development include positions 525, 227, and 232 in the amino acid sequence shown in SEQ ID NO: 2 encoded by the wild-type DDX41 gene. 1 or more selected from the group consisting of 1st, 191st, 183rd, 530th, 592th, 321st, 35th, 499th, 370th, 219th and 377th Somatic mutations in the DDX41 gene that result in mutations in the amino acids, more preferably mutations in one or more amino acids selected from the group consisting of positions 525, 227 and 232, are particularly preferred. In our study shown in the Examples, subjects with bone marrow tumors having one of the above DDX41 embryonic mutations in one of the allelic loci have a high probability of being in the other of the allelic loci. It was revealed that it has one of the somatic mutations of the above DDX41 gene. The mutation of arginine at position 525 in the amino acid sequence shown in SEQ ID NO: 2 includes, but is not limited to, substitution with histidine. The mutation of threonine at position 227 in the amino acid sequence shown in SEQ ID NO: 2 includes, but is not limited to, substitution with methionine or alanine. The mutation of threonine at position 232 in the amino acid sequence shown in SEQ ID NO: 2 includes, but is not limited to, substitution with alanine. As a "somatic mutation of the DDX41 gene" that predicts its existence or future development, a somatic mutation of the DDX41 gene that results in the substitution of arginine at position 525 with histidine is particularly preferable. Since such amino acid mutations in the DDX41 protein are effective as pharmaceutical targets for bone marrow tumors such as MDS and AML, the presence or future of somatic mutations in the DDX41 gene can be achieved by the method of the present invention. Predicting its presence aids in the selection of drugs for effective treatment or prevention of the subject.
<キット>
本発明のキットは、上記で説明した、ヒトにおけるMDS、AML等の骨髄腫瘍の発症又は発症リスクを検査する方法、並びに、ヒトにおけるDDX41遺伝子の体細胞変異の存在又は将来的な発生を予測する方法のうち少なくとも1つの方法に用いるキットである。
<Kit>
The kit of the present invention predicts the method for examining the onset or risk of developing bone marrow tumors such as MDS and AML in humans as described above, and the presence or future occurrence of somatic mutations in the DDX41 gene in humans. A kit used for at least one of the methods.
前記キットは、下記のプライマーセット、プローブ及び抗体からなる群から選択される1以上を備える。
前記キットに含まれるプライマーセットは、DDX41遺伝子のうち、それが変異した場合に、野生型DDX41遺伝子によりコードされるポリペプチドの配列番号2に示すアミノ酸配列において第500位、第259位、第363位、第364位、第3位、第7位、第35位、第187位及び第256位からなる群から選択される1以上のアミノ酸での変異を生じる塩基を1以上含む部位を特異的に増幅できるように設計されたプライマーセットである。
The kit comprises one or more selected from the group consisting of the following primer sets, probes and antibodies.
The primer set included in the kit is the 500th, 259th, and 363rd positions in the amino acid sequence shown in SEQ ID NO: 2 of the polypeptide encoded by the wild-type DDX41 gene when it is mutated among the DDX41 genes. Specific sites containing one or more bases that mutate at one or more amino acids selected from the group consisting of positions, 364, 3, 7, 7, 35, 187, and 256. It is a primer set designed so that it can be amplified.
DDX41遺伝子における前記塩基としては、配列番号1に示す野生型DDX41のcDNA塩基配列における位置として、
第1495位のシトシン及び第1496位のシトシンのうち一方又は両方の塩基、
第776位のアデニン、
第1088位のシトシン、第1089位のシトシン及び第1090位のチミンのうち1〜3個の塩基、又は、第1087位のチミン、第1088位のシトシン及び第1089位のシトシンのうち1〜3個の塩基、
第7位のグアニン、
第19位のグアニン、
第104位のシトシン、
第560位のアデニン、及び
第766位のグアニンからなる群から選択される少なくも1つの塩基に対応する位置にある塩基が特に好ましい。
The base in the DDX41 gene is the position in the cDNA base sequence of wild-type DDX41 shown in SEQ ID NO: 1.
One or both bases of cytosine at position 1495 and cytosine at position 1496,
776th place adenine,
1-3 bases of cytosine at position 1088, cytosine at position 1089 and thymine at position 1090, or thymine at position 1087, cytosine at position 1088 and cytosine at position 1089 1-3 Bases,
7th place guanine,
19th place guanine,
104th place cytosine,
A base at a position corresponding to at least one base selected from the group consisting of adenine at position 560 and guanine at position 766 is particularly preferred.
前記プライマーセットにおける各プライマーは、典型的には、塩基数が10以上、好ましくは15以上、50以下、好ましくは30以下のDNAを含み、必要に応じて増幅、検出、標識、固定化等の各種目的のためのDNA領域や、標識分子等が連結されたものであってもよい。 Each primer in the primer set typically contains DNA having 10 or more bases, preferably 15 or more, 50 or less, preferably 30 or less, and is amplified, detected, labeled, immobilized, etc. as necessary. A DNA region for various purposes, a labeled molecule, or the like may be linked.
前記プライマーセットは、DDX41遺伝子が前記塩基に関して野生型である場合と変異型である場合との両方において前記塩基を含む部位を増幅可能なように設計されていてもよいし、DDX41遺伝子が前記塩基に関して変異型である場合にのみ前記塩基を含む部位を増幅可能なように設計されていてもよいし、DDX41遺伝子が前記塩基に関して野生型である場合にのみ前記塩基を含む部位を増幅可能なように設計されていてもよい。 The primer set may be designed so that the site containing the base can be amplified in both the wild type and the mutant type of the DDX41 gene, and the DDX41 gene may be designed to amplify the base. It may be designed so that the site containing the base can be amplified only when it is a variant with respect to the base, or the site containing the base can be amplified only when the DDX41 gene is a wild type with respect to the base. It may be designed to.
前記プライマーセットを用いて増幅反応を行う場合の鋳型としてはDDX41遺伝子を含むゲノムDNA、mRNAから調製されたcDNA、これらの断片等を用いることができる。 As a template for performing an amplification reaction using the primer set, genomic DNA containing the DDX41 gene, cDNA prepared from mRNA, fragments thereof, or the like can be used.
前記プライマーセットを含む本発明のキットは、核酸増幅反応に必要な他の成分や、核酸シークエンシングに必要な他の成分を含むことができ、下記のプローブを含んでもよい。 The kit of the present invention containing the primer set can contain other components required for nucleic acid amplification reaction and other components required for nucleic acid sequencing, and may include the following probes.
前記キットに含まれるプローブは、DDX41遺伝子のうち、変異した場合に、野生型DDX41遺伝子によりコードされるポリペプチドの配列番号2に示すアミノ酸配列において第500位、第259位、第363位、第364位、第3位、第7位、第35位、第187位及び第256位からなる群から選択される1以上のアミノ酸での変異を生じる塩基を1以上含む部位と特異的に結合できるように設計されたプローブである。
The probe included in the kit is located at positions 500, 259, 363, and 363 of the amino acid sequence shown in SEQ ID NO: 2 of the polypeptide encoded by the wild-type DDX41 gene when mutated among the DDX41 genes. It can specifically bind to a site containing one or more bases that mutate with one or more amino acids selected from the group consisting of
DDX41遺伝子における前記塩基としては、配列番号1に示す野生型DDX41のcDNA塩基配列における位置として、
第1495位のシトシン及び第1496位のシトシンのうち一方又は両方の塩基、
第776位のアデニン、
第1088位のシトシン、第1089位のシトシン及び第1090位のチミンのうち1〜3個の塩基、又は、第1087位のチミン、第1088位のシトシン及び第1089位のシトシンのうち1〜3個の塩基、
第7位のグアニン、
第19位のグアニン、
第104位のシトシン、
第560位のアデニン、及び
第766位のグアニンからなる群から選択される少なくも1つの塩基に対応する位置にある塩基が特に好ましい。
The base in the DDX41 gene is the position in the cDNA base sequence of wild-type DDX41 shown in SEQ ID NO: 1.
One or both bases of cytosine at position 1495 and cytosine at position 1496,
776th place adenine,
1-3 bases of cytosine at position 1088, cytosine at position 1089 and thymine at position 1090, or thymine at position 1087, cytosine at position 1088 and cytosine at position 1089 1-3 Bases,
7th place guanine,
19th place guanine,
104th place cytosine,
A base at a position corresponding to at least one base selected from the group consisting of adenine at position 560 and guanine at position 766 is particularly preferred.
前記プローブは、典型的には、塩基数が10以上、好ましくは15以上、50以下、好ましくは40以下、より好ましくは30以下のDNAを含み、必要に応じて増幅、検出、標識、固定化等の各種目的のためのDNA領域や、標識分子等が連結されたものであってもよい。前記プローブはまた固相担体上に固定化されていてもよい。 The probe typically contains DNA having 10 or more bases, preferably 15 or more, 50 or less, preferably 40 or less, more preferably 30 or less, and is amplified, detected, labeled, and immobilized as needed. A DNA region for various purposes such as, or a labeled molecule or the like may be linked. The probe may also be immobilized on a solid phase carrier.
前記プローブは、DDX41遺伝子が前記塩基に関して野生型である場合と変異型である場合との両方において前記塩基を含む部位と結合可能なように設計されていてもよいし、DDX41遺伝子が前記塩基に関して変異型である場合にのみ前記塩基を含む部位と結合可能なように設計されていてもよいし、DDX41遺伝子が前記塩基に関して野生型である場合にのみ前記塩基を含む部位と結合可能なように設計されていてもよい。 The probe may be designed to be capable of binding to a site containing the base in both wild-type and mutant forms of the DDX41 gene with respect to the base. It may be designed so that it can bind to the site containing the base only when it is a mutant type, or it can bind to the site containing the base only when the DDX41 gene is a wild type with respect to the base. It may be designed.
前記プローブが結合するDDX41遺伝子としては、ゲノムDNA、mRNA、cDNA、これらの断片等を用いることができ、ゲノムDNA及びcDNAとは適宜一本鎖化された状態で前記プローブとの結合に用いることができる。 As the DDX41 gene to which the probe binds, genomic DNA, mRNA, cDNA, fragments thereof and the like can be used, and the genomic DNA and cDNA can be used for binding to the probe in an appropriately single-strand state. Can be done.
前記プローブを含む本発明のキットは、プローブとDDX41遺伝子との結合体の検出に必要な他の成分を含むことができる。該キットは前記プライマーセットと前記プローブとを組み合わせて含むことができる。 The kit of the present invention containing the probe can contain other components necessary for detecting a conjugate of the probe and the DDX41 gene. The kit can include the primer set and the probe in combination.
前記抗体は、DDX41遺伝子による翻訳産物であるポリペプチドのうち、配列番号2に示す野生型のアミノ酸配列において第500位、第259位、第363位、第364位、第3位、第7位、第35位、第187位及び第256位からなる群から選択される1以上のアミノ酸に対応するアミノ酸を含む部位を特異的に認識するする抗体である。
The antibody is located at
前記抗体は、必要に応じて検出、標識、固定化等の各種目的のためのタグ部分や、標識分子等が連結されたものであってもよい。前記抗体はまた固相担体上に固定化されていてもよい。 If necessary, the antibody may have a tag portion for various purposes such as detection, labeling, and immobilization, or a labeled molecule or the like linked thereto. The antibody may also be immobilized on a solid phase carrier.
前記抗体は、前記ポリペプチドにおいて、前記アミノ酸が変異型である場合にのみ前記アミノ酸を含む部位を認識可能なように設計されていてもよいし、前記アミノ酸が野生型である場合にのみ前記アミノ酸を含む部位を認識可能なように設計されていてもよい。 The antibody may be designed so that a site containing the amino acid can be recognized only when the amino acid is a mutant type in the polypeptide, and the amino acid may be recognized only when the amino acid is a wild type. It may be designed so that the site containing the above can be recognized.
前記ポリペプチドにおいて前記アミノ酸の変異型としては、配列番号2に示す野生型アミノ酸配列における、第500位のアラニンのフレームシフト変異、第259位のチロシンのシステインへの置換、第363位のセリン及び第364位のチロシンの、1つのチロシンへの置換(或いは第363位のセリンの欠失)、第3位のグルタミン酸のリジンへの置換、第7位のグルタミン酸のナンセンス変異、第35位のプロリンのアルギニンへの置換、第187位のリジンのアルギニンへの置換、及び、第256位のグルタミン酸のリジンへの置換からなる群から選択される1以上の変異型の場合が挙げられる。
Variants of the amino acid in the polypeptide include a frame-shifted mutation of arginine at position 500, substitution of tyrosine at position 259 with cysteine, serine at position 363 and the wild amino acid sequence shown in SEQ ID NO: 2. Substitution of tyrosine at
前記抗体を含む本発明のキットは、ELISA法、ウエスタンブロット法等の検出法に必要な成分を含むことができる。 The kit of the present invention containing the antibody can contain components necessary for a detection method such as an ELISA method and a Western blotting method.
本発明のキットは、CUX1遺伝子の変異を検出するための試薬を更に含むことが好ましい。CUX1遺伝子の変異としては、CUX1遺伝子がコードするポリペプチドのアミノ酸配列に変異を生じる変異であることが好ましく、CUX1遺伝子の変異の位置は特に限定されないが、例えば配列番号4のアミノ酸配列での第142位、第439位、第796位、第815位及び第890位からなる群から選択される1以上のアミノ酸での変異を生じるCUX1遺伝子の変異である。 The kit of the present invention preferably further contains a reagent for detecting a mutation in the CUX1 gene. The mutation of the CUX1 gene is preferably a mutation that causes a mutation in the amino acid sequence of the polypeptide encoded by the CUX1 gene, and the position of the mutation of the CUX1 gene is not particularly limited. For example, the mutation in the amino acid sequence of SEQ ID NO: 4 is the first. A mutation in the CUX1 gene that causes a mutation in one or more amino acids selected from the group consisting of positions 142, 439, 796, 815 and 890.
CUX1遺伝子の変異を検出するための試薬としては、CUX1遺伝子のうち上記変異を生じる塩基を1以上含む部位を特異的に増幅できるように設計されたプライマーセットや、CUX1遺伝子のうち上記変異を生じる塩基を1以上含む部位に特異的に結合できるように設計されたプローブや、CUX1遺伝子による翻訳産物であるポリペプチドのうち変異を生じ得るアミノ酸に対応するアミノ酸を含む部位を認識するする抗体が挙げられる。 As a reagent for detecting a mutation in the CUX1 gene, a primer set designed to specifically amplify a site containing one or more bases that cause the above mutation in the CUX1 gene, or a primer set designed to specifically amplify the above-mentioned mutation in the CUX1 gene is generated. Examples include probes designed to specifically bind to sites containing one or more bases, and antibodies that recognize sites containing amino acids that correspond to amino acids that can cause mutations in polypeptides that are translation products of the CUX1 gene. Be done.
<ヒトにおける骨髄腫瘍の発症又は発症リスクを検査する方法>
本発明の他の実施形態は、
ヒトにおける骨髄腫瘍の発症又は発症リスクを検査する方法であって、
野生型DDX41遺伝子によりコードされるポリペプチドの配列番号2に示すアミノ酸配列において第500位、第259位、第363位、第364位、第3位、第7位、第35位、第187位及び第256位からなる群から選択される1以上のアミノ酸での変異を生じるDDX41遺伝子の1以上の胚細胞変異を検出することを特徴とする方法
に関する。
<Method of testing the onset or risk of developing bone marrow tumor in humans>
Other embodiments of the present invention
A method of examining the onset or risk of developing bone marrow tumors in humans.
At position 500, position 259, position 363,
この実施形態における、各アミノ酸及び塩基の変異、検出方法、好ましい実施形態等については、<ヒトにおける骨髄腫瘍の発症又は発症リスクを検査するための指標の取得方法>の欄で説明したのと同様である。 Mutations of each amino acid and base, a detection method, a preferred embodiment, and the like in this embodiment are the same as those described in the column of <Method for obtaining an index for testing the onset or risk of developing bone marrow tumor in humans>. Is.
<ヒトにおけるDDX41遺伝子の体細胞変異の存在又は将来的な発生を予測する方法>
本発明の他の実施形態は、
ヒトにおけるDDX41遺伝子の体細胞変異の存在又は将来的な発生を予測する方法であって、
野生型DDX41遺伝子によりコードされるポリペプチドの配列番号2に示すアミノ酸配列において第500位、第259位、第363位、第364位、第3位、第7位、第35位、第187位及び第256位からなる群から選択される1以上のアミノ酸での変異を生じるDDX41遺伝子の1以上の胚細胞変異を検出することを特徴とする方法
に関する。
<Method of predicting the presence or future development of somatic mutations in the DDX41 gene in humans>
Other embodiments of the present invention
A method for predicting the presence or future development of somatic mutations in the DDX41 gene in humans.
At position 500, position 259, position 363,
この実施形態における、各アミノ酸及び塩基の変異、検出方法、好ましい実施形態等については、<ヒトにおける骨髄腫瘍の発症又は発症リスクを検査するための指標の取得方法>及び<ヒトにおけるDDX41遺伝子の体細胞変異の存在又は将来的な発生を予測するための指標の取得方法>の欄で説明したのと同様である。 For mutations of each amino acid and base, detection method, preferred embodiment, etc. in this embodiment, <method for obtaining an index for examining the onset or risk of developing bone marrow tumor in humans> and <body of DDX41 gene in humans>. It is the same as described in the column of> Method for obtaining an index for predicting the existence or future development of a cell mutation.
本発明について理解を深めるために、以下に本発明を実施例に示してより具体的に説明するが、本発明はこれら実施例に限定されるものではないことはいうまでもない。 In order to deepen the understanding of the present invention, the present invention will be described below with reference to Examples, but it goes without saying that the present invention is not limited to these Examples.
<骨髄異形成症候群(myelodysplastic syndromes; MDS)、急性骨髄性白血病(acute myeloid leukemia; AML)における遺伝子変異の同定>
本実施例では、MDSあるいはAMLと診断された患者であり、インフォームドコンセントが得られた患者について、京都大学の倫理委員会によって承認されたプロトコルに従って、本発明のための検体を採取し、網羅的な遺伝子変異解析を行った。調査した上記患者は全て東アジア人種の日本人であった。
<Identification of gene mutations in myelodysplastic syndromes (MDS) and acute myeloid leukemia (AML)>
In this example, for patients diagnosed with MDS or AML and for whom informed consent was obtained, a sample for the present invention was collected and covered according to a protocol approved by the Ethics Committee of Kyoto University. Genetic mutation analysis was performed. The above patients investigated were all Japanese of East Asian race.
本実施例では、1070例のMDSあるいはAMLの患者から採取した正常組織由来の検体及び腫瘍組織由来の検体を用いて、標的ディープシーケンス解析を行い、DDX41およびその他のMDS/AMLの発症に重要な遺伝子の変異解析を実施した。以上により、DDX41の胚細胞性および体細胞遺伝子異常を解明することを試みた。 In this example, targeted deep sequence analysis was performed using normal tissue-derived specimens and tumor tissue-derived specimens collected from 1070 MDS or AML patients, which are important for the development of DDX41 and other MDS / AML. A gene mutation analysis was performed. Based on the above, we attempted to elucidate the embryonic and somatic gene abnormalities of DDX41.
(1)標的ディープシーケンス解析による変異遺伝子の同定
まず、1070例のMDSとAML患者の正常組織および腫瘍組織由来の検体を対象とし、DNAについて標的ディープシーケンス解析を行った。ゲノム領域のうち、DDX41タンパク質をコードするエクソン領域を、SureSelect Target Enrichment(アジレント・テクノロジー株式会社)を用いて濃縮し、HiSeq2000(Illumina 社)を用いて塩基配列を決定した。胚細胞変異は正常組織由来DNA及び腫瘍組織由来DNAの両方に含まれるのに対して、体細胞変異は腫瘍組織由来DNAのみに含まれることから、腫瘍組織由来のDNAの塩基配列と正常組織由来のDNAの塩基配列を比較することにより、遺伝子の胚細胞性変異と体細胞変異を確認した。野生型DDX41ゲノムDNAにおける、DDX41タンパク質をコードするエクソン領域の塩基配列(GenBank Accession No. NM_016222)、すなわちcDNA配列を配列番号1に示し、配列番号1のcDNA塩基配列がコードするDDX41タンパク質のアミノ酸配列を配列番号2に示す。
(1) Identification of Mutant Genes by Targeted Deep Sequence Analysis First, targeted deep sequence analysis of DNA was performed on samples derived from normal tissues and tumor tissues of 1070 MDS and AML patients. Among the genomic regions, the exon region encoding the DDX41 protein was concentrated using SureSelect Target Enrichment (Agilent Technologies, Inc.) and sequenced using HiSeq2000 (Illumina). Since embryonic cell mutations are contained in both normal tissue-derived DNA and tumor tissue-derived DNA, somatic cell mutations are contained only in tumor tissue-derived DNA, so that the base sequence of the tumor tissue-derived DNA and the normal tissue-derived DNA are derived. By comparing the base sequences of the DNAs of the genes, embryonic mutations and somatic mutations of the genes were confirmed. The base sequence of the exon region encoding the DDX41 protein (GenBank Accession No. NM_016222) in the wild-type DDX41 genomic DNA, that is, the cDNA sequence is shown in SEQ ID NO: 1, and the amino acid sequence of the DDX41 protein encoded by the cDNA base sequence of SEQ ID NO: 1. Is shown in SEQ ID NO: 2.
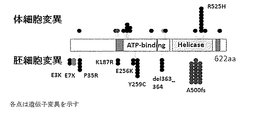
DDX41遺伝子についての標的ディープシーケンス解析の結果を下記表及び図1に示す。本実施例では、胚細胞遺伝子変異に関しては、2人以上の患者に由来する検体において検出された変異のみを胚細胞遺伝子変異として扱った。 The results of the targeted deep sequence analysis for the DDX41 gene are shown in the table below and FIG. In this example, regarding embryo cell gene mutations, only mutations detected in specimens derived from two or more patients were treated as embryo cell gene mutations.
標的ディープシーケンス解析により、我々は1070例の孤発性のMDS/AMLにおいて、44個(約4%)の胚細胞性遺伝子変異、23個(約2%)の体細胞変異を検出した。図2の「東アジア人種」のデータが上記試験からのデータであり、比較のために示す「コーカサス人種」のデータはPolprasert et al., 2015, Cancer Cell 27, 658-670に報告されたものである。 By targeted deep sequence analysis, we detected 44 (about 4%) embryonic gene mutations and 23 (about 2%) somatic mutations in 1070 sporadic MDS / AML. The data for "East Asian race" in Figure 2 is from the above study, and the data for "Caucasus race" shown for comparison is reported in Polprasert et al., 2015, Cancer Cell 27, 658-670. It is a thing.
(2)標的シーケンス解析による胚細胞変異と体細胞変異の合併頻度の同定および変異パターンの解析
我々のコホートの検索により、胚細胞遺伝子変異及び体細胞遺伝子変異の一方又は両方が認められた44例のうち、およそ50%の症例において、DDX41の胚細胞変異と体細胞変異が同時に認められた(図2「東アジア人種」)。DDX41の胚細胞変異陰性症例には、DDX41の体細胞変異がほとんど見つからず、DDX41の胚細胞変異と体細胞変異とは有意に対立遺伝子座に起こることを、サブクローニングの手法で明らかにした。また今回の調査の範囲では、DDX41胚細胞変異陽性患者はいずれも、1つのDDX41胚細胞変異のみを有しており、且つ、該変異を対立遺伝子座の一方のみに有していることがサブクローニングの手法で明らかとなった。以上からMDS/AMLの発症に関するDDX41の変異形式は2ヒット理論(同じ遺伝子起こる2回の変異が病因となる)によって説明される。
(2) Identification of mutation frequency of embryonic cell mutation and somatic mutation and analysis of mutation pattern by target sequence analysis 44 cases in which one or both of embryonic cell gene mutation and somatic gene mutation were found by searching our cohort. Of these, approximately 50% of cases had DDX41 embryonic and somatic mutations simultaneously (Fig. 2, “East Asian race”). It was clarified by a subcloning method that almost no somatic mutations in DDX41 were found in DDX41 embryonic mutation-negative cases, and that DDX41 embryonic mutations and somatic mutations significantly occur at allelic loci. In addition, within the scope of this study, it is subcloning that all DDX41 embryo cell mutation-positive patients have only one DDX41 embryo cell mutation and that mutation is present in only one of the allelic loci. It became clear by the method of. From the above, the mutation form of DDX41 regarding the onset of MDS / AML is explained by the two-hit theory (two mutations in the same gene are the cause).
図1に示す通り、DDX41遺伝子の標的ディープシーケンス解析の結果、少なくとも複数回認められた頻度の高いDDX41の胚細胞変異として、ホットスポットフレームシフト変異A500fs(22例)(計2.2%)、ホットスポットミスセンス変異Y259C(6例)、E256K(2例)、K187R(2例)、P35R(4例)、E3K(2例)(計2%)、インフレーム欠失変異363_364del(4例)(計0.4%)、ナンセンス変異E7X(2例)(計0.2%)を認めた。 As shown in FIG. 1, as a result of targeted deep sequence analysis of the DDX41 gene, hotspot frameshift mutation A500fs (22 cases) (2.2% in total) and hotspot were frequently observed as embryonic cell mutations of DDX41 at least multiple times. Missense mutation Y259C (6 cases), E256K (2 cases), K187R (2 cases), P35R (4 cases), E3K (2 cases) (2% total), inframe deletion mutation 363_364del (4 cases) (0.4 cases total) %) And nonsense mutation E7X (2 cases) (0.2% in total) were observed.
DDX41の体細胞変異としては、ホットスポットミスセンス変異R525H(8例)を始め、T227A/M(計3例)、T232A(2例)、A191fs、F183S、G530D、I592F、P321L、P35R、P499S、Q370X、R219H、T377N(それぞれ1例ずつ)を認めた。これらの変異のうち複数の症例において変異が認められたR525H、T232A、T227A/Mについて塩基の変異とアミノ酸の変異との対応関係を次表に示す。 DDX41 somatic mutations include hotspot missense mutation R525H (8 cases), T227A / M (3 cases in total), T232A (2 cases), A191fs, F183S, G530D, I592F, P321L, P35R, P499S, Q370X. , R219H, T377N (1 case each). The following table shows the correspondence between base mutations and amino acid mutations for R525H, T232A, and T227A / M in which mutations were found in multiple cases among these mutations.
これらの体細胞変異は、高頻度に胚細胞変異陽性例に合併して認められ(図2)、2ヒットの変異形式を呈していた。以上から、MDS/AMLにおいて、DDX41の胚細胞変異のみならず体細胞変異を検索することは、より詳細な病態を明らかにするのに有用である。また、DDX41の胚細胞変異の存在を指標として、DDX41タンパク質のR525H変異等の体細胞変異の存在又は将来的な発生を予測することができる。 These somatic mutations were frequently observed in patients with positive embryonic cell mutations (Fig. 2), and exhibited a 2-hit mutation form. From the above, in MDS / AML, searching for somatic mutations as well as embryonic mutations in DDX41 is useful for clarifying more detailed pathological conditions. In addition, the presence or future development of somatic mutations such as the R525H mutation of the DDX41 protein can be predicted using the presence of embryonic cell mutations in DDX41 as an index.
MDS/AML症例全体(1070)についてDDX41以外の遺伝子に関しても標的ディープシーケンスにて体細胞変異を検索すると、DDX41変異がある症例(44)において、有意に高頻度にCUX1体細胞変異の合併を認めた(図3)。野生型CUX1ゲノムDNAにおける、CUX1タンパク質をコードするエクソン領域の塩基配列(GenBank Accession No. NM_001202543)、すなわちcDNA配列を配列番号3に示し、配列番号3のcDNA塩基配列がコードするCUX1タンパク質のアミノ酸配列を配列番号4に示す。DDX41変異がある症例(44)において確認されたCUX1遺伝子の体細胞変異を下記表にまとめた。 Searching for somatic mutations in the target deep sequence for genes other than DDX41 for all MDS / AML cases (1070) revealed a significantly higher frequency of CUX1 somatic mutations in cases with DDX41 mutations (44). (Fig. 3). The base sequence of the exon region encoding the CUX1 protein (GenBank Accession No. NM_001202543) in the wild-type CUX1 genomic DNA, that is, the cDNA sequence is shown in SEQ ID NO: 3, and the amino acid sequence of the CUX1 protein encoded by the cDNA base sequence of SEQ ID NO: 3. Is shown in SEQ ID NO: 4. The somatic mutations of the CUX1 gene confirmed in the case with DDX41 mutation (44) are summarized in the table below.
CUX1は、MDS/AMLを始めとする骨髄腫瘍において、腫瘍抑制遺伝子として、予後不良な病型において機能消失型の変異あるいはハプロ欠失を来たすことを以前に我々は報告している。したがって、DDX41変異が認められた症例では、CUX1の変異が起きているか確認することで、不良な予後を予測できる。 We have previously reported that CUX1 causes a loss-of-function mutation or haplo deletion in myelodysplastic tumors such as MDS / AML as a tumor suppressor gene in a disease type with a poor prognosis. Therefore, in cases where DDX41 mutation is observed, poor prognosis can be predicted by confirming whether CUX1 mutation has occurred.
実際、MDS/AML症例全体に関して病型毎に変異頻度を解析した結果、骨髄芽球(幼若な骨髄系細胞)が骨髄で5%を超える進行型の病型を呈する症例では、より高頻度にDDX41胚細胞または体細胞変異を認めた(図4)。この結果は、DDX41変異を検索することがMDS/AMLの病型の鑑別および予後予測に有用である可能性を示唆している。なお、症例によって高リスク型か低リスク型かを評価できないものがあり、図4ではリスクを評価できた症例のみについてDDX41変異陽性患者の割合を示す。 In fact, as a result of analyzing the mutation frequency for each disease type in all MDS / AML cases, the frequency is higher in cases where myeloblasts (juvenile myeloid cells) exhibit a progressive disease type of more than 5% in the bone marrow. DDX41 embryonic cells or somatic mutations were found in (Fig. 4). This result suggests that searching for the DDX41 mutation may be useful for differentiating the type of MDS / AML and predicting the prognosis. Depending on the case, it is not possible to evaluate whether it is a high-risk type or a low-risk type, and Fig. 4 shows the proportion of DDX41 mutation-positive patients only in the cases for which the risk could be evaluated.
(3)DDX41の胚細胞変異の濃縮率と地域差の解析
図1に示した全てのDDX41胚細胞変異A500fs、Y259C、E256K、K187R、P35R、E3K、del363_364、E7Xに関して一般健常者における頻度を確認した。一般健常者でのDDX41遺伝子の変異の有無はthe Exome Aggregation Consortium (ExAC) データベース(Broad Institute)(URL: http://exac.broadinstitute.org)を用いて推定した(コーカサス人種: n=33,362 , 東アジア人種: n=4,327)。東アジア人種4327人中、A500fs(1例)、Y259C(3例)、K187R(3例)の変異は検出されたが、E256K、P35R、E3K、del363_364、E7Xは認められないほど稀であった。
(3) Analysis of DDX41 embryo cell mutation enrichment rate and regional differences Confirm the frequency of all DDX41 embryo cell mutations A500fs, Y259C, E256K, K187R, P35R, E3K, del363_364, and E7X shown in Fig. 1 in healthy subjects. did. The presence or absence of mutations in the DDX41 gene in healthy individuals was estimated using the Exome Aggregation Consortium (ExAC) database (Broad Institute) (URL: http://exac.broadinstitute.org) (Caucasus race: n = 33,362). , East Asian Race: n = 4,327). Mutations in A500fs (1 case), Y259C (3 cases), and K187R (3 cases) were detected in 4327 East Asians, but E256K, P35R, E3K, del363_364, and E7X were rarely observed. It was.
図5に、上記研究で求めた東アジア人種でのMDS/AML症例1070例での各DDX41胚細胞変異及びD140のフレームシフト変異が認められた例数と、Polprasert et al., 2015, Cancer Cell 27, 658-670にて報告されているコーカサス人種でのMDS/AML症例1045例での上記各DDX41胚細胞変異及びD140のフレームシフト変異が認められた例数と、上記データベースからのコーカサス人種及び東アジア人種での各DDX41胚細胞変異の例数とをそれぞれ示す。 Figure 5 shows the number of cases in which each DDX41 embryo cell mutation and D140 frame-shift mutation were observed in 1070 MDS / AML cases of the East Asian race determined in the above study, and Polprasert et al., 2015, Cancer. The number of cases in which each of the above DDX41 embryo cell mutations and D140 frame-shift mutations was observed in 1045 MDS / AML cases of the Caucasian race reported in Cell 27, 658-670, and Caucasian from the above database. The number of cases of each DDX41 embryo cell mutation in each race and East Asian race is shown.
健常人に対するMDS/AMLにおける、DDX41の胚細胞変異の濃縮度を評価する目的でオッズ比を求めると、それぞれA500fs(オッズ比=91; 95%信頼区間=15-3746 (p<0.0001))、Y259C(オッズ比=8.0; 95%信頼区間=1.7-50 (p=0.0004))、E256K(オッズ比=20; 95%信頼区間=0.97-422 (p=0.004))(*)、K187R(オッズ比=2.7; 95%信頼区間=0.23-24 (p=0.26))、P35R(オッズ比=36.5; 95%信頼区間=2.0-679 (p<0.0001))(*)、E3K(オッズ比=20; 95%信頼区間=0.97-422 (p=0.004))(*)、363_364del(オッズ比=36.5; 95%信頼区間=2.0-679 (p<0.0001))(*)、E7X(オッズ比=20; 95%信頼区間=0.97-422 (p=0.004))(*)であった(図5)。(*)はWoolf-Haldane補正を行った変異を指す。東アジア人種において確認されたこれらのDDX41胚細胞変異のオッズ比は、東アジア人種における、健常人に対するMDS/AML症例での各変異のオッズ比である。一方、コーカサス人種において確認されたDDX41胚細胞変異D140fsについて、コーカサス人種における、健常人に対するMDS/AML症例でのオッズ比を求めたところ、オッズ比=19, 95%信頼区間=5.8-59 (<p=0.001)であった(図5)。 The odds ratios for the purpose of evaluating the enrichment of embryonic cell mutations in DDX41 in MDS / AML for healthy individuals were A500fs (odds ratio = 91; 95% confidence interval = 15-3746 (p <0.0001)), respectively. Y259C (odds ratio = 8.0; 95% confidence interval = 1.7-50 (p = 0.0004)), E256K (odds ratio = 20; 95% confidence interval = 0.97-422 (p = 0.004)) (*), K187R (odds) Ratio = 2.7; 95% confidence interval = 0.23-24 (p = 0.26)), P35R (odds ratio = 36.5; 95% confidence interval = 2.0-679 (p <0.0001)) (*), E3K (odds ratio = 20) 95% confidence interval = 0.97-422 (p = 0.004)) (*), 363_364del (odds ratio = 36.5; 95% confidence interval = 2.0-679 (p <0.0001)) (*), E7X (odds ratio = 20) The 95% confidence interval was 0.97-422 (p = 0.004)) (*) (Fig. 5). (*) Refers to mutations with Woolf-Haldane correction. The odds ratios for these DDX41 embryonic mutations identified in East Asians are the odds ratios for each mutation in MDS / AML cases to healthy individuals in East Asians. On the other hand, for the DDX41 embryonic cell mutation D140fs confirmed in the Caucasian race, the odds ratio in MDS / AML cases to healthy subjects in the Caucasian race was calculated. The odds ratio = 19, 95% confidence interval = 5.8-59. It was (<p = 0.001) (Fig. 5).
全てのDDX41胚細胞変異A500fs、Y259C、E256K、K187R、P35R、E3K、del363_364、E7Xをまとめて計算すると、東アジア人種における、健常人に対するMDS/AML症例でのDDX41胚細胞変異を有するオッズ比は15; 95%信頼区間=2.3-961(p=0.0001)であった。DDX41の胚細胞変異は、全体として有意にMDS/AMLで濃縮していた。 All DDX41 embryonic mutations A500fs, Y259C, E256K, K187R, P35R, E3K, del363_364, E7X are calculated together to show the odds ratio of having DDX41 embryonic mutations in MDS / AML cases to healthy individuals in East Asian races. Was 15; 95% confidence interval = 2.3-961 (p = 0.0001). Embryonic cell mutations in DDX41 were significantly enriched in MDS / AML overall.
さらに、コーカサス人種33362人の検討により、E256K(1例)、E3K(2例)は認められたが、A500fs、Y259C、del363_364、E7X、K187R、P35Rは認められず、東アジア人種と分布は異なっていた。 Furthermore, in a study of 33362 Caucasian races, E256K (1 case) and E3K (2 cases) were found, but A500fs, Y259C, del363_364, E7X, K187R, P35R were not found, and distribution with East Asian races. Was different.
以上より、A500fs、Y259Cは東アジア人種に固有な変異であり、E256KとE3Kはより広い地域に分布する、コーカサス・アジア人種を含む全世界的に分布する胚細胞変異であることが確認された(図6)。 From the above, it was confirmed that A500fs and Y259C are mutations endemic to East Asian races, and E256K and E3K are embryonic cell mutations that are distributed over a wider area and are distributed worldwide including the Caucasus Asian races. Was done (Fig. 6).
これらの結果は、日本のみならず、地球上のどの地域でDDX41のシークエンスを行うかによって、異なる変異が予想されることを示している。東アジアで変異を調べる際には、A500fs、Y259Cを優先的に、続いてその他の変異を調べることが推奨される。 These results indicate that different mutations are expected depending on which region of the globe the DDX41 is sequenced, not just in Japan. When investigating mutations in East Asia, it is recommended to prioritize A500fs and Y259C, followed by other mutations.
(4)DDX41の胚細胞変異の臨床的意義
Polprasert et al., 2015, Cancer Cell 27, 658-670の報告によれば、DDX41の胚細胞変異は常染色体優性遺伝形式で発症するため、50%の確率で子供に遺伝し白血病の原因となる。したがって、家族性の高齢発症MDS/AML家系を認めた場合には、DDX41の胚細胞変異が原因である可能性がある。したがって、DDX41遺伝子をシークエンスし、変異の有無を確認すべきである。
(4) Clinical significance of embryonic cell mutation of DDX41
According to the report of Polprasert et al., 2015, Cancer Cell 27, 658-670, the embryonic cell mutation of DDX41 develops in an autosomal dominant inheritance, so there is a 50% chance that it will be inherited in children and cause leukemia. .. Therefore, if a familial elderly-onset MDS / AML family is found, it may be due to a mutation in the embryonic cells of DDX41. Therefore, the DDX41 gene should be sequenced to confirm the presence or absence of mutations.
さらに、家族歴が不明な孤発例のMDS/AMLであっても、DDX41の変異が認められた場合には、家族内に、MDS/AMLが高い確率で将来認められる可能性がある。保因者の家族が他の疾患で若年で死亡していたり、子供がまだ若年であれば、家族例は明らかとならないことがあるからである。DDX41の変異は、実子には50%の確率で遺伝し、同じ両親をもつ同胞(兄弟姉妹)にも、50%の確率で陽性者が存在する。この情報により、さもなければ発見されない疾患リスクを、発症よりも数年から数10年前に見積もることができる。 Furthermore, even in sporadic cases of MDS / AML with an unknown family history, if a mutation in DDX41 is found, there is a high probability that MDS / AML will be found in the family in the future. If the carrier's family died of other illnesses at a young age, or if the child was still young, the family case might not be clear. The DDX41 mutation is inherited in the offspring with a 50% chance, and there is a 50% chance that there are positives in siblings with the same parents. With this information, the risk of otherwise undiscovered disease can be estimated years to decades before the onset.
DDX41の胚細胞変異の検索は、MDS/AMLに対する造血幹細胞移植を考慮する際にも重要である。MDS/AML症例においてDDX41変異を検索し、陽性であれば、ドナー候補となる同胞、両親、子が同様の変異を持っていないか検索すべきである。 Searching for embryonic cell mutations in DDX41 is also important when considering hematopoietic stem cell transplantation for MDS / AML. The DDX41 mutation should be searched for in MDS / AML cases, and if positive, the potential donor sibs, parents, and offspring should be searched for similar mutations.
家族内の造血幹細胞移植ドナー候補にDDX41変異が陽性であれば、そのドナーから移植が行われた場合、移植後ドナー由来白血病の確率が高まる。したがって、ドナー候補としての優先順位は下がり、非血縁のドナー候補を考慮すべきである。 If a candidate hematopoietic stem cell transplant donor in the family is positive for the DDX41 mutation, the probability of post-transplant donor-derived leukemia increases if transplantation is performed from that donor. Therefore, the priority as a donor candidate should be lowered and unrelated donor candidates should be considered.
Claims (8)
被験体の正常組織から取得した試料において、野生型DDX41遺伝子によりコードされるポリペプチドの配列番号2に示すアミノ酸配列中の、
第500位のアラニンのフレームシフト変異
を生じる、DDX41遺伝子の1以上の変異を検出することを特徴とする方法。 A method for obtaining an index for examining the onset or risk of developing bone marrow tumor in humans.
In a sample obtained from the normal tissue of the subject, in the amino acid sequence shown in SEQ ID NO: 2 of the polypeptide encoded by the wild-type DDX41 gene,
# 500 of alanine of a frame-shift mutation
A method characterized by detecting one or more mutations in the DDX41 gene that results in.
第1496位のシトシンの重複
である、請求項1に記載の方法。 A mutation in the DDX41 gene is used as the position in the cDNA base sequence of wild-type DDX41 shown in SEQ ID NO: 1.
Duplicate of the 1496 position of cytosine
In a method according to claim 1.
被験体の正常組織から取得した試料において、野生型DDX41遺伝子によりコードされるポリペプチドの配列番号2に示すアミノ酸配列中の、
第500位のアラニンのフレームシフト変異
を生じる、DDX41遺伝子の1以上の変異を検出すること、並びに
前記DDX41遺伝子の体細胞変異が、野生型DDX41遺伝子によりコードされる配列番号2に示すアミノ酸配列における、第525位のアルギニンの変異を生じるDDX41遺伝子の体細胞変異であること
を特徴とする方法。 A method for obtaining an index for predicting the presence or future development of a somatic mutation in the DDX41 gene in humans.
In a sample obtained from the normal tissue of the subject, in the amino acid sequence shown in SEQ ID NO: 2 of the polypeptide encoded by the wild-type DDX41 gene,
# 500 of alanine of a frame-shift mutation
Cause, detecting one or more mutations of the DDX41 gene and somatic mutation of the DDX41 gene, in the amino acid sequence shown in SEQ ID NO: 2 encoded by the wild-type DDX41 gene, a mutation of # 525 arginine A method characterized by a somatic mutation in the resulting DDX41 gene.
前記DDX41遺伝子の体細胞変異が、野生型DDX41遺伝子によりコードされる配列番号2に示すアミノ酸配列における、第525位のアルギニンの変異を生じるDDX41遺伝子の体細胞変異であり、
DDX41遺伝子のうち、変異した場合に、野生型DDX41遺伝子によりコードされるポリペプチドの配列番号2に示すアミノ酸配列において第500位のアミノ酸での変異を生じる塩基を1以上含む部位を増幅できるように設計されたプライマーセット、
DDX41遺伝子のうち、変異した場合に、野生型DDX41遺伝子によりコードされるポリペプチドの配列番号2に示すアミノ酸配列において第500位のアミノ酸での変異を生じる塩基を1以上含む部位と結合できるように設計されたプローブ、及び
DDX41遺伝子による翻訳産物であるポリペプチドのうち、配列番号2に示す野生型のアミノ酸配列において第500位のアミノ酸に対応するアミノ酸を含む部位を認識する抗体
からなる群から選択される1種以上を含有し、
前記アミノ酸での変異が、配列番号2に示すアミノ酸配列中の、
第500位のアラニンのフレームシフト変異
である、キット。 A kit used for at least one method of testing the onset or risk of developing bone marrow tumors in humans and predicting the presence or future occurrence of somatic mutations in the DDX41 gene in humans.
The somatic mutation of the DDX41 gene is a somatic mutation of the DDX41 gene that causes a mutation of arginine at position 525 in the amino acid sequence shown in SEQ ID NO: 2 encoded by the wild-type DDX41 gene.
Of DDX41 gene, when mutated, so that it can amplify a region comprising a base which affords a mutation at the 500 position of the amino acid in the amino acid sequence shown in SEQ ID NO: 2 of the polypeptide encoded by the wild-type DDX41 gene 1 or more Designed primer set,
Of DDX41 gene, when mutated, so that it can be combined with site comprising wild-type DDX41 gene by a base which affords a mutation at the 500 position of the amino acid in the amino acid sequence shown in SEQ ID NO: 2 of the polypeptide encoded one or more Designed probe and
Among the polypeptides that are translation products of the DDX41 gene, one or more selected from the group consisting of antibodies that recognize the site containing the amino acid corresponding to the amino acid at position 500 in the wild-type amino acid sequence shown in SEQ ID NO: 2 Contains,
The mutation in the amino acid is in the amino acid sequence shown in SEQ ID NO: 2.
# 500 of alanine of a frame-shift mutation
In it, kit.
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2015239547A JP6817608B2 (en) | 2015-12-08 | 2015-12-08 | A method for obtaining an index for testing the onset or risk of developing bone marrow tumor in humans, a method for obtaining an index for predicting the presence or future occurrence of a somatic mutation of the DDX41 gene in humans, and for these tests or predictions. kit |
| JP2020131453A JP6952376B2 (en) | 2015-12-08 | 2020-08-03 | A method for obtaining an index for testing the onset or risk of developing bone marrow tumor in humans, a method for obtaining an index for predicting the presence or future occurrence of a somatic mutation of the DDX41 gene in humans, and for these tests or predictions. kit |
| JP2020131455A JP6964358B2 (en) | 2015-12-08 | 2020-08-03 | A method for obtaining an index for testing the onset or risk of developing bone marrow tumor in humans, a method for obtaining an index for predicting the presence or future occurrence of a somatic mutation of the DDX41 gene in humans, and for these tests or predictions. kit |
| JP2020131454A JP6959676B2 (en) | 2015-12-08 | 2020-08-03 | A method for obtaining an index for testing the onset or risk of developing bone marrow tumor in humans, a method for obtaining an index for predicting the presence or future occurrence of a somatic mutation of the DDX41 gene in humans, and for these tests or predictions. kit |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2015239547A JP6817608B2 (en) | 2015-12-08 | 2015-12-08 | A method for obtaining an index for testing the onset or risk of developing bone marrow tumor in humans, a method for obtaining an index for predicting the presence or future occurrence of a somatic mutation of the DDX41 gene in humans, and for these tests or predictions. kit |
Related Child Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020131455A Division JP6964358B2 (en) | 2015-12-08 | 2020-08-03 | A method for obtaining an index for testing the onset or risk of developing bone marrow tumor in humans, a method for obtaining an index for predicting the presence or future occurrence of a somatic mutation of the DDX41 gene in humans, and for these tests or predictions. kit |
| JP2020131453A Division JP6952376B2 (en) | 2015-12-08 | 2020-08-03 | A method for obtaining an index for testing the onset or risk of developing bone marrow tumor in humans, a method for obtaining an index for predicting the presence or future occurrence of a somatic mutation of the DDX41 gene in humans, and for these tests or predictions. kit |
| JP2020131454A Division JP6959676B2 (en) | 2015-12-08 | 2020-08-03 | A method for obtaining an index for testing the onset or risk of developing bone marrow tumor in humans, a method for obtaining an index for predicting the presence or future occurrence of a somatic mutation of the DDX41 gene in humans, and for these tests or predictions. kit |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2017104035A JP2017104035A (en) | 2017-06-15 |
| JP6817608B2 true JP6817608B2 (en) | 2021-01-20 |
Family
ID=59058122
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015239547A Active JP6817608B2 (en) | 2015-12-08 | 2015-12-08 | A method for obtaining an index for testing the onset or risk of developing bone marrow tumor in humans, a method for obtaining an index for predicting the presence or future occurrence of a somatic mutation of the DDX41 gene in humans, and for these tests or predictions. kit |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP6817608B2 (en) |
-
2015
- 2015-12-08 JP JP2015239547A patent/JP6817608B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| JP2017104035A (en) | 2017-06-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US11326212B2 (en) | Biomarkers for non-hodgkin lymphomas and uses thereof | |
| Tun et al. | Pathway analysis of primary central nervous system lymphoma | |
| Kote-Jarai et al. | Seven prostate cancer susceptibility loci identified by a multi-stage genome-wide association study | |
| JP2021525069A (en) | Cell-free DNA for assessing and / or treating cancer | |
| US20110224313A1 (en) | Compositions and methods for classifying lung cancer and prognosing lung cancer survival | |
| US20120164636A1 (en) | Mammalian oocyte development competency granulosa markers and uses thereof | |
| Leeman-Neill et al. | Noncoding mutations cause super-enhancer retargeting resulting in protein synthesis dysregulation during B cell lymphoma progression | |
| CN103374628B (en) | Associated Gene of Congenital Heart Disease FAM71A and application thereof | |
| CN109402252A (en) | Acute myeloid leukemia risk assessment gene markers and their applications | |
| JP6959676B2 (en) | A method for obtaining an index for testing the onset or risk of developing bone marrow tumor in humans, a method for obtaining an index for predicting the presence or future occurrence of a somatic mutation of the DDX41 gene in humans, and for these tests or predictions. kit | |
| JP6952376B2 (en) | A method for obtaining an index for testing the onset or risk of developing bone marrow tumor in humans, a method for obtaining an index for predicting the presence or future occurrence of a somatic mutation of the DDX41 gene in humans, and for these tests or predictions. kit | |
| JP6964358B2 (en) | A method for obtaining an index for testing the onset or risk of developing bone marrow tumor in humans, a method for obtaining an index for predicting the presence or future occurrence of a somatic mutation of the DDX41 gene in humans, and for these tests or predictions. kit | |
| AU2010277532A1 (en) | Processes and methods for diagnosis of Alzheimer's disease | |
| JP6817608B2 (en) | A method for obtaining an index for testing the onset or risk of developing bone marrow tumor in humans, a method for obtaining an index for predicting the presence or future occurrence of a somatic mutation of the DDX41 gene in humans, and for these tests or predictions. kit | |
| KR101547307B1 (en) | Biomaker for diagnosing epilepsy | |
| EP4464791A1 (en) | Non-invasive in-vitro method for somatic mutation detection | |
| Kudryavtsev et al. | The frequency of mutations in the ATP7B gene in Russia | |
| JP2013039111A (en) | Splicing variant | |
| JP2006166789A (en) | New diagnostic method for cancer | |
| KR101864331B1 (en) | Predicting kit for survival of lung cancer patients and the method of providing the information for predicting survival of lung cancer patients | |
| JP4207187B2 (en) | HURP gene as a molecular marker for bladder cancer | |
| KR102781057B1 (en) | Novel Biomarker for Diagnosing Charcot-Marie-Tooth Disease Comprising Mutation of MPZ Gene and Uses Thereof | |
| EP4317458A1 (en) | Follicular thyroid cancer-specific marker | |
| KR20180125911A (en) | Method for providing the information for predicting or diagnosing of inflammatory bowel disease using single nucleotide polymorphism to be identified from next generation sequencing screening | |
| Szőke et al. | The RR genotype of codon 72 of p53 gene reduces the development of intestinal metaplasia |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A80 | Written request to apply exceptions to lack of novelty of invention |
Free format text: JAPANESE INTERMEDIATE CODE: A80 Effective date: 20160104 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20181204 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20190911 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20190924 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20191122 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200122 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20200602 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200803 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20201201 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20201218 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6817608 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |