JP2023553323A - 腫瘍特異的に切断可能なリンカー - Google Patents
腫瘍特異的に切断可能なリンカー Download PDFInfo
- Publication number
- JP2023553323A JP2023553323A JP2023531600A JP2023531600A JP2023553323A JP 2023553323 A JP2023553323 A JP 2023553323A JP 2023531600 A JP2023531600 A JP 2023531600A JP 2023531600 A JP2023531600 A JP 2023531600A JP 2023553323 A JP2023553323 A JP 2023553323A
- Authority
- JP
- Japan
- Prior art keywords
- cytokine
- amino acid
- masked
- prodrug
- seq
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/62—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being a protein, peptide or polyamino acid
- A61K47/65—Peptidic linkers, binders or spacers, e.g. peptidic enzyme-labile linkers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/19—Cytokines; Lymphokines; Interferons
- A61K38/20—Interleukins [IL]
- A61K38/2013—IL-2
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/19—Cytokines; Lymphokines; Interferons
- A61K38/20—Interleukins [IL]
- A61K38/208—IL-12
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/19—Cytokines; Lymphokines; Interferons
- A61K38/20—Interleukins [IL]
- A61K38/2086—IL-13 to IL-16
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/62—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being a protein, peptide or polyamino acid
- A61K47/64—Drug-peptide, drug-protein or drug-polyamino acid conjugates, i.e. the modifying agent being a peptide, protein or polyamino acid which is covalently bonded or complexed to a therapeutically active agent
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6801—Drug-antibody or immunoglobulin conjugates defined by the pharmacologically or therapeutically active agent
- A61K47/6803—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates
- A61K47/6811—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates the drug being a protein or peptide, e.g. transferrin or bleomycin
- A61K47/6813—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates the drug being a protein or peptide, e.g. transferrin or bleomycin the drug being a peptidic cytokine, e.g. an interleukin or interferon
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6889—Conjugates wherein the antibody being the modifying agent and wherein the linker, binder or spacer confers particular properties to the conjugates, e.g. peptidic enzyme-labile linkers or acid-labile linkers, providing for an acid-labile immuno conjugate wherein the drug may be released from its antibody conjugated part in an acidic, e.g. tumoural or environment
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K7/00—Peptides having 5 to 20 amino acids in a fully defined sequence; Derivatives thereof
- C07K7/04—Linear peptides containing only normal peptide links
- C07K7/06—Linear peptides containing only normal peptide links having 5 to 11 amino acids
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K7/00—Peptides having 5 to 20 amino acids in a fully defined sequence; Derivatives thereof
- C07K7/04—Linear peptides containing only normal peptide links
- C07K7/08—Linear peptides containing only normal peptide links having 12 to 20 amino acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Organic Chemistry (AREA)
- Epidemiology (AREA)
- Immunology (AREA)
- Molecular Biology (AREA)
- Biochemistry (AREA)
- Genetics & Genomics (AREA)
- Biophysics (AREA)
- Gastroenterology & Hepatology (AREA)
- Zoology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Peptides Or Proteins (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicinal Preparation (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
Abstract
Description
本出願は、2020年11月25日に出願された米国仮特許出願第63/118,585号、および2021年10月6日に出願された第63/253,090号の優先権の利益を主張するものであり、その各々が参照によりその全体が本明細書に組み込まれる。
ASCIIテキストファイル上の以下の提出の内容は、その全体が参照により本明細書に組み込まれる:配列表のコンピュータ可読形態(CRF)(ファイル名:737762003040SEQLIST.TXT、記録日:2021年11月22日、サイズ:961KB)。
を含み、
第二のポリペプチド鎖は、
を含み、
式中、HL1は第一の半減期延長ドメインであり、L1は第一のリンカーであり、MMはマスキング部分であり、HL2は第二の半減期延長ドメインであり、L2は第二のリンカーであり、Cはサイトカイン部分であり、
第一の半減期延長部分が第二の半減期延長部分と会合し、
少なくとも第一のリンカーまたは第二のリンカーが、アミノ酸配列DLLAVVAASまたはISSGLLSGRSからなるタンパク質分解的に切断可能なペプチド(CP)を含む、タンパク質分解的に切断可能なペプチドリンカーである。
を含むポリペプチド鎖を含み、
式中、HLは半減期延長ドメインであり、L1は第一のリンカーであり、MMはマスキング部分であり、L2は第二のリンカーであり、Cはサイトカイン部分であり、少なくとも第一のリンカーは、アミノ酸配列DLLAVVAASまたはISSGLLSGRSからなるタンパク質分解的に切断可能なペプチド(CP)を含むタンパク質分解的に切断可能なペプチドリンカーを含む。タンパク質分解的に切断可能なペプチドリンカーは、本明細書のどこかに記載されるとおりであってもよい。一部の実施形態では、第一のリンカーは、アミノ酸配列DLLAVVAASからなるタンパク質分解的に切断可能なペプチド(CP)を含む、タンパク質分解的に切断可能なペプチドリンカーである。一部の実施形態では、第一のリンカーは、アミノ酸配列ISSGLLSGRSからなるタンパク質分解的に切断可能なペプチド(CP)を含む、タンパク質分解的に切断可能なペプチドリンカーである。一部の実施形態では、第一のリンカーは、タンパク質分解的に切断可能なペプチドリンカーであり、第二のリンカーは、切断不可能である。切断不可能なリンカーは、本明細書のどこかに記載されるとおりであってもよい。
を含む、ポリペプチド鎖を含み、
式中、HLは半減期延長ドメインであり、L1は第一のリンカーであり、MMはマスキング部分であり、L2は第二のリンカーであり、Cはそのサイトカイン部分であり、少なくとも第一のリンカーは、アミノ酸配列DLLAVVAASまたはISSGLLSGRSからなるタンパク質分解的に切断可能なペプチド(CP)を含むタンパク質分解的に切断可能なペプチドリンカーを含む。タンパク質分解的に切断可能なペプチドリンカーは、本明細書のどこかに記載されるとおりであってもよい。一部の実施形態では、第一のリンカーは、アミノ酸配列DLLAVVAASからなるタンパク質分解的に切断可能なペプチド(CP)を含む、タンパク質分解的に切断可能なペプチドリンカーである。一部の実施形態では、第一のリンカーは、アミノ酸配列ISSGLLSGRSからなるタンパク質分解的に切断可能なペプチド(CP)を含む、タンパク質分解的に切断可能なペプチドリンカーである。一部の実施形態では、第一のリンカーは、タンパク質分解的に切断可能なペプチドリンカーであり、第二のリンカーは、切断不可能である。切断不可能なリンカーは、本明細書のどこかに記載されるとおりであってもよい。
本発明は、新規の腫瘍特異的タンパク質分解的に切断可能なペプチドリンカー、および腫瘍細胞環境に治療部分を送達するためのポリペプチド薬物構築物におけるそれらの使用を提供する。タンパク質分解的に切断可能なペプチドリンカーは、ポリペプチド薬物構築物内に配置され、その結果、リンカーが腫瘍細胞環境でのプロテアーゼ作用によって切断されると、ポリペプチド薬物構築物が分離する。本発明はまた、該薬物構築物の切断産物、ならびにその使用に関連する方法に関する。
本明細書に記載のタンパク質分解的に切断可能なペプチドリンカーは、アミノ酸配列DLLAVVAASまたはISSGLLSGRSからなるタンパク質分解的に切断可能なペプチド(CP)を含む。
インビボでの長い半減期は、治療用タンパク質にとって重要である。
DKTHTCPPCPAPELLGG
PSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYN
STYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDE
LTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRW
QQGNVFSCSVMHEALHNHYTQKSLSLSPG
(配列番号7)
第一の半減期延長部分(Y349C;T366S;L38A;およびY407V)配列番号8:
DKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHE
DPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWL
NGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVCTLPPSRDELTKNQ
VSLSCAVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLVSKL
TVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
第二の半減期延長部分(S354CおよびT366W)配列番号11:
DKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSH
EDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDW
LNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPCRDELTK
NQVSLWCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFL
YSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
DKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHE
DPEVKFNWYVDGVEVHNAKTKPREEQYASTYRVVSVLTVLHQDWL
NGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVCTLPPSRDELTKNQ
VSLSCAVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLVSKL
TVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
第二の半減期延長部分(S354C、T366WおよびN297A)配列番号12:
DKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSH
EDPEVKFNWYVDGVEVHNAKTKPREEQYASTYRVVSVLTVLHQDW
LNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPCRDELTK
NQVSLWCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFL
YSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
DKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMASRTPEVTCVVVDVSHEDP
EVKFNWYVDGVEVHNAKTKPREEQYASTYRVVSVLTVLHQDWLNGKE
YKCKVSNKALPAPIEKTISKAKGQPREPQVCTLPPSRDELTKNQVSLSCA
VKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLVSKLTVDKSRW
QQGNVFSCSVMHEALHNHYTQKSLSLSPG
第二の半減期延長部分(S354C、T366W、N297AおよびI253A)配列番号13:
DKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMASRTPEVTCVVVDVSHEDP
EVKFNWYVDGVEVHNAKTKPREEQYASTYRVVSVLTVLHQDWLNGKEY
KCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPCRDELTKNQVSLWCLVK
GFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRW
QQGNVFSCSVMHEALHNHYTQKSLSLSPG
本明細書に記載される半減期延長部分は、二つの異なる半減期延長部分のヘテロ二量体化を促進する一つまたは複数の修飾を含み得る。一部の実施形態では、その正しいヘテロ二量体の形態での薬物構築物の生産が効率的に生産されるように、第一および第二の半減期延長部分のヘテロ二量体化を促進することが望ましい。このように、以下に記載される任意の戦略を含む、当技術分野で利用可能な任意の戦略を使用して、一つまたは複数のアミノ酸修飾を、第一の半減期延長部分に対して行い、一つまたは複数のアミノ酸修飾を、第二の半減期延長部分に対して行うことができる。Klein et al.(2012)、MAbs、4(6):653-663。例示的な戦略および修飾を以下に詳細に説明する。
二つの異なる半減期延長部分のヘテロ二量体化を促進するための一つの戦略は、「ノブ・イントゥ・ホール」と呼ばれるアプローチである。
一部の実施形態では、治療部分がサイトカイン部分である、サイトカインプロドラッグが本明細書に提供されている。サイトカインプロドラッグのマスキング部分は、サイトカイン受容体の細胞外ドメインのドメインを含み得る。したがって、サイトカインプロドラッグは、マスクされたサイトカインとみなされ得る。
サイトカインは、細胞シグナル伝達、特に免疫系の細胞において役割を果たす。本明細書において、マスクされたサイトカインまたはその切断産物で使用するためのサイトカイン(例えば、IL-2、IL-15またはIL-12サイトカイン)またはその機能的断片を含むサイトカイン部分が提供される。
一部の実施形態では、第一のポリペプチド鎖にマスキング部分を含み、第二のポリペプチド鎖にそのサイトカイン部分を含む、マスクされたサイトカインが本明細書に提供される。こうしたマスクされたサイトカインは、「ヘテロ二量体の」マスクされたサイトカインと呼んでもよい。
c)第一のリンカーを介して第一の半減期延長部分に連結されたマスキング部分を含む第一のポリペプチド鎖と、
d)第二のリンカーを介して第二の半減期延長部分に連結されたそのサイトカイン部分を含む第二のポリペプチド鎖とを含み、
第一の半減期延長部分が第二の半減期延長部分と会合し、
少なくとも第一のリンカーまたは第二のリンカーが、アミノ酸配列DLLAVVAASまたはISSGLLSGRSからなるタンパク質分解的に切断可能なペプチド(CP)を含む、タンパク質分解的に切断可能なペプチドリンカーである、タンパク質ヘテロ二量体を含む。
を含み、
第二のポリペプチド鎖は、
を含み、
式中、HL1は第一の半減期延長ドメインであり、L1は第一のリンカーであり、MMはマスキング部分であり、HL2は第二の半減期延長ドメインであり、L2は第二のリンカーであり、Cはそのサイトカイン部分であり、
一部の実施形態では、第二のリンカーは、タンパク質分解的に切断可能なリンカーであり、第一のリンカーは、切断不可能なリンカーである。この配置は、本明細書では「構造A」として記載される。一部の実施形態では、第一のポリペプチド鎖は、
を含み、
第二のポリペプチド鎖は、
を含む。
を含み、
第二のポリペプチド鎖は、
を含む。
一部の実施形態では、単一のポリペプチド鎖で連結されたマスキング部分と、そのサイトカイン部分とを含む、マスクされたサイトカインが本明細書に提供される。一部の実施形態では、マスクされたサイトカインは、以下の式:
を含むポリペプチド鎖を含み、
式中、HLは半減期延長ドメインであり、L1は第一のリンカーであり、MMはマスキング部分であり、L2は第二のリンカーであり、Cはそのサイトカイン部分であり、少なくとも第一のリンカーは、タンパク質分解的に切断可能なペプチドを含む。
を含む、ポリペプチド鎖を含み、
式中、HLは半減期延長ドメインであり、L1は第一のリンカーであり、MMはマスキング部分であり、L2は第二のリンカーであり、Cはそのサイトカイン部分であり、少なくとも第一のリンカーは、タンパク質分解的に切断可能なペプチドを含む。一部の実施形態では、第一のリンカーは、本明細書のどこかに記載される切断可能なリンカーである。一部の実施形態では、第二のリンカーは、本明細書のどこかに記載される切断不可能なリンカーである。一部の実施形態では、そのサイトカイン部分は、本明細書のどこかに記載されるとおりである。一部の実施形態では、半減期延長ドメイン(HL)は、抗体のFc領域(すなわち、免疫グロブリン重鎖のC末端領域)または二量体化Fcドメイン(HL1-HL2)を含むその断片を含む。免疫グロブリン重鎖のFc領域の境界は変化し得るが、ヒトIgG重鎖のFc領域は通常、Cys226の位置のアミノ酸残基、またはPro230の位置のアミノ酸残基から、そのカルボキシル末端に及ぶと画定される。一部の実施形態では、抗体(HL1-HL2)の二量体化Fcドメインは、本明細書のどこかに記載されるとおり、第一の半減期延長ドメインと第二の半減期延長ドメインとを含み、第一の半減期延長部分は、第一のFcドメインまたはその断片を含み、第二の半減期延長部分は、第二のFcドメインまたはその断片を含む。一部の実施形態では、HL2はポリペプチド鎖の構成要素であり、HL1はHL2に二量体化される。
本明細書に開示されるサイトカイン部分およびマスキング部分(例えば、IL-2、IL-12、およびIl-15サイトカイン部分およびマスキング部分)は、本明細書に開示される任意のポリペプチド薬物構築物で使用され得る。
(a)IL-2サイトカイン部分
一部の実施形態では、治療部分は、IL-2サイトカインまたはその機能的断片を含む。
IL-2はインターロイキンであり、白血球の活性を調節する免疫系のサイトカインシグナル伝達分子の一種である。
本明細書では、IL-2サイトカインまたはその機能的断片を含む治療部分をマスキングする際に使用するためのマスキング部分が提供される。
(a)IL-12サイトカイン部分
一部の実施形態では、治療部分は、IL-12サイトカインまたはその機能的断片を含む。
IL-12 p40サブユニット:
IL-12 p35サブユニット:
成熟形態は以下のとおりである。
IL-12 p40サブユニット:
IWELKKDVYVVELDWYPDAPGEMVVLTCDTPEEDGITWTLDQSSEVLGSGKTLTIQVKEFGDAGQYTCHKGGEVLSHSLLLLHKKEDGIWSTDILKDQ
KEPKNKTFLRCEAKNYSGRFTCWWLTTISTDLTFSVKSSRGSSDPQGVTCGAATLSAERV
RGDNKEYEYSVECQEDSACPAAEESLPIEVMVDAVHKLKYENYTSSFFIRDIIKPDPPKN
LQLKPLKNSRQVEVSWEYPDTWSTPHSYFSLTFCVQVQGKSKREKKDRVFTDKTSATVIC
RKNASISVRAQDRYYSSSWSEWASVPCS
IL-12 p35サブユニット:
RNLPVATPDPGMFPCLHHSQNLLRAVSNMLQKARQTLEFYPCTSEEIDHEDITKDKTSTVEACLPLELTKNESCLNSRETSFITNGSCLASRKTSFMM
ALCLSSIYEDLKMYQVEFKTMNAKLLMDPKRQIFLDQNMLAVIDELMQALNFNSETVPQK
SSLEEPDFYKTKIKLCILLHAFRIRAVTIDRVMSYLNAS
を含み、
第二のポリペプチド鎖が式:
を含むように、第一の半減期延長ドメインに結合されてもよく、
式中、「IL-12p40」はIL-12p40ポリペプチドまたはその機能的断片であり、「IL-12p35」はIL-12p35ポリペプチドまたはその機能的断片である。
本明細書では、IL-12サイトカインまたはその機能的断片を含む治療部分をマスキングする際に使用するためのマスキング部分が提供される。
(a) IL-15サイトカイン部分
一部の実施形態では、治療部分は、IL-15サイトカインまたはその機能的断片を含む。
MRISKPHLRSISIQCYLCLLLNSHFLTEAGIHVFILGCFSAGLPKTEANWVNVISDLKKIEDLIQSMHIDATLYTESDVHPSCKVTAMKCFLLELQVISLESGDASIHDTVENLIILANNSLSSNGNVTESGCKECEELEEKNIKEFLQSFVHIVQMFINTS
IL-15成熟ポリペプチド:
NWVNVISDLKKIEDLIQSMHIDATLYTESDVHPSCKVTAMKCFLLELQVISLESGDASIHDTVENLIILANNSLSSNGNVTESGCKECEELEEKNIKEFLQSFVHIVQMFINTS
本明細書では、IL-15サイトカインまたはその機能的断片を含む治療部分をマスキングする際に使用するためのマスキング部分が提供される。
本明細書に記載される薬物構築物またはその切断産物で使用するための切断不可能なペプチドリンカーが本明細書に提供される。本明細書に提供される切断不可能なリンカーは、本明細書に記述されたマスクされたサイトカインにおいて二つの機能的成分を一緒に連結するために使用される、さらに二つのアミノ酸のペプチドを指す。
を含み、
第二のポリペプチド鎖が式:
を含む。
を含み、
第二のポリペプチド鎖が式:
を含む。
本明細書のどこかに記載されるポリペプチド薬物構築物中のタンパク質分解的に切断可能なリンカーのタンパク質分解的切断によって調製可能な、活性治療部分を含む切断産物が、本明細書に提供される。
を含むポリペプチドを含み、
式中、PCPはタンパク質分解的に切断可能なペプチドの一部であり、SDはスペーサードメインであり、Cはサイトカイン部分である。
a) 第一の半減期延長部分を含む第一のポリペプチド鎖と、
b) 式:
を含むポリペプチドを含む第二のポリペプチド鎖であって、
式中、HL2は第二の半減期延長部分であり、L2は切断不可能なリンカーであり、Cはサイトカイン部分であり、第一の半減期延長部分は第二の半減期延長部分と関連している、第二のポリペプチド鎖と、を含むタンパク質ヘテロ二量体を含む。また、本明細書では、マスクされたサイトカインの単一構造から取得されたまたは取得可能な切断産物の分布が提供され、切断産物の分布内の各切断産物は、(i)標的タンパク質に結合することができ、(ii)以下:
a) 第一の半減期延長部分を含む第一のポリペプチド鎖と、
b) 式:
を含むポリペプチドを含む第二のポリペプチド鎖であって、
式中、HL2は第二の半減期延長部分であり、L2は切断不可能なリンカーであり、Cはサイトカイン部分であり、第一の半減期延長部分は第二の半減期延長部分と関連している、第二のポリペプチド鎖と、を含むタンパク質ヘテロ二量体を含む。
a) 式:
を含むポリペプチドを含む第一のポリペプチド鎖であって、
式中、HL1は、第一の半減期延長部分であり、SDは、スペーサードメインであり、PCPは、タンパク質分解的に切断可能なペプチドの一部である、第一のポリペプチド鎖と、
b) 式:
を含むポリペプチドを含む第二のポリペプチド鎖であって、
式中、HL2は第二の半減期延長部分であり、L2は切断不可能なリンカーであり、Cはサイトカイン部分であり、第一の半減期延長部分は第二の半減期延長部分と関連している、第二のポリペプチド鎖と、を含むタンパク質ヘテロ二量体を含む。
サイトカインまたはその機能的断片と、サイトカインまたはその機能的断片が特異的である結合パートナー(例えば、サイトカイン受容体などの標的タンパク質)との間などの免疫学的結合相互作用の強度、または親和性は、相互作用の解離定数(Kd)の観点から表すことができ、Kdが小さいほど親和性が高いことを表す。サイトカイン受容体へのサイトカインの結合は、Kdの観点から表され得る。一部の実施形態では、免疫学的結合相互作用は、マスクされたサイトカイン(プロテアーゼの存在下または非存在下)と、サイトカイン受容体などの標的タンパク質との間である。IL-2サイトカイン結合の文脈では、標的タンパク質は、IL-2R(IL-2Rα、IL-2Rβ、およびIL-2Rγ鎖を含む)、IL-2Rα鎖、IL-2Rβ鎖、またはIL-2Rα/β二量体複合体であり得る。タンパク質の免疫学的結合特性は、当該技術分野で周知の方法を使用して定量化することができる。例えば、一つの方法は、サイトカイン受容体(例えば、IL-2R)/サイトカイン(例えば、IL-2)複合体形成および解離の速度を測定することを含み、この速度は、複合体パートナーの濃度、相互作用の親和性、および両方向の速度に等しく影響する幾何学的パラメータに依存する。「オンレート定数」(Kon)および「オフレート定数」(Koff)の両方は、濃度ならびに会合および解離の実際の速度の計算によって決定することができる。Koff/Konの速度は、親和性に関連しないすべてのパラメータの削除を可能にし、解離定数Kdと等しい。Davies et al.,Annual Rev Biochem. 59:439-473,(1990)を参照されたい。
本明細書に記載されるマスクされたサイトカインは、当該技術分野で利用可能な技術を使用して調製され、その例示的な方法が記載される。
マスクされたサイトカインの一部の実施形態は、抗体またはその断片を含む。以下のセクションでは、本明細書に提供されるマスクされたサイトカインの一部の実施形態で使用され得る、抗体およびその抗体断片、バリアント、ならびに誘導体の産生についてさらに詳細を提供する。一部の実施形態では、マスクされたサイトカインは、ジスルフィド結合を介して結合するマスクされたサイトカインの二つのコピーによって産生される二量体の形態である。
本発明は、一部の実施形態では、抗体断片を包含する。抗体断片は、Fcドメイン、重鎖の一部、軽鎖の一部、Fab、Fv、またはscFvなどの任意の抗体断片であってもよい。抗体断片は、酵素消化などの従来の手段によって、または組換え技術によって生成され得る。ある特定の状況では、抗体全体ではなく、抗体断片を、本明細書に記載のマスクされたサイトカインに連結する利点がある。ある特定の抗体断片の概説については、Hudson et al. (2003)Nat. Med. 9:129-134を参照されたい。
本発明は、一部の実施形態では、ヒト化抗体またはその抗体断片を包含する。一部の実施形態では、ヒト化抗体は、任意の抗体断片を含む任意の抗体であってもよい。非ヒト抗体をヒト化するための様々な方法が当該技術分野で公知である。例えば、ヒト化抗体は、非ヒトである源から導入される一つまたは複数のアミノ酸残基を有し得る。これらの非ヒトアミノ酸残基は、しばしば、典型的には「輸入」可変ドメインから取り込まれる「輸入」残基と称される。ヒト化は、ヒト抗体の対応する配列に超可変領域の配列を置換することによって、Winterの方法(Jones et al.(1986)Nature 321:522-525、Riechmann et al.(1988)Nature 332:323-327、Verhoeyen et al.(1988)Science 239:1534-1536)の後に本質的に行われ得る。したがって、かかる「ヒト化」抗体は、キメラ抗体であり(米国特許第4,816,567号)、より実質的に少ないインタクトなヒト可変ドメインが、非ヒト種からの対応する配列によって置換されている。実際には、ヒト化抗体は、典型的には、いくつかの超可変領域残基および場合によりいくつかのFR残基が、げっ歯類抗体の類似部位からの残基によって置換されているヒト抗体である。ヒト化抗体は、本明細書に提供されるガイダンスに従って、本明細書に記述されるマスクされたサイトカインに連結され得る。
本発明の一部の実施形態のヒト抗体は、ヒト由来ファージディスプレイライブラリから選択されるFvクローン可変ドメイン配列を、公知のヒト定常ドメイン配列と組み合わせることによって構築することができる。あるいは、本発明の一部の実施形態のヒトモノクローナル抗体は、例えば、マウス、ラット、ウシ(bovine)(例えば、ウシ(cow))、またはウサギ細胞を使用して、例えばヒトモノクローナル抗体を産生するためにハイブリドーマ法によって作製することができる。一部の実施形態では、ヒト抗体およびヒトモノクローナル抗体は、任意の抗原に結合する抗体であってもよい。一部の実施形態では、本発明のヒトモノクローナル抗体は、ヒト免疫グロブリン座位を含む非ヒト動物を標的抗原で免疫し、抗体を免疫された動物または免疫された動物から誘導された細胞から単離することによって作製することができる。好適な非ヒト動物の例としては、HuMAb Mouse(登録商標)(Medarex, Inc.)、KM Mouse(登録商標)、「TCマウス」、およびXenomouse(商標)などのトランスジェニックまたはトランスクロモソミック動物が挙げられる。例えば、Lonberg, et al. (1994) Nature 368: 856-859;Fishwild,D.et al. (1996) Nature Biotechnology 14: 845-851、WO2002/43478、米国特許第 5,939,598号、6,075,181号、6,114,598号、6,150,584号、6,162,963号、およびTomizukaら (2000) Proc. Natl. Acad. Sci. USA 97:722-727を参照のこと。
二重特異性抗体は、少なくとも二つの異なる抗原に対する結合特異性を有するモノクローナル抗体である。ある特定の実施形態では、二重特異性抗体は、ヒトまたはヒト化抗体である。一部の実施形態では、結合特異性のうちの一つは、第一の抗原に対するものであり、他方の結合特異性は、第二の抗原に対するものであり、これは、同じ標的タンパク質上の二つの異なるエピトープ、または二つの異なる標的タンパク質上の二つの異なるエピトープのいずれかであってもよい。二重特異性抗体は、第一の抗原および/または第二の抗原を発現する細胞に細胞障害性薬剤を局在化するためにも使用され得る。二重特異性抗体は、例えば、癌細胞などの特定の細胞を殺すために、T細胞またはナチュラルキラー細胞などの細胞をリクルートするためにも使用され得る。二重特異性抗体は、完全長抗体または抗体断片(例えば、F(ab’)2二重特異性抗体)として調製することができる。二重特異性抗体は、本明細書に提供されるガイダンスに従って、本明細書に記述されるマスクされたサイトカインに連結され得る。
一部の実施形態では、単一ドメイン抗体は、本明細書に提供されるガイダンスに従ってマスクされたサイトカインに連結する。単一ドメイン抗体は、任意の抗体とすることができる。単一ドメイン抗体は、抗体の重鎖可変ドメインのすべてもしくは一部、または軽鎖可変ドメインのすべてもしくは一部を含む単一ポリペプチド鎖である。ある特定の実施形態では、単一ドメイン抗体は、ヒト単一ドメイン抗体である(Domantis,Inc.,Waltham,Mass.、例えば、米国特許第6,248,516B1を参照されたい)。一部の実施形態では、単一ドメイン抗体は、抗体の重鎖可変ドメインのすべてまたは一部からなる。一部の実施形態では、単一ドメイン抗体は、標的抗原でラクダを免疫化することによって得られたラクダ由来の抗体である。一部の実施形態では、単一ドメイン抗体は、標的抗原でサメを免疫化することによって得られたサメ由来の抗体である。一部の実施形態では、単一ドメイン抗体は、ナノボディである(例えば、WO2004041865A2およびUS20070269422A1を参照のこと)。
一部の実施形態では、本明細書に記載される抗体またはその断片のアミノ酸配列修飾が企図される。例えば、抗体のFcRn結合親和性および/またはpH依存性FcRn結合親和性を改善することが望ましい場合がある。また、特定のアミノ酸修飾を導入することによって、抗体重鎖のヘテロ二量体化を促進することが望ましい場合がある。抗体鎖のヘテロ二量体化を促進するための方法は、ヘテロ二量体化を促進するために作製され得る特定の修飾を含めて、Klein et al. (2012)、MAbs、4(6): 653-663に記載されている。
(1) 非極性: Ala(A)、Val(V)、Leu(L)、Iie(I)、Pro(P)、Phe(F)、Trp(W)、Met(M)
(2) 非荷電極性: Gly(G)、Ser(S)、Thr(T)、Cys(C)、Tyr(Y)、Asn(N)、Gin(Q)
(3) 酸性: Asp(D)、Glu(E)
(4) 塩基性: Lys(K)、Arg(R)、His(H)
あるいは、天然発生型残基は、以下の一般的な側鎖の特性に基づいてグループに分けられ得る:
(1) 疎水性: ノルロイシン、Met、Ala、Val、Leu、he;
(2) 中性親水性: Cys、Ser、Thr、Asn、Gin;
(3) 酸性: Asp、Glu;
(4) 塩基性: His、Lys、Arg;
(5) 鎖の方向性に影響を与える残基:Gly、Pro;
(6) 芳香族: Trp、Tyr、Phe。
非保存的置換は、これらのクラスのうちの一つのメンバーを別のクラスのものに交換することを伴う。かかる置換残基はまた、保存的置換部位、または残りの(非保存的)部位に導入されてもよい。
本発明はまた、本明細書に提供されるマスクされたサイトカインを含むマスクされたサイトカイン-薬物コンジュゲート(MCDC)も提供し、これは、一つまたは複数の薬剤にコンジュゲートされた、本明細書に開示される任意のマスクされたサイトカインであり得る。一部の実施形態では、一つまたは複数の薬剤は、化学療法剤または薬物などの細胞傷害剤、成長阻害剤、毒素(例えば、タンパク質毒素、
本発明のマスクされたサイトカインの組換え生成のために、それをコードする一つまたは複数の核酸を単離し、さらなるクローニング(DNAの増幅)または発現のために、複製可能なベクター内に挿入する。
a.ベクター構築
本発明のマスクされたサイトカインのポリペプチド成分をコードするポリヌクレオチド配列は、標準的な組換え技術を使用して得ることができる。抗体またはその抗体断片の所望のポリヌクレオチド配列は、ハイブリドーマ細胞などの抗体生成細胞から単離され、配列決定されてもよい。あるいは、ポリヌクレオチドは、ヌクレオチド合成器またはPGR技術を使用して合成することができ、または他の供給源から得ることができる。得られると、マスクされたサイトカインの成分をコードする配列は、原核宿主において異種ポリヌクレオチドを複製および発現することができる組換えベクターに挿入される。当該技術分野で利用可能かつ公知の多くのベクターを、本発明の目的のために使用することができる。適切なベクターの選択は、主に、ベクターに挿入される核酸のサイズ、およびベクターで形質転換される特定の宿主細胞に依存する。各ベクターは、その機能(異種ポリヌクレオチドの増幅もしくは発現、またはその両方)、およびそれが常駐する特定の宿主細胞とのその適合性に応じて、様々な構成要素を含む。ベクター構成要素には、概して、これらに限定されないが、複製の起源、選択マーカー遺伝子、プロモーター、リボソーム結合部位(RBS)、シグナル配列、異種核酸挿入、および転写終結配列が含まれる。
宿主細胞は、上述の発現ベクターで形質転換され、プロモーターを誘導するために、形質転換体を選択するために、または所望の配列をコードする遺伝子を増幅するために、適切な場合に修飾された従来の栄養素培地中で培養される。
一部の実施形態では、本明細書の生成されるマスクされたサイトカインは、さらなるアッセイおよび使用のために、実質的に均質な調製物を得るためにさらに精製される。当該技術分野で公知の標準的なタンパク質精製方法を用いることができる。以下の手順は、好適な精製手順の例である:免疫親和性カラムまたはイオン交換カラム上の分画、エタノール沈殿、逆相HPLC、シリカ上またはDEAEなどの陽イオン交換樹脂上でのクロマトグラフィー、クロマトフォーカシング、SDS-PAGE、硫酸アンモニウム沈殿、および例えば、Sephadex G-75を使用するゲル濾過。
真核宿主細胞で使用するためのベクターには、概して、以下の非限定的な構成要素:シグナル配列、複製の起源、一つまたは複数のマーカー遺伝子、エンハンサー要素、プロモーター、および転写終結配列のうちの一つまたは複数が含まれる。
真核宿主細胞で使用するためのベクターはまた、シグナル配列、または成熟タンパク質もしくは目的のポリペプチドのN末端に特定の切断部位を有する他のポリペプチドを含み得る。選択される異種シグナル配列は、宿主細胞によって認識および処理される(すなわち、シグナルペプチダーゼによって切断される)ものであり得る。哺乳動物細胞発現では、哺乳動物シグナル配列ならびにウイルス分泌リーダー、例えば、単純ヘルペスgDシグナルが利用可能である。
概して、複製構成要素の起源は、哺乳動物発現ベクターに必要とされない。例えば、SV40起源は、典型的には、早期プロモーターを含むためにのみ使用され得る。
発現ベクターおよびクローニングベクターは、選択遺伝子を含んでもよく、選択マーカーとも称される。典型的な選択遺伝子は、(a)抗生物質もしくは他の毒素、例えば、アンピシリン、ネオマイシン、メトトレキサート、もしくはテトラサイクリンに対する耐性を付与するタンパク質、(b)関連する場合、栄養要求性欠損を相補するタンパク質、または(c)複合培地から利用可能ではない重要な栄養素を供給するタンパク質をコードする。
発現ベクターおよびクローニングベクターは、通常、宿主生物によって認識され、かつ目的のマスクされたサイトカインをコードする核酸に動作可能に連結されるプロモーターを含み、これは本明細書に記載の任意のマスクされたサイトカインであり得る。プロモーター配列は、真核生物について公知である。例えば、ほぼすべての真核遺伝子は、転写が開始される部位からおよそ25~30塩基上流に位置するATリッチ領域を有する。多くの遺伝子の転写の開始から70~80塩基上流に見出される別の配列は、CNCAAT領域であり、Nは任意のヌクレオチドであってもよい。ほとんどの真核遺伝子の3’末端に、コード配列の3’末端へのポリAテールの付加のシグナルであり得るAATAAA配列がある。ある特定の実施形態では、これらの配列のうちのいずれかまたはすべては、真核生物発現ベクターに好適に挿入されてもよい。
より高い真核生物による本発明のマスクされたサイトカインをコードするDNAの転写は、エンハンサー配列をベクターに挿入することによってしばしば増加される。多くのエンハンサー配列は、現在、哺乳動物遺伝子(グロビン、エラスターゼ、アルブミン、a-フェトプロテイン、およびインスリン)から公知である。しかしながら、典型的には、一つは真核細胞ウイルス由来のエンハンサーを使用する。例としては、複製起源の後期側のSV40エンハンサー(bp100~270)、ヒトサイトメガロウイルス早期プロモーターエンハンサー、マウスサイトメガロウイルス早期プロモーターエンハンサー、複製起源の後期側のポリオーマエンハンサー、およびアデノウイルスエンハンサーが挙げられる。また、Yaniv,Nature 297:17-18(1982)も参照されたい(真核生物プロモーターの活性化のエンハンサー要素について記載している)。エンハンサーは、
真核宿主細胞で使用される発現ベクターはまた、転写の終結およびmRNAの安定化に必要な配列を含み得る。かかる配列は、真核またはウイルスのDNAまたはcDNAの5’および場合により3’の非翻訳領域から一般的に利用可能である。これらの領域は、マスクされたサイトカインをコードするmRNAの非翻訳部分にポリアデニル化断片として転写されたヌクレオチドセグメントを含む。一つの有用な転写終結構成要素は、ウシ成長ホルモンポリアデニル化領域である。WO94/11026およびその中に開示される発現ベクターを参照されたい。
本明細書のベクター中のDNAをクローニングまたは発現するための好適な宿主細胞は、脊椎動物宿主細胞を含む、本明細書に記載されるより高い真核細胞を含む。培養(組織培養)における脊椎動物細胞の増殖は、日常的な手順となっている。有用な哺乳動物宿主細胞株の例としては、SV40(COS-7、ATCC CRL 1651)により形質転換されたサル腎臓CV1株;ヒト胚腎臓株(懸濁培養での増殖用にサブクローニングされた293または293細胞、Graham et ah, J.Gen Virol.36:59(1977));ベビーハムスター腎臓細胞(BHK、ATCC CCL 10);チャイニーズハムスター卵巣細胞/-DHFR(CHO、Urlaub et ah, Proc.Natl.Acad.Sci.USA 77:4216(1980));マウスセルトリ細胞(TM4、Mather,Biol.Reprod.23:243-251(1980));サル腎臓細胞(CV1 ATCC CCL 70);アフリカミドリザル腎臓細胞(VERO-76、ATCC CRL-1587);ヒト子宮頸癌細胞(HELA、ATCC CCL2);イヌ腎臓細胞(MDCK、ATCC CCL34);バッファローラット肝臓細胞(BEL 3A、ATCC CRL 1442);ヒト肺細胞(W138、ATCC CCL 75);ヒト肝臓細胞(Hep G2、HB 8065);マウス乳癌腫瘍(MMT 060562、ATCC CCL51);TRI細胞(Mather et ah, Annals N.Y. Acad. Sci.383:44-68(1982));MRC5細胞;FS4細胞;およびヒト肝癌株(Hep G2)が挙げられる。
本発明のマスクされたサイトカインを生成するために使用される宿主細胞は、様々な培地中で培養されてもよい。ハムF10(Sigma)、最小必須培地((MEM)、Sigma)、RPMI-1640(Sigma)、およびダルベッコ改変イーグル培地((DMEM)、Sigma)などの市販の培地は、宿主細胞を培養するのに好適である。さらに、Ham et ah, Meth. Enz. 58:44(1979)、Barnes et ah, Anal. Biochem. 102:255(1980)、米国特許4,767,704号、4,657,866号、
組換え技術を使用する場合、マスクされたサイトカインは、細胞内で生成され得るか、または培地中に直接分泌され得る。マスクされたサイトカインが第一のステップとして細胞内で生成される場合、宿主細胞または溶解断片のいずれかである微粒子状破片は、例えば、遠心分離または限外濾過によって除去され得る。マスクされたサイトカインが培地中に分泌される場合、かかる発現系由来の上清は、最初に、市販のタンパク質濃度フィルター、例えば、AmiconまたはMillipore Pellicon限外濾過ユニットを使用して濃縮されてもよい。PMSFなどのプロテアーゼ阻害剤は、タンパク質分解を阻害するための前述のステップのうちのいずれかに含まれてもよく、抗生物質は、外来性汚染物質の成長を防止するために含まれてもよい。
一部の態様では、本明細書に記載されるマスクされたサイトカインのいずれかを含む組成物も本明細書に提供される。一部の実施形態では、組成物は、本明細書に記載のマスクされたサイトカインの例示的な実施形態のいずれかを含む。一部の実施形態では、組成物は、本明細書に記載のマスクされたサイトカインのいずれかの二量体を含む。一部の実施形態では、組成物は、医薬組成物である。一部の実施形態では、組成物は、マスクされたサイトカインを含み、以下に詳細に記載される構成要素のうちの一つまたは複数をさらに含む。例えば、一部の実施形態では、組成物は、一つまたは複数の薬学的に許容可能な担体、賦形剤、安定剤、緩衝剤、保存剤、等張化剤、非イオン性界面活性剤もしくは洗剤、または他の治療剤もしくは活性化合物、またはそれらの組み合わせを含む。組成物の様々な実施形態は、本明細書では製剤と呼ばれることがある。
本明細書では、対象において疾患を治療または予防する方法が提供され、本方法は、本明細書に記載のいずれかのマスクされたサイトカインまたはその組成物の有効量を対象に投与することを含む。一部の実施形態では、対象において疾患を治療または予防する方法が提供され、本方法は、本明細書に記載のいずれかの組成物を対象に投与することを含む。一部の実施形態では、対象(例えば、ヒト患者)は、癌と診断されたか、またはかかる障害を発症するリスクがある。一部の実施形態では、対象において疾患を治療または予防する方法が提供され、本方法は、本明細書に記載のいずれかのマスクされたサイトカインまたはその組成物の有効量を対象に投与することを含み、マスクされたサイトカインは、酵素で切断されると活性化する。一部の実施形態では、マスクされたサイトカインは、腫瘍微小環境で活性化される。マスクされたサイトカインは、切断された後、治療的に活性である。したがって、一部の実施形態では、活性薬剤は、切断産物である。
別の態様では、本明細書に記載の任意のマスクされたサイトカインを含む、製造品またはキットが提供される。製造物品またはキットは、本発明の方法におけるサイトカインの使用のための説明書をさらに含み得る。したがって、特定の実施形態では、製造物品またはキットは、有効量のマスクされたサイトカインを個体に投与することを含む、個体における障害(例えば、癌)を治療または予防する方法におけるマスクされたサイトカインの使用に関する指示を含む。例えば、特定の実施形態では、製造物品またはキットは、有効量のマスクされたポリペプチドを個体に投与することを含む、個体における障害(例えば、癌)を治療または予防する方法におけるマスクされたポリペプチドの使用に関する指示を含む。ある特定の実施形態では、個体は、ヒトである。一部の実施形態では、個体は、白血病、リンパ腫、頭頸部癌、結腸直腸癌、前立腺癌、脾臓癌、黒色腫、乳癌、神経芽細胞腫、肺癌、卵巣癌、骨肉腫、膀胱癌、子宮頸癌、肝臓癌、腎臓癌、皮膚癌、または精巣癌からなる群から選択される疾患を有する。
別途定義されない限り、本明細書で使用される全ての技術用語、表記、および他の技術用語および科学用語または専門用語は、請求される主題が関連する当業者によって一般的に理解されるものと同じ意味を有することが意図される。一部の事例では、一般的に理解される意味を有する用語は、明確にするため、および/またはすぐに参照できるように本明細書に定義され、本明細書にこうした定義を含めることは、当該技術分野で一般的に理解されるものとの実質的な差異を表すと必ずしも解釈されるべきではない。
100×画分X/Y
式中、Xは、そのプログラムのAおよびBの整列における配列によって同一の一致としてスコア付けされたアミノ酸残基の数であり、Yは、Bにおけるアミノ酸残基の総数である。アミノ酸配列Aの長さがアミノ酸配列Bの長さと等しくない場合、A対Bのアミノ酸配列同一性%は、B対Aのアミノ酸配列同一性%と等しくないことが理解されよう。
本発明は、以下の実施例を参照することにより、より十分に理解されるであろう。しかしながら、それらは、本発明の範囲を限定するものとして解釈されるべきではない。本明細書に記載される実施例および実施形態は、例示目的のためのみであり、それを考量したその様々な修飾または変更が当業者に提案され、本出願の趣旨および目的、ならびに添付の特許請求の範囲に含まれるべきであることが理解されるべきである。
マスクされたIL-2ポリペプチド構築物は、本明細書の教示に従って生成される。その後の実施例では、一部の実験は、単量体形態のマスクされたIL-2ポリペプチド構築物の使用を含み、一部の実験は、例えば、同じマスクされたポリペプチド構築物の二つのコピーを連結するジスルフィド結合を介して形成される二量体(ホモ二量体)、または二つの異なるポリペプチドによって形成されるヘテロ二量体などの、二量体形態のマスクされたIL-2構築物の使用を含む(例えば、表5を参照)。
実施例1で生成されたマスクされたIL-2ポリペプチド構築物は、インビトロでいくつかの細胞アッセイおよび機能アッセイを使用して特徴付けられる。
構築物(例えば、マスクされたIL-2ポリペプチド構築物)をコードするプラスミドを、Expi293細胞(Life Technologies A14527)またはHEK293-6E細胞(National Research Council、NRC)のいずれかにトランスフェクトした。トランスフェクションは、PEIpro(Polyplus Transfection、115-100)を使用して、全DNAと1:1の比率で、1mgの全DNAを用いて実施した。DNAおよびPEIをそれぞれ50mLのOptiMem(Life Technologies 31985088)培地に添加し、滅菌濾過した。DNAおよびPEIを10分間合わせて、Expi293細胞またはHEK293細胞の細胞密度がそれぞれ、1.8~2.8 x 106細胞/mLまたは0.85~1.20 x 106細胞/mで、生存率が少なくとも95%になるようにExpi293細胞に添加した。HEK293-6Eトランスフェクションは、Expi293トランスフェクションに使用されたのと同じプロトコルに従って、細胞密度および生存率が少なくとも95%で実施された。5~7日後、細胞を、3000×gで遠心分離することによってペレット化し、上清を0.2μmの膜を通して濾過した。タンパク質A樹脂(CaptivA、Repligen CA-PRI-0005)を、濾過された上清に加え、振とうしながら4℃で少なくとも2時間インキュベートした。樹脂をカラムに充填し、15カラム体積の20mMクエン酸塩、pH6.5で洗浄し、次いで15カラム体積の20mMクエン酸塩、500mM塩化ナトリウム、pH6.5で洗浄した。結合タンパク質を、20mMのクエン酸塩、100mMのNaCl、pH2.9でカラムから溶出した。
SDS-PAGE分析のために、タンパク質サンプルを4xLaemmliサンプル緩衝液(BioRadカタログ番号1610747)で作製した。還元されたサンプルについては、0.1MのBond Breaker TCEP溶液(Thermo Scientific 77720)を加え、サンプルを65°Cで5分間加熱した。12ウェルのNuPage 4~12 % Bis-Tris Protein Gel(Invitrogen NP0322BOX)に、ウェル当たり4μgのタンパク質を装填した。ゲルを、SimplyBlue SafeStain(Invitrogen LC6065)を使用して染色した。
レポーターバイオアッセイは、マスクされたIL-2ポリペプチド構築物、ならびにマスクされていない親構築物または他の対照で実施され、JAK-STAT経路などの下流経路の活性化を監視する。
実施例1で生成されたマスクされたIL-2ポリペプチド構築物の結合が評価される。ELISAプレートは、受容体サブユニット、例えばIL-2Rα(CD25とも呼ばれる)、IL-2Rβ(CD122とも呼ばれる)、またはIL-2Rγ(CD132とも呼ばれる)、またはそれらの組み合わせで被覆される。マスクされたIL-2ポリペプチド構築物の希釈は、受容体サブユニットに結合することができ、抗huFc-HRP検出抗体を使用して検出される。マスクされたIL-2ポリペプチド構築物の結合は、プロテアーゼ切断を伴う、または伴わない条件下で決定される。
実施例1で生成されたマスクされたIL-2ポリペプチド構築物のオンセル受容体結合が評価される。マスクされたIL-2ポリペプチド構築物の希釈は、CTLL2細胞などの末梢血リンパ球または組織培養細胞に結合することができ、抗huFc-FITCまたは抗アルブミン-FITC検出抗体を使用した蛍光標識細胞分取(FACS)によって検出される。マスクされたIL-2ポリペプチド構築物の結合は、プロテアーゼ切断を伴う、または伴わない条件下で決定される。
実施例1で生成されたマスクされたIL-2ポリペプチド構築物の結合親和性が評価される。マスクされたIL-2ポリペプチド構築物の結合親和性は、プロテアーゼ切断を伴う、または伴わない条件下で決定される。
マスクされたIL-2ポリペプチド構築物の切断率は、プロテアーゼの存在下または非存在下で、および存在する場合、プロテアーゼと共に、マスクされたIL-2ペプチド構築物のインキュベーション後、EDTAの添加などにより様々な時点で不活化した状態で、上述のように、受容体結合アッセイを実施することによって評価される。切断率はまた、還元および非還元ポリアクリルアミドゲル電気泳動(PAGE)、および質量分析による全質量およびペプチドマップ分析を用いて評価される。切断率はまた、マスクされたIL-2ポリペプチド構築物が、ヒト、マウス、またはカニクイザルの末梢血リンパ球、または正常なヒト組織もしくはヒト腫瘍組織に曝露されるエクスビボアッセイを使用して評価される。
実施例1で生成されたマスクされたIL-2ポリペプチド構築物を用いた処理後の、CTLL2、YT、TF1B、LGL、HH、およびCT6などのIL-2応答性組織培養細胞株の増殖が評価される。マスクされたIL-2ポリペプチド構築物が関与する実験では、細胞を、IL-2を欠く培地中で96ウェルの組織培養プレートに2~4時間播種し、次いで様々な濃度のマスクされたIL-2ポリペプチド構築物で処理する。37度で24~48時間インキュベーションした後、細胞数は、MTS、アラマーブルー、ルシフェラーゼ、または類似の代謝検出試薬の添加、およびプレート分光光度計リーダーによって検出された比色、蛍光、またはルシフェラーゼの読み取り値によって決定される。
実施例1で生成されたマスクされたIL-2ポリペプチド構築物による処理後のシグナル伝達性転写因子5(STAT5)の活性化も評価される。PBMCは、指定の期間、構築物で処理され、その後直ちに固定されて、STAT5などのタンパク質のリン酸化状態を維持する。一部の実験では、一部のPBMCは比較のために対照で処理される。一部の実験では、一部のPBMCは、マスクされたIL-2ポリペプチド処理の対照としてアルデスロイキンで処理される。一部の実験では、マスクされたIL-2ポリペプチド構築物を、プロテアーゼ切断(例えば、活性化)を伴う、または伴わない条件下で試験する。一部の実験では、PBMCは、10分、15分、20分、または25分間、処理される。一部の実験では、各構築物、ならびにアルデスロイキンおよび/または他の対照は、0.0001nM~500nMの範囲の一つまたは複数の濃度など、一つまたは複数の濃度で投与される。一部の実験では、固定および透過化PBMCは、次いで、リン酸化STAT5(ホスホ-STAT5)に特異的な抗体で染色され、フローサイトメトリーによって分析される。一部の実験では、STAT5の総レベルおよびリン酸化レベルが測定される。NK細胞、CD8+T細胞、CD4+T細胞、および/またはTreg細胞などの特定の細胞タイプのホスホ-STAT5状態は、特定の細胞タイプの染色によって決定される。一部の実験では、NK細胞はCD45+ CD3-CD56+として染色され、CD8+ T細胞はCD45+ CD3+ CD8+として染色され、CD4+ T細胞はCD45+ CD3+ CD4+ CD25-として染色され、Treg細胞はCD45+ CD3+ CD4+ CD25+ FOXP3+として染色される。
薬物動態
実施例1で生成されたマスクされたIL-2ポリペプチド構築物の薬物動態が、マウスモデルを使用してインビボで評価される。
実施例1で生成されたマスクされたIL-2ポリペプチド構築物のインビボでの生物活性が、C57BL/6マウスなどのマウスモデルを使用してインビボで評価される。マウスを構築物で処理し、インビボでの生物活性を評価する。一部の実験では、一部のマウスは比較のために対照で処理される。一部の実験では、一部のマウスは、マスクされたIL-2ポリペプチド処理の対照としてアルデスロイキンで処理される。一部の実験では、治療されるマウスは腫瘍を有する。一部の実験では、治療されるマウスは腫瘍を有さない。一部の実験では、免疫細胞の用量依存性拡大がマウスで評価される。一部の実験では、マウスは、構築物、アルデスロイキン、または他の対照の様々な用量で処置される。一部の実験では、マウスは二週間にわたって処置される。様々な時点でマウスから血液を採取し、次いで対象の免疫細胞マーカーに対する抗体を使用して染色する。一部の実験では、CD8+ T細胞、NK細胞、およびTreg細胞などの特定の循環細胞タイプの増殖および拡大の縦断的動態、ならびにCD8+ T細胞およびNK細胞とCD4+ CD25+ FoxP3+ Treg細胞との比率も決定される。一部の実験では、マウスは、器官の湿重量および組織学によって決定される肺および肝臓などの特定の器官における浮腫およびリンパ球浸潤を評価することによって、血管漏出について評価される。
実施例1で生成されたマスクされたIL-2ポリペプチド構築物で処置されたマウスモデルにおいて、インビボで腫瘍を浸潤する免疫細胞の表現型が評価される。マウスを構築物で処理し、腫瘍浸潤性免疫細胞の表現型を評価する。一部の実験では、一部のマウスは比較のために対照で処理される。一部の実験では、一部のマウスは、マスクされたIL-2ポリペプチド処理の対照としてアルデスロイキンで処理される。腫瘍担持マウスは、構築物、アルデスロイキン、または別の対照で治療され、腫瘍、肝臓、肺、および脾臓などの組織、ならびに血液は、初回投与の5日後、7日後、または10日後など、初回投与後の様々な時点で採取される。一部の実験では、免疫細胞は、腫瘍、組織、および血液から単離され、フローサイトメトリーを使用して表現型評価の対象となる。一部の実験では、単離された免疫細胞は、CD8+T細胞、メモリーCD8+T細胞、活性化NK細胞、CD4+T細胞、およびCD4+Treg細胞などの対象マーカーを使用して評価される。
マスクされたIL-2サイトカイン構築物のインビボでの切断が評価される。一部の研究では、対照抗体が比較のために投与される。一部の研究では、インビボでの切断は、マウスにおいて対象の構築物を投与し、一定期間後、ヒトIgGを捕捉し、次いで例えば、ヒトIgG、CD122、およびIL-2のレベルを測定することによって評価される。
実施例1で生成されたマスクされたIL-2ポリペプチド構築物が、腫瘍根絶を促進し、転移を阻害する能力は、同系MC38、CT26およびB16F10腫瘍モデルなどのマウスモデルを使用してインビボで評価される。
実施例1で生成されたマスクされたIL-2ポリペプチド構築物のインビボでの生物活性が、カニクイザルにおいてインビボで評価される。カニクイザルを構築物で処理し、インビボでの生物活性、薬物動態、および切断を評価する。一部の実験では、一部のサルは比較のために対照で処理される。一部の実験では、一部のサルは、マスクされたIL-2ポリペプチド処理の対照としてアルデスロイキンで処理される。一部の実験では、サルは、構築物、アルデスロイキン、または他の対照の様々な用量で処置される。血液は、様々な時点でサルから採取され、次いで、CD8+ T細胞、メモリーCD8+ T細胞、活性化NK細胞、CD4+ T細胞、およびCD4+ Treg細胞などの特定の細胞タイプ、および/または総リンパ球、Ki67+、および可溶性CD25の用量反応などの対象マーカーについて評価される。一部の実験では、特定の循環T細胞型およびNK細胞型の増殖および拡大の縦断的動態が評価される。一部の実験では、マスクされたIL-2ポリペプチド構築物の薬物動態および切断は、ELISA、PAGE、および質量分析によって決定される。
C57BL/6メスマウスをCharles River Laboratoriesから購入し、試験開始時に8~10週齢であった。MC38腫瘍細胞(マウス当たり5×105細胞)を、各マウスの右脇腹に皮下注射した。約100mm3サイズの腫瘍に到達すると(0日目)、マウスは、PBS中の様々なFc-IL-2構築物の高用量腹腔内投与を一回受けた。投与後5分、3日目、5日目、および7日目に血漿を採取した。
CD122のCysからSerへの変異の概要
CD122マスキングドメイン上の二つの遊離システインをセリンに変異させて、タンパク質の安定性を高め、理論、凝集、酸化、および免疫原性を含むがこれらに限定されない開発可能性のリスクを軽減した。変異体は、対照およびCysからSerへの変異体を、長時間(3週間)、高温(40℃)、複数のpHでインキュベートする加速安定性試験で評価した。システイン変異の影響を評価するために、様々な解析を実施した。結果は、CysからSerへの変異体が、ストレス下での凝集の有意な減少によって示されるように、タンパク質の安定性を明らかに高めたことを実証する。pH8.0で3週間インキュベーションした後、システイン変異を有する構築物は、システイン変異を含有しない対照構築物が、SEC-HPLCにより測定された場合、50パーセント超の凝集を有するのと比較して、低い凝集レベルを呈する。CE-SDSでは、変異システインを有する構築物が、pH6.0およびpH8.0のインキュベーションで非凝集のままであること(>99%)を示し、対照構築物は、最大15パーセントlの凝集レベルを含有した。
安定性試験
サンプルを、40℃に設定したGalaxy 170 S空気インキュベーター中でインキュベートした。20mMクエン酸塩pH5.0、20mMヒスチジンpH6.0、および20mMトリスpH8.0の三つの緩衝系を試験した。各々のpHを、室温で(約27C)較正し、緩衝液を、HCl/NaOHを用いて0.05pH単位内で調整した。緩衝液を0.22umのボトルトップフィルターで濾過した。サンプルを、スピン濃度を介して開始緩衝液におよそ3000倍緩衝液交換した。サンプルアリコートを、0、1、3、7、14、および21日目に滅菌条件下で除去し、-80℃で保存した後、以下の分析試験で評価した。
HPLCシステムを使用して、インキュベートされたサンプル中の凝集レベルを評価した。システムは、分子量標準と共に較正された。高分子量種(「HMWS」)のレベルを各サンプルで測定した。HMWSの増加は、凝集のレベルの増加を示した。
CE-SDSは、labchipマシンで実行した。一般に、還元剤は、還元条件下での実験に使用された。サンプルを高熱にかけた後、96ウェルPCRプレートにサンプルをロードした。組換えヒトIL-2を低分子量タンパク質対照として使用した。HMWSのレベルは、各サンプルで測定された。HMWSの増加は、凝集のレベルの増加を示した。
使用される構築物は以下の通りである:
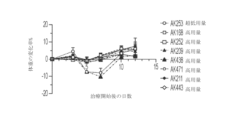
C57BL/6メスマウスをCharles River Laboratoriesから購入し、試験開始時に8~10週齢であった。MC38腫瘍細胞(マウス当たり5×105細胞)を、各マウスの右脇腹に皮下注射した。約100mm3サイズの腫瘍に到達すると(0日目)、マウスを無作為化して、PBS中のFc-IL-2構築物を投与した。0日目、3日目、および6日目にマウスに静脈内投与した。ダイヤルキャリパーを使用して腫瘍体積を計算し(長さ*(幅^2)/2)、体重を週に二回記録した。腫瘍量(2000mm3)または毒性による体重減少(20%)の人道的エンドポイントに到達したときにマウスを犠牲にした。
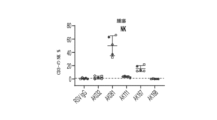
C57BL/6メスマウスをCharles River Laboratoriesから購入し、試験開始時に8~10週齢であった。MC38腫瘍細胞(マウス当たり5×105細胞)を、各マウスの右脇腹に皮下注射した。約100mm3サイズの腫瘍に到達すると(0日目)、マウスを無作為化して、PBS中の非常に低用量レベルのAK253、および高用量レベルの他のすべてのFc-IL-2構築物を投与した。0日目、3日目、および6日目にマウスに静脈内投与した。
C57BL/6メスマウスをCharles River Laboratoriesから購入し、試験開始時に8~10週齢であった。MC38腫瘍細胞(マウス当たり5×105細胞)を、各マウスの右脇腹に皮下注射した。約100mm3サイズの腫瘍に到達すると(0日目)、マウスを無作為化して、PBS中の非常に低用量レベルのAK253、および高用量レベルの他のすべてのFc-IL-2構築物を投与した。0日目、3日目、および6日目にマウスに静脈内投与した。ダイヤルキャリパーを使用して腫瘍体積を計算し(長さ*(幅^2)/2)、体重を週に二回記録した。腫瘍量(2000mm3)または毒性による体重減少(20%)の人道的エンドポイントに到達したときにマウスを犠牲にした。
C57BL/6メスマウスをCharles River Laboratoriesから購入し、試験開始時に8~10週齢であった。MC38腫瘍細胞(マウス当たり5×105細胞)を、各マウスの右脇腹に皮下注射した。約100mm3サイズの腫瘍に到達すると(0日目)、マウスを無作為化して、PBS中の非常に低用量レベルのAK253、および高用量レベルの他のすべてのFc-IL-2構築物を投与した。0日目、3日目、および6日目にマウスに静脈内投与した。
C57BL/6メスマウスをCharles River Laboratoriesから購入し、試験開始時に8~10週齢であった。MC38腫瘍細胞(マウス当たり5×105細胞)を、各マウスの右脇腹に皮下注射した。約100mm3サイズの腫瘍に到達すると(0日目)、マウスを無作為化して、PBS中の非常に低用量レベルのAK253、および高用量レベルの他のすべてのFc-IL-2構築物を投与した。0日目、3日目、および6日目にマウスに静脈内投与した。ダイヤルキャリパーを使用して腫瘍体積を計算し(長さ*(幅^2)/2)、体重を週に二回記録した。腫瘍量(2000mm3)または毒性による体重減少(20%)の人道的エンドポイントに到達したときにマウスを犠牲にした。
C57BL/6メスマウスをCharles River Laboratoriesから購入し、試験開始時に8~10週齢であった。MC38腫瘍細胞(マウス当たり5×105細胞)を、各マウスの右脇腹に皮下注射した。約100mm3サイズの腫瘍に到達すると(0日目)、マウスを無作為化して、PBS中の非常に低用量レベルのAK253、および高用量レベルの他のすべてのFc-IL-2構築物を投与した。0日目、3日目、および6日目にマウスに静脈内投与した。
C57BL/6メスマウスをCharles River Laboratoriesから購入し、試験開始時に8~10週齢であった。MC38腫瘍細胞(マウス当たり5×105細胞)を、各マウスの右脇腹に皮下注射した。約100mm3サイズの腫瘍に到達すると(0日目)、マウスを無作為化して、PBS中の非常に低用量レベルのAK253、および高用量レベルの他のすべてのFc-IL-2構築物を投与した。0日目、3日目、および6日目にマウスに静脈内投与した。ダイヤルキャリパーを使用して腫瘍体積を計算し(長さ*(幅^2)/2)、体重を週に二回記録した。腫瘍量(2000mm3)または毒性による体重減少(20%)の人道的エンドポイントに到達したときにマウスを犠牲にした。
C57BL/6メスマウスをCharles River Laboratoriesから購入し、試験開始時に8~10週齢であった。MC38腫瘍細胞(マウス当たり5×105細胞)を、各マウスの右脇腹に皮下注射した。約100mm3サイズの腫瘍に到達すると(0日目)、マウスを無作為化して、PBS中の非常に低用量レベルのAK253、および高用量レベルの他のすべてのFc-IL-2構築物を投与した。0日目、3日目、および6日目にマウスに静脈内投与した。
C57BL/6メスマウスをCharles River Laboratoriesから購入し、試験開始時に8~10週齢であった。MC38腫瘍細胞(マウス当たり5×105細胞)を、各マウスの右脇腹に皮下注射した。約100mm3サイズの腫瘍に到達すると(0日目)、マウスを無作為化して、PBS中の非常に低用量レベルのAK253、および高用量レベルの他のすべてのFc-IL-2構築物を投与した。0日目、3日目、および6日目にマウスに静脈内投与した。ダイヤルキャリパーを使用して腫瘍体積を計算し(長さ*(幅^2)/2)、体重を週に二回記録した。腫瘍量(2000mm3)または毒性による体重減少(20%)の人道的エンドポイントに到達したときにマウスを犠牲にした。
C57BL/6メスマウスをCharles River Laboratoriesから購入し、試験開始時に8~10週齢であった。MC38腫瘍細胞(マウス当たり5×105細胞)を、各マウスの右脇腹に皮下注射した。約100mm3サイズの腫瘍に到達すると(0日目)、マウスを無作為化して、PBS中の非常に低用量レベルのAK253、および高用量レベルの他のすべてのFc-IL-2構築物を投与した。0日目、3日目、および6日目にマウスに静脈内投与した。組織を採取し、6日目に計量した。
i.NAT対RCC培養上清によるペプチドの切断
切断ペプチドを含む配列(以下に太字で示される)を、各ペプチドの切断の特異性を試験するために、「NAT」(正常隣接組織)または「RCC」(腎細胞癌)培養上清のいずれかでインキュベートした。
この例では、以下の構築物を使用した。
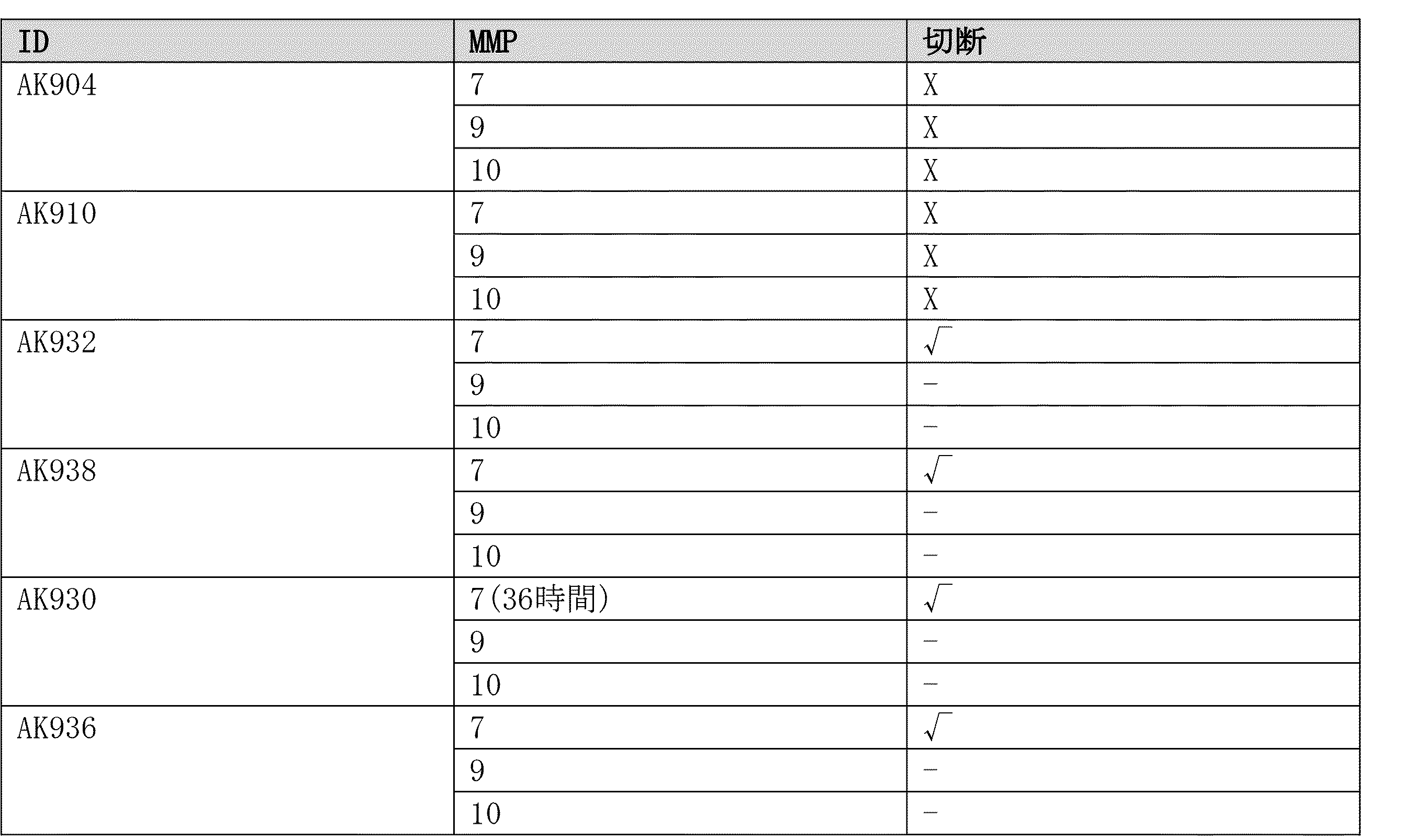
構築物を、MMP7、9および10とインキュベートした。各構築物の切断を、SDS-PAGEにより分析し、HEK-Blue IL-2バイオアッセイにより確認した。
HEK-Blueアッセイを以下のように実施した:
条件:細胞プレート:96ウェルプレート。細胞密度:50K cls/ウェル。HEK Blue検出の時点を試験した:1時間。構築物番号:試験した構築物の合計14個。
アッセイフローチャート:
本実施例は、例示的なIL-12構築物のマスキングおよび切断を示す。
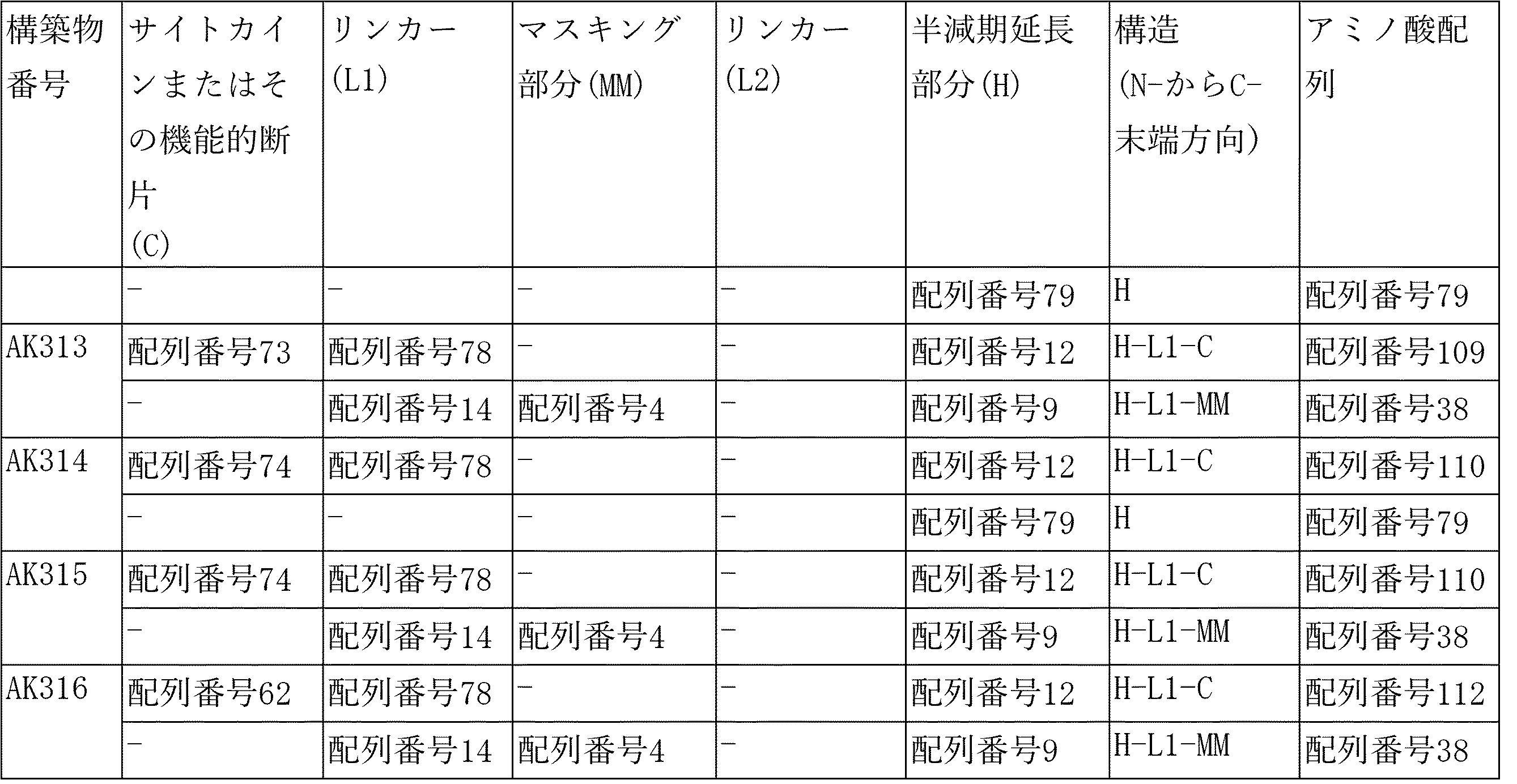
この例では、以下の構築物を使用した。
各構築物の切断ペプチドを、各カラムの最上部に示す。
IL-12構築物の1uMを、90ulのコンディショニング培地で一晩、または90ulの血漿と、37Cで、以下の時間(d1-d2-d4-d7-d9-d11)インキュベートした。切断率は、ウェスタンブロット抗ヒトIL-12および抗ヒトIL-12Rbを使用して、切断構築物/(切断構築物+インタクト構築物)の比率として計算される。ヒト組織条件培地によるこれらの構築物の活性化は、0.05x106 HEK-Blue細胞を37.5nMの構築物と共に24時間インキュベートした後、IL-12受容体シグナル伝達アッセイを使用して評価される。
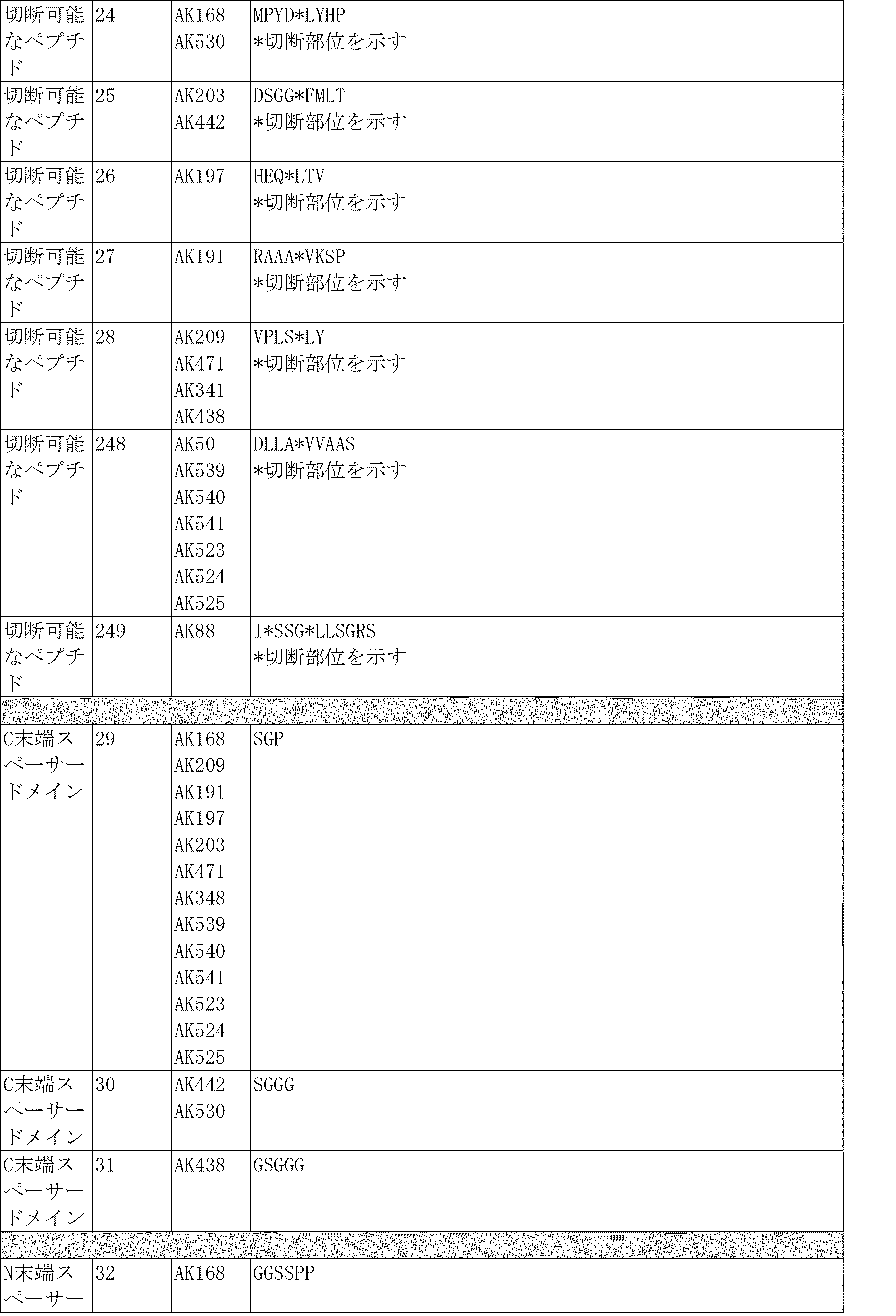
-RAAAVKSP
-ISSGLLSGRS
-MPYDLYHP
RAAAVKSP>ISSGLLSGRS>MPYDLYHP
HEK-Blue IL-12細胞を用いたIL-12分子の試験:
Invivogenにより開発されたHEK-Blue IL-12レポーター細胞は、JAK-STAT経路の活性化を監視するために特別に設計されている。これらの細胞は、HEK293細胞にヒトIL-12Rβ1およびIL-12Rβ2遺伝子、ならびにヒトTyK2、JAK2、およびSTAT4遺伝子を安定的トランスフェクションすることによって生成され、完全に機能的なIL-12シグナル伝達経路を得た。さらに、STAT4誘導性SEAPレポーター遺伝子も導入された。刺激を受けると、HEK-Blue(商標)IL-12細胞はSTAT4の活性化とその後のSEAPの分泌をトリガする。STAT4誘導性SEAPのレベルは、QUANTI-Blue(商標)を使用して容易に監視することができる。HEK-Blue IL-12細胞は、ヒトまたはマウスIL-12の機能性、毒性、および可変用量効果を検証するために使用することができる。HEK Blue IL-12細胞を、約80%のコンフルエントまで継代培地中で増殖させた。アッセイ培地中の洗浄された単一細胞懸濁液を播種し、アッセイ培地中のIL-12分子の段階希釈物を細胞に添加した。プレートを、37°Cで24時間インキュベートした。24時間後、Quanti-Blue溶液(Invivogen)を調製し、細胞上清をQuanti-Blue溶液に加え、37°Cで1~2時間インキュベートした。625nmでの吸光度を測定した。データ解析はGraphpad Prism、バージョン8.3で行った。生データからバックグラウンドを減算し、データは非線形にフィットさせた。[アゴニスト]対応答-可変勾配(四つのパラメータ)。各IL-12構築物のEC50値が報告された。
結果を以下の表、ならびに図47、図48A、および図48Bに示す。
構築物の切断は、例示的なプロテアーゼMMP7、9および10を使用して試験した。
バッチ1
バッチ2
バッチ3
この例では、以下の構築物を使用した。
-陽性対照:マスクされていないAK904
-切断対照:マスクされた、切断不可能AK910
- サイトカイン基質構築物:AK930
- マスク-サブステート構築物:AK936
Balb/cマウスにCT26細胞を皮下注射し、腫瘍増殖を監視した。腫瘍サイズが175~225mm3に達すると、動物を無作為化した(群当たりn=4)。被験物質の単回静脈内注射を、表に従って用量レベルで投与した。体重を0日目および5日目に測定した。5日目に、動物を犠牲にし、免疫表現型解析のために組織を採取した。
図55A:高用量のAK904およびAK931で処置されたマウス、ならびに低用量および高用量のAK936で処置されたマウスは、体重の有意な減少を示した。
図56Aおよび図56B:マウスは、血液および脾臓中のNK細胞%における用量依存的な増加を示した。
図57A、図57B、および図57C: マウスは、血液、脾臓、および腫瘍中のNK細胞において、増殖マーカーKi67の用量依存的な増加を示した。
図58A:マスクされていないAK904で処置されたマウスは、血液中のCD8 T細胞%の用量依存的な増加を示した。
図59Aおよび図59B:マウスは、血液および脾臓中のCD8 T細胞において、増殖マーカーKi67の用量依存的な増加を示した。
図60Aおよび図60B:AK904およびAK936で処置されたマウスは、血液および脾臓において用量依存的なCD8/Treg比の増加を示した。
C57BL/6JマウスにMC38細胞を皮下注射し、腫瘍増殖を監視した。腫瘍サイズが175~225mm3に達すると、動物は無作為化された(群当たりn=4、AK904および群当たりn=8を含有するビヒクル群を除く)。被験物質の単回静脈内注射を、表に従って用量レベルで投与した。PK解析のため、5分、2時間、6時間、および5日目に血漿を採取した。体重を0日目および5日目に測定した。5日目に、動物を犠牲にし、免疫表現型解析のために組織を採取した。
図61A:高用量のAK904およびAK936で処置されたマウスは、体重の有意な減少を示した。
図62A:分子AK910、AK930、およびAK936の間に類似のPKプロファイルが観察される。
図63A~図63C:マウスは、血液、脾臓、および腫瘍中のNK細胞%における用量依存的な増加を示した。
図64Aおよび図64B:AK904およびAK936で処置されたマウスは、血液および脾臓においてCD8 T細胞%の増加を示した。
図65Aおよび図65B:AK90およびAK936で処置されたマウスは、血液および脾臓においてCD8/Treg比の増加を示した。
この実施例では、以下の構築物を使用した。
ヒト原発腫瘍組織を穏やかに解離し、1、2または3日間培養した(30mlのRPMI中500mg)。腫瘍およびその微小環境によって分泌されるプロテアーゼを含有する条件培地(90μl)を収集し、AK923分子(1μM)と共に24時間、37Cでインキュベーションした。切断した分子の割合を、蛍光トリプレックスウェスタンブロットを使用して定量した。切断頻度は、薬物を切断できた腫瘍サンプルの割合を表す。結果を図66に示す。
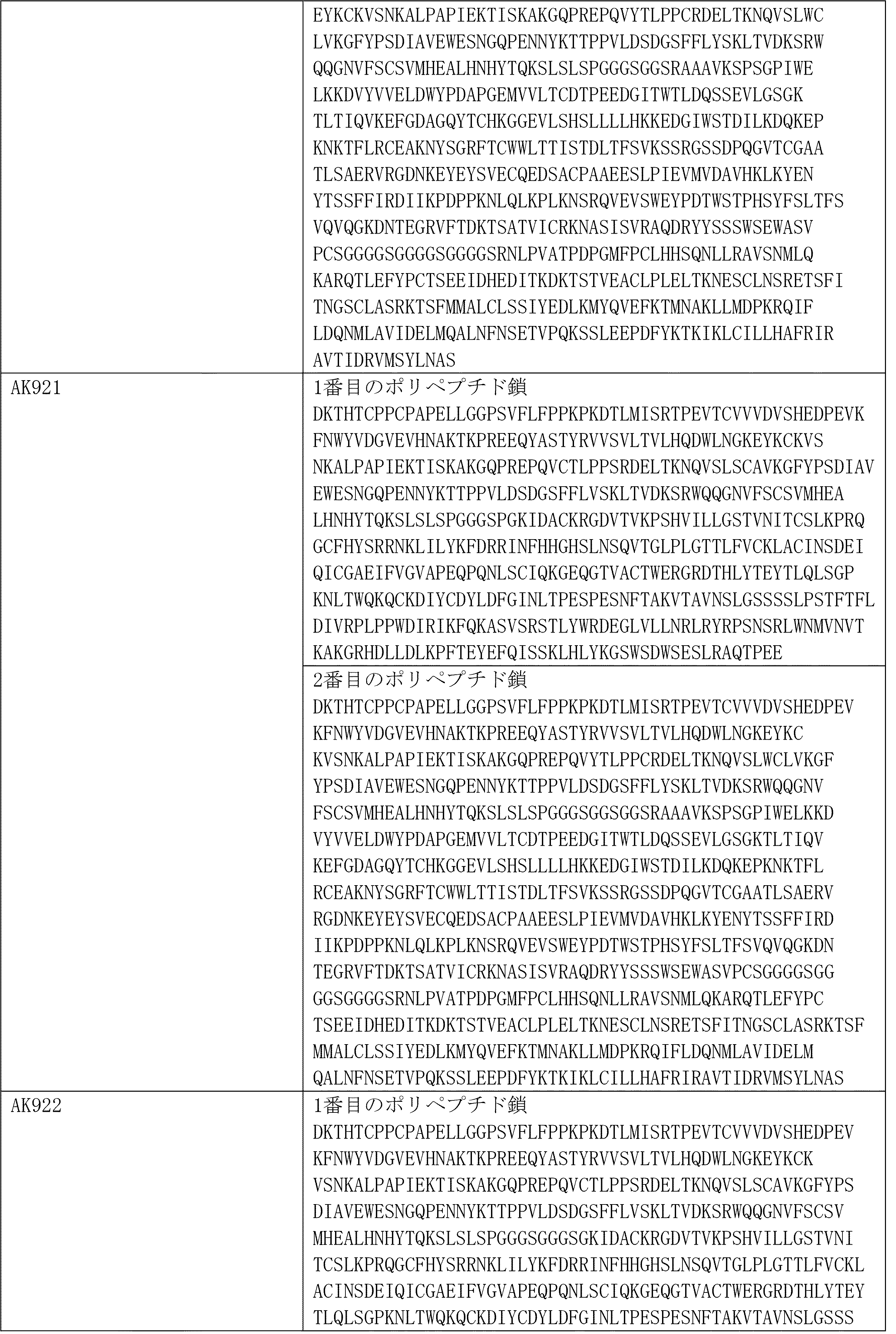
以下の表は、「AK」参照番号で標識された分子の完全な配列を示す。配列の構成要素部分、ならびにそれらが分子の鎖内で組み立てられる順番も示されている。個々の鎖は、「DNA」参照番号で標識されている:
Claims (203)
- (i)治療部分、(ii)担体部分、および(iii)アミノ酸配列DLLAVVAASまたはISSGLLSGRSからなるタンパク質分解的に切断可能なペプチド(CP)を含むタンパク質分解的に切断可能なペプチドリンカーを含む、ポリペプチド薬物構築物。
- 前記タンパク質分解的に切断可能なペプチドリンカーが、9~25アミノ酸長である、請求項2に記載のポリペプチド薬物構築物。
- 前記スペーサードメインは、アミノ酸残基G、SおよびPが豊富である、請求項2または請求項3に記載のポリペプチド薬物構築物。
- 前記スペーサードメインは、G、SおよびPからなる群から選択されるアミノ酸残基タイプのみを含む、請求項4に記載のポリペプチド薬物構築物。
- 前記第一のスペーサードメイン(SD1)が、3~6アミノ酸長である、請求項2~5のいずれか一項に記載のポリペプチド薬物構築物。
- 前記第二のスペーサードメイン(SD2)が、3~6アミノ酸長である、請求項2~6のいずれか一項に記載のポリペプチド薬物構築物。
- 前記第二のスペーサードメイン(SD2)が、前記アミノ酸配列SGPを含む、請求項2~7のいずれか一項に記載のポリペプチド薬物構築物。
- 前記第二のスペーサードメイン(SD2)SD2が、前記アミノ酸配列SGPを有する、請求項2~8のいずれか一項に記載のポリペプチド薬物構築物。
- 前記タンパク質分解的に切断可能なペプチドリンカーが、前記治療部分に直接共有結合している、請求項1~15のいずれか一項に記載のポリペプチド薬物構築物。
- 前記タンパク質分解的に切断可能なペプチドリンカーが、前記治療部分と前記担体部分との間の前記薬物構築物内に位置する、請求項1~16のいずれか一項に記載のポリペプチド薬物構築物。
- 前記タンパク質分解的に切断可能なペプチドリンカーが、前記担体部分内に位置する、請求項1~15のいずれか一項に記載のポリペプチド薬物構築物。
- 前記ポリペプチド薬物構築物が、単一のポリペプチド鎖を含む、請求項1~18のいずれか一項に記載のポリペプチド薬物構築物。
- 前記ポリペプチド薬物構築物が、二つ以上のポリペプチド鎖を含む、請求項1~19のいずれか一項に記載のポリペプチド薬物構築物。
- 前記タンパク質分解的に切断可能なペプチドリンカーが、前記治療部分と同じポリペプチド鎖に存在する、請求項20に記載のポリペプチド薬物構築物。
- 前記タンパク質分解的に切断可能なペプチドリンカーが、前記治療部分とは異なるポリペプチド鎖に存在する、請求項20に記載のポリペプチド薬物構築物。
- 前記ポリペプチド薬物構築物が、プロドラッグである、請求項1~22のいずれか一項に記載のポリペプチド薬物構築物。
- マスキング部分をさらに含む、請求項1~23のいずれか一項に記載のポリペプチド薬物構築物。
- 前記マスキング部分が、前記治療部分と同じポリペプチド鎖に存在する、請求項24に記載のポリペプチド薬物構築物。
- 前記マスキング部分が、前記治療部分とは異なるポリペプチド鎖に存在する、請求項24に記載のポリペプチド薬物構築物。
- 前記ポリペプチド薬物構築物が、半減期延長部分を含む、請求項1~26のいずれか一項に記載のポリペプチド薬物構築物。
- 前記半減期延長部分が、抗体またはその断片を含む、請求項27に記載のポリペプチド薬物構築物。
- 前記半減期延長部分が、第一および第二の半減期延長部分を含む、請求項27に記載のポリペプチド薬物構築物。
- 前記プロドラッグがサイトカインプロドラッグであり、前記治療部分がサイトカイン部分である、請求項1~29のいずれか一項に記載のポリペプチド薬物構築物。
- 前記サイトカインプロドラッグがマスキング部分を含み、前記マスキング部分がサイトカイン受容体の細胞外ドメインのドメインを含む、請求項30に記載のサイトカインプロドラッグ。
- マスクされたサイトカインであって、
a)第一のリンカーを介して第一の半減期延長部分に連結されたマスキング部分を含む第一のポリペプチド鎖と、
b)第二のリンカーを介して第二の半減期延長部分に連結されたそのサイトカイン部分を含む第二のポリペプチド鎖とを含み、
前記第一の半減期延長部分が前記第二の半減期延長部分と会合し、
少なくとも前記第一のリンカーまたは前記第二のリンカーが、アミノ酸配列DLLAVVAASまたはISSGLLSGRSからなるタンパク質分解的に切断可能なペプチド(CP)を含む、タンパク質分解的に切断可能なペプチドリンカーである、マスクされたサイトカイン。 - 前記第一のポリペプチド鎖が、
を含み、
前記第二のポリペプチド鎖が、
を含み、
式中、HL1は前記第一の半減期延長ドメインであり、L1は前記第一のリンカーであり、MMは前記マスキング部分であり、HL2は前記第二の半減期延長ドメインであり、L2は前記第二のリンカーであり、Cは前記サイトカイン部分であり、
前記第一の半減期延長部分が前記第二の半減期延長部分と会合し、
少なくとも前記第一のリンカーまたは前記第二のリンカーが、アミノ酸配列DLLAVVAASまたはISSGLLSGRSからなるタンパク質分解的に切断可能なペプチド(CP)を含む、タンパク質分解的に切断可能なペプチドリンカーである、請求項32に記載のマスクされたサイトカイン。 - 前記第二のリンカーが、前記タンパク質分解的に切断可能なリンカーであり、前記第一のリンカーが切断不可能なリンカーである、請求項33に記載のマスクされたサイトカイン。
- 前記第一のリンカーが、前記タンパク質分解的に切断可能なリンカーであり、前記第二のリンカーが切断不可能なリンカーである、請求項33に記載のマスクされたサイトカイン。
- 前記タンパク質分解的に切断可能なペプチドリンカーが、9~25アミノ酸長である、請求項38に記載のマスクされたサイトカイン。
- 前記スペーサードメインは、アミノ酸残基G、SおよびPが豊富である、請求項38または請求項39に記載のマスクされたサイトカイン。
- 前記スペーサードメインは、G、SおよびPからなる群から選択されるアミノ酸残基タイプのみを含む、請求項40に記載のマスクされたサイトカイン。
- 前記第一のスペーサードメイン(SD1)が、3~6アミノ酸長である、請求項38~41のいずれか一項に記載のマスクされたサイトカイン。
- 前記第二のスペーサードメイン(SD2)が、3~6アミノ酸長である、請求項38~42のいずれか一項に記載のマスクされたサイトカイン。
- 前記第二のスペーサードメイン(SD2)が、前記アミノ酸配列SGPを含む、請求項38~43のいずれか一項に記載のマスクされたサイトカイン。
- 前記第二のスペーサードメイン(SD2)が、前記アミノ酸配列SGPを有する、請求項38~44のいずれか一項に記載のマスクされたサイトカイン。
- 前記第二のリンカーが切断不可能なリンカーである、請求項36または請求項37に記載のマスクされたサイトカイン。
- 前記切断不可能なリンカーが、3~25アミノ酸長である、請求項34、請求項35、または請求項52に記載のマスクされたサイトカイン。
- 前記切断不可能なリンカーは、アミノ酸残基G、SおよびPが豊富である、請求項53に記載のマスクされたサイトカイン。
- 切断不可能なリンカーが、PGSGS(配列番号14)のアミノ酸配列を含む、請求項53または請求項54に記載のマスクされたサイトカイン。
- 前記切断不可能なリンカーが、GGSSPPGGGSSGGGSGP(配列番号23)のアミノ酸配列を含む、請求項53または請求項54に記載のマスクされたサイトカイン。
- 前記半減期延長ドメインが、第一の半減期延長ドメインおよび第二の半減期延長ドメインを含む、請求項36または請求項37に記載のマスクされたサイトカイン。
- 前記第一の半減期延長ドメインは、第一のFcドメインもしくはその断片を含み、前記第二のFcドメインは、Fcドメインもしくはその断片を含む、請求項29に記載のポリペプチド薬物構築物、または請求項33~35または請求項57に記載のマスクされたサイトカイン。
- 前記第一のFcドメインは、CH3ドメインまたはその断片を含み、前記第二のFcドメインは、CH3ドメインまたはその断片を含む、請求項58に記載のポリペプチド薬物構築物またはマスクされたサイトカイン。
- 前記第一および第二の半減期延長ドメインが、それぞれIgG1 Fcドメインまたはその断片である、請求項58に記載のポリペプチド薬物構築物またはマスクされたサイトカイン。
- 前記第一および/または第二のFcドメインがそれぞれ、前記第一および前記第二の半減期延長ドメインの非共有結合を促進する一つまたは複数の修飾を含有する、請求項58~60のいずれか一項に記載のポリペプチド薬物構築物またはマスクされたサイトカイン。
- 前記第一の半減期延長ドメインは、Kabat EUナンバリングシステムに従って番号付けされた、変異Y349C;T366S;L38AおよびY407Vを含むIgG1 Fcドメインまたはその断片を含んで、前記第一の半減期延長ドメインに「ホール」を形成し、前記第二の半減期延長ドメインは、変異S354CおよびT366Wを含むIgG1 Fcドメインまたはその断片を含んで、前記第二の半減期延長ドメインに「ノブ」を形成する、請求項61に記載のプリペプチド薬物構築物またはマスクされたサイトカイン。
- 前記第一および第二の半減期延長ドメインは、それぞれ、IgG1 Fcドメインまたはその断片であり、それぞれは、Kabat EUナンバリングシステムに従って番号付けされた位置297にアミノ置換を含む、請求項61または請求項62に記載のポリペプチド薬物構築物またはマスクされたサイトカイン。
- 前記第一および第二の半減期延長ドメインは、それぞれ、IgG1 Fcドメインまたはその断片であり、それぞれは、Kabat EUナンバリングシステムに従って番号付けされたN297Aのアミノ置換を含む、請求項63に記載のポリペプチド薬物構築物またはマスクされたサイトカイン。
- 前記第一および第二の半減期延長ドメインは、それぞれ、IgG1 Fcドメインまたはその断片であり、それぞれは、Kabat EUナンバリングシステムに従って番号付けされた位置253にアミノ置換を含む、請求項61~64のいずれか一項に記載のポリペプチド薬物構築物またはマスクされたサイトカイン。
- 前記第一および第二の半減期延長ドメインは、それぞれ、IgG1 Fcドメインまたはその断片であり、それぞれは、Kabat EUナンバリングシステムに従って番号付けされたI253Aのアミノ置換を含む、請求項65に記載のポリペプチド薬物構築物またはマスクされたサイトカイン。
- 前記第一の半減期延長ドメインは、配列番号9のアミノ酸配列を含み、その前記第二の半減期延長ドメインは、配列番号12のアミノ酸配列を含む、請求項58に記載のポリペプチド薬物構築物またはマスクされたサイトカイン。
- 前記第一の半減期延長ドメインは、配列番号10のアミノ酸配列を含み、その前記第二の半減期延長ドメインは、配列番号13のアミノ酸配列を含む、請求項58に記載のポリペプチド薬物構築物またはマスクされたサイトカイン。
- 前記サイトカイン部分が、野生型サイトカイン部分またはバリアントサイトカイン部分を含む、請求項31に記載のサイトカインプロドラッグ、または請求項32~68のいずれか一項に記載のマスクされたサイトカイン。
- 前記サイトカイン部分がIL-2サイトカイン部分である、請求項69に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-2サイトカイン部分がIL-2サイトカインまたはその断片を含む、請求項70に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-2サイトカインまたはその機能的断片が、配列番号2を有する成熟IL-2の配列と比較して修飾されている、請求項70または請求項71に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記修飾されたIL-2サイトカインまたはその機能的断片が、配列番号2を有する成熟IL-2の配列に対して、修飾R38A、F42A、Y45A、およびE62Aを含む、請求項72に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記修飾されたIL-2サイトカインまたはその機能的断片が、配列番号2を有する成熟IL-2の配列に対して、修飾C125Aを含む、請求項72または請求項73に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記修飾されたIL-2サイトカインまたはその機能的断片が、配列番号2を有する成熟IL-2の配列に対して、R38A、F42A、Y45A、E62AおよびC125Aを含む、請求項72に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-2サイトカインまたはその機能的断片が、配列番号3のアミノ酸配列を含む、請求項72に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記マスキング部分が、IL-2Rβまたはその断片、部分、もしくはバリアントを含む、請求項72~76のいずれか一項に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-2Rβまたはその断片、部分、もしくはバリアントが、配列番号4のアミノ酸配列を含む、請求項77に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-2Rβまたはその断片、部分、もしくはバリアントが、配列番号4のIL-2βと比較して、アミノ酸位置C122に変異を有する、請求項77に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-2Rβまたはその断片、部分、もしくはバリアントが、配列番号4のIL-2βと比較して、アミノ酸位置C168に変異を有する、請求項77または請求項79に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-2Rβまたはその断片、部分、もしくはバリアントが、配列番号4のIL-2βと比較して、アミノ酸位置C122およびC168に変異を有する、請求項80に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-2Rβまたはその断片、部分、もしくはバリアントが、配列番号4のIL-2βと比較して、変異C122SおよびC168Sを有する、請求項81に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-2Rβまたはその断片、部分、もしくはバリアントが、配列番号5のアミノ酸配列を含む、請求項77に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記サイトカイン部分がIL-12サイトカイン部分である、請求項69に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-2サイトカイン部分がIL-2サイトカインまたはその断片を含む、請求項84に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-12サイトカインまたはその機能的断片が、IL-12p35ポリペプチドまたはその機能的断片に共有結合したIL-12p40ポリペプチドまたはその機能的断片を含む、請求項85に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-12p40-IL-12p35リンカーが、5~20アミノ酸長である、請求項86に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-12p40-IL-12p35リンカーは、アミノ酸残基GおよびSが豊富である、請求項86または請求項87に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-12p40-IL-12p35リンカーが、配列番号 116(GGGGSGGGGSGGGGS)を含む、請求項86~88のいずれかに記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-12p40ポリペプチドが、配列番号204(本明細書のIL-12サイトカイン部分表に示される通り)、または配列番号1(本明細書のIL-12サイトカイン部分表に示される通り)のアミノ酸配列と比較して、少なくとも一つのアミノ酸修飾を有するアミノ酸配列を含む、請求項86~89のいずれかに記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- IL-12p40ポリペプチドが、配列番号1(本明細書のIL-12サイトカイン部分表に示される通り)を含む、請求項90に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- IL-12p40ポリペプチドが、配列番号204(本明細書のIL-12サイトカイン部分表に示される通り)のアミノ酸配列と比較して、GAG結合ドメイン(KSKREKKDRV)に対する少なくとも一つのアミノ酸修飾を含む、請求項90に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- IL-12p40ポリペプチドが、配列番号205(本明細書のIL-12サイトカイン部分表に示される通り)を含む、請求項92に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- IL-12p40ポリペプチドが、配列番号206(本明細書のIL-12サイトカイン部分表に示される通り)を含む、請求項92に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- IL-12p40ポリペプチドが、配列番号204(本明細書のIL-12サイトカイン部分表に示される通り)のアミノ酸配列と比較して、一つまたは複数のシステイン置換変異を有するアミノ酸配列を含む、請求項90~94のいずれかに記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-12p40ポリペプチドが、配列番号207(本明細書のIL-12サイトカイン部分表に示される通り)を含む、請求項95に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-12p40ポリペプチドが、配列番号208(本明細書のIL-12サイトカイン部分表に示される通り)を含む、請求項95に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-12p35ポリペプチドが、配列番号209、または配列番号209(本明細書のIL-12サイトカイン部分表に示される通り)のアミノ酸配列と比較して、少なくとも一つのアミノ酸修飾を有するアミノ酸配列を含む、請求項86~98のいずれかに記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-12p35ポリペプチドが、配列番号209(本明細書のIL-12サイトカイン部分表に示される通り)を含む、請求項98に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-12サイトカインまたはその機能的断片が、配列番号210(本明細書のIL-12サイトカイン部分表に示される通り)を含む、請求項86に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
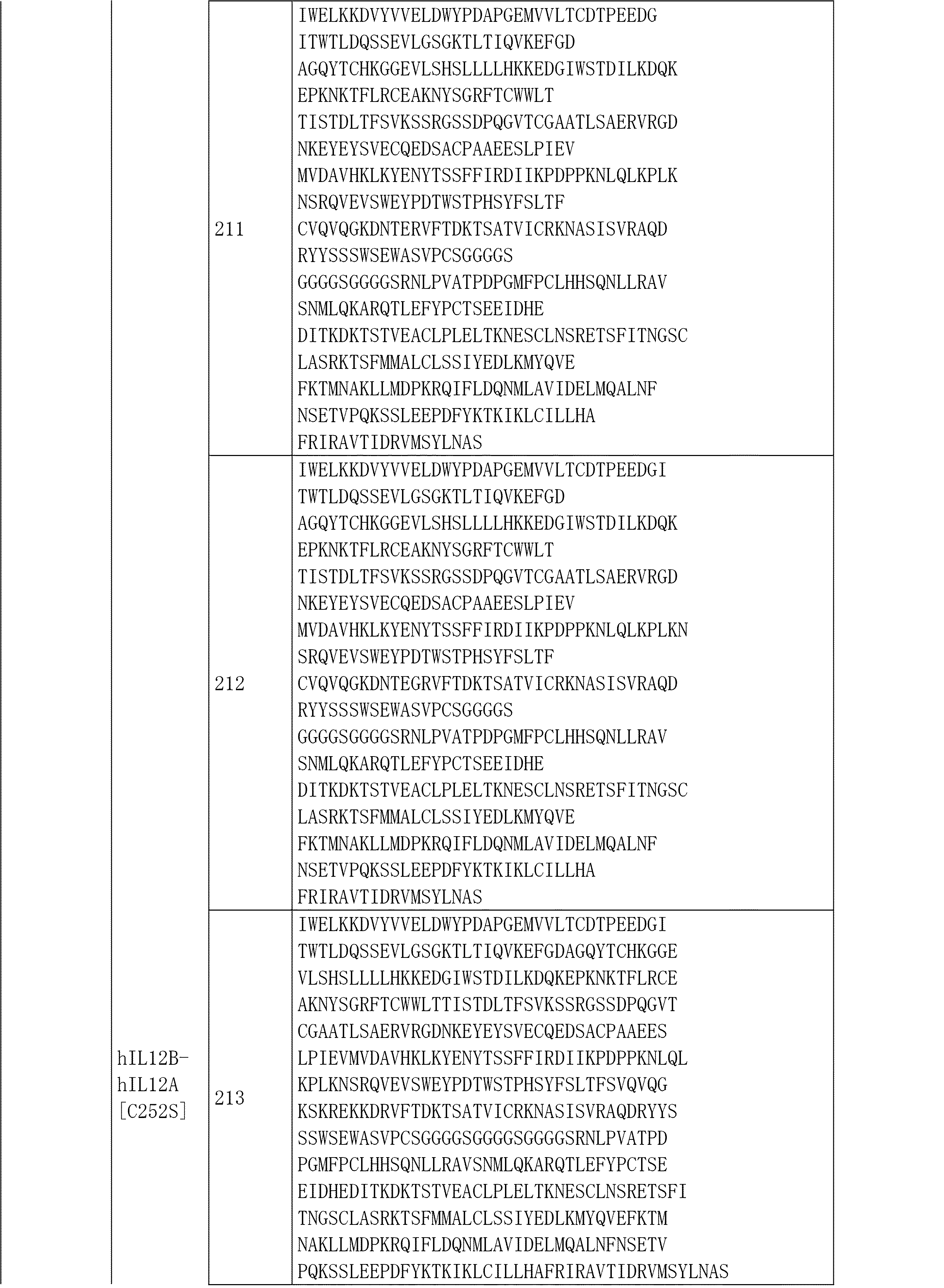
- 前記IL-12サイトカインまたはその機能的断片が、配列番号211(本明細書のIL-12サイトカイン部分表に示される通り)を含む、請求項86に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-12サイトカインまたはその機能的断片が、配列番号212(本明細書のIL-12サイトカイン部分表に示される通り)を含む、請求項86に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-12サイトカインまたはその機能的断片が、配列番号213(本明細書のIL-12サイトカイン部分表に示される通り)を含む、請求項86に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-12サイトカインまたはその機能的断片が、配列番号214(本明細書のIL-12サイトカイン部分表に示される通り)を含む、請求項86に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記マスキング部分がIL-12サイトカイン受容体、またはそのサブユニットもしくは機能的断片を含む、請求項84~104のいずれかに記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記マスキング部分が、ヒトIL-12Rβ1の細胞外ドメイン、またはIL-12に対する親和性を保持するか、そうでなければ実証するその断片、部分、もしくはバリアントを含む、請求項84~105のいずれかに記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記マスキング部分が、ヒトIL-12Rβ1の残基24~237、すなわち配列番号215を有する配列(本明細書のIL-12マスキング部分表に示される通り)を含む、請求項106に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記マスキング部分が、ヒトIL-12Rβ1の残基24~545、すなわち配列番号216を有する配列(本明細書のIL-12マスキング部分表に示される通り)を含む、請求項106に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記マスキング部分が、ヒトIL-12Rβ2の細胞外ドメイン、またはIL-12に対する親和性を保持するか、そうでなければ実証するその断片、部分、もしくはバリアントを含む、請求項84~105のいずれかに記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記マスキング部分が、ヒトIL-12Rβ2の残基24~212、すなわち配列番号217を有する配列(本明細書のIL-12マスキング部分表に示される通り)を含む、請求項109に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記マスキング部分が、ヒトIL-12Rβ2の残基24~222、すなわち配列番号218を有する配列を含むか、または前記マスキング部分が、ヒトIL-12Rβ2の残基24~227、すなわち配列番号222を有する配列(本明細書のIL-12マスキング部分表に示される通り)を含む、請求項109に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記マスキング部分が、ヒトIL-12Rβ2の残基24~319、すなわち配列番号219を有する配列(本明細書のIL-12マスキング部分表に示される通り)を含む、請求項109に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記マスキング部分が、配列番号219の配列と比較して、少なくとも一つのアミノ酸修飾を含み、任意選択的に、前記修飾が、システイン置換変異(本明細書のIL-12マスキング部分表に示される通り)である、請求項109に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記マスキング部分が、配列番号220(本明細書のIL-12マスキング部分表に示される通り)を含む、請求項109に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記マスキング部分が、ヒトIL-12Rβ2の残基24~622、すなわち配列番号221を有する配列(本明細書のIL-12マスキング部分表に示される通り)を含む、請求項109に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記サイトカイン部分がIL-15サイトカイン部分である、請求項69に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-2サイトカイン部分がIL-15サイトカインまたはその断片を含む、請求項116に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記マスクされたサイトカインが、IL-15Rαサブユニットまたはその機能的断片(「IL-15Rαドメイン」)を含むドメインをさらに含む、請求項116または請求項117に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記サイトカイン部分が、IL-15サイトカイン部分であり、前記マスクされたサイトカインが、IL-15Rαサブユニットまたはその機能的断片(「IL-15Rαドメイン」)を含むドメインをさらに含み、前記IL-15Rαドメインと前記IL-15サイトカイン部分は、前記構築物中の異なるポリペプチド鎖に存在し、前記IL-15Rαドメインは前記IL-15サイトカイン部分に非共有結合している、請求項118に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-15Rαドメインが、前記野生型スシドメインsIL-15Rαの配列と比較して、位置R26にアミノ酸置換を含む、請求項118または請求項119に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-15Rαドメインが、前記野生型スシドメインsIL-15Rαの配列と比較して、位置R35にアミノ酸置換を含む、請求項118~120のいずれか一項に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-15Rαドメインが、前記野生型スシドメインsIL-15Rαの配列と比較して、位置R26およびR35にアミノ酸置換を含む、請求項118~121のいずれか一項に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-15サイトカインまたはその断片が、配列番号2またはその機能的断片(本明細書のIL-15サイトカイン部分表に示される通り)を含む、請求項117~120のいずれか一項に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-15サイトカインまたはその機能的断片が、配列番号224(本明細書のIL-15サイトカイン部分表に示される通り)のアミノ酸配列を含む、請求項123に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-15サイトカインまたはその機能的断片が、配列番号224(本明細書のIL-15サイトカイン部分表に示される通り)のアミノ酸配列と比較して、少なくとも一つのアミノ酸修飾を有するアミノ酸配列を含む、請求項117~120のいずれか一項に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-15サイトカインまたはその機能的断片が、配列番号224(本明細書のIL-15サイトカイン部分表に示される通り)のアミノ酸配列と比較して、位置D22、E46、E53に一つまたは複数のアミノ酸置換を有するアミノ酸配列を含む、請求項125に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-15サイトカインまたはその機能的断片が、配列番号224(本明細書のIL-15サイトカイン部分表に示される通り)のアミノ酸配列と比較して、位置D22、E46、E53、N71、N79、またはN112に一つまたは複数のアミノ酸置換を有するアミノ酸配列を含む、請求項126に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-15サイトカインまたはその機能的断片が、配列番号224(本明細書のIL-15サイトカイン部分表に示される通り)のアミノ酸配列と比較して、位置N71およびN79にアミノ酸置換を有するアミノ酸配列を含む、請求項125~127のいずれか一項に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-15サイトカインまたはその機能的断片が、配列番号224(本明細書のIL-15サイトカイン部分表に示される通り)のアミノ酸配列と比較して、位置N71およびN112にアミノ酸置換を有するアミノ酸配列を含む、請求項125~128のいずれか一項に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-15サイトカインまたはその機能的断片が、配列番号224(本明細書のIL-15サイトカイン部分表に示される通り)のアミノ酸配列と比較して、位置N79およびN112にアミノ酸置換を有するアミノ酸配列を含む、請求項125~129のいずれか一項に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-15サイトカインまたはその機能的断片が、配列番号224(本明細書のIL-15サイトカイン部分表に示される通り)のアミノ酸配列と比較して、位置N71、N79およびN112にアミノ酸置換を有するアミノ酸配列を含む、請求項125~130のいずれか一項に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-15サイトカインまたはその機能的断片が、配列番号225(本明細書のIL-15サイトカイン部分表に示される通り)のアミノ酸配列を含む、請求項125に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-15サイトカインまたはその機能的断片が、配列番号226(本明細書のIL-15サイトカイン部分表に示される通り)のアミノ酸配列を含む、請求項125に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-15サイトカインまたはその機能的断片が、配列番号227(本明細書のIL-15サイトカイン部分表に示される通り)のアミノ酸配列を含む、請求項125に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
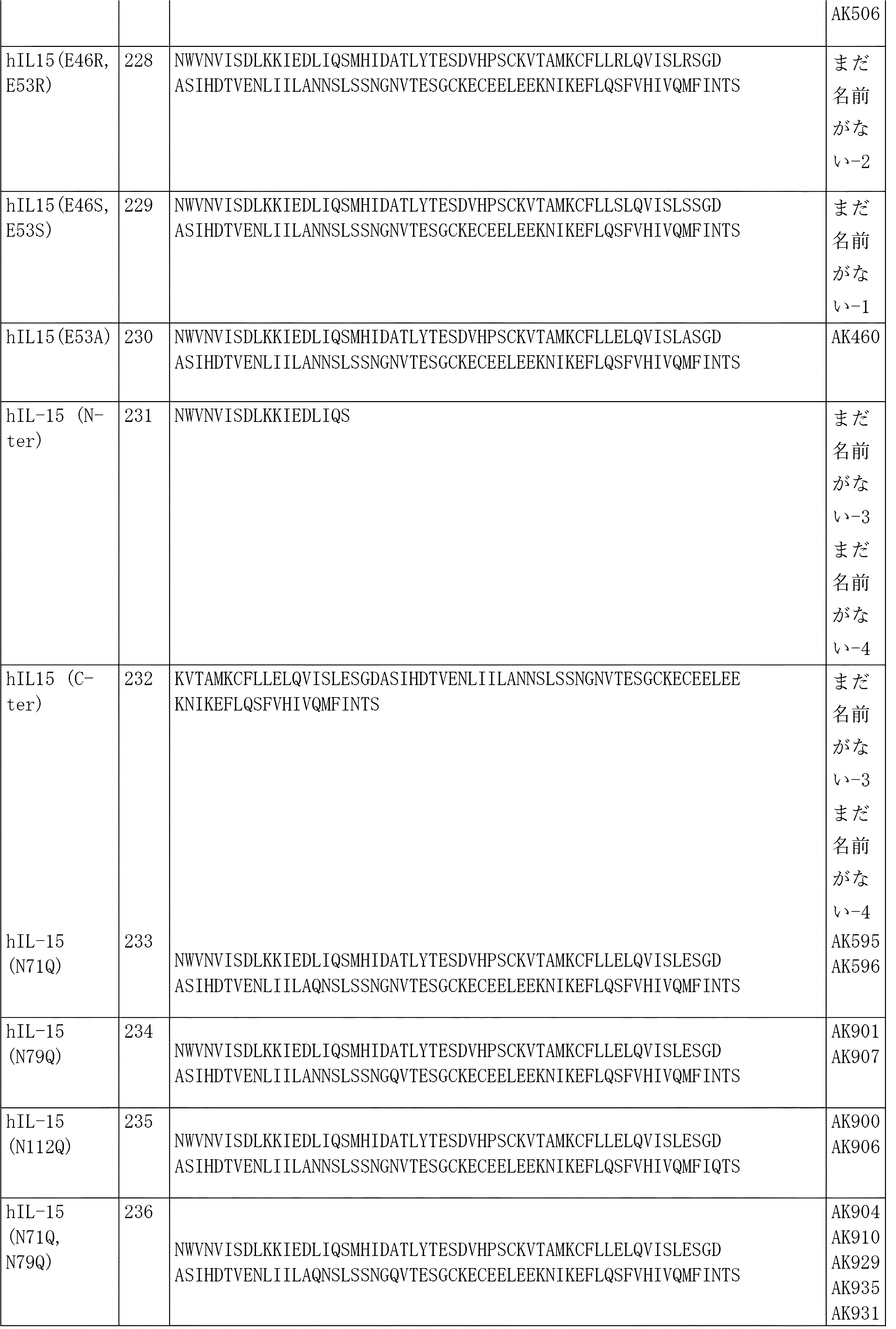
- 前記IL-15サイトカインまたはその機能的断片が、配列番号228(本明細書のIL-15サイトカイン部分表に示される通り)のアミノ酸配列を含む、請求項125に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-15サイトカインまたはその機能的断片が、配列番号229(本明細書のIL-15サイトカイン部分表に示される通り)のアミノ酸配列を含む、請求項125に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-15サイトカインまたはその機能的断片が、配列番号230(本明細書のIL-15サイトカイン部分表に示される通り)のアミノ酸配列を含む、請求項125に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-15サイトカインまたはその機能的断片が、配列番号233(本明細書のIL-15サイトカイン部分表に示される通り)のアミノ酸配列を含む、請求項125に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-15サイトカインまたはその機能的断片が、配列番号234(本明細書のIL-15サイトカイン部分表に示される通り)のアミノ酸配列を含む、請求項125に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-15サイトカインまたはその機能的断片が、配列番号235(本明細書のIL-15サイトカイン部分表に示される通り)のアミノ酸配列を含む、請求項125に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-15サイトカインまたはその機能的断片が、配列番号236(本明細書のIL-15サイトカイン部分表に示される通り)のアミノ酸配列を含む、請求項125に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-15サイトカインまたはその機能的断片が、配列番号237(本明細書のIL-15サイトカイン部分表に示される通り)のアミノ酸配列を含む、請求項125に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-15サイトカインまたはその機能的断片が、配列番号238(本明細書のIL-15サイトカイン部分表に示される通り)のアミノ酸配列を含む、請求項125に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-15サイトカインまたはその機能的断片が、配列番号239(本明細書のIL-15サイトカイン部分表に示される通り)のアミノ酸配列を含む、請求項125に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-15サイトカインまたはその機能的断片が、位置N71に追加の変異を含む、請求項125~131のいずれか一項に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-15サイトカインまたはその機能的断片が、位置S73に追加の変異を含む、請求項125~131または請求項145のいずれか一項に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記IL-15サイトカインまたはその機能的断片が、一つまたは複数のアミノ酸位置N72、N79、V80、T81、およびN112に追加の変異を含む、請求項125~131または請求項145または請求項146のいずれか一項に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記マスキング部分が、IL-15Rβまたはその断片もしくはバリアントを含む、請求項116~147のいずれか一項に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記マスキング部分が、配列番号240(本明細書のIL-15マスキング部分表に示される通り)のアミノ酸配列を含む、請求項148に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記マスキング部分が、位置C122にアミノ酸置換を有するIL-15Rβバリアントまたはその断片を含む、請求項148に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記マスキング部分が、アミノ酸置換C122Sを有するIL-15Rβバリアントまたはその断片を含む、請求項150に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記マスキング部分が、位置C168にアミノ酸置換を有するIL-15Rβバリアントまたはその断片を含む、請求項148または請求項150に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記マスキング部分が、アミノ酸置換C168Sを有するIL-15Rβバリアントまたはその断片を含む、請求項152に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 前記マスキング部分が、位置C122およびC168にアミノ酸置換を有するIL-15Rβバリアントまたはその断片を含む、請求項148に記載のサイトカインプロドラッグまたはマスクされたサイトカイン。
- 請求項1~30のいずれかに記載のポリペプチド薬物構築物、請求項31に記載のサイトカインプロドラッグ、または請求項32~154のいずれかに記載のマスクされたサイトカイン中の前記タンパク質分解的に切断可能なリンカーのタンパク質分解切断によって調製可能な活性治療部分を含むことが可能な、切断産物。
- 請求項1~30のいずれかに記載のポリペプチド薬物構築物をコードする核酸。
- 請求項31に記載のサイトカインプロドラッグ、または請求項32~154のいずれかに記載のマスクされたサイトカインをコードする核酸。
- 請求項155に記載の切断産物をコードする核酸。
- 請求項1~30のいずれかに記載のポリペプチド薬物構築物のポリペプチド鎖の一つをコードする核酸。
- 請求項31に記載のサイトカインプロドラッグのポリペプチド鎖の一つ、または請求項32~154のいずれかに記載のマスクされたサイトカインのポリペプチド鎖の一つをコードする核酸。
- 請求項155に記載の切断産物のポリペプチド鎖の一つをコードする核酸。
- 請求項156~161のいずれか一項に記載の核酸を含むベクター。
- 請求項156~161のいずれか一項に記載の核酸を含む宿主細胞。
- 前記宿主細胞が、HEK細胞またはCHO細胞である、請求項163に記載の宿主細胞。
- 請求項1~30のいずれかに記載のポリペプチド薬物構築物を含む、組成物。
- 請求項31に記載のサイトカインプロドラッグ、または請求項32~154のいずれかに記載のマスクされたサイトカインを含む、組成物。
- 請求項1~30のいずれかに記載のポリペプチド薬物構築物および薬学的に許容可能な担体を含む、医薬組成物。
- 請求項31に記載のサイトカインプロドラッグ、または請求項32~154のいずれかに記載のマスクされたサイトカイン、および薬学的に許容可能な担体を含む、医薬組成物。
- 前記医薬組成物が、単一単位剤形である、請求項167または請求項168に記載の医薬組成物。
- 前記医薬組成物が、静脈内投与用に製剤化され、単一単位剤形である、請求項169に記載の医薬組成物。
- 前記医薬組成物が、注射用に製剤化され、単一単位剤形である、請求項169に記載の医薬組成物。
- 前記医薬組成物が、液体であり、単一単位剤形である、請求項169に記載の医薬組成物。
- 請求項1~30のいずれかに記載のポリペプチド薬物構築物、または請求項31に記載のサイトカインプロドラッグ、または請求項32~154のいずれかに記載のマスクされたサイトカイン、または請求項165もしくは請求項166に記載の組成物、または請求項167~172に記載の医薬組成物を含む、キット。
- 前記マスクされたIL-12サイトカインを産生する条件下で、請求項82に記載の宿主細胞を培養することを含む、請求項32~154のいずれか一項に記載のマスクされたサイトカインを産生する方法。
- 請求項155に記載の切断産物を含む、組成物。
- 請求項155に記載の切断産物および薬学的に許容可能な担体を含む医薬組成物。
- 医療で使用するための、請求項1~30のいずれかに記載のポリペプチド薬物構築物。
- 医療で使用するための、請求項31に記載のサイトカインプロドラッグ。
- 医療で使用するための、請求項32~154のいずれかに記載のマスクされたサイトカイン。
- 医療で使用するための、請求項165または請求項166に記載の組成物。
- 医療で使用するための、請求項167~172に記載の医薬組成物。
- 医療で使用するための、請求項155に記載の切断産物。
- 対象において癌を治療または予防する方法であって、請求項1~30のいずれかに記載のポリペプチド薬物構築物の有効量を前記対象に投与することを含む、方法。
- 対象において癌を治療または予防する方法であって、請求項31に記載のサイトカインプロドラッグの有効量を前記対象に投与することを含む、方法。
- 対象において癌を治療または予防する方法であって、請求項32~154のいずれかに記載のマスクされたサイトカインの有効量を前記対象に投与することを含む、方法。
- 対象において癌を治療または予防する方法であって、請求項165または請求項166に記載の組成物の有効量を前記対象に投与することを含む、方法。
- 対象において癌を治療または予防する方法であって、請求項167~172に記載の医薬組成物の有効量を前記対象に投与することを含む、方法。
- 対象において癌を治療または予防する方法であって、請求項155に記載の切断産物の有効量を前記対象に投与することを含む、方法。
- 対象において癌を治療または予防する方法であって、請求項31に記載のサイトカインプロドラッグ、または請求項32~154のいずれかに記載のマスクされたサイトカインの有効量を前記対象に投与することを含み、それによって、前記サイトカインプロドラッグまたはマスクされたサイトカインが、インビボでタンパク質分解的に切断されて、請求項155に定義される切断産物を生成する、方法。
- 対象において癌を治療または予防する方法であって、その同族受容体に結合することができる切断産物をインビボで作製する工程を含み、前記切断産物は、請求項155に定義されるとおりである、方法。
- 前記癌が固形腫瘍である、請求項183~190のいずれか一項に記載の方法。
- 癌の治療または予防に使用するための、請求項1~72のいずれか一項に記載のマスクされたIL-12サイトカイン。
- 癌を治療または予防する方法で使用するための、請求項1~72のいずれか一項に記載のマスクされたIL-12サイトカインであって、前記方法は、有効量の前記マスクされたIL-12サイトカインを前記対象に投与することを含み、それによって、前記マスクされたサイトカインが、インビボでタンパク質分解的に切断され、請求項73~79のいずれか一項に記載の切断産物を生成する、マスクされたIL-12サイトカイン。
- 前記癌が固形腫瘍である、請求項103に記載の使用のためのマスクされたIL-12サイトカイン。
- 癌の治療または予防に使用するための、請求項1~30のいずれかに記載のポリペプチド薬物構築物。
- 癌の治療または予防に使用するための、請求項31に記載のサイトカインプロドラッグ。
- 癌の治療または予防に使用するための、請求項32~154のいずれかに記載のマスクされたサイトカイン。
- 癌の治療または予防に使用するための、請求項165または請求項166に記載の組成物。
- 癌の治療または予防に使用するための、請求項167~172に記載の医薬組成物。
- 癌の治療または予防に使用するための、請求項155に記載の切断産物。
- 前記癌が固形腫瘍である、請求項195に記載のポリペプチド薬物構築物、請求項196に記載の使用のためのサイトカインプロドラッグ、請求項197に記載の使用のためのマスクされたサイトカイン、請求項198に記載の使用のための組成物、請求項199に記載の使用のための医薬組成物、または請求項200に記載の使用のための切断産物。
- 癌を治療または予防する方法で使用するための、請求項155に記載の切断産物であって、前記方法は、請求項1~30のいずれかに記載のポリペプチド薬物構築物、請求項31に記載のサイトカインプロドラッグ、または請求項32~154のいずれかに記載のマスクされたサイトカインを患者に投与し、それによって、インビボで前記タンパク質分解的に切断可能なペプチドリンカーのタンパク質切断によって前記切断産物を産生する工程を含む、切断産物。
- 対象において癌を治療または予防する方法で使用するための請求項155に記載の切断産物であって、前記方法が、前記対象に投与された請求項1~30のいずれかに記載のポリペプチド薬物構築物、請求項31に記載のサイトカインプロドラッグ、または請求項32~154のいずれかに記載のマスクされたサイトカインのインビボでのタンパク質切断によって前記切断産物を産生する工程を含む、切断産物。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US202063118585P | 2020-11-25 | 2020-11-25 | |
| US63/118,585 | 2020-11-25 | ||
| US202163253090P | 2021-10-06 | 2021-10-06 | |
| US63/253,090 | 2021-10-06 | ||
| PCT/US2021/072603 WO2022115865A2 (en) | 2020-11-25 | 2021-11-24 | Tumor-specific cleavable linkers |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2023553323A true JP2023553323A (ja) | 2023-12-21 |
| JPWO2022115865A5 JPWO2022115865A5 (ja) | 2024-11-26 |
Family
ID=81756324
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2023531600A Pending JP2023553323A (ja) | 2020-11-25 | 2021-11-24 | 腫瘍特異的に切断可能なリンカー |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US12280120B2 (ja) |
| EP (1) | EP4251187A4 (ja) |
| JP (1) | JP2023553323A (ja) |
| KR (1) | KR20230113581A (ja) |
| CA (1) | CA3196844A1 (ja) |
| TW (1) | TW202235431A (ja) |
| WO (1) | WO2022115865A2 (ja) |
Families Citing this family (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3856764A4 (en) | 2018-09-27 | 2022-11-02 | Xilio Development, Inc. | MASKED CYTOKINE POLYPEPTIDES |
| JP2023553323A (ja) | 2020-11-25 | 2023-12-21 | エクシリオ デベロップメント, インコーポレイテッド | 腫瘍特異的に切断可能なリンカー |
| US20240116997A1 (en) | 2022-02-23 | 2024-04-11 | Bright Peak Therapeutics Ag | Activatable il-18 polypeptides |
| KR20240152853A (ko) * | 2022-02-28 | 2024-10-22 | 실리오 디벨럽먼트, 인크. | 표적화된 사이토카인 및 이의 사용 방법 |
| CA3259097A1 (en) * | 2022-07-15 | 2024-01-18 | Xilio Development, Inc. | Modified Clivable FC Domain Used as Carriers and its Methods of Use |
| WO2024150175A1 (en) | 2023-01-11 | 2024-07-18 | Bright Peak Therapeutics Ag | Conditionally activated proteins and methods of use |
| US20240417436A1 (en) | 2023-01-11 | 2024-12-19 | Bright Peak Therapeutics Ag | Conditionally activated immunocytokines and methods of use |
| CN120936384A (zh) * | 2023-04-12 | 2025-11-11 | 西托姆克斯治疗公司 | 掩蔽多肽、可活化细胞因子构建体以及相关组合物和方法 |
| CN120958015A (zh) * | 2023-04-12 | 2025-11-14 | 西托姆克斯治疗公司 | 掩蔽多肽、可活化细胞因子构建体以及相关组合物和方法 |
| US20250197467A1 (en) | 2023-08-23 | 2025-06-19 | Bright Peak Therapeutics Ag | Activatable il-18 immunocytokines and uses thereof |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2017523176A (ja) * | 2014-07-25 | 2017-08-17 | シトムクス セラピューティクス,インコーポレイティド | 抗−cd3抗体、活性化可能抗−cd3抗体、多重特異的抗−cd3抗体、多重特異的活性化可能抗−cd3抗体、及びそれらの使用方法 |
| JP2018504925A (ja) * | 2015-01-20 | 2018-02-22 | シトムクス セラピューティクス,インコーポレイティド | マトリックスメタロプロテアーゼ切断可能及びセリンプロテアーゼ切断可能な基質並びにそれらの使用方法 |
| WO2020069398A1 (en) * | 2018-09-27 | 2020-04-02 | Akrevia Therapeutics Inc. | Masked cytokine polypeptides |
| WO2020139920A2 (en) * | 2018-12-26 | 2020-07-02 | City Of Hope | Activatable masked anti-ctla4 binding proteins |
Family Cites Families (182)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| USRE30985E (en) | 1978-01-01 | 1982-06-29 | Serum-free cell culture media | |
| US4419446A (en) | 1980-12-31 | 1983-12-06 | The United States Of America As Represented By The Department Of Health And Human Services | Recombinant DNA process utilizing a papilloma virus DNA as a vector |
| US4601978A (en) | 1982-11-24 | 1986-07-22 | The Regents Of The University Of California | Mammalian metallothionein promoter system |
| US4560655A (en) | 1982-12-16 | 1985-12-24 | Immunex Corporation | Serum-free cell culture medium and process for making same |
| US4657866A (en) | 1982-12-21 | 1987-04-14 | Sudhir Kumar | Serum-free, synthetic, completely chemically defined tissue culture media |
| US4816567A (en) | 1983-04-08 | 1989-03-28 | Genentech, Inc. | Recombinant immunoglobin preparations |
| US4767704A (en) | 1983-10-07 | 1988-08-30 | Columbia University In The City Of New York | Protein-free culture medium |
| US4965199A (en) | 1984-04-20 | 1990-10-23 | Genentech, Inc. | Preparation of functional human factor VIII in mammalian cells using methotrexate based selection |
| GB8516415D0 (en) | 1985-06-28 | 1985-07-31 | Celltech Ltd | Culture of animal cells |
| US4676980A (en) | 1985-09-23 | 1987-06-30 | The United States Of America As Represented By The Secretary Of The Department Of Health And Human Services | Target specific cross-linked heteroantibodies |
| GB8601597D0 (en) | 1986-01-23 | 1986-02-26 | Wilson R H | Nucleotide sequences |
| US4927762A (en) | 1986-04-01 | 1990-05-22 | Cell Enterprises, Inc. | Cell culture medium with antioxidant |
| JPS63203626A (ja) | 1987-02-19 | 1988-08-23 | Ajinomoto Co Inc | 免疫抑制剤 |
| WO1988007089A1 (en) | 1987-03-18 | 1988-09-22 | Medical Research Council | Altered antibodies |
| US5770701A (en) | 1987-10-30 | 1998-06-23 | American Cyanamid Company | Process for preparing targeted forms of methyltrithio antitumor agents |
| US5606040A (en) | 1987-10-30 | 1997-02-25 | American Cyanamid Company | Antitumor and antibacterial substituted disulfide derivatives prepared from compounds possessing a methyl-trithio group |
| AU632065B2 (en) | 1988-09-23 | 1992-12-17 | Novartis Vaccines And Diagnostics, Inc. | Cell culture medium for enhanced cell growth, culture longevity and product expression |
| WO1990005144A1 (en) | 1988-11-11 | 1990-05-17 | Medical Research Council | Single domain ligands, receptors comprising said ligands, methods for their production, and use of said ligands and receptors |
| SE509359C2 (sv) | 1989-08-01 | 1999-01-18 | Cemu Bioteknik Ab | Användning av stabiliserade protein- eller peptidkonjugat för framställning av ett läkemedel |
| US5208020A (en) | 1989-10-25 | 1993-05-04 | Immunogen Inc. | Cytotoxic agents comprising maytansinoids and their therapeutic use |
| CA2026147C (en) | 1989-10-25 | 2006-02-07 | Ravi J. Chari | Cytotoxic agents comprising maytansinoids and their therapeutic use |
| US6673986B1 (en) | 1990-01-12 | 2004-01-06 | Abgenix, Inc. | Generation of xenogeneic antibodies |
| DK0463151T3 (da) | 1990-01-12 | 1996-07-01 | Cell Genesys Inc | Frembringelse af xenogene antistoffer |
| US6150584A (en) | 1990-01-12 | 2000-11-21 | Abgenix, Inc. | Human antibodies derived from immunized xenomice |
| US6075181A (en) | 1990-01-12 | 2000-06-13 | Abgenix, Inc. | Human antibodies derived from immunized xenomice |
| US5891693A (en) | 1990-01-25 | 1999-04-06 | Alusuisse Holdings A.G. | Recombinant DNA methods vectors and host cells |
| US5122469A (en) | 1990-10-03 | 1992-06-16 | Genentech, Inc. | Method for culturing Chinese hamster ovary cells to improve production of recombinant proteins |
| US5650150A (en) | 1990-11-09 | 1997-07-22 | Gillies; Stephen D. | Recombinant antibody cytokine fusion proteins |
| US5508192A (en) | 1990-11-09 | 1996-04-16 | Board Of Regents, The University Of Texas System | Bacterial host strains for producing proteolytically sensitive polypeptides |
| JPH09506761A (ja) | 1990-11-09 | 1997-07-08 | ステファン ディー.ギリーズ | サイトカインの免疫複合体 |
| US5264365A (en) | 1990-11-09 | 1993-11-23 | Board Of Regents, The University Of Texas System | Protease-deficient bacterial strains for production of proteolytically sensitive polypeptides |
| US5571894A (en) | 1991-02-05 | 1996-11-05 | Ciba-Geigy Corporation | Recombinant antibodies specific for a growth factor receptor |
| WO1993006217A1 (en) | 1991-09-19 | 1993-04-01 | Genentech, Inc. | EXPRESSION IN E. COLI OF ANTIBODY FRAGMENTS HAVING AT LEAST A CYSTEINE PRESENT AS A FREE THIOL, USE FOR THE PRODUCTION OF BIFUNCTIONAL F(ab')2 ANTIBODIES |
| FI941572L (fi) | 1991-10-07 | 1994-05-27 | Oncologix Inc | Anti-erbB-2-monoklonaalisten vasta-aineiden yhdistelmä ja käyttömenetelmä |
| WO1993008829A1 (en) | 1991-11-04 | 1993-05-13 | The Regents Of The University Of California | Compositions that mediate killing of hiv-infected cells |
| ATE503496T1 (de) | 1992-02-06 | 2011-04-15 | Novartis Vaccines & Diagnostic | Biosynthetisches bindeprotein für tumormarker |
| AU4116793A (en) | 1992-04-24 | 1993-11-29 | Board Of Regents, The University Of Texas System | Recombinant production of immunoglobulin-like domains in prokaryotic cells |
| ATE139900T1 (de) | 1992-11-13 | 1996-07-15 | Idec Pharma Corp | Therapeutische verwendung von chimerischen und markierten antikörper gegen menschlichen b lymphozyt beschränkter differenzierung antigen für die behandlung von b-zell-lymphoma |
| US5635483A (en) | 1992-12-03 | 1997-06-03 | Arizona Board Of Regents Acting On Behalf Of Arizona State University | Tumor inhibiting tetrapeptide bearing modified phenethyl amides |
| US5780588A (en) | 1993-01-26 | 1998-07-14 | Arizona Board Of Regents | Elucidation and synthesis of selected pentapeptides |
| CA2163345A1 (en) | 1993-06-16 | 1994-12-22 | Susan Adrienne Morgan | Antibodies |
| US5773001A (en) | 1994-06-03 | 1998-06-30 | American Cyanamid Company | Conjugates of methyltrithio antitumor agents and intermediates for their synthesis |
| US5639635A (en) | 1994-11-03 | 1997-06-17 | Genentech, Inc. | Process for bacterial production of polypeptides |
| US5731168A (en) | 1995-03-01 | 1998-03-24 | Genentech, Inc. | Method for making heteromultimeric polypeptides |
| US5641870A (en) | 1995-04-20 | 1997-06-24 | Genentech, Inc. | Low pH hydrophobic interaction chromatography for antibody purification |
| US5739277A (en) | 1995-04-14 | 1998-04-14 | Genentech Inc. | Altered polypeptides with increased half-life |
| US5869046A (en) | 1995-04-14 | 1999-02-09 | Genentech, Inc. | Altered polypeptides with increased half-life |
| US5712374A (en) | 1995-06-07 | 1998-01-27 | American Cyanamid Company | Method for the preparation of substantiallly monomeric calicheamicin derivative/carrier conjugates |
| US5714586A (en) | 1995-06-07 | 1998-02-03 | American Cyanamid Company | Methods for the preparation of monomeric calicheamicin derivative/carrier conjugates |
| GB9603256D0 (en) | 1996-02-16 | 1996-04-17 | Wellcome Found | Antibodies |
| US6027888A (en) | 1996-04-05 | 2000-02-22 | Board Of Regents, The University Of Texas System | Methods for producing soluble, biologically-active disulfide-bond containing eukaryotic proteins in bacterial cells |
| US5834597A (en) | 1996-05-20 | 1998-11-10 | Protein Design Labs, Inc. | Mutated nonactivating IgG2 domains and anti CD3 antibodies incorporating the same |
| US6277375B1 (en) | 1997-03-03 | 2001-08-21 | Board Of Regents, The University Of Texas System | Immunoglobulin-like domains with increased half-lives |
| US6083715A (en) | 1997-06-09 | 2000-07-04 | Board Of Regents, The University Of Texas System | Methods for producing heterologous disulfide bond-containing polypeptides in bacterial cells |
| ES2244066T3 (es) | 1997-06-24 | 2005-12-01 | Genentech, Inc. | Procedimiento y composiciones de glicoproteinas galactosiladas. |
| WO1999022764A1 (en) | 1997-10-31 | 1999-05-14 | Genentech, Inc. | Methods and compositions comprising glycoprotein glycoforms |
| DE19751857A1 (de) | 1997-11-22 | 1999-05-27 | Kronos Titan Gmbh | Phosphonatosiloxanbehandelte anorganische Partikel |
| DK1037927T3 (da) | 1997-12-08 | 2004-09-06 | Emd Lexigen Res Ct Corp | Heterodimere fusionsproteiner, der er nyttige til målrettet immunterapi og generel immunstimulering |
| ATE375365T1 (de) | 1998-04-02 | 2007-10-15 | Genentech Inc | Antikörper varianten und fragmente davon |
| US6194551B1 (en) | 1998-04-02 | 2001-02-27 | Genentech, Inc. | Polypeptide variants |
| PT1071700E (pt) | 1998-04-20 | 2010-04-23 | Glycart Biotechnology Ag | Modificação por glicosilação de anticorpos para melhorar a citotoxicidade celular dependente de anticorpos |
| EP1141024B1 (en) | 1999-01-15 | 2018-08-08 | Genentech, Inc. | POLYPEPTIDE COMPRISING A VARIANT HUMAN IgG1 Fc REGION |
| WO2001077137A1 (en) | 2000-04-12 | 2001-10-18 | Human Genome Sciences, Inc. | Albumin fusion proteins |
| ES2601882T5 (es) | 1999-04-09 | 2021-06-07 | Kyowa Kirin Co Ltd | Procedimiento para controlar la actividad de una molécula inmunofuncional |
| SK782002A3 (en) | 1999-07-21 | 2003-08-05 | Lexigen Pharm Corp | FC fusion proteins for enhancing the immunogenicity of protein and peptide antigens |
| CA2388245C (en) | 1999-10-19 | 2012-01-10 | Tatsuya Ogawa | The use of serum-free adapted rat cells for producing heterologous polypeptides |
| DK1242438T3 (da) | 1999-12-29 | 2007-02-12 | Immunogen Inc | Cytotoksiske midler omfattende modificerede doxorubiciner og daunorubiciner og deres terapeutiske anvendelse |
| DE10045592A1 (de) | 2000-09-15 | 2002-03-28 | Klaus Pfizenmaier | Ein Antikörper-TNF-TNF Inhibitor Fusionsprotein (TNF-Selektokin) als zielspezifisches Prozytokin zur Tumortherapie |
| US7064191B2 (en) | 2000-10-06 | 2006-06-20 | Kyowa Hakko Kogyo Co., Ltd. | Process for purifying antibody |
| US6946292B2 (en) | 2000-10-06 | 2005-09-20 | Kyowa Hakko Kogyo Co., Ltd. | Cells producing antibody compositions with increased antibody dependent cytotoxic activity |
| EP1916303B1 (en) | 2000-11-30 | 2013-02-27 | Medarex, Inc. | Nucleic acids encoding rearranged human immunoglobulin sequences from transgenic transchromosomal mice |
| EP1355919B1 (en) | 2000-12-12 | 2010-11-24 | MedImmune, LLC | Molecules with extended half-lives, compositions and uses thereof |
| US6942853B2 (en) | 2001-01-09 | 2005-09-13 | Queen Mary And Westfield College | Latent fusion protein |
| WO2002076489A1 (en) | 2001-03-09 | 2002-10-03 | Dyax Corp. | Serum albumin binding moieties |
| EP1423510A4 (en) | 2001-08-03 | 2005-06-01 | Glycart Biotechnology Ag | ANTIBODY GLYCOSYLATION VARIANTS WITH INCREASED ANTIBODY-DEPENDENT CELLULAR CYTOTOXICITY |
| HUP0600342A3 (en) | 2001-10-25 | 2011-03-28 | Genentech Inc | Glycoprotein compositions |
| CA2484556A1 (en) | 2001-12-21 | 2003-07-24 | Human Genome Sciences, Inc. | Albumin fusion proteins |
| US20040093621A1 (en) | 2001-12-25 | 2004-05-13 | Kyowa Hakko Kogyo Co., Ltd | Antibody composition which specifically binds to CD20 |
| CN102911987B (zh) | 2002-04-09 | 2015-09-30 | 协和发酵麒麟株式会社 | 基因组被修饰的细胞 |
| CA2481837A1 (en) | 2002-04-09 | 2003-10-16 | Kyowa Hakko Kogyo Co., Ltd. | Production process for antibody composition |
| CA2481656A1 (en) | 2002-04-09 | 2003-10-16 | Kyowa Hakko Kogyo Co., Ltd. | Cells in which activity of the protein involved in transportation of gdp-fucose is reduced or lost |
| US20050031613A1 (en) | 2002-04-09 | 2005-02-10 | Kazuyasu Nakamura | Therapeutic agent for patients having human FcgammaRIIIa |
| WO2003085119A1 (en) | 2002-04-09 | 2003-10-16 | Kyowa Hakko Kogyo Co., Ltd. | METHOD OF ENHANCING ACTIVITY OF ANTIBODY COMPOSITION OF BINDING TO FcϜ RECEPTOR IIIa |
| WO2003084569A1 (en) | 2002-04-09 | 2003-10-16 | Kyowa Hakko Kogyo Co., Ltd. | Drug containing antibody composition |
| CN1703423A (zh) | 2002-10-14 | 2005-11-30 | 豪夫迈-罗氏公司 | Il-15拮抗剂 |
| US7361740B2 (en) | 2002-10-15 | 2008-04-22 | Pdl Biopharma, Inc. | Alteration of FcRn binding affinities or serum half-lives of antibodies by mutagenesis |
| JP2006520584A (ja) | 2002-11-08 | 2006-09-14 | アブリンクス エン.ヴェー. | 安定化単一ドメイン抗体 |
| DK2289936T3 (en) | 2002-12-16 | 2017-07-31 | Genentech Inc | IMMUNGLOBULIN VARIATIONS AND APPLICATIONS THEREOF |
| WO2005035586A1 (ja) | 2003-10-08 | 2005-04-21 | Kyowa Hakko Kogyo Co., Ltd. | 融合蛋白質組成物 |
| WO2005035778A1 (ja) | 2003-10-09 | 2005-04-21 | Kyowa Hakko Kogyo Co., Ltd. | α1,6-フコシルトランスフェラーゼの機能を抑制するRNAを用いた抗体組成物の製造法 |
| DK2380910T3 (en) | 2003-11-05 | 2015-10-19 | Roche Glycart Ag | Antigen binding molecules with increased Fc receptor binding affinity and effector function |
| PT2489364E (pt) | 2003-11-06 | 2015-04-16 | Seattle Genetics Inc | Compostos de monometilvalina conjugados com anticorpos |
| WO2005053742A1 (ja) | 2003-12-04 | 2005-06-16 | Kyowa Hakko Kogyo Co., Ltd. | 抗体組成物を含有する医薬 |
| CA2554089C (en) | 2004-02-09 | 2013-10-22 | Human Genome Sciences, Inc. | Albumin fusion proteins |
| WO2006106905A1 (ja) | 2005-03-31 | 2006-10-12 | Chugai Seiyaku Kabushiki Kaisha | 会合制御によるポリペプチド製造方法 |
| MX2007015107A (es) | 2005-06-03 | 2008-02-15 | Genentech Inc | Metodo para producir anticuerpos con funcion mejorada. |
| EP1777294A1 (en) | 2005-10-20 | 2007-04-25 | Institut National De La Sante Et De La Recherche Medicale (Inserm) | IL-15Ralpha sushi domain as a selective and potent enhancer of IL-15 action through IL-15Rbeta/gamma, and hyperagonist (IL15Ralpha sushi -IL15) fusion proteins |
| US20070269422A1 (en) | 2006-05-17 | 2007-11-22 | Ablynx N.V. | Serum albumin binding proteins with long half-lives |
| EP2171052B1 (en) | 2007-07-12 | 2014-08-27 | Sangamo BioSciences, Inc. | Methods and compositions for inactivating alpha 1,6 fucosyltransferase (fut 8) gene expression |
| CN102481341B (zh) | 2009-02-23 | 2017-05-17 | 希托马克斯医疗有限公司 | 蛋白原及其使用方法 |
| US8871191B2 (en) | 2009-08-14 | 2014-10-28 | The United States Of America As Represented By The Secretary Of The Department Of Health And Human Services | Use of IL-15 preparations to treat lymphopenia |
| EP2536430B1 (en) | 2010-02-17 | 2016-12-14 | CSL Limited | Compositions and methods for targeting type 1 interferon producing cells |
| US8734774B2 (en) | 2010-04-02 | 2014-05-27 | University Of Rochester | Protease activated cytokines |
| US10233228B2 (en) | 2010-04-09 | 2019-03-19 | Albumedix Ltd | Albumin derivatives and variants |
| EP2619229B1 (en) | 2010-09-21 | 2016-04-06 | Altor BioScience Corporation | Multimeric il-15 soluble fusion molecules and methods of making and using same |
| WO2012059486A1 (en) | 2010-11-01 | 2012-05-10 | Novozymes Biopharma Dk A/S | Albumin variants |
| CU23923B1 (es) | 2010-11-12 | 2013-07-31 | Ct De Inmunología Molecular | Polipéptidos derivados de la il-2 con actividad agonista |
| RS55906B1 (sr) | 2010-12-23 | 2017-09-29 | Janssen Biotech Inc | Mutanti fc antitela koji su otporni na aktivnu proteazu |
| TWI666027B (zh) | 2011-02-10 | 2019-07-21 | 羅齊克雷雅公司 | 突變介白素-2多肽 |
| GB201203442D0 (en) | 2012-02-28 | 2012-04-11 | Univ Birmingham | Immunotherapeutic molecules and uses |
| MX2015001678A (es) | 2012-08-09 | 2015-08-14 | Roche Glycart Ag | Anticuerpos asgpr y sus usos. |
| US9388475B2 (en) | 2012-08-23 | 2016-07-12 | Lee Tech Llc | Method of and system for producing oil and valuable byproducts from grains in dry milling systems with a back-end dewater milling unit |
| US9605084B2 (en) | 2013-03-15 | 2017-03-28 | Xencor, Inc. | Heterodimeric proteins |
| EP2968587A2 (en) | 2013-03-13 | 2016-01-20 | Bristol-Myers Squibb Company | Fibronectin based scaffold domains linked to serum albumin or a moiety binding thereto |
| US20140302037A1 (en) | 2013-03-15 | 2014-10-09 | Amgen Inc. | BISPECIFIC-Fc MOLECULES |
| US9926245B2 (en) | 2013-09-30 | 2018-03-27 | Pioneer Energy | Fuels and chemicals from lower alkanes |
| AU2014377106B2 (en) | 2014-01-08 | 2019-10-03 | Jiangsu Hengrui Medicine Co., Ltd. | IL-15 heterodimeric protein and uses thereof |
| JP2017536098A (ja) | 2014-10-14 | 2017-12-07 | アルモ・バイオサイエンシーズ・インコーポレイテッド | インターロイキン−15組成物及びその使用 |
| CN104403004B (zh) | 2014-11-24 | 2017-10-13 | 苏州丁孚靶点生物技术有限公司 | 抗体‑干扰素异二聚体的制备和用途 |
| EP3064507A1 (en) | 2015-03-06 | 2016-09-07 | Deutsches Krebsforschungszentrum Stiftung des öffentlichen Rechts | Fusion proteins comprising a binding protein and an interleukin-15 polypeptide having a reduced affinity for IL15ra and therapeutic uses thereof |
| US20180171321A1 (en) | 2015-03-27 | 2018-06-21 | The University Of Queensland | Platform for a non-natural amino acid incorporation into proteins |
| US20160362469A1 (en) | 2015-06-12 | 2016-12-15 | Tianxin Wang | Methods for protein modification in pharmaceutical applications |
| US20170204154A1 (en) | 2016-01-20 | 2017-07-20 | Delinia, Inc. | Molecules that selectively activate regulatory t cells for the treatment of autoimmune diseases |
| WO2017165464A1 (en) | 2016-03-21 | 2017-09-28 | Elstar Therapeutics, Inc. | Multispecific and multifunctional molecules and uses thereof |
| WO2017198631A1 (en) | 2016-05-16 | 2017-11-23 | Istituto Nazionale Di Genetica Molecolare - Ingm | Markers selectively deregulated in tumor-infiltrating regulatory t cells |
| US9567399B1 (en) | 2016-06-20 | 2017-02-14 | Kymab Limited | Antibodies and immunocytokines |
| JP7142630B2 (ja) | 2016-10-14 | 2022-09-27 | ゼンコア インコーポレイテッド | IL15/IL15Rαヘテロ二量体FC-融合タンパク質 |
| NZ756674A (en) | 2017-02-16 | 2023-06-30 | Sonnet Biotherapeutics Inc | Albumin binding domain fusion proteins |
| WO2018184964A1 (en) | 2017-04-03 | 2018-10-11 | F. Hoffmann-La Roche Ag | Immunoconjugates of an anti-pd-1 antibody with a mutant il-2 or with il-15 |
| WO2018184965A1 (en) | 2017-04-03 | 2018-10-11 | F. Hoffmann-La Roche Ag | Immunoconjugates of il-2 with an anti-pd-1 and tim-3 bispecific antibody |
| JP7336457B2 (ja) | 2017-12-26 | 2023-08-31 | ナンジン、ジェンスクリプト、バイオテック、カンパニー、リミテッド | 抗体Fc領域を主鎖として用いた融合タンパク質二量体及びその使用 |
| CN108218993B (zh) | 2018-01-05 | 2020-11-17 | 阿思科力(苏州)生物科技有限公司 | 一种以robo1为靶点的双特异性抗体及其制备和应用 |
| TW201938196A (zh) | 2018-01-18 | 2019-10-01 | 美商南特生物科學股份有限公司 | 融合蛋白擴展 |
| CA3091857A1 (en) | 2018-02-26 | 2019-08-29 | Synthorx, Inc. | Il-15 conjugates and uses thereof |
| KR20200128116A (ko) | 2018-02-28 | 2020-11-11 | 화이자 인코포레이티드 | Il-15 변이체 및 이의 용도 |
| CA3115461A1 (en) | 2018-03-09 | 2019-09-12 | AskGene Pharma, Inc. | Novel cytokine prodrugs |
| AU2019243580A1 (en) | 2018-03-28 | 2020-11-12 | Orionis Biosciences BV | Bi-functional proteins and construction thereof |
| TWI853807B (zh) | 2018-03-28 | 2024-09-01 | 美商必治妥美雅史谷比公司 | 介白素-2/介白素-2受體阿法融合蛋白及其使用方法 |
| CU24554B1 (es) | 2018-05-07 | 2021-11-04 | Ct Inmunologia Molecular | Proteínas de fusión compuestas por una muteína de interleucina 2 e interferón tipo 1 |
| CN113840832A (zh) | 2018-05-14 | 2021-12-24 | 狼人治疗公司 | 可活化白介素-2多肽及其使用方法 |
| WO2019222294A1 (en) | 2018-05-14 | 2019-11-21 | Werewolf Therapeutics, Inc. | Activatable cytokine polypeptides and methods of use thereof |
| WO2019235426A1 (ja) | 2018-06-04 | 2019-12-12 | 中外製薬株式会社 | 細胞質内での半減期が変化した抗原結合分子 |
| JP7477885B2 (ja) | 2018-06-22 | 2024-05-02 | キュージーン インコーポレイテッド | サイトカインをベースとした生理活性化薬剤およびその使用方法 |
| CA3102821A1 (en) | 2018-06-22 | 2019-12-26 | Cugene Inc. | Novel interleukin-15 (1l-15) fusion proteins and uses thereof |
| CN112534052B (zh) | 2018-07-25 | 2024-09-20 | 奥美药业有限公司 | 全新il-21前药及使用方法 |
| CN112867503A (zh) | 2018-08-24 | 2021-05-28 | 希望之城 | 掩蔽的细胞因子缀合物 |
| CA3108949A1 (en) | 2018-08-30 | 2020-03-05 | HCW Biologics, Inc. | Multi-chain chimeric polypeptides and uses thereof |
| EP3856229A1 (en) | 2018-09-28 | 2021-08-04 | Pierre Fabre Medicament | New immunocytokines for the treatment of cancer |
| AU2019355971B2 (en) | 2018-10-03 | 2025-05-08 | Xencor, Inc. | IL-12 heterodimeric Fc-fusion proteins |
| EP3870598A1 (en) | 2018-10-23 | 2021-09-01 | Dragonfly Therapeutics, Inc. | Heterodimeric fc-fused proteins |
| US12378295B2 (en) | 2018-10-29 | 2025-08-05 | 1Globe Biomedical Co., Ltd. | Rationally designed protein compositions |
| CA3121813A1 (en) | 2018-12-14 | 2020-06-18 | Proviva Therapeutics (Hong Kong) Limited | Il-15 compositions and methods of use thereof |
| WO2020127369A1 (en) | 2018-12-21 | 2020-06-25 | Ose Immunotherapeutics | Bifunctional molecule directed against human pd-1 |
| MX2021008147A (es) | 2019-01-07 | 2021-08-11 | Inhibrx Inc | Polipeptidos que comprenden polipeptidos con il-2 modificada y usos de los mismos. |
| SG11202112541RA (en) | 2019-05-14 | 2021-12-30 | Werewolf Therapeutics Inc | Separation moieties and methods and use thereof |
| US11845801B2 (en) | 2019-06-12 | 2023-12-19 | AskGene Pharma, Inc. | IL-15 prodrugs and methods of use thereof |
| US20220235133A1 (en) | 2019-06-24 | 2022-07-28 | Nanjing GenScript Biotech Co., Ltd. | Monoclonal antibody-cytokine fusion protein dimer and application thereof |
| WO2021001289A1 (en) | 2019-07-02 | 2021-01-07 | F. Hoffmann-La Roche Ag | Immunoconjugates comprising a mutant interleukin-2 and an anti-cd8 antibody |
| EP4004026A4 (en) | 2019-07-25 | 2023-11-15 | Trutino Biosciences Inc. | IL-2 CYTOKINE PRODRUGS WITH A CLAVEABLE LINKER |
| JP7682150B2 (ja) | 2019-07-25 | 2025-05-23 | ザ・ユニバーシティ・オブ・シカゴ | プロテアーゼ活性化治療剤を含む組成物および方法 |
| WO2021030483A1 (en) | 2019-08-12 | 2021-02-18 | AskGene Pharma, Inc. | Il-2 fusion proteins that preferentially bind il-2ralpha |
| AU2020329290A1 (en) | 2019-08-13 | 2022-03-24 | Elpis Biopharmaceuticals | Engineered interleukin-2 receptor beta agonists |
| JP2022545439A (ja) | 2019-08-21 | 2022-10-27 | アスクジーン・ファーマ・インコーポレイテッド | 新規il-21プロドラッグおよびその使用方法 |
| WO2021041886A1 (en) | 2019-08-29 | 2021-03-04 | Nantbio, Inc. | Modified n-810 and methods therefor |
| RU2753282C2 (ru) | 2019-09-19 | 2021-08-12 | Закрытое Акционерное Общество "Биокад" | ИММУНОЦИТОКИН, ВКЛЮЧАЮЩИЙ ГЕТЕРОДИМЕРНЫЙ БЕЛКОВЫЙ КОМПЛЕКС НА ОСНОВЕ IL-15/IL-15Rα, И ЕГО ПРИМЕНЕНИЕ |
| EP4034551A1 (en) | 2019-09-28 | 2022-08-03 | AskGene Pharma, Inc. | Cytokine prodrugs and dual-prodrugs |
| WO2021092719A1 (zh) | 2019-11-11 | 2021-05-20 | 王盛典 | 一种靶向抗原特异性t细胞诱导其向记忆干性细胞分化的融合蛋白 |
| EP4072588A4 (en) | 2019-12-13 | 2024-02-14 | Cugene Inc. | NOVEL INTERLEUKIN 15 (IL-15) FUSION PROTEINS AND USES THEREOF |
| EP4072593A4 (en) | 2019-12-13 | 2024-01-03 | Cugene Inc. | BIOACTIVABLE CYTOKINE DRUGS AND ASSOCIATED METHODS OF USES |
| US12091440B2 (en) | 2019-12-20 | 2024-09-17 | Regeneron Pharmaceuticals, Inc. | IL2 and peptide-MHC complex fusion proteins and methods of use thereof |
| CA3165927A1 (en) | 2020-01-11 | 2021-07-15 | AskGene Pharma, Inc. | Novel masked cytokines and methods of use thereof |
| WO2021142476A1 (en) | 2020-01-12 | 2021-07-15 | Dragonfly Therapeutics, Inc. | Single-chain polypeptides |
| EP4093875A4 (en) | 2020-01-20 | 2024-02-28 | Chugai Seiyaku Kabushiki Kaisha | Ligand-binding fusion proteins |
| US20230147832A1 (en) | 2020-01-22 | 2023-05-11 | City Of Hope | Oncolytic virus compositions including il-15 complex and methods for the treatment of cancer |
| US20230122079A1 (en) | 2020-03-23 | 2023-04-20 | Zymeworks Inc. | Masked il12 fusion proteins and methods of use thereof |
| CN115734806A (zh) * | 2020-04-01 | 2023-03-03 | 西里欧发展公司 | 掩蔽的il-12细胞因子和其切割产物 |
| KR20220161404A (ko) * | 2020-04-01 | 2022-12-06 | 실리오 디벨럽먼트, 인크. | 마스킹된 il-2 사이토카인 및 이들의 절단 산물 |
| WO2021202673A2 (en) | 2020-04-01 | 2021-10-07 | Xilio Development, Inc. | Masked il-15 cytokines and their cleavage products |
| AU2021260960A1 (en) | 2020-04-22 | 2022-11-24 | Dragonfly Therapeutics, Inc. | Formulation, dosage regimen, and manufacturing process for heterodimeric Fc-fused proteins |
| GB2621482B (en) | 2020-05-13 | 2024-09-04 | Bonum Therapeutics Inc | Compositions of protein complexes and methods of use thereof |
| JP2023553323A (ja) | 2020-11-25 | 2023-12-21 | エクシリオ デベロップメント, インコーポレイテッド | 腫瘍特異的に切断可能なリンカー |
| CA3259097A1 (en) | 2022-07-15 | 2024-01-18 | Xilio Development, Inc. | Modified Clivable FC Domain Used as Carriers and its Methods of Use |
-
2021
- 2021-11-24 JP JP2023531600A patent/JP2023553323A/ja active Pending
- 2021-11-24 TW TW110143870A patent/TW202235431A/zh unknown
- 2021-11-24 US US17/535,451 patent/US12280120B2/en active Active
- 2021-11-24 KR KR1020237021302A patent/KR20230113581A/ko active Pending
- 2021-11-24 EP EP21899266.7A patent/EP4251187A4/en active Pending
- 2021-11-24 WO PCT/US2021/072603 patent/WO2022115865A2/en not_active Ceased
- 2021-11-24 CA CA3196844A patent/CA3196844A1/en active Pending
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2017523176A (ja) * | 2014-07-25 | 2017-08-17 | シトムクス セラピューティクス,インコーポレイティド | 抗−cd3抗体、活性化可能抗−cd3抗体、多重特異的抗−cd3抗体、多重特異的活性化可能抗−cd3抗体、及びそれらの使用方法 |
| JP2018504925A (ja) * | 2015-01-20 | 2018-02-22 | シトムクス セラピューティクス,インコーポレイティド | マトリックスメタロプロテアーゼ切断可能及びセリンプロテアーゼ切断可能な基質並びにそれらの使用方法 |
| WO2020069398A1 (en) * | 2018-09-27 | 2020-04-02 | Akrevia Therapeutics Inc. | Masked cytokine polypeptides |
| WO2020139920A2 (en) * | 2018-12-26 | 2020-07-02 | City Of Hope | Activatable masked anti-ctla4 binding proteins |
Also Published As
| Publication number | Publication date |
|---|---|
| US20230072822A1 (en) | 2023-03-09 |
| WO2022115865A2 (en) | 2022-06-02 |
| US12280120B2 (en) | 2025-04-22 |
| EP4251187A2 (en) | 2023-10-04 |
| WO2022115865A3 (en) | 2022-07-07 |
| CA3196844A1 (en) | 2022-06-02 |
| KR20230113581A (ko) | 2023-07-31 |
| EP4251187A4 (en) | 2025-09-10 |
| TW202235431A (zh) | 2022-09-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7771076B2 (ja) | マスクされたil-12サイトカイン及びその切断産物 | |
| JP7735306B2 (ja) | マスクされたil-2サイトカイン及びその切断産物 | |
| KR102874838B1 (ko) | 마스킹된 사이토카인 폴리펩타이드 | |
| US12280120B2 (en) | Tumor-specific cleavable linkers | |
| US20230331799A1 (en) | Masked il-15 cytokines and their cleavage products | |
| TWI906278B (zh) | 經遮蔽之il-12細胞激素及其裂解產物 | |
| HK40092028A (zh) | 掩蔽的il-2细胞因子和其切割产物 | |
| HK40090912A (zh) | 掩蔽的il-15细胞因子和其切割产物 | |
| EA049880B1 (ru) | Маскированные цитокиновые полипептиды |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20241118 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20241118 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20251014 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20251017 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20260114 |