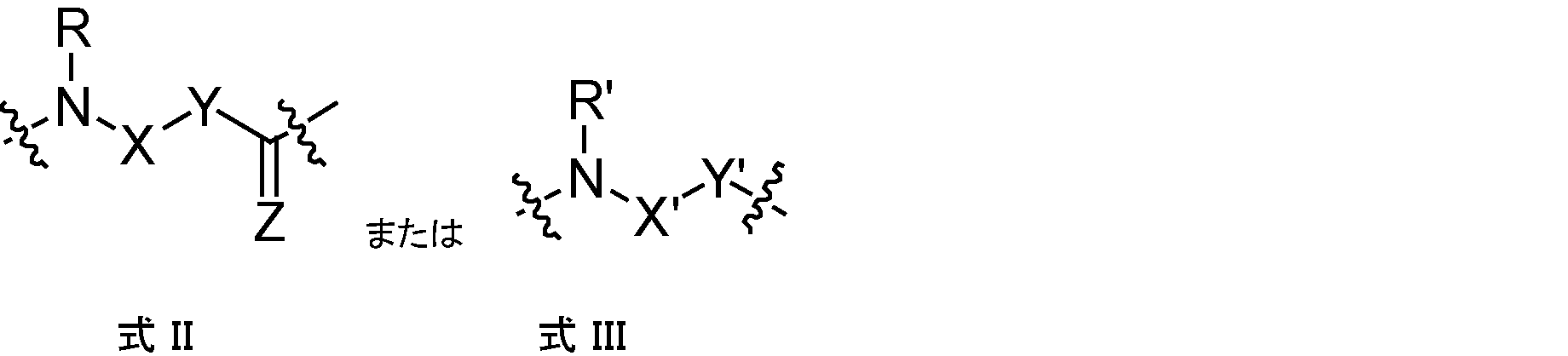JP2023510472A - アミノキシ酸系抗がん幹細胞化合物およびその方法 - Google Patents
アミノキシ酸系抗がん幹細胞化合物およびその方法 Download PDFInfo
- Publication number
- JP2023510472A JP2023510472A JP2022530744A JP2022530744A JP2023510472A JP 2023510472 A JP2023510472 A JP 2023510472A JP 2022530744 A JP2022530744 A JP 2022530744A JP 2022530744 A JP2022530744 A JP 2022530744A JP 2023510472 A JP2023510472 A JP 2023510472A
- Authority
- JP
- Japan
- Prior art keywords
- substituted
- unsubstituted
- alkyl
- compound
- sff
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C259/00—Compounds containing carboxyl groups, an oxygen atom of a carboxyl group being replaced by a nitrogen atom, this nitrogen atom being further bound to an oxygen atom and not being part of nitro or nitroso groups
- C07C259/04—Compounds containing carboxyl groups, an oxygen atom of a carboxyl group being replaced by a nitrogen atom, this nitrogen atom being further bound to an oxygen atom and not being part of nitro or nitroso groups without replacement of the other oxygen atom of the carboxyl group, e.g. hydroxamic acids
- C07C259/10—Compounds containing carboxyl groups, an oxygen atom of a carboxyl group being replaced by a nitrogen atom, this nitrogen atom being further bound to an oxygen atom and not being part of nitro or nitroso groups without replacement of the other oxygen atom of the carboxyl group, e.g. hydroxamic acids having carbon atoms of hydroxamic groups bound to carbon atoms of six-membered aromatic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/16—Amides, e.g. hydroxamic acids
- A61K31/165—Amides, e.g. hydroxamic acids having aromatic rings, e.g. colchicine, atenolol, progabide
- A61K31/166—Amides, e.g. hydroxamic acids having aromatic rings, e.g. colchicine, atenolol, progabide having the carbon of a carboxamide group directly attached to the aromatic ring, e.g. procainamide, procarbazine, metoclopramide, labetalol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
- A61K31/403—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil condensed with carbocyclic rings, e.g. carbazole
- A61K31/404—Indoles, e.g. pindolol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/02—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom condensed with one carbocyclic ring
- C07D209/04—Indoles; Hydrogenated indoles
- C07D209/10—Indoles; Hydrogenated indoles with substituted hydrocarbon radicals attached to carbon atoms of the hetero ring
- C07D209/12—Radicals substituted by oxygen atoms
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Organic Chemistry (AREA)
- Epidemiology (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
Description
アミノキシ酸は標準的なペプチドカップリングの手順で合成した。その構造を図1に示す。CSCは、浮遊条件下でスフェロイド培養することで得る。これらのスフェアは実際に、卵巣CSCを表し得ると報告されているCD133抗原表現型を有する細胞のポピュレーショが著しく多いことが確認されている(図2)。化合物で48時間処理した後、CELLTITER-GLO(登録商標)発光試薬でCSCの細胞生存率を測定した。化合物sff-3-85(「実施例2」)は用量10μMで用い、その他の化合物は全て濃度5μMで用いた。実験はいずれも3回実施され、データは平均値±SDで提示する。
CD133は卵巣CSCマーカーであることが報告されている。細胞を合成分子で処理した後、CD133+細胞のポピュレーションを測定した。HEY A8細胞をタキソール(100nM)、濃度15μMの化合物sff-2-112(「実施例1」)またはsff-2-132(「実施例4」)で処理した。0.1%DMSOを含有する培地をネガティブコントロールとして用いた。図5の結果から、sff-2-112(「実施例1」)および化合物sff-2-132(「実施例4」)は、DMSO処理群と比較して、CD133+細胞のポピュレーションを著しく減少させたことが明らかとなった。
化合物sff-2-112(「実施例1」)またはsff-2-132(「実施例4」)のミトコンドリア膜電位に対する効果をHey A8細胞およびCSCにおいて検討した(図8)。図8aに示すデータから、sff-2-112(「実施例1」)またはsff-2-132(「実施例4」)は、ミトコンドリア膜電位を用量依存的に脱分極できることがわかった。動態研究により、これら2種の分子が添加時に30秒以内にミトコンドリア膜電位を脱分極したことがわかった(図8b)。
下記の一般手順に従って、化合物sff-3-85、sff-3-100、sff-3-101(「実施例2、9、および10」)を合成した(スキームI)。
細胞培養
ヒト卵巣癌細胞株HEY A8およびSKOV3は、Alice Wong教授のグループ(香港大学)から寄贈された。10%FBSおよび1%ペニシリン/ストレプトマイシンを添加したダルベッコ改変イーグル(DMEM)培地において、5%CO2を含む加湿雰囲気中、37℃で細胞を成長させた。スフェアの単離および培養は、無血清の幹細胞選択的条件で、Ip etl.Oncogene 2014,5,9133-9149に記載の通り行った。要約すると、プレーティングから1~2週間後、非接着性球状細胞クラスターが観察でき、これらを低速遠心分離により単一細胞から分離した。8~10回目の継代後、非接着性球状細胞クラスターが明瞭なスフェアとして出現した。この選択条件を用いて、HEY A8スフェア(HEY A8 SP)またはSKOV3スフェア(SKOV3 SP)を酵素的に解離し、幹細胞選択的条件下で3日以内にスフェアに再形成させることができた。分化させるために、解離したスフェア細胞を、10%FBSおよび1%PSを添加した培地(MCDB105:M199=1:1)で組織培養プレートにプレーティングした。
100mmペトリ皿中の無血清MCDB105培地10mLに、HEY A8 SP細胞(5×104)をトリプリケートで7日間プレーティングしてスフェアを形成した。化合物を最終濃度5μMで添加した。さらに、細胞を37℃で48時間インキュベートした。その後、細胞を遠心分離で回収し、培地を除去した。次いで、CellTiter-Glo(登録商標)Luminescent Cell Viability試薬100μLを各管に添加して、振盪させながら10分間インキュベートした。その後、試薬を96ウェルプレートに移し、マイクロプレートリーダー(SpectraMax 340PC 384、Molecular Devices)で細胞生存率を測定した。
アミノキシ酸系化合物の小規模ライブラリをスクリーニングした後、sff-2-112、sff-3-85、sff-2-124、sff-2-132、sff-3-86、sff-3-87、sff-3-91、sff-3-98-2、sff-3-100、sff-3-101、Amy-1-4、Amy-1-8、sff-2-100、およびFPM-1-187(実施例1、2、3、4、5、6、7、8、9、10、11、12、13、および14)を含む14種の分子が、HEY A8 CSCの細胞生存率を著しく低下させた(図1)。なかでも、化合物sff-2-112、sff-2-132、およびsff-2-100が最も高い毒性を示した。
96ウェルプレート中の完全培地0.1mLに、HEY A8またはSKOV3がん細胞をトリプリケートで24時間プレーティングした。その後、培地を、様々な濃度の化合物を含む新たに調製した培地に交換した。細胞をさらに48時間インキュベートした。次いで、製造元の指示に従って、CellTiter-Glo(登録商標)Luminescent Cell Viability試薬で細胞生存率を測定した。マイクロプレートリーダー(SpectraMax 340PC 384、Molecular Devices)で550nmにおける発光を測定した。
図4に示すように、3種の化合物はいずれも、CSCよりも卵巣がん細胞に対して選択性を示した。とりわけ、化合物sff-2-132(「実施例4」)が最高の選択性を示した。化合物sff-2-132(「実施例4」)のHEY A8 CSCに対するIC50値は1.0±0.9μMであり、Hey A8がん細胞に対しては52.9±1.9μM、SKOV3 CSCに対しては1.0±0.9μM、SKOV3がん細胞に対しては63.4±8.9μMであった。さらなる検討では、化合物sff-2-112(「実施例1」)およびsff-2-132(「実施例4」)に注目した。
HEY A8細胞を濃度2.5×104細胞/mLでDMEM培地に懸濁させた懸濁液を60mm細胞培養ディッシュに播種した。5%CO2を含む加湿雰囲気で細胞を24時間37℃でインキュベートした後、新鮮な培地、またはパクリタキセル(100nM)、sff-2-112(15μM)、もしくは化合物sff-2-132(15μM)を含む培地4mLを添加した。0.1%DMSOを含む培地をネガティブコントロールとして用いた。3日後、培地を除去し、細胞を冷PBSで2回洗浄した後、製造元の指示に従ってPE結合CD133抗体で染色した。フローサイトメトリーで蛍光を測定した。
CD133は卵巣がん細胞のがん幹細胞マーカーであることが報告されている。化合物sff-2-112(「実施例1」)またはsff-2-132(「実施例4」)がCSCポピュレーションに与える具体的な影響を評価するために、HEY A8細胞のCD133をPE結合CD133抗体で測定した(図5)。最終濃度10nMのタキソールをネガティブコントロールとして用いた。化合物sff-2-112(「実施例1」)による処理後、CD133+細胞ポピュレーションは21.8%から12.6%に減少した。化合物sff-2-132(「実施例4」)による処理後、卵巣がん細胞中のCD133+細胞ポピュレーションは21.8%から1.9%と、約10分の1に減少した。対照的に、パクリタキセルによる処理では、CD133+細胞ポピュレーションは21.8%から31.6%に増加した。これらの結果から、化合物sff-2-112(「実施例1」)またはsff-2-132(「実施例4」)はHEY A8 CSCポピュレーションを選択的に減少させることができることが確認された。
濃度15μMもしくは30μMの化合物DMSO sff-2-112(「実施例1」)またはsff-2-132(「実施例4」)でHey A8細胞を48時間処理した。次いで、細胞培養ディッシュ中の完全培地で細胞を3日間回復および成長させた。その後、細胞を5×104細胞/mLの密度で低接着ディッシュに5日間移して、スフェアを形成させた。各ディッシュ中のスフェア数を数えた。
浮遊培養条件でのスフェロイド形成がCSCポピュレーションと相関することは周知である。卵巣がんHEY A8細胞の浮遊培養時スフェロイド形成能に対するsff-2-112(「実施例1」)またはsff-2-132(「実施例4」)の効果についても評価した。化合物sff-2-112(「実施例1」)またはsff-2-132(「実施例4」)での処理の結果、コントロールと比較して、スフェア数が著しく減少した(図6)。
化合物sff-2-112(「実施例1」)またはsff-2-132(「実施例4」)による処理後の細胞の生体内腫瘍播種能を評価した。タキソールをネガティブコントロールとして用いた。この実験のために、懸濁培地で2日間、HEY A8 CSCをsff-2-112(「実施例1」)、sff-2-132(「実施例4」)、またはタキソールによりそれぞれ前処理した。次いで、薬物を含まない完全培地で細胞を10日間増殖させた。その後、106個の細胞をマウスに皮下注射した。注射後25日間、腫瘍の大きさを測定した。
図7に示すように、化合物sff-2-112(「実施例1」)またはsff-2-132(「実施例4」)による前処理の結果、タキソールまたはDMSO前処理と比較して、腫瘍播種能が著しく低下した。これらの知見から、卵巣ポピュレーション内のCSCは、パクリタキセルに対しては抵抗性があるが、化合物sff-2-112(「実施例1」)またはsff-2-132(「実施例4」)による処理に対しては感受性があることがわかった。
HEY A8細胞を5×104細胞/mLの濃度でDMEM培地に懸濁させた懸濁液を30mm細胞培養ガラスボトムディッシュ(MatTek)に播種した。5%CO2を含む加湿雰囲気で細胞を24時間37℃でインキュベートした。培地を吸引し、細胞をPBSバッファで2回洗浄した。次いで、2.5μM JC-1を含むHBSSバッファ1mLを添加した。細胞を37℃で20分間インキュベートしてから、バッファを吸引した。細胞をPBSバッファで2回洗浄し、カチオントランスポーターで10分間処理した。ZEISS LSM780(赤チャンネル:λex=543nm、緑チャンネル:λex=488nm)を用いた共焦点イメージングで蛍光をモニターした。ZENおよびGraph Pad Prismソフトウェアパッケージを用いて定量データを得た。
図8aに示すように、化合物sff-2-112(「実施例1」)またはsff-2-132(「実施例4」)は、用量依存的にHEY A8細胞のミトコンドリア膜電位(MMP)を効果的に脱分極できる。また、HEY A8細胞中のMMPに関してこの化合物の動態研究を行った。最終濃度10μMの化合物sff-2-112(「実施例1」)またはsff-2-132(「実施例4」)を180秒の時点で添加した。各画像の間隔は30秒であった。JC-1の赤/緑蛍光比率が低下していることから、MMPが脱分極したことがわかる。図8bに示す結果から、化合物sff-2-112(「実施例1」)またはsff-2-132(「実施例4」)を添加した際、直ちにMMPが脱分極した。
HEY A8細胞を5×104細胞/mLの濃度でDMEM培地に懸濁させた懸濁液を30mm細胞培養ガラスボトムディッシュ(MatTek)に播種した。5%CO2を含む加湿雰囲気で細胞を24時間37℃でインキュベートした。培地を吸引し、細胞をPBSバッファで2回洗浄した。次いで、4μM HKSOX-2mを含むHBSSバッファ1mLを添加した。細胞を37℃で30分間インキュベートしてから、バッファを吸引し、HBSSバッファで2回洗浄した。HBSSバッファ0.8mL中で細胞をイメージングした。共焦点顕微鏡(ZEISS LSM710、赤チャンネル:λex=543nm)で蛍光をモニターした。t=180秒において、HBSSバッファ0.2mL中の化合物を添加して、最終濃度を5μMとした。ZENおよびGraph Pad Prismソフトウェアを用いて定量データを得た。
化合物sff-2-112(「実施例1」)またはsff-2-132(「実施例4」)の場合、30分以内にスーパーオキシド産生が約2倍に増加したことが検出された。
酸素消費率(OCR)を測定するXF24細胞外フラックスアナライザー(Seahorse、Bioscience)を用いて、細胞呼吸を測定した。接着Hey A8細胞を50000細胞/ウェルでその培養培地200mLに播種し、5%CO2を含む加湿雰囲気で24時間37℃でインキュベートした。次いで、1mMピルビン酸ナトリウムおよび2mM L-グルタミンを添加した無血清の高グルコースDMEM670μL/ウェルで培地を交換した。予めプログラムされた通り、オリゴマイシン(最終濃度1μMまで)、FCCP(最終濃度500nMまで)、アンチマイシンAおよびロテノン(最終濃度0.5μMまで)を添加した際、既定の時間間隔で細胞外フラックスアナライザー(Seahorse)を用いて酸素消費率(OCR)を測定した。
化合物sff-2-112(「実施例1」)または化合物sff-2-132(「実施例4」)を添加した後、OCRは直ちに上昇した。しかし、その後、続くFCCP、アンチマイシンA、およびロテノンの添加に対する細胞呼吸応答は著しく低下した(図10)。これらの結果から、呼吸鎖が両化合物から影響を受けることがわかった。このような効果は、合成分子の添加量が多いほど顕著であった。
HEY A8細胞を5×104細胞/mLの濃度でDMEM培地に懸濁させた懸濁液を60mm細胞培養ディッシュに播種した。5%CO2を含む加湿雰囲気で細胞を24時間37℃でインキュベートした後、新鮮な培地、または化合物sff-2-112(「実施例1」)もしくはsff-2-132(「実施例4」)を各種濃度で含む培地4mLを添加した。0.1%DMSO含む培地をネガティブコントロールとして用いた。2日後、培地を吸引し、細胞を冷PBSで2回洗浄した後、製造元の指示に従ってPIおよびアネキシンVで染色した(Dead Cell Apoptosis Kit with Annexin V Alexa Fluor(商標)488&Propidium Iodide、Thermo Fisher)。細胞をフローサイトメトリー(BD FACS CantoIIアナライザー)で分析した。
図11aに示すように、CSCのDMSO処理単独では、4.92%のアネキシンV陽性細胞が産生された。化合物sff-2-112(「実施例1」)により5μMで処理すると、21.0%のアネキシンV陽性細胞が産生された。化合物sff-2-132(「実施例4」)により5μMで処理すると、30.4%のアネキシンV陽性細胞が産生された。がん細胞の場合、DMSO処理単独では、1.73%のアネキシンV陽性細胞が産生された。化合物sff-2-112(「実施例1」)により30μMで処理すると、8.21%のアネキシンV陽性細胞が産生された。
HEY A8がん細胞およびCSCを化合物sff-2-112(「実施例1」)またはsff-2-132(「実施例4」)で24時間処理した。その後、細胞をPBSバッファで2回洗浄し、溶解させて免疫染色を行った。免疫染色方法は実施例10に記載した方法と同じであった。
CSC中のLC3-IIおよびp62のレベルがいずれも上昇していることから、オートファジーが抑制されたことがわかった。CSCにおいては、化合物sff-2-112(「実施例1」)またはsff-2-132(「実施例4」)の濃度ががん細胞の場合の濃度の10分の1であっても、このような効果はより顕著であった。
Huh-7細胞を、製造元の指示に従ってPE結合CD133抗体(HCCがん幹細胞マーカー)で染色した。その後、フローサイトメトリーでCD133+細胞(Huh7がん幹細胞)およびCD133-細胞を分別し、新鮮なDMEM培地を含む96ウェルプレートに播種した。24時間後、培地を、各種用量の化合物sff-2-112(「実施例1」)またはsff-2-124(「実施例3」)を含む新鮮な培地に変更した。48時間後、細胞生存率をCellTiter-Glo発光試薬で分析した。
化合物sff-2-112(「実施例1」)またはsff-2-124(「実施例3」)は、CD133-およびCD133+細胞の両方の死を誘導できる。化合物sff-2-124の場合、huh7がん幹細胞(CD133+ポピュレーション)に対する毒性がCD133-細胞に対する毒性よりも高かった。
Claims (27)
- 式I:
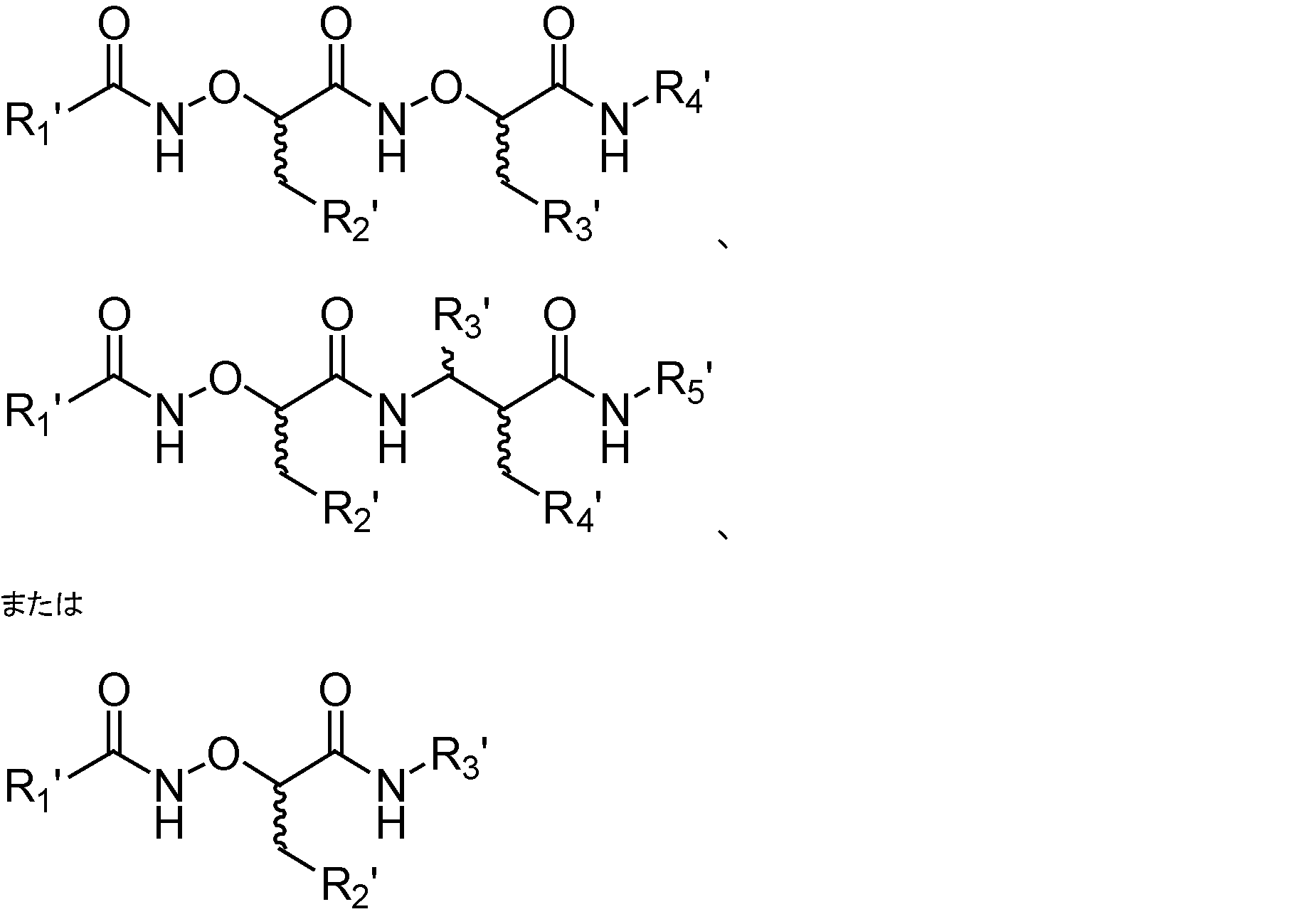
Bは、それぞれ独立して、下記構造:
Y、Y’、およびY’’は、独立して、置換もしくは非置換のアルキル、存在しない、O、S、NR3、置換もしくは非置換のアルキレン、置換もしくは非置換のアリール、置換もしくは非置換のヘテロアリール、置換もしくは非置換のポリアリール、置換もしくは非置換のポリヘテロアリール、置換もしくは非置換のアラルキル、置換もしくは非置換のヘテロアラルキル、置換もしくは非置換のヘテロアラルキル、置換もしくは非置換のポリアラルキル、置換もしくは非置換のポリヘテロアラルキル、置換もしくは非置換のC3-C20シクロアルキル、置換もしくは非置換のC3-C20シクロアルケニル、置換もしくは非置換のC3-C20シクロアルキニル、置換もしくは非置換のC3-C20ヘテロシクリル、または置換もしくは非置換のアミノアルキルであり;
Zは、O、S、またはNR4である)を有し;
L1およびL2は、独立して、-OC(O)-、-C(O)-、-S(O)2-、-O-、存在しない、-C(O)O-、-S(O)-、-C(O)NH-、-C(O)NRiv-、-NRivC(O)-、-C(O)OCH2-、-SO2NRiv-、-CH2Riv-、-NRivH-、-NRiv-、-OCONH-、-NHCOO-、-OCONRiv-、-NRivCOO-、-NHCONH-、-NRivCONH-、-NHCONRiv-、-NRivCONRiv-、-CHOH-、-CRivOH-、置換もしくは非置換のアルキル、置換もしくは非置換のアルキレン、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキルアミノ、置換もしくは非置換のアルキニル、置換もしくは非置換のアルコキシアルキル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のC3-C20シクロアルキル、置換もしくは非置換のC3-C20シクロアルケニル、置換もしくは非置換のC3-C20シクロアルキニル、置換もしくは非置換のC3-C20ヘテロシクリル、置換もしくは非置換のアミノアルキル、置換もしくは非置換のアリール、置換もしくは非置換のアルカリール、置換もしくは非置換のアリールアルキル、置換もしくは非置換のカルボキシアルキル、置換もしくは非置換のアルコキシカルボニル、置換もしくは非置換のアシル、または置換もしくは非置換のアミノカルボニルであり;
R1、R2、R3、R4、R5、R、R’、R’’、R’’’、およびRivは、独立して、水素、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のアルコキシアルキル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のC3-C20シクロアルキル、置換もしくは非置換のC3-C20シクロアルケニル、置換もしくは非置換のC3-C20シクロアルキニル、置換もしくは非置換のC3-C20ヘテロシクリル、置換もしくは非置換のアミノアルキル、置換もしくは非置換のアリール、置換もしくは非置換のアルカリール、置換もしくは非置換のアラルキル、または置換もしくは非置換のアシルであり;
Cは、置換もしくは非置換のアリール、置換もしくは非置換のヘテロアリール、置換もしくは非置換のポリアリール、置換もしくは非置換のポリヘテロアリール、置換もしくは非置換のアラルキル、置換もしくは非置換のヘテロアラルキル、置換もしくは非置換のポリアラルキル、置換もしくは非置換のポリヘテロアラルキル、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のC3-C20シクロアルキル、置換もしくは非置換のC3-C20シクロアルケニル、置換もしくは非置換のC3-C20シクロアルキニル、非置換もしくは置換C3-C20ヘテロシクリル、置換もしくは非置換のアミノアルキル、置換もしくは非置換のアルカリール、置換もしくは非置換のカルボキシアルキル、置換もしくは非置換のアルコキシカルボニル、置換もしくは非置換のアシル、または置換もしくは非置換のアミノカルボニル、またはHであり;
nは、1~5の整数である)を有する、細胞死を誘導可能な化合物。 - Aは、置換もしくは非置換のアリール、置換もしくは非置換のヘテロアリール、置換もしくは非置換のポリアリール、置換もしくは非置換のポリヘテロアリール、置換もしくは非置換のアラルキル、置換もしくは非置換のヘテロアラルキル、置換もしくは非置換のポリアラルキル、置換もしくは非置換のポリヘテロアラルキル、または置換もしくは非置換のアルキルであり;
L1は、-OC(O)-、-C(O)-、または-S(O)2-である、請求項1に記載の化合物。 - Aは、それぞれ式:(R7-)a(アリール)、(R7-)a(アラルキル)、または(R7-)a(アルキル)を有する置換もしくは非置換のアリール、置換もしくは非置換のアラルキル、または置換もしくは非置換のアルキルであり、R7は、それぞれ独立して、F3C-、F-、Cl-、O2N-、NC-、MeO-、HO-、HC(O)-、(R8)2N-であり、R8は、それぞれ独立して、H、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のアルコキシアルキル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のC3-C20シクロアルキル、置換もしくは非置換のC3-C20シクロアルケニル、置換もしくは非置換のC3-C20シクロアルキニル、置換もしくは非置換のC3-C20ヘテロシクリル、置換もしくは非置換のアミノアルキル、置換もしくは非置換のアリール、置換もしくは非置換のアルカリール、置換もしくは非置換のアラルキル、または置換もしくは非置換のアシルであり、aは、0、1、2、または3である、請求項2に記載の化合物。
- Aは電子吸引性基を含む、請求項1に記載の化合物。
- 上記電子吸引性基は、CF3、NO2、F、Cl、Br、I、CN、CHO、または置換もしくは非置換のカルボニル、スルホニル、トリフルオロアセチル、もしくはトリフルオロメチルスルホニルである、請求項4に記載の化合物。
- Aは、非置換もしくは置換C1-18アルキル、置換もしくは非置換のアリール、または置換もしくは非置換のアラルキルであり、上記置換C1-18アルキル、置換アリール、または置換アラルキルは、酸素含有、窒素含有、または硫黄含有部位を含む、請求項1に記載の化合物。
- L1およびL2は、Bに隣接する原子のうち少なくとも1つが酸素、窒素、または硫黄となるように選択される、請求項1に記載の化合物。
- Xは、置換もしくは非置換のヘテロシクリルであり、上記ヘテロシクリルは、酸素含有、窒素含有、もしくは硫黄含有部位または電子吸引性基で置換されていてもよい、請求項1~6のいずれか1項に記載の化合物。
- 上記電子吸引性基は、CF3、NO2、F、Cl、Br、I、CN、またはCHOである、請求項8に記載の化合物。
- Y、Y’、またはY’’は、それぞれ独立して、置換もしくは非置換のC1-10アルキル、置換もしくは非置換のアラルキルであり、上記置換アルキルまたは置換アラルキルは、酸素含有、窒素含有、もしくは硫黄含有部位または電子吸引性基を含む、請求項1~8のいずれか1項に記載の化合物。
- 上記電子吸引性基は、CF3、NO2、F、Cl、Br、I、CN、またはCHOである、請求項10に記載の化合物。
- L2は、NR10、O、S、または存在せず、R10は、H、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のアルコキシアルキル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のC3-C20シクロアルキル、置換もしくは非置換のC3-C20シクロアルケニル、置換もしくは非置換のC3-C20シクロアルキニル、置換もしくは非置換のC3-C20ヘテロシクリル、置換もしくは非置換のアミノアルキル、置換もしくは非置換のアリール、置換もしくは非置換のアルカリール、置換もしくは非置換のアリールアルキル、置換もしくは非置換のカルボキシアルキル、置換もしくは非置換のアルコキシカルボニル、置換もしくは非置換のアシル、または置換もしくは非置換のアミノカルボニルであり、
Cは、H、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のアルコキシアルキル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のC3-C20シクロアルキル、置換もしくは非置換のC3-C20シクロアルケニル、置換もしくは非置換のC3-C20シクロアルキニル、置換もしくは非置換のC3-C20ヘテロシクリル、アミノアルキル、置換もしくは非置換のアリール、置換もしくは非置換のアルカリール、置換もしくは非置換のC3-C20アラルキル、置換もしくは非置換のカルボキシアルキル、置換もしくは非置換のC3-C20アルコキシカルボニル、置換もしくは非置換のC3-C20アシル、または置換もしくは非置換のC3-C20アミノカルボニルである、請求項1~11のいずれか1項に記載の化合物。 - Cは、式:-(アリール)(-R11)bを有する置換もしくは非置換のアリール、-R11、または-O-R11であり、R11は、それぞれ独立して、-CF3、-F、C-Cl、-NO2、-CN、-O-Me、-OH、-NR12であり、R12は、それぞれ独立して、H、置換もしくは非置換のアルキル、置換もしくは非置換のアルケニル、置換もしくは非置換のアルキニル、置換もしくは非置換のアルコキシアルキル、置換もしくは非置換のヘテロアルキル、置換もしくは非置換のC3-C20シクロアルキル、置換もしくは非置換のC3-C20シクロアルケニル、置換もしくは非置換のC3-C20シクロアルキニル、置換もしくは非置換のC3-C20ヘテロシクリル、置換もしくは非置換のアミノアルキル、置換もしくは非置換のアリール、置換もしくは非置換のアルカリール、置換もしくは非置換のアリールアルキル、置換もしくは非置換のカルボキシアルキル、置換もしくは非置換のアルコキシカルボニル、置換もしくは非置換のアシル、または置換もしくは非置換のアミノカルボニルであり、bは、0、1、2、または3である、請求項12に記載の化合物。
- Bは、
Yは-CR13R14-であり、R13は、-CH2-C6H5、-CH2-O-C6H5、-C1-4アルキル、-O-C1-4アルキル、-CH2-(フェニル)(-R15)c、-CH2-O-(フェニル)(-R15)c、-C1-4アルキル-R15、または-O-C1-4アルキル-R15であり、R14はHであり、R15は、それぞれ独立して、-CF3、-F、C-Cl、-NO2、-CN、-O-Me、-OH、-NHであり、cは1または2であり、ZはOである)であり;
nは1であり;
Aは、(R7-)a(フェニル)-CO-、C6H5-CH2-、C6H5-O-CH2-、C1-4アルキル-、またはC1-4アルキル-O-であり、aは2であり、R7は、それぞれ独立して、F3C-、F-、Cl-、O2N-、NC-、MeO-、HO-、HN-であり;
L1は-C(O)-または存在せず;
Cは、-CH2-C6H5、-CH2-O-C6H5、-C1-4アルキル、-O-C1-4アルキル、-CH2-(フェニル)(-R16)d、-CH2-O-(フェニル)(-R16)d、-C1-4アルキル-R16、または-O-C1-4アルキル-R16であり、R16は、それぞれ独立して、-CF3、-F、C-Cl、-NO2、-CN、-O-Me、-OH、-NHであり、dは1または2であり;
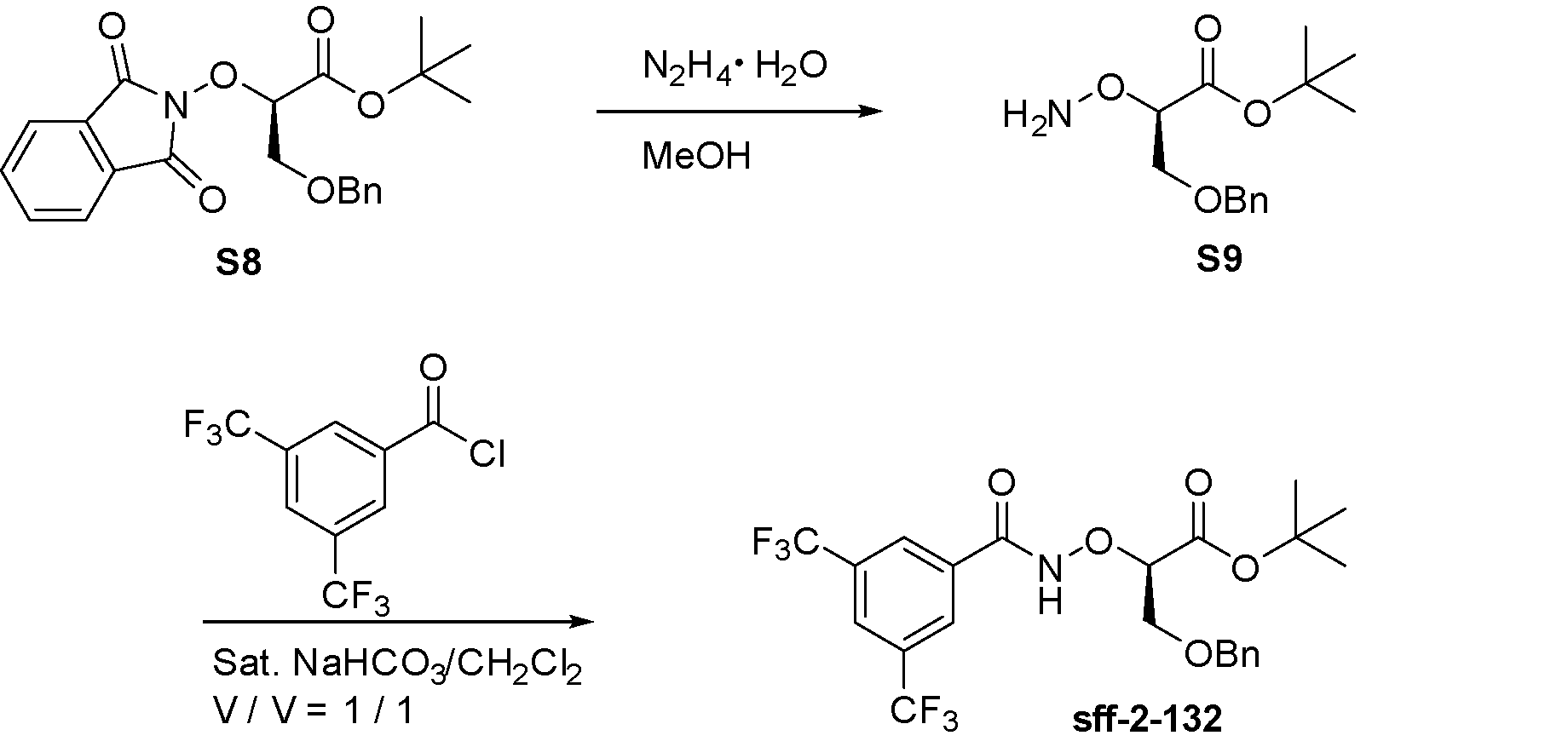
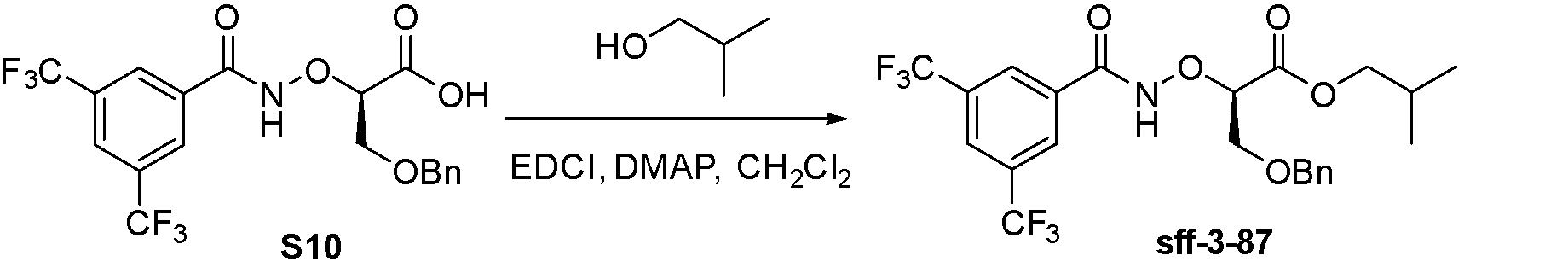
L2は、NH、O、またはSである、請求項1~13のいずれか1項に記載の化合物。 - 上記化合物は、
- 薬物として使用される、請求項1~17のいずれか1項に記載の化合物。
- がん、有利には卵巣がんおよび肝臓がんの治療に使用される、請求項18に記載の化合物。
- がん幹細胞の阻害によるがんの治療に使用される、請求項18に記載の化合物。
- がん幹細胞、有利には卵巣がん幹細胞および肝臓がん幹細胞の阻害に使用される、請求項18に記載の化合物。
- ミトコンドリア膜電位の脱分極、ミトコンドリアの形態変化、スーパーオキシド産生、および呼吸の減衰を含むがこれらに限定されないミトコンドリア機能に影響を与えることにより誘導されるがんまたは他の疾患の治療に使用される、請求項18に記載の化合物。
- 少なくとも、請求項1~17のいずれか1項に記載の式(I、II、III、IV)で表される化合物、その薬学的に許容される塩、溶媒和物、または水和物、および少なくとも1種の薬学的に許容される賦形剤を含み、有利には卵巣がんおよび肝臓がんなどのがんの治療に使用される、医薬組成物。
- 少なくとも、請求項1~17のいずれか1項に記載の式(I、II、III、IV)で表される化合物、その薬学的に許容される塩、溶媒和物、または水和物、および少なくとも1種の薬学的に許容される賦形剤を含み、有利には卵巣がん幹細胞および肝臓がん幹細胞などのがん幹細胞の阻害に使用される、医薬組成物。
- 化合物sff-2-112、その薬学的に許容される塩、溶媒和物、または水和物、および少なくとも1種の薬学的に許容される賦形剤を含み、卵巣がん幹細胞ではないがん幹細胞の阻害に使用される、医薬組成物。
- さらに、別の抗がん剤を含む、請求項23~25に記載の医薬組成物。
- 特にがん、有利には卵巣がんおよび肝臓がんの治療において、医薬として同時に、別々に、または時間差で使用される組み合わせ製品として、請求項1~22に記載の化合物および別の化学療法化合物を含む医薬製品。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201962939803P | 2019-11-25 | 2019-11-25 | |
| US62/939,803 | 2019-11-25 | ||
| US201962940601P | 2019-11-26 | 2019-11-26 | |
| US62/940,601 | 2019-11-26 | ||
| PCT/CN2020/130792 WO2021104199A1 (en) | 2019-11-25 | 2020-11-23 | Aminoxy acid-based anti-cancer stem cell compounds and methods thereof |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2023510472A true JP2023510472A (ja) | 2023-03-14 |
| JP7323238B2 JP7323238B2 (ja) | 2023-08-08 |
Family
ID=76129153
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022530744A Active JP7323238B2 (ja) | 2019-11-25 | 2020-11-23 | アミノキシ酸系抗がん幹細胞化合物およびその方法 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US12539284B2 (ja) |
| EP (1) | EP4065550B1 (ja) |
| JP (1) | JP7323238B2 (ja) |
| CN (1) | CN114929664B (ja) |
| WO (1) | WO2021104199A1 (ja) |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2006104751A2 (en) * | 2005-03-30 | 2006-10-05 | The Regents Of The University Of Michigan | Methods and compositions for modulating rho-mediated gene transcription |
| JP2010513332A (ja) * | 2006-12-19 | 2010-04-30 | バーシテック、リミテッド | 合成イオンチャネル |
| JP2018521962A (ja) * | 2015-04-30 | 2018-08-09 | ナント ホールディングス アイピー エルエルシーNant Holdings IP, LLC | 催奇形性医薬化合物を介した患者処置 |
| WO2019213570A1 (en) * | 2018-05-04 | 2019-11-07 | Remedy Plan, Inc. | Cancer treatments targeting cancer stem cells |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20240315992A1 (en) * | 2023-03-07 | 2024-09-26 | The University Of Hong Kong | Aminoxy acid-based antibacterial compounds and methods thereof |
-
2020
- 2020-11-23 JP JP2022530744A patent/JP7323238B2/ja active Active
- 2020-11-23 WO PCT/CN2020/130792 patent/WO2021104199A1/en not_active Ceased
- 2020-11-23 CN CN202080081778.3A patent/CN114929664B/zh active Active
- 2020-11-23 EP EP20893980.1A patent/EP4065550B1/en active Active
- 2020-11-23 US US17/779,379 patent/US12539284B2/en active Active
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2006104751A2 (en) * | 2005-03-30 | 2006-10-05 | The Regents Of The University Of Michigan | Methods and compositions for modulating rho-mediated gene transcription |
| JP2010513332A (ja) * | 2006-12-19 | 2010-04-30 | バーシテック、リミテッド | 合成イオンチャネル |
| JP2018521962A (ja) * | 2015-04-30 | 2018-08-09 | ナント ホールディングス アイピー エルエルシーNant Holdings IP, LLC | 催奇形性医薬化合物を介した患者処置 |
| WO2019213570A1 (en) * | 2018-05-04 | 2019-11-07 | Remedy Plan, Inc. | Cancer treatments targeting cancer stem cells |
Non-Patent Citations (2)
| Title |
|---|
| SHEN, FANG-FANG ET AL.: "Mediating K+/H+ Transport on Organelle Membranes to Selectively Eradicate Cancer Stem Cells with a S", JOURNAL OF THE AMERICAN CHEMICAL SOCIETY, vol. 142(24), JPN6023027178, 2020, pages 10769 - 10779, XP055815023, ISSN: 0005100956, DOI: 10.1021/jacs.0c02134 * |
| YANG, DAN ET AL.: "Novel Turns and Helices in Peptides of Chiral α-Aminoxy Acids", JOURNAL OF THE AMERICAN CHEMICAL SOCIETY, vol. 121(3), JPN6023027177, 1999, pages 589 - 590, XP009133359, ISSN: 0005100957, DOI: 10.1021/ja982528y * |
Also Published As
| Publication number | Publication date |
|---|---|
| EP4065550A1 (en) | 2022-10-05 |
| CN114929664A (zh) | 2022-08-19 |
| EP4065550A4 (en) | 2024-01-10 |
| JP7323238B2 (ja) | 2023-08-08 |
| WO2021104199A1 (en) | 2021-06-03 |
| EP4065550B1 (en) | 2024-09-04 |
| US20230301944A1 (en) | 2023-09-28 |
| US12539284B2 (en) | 2026-02-03 |
| CN114929664B (zh) | 2024-04-19 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP2668180B1 (en) | Bcl-2/bcl-xl inhibitors for use in the treatment of cancer | |
| KR102210316B1 (ko) | Bcl-2bcl-xl 억제제 및 그를 사용하는 치료 방법 | |
| US10905665B2 (en) | Chemical modulators of signaling pathways and therapeutic use | |
| US10207998B2 (en) | Substituted benzimidazole and substituted benzothiazole inhibitors of transforming growth factor-β kinase and methods of use thereof | |
| CN105246887B (zh) | 香豆素衍生物以及用于治疗过度增生性疾病的方法 | |
| US8883749B2 (en) | Transcription factor inhibitors and related compositions, formulations and methods | |
| WO2022029138A1 (en) | Low molecular weight protein degraders and their applications | |
| US7652033B2 (en) | HIF-1 inhibitors | |
| CN102311449A (zh) | 棉酚衍生物在制备抗肿瘤药物中的应用 | |
| US9867807B2 (en) | Compositions and methods for drug-sensitization or inhibition of a cancer cell | |
| WO2012129452A2 (en) | Propynoic acid carbamoyl methyl-almides and pharmaceutical compositions and methods based thereon | |
| JP7323238B2 (ja) | アミノキシ酸系抗がん幹細胞化合物およびその方法 | |
| US10689342B2 (en) | Aza-tanshinone derivatives, process for their preparation and their use in therapy | |
| TWI719217B (zh) | 具有抗腫瘤活性的新穎苯并-n-羥基醯胺化合物及藥學組成物 | |
| KR20220033689A (ko) | 히스톤 탈아세틸화효소 억제 활성을 갖는 신규 화합물 및 이의 용도 | |
| Omar et al. | Discovery, optimization, and cellular activities of 2-(aroylamino) cinnamamide derivatives against colon cancer | |
| WO2015123392A1 (en) | Compositions and methods for inhibition of angiogenesis and lymphangiogenesis | |
| NZ749473B2 (en) | Benzo-n-hydroxy amide compounds having antitumor activity |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20220729 Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220722 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20220722 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A711 Effective date: 20220729 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230206 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A711 Effective date: 20230216 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20230216 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230404 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230428 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20230622 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20230704 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20230720 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7323238 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |