JP2023050135A - Composition and light emitting element containing the same - Google Patents
Composition and light emitting element containing the same Download PDFInfo
- Publication number
- JP2023050135A JP2023050135A JP2022147451A JP2022147451A JP2023050135A JP 2023050135 A JP2023050135 A JP 2023050135A JP 2022147451 A JP2022147451 A JP 2022147451A JP 2022147451 A JP2022147451 A JP 2022147451A JP 2023050135 A JP2023050135 A JP 2023050135A
- Authority
- JP
- Japan
- Prior art keywords
- group
- ring
- compound
- bonded
- atom
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Classifications
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E10/00—Energy generation through renewable energy sources
- Y02E10/50—Photovoltaic [PV] energy
- Y02E10/549—Organic PV cells
Landscapes
- Electroluminescent Light Sources (AREA)
Abstract
【課題】駆動電圧の低い発光素子の製造に有用な組成物を提供すること、及び、当該組成物を含有する発光素子の提供。
【解決手段】式(1)で表される金属錯体及び高分子化合物(A)からなる群より選択される少なくとも1種と、低分子化合物(B)、及び、前記低分子化合物(B)から水素原子1個以上を除いた基を有する構成単位を含む高分子化合物(B)からなる群より選択される少なくとも1種と、式(H-1)で表される化合物、及び、高分子化合物からなる群より選択される少なくとも1種と、を含有する、組成物。
【選択図】なし
An object of the present invention is to provide a composition useful for manufacturing a light-emitting device with a low driving voltage, and to provide a light-emitting device containing the composition.
At least one selected from the group consisting of a metal complex represented by formula (1) and a polymer compound (A), a low-molecular-weight compound (B), and the low-molecular-weight compound (B) At least one selected from the group consisting of a polymer compound (B) containing a structural unit having a group from which one or more hydrogen atoms are removed, a compound represented by formula (H-1), and a polymer compound and at least one selected from the group consisting of
[Selection figure] None
Description
本開示は、組成物及びそれを含有する発光素子に関する。 The present disclosure relates to compositions and light emitting devices containing the same.
有機エレクトロルミネッセンス素子等の発光素子は、ディスプレイ及び照明の用途に好適に使用することが可能である。発光素子の発光層に用いられる発光材料として、例えば、特許文献1では、化合物H1と、金属錯体Firpicと、化合物B1とを含有する組成物が記載されている。 A light-emitting device such as an organic electroluminescence device can be suitably used for display and lighting applications. As a light-emitting material used for a light-emitting layer of a light-emitting element, for example, Patent Document 1 describes a composition containing a compound H1, a metal complex Firpic, and a compound B1.
しかし、上記の組成物を用いて作製される発光素子は、駆動電圧が必ずしも十分に低くなかった。
そこで、本開示の一実施形態は、駆動電圧の低い発光素子の製造に有用な組成物を提供すること、及び、当該組成物を含有する発光素子を提供することを目的とする。
However, a light-emitting element manufactured using the above composition does not necessarily have a sufficiently low driving voltage.
Accordingly, an object of one embodiment of the present disclosure is to provide a composition useful for manufacturing a light-emitting device with a low driving voltage, and to provide a light-emitting device containing the composition.
本開示は、以下の<1>~<13>を提供する。 The present disclosure provides the following <1> to <13>.
<1> 式(1)で表される金属錯体及び上記式(1)で表される金属錯体から水素原子1個以上を除いた基を有する構成単位を含む高分子化合物(A)からなる群より選択される少なくとも1種と、
ホウ素原子と、酸素原子、硫黄原子、セレン原子、sp3炭素原子及び窒素原子からなる群より選ばれる少なくとも1種とを環内に含む縮合複素環骨格(b)を有する低分子化合物(B)、並びに、上記低分子化合物(B)から水素原子1個以上を除いた基を有する構成単位を含む高分子化合物(B)からなる群より選択される少なくとも1種と、
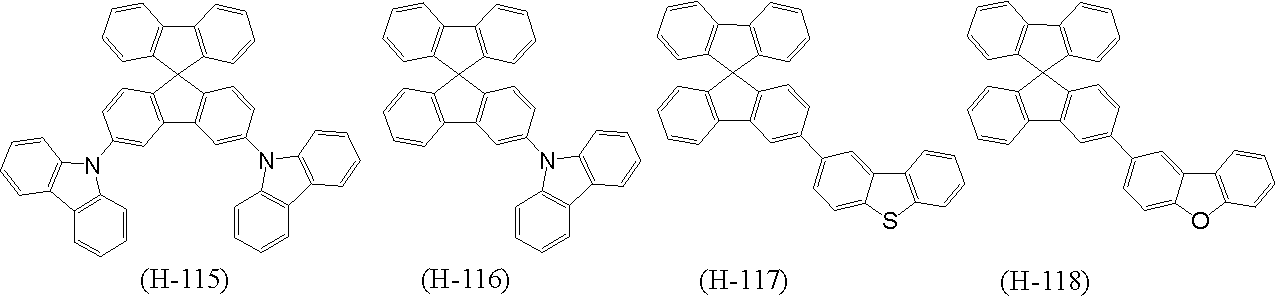
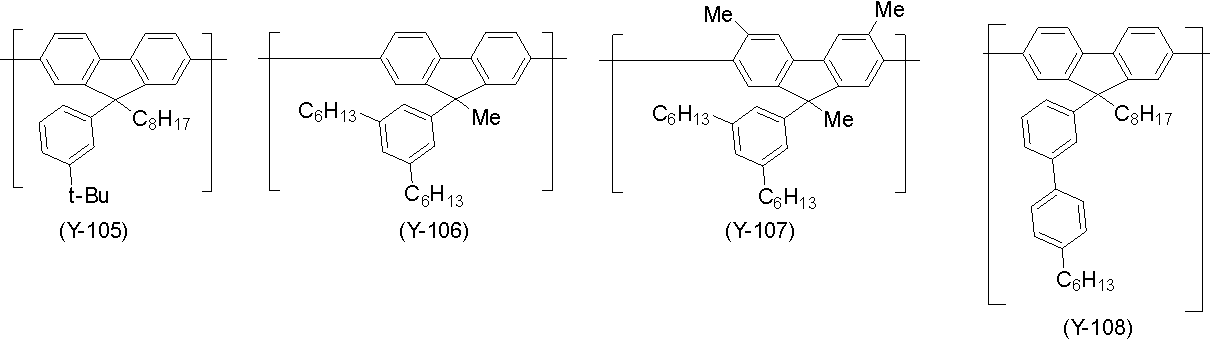
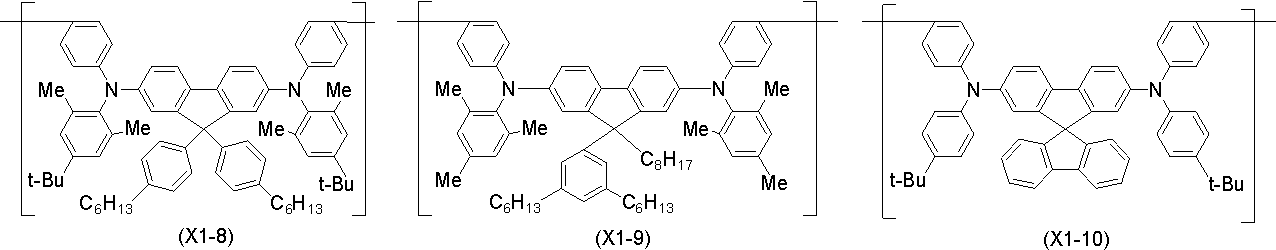
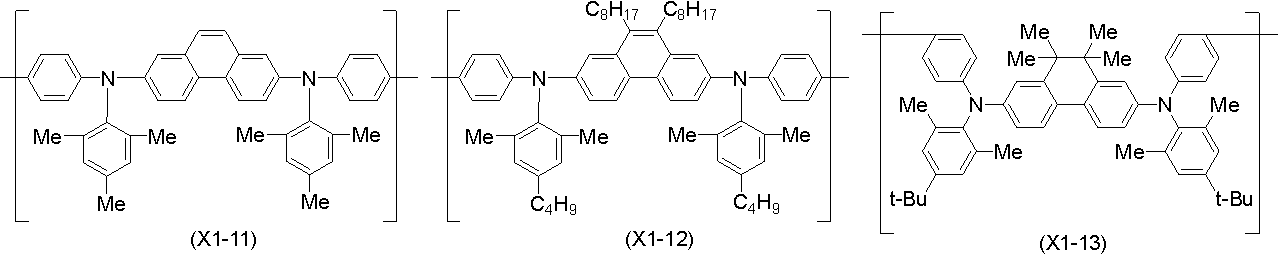
式(H-1)で表される化合物、並びに、式(X)で表される構成単位及び式(Y)で表される構成単位からなる群より選択される少なくとも1種の構成単位を含む高分子化合物からなる群より選択される少なくとも1種と、
を含有する、組成物。
<1> A group consisting of the metal complex represented by the formula (1) and the polymer compound (A) containing a structural unit having a group obtained by removing one or more hydrogen atoms from the metal complex represented by the above formula (1) at least one selected from
A low-molecular-weight compound (B) having a condensed heterocyclic skeleton (b) containing a boron atom and at least one selected from the group consisting of an oxygen atom, a sulfur atom, a selenium atom, an sp3 carbon atom and a nitrogen atom in the ring and at least one selected from the group consisting of a polymer compound (B) containing a structural unit having a group obtained by removing one or more hydrogen atoms from the low-molecular-weight compound (B),
A compound represented by formula (H-1) and at least one structural unit selected from the group consisting of structural units represented by formula (X) and structural units represented by formula (Y) at least one selected from the group consisting of polymer compounds;
A composition comprising
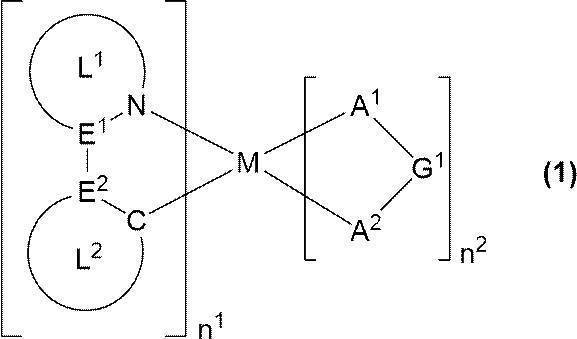
[式中、
Mは、ロジウム原子、パラジウム原子、イリジウム原子又は白金原子を表す。
n1は1以上の整数を表し、n2は0以上の整数を表す。但し、Mがロジウム原子又はイリジウム原子の場合、n1+n2は3であり、Mがパラジウム原子又は白金原子の場合、n1+n2は2である。
E1及びE2は、それぞれ独立に、炭素原子又は窒素原子を表す。E1及びE2が複数存在する場合、それらはそれぞれ同一でも異なっていてもよい。
環L1は、5員環を含む芳香族複素環を表し、該環は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。環L1が複数存在する場合、それらは同一でも異なっていてもよい。
環L2は、芳香族炭化水素環又は芳香族複素環を表し、これらの環は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。環L2が複数存在する場合、それらは同一でも異なっていてもよい。
環L1が有していてもよい置換基と、環L2が有していてもよい置換基とは、同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。
A1-G1-A2は、アニオン性の2座配位子を表す。A1及びA2は、それぞれ独立に、炭素原子、酸素原子又は窒素原子を表し、これらの原子は環を構成する原子であってもよい。G1は、単結合、又は、A1及びA2とともに2座配位子を構成する原子団を表す。A1-G1-A2が複数存在する場合、それらは同一でも異なっていてもよい。]
[In the formula,
M represents a rhodium atom, a palladium atom, an iridium atom or a platinum atom.
n1 represents an integer of 1 or more, and n2 represents an integer of 0 or more. However, n 1 +n 2 is 3 when M is a rhodium atom or an iridium atom, and n 1 +n 2 is 2 when M is a palladium atom or a platinum atom.
E 1 and E 2 each independently represent a carbon atom or a nitrogen atom. When multiple E 1 and E 2 are present, they may be the same or different.
Ring L 1 represents an aromatic heterocyclic ring containing a 5-membered ring, and the ring may have a substituent. When there are multiple such substituents, they may be the same or different, and may be bonded to each other to form a ring together with the atoms to which they are bonded. When multiple rings L 1 are present, they may be the same or different.
Ring L2 represents an aromatic hydrocarbon ring or an aromatic heterocyclic ring, and these rings may have a substituent. When there are multiple such substituents, they may be the same or different, and may be bonded to each other to form a ring together with the atoms to which they are bonded. When there is more than one ring L2 , they may be the same or different.
The substituent that ring L 1 may have and the substituent that ring L 2 may have may be the same or different, and are bonded to each other to form a ring together with the atoms to which they are bonded. may be formed.
A 1 -G 1 -A 2 represents an anionic bidentate ligand. A 1 and A 2 each independently represent a carbon atom, an oxygen atom or a nitrogen atom, and these atoms may be atoms constituting a ring. G 1 represents a single bond or an atomic group forming a bidentate ligand together with A 1 and A 2 . When multiple A 1 -G 1 -A 2 are present, they may be the same or different. ]
[式中、
ArH1及びArH2は、それぞれ独立に、アリール基、1価の複素環基又は置換アミノ基を表し、これらの基は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。
nH1は、0以上の整数を表す。
LH1は、2価の基を表し、該2価の基は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。LH1が複数存在する場合、それらは同一でも異なっていてもよく、それらは互いに、直接結合して、又は、2価の基を介して結合して、環を形成してもよい。
ArH1とArH2とは、直接結合して、又は、2価の基を介して結合して、環を形成してもよい。LH1とArH1とは、直接結合して、又は、2価の基を介して結合して、環を形成してもよい。LH1とArH2とは、直接結合して、又は、2価の基を介して結合して、環を形成してもよい。]
[In the formula,
Ar H1 and Ar H2 each independently represent an aryl group, a monovalent heterocyclic group or a substituted amino group, and these groups may have a substituent. When there are multiple such substituents, they may be the same or different, and may be bonded to each other to form a ring together with the atoms to which they are bonded.
n H1 represents an integer of 0 or more.
L H1 represents a divalent group, and the divalent group may have a substituent. When there are multiple such substituents, they may be the same or different, and may be bonded to each other to form a ring together with the atoms to which they are bonded. When multiple L H1 are present, they may be the same or different, and they may be directly bonded to each other or bonded via a divalent group to form a ring.
Ar H1 and Ar H2 may be directly bonded or bonded via a divalent group to form a ring. L H1 and Ar H1 may be directly bonded or bonded via a divalent group to form a ring. L H1 and Ar H2 may be directly bonded or bonded via a divalent group to form a ring. ]
[式中、
aX1及びaX2は、それぞれ独立に、0以上の整数を表す。
ArX1及びArX3は、それぞれ独立に、アリーレン基又は2価の複素環基を表し、これらの基は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。
ArX2及びArX4は、それぞれ独立に、アリーレン基、2価の複素環基、又は、少なくとも1種のアリーレン基と少なくとも1種の2価の複素環基とが直接結合した2価の基を表し、これらの基は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。ArX2が複数存在する場合、それらはそれぞれ同一でも異なっていてもよい。ArX4が複数存在する場合、それらはそれぞれ同一でも異なっていてもよい。
RX1、RX2及びRX3は、それぞれ独立に、水素原子、アルキル基、シクロアルキル基、アリール基又は1価の複素環基を表し、これらの基は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。RX2が複数存在する場合、それらは同一でも異なっていてもよい。RX3が複数存在する場合、それらは同一でも異なっていてもよい。]
[In the formula,
a X1 and a X2 each independently represent an integer of 0 or more.
Ar 1 X1 and Ar 2 X3 each independently represent an arylene group or a divalent heterocyclic group, and these groups may have a substituent. When there are multiple such substituents, they may be the same or different, and may be bonded to each other to form a ring together with the atoms to which they are bonded.
Ar X2 and Ar X4 each independently represent an arylene group, a divalent heterocyclic group, or a divalent group in which at least one arylene group and at least one divalent heterocyclic group are directly bonded; and these groups may have a substituent. When there are multiple such substituents, they may be the same or different, and may be bonded to each other to form a ring together with the atoms to which they are bonded. When multiple Ar X2 are present, they may be the same or different. When multiple Ar X4 are present, they may be the same or different.
R X1 , R X2 and R X3 each independently represent a hydrogen atom, an alkyl group, a cycloalkyl group, an aryl group or a monovalent heterocyclic group, and these groups may have a substituent. When there are multiple such substituents, they may be the same or different, and may be bonded to each other to form a ring together with the atoms to which they are bonded. When multiple R X2 are present, they may be the same or different. When multiple R X3 are present, they may be the same or different. ]
[式中、ArY1は、アリーレン基、2価の複素環基、又は、少なくとも1種のアリーレン基と少なくとも1種の2価の複素環基とが直接結合した2価の基を表し、これらの基は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。]
<2> 上記環L2が、5員環若しくは6員環を含む芳香族炭化水素環、又は、5員環若しくは6員環を含む芳香族複素環であり、これらの環は置換基を有していてもよい、上記<1>に記載の組成物。
<3> 上記環L2が、単環式、2環式若しくは3環式の芳香族炭化水素環、又は、単環式、2環式若しくは3環式の芳香族複素環であり、これらの環は置換基を有していてもよい、上記<1>又は<2>に記載の組成物。
<4> 上記環L2が、ベンゼン環、フルオレン環、ピリジン環、ジアザベンゼン環、カルバゾール環、ジベンゾフラン環又はジベンゾチオフェン環であり、これらの環は置換基を有していてもよい、上記<1>~<3>のいずれか1つに記載の組成物。
<5> 上記環L1が、ジアゾール環又はトリアゾール環であり、これらの環は置換基を有していてもよい、上記<1>~<4>のいずれか1つに記載の組成物。
<6> 上記環L1が、置換基を有していてもよいトリアゾール環である、上記<1>~<5>のいずれか1つに記載の組成物。
<7> 上記縮合複素環骨格(b)が、ホウ素原子と、酸素原子、硫黄原子及び窒素原子からなる群より選ばれる少なくとも1種と、を環内に含む、上記<1>~<6>のいずれか1つに記載の組成物。
<8> 上記縮合複素環骨格(b)が、ホウ素原子及び窒素原子を環内に含む、上記<1>~<7>のいずれか1つに記載の組成物。
<9> 上記低分子化合物(B)が、式(1-1)で表される化合物、式(1-2)で表される化合物又は式(1-3)で表される化合物である、上記<1>~<6>のいずれか1つに記載の組成物。
[Wherein, Ar Y represents an arylene group, a divalent heterocyclic group, or a divalent group in which at least one arylene group and at least one divalent heterocyclic group are directly bonded, The group may have a substituent. When there are multiple such substituents, they may be the same or different, and may be bonded to each other to form a ring together with the atoms to which they are bonded. ]
<2> The ring L 2 is an aromatic hydrocarbon ring containing a 5- or 6-membered ring, or an aromatic heterocyclic ring containing a 5- or 6-membered ring, and these rings have substituents. The composition according to <1> above.
<3> The ring L 2 is a monocyclic, bicyclic or tricyclic aromatic hydrocarbon ring, or a monocyclic, bicyclic or tricyclic aromatic heterocyclic ring, The composition according to <1> or <2> above, wherein the ring may have a substituent.
<4> The ring L2 is a benzene ring, a fluorene ring, a pyridine ring, a diazabenzene ring, a carbazole ring, a dibenzofuran ring or a dibenzothiophene ring, and these rings may have a substituent. > to the composition according to any one of <3>.
<5> The composition according to any one of <1> to <4> above, wherein the ring L 1 is a diazole ring or a triazole ring, and these rings may have a substituent.
<6> The composition according to any one of <1> to <5>, wherein the ring L 1 is an optionally substituted triazole ring.
<7> The above <1> to <6>, wherein the condensed heterocyclic skeleton (b) contains a boron atom and at least one selected from the group consisting of an oxygen atom, a sulfur atom and a nitrogen atom in the ring. The composition according to any one of
<8> The composition according to any one of <1> to <7>, wherein the condensed heterocyclic skeleton (b) contains a boron atom and a nitrogen atom in the ring.
<9> The low-molecular-weight compound (B) is a compound represented by formula (1-1), a compound represented by formula (1-2), or a compound represented by formula (1-3). The composition according to any one of <1> to <6> above.
[式中、
Ar1、Ar2及びAr3は、それぞれ独立に、芳香族炭化水素基又は複素環基を表し、これらの基は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。
Y1は、酸素原子、硫黄原子、セレン原子、-N(Ry)-で表される基、アルキレン基又はシクロアルキレン基を表し、これらの基は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。
Y2及びY3は、それぞれ独立に、単結合、酸素原子、硫黄原子、セレン原子、-N(Ry)-で表される基、-B(Ry)-で表される基、アルキレン基、シクロアルキレン基、アリーレン基又は2価の複素環基を表し、これらの基は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。
Ryは、水素原子、アルキル基、シクロアルキル基、アリール基又は1価の複素環基を表し、これらの基は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。Ryが複数存在する場合、同一であっても異なっていてもよい。
Y1とAr1とは、直接結合して、又は、2価の基を介して結合して、環を形成してもよい。Y1とAr2とは、直接結合して、又は、2価の基を介して結合して、環を形成してもよい。Y2とAr1とは、直接結合して、又は、2価の基を介して結合して、環を形成してもよい。Y2とAr3とは、直接結合して、又は、2価の基を介して結合して、環を形成してもよい。Y3とAr2とは、直接結合して、又は、2価の基を介して結合して、環を形成してもよい。Y3とAr3とは、直接結合して、又は、2価の基を介して結合して、環を形成してもよい。]
<10> 上記Y1、上記Y2及び上記Y3が、酸素原子、硫黄原子又は-N(Ry)-で表される基である、上記<9>に記載の組成物。
<11> 上記Y1、上記Y2及び上記Y3が、-N(Ry)-で表される基である、上記<9>又は<10>に記載の組成物。
<12> 正孔輸送材料、正孔注入材料、電子輸送材料、電子注入材料、発光材料、酸化防止剤及び溶媒からなる群より選ばれる少なくとも1種を更に含有する、上記<1>~<11>のいずれか1つに記載の組成物。
<13> 陽極と、陰極と、上記陽極及び上記陰極の間に設けられた有機層とを有する発光素子であり、
上記有機層が、上記<1>~<12>のいずれか1つに記載の組成物を含有する層である、発光素子。
[In the formula,
Ar 1 , Ar 2 and Ar 3 each independently represent an aromatic hydrocarbon group or a heterocyclic group, and these groups may have a substituent. When there are multiple such substituents, they may be the same or different, and may be bonded to each other to form a ring together with the atoms to which they are bonded.
Y 1 represents an oxygen atom, a sulfur atom, a selenium atom, a group represented by -N(Ry)-, an alkylene group or a cycloalkylene group, and these groups may have a substituent. When there are multiple such substituents, they may be the same or different, and may be bonded to each other to form a ring together with the atoms to which they are bonded.
Y 2 and Y 3 each independently represent a single bond, an oxygen atom, a sulfur atom, a selenium atom, a group represented by -N(Ry)-, a group represented by -B(Ry)-, an alkylene group, It represents a cycloalkylene group, an arylene group or a divalent heterocyclic group, and these groups may have a substituent. When there are multiple such substituents, they may be the same or different, and may be bonded to each other to form a ring together with the atoms to which they are bonded.
Ry represents a hydrogen atom, an alkyl group, a cycloalkyl group, an aryl group or a monovalent heterocyclic group, and these groups may have a substituent. When there are multiple such substituents, they may be the same or different, and may be bonded to each other to form a ring together with the atoms to which they are bonded. When two or more Ry are present, they may be the same or different.
Y 1 and Ar 1 may be directly bonded or bonded via a divalent group to form a ring. Y 1 and Ar 2 may be directly bonded or bonded via a divalent group to form a ring. Y 2 and Ar 1 may be directly bonded or bonded via a divalent group to form a ring. Y 2 and Ar 3 may be directly bonded or bonded via a divalent group to form a ring. Y 3 and Ar 2 may be directly bonded or bonded via a divalent group to form a ring. Y 3 and Ar 3 may be directly bonded or bonded via a divalent group to form a ring. ]
<10> The composition according to <9>, wherein Y 1 , Y 2 and Y 3 are an oxygen atom, a sulfur atom or a group represented by -N(Ry)-.
<11> The composition according to <9> or <10>, wherein Y 1 , Y 2 and Y 3 are groups represented by -N(Ry)-.
<12> The above <1> to <11, further containing at least one selected from the group consisting of a hole transport material, a hole injection material, an electron transport material, an electron injection material, a light emitting material, an antioxidant and a solvent. The composition according to any one of .
<13> A light-emitting element having an anode, a cathode, and an organic layer provided between the anode and the cathode,
A light-emitting device, wherein the organic layer is a layer containing the composition according to any one of <1> to <12>.
本開示の一実施形態によれば、駆動電圧の低い発光素子の製造に有用な組成物を提供することができる。また、本開示の一実施形態によれば、当該組成物を含有する発光素子を提供することができる。 According to one embodiment of the present disclosure, it is possible to provide a composition useful for manufacturing a light-emitting device with low driving voltage. Further, according to one embodiment of the present disclosure, a light-emitting device containing the composition can be provided.
以下、本開示の好適な実施形態について詳細に説明する。 Preferred embodiments of the present disclosure are described in detail below.
<共通する用語の説明>
本明細書で共通して用いられる用語は、特記しない限り、以下の意味である。
<Description of common terms>
Terms commonly used in this specification have the following meanings unless otherwise specified.
「室温」とは、25℃を意味する。
Meはメチル基、Etはエチル基、Buはブチル基、i-Prはイソプロピル基、t-Buはtert-ブチル基を表す。
水素原子は、重水素原子であっても、軽水素原子であってもよい。
金属錯体を表す式中、中心金属との結合を表す実線は、イオン結合、共有結合又は配位結合を意味する。
"Room temperature" means 25°C.
Me is a methyl group, Et is an ethyl group, Bu is a butyl group, i-Pr is an isopropyl group, and t-Bu is a tert-butyl group.
A hydrogen atom may be a deuterium atom or a protium atom.
In the formulas representing the metal complexes, solid lines representing bonds with the central metal mean ionic bonds, covalent bonds or coordinate bonds.
「低分子化合物」とは、分子量分布を有さず、分子量が1×104以下の化合物を意味する。
「高分子化合物」とは、分子量分布を有し、ポリスチレン換算の数平均分子量が1×103以上(例えば、1×103~1×108)である重合体を意味する。
「構成単位」とは、高分子化合物中に1個以上存在する単位を意味する。高分子化合物中に2個以上存在する構成単位は、一般に、「繰り返し単位」とも呼ばれる。
高分子化合物は、ブロック共重合体、ランダム共重合体、交互共重合体、グラフト共重合体のいずれであってもよいし、その他の態様であってもよい。
高分子化合物の末端基は、発光素子の発光特性等の観点から、安定な基であることが好ましい。
高分子化合物の末端基としては、好ましくは、高分子化合物の主鎖と共役結合している基であり、例えば、炭素-炭素結合を介して高分子化合物の主鎖と結合するアリール基又は1価の複素環基が挙げられる。
A "low-molecular-weight compound" means a compound having no molecular weight distribution and a molecular weight of 1×10 4 or less.
A "polymer compound" means a polymer having a molecular weight distribution and a polystyrene-equivalent number average molecular weight of 1×10 3 or more (for example, 1×10 3 to 1×10 8 ).
A "structural unit" means a unit that exists at least one in a polymer compound. Two or more structural units present in a polymer compound are generally called "repeating units".
The polymer compound may be a block copolymer, a random copolymer, an alternating copolymer, a graft copolymer, or other forms.
The terminal group of the polymer compound is preferably a stable group from the viewpoint of the light emitting properties of the light emitting device.
The terminal group of the polymer compound is preferably a group conjugated to the main chain of the polymer compound, for example, an aryl group or 1 valent heterocyclic groups.
「アルキル基」は、直鎖及び分岐のいずれでもよい。直鎖のアルキル基の炭素原子数は、置換基の炭素原子数を含めないで、通常1~50であり、好ましくは1~20であり、より好ましくは1~10である。分岐のアルキル基の炭素原子数は、置換基の炭素原子数を含めないで、通常3~50であり、好ましくは3~20であり、より好ましくは4~10である。
アルキル基は、置換基を有していてもよい。アルキル基としては、例えば、メチル基、エチル基、プロピル基、イソプロピル基、ブチル基、2-ブチル基、イソブチル基、tert-ブチル基、ペンチル基、イソアミル基、2-エチルブチル基、ヘキシル基、ヘプチル基、オクチル基、2-エチルヘキシル基、3-プロピルヘプチル基、デシル基、3,7-ジメチルオクチル基、2-エチルオクチル基、2-ヘキシルデシル基、ドデシル基、及び、これらの基における水素原子の一部又は全部が、置換基で置換された基(例えば、トリフルオロメチル基、ペンタフルオロエチル基、パーフルオロブチル基、パーフルオロヘキシル基、パーフルオロオクチル基、3-フェニルプロピル基、3-(4-メチルフェニル)プロピル基、3-(3,5-ジ-ヘキシルフェニル)プロピル基及び6-エチルオキシヘキシル基)であってもよい。
「シクロアルキル基」の炭素原子数は、置換基の炭素原子数を含めないで、通常3~50であり、好ましくは3~20であり、より好ましくは4~10である。
シクロアルキル基は、置換基を有していてもよい。シクロアルキル基としては、例えば、シクロヘキシル基、及び、該基における水素原子の一部又は全部が置換基で置換された基が挙げられる。
「アルキレン基」の炭素原子数は、置換基の炭素原子数を含めないで、通常1~20であり、好ましくは1~15であり、より好ましくは1~10である。
アルキレン基は、置換基を有していてもよい。アルキレン基としては、例えば、メチレン基、エチレン基、プロピレン基、ブチレン基、ヘキシレン基、オクチレン基、及び、これらの基における水素原子の一部又は全部が置換基で置換された基が挙げられる。
「シクロアルキレン基」の炭素原子数は、置換基の炭素原子数を含めないで、通常3~20であり、好ましくは4~10であり、より好ましくは5~7である。
シクロアルキレン基は、置換基を有していてもよい。シクロアルキレン基としては、例えば、シクロヘキシレン基、及び、該基における水素原子の一部又は全部が置換基で置換された基が挙げられる。
The "alkyl group" may be either linear or branched. The number of carbon atoms in the linear alkyl group is generally 1-50, preferably 1-20, more preferably 1-10, not including the number of carbon atoms in the substituents. The number of carbon atoms in the branched alkyl group is usually 3-50, preferably 3-20, more preferably 4-10, not including the number of carbon atoms in the substituent.
The alkyl group may have a substituent. Examples of alkyl groups include methyl group, ethyl group, propyl group, isopropyl group, butyl group, 2-butyl group, isobutyl group, tert-butyl group, pentyl group, isoamyl group, 2-ethylbutyl group, hexyl group and heptyl. group, octyl group, 2-ethylhexyl group, 3-propylheptyl group, decyl group, 3,7-dimethyloctyl group, 2-ethyloctyl group, 2-hexyldecyl group, dodecyl group, and hydrogen atoms in these groups Some or all of the groups substituted with substituents (e.g., trifluoromethyl group, pentafluoroethyl group, perfluorobutyl group, perfluorohexyl group, perfluorooctyl group, 3-phenylpropyl group, 3- (4-methylphenyl)propyl group, 3-(3,5-di-hexylphenyl)propyl group and 6-ethyloxyhexyl group).
The number of carbon atoms in the "cycloalkyl group" is usually 3-50, preferably 3-20, more preferably 4-10, not including the number of carbon atoms in the substituents.
A cycloalkyl group may have a substituent. Cycloalkyl groups include, for example, cyclohexyl groups and groups in which some or all of the hydrogen atoms in the groups are substituted with substituents.
The number of carbon atoms in the "alkylene group" is generally 1-20, preferably 1-15, more preferably 1-10, not including the number of carbon atoms in the substituents.
The alkylene group may have a substituent. The alkylene group includes, for example, a methylene group, an ethylene group, a propylene group, a butylene group, a hexylene group, an octylene group, and groups in which some or all of the hydrogen atoms in these groups are substituted with substituents.
The number of carbon atoms in the "cycloalkylene group" is usually 3 to 20, preferably 4 to 10, more preferably 5 to 7, not including the number of carbon atoms in substituents.
A cycloalkylene group may have a substituent. The cycloalkylene group includes, for example, a cyclohexylene group and a group in which some or all of the hydrogen atoms in the group are substituted with substituents.
「芳香族炭化水素基」は、芳香族炭化水素から環を構成する炭素原子に直接結合する水素原子1個以上を除いた基を意味する。芳香族炭化水素から環を構成する炭素原子に直接結合する水素原子1個を除いた基を「アリール基」ともいう。芳香族炭化水素から環を構成する炭素原子に直接結合する水素原子2個を除いた基を「アリーレン基」ともいう。
芳香族炭化水素基の炭素原子数は、置換基の炭素原子数を含めないで、通常6~60であり、好ましくは6~40であり、より好ましくは6~20である。
「芳香族炭化水素基」としては、例えば、単環式の芳香族炭化水素(例えば、ベンゼンが挙げられる。)、又は、多環式の芳香族炭化水素(例えば、ナフタレン、インデン、ナフトキノン、インデノン及びテトラロン等の2環式の芳香族炭化水素;アントラセン、フェナントレン、ジヒドロフェナントレン、フルオレン、アントラキノン、フェナントキノン及びフルオレノン等の3環式の芳香族炭化水素;ベンゾアントラセン、ベンゾフェナントレン及びベンゾフルオレン等の4環式の芳香族炭化水素;ジベンゾアントラセン、ジベンゾフェナントレン、ジベンゾフルオレン、インデノフルオレン及びベンゾフルオランテン等の5環式の芳香族炭化水素;スピロビフルオレン等の6環式の芳香族炭化水素;並びに、ベンゾスピロビフルオレン及びアセナフトフルオランテン等の7環式の芳香族炭化水素が挙げられる。)から、環を構成する炭素原子に直接結合する水素原子1個以上を除いた基が挙げられる。芳香族炭化水素基は、単環式の芳香族炭化水素又は多環式の芳香族炭化水素から、環を構成する炭素原子に直接結合する水素原子1個以上を除いた基が複数結合した基であってもよい。芳香族炭化水素基は置換基を有していてもよい。
“Aromatic hydrocarbon group” means a group obtained by removing one or more hydrogen atoms directly bonded to carbon atoms constituting a ring from an aromatic hydrocarbon. A group obtained by removing one hydrogen atom directly bonded to a carbon atom constituting a ring from an aromatic hydrocarbon is also referred to as an "aryl group". A group obtained by removing two hydrogen atoms directly bonded to carbon atoms forming a ring from an aromatic hydrocarbon is also referred to as an "arylene group".
The number of carbon atoms in the aromatic hydrocarbon group is generally 6-60, preferably 6-40, more preferably 6-20, not including the number of carbon atoms in the substituents.
The "aromatic hydrocarbon group" includes, for example, monocyclic aromatic hydrocarbons (e.g., benzene), or polycyclic aromatic hydrocarbons (e.g., naphthalene, indene, naphthoquinone, indenone and tetralone; tricyclic aromatic hydrocarbons such as anthracene, phenanthrene, dihydrophenanthrene, fluorene, anthraquinone, phenanthoquinone and fluorenone; benzoanthracene, benzophenanthrene and benzofluorene. tetracyclic aromatic hydrocarbons; pentacyclic aromatic hydrocarbons such as dibenzoanthracene, dibenzophenanthrene, dibenzofluorene, indenofluorene and benzofluoranthene; hexacyclic aromatic hydrocarbons such as spirobifluorene ; and seven-ring aromatic hydrocarbons such as benzospirobifluorene and acenaphthofluoranthene). mentioned. Aromatic hydrocarbon group is a monocyclic aromatic hydrocarbon or polycyclic aromatic hydrocarbon group in which one or more hydrogen atoms directly bonded to the carbon atoms constituting the ring are removed, and a plurality of groups are bonded. may be The aromatic hydrocarbon group may have a substituent.
「アルコキシ基」は、直鎖及び分岐のいずれでもよい。直鎖のアルコキシ基の炭素原子数は、置換基の炭素原子数を含めないで、通常1~40であり、好ましくは1~20であり、より好ましくは1~10である。分岐のアルコキシ基の炭素原子数は、置換基の炭素原子数を含めないで、通常3~40であり、好ましくは3~20であり、より好ましくは4~10である。
アルコキシ基は、置換基を有していてもよい。アルコキシ基としては、例えば、メトキシ基、エトキシ基、イソプロピルオキシ基、ブチルオキシ基、ヘキシルオキシ基、2-エチルヘキシルオキシ基、3,7-ジメチルオクチルオキシ基、ラウリルオキシ基、及び、これらの基における水素原子の一部又は全部が置換基で置換された基が挙げられる。
「シクロアルコキシ基」の炭素原子数は、置換基の炭素原子数を含めないで、通常3~40であり、好ましくは3~20であり、より好ましくは4~10である。
シクロアルコキシ基は、置換基を有していてもよい。シクロアルコキシ基としては、例えば、シクロヘキシルオキシ基、及び、該基における水素原子の一部又は全部が置換基で置換された基が挙げられる。
「アリールオキシ基」の炭素原子数は、置換基の炭素原子数を含めないで、通常6~60であり、好ましくは6~40であり、より好ましくは6~20である。
アリールオキシ基は、置換基を有していてもよい。アリールオキシ基としては、例えば、フェノキシ基、ナフチルオキシ基、アントラセニルオキシ基、ピレニルオキシ基、及び、これらの基における水素原子の一部又は全部が置換基で置換された基が挙げられる。
An "alkoxy group" may be either linear or branched. The straight-chain alkoxy group usually has 1 to 40 carbon atoms, preferably 1 to 20 carbon atoms, more preferably 1 to 10 carbon atoms, not including the carbon atoms of the substituents. The number of carbon atoms in the branched alkoxy group is usually 3-40, preferably 3-20, more preferably 4-10, not including the number of carbon atoms in the substituent.
The alkoxy group may have a substituent. Examples of alkoxy groups include methoxy, ethoxy, isopropyloxy, butyloxy, hexyloxy, 2-ethylhexyloxy, 3,7-dimethyloctyloxy, lauryloxy, and hydrogen in these groups. Groups in which some or all of the atoms are substituted with substituents are included.
The number of carbon atoms in the "cycloalkoxy group" is usually 3-40, preferably 3-20, more preferably 4-10, not including the number of carbon atoms in the substituents.
A cycloalkoxy group may have a substituent. Cycloalkoxy groups include, for example, cyclohexyloxy groups and groups in which some or all of the hydrogen atoms in the groups are substituted with substituents.
The number of carbon atoms in the "aryloxy group" is generally 6-60, preferably 6-40, more preferably 6-20, not including the number of carbon atoms in the substituents.
The aryloxy group may have a substituent. Examples of the aryloxy group include phenoxy group, naphthyloxy group, anthracenyloxy group, pyrenyloxy group, and groups in which some or all of the hydrogen atoms in these groups have been substituted with substituents.
「複素環基」とは、複素環式化合物から環を構成する原子(炭素原子又はヘテロ原子)に直接結合する水素原子1個以上を除いた基を意味する。複素環基の中でも、芳香族複素環式化合物から環を構成する原子に直接結合する水素原子1個以上を除いた基である「芳香族複素環基」が好ましい。複素環式化合物から環を構成する原子に直接結合する水素原子p個(pは、1以上の整数を表す。)を除いた基を「p価の複素環基」ともいう。芳香族複素環式化合物から環を構成する原子に直接結合する水素原子p個を除いた基を「p価の芳香族複素環基」ともいう。
「芳香族複素環式化合物」としては、例えば、アゾール、チオフェン、フラン、ピリジン、ジアザベンゼン、トリアジン、アザナフタレン、ジアザナフタレン及びカルバゾール等の複素環自体が芳香族性を示す化合物、並びに、フェノキサジン、フェノチアジン及びベンゾピラン等の複素環自体は芳香族性を示さなくとも、複素環に芳香環が縮環されている化合物が挙げられる。
複素環基の炭素原子数は、置換基の炭素原子数を含めないで、通常1~60であり、好ましくは2~40であり、より好ましくは3~20である。複素環基のヘテロ原子数は、置換基のヘテロ原子数を含めないで、通常1~30であり、好ましくは1~10であり、より好ましくは1~5であり、更に好ましくは1~3である。
複素環基としては、例えば、単環式の複素環式化合物(例えば、フラン、チオフェン、オキサジアゾール、チアジアゾール、ピロール、ジアゾール、トリアゾール、テトラゾール、ピリジン、ジアザベンゼン及びトリアジンが挙げられる。)、又は、多環式の複素環式化合物(例えば、アザナフタレン、ジアザナフタレン、ベンゾフラン、ベンゾチオフェン、インドール、アザインドール、ジアザインドール、ベンゾジアゾール、ベンゾチアジアゾール、ベンゾトリアゾール、ベンゾチオフェンジオキシド、ベンゾチオフェンオキシド及びベンゾピラノン等の2環式の複素環式化合物;ジベンゾフラン、ジベンゾチオフェン、ジベンゾチオフェンジオキシド、ジベンゾチオフェンオキシド、ジベンゾピラノン、ジベンゾボロール、ジベンゾシロール、ジベンゾホスホール、ジベンゾセレノフェン、カルバゾール、アザカルバゾール、ジアザカルバゾール、フェノキサジン、フェノチアジン、9,10-ジヒドロアクリジン、5,10-ジヒドロフェナジン、アクリドン、フェナザボリン、フェノホスファジン、フェノセレナジン、フェナザシリン、アザアントラセン、ジアザアントラセン、アザフェナントレン及びジアザフェナントレン等の3環式の複素環式化合物;ヘキサアザトリフェニレン、ベンゾカルバゾール、アザベンゾカルバゾール、ジアザベンゾカルバゾール、ベンゾナフトフラン及びベンゾナフトチオフェン等の4環式の複素環式化合物;ジベンゾカルバゾール、インドロカルバゾール、インデノカルバゾール、アザインドロカルバゾール、ジアザインドロカルバゾール、アザインデノカルバゾール及びジアザインデノカルバゾール等の5環式の複素環式化合物;カルバゾロカルバゾール、ベンゾインドロカルバゾール及びベンゾインデノカルバゾール等の6環式の複素環式化合物;並びに、ジベンゾインドロカルバゾール及びジベンゾインデノカルバゾール等の7環式の複素環式化合物が挙げられる。)から、環を構成する原子に直接結合する水素原子1個以上を除いた基が挙げられる。複素環基は、単環式の複素環式化合物又は多環式の複素環式化合物から、環を構成する原子に直接結合する水素原子1個以上を除いた基が複数結合した基であってもよい。複素環基は置換基を有していてもよい。
A “heterocyclic group” means a group obtained by removing one or more hydrogen atoms directly bonded to atoms (carbon atoms or heteroatoms) constituting a ring from a heterocyclic compound. Among the heterocyclic groups, an "aromatic heterocyclic group", which is a group obtained by removing one or more hydrogen atoms directly bonded to atoms constituting a ring from an aromatic heterocyclic compound, is preferred. A group obtained by removing p hydrogen atoms (p represents an integer of 1 or more) directly bonded to atoms constituting a ring from a heterocyclic compound is also referred to as a "p-valent heterocyclic group". A group obtained by removing p hydrogen atoms directly bonded to atoms constituting a ring from an aromatic heterocyclic compound is also referred to as a "p-valent aromatic heterocyclic group".
Examples of the "aromatic heterocyclic compound" include compounds in which the heterocycle itself exhibits aromaticity, such as azole, thiophene, furan, pyridine, diazabenzene, triazine, azanaphthalene, diazanaphthalene, and carbazole, and phenoxazine. , phenothiazine, benzopyran, and the like, compounds in which an aromatic ring is condensed to a heterocyclic ring, even if the heterocyclic ring itself does not exhibit aromaticity.
The number of carbon atoms in the heterocyclic group is generally 1-60, preferably 2-40, more preferably 3-20, not including the number of carbon atoms in the substituent. The number of heteroatoms in the heterocyclic group, not including the number of heteroatoms in the substituent, is usually 1 to 30, preferably 1 to 10, more preferably 1 to 5, and still more preferably 1 to 3. is.
Heterocyclic groups include, for example, monocyclic heterocyclic compounds such as furan, thiophene, oxadiazole, thiadiazole, pyrrole, diazole, triazole, tetrazole, pyridine, diazabenzene and triazine, or Polycyclic heterocyclic compounds (e.g. azanaphthalene, diazanaphthalene, benzofuran, benzothiophene, indole, azaindole, diazaindole, benzodiazole, benzothiadiazole, benzotriazole, benzothiophene dioxide, benzothiophene oxide and bicyclic heterocyclic compounds such as benzopyranone; dibenzofuran, dibenzothiophene, dibenzothiophene dioxide, dibenzothiophene oxide, dibenzopyranone, dibenzoborol, dibenzosilol, dibenzophosphole, dibenzoselenophene, carbazole, azacarbazole , diazacarbazole, phenoxazine, phenothiazine, 9,10-dihydroacridine, 5,10-dihydrophenazine, acridone, phenazaborine, phenophosphadine, phenoselenazine, phenazacillin, azaanthracene, diazaanthracene, azaphenanthrene and diaza tricyclic heterocyclic compounds such as phenanthrene; tetracyclic heterocyclic compounds such as hexaazatriphenylene, benzocarbazole, azabenzocarbazole, diazabenzocarbazole, benzonaphthofuran and benzonaphthothiophene; dibenzocarbazole, India Pentacyclic heterocyclic compounds such as locarbazole, indenocarbazole, azaindolocarbazole, diazaindolocarbazole, azaindenocarbazole and diazaindenocarbazole; carbazolocarbazole, benzoindolocarbazole and benzoindenocarbazole Hexacyclic heterocyclic compounds such as; and heptacyclic heterocyclic compounds such as dibenzoindolocarbazole and dibenzoindenocarbazole. Groups excluding one or more may be mentioned. A heterocyclic group is a group in which a plurality of groups are bonded by removing one or more hydrogen atoms directly bonded to the atoms constituting the ring from a monocyclic heterocyclic compound or a polycyclic heterocyclic compound, good too. The heterocyclic group may have a substituent.
「ハロゲン原子」とは、フッ素原子、塩素原子、臭素原子又はヨウ素原子を示す。 A "halogen atom" means a fluorine atom, a chlorine atom, a bromine atom or an iodine atom.
「アミノ基」は、置換基を有していてもよく、置換アミノ基(即ち、第2級アミノ基又は第3級アミノ基、より好ましくは第3級アミノ基)が好ましい。アミノ基が有する置換基としては、アルキル基、シクロアルキル基、アリール基又は1価の複素環基が好ましく、これらの基は更に置換基を有していてもよい。アミノ基が有する置換基が複数存在する場合、それらは同一で異なっていてもよく、互いに結合して、それぞれが結合する窒素原子とともに環を形成していてもよい。
置換アミノ基としては、例えば、ジアルキルアミノ基、ジシクロアルキルアミノ基、ジアリールアミノ基、及び、これらの基における水素原子の一部又は全部が置換基で更に置換された基が挙げられる。
置換アミノ基としては、例えば、ジメチルアミノ基、ジエチルアミノ基、ジフェニルアミノ基、ビス(メチルフェニル)アミノ基、ビス(3,5-ジ-tert-ブチルフェニル)アミノ基、及び、これらの基における水素原子の一部又は全部が置換基で更に置換された基が挙げられる。
The "amino group" may have a substituent, preferably a substituted amino group (that is, a secondary amino group or a tertiary amino group, more preferably a tertiary amino group). Preferred substituents on the amino group are alkyl groups, cycloalkyl groups, aryl groups and monovalent heterocyclic groups, and these groups may further have substituents. When the amino group has a plurality of substituents, they may be the same or different, and may be bonded to each other to form a ring together with the nitrogen atom to which each is bonded.
Substituted amino groups include, for example, dialkylamino groups, dicycloalkylamino groups, diarylamino groups, and groups in which some or all of the hydrogen atoms in these groups have been further substituted with substituents.
Substituted amino groups include, for example, dimethylamino group, diethylamino group, diphenylamino group, bis(methylphenyl)amino group, bis(3,5-di-tert-butylphenyl)amino group, and hydrogen in these groups. Groups in which some or all of the atoms are further substituted with substituents are included.
「アルケニル基」は、直鎖及び分岐のいずれでもよい。直鎖のアルケニル基の炭素原子数は、置換基の炭素原子数を含めないで、通常2~30であり、好ましくは3~20であり、より好ましくは3~10である。分岐のアルケニル基の炭素原子数は、置換基の炭素原子数を含めないで、通常3~30であり、好ましくは4~20であり、より好ましくは4~10である。
「シクロアルケニル基」の炭素原子数は、置換基の炭素原子数を含めないで、通常3~30であり、好ましくは4~20であり、より好ましくは5~10である。
アルケニル基及びシクロアルケニル基は、置換基を有していてもよい。アルケニル基としては、例えば、ビニル基、1-プロペニル基、2-ブテニル基、3-ブテニル基、3-ペンテニル基、4-ペンテニル基、1-ヘキセニル基、5-ヘキセニル基、7-オクテニル基、及び、これらの基における水素原子の一部又は全部が置換基で置換された基が挙げられる。シクロアルケニル基としては、例えば、シクロヘキセニル基、シクロヘキサジエニル基、シクロオクタトリエニル基、ノルボルニレニル基、及び、これらの基における水素原子の一部又は全部が置換基で置換された基が挙げられる。
「アルキニル基」は、直鎖及び分岐のいずれでもよい。アルキニル基の炭素原子数は、置換基の炭素原子を含めないで、通常2~30であり、好ましくは3~10である。分岐のアルキニル基の炭素原子数は、置換基の炭素原子を含めないで、通常4~30であり、好ましくは4~10である。
「シクロアルキニル基」の炭素原子数は、置換基の炭素原子を含めないで、通常4~30であり、好ましくは4~10である。
アルキニル基及びシクロアルキニル基は、置換基を有していてもよい。アルキニル基としては、例えば、エチニル基、1-プロピニル基、2-プロピニル基、2-ブチニル基、3-ブチニル基、3-ペンチニル基、4-ペンチニル基、1-ヘキシニル基、5-ヘキシニル基、及び、これらの基における水素原子の一部又は全部が置換基で置換された基が挙げられる。シクロアルキニル基としては、例えば、シクロオクチニル基、及び、該基における水素原子の一部又は全部が置換基で置換された基が挙げられる。
An "alkenyl group" may be either linear or branched. The straight-chain alkenyl group usually has 2 to 30 carbon atoms, preferably 3 to 20 carbon atoms, more preferably 3 to 10 carbon atoms, not including the carbon atoms of the substituents. The number of carbon atoms in the branched alkenyl group is generally 3-30, preferably 4-20, more preferably 4-10, not including the number of carbon atoms in the substituent.
The number of carbon atoms in the "cycloalkenyl group" is generally 3-30, preferably 4-20, more preferably 5-10, not including the number of carbon atoms in the substituents.
Alkenyl groups and cycloalkenyl groups may have a substituent. Examples of alkenyl groups include vinyl group, 1-propenyl group, 2-butenyl group, 3-butenyl group, 3-pentenyl group, 4-pentenyl group, 1-hexenyl group, 5-hexenyl group, 7-octenyl group, and groups in which some or all of the hydrogen atoms in these groups have been substituted with substituents. The cycloalkenyl group includes, for example, a cyclohexenyl group, a cyclohexadienyl group, a cyclooctatrienyl group, a norbornylenyl group, and groups in which some or all of the hydrogen atoms in these groups are substituted with substituents. .
An "alkynyl group" may be either linear or branched. The number of carbon atoms in the alkynyl group is usually 2-30, preferably 3-10, not including the carbon atoms of the substituents. The number of carbon atoms in the branched alkynyl group is generally 4-30, preferably 4-10, not including the carbon atoms of the substituents.
The number of carbon atoms in the "cycloalkynyl group" is usually 4-30, preferably 4-10, not including the carbon atoms of the substituents.
The alkynyl group and cycloalkynyl group may have a substituent. Examples of alkynyl groups include ethynyl, 1-propynyl, 2-propynyl, 2-butynyl, 3-butynyl, 3-pentynyl, 4-pentynyl, 1-hexynyl, 5-hexynyl, and groups in which some or all of the hydrogen atoms in these groups have been substituted with substituents. Cycloalkynyl groups include, for example, cyclooctynyl groups and groups in which some or all of the hydrogen atoms in the groups are substituted with substituents.
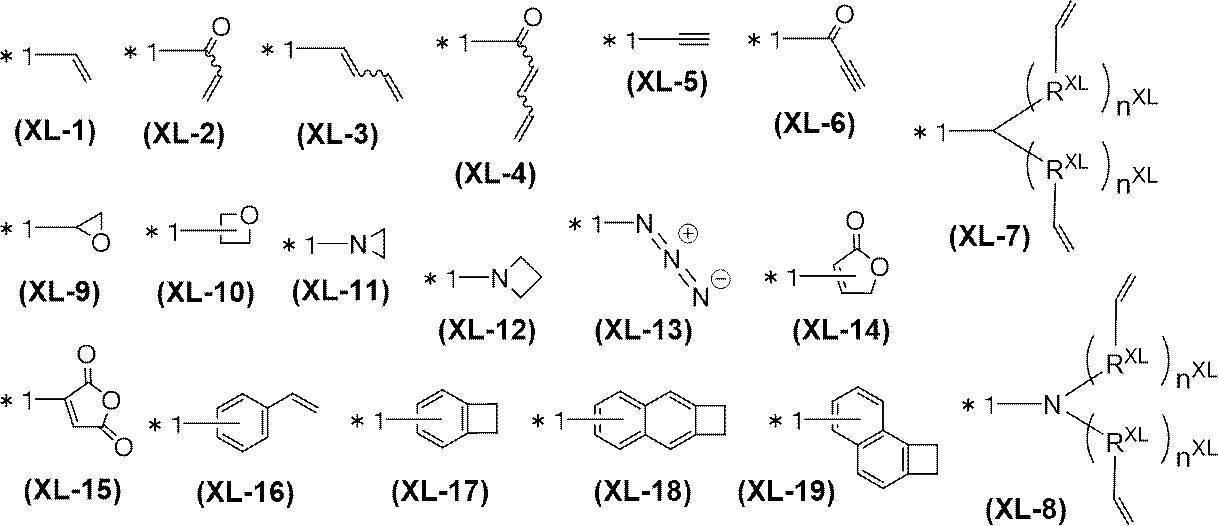
「架橋基」とは、加熱、紫外線照射、近紫外線照射、可視光照射、赤外線照射、ラジカル反応等に供することにより、新たな結合を生成することが可能な基である。架橋基としては、架橋基A群から選ばれる少なくとも1種の架橋基(即ち、式(XL-1)~式(XL-19)で表される基から選ばれる少なくとも1種の基)が好ましい。
(架橋基A群)
A “crosslinking group” is a group capable of forming a new bond by subjecting it to heating, ultraviolet irradiation, near-ultraviolet irradiation, visible light irradiation, infrared irradiation, radical reaction, or the like. The cross-linking group is preferably at least one cross-linking group selected from Group A of cross-linking groups (that is, at least one group selected from groups represented by formulas (XL-1) to (XL-19)). .
(Crosslinking group A group)
[式中、RXLは、メチレン基、酸素原子又は硫黄原子を表し、nXLは、0~5の整数を表す。RXLが複数存在する場合、それらは同一でも異なっていてもよい。nXLが複数存在する場合、それらは同一でも異なっていてもよい。*1は結合位置を表す。これらの架橋基は置換基を有していてもよく、該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。] [In the formula, R XL represents a methylene group, an oxygen atom or a sulfur atom, and n XL represents an integer of 0 to 5. When multiple R XL are present, they may be the same or different. When multiple nXL are present, they may be the same or different. *1 represents the binding position. These bridging groups may have substituents, and when there are multiple substituents, they may be the same or different, and are bonded to each other to form a ring together with the atoms to which they are bonded. may ]
「置換基」としては、例えば、ハロゲン原子、シアノ基、アルキル基、シクロアルキル基、アリール基、1価の複素環基、アルコキシ基、シクロアルコキシ基、アリールオキシ基、アミノ基、置換アミノ基、アルケニル基、シクロアルケニル基、アルキニル基及びシクロアルキニル基が挙げられる。置換基は架橋基であってもよい。なお、置換基が複数存在する場合、それらは同一でも異なっていてもよい。また、置換基が複数存在する場合、それらは互いに結合して、それぞれが結合する原子とともに環を形成していてもよいが、環を形成しないことが好ましい。 The "substituent" includes, for example, a halogen atom, a cyano group, an alkyl group, a cycloalkyl group, an aryl group, a monovalent heterocyclic group, an alkoxy group, a cycloalkoxy group, an aryloxy group, an amino group, a substituted amino group, Alkenyl groups, cycloalkenyl groups, alkynyl groups and cycloalkynyl groups are included. A substituent may be a bridging group. In addition, when multiple substituents are present, they may be the same or different. In addition, when there are multiple substituents, they may bond with each other to form a ring together with the atoms to which they are bonded, but preferably do not form a ring.
「2価の基」としては、例えば、アルキレン基、シクロアルキレン基、アリーレン基、2価の複素環基、-N(R0)-で表される基、-B(R0)-で表される基、-P(R0)-で表される基、-(O=)P(R0)-で表される基、-O-で表される基、-S-で表される基、-Se-で表される基、-S(=O)-で表される基、-S(=O)2-で表される基及び-C(=O)-で表される基が挙げられる。2価の基は、これらの基が複数結合した基であってもよい。2価の基は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。R0は、水素原子又は置換基を表す。
R0としては、例えば、水素原子、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基、アリールオキシ基、1価の複素環基、置換アミノ基、ハロゲン原子及びシアノ基が挙げられ、好ましくは、水素原子、アルキル基、シクロアルキル基、アリール基又は1価の複素環基であり、これらの基は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。
The "divalent group" includes, for example, an alkylene group, a cycloalkylene group, an arylene group, a divalent heterocyclic group, a group represented by -N(R 0 )-, represented by -B(R 0 )- group represented by -P(R 0 )-, group represented by -(O=)P(R 0 )-, group represented by -O-, represented by -S- a group represented by -Se-, a group represented by -S(=O)-, a group represented by -S(=O) 2 - and a group represented by -C(=O)- are mentioned. The divalent group may be a group in which a plurality of these groups are bonded. A divalent group may have a substituent. When there are multiple such substituents, they may be the same or different, and may be bonded to each other to form a ring together with the atoms to which they are bonded. R 0 represents a hydrogen atom or a substituent.
R 0 includes, for example, a hydrogen atom, an alkyl group, a cycloalkyl group, an alkoxy group, a cycloalkoxy group, an aryl group, an aryloxy group, a monovalent heterocyclic group, a substituted amino group, a halogen atom and a cyano group. , preferably a hydrogen atom, an alkyl group, a cycloalkyl group, an aryl group or a monovalent heterocyclic group, and these groups may have a substituent. When there are multiple such substituents, they may be the same or different, and may be bonded to each other to form a ring together with the atoms to which they are bonded.
本明細書中、最低三重項励起状態のエネルギー準位と最低一重項励起状態のエネルギー準位との差の絶対値(以下、「ΔEST」ともいう。)の値の算出は、以下の方法で求められる。まず、B3LYPレベルの密度汎関数法により、化合物の基底状態を構造最適化する。その際、基底関数としては、6-31G*を用いる。そして、得られた構造最適化された構造を用いて、B3LYPレベルの時間依存密度汎関数法により、化合物のΔESTを算出する。但し、6-31G*が使用できない原子を含む場合は、該原子に対してはLANL2DZを用いる。なお、量子化学計算プログラムとしては、Gaussian09を用いて計算する。 In this specification, the absolute value of the difference between the energy level of the lowest triplet excited state and the energy level of the lowest singlet excited state (hereinafter also referred to as “ΔE ST ”) is calculated by the following method. is required. First, the ground state of the compound is structurally optimized by density functional theory at the B3LYP level. At that time, 6-31G* is used as a basis function. Then, using the obtained structurally optimized structure, ΔEST of the compound is calculated by B3LYP-level time-dependent density functional theory. However, when 6-31G* contains an atom that cannot be used, LANL2DZ is used for that atom. Gaussian09 is used as a quantum chemical calculation program.
<組成物>
本開示の組成物は、式(1)で表される金属錯体及び高分子化合物(A)からなる群より選択される少なくとも1種の化合物(以下、「化合物(A)」ともいう。)と、低分子化合物(B)及び高分子化合物(B)からなる群より選択される少なくとも1種の化合物(以下、「化合物(B)」ともいう。)と、式(H-1)で表される化合物、並びに、式(X)で表される構成単位及び式(Y)で表される構成単位からなる群より選択される少なくとも1種の構成単位を含む高分子化合物(以下、「第1の高分子化合物」ともいう。)からなる群より選択される少なくとも1種の化合物(以下、「第1の化合物」ともいう。)と、を含有する組成物である。即ち、本実施形態の組成物は、化合物(A)と、化合物(B)と、第1の化合物とを含有する組成物である。
<Composition>
The composition of the present disclosure comprises at least one compound (hereinafter also referred to as "compound (A)") selected from the group consisting of the metal complex represented by formula (1) and the polymer compound (A). , at least one compound (hereinafter also referred to as “compound (B)”) selected from the group consisting of low-molecular compound (B) and high-molecular compound (B), and represented by formula (H-1) and a polymer compound (hereinafter referred to as "first and at least one compound selected from the group consisting of (hereinafter also referred to as "first compound"). That is, the composition of this embodiment is a composition containing compound (A), compound (B), and a first compound.
本開示の組成物は、例えば、発光素子用組成物として好適に用いることができる。また、本開示の組成物を含む発光素子(以下、「本開示の発光素子」ともいう。)は、駆動電圧がより低くなる。 The composition of the present disclosure can be suitably used, for example, as a composition for light-emitting devices. In addition, a light-emitting device containing the composition of the present disclosure (hereinafter also referred to as a “light-emitting device of the present disclosure”) has a lower driving voltage.
一実施形態において、本開示の組成物は、化合物(A)、化合物(B)及び第1の化合物を、それぞれ、1種のみ含有していてもよく、2種以上含有していてもよい。 In one embodiment, the composition of the present disclosure may contain only one type of compound (A), compound (B) and first compound, respectively, or may contain two or more types.
本開示の組成物において、化合物(A)、化合物(B)及び第1の化合物の合計の含有量は、組成物(例えば、発光素子用組成物であり、以下、同様である。)としての機能が奏される範囲であればよい。
本開示の組成物の一実施形態において、化合物(A)、化合物(B)及び第1の化合物の合計の含有量は、例えば、組成物の全量基準で1~100質量%であってもよく、本開示の発光素子の駆動電圧がより低くなるので、好ましくは10~100質量%であり、より好ましくは30~100質量%であり、更に好ましくは50~100質量%であり、特に好ましくは70~100質量%であり、とりわけ好ましくは90~100質量%である。
本開示の組成物において、化合物(B)の含有量は、組成物としての機能が奏される範囲であればよい。
本開示の組成物の一実施形態において、化合物(B)の含有量は、化合物(A)、化合物(B)及び第1の化合物の合計の含有量を100質量部とした場合、例えば、0.01~99質量部であり、本開示の発光素子の駆動電圧がより低くなるので、好ましくは0.01~90質量部であり、より好ましくは0.05~70質量部であり、更に好ましくは0.1~50質量部であり、特に好ましくは0.5~30質量部であり、とりわけ好ましくは1~25質量部である。
本開示の組成物において、化合物(A)の含有量は、組成物としての機能が奏される範囲であればよい。本開示の組成物において、化合物(A)の含有量は、化合物(A)、化合物(B)及び第1の化合物の合計の含有量を100質量部とした場合、例えば、0.01~99質量部であり、本開示の発光素子の駆動電圧がより低くなるので、好ましくは0.1~95質量部であり、より好ましくは0.5~90質量部であり、更に好ましくは1~70質量部であり、特に好ましくは5~50質量部であり、とりわけ好ましくは10~30質量部である。
In the composition of the present disclosure, the total content of the compound (A), the compound (B) and the first compound is Any range is acceptable as long as the function can be achieved.
In one embodiment of the composition of the present disclosure, the total content of compound (A), compound (B) and the first compound may be, for example, 1 to 100% by mass based on the total amount of the composition. , Since the driving voltage of the light emitting device of the present disclosure is lower, it is preferably 10 to 100% by mass, more preferably 30 to 100% by mass, still more preferably 50 to 100% by mass, and particularly preferably 70 to 100% by mass, particularly preferably 90 to 100% by mass.
In the composition of the present disclosure, the content of compound (B) may be within a range in which the function of the composition is exhibited.
In one embodiment of the composition of the present disclosure, the content of the compound (B) is, for example, 0 when the total content of the compound (A), the compound (B) and the first compound is 100 parts by mass. 0.01 to 99 parts by mass, and the drive voltage of the light-emitting device of the present disclosure is lower, so it is preferably 0.01 to 90 parts by mass, more preferably 0.05 to 70 parts by mass, and even more preferably is 0.1 to 50 parts by mass, particularly preferably 0.5 to 30 parts by mass, particularly preferably 1 to 25 parts by mass.
In the composition of the present disclosure, the content of compound (A) may be within a range in which the function of the composition is exhibited. In the composition of the present disclosure, the content of compound (A) is, for example, 0.01 to 99 when the total content of compound (A), compound (B) and the first compound is 100 parts by mass. It is preferably 0.1 to 95 parts by mass, more preferably 0.5 to 90 parts by mass, and even more preferably 1 to 70 parts by mass, since the driving voltage of the light emitting device of the present disclosure is lower. parts by mass, particularly preferably 5 to 50 parts by mass, particularly preferably 10 to 30 parts by mass.
本開示の組成物の一実施形態において、化合物(A)と化合物(B)と第1の化合物とは、物理的、化学的又は電気的に相互作用することが好ましい。この相互作用により、例えば、本開示の組成物の発光特性、電荷輸送特性又は電荷注入特性を向上又は調整することが可能となり、本開示の発光素子の駆動電圧がより低くなる。 In one embodiment of the composition of the present disclosure, it is preferred that compound (A), compound (B) and the first compound interact physically, chemically or electrically. This interaction can, for example, enhance or tune the light emitting properties, charge transport properties or charge injection properties of the compositions of the present disclosure, resulting in lower driving voltages for the light emitting devices of the present disclosure.
本開示の組成物の一実施形態において、発光材料を一例として説明すれば、第1の化合物と化合物(A)と化合物(B)とが電気的に相互作用し、第1の化合物から化合物(A)へ効率的に電気エネルギーを渡し、更に、化合物(A)から化合物(B)へ効率的に電気エネルギーを渡すことで、化合物(B)をより効率的に発光させることができ、本開示の発光素子の駆動電圧がより低くなる。 In one embodiment of the composition of the present disclosure, taking the luminescent material as an example, the first compound, the compound (A), and the compound (B) electrically interact, and the first compound to the compound ( By efficiently transferring electric energy to A) and further efficiently transferring electric energy from compound (A) to compound (B), compound (B) can be made to emit light more efficiently, and the present disclosure , the driving voltage of the light emitting element becomes lower.
上記観点から、本開示の組成物の一実施形態において、本開示の発光素子の駆動電圧がより低くなるので、第1の化合物は、正孔注入性、正孔輸送性、電子注入性及び電子輸送性から選ばれる少なくとも1つの機能を有することがより好ましい。
上記観点から、本開示の組成物の一実施形態において、本開示の発光素子の駆動電圧がより低くなるので、化合物(A)は、正孔注入性、正孔輸送性、電子注入性及び電子輸送性から選ばれる少なくとも1つの機能を有することがより好ましい。
上記観点から、本開示の組成物の一実施形態において、本開示の発光素子の駆動電圧がより低くなるので、化合物(B)は、発光性を有することがより好ましい。
上記観点から、本開示の組成物の一実施形態において、第1の化合物の有する最低励起一重項状態(S1)は、本開示の発光素子の駆動電圧がより低くなるので、化合物(A)の有する最低励起一重項状態(S1)より高いエネルギー準位であることが好ましい。
上記観点から、本開示の組成物の一実施形態において、第1の化合物の有する最低励起一重項状態(S1)は、本開示の発光素子の駆動電圧がより低くなるので、化合物(B)の有する最低励起一重項状態(S1)より高いエネルギー準位であることが好ましい。
上記観点から、本開示の組成物の一実施形態において、化合物(A)の有する最低励起一重項状態(S1)は、本開示の発光素子の駆動電圧がより低くなるので、化合物(B)の有する最低励起一重項状態(S1)より高いエネルギー準位であることが好ましい。
上記観点から、本開示の組成物の一実施形態において、第1の化合物の有する最低励起三重項状態(T1)は、本開示の発光素子の駆動電圧がより低くなるので、化合物(A)の有する最低励起三重項状態(T1)より高いエネルギー準位であることが好ましい。
上記観点から、本開示の組成物の一実施形態において、第1の化合物の有する最低励起三重項状態(T1)は、本開示の発光素子の駆動電圧がより低くなるので、化合物(B)の有する最低励起三重項状態(T1)より高いエネルギー準位であることが好ましい。
上記観点から、本開示の組成物の一実施形態において、化合物(A)の有する最低励起三重項状態(T1)は、本開示の発光素子の駆動電圧がより低くなるので、化合物(B)の有する最低励起三重項状態(T1)より高いエネルギー準位であることが好ましい。
In view of the above, in one embodiment of the composition of the present disclosure, the first compound has hole-injecting properties, hole-transporting properties, electron-injecting properties, and electron More preferably, it has at least one function selected from transportability.
From the above viewpoint, in one embodiment of the composition of the present disclosure, the driving voltage of the light-emitting device of the present disclosure is lower, so the compound (A) has hole-injecting, hole-transporting, electron-injecting, and electron More preferably, it has at least one function selected from transportability.
From the above point of view, in one embodiment of the composition of the present disclosure, the compound (B) more preferably has light-emitting properties, since the driving voltage of the light-emitting device of the present disclosure is lower.
From the above viewpoint, in one embodiment of the composition of the present disclosure, the lowest excited singlet state (S 1 ) possessed by the first compound lowers the driving voltage of the light-emitting device of the present disclosure. is preferably a higher energy level than the lowest excited singlet state (S 1 ) possessed by .
From the above viewpoint, in one embodiment of the composition of the present disclosure, the lowest excited singlet state (S 1 ) possessed by the first compound lowers the driving voltage of the light-emitting device of the present disclosure. is preferably a higher energy level than the lowest excited singlet state (S 1 ) possessed by .
From the above point of view, in one embodiment of the composition of the present disclosure, the lowest excited singlet state (S 1 ) possessed by compound (A) lowers the driving voltage of the light-emitting device of the present disclosure. is preferably a higher energy level than the lowest excited singlet state (S 1 ) possessed by .
From the above viewpoint, in one embodiment of the composition of the present disclosure, the lowest excited triplet state (T 1 ) possessed by the first compound lowers the driving voltage of the light-emitting device of the present disclosure. is preferably at an energy level higher than the lowest excited triplet state (T 1 ) of .
From the above point of view, in one embodiment of the composition of the present disclosure, the lowest excited triplet state (T 1 ) possessed by the first compound lowers the driving voltage of the light-emitting device of the present disclosure. is preferably at an energy level higher than the lowest excited triplet state (T 1 ) of .
From the above point of view, in one embodiment of the composition of the present disclosure, the lowest excited triplet state (T 1 ) possessed by compound (A) lowers the driving voltage of the light-emitting device of the present disclosure. is preferably at an energy level higher than the lowest excited triplet state (T 1 ) of .
化合物(A)としては、本開示の発光素子を湿式法で作製できるので、化合物(B)を溶解することが可能な溶媒に対して溶解性を示すものであることが好ましい。
第1の化合物としては、本開示の発光素子を湿式法で作製できるので、化合物(B)及び化合物(A)を溶解することが可能な溶媒に対して溶解性を示すものであることが好ましい。
The compound (A) preferably exhibits solubility in a solvent capable of dissolving the compound (B), since the light-emitting device of the present disclosure can be produced by a wet method.
The first compound preferably exhibits solubility in a solvent capable of dissolving the compound (B) and the compound (A), since the light-emitting device of the present disclosure can be produced by a wet method. .
本開示の組成物の一実施形態において、第1の化合物は、本開示の発光素子の駆動電圧がより低くなるので、ホスト材料、アシストドーパント材料又はドーパント材料であることが好ましく、ホスト材料又はアシストドーパント材料であることがより好ましく、ホスト材料であることが更に好ましい。
本開示の組成物の一実施形態において、化合物(A)は、本開示の発光素子の駆動電圧がより低くなるので、ホスト材料、アシストドーパント材料又はドーパント材料であることが好ましく、アシストドーパント材料又はドーパント材料であることがより好ましく、アシストドーパント材料であることが更に好ましい。
本開示の組成物の一実施形態において、化合物(B)は、本開示の発光素子の駆動電圧がより低くなるので、ホスト材料、アシストドーパント材料又はドーパント材料であることが好ましく、アシストドーパント材料又はドーパント材料であることがより好ましく、ドーパント材料であることが更に好ましい。
In one embodiment of the composition of the present disclosure, the first compound is preferably a host material, an assisting dopant material, or a dopant material because the driving voltage of the light-emitting device of the present disclosure is lower. It is more preferably a dopant material, and even more preferably a host material.
In one embodiment of the composition of the present disclosure, the compound (A) is preferably a host material, an assist dopant material, or a dopant material because the driving voltage of the light-emitting device of the present disclosure is lower. A dopant material is more preferred, and an assist dopant material is even more preferred.
In one embodiment of the composition of the present disclosure, the compound (B) is preferably a host material, an assist dopant material, or a dopant material because the driving voltage of the light-emitting device of the present disclosure is lower. Dopant materials are more preferred, and dopant materials are even more preferred.
本開示の組成物の一実施形態において、ホスト材料は、アシストドーパント材料と、物理的、化学的又は電気的に相互作用する材料であることが好ましい。本開示の組成物の一実施形態において、ホスト材料は、ドーパント材料と、物理的、化学的又は電気的に相互作用する材料であることが好ましい。本開示の組成物の一実施形態において、アシストドーパント材料は、ドーパント材料と、物理的、化学的又は電気的に相互作用する材料であることが好ましい。本開示の組成物の一実施形態において、ホスト材料とアシストドーパント材料とドーパント材料とは物理的、化学的又は電気的に相互作用することが好ましい。これらの相互作用により、例えば、本開示の組成物の発光特性、電荷輸送特性又は電荷注入特性を向上又は調整することが可能となり、本開示の発光素子の駆動電圧がより低くなる。 In one embodiment of the composition of the present disclosure, the host material is preferably a material that physically, chemically or electrically interacts with the assisting dopant material. In one embodiment of the composition of the present disclosure, the host material is preferably a material that physically, chemically or electrically interacts with the dopant material. In one embodiment of the composition of the present disclosure, the assisting dopant material is preferably a material that physically, chemically or electrically interacts with the dopant material. In one embodiment of the composition of the present disclosure, it is preferred that the host material, assisting dopant material and dopant material interact physically, chemically or electrically. These interactions make it possible, for example, to enhance or tune the light emitting properties, charge transport properties or charge injection properties of the compositions of the present disclosure, resulting in lower driving voltages of the light emitting devices of the present disclosure.
本開示の組成物において、発光材料を一例として説明すれば、ホスト材料とアシストドーパント材料とドーパント材料とが電気的に相互作用し、ホスト材料からアシストドーパント材料へ効率的に電気エネルギーを渡し、更に、アシストドーパント材料からドーパント材料へ効率的に電気エネルギーを渡すことで、ドーパント材料をより効率的に発光させることができ、本開示の発光素子の駆動電圧がより低くなる。 In the composition of the present disclosure, taking the light-emitting material as an example, the host material, the assisting dopant material, and the dopant material electrically interact to efficiently transfer electrical energy from the host material to the assisting dopant material, and further By efficiently transferring electrical energy from the assisting dopant material to the dopant material, the dopant material can emit light more efficiently, resulting in a lower driving voltage for the light emitting device of the present disclosure.
上記観点から、本開示の組成物の一実施形態において、本開示の発光素子の駆動電圧がより低くなるので、ホスト材料は、正孔注入性、正孔輸送性、電子注入性及び電子輸送性から選ばれる少なくとも1つの機能を有することがより好ましい。
上記観点から、本開示の組成物の一実施形態において、本開示の発光素子の駆動電圧がより低くなるので、アシストドーパント材料は、正孔注入性、正孔輸送性、電子注入性及び電子輸送性から選ばれる少なくとも1つの機能を有することがより好ましい。
上記観点から、本開示の組成物の一実施形態において、本開示の発光素子の駆動電圧がより低くなるので、ドーパント材料は、発光性を有することが好ましい。
上記観点から、本開示の組成物の一実施形態において、ホスト材料の有する最低励起一重項状態(S1)は、本開示の発光素子の駆動電圧がより低くなるので、アシストドーパント材料の有する最低励起一重項状態(S1)より高いエネルギー準位であることが好ましい。
上記観点から、本開示の組成物の一実施形態において、ホスト材料の有する最低励起一重項状態(S1)は、本開示の発光素子の駆動電圧がより低くなるので、ドーパント材料の有する最低励起一重項状態(S1)より高いエネルギー準位であることが好ましい。
上記観点から、本開示の組成物の一実施形態において、アシストドーパント材料の有する最低励起一重項状態(S1)は、本開示の発光素子の駆動電圧がより低くなるので、ドーパント材料の有する最低励起一重項状態(S1)より高いエネルギー準位であることが好ましい。
上記観点から、本開示の組成物の一実施形態において、ホスト材料の有する最低励起三重項状態(T1)は、本開示の発光素子の駆動電圧がより低くなるので、アシストドーパント材料の有する最低励起三重項状態(T1)より高いエネルギー準位であることが好ましい。
上記観点から、本開示の組成物の一実施形態において、ホスト材料の有する最低励起三重項状態(T1)は、本開示の発光素子の駆動電圧がより低くなるので、ドーパント材料の有する最低励起三重項状態(T1)より高いエネルギー準位であることが好ましい。
上記観点から、本開示の組成物の一実施形態において、アシストドーパント材料の有する最低励起三重項状態(T1)は、本開示の発光素子の駆動電圧がより低くなるので、ドーパント材料の有する最低励起三重項状態(T1)より高いエネルギー準位であることが好ましい。
In view of the above, in one embodiment of the composition of the present disclosure, the host material has hole-injecting, hole-transporting, electron-injecting and electron-transporting properties, as the driving voltage of the light-emitting device of the present disclosure is lower. It is more preferable to have at least one function selected from
In view of the above, in one embodiment of the composition of the present disclosure, the assist dopant material has hole-injecting, hole-transporting, electron-injecting and electron-transporting properties, so that the driving voltage of the light-emitting device of the present disclosure is lower. It is more preferable to have at least one function selected from nature.
From the above point of view, in one embodiment of the composition of the present disclosure, the dopant material is preferably luminescent, since the driving voltage of the light emitting device of the present disclosure is lower.
From the above point of view, in one embodiment of the composition of the present disclosure, the lowest excited singlet state (S 1 ) of the host material is the lowest of the assist dopant material, since the driving voltage of the light emitting device of the present disclosure is lower. An energy level higher than the excited singlet state (S 1 ) is preferred.
From the above point of view, in one embodiment of the composition of the present disclosure, the lowest excited singlet state (S 1 ) of the host material is the lowest excited singlet state of the dopant material, since the light-emitting device of the present disclosure has a lower driving voltage. An energy level higher than the singlet state (S 1 ) is preferred.
From the above viewpoint, in one embodiment of the composition of the present disclosure, the lowest excited singlet state (S 1 ) possessed by the assist dopant material is the lowest excited singlet state (S 1 ) possessed by the dopant material, since the driving voltage of the light emitting device of the present disclosure is lower. An energy level higher than the excited singlet state (S 1 ) is preferred.
From the above viewpoint, in one embodiment of the composition of the present disclosure, the lowest excited triplet state (T 1 ) of the host material is the lowest of the assist dopant material, since the driving voltage of the light emitting device of the present disclosure is lower. An energy level higher than the excited triplet state (T 1 ) is preferred.
From the above viewpoint, in one embodiment of the composition of the present disclosure, the lowest excited triplet state (T 1 ) possessed by the host material is the lowest excited triplet state possessed by the dopant material, since the driving voltage of the light emitting device of the present disclosure is lower. An energy level higher than the triplet state (T 1 ) is preferred.
From the above point of view, in one embodiment of the composition of the present disclosure, the lowest excited triplet state (T 1 ) possessed by the assist dopant material is the lowest excited triplet state (T 1 ) possessed by the dopant material, since the driving voltage of the light emitting device of the present disclosure is lower. An energy level higher than the excited triplet state (T 1 ) is preferred.
本開示の組成物において、ホスト材料、アシストドーパント材料及びドーパント材料の合計の含有量は、組成物としての機能が奏される範囲であればよい。本開示の組成物の一実施形態において、ホスト材料、アシストドーパント材料及びドーパント材料の合計の含有量は、例えば、組成物の全量基準で1~100質量%であってもよく、本開示の発光素子の駆動電圧がより低くなるので、好ましくは10~100質量%であり、より好ましくは30~100質量%であり、更に好ましくは50~100質量%であり、特に好ましくは70~100質量%であり、とりわけ好ましくは90~100質量%である。
本開示の組成物において、ドーパント材料の含有量は、組成物としての機能が奏される範囲であればよい。本開示の組成物の一実施形態において、ドーパント材料の含有量は、ホスト材料、アシストドーパント材料及びドーパント材料の合計の含有量を100質量部とした場合、例えば、0.01~99質量部であり、本開示の発光素子の駆動電圧がより低くなるので、好ましくは0.01~90質量部であり、より好ましくは0.05~70質量部であり、更に好ましくは0.1~50質量部であり、特に好ましくは0.5~30質量部であり、とりわけ好ましくは1~10質量部である。
本開示の組成物において、アシストドーパント材料の含有量は、組成物としての機能が奏される範囲であればよい。本開示の組成物の一実施形態において、アシストドーパント材料の含有量は、ホスト材料、アシストドーパント材料及びドーパント材料の合計の含有量を100質量部とした場合、例えば、0.01~99質量部であり、本開示の発光素子の駆動電圧がより低くなるので、好ましくは0.1~95質量部であり、より好ましくは0.5~90質量部であり、更に好ましくは1~70質量部であり、特に好ましくは5~50質量部であり、とりわけ好ましくは10~30質量部である。
In the composition of the present disclosure, the total content of the host material, the assist dopant material, and the dopant material may be within a range in which the composition functions. In one embodiment of the composition of the present disclosure, the total content of the host material, the assisting dopant material and the dopant material may be, for example, 1 to 100% by mass based on the total amount of the composition. Since the drive voltage of the device becomes lower, it is preferably 10 to 100% by mass, more preferably 30 to 100% by mass, still more preferably 50 to 100% by mass, and particularly preferably 70 to 100% by mass. and particularly preferably 90 to 100% by mass.
In the composition of the present disclosure, the content of the dopant material may be within a range in which the function of the composition is exhibited. In one embodiment of the composition of the present disclosure, the content of the dopant material is, for example, 0.01 to 99 parts by mass when the total content of the host material, assist dopant material and dopant material is 100 parts by mass. Since the driving voltage of the light emitting device of the present disclosure is lower, it is preferably 0.01 to 90 parts by mass, more preferably 0.05 to 70 parts by mass, and still more preferably 0.1 to 50 parts by mass. parts, particularly preferably 0.5 to 30 parts by mass, particularly preferably 1 to 10 parts by mass.
In the composition of the present disclosure, the content of the assist dopant material may be within a range in which the function of the composition is exhibited. In one embodiment of the composition of the present disclosure, the content of the assist dopant material is, for example, 0.01 to 99 parts by mass when the total content of the host material, the assist dopant material and the dopant material is 100 parts by mass. is preferably 0.1 to 95 parts by mass, more preferably 0.5 to 90 parts by mass, and still more preferably 1 to 70 parts by mass, since the driving voltage of the light emitting device of the present disclosure is lower. , particularly preferably 5 to 50 parts by mass, particularly preferably 10 to 30 parts by mass.
アシストドーパント材料としては、本開示の発光素子を湿式法で作製できるので、ドーパント材料を溶解することが可能な溶媒に対して溶解性を示すものであることが好ましい。ホスト材料としては、本開示の発光素子を湿式法で作製できるので、アシストドーパント材料及びドーパント材料を溶解することが可能な溶媒に対して溶解性を示すものであることが好ましい。 The assist dopant material preferably exhibits solubility in a solvent capable of dissolving the dopant material, since the light-emitting device of the present disclosure can be produced by a wet method. The host material preferably exhibits solubility in a solvent capable of dissolving the assist dopant material and the dopant material, since the light-emitting device of the present disclosure can be produced by a wet method.
[化合物(B)]
化合物(B)は、低分子化合物(B)及び高分子化合物(B)からなる群より選択される少なくとも1種である。
[Compound (B)]
The compound (B) is at least one selected from the group consisting of low-molecular-weight compounds (B) and high-molecular-weight compounds (B).
(低分子化合物(B))
低分子化合物(B)は、ホウ素原子と、酸素原子、硫黄原子、セレン原子、sp3炭素原子及び窒素原子からなる群より選ばれる少なくとも1種と、を環内に含む縮合複素環骨格(b)を有する低分子化合物である。
低分子化合物(B)において、縮合複素環骨格(b)が窒素原子を含む場合、縮合複素環骨格(b)に含まれる窒素原子のうち、少なくとも1つは二重結合を形成していない窒素原子であることが好ましく、縮合複素環骨格(b)に含まれる窒素原子の全てが二重結合を形成していない窒素原子であることがより好ましい。
低分子化合物(B)は、遷移金属元素を含まない低分子化合物(即ち、典型元素のみから構成される低分子化合物)であることが好ましい。
(Low molecular weight compound (B))
The low - molecular-weight compound (B) is a condensed heterocyclic skeleton (b ) is a low-molecular-weight compound.
In the low-molecular-weight compound (B), when the condensed heterocyclic skeleton (b) contains a nitrogen atom, at least one of the nitrogen atoms contained in the condensed heterocyclic skeleton (b) is a nitrogen that does not form a double bond. It is preferably an atom, and more preferably all of the nitrogen atoms contained in the condensed heterocyclic skeleton (b) are nitrogen atoms that do not form double bonds.
The low-molecular-weight compound (B) is preferably a low-molecular-weight compound containing no transition metal element (that is, a low-molecular-weight compound composed only of typical elements).
縮合複素環骨格(b)の炭素原子数は、置換基の炭素原子数を含めないで、通常1~60であり、好ましくは5~40であり、より好ましくは10~25である。
縮合複素環骨格(b)のヘテロ原子数は、置換基のヘテロ原子数を含めないで、通常2~30であり、好ましくは2~15であり、より好ましくは2~10であり、更に好ましくは2~5であり、特に好ましくは2又は3である。
縮合複素環骨格(b)のホウ素原子数は、置換基のホウ素原子数を含めないで、通常1~10であり、好ましくは1~5であり、より好ましくは1~3であり、更に好ましくは1である。
縮合複素環骨格(b)の酸素原子、硫黄原子、セレン原子、sp3炭素原子及び窒素原子の合計個数は、置換基の原子数を含めないで、通常1~20であり、好ましくは1~10であり、より好ましくは1~5であり、更に好ましくは1~3であり、特に好ましくは2である。
The number of carbon atoms in the condensed heterocyclic skeleton (b) is generally 1 to 60, preferably 5 to 40, more preferably 10 to 25, not including the number of carbon atoms of substituents.
The number of heteroatoms in the condensed heterocyclic skeleton (b) is usually 2 to 30, preferably 2 to 15, more preferably 2 to 10, more preferably 2 to 10, not including the number of heteroatoms in the substituents. is 2 to 5, particularly preferably 2 or 3.
The number of boron atoms in the condensed heterocyclic skeleton (b) is usually 1 to 10, preferably 1 to 5, more preferably 1 to 3, still more preferably 1 to 3, not including the number of boron atoms in the substituents. is 1.
The total number of oxygen atoms, sulfur atoms, selenium atoms, sp3 carbon atoms and nitrogen atoms in the condensed heterocyclic skeleton (b) is usually 1 to 20, preferably 1 to 20, not including the number of substituent atoms. 10, more preferably 1 to 5, still more preferably 1 to 3, and particularly preferably 2.
縮合複素環骨格(b)は、本開示の発光素子の駆動電圧がより低くなるので、ホウ素原子と、酸素原子、硫黄原子及び窒素原子からなる群より選ばれる少なくとも1種とを環内に含むことが好ましく、ホウ素原子及び窒素原子を環内に含むことがより好ましく、ホウ素原子と二重結合を形成していない窒素原子とを環内に含むことが更に好ましい。 The condensed heterocyclic skeleton (b) contains a boron atom and at least one selected from the group consisting of an oxygen atom, a sulfur atom and a nitrogen atom in the ring, since the driving voltage of the light-emitting device of the present disclosure is lower. It is more preferable to contain a boron atom and a nitrogen atom in the ring, and it is even more preferable to contain a nitrogen atom that does not form a double bond with the boron atom in the ring.
縮合複素環骨格(b)は、本開示の発光素子の駆動電圧がより低くなるので、好ましくは3~12環式縮合複素環骨格であり、より好ましくは3~6環式縮合複素環骨格であり、更に好ましくは5環式縮合複素環骨格である。 The condensed heterocyclic skeleton (b) is preferably a 3- to 12-ring condensed heterocyclic skeleton, more preferably a 3- to 6-ring condensed heterocyclic skeleton, because the driving voltage of the light-emitting device of the present disclosure is lower. and more preferably a pentacyclic condensed heterocyclic skeleton.
縮合複素環骨格(b)は、縮合複素環骨格(b)を含む複素環基(b’)を有する化合物ということもできる。 The condensed heterocyclic skeleton (b) can also be referred to as a compound having a heterocyclic group (b') containing the condensed heterocyclic skeleton (b).
複素環基(b’)は、ホウ素原子と、酸素原子、硫黄原子、セレン原子、sp3炭素原子及び窒素原子からなる群より選ばれる少なくとも1種とを環内に含む、多環式の複素環式化合物から、環を構成する原子に直接結合する水素原子1個以上を除いた基であってよく、該基は置換基を有していてもよい。
複素環基(b’)において、多環式の複素環式化合物は、本開示の発光素子の駆動電圧がより低くなるので、好ましくは、ホウ素原子と、酸素原子、硫黄原子及び窒素原子からなる群より選ばれる少なくとも1種とを環内に含む、多環式の複素環式化合物であり、より好ましくは、ホウ素原子及び窒素原子を環内に含む、多環式の複素環式化合物であり、更に好ましくは、ホウ素原子と二重結合を形成していない窒素原子とを環内に含む、多環式の複素環式化合物である。
複素環基(b’)において、多環式の複素環式化合物は、本開示の発光素子の駆動電圧がより低くなるので、好ましくは3~12環式の複素環式化合物であり、より好ましくは3~6環式の複素環式化合物であり、更に好ましくは5環式の複素環式化合物である。
The heterocyclic group (b') is a polycyclic heterocyclic group containing a boron atom and at least one selected from the group consisting of an oxygen atom, a sulfur atom, a selenium atom, an sp3 carbon atom and a nitrogen atom in the ring. It may be a group obtained by removing one or more hydrogen atoms directly bonded to atoms constituting a ring from a cyclic compound, and the group may have a substituent.
In the heterocyclic group (b′), a polycyclic heterocyclic compound preferably consists of boron atoms, oxygen atoms, sulfur atoms and nitrogen atoms, because the driving voltage of the light-emitting device of the present disclosure is lower. A polycyclic heterocyclic compound containing in the ring at least one selected from the group, more preferably a polycyclic heterocyclic compound containing a boron atom and a nitrogen atom in the ring More preferably, it is a polycyclic heterocyclic compound containing a boron atom and a nitrogen atom not forming a double bond in the ring.
In the heterocyclic group (b′), the polycyclic heterocyclic compound is preferably a 3- to 12-cyclic heterocyclic compound, more preferably a heterocyclic compound, since the driving voltage of the light-emitting device of the present disclosure is lower. is a 3- to 6-ring heterocyclic compound, more preferably a pentacyclic heterocyclic compound.
複素環基(b’)が有していてもよい置換基としては、ハロゲン原子、シアノ基、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリールオキシ基、アリール基、1価の複素環基又は置換アミノ基が好ましく、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基、1価の複素環基又は置換アミノ基がより好ましく、アルキル基、シクロアルキル基、アリール基、1価の複素環基又は置換アミノ基が更に好ましく、アルキル基、シクロアルキル基又はアリール基が特に好ましく、これらの基は更に置換基を有していてもよい。 Examples of substituents that the heterocyclic group (b′) may have include halogen atoms, cyano groups, alkyl groups, cycloalkyl groups, alkoxy groups, cycloalkoxy groups, aryloxy groups, aryl groups, monovalent heterocyclic groups. A cyclic group or a substituted amino group is preferable, an alkyl group, a cycloalkyl group, an alkoxy group, a cycloalkoxy group, an aryl group, a monovalent heterocyclic group or a substituted amino group is more preferable, an alkyl group, a cycloalkyl group, an aryl group, A monovalent heterocyclic group or a substituted amino group is more preferred, and an alkyl group, cycloalkyl group or aryl group is particularly preferred, and these groups may further have a substituent.
複素環基(b’)が有していてもよい置換基における、アリール基としては、好ましくは、単環式又は2環式~6環式の芳香族炭化水素から、環を構成する原子に直接結合する水素原子1個を除いた基であり、より好ましくは、単環式、2環式又は3環式の芳香族炭化水素から、環を構成する原子に直接結合する水素原子1個を除いた基であり、更に好ましくは、ベンゼン、ナフタレン、アントラセン、フェナントレン又はフルオレンから環を構成する原子に直接結合する水素原子1個を除いた基であり、特に好ましくは、フェニル基であり、これらの基は置換基を有していてもよい。
複素環基(b’)が有していてもよい置換基における、1価の複素環基としては、好ましくは、単環式又は2環式~6環式の複素環式化合物から、環を構成する原子に直接結合する水素原子1個を除いた基であり、単環式、2環式又は3環式の複素環式化合物から、環を構成する原子に直接結合する水素原子1個を除いた基であり、更に好ましくは、ピリジン、ジアザベンゼン、トリアジン、アザナフタレン、ジアザナフタレン、カルバゾール、ジベンゾフラン、ジベンゾチオフェン、フェノキサジン又はフェノチアジンから環を構成する原子に直接結合する水素原子1個を除いた基であり、特に好ましくは、ピリジン、ジアザベンゼン又はトリアジンから環を構成する原子に直接結合する水素原子1個を除いた基であり、これらの基は置換基を有していてもよい。
複素環基(b’)が有していてもよい置換基における置換アミノ基において、アミノ基が有する置換基としては、アリール基又は1価の複素環基が好ましく、アリール基がより好ましく、これらの基は更に置換基を有していてもよい。アミノ基が有する置換基におけるアリール基及び1価の複素環基の例及び好ましい範囲は、それぞれ、複素環基(b’)が有していてもよい置換基におけるアリール基及び1価の複素環基の例及び好ましい範囲と同じである。
The aryl group in the substituent optionally possessed by the heterocyclic group (b′) is preferably a monocyclic or bicyclic to hexacyclic aromatic hydrocarbon to an atom constituting the ring. A group excluding one directly bonded hydrogen atom, more preferably a monocyclic, bicyclic or tricyclic aromatic hydrocarbon in which one hydrogen atom directly bonded to a ring-constituting atom is more preferably benzene, naphthalene, anthracene, phenanthrene or fluorene from which one hydrogen atom directly bonded to a ring-constituting atom has been removed, particularly preferably a phenyl group; The group may have a substituent.
The monovalent heterocyclic group in the substituent that the heterocyclic group (b') may have is preferably a monocyclic or bicyclic to hexacyclic heterocyclic compound, A group in which one hydrogen atom directly bonded to a constituent atom is removed, and one hydrogen atom directly bonded to a ring-constituting atom is removed from a monocyclic, bicyclic or tricyclic heterocyclic compound. more preferably pyridine, diazabenzene, triazine, azanaphthalene, diazanaphthalene, carbazole, dibenzofuran, dibenzothiophene, phenoxazine or phenothiazine, excluding one hydrogen atom directly bonded to a ring-constituting atom and particularly preferably a group obtained by removing one hydrogen atom directly bonded to a ring-constituting atom from pyridine, diazabenzene or triazine, and these groups may have a substituent.
In the substituted amino group in the substituent optionally possessed by the heterocyclic group (b′), the substituent possessed by the amino group is preferably an aryl group or a monovalent heterocyclic group, more preferably an aryl group. The group may further have a substituent. Examples and preferred ranges of the aryl group and the monovalent heterocyclic group in the substituents of the amino group are, respectively, the aryl group and the monovalent heterocyclic ring in the substituents that the heterocyclic group (b') may have It is the same as the example and preferred range of the group.
複素環基(b’)が有していてもよい置換基が更に有していてもよい置換基としては、ハロゲン原子、シアノ基、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリールオキシ基、アリール基、1価の複素環基又は置換アミノ基が好ましく、アルキル基、シクロアルキル基、アリール基、1価の複素環基又は置換アミノ基がより好ましく、アルキル基、シクロアルキル基又はアリール基が更に好ましく、アルキル基又はシクロアルキル基が特に好ましく、これらの基は更に置換基を有していてもよいが、更に置換基を有さないことが好ましい。
複素環基(b’)が有していてもよい置換基が更に有していてもよい置換基におけるアリール基、1価の複素環基及び置換アミノ基の例及び好ましい範囲は、それぞれ、複素環基(b’)が有していてもよい置換基におけるアリール基、1価の複素環基及び置換アミノ基の例及び好ましい範囲と同じである。
Substituents which the heterocyclic group (b′) may further have include halogen atoms, cyano groups, alkyl groups, cycloalkyl groups, alkoxy groups, cycloalkoxy groups, aryl An oxy group, an aryl group, a monovalent heterocyclic group or a substituted amino group is preferred, an alkyl group, a cycloalkyl group, an aryl group, a monovalent heterocyclic group or a substituted amino group is more preferred, an alkyl group, a cycloalkyl group or An aryl group is more preferred, and an alkyl group or a cycloalkyl group is particularly preferred. These groups may further have a substituent, but preferably have no further substituent.
Examples and preferred ranges of the aryl group, the monovalent heterocyclic group and the substituted amino group in the substituent that the heterocyclic group (b′) may further have are The same as the examples and preferred ranges of the aryl group, monovalent heterocyclic group and substituted amino group in the substituents that the ring group (b') may have.
「二重結合を形成していない窒素原子」とは、他の3つの原子とそれぞれ単結合で結合する窒素原子を意味する。
「環内に二重結合を形成していない窒素原子を含む」とは、環内に-N(-RN)-(式中、RNは水素原子又は置換基を表す。)又は式:
A "nitrogen atom that does not form a double bond" means a nitrogen atom that is bonded to three other atoms via single bonds.
"Containing a nitrogen atom that does not form a double bond in the ring" means -N(-R N )- (wherein R N represents a hydrogen atom or a substituent) or the formula:
で表される基を含むことを意味する。 It means that the group represented by is included.
低分子化合物(B)は、本開示の発光素子の駆動電圧がより低くなるので、熱活性化遅延蛍光(TADF)性化合物であることが好ましい。
ここで、熱活性化遅延蛍光性化合物とは、熱活性化遅延蛍光性を有する化合物である。
The low-molecular-weight compound (B) is preferably a thermally activated delayed fluorescence (TADF) compound, since the driving voltage of the light-emitting device of the present disclosure is lower.
Here, the heat-activated delayed fluorescence compound is a compound having heat-activated delayed fluorescence.
低分子化合物(B)のΔESTは、2.0eV以下であってもよく、1.5eV以下であってもよく、1.0eV以下であってもよく、0.80eV以下であってもよいが、本開示の発光素子の駆動電圧がより低くなるので、好ましくは0.60eV以下であり、より好ましくは0.55eV以下であり、更に好ましくは0.50eV以下である。また、低分子化合物(B)のΔESTは、0.001eV以上であってもよく、0.01eV以上であってもよく、0.10eV以上であってもよく、0.20eV以上であってもよく、0.30eV以上であってもよく、0.40eV以上であってもよい。 ΔEST of the low-molecular-weight compound (B) may be 2.0 eV or less, 1.5 eV or less, 1.0 eV or less, or 0.80 eV or less. However, it is preferably 0.60 eV or less, more preferably 0.55 eV or less, and even more preferably 0.50 eV or less, because the driving voltage of the light-emitting device of the present disclosure becomes lower. ΔEST of the low-molecular-weight compound (B) may be 0.001 eV or more, 0.01 eV or more, 0.10 eV or more, or 0.20 eV or more. may be 0.30 eV or more, or 0.40 eV or more.
低分子化合物(B)の分子量は、好ましくは1×102~5×103であり、より好ましくは2×102~3×103であり、更に好ましくは3×102~1.5×103であり、特に好ましくは4×102~1×103である。 The molecular weight of the low molecular weight compound (B) is preferably 1×10 2 to 5×10 3 , more preferably 2×10 2 to 3×10 3 , still more preferably 3×10 2 to 1.5. ×10 3 , particularly preferably 4×10 2 to 1×10 3 .
請求項6
低分子化合物(B)は、本開示の発光素子の駆動電圧がより低くなるので、式(1-1)、式(1-2)又は式(1-3)で表される化合物であることが好ましく、式(1-2)又は式(1-3)で表される化合物であることがより好ましく、式(1-2)で表される化合物であることが更に好ましい。
Claim 6
The low-molecular-weight compound (B) is a compound represented by formula (1-1), formula (1-2), or formula (1-3) because the driving voltage of the light-emitting device of the present disclosure is lower. is preferred, a compound represented by formula (1-2) or formula (1-3) is more preferred, and a compound represented by formula (1-2) is even more preferred.
Ar1、Ar2及びAr3は、本開示の発光素子の駆動電圧がより低くなるので、好ましくは、単環式若しくは2環式~6環式の芳香族炭化水素、又は、単環式若しくは2環式~6環式の複素環式化合物から、環を構成する原子に直接結合する水素原子1個以上を除いた基であり、より好ましくは、単環式、2環式若しくは3環式の芳香族炭化水素、又は、単環式、2環式若しくは3環式の複素環式化合物から、環を構成する原子に直接結合する水素原子1個以上を除いた基であり、更に好ましくは、単環式の芳香族炭化水素又は単環式の複素環式化合物から、環を構成する原子に直接結合する水素原子1個以上を除いた基であり、特に好ましくは、ベンゼン、ピリジン又はジアザベンゼンから、環を構成する原子に直接結合する水素原子1個以上を除いた基であり、とりわけ好ましくは、ベンゼンから、環を構成する原子に直接結合する水素原子1個以上を除いた基であり、これらの基は置換基を有していてもよい。
Ar1、Ar2及びAr3が有していてもよい置換基の例及び好ましい範囲は、複素環基(b’)が有していてもよい置換基の例及び好ましい範囲と同じである。
Ar 1 , Ar 2 and Ar 3 are preferably monocyclic or bicyclic to hexacyclic aromatic hydrocarbons, or monocyclic or A group obtained by removing one or more hydrogen atoms directly bonded to atoms constituting a ring from a bicyclic to hexacyclic heterocyclic compound, more preferably monocyclic, bicyclic or tricyclic or a group obtained by removing one or more hydrogen atoms directly bonded to the atoms constituting the ring from a monocyclic, bicyclic or tricyclic heterocyclic compound, more preferably , a group obtained by removing one or more hydrogen atoms directly bonded to the atoms constituting the ring from a monocyclic aromatic hydrocarbon or a monocyclic heterocyclic compound, particularly preferably benzene, pyridine or diazabenzene is a group obtained by removing one or more hydrogen atoms directly bonded to ring-constituting atoms from benzene, and particularly preferably a group obtained by removing one or more hydrogen atoms directly bonded to ring-constituting atoms from benzene. , these groups may have a substituent.
Examples and preferred ranges of substituents that Ar 1 , Ar 2 and Ar 3 may have are the same as examples and preferred ranges of substituents that the heterocyclic group (b′) may have.
Y1は、本開示の発光素子の駆動電圧がより低くなるので、好ましくは、酸素原子、硫黄原子、-N(Ry)-で表される基又はアルキレン基であり、より好ましくは、酸素原子、硫黄原子又は-N(Ry)-で表される基であり、更に好ましくは、-N(Ry)-で表される基であり、これらの基は置換基を有していてもよい。 Y 1 is preferably an oxygen atom, a sulfur atom, a group represented by -N(Ry)- or an alkylene group, more preferably an oxygen atom, since the driving voltage of the light-emitting device of the present disclosure is lower. , a sulfur atom or a group represented by -N(Ry)-, more preferably a group represented by -N(Ry)-, and these groups may have a substituent.
Y2及びY3は、本開示の発光素子の駆動電圧がより低くなるので、好ましくは、単結合、酸素原子、硫黄原子、セレン原子、-N(Ry)-で表される基、-B(Ry)-で表される基、アルキレン基又はシクロアルキレン基であり、より好ましくは、単結合、酸素原子、硫黄原子、-N(Ry)-で表される基、-B(Ry)-で表される基又はアルキレン基であり、更に好ましくは、酸素原子、硫黄原子、-N(Ry)-で表される基又はアルキレン基であり、特に好ましくは、酸素原子、硫黄原子又は-N(Ry)-で表される基であり、とりわけ好ましくは、-N(Ry)-で表される基であり、これらの基は置換基を有していてもよい。 Y 2 and Y 3 are preferably a single bond, an oxygen atom, a sulfur atom, a selenium atom, a group represented by -N(Ry)-, -B A group represented by (Ry)-, an alkylene group or a cycloalkylene group, more preferably a single bond, an oxygen atom, a sulfur atom, a group represented by -N(Ry)-, or -B(Ry)- A group or an alkylene group represented by, more preferably an oxygen atom, a sulfur atom, a group represented by -N(Ry)- or an alkylene group, particularly preferably an oxygen atom, a sulfur atom or -N It is a group represented by (Ry)-, particularly preferably a group represented by -N(Ry)-, and these groups may have a substituent.
Y2及びY3におけるアリーレン基としては、好ましくは、単環式又は2環式~6環式の芳香族炭化水素から、環を構成する炭素原子に直接結合する水素原子2個を除いた基であり、より好ましくは、単環式、2環式又は3環式の芳香族炭化水素から、環を構成する炭素原子に直接結合する水素原子2個を除いた基であり、更に好ましくは、ベンゼン、ナフタレン、アントラセン、フェナントレン、ジヒドロフェナントレン又はフルオレンから、環を構成する炭素原子に直接結合する水素原子2個を除いた基であり、特に好ましくは、ベンゼン、ナフタレン又はフルオレンから、環を構成する炭素原子に直接結合する水素原子2個を除いた基であり、とりわけ好ましくは、フェニレン基であり、これらの基は置換基を有していてもよい。
Y2及びY3における2価の複素環基としては、好ましくは、単環式又は2環式~6環式の複素環式化合物から、環を構成する原子(好ましくは炭素原子)に直接結合する水素原子2個を除いた基であり、より好ましくは、単環式、2環式又は3環式の複素環式化合物から、環を構成する原子(好ましくは炭素原子)に直接結合する水素原子2個を除いた基であり、更に好ましくは、ピリジン、ジアザベンゼン、トリアジン、アザナフタレン、ジアザナフタレン、ジベンゾフラン、ジベンゾチオフェン、カルバゾール、アザカルバゾール、ジアザカルバゾール、フェノキサジン、フェノチアジン、9,10-ジヒドロアクリジン又は5,10-ジヒドロフェナジンから、環を構成する原子(好ましくは炭素原子)に直接結合する水素原子2個を除いた基であり、特に好ましくは、ピリジン、ジアザベンゼン、トリアジン、カルバゾール、フェノキサジン、フェノチアジン、9,10-ジヒドロアクリジン又は5,10-ジヒドロフェナジンから、環を構成する原子(好ましくは炭素原子)に直接結合する水素原子2個を除いた基であり、とりわけ好ましくは、ピリジン、ジアザベンゼン又はトリアジンから、環を構成する原子(好ましくは炭素原子)に直接結合する水素原子2個を除いた基であり、これらの基は置換基を有していてもよい。
Y1、Y2及びY3におけるアルキレン基としては、好ましくは、メチレン基、エチレン基又はプロピレン基であり、より好ましくはメチレン基であり、これらの基は置換基を有していてもよい。
The arylene group for Y 2 and Y 3 is preferably a group obtained by removing two hydrogen atoms directly bonded to the carbon atoms constituting the ring from a monocyclic or bicyclic to hexacyclic aromatic hydrocarbon. and more preferably a group obtained by removing two hydrogen atoms directly bonded to the carbon atoms constituting the ring from a monocyclic, bicyclic or tricyclic aromatic hydrocarbon, more preferably benzene, naphthalene, anthracene, phenanthrene, dihydrophenanthrene or fluorene from which two hydrogen atoms directly bonded to carbon atoms constituting a ring are removed; particularly preferably, benzene, naphthalene or fluorene constitutes a ring; It is a group excluding two hydrogen atoms directly bonded to a carbon atom, particularly preferably a phenylene group, and these groups may have a substituent.
The divalent heterocyclic group for Y 2 and Y 3 is preferably a monocyclic or bicyclic to hexacyclic heterocyclic compound directly bonded to a ring-constituting atom (preferably a carbon atom). A group excluding two hydrogen atoms, more preferably a monocyclic, bicyclic or tricyclic heterocyclic compound, a hydrogen directly bonded to an atom (preferably a carbon atom) constituting a ring A group with two atoms removed, more preferably pyridine, diazabenzene, triazine, azanaphthalene, diazanaphthalene, dibenzofuran, dibenzothiophene, carbazole, azacarbazole, diazacarbazole, phenoxazine, phenothiazine, 9,10- A group obtained by removing two hydrogen atoms directly bonded to ring-constituting atoms (preferably carbon atoms) from dihydroacridine or 5,10-dihydrophenazine, particularly preferably pyridine, diazabenzene, triazine, carbazole, phenoxy a group obtained by removing two hydrogen atoms directly bonded to ring-constituting atoms (preferably carbon atoms) from sazine, phenothiazine, 9,10-dihydroacridine or 5,10-dihydrophenazine, particularly preferably pyridine , diazabenzene or triazine by removing two hydrogen atoms directly bonded to atoms (preferably carbon atoms) constituting the ring, and these groups may have a substituent.
The alkylene group for Y 1 , Y 2 and Y 3 is preferably a methylene group, an ethylene group or a propylene group, more preferably a methylene group, and these groups may have a substituent.
本開示の発光素子の駆動電圧がより低くなるので、Y1、Y2及びY3の全てが、酸素原子、硫黄原子又は-N(Ry)-で表される基であることが好ましく、Y1、Y2及びY3の全てが、-N(Ry)-で表される基であることがより好ましい。 Since the driving voltage of the light-emitting device of the present disclosure is lower, all of Y 1 , Y 2 and Y 3 are preferably an oxygen atom, a sulfur atom or a group represented by -N(Ry)-, and Y All of 1 , Y 2 and Y 3 are more preferably groups represented by -N(Ry)-.
Y1、Y2及びY3が有していてもよい置換基の例及び好ましい範囲は、複素環基(b’)が有していてもよい置換基の例及び好ましい範囲と同じである。 Examples and preferred ranges of substituents that Y 1 , Y 2 and Y 3 may have are the same as examples and preferred ranges of substituents that the heterocyclic group (b′) may have.
Ryは、好ましくは、アルキル基、シクロアルキル基、アリール基又は1価の複素環基であり、より好ましくはアリール基又は1価の複素環基であり、更に好ましくはアリール基であり、これらの基は置換基を有していてもよい。
Ryにおけるアリール基及び1価の複素環基の例及び好ましい範囲は、それぞれ、複素環基(b’)が有していてもよい置換基におけるアリール基及び1価の複素環基の例及び好ましい範囲と同じである。
Ryが有していてもよい置換基の例及び好ましい範囲は、複素環基(b’)が有していてもよい置換基の例及び好ましい範囲と同じである。
Ry is preferably an alkyl group, a cycloalkyl group, an aryl group or a monovalent heterocyclic group, more preferably an aryl group or a monovalent heterocyclic group, still more preferably an aryl group; The group may have a substituent.
Examples and preferred ranges of the aryl group and monovalent heterocyclic group in Ry are respectively examples and preferred examples of the aryl group and monovalent heterocyclic group in the substituent that the heterocyclic group (b′) may have Same as range.
Examples and preferred ranges of substituents that Ry may have are the same as examples and preferred ranges of substituents that the heterocyclic group (b') may have.
Y1とAr1とは、直接結合して、又は、2価の基を介して結合して、環を形成してもよいが、低分子化合物(B)の合成が容易なので、環を形成しないことが好ましい。
Y1とAr1とが、2価の基を介して結合して、環を形成する場合において、2価の基としては、好ましくは、アルキレン基、シクロアルキレン基、アリーレン基、2価の複素環基、-N(R0)-で表される基、-B(R0)-で表される基、-O-で表される基、-S-で表される基又は-Se-で表される基であり、より好ましくは、アルキレン基、シクロアルキレン基、-N(R0)-で表される基、-B(R0)-で表される基、-O-で表される基、-S-で表される基又は-Se-で表される基であり、更に好ましくは、アルキレン基、-N(R0)-で表される基、-O-で表される基又は-S-で表される基であり、特に好ましくは、-O-で表される基、-S-で表される基又は-N(R0)-で表される基であり、とりわけ好ましくは、-N(R0)-で表される基であり、これらの基は置換基を有していてもよい。
Y1とAr1とが、2価の基を介して結合して、環を形成する場合において、2価の基におけるアリーレン基、2価の複素環基及びアルキレン基の例及び好ましい範囲は、それぞれ、Y2及びY3におけるアリーレン基、2価の複素環基及びアルキレン基の例及び好ましい範囲と同じである。
Y1とAr1とが、2価の基を介して結合して、環を形成する場合において、2価の基が有していてもよい置換基の例及び好ましい範囲は、Y2及びY3が有していてもよい置換基の例及び好ましい範囲と同じである。
Y1とAr1とが、2価の基を介して結合して、環を形成する場合において、2価の基におけるR0の例及び好ましい範囲は、Ryの例及び好ましい範囲と同じである。
Y 1 and Ar 1 may be directly bonded or bonded via a divalent group to form a ring. preferably not.
When Y 1 and Ar 1 are bonded through a divalent group to form a ring, the divalent group is preferably an alkylene group, a cycloalkylene group, an arylene group, a divalent hetero a cyclic group, a group represented by -N(R 0 )-, a group represented by -B(R 0 )-, a group represented by -O-, a group represented by -S- or -Se- and more preferably an alkylene group, a cycloalkylene group, a group represented by -N(R 0 )-, a group represented by -B(R 0 )-, and a group represented by -O- a group represented by -S- or a group represented by -Se-, more preferably an alkylene group, a group represented by -N(R 0 )-, a group represented by -O- or a group represented by -S-, particularly preferably a group represented by -O-, a group represented by -S- or a group represented by -N(R 0 )- , particularly preferably a group represented by -N(R 0 )-, and these groups may have a substituent.
When Y 1 and Ar 1 are bonded via a divalent group to form a ring, examples and preferred ranges of the arylene group, divalent heterocyclic group and alkylene group in the divalent group are They are the same as the examples and preferred ranges of the arylene group, divalent heterocyclic group and alkylene group for Y2 and Y3 , respectively.
When Y 1 and Ar 1 are bonded via a divalent group to form a ring, examples and preferred ranges of substituents that the divalent group may have include Y 2 and Y It is the same as the examples and preferred range of the substituent that 3 may have.
When Y 1 and Ar 1 are bonded through a divalent group to form a ring, examples and preferred ranges of R 0 in the divalent group are the same as examples and preferred ranges of Ry .
Y1とAr2とは、直接結合して、又は、2価の基を介して結合して、環を形成してもよいが、低分子化合物(B)の合成が容易なので、環を形成しないことが好ましい。Y1とAr2とが、2価の基を介して結合して、環を形成する場合における2価の基の例及び好ましい範囲は、Y1とAr1とが、2価の基を介して結合して、環を形成する場合における2価の基の例及び好ましい範囲と同じである。
Y2とAr1とは、直接結合して、又は、2価の基を介して結合して、環を形成してもよいが、低分子化合物(B)の合成が容易なので、環を形成しないことが好ましい。Y2とAr1とが、2価の基を介して結合して、環を形成する場合における2価の基の例及び好ましい範囲は、Y1とAr1とが、2価の基を介して結合して、環を形成する場合における2価の基の例及び好ましい範囲と同じである。
Y2とAr3とは、直接結合して、又は、2価の基を介して結合して、環を形成してもよいが、低分子化合物(B)の合成が容易なので、環を形成しないことが好ましい。Y2とAr3とが、2価の基を介して結合して、環を形成する場合における2価の基の例及び好ましい範囲は、Y1とAr1とが、2価の基を介して結合して、環を形成する場合における2価の基の例及び好ましい範囲と同じである。
Y3とAr2とは、直接結合して、又は、2価の基を介して結合して、環を形成してもよいが、低分子化合物(B)の合成が容易なので、環を形成しないことが好ましい。Y3とAr2とが、2価の基を介して結合して、環を形成する場合における2価の基の例及び好ましい範囲は、Y1とAr1とが、2価の基を介して結合して、環を形成する場合における2価の基の例及び好ましい範囲と同じである。
Y3とAr3とは、直接結合して、又は、2価の基を介して結合して、環を形成してもよいが、低分子化合物(B)の合成が容易なので、環を形成しないことが好ましい。Y3とAr3とが、2価の基を介して結合して、環を形成する場合における2価の基の例及び好ましい範囲は、Y1とAr1とが、2価の基を介して結合して、環を形成する場合における2価の基の例及び好ましい範囲と同じである。
Y 1 and Ar 2 may be directly bonded or bonded via a divalent group to form a ring. preferably not. Examples and preferred ranges of the divalent group when Y 1 and Ar 2 are bonded via a divalent group to form a ring are Y 1 and Ar 1 via a divalent group are the same as the examples and preferred ranges of the divalent group in the case of forming a ring by combining with each other.
Y 2 and Ar 1 may be directly bonded or bonded via a divalent group to form a ring. preferably not. Examples and preferred ranges of the divalent group when Y 2 and Ar 1 are bonded via a divalent group to form a ring are Y 1 and Ar 1 via a divalent group are the same as the examples and preferred ranges of the divalent group in the case of forming a ring by combining with each other.
Y 2 and Ar 3 may be directly bonded or bonded via a divalent group to form a ring. preferably not. Examples and preferred ranges of the divalent group when Y 2 and Ar 3 are bonded via a divalent group to form a ring are Y 1 and Ar 1 via a divalent group are the same as the examples and preferred ranges of the divalent group in the case of forming a ring by combining with each other.
Y 3 and Ar 2 may be directly bonded or bonded via a divalent group to form a ring. preferably not. Examples and preferred ranges of the divalent group when Y 3 and Ar 2 are bonded via a divalent group to form a ring are Y 1 and Ar 1 via a divalent group are the same as the examples and preferred ranges of the divalent group in the case of forming a ring by combining with each other.
Y 3 and Ar 3 may be directly bonded or bonded via a divalent group to form a ring. preferably not. Examples and preferred ranges of the divalent group when Y 3 and Ar 3 are bonded via a divalent group to form a ring are Y 1 and Ar 1 via a divalent group are the same as the examples and preferred ranges of the divalent group in the case of forming a ring by combining with each other.
低分子化合物(B)としては、下記式で表される化合物、及び、後述の化合物B1~B11が例示される。なお、式中、Z1は、酸素原子又は硫黄原子を表す。Z1が複数存在する場合、それらは同一でも異なっていてもよい。 Examples of the low-molecular-weight compound (B) include compounds represented by the following formula and compounds B1 to B11 described later. In the formula, Z 1 represents an oxygen atom or a sulfur atom. When multiple Z 1 are present, they may be the same or different.
低分子化合物(B)の25℃における発光スペクトルの最大ピーク波長は、好ましくは380nm以上であり、より好ましくは400nm以上であり、更に好ましくは420nm以上であり、特に好ましくは440nm以上である。低分子化合物(B)の25℃における発光スペクトルの最大ピーク波長は、好ましくは750nm以下であり、より好ましくは620nm以下であり、更に好ましくは570nm以下であり、特に好ましくは495nm以下であり、とりわけ好ましくは480nm以下である。
低分子化合物(B)の25℃における発光スペクトルの最大ピークの半値幅は、好ましくは50nm以下であり、より好ましくは40nm以下であり、更に好ましくは30nm以下であり、特に好ましくは25nm以下である。
化合物の室温における発光スペクトルの最大ピーク波長は、化合物を、キシレン、トルエン、クロロホルム、テトラヒドロフラン等の有機溶媒に溶解させ、希薄溶液を調製し(1×10-6質量%~1×10-3質量%)、該希薄溶液のPLスペクトルを室温で測定することで評価することができる。化合物を溶解させる有機溶媒としては、キシレンが好ましい。
The maximum peak wavelength of the emission spectrum of the low-molecular-weight compound (B) at 25° C. is preferably 380 nm or longer, more preferably 400 nm or longer, even more preferably 420 nm or longer, and particularly preferably 440 nm or longer. The maximum peak wavelength of the emission spectrum of the low-molecular-weight compound (B) at 25° C. is preferably 750 nm or less, more preferably 620 nm or less, even more preferably 570 nm or less, particularly preferably 495 nm or less. It is preferably 480 nm or less.
The half width of the maximum peak of the emission spectrum of the low-molecular-weight compound (B) at 25° C. is preferably 50 nm or less, more preferably 40 nm or less, even more preferably 30 nm or less, and particularly preferably 25 nm or less. .
The maximum peak wavelength of the emission spectrum of the compound at room temperature can be determined by dissolving the compound in an organic solvent such as xylene, toluene, chloroform, or tetrahydrofuran to prepare a dilute solution (1×10 −6 mass % to 1×10 −3 mass %). %), which can be evaluated by measuring the PL spectrum of the dilute solution at room temperature. Xylene is preferred as the organic solvent for dissolving the compound.
(高分子化合物(B))
高分子化合物(B)は、低分子化合物(B)から水素原子1個以上を除いた基を有する構成単位(以下、「構成単位(B)」ともいう。)を含む高分子化合物である。
構成単位(B)は、高分子化合物(B)の合成が容易なので、好ましくは、低分子化合物(B)から水素原子1個以上5個以下を除いた基を有する構成単位であり、より好ましくは、低分子化合物(B)から水素原子1個以上3個以下を除いた基を有する構成単位であり、更に好ましくは、低分子化合物(B)から水素原子1個又は2個を除いた基を有する構成単位である。
構成単位(B)は、高分子化合物(B)の合成が容易であり、且つ、本開示の発光素子の駆動電圧がより低くなるので、好ましくは、式(BP-1)、式(BP-2)又は式(BP-3)で表される構成単位であり、より好ましくは、式(BP-1)又は式(BP-2)で表される構成単位である。
(Polymer compound (B))
The polymer compound (B) is a polymer compound containing a structural unit (hereinafter also referred to as “structural unit (B)”) having a group obtained by removing one or more hydrogen atoms from the low molecular weight compound (B).
The structural unit (B) is preferably a structural unit having a group obtained by removing 1 or more and 5 or less hydrogen atoms from the low-molecular-weight compound (B), and more preferably, because the synthesis of the polymer compound (B) is easy. is a structural unit having a group in which 1 to 3 hydrogen atoms are removed from the low-molecular-weight compound (B), more preferably a group in which 1 or 2 hydrogen atoms are removed from the low-molecular-weight compound (B) is a structural unit having
The structural unit (B) is preferably represented by the formula (BP-1) or the formula (BP- 2) or a structural unit represented by formula (BP-3), more preferably a structural unit represented by formula (BP-1) or formula (BP-2).
[式中、
MBP1は、低分子化合物(B)から水素原子1個を除いた基を表す。
MBP2は、低分子化合物(B)から水素原子2個を除いた基を表す。
MBP3は、低分子化合物(B)から水素原子3個を除いた基を表す。
LBP1は、それぞれ独立に、アルキレン基、シクロアルキレン基、アリーレン基、2価の複素環基、-N(RBP1)-で表される基、酸素原子又は硫黄原子を表し、これらの基は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。RBP1は、水素原子、アルキル基、シクロアルキル基、アリール基又は1価の複素環基を表し、これらの基は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。LBP1が複数存在する場合、それらはそれぞれ同一でも異なっていてもよい。
nBP1は、0以上10以下の整数を表す。
ArBP1は、炭化水素基又は複素環基を表し、これらの基は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。]
[In the formula,
MBP1 represents a group obtained by removing one hydrogen atom from the low-molecular-weight compound (B).
MBP2 represents a group obtained by removing two hydrogen atoms from the low-molecular-weight compound (B).
MBP3 represents a group obtained by removing three hydrogen atoms from the low-molecular-weight compound (B).
L BP1 each independently represents an alkylene group, a cycloalkylene group, an arylene group, a divalent heterocyclic group, a group represented by -N(R BP1 )-, an oxygen atom or a sulfur atom, and these groups are It may have a substituent. When there are multiple such substituents, they may be the same or different, and may be bonded to each other to form a ring together with the atoms to which they are bonded. RBP1 represents a hydrogen atom, an alkyl group, a cycloalkyl group, an aryl group or a monovalent heterocyclic group, and these groups may have a substituent. When there are multiple such substituents, they may be the same or different, and may be bonded to each other to form a ring together with the atoms to which they are bonded. When multiple LBP1 are present, they may be the same or different.
nBP1 represents an integer of 0 or more and 10 or less.
Ar BP1 represents a hydrocarbon group or a heterocyclic group, and these groups may have a substituent. When there are multiple such substituents, they may be the same or different, and may be bonded to each other to form a ring together with the atoms to which they are bonded. ]
LBP1は、アルキレン基、シクロアルキレン基、アリーレン基又は2価の複素環基であることが好ましく、アルキレン基又はアリーレン基であることがより好ましく、アリーレン基であることが更に好ましく、これらの基は置換基を有していてもよい。
LBP1におけるアリーレン基及び2価の複素環基の例及び好ましい範囲は、それぞれ、後述のArY1におけるアリーレン基及び2価の複素環基の例及び好ましい範囲と同じである。
LBP1におけるアルキレン基としては、好ましくは、メチレン基、エチレン基又はプロピレン基であり、より好ましくはメチレン基であり、これらの基は置換基を有していてもよい。
RBP1の例及び好ましい範囲は、後述のRX1~RX3の例及び好ましい範囲と同じである。
L BP1 is preferably an alkylene group, a cycloalkylene group, an arylene group or a divalent heterocyclic group, more preferably an alkylene group or an arylene group, still more preferably an arylene group, these groups may have a substituent.
Examples and preferred ranges of the arylene group and divalent heterocyclic group in LBP1 are the same as those of the arylene group and divalent heterocyclic group in Ar Y1 described below.
The alkylene group in LBP1 is preferably a methylene group, an ethylene group or a propylene group, more preferably a methylene group, and these groups may have a substituent.
Examples and preferred ranges of R BP1 are the same as examples and preferred ranges of R X1 to R X3 described later.
nBP1は、好ましくは0~5の整数であり、好ましくは0~3の整数であり、より好ましくは0又は1であり、更に好ましくは0である。 nBP1 is preferably an integer of 0 to 5, preferably an integer of 0 to 3, more preferably 0 or 1, still more preferably 0.
ArBP1における炭化水素基としては、置換基を有していてもよい芳香族炭化水素基及び置換基を有していてもよい脂肪族炭化水素基が挙げられる。ArBP1における炭化水素基は、これらの基が複数結合した基を含む。
ArBP1において、脂肪族炭化水素基としては、アルキレン基又はシクロアルキレン基から水素原子nBP1個を除いた基が挙げられ、好ましくは、アルキレン基から水素原子nBP1個を除いた基であり、これらの基は置換基を有していてもよい。このアルキレン基の例及び好ましい範囲としては、後述のLH1におけるアルキレン基の例及び好ましい範囲が挙げられる。
ArBP1において、芳香族炭化水素基としては、アリーレン基から水素原子nBP1個を除いた基が挙げられ、この基は置換基を有していてもよい。このアリーレン基の例及び好ましい範囲としては、後述のArY1におけるアリーレン基の例及び好ましい範囲が挙げられる。
ArBP1における複素環基としては、2価の複素環基から水素原子nBP1個を除いた基が挙げられ、この基は置換基を有していてもよい。この2価の複素環基の例及び好ましい範囲としては、後述のArY1における2価の複素環基の例及び好ましい範囲が挙げられる。
LBP1及びArBP1が有していてもよい置換基の例及び好ましい例は、後述のArY1で表される基が有してもよい置換基の例及び好ましい範囲と同じである。
The hydrocarbon group for Ar BP1 includes an optionally substituted aromatic hydrocarbon group and an optionally substituted aliphatic hydrocarbon group. The hydrocarbon group in Ar BP1 includes groups in which multiple of these groups are bonded.
In Ar BP1 , the aliphatic hydrocarbon group includes a group obtained by removing one hydrogen atom nBP from an alkylene group or a cycloalkylene group, preferably a group obtained by removing one hydrogen atom nBP from an alkylene group, These groups may have a substituent. Examples and preferred range of this alkylene group include the examples and preferred range of the alkylene group in L H1 described later.
In Ar BP1 , the aromatic hydrocarbon group includes a group obtained by removing one hydrogen atom n BP from an arylene group, and this group may have a substituent. Examples and preferred ranges of the arylene group include the examples and preferred ranges of the arylene group in Ar Y1 described later.
The heterocyclic group for Ar BP1 includes a group obtained by removing one hydrogen atom n BP from a divalent heterocyclic group, and this group may have a substituent. Examples and preferred ranges of the divalent heterocyclic group include the examples and preferred ranges of the divalent heterocyclic group in Ar Y1 described later.
Examples and preferred examples of substituents that L BP1 and Ar 2 BP1 may have are the same as examples and preferred ranges of substituents that the group represented by Ar Y1 may have, which will be described later.
構成単位(B)としては、例えば、下記式で表される構成単位が挙げられる。 Examples of the structural unit (B) include structural units represented by the following formula.
[式中、
RTSは、水素原子、アルキル基、シクロアルキル基、アリール基、1価の複素環基又は置換アミノ基であり、これらの基は更に置換基を有していてもよい。複数存在するRTSは、同一でも異なっていてもよい。]
[In the formula,
RTS is a hydrogen atom, an alkyl group, a cycloalkyl group, an aryl group, a monovalent heterocyclic group or a substituted amino group, and these groups may further have a substituent. A plurality of R TS may be the same or different. ]
RTSにおけるアリール基、1価の複素環基及び置換アミノ基の例及び好ましい範囲は、それぞれ、後述のArY1で表される基が有してもよい置換基におけるアリール基、1価の複素環基及び置換アミノ基の例及び好ましい範囲と同じである。
RTSが有してもよい置換基の例及び好ましい範囲は、後述のArY1で表される基が有してもよい置換基が更に有していてもよい置換基の例及び好ましい範囲と同じである。
Examples and preferred ranges of the aryl group , monovalent heterocyclic group and substituted amino group in R TS are, respectively, the aryl group, monovalent heterocyclic It is the same as the examples and preferred ranges of the cyclic group and the substituted amino group.
Examples and preferred ranges of substituents that R TS may have include examples and preferred ranges of substituents that the group represented by Ar Y1 described later may further have. are the same.
高分子化合物(B)に含まれる構成単位(B)の含有量は、高分子化合物(B)としての機能が奏される範囲であればよい。高分子化合物(B)に含まれる構成単位(B)の含有量は、高分子化合物(B)に含まれる構成単位の合計の含有量に対して、例えば、0.01~100モル%であり、本開示の発光素子の駆動電圧がより低くなるので、好ましくは0.05~90モル%であり、より好ましくは0.1~70モル%であり、更に好ましくは0.2~50モル%であり、特に好ましくは0.5~30モル%であり、とりわけ好ましくは1~10モル%である。構成単位(B)は、高分子化合物(B)中に、1種のみ含まれていてもよく、2種以上含まれていてもよい。 The content of the structural unit (B) contained in the polymer compound (B) may be within a range where the function of the polymer compound (B) is exhibited. The content of the structural unit (B) contained in the polymer compound (B) is, for example, 0.01 to 100 mol% with respect to the total content of the structural units contained in the polymer compound (B). , preferably 0.05 to 90 mol%, more preferably 0.1 to 70 mol%, still more preferably 0.2 to 50 mol%, because the driving voltage of the light-emitting device of the present disclosure is lower. , particularly preferably 0.5 to 30 mol %, particularly preferably 1 to 10 mol %. Only one type of structural unit (B) may be contained in the polymer compound (B), or two or more types thereof may be contained.
高分子化合物(B)は、本開示の発光素子の駆動電圧がより低くなるので、後述の式(X)で表される構成単位及び後述の式(Y)で表される構成単位からなる群より選ばれる少なくとも1種の構成単位を更に含むことが好ましい。即ち、高分子化合物(B)は、後述の式(X)で表される構成単位及び後述の式(Y)で表される構成単位からなる群より選ばれる少なくとも1種の構成単位と、構成単位(B)とを含む高分子化合物であることが好ましい。
高分子化合物(B)が、後述の式(X)で表される構成単位及び後述の式(Y)で表される構成単位からなる群より選ばれる少なくとも1種の構成単位と、構成単位(B)とを含む場合、構成単位(B)と、後述の式(X)で表される構成単位及び後述の式(Y)で表される構成単位とは異なることが好ましい。
高分子化合物(B)は、本開示の発光素子の駆動電圧がより低くなるので、後述の式(Y)で表される構成単位を更に含むことが好ましい。
高分子化合物(B)は、高分子化合物(B)の正孔輸送性が優れ、且つ、本開示の発光素子の駆動電圧がより低くなるので、後述の式(X)で表される構成単位を更に含むことが好ましい。
高分子化合物(B)は、高分子化合物(B)の正孔輸送性が優れ、且つ、本開示の発光素子の駆動電圧が更に低くなるので、後述の式(X)で表される構成単位及び後述の式(Y)で表される構成単位を更に含むことが好ましい。
Since the polymer compound (B) lowers the driving voltage of the light emitting device of the present disclosure, it is a group consisting of a structural unit represented by the formula (X) described later and a structural unit represented by the formula (Y) described later. It is preferable to further contain at least one structural unit selected from the above. That is, the polymer compound (B) contains at least one structural unit selected from the group consisting of structural units represented by the formula (X) described later and structural units represented by the formula (Y) described later; It is preferably a polymer compound containing the unit (B).
The polymer compound (B) comprises at least one structural unit selected from the group consisting of structural units represented by the formula (X) described later and structural units represented by the formula (Y) described later, and a structural unit ( B), the structural unit (B) is preferably different from the structural unit represented by the formula (X) described later and the structural unit represented by the formula (Y) described later.
The polymer compound (B) preferably further contains a structural unit represented by the formula (Y) described below, since the driving voltage of the light-emitting device of the present disclosure is lower.
The polymer compound (B) has an excellent hole-transporting property of the polymer compound (B), and the driving voltage of the light-emitting device of the present disclosure is lower. is preferably further included.
The polymer compound (B) has an excellent hole-transport property of the polymer compound (B) and further lowers the driving voltage of the light-emitting device of the present disclosure. and preferably further comprises a structural unit represented by formula (Y) described later.
高分子化合物(B)が後述の式(X)で表される構成単位を含む場合、後述の式(X)で表される構成単位の含有量は、高分子化合物(B)としての機能が奏される範囲であればよい。高分子化合物(B)が後述の式(X)で表される構成単位を含む場合、後述の式(X)で表される構成単位の含有量は、高分子化合物(B)に含まれる構成単位の合計の含有量に対して、例えば、0.01~99.9モル%であり、高分子化合物(B)の正孔輸送性が優れ、且つ、本開示の発光素子の駆動電圧がより低くなるので、好ましくは0.05~90モル%であり、より好ましくは0.1~70モル%であり、更に好ましくは0.2~50モル%であり、特に好ましくは0.5~30モル%であり、とりわけ好ましくは1~10モル%である。
式(X)で表される構成単位は、高分子化合物(B)中に、1種のみ含まれていてもよく、2種以上含まれていてもよい。
When the polymer compound (B) contains a structural unit represented by the below-described formula (X), the content of the structural unit represented by the below-described formula (X) is such that the polymer compound (B) functions as It can be any range as long as it can be played. When the polymer compound (B) contains a structural unit represented by the below-described formula (X), the content of the structural unit represented by the below-described formula (X) is the constitution contained in the polymer compound (B). For example, it is 0.01 to 99.9 mol% with respect to the total content of the units, the hole transport property of the polymer compound (B) is excellent, and the driving voltage of the light emitting device of the present disclosure is higher. Since the mol %, particularly preferably 1 to 10 mol %.
The structural unit represented by formula (X) may be contained in the polymer compound (B) singly or in combination of two or more.
高分子化合物(B)が式(Y)で表される構成単位を含む場合、式(Y)で表される構成単位の含有量は、高分子化合物(B)としての機能が奏される範囲であればよい。高分子化合物(B)が式(Y)で表される構成単位を含む場合、式(Y)で表される構成単位の含有量は、高分子化合物(B)に含まれる構成単位の合計の含有量に対して、例えば、1~99.99モル%であり、本開示の発光素子の駆動電圧がより低くなるので、好ましくは10~99.95モル%であり、より好ましくは30~99.9モル%であり、更に好ましくは50~99.8モル%であり、特に好ましくは70~99.5モル%であり、とりわけ好ましくは90~99モル%である。
式(Y)で表される構成単位は、高分子化合物(B)中に、1種のみ含まれていてもよく、2種以上含まれていてもよい。
When the polymer compound (B) contains the structural unit represented by the formula (Y), the content of the structural unit represented by the formula (Y) is within a range in which the polymer compound (B) functions. If it is When the polymer compound (B) contains the structural unit represented by the formula (Y), the content of the structural unit represented by the formula (Y) is the total of the structural units contained in the polymer compound (B). With respect to the content, it is, for example, 1 to 99.99 mol %, and since the driving voltage of the light-emitting device of the present disclosure is lower, it is preferably 10 to 99.95 mol %, more preferably 30 to 99 mol %. 0.9 mol %, more preferably 50 to 99.8 mol %, particularly preferably 70 to 99.5 mol %, particularly preferably 90 to 99 mol %.
The structural unit represented by formula (Y) may be contained in the polymer compound (B) singly or in combination of two or more.
高分子化合物(B)が、式(X)で表される構成単位及び/又は式(Y)で表される構成単位、並びに、構成単位(B)を含む場合、式(X)で表される構成単位、式(Y)で表される構成単位及び構成単位(B)の合計の含有量は、高分子化合物(B)としての機能が奏される範囲であればよい。高分子化合物(B)が、式(X)で表される構成単位及び/又は式(Y)で表される構成単位、並びに、構成単位(B)を含む場合、式(X)で表される構成単位、式(Y)で表される構成単位及び構成単位(B)の合計の含有量は、高分子化合物(B)に含まれる構成単位の合計の含有量に対して、例えば、1~100モル%であり、高分子化合物(B)の正孔輸送性が優れ、且つ、本開示の発光素子の駆動電圧がより低くなるので、好ましくは10~100モル%であり、より好ましくは30~100モル%であり、更に好ましくは50~100モル%であり、特に好ましくは70~100モル%であり、とりわけ好ましくは90~100モル%である。 When the polymer compound (B) contains the structural unit represented by the formula (X) and/or the structural unit represented by the formula (Y), and the structural unit (B), it is represented by the formula (X) The total content of the structural unit represented by the formula (Y) and the structural unit (B) may be within a range in which the function of the polymer compound (B) can be exhibited. When the polymer compound (B) contains the structural unit represented by the formula (X) and/or the structural unit represented by the formula (Y), and the structural unit (B), it is represented by the formula (X) The total content of the structural unit represented by the formula (Y) and the structural unit (B) is, for example, 1 It is preferably 10 to 100 mol %, more preferably 10 to 100 mol %, because the hole transport property of the polymer compound (B) is excellent and the driving voltage of the light emitting device of the present disclosure is lower. It is 30 to 100 mol %, more preferably 50 to 100 mol %, particularly preferably 70 to 100 mol %, particularly preferably 90 to 100 mol %.
高分子化合物(B)としては、例えば、高分子化合物BP-1~BP-4が挙げられる。ここで、「その他」とは、構成単位(B)、式(X)で表される構成単位及び式(Y)で表される構成単位以外の構成単位を意味する。 Examples of the polymer compound (B) include polymer compounds BP-1 to BP-4. Here, "other" means a structural unit other than the structural unit (B), the structural unit represented by formula (X), and the structural unit represented by formula (Y).
[表中、pb、qb、rb及びsbは、各構成単位のモル比率(モル%)を表す。pb+qb+rb+sb=100であり、且つ、70≦pb+qb+rb≦100である。] [In the table, p b , q b , r b and s b represent the molar ratio (mol %) of each structural unit. p b +q b +r b +s b =100 and 70≦p b +q b +r b ≦100. ]
高分子化合物(B)は、ブロック共重合体、ランダム共重合体、交互共重合体、グラフト共重合体のいずれであってもよいし、その他の態様であってもよいが、複数種の原料モノマーを共重合した共重合体であることが好ましい。 The polymer compound (B) may be any of a block copolymer, a random copolymer, an alternating copolymer, a graft copolymer, or other modes. It is preferably a copolymer obtained by copolymerizing monomers.
高分子化合物(B)のポリスチレン換算の数平均分子量の例及び好ましい範囲は、後述の第1の高分子化合物のポリスチレン換算の数平均分子量の例及び好ましい範囲と同じである。高分子化合物(B)のポリスチレン換算の重量平均分子量の例及び好ましい範囲は、後述の第1の高分子化合物のポリスチレン換算の重量平均分子量の例及び好ましい範囲と同じである。 The example and preferred range of the polystyrene-equivalent number average molecular weight of the polymer compound (B) are the same as the example and preferred range of the polystyrene-equivalent number average molecular weight of the first polymer compound described below. The example and preferred range of the polystyrene-equivalent weight average molecular weight of the polymer compound (B) are the same as the example and preferred range of the polystyrene-equivalent weight average molecular weight of the first polymer compound described below.
(高分子化合物(B)の製造方法)
高分子化合物(B)は、後述の第1の高分子化合物の製造方法と同様の方法で製造することができる。
(Method for producing polymer compound (B))
The polymer compound (B) can be produced by the same method as the method for producing the first polymer compound described below.
[化合物(A)]
化合物(A)は、式(1)で表される金属錯体及び高分子化合物(A)からなる群より選択される少なくとも1種である。
[Compound (A)]
The compound (A) is at least one selected from the group consisting of the metal complex represented by Formula (1) and the polymer compound (A).
(式(1)で表される金属錯体)
式(1)で表される金属錯体は、低分子化合物であることが好ましい。
式(1)で表される金属錯体の分子量は、好ましくは、3×102~1×104であり、より好ましくは、4×102~7×103あり、更に好ましくは、5×102~5×103であり、特に好ましくは、6×102~3×103であり、とりわけ好ましくは、7×102~2×103である。
(Metal complex represented by formula (1))
The metal complex represented by formula (1) is preferably a low-molecular-weight compound.
The molecular weight of the metal complex represented by formula (1) is preferably 3×10 2 to 1×10 4 , more preferably 4×10 2 to 7×10 3 , still more preferably 5×10 2 to 7×10 3 . 10 2 to 5×10 3 , particularly preferably 6×10 2 to 3×10 3 , particularly preferably 7×10 2 to 2×10 3 .
Mは、本開示の発光素子の駆動電圧がより低くなるので、イリジウム原子又は白金原子であることが好ましく、イリジウム原子であることがより好ましい。
Mがロジウム原子又はイリジウム原子の場合、n1は2又は3であることが好ましく、3であることがより好ましい。
Mがパラジウム原子又は白金原子の場合、n1は2であることが好ましい。
M is preferably an iridium atom or a platinum atom, more preferably an iridium atom, since the driving voltage of the light-emitting device of the present disclosure is lower.
When M is a rhodium atom or an iridium atom, n1 is preferably 2 or 3, more preferably 3.
n1 is preferably 2 when M is a palladium atom or a platinum atom.
E1及びE2の少なくとも一方が炭素原子であることが好ましく、E1及びE2が炭素原子であることがより好ましい。
式(1)で表される金属錯体を容易に合成できるので、E1とE2とは同一であることが好ましい。また、式(1)で表される金属錯体を容易に合成できるので、E1が複数存在する場合、複数存在するE1のうち、少なくとも2つが同一であることが好ましく、複数存在するE1のすべてが同一であることがより好ましい。また、式(1)で表される金属錯体を容易に合成できるので、E2が複数存在する場合、複数存在するE2のうち、少なくとも2つが同一であることが好ましく、複数存在するE2のすべてが同一であることがより好ましい。
At least one of E 1 and E 2 is preferably a carbon atom, more preferably E 1 and E 2 are carbon atoms.
E 1 and E 2 are preferably the same because the metal complex represented by formula (1) can be easily synthesized. In addition, since the metal complex represented by formula (1) can be easily synthesized, when there are a plurality of E 1 's, it is preferable that at least two of the plurality of E 1 's are the same. are all the same. In addition, since the metal complex represented by formula ( 1) can be easily synthesized, when there are a plurality of E 2 , it is preferable that at least two of the plurality of E 2 are the same. are all the same.
環L1における5員環を含む芳香族複素環の炭素原子数は、置換基の炭素原子数を含めないで、好ましくは1~30であり、より好ましくは1~10であり、更に好ましくは1~5であり、特に好ましくは1~3である。
環L1における芳香族複素環のヘテロ原子数は、置換基のヘテロ原子数を含めないで、好ましくは1~30であり、より好ましくは1~10であり、更に好ましくは1~5であり、特に好ましくは1~3である。
環L1としては、例えば、前述の複素環基の項で例示した芳香族複素環の中で、環内に1つ以上の窒素原子を含む5員環を含む芳香族複素環が挙げられ、該芳香族複素環は置換基を有していてもよい。この中でも、環L1は、本開示の発光素子の駆動電圧がより低くなるので、好ましくは、環内に2つ以上4つ以下の窒素原子を含む5員環を含む芳香族複素環であり、より好ましくは、環内に2つ又は3つの窒素原子を含む5員環を含む芳香族複素環であり、更に好ましくは、環内に3つの窒素原子を含む5員環を含む芳香族複素環であり、これらの環は置換基を有していてもよい。
環L1は、本開示の発光素子の駆動電圧がより低くなるので、好ましくは、ピロール環、ジアゾール環、トリアゾール環又はテトラゾール環であり、より好ましくは、ジアゾール環、トリアゾール環又はテトラゾール環であり、更に好ましくは、ジアゾール環又はトリアゾール環であり、特に好ましくは、トリアゾール環であり、これらの環は置換基を有していてもよい。
式(1)で表される金属錯体を容易に合成できるので、環L1が複数存在する場合、複数存在する環L1のうち、少なくとも2つが同一であることが好ましく、複数存在する環L1のすべてが同一であることがより好ましい。
The number of carbon atoms in the aromatic heterocyclic ring containing a 5-membered ring in ring L 1 is preferably 1 to 30, more preferably 1 to 10, more preferably 1 to 10, not including the number of carbon atoms in the substituents. 1 to 5, particularly preferably 1 to 3.
The number of heteroatoms in the aromatic heterocyclic ring in ring L 1 is preferably 1 to 30, more preferably 1 to 10, still more preferably 1 to 5, not including the number of heteroatoms in the substituents. , particularly preferably 1 to 3.
Examples of the ring L 1 include, among the aromatic heterocycles exemplified in the section of the heterocyclic group described above, an aromatic heterocycle containing a 5-membered ring containing one or more nitrogen atoms in the ring, The aromatic heterocycle may have a substituent. Among these, ring L 1 is preferably an aromatic heterocyclic ring containing a 5-membered ring containing 2 or more and 4 or less nitrogen atoms in the ring, because the driving voltage of the light-emitting device of the present disclosure is lower. , more preferably an aromatic heterocyclic ring containing a 5-membered ring containing 2 or 3 nitrogen atoms in the ring, still more preferably an aromatic heterocyclic ring containing a 5-membered ring containing 3 nitrogen atoms in the ring ring, and these rings may have a substituent.
Ring L 1 is preferably a pyrrole ring, a diazole ring, a triazole ring or a tetrazole ring, more preferably a diazole ring, a triazole ring or a tetrazole ring, since the driving voltage of the light-emitting device of the present disclosure is lower. A diazole ring or a triazole ring is more preferred, and a triazole ring is particularly preferred, and these rings may have a substituent.
Since the metal complex represented by formula (1) can be easily synthesized, when a plurality of ring L 1 are present, it is preferable that at least two of the plurality of ring L 1 are the same. 1 are more preferably the same.
環L2における芳香族炭化水素環の炭素原子数は、置換基の炭素原子数を含めないで、好ましくは6~60であり、より好ましくは6~40であり、更に好ましくは6~20である。
環L2における芳香族炭化水素環としては、例えば、前述の芳香族炭化水素基の項で例示した芳香族炭化水素環が挙げられ、好ましくは、5員環又は6員環を含む芳香族炭化水素環であり、これらの芳香族炭化水素環は置換基を有していてもよい。この中でも、環L2における芳香族炭化水素環は、本開示の発光素子の駆動電圧がより低くなるので、好ましくは、前述の芳香族炭化水素基の項で例示した、単環式、2環式又は3環式の芳香族炭化水素環(好ましくは5員環又は6員環を含む芳香族炭化水素環)であり、より好ましくは、ベンゼン環、ナフタレン環、フルオレン環、フェナントレン環又はジヒドロフェナントレン環であり、更に好ましくは、ベンゼン環又はフルオレン環であり、特に好ましくは、ベンゼン環であり、これらの環は置換基を有していてもよい。
環L2における芳香族複素環の炭素原子数は、置換基の炭素原子数を含めないで、好ましくは1~60であり、より好ましくは2~40であり、更に好ましくは3~20である。環L2における芳香族複素環のヘテロ原子数は、置換基のヘテロ原子数を含めないで、好ましくは1~10であり、より好ましくは1~5であり、更に好ましくは1~3である。
環L2における芳香族複素環としては、例えば、前述の複素環基の項で例示した芳香族複素環が挙げられ、好ましくは、5員環若しくは6員環を含む芳香族複素環であり、これらの芳香族複素環は置換基を有していてもよい。この中でも、環L2における芳香族複素環は、本開示の発光素子の駆動電圧がより低くなるので、好ましくは、前述の複素環基の項で例示した、単環式、2環式又は3環式の芳香族複素環(好ましくは、5員環若しくは6員環を含む芳香族複素環)であり、より好ましくは、ピリジン環、ジアザベンゼン環、アザナフタレン環、ジアザナフタレン環、インドール環、ベンゾフラン環、ベンゾチオフェン環、カルバゾール環、アザカルバゾール環、ジアザカルバゾール環、ジベンゾフラン環又はジベンゾチオフェン環であり、更に好ましくは、ピリジン環、ジアザベンゼン環、カルバゾール環、ジベンゾフラン環又はジベンゾチオフェン環であり、特に好ましくは、ジベンゾチオフェン環又はジベンゾフラン環であり、これらの環は置換基を有していてもよい。
環L2は、本開示の発光素子の駆動電圧がより低くなるので、好ましくは、5員環若しくは6員環を含む芳香族炭化水素環、又は、5員環若しくは6員環を含む芳香族複素環であることが好ましく、これらの環は置換基を有していてもよい。
環L2は、本開示の発光素子の駆動電圧が更に低くなるので、好ましくは、単環式、2環式若しくは3環式の芳香族炭化水素環(好ましくは、5員環若しくは6員環を含む芳香族炭化水素環)、又は、単環式、2環式若しくは3環式の芳香族複素環(好ましくは、5員環若しくは6員環を含む芳香族複素環)であり、より好ましくは、ベンゼン環、フルオレン環、ピリジン環、ジアザベンゼン環、カルバゾール環、ジベンゾフラン環又はジベンゾチオフェン環であり、更に好ましくは、ベンゼン環、ジベンゾチオフェン環又はジベンゾフラン環であり、これらの環は置換基を有していてもよい。
式(1)で表される金属錯体を容易に合成できるので、環L2が複数存在する場合、複数存在する環L2のうち、少なくとも2つが同一であることが好ましく、複数存在する環L2のすべてが同一であることがより好ましい。
The number of carbon atoms in the aromatic hydrocarbon ring in ring L 2 is preferably 6 to 60, more preferably 6 to 40, still more preferably 6 to 20, not including the number of carbon atoms in substituents. be.
Examples of the aromatic hydrocarbon ring in the ring L 2 include the aromatic hydrocarbon rings exemplified in the section of the aromatic hydrocarbon group above, preferably an aromatic hydrocarbon ring containing a 5- or 6-membered ring. It is a hydrogen ring, and these aromatic hydrocarbon rings may have a substituent. Among these, the aromatic hydrocarbon ring in the ring L 2 is preferably a monocyclic or bicyclic ring exemplified in the section of the aromatic hydrocarbon group above, because the driving voltage of the light-emitting element of the present disclosure is lower. a cyclic or tricyclic aromatic hydrocarbon ring (preferably an aromatic hydrocarbon ring containing a 5- or 6-membered ring), more preferably a benzene ring, a naphthalene ring, a fluorene ring, a phenanthrene ring or a dihydrophenanthrene It is a ring, more preferably a benzene ring or a fluorene ring, particularly preferably a benzene ring, and these rings may have a substituent.
The number of carbon atoms in the aromatic heterocyclic ring in ring L 2 is preferably 1 to 60, more preferably 2 to 40, still more preferably 3 to 20, not including the number of carbon atoms in substituents. . The number of heteroatoms in the aromatic heterocyclic ring in ring L 2 is preferably 1 to 10, more preferably 1 to 5, still more preferably 1 to 3, not including the number of heteroatoms in substituents. .
Examples of the aromatic heterocyclic ring in ring L 2 include the aromatic heterocyclic rings exemplified in the section of the heterocyclic group described above, preferably an aromatic heterocyclic ring containing a 5- or 6-membered ring, These aromatic heterocycles may have a substituent. Among these, the aromatic heterocyclic ring in the ring L 2 is preferably monocyclic, bicyclic or tricyclic, as exemplified in the section of the heterocyclic group above, since the driving voltage of the light-emitting device of the present disclosure is lower. cyclic aromatic heterocycle (preferably aromatic heterocycle containing 5- or 6-membered ring), more preferably pyridine ring, diazabenzene ring, azanaphthalene ring, diazanaphthalene ring, indole ring, benzofuran ring, benzothiophene ring, carbazole ring, azacarbazole ring, diazacarbazole ring, dibenzofuran ring or dibenzothiophene ring, more preferably pyridine ring, diazabenzene ring, carbazole ring, dibenzofuran ring or dibenzothiophene ring; A dibenzothiophene ring or a dibenzofuran ring is particularly preferred, and these rings may have a substituent.
Ring L 2 is preferably an aromatic hydrocarbon ring containing a 5- or 6-membered ring, or an aromatic A heterocyclic ring is preferable, and these rings may have a substituent.
Ring L 2 is preferably a monocyclic, bicyclic or tricyclic aromatic hydrocarbon ring (preferably a 5-membered ring or 6-membered ring (an aromatic hydrocarbon ring containing is a benzene ring, a fluorene ring, a pyridine ring, a diazabenzene ring, a carbazole ring, a dibenzofuran ring or a dibenzothiophene ring, more preferably a benzene ring, a dibenzothiophene ring or a dibenzofuran ring, and these rings have substituents. You may have
Since the metal complex represented by formula (1) can be easily synthesized, when there are a plurality of ring L 2 , it is preferable that at least two of the plurality of ring L 2 are the same. 2 are more preferably the same.
本開示の発光素子の駆動電圧が更に低くなるので、環L1がピロール環、ジアゾール環、トリアゾール環又はテトラゾール環であり、且つ、環L2がベンゼン環、フルオレン環、ピリジン環、ジアザベンゼン環、カルバゾール環、ジベンゾフラン環又はジベンゾチオフェン環であることが好ましく、環L1がジアゾール環又はトリアゾール環であり、且つ、環L2がベンゼン環、フルオレン環、ピリジン環、ジアザベンゼン環、カルバゾール環、ジベンゾフラン環又はジベンゾチオフェン環であることがより好ましく、環L1がトリアゾール環であり、且つ、環L2がベンゼン環、フルオレン環、ピリジン環、ジアザベンゼン環、カルバゾール環、ジベンゾフラン環又はジベンゾチオフェン環であることが更に好ましく、環L1がトリアゾール環であり、且つ、環L2がベンゼン環、ジベンゾチオフェン環又はジベンゾフラン環であることが特に好ましく、これらの環は置換基を有していてもよい。 Since the driving voltage of the light-emitting device of the present disclosure is further lowered, ring L 1 is a pyrrole ring, diazole ring, triazole ring or tetrazole ring, and ring L 2 is a benzene ring, a fluorene ring, a pyridine ring, a diazabenzene ring, A carbazole ring, a dibenzofuran ring, or a dibenzothiophene ring is preferable, ring L 1 is a diazole ring or triazole ring, and ring L 2 is a benzene ring, fluorene ring, pyridine ring, diazabenzene ring, carbazole ring, or dibenzofuran ring. or more preferably a dibenzothiophene ring, ring L 1 is a triazole ring, and ring L 2 is a benzene ring, fluorene ring, pyridine ring, diazabenzene ring, carbazole ring, dibenzofuran ring or dibenzothiophene ring. is more preferred, and it is particularly preferred that ring L 1 is a triazole ring and ring L 2 is a benzene ring, dibenzothiophene ring or dibenzofuran ring, and these rings may have a substituent.
環L1及び環L2が有していてもよい置換基(以下、「一次置換基」ともいう。)としては、好ましくは、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基、アリールオキシ基、1価の複素環基、置換アミノ基又はフッ素原子であり、より好ましくは、アルキル基、シクロアルキル基、アリール基、1価の複素環基又は置換アミノ基であり、更に好ましくは、アルキル基、シクロアルキル基、アリール基又は1価の複素環基であり、特に好ましくはアルキル基、シクロアルキル基又はアリール基であり、これらの基は更に置換基(以下、「二次置換基」ともいう。)を有していてもよい。 Preferred substituents that the ring L 1 and ring L 2 may have (hereinafter also referred to as "primary substituents") include an alkyl group, a cycloalkyl group, an alkoxy group, a cycloalkoxy group and an aryl group. , an aryloxy group, a monovalent heterocyclic group, a substituted amino group or a fluorine atom, more preferably an alkyl group, a cycloalkyl group, an aryl group, a monovalent heterocyclic group or a substituted amino group, still more preferably is an alkyl group, a cycloalkyl group, an aryl group or a monovalent heterocyclic group, particularly preferably an alkyl group, a cycloalkyl group or an aryl group, and these groups are further substituted (hereinafter referred to as "secondary substituted Also referred to as "group").
環L1及び環L2のうちの少なくとも1つは、本開示の発光素子の駆動電圧がより低くなるので、一次置換基を有することが好ましい。
式(1)で表される金属錯体において、環L1及び環L2のうちの少なくとも1つが一次置換基を有し、且つ、環L1及び環L2が複数存在する場合、複数存在する環L1及び環L2のうちの少なくとも1つの環が一次置換基を有していればよいが、本開示の発光素子の駆動電圧がより低くなるので、複数存在する環L1及び環L2のうちの少なくとも2つが一次置換基を有することが好ましく、複数存在する環L1及び環L2のうちの少なくとも3つが一次置換基を有することがより好ましい。また、式(1)で表される金属錯体において、環L1及び環L2のうちの少なくとも1つが一次置換基を有し、且つ、環L1及び環L2が複数存在する場合、本開示の発光素子の駆動電圧がより低くなるので、複数存在する環L1のうちの少なくとも2つが一次置換基を有すること、又は、複数存在する環L2のうちの少なくとも2つが一次置換基を有することが好ましく、複数存在する環L1の全てが一次置換基を有すること、又は、複数存在する環L2の全てが一次置換基を有することがより好ましく、複数存在する環L1の全てが一次置換基を有することが更に好ましい。
式(1)で表される金属錯体において、環L1及び環L2のうちの少なくとも1つが一次置換基を有する場合、環L1及び環L2のうちの少なくとも1つが有する一次置換基の個数は、通常1個~10個であり、式(1)で表される金属錯体を容易に合成でき、且つ、本開示の発光素子の駆動電圧がより低くなるので、好ましくは1個~5個であり、より好ましくは1個~3個であり、更に好ましくは1個又は2個である。
式(1)で表される金属錯体において、環L1及び環L2のうちの少なくとも1つが一次置換基を有し、且つ、Mがロジウム原子又はイリジウム原子である場合、環L1及び環L2が有する一次置換基の合計の個数は、通常、1個~30個であり、式(1)で表される金属錯体を容易に合成でき、且つ、本開示の発光素子の駆動電圧がより低くなるので、好ましくは1個~18個であり、より好ましくは2個~12個であり、更に好ましくは3個~6個である。
式(1)で表される金属錯体において、環L1及び環L2のうちの少なくとも1つが一次置換基を有し、且つ、Mがパラジウム原子又は白金原子である場合、環L1及び環L2が有する一次置換基の合計の個数は、通常、1個~20個であり、式(1)で表される金属錯体を容易に合成でき、且つ、本開示の発光素子の駆動電圧がより低くなるので、好ましくは1個~12個であり、より好ましくは1個~8個であり、更に好ましくは2個~4個である。
At least one of ring L 1 and ring L 2 preferably has a primary substituent, as this results in a lower driving voltage for the light-emitting device of the present disclosure.
In the metal complex represented by formula (1), when at least one of ring L 1 and ring L 2 has a primary substituent and there are a plurality of ring L 1 and ring L 2, a plurality of ring L 1 and ring L 2 are present At least one ring out of ring L 1 and ring L 2 should have a primary substituent, but the driving voltage of the light-emitting device of the present disclosure is lower. At least two of 2 preferably have a primary substituent, and more preferably at least three of the plurality of ring L 1 and ring L 2 have a primary substituent. Further, in the metal complex represented by formula (1), when at least one of ring L 1 and ring L 2 has a primary substituent, and a plurality of ring L 1 and ring L 2 are present, the present Since the driving voltage of the disclosed light-emitting device is lower, at least two of the plurality of rings L 1 have primary substituents, or at least two of the plurality of rings L 2 have primary substituents. More preferably, all of the plurality of ring L 1 have a primary substituent, or all of the plurality of ring L 2 have a primary substituent, and all of the plurality of ring L 1 It is further preferred that has a primary substituent.
In the metal complex represented by formula (1), when at least one of ring L 1 and ring L 2 has a primary substituent, at least one of ring L 1 and ring L 2 has a primary substituent The number is usually 1 to 10, and preferably 1 to 5 because the metal complex represented by formula (1) can be easily synthesized and the driving voltage of the light emitting device of the present disclosure is lower. , more preferably 1 to 3, still more preferably 1 or 2.
In the metal complex represented by formula (1), when at least one of ring L 1 and ring L 2 has a primary substituent and M is a rhodium atom or an iridium atom, ring L 1 and ring The total number of primary substituents that L 2 has is usually 1 to 30, the metal complex represented by formula (1) can be easily synthesized, and the driving voltage of the light-emitting device of the present disclosure is Since it becomes lower, it is preferably 1 to 18, more preferably 2 to 12, and still more preferably 3 to 6.
In the metal complex represented by formula (1), when at least one of ring L 1 and ring L 2 has a primary substituent and M is a palladium atom or a platinum atom, ring L 1 and ring The total number of primary substituents that L 2 has is usually 1 to 20, the metal complex represented by formula (1) can be easily synthesized, and the driving voltage of the light-emitting device of the present disclosure is Since it becomes lower, it is preferably 1 to 12, more preferably 1 to 8, and still more preferably 2 to 4.
一次置換基におけるアリール基としては、好ましくは、単環式、2環式又は3環式の芳香族炭化水素から環を構成する炭素原子に直接結合する水素原子1個を除いた基であり、より好ましくは、フェニル基、ナフチル基又はフルオレニル基であり、更に好ましくは、フェニル基であり、これらの基は置換基を有していてもよい。
一次置換基における1価の複素環基としては、好ましくは、単環式、2環式又は3環式の複素環式化合物から環を構成する炭素原子又はヘテロ原子に直接結合する水素原子1個を除いた基であり、より好ましくは、ピリジン環、ジアザベンゼン環、トリアジン環、アザナフタレン環、ジアザナフタレン環、カルバゾール環、ジベンゾフラン環又はジベンゾチオフェン環から環を構成する炭素原子又はヘテロ原子に直接結合する水素原子1個を除いた基であり、更に好ましくは、ピリジン環、ジアザベンゼン環又はトリアジン環から環を構成する炭素原子に直接結合する水素原子1個を除いた基であり、これらの基は置換基を有していてもよい。
一次置換基における置換アミノ基において、アミノ基が有する置換基としては、アリール基又は1価の複素環基が好ましく、アリール基がより好ましく、これらの基は更に置換基を有していてもよい。アミノ基が有する置換基におけるアリール基及び1価の複素環基の例及び好ましい範囲は、それぞれ、一次置換基におけるアリール基及び1価の複素環基の例及び好ましい範囲と同じである。
The aryl group in the primary substituent is preferably a monocyclic, bicyclic or tricyclic aromatic hydrocarbon group excluding one hydrogen atom directly bonded to a carbon atom constituting the ring, A phenyl group, a naphthyl group or a fluorenyl group is more preferred, and a phenyl group is even more preferred, and these groups may have a substituent.
As the monovalent heterocyclic group in the primary substituent, preferably, one hydrogen atom directly bonded to a carbon atom or heteroatom constituting a ring from a monocyclic, bicyclic or tricyclic heterocyclic compound and more preferably a pyridine ring, diazabenzene ring, triazine ring, azanaphthalene ring, diazanaphthalene ring, carbazole ring, dibenzofuran ring or dibenzothiophene ring directly to a carbon atom or heteroatom constituting the ring. A group in which one hydrogen atom is removed, more preferably a group in which one hydrogen atom directly bonded to a ring-constituting carbon atom is removed from a pyridine ring, a diazabenzene ring or a triazine ring, and these groups may have a substituent.
In the substituted amino group in the primary substituent, the substituent possessed by the amino group is preferably an aryl group or a monovalent heterocyclic group, more preferably an aryl group, and these groups may further have a substituent. . Examples and preferred ranges of the aryl group and monovalent heterocyclic group in the substituent of the amino group are the same as those of the aryl group and monovalent heterocyclic group in the primary substituent.
二次置換基(一次置換基が更に有していてもよい置換基)の例及び好ましい範囲は、一次置換基の例及び好ましい範囲と同じである。
二次置換基は更に置換基(以下、「三次置換基」ともいう。)を有していてもよい。三次置換基(二次置換基が更に有していてもよい置換基)の例及び好ましい範囲は、一次置換基の例及び好ましい範囲と同じである。
三次置換基は更に置換基(以下、「四次置換基」ともいう。)を有していてもよい。四次置換基(三次置換基が更に有していてもよい置換基)としては、好ましくは、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基、アリールオキシ基、1価の複素環基、置換アミノ基又はフッ素原子であり、より好ましくは、アルキル基、シクロアルキル基、アリール基、1価の複素環基又は置換アミノ基であり、更に好ましくは、アルキル基、シクロアルキル基又はアリール基であり、特に好ましくは、アルキル基又はシクロアルキル基であり、これらの基は更に置換基を有していてもよいが、式(1)で表される金属錯体を容易に合成できるので、更に置換基を有さないことが好ましい。
二次置換基、三次置換基及び四次置換基におけるアリール基、1価の複素環基及び置換アミノ基の例及び好ましい範囲は、それぞれ、一次置換基におけるアリール基、1価の複素環基及び置換アミノ基の例及び好ましい範囲と同じである。
Examples and preferred ranges of the secondary substituents (substituents that the primary substituent may further have) are the same as the examples and preferred ranges of the primary substituents.
The secondary substituent may further have a substituent (hereinafter also referred to as "tertiary substituent"). Examples and preferred ranges of tertiary substituents (substituents that secondary substituents may further have) are the same as examples and preferred ranges of primary substituents.
The tertiary substituent may further have a substituent (hereinafter also referred to as "quaternary substituent"). The quaternary substituent (substituent that the tertiary substituent may further have) is preferably an alkyl group, a cycloalkyl group, an alkoxy group, a cycloalkoxy group, an aryl group, an aryloxy group, a monovalent a cyclic group, a substituted amino group or a fluorine atom, more preferably an alkyl group, a cycloalkyl group, an aryl group, a monovalent heterocyclic group or a substituted amino group, still more preferably an alkyl group, a cycloalkyl group or An aryl group, particularly preferably an alkyl group or a cycloalkyl group, which may further have a substituent, because the metal complex represented by the formula (1) can be easily synthesized. , and preferably have no substituents.
Examples and preferred ranges of the aryl group, monovalent heterocyclic group and substituted amino group in the secondary substituent, tertiary substituent and quaternary substituent are respectively the aryl group, monovalent heterocyclic group and It is the same as the example and preferred range of the substituted amino group.
(アニオン性の2座配位子)
A1-G1-A2で表されるアニオン性の2座配位子としては、例えば、下記式で表され
る配位子が挙げられる。但し、A1-G1-A2で表されるアニオン性の2座配位子は、添
え字n1でその数を定義されている配位子とは異なる。
(anionic bidentate ligand)
Examples of the anionic bidentate ligand represented by A 1 -G 1 -A 2 include ligands represented by the following formulae. However, the anionic bidentate ligand represented by A 1 -G 1 -A 2 is different from the ligand whose number is defined by the subscript n 1 .
[式中、*は、Mと結合する部位を表す。] [In the formula, * represents a site that binds to M. ]
式(1)で表される金属錯体としては、例えば、以下に示す金属錯体、及び、後述の金属錯体MC5~MC9が例示される。 Examples of the metal complex represented by formula (1) include the metal complexes shown below and metal complexes MC5 to MC9 described later.
(高分子化合物(A))
高分子化合物(A)は、式(1)で表される金属錯体から水素原子1個以上を除いた基を有する構成単位(以下、「構成単位(A)」ともいう。)を含む高分子化合物である。
構成単位(A)は、高分子化合物(A)の合成が容易なので、好ましくは、式(1)で表される金属錯体から水素原子1個以上5個以下を除いた基を有する構成単位であり、より好ましくは、式(1)で表される金属錯体から水素原子1個以上3個以下を除いた基を有する構成単位であり、更に好ましくは、式(1)で表される金属錯体から水素原子1個又は2個を除いた基を有する構成単位である。
構成単位(A)は、高分子化合物(A)の合成が容易であり、且つ、本開示の発光素子の駆動電圧がより低くなるので、好ましくは、式(AP-1)、式(AP-2)又は式(AP-3)で表される構成単位であり、より好ましくは、式(AP-1)又は式(AP-2)で表される構成単位であり、更に好ましくは、式(AP-1)で表される構成単位である。
(Polymer compound (A))
The polymer compound (A) is a polymer containing a structural unit having a group obtained by removing one or more hydrogen atoms from the metal complex represented by formula (1) (hereinafter also referred to as "structural unit (A)"). is a compound.
Structural unit (A) is preferably a structural unit having a group obtained by removing 1 or more and 5 or less hydrogen atoms from the metal complex represented by formula (1), since synthesis of polymer compound (A) is easy. more preferably a structural unit having a group obtained by removing 1 or more and 3 or less hydrogen atoms from the metal complex represented by formula (1), and still more preferably a metal complex represented by formula (1) It is a structural unit having a group obtained by removing one or two hydrogen atoms from
The structural unit (A) is preferably represented by formula (AP-1) or formula (AP- 2) or a structural unit represented by formula (AP-3), more preferably a structural unit represented by formula (AP-1) or formula (AP-2), still more preferably a structural unit represented by formula ( It is a structural unit represented by AP-1).
[式中、
MAP1は、式(1)で表される金属錯体から水素原子1個を除いた基を表す。
MAP2は、式(1)で表される金属錯体から水素原子2個を除いた基を表す。
MAP3は、式(1)で表される金属錯体から水素原子3個を除いた基を表す。
LAP1は、それぞれ独立に、アルキレン基、シクロアルキレン基、アリーレン基、2価の複素環基、-N(RAP1)-で表される基、酸素原子又は硫黄原子を表し、これらの基は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。RAP1は、水素原子、アルキル基、シクロアルキル基、アリール基又は1価の複素環基を表し、これらの基は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。LAP1が複数存在する場合、それらはそれぞれ同一でも異なっていてもよい。
nAP1は、0以上10以下の整数を表す。
ArAP1は、炭化水素基又は複素環基を表し、これらの基は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。]
[In the formula,
MAP1 represents a group obtained by removing one hydrogen atom from the metal complex represented by formula (1).
MAP2 represents a group obtained by removing two hydrogen atoms from the metal complex represented by formula (1).
MAP3 represents a group obtained by removing three hydrogen atoms from the metal complex represented by formula (1).
L AP1 each independently represents an alkylene group, a cycloalkylene group, an arylene group, a divalent heterocyclic group, a group represented by -N(R AP1 )-, an oxygen atom or a sulfur atom, and these groups are It may have a substituent. When there are multiple such substituents, they may be the same or different, and may be bonded to each other to form a ring together with the atoms to which they are bonded. RAP1 represents a hydrogen atom, an alkyl group, a cycloalkyl group, an aryl group or a monovalent heterocyclic group, and these groups may have a substituent. When there are multiple such substituents, they may be the same or different, and may be bonded to each other to form a ring together with the atoms to which they are bonded. When multiple LAP1 are present, they may be the same or different.
n AP1 represents an integer of 0 or more and 10 or less.
Ar AP1 represents a hydrocarbon group or a heterocyclic group, and these groups may have a substituent. When there are multiple such substituents, they may be the same or different, and may be bonded to each other to form a ring together with the atoms to which they are bonded. ]
LAP1の例及び好ましい範囲は、LBP1の例及び好ましい範囲と同じである。
RAP1の例及び好ましい範囲は、RBP1の例及び好ましい範囲と同じである。
nAP1の例及び好ましい範囲は、nBP1の例及び好ましい範囲と同じである。
ArAP1の例及び好ましい範囲は、ArBP1の例及び好ましい範囲と同じである。
The examples and preferred ranges of L AP1 are the same as the examples and preferred ranges of L BP1 .
The examples and preferred ranges of RAP1 are the same as the examples and preferred ranges of RBP1 .
The examples and preferred ranges of nAP1 are the same as the examples and preferred ranges of nBP1 .
The examples and preferred ranges of Ar AP1 are the same as the examples and preferred ranges of Ar BP1 .
構成単位(A)としては、例えば、下記式で表される構成単位が挙げられる。 Examples of structural units (A) include structural units represented by the following formulas.
[式中、
Z2は、-CH=で表される基又は-N=で表される基を表す。Z2が複数存在する場合、それらは同一でも異なっていてもよい。
RAは、水素原子又は一次置換基を表す。RAが複数存在する場合、それらは同一でも異なっていてもよい。]
[In the formula,
Z 2 represents a group represented by -CH= or a group represented by -N=. When multiple Z 2 are present, they may be the same or different.
RA represents a hydrogen atom or a primary substituent. When multiple RAs are present, they may be the same or different. ]
高分子化合物(A)に含まれる構成単位(A)の含有量は、高分子化合物(A)としての機能が奏される範囲であればよい。高分子化合物(A)に含まれる構成単位(A)の含有量は、高分子化合物(A)に含まれる構成単位の合計の含有量に対して、例えば、0.01~100モル%であり、本開示の発光素子の駆動電圧がより低くなるので、好ましくは0.1~99モル%であり、より好ましくは0.5~90モル%であり、更に好ましくは1~70モル%であり、特に好ましくは5~50モル%であり、とりわけ好ましくは10~30モル%である。構成単位(A)は、高分子化合物(A)中に、1種のみ含まれていてもよく、2種以上含まれていてもよい。 The content of the structural unit (A) contained in the polymer compound (A) may be within a range in which the function of the polymer compound (A) is exhibited. The content of the structural unit (A) contained in the polymer compound (A) is, for example, 0.01 to 100 mol% with respect to the total content of the structural units contained in the polymer compound (A). is preferably 0.1 to 99 mol%, more preferably 0.5 to 90 mol%, still more preferably 1 to 70 mol%, because the driving voltage of the light-emitting device of the present disclosure is lower. , particularly preferably 5 to 50 mol %, particularly preferably 10 to 30 mol %. 1 type of structural units (A) may be contained in the polymer compound (A), and 2 or more types may be contained.
高分子化合物(A)は、本開示の発光素子の駆動電圧がより低くなるので、後述の式(X)で表される構成単位及び後述の式(Y)で表される構成単位からなる群より選ばれる少なくとも1種の構成単位を更に含むことが好ましい。即ち、高分子化合物(A)は、後述の式(X)で表される構成単位及び後述の式(Y)で表される構成単位からなる群より選ばれる少なくとも1種の構成単位と、構成単位(A)とを含む高分子化合物であることが好ましい。
高分子化合物(A)が、後述の式(X)で表される構成単位及び後述の式(Y)で表される構成単位からなる群より選ばれる少なくとも1種の構成単位と、構成単位(A)とを含む場合、構成単位(A)と、後述の式(X)で表される構成単位及び後述の式(Y)で表される構成単位とは異なることが好ましい。
高分子化合物(A)は、本開示の発光素子の駆動電圧がより低くなるので、後述の式(Y)で表される構成単位を更に含むことが好ましい。
高分子化合物(A)は、高分子化合物(A)の正孔輸送性が優れ、且つ、本開示の発光素子の駆動電圧がより低くなるので、後述の式(X)で表される構成単位を更に含むことが好ましい。
高分子化合物(A)は、高分子化合物(A)の正孔輸送性が優れ、且つ、本開示の発光素子の駆動電圧がより低くなるので、後述の式(X)で表される構成単位及び後述の式(Y)で表される構成単位を更に含むことが好ましい。
Since the polymer compound (A) lowers the driving voltage of the light emitting device of the present disclosure, it is a group consisting of a structural unit represented by the formula (X) described later and a structural unit represented by the formula (Y) described later. It is preferable to further contain at least one structural unit selected from the above. That is, the polymer compound (A) includes at least one structural unit selected from the group consisting of structural units represented by the formula (X) described later and structural units represented by the formula (Y) described later; It is preferably a polymer compound containing the unit (A).
The polymer compound (A) comprises at least one structural unit selected from the group consisting of structural units represented by the formula (X) described later and structural units represented by the formula (Y) described later, and a structural unit ( A), the structural unit (A) is preferably different from the structural unit represented by the formula (X) described later and the structural unit represented by the formula (Y) described later.
It is preferable that the polymer compound (A) further contains a structural unit represented by formula (Y), which will be described later, since the driving voltage of the light-emitting device of the present disclosure is lower.
The polymer compound (A) has an excellent hole-transport property, and the driving voltage of the light-emitting device of the present disclosure is lower. It is preferable to further include
The polymer compound (A) has an excellent hole-transport property, and the driving voltage of the light-emitting device of the present disclosure is lower. and preferably further comprises a structural unit represented by formula (Y) described later.
高分子化合物(A)が後述の式(X)で表される構成単位を含む場合、後述の式(X)で表される構成単位の含有量は、高分子化合物(A)としての機能が奏される範囲であればよい。高分子化合物(A)が後述の式(X)で表される構成単位を含む場合、後述の式(X)で表される構成単位の含有量は、高分子化合物(A)に含まれる構成単位の合計の含有量に対して、例えば、0.01~99.9モル%であり、高分子化合物(B)の正孔輸送性が優れ、且つ、本開示の発光素子の駆動電圧がより低くなるので、好ましくは0.05~90モル%であり、より好ましくは0.1~70モル%であり、更に好ましくは0.2~50モル%であり、特に好ましくは0.5~30モル%であり、とりわけ好ましくは1~10モル%である。
式(X)で表される構成単位は、高分子化合物(A)中に、1種のみ含まれていてもよく、2種以上含まれていてもよい。
When the polymer compound (A) contains a structural unit represented by formula (X) described later, the content of the structural unit represented by formula (X) described later is such that the function of the polymer compound (A) is It can be any range as long as it can be played. When the polymer compound (A) contains a structural unit represented by the formula (X) described below, the content of the structural unit represented by the formula (X) described below is the constitution included in the polymer compound (A). For example, it is 0.01 to 99.9 mol% with respect to the total content of the units, the hole transport property of the polymer compound (B) is excellent, and the driving voltage of the light emitting device of the present disclosure is higher. Since the mol %, particularly preferably 1 to 10 mol %.
The structural unit represented by formula (X) may be contained in the polymer compound (A) singly or in combination of two or more.
高分子化合物(A)が式(Y)で表される構成単位を含む場合、式(Y)で表される構成単位の含有量は、高分子化合物(A)としての機能が奏される範囲であればよい。高分子化合物(A)が式(Y)で表される構成単位を含む場合、式(Y)で表される構成単位の含有量は、高分子化合物(A)に含まれる構成単位の合計の含有量に対して、例えば、0.1~99.99モル%であり、本開示の発光素子の駆動電圧がより低くなるので、好ましくは1~99.9モル%であり、より好ましくは10~99.5モル%であり、更に好ましくは30~99モル%であり、特に好ましくは50~95モル%であり、とりわけ好ましくは70~90モル%である。
式(Y)で表される構成単位は、高分子化合物(A)中に、1種のみ含まれていてもよく、2種以上含まれていてもよい。
When the polymer compound (A) contains the structural unit represented by the formula (Y), the content of the structural unit represented by the formula (Y) is within the range in which the polymer compound (A) functions. If it is When the polymer compound (A) contains the structural unit represented by the formula (Y), the content of the structural unit represented by the formula (Y) is the total of the structural units contained in the polymer compound (A). With respect to the content, it is, for example, 0.1 to 99.99 mol%, and since the driving voltage of the light-emitting device of the present disclosure is lower, it is preferably 1 to 99.9 mol%, more preferably 10 99.5 mol %, more preferably 30 to 99 mol %, particularly preferably 50 to 95 mol %, particularly preferably 70 to 90 mol %.
The structural unit represented by formula (Y) may be contained in the polymer compound (A) singly or in combination of two or more.
高分子化合物(A)が、式(X)で表される構成単位及び/又は式(Y)で表される構成単位、並びに、構成単位(A)を含む場合、式(X)で表される構成単位、式(Y)で表される構成単位及び構成単位(A)の合計の含有量は、高分子化合物(A)としての機能が奏される範囲であればよい。高分子化合物(A)が、式(X)で表される構成単位及び/又は式(Y)で表される構成単位、並びに、構成単位(A)を含む場合、式(X)で表される構成単位、式(Y)で表される構成単位及び構成単位(A)の合計の含有量は、高分子化合物(A)に含まれる構成単位の合計の含有量に対して、例えば、1~100モル%であり、高分子化合物(A)の正孔輸送性が優れ、且つ、本開示の発光素子の駆動電圧がより低くなるので、好ましくは10~100モル%であり、より好ましくは30~100モル%であり、更に好ましくは50~100モル%であり、特に好ましくは70~100モル%であり、とりわけ好ましくは90~100モル%である。 When the polymer compound (A) contains the structural unit represented by the formula (X) and/or the structural unit represented by the formula (Y), and the structural unit (A), it is represented by the formula (X) The total content of the structural unit represented by the formula (Y), the structural unit represented by the formula (Y), and the structural unit (A) may be within a range in which the function of the polymer compound (A) can be exhibited. When the polymer compound (A) contains the structural unit represented by the formula (X) and/or the structural unit represented by the formula (Y), and the structural unit (A), it is represented by the formula (X) The total content of the structural unit represented by the formula (Y) and the structural unit (A) is, for example, 1 It is preferably 10 to 100 mol %, more preferably 10 to 100 mol %, because the hole transport property of the polymer compound (A) is excellent and the driving voltage of the light emitting device of the present disclosure is lower. It is 30 to 100 mol %, more preferably 50 to 100 mol %, particularly preferably 70 to 100 mol %, particularly preferably 90 to 100 mol %.
高分子化合物(A)としては、例えば、高分子化合物AP-1~AP-4が挙げられる。ここで、「その他」とは、構成単位(A)、式(X)で表される構成単位及び式(Y)で表される構成単位以外の構成単位を意味する。 Examples of the polymer compound (A) include polymer compounds AP-1 to AP-4. Here, "other" means a structural unit other than the structural unit (A), the structural unit represented by formula (X), and the structural unit represented by formula (Y).
[表中、pa、qa、ra及びsaは、各構成単位のモル比率(モル%)を表す。pa+qa+ra+sa=100であり、且つ、70≦pa+qa+ra≦100である。] [In the table, p a , q a , r a and sa represent the molar ratio (mol %) of each structural unit. p a +q a + ra +s a =100 and 70≦ pa +q a + ra ≦100. ]
高分子化合物(A)は、ブロック共重合体、ランダム共重合体、交互共重合体、グラフト共重合体のいずれであってもよいし、その他の態様であってもよいが、複数種の原料モノマーを共重合した共重合体であることが好ましい。 The polymer compound (A) may be any of a block copolymer, a random copolymer, an alternating copolymer, a graft copolymer, or may be in other forms. It is preferably a copolymer obtained by copolymerizing monomers.
高分子化合物(A)のポリスチレン換算の数平均分子量の例及び好ましい範囲は、後述の第1の高分子化合物のポリスチレン換算の数平均分子量の例及び好ましい範囲と同じである。高分子化合物(A)のポリスチレン換算の重量平均分子量の例及び好ましい範囲は、後述の第1の高分子化合物のポリスチレン換算の重量平均分子量の例及び好ましい範囲と同じである。 The example and preferred range of the polystyrene-equivalent number average molecular weight of the polymer compound (A) are the same as the example and preferred range of the polystyrene-equivalent number average molecular weight of the first polymer compound described below. The example and preferred range of the polystyrene-equivalent weight average molecular weight of the polymer compound (A) are the same as the example and preferred range of the polystyrene-equivalent weight average molecular weight of the first polymer compound described below.
(高分子化合物(A)の製造方法)
高分子化合物(A)は、後述の第1の高分子化合物の製造方法と同様の方法で製造することができる。
(Method for producing polymer compound (A))
The polymer compound (A) can be produced by a method similar to the method for producing the first polymer compound described below.
[第1の化合物]
第1の化合物は、式(H-1)で表される化合物及び第1の高分子化合物からなる群より選択される少なくとも1種である。
[First compound]
The first compound is at least one selected from the group consisting of the compound represented by formula (H-1) and the first polymer compound.
(式(H-1)で表される化合物)
式(H-1)で表される化合物は、低分子化合物であることが好ましい。
本開示の発光素子の駆動電圧が更に低くなるので、式(H-1)で表される化合物の分子量は、好ましくは1×102~5×103であり、より好ましくは2×102~3×103であり、更に好ましくは3×102~1.5×103であり、特に好ましくは4×102~1×103である。
式(H-1)で表される化合物は、化合物(B)と異なる化合物であることが好ましく、化合物中に、縮合複素環骨格(b)を有さない化合物であることがより好ましい。
(Compound represented by formula (H-1))
The compound represented by formula (H-1) is preferably a low-molecular-weight compound.
Since the driving voltage of the light-emitting device of the present disclosure is further lowered, the molecular weight of the compound represented by formula (H-1) is preferably 1×10 2 to 5×10 3 , more preferably 2×10 2 . 3×10 3 to 3×10 3 , more preferably 3×10 2 to 1.5×10 3 , particularly preferably 4×10 2 to 1×10 3 .
The compound represented by formula (H-1) is preferably a compound different from compound (B), and more preferably a compound that does not have a condensed heterocyclic skeleton (b).
ArH1及びArH2におけるアリール基は、本開示の発光素子の駆動電圧がより低くなるので、好ましくは、単環式又は2~7環式の芳香族炭化水素から環を構成する原子に直接結合する水素原子1個を除いた基であり、より好ましくは、単環式又は2~5環式の芳香族炭化水素から環を構成する原子に直接結合する水素原子1個を除いた基であり、更に好ましくは、単環式、2環式又は3環式の芳香族炭化水素から環を構成する原子に直接結合する水素原子1個を除いた基であり、これらの基は置換基を有していてもよい。
ArH1及びArH2におけるアリール基は、本開示の発光素子の駆動電圧が更に低くなるので、好ましくは、ベンゼン、ナフタレン、アントラセン、フェナントレン、ジヒドロフェナントレン、フルオレン、ベンゾアントラセン、ベンゾフェナントレン、ベンゾフルオレン、ジベンゾアントラセン、ジベンゾフェナントレン、ジベンゾフルオレン、インデノフルオレン又はベンゾフルオランテンから、環を構成する原子に直接結合する水素原子1個を除いた基であり、より好ましくは、ベンゼン、ナフタレン、アントラセン、フェナントレン、ジヒドロフェナントレン、フルオレン、ベンゾアントラセン、ベンゾフェナントレン又はベンゾフルオレンから、環を構成する原子に直接結合する水素原子1個を除いた基であり、更に好ましくは、ベンゼン、ナフタレン、アントラセン、フェナントレン、ジヒドロフェナントレン又はフルオレンから、環を構成する原子に直接結合する水素原子1個を除いた基であり、特に好ましくは、ベンゼン、ナフタレン又はアントラセンから、環を構成する原子に直接結合する水素原子1個を除いた基であり、これらの基は置換基を有していてもよい。
The aryl groups in Ar H1 and Ar H2 are preferably directly bonded to ring-constituting atoms of monocyclic or 2- to 7-cyclic aromatic hydrocarbons, because the driving voltage of the light-emitting device of the present disclosure is lower. is a group in which one hydrogen atom is removed, more preferably a monocyclic or bi- to five-ring aromatic hydrocarbon group in which one hydrogen atom directly bonded to an atom constituting a ring is removed More preferably, it is a group obtained by removing one hydrogen atom directly bonded to an atom constituting a ring from a monocyclic, bicyclic or tricyclic aromatic hydrocarbon, and these groups have substituents. You may have
Aryl groups in Ar H1 and Ar H2 are preferably benzene, naphthalene, anthracene, phenanthrene, dihydrophenanthrene, fluorene, benzanthracene, benzophenanthrene, benzofluorene, dibenzo a group obtained by removing one hydrogen atom directly bonded to a ring-constituting atom from anthracene, dibenzophenanthrene, dibenzofluorene, indenofluorene or benzofluoranthene, more preferably benzene, naphthalene, anthracene, phenanthrene, dihydrophenanthrene, fluorene, benzanthracene, benzophenanthrene or benzofluorene, from which one hydrogen atom directly bonded to a ring-constituting atom is removed, more preferably benzene, naphthalene, anthracene, phenanthrene, dihydrophenanthrene or A group obtained by removing one hydrogen atom directly bonded to a ring-constituting atom from fluorene, particularly preferably benzene, naphthalene or anthracene, with one hydrogen atom directly bonded to a ring-constituting atom removed. groups, and these groups may have a substituent.
ArH1及びArH2における1価の複素環基は、縮合複素環骨格(b)を含まない複素環式化合物から、環を構成する原子に直接結合する水素原子1個を除いた基であることが好ましく、この基は置換基を有していてもよい。ArH1及びArH2における1価の複素環基において、縮合複素環骨格(b)を含まない複素環式化合物としては、例えば、前述の複素環基の項で説明した複素環式化合物の中で、ホウ素原子と、酸素原子、硫黄原子、セレン原子、sp3炭素原子及び窒素原子からなる群より選ばれる少なくとも1種とを環内に含まない複素環式化合物が挙げられる。
ArH1及びArH2における1価の複素環基は、本開示の発光素子の駆動電圧がより低くなるので、好ましくは、単環式又は2~7環式の複素環式化合物(好ましくは、縮合複素環骨格(b)を含まない、単環式又は2~7環式の複素環式化合物)から環を構成する原子に直接結合する水素原子1個を除いた基であり、より好ましくは、単環式又は2~5環式の複素環式化合物(好ましくは、縮合複素環骨格(b)を含まない、単環式又は2~5環式の複素環式化合物)から環を構成する原子に直接結合する水素原子1個を除いた基であり、更に好ましくは、単環式、2環式又は3環式の複素環式化合物(好ましくは、縮合複素環骨格(b)を含まない、単環式、2環式又は3環式の複素環式化合物)から環を構成する原子に直接結合する水素原子1個を除いた基であり、特に好ましくは、3環式の複素環式化合物(好ましくは、縮合複素環骨格(b)を含まない、3環式の複素環式化合物)から環を構成する原子に直接結合する水素原子1個を除いた基であり、これらの基は置換基を有していてもよい。
ArH1及びArH2における1価の複素環基は、本開示の発光素子の駆動電圧が更に低くなるので、好ましくは、フラン、チオフェン、オキサジアゾール、チアジアゾール、ピロール、ジアゾール、トリアゾール、ピリジン、ジアザベンゼン、トリアジン、アザナフタレン、ジアザナフタレン、ベンゾフラン、ベンゾチオフェン、インドール、アザインドール、ジアザインドール、ベンゾジアゾール、ベンゾチアジアゾール、ベンゾトリアゾール、ジベンゾフラン、ジベンゾチオフェン、カルバゾール、アザカルバゾール、ジアザカルバゾール、フェノキサジン、フェノチアジン、9,10-ジヒドロアクリジン、5,10-ジヒドロフェナジン、アザアントラセン、ジアザアントラセン、アザフェナントレン、ジアザフェナントレン、ベンゾカルバゾール、アザベンゾカルバゾール、ジアザベンゾカルバゾール、ベンゾナフトフラン、ベンゾナフトチオフェン、ジベンゾカルバゾール、インドロカルバゾール、インデノカルバゾール、アザインドロカルバゾール、ジアザインドロカルバゾール、アザインデノカルバゾール又はジアザインデノカルバゾールから環を構成する原子に直接結合する水素原子1個を除いた基であり、より好ましくは、ピリジン、ジアザベンゼン、トリアジン、アザナフタレン、ジアザナフタレン、ジベンゾフラン、ジベンゾチオフェン、カルバゾール、アザカルバゾール、ジアザカルバゾール、フェノキサジン、フェノチアジン、9,10-ジヒドロアクリジン、5,10-ジヒドロフェナジン、ベンゾカルバゾール、アザベンゾカルバゾール、ジアザベンゾカルバゾール、ベンゾナフトフラン、ベンゾナフトチオフェン、ジベンゾカルバゾール、インドロカルバゾール、インデノカルバゾール、アザインドロカルバゾール、ジアザインドロカルバゾール、アザインデノカルバゾール又はジアザインデノカルバゾールから環を構成する原子に直接結合する水素原子1個を除いた基であり、更に好ましくは、ピリジン、ジアザベンゼン、トリアジン、アザナフタレン、ジアザナフタレン、ジベンゾフラン、ジベンゾチオフェン、カルバゾール、アザカルバゾール、ジアザカルバゾール、フェノキサジン、フェノチアジン、9,10-ジヒドロアクリジン又は5,10-ジヒドロフェナジンから環を構成する原子に直接結合する水素原子1個を除いた基であり、特に好ましくは、ピリジン、ジアザベンゼン、トリアジン、アザナフタレン、ジアザナフタレン、ジベンゾフラン、ジベンゾチオフェン又はカルバゾールから環を構成する原子に直接結合する水素原子1個を除いた基であり、とりわけ好ましくは、ジベンゾフラン、ジベンゾチオフェン又はカルバゾールから環を構成する原子に直接結合する水素原子1個を除いた基であり、これらの基は置換基を有していてもよい。
The monovalent heterocyclic group in Ar H1 and Ar H2 is a group obtained by removing one hydrogen atom directly bonded to a ring-constituting atom from a heterocyclic compound that does not contain a condensed heterocyclic skeleton (b). is preferred, and this group may have a substituent. In the monovalent heterocyclic group for Ar H1 and Ar H2 , the heterocyclic compound that does not contain a condensed heterocyclic skeleton (b) includes, for example, among the heterocyclic compounds described in the section on the heterocyclic group above, , a boron atom and at least one selected from the group consisting of an oxygen atom, a sulfur atom, a selenium atom, an sp3 carbon atom and a nitrogen atom in the ring.
The monovalent heterocyclic groups in Ar H1 and Ar H2 are preferably monocyclic or di- to hepta-cyclic heterocyclic compounds (preferably condensed A group obtained by removing one hydrogen atom directly bonded to a ring-constituting atom from a monocyclic or 2- to 7-ring heterocyclic compound containing no heterocyclic skeleton (b)), more preferably Atoms constituting a ring from a monocyclic or bi- to pentacyclic heterocyclic compound (preferably a monocyclic or bi- to pentacyclic heterocyclic compound containing no condensed heterocyclic skeleton (b)) is a group excluding one hydrogen atom directly bonded to the (monocyclic, bicyclic or tricyclic heterocyclic compound) by removing one hydrogen atom directly bonded to an atom constituting the ring, particularly preferably tricyclic heterocyclic compound (Preferably, a tricyclic heterocyclic compound that does not contain a condensed heterocyclic skeleton (b)) is a group in which one hydrogen atom directly bonded to an atom constituting the ring is removed, and these groups are substituted You may have a group.
The monovalent heterocyclic groups in Ar H1 and Ar H2 are preferably furan, thiophene, oxadiazole, thiadiazole, pyrrole, diazole, triazole, pyridine, diazabenzene, since the driving voltage of the light-emitting device of the present disclosure is further lowered. , triazine, azanaphthalene, diazanaphthalene, benzofuran, benzothiophene, indole, azaindole, diazaindole, benzodiazole, benzothiadiazole, benzotriazole, dibenzofuran, dibenzothiophene, carbazole, azacarbazole, diazacarbazole, phenoxazine , phenothiazine, 9,10-dihydroacridine, 5,10-dihydrophenazine, azaanthracene, diazaanthracene, azaphenanthrene, diazaphenanthrene, benzocarbazole, azabenzocarbazole, diazabenzocarbazole, benzonaphthofuran, benzonaphthothiophene , dibenzocarbazole, indolocarbazole, indenocarbazole, azaindolocarbazole, diazaindolocarbazole, azaindenocarbazole or diazaindenocarbazole, with one hydrogen atom directly bonded to a ring-constituting atom removed. and more preferably pyridine, diazabenzene, triazine, azanaphthalene, diazanaphthalene, dibenzofuran, dibenzothiophene, carbazole, azacarbazole, diazacarbazole, phenoxazine, phenothiazine, 9,10-dihydroacridine, 5,10- dihydrophenazine, benzocarbazole, azabenzocarbazole, diazabenzocarbazole, benzonaphthofuran, benzonaphthothiophene, dibenzocarbazole, indolocarbazole, indenocarbazole, azaindolocarbazole, diazaindolocarbazole, azaindenocarbazole or di A group obtained by removing one hydrogen atom directly bonded to a ring-constituting atom from zaindenocarbazole, more preferably pyridine, diazabenzene, triazine, azanaphthalene, diazanaphthalene, dibenzofuran, dibenzothiophene, carbazole, aza carbazole, diazacarbazole, phenoxazine, phenothiazine, 9,10-dihydroacridine or 5,10-dihydrophenazine with one hydrogen atom directly bonded to a ring-constituting atom removed, particularly preferably pyridine , diazabenzene, triazine, azanaphthalene, diazanaphthalene, dibenzofuran, dibenzothiophene, or carbazole from which one hydrogen atom directly bonded to a ring-constituting atom is removed, particularly preferably dibenzofuran, dibenzothiophene, or carbazole. It is a group in which one hydrogen atom is directly bonded to a ring-constituting atom, and these groups may have a substituent.
ArH1及びArH2における置換アミノ基において、アミノ基が有する置換基としては、アリール基又は1価の複素環基が好ましく、アリール基がより好ましく、これらの基は更に置換基を有していてもよい。アミノ基が有する置換基であるアリール基の例及び好ましい範囲は、ArH1及びArH2におけるアリール基の例及び好ましい範囲と同じである。アミノ基が有する置換基である1価の複素環基の例及び好ましい範囲は、ArH1及びArH2における1価の複素環基の例及び好ましい範囲と同じである。 In the substituted amino group for Ar H1 and Ar H2 , the substituent of the amino group is preferably an aryl group or a monovalent heterocyclic group, more preferably an aryl group, and these groups further have a substituent. good too. Examples and preferred ranges of the aryl group, which is a substituent of the amino group, are the same as the examples and preferred ranges of the aryl group in Ar H1 and Ar H2 . Examples and preferred ranges of the monovalent heterocyclic group which is a substituent of the amino group are the same as the examples and preferred range of the monovalent heterocyclic group in Ar 1 H1 and Ar 2 H2 .
本開示の発光素子の駆動電圧がより低くなるので、ArH1及びArH2の少なくとも1つは、アリール基又は1価の複素環基であることが好ましく、ArH1及びArH2の両方が、アリール基又は1価の複素環基であることがより好ましく、これらの基は置換基を有していてもよい。
ArH1及びArH2におけるアリール基及び1価の複素環基としては、本開示の発光素子の駆動電圧がより低くなるので、単環式、2環式若しくは3環式の芳香族炭化水素、又は、単環式、2環式若しくは3環式の複素環式化合物(好ましくは、縮合複素環骨格(b)を含まない、単環式、2環式又は3環式の複素環式化合物)から、環を構成する原子に直接結合する水素原子1個を除いた基が好ましく、ベンゼン、ナフタレン、フルオレン、ピリジン、ジアザベンゼン、トリアジン、アザナフタレン、ジアザナフタレン、ジベンゾフラン、ジベンゾチオフェン又はカルバゾールから、環を構成する原子に直接結合する水素原子1個を除いた基がより好ましく、フェニル基、ナフチル基、フルオレニル基、カルバゾリル基、ジベンゾチエニル基又はジベンゾフリル基が更に好ましく、フェニル基、ナフチル基又はカルバゾリル基が特に好ましく、これらの基は置換基を有していてもよい。
At least one of Ar H1 and Ar H2 is preferably an aryl group or a monovalent heterocyclic group, and both Ar H1 and Ar H2 are aryl group or a monovalent heterocyclic group, and these groups may have a substituent.
The aryl group and monovalent heterocyclic group in Ar H1 and Ar H2 are monocyclic, bicyclic or tricyclic aromatic hydrocarbons, or , a monocyclic, bicyclic or tricyclic heterocyclic compound (preferably a monocyclic, bicyclic or tricyclic heterocyclic compound that does not contain a condensed heterocyclic skeleton (b)) , is preferably a group in which one hydrogen atom directly bonded to an atom constituting the ring is removed, and the ring is selected from benzene, naphthalene, fluorene, pyridine, diazabenzene, triazine, azanaphthalene, diazanaphthalene, dibenzofuran, dibenzothiophene, or carbazole. A group in which one hydrogen atom directly bonded to a constituent atom is removed is more preferable, and a phenyl group, a naphthyl group, a fluorenyl group, a carbazolyl group, a dibenzothienyl group or a dibenzofuryl group is more preferable, and a phenyl group, a naphthyl group or a carbazolyl group. is particularly preferred, and these groups may have a substituent.
ArH1及びArH2が有していてもよい置換基としては、好ましくは、ハロゲン原子、シアノ基、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリールオキシ基、アリール基、1価の複素環基又は置換アミノ基であり、より好ましくは、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基、1価の複素環基又は置換アミノ基であり、更に好ましくは、アルキル基、シクロアルキル基、アリール基、1価の複素環基又は置換アミノ基であり、特に好ましくは、アルキル基、シクロアルキル基又はアリール基であり、これらの基は更に置換基を有していてもよい。
ArH1及びArH2が有していてもよい置換基におけるアリール基、1価の複素環基及び置換アミノ基の例及び好ましい範囲は、それぞれ、ArH1及びArH2におけるアリール基、1価の複素環基及び置換アミノ基の例及び好ましい範囲と同じである。
Preferred substituents that Ar H1 and Ar H2 may have are a halogen atom, a cyano group, an alkyl group, a cycloalkyl group, an alkoxy group, a cycloalkoxy group, an aryloxy group, an aryl group, and a monovalent A heterocyclic group or a substituted amino group, more preferably an alkyl group, a cycloalkyl group, an alkoxy group, a cycloalkoxy group, an aryl group, a monovalent heterocyclic group or a substituted amino group, still more preferably an alkyl group , a cycloalkyl group, an aryl group, a monovalent heterocyclic group or a substituted amino group, particularly preferably an alkyl group, a cycloalkyl group or an aryl group, even if these groups further have a substituent good.
Examples and preferred ranges of the aryl group, monovalent heterocyclic group and substituted amino group in the substituents that Ar H1 and Ar H2 may have are the aryl group and monovalent heterocyclic group in Ar H1 and Ar H2 , respectively. It is the same as the examples and preferred ranges of the cyclic group and the substituted amino group.
ArH1及びArH2が有していてもよい置換基が更に有していてもよい置換基としては、好ましくは、ハロゲン原子、シアノ基、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリールオキシ基、アリール基、1価の複素環基又は置換アミノ基であり、より好ましくは、アルキル基、シクロアルキル基、アリール基、1価の複素環基又は置換アミノ基であり、更に好ましくは、アルキル基、シクロアルキル基又はアリール基であり、特に好ましくは、アルキル基又はシクロアルキル基であり、これらの基は更に置換基を有していてもよいが、更に置換基を有さないことが好ましい。
ArH1及びArH2が有していてもよい置換基が更に有していてもよい置換基におけるアリール基、1価の複素環基及び置換アミノ基の例及び好ましい範囲は、それぞれ、ArH1及びArH2におけるアリール基、1価の複素環基及び置換アミノ基の例及び好ましい範囲と同じである。
Preferred substituents that the substituents Ar H1 and Ar H2 may further have include a halogen atom, a cyano group, an alkyl group, a cycloalkyl group, an alkoxy group, a cycloalkoxy group, an aryloxy group, an aryl group, a monovalent heterocyclic group or a substituted amino group, more preferably an alkyl group, a cycloalkyl group, an aryl group, a monovalent heterocyclic group or a substituted amino group, still more preferably , an alkyl group, a cycloalkyl group or an aryl group, particularly preferably an alkyl group or a cycloalkyl group, and these groups may further have a substituent, but should not have a further substituent. is preferred.
Examples and preferred ranges of the aryl group, monovalent heterocyclic group and substituted amino group in the substituents which the substituents which Ar H1 and Ar H2 may further have are respectively Ar H1 and The same as the examples and preferred ranges of the aryl group, monovalent heterocyclic group and substituted amino group in Ar H2 .
LH1における2価の基としては、好ましくは、本開示の発光素子の駆動電圧がより低くなるので、アルキレン基、シクロアルキレン基、アリーレン基、2価の複素環基、-N(R0)-で表される基、-(O=)P(R0)-で表される基、-O-で表される基、-S-で表される基、-S(=O)2-で表される基又は-C(=O)-で表される基であり、より好ましくは、アルキレン基、シクロアルキレン基、アリーレン基、2価の複素環基、-N(R0)-で表される基、-O-で表される基又は-S-で表される基であり、更に好ましくは、アルキレン基、シクロアルキレン基、アリーレン基又は2価の複素環基であり、特に好ましくは、アリーレン基又は2価の複素環基であり、これらの基は置換基を有していてもよい。
LH1における2価の基の少なくとも1つは、本開示の発光素子の駆動電圧がより低くなるので、好ましくは、アルキレン基、シクロアルキレン基、アリーレン基又は2価の複素環基であり、より好ましくは、アリーレン基又は2価の複素環基であり、これらの基は置換基を有していてもよい。
The divalent group for L H1 is preferably an alkylene group, a cycloalkylene group, an arylene group, a divalent heterocyclic group, —N(R 0 ), since the driving voltage of the light-emitting device of the present disclosure is lower. A group represented by -, a group represented by -(O=)P(R 0 )-, a group represented by -O-, a group represented by -S-, and -S(=O) 2 - or a group represented by -C(=O)-, more preferably an alkylene group, a cycloalkylene group, an arylene group, a divalent heterocyclic group, or -N(R 0 )- a group represented by -O- or a group represented by -S-, more preferably an alkylene group, a cycloalkylene group, an arylene group or a divalent heterocyclic group, particularly preferably is an arylene group or a divalent heterocyclic group, and these groups may have a substituent.
At least one of the divalent groups in L H1 is preferably an alkylene group, a cycloalkylene group, an arylene group, or a divalent heterocyclic group, since the driving voltage of the light emitting device of the present disclosure is lower, and more An arylene group or a divalent heterocyclic group is preferable, and these groups may have a substituent.
LH1における2価の基において、アリーレン基は、本開示の発光素子の駆動電圧がより低くなるので、好ましくは、単環式又は2~7環式の芳香族炭化水素から環を構成する原子に直接結合する水素原子2個を除いた基であり、より好ましくは、単環式又は2~5環式の芳香族炭化水素から環を構成する原子に直接結合する水素原子2個を除いた基であり、更に好ましくは、単環式、2環式又は3環式の芳香族炭化水素から環を構成する原子に直接結合する水素原子2個を除いた基であり、これらの基は置換基を有していてもよい。
LH1における2価の基において、アリーレン基は、本開示の発光素子の駆動電圧が更に低くなるので、好ましくは、ベンゼン、ナフタレン、アントラセン、フェナントレン、ジヒドロフェナントレン、フルオレン、ベンゾアントラセン、ベンゾフェナントレン、ベンゾフルオレン、ジベンゾアントラセン、ジベンゾフェナントレン、ジベンゾフルオレン、インデノフルオレン又はベンゾフルオランテンから、環を構成する原子に直接結合する水素原子2個を除いた基であり、より好ましくは、ベンゼン、ナフタレン、アントラセン、フェナントレン、ジヒドロフェナントレン、フルオレン、ベンゾアントラセン、ベンゾフェナントレン又はベンゾフルオレンから、環を構成する原子に直接結合する水素原子2個を除いた基であり、更に好ましくは、ベンゼン、ナフタレン、アントラセン、フェナントレン、ジヒドロフェナントレン又はフルオレンから、環を構成する原子に直接結合する水素原子2個を除いた基であり、特に好ましくは、ベンゼン、ナフタレン又はアントラセンから、環を構成する原子に直接結合する水素原子2個を除いた基であり、これらの基は置換基を有していてもよい。
Among the divalent groups in L H1 , the arylene group is preferably a monocyclic or bi- to seven-cyclic aromatic hydrocarbon ring-constituting atom because the driving voltage of the light-emitting device of the present disclosure is lower. A group in which two hydrogen atoms directly bonded to are removed, more preferably a monocyclic or 2- to 5-cyclic aromatic hydrocarbon in which two hydrogen atoms directly bonded to the atoms constituting the ring are removed group, more preferably a group obtained by removing two hydrogen atoms directly bonded to atoms constituting the ring from a monocyclic, bicyclic or tricyclic aromatic hydrocarbon, and these groups are substituted You may have a group.
Among the divalent groups in L H1 , arylene groups are preferably benzene, naphthalene, anthracene, phenanthrene, dihydrophenanthrene, fluorene, benzoanthracene, benzophenanthrene, benzo a group obtained by removing two hydrogen atoms directly bonded to ring-constituting atoms from fluorene, dibenzoanthracene, dibenzophenanthrene, dibenzofluorene, indenofluorene or benzofluoranthene, more preferably benzene, naphthalene or anthracene , phenanthrene, dihydrophenanthrene, fluorene, benzanthracene, benzophenanthrene or benzofluorene, from which two hydrogen atoms directly bonded to atoms constituting the ring are removed, more preferably benzene, naphthalene, anthracene, phenanthrene, A group obtained by removing two hydrogen atoms directly bonded to ring-constituting atoms from dihydrophenanthrene or fluorene, and particularly preferably benzene, naphthalene or anthracene with two hydrogen atoms directly bonded to ring-constituting atoms. These groups may have a substituent.
LH1における2価の基において、2価の複素環基は、縮合複素環骨格(b)を含まない複素環式化合物から、環を構成する原子(好ましくは炭素原子)に直接結合する水素原子2個を除いた基であることが好ましく、この基は置換基を有していてもよい。LH1における2価の基において、2価の複素環基における縮合複素環骨格(b)を含まない複素環式化合物としては、前述の複素環基の項で説明した複素環式化合物の中で、ホウ素原子と、酸素原子、硫黄原子、セレン原子、sp3炭素原子及び窒素原子からなる群より選ばれる少なくとも1種とを環内に含まない複素環式化合物が挙げられる。
LH1における2価の基において、2価の複素環基は、本開示の発光素子の駆動電圧がより低くなるので、好ましくは、単環式又は2~7環式の複素環式化合物(好ましくは、縮合複素環骨格(b)を含まない、単環式又は2~7環式の複素環式化合物)から環を構成する原子(好ましくは炭素原子)に直接結合する水素原子2個を除いた基であり、より好ましくは、単環式又は2~5環式の複素環式化合物(好ましくは、縮合複素環骨格(b)を含まない、単環式又は2~5環式の複素環式化合物)から環を構成する原子(好ましくは炭素原子)に直接結合する水素原子2個を除いた基であり、更に好ましくは、単環式、2環式又は3環式の複素環式化合物(好ましくは、縮合複素環骨格(b)を含まない、単環式、2環式又は3環式の複素環式化合物)から環を構成する原子(好ましくは炭素原子)に直接結合する水素原子2個を除いた基であり、特に好ましくは、3環式の複素環式化合物(好ましくは、縮合複素環骨格(b)を含まない、3環式の複素環式化合物)から環を構成する原子(好ましくは炭素原子)に直接結合する水素原子2個を除いた基であり、これらの基は置換基を有していてもよい。
LH1における2価の基において、2価の複素環基は、本開示の発光素子の駆動電圧が更に低くなるので、好ましくは、フラン、チオフェン、オキサジアゾール、チアジアゾール、ピロール、ジアゾール、トリアゾール、ピリジン、ジアザベンゼン、トリアジン、アザナフタレン、ジアザナフタレン、ベンゾフラン、ベンゾチオフェン、インドール、アザインドール、ジアザインドール、ベンゾジアゾール、ベンゾチアジアゾール、ベンゾトリアゾール、ジベンゾフラン、ジベンゾチオフェン、カルバゾール、アザカルバゾール、ジアザカルバゾール、フェノキサジン、フェノチアジン、9,10-ジヒドロアクリジン、5,10-ジヒドロフェナジン、アザアントラセン、ジアザアントラセン、アザフェナントレン、ジアザフェナントレン、ベンゾカルバゾール、アザベンゾカルバゾール、ジアザベンゾカルバゾール、ベンゾナフトフラン、ベンゾナフトチオフェン、ジベンゾカルバゾール、インドロカルバゾール、インデノカルバゾール、アザインドロカルバゾール、ジアザインドロカルバゾール、アザインデノカルバゾール又はジアザインデノカルバゾールから環を構成する原子(好ましくは炭素原子)に直接結合する水素原子2個を除いた基であり、より好ましくは、ピリジン、ジアザベンゼン、トリアジン、アザナフタレン、ジアザナフタレン、ジベンゾフラン、ジベンゾチオフェン、カルバゾール、アザカルバゾール、ジアザカルバゾール、フェノキサジン、フェノチアジン、9,10-ジヒドロアクリジン、5,10-ジヒドロフェナジン、ベンゾカルバゾール、アザベンゾカルバゾール、ジアザベンゾカルバゾール、ベンゾナフトフラン、ベンゾナフトチオフェン、ジベンゾカルバゾール、インドロカルバゾール、インデノカルバゾール、アザインドロカルバゾール、ジアザインドロカルバゾール、アザインデノカルバゾール又はジアザインデノカルバゾールから環を構成する原子(好ましくは炭素原子)に直接結合する水素原子2個を除いた基であり、更に好ましくは、ピリジン、ジアザベンゼン、トリアジン、アザナフタレン、ジアザナフタレン、ジベンゾフラン、ジベンゾチオフェン、カルバゾール、アザカルバゾール、ジアザカルバゾール、フェノキサジン、フェノチアジン、9,10-ジヒドロアクリジン又は5,10-ジヒドロフェナジンから環を構成する原子(好ましくは炭素原子)に直接結合する水素原子2個を除いた基であり、特に好ましくは、ピリジン、ジアザベンゼン、トリアジン、アザナフタレン、ジアザナフタレン、ジベンゾフラン、ジベンゾチオフェン又はカルバゾールから環を構成する原子(好ましくは炭素原子)に直接結合する水素原子2個を除いた基であり、とりわけ好ましくは、ジベンゾフラン、ジベンゾチオフェン又はカルバゾールから環を構成する原子(好ましくは炭素原子)に直接結合する水素原子2個を除いた基であり、これらの基は置換基を有していてもよい。
In the divalent group in L H1 , the divalent heterocyclic group is a hydrogen atom directly bonded to a ring-constituting atom (preferably a carbon atom) from a heterocyclic compound that does not contain a condensed heterocyclic skeleton (b). It is preferably a group excluding two, and this group may have a substituent. In the divalent group in L H1 , the heterocyclic compound that does not contain a condensed heterocyclic skeleton (b) in the divalent heterocyclic group includes the heterocyclic compounds described in the section on the heterocyclic group above. , a boron atom and at least one selected from the group consisting of an oxygen atom, a sulfur atom, a selenium atom, an sp3 carbon atom and a nitrogen atom in the ring.
Among the divalent groups in L H1 , a divalent heterocyclic group is preferably a monocyclic or di- to hepta-cyclic heterocyclic compound (preferably is a monocyclic or 2- to 7-ring heterocyclic compound that does not contain a condensed heterocyclic skeleton (b)), except for two hydrogen atoms directly bonded to the atoms (preferably carbon atoms) constituting the ring more preferably a monocyclic or bi- to pentacyclic heterocyclic compound (preferably a monocyclic or bi- to pentacyclic heterocyclic ring that does not contain a condensed heterocyclic skeleton (b) A group obtained by removing two hydrogen atoms directly bonded to atoms (preferably carbon atoms) constituting a ring from the formula compound), more preferably a monocyclic, bicyclic or tricyclic heterocyclic compound A hydrogen atom directly bonded to an atom (preferably a carbon atom) constituting a ring from (preferably a monocyclic, bicyclic or tricyclic heterocyclic compound that does not contain a condensed heterocyclic skeleton (b)) A group excluding two, particularly preferably a tricyclic heterocyclic compound (preferably a tricyclic heterocyclic compound containing no condensed heterocyclic skeleton (b)) to form a ring. It is a group excluding two hydrogen atoms directly bonded to an atom (preferably a carbon atom), and these groups may have a substituent.
Among the divalent groups in L H1 , divalent heterocyclic groups are preferably furan, thiophene, oxadiazole, thiadiazole, pyrrole, diazole, triazole, pyridine, diazabenzene, triazine, azanaphthalene, diazanaphthalene, benzofuran, benzothiophene, indole, azaindole, diazaindole, benzodiazole, benzothiadiazole, benzotriazole, dibenzofuran, dibenzothiophene, carbazole, azacarbazole, diazacarbazole , phenoxazine, phenothiazine, 9,10-dihydroacridine, 5,10-dihydrophenazine, azaanthracene, diazaanthracene, azaphenanthrene, diazaphenanthrene, benzocarbazole, azabenzocarbazole, diazabenzocarbazole, benzonaphthofuran, directly bonded to a ring-constituting atom (preferably a carbon atom) of benzonaphthothiophene, dibenzocarbazole, indolocarbazole, indenocarbazole, azaindolocarbazole, diazaindolocarbazole, azaindenocarbazole or diazaindenocarbazole; more preferably pyridine, diazabenzene, triazine, azanaphthalene, diazanaphthalene, dibenzofuran, dibenzothiophene, carbazole, azacarbazole, diazacarbazole, phenoxazine, phenothiazine, 9, 10-dihydroacridine, 5,10-dihydrophenazine, benzocarbazole, azabenzocarbazole, diazabenzocarbazole, benzonaphthofuran, benzonaphthothiophene, dibenzocarbazole, indolocarbazole, indenocarbazole, azaindolocarbazole, diazaine dolocarbazole, azaindenocarbazole or diazaindenocarbazole without two hydrogen atoms directly bonded to atoms (preferably carbon atoms) constituting the ring, more preferably pyridine, diazabenzene, triazine, Ring-constituting atoms (preferably carbon atoms) of azanaphthalene, diazanaphthalene, dibenzofuran, dibenzothiophene, carbazole, azacarbazole, diazacarbazole, phenoxazine, phenothiazine, 9,10-dihydroacridine or 5,10-dihydrophenazine ) excluding two hydrogen atoms directly bonded to ), particularly preferably pyridine, diazabenzene, triazine, azanaphthalene, diazanaphthalene, dibenzofuran, dibenzothiophene, or carbazole atoms forming a ring (preferably carbon atoms ) in which two hydrogen atoms are directly bonded to ), and particularly preferably a group in which two hydrogen atoms are directly bonded to a ring-constituting atom (preferably a carbon atom) from dibenzofuran, dibenzothiophene or carbazole. and these groups may have a substituent.
LH1における2価の基において、アルキレン基としては、好ましくは、メチレン基、エチレン基又はプロピレン基であり、より好ましくはメチレン基であり、これらの基は置換基を有していてもよい。 In the divalent group for L H1 , the alkylene group is preferably a methylene group, an ethylene group or a propylene group, more preferably a methylene group, and these groups may have a substituent.
LH1が有していてもよい置換基の例及び好ましい範囲は、ArH1及びArH2が有していてもよい置換基の例及び好ましい範囲と同じである。 Examples and preferred ranges of substituents that L H1 may have are the same as examples and preferred ranges of substituents that Ar H1 and Ar H2 may have.
LH1における2価の基において、R0は、好ましくは、アルキル基、シクロアルキル基、アリール基又は1価の複素環基であり、より好ましくはアリール基又は1価の複素環基であり、更に好ましくはアリール基であり、これらの基は置換基を有していてもよい。
LH1における2価の基において、R0におけるアリール基及び1価の複素環基の例及び好ましい範囲は、それぞれ、ArH1及びArH2におけるアリール基及び1価の複素環基の例及び好ましい範囲と同じである。
LH1における2価の基において、R0が有していてもよい置換基の例及び好ましい範囲は、ArH1及びArH2が有していてもよい置換基の例及び好ましい範囲と同じである。
In the divalent group for L H1 , R 0 is preferably an alkyl group, a cycloalkyl group, an aryl group or a monovalent heterocyclic group, more preferably an aryl group or a monovalent heterocyclic group, An aryl group is more preferable, and these groups may have a substituent.
Examples and preferred ranges of the aryl group and monovalent heterocyclic group for R 0 in the divalent group for L H1 are the examples and preferred ranges for the aryl group and monovalent heterocyclic group for Ar H1 and Ar H2 , respectively. is the same as
In the divalent group L H1 , examples and preferred ranges of substituents R 0 may have are the same as examples and preferred ranges of substituents Ar H1 and Ar H2 may have. .
nH1は、通常、0以上10以下の整数であり、好ましくは0以上7以下の整数であり、より好ましくは1以上5以下の整数であり、更に好ましくは1以上3以下の整数であり、特に好ましくは1又は2である。 n H1 is usually an integer of 0 or more and 10 or less, preferably an integer of 0 or more and 7 or less, more preferably an integer of 1 or more and 5 or less, and still more preferably an integer of 1 or more and 3 or less, 1 or 2 is particularly preferred.
ArH1とArH2とは、直接結合して、又は、2価の基を介して結合して、環を形成してもよいが、式(H-1)で表される化合物の合成が容易なので、環を形成しないことが好ましい。
ArH1とArH2とが、2価の基を介して結合して、環を形成する場合において、2価の基としては、好ましくは、アルキレン基、シクロアルキレン基、アリーレン基、2価の複素環基、-N(R0)-で表される基、-(O=)P(R0)-で表される基、-O-で表される基、-S-で表される基、-S(=O)2-で表される基又は-C(=O)-で表される基であり、より好ましくは、アルキレン基、シクロアルキレン基、-N(R0)-で表される基、-O-で表される基又は-S-で表される基であり、更に好ましくは、アルキレン基、-O-で表される基又は-S-で表される基であり、これらの基は置換基を有していてもよい。
ArH1とArH2とが、2価の基を介して結合して、環を形成する場合において、2価の基におけるアリーレン基、2価の複素環基及びアルキレン基の例及び好ましい範囲は、それぞれ、LH1におけるアリーレン基、2価の複素環基及びアルキレン基の例及び好ましい範囲と同じである。
ArH1とArH2とが、2価の基を介して結合して、環を形成する場合において、2価の基におけるR0の例及び好ましい範囲は、LH1の2価の基におけるR0の例及び好ましい範囲と同じである。
ArH1とArH2とが、2価の基を介して結合して、環を形成する場合において、2価の基が有していてもよい置換基の例及び好ましい範囲は、ArH1及びArH2が有していてもよい置換基の例及び好ましい範囲と同じである。
Ar H1 and Ar H2 may be directly bonded or bonded via a divalent group to form a ring, but the compound represented by formula (H-1) is easy to synthesize. Therefore, it is preferred not to form a ring.
When Ar H1 and Ar H2 are bonded via a divalent group to form a ring, the divalent group is preferably an alkylene group, a cycloalkylene group, an arylene group, a divalent hetero A cyclic group, a group represented by -N(R 0 )-, a group represented by -(O=)P(R 0 )-, a group represented by -O-, a group represented by -S- , a group represented by -S(=O) 2 - or a group represented by -C(=O)-, more preferably an alkylene group, a cycloalkylene group, or a group represented by -N(R 0 )- a group represented by -O- or a group represented by -S-, more preferably an alkylene group, a group represented by -O- or a group represented by -S- , these groups may have a substituent.
When Ar H1 and Ar H2 are bonded via a divalent group to form a ring, examples and preferred ranges of the arylene group, divalent heterocyclic group and alkylene group in the divalent group are They are the same as the examples and preferred ranges of the arylene group, divalent heterocyclic group and alkylene group in L H1 , respectively.
When Ar H1 and Ar H2 are bonded through a divalent group to form a ring, examples and preferred ranges of R 0 in the divalent group are R 0 in the divalent group of L H1 is the same as the example and preferred range of
When Ar 1 H1 and Ar 2 H2 are bonded via a divalent group to form a ring, examples and preferred ranges of substituents that the divalent group may have include Ar H1 and Ar It is the same as the example and preferred range of the substituent that H2 may have.
LH1とArH1とは、直接結合して、又は、2価の基を介して結合して、環を形成してもよいが、式(H-1)で表される化合物の合成が容易なので、環を形成しないことが好ましい。LH1とArH1とが、2価の基を介して結合して、環を形成する場合における2価の基の例及び好ましい範囲は、ArH1とArH2とが、2価の基を介して結合して、環を形成する場合における2価の基の例及び好ましい範囲と同じである。
LH1とArH2とは、直接結合して、又は、2価の基を介して結合して、環を形成してもよいが、式(H-1)で表される化合物の合成が容易なので、環を形成しないことが好ましい。LH1とArH2とが、2価の基を介して結合して、環を形成する場合における2価の基の例及び好ましい範囲は、ArH1とArH2とが、2価の基を介して結合して、環を形成する場合における2価の基の例及び好ましい範囲と同じである。
L 1 H1 and Ar 1 H1 may be directly bonded or bonded via a divalent group to form a ring, but the compound represented by formula (H-1) is easy to synthesize. Therefore, it is preferred not to form a ring. Examples and preferred ranges of the divalent group in the case where L H1 and Ar H1 are bonded via a divalent group to form a ring are: are the same as the examples and preferred ranges of the divalent group in the case of forming a ring by combining with each other.
L H1 and Ar H2 may be directly bonded or bonded via a divalent group to form a ring, but the compound represented by formula (H-1) is easily synthesized. Therefore, it is preferred not to form a ring. Examples and preferred ranges of the divalent group in the case where L H1 and Ar H2 are bonded via a divalent group to form a ring are: are the same as the examples and preferred ranges of the divalent group in the case of forming a ring by combining with each other.
式(H-1)で表される化合物としては、例えば、下記式で表される化合物が挙げられる。 Examples of the compound represented by formula (H-1) include compounds represented by the following formula.
(第1の高分子化合物)
第1の高分子化合物は、式(X)で表される構成単位及び式(Y)で表される構成単位からなる群より選ばれる少なくとも1種の構成単位を含む高分子化合物である。
第1の高分子化合物は、高分子化合物(A)及び高分子化合物(B)とは異なる高分子化合物であることが好ましく、構成単位(A)及び構成単位(B)を含まない高分子化合物であることがより好ましい。
(First polymer compound)
The first polymer compound is a polymer compound containing at least one structural unit selected from the group consisting of structural units represented by formula (X) and structural units represented by formula (Y).
The first polymer compound is preferably a polymer compound different from the polymer compound (A) and the polymer compound (B), and is a polymer compound that does not contain the structural unit (A) and the structural unit (B). is more preferable.
第1の高分子化合物は、本開示の発光素子の駆動電圧がより低くなるので、式(Y)で表される構成単位を含むことが好ましい。
第1の高分子化合物が式(Y)で表される構成単位を含む場合、第1の高分子化合物中に含まれる式(Y)で表される構成単位の含有量は、第1の高分子化合物としての機能が奏される範囲であればよい。第1の高分子化合物が式(Y)で表される構成単位を含む場合、第1の高分子化合物中に含まれる式(Y)で表される構成単位の含有量は、第1の高分子化合物に含まれる構成単位の合計の含有量に対して、例えば、1~100モル%であり、本開示の発光素子の駆動電圧がより低くなるので、好ましくは10~100モル%であり、より好ましくは30~100モル%であり、更に好ましくは50~100モル%であり、特に好ましくは70~100モル%であり、とりわけ好ましくは90~100モル%である。
第1の高分子化合物において、式(Y)で表される構成単位は、第1の高分子化合物中に、1種のみ含まれていてもよく、2種以上含まれていてもよい。
The first polymer compound preferably contains a structural unit represented by formula (Y), since the driving voltage of the light-emitting device of the present disclosure is lower.
When the first polymer compound contains a structural unit represented by formula (Y), the content of the structural unit represented by formula (Y) contained in the first polymer compound is Any range is acceptable as long as it functions as a molecular compound. When the first polymer compound contains a structural unit represented by formula (Y), the content of the structural unit represented by formula (Y) contained in the first polymer compound is For example, it is 1 to 100 mol% with respect to the total content of structural units contained in the molecular compound, and is preferably 10 to 100 mol% because the driving voltage of the light-emitting device of the present disclosure is lower, It is more preferably 30 to 100 mol %, still more preferably 50 to 100 mol %, particularly preferably 70 to 100 mol %, particularly preferably 90 to 100 mol %.
In the first polymer compound, the structural unit represented by the formula (Y) may be contained alone or in combination of two or more.
第1の高分子化合物は、第1の高分子化合物の正孔輸送性が優れ、且つ、本開示の発光素子の駆動電圧がより低くなるので、式(X)で表される構成単位を含むことが好ましい。
第1の高分子化合物が式(X)で表される構成単位を含む場合、第1の高分子化合物中に含まれる式(X)で表される構成単位の含有量は、第1の高分子化合物としての機能が奏される範囲であればよい。第1の高分子化合物が式(X)で表される構成単位を含む場合、第1の高分子化合物中に含まれる式(X)で表される構成単位の含有量は、第1の高分子化合物に含まれる構成単位の合計の含有量に対して、例えば、0.01~100モル%であり、第1の高分子化合物の正孔輸送性が優れ、且つ、本開示の発光素子の駆動電圧がより低くなるので、好ましくは0.05~90モル%であり、より好ましくは0.1~70モル%であり、更に好ましくは0.2~50モル%であり、特に好ましくは0.5~30モル%であり、とりわけ好ましくは1~10モル%である。
第1の高分子化合物において、式(X)で表される構成単位は、第1の高分子化合物中に、1種のみ含まれていてもよく、2種以上含まれていてもよい。
The first polymer compound contains a structural unit represented by formula (X) because the first polymer compound has excellent hole-transport properties and the driving voltage of the light-emitting device of the present disclosure is lower. is preferred.
When the first polymer compound contains a structural unit represented by formula (X), the content of the structural unit represented by formula (X) contained in the first polymer compound is Any range is acceptable as long as the function as a molecular compound is exhibited. When the first polymer compound contains a structural unit represented by formula (X), the content of the structural unit represented by formula (X) contained in the first polymer compound is For example, it is 0.01 to 100 mol% with respect to the total content of the structural units contained in the molecular compound, the hole transport property of the first polymer compound is excellent, and the light emitting device of the present disclosure is obtained. Since the driving voltage becomes lower, it is preferably 0.05 to 90 mol%, more preferably 0.1 to 70 mol%, still more preferably 0.2 to 50 mol%, particularly preferably 0 .5 to 30 mol %, particularly preferably 1 to 10 mol %.
In the first polymer compound, the structural unit represented by formula (X) may be contained alone or in combination of two or more.
第1の高分子化合物は、第1の高分子化合物の正孔輸送性が優れ、且つ、本開示の発光素子の駆動電圧が更に低くなるので、式(Y)で表される構成単位及び式(X)で表される構成単位を含むことが好ましい。
第1の高分子化合物が式(Y)で表される構成単位及び式(X)で表される構成単位を含む場合、第1の高分子化合物中に含まれる式(Y)で表される構成単位及び式(X)で表される構成単位の合計の含有量は、第1の高分子化合物としての機能が奏される範囲であればよい。第1の高分子化合物が式(Y)で表される構成単位及び式(X)で表される構成単位を含む場合、第1の高分子化合物中に含まれる式(Y)で表される構成単位及び式(X)で表される構成単位の合計の含有量は、例えば、1~100モル%であり、第1の高分子化合物の正孔輸送性が優れ、且つ、本開示の発光素子の駆動電圧が更に低くなるので、好ましくは10~100モル%であり、より好ましくは30~100モル%であり、更に好ましくは50~100モル%であり、特に好ましくは70~100モル%であり、とりわけ好ましくは90~100モル%である。
Since the first polymer compound has an excellent hole-transport property and the driving voltage of the light-emitting device of the present disclosure is further lowered, the structural unit represented by formula (Y) and the formula It preferably contains a structural unit represented by (X).
When the first polymer compound contains a structural unit represented by the formula (Y) and a structural unit represented by the formula (X), it is represented by the formula (Y) contained in the first polymer compound The total content of the structural units and the structural units represented by formula (X) may be within a range in which the function as the first polymer compound can be exhibited. When the first polymer compound contains a structural unit represented by the formula (Y) and a structural unit represented by the formula (X), it is represented by the formula (Y) contained in the first polymer compound The total content of the structural units and the structural units represented by the formula (X) is, for example, 1 to 100 mol%, the hole transport property of the first polymer compound is excellent, and the light emission of the present disclosure Since the drive voltage of the device is further lowered, it is preferably 10 to 100 mol%, more preferably 30 to 100 mol%, even more preferably 50 to 100 mol%, and particularly preferably 70 to 100 mol%. and particularly preferably 90 to 100 mol %.
・式(Y)で表される構成単位
ArY1で表されるアリーレン基は、本開示の発光素子の駆動電圧がより低くなるので、好ましくは、単環式又は2環式~6環式の芳香族炭化水素から、環を構成する原子に直接結合する水素原子2個を除いた基であり、より好ましくは、単環式、2環式又は3環式の芳香族炭化水素から、環を構成する原子に直接結合する水素原子2個を除いた基であり、更に好ましくは、ベンゼン、ナフタレン、アントラセン、フェナントレン、ジヒドロフェナントレン又はフルオレンから、環を構成する原子に直接結合する水素原子2個を除いた基であり、特に好ましくは、ベンゼン、フェナントレン、ジヒドロフェナントレン又はフルオレンから、環を構成する原子に直接結合する水素原子2個を除いた基であり、これらの基は置換基を有していてもよい。
ArY1で表される2価の複素環基は、本開示の発光素子の駆動電圧がより低くなるので、好ましくは、単環式又は2環式~6環式の複素環式化合物から、環を構成する原子に直接結合する水素原子2個を除いた基であり、より好ましくは、単環式、2環式又は3環式の複素環式化合物から、環を構成する原子に直接結合する水素原子2個を除いた基であり、更に好ましくは、ピリジン、ジアザベンゼン、トリアジン、アザナフタレン、ジアザナフタレン、カルバゾール、ジベンゾフラン、ジベンゾチオフェン、フェノキサジン、フェノチアジン、9,10-ジヒドロアクリジン又は5,10-ジヒドロフェナジンから、環を構成する原子(好ましくは炭素原子又は窒素原子、より好ましくは炭素原子)に直接結合する水素原子2個を除いた基であり、特に好ましくは、ピリジン、ジアザベンゼン、トリアジン、カルバゾール、ジベンゾフラン、ジベンゾチオフェン、フェノキサジン又はフェノチアジンから、環を構成する原子(好ましくは炭素原子又は窒素原子、より好ましくは炭素原子)に直接結合する水素原子2個を除いた基であり、これらの基は置換基を有していてもよい。
ArY1で表される少なくとも1種のアリーレン基と少なくとも1種の2価の複素環基とが直接結合した2価の基における、アリーレン基及び2価の複素環基の好ましい範囲は、それぞれ、ArY1で表されるアリーレン基及び2価の複素環基の好ましい範囲と同じである。
The arylene group represented by the structural unit Ar Y1 represented by the formula (Y) is preferably monocyclic or bicyclic to hexacyclic because the driving voltage of the light-emitting device of the present disclosure is lower. A group obtained by removing two hydrogen atoms directly bonded to atoms constituting a ring from an aromatic hydrocarbon, more preferably a monocyclic, bicyclic or tricyclic aromatic hydrocarbon, A group in which two hydrogen atoms directly bonded to the constituent atoms are removed, more preferably benzene, naphthalene, anthracene, phenanthrene, dihydrophenanthrene or fluorene, and two hydrogen atoms directly bonded to the ring-constituting atoms are removed. is a group from which benzene, phenanthrene, dihydrophenanthrene or fluorene is removed, and particularly preferably a group from which two hydrogen atoms directly bonded to atoms constituting the ring are removed from benzene, phenanthrene, dihydrophenanthrene or fluorene; may
The divalent heterocyclic group represented by Ar 2 Y1 is preferably selected from monocyclic or bicyclic to hexacyclic heterocyclic compounds, since the driving voltage of the light-emitting device of the present disclosure is lower. is a group excluding two hydrogen atoms that are directly bonded to the atoms that constitute a group with two hydrogen atoms removed, more preferably pyridine, diazabenzene, triazine, azanaphthalene, diazanaphthalene, carbazole, dibenzofuran, dibenzothiophene, phenoxazine, phenothiazine, 9,10-dihydroacridine or 5,10 - A group obtained by removing two hydrogen atoms directly bonded to a ring-constituting atom (preferably a carbon atom or a nitrogen atom, more preferably a carbon atom) from dihydrophenazine, particularly preferably pyridine, diazabenzene, triazine, A group obtained by removing two hydrogen atoms directly bonded to a ring-constituting atom (preferably a carbon atom or a nitrogen atom, more preferably a carbon atom) from carbazole, dibenzofuran, dibenzothiophene, phenoxazine or phenothiazine, and The group may have a substituent.
In the divalent group in which at least one arylene group and at least one divalent heterocyclic group represented by Ar Y1 are directly bonded, the preferred ranges of the arylene group and the divalent heterocyclic group are, respectively, It is the same as the preferred range of the arylene group and divalent heterocyclic group represented by Ar Y1 .
ArY1において、「少なくとも1種のアリーレン基と少なくとも1種の2価の複素環基とが直接結合した2価の基」としては、例えば、下記式で表される基が挙げられ、これらの基は置換基を有していてもよい。 In Ar Y1 , the "divalent group in which at least one arylene group and at least one divalent heterocyclic group are directly bonded" includes, for example, groups represented by the following formulae, The group may have a substituent.
ArY1は、本開示の発光素子の駆動電圧がより低くなるので、置換基を有していてもよいアリーレン基であることが好ましい。 Ar 2 Y1 is preferably an optionally substituted arylene group because the driving voltage of the light-emitting device of the present disclosure is lower.
ArY1で表される基が有してもよい置換基は、好ましくは、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基、アリールオキシ基、1価の複素環基、置換アミノ基又はフッ素原子であり、より好ましくは、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基、1価の複素環基又は置換アミノ基であり、更に好ましくは、アルキル基、シクロアルキル基、アリール基、1価の複素環基又は置換アミノ基であり、特に好ましくは、アルキル基、シクロアルキル基又はアリール基であり、これらの基は更に置換基を有していてもよい。
ArY1で表される基が有してもよい置換基におけるアリール基は、本開示の発光素子の駆動電圧がより低くなるので、好ましくは、単環式又は2環式~6環式の芳香族炭化水素から、環を構成する原子に直接結合する水素原子1個を除いた基であり、より好ましくは、単環式、2環式又は3環式の芳香族炭化水素から、環を構成する原子に直接結合する水素原子1個を除いた基であり、更に好ましくは、ベンゼン、ナフタレン、アントラセン、フェナントレン、ジヒドロフェナントレン又はフルオレンから、環を構成する原子に直接結合する水素原子1個を除いた基であり、特に好ましくは、ベンゼン、フェナントレン、ジヒドロフェナントレン又はフルオレンから、環を構成する原子に直接結合する水素原子1個を除いた基であり、これらの基は更に置換基を有していてもよい。
ArY1で表される基が有してもよい置換基における1価の複素環基は、本開示の発光素子の駆動電圧がより低くなるので、好ましくは、単環式又は2環式~6環式の複素環式化合物から、環を構成する原子に直接結合する水素原子1個を除いた基であり、より好ましくは、単環式、2環式又は3環式の複素環式化合物から、環を構成する原子に直接結合する水素原子1個を除いた基であり、更に好ましくは、ピリジン、ジアザベンゼン、トリアジン、アザナフタレン、ジアザナフタレン、カルバゾール、ジベンゾフラン、ジベンゾチオフェン、フェノキサジン、フェノチアジン、9,10-ジヒドロアクリジン又は5,10-ジヒドロフェナジンから、環を構成する原子(好ましくは炭素原子又は窒素原子)に直接結合する水素原子1個を除いた基であり、特に好ましくは、ピリジン、ジアザベンゼン、トリアジン、カルバゾール、ジベンゾフラン、ジベンゾチオフェン、フェノキサジン又はフェノチアジンから、環を構成する原子(好ましくは炭素原子又は窒素原子)に直接結合する水素原子1個を除いた基であり、これらの基は更に置換基を有していてもよい。
ArY1で表される基が有してもよい置換基における置換アミノ基において、アミノ基が有する置換基としては、アリール基又は1価の複素環基が好ましく、アリール基がより好ましく、これらの基は更に置換基を有していてもよい。アミノ基が有する置換基におけるアリール基及び1価の複素環基の例及び好ましい範囲は、それぞれ、ArY1で表される基が有してもよい置換基におけるアリール基及び1価の複素環基の例及び好ましい範囲と同じである。
The substituent that the group represented by Ar Y1 may have is preferably an alkyl group, a cycloalkyl group, an alkoxy group, a cycloalkoxy group, an aryl group, an aryloxy group, a monovalent heterocyclic group, a substituted amino or a fluorine atom, more preferably an alkyl group, a cycloalkyl group, an alkoxy group, a cycloalkoxy group, an aryl group, a monovalent heterocyclic group or a substituted amino group, still more preferably an alkyl group or a cycloalkyl A group, an aryl group, a monovalent heterocyclic group or a substituted amino group, particularly preferably an alkyl group, a cycloalkyl group or an aryl group, and these groups may further have a substituent.
The aryl group in the substituent that the group represented by Ar Y1 may have is preferably a monocyclic or bicyclic to hexacyclic aromatic group because the driving voltage of the light-emitting element of the present disclosure is lower. a group obtained by removing one hydrogen atom directly bonded to an atom constituting a ring from a group hydrocarbon, more preferably a monocyclic, bicyclic or tricyclic aromatic hydrocarbon more preferably benzene, naphthalene, anthracene, phenanthrene, dihydrophenanthrene or fluorene, excluding one hydrogen atom directly bonded to a ring-constituting atom. and particularly preferably a group obtained by removing one hydrogen atom directly bonded to a ring-constituting atom from benzene, phenanthrene, dihydrophenanthrene or fluorene, and these groups further have a substituent. may
The monovalent heterocyclic group in the substituent that the group represented by Ar Y1 may have is preferably monocyclic or bicyclic to 6 A group obtained by removing one hydrogen atom directly bonded to an atom constituting a ring from a cyclic heterocyclic compound, more preferably a monocyclic, bicyclic or tricyclic heterocyclic compound , a group in which one hydrogen atom directly bonded to a ring-constituting atom is removed, more preferably pyridine, diazabenzene, triazine, azanaphthalene, diazanaphthalene, carbazole, dibenzofuran, dibenzothiophene, phenoxazine, phenothiazine, 9,10-dihydroacridine or 5,10-dihydrophenazine, excluding one hydrogen atom directly bonded to an atom (preferably a carbon atom or a nitrogen atom) constituting a ring, particularly preferably pyridine, diazabenzene, triazine, carbazole, dibenzofuran, dibenzothiophene, phenoxazine or phenothiazine, with one hydrogen atom directly bonded to a ring-constituting atom (preferably a carbon atom or a nitrogen atom) removed, and these groups are Furthermore, it may have a substituent.
In the substituted amino group in the substituent that may be possessed by the group represented by Ar Y1 , the substituent possessed by the amino group is preferably an aryl group or a monovalent heterocyclic group, more preferably an aryl group. The group may further have a substituent. Examples and preferred ranges of the aryl group and monovalent heterocyclic group in the substituent of the amino group are the aryl group and monovalent heterocyclic group in the substituent that the group represented by Ar Y1 may have, respectively. is the same as the example and preferred range of
ArY1で表される基が有してもよい置換基が更に有していてもよい置換基としては、好ましくは、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基、アリールオキシ基、1価の複素環基、置換アミノ基又はフッ素原子であり、より好ましくは、アルキル基、シクロアルキル基、アリール基、1価の複素環基又は置換アミノ基であり、更に好ましくは、アルキル基、シクロアルキル基又はアリール基であり、特に好ましくは、アルキル基又はシクロアルキル基であり、これらの基は更に置換基を有していてもよいが、更に置換基を有さないことが好ましい。
ArY1で表される基が有してもよい置換基が更に有していてもよい置換基におけるアリール基、1価の複素環基及び置換アミノ基の例及び好ましい範囲は、それぞれ、ArY1で表される基が有してもよい置換基におけるアリール基、1価の複素環基及び置換アミノ基の例及び好ましい範囲と同じである。
The substituent that the group represented by Ar Y1 may further have preferably has an alkyl group, a cycloalkyl group, an alkoxy group, a cycloalkoxy group, an aryl group, an aryloxy group, monovalent heterocyclic group, substituted amino group or fluorine atom, more preferably alkyl group, cycloalkyl group, aryl group, monovalent heterocyclic group or substituted amino group, still more preferably alkyl group, a cycloalkyl group or an aryl group, particularly preferably an alkyl group or a cycloalkyl group. These groups may further have a substituent, but preferably have no further substituent. .
Examples and preferred ranges of the aryl group, monovalent heterocyclic group and substituted amino group in the substituent that the group represented by Ar Y1 may further have are Ar Y1 are the same as the examples and preferred ranges of the aryl group, monovalent heterocyclic group and substituted amino group in the substituents that the group may have.
式(Y)で表される構成単位は、本開示の発光素子の駆動電圧がより低くなるので、好ましくは、式(Y-1)又は式(Y-2)で表される構成単位である。 The structural unit represented by formula (Y) is preferably a structural unit represented by formula (Y-1) or formula (Y-2) because the driving voltage of the light-emitting device of the present disclosure is lower. .
[式中、
RY1は、水素原子、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基、アリールオキシ基、1価の複素環基、置換アミノ基又はフッ素原子を表し、これらの基は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。複数存在するRY1は、同一でも異なっていてもよく、互いに結合して、それぞれが結合する炭素原子とともに環を形成していてもよい。
XY1は、-C(RY2)2-、-C(RY2)=C(RY2)-又は-C(RY2)2-C(RY2)2-で表される基を表す。RY2は、水素原子、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基、アリールオキシ基、1価の複素環基、置換アミノ基又はフッ素原子を表し、これらの基は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。複数存在するRY2は、同一でも異なっていてもよく、互いに結合して、それぞれが結合する炭素原子とともに環を形成していてもよい。]
[In the formula,
R Y1 represents a hydrogen atom, an alkyl group, a cycloalkyl group, an alkoxy group, a cycloalkoxy group, an aryl group, an aryloxy group, a monovalent heterocyclic group, a substituted amino group or a fluorine atom, and these groups are substituents may have When there are multiple such substituents, they may be the same or different, and may be bonded to each other to form a ring together with the atoms to which they are bonded. A plurality of R Y1 may be the same or different, and may be bonded to each other to form a ring together with the carbon atoms to which they are bonded.
X Y1 represents a group represented by -C(R Y2 ) 2 -, -C(R Y2 )=C(R Y2 )- or -C(R Y2 ) 2 -C(R Y2 ) 2 -. R Y2 represents a hydrogen atom, an alkyl group, a cycloalkyl group, an alkoxy group, a cycloalkoxy group, an aryl group, an aryloxy group, a monovalent heterocyclic group, a substituted amino group or a fluorine atom, and these groups are substituents may have When there are multiple such substituents, they may be the same or different, and may be bonded to each other to form a ring together with the atoms to which they are bonded. A plurality of RY2 may be the same or different, and may be bonded to each other to form a ring together with the carbon atoms to which they are bonded. ]
RY1は、好ましくは、水素原子、アルキル基、シクロアルキル基、アリール基、1価の複素環基又は置換アミノ基であり、より好ましくは、水素原子、アルキル基、シクロアルキル基又はアリール基であり、更に好ましくは、水素原子又はアルキル基であり、これらの基は置換基を有していてもよい。 R Y1 is preferably a hydrogen atom, an alkyl group, a cycloalkyl group, an aryl group, a monovalent heterocyclic group or a substituted amino group, more preferably a hydrogen atom, an alkyl group, a cycloalkyl group or an aryl group. more preferably a hydrogen atom or an alkyl group, and these groups may have a substituent.
式(Y-1)において、RY1の少なくとも1つは(好ましくは、RY1の少なくとも2つは)、本開示の発光素子の駆動電圧がより低くなるので、好ましくは、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基、アリールオキシ基、1価の複素環基、置換アミノ基又はフッ素原子であり、より好ましくは、アルキル基、シクロアルキル基、アリール基、1価の複素環基又は置換アミノ基であり、更に好ましくは、アルキル基、シクロアルキル基又はアリール基であり、特に好ましくは、アルキル基であり、これらの基は置換基を有していてもよい。 In formula (Y-1), at least one of R 1 Y1 (preferably at least two of R 1 Y1 ) is preferably an alkyl group, a cycloalkyl group, alkoxy group, cycloalkoxy group, aryl group, aryloxy group, monovalent heterocyclic group, substituted amino group or fluorine atom, more preferably alkyl group, cycloalkyl group, aryl group, monovalent heterocyclic group It is a cyclic group or a substituted amino group, more preferably an alkyl group, a cycloalkyl group or an aryl group, particularly preferably an alkyl group, and these groups may have a substituent.
RY2は、本開示の発光素子の駆動電圧がより低くなるので、好ましくは、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基、1価の複素環基又は置換アミノ基であり、より好ましくは、アルキル基、シクロアルキル基、アリール基又は1価の複素環基であり、更に好ましくは、アルキル基、シクロアルキル基又はアリール基であり、これらの基は置換基を有していてもよい。 R Y2 is preferably an alkyl group, a cycloalkyl group, an alkoxy group, a cycloalkoxy group, an aryl group, a monovalent heterocyclic group, or a substituted amino group, since the driving voltage of the light emitting device of the present disclosure is lower. , more preferably an alkyl group, a cycloalkyl group, an aryl group or a monovalent heterocyclic group, more preferably an alkyl group, a cycloalkyl group or an aryl group, and these groups have substituents. may
RY1及びRY2におけるアリール基、1価の複素環基及び置換アミノ基の例及び好ましい範囲は、それぞれ、ArY1で表される基が有してもよい置換基におけるアリール基、1価の複素環基及び置換アミノ基の例及び好ましい範囲と同じである。
RY1及びRY2が有していてもよい置換基の例及び好ましい範囲は、ArY1で表される基が有してもよい置換基の例及び好ましい範囲と同じである。
Examples and preferred ranges of the aryl group, monovalent heterocyclic group and substituted amino group for R Y1 and R Y2 are, respectively, the aryl group and the monovalent It is the same as the examples and preferred ranges of the heterocyclic group and the substituted amino group.
Examples and preferred ranges of substituents that R Y1 and R Y2 may have are the same as examples and preferred ranges of substituents that the group represented by Ar Y1 may have.
XY1は、本開示の発光素子の駆動電圧がより低くなるので、好ましくは、-C(RY2)2-又は-C(RY2)2-C(RY2)2-で表される基であり、より好ましくは、-C(RY2)2-で表される基である。 X Y1 is preferably a group represented by -C(R Y2 ) 2 - or -C(R Y2 ) 2 -C(R Y2 ) 2 -, since the driving voltage of the light-emitting element of the present disclosure is lower. and more preferably a group represented by —C(R Y2 ) 2 —.
式(Y)で表される構成単位としては、例えば、式(Y-101)~式(Y-141)で表される少なくとも1種のアリーレン基からなる構成単位、式(Y-201)~式(Y-209)で表される少なくとも1種の2価の複素環基からなる構成単位、式(Y-301)~式(Y-306)で表される少なくとも1種のアリーレン基と少なくとも1種の2価の複素環基とが直接結合した2価の基からなる構成単位が挙げられる。 Examples of structural units represented by formula (Y) include structural units comprising at least one arylene group represented by formulas (Y-101) to (Y-141), formulas (Y-201) to A structural unit consisting of at least one divalent heterocyclic group represented by formula (Y-209), at least one arylene group represented by formulas (Y-301) to (Y-306) and at least Structural units composed of a divalent group directly bonded to one type of divalent heterocyclic group can be mentioned.
・式(X)で表される構成単位
aX1及びaX2は、通常0~10の整数であり、本開示の発光素子の駆動電圧がより低くなるので、好ましくは0~5の整数であり、より好ましくは0~3の整数であり、更に好ましくは0~2の整数であり、特に好ましくは0又は1である。
Structural units a X1 and a X2 represented by formula (X) are usually integers of 0 to 10, and are preferably integers of 0 to 5 because the driving voltage of the light-emitting device of the present disclosure is lower. , more preferably an integer of 0 to 3, more preferably an integer of 0 to 2, and particularly preferably 0 or 1.
RX1、RX2及びRX3は、本開示の発光素子の駆動電圧がより低くなるので、好ましくはアルキル基、シクロアルキル基、アリール基又は1価の複素環基であり、より好ましくはアリール基又は1価の複素環基であり、更に好ましくはアリール基であり、これらの基は置換基を有していてもよい。
RX1、RX2及びRX3におけるアリール基及び1価の複素環基の例及び好ましい範囲は、それぞれ、ArY1で表される基が有してもよい置換基におけるアリール基及び1価の複素環基の例及び好ましい範囲と同じである。
R X1 , R X2 and R X3 are preferably an alkyl group, a cycloalkyl group, an aryl group or a monovalent heterocyclic group, more preferably an aryl group, because the driving voltage of the light-emitting device of the present disclosure is lower. or a monovalent heterocyclic group, more preferably an aryl group, and these groups may have a substituent.
Examples and preferred ranges of the aryl group and the monovalent heterocyclic group in R X1 , R X2 and R X3 are, respectively, the aryl group and the monovalent heterocyclic group in the substituent that the group represented by Ar Y1 may have. It is the same as the example and preferred range of the cyclic group.
ArX1、ArX2、ArX3及びArX4は、本開示の発光素子の駆動電圧がより低くなるので、好ましくは置換基を有していてもよいアリーレン基である。
ArX1、ArX2、ArX3及びArX4におけるアリーレン基及び2価の複素環基の例及び好ましい範囲は、それぞれ、ArY1におけるアリーレン基及び2価の複素環基の例及び好ましい範囲と同じである。
ArX2及びArX4で表される少なくとも1種のアリーレン基と少なくとも1種の2価の複素環基とが直接結合した2価の基における、アリーレン基及び2価の複素環基の例及び好ましい範囲は、それぞれ、ArY1におけるアリーレン基及び2価の複素環基の例及び好ましい範囲と同じである。
ArX2及びArX4における少なくとも1種のアリーレン基と少なくとも1種の2価の複素環基とが直接結合した2価の基としては、ArY1における少なくとも1種のアリーレン基と少なくとも1種の2価の複素環基とが直接結合した2価の基と同様のものが挙げられる。
Ar X1 , Ar X2 , Ar X3 and Ar X4 are preferably arylene groups optionally having substituents, since the driving voltage of the light-emitting device of the present disclosure becomes lower.
Examples and preferred ranges of the arylene group and divalent heterocyclic group for Ar X1 , Ar X2 , Ar X3 and Ar X4 are the same as the examples and preferred ranges of the arylene group and divalent heterocyclic group for Ar Y1 respectively. be.
Examples and preferred arylene groups and divalent heterocyclic groups in the divalent group in which at least one arylene group and at least one divalent heterocyclic group represented by Ar X2 and Ar X4 are directly bonded The ranges are the same as the examples and preferred ranges of the arylene group and the divalent heterocyclic group in Ar Y1 , respectively.
The divalent group in which at least one arylene group and at least one divalent heterocyclic group in Ar X2 and Ar X4 are directly bonded includes at least one arylene group and at least one divalent heterocyclic group in Ar Y1 . Examples thereof include the same divalent groups to which a valent heterocyclic group is directly bonded.
ArX1~ArX4及びRX1~RX3で表される基が有してもよい置換基の例及び好ましい範囲は、ArY1で表される基が有してもよい置換基の例及び好ましい範囲と同じである。 Examples and preferred ranges of the substituents that the groups represented by Ar X1 to Ar X4 and R X1 to R X3 may have are the examples and preferred ranges of the substituents that the group represented by Ar Y1 may have. Same as range.
式(X)で表される構成単位としては、下記式で表される構成単位が挙げられる。 Examples of structural units represented by formula (X) include structural units represented by the following formulas.
第1の高分子化合物としては、例えば、高分子化合物HP-1~HP-3が挙げられる。 Examples of the first polymer compound include polymer compounds HP-1 to HP-3.
[表中、p、q及びrは、各構成単位のモル比率(モル%)を示す。p+q+r=100であり、且つ、100≧p+q≧70である。その他の構成単位とは、式(Y)で表される構成単位及び式(X)で表される構成単位以外の構成単位を意味する。] [In the table, p, q and r indicate the molar ratio (mol %) of each structural unit. p+q+r=100 and 100≧p+q≧70. Other structural units mean structural units other than the structural units represented by the formula (Y) and the structural units represented by the formula (X). ]
第1の高分子化合物は、ブロック共重合体、ランダム共重合体、交互共重合体、グラフト共重合体のいずれであってもよいし、その他の態様であってもよいが、複数種の原料モノマーを共重合した共重合体であることが好ましい。
第1の高分子化合物のポリスチレン換算の数平均分子量は、好ましくは5×103~1×106であり、より好ましくは1×104~5×105であり、更に好ましくは2×104~2×105である。第1の高分子化合物のポリスチレン換算の重量平均分子量は、好ましくは1×104~2×106であり、より好ましくは2×104~1×106であり、更に好ましくは5×104~5×105である。
The first polymer compound may be a block copolymer, a random copolymer, an alternating copolymer, or a graft copolymer. It is preferably a copolymer obtained by copolymerizing monomers.
The polystyrene equivalent number average molecular weight of the first polymer compound is preferably 5×10 3 to 1×10 6 , more preferably 1×10 4 to 5×10 5 , still more preferably 2×10 4 to 2×10 5 . The polystyrene equivalent weight average molecular weight of the first polymer compound is preferably 1×10 4 to 2×10 6 , more preferably 2×10 4 to 1×10 6 , still more preferably 5×10 4 to 5×10 5 .
(第1の高分子化合物の製造方法)
第1の高分子化合物は、ケミカルレビュー(Chem. Rev.),第109巻,897-1091頁(2009年)等に記載の公知の重合方法を用いて製造することができ、Suzuki反応、Yamamoto反応、Buchwald反応、Stille反応、Negishi反応及びKumada反応等の遷移金属触媒を用いるカップリング反応により重合させる方法が例示される。
上記重合方法において、単量体を仕込む方法としては、単量体全量を反応系に一括して仕込む方法、単量体の一部を仕込んで反応させた後、残りの単量体を一括、連続又は分割して仕込む方法、単量体を連続又は分割して仕込む方法等が挙げられる。
遷移金属触媒としては、パラジウム触媒、ニッケル触媒等が挙げられる。
重合反応の後処理は、公知の方法、例えば、分液により水溶性不純物を除去する方法、メタノール等の低級アルコールに重合反応後の反応液を加えて、析出させた沈殿を濾過した後、乾燥させる方法等を単独又は組み合わせて行う。第1の高分子化合物の純度が低い場合、例えば、再結晶、再沈殿、ソックスレー抽出器による連続抽出、カラムクロマトグラフィー等の通常の方法にて精製することができる。
(Method for producing first polymer compound)
The first polymer compound can be produced using a known polymerization method described in Chemical Review (Chem. Rev.), Vol. 109, pp. 897-1091 (2009), Suzuki reaction, Yamamoto , Buchwald reaction, Stille reaction, Negishi reaction, Kumada reaction, and other coupling reactions using a transition metal catalyst.
In the above polymerization method, the method of charging the monomers includes a method of charging the entire amount of the monomers into the reaction system at once, a method of charging a part of the monomers and reacting them, and then charging the remaining monomers all at once. Examples thereof include a method of continuously or dividedly charging, a method of continuously or dividingly charging a monomer, and the like.
Examples of transition metal catalysts include palladium catalysts and nickel catalysts.
The post-treatment of the polymerization reaction is performed by a known method, for example, a method of removing water-soluble impurities by liquid separation, adding the reaction solution after the polymerization reaction to a lower alcohol such as methanol, filtering the deposited precipitate, and drying it. method, etc., is performed singly or in combination. When the purity of the first polymer compound is low, it can be purified by ordinary methods such as recrystallization, reprecipitation, continuous extraction using a Soxhlet extractor, and column chromatography.
[その他の成分]
本開示の組成物は、化合物(A)と、化合物(B)と、第1の化合物と、正孔輸送材料、正孔注入材料、電子輸送材料、電子注入材料、発光材料、酸化防止剤及び溶媒からなる群より選ばれる少なくとも1種とを含有する組成物であってもよい。但し、正孔輸送材料、正孔注入材料、電子輸送材料、電子注入材料及び発光材料は、化合物(A)、化合物(B)及び第1の化合物とは異なる。
[Other ingredients]
The composition of the present disclosure comprises a compound (A), a compound (B), a first compound, a hole-transporting material, a hole-injecting material, an electron-transporting material, an electron-injecting material, a light-emitting material, an antioxidant and It may be a composition containing at least one selected from the group consisting of solvents. However, the hole-transporting material, hole-injecting material, electron-transporting material, electron-injecting material, and light-emitting material are different from the compound (A), the compound (B), and the first compound.
化合物(A)と、化合物(B)と、第1の化合物と、溶媒とを含有する組成物(以下、「インク」と言う。)は、例えば、スピンコート法、キャスティング法、マイクログラビアコート法、グラビアコート法、バーコート法、ロールコート法、ワイヤーバーコート法、ディップコート法、スプレーコート法、スクリーン印刷法、フレキソ印刷法、オフセット印刷法、インクジェット印刷法、キャピラリ-コート法、ノズルコート法等を用いた発光素子の作製に好適である。
インクの粘度は、印刷法の種類によって調整すればよいが、インクジェットプリント法等の溶液が吐出装置を経由する印刷法に適用する場合には、吐出時の目づまりと飛行曲がりを防止するために、好ましくは25℃において1mPa・s~20mPa・sである。
A composition containing the compound (A), the compound (B), the first compound, and a solvent (hereinafter referred to as "ink") can be prepared by, for example, a spin coating method, a casting method, or a microgravure coating method. , gravure coating method, bar coating method, roll coating method, wire bar coating method, dip coating method, spray coating method, screen printing method, flexographic printing method, offset printing method, inkjet printing method, capillary coating method, nozzle coating method It is suitable for fabricating a light-emitting device using, for example.
The viscosity of the ink may be adjusted depending on the type of printing method, but when applying to a printing method such as an inkjet printing method in which a solution passes through an ejection device, it is necessary to prevent clogging and flight deflection during ejection. , preferably 1 mPa·s to 20 mPa·s at 25°C.
インクに含まれる溶媒は、該インク中の固形分を溶解又は均一に分散できる溶媒が好ましい。溶媒としては、例えば、1,2-ジクロロエタン、1,1,2-トリクロロエタン、クロロベンゼン、o-ジクロロベンゼン等の塩素系溶媒;テトラヒドロフラン、ジオキサン、アニソール、4-メチルアニソール等のエーテル系溶媒;トルエン、キシレン、メシチレン、エチルベンゼン、n-ヘキシルベンゼン、シクロヘキシルベンゼン等の芳香族炭化水素系溶媒;シクロヘキサン、メチルシクロヘキサン、n-ペンタン、n-ヘキサン、n-へプタン、n-オクタン、n-ノナン、n-デカン、n-ドデカン、ビシクロヘキシル等の脂肪族炭化水素系溶媒;アセトン、メチルエチルケトン、シクロヘキサノン、アセトフェノン等のケトン系溶媒;酢酸エチル、酢酸ブチル、エチルセルソルブアセテート、安息香酸メチル、酢酸フェニル等のエステル系溶媒;エチレングリコール、グリセリン、1,2-ヘキサンジオール等の多価アルコール系溶媒;イソプロピルアルコール、シクロヘキサノール等のアルコール系溶媒;ジメチルスルホキシド等のスルホキシド系溶媒;N-メチル-2-ピロリドン、N,N-ジメチルホルムアミド等のアミド系溶媒が挙げられる。溶媒は、一種単独で用いても二種以上を併用してもよい。 The solvent contained in the ink is preferably a solvent capable of dissolving or uniformly dispersing the solid content in the ink. Examples of solvents include chlorine solvents such as 1,2-dichloroethane, 1,1,2-trichloroethane, chlorobenzene and o-dichlorobenzene; ether solvents such as tetrahydrofuran, dioxane, anisole and 4-methylanisole; Aromatic hydrocarbon solvents such as xylene, mesitylene, ethylbenzene, n-hexylbenzene, cyclohexylbenzene; cyclohexane, methylcyclohexane, n-pentane, n-hexane, n-heptane, n-octane, n-nonane, n- Aliphatic hydrocarbon solvents such as decane, n-dodecane and bicyclohexyl; ketone solvents such as acetone, methyl ethyl ketone, cyclohexanone and acetophenone; esters such as ethyl acetate, butyl acetate, ethyl cellosolve acetate, methyl benzoate and phenyl acetate. polyhydric alcohol solvents such as ethylene glycol, glycerin, and 1,2-hexanediol; alcohol solvents such as isopropyl alcohol and cyclohexanol; sulfoxide solvents such as dimethyl sulfoxide; N-methyl-2-pyrrolidone, N , and N-dimethylformamide. A solvent may be used individually by 1 type, or may use 2 or more types together.
インクにおいて、溶媒の含有量は、化合物(A)と化合物(B)と第1の化合物との合計の含有量を100質量部とした場合、通常、1000質量部~1000000質量部である。 In the ink, the content of the solvent is usually 1000 parts by mass to 1000000 parts by mass when the total content of the compound (A), the compound (B) and the first compound is 100 parts by mass.
(正孔輸送材料)
正孔輸送材料は、低分子化合物と高分子化合物とに分類される。正孔輸送材料は、架橋基を有していてもよい。
低分子化合物としては、例えば、トリフェニルアミン及びその誘導体、N,N’-ジ-1-ナフチル-N,N’-ジフェニルベンジジン(α-NPD)、並びに、N,N’-ジフェニル-N,N’-ジ(m-トリル)ベンジジン(TPD)等の芳香族アミン化合物が挙げられる。
高分子化合物としては、例えば、ポリビニルカルバゾール及びその誘導体;側鎖又は主鎖に芳香族アミン構造を有するポリアリーレン及びその誘導体が挙げられる。高分子化合物は、フラーレン、テトラフルオロテトラシアノキノジメタン、テトラシアノエチレン及びトリニトロフルオレノン等の電子受容性部位が結合された化合物でもよい。
本開示の組成物の一実施形態において、正孔輸送材料が含まれる場合、正孔輸送材料の含有量は、化合物(A)と化合物(B)と第1の化合物との合計の含有量を100質量部とした場合、通常、1~1000質量部である。
正孔輸送材料は、一種単独で用いても二種以上を併用してもよい。
(Hole transport material)
Hole-transporting materials are classified into low-molecular-weight compounds and high-molecular-weight compounds. The hole-transporting material may have a cross-linking group.
Examples of low-molecular-weight compounds include triphenylamine and its derivatives, N,N'-di-1-naphthyl-N,N'-diphenylbenzidine (α-NPD), and N,N'-diphenyl-N, Aromatic amine compounds such as N'-di(m-tolyl)benzidine (TPD) can be mentioned.
Polymer compounds include, for example, polyvinylcarbazole and derivatives thereof; polyarylenes and derivatives thereof having aromatic amine structures in side chains or main chains. The polymer compound may be a compound having electron-accepting moieties such as fullerene, tetrafluorotetracyanoquinodimethane, tetracyanoethylene and trinitrofluorenone bound thereto.
In one embodiment of the composition of the present disclosure, when a hole-transporting material is included, the content of the hole-transporting material is the total content of the compound (A), the compound (B), and the first compound. When 100 parts by mass, it is usually 1 to 1000 parts by mass.
The hole transport materials may be used singly or in combination of two or more.
(電子輸送材料)
電子輸送材料は、低分子化合物と高分子化合物とに分類される。電子輸送材料は、架橋基を有していてもよい。
低分子化合物としては、例えば、8-ヒドロキシキノリンを配位子とする金属錯体、オキサジアゾール、アントラキノジメタン、ベンゾキノン、ナフトキノン、アントラキノン、テトラシアノアントラキノジメタン、フルオレノン、ジフェニルジシアノエチレン及びジフェノキノン、並びに、これらの誘導体が挙げられる。
高分子化合物としては、例えば、ポリフェニレン、ポリフルオレン、及び、これらの誘導体が挙げられる。高分子化合物は、金属でドープされていてもよい。
本開示の組成物の一実施形態において、電子輸送材料が含まれる場合、電子輸送材料の含有量は、化合物(A)と化合物(B)と第1の化合物との合計の含有量を100質量部とした場合、通常、1~1000質量部である。
電子輸送材料は、一種単独で用いても二種以上を併用してもよい。
(Electron transport material)
Electron transport materials are classified into low-molecular-weight compounds and high-molecular-weight compounds. The electron transport material may have a cross-linking group.
Examples of low-molecular-weight compounds include metal complexes having 8-hydroxyquinoline as a ligand, oxadiazole, anthraquinodimethane, benzoquinone, naphthoquinone, anthraquinone, tetracyanoanthraquinodimethane, fluorenone, diphenyldicyanoethylene and diphenoquinone. , as well as derivatives thereof.
Polymer compounds include, for example, polyphenylene, polyfluorene, and derivatives thereof. The polymeric compounds may be doped with metals.
In one embodiment of the composition of the present disclosure, when an electron-transporting material is included, the content of the electron-transporting material is the total content of the compound (A), the compound (B), and the first compound, which is 100 mass When expressed as parts, it is usually 1 to 1000 parts by mass.
The electron transport materials may be used singly or in combination of two or more.
(正孔注入材料及び電子注入材料)
正孔注入材料及び電子注入材料は、各々、低分子化合物と高分子化合物とに分類される。正孔注入材料及び電子注入材料は、架橋基を有していてもよい。
低分子化合物としては、例えば、銅フタロシアニン等の金属フタロシアニン;カーボン;モリブデン、タングステン等の金属酸化物;フッ化リチウム、フッ化ナトリウム、フッ化セシウム、フッ化カリウム等の金属フッ化物が挙げられる。
高分子化合物としては、例えば、ポリアニリン、ポリチオフェン、ポリピロール、ポリフェニレンビニレン、ポリチエニレンビニレン、ポリキノリン及びポリキノキサリン、並びに、これらの誘導体;芳香族アミン構造を主鎖又は側鎖に含む重合体等の導電性高分子が挙げられる。
本開示の組成物の一実施形態において、正孔注入材料及び/又は電子注入材料が含まれる場合、正孔注入材料及び電子注入材料の含有量は、各々、化合物(A)と化合物(B)と第1の化合物との合計の含有量を100質量部とした場合、通常、1~1000質量部である。
正孔注入材料及び電子注入材料は、各々、一種単独で用いても二種以上を併用してもよい。
(Hole injection material and electron injection material)
Hole-injecting materials and electron-injecting materials are classified into low-molecular-weight compounds and high-molecular-weight compounds, respectively. The hole-injecting material and the electron-injecting material may have cross-linking groups.
Examples of low-molecular compounds include metal phthalocyanines such as copper phthalocyanine; carbon; metal oxides such as molybdenum and tungsten; and metal fluorides such as lithium fluoride, sodium fluoride, cesium fluoride and potassium fluoride.
Polymer compounds include, for example, polyaniline, polythiophene, polypyrrole, polyphenylene vinylene, polythienylene vinylene, polyquinoline and polyquinoxaline, and derivatives thereof; conductive polymers such as polymers containing an aromatic amine structure in the main chain or side chain; and a flexible polymer.
In one embodiment of the composition of the present disclosure, when a hole-injection material and/or an electron-injection material is included, the content of the hole-injection material and the electron-injection material is, respectively, compound (A) and compound (B) When the total content of and the first compound is 100 parts by mass, it is usually 1 to 1000 parts by mass.
Each of the hole injection material and the electron injection material may be used alone or in combination of two or more.
・イオンドープ
正孔注入材料又は電子注入材料は、イオンがドープされていてもよい。例えば、正孔注入材料又は電子注入材料が導電性高分子を含む場合、導電性高分子の電気伝導度は、好ましくは1×10-5S/cm~1×103S/cmである。導電性高分子の電気伝導度をかかる範囲とするために、導電性高分子に適量のイオンをドープすることができる。
正孔注入材料又は電子注入材料にドープするイオンの種類は、例えば、正孔注入材料であればアニオンが挙げられ、電子注入材料であればカチオンが挙げられる。アニオンとしては、例えば、ポリスチレンスルホン酸イオン、アルキルベンゼンスルホン酸イオン及び樟脳スルホン酸イオンが挙げられる。カチオンとしては、例えば、リチウムイオン、ナトリウムイオン、カリウムイオン及びテトラブチルアンモニウムイオンが挙げられる。
ドープするイオンは、一種単独で用いても二種以上を併用してもよい。
- Ion doping The hole-injecting material or the electron-injecting material may be doped with ions. For example, if the hole-injecting material or electron-injecting material comprises a conductive polymer, the electrical conductivity of the conductive polymer is preferably between 1×10 −5 S/cm and 1×10 3 S/cm. The conductive polymer can be doped with an appropriate amount of ions in order to set the electrical conductivity of the conductive polymer within this range.
The type of ions to be doped into the hole injection material or the electron injection material is, for example, an anion for the hole injection material, and a cation for the electron injection material. Anions include, for example, polystyrene sulfonate, alkylbenzene sulfonate, and camphor sulfonate. Cations include, for example, lithium ion, sodium ion, potassium ion and tetrabutylammonium ion.
Ions for doping may be used alone or in combination of two or more.
(発光材料)
発光材料は、低分子化合物と高分子化合物とに分類される。発光材料は、架橋基を有していてもよい。
低分子化合物としては、例えば、ナフタレン及びその誘導体、アントラセン及びその誘導体、ペリレン及びその誘導体、並びに、イリジウム、白金又はユーロピウムを中心金属とする燐光発光性化合物が挙げられる。
高分子化合物としては、例えば、式(Y)で表される構成単位及び/又は式(X)で表される構成単位を含む高分子化合物が挙げられる。
(Luminous material)
Light-emitting materials are classified into low-molecular-weight compounds and high-molecular-weight compounds. The luminescent material may have a cross-linking group.
Examples of low-molecular-weight compounds include naphthalene and its derivatives, anthracene and its derivatives, perylene and its derivatives, and phosphorescent compounds having iridium, platinum, or europium as a central metal.
Examples of polymer compounds include polymer compounds containing structural units represented by formula (Y) and/or structural units represented by formula (X).
燐光発光性化合物としては、例えば、以下に示す金属錯体が挙げられる。 Examples of the phosphorescent compound include metal complexes shown below.
本開示の組成物の一実施形態において、発光材料が含まれる場合、発光材料の含有量は、化合物(A)と化合物(B)と第1の化合物との合計の含有量を100質量部とした場合、通常、1~1000質量部である。
発光材料は、一種単独で用いても二種以上を併用してもよい。
In one embodiment of the composition of the present disclosure, when a light-emitting material is included, the content of the light-emitting material is 100 parts by mass of the total content of the compound (A), the compound (B), and the first compound. When used, it is usually 1 to 1000 parts by mass.
A luminescent material may be used individually by 1 type, or may use 2 or more types together.
(酸化防止剤)
酸化防止剤は、化合物(A)、化合物(B)及び第1の化合物と同じ溶媒に可溶であり、発光及び電荷輸送を阻害しない化合物であればよく、例えば、フェノール系酸化防止剤、リン系酸化防止剤等が挙げられる。
本開示の組成物の一実施形態において、酸化防止剤が含まれる場合、酸化防止剤の含有量は、化合物(A)と化合物(B)と第1の化合物との合計の含有量を100質量部とした場合、通常、0.001~10質量部である。
酸化防止剤は、一種単独で用いても二種以上を併用してもよい。
(Antioxidant)
The antioxidant may be a compound that is soluble in the same solvent as the compound (A), the compound (B), and the first compound and does not inhibit light emission and charge transport. system antioxidants and the like.
In one embodiment of the composition of the present disclosure, when an antioxidant is included, the content of the antioxidant is the total content of the compound (A), the compound (B), and the first compound, which is 100 mass When expressed as parts, it is usually 0.001 to 10 parts by mass.
Antioxidants may be used singly or in combination of two or more.
<膜>
本開示の膜は、上述した本開示の組成物を含有する。
本開示の膜は、発光素子における発光層として好適である。本開示の膜は、例えば、インクを用いて、湿式法により作製することができる。また、本開示の膜は、例えば、真空蒸着法等の乾式法により作製することができる。本開示の膜を乾式法により作製する方法としては、例えば、上述の組成物を蒸着する方法、及び、化合物(A)、化合物(B)及び第1の化合物を共蒸着する方法が挙げられる。
膜の厚さは、通常、1nm~10μmである。
<Membrane>
The membranes of the present disclosure contain the compositions of the present disclosure described above.
The film of the present disclosure is suitable as a light-emitting layer in a light-emitting device. The membranes of the present disclosure can be made by wet methods, using inks, for example. In addition, the film of the present disclosure can be produced, for example, by a dry method such as a vacuum deposition method. Methods for producing the film of the present disclosure by a dry method include, for example, a method of vapor-depositing the composition described above and a method of co-depositing compound (A), compound (B), and the first compound.
The film thickness is typically between 1 nm and 10 μm.
<発光素子>
本開示の発光素子は、上述の組成物を含有する。
本開示の発光素子は、例えば、陽極と、陰極と、陽極及び陰極の間に設けられた上述の組成物を含有する有機層と、を備えるものであってよい。
<Light emitting element>
The light-emitting device of the present disclosure contains the composition described above.
A light-emitting device of the present disclosure may comprise, for example, an anode, a cathode, and an organic layer containing the composition described above provided between the anode and the cathode.
[層構成]
本開示の組成物を含有する層は、通常、発光層、正孔輸送層、正孔注入層、電子輸送層及び電子注入層からなる群から選ばれる1種以上の層であり、好ましくは、発光層である。これらの層は、各々、発光材料、正孔輸送材料、正孔注入材料、電子輸送材料、電子注入材料を含む。これらの層は、各々、発光材料、正孔輸送材料、正孔注入材料、電子輸送材料、電子注入材料を、上述した膜の作製と同様の方法を用いて形成することができる。
[Layer structure]
The layer containing the composition of the present disclosure is usually one or more layers selected from the group consisting of a light-emitting layer, a hole-transporting layer, a hole-injecting layer, an electron-transporting layer and an electron-injecting layer, preferably This is the light-emitting layer. These layers each contain a light-emitting material, a hole-transporting material, a hole-injecting material, an electron-transporting material, and an electron-injecting material. Each of these layers can be formed from a light-emitting material, a hole-transporting material, a hole-injecting material, an electron-transporting material, and an electron-injecting material using the same method as for the above-described films.
発光素子は、陽極と陰極の間に発光層を有する。本開示の発光素子は、正孔注入性及び正孔輸送性の観点からは、陽極と発光層との間に、正孔注入層及び正孔輸送層の少なくとも1層を有することが好ましく、電子注入性及び電子輸送性の観点からは、陰極と発光層の間に、電子注入層及び電子輸送層の少なくとも1層を有することが好ましい。 A light-emitting element has a light-emitting layer between an anode and a cathode. From the viewpoint of hole injection and hole transport properties, the light emitting device of the present disclosure preferably has at least one layer of a hole injection layer and a hole transport layer between the anode and the light emitting layer. From the viewpoint of injection properties and electron transport properties, it is preferable to have at least one layer of an electron injection layer and an electron transport layer between the cathode and the light emitting layer.
正孔輸送層、電子輸送層、発光層、正孔注入層及び電子注入層の材料としては、本開示の組成物の他、各々、上述した正孔輸送材料、電子輸送材料、発光材料、正孔注入材料及び電子注入材料等が挙げられる。 Materials for the hole-transporting layer, electron-transporting layer, light-emitting layer, hole-injecting layer, and electron-injecting layer include, in addition to the composition of the present disclosure, the hole-transporting material, electron-transporting material, light-emitting material, and electron-injecting layer described above, respectively. Examples include hole-injecting materials and electron-injecting materials.
正孔輸送層の材料、電子輸送層の材料及び発光層の材料は、発光素子の作製において、各々、正孔輸送層、電子輸送層及び発光層に隣接する層の形成時に使用される溶媒に溶解する場合、該溶媒に該材料が溶解することを回避するために、該材料が架橋基を有することが好ましい。架橋基を有する材料を用いて各層を形成した後、該架橋基を架橋させることにより、該層を不溶化させることができる。 The materials for the hole-transporting layer, the electron-transporting layer, and the light-emitting layer are selected from the solvents used in forming the layers adjacent to the hole-transporting layer, the electron-transporting layer, and the light-emitting layer, respectively, in the manufacture of the light-emitting device. When dissolved, it is preferred that the material has cross-linking groups to avoid dissolving the material in the solvent. After forming each layer using a material having a cross-linking group, the layer can be made insoluble by cross-linking the cross-linking group.
本開示の発光素子において、発光層、正孔輸送層、電子輸送層、正孔注入層、電子注入層等の各層の形成方法としては、低分子化合物を用いる場合、例えば、粉末からの真空蒸着法等の乾式法、溶液又は溶融状態からの成膜による方法等の湿式法が挙げられ、高分子化合物を用いる場合、例えば、溶液又は溶融状態からの成膜による方法等の湿式法が挙げられる。積層する層の順番、数及び厚さは、例えば、駆動電圧等を勘案して調整する。 In the light-emitting device of the present disclosure, as a method for forming each layer such as the light-emitting layer, the hole transport layer, the electron transport layer, the hole injection layer, and the electron injection layer, when using a low-molecular compound, for example, vacuum deposition from powder Dry methods such as methods, wet methods such as methods by film formation from a solution or a molten state, and wet methods such as methods by film formation from a solution or a molten state, for example, when using a polymer compound. . The order, number and thickness of the layers to be laminated are adjusted in consideration of, for example, driving voltage and the like.
[基板/電極]
発光素子における基板は、電極を形成することができ、かつ、有機層を形成する際に化学的に変化しない基板であればよく、例えば、ガラス、プラスチック、シリコン等の材料からなる基板である。不透明な基板の場合には、基板から最も遠くにある電極が透明又は半透明であることが好ましい。
陽極の材料としては、例えば、導電性の金属酸化物、半透明の金属が挙げられ、好ましくは、酸化インジウム、酸化亜鉛、酸化スズ;インジウム・スズ・オキサイド(ITO)、インジウム・亜鉛・オキサイド等の導電性化合物;銀とパラジウムと銅との複合体(APC);NESA、金、白金、銀、銅である。
陰極の材料としては、例えば、リチウム、ナトリウム、カリウム、ルビジウム、セシウム、ベリリウム、マグネシウム、カルシウム、ストロンチウム、バリウム、アルミニウム、亜鉛、インジウム等の金属;それらのうち2種以上の合金;それらのうち1種以上と、銀、銅、マンガン、チタン、コバルト、ニッケル、タングステン、錫のうち1種以上との合金;並びに、グラファイト及びグラファイト層間化合物が挙げられる。合金としては、例えば、マグネシウム-銀合金、マグネシウム-インジウム合金、マグネシウム-アルミニウム合金、インジウム-銀合金、リチウム-アルミニウム合金、リチウム-マグネシウム合金、リチウム-インジウム合金、カルシウム-アルミニウム合金が挙げられる。
陽極及び陰極は、各々、2層以上の積層構造としてもよい。
[Substrate/Electrode]
The substrate in the light emitting device may be a substrate on which an electrode can be formed and which does not change chemically when the organic layer is formed. In the case of opaque substrates, it is preferred that the electrodes furthest from the substrate be transparent or translucent.
Examples of materials for the anode include conductive metal oxides and translucent metals, preferably indium oxide, zinc oxide, tin oxide; indium-tin-oxide (ITO), indium-zinc-oxide, etc. conductive compounds of; silver-palladium-copper composite (APC); NESA, gold, platinum, silver, copper.
Examples of cathode materials include metals such as lithium, sodium, potassium, rubidium, cesium, beryllium, magnesium, calcium, strontium, barium, aluminum, zinc, and indium; alloys of two or more of them; alloys of one or more species with one or more of silver, copper, manganese, titanium, cobalt, nickel, tungsten, tin; and graphite and graphite intercalation compounds. Examples of alloys include magnesium-silver alloys, magnesium-indium alloys, magnesium-aluminum alloys, indium-silver alloys, lithium-aluminum alloys, lithium-magnesium alloys, lithium-indium alloys, and calcium-aluminum alloys.
Each of the anode and the cathode may have a laminated structure of two or more layers.
[用途]
本開示の発光素子は、液晶表示装置のバックライト用の光源、照明用の光源、有機EL照明、コンピュータ、テレビ及び携帯端末等の表示装置(例えば、有機ELディスプレイ及び有機ELテレビ)として好適に用いることができる。
[Use]
The light-emitting element of the present disclosure is suitable as a light source for backlight of a liquid crystal display device, a light source for illumination, organic EL lighting, a display device such as a computer, a television, and a mobile terminal (e.g., an organic EL display and an organic EL television). can be used.
以下、実施例によって本開示の一実施形態を更に詳細に説明するが、本開示はこれらの実施例に限定されるものではない。 Hereinafter, one embodiment of the present disclosure will be described in more detail with reference to Examples, but the present disclosure is not limited to these Examples.
実施例において、高分子化合物のポリスチレン換算の数平均分子量(Mn)及びポリスチレン換算の重量平均分子量(Mw)は、移動相にテトラヒドロフランを用い、サイズエクスクルージョンクロマトグラフィー(SEC)により求めた。なお、SECの各測定条件は、次のとおりである。
測定する高分子化合物を約0.05質量%の濃度でテトラヒドロフランに溶解させ、SECに10μL注入した。移動相は、2.0mL/分の流量で流した。カラムとして、PLgel MIXED-B(ポリマーラボラトリーズ社製)を用いた。検出器にはUV-VIS検出器(株式会社島津製作所製、商品名:SPD-10Avp)を用いた。
In the examples, the polystyrene-equivalent number-average molecular weight (Mn) and polystyrene-equivalent weight-average molecular weight (Mw) of the polymer compound were determined by size exclusion chromatography (SEC) using tetrahydrofuran as a mobile phase. In addition, each measurement condition of SEC is as follows.
A polymer compound to be measured was dissolved in tetrahydrofuran at a concentration of about 0.05% by mass, and 10 μL of the solution was injected into SEC. Mobile phase was run at a flow rate of 2.0 mL/min. As a column, PLgel MIXED-B (manufactured by Polymer Laboratories) was used. A UV-VIS detector (manufactured by Shimadzu Corporation, trade name: SPD-10Avp) was used as a detector.
LC-MSは、下記の方法で測定した。
測定試料を約2mg/mLの濃度になるようにクロロホルム又はテトラヒドロフランに溶解させ、LC-MS(Agilent社製、商品名:1100LCMSD)に約1μL注入した。LC-MSの移動相には、アセトニトリル及びテトラヒドロフランの比率を変化させながら用い、0.2mL/分の流量で流した。カラムは、L-column 2 ODS(3μm)(化学物質評価研究機構製、内径:2.1mm、長さ:100mm、粒径3μm)を用いた。
LC-MS was measured by the following method.
A sample to be measured was dissolved in chloroform or tetrahydrofuran to a concentration of about 2 mg/mL, and about 1 μL was injected into an LC-MS (manufactured by Agilent, trade name: 1100LCMSD). The mobile phase for LC-MS was acetonitrile and tetrahydrofuran with varying ratios and flowed at a flow rate of 0.2 mL/min. The column used was L-column 2 ODS (3 μm) (manufactured by Chemicals Evaluation and Research Institute, inner diameter: 2.1 mm, length: 100 mm, particle size: 3 μm).
TLC-MSは、下記の方法で測定した。
測定試料をトルエン、テトラヒドロフラン及びクロロホルムのいずれかの溶媒に任意の濃度で溶解させ、DART用TLCプレート(テクノアプリケーションズ社製、商品名:YSK5-100)上に塗布し、TLC-MS(日本電子社製、商品名:JMS-T100TD(The AccuTOF TLC))を用いて測定した。測定時のヘリウムガス温度は、200~400℃の範囲で調節した。
TLC-MS was measured by the following method.
The measurement sample is dissolved in any solvent of toluene, tetrahydrofuran and chloroform at an arbitrary concentration, applied to a DART TLC plate (manufactured by Techno Applications, trade name: YSK5-100), and subjected to TLC-MS (JEOL Ltd. The measurement was performed using a JMS-T100TD (The AccuTOF TLC) manufactured by Manufacture, trade name. The helium gas temperature during measurement was adjusted in the range of 200 to 400.degree.
NMRは、下記の方法で測定した。
5~10mgの測定試料を約0.5mLの重クロロホルム(CDCl3)、重テトラヒ
ドロフラン、重ジメチルスルホキシド、重アセトン、重N,N-ジメチルホルムアミド、重トルエン、重メタノール、重エタノール、重2-プロパノール又は重塩化メチレンに溶解させ、NMR装置(Agilent社製、商品名:INOVA300又はMERCURY
400VX)を用いて測定した。
NMR was measured by the following method.
5 to 10 mg of a measurement sample was added to about 0.5 mL of heavy chloroform (CDCl 3 ), heavy tetrahydrofuran, heavy dimethylsulfoxide, heavy acetone, heavy N,N-dimethylformamide, heavy toluene, heavy methanol, heavy ethanol, heavy 2-propanol. Or dissolved in methylene dichloride, NMR equipment (manufactured by Agilent, trade name: INOVA300 or MERCURY
400 VX).
化合物の純度の指標として、高速液体クロマトグラフィー(HPLC)面積百分率の値を用いた。この値は、特に記載がない限り、HPLC(株式会社島津製作所製、商品名:LC-20A)でのUV=254nmにおける値とする。この際、測定する化合物は、0.01~0.2質量%の濃度になるようにテトラヒドロフラン又はクロロホルムに溶解させ、濃度に応じてHPLCに1~10μL注入した。HPLCの移動相には、アセトニトリル/テトラヒドロフランの比率を100/0~0/100(容積比)まで変化させながら用い、1.0mL/分の流量で流した。カラムは、Kaseisorb LC ODS
2000(東京化成工業株式会社製)又は同等の性能を有するODSカラムを用いた。検出器には、フォトダイオードアレイ検出器(株式会社島津製作所製、商品名:SPD-M20A)を用いた。
High performance liquid chromatography (HPLC) area percentage values were used as an index of compound purity. Unless otherwise specified, this value is the value at UV=254 nm in HPLC (trade name: LC-20A, manufactured by Shimadzu Corporation). At this time, the compound to be measured was dissolved in tetrahydrofuran or chloroform to a concentration of 0.01 to 0.2% by mass, and 1 to 10 μL was injected into the HPLC depending on the concentration. Acetonitrile/tetrahydrofuran was used as the mobile phase for HPLC while changing the ratio from 100/0 to 0/100 (volume ratio), and flowed at a flow rate of 1.0 mL/min. The column was a Kaseisorb LC ODS
2000 (manufactured by Tokyo Kasei Kogyo Co., Ltd.) or an ODS column having equivalent performance was used. A photodiode array detector (manufactured by Shimadzu Corporation, trade name: SPD-M20A) was used as the detector.
化合物のΔESTの値の算出は、以下のようにして行った。
まず、B3LYPレベルの密度汎関数法により、化合物の基底状態を構造最適化した。その際、基底関数として、6-31G*を用いた。
そして、得られた構造最適化された構造を用いて、B3LYPレベルの時間依存密度汎関数法により、化合物のΔESTを算出した。なお、量子化学計算プログラムとして、Gaussian09を用いて計算した。
Calculation of the ΔEST value of the compound was performed as follows.
First, the ground state of the compound was structurally optimized by density functional theory at the B3LYP level. At that time, 6-31G* was used as a basis function.
Then, using the obtained optimized structure, ΔEST of the compound was calculated by time-dependent density functional theory at the B3LYP level. The calculation was performed using Gaussian09 as a quantum chemical calculation program.
化合物の室温における発光スペクトルの最大ピーク波長は、分光光度計(日本分光株式会社製、FP-6500)により室温にて測定した。化合物をキシレンに、約8×10-4質量%の濃度で溶解させたキシレン溶液を試料として用いた。励起光としては、波長325nmの紫外(UV)光を用いた。 The maximum peak wavelength of the emission spectrum of the compound at room temperature was measured at room temperature with a spectrophotometer (manufactured by JASCO Corporation, FP-6500). A xylene solution in which a compound was dissolved in xylene at a concentration of about 8×10 −4 mass % was used as a sample. Ultraviolet (UV) light with a wavelength of 325 nm was used as excitation light.
<化合物H1~H3、高分子化合物HP4及び化合物ET1の合成及び入手>
化合物H1~H3、高分子化合物HP4及び化合物ET1は、Luminescence Technology社製を用いた。
<Synthesis and acquisition of compounds H1 to H3, polymer compound HP4 and compound ET1>
Compounds H1 to H3, polymer compound HP4 and compound ET1 were manufactured by Luminescence Technology.
<金属錯体MC1~MC11の合成及び入手>
金属錯体MC1及びMC4は、特開2013-147551号公報に記載の方法に従って合成した。
金属錯体MC2は、国際公開第2017/130977号に記載の方法に準じて合成した。
金属錯体MC3(金属錯体Firpic)は、Luminescence Technology社製を用いた。
金属錯体MC5は、国際公開第2017/170916号に記載の方法に準じて合成した。
金属錯体MC6~MC8及びMC10は、後述の方法で合成した。
金属錯体MC9は、国際公開第2016/006523号に記載の方法に従って合成した。
金属錯体MC11は、国際公開第2008/090795号及び国際公開第2006/121811号に記載の方法に準じて合成した。
<Synthesis and acquisition of metal complexes MC1 to MC11>
Metal complexes MC1 and MC4 were synthesized according to the method described in JP-A-2013-147551.
Metal complex MC2 was synthesized according to the method described in WO2017/130977.
A metal complex MC3 (metal complex Firpic) manufactured by Luminescence Technology was used.
Metal complex MC5 was synthesized according to the method described in WO2017/170916.
Metal complexes MC6 to MC8 and MC10 were synthesized by the method described below.
Metal complex MC9 was synthesized according to the method described in WO2016/006523.
Metal complex MC11 was synthesized according to the methods described in WO2008/090795 and WO2006/121811.
<金属錯体MC6の合成>
下記の方法で、金属錯体MC6を合成した。
<Synthesis of metal complex MC6>
A metal complex MC6 was synthesized by the following method.
反応容器内をアルゴン雰囲気とした後、2,2’-ジメチルヘキサン酸(23.8g)、クロロホルム(143mL)、及び、N,N’-ジメチルホルムアミド(0.12g)を加え、50℃で撹拌した。そこに塩化チオニル(21.6g)を滴下し、50℃で3時間撹拌し2,2’-ジメチルヘキサノイルクロライドを発生させた。
別途用意した反応容器内を窒素ガス雰囲気とした後、5-ブロモ-2-メチルアニリン(29.3g)、クロロホルム(293mL)、及び、トリエチルアミン(21.9mL)を加え、撹拌した。その後、反応容器を氷浴で冷却し、そこに上記で調製した2,2’-ジメチルヘキサノイルクロライドを滴下した。滴下後、室温で2.5時間撹拌を継続し、その後、1mol/L炭酸ナトリウム水溶液(165mL)を加え室温で撹拌した。分液し、得られた有機層に1mol/L塩酸(83mL)を加え室温で撹拌した。分液し、イオン交換水で洗浄した。得られた洗浄液を分液し、得られた有機層を硫酸マグネシウムで乾燥させた後、ろ過した。得られたろ液を減圧濃縮した後、ヘプタンを用いて2回再結晶を行い、40℃で減圧乾燥させることで化合物MC6A(39g、白色固体)を収率76%で得た。化合物MC6AのHPLC面積百分率値は98.7%であった。
After making the inside of the reaction vessel an argon atmosphere, 2,2'-dimethylhexanoic acid (23.8 g), chloroform (143 mL), and N,N'-dimethylformamide (0.12 g) were added and stirred at 50°C. bottom. Thionyl chloride (21.6 g) was added dropwise thereto, and the mixture was stirred at 50°C for 3 hours to generate 2,2'-dimethylhexanoyl chloride.
After a nitrogen gas atmosphere was created in a separately prepared reaction vessel, 5-bromo-2-methylaniline (29.3 g), chloroform (293 mL), and triethylamine (21.9 mL) were added and stirred. After that, the reaction vessel was cooled with an ice bath, and 2,2'-dimethylhexanoyl chloride prepared above was added dropwise thereto. After the dropwise addition, stirring was continued at room temperature for 2.5 hours, then 1 mol/L sodium carbonate aqueous solution (165 mL) was added and the mixture was stirred at room temperature. After liquid separation, 1 mol/L hydrochloric acid (83 mL) was added to the obtained organic layer and the mixture was stirred at room temperature. It was separated and washed with deionized water. The obtained washing liquid was separated, and the obtained organic layer was dried with magnesium sulfate and then filtered. The resulting filtrate was concentrated under reduced pressure, recrystallized twice using heptane, and dried under reduced pressure at 40° C. to obtain compound MC6A (39 g, white solid) with a yield of 76%. The HPLC area percentage value of compound MC6A was 98.7%.
化合物MC6AのNMRの測定結果は、以下のとおりであった。
1H-NMR(400MHz、CDCl3)δ(ppm)=8.06(1H,d),7.25-7.11(2H,m),7.04(1H,d),2.17(3H,s),1.60-1.53(2H,m),1.32-1.22(10H,m),0.87(3H,s).
The NMR measurement results of compound MC6A were as follows.
1 H-NMR (400 MHz, CDCl 3 ) δ (ppm) = 8.06 (1H, d), 7.25-7.11 (2H, m), 7.04 (1H, d), 2.17 ( 3H, s), 1.60-1.53 (2H, m), 1.32-1.22 (10 H, m), 0.87 (3H, s).
反応容器内をアルゴンガス雰囲気とした後、化合物MC6A(25g)、モノクロロベンゼン(200mL)、2-フルオロピリジン(7.6mL)及びトリフルオロメタンスルホン酸無水物(15mL)を加え、室温下で30分撹拌した。そこへ、ベンゾイルヒドラジン(12g)を加え、90℃で3.5時間撹拌した。その後、そこへイオン交換水(250mL)を加えて有機層を洗浄した。分液後、得られた有機層に1mol/L炭酸水素ナトリウム水溶液(66mL)を加え有機層を抽出し、得られた有機層をイオン交換水で洗浄した。得られた有機層を減圧濃縮することで油状物を得た。得られた油状物にクロロホルムとTHFの混合溶媒(体積比8:2、50mL)を加え溶解させた後、シリカゲルを敷いたろ過器でろ過して得られたろ液を減圧濃縮した。その後、ヘプタンを用いて再結晶し、50℃で減圧乾燥させることにより、化合物MC6B(27.3g)を白色固体として収率83%で得た。化合物MC6BのHPLC面積百分率値は99.1%であった。 After making the inside of the reaction vessel an argon gas atmosphere, compound MC6A (25 g), monochlorobenzene (200 mL), 2-fluoropyridine (7.6 mL) and trifluoromethanesulfonic anhydride (15 mL) were added, and the mixture was stirred at room temperature for 30 minutes. Stirred. Benzoyl hydrazine (12 g) was added thereto, and the mixture was stirred at 90° C. for 3.5 hours. After that, ion-exchanged water (250 mL) was added thereto to wash the organic layer. After liquid separation, a 1 mol/L sodium hydrogencarbonate aqueous solution (66 mL) was added to the obtained organic layer to extract the organic layer, and the obtained organic layer was washed with ion-exchanged water. An oily matter was obtained by concentrating the obtained organic layer under reduced pressure. A mixed solvent of chloroform and THF (volume ratio: 8:2, 50 mL) was added to the resulting oil to dissolve it, followed by filtration through a filter lined with silica gel, and the resulting filtrate was concentrated under reduced pressure. After that, it was recrystallized using heptane and dried at 50° C. under reduced pressure to obtain compound MC6B (27.3 g) as a white solid with a yield of 83%. The HPLC area percentage value of compound MC6B was 99.1%.
化合物MC6BのNMRの測定結果は、以下のとおりであった。
1H-NMR(400MHz、CDCl3)δ(ppm)=7.58-7.50(2H,m),7.35-7.22(5H,m),7.12-7.07(1H,d),1.71(3H,s),1.67-1.57(1H,m),1.45-1.07(11H,m),0.88(3H,t).
The NMR measurement results of compound MC6B were as follows.
1 H-NMR (400 MHz, CDCl 3 ) δ (ppm) = 7.58-7.50 (2H, m), 7.35-7.22 (5H, m), 7.12-7.07 (1H , d), 1.71 (3H, s), 1.67-1.57 (1H, m), 1.45-1.07 (11H, m), 0.88 (3H, t).
反応容器内をアルゴンガス雰囲気とした後、化合物MC6B(7.0g)、2-([1,1’-ビフェニル]-3-イル)-4,4,5,5-テトラメチル-1,3,2-ジオキサボロラン(5.2g)、及び、トルエンを加え室温で撹拌した。そこに、ビス(ジ-tert-ブチル(4-ジメチルアミノビフェニル)ホスフィン)ジクロロパラジウム(60mg)を加え、80℃に加熱した。その後、40質量%テトラブチルアンモニウム水溶液(66g)を滴下し、80℃で16時間撹拌した。その後、反応容器を室温まで冷却し、分液した。得られた有機層をイオン交換水で洗浄した。得られた洗浄液を分液し、得られた有機層をイオン交換水で洗浄した。得られた洗浄液を分液し、得られた有機層を硫酸マグネシウムで乾燥させた後、ろ過した。得られたろ液に活性炭を加え、室温で30分間撹拌した後、セライトを敷いたろ過器でろ過した。得られたろ液を減圧濃縮した後、トルエンと酢酸エチルの混合溶媒(体積比9:1)を用いてシリカゲルカラム精製を行った。その後、ヘプタンと2-プロパノールの混合溶媒(体積比5:1)を用いて再結晶を3回行い、50℃で減圧乾燥させることで化合物MC6C(5.5g、白色固体)を収率66%で得た。化合物MC6CのHPLC面積百分率値は99.5%以上であった。 After making the inside of the reaction vessel an argon gas atmosphere, compound MC6B (7.0 g), 2-([1,1′-biphenyl]-3-yl)-4,4,5,5-tetramethyl-1,3 , 2-dioxaborolan (5.2 g) and toluene were added and stirred at room temperature. Bis(di-tert-butyl(4-dimethylaminobiphenyl)phosphine)dichloropalladium (60 mg) was added thereto and heated to 80°C. After that, a 40% by mass tetrabutylammonium aqueous solution (66 g) was added dropwise, and the mixture was stirred at 80° C. for 16 hours. After that, the reaction vessel was cooled to room temperature and separated. The obtained organic layer was washed with deionized water. The obtained washing liquid was separated, and the obtained organic layer was washed with ion-exchanged water. The obtained washing liquid was separated, and the obtained organic layer was dried with magnesium sulfate and then filtered. Activated carbon was added to the obtained filtrate, and the mixture was stirred at room temperature for 30 minutes and then filtered through a filter covered with celite. After the obtained filtrate was concentrated under reduced pressure, silica gel column purification was performed using a mixed solvent of toluene and ethyl acetate (volume ratio 9:1). Thereafter, recrystallization was performed three times using a mixed solvent of heptane and 2-propanol (volume ratio: 5:1), followed by drying at 50°C under reduced pressure to obtain compound MC6C (5.5 g, white solid) with a yield of 66%. I got it in The HPLC area percentage value of compound MC6C was greater than 99.5%.
化合物MC6CのLC-MS及びNMRの測定結果は、以下のとおりであった。
LC-MS(APCI,positive):m/z=542[M+H]+
1H-NMR(400MHz、CDCl3)δ(ppm)=7.82 (1H,t),
7.73-7.71(2H,m),7.64-7.57(4H,m),7.53(1H,t),7.45(2H,t),7.40-7.33(3H,m),7.32-7.25(2H,m),7.22(2H,t),1.80(3H,s),1.78-1.67(1H,m),1.52-1.42(1H,m),1.37(3H,s),1.35-1.16(4H,m),1.14(3H,s),0.82(3H,t).
The measurement results of LC-MS and NMR of compound MC6C were as follows.
LC-MS (APCI, positive): m/z=542 [M+H] +
1 H-NMR (400 MHz, CDCl 3 ) δ (ppm) = 7.82 (1H, t),
7.73-7.71 (2H, m), 7.64-7.57 (4H, m), 7.53 (1H, t), 7.45 (2H, t), 7.40-7. 33 (3H, m), 7.32-7.25 (2H, m), 7.22 (2H, t), 1.80 (3H, s), 1.78-1.67 (1H, m) , 1.52-1.42 (1H, m), 1.37 (3H, s), 1.35-1.16 (4H, m), 1.14 (3H, s), 0.82 (3H , t).
反応容器内をアルゴンガス雰囲気とした後、トリスアセチルアセトナトイリジウム(1.2g)、化合物MC6C(5.0g)及びペンタデカン(25mL)を加え、加熱還流下で55時間攪拌した。その後、そこへ、トルエンを加え、シリカゲルを敷いたろ過器でろ過した後、トルエン及び酢酸エチルの混合溶媒を用いて金属錯体MC6を含む黄色溶液を抽出した。得られた溶液を減圧濃縮することで固体を得た後、得られた固体をシリカゲルカラムクロマトグラフィー(移動相溶媒:トルエン及び酢酸エチルの混合溶媒)で精製することにより、固体を得た。得られた固体をトルエン及びアセトニトリルの混合溶媒を用いての再結晶、並びに、トルエン及びエタノールの混合溶媒を用いての再結晶を複数回繰り返し、50℃で減圧乾燥させることにより金属錯体MC6(3.5g、黄色固体)を収率82%で得た。金属錯体MC6のHPLC面積百分率値は96%であった。 After the inside of the reaction vessel was replaced with an argon gas atmosphere, trisacetylacetonatoiridium (1.2 g), compound MC6C (5.0 g) and pentadecane (25 mL) were added, and the mixture was stirred under reflux with heating for 55 hours. After that, toluene was added thereto, and after filtering through a filter covered with silica gel, a yellow solution containing metal complex MC6 was extracted using a mixed solvent of toluene and ethyl acetate. The obtained solution was concentrated under reduced pressure to obtain a solid, and then the obtained solid was purified by silica gel column chromatography (mobile phase solvent: mixed solvent of toluene and ethyl acetate) to obtain a solid. The obtained solid was recrystallized using a mixed solvent of toluene and acetonitrile, and recrystallized using a mixed solvent of toluene and ethanol several times, and dried under reduced pressure at 50 ° C. to obtain metal complex MC6 (3 .5 g, yellow solid) was obtained in 82% yield. The HPLC area percentage value for metal complex MC6 was 96%.
金属錯体MC6のLC-MS及びNMRの測定結果は、以下のとおりであった。
LC-MS(APPI,positive):m/z=1645.8[M+H]+
1H-NMR(400MHz、CD2Cl2)δ(ppm)=7.89-7.69(9H,m),7.67-7.31(27H,m),6.99-6.38(9H,m),6.12-6.10(3H,m),2.23-1.82(9H,m),1.47-0.84(36H,m),0.78-0.46(9H,m).
The LC-MS and NMR measurement results of the metal complex MC6 were as follows.
LC-MS (APPI, positive): m/z = 1645.8 [M+H] +
1 H-NMR (400 MHz, CD 2 Cl 2 ) δ (ppm) = 7.89-7.69 (9H, m), 7.67-7.31 (27H, m), 6.99-6.38 (9H, m), 6.12-6.10 (3H, m), 2.23-1.82 (9H, m), 1.47-0.84 (36H, m), 0.78-0 .46(9H, m).
<金属錯体MC7の合成>
下記の方法で、金属錯体MC7を合成した。
<Synthesis of metal complex MC7>
A metal complex MC7 was synthesized by the following method.
反応容器内をアルゴン雰囲気とした後、2,2’-ジメチルヘキサン酸(11.8g)、クロロホルム(60mL)、N,N’-ジメチルホルムアミド(0.07g)を加え、50℃で撹拌した。そこに塩化チオニル(11.3g)を滴下し、50℃で3時間撹拌し2,2’-ジメチルヘキサノイルクロライドを発生させた。
別途用意した反応容器内を窒素ガス雰囲気とした後、2-メチル-5-(3-フェニルフェニル)アニリン塩酸塩(22.0g)、クロロホルム(176mL)、トリエチルアミン(20.7mL)を加え、撹拌した。その後、反応容器を氷浴で冷却し、そこに上記で調製した2,2’-ジメチルヘキサノイルクロライド溶液を滴下した。滴下後、室温で2.5時間撹拌を継続し、その後、1mol/L炭酸ナトリウム水溶液(82mL)を加え室温で撹拌した。分液し、得られた有機層に1mol/L塩酸(41mL)を加え室温で撹拌した。分液し、イオン交換水で洗浄した。得られた洗浄液を分液し、得られた有機層を硫酸マグネシウムで乾燥させた後、ろ過した。得られたろ液を減圧濃縮した後、ヘプタンを用いて再結晶を行い、40℃で減圧乾燥させることで化合物MC7D(27g、白色固体)を収率94%で得た。化合物MC7DのHPLC面積百分率値は99.5%以上であった。
After the inside of the reaction vessel was replaced with an argon atmosphere, 2,2'-dimethylhexanoic acid (11.8 g), chloroform (60 mL) and N,N'-dimethylformamide (0.07 g) were added and stirred at 50°C. Thionyl chloride (11.3 g) was added dropwise thereto, and the mixture was stirred at 50°C for 3 hours to generate 2,2'-dimethylhexanoyl chloride.
After making the inside of a separately prepared reaction vessel a nitrogen gas atmosphere, 2-methyl-5-(3-phenylphenyl)aniline hydrochloride (22.0 g), chloroform (176 mL) and triethylamine (20.7 mL) were added and stirred. bottom. After that, the reaction vessel was cooled with an ice bath, and the 2,2'-dimethylhexanoyl chloride solution prepared above was added dropwise thereto. After the dropwise addition, stirring was continued at room temperature for 2.5 hours, then 1 mol/L sodium carbonate aqueous solution (82 mL) was added and the mixture was stirred at room temperature. After liquid separation, 1 mol/L hydrochloric acid (41 mL) was added to the obtained organic layer and the mixture was stirred at room temperature. It was separated and washed with deionized water. The obtained washing liquid was separated, and the obtained organic layer was dried with magnesium sulfate and then filtered. The resulting filtrate was concentrated under reduced pressure, recrystallized using heptane, and dried under reduced pressure at 40° C. to obtain compound MC7D (27 g, white solid) with a yield of 94%. The HPLC area percentage value of compound MC7D was greater than 99.5%.
化合物MC7DのNMRの測定結果は、以下のとおりであった。
1H-NMR(400MHz、CDCl3)δ(ppm)=8.08 (1H, d),7.91(1H, t),7.64(2H, d),7.57(2H, t),7.51-7.41(3H,m),7.38-7.31 (2H, m),7.28 (1H, d),7.24(1H, br),2.28 (3H,s),1.60(2H,m),1.37-1.30
(10H,m),0.88(3H,t)
The NMR measurement results of compound MC7D were as follows.
1 H-NMR (400 MHz, CDCl 3 ) δ (ppm) = 8.08 (1H, d), 7.91 (1H, t), 7.64 (2H, d), 7.57 (2H, t) , 7.51-7.41 (3H, m), 7.38-7.31 (2H, m), 7.28 (1H, d), 7.24 (1H, br), 2.28 (3H , s), 1.60 (2H, m), 1.37-1.30
(10H, m), 0.88 (3H, t)
反応容器内をアルゴンガス雰囲気とした後、化合物MC7D(25g)、モノクロロベンゼン(84mL)、2-フルオロピリジン(2.6mL)及びトリフルオロメタンスルホン酸無水物(5mL)を加え、室温下で30分撹拌した。そこへ、3-ブロモベンゾイルヒドラジン(6.4g)を加え、90℃で4.5時間撹拌した。その後、そこへイオン交換水(105mL)及びヘプタン(105mL)を加えて有機層を洗浄した。分液後得られた有機層に1mol/L炭酸水素ナトリウム水溶液(45mL)を加え有機層を抽出し、得られた有機層をイオン交換水で洗浄した。得られた有機層を減圧濃縮することで油状物を得た。得られた油状物にクロロホルムとTHFの混合溶媒(体積比8:2、50mL)を加え溶解させた後、シリカゲルを敷いたろ過器でろ過して得られたろ液を減圧濃縮した。その後、ヘプタンを用いて再結晶し、50℃で減圧乾燥させることにより、化合物MC7E(14.3g)を白色固体として収率93%で得た。化合物MC7EのHPLC面積百分率値は99.5%以上であった。 After making the inside of the reaction vessel an argon gas atmosphere, compound MC7D (25 g), monochlorobenzene (84 mL), 2-fluoropyridine (2.6 mL) and trifluoromethanesulfonic anhydride (5 mL) were added, and the mixture was stirred at room temperature for 30 minutes. Stirred. 3-Bromobenzoylhydrazine (6.4 g) was added thereto and stirred at 90° C. for 4.5 hours. After that, ion-exchanged water (105 mL) and heptane (105 mL) were added thereto to wash the organic layer. After liquid separation, a 1 mol/L sodium hydrogencarbonate aqueous solution (45 mL) was added to the organic layer to extract the organic layer, and the resulting organic layer was washed with ion-exchanged water. An oily matter was obtained by concentrating the obtained organic layer under reduced pressure. A mixed solvent of chloroform and THF (volume ratio: 8:2, 50 mL) was added to the resulting oil to dissolve it, followed by filtration through a filter lined with silica gel, and the resulting filtrate was concentrated under reduced pressure. After that, it was recrystallized using heptane and dried under reduced pressure at 50° C. to obtain compound MC7E (14.3 g) as a white solid with a yield of 93%. The HPLC area percentage value of compound MC7E was greater than 99.5%.
反応容器内をアルゴンガス雰囲気とした後、化合物MC7E(13.6g)、2-フェニル-4,4,5,5-テトラメチル-1,3,2-ジオキサボロラン(5.4g)、トルエン(136mL)を加え室温で撹拌した。そこに[(ジ(1-アダマンチル)-N-ブチルホスフィン)-2-(2’-アミノ-1,1’-ビフェニル)]パラジウム(II)メタンスルホン酸塩(175mg)を加え、80℃に加熱した。その後、40質量%テトラブチルアンモニウム水溶液(38g)及びイオン交換水(56mL)の混合液を滴下し、80℃で16時間撹拌した。その後、反応容器を室温まで冷却し、分液した。得られた有機層をイオン交換水で洗浄した。得られた洗浄液を分液し、得られた有機層をイオン交換水で洗浄した。得られた洗浄液を分液し、得られた有機層を硫酸マグネシウムで乾燥させた後、ろ過した。得られたろ液にシリカゲル(49g)を加え、室温で30分間撹拌した後、セライトを敷いたろ過器でろ過した。クロロホルムとテトラヒドロフランの混合溶媒(体積比:1)でろ上を洗浄した。得られたろ液を減圧濃縮した後、ヘプタンと2-プロパノールの混合溶媒(体積比8:1)を用いて再結晶を3回行い、50℃で減圧乾燥させることで化合物MC7F(12.2g、白色固体)を収率90%で得た。化合物MC7FのHPLC面積百分率値は99.5%以上であった。 After making the inside of the reaction vessel an argon gas atmosphere, compound MC7E (13.6 g), 2-phenyl-4,4,5,5-tetramethyl-1,3,2-dioxaborolane (5.4 g), toluene (136 mL) ) was added and stirred at room temperature. [(Di(1-adamantyl)-N-butylphosphine)-2-(2'-amino-1,1'-biphenyl)]palladium(II) methanesulfonate (175 mg) was added thereto and heated to 80°C. heated. After that, a mixed liquid of 40% by mass tetrabutylammonium aqueous solution (38 g) and ion-exchanged water (56 mL) was added dropwise, and the mixture was stirred at 80° C. for 16 hours. After that, the reaction vessel was cooled to room temperature and separated. The obtained organic layer was washed with deionized water. The obtained washing liquid was separated, and the obtained organic layer was washed with ion-exchanged water. The obtained washing liquid was separated, and the obtained organic layer was dried with magnesium sulfate and then filtered. Silica gel (49 g) was added to the obtained filtrate, and the mixture was stirred at room temperature for 30 minutes and then filtered through a filter covered with celite. The filter top was washed with a mixed solvent of chloroform and tetrahydrofuran (volume ratio: 1). The resulting filtrate was concentrated under reduced pressure, recrystallized three times using a mixed solvent of heptane and 2-propanol (volume ratio 8:1), and dried under reduced pressure at 50°C to obtain compound MC7F (12.2 g, white solid) was obtained in 90% yield. The HPLC area percentage value of compound MC7F was greater than 99.5%.
化合物MC7FのLC-MS及びNMRの測定結果は、以下のとおりであった。
LC-MS(APPI,positive):m/z=562[M+H]+
1H-NMR(400MHz、CDCl3)δ(ppm)=7.82(2H,t),
7.75(1H,d),7.63-7.60(4H,m),7.59-7.53(3H,m),7.49-7.43(3H,m),7.38-7.33(3H,m),7.26-7.22(5H,m),1.80-1.73(4H,m),1.56-1.40(4
H,m),1.35-1.18(7H,m),0.82(3H,t).
The measurement results of LC-MS and NMR of compound MC7F were as follows.
LC-MS (APPI, positive): m/z = 562 [M+H] +
1 H-NMR (400 MHz, CDCl 3 ) δ (ppm) = 7.82 (2H, t),
7.75 (1H, d), 7.63-7.60 (4H, m), 7.59-7.53 (3H, m), 7.49-7.43 (3H, m), 7. 38-7.33 (3H, m), 7.26-7.22 (5H, m), 1.80-1.73 (4H, m), 1.56-1.40 (4
H, m), 1.35-1.18 (7H, m), 0.82 (3H, t).
反応容器内をアルゴンガス雰囲気とした後、トリスアセチルアセトナトイリジウム(2.2g)、化合物MC7F(10g)及びペンタデカン(40mL)を加え、加熱還流下で67時間攪拌した。その後、そこへ、トルエンを加え、シリカゲルを敷いたろ過器でろ過した後、トルエン及び酢酸エチルの混合溶媒を用いて金属錯体MC7を含む黄色溶液を抽出した。得られた溶液を減圧濃縮することで固体を得た後、得られた固体をシリカゲルカラムクロマトグラフィー(移動相溶媒:トルエン及び酢酸エチルの混合溶媒)で精製することにより、固体を得た。得られた固体をトルエン及びアセトニトリルの混合溶媒を用いての再結晶、並びに、トルエン及びエタノールの混合溶媒を用いての再結晶を複数回繰り返し、50℃で減圧乾燥させることにより金属錯体MC7(3.5g、黄色固体)を収率82%で得た。金属錯体MC7のHPLC面積百分率値は99.5%以上であった。 After the inside of the reaction vessel was replaced with an argon gas atmosphere, trisacetylacetonatoiridium (2.2 g), compound MC7F (10 g) and pentadecane (40 mL) were added, and the mixture was stirred under reflux with heating for 67 hours. After that, toluene was added thereto, and after filtering through a filter covered with silica gel, a yellow solution containing metal complex MC7 was extracted using a mixed solvent of toluene and ethyl acetate. The obtained solution was concentrated under reduced pressure to obtain a solid, and then the obtained solid was purified by silica gel column chromatography (mobile phase solvent: mixed solvent of toluene and ethyl acetate) to obtain a solid. The obtained solid was recrystallized using a mixed solvent of toluene and acetonitrile, and recrystallized using a mixed solvent of toluene and ethanol several times, and dried under reduced pressure at 50 ° C. to obtain metal complex MC7 (3 .5 g, yellow solid) was obtained in 82% yield. The HPLC area percentage value of metal complex MC7 was 99.5% or higher.
金属錯体MC7のLC-MS及びNMRの測定結果は、以下のとおりであった。
LC-MS(APCI,positive):m/z=1874.9[M+H]+
1H-NMR(400MHz、CD2Cl2)δ(ppm)=7.93-7.68(m,9H),7.65-7.28(m,27H),7.21-7.04(m,15H),7.00-6.71(m,6H),6.40-6.25(m,3H),2.33-1.82(m,9H),1.80-1.54(m,3H),1.48-0.80(m,33H),0.79-0.32(m,9H).
The measurement results of LC-MS and NMR of metal complex MC7 were as follows.
LC-MS (APCI, positive): m/z=1874.9 [M+H] +
1 H-NMR (400 MHz, CD 2 Cl 2 ) δ (ppm) = 7.93-7.68 (m, 9H), 7.65-7.28 (m, 27H), 7.21-7.04 (m, 15H), 7.00-6.71 (m, 6H), 6.40-6.25 (m, 3H), 2.33-1.82 (m, 9H), 1.80-1 .54 (m, 3H), 1.48-0.80 (m, 33H), 0.79-0.32 (m, 9H).
<金属錯体MC8の合成>
下記の方法で、金属錯体MC8を合成した。
<Synthesis of metal complex MC8>
A metal complex MC8 was synthesized by the following method.
反応容器内をアルゴンガス雰囲気とした後、化合物MC7D(40g)、モノクロロベンゼン(320mL)、2-フルオロピリジン(9.8mL)及びトリフルオロメタンスルホン酸無水物(19mL)を加え、室温下で30分撹拌した。そこへ、3-tert-ブチルベンゾイルヒドラジン(22g)を加え、90℃で3.5時間撹拌した。その後、そこへイオン交換水(360mL)を加えて有機層を洗浄した。分液後、得られた有機層に1mol/L炭酸水素ナトリウム水溶液(77mL)を加え有機層を抽出し、得られた有機層をイオン交換水で洗浄した。得られた有機層を減圧濃縮することで油状物を得た。得られた油状物にクロロホルムとTHFの混合溶媒(体積比8:2、90mL)を加え溶解させた後、シリカゲルを敷いたろ過器でろ過して得られたろ液を減圧濃縮した。その後、ヘプタンと2-プロパノールの混合溶媒(体積比5:0.3、295mL)を用いて再結晶し、50℃で減圧乾燥させることにより、化合物MC8G(47.6g)を白色固体として収率85%で得た。化合物MC8GのHPLC面積百分率値は99.9%であった。 After making the inside of the reaction vessel an argon gas atmosphere, compound MC7D (40 g), monochlorobenzene (320 mL), 2-fluoropyridine (9.8 mL) and trifluoromethanesulfonic anhydride (19 mL) were added, and the mixture was stirred at room temperature for 30 minutes. Stirred. 3-tert-Butylbenzoylhydrazine (22 g) was added thereto and stirred at 90° C. for 3.5 hours. After that, ion-exchanged water (360 mL) was added thereto to wash the organic layer. After liquid separation, a 1 mol/L sodium hydrogencarbonate aqueous solution (77 mL) was added to the obtained organic layer to extract the organic layer, and the obtained organic layer was washed with ion-exchanged water. An oily matter was obtained by concentrating the obtained organic layer under reduced pressure. A mixed solvent of chloroform and THF (volume ratio: 8:2, 90 mL) was added to the resulting oil to dissolve it, followed by filtration through a filter lined with silica gel, and the resulting filtrate was concentrated under reduced pressure. Thereafter, recrystallization was performed using a mixed solvent of heptane and 2-propanol (volume ratio 5:0.3, 295 mL), and dried under reduced pressure at 50°C to yield compound MC8G (47.6 g) as a white solid. 85% obtained. The HPLC area percentage value of compound MC8G was 99.9%.
化合物MC8GのNMRの測定結果は、以下のとおりであった。
1H-NMR(400MHz、CD2Cl2)δ(ppm)=7.79(1H,t),7.73(1H,d),7.68(1H,dd),7.65-7.58(3H,m),7.58-7.50(2H,m),7.48-7.40(3H,m),7.35(1H,tt),7.33-7.27(2H,m),7,23-7.18(2H,m),1.80(3H,s),1.78-1.68(1H,m),1.53-1.41(1H,m),1.38(3H,s),1.35-1.18(4H,m),1.16(3H,s),1.06(9H,s),0.81(3H,t).
TLC-MS(positive):m/z=542.3[M+H]+
The NMR measurement results of compound MC8G were as follows.
1 H-NMR (400 MHz, CD 2 Cl 2 ) δ (ppm) = 7.79 (1H, t), 7.73 (1H, d), 7.68 (1H, dd), 7.65-7. 58 (3H, m), 7.58-7.50 (2H, m), 7.48-7.40 (3H, m), 7.35 (1H, tt), 7.33-7.27 ( 2H, m), 7, 23-7.18 (2H, m), 1.80 (3H, s), 1.78-1.68 (1H, m), 1.53-1.41 (1H, m), 1.38 (3H, s), 1.35-1.18 (4H, m), 1.16 (3H, s), 1.06 (9H, s), 0.81 (3H, t ).
TLC-MS (positive): m/z=542.3 [M+H] +
反応容器内をアルゴンガス雰囲気とした後、トリスアセチルアセトナトイリジウム(1.5g)、化合物MC8G(6.8g)及びペンタデカン(34mL)を加え、加熱還流下で30時間攪拌した。その後、そこへ、トルエンを加え、シリカゲルを敷いたろ過器でろ過した後、トルエン及び酢酸エチルの混合溶媒を用いて金属錯体MC8を含む黄色溶液を抽出した。得られた溶液を減圧濃縮することで固体を得た後、得られた固体をシリカゲルカラムクロマトグラフィー(移動相溶媒:トルエン及び酢酸エチルの混合溶媒)で精製することにより、固体を得た。得られた固体をヘプタン及び2-プロパノールの混合溶媒を用いての再結晶を複数回繰り返し、50℃で減圧乾燥させることにより金属錯体MC8(4.3g、黄色固体)を収率75%で得た。金属錯体MC8のHPLC面積百分率値は94%であった。 After the inside of the reaction vessel was replaced with an argon gas atmosphere, trisacetylacetonatoiridium (1.5 g), compound MC8G (6.8 g) and pentadecane (34 mL) were added, and the mixture was stirred under heating under reflux for 30 hours. After that, toluene was added thereto, and after filtering through a filter covered with silica gel, a yellow solution containing metal complex MC8 was extracted using a mixed solvent of toluene and ethyl acetate. The obtained solution was concentrated under reduced pressure to obtain a solid, and then the obtained solid was purified by silica gel column chromatography (mobile phase solvent: mixed solvent of toluene and ethyl acetate) to obtain a solid. The obtained solid was recrystallized several times using a mixed solvent of heptane and 2-propanol, and dried under reduced pressure at 50°C to obtain metal complex MC8 (4.3 g, yellow solid) with a yield of 75%. rice field. The HPLC area percentage value of metal complex MC8 was 94%.
金属錯体MC8のLC-MS及びNMRの測定結果は、以下のとおりであった。
TLC-MS(positive):m/z=1814.7[M+H]+
1H-NMR(400MHz、CD2Cl2)δ(ppm)=7.89-7.28(72H,m),6.95-6.30(6H,m),6.02-6.20(3H,m),2.23-0.50(45H,m).
The measurement results of LC-MS and NMR of metal complex MC8 were as follows.
TLC-MS (positive): m/z=1814.7 [M+H] +
1 H-NMR (400 MHz, CD 2 Cl 2 ) δ (ppm) = 7.89-7.28 (72H, m), 6.95-6.30 (6H, m), 6.02-6.20 (3H, m), 2.23-0.50 (45H, m).
<金属錯体MC10の合成>
下記の方法で、金属錯体MC10を合成した。
<Synthesis of metal complex MC10>
Metal complex MC10 was synthesized by the following method.
反応容器内をアルゴンガス雰囲気とした後、2,6-ジメチル-4-tert-ブチルフェニルヒドラジン塩酸塩(101g)及びtert-ブチルメチルエーテル(1070mL)を加え、反応容器を氷浴に設置して冷却した。その後、そこへ、水酸化ナトリウム水溶液(1mol/L、1330mL)を加え、反応容器を氷浴で冷却しながら30分間撹拌した。得られた反応液の有機層を抽出し、有機層であるtert-ブチルメチルエーテル溶液を得た。
別途用意した反応容器内をアルゴンガス雰囲気とした後、化合物MC10-c(145g)及びクロロホルム(3200mL)を加え、反応容器を氷浴に設置して冷却した。その後、そこへ、上記で得られたtert-ブチルメチルエーテル溶液を加えた。その後、反応容器を氷浴で冷却しながら7時間攪拌し、次いで、室温で70時間攪拌した。得られた反応液にイオン交換水(3200mL)を加え、有機層を抽出し、トルエン(500mL)を加えて有機層を一部減圧濃縮しトルエン溶液を得た。得られたトルエン溶液をシリカゲルカラムクロマトグラフィー(移動相溶媒:トルエン溶媒)で精製した後、エタノールとメタノールの混合溶媒(質量比1:1)を用いて2回再結晶した。その後、50℃で減圧乾燥させることにより、化合物(H)(129g、収率66%)を白色固体として得た。化合物(H)のHPLC面積百分率値は99.5%以上であった。
After making the inside of the reaction vessel an argon gas atmosphere, 2,6-dimethyl-4-tert-butylphenylhydrazine hydrochloride (101 g) and tert-butyl methyl ether (1070 mL) were added, and the reaction vessel was placed in an ice bath. cooled. After that, an aqueous sodium hydroxide solution (1 mol/L, 1330 mL) was added thereto, and the mixture was stirred for 30 minutes while cooling the reaction vessel in an ice bath. The organic layer of the resulting reaction solution was extracted to obtain a tert-butyl methyl ether solution as the organic layer.
After the inside of a separately prepared reaction vessel was filled with an argon gas atmosphere, compound MC10-c (145 g) and chloroform (3200 mL) were added, and the reaction vessel was placed in an ice bath for cooling. Then, the tert-butyl methyl ether solution obtained above was added thereto. After that, the reaction vessel was stirred for 7 hours while cooling in an ice bath, and then stirred at room temperature for 70 hours. Ion-exchanged water (3200 mL) was added to the resulting reaction solution, the organic layer was extracted, toluene (500 mL) was added, and the organic layer was partially concentrated under reduced pressure to obtain a toluene solution. The resulting toluene solution was purified by silica gel column chromatography (mobile phase solvent: toluene solvent), and then recrystallized twice using a mixed solvent of ethanol and methanol (mass ratio 1:1). After that, by drying under reduced pressure at 50°C, compound (H) (129 g, yield 66%) was obtained as a white solid. The HPLC area percentage value of compound (H) was 99.5% or more.
化合物(H)のLC-MS及びNMRの測定結果は、以下のとおりであった。
LC-MS(ESI,positive):m/z=542.4[M+H]+
1H-NMR(CDCl3,400MHz):δ(ppm)=7.90(2H,s),7.80(1H,d),7.58-7.55(1H,m),7.48(1H,d),7.
38(1H,t),7.27-7.10(3H,m),2.35(6H,s),1.94(6H,s),1.34(9H,s).
The measurement results of LC-MS and NMR of compound (H) were as follows.
LC-MS (ESI, positive): m/z=542.4 [M+H] +
1 H-NMR (CDCl 3 , 400 MHz): δ (ppm) = 7.90 (2H, s), 7.80 (1H, d), 7.58-7.55 (1H, m), 7.48 (1H, d), 7.
38 (1H, t), 7.27-7.10 (3H, m), 2.35 (6H, s), 1.94 (6H, s), 1.34 (9H, s).
反応容器内をアルゴンガス雰囲気とした後、化合物(H)(87g)、4-tert-ブチルフェニルボロン酸(35g)、ビス(ジ-tert-ブチル(4-ジメチルアミノフェニル)ホスフィン)ジクロロパラジウム(II)(1.3g)、トルエン(1500mL)及び20質量%テトラブチルアンモニウムヒドロキシド水溶液(555g)を加え、加熱還流下で4時間撹拌した。室温まで冷却後、そこへ、イオン交換水を加え、有機層を抽出した。得られた有機層をイオン交換水で洗浄し、有機層を得た。得られた有機層を無水硫酸ナトリウムで乾燥させた後、シリカゲル(170g)を加えてろ過し、得られたろ液を減圧濃縮することにより固体を得た。得られた固体を酢酸エチルとアセトニトリル(体積比1:1)の混合溶媒を用いて2回再結晶した。その後、50℃で減圧乾燥させることにより、化合物(I)(73g、収率76%)を白色固体として得た。化合物(I)のHPLC面積百分率値は99.5%以上であった。 After making the inside of the reaction vessel an argon gas atmosphere, compound (H) (87 g), 4-tert-butylphenylboronic acid (35 g), bis(di-tert-butyl(4-dimethylaminophenyl)phosphine)dichloropalladium ( II) (1.3 g), toluene (1500 mL) and 20 mass % tetrabutylammonium hydroxide aqueous solution (555 g) were added, and the mixture was stirred under reflux with heating for 4 hours. After cooling to room temperature, ion-exchanged water was added thereto, and the organic layer was extracted. The obtained organic layer was washed with ion-exchanged water to obtain an organic layer. After drying the obtained organic layer with anhydrous sodium sulfate, silica gel (170 g) was added and filtered, and the obtained filtrate was concentrated under reduced pressure to obtain a solid. The resulting solid was recrystallized twice using a mixed solvent of ethyl acetate and acetonitrile (volume ratio 1:1). Then, it was dried under reduced pressure at 50° C. to obtain compound (I) (73 g, yield 76%) as a white solid. The HPLC area percentage value of compound (I) was 99.5% or more.
化合物(I)のLC-MSの測定結果は、以下のとおりであった。
LC-MS(ESI,positive):m/z=486.3[M+H]+
The LC-MS measurement results of compound (I) were as follows.
LC-MS (ESI, positive): m/z = 486.3 [M+H] +
反応容器内をアルゴンガス雰囲気とした後、塩化イリジウムn水和物(10.1g)、化合物(I)(32.3g)、イオン交換水(81mL)及びジグライム(253mL)を加え、140℃で48時間加熱攪拌した。その後、そこへ、トルエンを加え、イオン交換水で洗浄し、有機層を得た。得られた有機層を減圧濃縮することにより固体を得た。得られた固体をシリカゲルクロマトグラフィー(移動相溶媒:トルエンとエタノールの混合溶媒)で精製した。その後、50℃で減圧乾燥させることにより、黄褐色固体(38.0g)を得た。
別途用意した反応容器内をアルゴンガス雰囲気とした後、上記で得られた固体(30.8g)、トリフルオロメタンスルホン酸銀(11.2g)、化合物(I)(19.7g)、ジフェニルエーテル(76mL)及び2,6-ルチジン(16.9mL)を加え、165℃で50時間加熱攪拌した。その後室温まで冷却してトルエンを加え、セライトを敷いたろ過器でろ過し、得られたろ液にシリカゲル(228g)を加えてろ過し、得られたろ液を減圧濃縮することにより黄色液体を得た。得られた液体にヘキサン(760mL)を加えて0℃で1時間撹拌することにより沈殿を析出させた。沈殿物をろ過して回収し、得られた沈殿物トルエンとヘプタン(体積比3:10)の混合溶媒を用いて2回再結晶した。その後、50℃で減圧乾燥させることにより、金属錯体MC10(15.8g、収率30%)を黄色固体として得た。金属錯体MC10のHPLC面積百分率値は99.5%以上であった。
After making the inside of the reaction vessel an argon gas atmosphere, iridium chloride n-hydrate (10.1 g), compound (I) (32.3 g), ion-exchanged water (81 mL) and diglyme (253 mL) were added, and the mixture was heated at 140°C. The mixture was heated and stirred for 48 hours. After that, toluene was added thereto and washed with ion-exchanged water to obtain an organic layer. A solid was obtained by concentrating the obtained organic layer under reduced pressure. The resulting solid was purified by silica gel chromatography (mobile phase solvent: mixed solvent of toluene and ethanol). Then, it was dried under reduced pressure at 50° C. to obtain a yellowish brown solid (38.0 g).
After an argon gas atmosphere was created in a separately prepared reaction vessel, the solid obtained above (30.8 g), silver trifluoromethanesulfonate (11.2 g), compound (I) (19.7 g), and diphenyl ether (76 mL) were mixed. ) and 2,6-lutidine (16.9 mL) were added, and the mixture was heated and stirred at 165° C. for 50 hours. After that, the mixture was cooled to room temperature, toluene was added, and the mixture was filtered through a filter covered with celite. Silica gel (228 g) was added to the obtained filtrate, the obtained filtrate was filtered, and the obtained filtrate was concentrated under reduced pressure to obtain a yellow liquid. . Hexane (760 mL) was added to the resulting liquid, and the mixture was stirred at 0°C for 1 hour to precipitate a precipitate. The precipitate was collected by filtration, and the obtained precipitate was recrystallized twice using a mixed solvent of toluene and heptane (volume ratio: 3:10). Then, by drying under reduced pressure at 50° C., metal complex MC10 (15.8 g, yield 30%) was obtained as a yellow solid. The HPLC area percentage value of metal complex MC10 was 99.5% or more.
金属錯体MC10のLC-MS及びNMRの測定結果は、以下のとおりであった。
LC-MS(APCI,positive):m/z=1815.0[M+H]+
1H-NMR(CD2Cl2,300MHz):δ(ppm)=8.03(s,6H),7.35(s,6H),7.31-7.26(m,6H),7.11-7.03(m,6H),6.98-6.90(m,6H)6.62-6.57(m,3H),6.52(d,3H),2.11(s,18H),1.97(s,9H),1.68(s,9H),1
.46(s,27H),1.33(s,27H).
The LC-MS and NMR measurement results of the metal complex MC10 were as follows.
LC-MS (APCI, positive): m/z=1815.0 [M+H] +
1 H-NMR (CD 2 Cl 2 , 300 MHz): δ (ppm) = 8.03 (s, 6H), 7.35 (s, 6H), 7.31-7.26 (m, 6H), 7 .11-7.03 (m, 6H), 6.98-6.90 (m, 6H) 6.62-6.57 (m, 3H), 6.52 (d, 3H), 2.11 ( s, 18H), 1.97 (s, 9H), 1.68 (s, 9H), 1
. 46 (s, 27H), 1.33 (s, 27H).
<化合物B1~B9の合成及び入手>
化合物B1は、Luminescence Technology社製を用いた。
化合物B2は、後述の方法で合成した。
化合物B3及びB4は、国際公開第2015/102118号に記載の方法に準じて合成した。
化合物B5~B8は、以下の方法で合成した。
化合物B9は、Angew.Chem.Int.Ed.2020,59,17442-17446に記載の方法に準じて合成した。
<Synthesis and acquisition of compounds B1 to B9>
The compound B1 used was manufactured by Luminescence Technology.
Compound B2 was synthesized by the method described below.
Compounds B3 and B4 were synthesized according to the method described in WO2015/102118.
Compounds B5 to B8 were synthesized by the following method.
Compound B9 is described in Angew. Chem. Int. Ed. 2020, 59, 17442-17446.
化合物B1のΔESTは、0.49eVであった。化合物B1の室温における発光スペクトルの最大ピーク波長は452nmであった。化合物B1の室温における発光スペクトルの最大ピークの半値幅は、22nmであった。
化合物B2のΔESTは、0.43eVであった。化合物B2の室温における発光スペクトルの最大ピーク波長は465nmであった。化合物B2の室温における発光スペクトルの最大ピークの半値幅は、21nmであった。
化合物B3のΔESTは、0.46eVであった。化合物B3の室温における発光スペクトルの最大ピーク波長は454nmであった。化合物B3の室温における発光スペクトルの最大ピークの半値幅は、21nmであった。
化合物B4のΔESTは、0.47eVであった。化合物B4の室温における発光スペクトルの最大ピーク波長は440nmであった。化合物B4の室温における発光スペクトルの最大ピークの半値幅は、19nmであった。
化合物B5のΔESTは、0.45eVであった。化合物B5の室温における発光スペクトルの最大ピーク波長は465nmであった。化合物B5の室温における発光スペクトルの最大ピークの半値幅は、18nmであった。
化合物B6のΔESTは、0.46eVであった。化合物B6の室温における発光スペクトルの最大ピーク波長は469nmであった。化合物B6の室温における発光スペクトルの最大ピークの半値幅は、19nmであった。
化合物B7のΔESTは、0.38eVであった。化合物B7の室温における発光スペクトルの最大ピーク波長は471nmであった。化合物B7の室温における発光スペクトルの最大ピークの半値幅は、20nmであった。
化合物B8のΔESTは、0.41eVであった。化合物B8の室温における発光スペクトルの最大ピーク波長は477nmであった。化合物B8の室温における発光スペクトルの最大ピークの半値幅は、21nmであった。
化合物B9のΔESTは、0.32eVであった。化合物B9の室温における発光スペクトルの最大ピーク波長は514nmであった。化合物B9の室温における発光スペクトルの最大ピークの半値幅は、38nmであった。
The ΔEST of compound B1 was 0.49 eV. The maximum peak wavelength of the emission spectrum of compound B1 at room temperature was 452 nm. The maximum peak half width of the emission spectrum of compound B1 at room temperature was 22 nm.
The ΔEST of compound B2 was 0.43 eV. The maximum peak wavelength of the emission spectrum of compound B2 at room temperature was 465 nm. The maximum peak half width of the emission spectrum of compound B2 at room temperature was 21 nm.
The ΔEST of compound B3 was 0.46 eV. The maximum peak wavelength of the emission spectrum of compound B3 at room temperature was 454 nm. The maximum peak half width of the emission spectrum of compound B3 at room temperature was 21 nm.
The ΔEST of compound B4 was 0.47 eV. The maximum peak wavelength of the emission spectrum of compound B4 at room temperature was 440 nm. The maximum peak half width of the emission spectrum of compound B4 at room temperature was 19 nm.
The ΔEST of compound B5 was 0.45 eV. The maximum peak wavelength of the emission spectrum of compound B5 at room temperature was 465 nm. The maximum peak half width of the emission spectrum of compound B5 at room temperature was 18 nm.
The ΔEST of compound B6 was 0.46 eV. The maximum peak wavelength of the emission spectrum of compound B6 at room temperature was 469 nm. The maximum peak half width of the emission spectrum of compound B6 at room temperature was 19 nm.
The ΔEST of compound B7 was 0.38 eV. The maximum peak wavelength of the emission spectrum of compound B7 at room temperature was 471 nm. The maximum peak half width of the emission spectrum of compound B7 at room temperature was 20 nm.
The ΔEST of compound B8 was 0.41 eV. The maximum peak wavelength of the emission spectrum of compound B8 at room temperature was 477 nm. The maximum peak half width of the emission spectrum of compound B8 at room temperature was 21 nm.
The ΔEST of compound B9 was 0.32 eV. The maximum peak wavelength of the emission spectrum of compound B9 at room temperature was 514 nm. The half width of the maximum peak of the emission spectrum of compound B9 at room temperature was 38 nm.
<化合物B2の合成>
下記の方法で、化合物B2を合成した。
<Synthesis of Compound B2>
Compound B2 was synthesized by the following method.
反応容器内を窒素ガス雰囲気とした後、アンゲヴァンテ・ケミー・インターナショナル・エディション(Angewandte Chemie, International Edition),2018年,第57巻,11316-11320頁に記載の方法で合成した化合物B2A(22.5g)とクロロベンゼンを加え攪
拌したところに、三ヨウ化ホウ素(16.4g)を加え、90℃で6時間加熱撹拌した。その後、室温まで冷却し、N,N-ジイソプロピルエチルアミン(14.3mL)を滴下し、室温で15分攪拌を継続した。得られた溶液に10質量%亜硫酸ナトリウム水溶液(70mL)を加えた。以上の操作を二度繰り返し、得られた有機層を混合し、10質量%亜硫酸ナトリウム水溶液及びイオン交換で洗浄した。得られた洗浄液を分液し、得られた有機層を硫酸マグネシウムで乾燥させた後、フロリジル45gを積んだ濾過器でろ過した。得られたろ液を濃縮した後、そこにアセトニトリル(340mL)を加え、1時間撹拌し、得られた固体を濾過した。得られた固体をトルエン(790mL)に溶解させた。得られた溶液にカルボラフィン(33g)を加えて1時間攪拌した後、セライトを敷いた濾過器で濾過をする操作を3回行った。得られた溶液を減圧濃縮し、得られた固体をトルエン及びアセトニトリルの混合溶媒、トルエン及びエタノールの混合溶媒を用いて複数回再結晶し、50℃で減圧乾燥させることで化合物B2(30.9g、黄色固体)を得た。
After making the inside of the reaction vessel a nitrogen gas atmosphere, compound B2A (22.5 g) synthesized by the method described in Angewandte Chemie, International Edition, 2018, Vol. 57, pp. 11316-11320 ) and chlorobenzene were added and stirred, boron triiodide (16.4 g) was added, and the mixture was heated and stirred at 90° C. for 6 hours. Then, it was cooled to room temperature, N,N-diisopropylethylamine (14.3 mL) was added dropwise, and stirring was continued at room temperature for 15 minutes. A 10% by mass sodium sulfite aqueous solution (70 mL) was added to the resulting solution. The above operation was repeated twice, and the obtained organic layers were mixed and washed with a 10 mass % sodium sulfite aqueous solution and ion exchange. The obtained washing liquid was separated, and the obtained organic layer was dried with magnesium sulfate, and then filtered through a filter loaded with 45 g of florisil. After concentrating the obtained filtrate, acetonitrile (340 mL) was added thereto, stirred for 1 hour, and the obtained solid was filtered. The resulting solid was dissolved in toluene (790 mL). Carborafin (33 g) was added to the resulting solution, and the mixture was stirred for 1 hour and then filtered through a filter covered with celite, which was repeated three times. The resulting solution was concentrated under reduced pressure, and the resulting solid was recrystallized multiple times using a mixed solvent of toluene and acetonitrile and a mixed solvent of toluene and ethanol, and dried under reduced pressure at 50°C to obtain compound B2 (30.9 g , yellow solid).
化合物B2のLC-MS及びNMRの測定結果は、以下のとおりであった。
LC-MS(APCI,positive):m/z=922[M+H]+
1H-NMR(CDCl3,400MHz)δ(ppm)=9.05(d,1H),9.00(d,1H),8.32(d,1H),8.15(d,1H),7.52(td,2H),7.43(d,1H)7.38(d,1H),7.32-7.22(m,6H),7.20(td,2H)7.13(td,4H),6.65(d,1H),6.16(d,1H),1.62(s,9H),1.48(s,9H),1.43(s,9H),1.36(s,18H),1.34(s,9H).
The measurement results of LC-MS and NMR of compound B2 were as follows.
LC-MS (APCI, positive): m/z = 922 [M+H] +
1 H-NMR (CDCl 3 , 400 MHz) δ (ppm) = 9.05 (d, 1H), 9.00 (d, 1H), 8.32 (d, 1H), 8.15 (d, 1H) , 7.52 (td, 2H), 7.43 (d, 1H) 7.38 (d, 1H), 7.32-7.22 (m, 6H), 7.20 (td, 2H)7. 13 (td, 4H), 6.65 (d, 1H), 6.16 (d, 1H), 1.62 (s, 9H), 1.48 (s, 9H), 1.43 (s, 9H) ), 1.36(s, 18H), 1.34(s, 9H).
<化合物B5の合成>
下記の方法で、化合物B5を合成した。
<Synthesis of compound B5>
Compound B5 was synthesized by the following method.
反応容器内をアルゴン雰囲気とした後、4-ブロモ-4’-tert-ブチルビフェニル(30g)、4-クロロ-2,6-ジメチルアニリン(17.76g)、Pd2(dba)3(dba)0.92(0.88g)、t-Bu3PHBF4(0.95g)、t-BuONa(14.95g)、及びトルエン(900mL)を加え、50℃で4時間撹拌した。その後、室温まで冷却し、反応液を、シリカゲル・セライトを積層したショートカラムでろ過した。ろ液を減圧濃縮することにより粗生成物を得た。この粗生成物をシリカゲルカラムクロマトグラフィー(ヘキサン及びトルエンの混合溶媒)により精製した後、減圧濃縮した。その後、トルエン及びイソプロピルアルコールの混合液で再結晶した後乾燥させることにより、化合物B5A(25.2g、白色固体)を得た。化合物B5AのHPLC面積百分率値は99%であった。 After making the inside of the reaction vessel an argon atmosphere, 4-bromo-4′-tert-butylbiphenyl (30 g), 4-chloro-2,6-dimethylaniline (17.76 g), Pd 2 (dba) 3 (dba) 0.92 (0.88 g), t-Bu 3 PHBF 4 (0.95 g), t-BuONa (14.95 g) and toluene (900 mL) were added and stirred at 50° C. for 4 hours. Then, it was cooled to room temperature, and the reaction solution was filtered through a short column laminated with silica gel and celite. A crude product was obtained by concentrating the filtrate under reduced pressure. This crude product was purified by silica gel column chromatography (mixed solvent of hexane and toluene) and concentrated under reduced pressure. After that, it was recrystallized with a mixed solution of toluene and isopropyl alcohol and then dried to obtain compound B5A (25.2 g, white solid). The HPLC area percentage value for compound B5A was 99%.
化合物B5AのNMRの測定結果は、以下のとおりであった。
1H-NMR(CD2Cl2-d2,400MHz):δ(ppm)=7.44-7.36(m,6H),7.11(s,2H),6.52(td,2H),5.26(br,1H),2.18(s,6H),1.31(s,9H)
The NMR measurement results of compound B5A were as follows.
1 H-NMR (CD 2 Cl 2 -d 2 , 400 MHz): δ (ppm) = 7.44-7.36 (m, 6H), 7.11 (s, 2H), 6.52 (td, 2H ), 5.26 (br, 1H), 2.18 (s, 6H), 1.31 (s, 9H)
反応容器内をアルゴン雰囲気とした後、化合物B5A(24.30g)、1,3-ジブロモ-5-tert-ブチルベンゼン(9.7g)、Pd2(dba)3(dba)0.92(0.56g)、t-Bu3PHBF4(0.60g)、t-BuONa(7.98g)、及びトルエン(291mL)を加え、50℃で4時間撹拌した。その後、室温まで冷却し、反応液を、シリカゲル・セライトを積層したショートカラムでろ過した。ろ液を減圧濃縮することにより粗生成物を得た。この粗生成物をシリカゲルカラムクロマトグラフィー(ヘキサン及びトルエンの混合溶媒)により精製した後、減圧濃縮し、乾燥させることにより、化合物B5B(18.1g、白色固体)を得た。化合物B5BのHPLC面積百分率値は99%であった。 After making the inside of the reaction vessel an argon atmosphere, compound B5A (24.30 g), 1,3-dibromo-5-tert-butylbenzene (9.7 g), Pd 2 (dba) 3 (dba) 0.92 (0 .56 g), t-Bu 3 PHBF 4 (0.60 g), t-BuONa (7.98 g) and toluene (291 mL) were added and stirred at 50° C. for 4 hours. Then, it was cooled to room temperature, and the reaction solution was filtered through a short column laminated with silica gel and celite. A crude product was obtained by concentrating the filtrate under reduced pressure. The crude product was purified by silica gel column chromatography (mixed solvent of hexane and toluene), concentrated under reduced pressure, and dried to obtain compound B5B (18.1 g, white solid). The HPLC area percentage value for compound B5B was 99%.
化合物B5BのNMRの測定結果は、以下のとおりであった。
1H-NMR(CD2Cl2-d2,400MHz):δ(ppm)=7.47-7.45(m,4H),7.41-7.38(m,8H),7.09(s,4H),6.92(td,4H),6.52(d,2H),6.48(t,1H),1.97(s,12H),1.32(s,18H),1.10(s,9H).
The NMR measurement results of compound B5B were as follows.
1 H-NMR (CD 2 Cl 2 -d 2 , 400 MHz): δ (ppm) = 7.47-7.45 (m, 4H), 7.41-7.38 (m, 8H), 7.09 (s, 4H), 6.92 (td, 4H), 6.52 (d, 2H), 6.48 (t, 1H), 1.97 (s, 12H), 1.32 (s, 18H) , 1.10(s, 9H).
反応容器内をアルゴン雰囲気とした後、化合物B5B(18.1g)及びクロロホルム
(363mL)を加え、0℃まで冷却した後、そこに、N-ブロモスクシンイミド(3.93g)を分割して加え攪拌した。その後、亜硫酸ナトリウム水溶液で洗浄後、減圧濃縮した。その後、トルエン(180mL)を加え、シリカゲル・セライトを積層したショートカラムでろ過し、減圧濃縮した。その後、トルエン及びエタノールの混合液で再結晶した後乾燥させることにより、化合物B5C(17.5g、白色固体)を得た。化合物B5CのHPLC面積百分率値は99%であった。
After making the inside of the reaction vessel an argon atmosphere, compound B5B (18.1 g) and chloroform (363 mL) were added, and after cooling to 0° C., N-bromosuccinimide (3.93 g) was added in portions and stirred. bottom. After that, the extract was washed with an aqueous sodium sulfite solution and then concentrated under reduced pressure. After that, toluene (180 mL) was added, filtered through a short column laminated with silica gel/Celite, and concentrated under reduced pressure. Thereafter, the compound B5C (17.5 g, white solid) was obtained by recrystallizing with a mixed solution of toluene and ethanol and then drying. The HPLC area percentage value for compound B5C was 99%.
化合物B5CのNMRの測定結果は、以下のとおりであった。
1H-NMR(CD2Cl2-d2,400MHz):δ(ppm)=7.49-7.33(m,14H),7.06(s,2H),6.99(s,2H),6.88(s,1H),6.84(d,2H),6.65(br,2H),6.32(s,1H),1.89(s,12H),1.42(s,9H),1.31(s,18H).
The NMR measurement results of Compound B5C were as follows.
1 H-NMR (CD 2 Cl 2 -d 2 , 400 MHz): δ (ppm) = 7.49-7.33 (m, 14H), 7.06 (s, 2H), 6.99 (s, 2H ), 6.88 (s, 1H), 6.84 (d, 2H), 6.65 (br, 2H), 6.32 (s, 1H), 1.89 (s, 12H), 1.42 (s, 9H), 1.31 (s, 18H).
反応容器内をアルゴン雰囲気とした後、化合物B5C及びキシレン(429.5mL)を加え、-40℃に冷却した後、そこに、sec-BuLi・シクロヘキサン溶液(1.0M,18.3mL)をゆっくりと加えた。反応液を-10℃で1時間撹拌した。その後、反応液を-60℃まで冷却し、BBr3(3.57mL)を加え、1時間撹拌した。その後90℃まで徐々に昇温し反応させた。その後、反応液を室温まで冷却し、N,N-ジイソプロピルアミン(31.4mL)及びトルエン(258mL)を加え、有機層を亜硫酸ナトリウム水溶液及びイオン交換水で洗浄した。得られた有機層を減圧濃縮することにより黄色固体を得た。得られた固体を、シリカゲルカラムクロマトグラフィー(移動相溶媒:ヘキサン及びトルエンの混合溶媒)により精製した後、減圧濃縮し、乾燥させた。その後、トルエン及びエタノールの混合液で再結晶した後乾燥させることにより、化合物B5D(6.6g、黄色固体)を得た。化合物B5DのHPLC面積百分率値は99%であった。 After making the inside of the reaction vessel an argon atmosphere, compound B5C and xylene (429.5 mL) were added, and after cooling to -40°C, a sec-BuLi/cyclohexane solution (1.0 M, 18.3 mL) was slowly added thereto. added. The reaction was stirred at -10°C for 1 hour. The reaction was then cooled to −60° C., BBr 3 (3.57 mL) was added and stirred for 1 hour. After that, the temperature was gradually raised to 90° C. to cause the reaction. After that, the reaction solution was cooled to room temperature, N,N-diisopropylamine (31.4 mL) and toluene (258 mL) were added, and the organic layer was washed with an aqueous sodium sulfite solution and deionized water. The obtained organic layer was concentrated under reduced pressure to obtain a yellow solid. The resulting solid was purified by silica gel column chromatography (mobile phase solvent: mixed solvent of hexane and toluene), concentrated under reduced pressure, and dried. After that, it was recrystallized with a mixed solution of toluene and ethanol and then dried to obtain compound B5D (6.6 g, yellow solid). The HPLC area percentage value for compound B5D was 99%.
化合物B5DのNMRの測定結果は、以下のとおりであった。
1H-NMR(CD2Cl2-d2,400MHz):δ(ppm)=9.36(d,2H),7.75-7.71(m,6H),7.51(d,4H),7.39(s,4H),6.74(d,2H),6.18(s,2H),1.91(s,12H),1.37(s,18H),1.04(s,9H).
The NMR measurement results of compound B5D were as follows.
1 H-NMR (CD 2 Cl 2 -d 2 , 400 MHz): δ (ppm) = 9.36 (d, 2H), 7.75-7.71 (m, 6H), 7.51 (d, 4H ), 7.39 (s, 4H), 6.74 (d, 2H), 6.18 (s, 2H), 1.91 (s, 12H), 1.37 (s, 18H), 1.04 (s, 9H).
反応容器内をアルゴン雰囲気とした後、化合物B5D(10g)、ビス(ピナコラト)ジボロン(5.72g)、酢酸カリウム(6.5g)、Pd2(dba)3(dba)0.92(0.21g)、2-ジシクロヘキシルホスフィノ-2’,4’,6’-トリイソプロピルビフェニル(0.38g)、シクロペンチルメチルエーテル(130mL)加え、45時間加熱攪拌した。その後、トルエン(130ml)を加え、セライトを敷いたろ過器でろ過し、得られたろ液を減圧濃縮し、アセトニトリルを加え、得られた固体をろ取した。その後、トルエン及び活性炭を加え、室温で30分攪拌した後、セライトを敷いたろ過器でろ過し、得られたろ液を減圧濃縮し、更にトルエン及びアセトニトリルの混合溶媒で再結晶することにより、化合物B5E(5.8g)を黄色固体として得た。化合物B5EのHPLC面積百分率値は99.5%以上を示した。 After the inside of the reaction vessel was replaced with an argon atmosphere, compound B5D (10 g), bis(pinacolato)diboron (5.72 g), potassium acetate (6.5 g), Pd 2 (dba) 3 (dba) 0.92 (0.92 g) were added. 21 g), 2-dicyclohexylphosphino-2′,4′,6′-triisopropylbiphenyl (0.38 g) and cyclopentyl methyl ether (130 mL) were added and heated with stirring for 45 hours. After that, toluene (130 ml) was added, the mixture was filtered through a filter lined with celite, the obtained filtrate was concentrated under reduced pressure, acetonitrile was added, and the obtained solid was collected by filtration. Then, toluene and activated carbon are added, and the mixture is stirred at room temperature for 30 minutes, filtered through a filter lined with celite, the resulting filtrate is concentrated under reduced pressure, and further recrystallized with a mixed solvent of toluene and acetonitrile to give the compound. B5E (5.8 g) was obtained as a yellow solid. The HPLC area percentage value of compound B5E showed more than 99.5%.
化合物B5EのNMRの測定結果は、以下のとおりであった。
1H-NMR(CD2Cl2-d2,400MHz):δ(ppm)=9.37(d,2H),7.77(s,4H),7.73(d,4H),7.68(dd,2H),7.51(d,4H),6.68(d,2H),6.19(s,2H),1.93(s,12H),1.38-1.37(m,42H),1.00(s,9H).
The NMR measurement results of compound B5E were as follows.
1 H-NMR (CD 2 Cl 2 -d 2 , 400 MHz): δ (ppm) = 9.37 (d, 2H), 7.77 (s, 4H), 7.73 (d, 4H), 7. 68 (dd, 2H), 7.51 (d, 4H), 6.68 (d, 2H), 6.19 (s, 2H), 1.93 (s, 12H), 1.38-1.37 (m, 42H), 1.00 (s, 9H).
反応容器内をアルゴン雰囲気とした後、化合物B5E(2.3g)、2-ブロモ-4,6-ジ(4-tert-ブチルフェニル)ベンゼン(1.9g)、Pd2(dba)3(dba)0.92(0.02g)、2-ジシクロヘキシルホスフィノ-2’,6’-ジメトキシビフェニル(0.04g)、トルエン(115ml)及び、40質量%テトラブチルアンモニウムヒドロキシド水溶液(7.1g)、イオン交換水(28mL)加え、1時間加熱攪拌した。得られた反応液を室温まで冷却した後、イオン交換水(40mL)を加え、水層を除去した。得られた有機層をイオン交換水で洗浄後、無水硫酸マグネシウムで乾燥、ろ過し、得られたろ液を減圧濃縮した。トルエン及び活性炭を加え、室温で30分攪拌した後、セライトを敷いたろ過器でろ過し、得られたろ液を減圧濃縮した。トルエン及びアセトニトリルの混合溶媒で再結晶することにより、化合物B5(3.0g)を黄色固体として得た。化合物B5のHPLC面積百分率値は99.0%以上を示した。 After making the inside of the reaction vessel an argon atmosphere, compound B5E (2.3 g), 2-bromo-4,6-di(4-tert-butylphenyl)benzene (1.9 g), Pd 2 (dba) 3 (dba) ) 0.92 (0.02 g), 2-dicyclohexylphosphino-2′,6′-dimethoxybiphenyl (0.04 g), toluene (115 ml), and 40 mass % tetrabutylammonium hydroxide aqueous solution (7.1 g) , ion-exchanged water (28 mL) was added, and the mixture was heated and stirred for 1 hour. After cooling the resulting reaction solution to room temperature, ion-exchanged water (40 mL) was added, and the aqueous layer was removed. The resulting organic layer was washed with ion-exchanged water, dried over anhydrous magnesium sulfate, filtered, and the resulting filtrate was concentrated under reduced pressure. Toluene and activated carbon were added, the mixture was stirred at room temperature for 30 minutes, filtered through a filter covered with celite, and the resulting filtrate was concentrated under reduced pressure. Compound B5 (3.0 g) was obtained as a yellow solid by recrystallization with a mixed solvent of toluene and acetonitrile. The HPLC area percentage value of compound B5 showed 99.0% or more.
化合物B5のLC-MS及びNMRの測定結果は、以下のとおりであった。
LC-MS(APCI positive):m/z=1476.9[M+H]+
1H-NMR(CD2Cl2-d2,400MHz):δ(ppm)= 9.46(d,2H),7.98(d,4H),7.88(t,2H),7.74-7.82(m, 18H),7.54-7.59(m,12H),6.94(d,2H),6.35(s,2H),2.07(t,12H),1.34-1.45(m,54H),1.04-1.08(m,9H)
The measurement results of LC-MS and NMR of compound B5 were as follows.
LC-MS (APCI positive): m/z=1476.9 [M+H] +
1 H-NMR (CD 2 Cl 2 -d 2 , 400 MHz): δ (ppm) = 9.46 (d, 2H), 7.98 (d, 4H), 7.88 (t, 2H), 7. 74-7.82 (m, 18H), 7.54-7.59 (m, 12H), 6.94 (d, 2H), 6.35 (s, 2H), 2.07 (t, 12H) , 1.34-1.45 (m, 54H), 1.04-1.08 (m, 9H)
<化合物B6の合成>
下記の方法で、化合物B6を合成した。
<Synthesis of Compound B6>
Compound B6 was synthesized by the following method.
反応容器内をアルゴン雰囲気とした後、N-(3-クロロ-4-メチルフェニル)-2,6-ジメチル-ベンゼンアミン(20.0g)、1,3-ジブロモ-5-tert-ブチルベンゼン(11.7g)、トリス(ジベンジリデンアセトン)ジパラジウム(1.1g)、トリ-tert-ブチルホスホニウムテトラフルオロボラート(0.72g)、ナトリウムtert-ブトキシド(9.6g)、及びトルエン(500mL)を加え、50℃で4時間撹拌した。その後、水(400mL)を加え室温で撹拌した。反応液を分液し、イオン交換水で洗浄した。得られた洗浄液を分液し、得られた有機層を硫酸マグネシウムで乾燥させた後、ろ過した。得られたろ液を減圧濃縮した後、得られた油状物にトルエンを加え溶解させた後、シリカゲルを敷いたろ過器でろ過して得られたろ液を減圧濃縮した。その後、トルエンと酢酸エチルとアセトニトリルの混合溶媒を用いて2回再結晶を行い、40℃で減圧乾燥させることで、化合物B6A(19.2g、白色固体)を収率77%で得た。化合物B6AのLC面積百分率値は98.6%であった。 After making the inside of the reaction vessel an argon atmosphere, N-(3-chloro-4-methylphenyl)-2,6-dimethyl-benzenamine (20.0 g), 1,3-dibromo-5-tert-butylbenzene ( 11.7 g), tris(dibenzylideneacetone) dipalladium (1.1 g), tri-tert-butylphosphonium tetrafluoroborate (0.72 g), sodium tert-butoxide (9.6 g), and toluene (500 mL) was added and stirred at 50° C. for 4 hours. After that, water (400 mL) was added and stirred at room temperature. The reaction liquid was liquid-separated and washed with ion-exchanged water. The obtained washing liquid was separated, and the obtained organic layer was dried with magnesium sulfate and then filtered. After the obtained filtrate was concentrated under reduced pressure, toluene was added to the obtained oily substance to dissolve it, followed by filtration through a filter covered with silica gel, and the obtained filtrate was concentrated under reduced pressure. Thereafter, recrystallization was performed twice using a mixed solvent of toluene, ethyl acetate, and acetonitrile, and dried under reduced pressure at 40°C to obtain compound B6A (19.2 g, white solid) with a yield of 77%. The LC area percentage value of compound B6A was 98.6%.
化合物B6AのNMRの測定結果は、以下のとおりであった。
1H-NMR(400MHz、CDCl3)δ(ppm)=7.11-7.03(m,6H),6.97(d,2H),6.88(d,2H),6.67(dd,2H),6.51(t,1H),6.42(d,2H),2.34(s,6H),1.92(s,12H),1.07(s ,9H).
The NMR measurement results of compound B6A were as follows.
1 H-NMR (400 MHz, CDCl 3 ) δ (ppm) = 7.11-7.03 (m, 6H), 6.97 (d, 2H), 6.88 (d, 2H), 6.67 ( dd, 2H), 6.51 (t, 1H), 6.42 (d, 2H), 2.34 (s, 6H), 1.92 (s, 12H), 1.07 (s, 9H).
反応容器内をアルゴン雰囲気とした後、化合物B6A(5.5g)、三ヨウ化ホウ素(6.9g)、及び、1,2-ジクロロベンゼン(66mL)を加え、120℃で75時間撹拌した。その後、N,N-ジイソプロピルエチルアミン(6.8mL)、及び、10質量%亜硫酸ナトリウム水溶液(23mL)を加え室温で撹拌した。分液し、イオン交換水で洗浄した。得られた洗浄液を分液し、得られた有機層を硫酸マグネシウムで乾燥させた後、ろ過した。得られたろ液を減圧濃縮した後、トルエンとアセトニトリルの混合溶媒を用いて1回再結晶を行い、40℃で減圧乾燥させることで化合物B6B(2.0g、黄色固体)を収率40%で得た。化合物B6BのLC面積百分率値は96.9%であった。以上の工程を繰り返すことにより、化合物B6Bを必要量得た。 After the inside of the reaction vessel was replaced with an argon atmosphere, compound B6A (5.5 g), boron triiodide (6.9 g) and 1,2-dichlorobenzene (66 mL) were added and stirred at 120° C. for 75 hours. After that, N,N-diisopropylethylamine (6.8 mL) and 10% by mass sodium sulfite aqueous solution (23 mL) were added and stirred at room temperature. It was separated and washed with deionized water. The obtained washing liquid was separated, and the obtained organic layer was dried with magnesium sulfate and then filtered. The resulting filtrate was concentrated under reduced pressure, recrystallized once using a mixed solvent of toluene and acetonitrile, and dried under reduced pressure at 40° C. to give compound B6B (2.0 g, yellow solid) with a yield of 40%. Obtained. The LC area percentage value of compound B6B was 96.9%. The required amount of compound B6B was obtained by repeating the above steps.
化合物B6BのNMRの測定結果は、以下のとおりであった。
1H-NMR(400MHz、CDCl3)δ(ppm)=8.74(s,2H),7.41-7.29(md,6H),6.68(s,2H),6.05(s,2H),2.56(s,6H),1.90(s,12H),0.98(s,9H).
The NMR measurement results of compound B6B were as follows.
1 H-NMR (400 MHz, CDCl 3 ) δ (ppm) = 8.74 (s, 2H), 7.41-7.29 (md, 6H), 6.68 (s, 2H), 6.05 ( s, 2H), 2.56 (s, 6H), 1.90 (s, 12H), 0.98 (s, 9H).
反応容器内をアルゴン雰囲気とした後、化合物B6B(8.0g)、3,6-ジ-tert-ブチルカルバゾール(7.1g)、トリス(ジベンジリデンアセトン)ジパラジウム(0.45g)、2-ジ-tert-ブチルホスフィノ-2’,4’,6’-トリイソプロピルビフェニル(0.66g)、リチウム(ビストリメチルシリル)アミドのトルエン溶液(1mol/L、28mL)、及び、キシレン(76mL)を加え、130℃で6時間撹拌した。その後、分液し、イオン交換水で洗浄した。得られた洗浄液を分液し、得られた有機層を硫酸マグネシウムで乾燥させた後、ろ過した。得られたろ液を減圧濃縮した後、トルエンとヘプタンの混合溶媒を用いてシリカゲルカラム精製を行った。その後、トルエンとアセトニトリルの混合溶媒を用いて複数回再結晶を行い、40℃で減圧乾燥させることで化合物B6(4.0g、黄色固体)を収率28%で得た。化合物B6のLC面積百分率値は97.0%であった。 After making the inside of the reaction vessel an argon atmosphere, compound B6B (8.0 g), 3,6-di-tert-butylcarbazole (7.1 g), tris(dibenzylideneacetone) dipalladium (0.45 g), 2- Di-tert-butylphosphino-2',4',6'-triisopropylbiphenyl (0.66 g), a toluene solution of lithium (bistrimethylsilyl)amide (1 mol/L, 28 mL), and xylene (76 mL) and stirred at 130° C. for 6 hours. Then, it was separated and washed with ion-exchanged water. The obtained washing liquid was separated, and the obtained organic layer was dried with magnesium sulfate and then filtered. After the obtained filtrate was concentrated under reduced pressure, silica gel column purification was performed using a mixed solvent of toluene and heptane. Thereafter, recrystallization was performed multiple times using a mixed solvent of toluene and acetonitrile, and drying was performed under reduced pressure at 40°C to obtain compound B6 (4.0 g, yellow solid) with a yield of 28%. The LC area percentage value of compound B6 was 97.0%.
化合物B6のNMRの測定結果は、以下のとおりであった。
1H-NMR(400MHz、CDCl3)δ(ppm)=9.09(s,2H),8.13(d,4H),7.42(dd,4H),7.24(d,6H),7.00(d,4H),6.82(s,2H),6.12(s,2H),2.11(s,6H),1.99(s,12H),1.47(s,36H),1.00(s,9H).
LC-MS(APCI、positive):m/z=1115.7[M+H]+
The NMR measurement results of compound B6 were as follows.
1 H-NMR (400 MHz, CDCl 3 ) δ (ppm) = 9.09 (s, 2H), 8.13 (d, 4H), 7.42 (dd, 4H), 7.24 (d, 6H) , 7.00 (d, 4H), 6.82 (s, 2H), 6.12 (s, 2H), 2.11 (s, 6H), 1.99 (s, 12H), 1.47 ( s, 36H), 1.00 (s, 9H).
LC-MS (APCI, positive): m/z=1115.7 [M+H] +
<化合物B7の合成>
下記の方法で、化合物B7を合成した。
<Synthesis of compound B7>
Compound B7 was synthesized by the following method.
反応容器内をアルゴン雰囲気とした後、N-(3-クロロフェニル)-2,6-ジメチル-ベンゼンアミン(10.0g)、1,3-ジブロモ-5-tert-ブチルベンゼン(5.8g)、トリス(ジベンジリデンアセトン)ジパラジウム(0.35g)、トリ-tert-ブチルホスホニウムテトラフルオロボラート(0.34g)、ナトリウムtert-ブトキシド(5.7g)、及び、トルエン(250mL)を加え、50℃で5時間撹拌した。その後、水(100mL)を加え室温で撹拌した。分液し、イオン交換水で洗浄した。得られた洗浄液を分液し、得られた有機層を硫酸マグネシウムで乾燥させた後、ろ過した。得られたろ液を減圧濃縮した後、トルエンとヘプタンの混合溶媒(体積比1:9)を用いてシリカゲルカラム精製を行った。その後、トルエンと酢酸エチルとメタノールの混合溶媒を用いて1回再結晶を行い、40℃で減圧乾燥させることで化合物B7A(8.3g、白色固体)を収率71%で得た。化合物B7AのLC面積百分率値は97.8%であった。 After making the inside of the reaction vessel an argon atmosphere, N-(3-chlorophenyl)-2,6-dimethyl-benzenamine (10.0 g), 1,3-dibromo-5-tert-butylbenzene (5.8 g), Tris(dibenzylideneacetone) dipalladium (0.35 g), tri-tert-butylphosphonium tetrafluoroborate (0.34 g), sodium tert-butoxide (5.7 g), and toluene (250 mL) were added and C. for 5 hours. After that, water (100 mL) was added and stirred at room temperature. It was separated and washed with deionized water. The obtained washing liquid was separated, and the obtained organic layer was dried with magnesium sulfate and then filtered. After the obtained filtrate was concentrated under reduced pressure, silica gel column purification was performed using a mixed solvent of toluene and heptane (volume ratio 1:9). Thereafter, recrystallization was performed once using a mixed solvent of toluene, ethyl acetate and methanol, and drying was performed under reduced pressure at 40° C. to obtain compound B7A (8.3 g, white solid) with a yield of 71%. The LC area percentage value for compound B7A was 97.8%.
化合物B7AのNMRの測定結果は、以下のとおりであった。
1H-NMR(400MHz、CD2Cl2)δ(ppm)=7.14-7.02(8H,m),6.79(2H,t),6.73(4H,td),6.53(1H,t),6.50(2H,d),1.95(12H,s),1.05(9H,s).
TLC-MS(positive):m/z=593.2[M+H]+
The NMR measurement results of compound B7A were as follows.
1 H-NMR (400 MHz, CD 2 Cl 2 ) δ (ppm) = 7.14-7.02 (8H, m), 6.79 (2H, t), 6.73 (4H, td), 6. 53 (1H, t), 6.50 (2H, d), 1.95 (12H, s), 1.05 (9H, s).
TLC-MS (positive): m/z = 593.2 [M+H] +
反応容器内をアルゴン雰囲気とした後、化合物B7A(2.0g)、三ヨウ化ホウ素(2.6g)、及び、1,2-ジクロロベンゼン(40mL)を加え、120℃で90時間撹拌した。その後、N,N-ジイソプロピルエチルアミン(8.9g)、及び10質量%亜硫酸ナトリウム水溶液(20mL)を加え室温で撹拌した。分液し、イオン交換水で洗浄した。得られた洗浄液を分液し、得られた有機層を硫酸マグネシウムで乾燥させた後、ろ過した。得られたろ液を減圧濃縮した後、トルエンとアセトニトリルの混合溶媒を用いて1回再結晶を行い、40℃で減圧乾燥させることで化合物B7B(0.76g、黄色固体)を収率30%で得た。化合物B7BのLC面積百分率値は97.6%であった。 After the inside of the reaction vessel was replaced with an argon atmosphere, compound B7A (2.0 g), boron triiodide (2.6 g) and 1,2-dichlorobenzene (40 mL) were added and stirred at 120° C. for 90 hours. After that, N,N-diisopropylethylamine (8.9 g) and 10 mass % sodium sulfite aqueous solution (20 mL) were added and stirred at room temperature. It was separated and washed with deionized water. The obtained washing liquid was separated, and the obtained organic layer was dried with magnesium sulfate and then filtered. The obtained filtrate was concentrated under reduced pressure, recrystallized once using a mixed solvent of toluene and acetonitrile, and dried under reduced pressure at 40° C. to give compound B7B (0.76 g, yellow solid) with a yield of 30%. Obtained. The LC area percentage value of compound B7B was 97.6%.
化合物B7BのNMRの測定結果は、以下のとおりであった。
1H-NMR(400MHz、CD2Cl2)δ(ppm)=8.81(2H,d),7.43-7.32(6H,m),7.20(2H,dd),6.65(2H,d),6.12(2H,s),1.88(12H,s),0.95(9H,s).
TLC-MS(positive):m/z=601.2[M+H]+
The NMR measurement results of compound B7B were as follows.
1 H-NMR (400 MHz, CD 2 Cl 2 ) δ (ppm) = 8.81 (2H, d), 7.43-7.32 (6H, m), 7.20 (2H, dd), 6. 65 (2H,d), 6.12 (2H,s), 1.88 (12H,s), 0.95 (9H,s).
TLC-MS (positive): m/z = 601.2 [M+H] +
反応容器内をアルゴン雰囲気とした後、化合物B7B(0.10g)、4-(1,1-ジメチルエチル)-N-[4-(1,1-ジメチルエチル)フェニル]-N-[4-(4,4,5,5-テトラメチル-1,3,2-ジオキサボロラン-2-イル)フェニル]-ベンゼンアミン(0.18g)、[(ジ(1-アダマンチル)-N-ブチルホスフィン)-2-(2’-アミノ-1,1’-ビフェニル)]パラジウム(II)メタンスルホン酸塩(4.8mg)、5質量%炭酸ナトリウム水溶液(13mL)、及び、トルエン(10mL)を加え、80℃で5時間撹拌した。その後、分液し、イオン交換水で洗浄した。得られた洗浄液を分液し、得られた有機層を硫酸マグネシウムで乾燥させた後、ろ過した。得られたろ液を減圧濃縮した後、トルエンとヘプタンの混合溶媒を用いてシリカゲルカラム精製を行った。その後、トルエンとアセトニトリルの混合溶媒を用いて1回再結晶を行い、40℃で減圧乾燥させることで化合物B7(0.19g、黄色固体)を収率83%で得た。化合物B7のLC面積百分率値は99.9%であった。 After making the inside of the reaction vessel an argon atmosphere, compound B7B (0.10 g), 4-(1,1-dimethylethyl)-N-[4-(1,1-dimethylethyl)phenyl]-N-[4- (4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)phenyl]-benzenamine (0.18 g), [(di(1-adamantyl)-N-butylphosphine)- 2-(2′-Amino-1,1′-biphenyl)]palladium (II) methanesulfonate (4.8 mg), 5% by mass sodium carbonate aqueous solution (13 mL), and toluene (10 mL) were added, and 80 C. for 5 hours. Then, it was separated and washed with ion-exchanged water. The obtained washing liquid was separated, and the obtained organic layer was dried with magnesium sulfate and then filtered. After the obtained filtrate was concentrated under reduced pressure, silica gel column purification was performed using a mixed solvent of toluene and heptane. Thereafter, recrystallization was performed once using a mixed solvent of toluene and acetonitrile, and dried under reduced pressure at 40° C. to obtain compound B7 (0.19 g, yellow solid) with a yield of 83%. The LC area percentage value of compound B7 was 99.9%.
化合物B7のNMRの測定結果は、以下のとおりであった。
1H-NMR(400MHz、CD2Cl2)δ(ppm)=9.01(2H,d),7.48(2H,d),7.42-7.30(10H,m),7.28(8H,d),7.03-6.95(12H,m),6.85(2H,d),6.12(2H,s),1.
92(12H,s),1.29(36H,s),0.98(9H,s).
TLC-MS(positive):m/z=1243.5[M+H]+
The NMR measurement results of compound B7 were as follows.
1 H-NMR (400 MHz, CD 2 Cl 2 ) δ (ppm) = 9.01 (2H, d), 7.48 (2H, d), 7.42-7.30 (10H, m), 7. 28 (8H, d), 7.03-6.95 (12H, m), 6.85 (2H, d), 6.12 (2H, s), 1.
92 (12H,s), 1.29 (36H,s), 0.98 (9H,s).
TLC-MS (positive): m/z=1243.5 [M+H] +
<化合物B8の合成>
下記の方法で、化合物B8を合成した。
<Synthesis of compound B8>
Compound B8 was synthesized by the following method.
反応容器内をアルゴン雰囲気とした後、2-ブロモ-5-tert-ブチル-1,3-ジメチルベンゼン(5.0g)、3-クロロアニリン(3.2g)、トリス(ジベンジリデンアセトン)ジパラジウム(0.10g)、トリ-tert-ブチルホスホニウムテトラフルオロボラート(0.10g)、ナトリウムtert-ブトキシド(4.0g)、及び、トルエン(90mL)を加え、50℃で5時間撹拌した。その後、水(10mL)を加え室温で撹拌した。分液し、イオン交換水で洗浄した。得られた洗浄液を分液し、得られた有機層を硫酸マグネシウムで乾燥させた後、ろ過した。得られたろ液を減圧濃縮した後、トルエンとヘプタンの混合溶媒(体積比2:8)を用いてシリカゲルカラム精製を行った。その後、メタノールを用いて1回再結晶を行い、40℃で減圧乾燥させることで化合物B8A(3.8g、白色固体)を収率64%で得た。化合物B8AのGC面積百分率
値は99.7%であった。
After making the inside of the reaction vessel an argon atmosphere, 2-bromo-5-tert-butyl-1,3-dimethylbenzene (5.0 g), 3-chloroaniline (3.2 g), tris(dibenzylideneacetone) dipalladium (0.10 g), tri-tert-butylphosphonium tetrafluoroborate (0.10 g), sodium tert-butoxide (4.0 g) and toluene (90 mL) were added and stirred at 50° C. for 5 hours. After that, water (10 mL) was added and the mixture was stirred at room temperature. It was separated and washed with deionized water. The obtained washing liquid was separated, and the obtained organic layer was dried with magnesium sulfate and then filtered. After the obtained filtrate was concentrated under reduced pressure, silica gel column purification was performed using a mixed solvent of toluene and heptane (volume ratio 2:8). Then, it was recrystallized once using methanol and dried under reduced pressure at 40° C. to obtain compound B8A (3.8 g, white solid) with a yield of 64%. The GC area percentage value of compound B8A was 99.7%.
化合物B8AのNMRの測定結果は、以下のとおりであった。
1H-NMR(400MHz、CD2Cl2)δ(ppm)=7.12-7.07(3H,m),7.04(1H,t),6.69(1H,t),6.82(1H,d),6.77(1H,d),6.44(1H,d),6.17(1H,d),6.10(1H,t),5.70(1H,broad-s),5.19(1H,broad-s),2.19(6H,s),1.29(9H,s).
TLC-MS(positive):m/z=288.1[M+H]+
The NMR measurement results of compound B8A were as follows.
1 H-NMR (400 MHz, CD 2 Cl 2 ) δ (ppm) = 7.12-7.07 (3H, m), 7.04 (1H, t), 6.69 (1H, t), 6.69 (1H, t); 82 (1H, d), 6.77 (1H, d), 6.44 (1H, d), 6.17 (1H, d), 6.10 (1H, t), 5.70 (1H, broad -s), 5.19 (1H, broad-s), 2.19 (6H, s), 1.29 (9H, s).
TLC-MS (positive): m/z = 288.1 [M+H] +
反応容器内をアルゴン雰囲気とした後、化合物B8A(3.7g)、1,3-ジブロモ-5-tert-ブチルベンゼン(1.9g)、トリス(ジベンジリデンアセトン)ジパラジウム(0.11g)、トリ-tert-ブチルホスホニウムテトラフルオロボラート(0.11g)、ナトリウムtert-ブトキシド(1.8g)、及び、トルエン(44mL)を加え、50℃で5時間撹拌した。その後、水(20mL)を加え室温で撹拌した。分液し、イオン交換水で洗浄した。得られた洗浄液を分液し、得られた有機層を硫酸マグネシウムで乾燥させた後、ろ過した。得られたろ液を減圧濃縮した後、トルエンとヘプタンの混合溶媒(体積比1:9)を用いてシリカゲルカラム精製を行った。その後、トルエンと酢酸エチルとアセトニトリルの混合溶媒を用いて1回再結晶を行い、40℃で減圧乾燥させることで化合物B8B(2.5g、白色固体)を収率55%で得た。化合物B8BのLC面積百分率値は97.7%であった。 After making the inside of the reaction vessel an argon atmosphere, compound B8A (3.7 g), 1,3-dibromo-5-tert-butylbenzene (1.9 g), tris(dibenzylideneacetone) dipalladium (0.11 g), Tri-tert-butylphosphonium tetrafluoroborate (0.11 g), sodium tert-butoxide (1.8 g) and toluene (44 mL) were added and stirred at 50° C. for 5 hours. After that, water (20 mL) was added and stirred at room temperature. It was separated and washed with deionized water. The obtained washing liquid was separated, and the obtained organic layer was dried with magnesium sulfate and then filtered. After the obtained filtrate was concentrated under reduced pressure, silica gel column purification was performed using a mixed solvent of toluene and heptane (volume ratio 1:9). Thereafter, recrystallization was performed once using a mixed solvent of toluene, ethyl acetate, and acetonitrile, and dried under reduced pressure at 40°C to obtain compound B8B (2.5 g, white solid) with a yield of 55%. The LC area percentage value for compound B8B was 97.7%.
化合物B8BのNMRの測定結果は、以下のとおりであった。
1H-NMR(400MHz、CD2Cl2)δ(ppm)=7.06(4H,s),7.02(2H,t),6.78(2H,t),6.73-6.68(4H,m),6.58(2H,d),6.36(1H,t),1.92(12H,s),1.30(18H,s),1.08(9H,s).
TLC-MS(positive):m/z=705.3[M+H]+
The NMR measurement results of compound B8B were as follows.
1 H-NMR (400 MHz, CD 2 Cl 2 ) δ (ppm) = 7.06 (4H, s), 7.02 (2H, t), 6.78 (2H, t), 6.73-6. 68 (4H,m), 6.58 (2H,d), 6.36 (1H,t), 1.92 (12H,s), 1.30 (18H,s), 1.08 (9H,s) ).
TLC-MS (positive): m/z=705.3 [M+H] +
反応容器内をアルゴン雰囲気とした後、化合物B8B(2.0g)、三ヨウ化ホウ素(2.2g)、及び、1,2-ジクロロベンゼン(40mL)を加え、120℃で90時間撹拌した。その後、N,N-ジイソプロピルエチルアミン(7.5g)、10質量%亜硫酸ナトリウム水溶液(20mL)を加え室温で撹拌した。分液し、イオン交換水で洗浄した。得られた洗浄液を分液し、得られた有機層を硫酸マグネシウムで乾燥させた後、ろ過した。得られたろ液を減圧濃縮した後、トルエンとアセトニトリルの混合溶媒を用いて1回再結晶を行い、40℃で減圧乾燥させることで化合物B8C(1.1g、黄色固体)を収率50%で得た。化合物B8CのLC面積百分率値は92.0%であった。 After the inside of the reaction vessel was replaced with an argon atmosphere, compound B8B (2.0 g), boron triiodide (2.2 g) and 1,2-dichlorobenzene (40 mL) were added and stirred at 120° C. for 90 hours. After that, N,N-diisopropylethylamine (7.5 g) and 10 mass % sodium sulfite aqueous solution (20 mL) were added and stirred at room temperature. It was separated and washed with deionized water. The obtained washing liquid was separated, and the obtained organic layer was dried with magnesium sulfate and then filtered. The resulting filtrate was concentrated under reduced pressure, recrystallized once using a mixed solvent of toluene and acetonitrile, and dried under reduced pressure at 40° C. to give compound B8C (1.1 g, yellow solid) with a yield of 50%. Obtained. The LC area percentage value of compound B8C was 92.0%.
化合物B8CのNMRの測定結果は、以下のとおりであった。
1H-NMR(400MHz、CD2Cl2)δ(ppm)=8.80(2H,d),7.36(4H,s),7.19(2H,dd),6.72(2H,d),6.07(2H,s),1.85(12H,s),1.41(18H,s),0.94(9H,s).
TLC-MS(positive):m/z=713.3[M+H]+
The NMR measurement results of compound B8C were as follows.
1 H-NMR (400 MHz, CD 2 Cl 2 ) δ (ppm) = 8.80 (2H, d), 7.36 (4H, s), 7.19 (2H, dd), 6.72 (2H, d), 6.07 (2H,s), 1.85 (12H,s), 1.41 (18H,s), 0.94 (9H,s).
TLC-MS (positive): m/z=713.3 [M+H] +
反応容器内をアルゴン雰囲気とした後、化合物B8C(0.30g)、2-[4,4’-ビス(1,1-ジメチルエチル)[1,1’:3’,1’-ターフェニル]-5’-イル]-4,4,5,5-テトラメチル-1,3,2-ジオキサボロラン(0.43g)、[(ジ(1-アダマンチル)-N-ブチルホスフィン)-2-(2’-アミノ-1,1’-ビフェニル)]パラジウム(II)メタンスルホン酸塩(12mg)、5質量%炭酸ナトリウム水溶液(15mL)、及び、トルエン(15mL)を加え、80℃で5時間撹拌した
。その後、分液し、イオン交換水で洗浄した。得られた洗浄液を分液し、得られた有機層を硫酸マグネシウムで乾燥させた後、ろ過した。得られたろ液を減圧濃縮した後、トルエンとヘプタンの混合溶媒を用いてシリカゲルカラム精製を行った。その後、トルエンとアセトニトリルの混合溶媒を用いて1回再結晶を行い、40℃で減圧乾燥させることで化合物B8(0.34g、黄色固体)を収率61%で得た。化合物B8のLC面積百分率値は99.7%であった。
After making the inside of the reaction vessel an argon atmosphere, compound B8C (0.30 g), 2-[4,4′-bis(1,1-dimethylethyl)[1,1′:3′,1′-terphenyl] -5′-yl]-4,4,5,5-tetramethyl-1,3,2-dioxaborolane (0.43 g), [(di(1-adamantyl)-N-butylphosphine)-2-(2 '-Amino-1,1'-biphenyl)]palladium (II) methanesulfonate (12 mg), 5 wt% sodium carbonate aqueous solution (15 mL), and toluene (15 mL) were added and stirred at 80°C for 5 hours. . Then, it was separated and washed with ion-exchanged water. The obtained washing liquid was separated, and the obtained organic layer was dried with magnesium sulfate and then filtered. After the obtained filtrate was concentrated under reduced pressure, silica gel column purification was performed using a mixed solvent of toluene and heptane. After that, recrystallization was performed once using a mixed solvent of toluene and acetonitrile, and dried under reduced pressure at 40° C. to obtain compound B8 (0.34 g, yellow solid) with a yield of 61%. The LC area percentage value of compound B8 was 99.7%.
化合物B8のNMRの測定結果は、以下のとおりであった。
1H-NMR(400MHz、CD2Cl2)δ(ppm)=9.11(2H,d),
7.75(2H,t),7.70(4H,d),7.66(2H,dd),7.57(8H,d),7.48(8H,d),7.40(4H,s),7.06(2H,d),6.26(2H,s),1.94(12H,s),1.41(18H,s),1.36(36H,s),1.12(9H,s).
TLC-MS(positive):m/z=1324.6[M+H]+
The NMR measurement results of compound B8 were as follows.
1 H-NMR (400 MHz, CD 2 Cl 2 ) δ (ppm) = 9.11 (2H, d),
7.75 (2H, t), 7.70 (4H, d), 7.66 (2H, dd), 7.57 (8H, d), 7.48 (8H, d), 7.40 (4H , s), 7.06 (2H, d), 6.26 (2H, s), 1.94 (12H, s), 1.41 (18H, s), 1.36 (36H, s), 1 .12(9H,s).
TLC-MS (positive): m/z=1324.6 [M+H] +
<化合物M1~M12、B10及びB11、金属錯体MC12の合成>
化合物M1は、国際公開第2015/145871号に記載の方法に従って合成した。
化合物M2は、国際公開第2013/146806号に記載の方法に従って合成した。
化合物M3は、国際公開第2005/049546号に記載の方法に従って合成した。
化合物M4は、特開2010-180630号公報に記載の方法に従って合成した。
化合物M5は、国際公開第2013/191088号に記載の方法に準じて合成した。
化合物M6は、国際公開第2015/145871号に記載の方法に従って合成した。
化合物M7は、特開2011-174062号公報に記載の方法に従って合成した。
化合物M8及び化合物M9は、市販品を用いた。
化合物M10は、国際公開第2012/086671号に記載の方法に従って合成した。
化合物M11は、国際公開第2016/031639号に記載の方法に従って合成した。
化合物M12は、特開2012-036388号公報に記載の方法に準じて合成した。
化合物B10及びB11は、国際公開第2019/004248号に記載の方法に準じて合成した。
金属錯体MC12は、特開2015-038195号公報に記載の方法に従って合成した。
<Synthesis of Compounds M1 to M12, B10 and B11, and Metal Complex MC12>
Compound M1 was synthesized according to the method described in WO2015/145871.
Compound M2 was synthesized according to the method described in WO2013/146806.
Compound M3 was synthesized according to the method described in WO2005/049546.
Compound M4 was synthesized according to the method described in JP-A-2010-180630.
Compound M5 was synthesized according to the method described in International Publication No. 2013/191088.
Compound M6 was synthesized according to the method described in WO2015/145871.
Compound M7 was synthesized according to the method described in JP-A-2011-174062.
Commercially available products were used for compound M8 and compound M9.
Compound M10 was synthesized according to the method described in WO2012/086671.
Compound M11 was synthesized according to the method described in WO2016/031639.
Compound M12 was synthesized according to the method described in JP-A-2012-036388.
Compounds B10 and B11 were synthesized according to the method described in WO2019/004248.
Metal complex MC12 was synthesized according to the method described in JP-A-2015-038195.
<高分子化合物HTL-1の合成>
高分子化合物HTL-1は、化合物M1、化合物M2及び化合物M3を用いて、国際公開第2015/145871号に記載の方法に従って合成した。高分子化合物HTL-1のMnは2.3×104であり、Mwは1.2×105であった。
高分子化合物HTL-1は、仕込み原料の量から求めた理論値では、化合物M1から誘導される構成単位と、化合物M2から誘導される構成単位と、化合物M3から誘導される構成単位とが、45:5:50のモル比で構成されてなる共重合体である。
<Synthesis of polymer compound HTL-1>
Polymer compound HTL-1 was synthesized using compound M1, compound M2 and compound M3 according to the method described in WO 2015/145871. The Mn of the polymer compound HTL-1 was 2.3×10 4 and the Mw was 1.2×10 5 .
In the polymer compound HTL-1, the theoretical values obtained from the amounts of the raw materials charged are the structural units derived from the compound M1, the structural units derived from the compound M2, and the structural units derived from the compound M3. It is a copolymer composed of a molar ratio of 45:5:50.
<高分子化合物BP1の合成>
(工程1)反応容器内を不活性ガス雰囲気とした後、化合物M4(0.3444g)、化合物M5(0.5762g)、化合物B10(0.0851g)、ジクロロビス(トリス-o-メトキシフェニルホスフィン)パラジウム(0.27mg)及びトルエン(30mL)を加え、80℃に加熱した。
(工程2)その後、そこへ、20質量%水酸化テトラエチルアンモニウム水溶液(16.0g)を滴下し、6時間還流させた。
(工程3)その後、そこへ、フェニルボロン酸(45.7mg)及びジクロロビス(トリス-o-メトキシフェニルホスフィン)パラジウム(0.27mg)を加え、80℃で3時間撹拌した。
(工程4)反応混合物を冷却した後、ジエチルジチアカルバミン酸ナトリウム水溶液を加え、40℃で1時間撹拌した。反応液を冷却し、水層を除去した後、得られた有機層を、3質量%アンモニア水で2回、水で2回洗浄した。得られた溶液をメタノールに滴下し、攪拌したところ、沈澱が生じた。沈殿物をトルエン(44mL)に溶解させ、アルミナ(26g)加え3時間撹拌した後、得られた懸濁液をシリカゲルカラムに通液することにより精製した。得られた溶液をメタノールに滴下し、撹拌したところ、沈殿が生じた。得られた沈殿物をろ取し、乾燥させることにより、高分子化合物BP1を0.51g得た。高分子化合物BP1のMnは6.2×104であり、Mwは1.5×105であった。
高分子化合物BP1は、仕込み原料の量から求めた理論値では、化合物M4から誘導される構成単位と、化合物M5から誘導される構成単位と、化合物B10から誘導される構成単位とが、50:45:5のモル比で構成された共重合体である。
<Synthesis of polymer compound BP1>
(Step 1) After making the inside of the reaction vessel an inert gas atmosphere, compound M4 (0.3444 g), compound M5 (0.5762 g), compound B10 (0.0851 g), dichlorobis(tris-o-methoxyphenylphosphine) Palladium (0.27 mg) and toluene (30 mL) were added and heated to 80°C.
(Step 2) Thereafter, a 20% by mass tetraethylammonium hydroxide aqueous solution (16.0 g) was added dropwise thereto, and refluxed for 6 hours.
(Step 3) After that, phenylboronic acid (45.7 mg) and dichlorobis(tris-o-methoxyphenylphosphine)palladium (0.27 mg) were added thereto and stirred at 80° C. for 3 hours.
(Step 4) After cooling the reaction mixture, an aqueous sodium diethyldithiacarbamate solution was added, and the mixture was stirred at 40°C for 1 hour. After cooling the reaction solution and removing the aqueous layer, the resulting organic layer was washed twice with 3 mass % aqueous ammonia and twice with water. The resulting solution was added dropwise to methanol and stirred to cause precipitation. The precipitate was dissolved in toluene (44 mL), alumina (26 g) was added, and the mixture was stirred for 3 hours, and the resulting suspension was passed through a silica gel column for purification. The resulting solution was added dropwise to methanol and stirred to produce a precipitate. The resulting precipitate was collected by filtration and dried to obtain 0.51 g of polymer compound BP1. Mn of the polymer compound BP1 was 6.2×10 4 and Mw was 1.5×10 5 .
In the polymer compound BP1, the theoretical value obtained from the amount of the raw material charged is that the structural unit derived from the compound M4, the structural unit derived from the compound M5, and the structural unit derived from the compound B10 are 50: It is a copolymer made up of a 45:5 molar ratio.
<高分子化合物BP2の合成>
(工程1)反応容器内を不活性ガス雰囲気とした後、化合物M4(0.3070g)、化合物M5(0.6403g)、化合物B11(0.0927g)、ジクロロビス(トリス-o-メトキシフェニルホスフィン)パラジウム(0.27mg)及びトルエン(31mL)を加え、80℃に加熱した。
(工程2)その後、そこへ、20質量%水酸化テトラエチルアンモニウム水溶液(15.7g)を滴下し、6時間還流させた。
(工程3)その後、そこへ、フェニルボロン酸(45.7mg)及びジクロロビス(トリス-o-メトキシフェニルホスフィン)パラジウム(0.27mg)を加え、80℃で3時間撹拌した。
(工程4)反応混合物を冷却した後、ジエチルジチアカルバミン酸ナトリウム水溶液を加え、40℃で1時間撹拌した。反応液を冷却し、水層を除去した後、得られた有機層を、3質量%アンモニア水で2回、水で2回洗浄した。得られた溶液をメタノールに滴下し、攪拌したところ、沈澱が生じた。沈殿物をトルエン(44mL)に溶解させ、アルミナ(27g)加え3時間撹拌した後、得られた懸濁液をシリカゲルカラムに通液することにより精製した。得られた溶液をメタノールに滴下し、撹拌したところ、沈殿が生じた。沈殿物をろ取し、乾燥させることにより、高分子化合物BP2を0.52g得た。
高分子化合物BP2のMnは6.3×104であり、Mwは1.5×105であった。
高分子化合物BP2は、仕込み原料の量から求めた理論値では、化合物M4から誘導される構成単位と、化合物M5から誘導される構成単位と、化合物B11から誘導される構成単位とが、45:50:5のモル比で構成された共重合体である。
<Synthesis of polymer compound BP2>
(Step 1) After making the inside of the reaction vessel an inert gas atmosphere, compound M4 (0.3070 g), compound M5 (0.6403 g), compound B11 (0.0927 g), dichlorobis(tris-o-methoxyphenylphosphine) Palladium (0.27 mg) and toluene (31 mL) were added and heated to 80°C.
(Step 2) Thereafter, a 20% by mass tetraethylammonium hydroxide aqueous solution (15.7 g) was added dropwise thereto, and refluxed for 6 hours.
(Step 3) After that, phenylboronic acid (45.7 mg) and dichlorobis(tris-o-methoxyphenylphosphine)palladium (0.27 mg) were added thereto and stirred at 80° C. for 3 hours.
(Step 4) After cooling the reaction mixture, an aqueous sodium diethyldithiacarbamate solution was added, and the mixture was stirred at 40°C for 1 hour. After cooling the reaction solution and removing the aqueous layer, the resulting organic layer was washed twice with 3 mass % aqueous ammonia and twice with water. The resulting solution was added dropwise to methanol and stirred to cause precipitation. After the precipitate was dissolved in toluene (44 mL), alumina (27 g) was added, and the mixture was stirred for 3 hours, the resulting suspension was passed through a silica gel column for purification. The resulting solution was added dropwise to methanol and stirred to produce a precipitate. The precipitate was collected by filtration and dried to obtain 0.52 g of polymer compound BP2.
The polymer compound BP2 had Mn of 6.3×10 4 and Mw of 1.5×10 5 .
In the polymer compound BP2, the theoretical value obtained from the amount of the charged raw material is 45: It is a copolymer made up of a 50:5 molar ratio.
(高分子化合物BP3の合成)
高分子化合物BP3は、化合物M9、化合物M11、化合物M10及び化合物B10を用いて、国際公開第2019/004248号に記載の方法に従って合成した。高分子化合物BP3のMnは4.5×104であり、Mwは1.1×105であった。
高分子化合物BP3は、仕込み原料の量から求めた理論値では、化合物M9から誘導される構成単位と、化合物M11から誘導される構成単位と、化合物M9から誘導される構成単位と、化合物B10から誘導される構成単位とが、45:5:49:1のモル比で構成された共重合体である。
(Synthesis of polymer compound BP3)
Polymer compound BP3 was synthesized using compound M9, compound M11, compound M10 and compound B10 according to the method described in WO2019/004248. The polymer compound BP3 had an Mn of 4.5×10 4 and an Mw of 1.1×10 5 .
According to the theoretical values obtained from the amount of the starting material, the polymer compound BP3 has a structural unit derived from the compound M9, a structural unit derived from the compound M11, a structural unit derived from the compound M9, and a structural unit derived from the compound B10. The derived structural units are copolymers made up in a molar ratio of 45:5:49:1.
(高分子化合物MP1の合成)
高分子化合物MP1は、化合物M4、化合物M5、化合物M6、及び金属錯体MC12を用いて、特開2015-038195号に記載の方法に従って合成した。高分子化合物MP1のMnは9.0×104であり、Mwは2.3×105であった。
高分子化合物MP1は、仕込み原料の量から求めた理論値では、化合物M4から誘導される構成単位と、化合物M5から誘導される構成単位と、化合物M6から誘導される構成単位と、金属錯体MC12から誘導される構成単位とが、50:15:20.5:14.5のモル比で構成された共重合体である。
(Synthesis of polymer compound MP1)
Polymer compound MP1 was synthesized using compound M4, compound M5, compound M6, and metal complex MC12 according to the method described in JP-A-2015-038195. The Mn of the polymer compound MP1 was 9.0×10 4 and the Mw was 2.3×10 5 .
According to the theoretical values obtained from the amount of the charged raw material, the polymer compound MP1 has a structural unit derived from the compound M4, a structural unit derived from the compound M5, a structural unit derived from the compound M6, and a metal complex MC12. is a copolymer composed of structural units derived from and in a molar ratio of 50:15:20.5:14.5.
<合成例ET2> 高分子化合物ET2の合成
(高分子化合物ET2aの合成)
高分子化合物ET2aは、特開2012-33845号公報に記載の方法に従って合成した化合物ET2-1、及び、特開2012-33845号公報に記載の方法に従って合成した化合物ET2-2を用いて、特開2012-33845号公報に記載の方法に従って合成した。
<Synthesis Example ET2> Synthesis of Polymer Compound ET2 (Synthesis of Polymer Compound ET2a)
Polymer compound ET2a is compound ET2-1 synthesized according to the method described in JP-A-2012-33845, and compound ET2-2 synthesized according to the method described in JP-A-2012-33845. It was synthesized according to the method described in JP-A-2012-33845.
高分子化合物ET2aのMnは5.2×104であった。 Mn of the polymer compound ET2a was 5.2×10 4 .
高分子化合物ET2aは、仕込み原料の量から求めた理論値では、化合物ET2-1から誘導される構成単位と、化合物ET2-2から誘導される構成単位とが、50:50のモル比で構成された共重合体である。 The polymer compound ET2a is composed of structural units derived from the compound ET2-1 and structural units derived from the compound ET2-2 at a molar ratio of 50:50, according to the theoretical values obtained from the amounts of the raw materials. It is a copolymer that has been
(高分子化合物ET2の合成)
反応容器内を不活性ガス雰囲気とした後、高分子化合物ET2a(200mg)、テトラヒドロフラン(20mL)及びエタノール(20mL)を加え、55℃に加熱した。その後、そこへ、水(2mL)に溶解させた水酸化セシウム(200mg)を加え、55℃で6時間撹拌した。その後、室温まで冷却した後、減圧濃縮することにより、固体を得た。得られた固体を水で洗浄した後、減圧乾燥させることにより、高分子化合物ET2(150mg、薄黄色固体)を得た。得られた高分子化合物ET2のNMRスペクトルにより、高分子化合物ET2aのエチルエステル部位のエチル基由来のシグナルが完全に消失していることを確認した。
(Synthesis of polymer compound ET2)
After making the inside of reaction container into inert gas atmosphere, high molecular compound ET2a (200 mg), tetrahydrofuran (20 mL), and ethanol (20 mL) were added, and it heated at 55 degreeC. After that, cesium hydroxide (200 mg) dissolved in water (2 mL) was added thereto, and the mixture was stirred at 55°C for 6 hours. Then, after cooling to room temperature, a solid was obtained by concentrating under reduced pressure. The resulting solid was washed with water and dried under reduced pressure to obtain polymer compound ET2 (150 mg, pale yellow solid). From the NMR spectrum of the polymer compound ET2 obtained, it was confirmed that the signal derived from the ethyl group in the ethyl ester moiety of the polymer compound ET2a completely disappeared.
<高分子化合物HP1の合成>
高分子化合物HP1は、化合物M7及び化合物M8を用いて、国際公開第2012/086670号に記載の方法に従って合成した。
高分子化合物HP1のMnは1.3×105であり、Mwは3.6×105であった。
高分子化合物HP1は、仕込み原料の量から求めた理論値では、化合物M7から誘導される構成単位と、化合物M8から誘導される構成単位とが、50:50のモル比で構成された共重合体である。
<Synthesis of polymer compound HP1>
Polymer compound HP1 was synthesized using compound M7 and compound M8 according to the method described in International Publication No. 2012/086670.
The polymer compound HP1 had an Mn of 1.3×10 5 and an Mw of 3.6×10 5 .
According to the theoretical value obtained from the amount of the raw material charged, the polymer compound HP1 is a copolymer composed of structural units derived from the compound M7 and structural units derived from the compound M8 at a molar ratio of 50:50. It is a coalescence.
<高分子化合物HP2の合成>
高分子化合物HP2は、化合物M4、化合物M10及び化合物M12を用いて、特開2012-36388号公報に記載の方法に従って合成した。
高分子化合物HP2のMnは9.6×104であり、Mwは2.2×105であった。
高分子化合物HP2は、仕込み原料の量から求めた理論値では、化合物M4から誘導される構成単位と、化合物M10から誘導される構成単位と、化合物M12から誘導される構成単位とが、50:40:10のモル比で構成された共重合体である。
<Synthesis of polymer compound HP2>
Polymer compound HP2 was synthesized using compound M4, compound M10 and compound M12 according to the method described in JP-A-2012-36388.
The polymer compound HP2 had an Mn of 9.6×10 4 and an Mw of 2.2×10 5 .
In the polymer compound HP2, the theoretical value obtained from the amount of the raw material charged is that the structural unit derived from the compound M4, the structural unit derived from the compound M10, and the structural unit derived from the compound M12 are 50: It is a copolymer made up of a 40:10 molar ratio.
<高分子化合物HP3の合成>
高分子化合物HP3は、化合物M4、化合物M5及び化合物M6を用いて、国際公開第2015/008851号に記載の方法に従って合成した。
高分子化合物HP3のMnは8.5×104であり、Mwは2.2×105であった。
高分子化合物HP3は、仕込み原料の量から求めた理論値では、化合物M4から誘導される構成単位と、化合物M5から誘導される構成単位と、化合物M6から誘導される構成単位とが、50:26:24のモル比で構成された共重合体である。
<Synthesis of polymer compound HP3>
Polymer compound HP3 was synthesized using compound M4, compound M5 and compound M6 according to the method described in WO 2015/008851.
The Mn of the polymer compound HP3 was 8.5×10 4 and the Mw was 2.2×10 5 .
In the polymer compound HP3, the theoretical value obtained from the amount of the raw material charged is that the structural unit derived from the compound M4, the structural unit derived from the compound M5, and the structural unit derived from the compound M6 are 50: It is a copolymer made up of a 26:24 molar ratio.
<実施例D1> 発光素子D1の作製と評価
(陽極及び正孔注入層の形成)
ガラス基板にスパッタ法により45nmの厚さでITO膜を付けることにより、陽極を形成した。該陽極上に、正孔注入材料であるND-3202(日産化学工業株式会社製)をスピンコート法により35nmの厚さで成膜し、塗膜を形成した。塗膜を形成した基板を大気雰囲気下において、ホットプレート上で50℃、3分間加熱し、更に230℃、15分間加熱することにより正孔注入層を形成した。
<Example D1> Production and evaluation of light emitting device D1 (formation of anode and hole injection layer)
An anode was formed by attaching an ITO film with a thickness of 45 nm to a glass substrate by a sputtering method. On the anode, ND-3202 (manufactured by Nissan Chemical Industries, Ltd.), which is a hole injection material, was formed into a film with a thickness of 35 nm by a spin coating method to form a coating film. The substrate on which the coating film was formed was heated on a hot plate at 50° C. for 3 minutes in an air atmosphere, and further heated at 230° C. for 15 minutes to form a hole injection layer.
(正孔輸送層の形成)
キシレンに、高分子化合物HTL-1を0.7質量%の濃度で溶解させた。得られたキシレン溶液を用いて、正孔注入層の上にスピンコート法により20nmの厚さで成膜し、窒素ガス雰囲気下において、ホットプレート上で180℃、60分間加熱することにより、正孔輸送層を形成した。この加熱により、高分子化合物HTL-1は、架橋した状態となった。
(Formation of hole transport layer)
A polymer compound HTL-1 was dissolved in xylene at a concentration of 0.7% by mass. Using the xylene solution thus obtained, a film having a thickness of 20 nm was formed on the hole injection layer by a spin coating method. A pore transport layer was formed. By this heating, the polymer compound HTL-1 was in a crosslinked state.
(発光層の形成)
トルエンに、化合物H1、金属錯体MC1及び化合物B1(化合物H1/金属錯体MC1/化合物B1=73質量%/25質量%/2質量%)を1.8質量%の濃度で溶解させた。得られたトルエン溶液を用いて、正孔輸送層の上にスピンコート法により60nmの厚さで成膜し、窒素ガス雰囲気下において、130℃、10分間加熱することにより、発光層を形成した。
(Formation of light-emitting layer)
Compound H1, metal complex MC1 and compound B1 (compound H1/metal complex MC1/compound B1=73 mass %/25 mass %/2 mass %) were dissolved in toluene at a concentration of 1.8 mass %. Using the obtained toluene solution, a film having a thickness of 60 nm was formed on the hole transport layer by a spin coating method, and the film was heated at 130° C. for 10 minutes in a nitrogen gas atmosphere to form a light emitting layer. .
(陰極の形成)
発光層を形成した基板を蒸着機内において、1.0×10-4Pa以下にまで減圧した後、陰極として、発光層の上にフッ化ナトリウムを約4nm、次いで、フッ化ナトリウム層の上にアルミニウムを約80nm蒸着した。蒸着後、陰極を形成した基板をガラス基板で封止することにより、発光素子D1を作製した。
(Formation of cathode)
After reducing the pressure of the substrate on which the light-emitting layer is formed to 1.0×10 −4 Pa or less in a vapor deposition machine, sodium fluoride of about 4 nm is deposited on the light-emitting layer as a cathode, and then on the sodium fluoride layer. About 80 nm of aluminum was evaporated. After vapor deposition, the substrate on which the cathode was formed was sealed with a glass substrate to produce a light-emitting device D1.
(発光素子の評価)
発光素子D1に電圧を印加することによりEL発光が観測された。発光素子D1の10mA/cm2における駆動電圧[V]及びCIE色度座標を測定した。
(Evaluation of Light Emitting Element)
EL light emission was observed by applying a voltage to the light emitting element D1. The driving voltage [V] and CIE chromaticity coordinates of the light-emitting element D1 at 10 mA/cm 2 were measured.
<実施例D2> 発光素子D2の作製と評価
実施例D1の(発光層の形成)における、「金属錯体MC1」に代えて、「金属錯体MC2」を用いた以外は実施例D1と同様にして、発光素子D2を作製した。
発光素子D2に電圧を印加することによりEL発光が観測された。発光素子D2の10mA/cm2における駆動電圧[V]及びCIE色度座標を測定した。
<Example D2> Preparation and evaluation of light-emitting element D2 In the same manner as in Example D1 except that "metal complex MC2" was used instead of "metal complex MC1" in (formation of light-emitting layer) of Example D1. , a light-emitting device D2 was produced.
EL light emission was observed by applying a voltage to the light emitting element D2. The driving voltage [V] and CIE chromaticity coordinates of the light-emitting element D2 at 10 mA/cm 2 were measured.
<比較例CD1> 発光素子CD1の作製と評価
実施例D1の(発光層の形成)を(発光層の形成CD1)とした以外は実施例D1と同様にして、発光素子CD1を作製した。
<Comparative Example CD1> Production and evaluation of light-emitting element CD1 A light-emitting element CD1 was produced in the same manner as in Example D1, except that (formation of light-emitting layer) of Example D1 was changed to (formation of light-emitting layer CD1).
(発光層の形成CD1)
クロロベンゼンに、化合物H1、金属錯体MC3及び化合物B1(化合物H1/金属錯体MC3/化合物B1=73質量%/25質量%/2質量%)を1.8質量%の濃度で溶解させた。得られたクロロベンゼン溶液を用いて、正孔輸送層の上にスピンコート法により60nmの厚さで成膜し、窒素ガス雰囲気下において、130℃、10分間加熱することにより、発光層を形成した。
発光素子CD1に電圧を印加することによりEL発光が観測された。発光素子CD1の10mA/cm2における駆動電圧[V]及びCIE色度座標を測定した。
(Formation of light-emitting layer CD1)
Compound H1, metal complex MC3 and compound B1 (compound H1/metal complex MC3/compound B1=73 mass %/25 mass %/2 mass %) were dissolved in chlorobenzene at a concentration of 1.8 mass %. Using the obtained chlorobenzene solution, a film having a thickness of 60 nm was formed on the hole transport layer by spin coating, and the film was heated at 130° C. for 10 minutes in a nitrogen gas atmosphere to form a light emitting layer. .
EL light emission was observed by applying a voltage to the light emitting element CD1. The driving voltage [V] and CIE chromaticity coordinates of the light emitting element CD1 at 10 mA/cm 2 were measured.
実施例D1~D2及び比較例CD1の結果を表4に示す。表4において、駆動電圧差[V]とは、発光素子CD1の駆動電圧[V]に対する、発光素子D1及びD2の駆動電圧[V]の差を示す。 Table 4 shows the results of Examples D1 to D2 and Comparative Example CD1. In Table 4, the driving voltage difference [V] indicates the difference between the driving voltage [V] of the light emitting element CD1 and the driving voltage [V] of the light emitting elements D1 and D2.
<実施例D3> 発光素子D3の作製と評価
(陽極及び正孔注入層の形成)
ガラス基板にスパッタ法により45nmの厚さでITO膜を付けることにより、陽極を形成した。該陽極上に、正孔注入材料であるND-3202(日産化学工業株式会社製)をスピンコート法により35nmの厚さで成膜し、塗膜を形成した。塗膜を形成した基板を大気雰囲気下において、ホットプレート上で50℃、3分間加熱し、更に230℃、15分間加熱することにより正孔注入層を形成した。
<Example D3> Production and evaluation of light emitting device D3 (formation of anode and hole injection layer)
An anode was formed by attaching an ITO film with a thickness of 45 nm to a glass substrate by a sputtering method. On the anode, ND-3202 (manufactured by Nissan Chemical Industries, Ltd.), which is a hole injection material, was formed into a film with a thickness of 35 nm by a spin coating method to form a coating film. The substrate on which the coating film was formed was heated on a hot plate at 50° C. for 3 minutes in an air atmosphere, and further heated at 230° C. for 15 minutes to form a hole injection layer.
(正孔輸送層の形成)
キシレンに、高分子化合物HTL-1を0.7質量%の濃度で溶解させた。得られたキシレン溶液を用いて、正孔注入層の上にスピンコート法により20nmの厚さで成膜し、窒素ガス雰囲気下において、ホットプレート上で180℃、60分間加熱することにより、正孔輸送層を形成した。この加熱により、高分子化合物HTL-1は、架橋した状態となった。
(Formation of hole transport layer)
A polymer compound HTL-1 was dissolved in xylene at a concentration of 0.7% by mass. Using the xylene solution thus obtained, a film having a thickness of 20 nm was formed on the hole injection layer by a spin coating method. A pore transport layer was formed. By this heating, the polymer compound HTL-1 was in a crosslinked state.
(発光層の形成)
クロロベンゼンに、化合物H1、金属錯体MC1及び化合物B1(化合物H1/金属錯体MC1/化合物B1=73質量%/25質量%/2質量%)を1.8質量%の濃度で溶解させた。得られたトルエン溶液を用いて、正孔輸送層の上にスピンコート法により60nmの厚さで成膜し、窒素ガス雰囲気下において、130℃、10分間加熱することにより、発光層を形成した。
(Formation of light-emitting layer)
Compound H1, metal complex MC1 and compound B1 (compound H1/metal complex MC1/compound B1=73% by mass/25% by mass/2% by mass) were dissolved in chlorobenzene at a concentration of 1.8% by mass. Using the obtained toluene solution, a film having a thickness of 60 nm was formed on the hole transport layer by a spin coating method, and the film was heated at 130° C. for 10 minutes in a nitrogen gas atmosphere to form a light emitting layer. .
(電子輸送層の形成)
2,2,3,3,4,4,5,5-オクタフルオロ-1-ペンタノールに、化合物ET1を0.4質量%の濃度で溶解させた。得られた2,2,3,3,4,4,5,5-オクタフルオロ-1-ペンタノール溶液を用いて、発光層の上にスピンコート法により20nmの厚さで成膜し、窒素ガス雰囲気下において、130℃、10分間加熱することにより電子輸送層を形成した。
(Formation of electron transport layer)
Compound ET1 was dissolved in 2,2,3,3,4,4,5,5-octafluoro-1-pentanol at a concentration of 0.4% by mass. Using the obtained 2,2,3,3,4,4,5,5-octafluoro-1-pentanol solution, a film having a thickness of 20 nm was formed on the light-emitting layer by spin coating. An electron transport layer was formed by heating at 130° C. for 10 minutes in a gas atmosphere.
(陰極の形成)
電子輸送層を形成した基板を蒸着機内において、1.0×10-4Pa以下にまで減圧した後、陰極として、発光層の上にフッ化ナトリウムを約4nm、次いで、フッ化ナトリウム層の上にアルミニウムを約80nm蒸着した。蒸着後、陰極を形成した基板をガラス基板で封止することにより、発光素子D3を作製した。
(Formation of cathode)
After reducing the pressure of the substrate on which the electron transport layer was formed to 1.0 × 10 -4 Pa or less in a vapor deposition machine, as a cathode, sodium fluoride was deposited on the light emitting layer to about 4 nm, and then on the sodium fluoride layer. About 80 nm of aluminum was vapor-deposited on the substrate. After vapor deposition, the substrate on which the cathode was formed was sealed with a glass substrate to produce a light-emitting element D3.
(発光素子の評価)
発光素子D3に電圧を印加することによりEL発光が観測された。発光素子D3の50mA/cm2における駆動電圧[V]及びCIE色度座標を測定した。
(Evaluation of Light Emitting Element)
EL light emission was observed by applying a voltage to the light emitting element D3. The driving voltage [V] and CIE chromaticity coordinates of the light-emitting element D3 at 50 mA/cm 2 were measured.
<実施例D4> 発光素子D4の作製と評価
実施例D3の(発光層の形成)における、「金属錯体MC1」に代えて、「金属錯体MC2」を用いた以外は実施例D3と同様にして、発光素子D4を作製した。
発光素子D4に電圧を印加することによりEL発光が観測された。発光素子D4の50mA/cm2における駆動電圧[V]及びCIE色度座標を測定した。
<Example D4> Production and evaluation of light-emitting element D4 In the same manner as in Example D3, except that "metal complex MC2" was used instead of "metal complex MC1" in (formation of light-emitting layer) of Example D3. , a light-emitting device D4 was produced.
EL light emission was observed by applying a voltage to the light emitting element D4. The driving voltage [V] and CIE chromaticity coordinates of the light-emitting element D4 at 50 mA/cm 2 were measured.
<比較例CD2> 発光素子CD2の作製と評価
実施例D3の(発光層の形成)における、「金属錯体MC1」に代えて、「金属錯体MC3」を用いた以外は実施例D3と同様にして、発光素子CD2を作製した。
発光素子CD2に電圧を印加することによりEL発光が観測された。発光素子CD2の50mA/cm2における駆動電圧[V]及びCIE色度座標を測定した。
<Comparative Example CD2> Preparation and Evaluation of Light-Emitting Element CD2 In the same manner as in Example D3, except that "Metal Complex MC3" was used instead of "Metal Complex MC1" in (Formation of Light-Emitting Layer) of Example D3. , a light-emitting device CD2 was fabricated.
EL light emission was observed by applying a voltage to the light emitting element CD2. The driving voltage [V] and CIE chromaticity coordinates of the light emitting device CD2 at 50 mA/cm 2 were measured.
実施例D3~D4及び比較例CD2の結果を表5に示す。表5において、駆動電圧差[V]とは、発光素子CD2の駆動電圧[V]に対する、発光素子D3及びD4の駆動電圧[V]の差を示す。 Table 5 shows the results of Examples D3 to D4 and Comparative Example CD2. In Table 5, the driving voltage difference [V] indicates the difference between the driving voltage [V] of the light emitting element CD2 and the driving voltage [V] of the light emitting elements D3 and D4.
<実施例D5~D21及び比較例CD3> 発光素子D5~D21及び発光素子CD3の作製と評価
実施例D3の(発光層の形成)における、「化合物H1、金属錯体MC1及び化合物B1」に代えて、表6に示す材料を用いた以外は実施例D3と同様にして、発光素子D5~D21及び発光素子CD3を作製した。
発光素子D5~D21及び発光素子CD3に電圧を印加することによりEL発光が観測された。発光素子D5~D21及び発光素子CD3の1mA/cm2における駆動電圧[V]及びCIE色度座標を測定した。
<Examples D5 to D21 and Comparative Example CD3> Production and Evaluation of Light-Emitting Elements D5 to D21 and Light-Emitting Element CD3 Instead of "Compound H1, Metal Complex MC1 and Compound B1" in (Formation of Light-Emitting Layer) of Example D3 , Light-emitting elements D5 to D21 and light-emitting element CD3 were fabricated in the same manner as in Example D3, except that the materials shown in Table 6 were used.
EL light emission was observed by applying a voltage to the light emitting elements D5 to D21 and the light emitting element CD3. Driving voltage [V] and CIE chromaticity coordinates at 1 mA/cm 2 of the light emitting elements D5 to D21 and the light emitting element CD3 were measured.
実施例D5~D21及び比較例CD3の結果を表6に示す。表6において、駆動電圧差[V]とは、発光素子CD3の駆動電圧[V]に対する、発光素子D5~D21の駆動電圧[V]の差を示す。 Table 6 shows the results of Examples D5 to D21 and Comparative Example CD3. In Table 6, the driving voltage difference [V] indicates the difference between the driving voltage [V] of the light emitting element CD3 and the driving voltage [V] of the light emitting elements D5 to D21.
<実施例D22~D27> 発光素子D22~D27の作製と評価
実施例D3の(発光層の形成)における、「化合物H1、金属錯体MC1及び化合物B1」に代えて、表7に示す材料を用いた以外は実施例D3と同様にして、発光素子D22~D27を作製した。
発光素子D22~D27に電圧を印加することによりEL発光が観測された。発光素子D22~D27の10mA/cm2における駆動電圧[V]及びCIE色度座標を測定した。
<Examples D22 to D27> Production and evaluation of light-emitting elements D22 to D27 Instead of “compound H1, metal complex MC1 and compound B1” in (formation of light-emitting layer) of Example D3, the materials shown in Table 7 were used. Light-emitting devices D22 to D27 were produced in the same manner as in Example D3, except that
EL light emission was observed by applying a voltage to the light emitting elements D22 to D27. The driving voltage [V] and CIE chromaticity coordinates of the light emitting elements D22 to D27 at 10 mA/cm 2 were measured.
実施例D22~D27の結果を表7に示す。表7において、駆動電圧差[V]とは、発光素子D27の駆動電圧[V]に対する、発光素子D22~D26の駆動電圧[V]の差を示す。 Table 7 shows the results of Examples D22 to D27. In Table 7, the driving voltage difference [V] indicates the difference between the driving voltage [V] of the light emitting element D27 and the driving voltage [V] of the light emitting elements D22 to D26.
<実施例D28~D33及び比較例CD4> 発光素子D28~D33及び発光素子CD4の作製と評価
実施例D3の(発光層の形成)における、「化合物H1、金属錯体MC1及び化合物B1(化合物H1/金属錯体MC1/化合物B1=73質量%/25質量%/2質量%)」に代えて、表8に示す材料及び組成比(質量%)を用いた以外は実施例D3と同様にして、発光素子D28~D33及び発光素子CD4を作製した。
発光素子D28~D33及び発光素子CD4に電圧を印加することによりEL発光が観測された。発光素子D28~D33の5mA/cm2における駆動電圧[V]及びCIE色度座標を測定した。
<Examples D28 to D33 and Comparative Example CD4> Production and evaluation of light emitting elements D28 to D33 and light emitting element CD4 Light emission was performed in the same manner as in Example D3 except that the materials and composition ratios (% by mass) shown in Table 8 were used instead of "metal complex MC1/compound B1 = 73% by mass/25% by mass/2% by mass)". Devices D28 to D33 and light-emitting device CD4 were produced.
EL light emission was observed by applying a voltage to the light emitting elements D28 to D33 and the light emitting element CD4. The driving voltage [V] and CIE chromaticity coordinates of the light emitting elements D28 to D33 at 5 mA/cm 2 were measured.
実施例D28~D33及び比較例CD4の結果を表8に示す。表8において、駆動電圧差[V]とは、発光素子CD4の駆動電圧[V]に対する、発光素子D28~D33の駆動電圧[V]の差を示す。 Table 8 shows the results of Examples D28 to D33 and Comparative Example CD4. In Table 8, the drive voltage difference [V] indicates the difference between the drive voltage [V] of the light emitting elements D28 to D33 with respect to the drive voltage [V] of the light emitting element CD4.
<実施例D34> 発光素子D34の作製と評価
(陽極及び正孔注入層の形成)
ガラス基板にスパッタ法により45nmの厚さでITO膜を付けることにより、陽極を形成した。該陽極上に、正孔注入材料であるND-3202(日産化学工業株式会社製)をスピンコート法により35nmの厚さで成膜し、塗膜を形成した。塗膜を形成した基板を大気雰囲気下において、ホットプレート上で50℃、3分間加熱し、更に230℃、15分間加熱することにより正孔注入層を形成した。
<Example D34> Preparation and evaluation of light emitting device D34 (formation of anode and hole injection layer)
An anode was formed by attaching an ITO film with a thickness of 45 nm to a glass substrate by a sputtering method. On the anode, ND-3202 (manufactured by Nissan Chemical Industries, Ltd.), which is a hole injection material, was formed into a film with a thickness of 35 nm by a spin coating method to form a coating film. The substrate on which the coating film was formed was heated on a hot plate at 50° C. for 3 minutes in an air atmosphere, and further heated at 230° C. for 15 minutes to form a hole injection layer.
(正孔輸送層の形成)
キシレンに、高分子化合物HTL-1を0.7質量%の濃度で溶解させた。得られたキシレン溶液を用いて、正孔注入層の上にスピンコート法により20nmの厚さで成膜し、窒素ガス雰囲気下において、ホットプレート上で180℃、60分間加熱することにより、正孔輸送層を形成した。この加熱により、高分子化合物HTL-1は、架橋した状態となった。
(Formation of hole transport layer)
A polymer compound HTL-1 was dissolved in xylene at a concentration of 0.7% by mass. Using the xylene solution thus obtained, a film having a thickness of 20 nm was formed on the hole injection layer by a spin coating method. A pore transport layer was formed. By this heating, the polymer compound HTL-1 was in a crosslinked state.
(発光層の形成)
トルエンに、化合物H1、金属錯体MC1及び化合物B1(化合物H1/金属錯
体MC1/化合物B1=73質量%/25質量%/2質量%)を1.8質量%の濃度で溶解させた。得られたトルエン溶液を用いて、正孔輸送層の上にスピンコート法により60nmの厚さで成膜し、窒素ガス雰囲気下において、130℃、10分間加熱することにより、発光層を形成した。
(Formation of light-emitting layer)
Compound H1, metal complex MC1 and compound B1 (compound H1/metal complex MC1/compound B1=73 mass %/25 mass %/2 mass %) were dissolved in toluene at a concentration of 1.8 mass %. Using the obtained toluene solution, a film having a thickness of 60 nm was formed on the hole transport layer by a spin coating method, and the film was heated at 130° C. for 10 minutes in a nitrogen gas atmosphere to form a light emitting layer. .
(電子輸送層の形成)
2,2,3,3,4,4,5,5-オクタフルオロ-1-ペンタノールに、高分子化合物ET2を0.4質量%の濃度で溶解させた。得られた2,2,3,3,4,4,5,5-オクタフルオロ-1-ペンタノール溶液を用いて、発光層の上にスピンコート法により20nmの厚さで成膜し、窒素ガス雰囲気下において、130℃、10分間加熱することにより電子輸送層を形成した。
(Formation of electron transport layer)
A polymer compound ET2 was dissolved in 2,2,3,3,4,4,5,5-octafluoro-1-pentanol at a concentration of 0.4% by mass. Using the obtained 2,2,3,3,4,4,5,5-octafluoro-1-pentanol solution, a film having a thickness of 20 nm was formed on the light-emitting layer by spin coating. An electron transport layer was formed by heating at 130° C. for 10 minutes in a gas atmosphere.
(陰極の形成)
電子輸送層を形成した基板を蒸着機内において、1.0×10-4Pa以下にまで減圧した後、陰極として、発光層の上にフッ化ナトリウムを約4nm、次いで、フッ化ナトリウム層の上にアルミニウムを約80nm蒸着した。蒸着後、陰極を形成した基板をガラス基板で封止することにより、発光素子D34を作製した。
(Formation of cathode)
After reducing the pressure of the substrate on which the electron transport layer was formed to 1.0 × 10 -4 Pa or less in a vapor deposition machine, as a cathode, sodium fluoride was deposited on the light emitting layer to about 4 nm, and then on the sodium fluoride layer. About 80 nm of aluminum was vapor-deposited on the substrate. After vapor deposition, the substrate on which the cathode was formed was sealed with a glass substrate to produce a light-emitting device D34.
(発光素子の評価)
発光素子D34に電圧を印加することによりEL発光が観測された。発光素子D34の10mA/cm2における駆動電圧[V]及びCIE色度座標を測定した。
(Evaluation of Light Emitting Element)
EL light emission was observed by applying a voltage to the light emitting element D34. The driving voltage [V] and CIE chromaticity coordinates of the light-emitting element D34 at 10 mA/cm 2 were measured.
<実施例D35~D41> 発光素子D35~D41の作製と評価
実施例D34の(発光層の形成)における、「化合物H1、金属錯体MC1及び化合物B1(化合物H1/金属錯体MC1/化合物B1=73質量%/25質量%/2質量%)」に代えて、表9に示す材料及び組成比(質量%)を用いた以外は実施例D34と同様にして、発光素子D35~D41を作製した。
発光素子D35~D41に電圧を印加することによりEL発光が観測された。発光素子D35~D41の10mA/cm2における駆動電圧[V]及びCIE色度座標を測定した。
<Examples D35 to D41> Production and evaluation of light emitting elements D35 to D41 In (formation of light emitting layer) of Example D34, “Compound H1, metal complex MC1 and compound B1 (compound H1/metal complex MC1/compound B1 = 73 Light-emitting elements D35 to D41 were produced in the same manner as in Example D34, except that the materials and composition ratios (% by mass) shown in Table 9 were used instead of "% by mass/25% by mass/2% by mass."
EL light emission was observed by applying a voltage to the light emitting elements D35 to D41. Driving voltage [V] and CIE chromaticity coordinates of the light-emitting elements D35 to D41 at 10 mA/cm 2 were measured.
<比較例CD5> 発光素子CD5の作製と評価
実施例D34の(発光層の形成)を、下記(発光層の形成CD-5)とした以外は、実施例D34と同様にして、発光素子CD5を作製した。
発光素子CD5に電圧を印加することによりEL発光が観測された。発光素子CD5の10mA/cm2における駆動電圧[V]及びCIE色度座標を測定した。
<Comparative Example CD5> Preparation and evaluation of light-emitting element CD5 Light-emitting element CD5 was produced in the same manner as in Example D34, except that (formation of light-emitting layer) of Example D34 was changed to the following (formation of light-emitting layer CD-5). was made.
EL light emission was observed by applying a voltage to the light emitting element CD5. The driving voltage [V] and CIE chromaticity coordinates of the light emitting element CD5 at 10 mA/cm 2 were measured.
(発光層の形成CD-5)
トルエンに、高分子化合物MP1及び高分子化合物BP2(高分子化合物MP1/高分子化合物BP2=25質量%/75質量%)を1.0質量%の濃度で溶解させた。得られたトルエン溶液を用いて、正孔輸送層の上にスピンコート法により60nmの厚さで成膜し、窒素ガス雰囲気下において、130℃、10分間加熱することにより、発光層を形成した。
(Formation of light-emitting layer CD-5)
Polymer compound MP1 and polymer compound BP2 (polymer compound MP1/polymer compound BP2=25% by mass/75% by mass) were dissolved in toluene at a concentration of 1.0% by mass. Using the obtained toluene solution, a film having a thickness of 60 nm was formed on the hole transport layer by a spin coating method, and the film was heated at 130° C. for 10 minutes in a nitrogen gas atmosphere to form a light emitting layer. .
実施例D34~D41及び比較例CD5の結果を表9に示す。表10において、駆動電圧差[V]とは、発光素子CD5の駆動電圧[V]に対する、発光素子D34~D41の駆動電圧[V]の差を示す。 Table 9 shows the results of Examples D34 to D41 and Comparative Example CD5. In Table 10, the driving voltage difference [V] indicates the difference between the driving voltage [V] of the light emitting element CD5 and the driving voltage [V] of the light emitting elements D34 to D41.
<実施例D42> 発光素子D42の作製と評価
(陽極及び正孔注入層の形成)
ガラス基板にスパッタ法により45nmの厚さでITO膜を付けることにより、陽極を形成した。該陽極上に、正孔注入材料であるND-3202(日産化学工業株式会社製)をスピンコート法により35nmの厚さで成膜し、塗膜を形成した。塗膜を形成した基板を大気雰囲気下において、ホットプレート上で50℃、3分間加熱し、更に230℃、15分間加熱することにより正孔注入層を形成した。
<Example D42> Production and evaluation of light emitting device D42 (formation of anode and hole injection layer)
An anode was formed by attaching an ITO film with a thickness of 45 nm to a glass substrate by a sputtering method. On the anode, ND-3202 (manufactured by Nissan Chemical Industries, Ltd.), which is a hole injection material, was formed into a film with a thickness of 35 nm by a spin coating method to form a coating film. The substrate on which the coating film was formed was heated on a hot plate at 50° C. for 3 minutes in an air atmosphere, and further heated at 230° C. for 15 minutes to form a hole injection layer.
(正孔輸送層の形成)
キシレンに、高分子化合物HTL-1を0.7質量%の濃度で溶解させた。得られたキシレン溶液を用いて、正孔注入層の上にスピンコート法により20nmの厚さで成膜し、窒素ガス雰囲気下において、ホットプレート上で180℃、60分間加熱することにより、正孔輸送層を形成した。この加熱により、高分子化合物HTL-1は、架橋した状態となった。
(Formation of hole transport layer)
A polymer compound HTL-1 was dissolved in xylene at a concentration of 0.7% by mass. Using the xylene solution thus obtained, a film having a thickness of 20 nm was formed on the hole injection layer by a spin coating method. A pore transport layer was formed. By this heating, the polymer compound HTL-1 was in a crosslinked state.
(発光層の形成)
トルエンに、化合物H1、金属錯体MC4及び化合物B1(化合物H1/金属錯
体MC4/化合物B1=73質量%/25質量%/2質量%)を1.8質量%の濃度で溶解させた。得られたトルエン溶液を用いて、正孔輸送層の上にスピンコート法により60nmの厚さで成膜し、窒素ガス雰囲気下において、130℃、10分間加熱することにより、発光層を形成した。
(Formation of light-emitting layer)
Compound H1, metal complex MC4 and compound B1 (compound H1/metal complex MC4/compound B1=73% by mass/25% by mass/2% by mass) were dissolved in toluene at a concentration of 1.8% by mass. Using the obtained toluene solution, a film having a thickness of 60 nm was formed on the hole transport layer by a spin coating method, and the film was heated at 130° C. for 10 minutes in a nitrogen gas atmosphere to form a light emitting layer. .
(電子輸送層の形成)
2,2,3,3,4,4,5,5-オクタフルオロ-1-ペンタノールに、高分子化合物ET2を0.4質量%の濃度で溶解させた。得られた2,2,3,3,4,4,5,5-オクタフルオロ-1-ペンタノール溶液を用いて、発光層の上にスピンコート法により20nmの厚さで成膜し、窒素ガス雰囲気下において、130℃、10分間加熱することにより電子輸送層を形成した。
(Formation of electron transport layer)
A polymer compound ET2 was dissolved in 2,2,3,3,4,4,5,5-octafluoro-1-pentanol at a concentration of 0.4% by mass. Using the obtained 2,2,3,3,4,4,5,5-octafluoro-1-pentanol solution, a film having a thickness of 20 nm was formed on the light-emitting layer by spin coating. An electron transport layer was formed by heating at 130° C. for 10 minutes in a gas atmosphere.
(陰極の形成)
電子輸送層を形成した基板を蒸着機内において、1.0×10-4Pa以下にまで減圧した後、陰極として、発光層の上にフッ化ナトリウムを約4nm、次いで、フッ化ナトリウム層の上にアルミニウムを約80nm蒸着した。蒸着後、陰極を形成した基板をガラス基板で封止することにより、発光素子D42を作製した。
(Formation of cathode)
After reducing the pressure of the substrate on which the electron transport layer was formed to 1.0 × 10 -4 Pa or less in a vapor deposition machine, as a cathode, sodium fluoride was deposited on the light emitting layer to about 4 nm, and then on the sodium fluoride layer. About 80 nm of aluminum was vapor-deposited on the substrate. After vapor deposition, the substrate on which the cathode was formed was sealed with a glass substrate to produce a light-emitting device D42.
(発光素子の評価)
発光素子D42に電圧を印加することによりEL発光が観測された。発光素子D42の1mA/cm2における駆動電圧[V]及びCIE色度座標を測定した。
(Evaluation of Light Emitting Element)
EL light emission was observed by applying a voltage to the light emitting element D42. The driving voltage [V] and CIE chromaticity coordinates of the light-emitting element D42 at 1 mA/cm 2 were measured.
<実施例D43~D44> 発光素子D43~D44の作製と評価
実施例D42の(発光層の形成)における、「化合物H1、金属錯体MC4及び化合物B1(化合物H1/金属錯体MC4/化合物B1=73質量%/25質量%/2質量%)」に代えて、表10に示す材料及び組成比(質量%)を用いた以外は実施例D42と同様にして、発光素子D43~D44を作製した。
発光素子D43~D44に電圧を印加することによりEL発光が観測された。発光素子D43~D44の1mA/cm2における駆動電圧[V]及びCIE色度座標を測定した。
<Examples D43 to D44> Preparation and evaluation of light emitting elements D43 to D44 In (formation of light emitting layer) of Example D42, “Compound H1, metal complex MC4 and compound B1 (compound H1/metal complex MC4/compound B1 = 73 Light-emitting elements D43 to D44 were produced in the same manner as in Example D42, except that the materials and composition ratios (% by mass) shown in Table 10 were used instead of "% by mass/25% by mass/2% by mass."
EL light emission was observed by applying a voltage to the light emitting elements D43 and D44. Driving voltage [V] and CIE chromaticity coordinates of the light-emitting elements D43 to D44 at 1 mA/cm 2 were measured.
<実施例D45> 発光素子D45の作製と評価
実施例D42の(発光層の形成)を、下記(発光層の形成D-45)とした以外は、実施例D42と同様にして、発光素子D45を作製した。
発光素子D45に電圧を印加することによりEL発光が観測された。発光素子D45の1mA/cm2における駆動電圧[V]及びCIE色度座標を測定した。
<Example D45> Preparation and evaluation of light-emitting element D45 Light-emitting element D45 was produced in the same manner as in Example D42, except that (formation of light-emitting layer) of Example D42 was changed to the following (formation of light-emitting layer D-45). was made.
EL light emission was observed by applying a voltage to the light emitting element D45. The driving voltage [V] and CIE chromaticity coordinates of the light-emitting element D45 at 1 mA/cm 2 were measured.
(発光層の形成D-45)
トルエンに、高分子化合物HP1、金属錯体MC4及び化合物B1(高分子化合物HP1/金属錯体MC4/化合物B1=73質量%/25質量%/2質量%)を1.2質量%の濃度で溶解させた。得られたトルエン溶液を用いて、正孔輸送層の上にスピンコート法により60nmの厚さで成膜し、窒素ガス雰囲気下において、130℃、10分間加熱することにより、発光層を形成した。
(Formation of light-emitting layer D-45)
Polymer compound HP1, metal complex MC4, and compound B1 (polymer compound HP1/metal complex MC4/compound B1=73% by mass/25% by mass/2% by mass) were dissolved in toluene at a concentration of 1.2% by mass. rice field. Using the obtained toluene solution, a film having a thickness of 60 nm was formed on the hole transport layer by a spin coating method, and the film was heated at 130° C. for 10 minutes in a nitrogen gas atmosphere to form a light emitting layer. .
<実施例D46> 発光素子D46の作製と評価
実施例D42の(発光層の形成)を、下記(発光層の形成D-46)とした以外は、実施例D42と同様にして、発光素子D46を作製した。
発光素子D46に電圧を印加することによりEL発光が観測された。発光素子D46の1mA/cm2における駆動電圧[V]及びCIE色度座標を測定した。
<Example D46> Production and evaluation of light-emitting element D46 Light-emitting element D46 was prepared in the same manner as in Example D42, except that (formation of light-emitting layer) of Example D42 was changed to the following (formation of light-emitting layer D-46). was made.
EL light emission was observed by applying a voltage to the light emitting element D46. The driving voltage [V] and CIE chromaticity coordinates of the light-emitting element D46 at 1 mA/cm 2 were measured.
(発光層の形成D-46)
トルエンに、高分子化合物HP2、金属錯体MC4及び化合物B1(高分子化合物HP2/金属錯体MC4/化合物B1=73質量%/25質量%/2質量%)を1.0質量%の濃度で溶解させた。得られたトルエン溶液を用いて、正孔輸送層の上にスピンコート法により60nmの厚さで成膜し、窒素ガス雰囲気下において、130℃、10分間加熱することにより、発光層を形成した。
(Formation of light-emitting layer D-46)
Polymer compound HP2, metal complex MC4, and compound B1 (polymer compound HP2/metal complex MC4/compound B1=73% by mass/25% by mass/2% by mass) were dissolved in toluene at a concentration of 1.0% by mass. rice field. Using the obtained toluene solution, a film having a thickness of 60 nm was formed on the hole transport layer by a spin coating method, and the film was heated at 130° C. for 10 minutes in a nitrogen gas atmosphere to form a light emitting layer. .
<実施例D47> 発光素子D47の作製と評価
実施例D42の(発光層の形成)を、下記(発光層の形成D-47)とした以外は、実施例D42と同様にして、発光素子D47を作製した。
発光素子D47に電圧を印加することによりEL発光が観測された。発光素子D47の1mA/cm2における駆動電圧[V]及びCIE色度座標を測定した。
<Example D47> Preparation and evaluation of light-emitting element D47 Light-emitting element D47 was prepared in the same manner as in Example D42, except that (formation of light-emitting layer) of Example D42 was changed to the following (formation of light-emitting layer D-47). was made.
EL light emission was observed by applying a voltage to the light emitting element D47. The driving voltage [V] and CIE chromaticity coordinates of the light-emitting element D47 at 1 mA/cm 2 were measured.
(発光層の形成D-47)
トルエンに、高分子化合物HP3、金属錯体MC4及び化合物B1(高分子化合物HP3/金属錯体MC4/化合物B1=73質量%/25質量%/2質量%)を1.2質量%の濃度で溶解させた。得られたトルエン溶液を用いて、正孔輸送層の上にスピンコート法により60nmの厚さで成膜し、窒素ガス雰囲気下において、130℃、10分間加熱することにより、発光層を形成した。
(Formation of light-emitting layer D-47)
Polymer compound HP3, metal complex MC4 and compound B1 (polymer compound HP3/metal complex MC4/compound B1=73% by mass/25% by mass/2% by mass) were dissolved in toluene at a concentration of 1.2% by mass. rice field. Using the obtained toluene solution, a film having a thickness of 60 nm was formed on the hole transport layer by a spin coating method, and the film was heated at 130° C. for 10 minutes in a nitrogen gas atmosphere to form a light emitting layer. .
<比較例CD6> 発光素子CD6の作製と評価
実施例D42の(発光層の形成)を、下記(発光層の形成CD-6)とした以外は、実施例D42と同様にして、発光素子CD6を作製した。
発光素子CD6に電圧を印加することによりEL発光が観測された。発光素子CD6の1mA/cm2における駆動電圧[V]及びCIE色度座標を測定した。
<Comparative Example CD6> Preparation and evaluation of light-emitting element CD6 Light-emitting element CD6 was prepared in the same manner as in Example D42, except that (formation of light-emitting layer) of Example D42 was changed to the following (formation of light-emitting layer CD-6). was made.
EL light emission was observed by applying a voltage to the light emitting element CD6. The driving voltage [V] and CIE chromaticity coordinates of the light emitting device CD6 at 1 mA/cm 2 were measured.
(発光層の形成CD-6)
クロロベンゼンに、高分子化合物HP4、金属錯体MC4及び化合物B1(高分子化合物HP4/金属錯体MC4/化合物B1=73質量%/25質量%/2質量%)を1.6質量%の濃度で溶解させた。得られたクロロベンゼン溶液を用いて、正孔輸送層の上にスピンコート法により60nmの厚さで成膜し、窒素ガス雰囲気下において、130℃、10分間加熱することにより、発光層を形成した。
(Formation of light-emitting layer CD-6)
Polymer compound HP4, metal complex MC4, and compound B1 (polymer compound HP4/metal complex MC4/compound B1=73% by mass/25% by mass/2% by mass) were dissolved in chlorobenzene at a concentration of 1.6% by mass. rice field. Using the obtained chlorobenzene solution, a film having a thickness of 60 nm was formed on the hole transport layer by spin coating, and the film was heated at 130° C. for 10 minutes in a nitrogen gas atmosphere to form a light emitting layer. .
実施例D42~D47及び比較例CD6の結果を表10に示す。表10において、駆動電圧差[V]とは、発光素子CD6の駆動電圧[V]に対する、発光素子D42~D47の駆動電圧[V]の差を示す。 Table 10 shows the results of Examples D42 to D47 and Comparative Example CD6. In Table 10, the driving voltage difference [V] indicates the difference between the driving voltage [V] of the light emitting element CD6 and the driving voltage [V] of the light emitting elements D42 to D47.
表4~6からも明らかなように、5員環を含む芳香族複素環を有する化合物(A)を含有する組成物を含む実施例の発光素子は、化合物(A)を含有しない組成物を含む比較例
の発光素子に比べ、駆動電圧が低いことが分かる。
As is clear from Tables 4 to 6, the light-emitting devices of Examples containing the composition containing the compound (A) having an aromatic heterocyclic ring containing a 5-membered ring were compositions containing no compound (A). It can be seen that the driving voltage is lower than that of the light emitting element of the comparative example.
表8~表10からも明らかなように、第1の化合物を含有する組成物を含む実施例の発光素子は、第1の化合物を含有しない組成物を含む比較例の発光素子に比べ、駆動電圧が低いことが分かる。 As is clear from Tables 8 to 10, the light-emitting elements of Examples containing the composition containing the first compound are driven more than the light-emitting elements of Comparative Examples containing compositions not containing the first compound. It can be seen that the voltage is low.
Claims (13)
ホウ素原子と、酸素原子、硫黄原子、セレン原子、sp3炭素原子及び窒素原子からなる群より選ばれる少なくとも1種とを環内に含む縮合複素環骨格(b)を有する低分子化合物(B)、並びに、前記低分子化合物(B)から水素原子1個以上を除いた基を有する構成単位を含む高分子化合物(B)からなる群より選択される少なくとも1種と、
式(H-1)で表される化合物、並びに、式(X)で表される構成単位及び式(Y)で表される構成単位からなる群より選択される少なくとも1種の構成単位を含む高分子化合物からなる群より選択される少なくとも1種と、
を含有する、組成物。
[式中、
Mは、ロジウム原子、パラジウム原子、イリジウム原子又は白金原子を表す。
n1は1以上の整数を表し、n2は0以上の整数を表す。但し、Mがロジウム原子又はイリジウム原子の場合、n1+n2は3であり、Mがパラジウム原子又は白金原子の場合、n1+n2は2である。
E1及びE2は、それぞれ独立に、炭素原子又は窒素原子を表す。E1及びE2が複数存在する場合、それらはそれぞれ同一でも異なっていてもよい。
環L1は、5員環を含む芳香族複素環を表し、該環は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。環L1が複数存在する場合、それらは同一でも異なっていてもよい。
環L2は、芳香族炭化水素環又は芳香族複素環を表し、これらの環は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。環L2が複数存在する場合、それらは同一でも異なっていてもよい。
環L1が有していてもよい置換基と、環L2が有していてもよい置換基とは、同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。
A1-G1-A2は、アニオン性の2座配位子を表す。A1及びA2は、それぞれ独立に、炭素原子、酸素原子又は窒素原子を表し、これらの原子は環を構成する原子であってもよい。G1は、単結合、又は、A1及びA2とともに2座配位子を構成する原子団を表す。A1-G1-A2が複数存在する場合、それらは同一でも異なっていてもよい。]
[式中、
ArH1及びArH2は、それぞれ独立に、アリール基、1価の複素環基又は置換アミノ基を表し、これらの基は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。
nH1は、0以上の整数を表す。
LH1は、2価の基を表し、該2価の基は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。LH1が複数存在する場合、それらは同一でも異なっていてもよく、それらは互いに、直接結合して、又は、2価の基を介して結合して、環を形成してもよい。
ArH1とArH2とは、直接結合して、又は、2価の基を介して結合して、環を形成してもよい。LH1とArH1とは、直接結合して、又は、2価の基を介して結合して、環を形成してもよい。LH1とArH2とは、直接結合して、又は、2価の基を介して結合して、環を形成してもよい。]
[式中、
aX1及びaX2は、それぞれ独立に、0以上の整数を表す。
ArX1及びArX3は、それぞれ独立に、アリーレン基又は2価の複素環基を表し、これらの基は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。
ArX2及びArX4は、それぞれ独立に、アリーレン基、2価の複素環基、又は、少なくとも1種のアリーレン基と少なくとも1種の2価の複素環基とが直接結合した2価の基を表し、これらの基は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。ArX2が複数存在する場合、それらはそれぞれ同一でも異なっていてもよい。ArX4が複数存在する場合、それらはそれぞれ同一でも異なっていてもよい。
RX1、RX2及びRX3は、それぞれ独立に、水素原子、アルキル基、シクロアルキル基、アリール基又は1価の複素環基を表し、これらの基は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。RX2が複数存在する場合、それらは同一でも異なっていてもよい。RX3が複数存在する場合、それらは同一でも異なっていてもよい。]
[式中、ArY1は、アリーレン基、2価の複素環基、又は、少なくとも1種のアリーレ
ン基と少なくとも1種の2価の複素環基とが直接結合した2価の基を表し、これらの基は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。] selected from the group consisting of a metal complex represented by formula (1) and a polymer compound (A) containing a structural unit having a group obtained by removing one or more hydrogen atoms from the metal complex represented by formula (1) and at least one
A low-molecular-weight compound (B) having a condensed heterocyclic skeleton (b) containing a boron atom and at least one selected from the group consisting of an oxygen atom, a sulfur atom, a selenium atom, an sp3 carbon atom and a nitrogen atom in the ring and at least one selected from the group consisting of a polymer compound (B) containing a structural unit having a group obtained by removing one or more hydrogen atoms from the low-molecular-weight compound (B),
A compound represented by formula (H-1) and at least one structural unit selected from the group consisting of structural units represented by formula (X) and structural units represented by formula (Y) at least one selected from the group consisting of polymer compounds;
A composition comprising
[In the formula,
M represents a rhodium atom, a palladium atom, an iridium atom or a platinum atom.
n1 represents an integer of 1 or more, and n2 represents an integer of 0 or more. However, n 1 +n 2 is 3 when M is a rhodium atom or an iridium atom, and n 1 +n 2 is 2 when M is a palladium atom or a platinum atom.
E 1 and E 2 each independently represent a carbon atom or a nitrogen atom. When multiple E 1 and E 2 are present, they may be the same or different.
Ring L 1 represents an aromatic heterocyclic ring containing a 5-membered ring, and the ring may have a substituent. When there are multiple such substituents, they may be the same or different, and may be bonded to each other to form a ring together with the atoms to which they are bonded. When multiple rings L 1 are present, they may be the same or different.
Ring L2 represents an aromatic hydrocarbon ring or an aromatic heterocyclic ring, and these rings may have a substituent. When there are multiple such substituents, they may be the same or different, and may be bonded to each other to form a ring together with the atoms to which they are bonded. When there is more than one ring L2 , they may be the same or different.
The substituent that ring L 1 may have and the substituent that ring L 2 may have may be the same or different, and are bonded to each other to form a ring together with the atoms to which they are bonded. may be formed.
A 1 -G 1 -A 2 represents an anionic bidentate ligand. A 1 and A 2 each independently represent a carbon atom, an oxygen atom or a nitrogen atom, and these atoms may be atoms constituting a ring. G 1 represents a single bond or an atomic group forming a bidentate ligand together with A 1 and A 2 . When multiple A 1 -G 1 -A 2 are present, they may be the same or different. ]
[In the formula,
Ar H1 and Ar H2 each independently represent an aryl group, a monovalent heterocyclic group or a substituted amino group, and these groups may have a substituent. When there are multiple such substituents, they may be the same or different, and may be bonded to each other to form a ring together with the atoms to which they are bonded.
n H1 represents an integer of 0 or more.
L H1 represents a divalent group, and the divalent group may have a substituent. When there are multiple such substituents, they may be the same or different, and may be bonded to each other to form a ring together with the atoms to which they are bonded. When multiple L H1 are present, they may be the same or different, and they may be directly bonded to each other or bonded via a divalent group to form a ring.
Ar H1 and Ar H2 may be directly bonded or bonded via a divalent group to form a ring. L H1 and Ar H1 may be directly bonded or bonded via a divalent group to form a ring. L H1 and Ar H2 may be directly bonded or bonded via a divalent group to form a ring. ]
[In the formula,
a X1 and a X2 each independently represent an integer of 0 or more.
Ar 1 X1 and Ar 2 X3 each independently represent an arylene group or a divalent heterocyclic group, and these groups may have a substituent. When there are multiple such substituents, they may be the same or different, and may be bonded to each other to form a ring together with the atoms to which they are bonded.
Ar X2 and Ar X4 each independently represent an arylene group, a divalent heterocyclic group, or a divalent group in which at least one arylene group and at least one divalent heterocyclic group are directly bonded; and these groups may have a substituent. When there are multiple such substituents, they may be the same or different, and may be bonded to each other to form a ring together with the atoms to which they are bonded. When multiple Ar X2 are present, they may be the same or different. When multiple Ar X4 are present, they may be the same or different.
R X1 , R X2 and R X3 each independently represent a hydrogen atom, an alkyl group, a cycloalkyl group, an aryl group or a monovalent heterocyclic group, and these groups may have a substituent. When there are multiple such substituents, they may be the same or different, and may be bonded to each other to form a ring together with the atoms to which they are bonded. When multiple R X2 are present, they may be the same or different. When multiple R X3 are present, they may be the same or different. ]
[Wherein, Ar Y represents an arylene group, a divalent heterocyclic group, or a divalent group in which at least one arylene group and at least one divalent heterocyclic group are directly bonded, The group may have a substituent. When there are multiple such substituents, they may be the same or different, and may be bonded to each other to form a ring together with the atoms to which they are bonded. ]
[式中、
Ar1、Ar2及びAr3は、それぞれ独立に、芳香族炭化水素基又は複素環基を表し、これらの基は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。
Y1は、酸素原子、硫黄原子、セレン原子、-N(Ry)-で表される基、アルキレン基又はシクロアルキレン基を表し、これらの基は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが
結合する原子とともに環を形成していてもよい。
Y2及びY3は、それぞれ独立に、単結合、酸素原子、硫黄原子、セレン原子、-N(Ry)-で表される基、-B(Ry)-で表される基、アルキレン基、シクロアルキレン基、アリーレン基又は2価の複素環基を表し、これらの基は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。
Ryは、水素原子、アルキル基、シクロアルキル基、アリール基又は1価の複素環基を表し、これらの基は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。Ryが複数存在する場合、同一であっても異なっていてもよい。
Y1とAr1とは、直接結合して、又は、2価の基を介して結合して、環を形成してもよい。Y1とAr2とは、直接結合して、又は、2価の基を介して結合して、環を形成してもよい。Y2とAr1とは、直接結合して、又は、2価の基を介して結合して、環を形成してもよい。Y2とAr3とは、直接結合して、又は、2価の基を介して結合して、環を形成してもよい。Y3とAr2とは、直接結合して、又は、2価の基を介して結合して、環を形成してもよい。Y3とAr3とは、直接結合して、又は、2価の基を介して結合して、環を形成してもよい。] Claim 1, wherein the low-molecular-weight compound (B) is a compound represented by formula (1-1), a compound represented by formula (1-2), or a compound represented by formula (1-3). A composition according to any one of claims 1 to 4.
[In the formula,
Ar 1 , Ar 2 and Ar 3 each independently represent an aromatic hydrocarbon group or a heterocyclic group, and these groups may have a substituent. When there are multiple such substituents, they may be the same or different, and may be bonded to each other to form a ring together with the atoms to which they are bonded.
Y 1 represents an oxygen atom, a sulfur atom, a selenium atom, a group represented by -N(Ry)-, an alkylene group or a cycloalkylene group, and these groups may have a substituent. When there are multiple such substituents, they may be the same or different, and may be bonded to each other to form a ring together with the atoms to which they are bonded.
Y 2 and Y 3 each independently represent a single bond, an oxygen atom, a sulfur atom, a selenium atom, a group represented by -N(Ry)-, a group represented by -B(Ry)-, an alkylene group, It represents a cycloalkylene group, an arylene group or a divalent heterocyclic group, and these groups may have a substituent. When there are multiple such substituents, they may be the same or different, and may be bonded to each other to form a ring together with the atoms to which they are bonded.
Ry represents a hydrogen atom, an alkyl group, a cycloalkyl group, an aryl group or a monovalent heterocyclic group, and these groups may have a substituent. When there are multiple such substituents, they may be the same or different, and may be bonded to each other to form a ring together with the atoms to which they are bonded. When two or more Ry are present, they may be the same or different.
Y 1 and Ar 1 may be directly bonded or bonded via a divalent group to form a ring. Y 1 and Ar 2 may be directly bonded or bonded via a divalent group to form a ring. Y 2 and Ar 1 may be directly bonded or bonded via a divalent group to form a ring. Y 2 and Ar 3 may be directly bonded or bonded via a divalent group to form a ring. Y 3 and Ar 2 may be directly bonded or bonded via a divalent group to form a ring. Y 3 and Ar 3 may be directly bonded or bonded via a divalent group to form a ring. ]
前記有機層が、請求項1~請求項4のいずれか一項に記載の組成物を含有する層である、発光素子。
A light-emitting element having an anode, a cathode, and an organic layer provided between the anode and the cathode,
A light-emitting device, wherein the organic layer is a layer containing the composition according to any one of claims 1 to 4.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2021160164 | 2021-09-29 | ||
| JP2021160164 | 2021-09-29 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2023050135A true JP2023050135A (en) | 2023-04-10 |
Family
ID=85802135
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022147451A Pending JP2023050135A (en) | 2021-09-29 | 2022-09-15 | Composition and light emitting element containing the same |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2023050135A (en) |
-
2022
- 2022-09-15 JP JP2022147451A patent/JP2023050135A/en active Pending
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7216754B2 (en) | COMPOSITION AND LIGHT-EMITTING DEVICE CONTAINING THE SAME | |
| WO2018062276A1 (en) | Light-emitting element | |
| WO2016194695A1 (en) | Light-emitting element and method for manufacturing same | |
| WO2018062277A1 (en) | Light-emitting element | |
| JP6923692B2 (en) | Manufacturing method of light emitting element | |
| JP2023050135A (en) | Composition and light emitting element containing the same | |
| JP2023050141A (en) | Composition and light emitting element containing the same | |
| JP2022052727A (en) | Light emitting element | |
| JP7086259B2 (en) | Light emitting device and composition | |
| JP7058792B2 (en) | Light emitting device and composition | |
| JP2023050138A (en) | Light-emitting element | |
| WO2023054109A1 (en) | Composition and light-emitting element comprising same | |
| JP7086258B2 (en) | Light emitting device and composition | |
| JP7079883B2 (en) | Light emitting device and composition | |
| JP7663487B2 (en) | Polymer compound, composition and light-emitting device | |
| JP2023050139A (en) | Composition and light-emitting element containing the same | |
| JP7321912B2 (en) | COMPOSITION FOR LIGHT-EMITTING DEVICE AND FILM AND LIGHT-EMITTING DEVICE USING THE SAME | |
| JP7261729B2 (en) | Polymer compound and light-emitting device using the same | |
| JP2023050137A (en) | Composition and light emitting element containing the same | |
| JP2023050140A (en) | Light-emitting element | |
| JP2023050142A (en) | Light-emitting element | |
| JP2023050143A (en) | Light-emitting element | |
| WO2018088573A1 (en) | Light emitting element, and metal oxide and composition used in same | |
| JP2023050129A (en) | light emitting element | |
| JP2023050131A (en) | light emitting element |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| AA64 | Notification of invalidation of claim of internal priority (with term) |
Free format text: JAPANESE INTERMEDIATE CODE: A241764 Effective date: 20221004 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20221021 |