JP2022550316A - 修飾ehd2ドメインを含む結合モジュール - Google Patents
修飾ehd2ドメインを含む結合モジュール Download PDFInfo
- Publication number
- JP2022550316A JP2022550316A JP2022518946A JP2022518946A JP2022550316A JP 2022550316 A JP2022550316 A JP 2022550316A JP 2022518946 A JP2022518946 A JP 2022518946A JP 2022518946 A JP2022518946 A JP 2022518946A JP 2022550316 A JP2022550316 A JP 2022550316A
- Authority
- JP
- Japan
- Prior art keywords
- ehd2
- domain
- binding
- amino acid
- seq
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/46—Hybrid immunoglobulins
- C07K16/468—Immunoglobulins having two or more different antigen binding sites, e.g. multifunctional antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/24—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against cytokines, lymphokines or interferons
- C07K16/241—Tumor Necrosis Factors
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
- C07K16/2809—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily against the T-cell receptor (TcR)-CD3 complex
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2863—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against receptors for growth factors, growth regulators
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/32—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against translation products of oncogenes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/31—Immunoglobulins specific features characterized by aspects of specificity or valency multispecific
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/35—Valency
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/52—Constant or Fc region; Isotype
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/52—Constant or Fc region; Isotype
- C07K2317/524—CH2 domain
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/60—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/60—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments
- C07K2317/64—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments comprising a combination of variable region and constant region components
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Immunology (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Biophysics (AREA)
- Genetics & Genomics (AREA)
- Molecular Biology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Biochemistry (AREA)
- Oncology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- General Chemical & Material Sciences (AREA)
- Peptides Or Proteins (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Abstract
Description
(i)CH1ドメイン、
(ii)CLドメイン、
(iii)第1の修飾EHD2ドメイン(EHD2-1)、および
(iv)第2の修飾EHD2ドメイン(EHD2-2)の1つをさらに含み、そして、
ここで、BD4を含む第4のポリペプチド鎖は、
(i)の場合にはCLドメイン、
(ii)の場合にはCH1ドメイン、
(iii)の場合には第2の修飾EHD2ドメイン(EHD2-2)、および、
(iv)の場合には第1の修飾EHD2ドメイン(EHD2-1)、をさらに含み、
ここで、EHD2-1およびEHD2-2のアミノ酸配列は、互いに異なっており、そしてそれぞれは、配列番号:1に対して少なくとも70%のアミノ酸同一性を有し、かつ14位にCysを有しないアミノ酸配列、または配列番号:1に対して少なくとも70%のアミノ酸同一性を有し、かつ102位にCysを有しないアミノ酸配列、から選択される。
BD5に結合する、
(i)CH1ドメイン、
(ii)CLドメイン、
(iii)第1の修飾EHD2ドメイン(EHD2-1)、または
(iv)第2の修飾EHD2ドメイン(EHD2-2)、
および
BD6に結合する、
(i)の場合にはCLドメイン、
(ii)の場合にはCH1ドメイン、
(iii)の場合には第2の修飾EHD2ドメイン(EHD2-2)、そして
(iv)の場合には第1の修飾EHD2ドメイン(EHD2-1)、を含み、ここで、EHD2-1およびEHD2-2のアミノ酸配列は、互いに異なっており、そしてそれぞれは、配列番号:1に対して少なくとも70%のアミノ酸同一性を有し、かつ14位にCysを有しないアミノ酸配列、または配列番号:1に対して少なくとも70%のアミノ酸同一性を有し、かつ102位にCysを有しないアミノ酸配列、から選択される。
BD7に結合する、
(i)CH1ドメイン、
(ii)CLドメイン、
(iii)第1の修飾EHD2ドメイン(EHD2-1)、または
(iv)第2の修飾EHD2ドメイン(EHD2-2)、
および、
BD8に結合する、
(i)の場合にはCLドメイン、
(ii)の場合にはCH1ドメイン、
(iii)の場合には第2の修飾EHD2ドメイン(EHD2-2)、そして
(iv)の場合には第1の修飾EHD2ドメイン(EHD2-1)、をさらに含み、ここで、EHD2-1およびEHD2-2のアミノ酸配列は、互いに異なっており、そしてそれぞれは、配列番号:1に対して少なくとも70%のアミノ酸同一性を有し、かつ14位にCysを有しないアミノ酸配列、または配列番号:1に対して少なくとも70%のアミノ酸同一性を有し、かつ102位にCysを有しないアミノ酸配列、から選択される。
配列番号:1
(wtヒトEHD2コアアミノ酸配列;C14位、N39位およびC102位に下線付き)
DFTPPTVKIL QSSCDGGGHF PPTIQLLCLV SGYTPGTINI TWLEDGQVMD VDLSTASTTQ EGELASTQSE LTLSQKHWLS DRTYTCQVTY QGHTFEDSTK KCADSN
(14位にCysの置換を有する修飾EHD2アミノ酸配列;X=Cys以外のいずれかのアミノ酸、好ましくはSer、Gly、Ala、Thr、Gln、Asn、またはTyr、最も好ましくはSer)
DFTPPTVKIL QSSXDGGGHF PPTIQLLCLV SGYTPGTINI TWLEDGQVMD VDLSTASTTQ EGELASTQSE LTLSQKHWLS DRTYTCQVTY QGHTFEDSTK KCADSN
(102位にCysの置換を有する修飾EHD2アミノ酸配列;X=Cys以外のいずれかのアミノ酸、好ましくはSer、Gly、Ala、Thr、Gln、Asn、またはTyr、最も好ましくはSer)
DFTPPTVKIL QSSCDGGGHF PPTIQLLCLV SGYTPGTINI TWLEDGQVMD VDLSTASTTQ EGELASTQSE LTLSQKHWLS DRTYTCQVTY QGHTFEDSTK KXADSN
(14位にCysを含む修飾EHD2アミノ酸配列)
DFTPPTVKIL QSSSDGGGHF PPTIQLLCLV SGYTPGTINI TWLEDGQVMD VDLSTASTTQ EGELASTQSE LTLSQKHWLS DRTYTCQVTY QGHTFEDSTK KCADSN
(14位にSer、39位にGlnを含む修飾EHD2アミノ酸配列)
DFTPPTVKIL QSSSDGGGHF PPTIQLLCLV SGYTPGTIQI TWLEDGQVMD VDLSTASTTQ EGELASTQSE LTLSQKHWLS DRTYTCQVTY QGHTFEDSTK KCADSN
(102位にSerを含む修飾EHD2アミノ酸配列)
DFTPPTVKIL QSSCDGGGHF PPTIQLLCLV SGYTPGTINI TWLEDGQVMD VDLSTASTTQ EGELASTQSE LTLSQKHWLS DRTYTCQVTY QGHTFEDSTK KSADSN
(102位にSer、39位にGlnを含む修飾EHD2アミノ酸配列)
DFTPPTVKIL QSSCDGGGHF PPTIQLLCLV SGYTPGTIQI TWLEDGQVMD VDLSTASTTQ EGELASTQSE LTLSQKHWLS DRTYTCQVTY QGHTFEDSTK KSADSN
(Igκリーダー配列)
METDTLLLWVLLLWVPGSTG
(VL5D5-EHD2-1 (N39Q))
DIQMTQSPSSLSASVGDRVTITCKSSQSLLYTSSQKNYLAWYQQKPGKAPKLLIYWASTRESGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQYYAYPWTFGQGTKVEIKRTDFTPPTVKILQSSSDGGGHFPPTIQLLCLVSGYTPGTIQITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKCADSN
(VH5D5-EHD2-2-Fchole)
EVQLVESGGGLVQPGGSLRLSCAASGYTFTSYWLHWVRQAPGKGLEWVGMIDPSNSDTRFNPNFKDRFTISADTSKNTAYLQMNSLRAEDTAVYYCATYRSYVTPLDYWGQGTLVTVSSDFTPPTVKILQSSCDGGGHFPPTIQLLCLVSGYTPGTINITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKSADSNGTDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVCTLPPSRDELTKNQVSLSCAVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLVSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
(VL5D5-EHD2-2)
DIQMTQSPSSLSASVGDRVTITCKSSQSLLYTSSQKNYLAWYQQKPGKAPKLLIYWASTRESGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQYYAYPWTFGQGTKVEIKRTDFTPPTVKILQSSCDGGGHFPPTIQLLCLVSGYTPGTINITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKSADSN
(VH5D5-EHD2-1(N39Q)-Fchole)
EVQLVESGGGLVQPGGSLRLSCAASGYTFTSYWLHWVRQAPGKGLEWVGMIDPSNSDTRFNPNFKDRFTISADTSKNTAYLQMNSLRAEDTAVYYCATYRSYVTPLDYWGQGTLVTVSSDFTPPTVKILQSSSDGGGHFPPTIQLLCLVSGYTPGTIQITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKCADSNGTDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVCTLPPSRDELTKNQVSLSCAVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLVSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
(VL3-43-CLλ)
QAGLTQPPAVSVAPGQTASITCGRDNIGSRSVHWYQQKPGQAPVLVVYDDSDRPAGIPERFSGSNYENTATLTISRVEAGDEADYYCQVWGITSDHVVFGGGTKLTVLGQPKAAPSVTLFPPSSEELQANKATLVCLISDFYPGAVTVAWKADSSPVKAGVETTTPSKQSNNKYAASSYLSLTPEQWKSHRSYSCQVTHEGSTVEKTVAPTECS
(VH3-43-CH1-Fcknob)
QVQLQQSGPGLVKPSQTLSLTCAISGDSVSSNRAAWNWIRQSPSRGLEWLGRTYYRSKWYNDYAQSLKSRITINPDTPKNQFSLQLNSVTPEDTAVYYCARDGQLGLDALDIWGQGTMVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCGTDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPCRDELTKNQVSLWCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
(VLhuU3-EHD2-1(N39Q))
DIQMTQSPSSLSASVGDRVTITCRASQDIRNYLNWYQQKPGKAPKLLIYYTSRLHSGVPSRFSGSGSGTDFTFTISSLQPEDIATYYCQQGNTLPWTFGQGTKLEIKRTDFTPPTVKILQSSSDGGGHFPPTIQLLCLVSGYTPGTIQITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKCADSN
(VHhuU3-EHD2-2-Fchole)
QVQLVQSGAEVKKPGSSVKVSCKASGGTFSGYTMNWVRQAPGQGLEWMGLINPYKGVSTYNGKFKDRVTITADKSTSTAYMELSSLRSEDTAVYYCARSGYYGDSDWYFDVWGQGTLVTVSSDFTPPTVKILQSSCDGGGHFPPTIQLLCLVSGYTPGTINITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKSADSNGTDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVCTLPPSRDELTKNQVSLSCAVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLVSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
(VH5D5-EHD2-2-リンカー-VH3-43-CH1)
EVQLVESGGGLVQPGGSLRLSCAASGYTFTSYWLHWVRQAPGKGLEWVGMIDPSNSDTRFNPNFKDRFTISADTSKNTAYLQMNSLRAEDTAVYYCATYRSYVTPLDYWGQGTLVTVSSDFTPPTVKILQSSCDGGGHFPPTIQLLCLVSGYTPGTINITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKSADSNGTGGSGGGGSGGQVQLQQSGPGLVKPSQTLSLTCAISGDSVSSNRAAWNWIRQSPSRGLEWLGRTYYRSKWYNDYAQSLKSRITINPDTPKNQFSLQLNSVTPEDTAVYYCARDGQLGLDALDIWGQGTMVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSC
(VH3-43-CH1-リンカー-VH5D5-EHD2-2)
QVQLQQSGPGLVKPSQTLSLTCAISGDSVSSNRAAWNWIRQSPSRGLEWLGRTYYRSKWYNDYAQSLKSRITINPDTPKNQFSLQLNSVTPEDTAVYYCARDGQLGLDALDIWGQGTMVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCGTGGSGGGGSGGEVQLVESGGGLVQPGGSLRLSCAASGYTFTSYWLHWVRQAPGKGLEWVGMIDPSNSDTRFNPNFKDRFTISADTSKNTAYLQMNSLRAEDTAVYYCATYRSYVTPLDYWGQGTLVTVSSDFTPPTVKILQSSCDGGGHFPPTIQLLCLVSGYTPGTINITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKSADSN
(VH3-43-CH1-リンカー-VH5D5-EHD2-2-Fchole)
QVQLQQSGPGLVKPSQTLSLTCAISGDSVSSNRAAWNWIRQSPSRGLEWLGRTYYRSKWYNDYAQSLKSRITINPDTPKNQFSLQLNSVTPEDTAVYYCARDGQLGLDALDIWGQGTMVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCGTGGSGGGGSGGEVQLVESGGGLVQPGGSLRLSCAASGYTFTSYWLHWVRQAPGKGLEWVGMIDPSNSDTRFNPNFKDRFTISADTSKNTAYLQMNSLRAEDTAVYYCATYRSYVTPLDYWGQGTLVTVSSDFTPPTVKILQSSCDGGGHFPPTIQLLCLVSGYTPGTINITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKSADSNGTDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVCTLPPSRDELTKNQVSLSCAVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLVSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
(VH3-43-CH1-リンカー-VH3-43-CH1-Fcknob)
QVQLQQSGPGLVKPSQTLSLTCAISGDSVSSNRAAWNWIRQSPSRGLEWLGRTYYRSKWYNDYAQSLKSRITINPDTPKNQFSLQLNSVTPEDTAVYYCARDGQLGLDALDIWGQGTMVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCGTGGSGGGGSGGQVQLQQSGPGLVKPSQTLSLTCAISGDSVSSNRAAWNWIRQSPSRGLEWLGRTYYRSKWYNDYAQSLKSRITINPDTPKNQFSLQLNSVTPEDTAVYYCARDGQLGLDALDIWGQGTMVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCGTDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPCRDELTKNQVSLWCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
(VH5D5-EHD2-2-リンカー-VH3-43-CH1-Fchole)
EVQLVESGGGLVQPGGSLRLSCAASGYTFTSYWLHWVRQAPGKGLEWVGMIDPSNSDTRFNPNFKDRFTISADTSKNTAYLQMNSLRAEDTAVYYCATYRSYVTPLDYWGQGTLVTVSSDFTPPTVKILQSSCDGGGHFPPTIQLLCLVSGYTPGTINITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKSADSNGTGGSGGGGSGGQVQLQQSGPGLVKPSQTLSLTCAISGDSVSSNRAAWNWIRQSPSRGLEWLGRTYYRSKWYNDYAQSLKSRITINPDTPKNQFSLQLNSVTPEDTAVYYCARDGQLGLDALDIWGQGTMVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVCTLPPSRDELTKNQVSLSCAVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLVSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
(VH3-43-EHD2-2-Fc)
QVQLQQSGPGLVKPSQTLSLTCAISGDSVSSNRAAWNWIRQSPSRGLEWLGRTYYRSKWYNDYAQSLKSRITINPDTPKNQFSLQLNSVTPEDTAVYYCARDGQLGLDALDIWGQGTMVTVSSDFTPPTVKILQSSCDGGGHFPPTIQLLCLVSGYTPGTINITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKSADSNGTDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
(VL3-43-EHD2-1(N39Q))
QAGLTQPPAVSVAPGQTASITCGRDNIGSRSVHWYQQKPGQAPVLVVYDDSDRPAGIPERFSGSNYENTATLTISRVEAGDEADYYCQVWGITSDHVVFGGGTKLTVLGTDFTPPTVKILQSSSDGGGHFPPTIQLLCLVSGYTPGTIQITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKCADSN
(VHhu225-CH1-リンカー-VH3-43-EHD2-2-Fc)
EVQLVESGGGLVQPGGSLRLSCAASGFSLTNYGVHWVRQAPGKGLEWLGVIWSGGNTDYNTPFTSRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARALTYYDYEFAYWGQGTTVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKRVEPKSCGGSGGGGSGGQVQLQQSGPGLVKPSQTLSLTCAISGDSVSSNRAAWNWIRQSPSRGLEWLGRTYYRSKWYNDYAQSLKSRITINPDTPKNQFSLQLNSVTPEDTAVYYCARDGQLGLDALDIWGQGTMVTVSSDFTPPTVKILQSSCDGGGHFPPTIQLLCLVSGYTPGTINITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKSADSNGTDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
(VLhu225-CLk)
DIQLTQSPSFLSASVGDRVTITCRASQSIGTNIHWYQQKPGKAPKLLIKYASESISGVPSRFSGSGSGTEFTLTISSLQPEDFATYYCQQNNNWPTTFGAGTKLEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
(VH3-43-EHD2-2-リンカー-VHhu225-CH1-Fc)
QVQLQQSGPGLVKPSQTLSLTCAISGDSVSSNRAAWNWIRQSPSRGLEWLGRTYYRSKWYNDYAQSLKSRITINPDTPKNQFSLQLNSVTPEDTAVYYCARDGQLGLDALDIWGQGTMVTVSSDFTPPTVKILQSSCDGGGHFPPTIQLLCLVSGYTPGTINITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKSADSNGTGGSGGGGSGGEVQLVESGGGLVQPGGSLRLSCAASGFSLTNYGVHWVRQAPGKGLEWLGVIWSGGNTDYNTPFTSRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARALTYYDYEFAYWGQGTTVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKRVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
(VH3-43-EHD2-2(C102A)-His)
QVQLQQSGPGLVKPSQTLSLTCAISGDSVSSNRAAWNWIRQSPSRGLEWLGRTYYRSKWYNDYAQSLKSRITINPDTPKNQFSLQLNSVTPEDTAVYYCARDGQLGLDALDIWGQGTMVTVSSDFTPPTVKILQSSCDGGGHFPPTIQLLCLVSGYTPGTINITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKAADSNAAAHHHHHH
(VH3-43-EHD2-2(C102W)-His)
QVQLQQSGPGLVKPSQTLSLTCAISGDSVSSNRAAWNWIRQSPSRGLEWLGRTYYRSKWYNDYAQSLKSRITINPDTPKNQFSLQLNSVTPEDTAVYYCARDGQLGLDALDIWGQGTMVTVSSDFTPPTVKILQSSCDGGGHFPPTIQLLCLVSGYTPGTINITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKWADSNAAAHHHHHH
(VH3-43-EHD2-2(C102N)-His)
QVQLQQSGPGLVKPSQTLSLTCAISGDSVSSNRAAWNWIRQSPSRGLEWLGRTYYRSKWYNDYAQSLKSRITINPDTPKNQFSLQLNSVTPEDTAVYYCARDGQLGLDALDIWGQGTMVTVSSDFTPPTVKILQSSCDGGGHFPPTIQLLCLVSGYTPGTINITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKNADSNAAAHHHHHH
(VH3-43-EHD2-2(C102T)-His)
QVQLQQSGPGLVKPSQTLSLTCAISGDSVSSNRAAWNWIRQSPSRGLEWLGRTYYRSKWYNDYAQSLKSRITINPDTPKNQFSLQLNSVTPEDTAVYYCARDGQLGLDALDIWGQGTMVTVSSDFTPPTVKILQSSCDGGGHFPPTIQLLCLVSGYTPGTINITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKTADSNAAAHHHHHH
(VH3-43-EHD2-2(C102S)-His)
QVQLQQSGPGLVKPSQTLSLTCAISGDSVSSNRAAWNWIRQSPSRGLEWLGRTYYRSKWYNDYAQSLKSRITINPDTPKNQFSLQLNSVTPEDTAVYYCARDGQLGLDALDIWGQGTMVTVSSDFTPPTVKILQSSCDGGGHFPPTIQLLCLVSGYTPGTINITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKSADSNAAAHHHHHH
(VL3-43-EHD2-1(C14A, N39Q))
QAGLTQPPAVSVAPGQTASITCGRDNIGSRSVHWYQQKPGQAPVLVVYDDSDRPAGIPERFSGSNYENTATLTISRVEAGDEADYYCQVWGITSDHVVFGGGTKLTVLDFTPPTVKILQSSADGGGHFPPTIQLLCLVSGYTPGTIQITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKCADSN
(VL3-43-EHD2-1(C14T, N39Q))
QAGLTQPPAVSVAPGQTASITCGRDNIGSRSVHWYQQKPGQAPVLVVYDDSDRPAGIPERFSGSNYENTATLTISRVEAGDEADYYCQVWGITSDHVVFGGGTKLTVLDFTPPTVKILQSSTDGGGHFPPTIQLLCLVSGYTPGTIQITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKCADSN
(VL3-43-EHD2-1(C14N, N39Q))
QAGLTQPPAVSVAPGQTASITCGRDNIGSRSVHWYQQKPGQAPVLVVYDDSDRPAGIPERFSGSNYENTATLTISRVEAGDEADYYCQVWGITSDHVVFGGGTKLTVLDFTPPTVKILQSSNDGGGHFPPTIQLLCLVSGYTPGTIQITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKCADSN
(VL3-43-EHD2-1(C14W, N39Q))
QAGLTQPPAVSVAPGQTASITCGRDNIGSRSVHWYQQKPGQAPVLVVYDDSDRPAGIPERFSGSNYENTATLTISRVEAGDEADYYCQVWGITSDHVVFGGGTKLTVLDFTPPTVKILQSSWDGGGHFPPTIQLLCLVSGYTPGTIQITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKCADSN
(VL3-43-EHD2-1(C14S, N39Q))
QAGLTQPPAVSVAPGQTASITCGRDNIGSRSVHWYQQKPGQAPVLVVYDDSDRPAGIPERFSGSNYENTATLTISRVEAGDEADYYCQVWGITSDHVVFGGGTKLTVLDFTPPTVKILQSSSDGGGHFPPTIQLLCLVSGYTPGTIQITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKCADSN
(VL3-43-EHD2-1(C14S))
QAGLTQPPAVSVAPGQTASITCGRDNIGSRSVHWYQQKPGQAPVLVVYDDSDRPAGIPERFSGSNYENTATLTISRVEAGDEADYYCQVWGITSDHVVFGGGTKLTVLDFTPPTVKILQSSSDGGGHFPPTIQLLCLVSGYTPGTINITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKCADSN
(VH3-43-EHD2-2(N39Q, C102S)-His)
QVQLQQSGPGLVKPSQTLSLTCAISGDSVSSNRAAWNWIRQSPSRGLEWLGRTYYRSKWYNDYAQSLKSRITINPDTPKNQFSLQLNSVTPEDTAVYYCARDGQLGLDALDIWGQGTMVTVSSDFTPPTVKILQSSCDGGGHFPPTIQLLCLVSGYTPGTIQITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKSADSNAAAHHHHHH
(VHhuU3-EHD2-2-リンカー-VH3-43-CH1-Fcknob)
QVQLVQSGAEVKKPGSSVKVSCKASGGTFSGYTMNWVRQAPGQGLEWMGLINPYKGVSTYNGKFKDRVTITADKSTSTAYMELSSLRSEDTAVYYCARSGYYGDSDWYFDVWGQGTLVTVSSDFTPPTVKILQSSCDGGGHFPPTIQLLCLVSGYTPGTINITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKSADSNGGSGGGGSGGQVQLQQSGPGLVKPSQTLSLTCAISGDSVSSNRAAWNWIRQSPSRGLEWLGRTYYRSKWYNDYAQSLKSRITINPDTPKNQFSLQLNSVTPEDTAVYYCARDGQLGLDALDIWGQGTMVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCGTDKTHTCPPCPAPPVAGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPCRDELTKNQVSLWCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
(VH3-43-CH1-Fchole)
QVQLQQSGPGLVKPSQTLSLTCAISGDSVSSNRAAWNWIRQSPSRGLEWLGRTYYRSKWYNDYAQSLKSRITINPDTPKNQFSLQLNSVTPEDTAVYYCARDGQLGLDALDIWGQGTMVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCGTDKTHTCPPCPAPPVAGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVCTLPPSRDELTKNQVSLSCAVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLVSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
(VH3-43- CH1-リンカー-VHhuU3-EHD2-2- Fchole)
QVQLQQSGPGLVKPSQTLSLTCAISGDSVSSNRAAWNWIRQSPSRGLEWLGRTYYRSKWYNDYAQSLKSRITINPDTPKNQFSLQLNSVTPEDTAVYYCARDGQLGLDALDIWGQGTMVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCGGSGGGGSGGQVQLVQSGAEVKKPGSSVKVSCKASGGTFSGYTMNWVRQAPGQGLEWMGLINPYKGVSTYNGKFKDRVTITADKSTSTAYMELSSLRSEDTAVYYCARSGYYGDSDWYFDVWGQGTLVTVSSDFTPPTVKILQSSCDGGGHFPPTIQLLCLVSGYTPGTINITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKSADSNGTDKTHTCPPCPAPPVAGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVCTLPPSRDELTKNQVSLSCAVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLVSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
(VHhu36-EHD2-2-Fchole)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTENIIHWVRQAPGQGLEWMGWFHPGSGSIKYNEKFKDRVTMTADTSTSTVYMELSSLRSEDTAVYYCARHGGTGRGAMDYWGQGTLVTVSSDFTPPTVKILQSSCDGGGHFPPTIQLLCLVSGYTPGTINITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKSADSNGTDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVCTLPPSRDELTKNQVSLSCAVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLVSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
(VLhu36-EHD2-1(N39Q))
DIQMTQSPSSLSASVGDRVTITCRASKSVSTSAYSYMHWYQQKPGKAPKLLIYLASNLESGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQHSRELPYTFGQGTKLEIKRDFTPPTVKILQSSSDGGGHFPPTIQLLCLVSGYTPGTIQITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKCADSN
(VHhu225-CH1-リンカー-VH3-43-EHD2-2-His)
EVQLVESGGGLVQPGGSLRLSCAASGFSLTNYGVHWVRQAPGKGLEWLGVIWSGGNTDYNTPFTSRFTISRDNSKNTLYLQMNSLRAEDTAVYYCARALTYYDYEFAYWGQGTTVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCGGSGGGGSGGQVQLQQSGPGLVKPSQTLSLTCAISGDSVSSNRAAWNWIRQSPSRGLEWLGRTYYRSKWYNDYAQSLKSRITINPDTPKNQFSLQLNSVTPEDTAVYYCARDGQLGLDALDIWGQGTMVTVSSDFTPPTVKILQSSCDGGGHFPPTIQLLCLVSGYTPGTINITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKSADSNAAAHHHHHH
(VLhu36-CLκ)
DIQMTQSPSSLSASVGDRVTITCRASKSVSTSAYSYMHWYQQKPGKAPKLLIYLASNLESGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQHSRELPYTFGQGTKLEIKRRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
(VHhu36-CH1-Fchole)
QVQLVQSGAEVKKPGASVKVSCKASGYTFTENIIHWVRQAPGQGLEWMGWFHPGSGSIKYNEKFKDRVTMTADTSTSTVYMELSSLRSEDTAVYYCARHGGTGRGAMDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCGTDKTHTCPPCPAPPVAGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVCTLPPSRDELTKNQVSLSCAVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLVSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
(VH2C11-EHD2-1(N39Q))
EVQLVESGGGLVQPGKSLKLSCEASGFTFSGYGMHWVRQAPGRGLESVAYITSSSINIKYADAVKGRFTVSRDNAKNLLFLQMNILKSEDTAMYYCARFDWDKNYWGQGTMVTVSSDFTPPTVKILQSSSDGGGHFPPTIQLLCLVSGYTPGTIQITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKCADSN
(VL2C11-EHD2-2-Fcknob)
DIQMTQSPSSLPASLGDRVTINCQASQDISNYLNWYQQKPGKAPKLLIYYTNKLADGVPSRFSGSGSGRDSSFTISSLESEDIGSYYCQQYYNYPWTFGPGTKLEIKDFTPPTVKILQSSCDGGGHFPPTIQLLCLVSGYTPGTINITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKSADSNGTDKTHTCPPCPAPPVAGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPCRDELTKNQVSLWCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
(VL2C11-EHD2-1(N39Q))
DIQMTQSPSSLPASLGDRVTINCQASQDISNYLNWYQQKPGKAPKLLIYYTNKLADGVPSRFSGSGSGRDSSFTISSLESEDIGSYYCQQYYNYPWTFGPGTKLEIKDFTPPTVKILQSSSDGGGHFPPTIQLLCLVSGYTPGTIQITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKCADSN
(VH2C11-EHD2-2-Fcknob)
EVQLVESGGGLVQPGKSLKLSCEASGFTFSGYGMHWVRQAPGRGLESVAYITSSSINIKYADAVKGRFTVSRDNAKNLLFLQMNILKSEDTAMYYCARFDWDKNYWGQGTMVTVSSDFTPPTVKILQSSCDGGGHFPPTIQLLCLVSGYTPGTINITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKSADSNGTDKTHTCPPCPAPPVAGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPCRDELTKNQVSLWCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
(VLS309-CLκ)
EIVLTQSPGTLSLSPGERATLSCRASQTVSSTSLAWYQQKPGQAPRLLIYGASSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQHDTSLTFGGGTKVEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
(VLP2B-2F6-EHD2-1(N39Q))
QSALTQPPSASGSPGQSVTISCTGTSSDVGGYNYVSWYQQHPGKAPKLMIYEVSKRPSGVPDRFSGSKSGNTASLTVSGLQAEDEADYYCSSYAGSNNLVCGGGTKLTVLDFTPPTVKILQSSSDGGGHFPPTIQLLCLVSGYTPGTIQITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKCADSN
(VHS309-CH1-VHP2B-2F6-EHD2-2-Fc)
QVQLVQSGAEVKKPGASVKVSCKASGYPFTSYGISWVRQAPGQGLEWMGWISTYNGNTNYAQKFQGRVTMTTDTSTTTGYMELRRLRSDDTAVYYCARDYTRGAWFGESLIGGFDNWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCGGSGGGGSGGQVQLQESGPGLVKPSETLSLTCTVSGYSISSGYYWGWIRQPPGKGLEWIGSIYHSGSTYYNPSLKTRVTISVDTSKNQFSLKLSSVTAADTAVYYCARAVVGIVVVPAAGRRAFDIWGQGTMVTVSSDFTPPTVKILQSSCDGGGHFPPTIQLLCLVSGYTPGTINITWLEDGQVMDVDLSTASTTQEGELASTQSELTLSQKHWLSDRTYTCQVTYQGHTFEDSTKKSADSNDKTHTCPPCPAPPVAGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
本発明を以下に詳細に説明する前に、本発明は、本明細書に記載の特定の方法論、プロトコルおよび試薬に限定されないと理解される。また、本明細書で使用される用語は、特定の実施態様を説明する目的だけのものであり、添付の特許請求の範囲によってのみ限定される本発明の範囲を限定することを意図していないと理解される。他に定義されない限り、本明細書で使用されるすべての技術用語および科学用語は、当業者によって一般的に理解されるのと同じ意味を有する。
以下では、本発明のさまざまな態様をより詳細に定義する。このように定義されている各態様は、反対のことが明確に示されない限り、他の任意の態様(複数可)と組み合わされ得る。特に、好ましいまたは有利であると示されている任意の特徴は、好ましいまたは有利であると示されている任意の他の特徴(複数可)と組み合わされ得る。
(i)BD3-CH1およびBD4-CL;
(ii)BD3-CLおよびBD4-CH1;
(iii)BD3-EHD2-1およびBD4-EHD2-2;または
(iv)BD3-EHD2-2およびBD4-EHD2-1、
を含む第3のポリペプチド鎖および第4のポリペプチド鎖を含み得る。
(i)BD1-(任意のリンカー)-EHD2-2-リンカー-BD3-(任意のリンカー)-CH1
(ii)BD2-(任意のリンカー)-EHD2-1
(iii)BD4-(任意のリンカー)-CL
(i)BD3-(任意のリンカー)-CH1-リンカー-BD1-(任意のリンカー)-EHD2-2
(ii)BD2-(任意のリンカー)-EHD2-1
(iii)BD4-(任意のリンカー)-CL
(i)BD1-(任意のリンカー)-EHD2-1-Fc
(ii)BD2-(任意のリンカー)-EHD2-2
(iii)BD3-(任意のリンカー)-CH1-Fc
(iv)BD4-(任意のリンカー)-CL。
(i)BD1およびBD2、ならびに修飾EHD2ドメインEHD2-1およびEHD2-2を含む第1および第2のポリペプチド鎖;
(ii)BD3およびBD4、ならびに、修飾EHD2ドメインEHD2-1およびEHD2-2、またはドメインCH1およびCLのどちらか一方を含む第3および第4のポリペプチド鎖;および
(iii)修飾EHD2ドメインEHD2-1およびEHD2-2、またはドメインCH1およびCLのどちから一方に結合するBD5およびBD6。
(i)BD5-(任意のリンカー)-CH1-リンカー-BD1-(任意のリンカー)-EHD2-1-(任意のリンカー)-Fc
(ii)BD2-(任意のリンカー)-EHD2-2
(iii)BD3-(任意のリンカー)-CH1-Fc
(iv)BD4-(任意のリンカー)-CL
(v)BD6-(任意のリンカー)-CL。
(i)BD1-(任意のリンカー)-EHD2-1-(任意のリンカー)-Fc
(ii)BD2-(任意のリンカー)-EHD2-2
(iii)BD5-(任意のリンカー)-CH1-リンカー-BD3-(任意のリンカー)-CH1-(任意のリンカー)-Fc
(iv)BD4-(任意のリンカー)-CL
(v)BD6-(任意のリンカー)-CL。
(i)BD1-(任意のリンカー)-EHD2-1-リンカー-BD3-(任意のリンカー)-CH1-(任意のリンカー)-Fc
(ii)BD2-(任意のリンカー)-EHD2-2
(iii)BD5-(任意のリンカー)-CH1-(任意のリンカー)-Fc
(iv)BD4-(任意のリンカー)-CL
(v)BD6-(任意のリンカー)-CL。
(i)BD1およびBD2、ならびに修飾EHD2ドメインEHD2-1およびEHD2-2を含む第1および第2のポリペプチド鎖;
(ii)BD3およびBD4、ならびに、修飾EHD2ドメインEHD2-1およびEHD2-2、またはドメインCH1およびCLのどちらか一方を含む第3および第4のポリペプチド鎖;
(iii)修飾EHD2ドメインEHD2-1およびEHD2-2、またはドメインCH1およびCLのどちらか一方に結合するBD5およびBD6;および
(iv)修飾EHD2ドメインEHD2-1およびEHD2-2、またはドメインCH1およびCLのどちらか一方に結合するBD7およびBD8。
(i)BD5-(任意のリンカー)-CH1-リンカー-BD1-(任意のリンカー)-EHD2-1-(任意のリンカー)-Fc
(ii)BD2-(任意のリンカー)-EHD2-2
(iii)BD7-(任意のリンカー)-CH1-リンカー-BD3-(任意のリンカー)-EHD2-1-(任意のリンカー)-Fc
(iv)BD4-(任意のリンカー)-EHD2-2
(v)BD6-(任意のリンカー)-CL
(vi)BD8-(任意のリンカー)-CL。
(i)BD1-(任意のリンカー)-EHD2-1-リンカー-BD5-(任意のリンカー)-CH1-(任意のリンカー)-Fc
(ii)BD2-(任意のリンカー)-EHD2-2
(iii)BD3-(任意のリンカー)-EHD2-1-リンカー-BD7-(任意のリンカー)-CH1-(任意のリンカー)-Fc
(iv)BD4-(任意のリンカー)-EHD2-2
(v)BD6-(任意のリンカー)-CL
(vi)BD8-(任意のリンカー)-CL。
(1)疎水性:Met、Ala、Val、Leu、Ile;
(2)中性親水性:Cys、Ser、Thr、Asn、Gln;
(3)酸性:Asp、Glu;
(4)塩基性:His、Lys、Arg;
(5)鎖の配向に影響を与える残基:Gly、Pro;および
(6)芳香族:Trp、Tyr、Phe。
(1)軽鎖VL3-43-CLλ(配列番号:13)および重鎖VH3-43-CH1-Fcknob(配列番号:14)を有する定常部分と、(i)eIgG1という結果になるHC1-LC2(重鎖:VH5D5-EHD2-1(N39Q)-Fchole(配列番号:12)、軽鎖:VL5D5-EHD2-2 (配列番号:11))、または(ii)eIgG2という結果になるHC2-LC1(重鎖:VH5D5-EHD2-2-Fchole(配列番号:10)、軽鎖:VL5D5-EHD2-1(N39Q)(配列番号:9))のどちらか一方との組み合わせ;
(2)軽鎖のVL3-43-CLλ(配列番号:13)および重鎖のVH3-43-CH1-Fcknob(配列番号:14)とeIgG(重鎖:VHhuU3-EHD2-2-Fchole(配列番号:16)、軽鎖:VLhuU3-EHD2-1(N39Q)(配列番号:15));
(3)配列番号:13または15に特定される軽鎖、および配列番号:14、16、20、39、40または41に特定される重鎖;
(4)軽鎖のVL3-43-CLλ(配列番号:13)と重鎖のVH3-43-CH1-Fcknob(配列番号:14)との対合、および軽鎖のVLhu36-EHD2-1(N39Q)(配列番号:43)と重鎖のVHhu36-EHD2-2-Fchole(配列番号:42)との対合;
(5)軽鎖のVL3-43-EHD2-1(N39Q)(配列番号:23)および重鎖のVH3-43-EHD2-2-Fc(配列番号:22);
(6)軽鎖のVL3-43-EHD2-1(N39Q)(配列番号:23)およびVLhu225-CLκ(配列番号:25)、ならびに重鎖のVHhu225-CH1-VH3-43-EHD2-2-Fc(配列番号:24);
(7)軽鎖のVL3-43-EHD2-1(N39Q)(配列番号:23)およびVLhu225-CLκ(配列番号:25)、重鎖のVHhu225-CH1-VH3-43-EHD2-2(配列番号:44);
(8)軽鎖のVLhu36-CLκ(配列番号:45)および重鎖のVHhu36-CH1-Fc(hole)(配列番号:46)を含む第1の分子であって、軽鎖のVH2C11-EHD2-1(N39Q)(配列番号:47)および重鎖のVL2C11-EHD2-2-Fc(knob)(配列番号:48)を有するCD3-標的アームを有する分子、および軽鎖のVL2C11-EHD2-1(N39Q)(配列番号:49)および重鎖のVH2C11-EHD2-2-Fc(knob)(配列番号:50)を含む第2の分子;
(9)軽鎖のVLS309-CLκ(配列番号:51)およびVLP2B-2F6-EHD2-1(N39Q)(配列番号:52)、ならびに重鎖のVHS309-CH1-VHP2B-2F6-EHD2-2-Fc(配列番号:53)、を含む。
(i)配列番号:13、14、15および16;
(ii)配列番号:13、15、16および20;
(iii)配列番号:13、15、39および40;
(iv)配列番号:13、14、15および41;
(v)配列番号:23、24および25、を含む。
第1の結合ドメイン(BD1)および第1の修飾EHD2ドメイン(EHD2-1)を含む第1のポリペプチド鎖、および
第2の結合ドメイン(BD2)および第2の修飾EHD2ドメイン(EHD2-2)を含む第2のポリペプチド鎖、を含む結合分子であって
EHD2-1およびEHD2-2のアミノ酸配列は、互いに異なっており、そしてそれぞれは、(i)配列番号:1に対して少なくとも70%のアミノ酸同一性を有し、かつ14位にCysを有しないアミノ酸配列、または(ii)配列番号:1に対して少なくとも70%のアミノ酸同一性を有し、かつ102位にCysを有しないアミノ酸配列、から選択され、
BD1およびBD2は一緒になって抗原結合部位を形成し、ここで、EHD2-1およびEHD2-2は互いに共有結合している、結合分子。
修飾EHD2ドメインの一方または両方が、N39位に単一アミノ酸置換をさらに含む、項目1に記載の結合分子。
BD1およびBD2が、互いに異なっており、そしてそれぞれは、VHおよびVLから選択されるか、またはTCR α-鎖の可変領域およびTCR β-鎖の可変領域から選択される、項目1~2のいずれか一項に記載の結合分子。
第1のFc鎖をさらに含む、項目1~3のいずれか一項に記載の結合分子。
第3の結合ドメイン(BD3)および第4の結合ドメイン(BD4)をさらに含み、ここで、BD3およびBD4は一緒になって抗原結合部位を形成する、請求項1~4のいずれか一項に記載の結合分子。
BD3およびBD4が、互いに異なっており、そしてそれぞれは、VHおよびVLから選択されるか、またはTCR α-鎖の可変領域およびTCR β-鎖の可変領域から選択される、項目5に記載の結合分子。
第3のポリペプチド鎖をさらに含み、好ましくは第3のポリペプチド鎖および第4のポリペプチド鎖をさらに含む、項目5または6に記載の結合分子。
第2のFc鎖をさらに含む、項目5~7のいずれか一項に記載の結合分子。
第1のFc鎖および第2のFc鎖が、互いに異なっており、そしてヘテロ二量体のFcを形成する、項目8に記載の結合分子。
単一特異性であるかまたは二重特異性である、項目5~9のいずれか一項に記載の結合分子。
BD3を含む第3のポリペプチド鎖が、
(i)CH1ドメイン、
(ii)CLドメイン、
(iii)第1の修飾EHD2ドメイン(EHD2-1)、および
(iv)第2の修飾EHD2ドメイン(EHD2-2)、の1つをさらに含み、
BD4を含む第4のポリペプチド鎖が、
(i)の場合にはCLドメイン、
(ii)の場合にはCH1ドメイン、
(iii)の場合には第2の修飾EHD2ドメイン(EHD2-2)、および
(iv)の場合には第1の修飾EHD2ドメイン(EHD2-1)、をさらに含み、
ここで、EHD2-1およびEHD2-2のアミノ酸配列は、互いに異なっており、そしてそれぞれは、配列番号:1に対して少なくとも70%のアミノ酸同一性を有し、かつ14位にCysを有しないアミノ酸配列、または配列番号:1に対して少なくとも70%のアミノ酸同一性を有し、かつ102位にCysを有しないアミノ酸配列、から選択される、項目5~10のいずれか一項に記載の結合分子。
第3のポリペプチド鎖または第4のポリペプチド鎖の修飾EHD2ドメインの一方または両方が、N39位に単一アミノ酸置換をさらに含む、項目11に記載の結合分子。
第5の結合ドメイン(BD5)および第6の結合ドメイン(BD6)をさらに含み、ここで、BD5およびBD6は一緒になって抗原結合部位を形成する、項目5~12のいずれか一項に記載の結合分子。
BD5に結合する、
(i)CH1ドメイン、
(ii)CLドメイン、
(iii)第1の修飾EHD2ドメイン(EHD2-1)、または
(iv)第2の修飾EHD2ドメイン(EHD2-2)、および
BD6に結合する、
(i)の場合にはCLドメイン、
(ii)の場合にはCH1ドメイン、
(iii)の場合には第2の修飾EHD2ドメイン(EHD2-2)、そして
(iv)の場合には第1の修飾EHD2ドメイン(EHD2-1)、
をさらに含み、ここで、EHD2-1およびEHD2-2のアミノ酸配列は、互いに異なっており、そしてそれぞれは、配列番号:1に対して少なくとも70%のアミノ酸同一性を有し、かつ14位にCysを有しないアミノ酸配列、または配列番号:1に対して少なくとも70%のアミノ酸同一性を有し、かつ102位にCysを有しないアミノ酸配列、から選択される、項目13に記載の結合分子。
BD5またはBD6に結合する修飾EHD2ドメインの一方または両方が、N39位に単一アミノ酸置換をさらに含む、項目14に記載の結合分子。
BD5およびBD6が、互いに異なっており、そしてそれぞれは、VHおよびVLから選択されるか、またはTCR α-鎖の可変領域およびTCR β-鎖の可変領域から選択される、項目14または15に記載の結合分子。
BD5またはBD6に結合するCH1ドメイン、CLドメイン、EHD2-1またはEHD2-2が、リンカーを介してBD1、BD2、BD3またはBD4の1つに結合する、項目14~16のいずれか一項に記載の結合分子。
単一特異性、二重特異性、または三重特異性である、項目11~17のいずれか一項に記載の結合分子。
第7の結合ドメイン(BD7)および第8の結合ドメイン(BD8)をさらに含み、ここで、BD7およびBD8は一緒になって抗原結合部位を形成する、項目11~18のいずれか一項に記載の結合分子。
BD7に結合する、
(i)CH1ドメイン、
(ii)CLドメイン、
(iii)第1の修飾EHD2ドメイン(EHD2-1)、または
(iv)第2の修飾EHD2ドメイン(EHD2-2)、
および
BD8に結合する、
(i)の場合にはCLドメイン、
(ii)の場合にはCH1ドメイン、
(iii)の場合には第2の修飾EHD2ドメイン(EHD2-2)、そして
(iv)の場合には第1の修飾EHD2ドメイン(EHD2-1)、
をさらに含み、ここで、EHD2-1およびEHD2-2のアミノ酸配列は、互いに異なっており、そしてそれぞれは、配列番号:1に対して少なくとも70%のアミノ酸同一性を有し、かつ14位にCysを有しないアミノ酸配列、または配列番号:1に対して少なくとも70%のアミノ酸同一性を有し、かつ102位にCysを有しない102アミノ酸配列、から選択される、項目19に記載の結合分子。
BD7またはBD8に結合する修飾EHD2ドメインの一方または両方が、N39位に単一アミノ酸置換をさらに含む、項目20に記載の結合分子。
BD7およびBD8が、互いに異なっており、そしてそれぞれは、VHおよびVLから選択されるか、またはTCR α-鎖の可変領域およびTCR β-鎖の可変領域から選択される、項目21に記載の結合分子。
BD7またはBD8に結合するCH1ドメイン、CLドメイン、EHD2-1またはEHD2-2が、リンカーを介してBD5またはBD6に結合していないBD1、BD2、BD3またはBD4の1つに結合する、項目20~22のいずれか一項に記載の結合分子。
単一特異性、二重特異性、三重特異性または四重特異性である、項目19~23のいずれか一項に記載の結合分子。
修飾EHD2ドメインのいずれも1つのN-グリカンを担持しないか、1つまたはそれ以上の修飾EHD2ドメインが1つのN-グリカンを担持する、項目1~24のいずれか一項の記載の結合分子。
配列番号:1の14位のCysが、Ser、Gly、Ala、Thr、Gln、Asn、およびTyrからなる群から選択されるアミノ酸、好ましくはSerによって置換されている、項目1~25のいずれか一項に記載の結合分子。
配列番号:1の102位のCysが、Ser、Gly、Ala、Thr、Gln、Asn、およびTyrからなる群から選択されるアミノ酸、好ましくはSerによって置換されている、項目1~26のいずれか一項に記載の結合分子。
N39位における単一アミノ酸置換が、N39Qである、項目1~27のいずれか一項に記載の結合分子。
項目1~28のいずれか一項に記載の結合分子をコードする核酸または核酸のセット。
項目29の核酸または核酸のセットを含むベクター。
項目30に記載のベクターを含む宿主細胞。
項目1~28のいずれか一項に記載の結合分子、項目29に記載の核酸もしくは核酸のセット、項目30に記載のベクター、または項目31に記載の宿主細胞、および薬学的に許容される担体、を含む医薬組成物。
配列番号:13、配列番号:14、配列番号:15および配列番号:16を含む結合分子。
配列番号:13、配列番号:15、配列番号:16および配列番号:20を含む結合分子。
配列番号:13、配列番号:15、配列番号:39および配列番号:40を含む結合分子。
配列番号:13、配列番号:14、配列番号:15および配列番号:41を含む結合分子。
配列番号:23、配列番号:24および配列番号:25を含む結合分子。
項目33~37のいずれか一項に記載の結合分子をコードする核酸または核酸のセット。
項目38の核酸または核酸のセットを含むベクター。
項目39に記載のベクターを含む宿主細胞。
項目33~37のいずれか一項に記載の結合分子、項目38に記載の核酸もしくは核酸のセット、項目39に記載のベクター、または項目40に記載の宿主細胞、および薬学的に許容される担体を含む医薬組成物。
医薬に使用するための、好ましくは癌の処置に使用するための、項目33~37のいずれか一項に記載の結合分子、項目38に記載の核酸もしくは核酸のセット、項目39に記載のベクター、項目40に記載の宿主細胞、または項目41に記載の医薬組成物。
処置を必要とする患者に、治療有効量の項目33~37のいずれか一項に記載の結合分子、項目38に記載の核酸もしくは核酸のセット、項目39に記載のベクター、項目40に記載の宿主細胞、または項目41に記載の医薬組成物を投与することを含む処置方法。
癌を処置する方法であって、それを必要とする患者に、治療有効量の項目33~37のいずれか一項に記載の結合分子、項目38に記載の核酸または核酸のセット、項目39に記載のベクター、項目40に記載の宿主細胞、または項目41に記載の医薬組成物を投与することを含む方法。
医薬に使用するための、好ましくは癌の処置に使用するための、項目1~28のいずれか一項に記載の結合分子、項目29に記載の核酸もしくは核酸のセット、項目30に記載のベクター、項目31に記載の宿主細胞、または項目32に記載の医薬組成物。
処置を必要とする患者に、治療有効量の項目1~28のいずれか一項に記載の結合分子、項目29に記載の核酸もしくは核酸のセット、項目30に記載のベクター、項目31に記載の宿主細胞、または項目32に記載の医薬組成物を投与することを含む処置方法。
癌を処置する方法であって、それを必要とする患者に、治療有効量の項目1~28のいずれか一項に記載の結合分子、項目30に記載の核酸もしくは核酸のセット、項目30に記載のベクター、項目31に記載の宿主細胞、または項目32に記載の医薬組成物を投与することを含む方法。
二重特異性2価eIgG分子は、HER3(3-43)に特異的なFvドメイン(Schmitt et al., 2017, mAbs 9, 831-843)をIgG1のCH1/CLヘテロ二量体と組み合わせ、MET(5D5)に特異的なFvドメイン(Jin et al., 2008, Cancer Res. 68, 4360-4368)をIgEの修飾CH2ドメイン(hetEHD2)と組み合わせ、そしてヘテロ二量体のFc部分(knob-into-hole技術)とすることによって作製した。このように、二重特異性分子は、4つの異なるポリペプチド鎖からなる。さまざまな抗体の定常部分は、軽鎖のVL3-43-CLλ(配列番号:13)および重鎖のVH3-43-CH1-Fcknob(配列番号:14)からなる。第2の部分は、eIgG1という結果になるHC1-LC2(重鎖:VH5D5-EHD2-1(N39Q)-Fchole(配列番号:12);軽鎖:VL5D5-EHD2-2(配列番号:11))、またはeIgG2という結果になるHC2-LC1(重鎖:VH5D5-EHD2-2-Fchole(配列番号:10);軽鎖:VL5D5-EHD2-1(N39Q)(配列番号:9))のどちらか一方のEHD2配置からなる。二重特異性2価eIgG分子は、HER3に対する抗原結合部位1つおよびMETに対する結合部位1つを示す。それぞれのポリペプチド鎖は、図5Aに例示的かつ概略的に示し、得られた結合分子は、図5Bに概略的に示す。
二重特異性2価eIgG分子は、HER3(3-43)に特異的なFvドメイン(Schmitt et al., 2017, mAbs 9, 831-843)をIgG1のCH1/CLヘテロ二量体と組み合わせ、CD3(huU3)に特異的なFvドメインをIgEの修飾CH2ドメイン(hetEHD2)と組み合わせ、そしてヘテロ二量体のFc部分(knob-into-hole技術)を組み合わせることによって作製した。CD3結合部位は、抗CD3 mAb UCHT1のヒト化バージョンからなる。このように、二重特異性分子は、4つの異なるポリペプチド鎖からなる。さまざまな抗体の第1の部分は、軽鎖のVL3-43-CLλ(配列番号:13)および重鎖のVH3-43-CH1-Fcknob(配列番号:14)からなる。第2の部分は、eIgGという結果になるHC2-LC1(重鎖:VHhuU3-EHD2-2-Fchole(配列番号:16);軽鎖:VLhuU3-EHD2-1(N39Q)(配列番号:15))のEHD2配置からなる。二重特異性2価eIgG分子は、HER3対する抗原結合部位1つおよびCD3に対する結合部位1つを示す。それぞれのポリペプチド鎖は、図6Aに例示的かつ概略的に示し、得られた結合分子は、図6Bに概略的に示す。
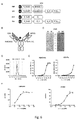
鎖A上の位置C14および鎖B上の位置C102をさまざまな残基(A、T、N、S、W)で置換し、機能的なヘテロ二量体のeFab分子(hetE-Fab)の形成に対するそれらの影響を評価した。モデルとして、2つのhetEHD2ドメインに融合させた、IgG3-43(抗HER3標的)の可変ドメインからなるhetE-Fabを使用した(図1A)。分子は、Q5(登録商標)部位特異的変異誘発キット(NEB)を用いて部位特異的変異誘発により生成させた。さまざまな残基の正しい置換を確認した後、HEK293-6E細胞に2つのプラスミドの異なる組み合わせをコトランスフェクトし(図7Aおよび表1)、すべての分子がVH-hetEHD2鎖上にHisタグを含んでいるので、Ni-NTA樹脂を用いて親和性クロマトグラフィーにより細胞培養上清からタンパク質を精製した。分子の濃度は、NanoDrop ND-1000を用いて280nMで測光法で決定し、収量は使用した上清の容量に対して計算した。
EHD2ヘテロ二量体の形成のための新規設計に基づき、両鎖上のセリン置換(鎖A:C14S;鎖B:C102S)を用いて、hetEHD2ドメインのN-グリコシル化の変化が発現および機能的ヘテロ二量体の形成に及ぼす影響を研究した。当然ながら、EHD2ドメインは位置N39にN-グリカンを担持する。HER3を標的とするeFabを用い、両方のEHD2ドメインにN-グリカンを有するeFab(eFab1)(C14S、N39(配列番号:37):N39、C102S(配列番号:31))、グリコシル化EHD2部位を1つのみ有する2つのeFab(eFab2: C14S、N39Q(配列番号: 36):N39、C102S(配列番号:31);eFab3:C14S、N39(配列番号:37):N39Q、C102S(配列番号:38))、およびEHD2にいかなるN-グリコシル化もない1つの分子(eFab4)(C14S、N39Q(配列番号:36):N39Q、C102S(配列番号:38))を作製した。得られた分子は図9Aに概略的に示す。VH-hetEHD2鎖は、精製および検出のためにHis-タグをさらに含んでいた。1価eFab分子を、ポリエチレンイミンをトランスフェクション試薬として用い、VH-hetEHD2-2鎖およびVL-hetEHD2-1鎖をコードする2つのプラスミドの一過性コトランスフェクション後にHEK293-6E細胞内で発現させた。細胞培養上清に分泌されたタンパク質はNi-NTA親和性クロマトグラフィーを用いて精製した。SDS-PAGE分析における非還元条件下で、2つの異なるポリペプチド鎖からなるインタクトなeFab分子に該当する約50kDaの1つの主要なバンドが観察された(図9B)。
二重特異性2価eIg-Fab分子の作製、すなわちFab断片のeIg分子への融合のために、i)抗体3-43(抗HER3;Schmitt et al, 2017, mAbs, 9:831-843)に由来するFabドメイン2つ、すなわちIgG1のCH1/CLヘテロ二量体に融合される、HER3に特異的なFvドメイン、ii)IgEの修飾CH2ドメイン(hetEHD2)に融合される、CD3に特異的なFabドメイン1つ、iii)ヘテロ二量体のFc部分(knob-into-hole技術)、のさまざまな組み合わせを使用した(図4)。CD3結合部位は、抗CD3 mAb UCHT1のヒト化バージョンに由来するものであった。二重特異性3価eIg-Fab分子は、HER3結合部位およびCD3結合部位の配置が異なる4つの異なるポリペプチド鎖からなる(詳細は、図4を参照)。このように、二重特異性3価eIg-Fab分子は、HER3に対する2つの抗原結合部位およびCD3に対する1つの結合部位を示す。HER3に対する1つの結合部位、CD3に対する1つの結合部位を有する二重特異性2価eIg分子(eIg1)の分子構造は、実施例2に記載する。軽鎖および重鎖の配列は、表2に記載する。
治療用抗体からの異なる可変ドメインに基づき、i)HER3に特異的なFvドメイン(抗体3-43;Schmitt et al, 2017, mAbs 9, 831-843)をIgG1のCH1/CLヘテロ二量体と組み合わせ、ii)線維芽細胞活性化タンパク質(FAP; hu36; Fabre et al., 2020, Clin. Cancer Res. 26, 3420-3430)に特異的なFvドメインをIgEの修飾CH2ドメイン(hetEHD2)と組み合わせ、iii)ヘテロダイマーのFc部分に融合させることにより(knob-into-hole技術)、二重特異性かつ2価eIg分子を作製した。このように、二重特異性分子は、4つの異なるポリペプチド鎖からなる:軽鎖のVL3-43-CLλ(配列番号:13)は重鎖のVH3-43-CH1-Fcknob(配列番号:14)と対合し、軽鎖のVLhu36-EHD2-1(N39Q)(配列番号:43))は重鎖のVHhu36-EHD2-2-Fchole(配列番号:42)と対合する。二重特異性2価eIg分子は、HER3に対する1つの抗原結合部位およびFAPに対する1つの結合部位を示す。それぞれのポリペプチド鎖は図13Aに例示的に示し、得られた抗体分子は図13Bに概略的に示す。
抗HER3 2価eIg分子は、抗HER3抗体(3-43)(Schmitt et al., 2017, mAbs 9, 831-843)の可変ドメインをIgEの修飾CH2ドメイン(hetEHD2)と組み合わせ、さらにホモ二量体化Fc領域に融合させることによって作製した。このように、この分子は、2つの異なるポリペプチド鎖からなる:軽鎖のVL3-43-EHD2-1(配列番号:23)および重鎖のVH3-43-EHD2-2-Fc(配列番号:22)。単一特異性2価eIg分子は、HER3に対して2つの同一の抗原-結合部位を示す。それぞれのポリペプチド鎖は図14Aに例示的に示し、得られた抗体分子は図14Bに概略的に示す。
二重特異性4価eIg-Fab分子は、抗EGFR抗体(hu225; Seifert et al., 2014, Mol Cancer Ther 13, 101-111)の可変ドメインとIgG1のCH1/CLヘテロ二量体、および抗HER3(3-43; Schmitt et al., 2017, mAbs 9, 831-843)の可変ドメインとIgEの修飾CH2ドメイン(hetEHD2)を組み合わせて、さらに、ホモ二量体化Fc部分と組み合わせることによって作製した。このように、4価の二重特異性分子は、3つの異なるポリペプチド鎖からなる:軽鎖のVL3-43-EHD2-1(配列番号:23)およびVLhu225-CLκ(配列番号:25)、ならびに重鎖のVHhu225-CH1-VH3-43-EHD2-2-Fc(配列番号:24)。重鎖における2つのFab部分は、10個のアミノ酸を含むリンカー(GGSGG)2により分離させた。この二重特異性4価eIg分子は、EGFRに対する2つの抗原結合部位とHER3に対する2つの結合部位を示している。それぞれのポリペプチド鎖は図15Aに例示的に示し、得られた結合分子は図15Bに概略的に示す。
抗EGFR(hu225; Seifert et al., 2014, Mol Cancer Ther 13, 101-111)の可変ドメインとIgG1のCH1/CLヘテロ二量体、抗HER3(3-43; Schmitt et al., 2017, mAbs 9, 831-843)の可変ドメインとIgEの修飾CH2ドメイン(hetEHD2)を組み合わせることによって二重特異性2価Fab-eFab分子、すなわちFc領域のないものを作製した。Fab-eFab分子は、軽鎖のVL3-43-EHD2-1(配列番号:23)およびVLhu225-CLκ(配列番号:25)、ならびに「重鎖」のVHhu225-CH1-VH3-43-EHD2-2(配列番号:44)からなる。この二重特異性2価Fab-eFab分子は、EGFRに対する1つの抗原結合部位およびER3に対する1つの結合部位を示した。重鎖は、分子の精製および検出のために、C-末端にHisタグを含んでいた。2つのFab/eFab部分は、10個のアミノ酸を含むリンカー(GGSGG)2を介して結合していた。それぞれのポリペプチド鎖は図16Aに例示的に示し、得られた抗体分子は図16Bに概略的に示す。Fab-eFab分子の純度、完全性および均質性は、サイズ排除クロマトグラフィーにより確認した(図16C)。
二重特異性2価eIg分子は、抗線維芽細胞活性化タンパク質(FAP)抗体(hu36; Fabre et al., 2020, Clin Cancer Res. 26, 3420-3430)をIgG1のCH1/CLヘテロ二量体と組み合わせ、抗マウスCD3(2C11; Leo et al., 1987, Proc Natl Acad USA 84, 1374-1378)をIgEの修飾CH2ドメイン(hetEHD2)と組み合わせ、さらにヘテロ二量化Fc部分(knob-into-hole技術)に融合させることにより作製した。ポリペプチド鎖の組成は、図17Aに示す。このように、eIg分子の第1の部分は、軽鎖のVLhu36-CLκ(配列番号:45)および重鎖のVHhu36-CH1-Fc(hole)(配列番号:46)を有するFAP-標的化アームからなる。分子Iは追加的に、軽鎖のVH2C11-EHD2-1(配列番号:47)および重鎖のVL2C11-EHD2-2-Fc(knob)(配列番号:48)を有するマウスCD3標的化アームからなる。第2の分子は、軽鎖のVL2C11-EHD2-1(配列番号:49)および重鎖のVH2C11-EHD2-2-Fc(knob)(配列番号:50)からなる。得られた抗体分子は、図17Bに概略的に示す。両方のeIg分子の純度、完全性および均質性は、サイズ排除クロマトグラフィーにより確認した(図17C)。
eIg技術において、ヒトIgEに由来する修飾CH2ドメインがヘテロ二量体化モジュールとして使用されている。そこで、hetEHD2を含む抗体分子が、高親和性IgE受容体FcεRIへの結合を欠くかどうかを調べた。FcεRIは、FcεRIの細胞外領域を含むFc融合タンパク質として作製した。ELISA実験(図18)において、精製したFcεRIを、HER3およびCD3に特異的なeIg(実施例5)、EGFRおよびHER3に特異的な4価の二重特異性eIg-Fab(実施例10)、およびEGFRおよびHER3に特異的な2価の二重特異性Fab-eFab(実施例9)を含むさまざまなeIg誘導体でインキュベートした固定化抗原として使用した。対照として、EGFRおよびHER3を追加の固定化抗原として使用し、抗体のこれらの受容体への結合を確認した。FcεRI、EGFRおよびHER3を、PBSで希釈した2μg/mlの濃度でポリスチレン製マイクロタイタープレート上にコーティングした。残りの結合部位は、PBS、2%脱脂乳(MPBS)でブロックした。次に、プレートを、50nM eIg、またはeIg-Fab、およびFab-eFab分子でインキュベートして、異なる固定化受容体への結合を研究した。さらに、Fcε受容体への結合を確認するために、ヒトIgEをこの実験に含めた。洗浄後、結合した抗体は抗ヒトFab抗体で検出した。TMBおよびH2O2を基質として使用した。IgEはFcεRIに特異的に結合した。3つのeIg誘導体はFcεRIへの結合を示さなかったが、それぞれの標的抗原を強く認識し、すなわち、eIg HER3xCD3はHER3に結合し、eIg-Fab EGFRxHER3およびFab-eFab EGFRxHER3はEGFRおよびHER3に結合した。HER3結合部位の由来である対照抗体IgG 3-43はHER3に結合し、EGFR結合部位の由来であるIgG hu225はEGFRに結合した。これら2つの対照IgG抗体では、FcεRIへの結合は見られなかった(図18)。このように、この実験では、eIg分子が、肥満細胞および好塩基球によって発現されるIgE受容体FcεRIへの結合を欠いていることを実証している。したがって、EHD2またはhetEHD2を含む分子が、FcεRIに結合することによってこれらの免疫細胞の活性化をもたらすことを除外することができる。
SARS-CoV-2ウイルスのスパイクタンパク質の異なるエピトープを二重標的化するために、二重特異性eIg-Fab分子を作製した。このアプローチでは、ウイルスのスパイクタンパク質のRBDドメインに結合する、公開されている抗体を使用した:P2B-2F6(Ju et al., 2020, Nature 584, 115-119)およびS309(Pinto et al., 2020, Nature 583, 290-295)。S309の可変ドメインをIgG1のCH1/CLヘテロ二量体と組み合わせ、P2B-2F6の可変ドメインをhetEHD2ドメインと組み合わせ、さらにホモ二量体化Fc部と組み合わせて対称型4価の二重特異性eIg-Fab分子を作製した。この抗体は、軽鎖のVLS309-CLκ(配列番号:51)およびVLP2B-2F6-EHD2-1(配列番号:52)、ならびに重鎖のVHS309-CH1-VHP2B-2F6-EHD2-2-Fc(配列番号:53)からなる。それぞれのポリペプチド鎖は図19Aに例示的に示し、得られた抗体分子は図19Bに概略的に示す。
Claims (16)
- 第1の結合ドメイン(BD1)および第1の修飾EHD2ドメイン(EHD2-1)を含む第1のポリペプチド鎖、ならびに
第2の結合ドメイン(BD2)および第2の修飾EHD2ドメイン(EHD2-2)を含む第2のポリペプチド鎖、を含む結合分子であって、
EHD2-1およびEHD2-2のアミノ酸配列は、互いに異なっており、そしてそれぞれは、(i)配列番号:1に対して少なくとも70%のアミノ酸同一性を有し、かつ14位にCysを有しないアミノ酸配列、または(ii)配列番号:1に対して少なくとも70%のアミノ酸同一性を有し、かつ102位にCysを有しないアミノ酸配列、から選択され、
BD1およびBD2は一緒になって抗原結合部位を形成し、EHD2-1およびEHD2-2は互いに共有結合している、結合分子。 - BD1およびBD2が、互いに異なっており、そしてそれぞれは、VHおよびVLから選択されるか、またはTCR α-鎖の可変領域およびTCR β-鎖の可変領域から選択される、請求項1に記載の結合分子。
- 第1のFc鎖をさらに含む、請求項1~2のいずれか一項に記載の結合分子。
- 第3の結合ドメイン(BD3)および第4の結合ドメイン(BD4)をさらに含み、ここで、BD3およびBD4は一緒になって抗原結合部位を形成し、好ましくは、BD3およびBD4は、互いに異なっており、そしてそれぞれは、VHおよびVLから選択されるか、またはTCR α-鎖の可変領域およびTCR β-鎖の可変領域から選択される、請求項1~3のいずれか一項に記載の結合分子。
- 第3のポリペプチド鎖をさらに含み、好ましくは第3のポリペプチド鎖および第4のポリペプチド鎖をさらに含み、より好ましくは第2のFc鎖をさらに含む、請求項4または6に記載の結合分子。
- BD3を含む第3のポリペプチド鎖が、
(i)CH1ドメイン、
(ii)CLドメイン、
(iii)第1の修飾EHD2ドメイン(EHD2-1)、および
(iv)第2の修飾EHD2ドメイン(EHD2-2)、の1つをさらに含み、
BD4を含む第4のポリペプチド鎖が、
(i)の場合にはCLドメイン、
(ii)の場合にはCH1ドメイン、
(iii)の場合には第2の修飾EHD2ドメイン(EHD2-2)、および
(iv)の場合には第1の修飾EHD2ドメイン(EHD2-1)、をさらに含み、
ここで、EHD2-1およびEHD2-2のアミノ酸配列は、互いに異なっており、そしてそれぞれは、配列番号:1に対して少なくとも70%のアミノ酸同一性を有し、かつ14位にCysを有しないアミノ酸配列、または配列番号:1に対して少なくとも70%のアミノ酸同一性を有し、かつ102位にCysを有しないアミノ酸配列、から選択される、請求項5に記載の結合分子。 - 第5の結合ドメイン(BD5)および第6の結合ドメイン(BD6)をさらに含み、ここで、BD5およびBD6は一緒になって抗原結合部位を形成し、好ましくは、BD5およびBD6は、互いに異なっており、そしてそれぞれは、VHおよびVLから選択されるか、またはTCR α-鎖の可変領域およびTCR β-鎖の可変領域から選択される、請求項4~6のいずれか一項に記載の結合分子、より好ましくは、
BD5に結合する、
(i)CH1ドメイン、
(ii)CLドメイン、
(iii)第1の修飾EHD2ドメイン(EHD2-1)、または
(iv)第2の修飾EHD2ドメイン(EHD2-2)、
および
BD6に結合する、
(i)の場合にはCLドメイン、
(ii)の場合にはCH1ドメイン、
(iii)の場合には第2の修飾EHD2ドメイン(EHD2-2)、そして、
(iv)の場合には第1の修飾EHD2ドメイン(EHD2-1)、
をさらに含み、
ここで、EHD2-1およびEHD2-2のアミノ酸配列は、互いに異なっており、そしてそれぞれは、配列番号:1に対して少なくとも70%のアミノ酸同一性を有し、かつ14位にCysを有しないアミノ酸配列、または配列番号:1に対して少なくとも70%のアミノ酸同一性を有し、かつ102位にCysを有しないアミノ酸配列、から選択される、請求項4~6のいずれか一項に記載の結合分子。 - 第7の結合ドメイン(BD7)および第8の結合ドメイン(BD8)をさらに含み、ここで、BD7およびBD8は一緒になって抗原結合部位を形成し、好ましくは、BD7およびBD8は、互いに異なっており、そしてそれぞれは、VHおよびVLから選択されるか、またはTCR α-鎖可変領域およびTCR β-鎖の可変領域から選択される、請求項6~7のいずれか一項に記載の結合分子。
- BD7に結合する、
(i)CH1ドメイン、
(ii)CLドメイン、
(iii)第1の修飾EHD2ドメイン(EHD2-1)、または
(iv)第2の修飾EHD2ドメイン(EHD2-2)、
および
BD8に結合する、
(i)の場合にはCLドメイン、
(ii)の場合にはCH1ドメイン、
(iii)の場合には第2の修飾EHD2ドメイン(EHD2-2)、そして、
(iv)の場合には第1の修飾EHD2ドメイン(EHD2-1)、
をさらに含み、
ここで、EHD2-1およびEHD2-2のアミノ酸配列は、互いに異なっており、そしてそれぞれは、配列番号:1に対して少なくとも70%のアミノ酸同一性を有し、かつ14位にCysを有しないアミノ酸配列、または配列番号:1に対して少なくとも70%のアミノ酸同一性を有し、かつ102位にCysを有しないアミノ酸配列、から選択される、請求項8に記載の結合分子。 - 修飾EHD2ドメインのいずれも1つのN-グリカンを担持しないか、または1つまたはそれ以上の修飾EHD2ドメインが1つのN-グリカンを担持する、請求項1~9のいずれか一項に記載の結合分子。
- 配列番号:1の14位のCysが、Ser、Gly、Ala、Thr、Gln、Asn、およびTyrからなる群から選択されるアミノ酸、好ましくはSerによって置換されており、および/または
配列番号:1の102位のCysが、Ser、Gly、Ala、Thr、Gln、Asn、およびTyrからなる群から選択されるアミノ酸、好ましくはSerによって置換されている、請求項1~10のいずれか一項に記載の結合分子。 - 1つまたはそれ以上の修飾EHD2ドメインのN39位に単一アミノ酸置換をさらに含み、好ましくは、単一アミノ酸置換がN39Qである、請求項1~11のいずれか一項に記載の結合分子。
- 請求項1~12のいずれか一項に記載の結合分子をコードする核酸または核酸のセット。
- 請求項13に記載の核酸または核酸のセットを含むベクター。
- 請求項14に記載のベクターを含む宿主細胞。
- 請求項1~12のいずれか一項に記載の結合分子、請求項13に記載の核酸もしくは核酸のセット、請求項14に記載のベクター、または請求項15に記載の宿主細胞、および薬学的に許容される担体、を含む医薬組成物。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2025014991A JP2025081354A (ja) | 2019-09-25 | 2025-01-31 | 修飾ehd2ドメインを含む結合モジュール |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP19199639 | 2019-09-25 | ||
| EP19199639.6 | 2019-09-25 | ||
| PCT/EP2020/077008 WO2021058804A1 (en) | 2019-09-25 | 2020-09-25 | Binding modules comprising modified ehd2 domains |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2025014991A Division JP2025081354A (ja) | 2019-09-25 | 2025-01-31 | 修飾ehd2ドメインを含む結合モジュール |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2022550316A true JP2022550316A (ja) | 2022-12-01 |
| JPWO2021058804A5 JPWO2021058804A5 (ja) | 2023-04-18 |
Family
ID=68109107
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022518946A Pending JP2022550316A (ja) | 2019-09-25 | 2020-09-25 | 修飾ehd2ドメインを含む結合モジュール |
| JP2025014991A Withdrawn JP2025081354A (ja) | 2019-09-25 | 2025-01-31 | 修飾ehd2ドメインを含む結合モジュール |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2025014991A Withdrawn JP2025081354A (ja) | 2019-09-25 | 2025-01-31 | 修飾ehd2ドメインを含む結合モジュール |
Country Status (9)
| Country | Link |
|---|---|
| US (1) | US20220372147A1 (ja) |
| EP (1) | EP4034244A1 (ja) |
| JP (2) | JP2022550316A (ja) |
| KR (1) | KR20220071210A (ja) |
| CN (1) | CN115066275A (ja) |
| AU (1) | AU2020356407A1 (ja) |
| CA (1) | CA3155725A1 (ja) |
| MX (1) | MX2022003507A (ja) |
| WO (1) | WO2021058804A1 (ja) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP4454706A1 (en) | 2023-04-24 | 2024-10-30 | Universität Stuttgart | Novel egfr binding proteins |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2018037092A1 (en) * | 2016-08-26 | 2018-03-01 | Sanofi | Multispecific antibodies facilitating selective light chain pairing |
| JP2019502694A (ja) * | 2015-12-18 | 2019-01-31 | バイオジェン・エムエイ・インコーポレイテッドBiogen MA Inc. | 二特異性抗体基幹 |
Family Cites Families (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5731168A (en) | 1995-03-01 | 1998-03-24 | Genentech, Inc. | Method for making heteromultimeric polypeptides |
| US7829084B2 (en) * | 2001-01-17 | 2010-11-09 | Trubion Pharmaceuticals, Inc. | Binding constructs and methods for use thereof |
| WO2010042904A2 (en) * | 2008-10-10 | 2010-04-15 | Trubion Pharmaceuticals, Inc. | Tcr complex immunotherapeutics |
| HUE029257T2 (en) * | 2009-12-29 | 2017-02-28 | Aptevo Res And Dev Llc | Heterodimer binding proteins and their use |
| JP6400470B2 (ja) * | 2011-05-16 | 2018-10-03 | ジェネロン(シャンハイ)コーポレイション リミテッド | 多重特異性Fab融合タンパク質および使用法 |
| WO2013075027A2 (en) * | 2011-11-17 | 2013-05-23 | Emergent Product Development Seattle, Llc | Anti-sil6xr complex binding domains and methods of use |
| WO2013156054A1 (en) * | 2012-04-16 | 2013-10-24 | Universität Stuttgart | The igm and ige heavy chain domain 2 as covalently linked homodimerization modules for the generation of fusion proteins with dual specificity |
| CA2964973C (en) * | 2014-11-14 | 2020-11-03 | The Procter & Gamble Company | Silicone compounds |
| WO2016146818A1 (en) * | 2015-03-18 | 2016-09-22 | Universität Stuttgart | Single-chain tnf ligand family molecules and fusion proteins and derivatives thereof |
| WO2017011342A1 (en) * | 2015-07-10 | 2017-01-19 | Abbvie Inc. | Igm-or-ige-modified binding proteins and uses thereof |
| US11008402B2 (en) * | 2016-09-15 | 2021-05-18 | Universitat Stuttgart | Antigen binding protein against HER3 |
| EP3768705A1 (en) * | 2018-03-22 | 2021-01-27 | Universität Stuttgart | Multivalent binding molecules |
| WO2021058807A1 (en) * | 2019-09-25 | 2021-04-01 | Universität Stuttgart | Trivalent binding molecules |
| EP4245373A3 (en) * | 2020-02-26 | 2023-12-20 | VIR Biotechnology, Inc. | Antibodies against sars-cov-2 |
| TW202204397A (zh) * | 2020-04-10 | 2022-02-01 | 美商亞得捷歐治療公司 | 對冠狀病毒s蛋白質具特異性之化合物及其用途 |
| US11440952B2 (en) * | 2020-10-16 | 2022-09-13 | Invisishield Technologies Ltd. | Compositions for preventing or treating viral and other microbial infections |
-
2020
- 2020-09-25 JP JP2022518946A patent/JP2022550316A/ja active Pending
- 2020-09-25 US US17/762,463 patent/US20220372147A1/en active Pending
- 2020-09-25 AU AU2020356407A patent/AU2020356407A1/en active Pending
- 2020-09-25 CN CN202080082634.XA patent/CN115066275A/zh active Pending
- 2020-09-25 KR KR1020227012195A patent/KR20220071210A/ko active Pending
- 2020-09-25 EP EP20785700.4A patent/EP4034244A1/en active Pending
- 2020-09-25 WO PCT/EP2020/077008 patent/WO2021058804A1/en not_active Ceased
- 2020-09-25 MX MX2022003507A patent/MX2022003507A/es unknown
- 2020-09-25 CA CA3155725A patent/CA3155725A1/en active Pending
-
2025
- 2025-01-31 JP JP2025014991A patent/JP2025081354A/ja not_active Withdrawn
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2019502694A (ja) * | 2015-12-18 | 2019-01-31 | バイオジェン・エムエイ・インコーポレイテッドBiogen MA Inc. | 二特異性抗体基幹 |
| WO2018037092A1 (en) * | 2016-08-26 | 2018-03-01 | Sanofi | Multispecific antibodies facilitating selective light chain pairing |
Non-Patent Citations (3)
| Title |
|---|
| BENNICH, H. H. ET AL.: "RecName: Full=Immunoglobulin heavy constant epsilon; AltName: Full=Ig epsilon chain C region; AltNam", UNIPROTKB, JPN6024010679, 18 September 2019 (2019-09-18), ISSN: 0005587080 * |
| OLIVER SEIFERT ET AL.: ""Diabody-Ig: a novel platform for the generation of multivalent and multispecific antibody molecule", MABS, vol. 11, no. 5, JPN6024010681, 3 May 2019 (2019-05-03), pages 919 - 929, ISSN: 0005587078 * |
| OLIVER SEIFERT ET AL.: ""Tetravalent Antibody-scTRAIL Fusion Proteins with Improved Properties"", MOLECULAR CANCER THERAPEUTICS, vol. 13, no. 1, JPN6024010680, 1 January 2014 (2014-01-01), pages 101 - 111, ISSN: 0005587079 * |
Also Published As
| Publication number | Publication date |
|---|---|
| MX2022003507A (es) | 2022-04-25 |
| WO2021058804A1 (en) | 2021-04-01 |
| CN115066275A (zh) | 2022-09-16 |
| KR20220071210A (ko) | 2022-05-31 |
| AU2020356407A1 (en) | 2022-04-07 |
| US20220372147A1 (en) | 2022-11-24 |
| CA3155725A1 (en) | 2021-04-01 |
| EP4034244A1 (en) | 2022-08-03 |
| JP2025081354A (ja) | 2025-05-27 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7599427B2 (ja) | 多量体 | |
| US12522663B2 (en) | Multivalent binding molecules | |
| JP2025029067A (ja) | 多量体、四量体および八量体 | |
| JP7483896B2 (ja) | オフターゲット毒性を低下させるプロ抗体 | |
| US12331109B2 (en) | Antigen binding molecule formats | |
| EP4090686A2 (en) | Pro-antibody that reduces off-target toxicity | |
| JP2025081354A (ja) | 修飾ehd2ドメインを含む結合モジュール | |
| JP6919100B2 (ja) | 新規多重特異的結合タンパク質 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230407 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20230407 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20240318 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240319 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240618 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20241001 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20250131 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20250131 |