JP2022135147A - Tablets containing saxagliptin - Google Patents
Tablets containing saxagliptin Download PDFInfo
- Publication number
- JP2022135147A JP2022135147A JP2021034765A JP2021034765A JP2022135147A JP 2022135147 A JP2022135147 A JP 2022135147A JP 2021034765 A JP2021034765 A JP 2021034765A JP 2021034765 A JP2021034765 A JP 2021034765A JP 2022135147 A JP2022135147 A JP 2022135147A
- Authority
- JP
- Japan
- Prior art keywords
- film
- saxagliptin
- tablet
- manufactured
- uncoated
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Landscapes
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicinal Preparation (AREA)
Abstract
Description
本発明は、サキサグリプチンを含有する錠剤に関する。 The present invention relates to tablets containing saxagliptin.
サキサグリプチンは、GLP-1を分解するDPP-4活性を阻害することにより活性型GLP-1の血中濃度を上昇させ、インスリン分泌促進作用を介して血糖低下作用を発揮する2型糖尿病治療剤である。 Saxagliptin is a therapeutic agent for type 2 diabetes that inhibits the activity of DPP-4, which degrades GLP-1, thereby increasing the blood concentration of active GLP-1 and exerting a hypoglycemic effect through an insulin secretagogue effect. be.
サキサグリプチンは、分子内環化反応によりサイクリックアミジン(主としてシス-サイクリックアミジン)を生成する不安定な化合物であり、当該分子内環化反応は、通常の錠剤化プロセス、例えば湿式造粒法、ローラー圧縮、錠剤化を受けるときに加速されることが知られている(特許文献1)。
この課題を解決するため、特許文献1では、錠剤内部ではなく、インナーシールコーティング層と第2フィルムコーティング層を設け、当該第2フィルムコーティング層中にサキサグリプチンを含有させた錠剤が開示されている。
また、特許文献2には、サキサグリプチンとヒドロキシプロピルセルロースなどのポリマーとを溶媒に溶解し、pHを調整していない状態のpHより高く且つ4.0未満に調整して溶液を調製し、溶液を乾燥させて粉末とすることにより、サキサグリプチンの安定化を図る方法が開示されている。
Saxagliptin is an unstable compound that produces cyclic amidines (mainly cis-cyclic amidines) through an intramolecular cyclization reaction, which is commonly used in tableting processes such as wet granulation, It is known to be accelerated when subjected to roller compaction, tableting (Patent Document 1).
In order to solve this problem, Patent Document 1 discloses a tablet in which an inner seal coating layer and a second film coating layer are provided instead of inside the tablet, and saxagliptin is contained in the second film coating layer.
Further, in Patent Document 2, saxagliptin and a polymer such as hydroxypropylcellulose are dissolved in a solvent, and the pH is adjusted to be higher than the unadjusted pH and less than 4.0 to prepare a solution, and the solution is prepared. A method for stabilizing saxagliptin by drying and powdering is disclosed.
しかしながら、特許文献1記載の第2フィルムコーティング層中にサキサグリプチンを含有させた錠剤は、サキサグリプチンを含有させるフィルムコーティング層以外にインナーシールコーティング層を必要とし、製造工程が複雑になり、製造効率が良好とは言えない。また、特許文献2では、安定なサキサグリプチン含有粉末が得られているが、この粉末を錠剤化した場合の安定性については全く記載されていない。 However, the tablet containing saxagliptin in the second film coating layer described in Patent Document 1 requires an inner seal coating layer in addition to the film coating layer containing saxagliptin, which complicates the manufacturing process and improves manufacturing efficiency. It can not be said. Moreover, although Patent Document 2 provides a stable saxagliptin-containing powder, it does not describe the stability of this powder when it is tableted.
従って、本発明の課題は、製造工程が複雑でなく、サキサグリプチンを安定に維持するサキサグリプチン含有錠剤を提供することにある。 Accordingly, an object of the present invention is to provide a saxagliptin-containing tablet that has a simple manufacturing process and that stably maintains saxagliptin.
そこで本発明者は、種々の製剤添加物を配合した素錠を作成し、アンダーコート層を設けず、サキサグリプチンをフィルムコート層に含有させた錠剤を製造し、その安定性を評価してきたところ、素錠中に結晶セルロースという汎用の賦形剤を含有させると、サキサグリプチンが分解し、素錠中にマンニトール及び/又は乳糖を含有させるとサキサグリプチンは安定に維持されることを見出し、本発明を完成した。 Therefore, the present inventors prepared uncoated tablets containing various formulation additives, produced tablets containing saxagliptin in the film coat layer without providing an undercoat layer, and evaluated the stability thereof. It was found that saxagliptin is degraded when a general-purpose excipient called crystalline cellulose is contained in the uncoated tablet, and saxagliptin is stably maintained when mannitol and/or lactose is contained in the uncoated tablet, thus completing the present invention. did.
すなわち、本発明は、次の発明[1]~[4]を提供するものである。
[1]マンニトール及び/又は乳糖を含有し、結晶セルロースを含まない素錠のフィルムコート錠であって、アンダーコート層を有さず、フィルム部にサキサグリプチンを含有するフィルムコート錠。
[2]素錠中にクロスカルメロース又はその塩を含まない[1]記載のフィルムコート錠。
[3]素錠中に崩壊剤及び滑沢剤を含まない[1]又は[2]記載のフィルムコート錠。
[4]素錠が、湿製素錠である[1]~[3]のいずれかに記載のフィルムコート錠。
That is, the present invention provides the following inventions [1] to [4].
[1] An uncoated film-coated tablet containing mannitol and/or lactose and not containing crystalline cellulose, which does not have an undercoat layer and contains saxagliptin in the film portion.
[2] The film-coated tablet according to [1], which does not contain croscarmellose or a salt thereof in the uncoated tablet.
[3] The film-coated tablet according to [1] or [2], which does not contain a disintegrant and a lubricant in the uncoated tablet.
[4] The film-coated tablet according to any one of [1] to [3], wherein the uncoated tablet is a wet uncoated tablet.
本発明のフィルムコート錠は、フィルムコート層が一層であるにもかかわらずサキサグリプチンが安定に維持されるため、製造工程が複雑にならない。 In the film-coated tablet of the present invention, saxagliptin is stably maintained in spite of having a single film-coated layer, so the production process is not complicated.
本発明のフィルムコート錠は、マンニトール及び/又は乳糖を含有し結晶セルロースを含まない素錠のフィルムコート錠であって、アンダーコート層を有さず、フィルム部にサキサグリプチンを含有することを特徴とする。 The film-coated tablet of the present invention is an uncoated film-coated tablet that contains mannitol and/or lactose and does not contain crystalline cellulose, does not have an undercoat layer, and contains saxagliptin in the film portion. do.
本発明の医薬の有効成分はサキサグリプチンである。サキサグリプチンは、化学名(1S,3S,5S)-2-[(2S)-2-アミノ-2-(3-ヒドロキシトリシクロ[3.3.1.13,7]デシ-1-イル)アセチル]-2-アザビシクロ[3.1.0]ヘキサン-3-カルボニトリルであり、水和物として用いるのが好ましい。
サキサグリプチンは、DPP-4活性を阻害することにより活性型GLP-1の血中濃度を上昇させ、インスリン分泌促進作用を介して血糖低下作用を発揮するので、本発明の医薬は2型糖尿病治療剤として用いられる。
The active ingredient of the pharmaceutical of the present invention is saxagliptin. Saxagliptin has the chemical name (1S,3S,5S)-2-[(2S)-2-amino-2-(3-hydroxytricyclo[3.3.1.13,7]dec-1-yl)acetyl ]-2-Azabicyclo[3.1.0]hexane-3-carbonitrile, preferably used as a hydrate.
Saxagliptin increases the blood level of active GLP-1 by inhibiting DPP-4 activity, and exerts a hypoglycemic effect through an insulin secretagogue effect, so the pharmaceutical of the present invention is a therapeutic agent for type 2 diabetes. used as
本発明のフィルムコート錠は、アンダーコート層を有さず、サキサグリプチンをフィルム部に含有する。
サキサグリプチンを含有させるフィルムコート層を形成するフィルムコーティング剤としては、ヒドロキシプロピルメチルセルロース、ポリビニルアルコール、エチルセルロース、メタクリル酸系ポリマー、ヒドロキシプロピルセルロースなどが挙げられる。このうち、ポリビニルアルコールがより好ましい。
フィルムコート層には、トリアセチン、フタル酸ジエチル、セバシン酸トリブチル、ポリエチレングリコール、クエン酸トリエチルなどの可塑剤、タルク、ヒュームドシリカ、ステアリン酸マグネシウムなどの流動化剤、二酸化チタン、酸化鉄などの着色剤を含有してもよい。
フィルムコート層中のサキサグリプチン含有量は、サキサグリプチンの安定性維持の観点から、3.0~50.0質量%が好ましく、5.0~40.0質量%がより好ましく、10.0~30.0 質量%がさらに好ましい。
また、本発明のフィルムコート錠中のサキサグリプチン含有量は、サキサグリプチンの安定性維持の観点から、0.5~15.0質量%が好ましく、1.0~10.0質量%がより好ましく、1.0~5.0質量%がさらに好ましい。
The film-coated tablet of the present invention does not have an undercoat layer and contains saxagliptin in the film portion.
Examples of film coating agents for forming a film coat layer containing saxagliptin include hydroxypropylmethylcellulose, polyvinyl alcohol, ethylcellulose, methacrylic acid-based polymers, and hydroxypropylcellulose. Among these, polyvinyl alcohol is more preferable.
The film coat layer contains plasticizers such as triacetin, diethyl phthalate, tributyl sebacate, polyethylene glycol and triethyl citrate, fluidizers such as talc, fumed silica and magnesium stearate, and coloring agents such as titanium dioxide and iron oxide. It may contain an agent.
The content of saxagliptin in the film coat layer is preferably 3.0 to 50.0% by mass, more preferably 5.0 to 40.0% by mass, more preferably 10.0 to 30.0% by mass, from the viewpoint of maintaining the stability of saxagliptin. 0% by mass is more preferred.
The content of saxagliptin in the film-coated tablet of the present invention is preferably 0.5 to 15.0% by mass, more preferably 1.0 to 10.0% by mass, from the viewpoint of maintaining the stability of saxagliptin. 0 to 5.0% by mass is more preferable.
サキサグリプチンを含有するフィルムコート層の形成は、例えばサキサグリプチンを含有するpH1~3の水溶液又は含水有機溶媒溶液とフィルムコーティング剤を混合し、得られたコーティング液を用いて素錠の表面をコーティングすることにより行うのが好ましい。ここで、pH調整には、塩酸、水酸化ナトリウムなどが用いられる。また、含水有機溶媒としては含水エタノールが挙げられる。
本発明のフィルムコート錠は、サキサグリプチン含有フィルムコート層以外にアンダーコート層を含有しないから、素錠(湿製錠を含む)の表面に、サキサグリプチン含有フィルムコート層を形成すればよい。
The film coating layer containing saxagliptin is formed by, for example, mixing an aqueous solution of pH 1 to 3 or a water-containing organic solvent solution containing saxagliptin with a film coating agent, and coating the surface of the uncoated tablet with the obtained coating liquid. It is preferable to carry out by Here, hydrochloric acid, sodium hydroxide, or the like is used for pH adjustment. Moreover, water-containing ethanol is mentioned as a water-containing organic solvent.
Since the film-coated tablet of the present invention does not contain an undercoat layer other than the saxagliptin-containing film-coat layer, the saxagliptin-containing film-coat layer may be formed on the surface of the uncoated tablet (including wet tablets).
本発明のフィルムコート錠の素錠は、マンニトール及び/又は乳糖を含有し、汎用の賦形剤である結晶セルロースを含まない。素錠中に結晶セルロースを含有すると、フィルムコート層中のサキサグリプチンの安定性が損なわれる。本発明のフィルムコート錠の素錠には、マンニトール、乳糖、又はマンニトールと乳糖の組み合わせが含まれるが、マンニトールを含む場合がより好ましい。
本発明のフィルムコート錠中のマンニトール及び/又は乳糖の含有量は、フィルムコート層中サキサグリプチンの安定性維持の観点から、20.0~99.5質量%が好ましく、50.0~99.5質量%がより好ましく、70.0~99.5質量%がさらに好ましい。
The uncoated tablet of the film-coated tablet of the present invention contains mannitol and/or lactose and does not contain crystalline cellulose, which is a general-purpose excipient. The inclusion of crystalline cellulose in the uncoated tablet impairs the stability of saxagliptin in the film coat layer. The uncoated tablet of the film-coated tablet of the present invention contains mannitol, lactose, or a combination of mannitol and lactose, and more preferably contains mannitol.
The content of mannitol and/or lactose in the film-coated tablet of the present invention is preferably 20.0 to 99.5 mass%, preferably 50.0 to 99.5, from the viewpoint of maintaining the stability of saxagliptin in the film-coated tablet. % by mass is more preferred, and 70.0 to 99.5% by mass is even more preferred.
素錠中には、マンニトール及び乳糖以外に、結晶セルロース以外の賦形剤、崩壊剤、滑沢剤、結合剤、矯味剤、着色剤、香料等が含まれる。
ここでマンニトール、乳糖及び結晶セルロース以外の賦形剤としては、ソルビトール、キシリトール、エリスリトール、無水リン酸二水素カルシウム、トウモロコシデンプンが挙げられる。
The uncoated tablet contains, in addition to mannitol and lactose, excipients other than crystalline cellulose, disintegrants, lubricants, binders, corrigents, coloring agents, perfumes, and the like.
Excipients other than mannitol, lactose and crystalline cellulose include sorbitol, xylitol, erythritol, anhydrous calcium dihydrogen phosphate and corn starch.
また、崩壊剤としては、クロスカルメロース又はその塩、部分α化でんぷん、クロスポビドン、低置換度ヒドロキシプロピルセルロース、デンプングリコール酸ナトリウム、カルメロース、カルメロースカルシウム等が挙げられる。これらの崩壊剤のうち、クロスカルメロース又はその塩は、サキサグリプチンの安定性維持の観点から含有しないのが好ましい。
素錠中の崩壊剤の含有量は、サキサグリプチンの安定性維持の点から、0~10.0質量%が好ましく、0~7.0質量%がより好ましく、0~5.0質量%がさらに好ましく、含有しないのが好ましい。
Disintegrants include croscarmellose or salts thereof, partially pregelatinized starch, crospovidone, low-substituted hydroxypropyl cellulose, sodium starch glycolate, carmellose, carmellose calcium and the like. Among these disintegrants, croscarmellose or a salt thereof is preferably not contained from the viewpoint of maintaining the stability of saxagliptin.
The content of the disintegrant in the uncoated tablet is preferably 0 to 10.0% by mass, more preferably 0 to 7.0% by mass, more preferably 0 to 5.0% by mass, from the viewpoint of maintaining the stability of saxagliptin. Preferably, it is not contained.
滑沢剤としては、ステアリン酸マグネシウム、ステアリン酸亜鉛、ステアリン酸カルシウム、フマル酸ステアリルナトリウムなどが挙げられ、このうち、ステアリン酸マグネシウム、フマル酸ステアリルナトリウムが好ましい。
素錠中の滑沢剤の含有量は、サキサグリプチンの安定性維持の点から、0~5.0質量%が好ましく、0~3.0質量%がより好ましく、0~1.0質量%がさらに好ましく、含有しないのが好ましい。
Lubricants include magnesium stearate, zinc stearate, calcium stearate, sodium stearyl fumarate and the like, among which magnesium stearate and sodium stearyl fumarate are preferred.
The content of the lubricant in the uncoated tablet is preferably 0 to 5.0% by mass, more preferably 0 to 3.0% by mass, more preferably 0 to 1.0% by mass, from the viewpoint of maintaining the stability of saxagliptin. More preferably, it is preferably not contained.
結合剤としては、ポリビニルアルコール、ポリビニルピロリドン、ヒドロキシプロピルセルロース、ヒドロキシプロピルメチルセルロース、ポリビニルアルコール-ポリエチレングリコールグラフトコポリマー、ポリビニルアルコール-アクリル酸-メタクリル酸メチル共重合体、デンプングリコール酸ナトリウム及びヒドロキシエチルセルロースから選ばれる1種以上が好ましく、ポリビニルアルコール、ポリビニルピロリドン、ヒドロキシプロピルセルロース、ヒドロキシプロピルメチルセルロース及びポリビニルアルコール-ポリエチレングリコールグラフトコポリマーから選ばれる1種以上がより好ましい。
これらの結合剤は、本発明のフィルムコート錠中に0質量%~5質量%含有するのが好ましく、0質量%~3質量%含有するのがより好ましく、0質量%~2質量%含有するのが更に好ましい。
The binder is selected from polyvinyl alcohol, polyvinylpyrrolidone, hydroxypropylcellulose, hydroxypropylmethylcellulose, polyvinyl alcohol-polyethylene glycol graft copolymer, polyvinyl alcohol-acrylic acid-methyl methacrylate copolymer, sodium starch glycolate and hydroxyethylcellulose. One or more is preferred, and one or more selected from polyvinyl alcohol, polyvinylpyrrolidone, hydroxypropylcellulose, hydroxypropylmethylcellulose and polyvinyl alcohol-polyethylene glycol graft copolymer is more preferred.
These binders are preferably contained in the film-coated tablet of the present invention in an amount of 0% to 5% by weight, more preferably 0% to 3% by weight, and 0% to 2% by weight. is more preferred.
本発明においては、素錠は湿製素錠であるのが、サキサグリプチンの安定性維持の点から好ましい。
ここで、湿製錠剤とは、第17改正日本薬局方に薬品を含む湿潤した練合物を一定の型にはめ込んで成形した後、乾燥して製される錠剤と定義されており、通常、有効成分又は有効成分を含む主薬顆粒と賦形剤との混合物に、結合剤を溶解した水又は含水有機溶媒を加えて練合して練合物を得、当該練合物を低圧で圧縮成形し、乾燥して得られる錠剤;あるいは有効成分又は有効成分と結合剤を溶解した水又は含水有機溶媒の溶液に賦形剤を加えて練合して練合物を得、当該練合物を低圧で圧縮成形し、乾燥して得られる錠剤である。ただし、本発明では、湿製素錠中には、有効成分であるサキサグリプチンを含まず、マンニトールを含有し、結晶セルロースを含まない。また、湿製素錠の打錠圧は、50N~350Nが好ましい。
In the present invention, the uncoated tablet is preferably a wet-processed uncoated tablet from the viewpoint of maintaining the stability of saxagliptin.
Here, the wet tablet is defined in the Japanese Pharmacopoeia 17th Edition as a tablet produced by fitting a wet kneaded mixture containing a drug into a certain mold, molding it, and then drying it. An active ingredient or a mixture of active ingredient granules and excipients is added with water in which a binder is dissolved or a water-containing organic solvent is added and kneaded to obtain a kneaded material, and the kneaded material is compression-molded at low pressure. tablets obtained by drying; It is a tablet obtained by compression molding under low pressure and drying. However, in the present invention, the wet uncoated tablet does not contain saxagliptin as an active ingredient, contains mannitol, and does not contain crystalline cellulose. In addition, the tableting pressure of wet uncoated tablets is preferably 50N to 350N.
本発明のフィルムコーティング錠は、例えば、マンニトール及び/又は乳糖を含有し、結晶セルロースを含まない素錠を製造し、次いで素錠の表面にサキサグリプチンを含有するフィルムコーティング層を形成させることにより製造される。
素錠の製造法としては、通常の圧縮打錠法又は前記湿式打錠法が挙げられる。
The film-coated tablet of the present invention is produced, for example, by producing an uncoated tablet containing mannitol and/or lactose and not containing crystalline cellulose, and then forming a film coating layer containing saxagliptin on the surface of the uncoated tablet. be.
Examples of the method for producing the uncoated tablet include the usual compression tableting method and the above wet tableting method.
次に実施例を挙げて、本発明をさらに詳細に説明するが、本発明はこれら実施例に限定されるものではない。 EXAMPLES Next, the present invention will be described in more detail with reference to Examples, but the present invention is not limited to these Examples.
比較例1
乳糖水和物(Super Tab 30GR、DFE pharma製)1485g、結晶セルロース1350g(セオラスUF-711、旭化成製)、クロスカルメロースナトリウム(Ac-Di-Sol、FMC製)150gを袋の中で混合した。次に、打錠末全体に対して0.5%量のステアリン酸マグネシウム(ステアリン酸マグネシウム-S、日油製)を添加して混合後、小型高速起点式打錠機(菊水製作所製VIRGO)で圧縮成形し、200mgプラセボ錠剤を得た。
次に6M 塩酸(富士フィルム和光純薬製)を希釈して調整した0.1N 塩酸 (約600g)にサキサグリプチン水和物(三洋化学研究所製)7.94gを添加して混合させた後、6M 水酸化ナトリウム溶液(キシダ化学製)でpH2に調整する。その後コーティング剤(OPADRY II WHITE、カラコン製)60gを添加し6M塩酸(富士フィルム和光純薬製)でpH2に調整する。錠剤コーティング装置HC-Labo(フロイント産業製)にプラセボ錠剤約300gを投入し、pHを調整した液を添加してフィルムコーティングを行い、フィルム層にサキサグリプチンを含有する錠剤を得た。
Comparative example 1
1485 g of lactose hydrate (Super Tab 30GR, manufactured by DFE Pharma), 1350 g of crystalline cellulose (Seolus UF-711, manufactured by Asahi Kasei), and 150 g of croscarmellose sodium (Ac-Di-Sol, manufactured by FMC) were mixed in a bag. . Next, after adding and mixing 0.5% magnesium stearate (magnesium stearate-S, manufactured by NOF Corporation) with respect to the entire tableting powder, a small high-speed starting tableting machine (VIRGO manufactured by Kikusui Seisakusho) to obtain 200 mg placebo tablets.
Next, 7.94 g of saxagliptin hydrate (manufactured by Sanyo Kagaku Kenkyusho) was added to 0.1N hydrochloric acid (approximately 600 g) prepared by diluting 6 M hydrochloric acid (manufactured by Fujifilm Wako Pure Chemical Industries) and mixed. Adjust to pH 2 with 6M sodium hydroxide solution (manufactured by Kishida Chemical). After that, 60 g of a coating agent (OPADRY II WHITE, manufactured by Colorcon) is added, and the pH is adjusted to 2 with 6M hydrochloric acid (manufactured by Fuji Film Wako Pure Chemical Industries). About 300 g of the placebo tablet was placed in a tablet coating apparatus HC-Labo (manufactured by Freund Corporation), and a pH-adjusted liquid was added to perform film coating to obtain a tablet containing saxagliptin in the film layer.
比較例2
乳糖水和物(Super Tab 30GR、DFE pharma製)1485g、結晶セルロース1350g(セオラスUF-711、旭化成製)、クロスカルメロースナトリウム(Ac-Di-Sol、FMC製)150gを袋の中で混合した。次に、打錠末全体に対して0.5%量の混合物にステアリン酸マグネシウム(ステアリン酸マグネシウム-S、日油製)を添加して混合後、小型高速起点式打錠機(菊水製作所製VIRGO)で圧縮成形し、200mgプラセボ錠剤を得た。6M塩酸(富士フィルム和光純薬製)を希釈して調整した0.1N 塩酸(約340g)にコーティング剤(OPADRY II WHITE、カラコン製)60gを混合し、6M塩酸(富士フィルム和光純薬製)及び6M 水酸化ナトリウム溶液(キシダ化学製)でpH2にpHを調整する。錠剤コーティング装置HC-Labo(フロイント産業製)にプラセボ錠剤約300gを投入し、pHを調整した液を添加してフィルムコーティングを行い、インナーシール層をプラセボ錠剤にコートした。
次に6M 塩酸(富士フィルム和光純薬製)を希釈して調整した0.1N 塩酸(約600g)にサキサグリプチン水和物(三洋化学研究所製)7.94gを添加して混合させた後、6M水酸化ナトリウム溶液(キシダ化学製)でpH2に調整する。その後コーティング剤(OPADRY II WHITE、カラコン製)60gを添加し 6M塩酸(富士フィルム和光純薬製)でpH2に調整する。錠剤コーティング装置HC-Labo(フロイント産業製)にインナーシール層をコートしたプラセボ錠剤約300gを投入し、pHを調整した液を添加してフィルムコーティングを行い、第1層にインナーシール層、第2層にサキサグリプチンを含有する層を有する錠剤を得た。
Comparative example 2
1485 g of lactose hydrate (Super Tab 30GR, manufactured by DFE Pharma), 1350 g of microcrystalline cellulose (Seolus UF-711, manufactured by Asahi Kasei), and 150 g of croscarmellose sodium (Ac-Di-Sol, manufactured by FMC) were mixed in a bag. . Next, magnesium stearate (magnesium stearate-S, manufactured by NOF Corporation) was added to the mixture in an amount of 0.5% based on the whole tableting powder, and after mixing, a small high-speed starting tableting machine (manufactured by Kikusui Seisakusho) VIRGO) to obtain 200 mg placebo tablets. 0.1 N hydrochloric acid (about 340 g) prepared by diluting 6 M hydrochloric acid (manufactured by Fujifilm Wako Pure Chemical Industries) was mixed with 60 g of a coating agent (OPADRY II WHITE, manufactured by Colorcon), and 6M hydrochloric acid (manufactured by Fuji Film Wako Pure Chemical Industries) was added. and 6M sodium hydroxide solution (manufactured by Kishida Chemical Co., Ltd.) to adjust the pH to pH 2. About 300 g of the placebo tablet was placed in a tablet coating apparatus HC-Labo (manufactured by Freund Corporation), and a pH-adjusted liquid was added to perform film coating to coat the placebo tablet with an inner seal layer.
Next, 7.94 g of saxagliptin hydrate (manufactured by Sanyo Kagaku Kenkyusho) was added to 0.1N hydrochloric acid (about 600 g) prepared by diluting 6 M hydrochloric acid (manufactured by Fujifilm Wako Pure Chemical Industries) and mixed. Adjust to pH 2 with 6M sodium hydroxide solution (manufactured by Kishida Chemical). After that, 60 g of a coating agent (OPADRY II WHITE, manufactured by Colorcon) is added, and the pH is adjusted to 2 with 6M hydrochloric acid (manufactured by Fujifilm Wako Pure Chemical Industries, Ltd.). About 300 g of placebo tablets coated with an inner seal layer are put into a tablet coating device HC-Labo (manufactured by Freund Corporation), and a pH-adjusted liquid is added to perform film coating. A tablet having a layer containing saxagliptin in the layer was obtained.
比較例3
乳糖水和物(Super Tab 30GR、DFE pharma製)594g、結晶セルロース540g(セオラスUF-711、旭化成製)、クロスカルメロースナトリウム(プリメロース、DFE pharma製)60gを袋の中で混合した。次に、打錠末全体に対して0.5%量のステアリン酸マグネシウム(ステアリン酸マグネシウム-S、日油製)を添加して混合後、小型高速起点式打錠機(菊水製作所製VIRGO)で圧縮成形し、200mgプラセボ錠剤を得た。
次に6M塩酸(富士フィルム和光純薬製)を希釈して調整した0.1N 塩酸(約600g)にサキサグリプチン水和物(三洋化学研究所製)7.94gを添加して混合させた後、6M 水酸化ナトリウム溶液(キシダ化学製)でpH2に調整する。その後コーティング剤(OPADRY II WHITE、カラコン製)60gを添加し6M塩酸(富士フィルム和光純薬製)でpH2に調整する。錠剤コーティング装置HC-Labo(フロイント産業製)にプラセボ錠剤約300gを投入し、pHを調整した液を添加してフィルムコーティングを行い、フィルム層にサキサグリプチンを含有する錠剤を得た。
Comparative example 3
594 g of lactose hydrate (Super Tab 30GR, manufactured by DFE Pharma), 540 g of crystalline cellulose (Seolus UF-711, manufactured by Asahi Kasei), and 60 g of croscarmellose sodium (primerose, manufactured by DFE Pharma) were mixed in a bag. Next, after adding and mixing 0.5% magnesium stearate (magnesium stearate-S, manufactured by NOF Corporation) with respect to the entire tableting powder, a small high-speed starting tableting machine (VIRGO manufactured by Kikusui Seisakusho) to obtain 200 mg placebo tablets.
Next, 7.94 g of saxagliptin hydrate (manufactured by Sanyo Chemical Research Institute) was added to 0.1 N hydrochloric acid (about 600 g) prepared by diluting 6 M hydrochloric acid (manufactured by Fuji Film Wako Pure Chemical Industries) and mixed. Adjust to pH 2 with 6M sodium hydroxide solution (manufactured by Kishida Chemical). After that, 60 g of a coating agent (OPADRY II WHITE, manufactured by Colorcon) is added, and the pH is adjusted to 2 with 6M hydrochloric acid (manufactured by Fuji Film Wako Pure Chemical Industries). About 300 g of the placebo tablet was placed in a tablet coating apparatus HC-Labo (manufactured by Freund Corporation), and a pH-adjusted liquid was added to perform film coating to obtain a tablet containing saxagliptin in the film layer.
比較例4
比較例3のステアリン酸マグネシウムを2.0%に、乳糖水和物を576gに変更したこと以外は比較例3と同様に製造し、フィルム層にサキサグリプチンを含有する錠剤を得た。
Comparative example 4
Tablets containing saxagliptin in the film layer were obtained in the same manner as in Comparative Example 3, except that the amount of magnesium stearate in Comparative Example 3 was changed to 2.0% and the amount of lactose hydrate was changed to 576 g.
比較例5
比較例4の乳糖水和物(Super Tab 30GR、DFE pharma製)をSuperTab 21AN(無水乳糖)に変更したこと以外は同様に製造し、フィルム層にサキサグリプチンを含有する錠剤を得た。
Comparative example 5
A tablet containing saxagliptin in the film layer was obtained in the same manner except that the lactose hydrate of Comparative Example 4 (Super Tab 30GR, manufactured by DFE Pharma) was changed to SuperTab 21AN (anhydrous lactose).
比較例6
比較例4の乳糖水和物(Super Tab 30GR、DFE pharma製)をD-マンニトール(グラニュトールR)に変更したこと以外は同様に製造し、フィルム層にサキサグリプチンを含有する錠剤を得た。
Comparative example 6
Tablets containing saxagliptin in the film layer were obtained in the same manner as in Comparative Example 4, except that the lactose hydrate (Super Tab 30GR, manufactured by DFE Pharma) was changed to D-mannitol (Granutol R).
実施例1
比較例6の結晶セルロース540g(セオラスUF-711、旭化成製)をD-マンニトール(グラニュトールR、フロイント産業製)に変更したこと以外は同様に製造し、フィルム層にサキサグリプチンを含有する錠剤を得た。
Example 1
A tablet containing saxagliptin in the film layer was obtained in the same manner as in Comparative Example 6 except that 540 g of crystalline cellulose (Seolus UF-711, manufactured by Asahi Kasei Corporation) was changed to D-mannitol (Granitol R, manufactured by Freund Corporation). rice field.
実施例2
実施例1のクロスカルメロースナトリウム(プリメロース、DFE pharma製)を部分α化デンプン(PCS、旭化成製)に変更したこと以外は同様に製造し、フィルム層にサキサグリプチンを含有する錠剤を得た。
Example 2
Tablets containing saxagliptin in the film layer were obtained in the same manner as in Example 1, except that croscarmellose sodium (primerose, DFE Pharma) was replaced with partially pregelatinized starch (PCS, Asahi Kasei).
実施例3
実施例1のクロスカルメロースナトリウム(プリメロース、DFE pharma製)をクロスポビドン(コリドンCL-F、BASF製)に変更したこと以外は同様に製造し、フィルム層にサキサグリプチンを含有する錠剤を得た。
Example 3
Tablets containing saxagliptin in the film layer were obtained in the same manner as in Example 1, except that croscarmellose sodium (primerose, DFE Pharma) was changed to crospovidone (Kollidon CL-F, BASF).
実施例4
実施例1のクロスカルメロースナトリウム(プリメロース、DFE pharma製)をクロスポビドン(ポリプラスドンUltra-10、Ashland製)に変更したこと以外は同様に製造し、フィルム層にサキサグリプチンを含有する錠剤を得た。
Example 4
A tablet containing saxagliptin in the film layer was obtained in the same manner as in Example 1 except that croscarmellose sodium (primerose, DFE Pharma) was changed to crospovidone (Polyplasdon Ultra-10, Ashland). rice field.
実施例5
実施例1のクロスカルメロースナトリウム(プリメロース、DFE pharma製)を低置換度ヒドロキシプロピルセルロース(LH21、信越化学工業製)に変更したこと以外は同様に製造し、フィルム層にサキサグリプチンを含有する錠剤を得た。
Example 5
Tablets containing saxagliptin in the film layer were produced in the same manner as in Example 1 except that croscarmellose sodium (primerose, manufactured by DFE Pharma) was changed to low-substituted hydroxypropyl cellulose (LH21, manufactured by Shin-Etsu Chemical Co., Ltd.). Obtained.
実施例6
実施例5のステアリン酸マグネシウム(ステアリン酸マグネシウム-S、日油製)をフマル酸ステアリルナトリウム(PRUV、FMC製)に変更したこと以外は同様に製造し、フィルム層にサキサグリプチンを含有する錠剤を得た。
Example 6
A tablet containing saxagliptin in the film layer was obtained in the same manner as in Example 5 except that magnesium stearate (magnesium stearate-S, manufactured by NOF Corporation) was changed to sodium stearyl fumarate (PRUV, manufactured by FMC). rice field.
実施例7
精製水67.2g、無水エタノール(エタノール(99.5)、富士フィルム和光純薬製)28.8gにポリビニルアルコール(ゴーセノールEG-03P、日本合成化学工業製)4.8gを溶解させた液を練合液とした。
D-マンニトール(マンニットP、三菱商事ライフサイエンス製)955.2gを攪拌造粒(VG-05、パウレック製)に投入し、練合液を加えて練合し、湿式打錠用の打錠用粉体を得た。
この粉体を湿式打錠機 ( EMT-18、三共製作所製)で打錠圧150Nの条件下で圧縮成形し、ベルトコンベア式乾燥機(ETD-18、三共製作所製)を用いて、85℃の温度で約5分間乾燥し、プラセボ錠剤(=湿製素錠)を得た。
次に6M塩酸(富士フィルム和光純薬製)を希釈して調整した0.1N塩酸(約600g)にサキサグリプチン水和物(三洋化学研究所製)7.94gを添加して混合させた後、6M水酸化ナトリウム溶液(キシダ化学製)でpH2に調整する。その後コーティング剤(OPADRY II WHITE、カラコン製)60gを添加し 6M塩酸(富士フィルム和光純薬製)でpH2に調整する。錠剤コーティング装置HC-Labo(フロイント産業製)にプラセボ錠剤約300gを投入し、pHを調整した液を添加してフィルムコーティングを行い、フィルム層にサキサグリプチンを含有する錠剤を得た。
Example 7
67.2 g of purified water, 28.8 g of anhydrous ethanol (ethanol (99.5), manufactured by Fuji Film Wako Pure Chemical Industries) and 4.8 g of polyvinyl alcohol (Gosenol EG-03P, manufactured by Nippon Synthetic Chemical Industry) were dissolved in a solution. It was used as a kneading liquid.
955.2 g of D-mannitol (Mannitol P, manufactured by Mitsubishi Corporation Life Science) is added to stirring granulation (VG-05, manufactured by Powrex), kneaded by adding a kneading liquid, and tableting for wet tableting. We obtained a powder for
This powder was compression-molded with a wet tableting machine (EMT-18, manufactured by Sankyo Seisakusho) at a tableting pressure of 150 N, and dried at 85°C using a belt conveyor dryer (ETD-18, manufactured by Sankyo Seisakusho). for about 5 minutes to obtain a placebo tablet (=wet uncoated tablet).
Next, 7.94 g of saxagliptin hydrate (manufactured by Sanyo Chemical Research Institute) was added to 0.1N hydrochloric acid (about 600 g) prepared by diluting 6M hydrochloric acid (manufactured by Fuji Film Wako Pure Chemical Industries) and mixed. Adjust to pH 2 with 6M sodium hydroxide solution (manufactured by Kishida Chemical). After that, 60 g of a coating agent (OPADRY II WHITE, manufactured by Colorcon) is added, and the pH is adjusted to 2 with 6M hydrochloric acid (manufactured by Fujifilm Wako Pure Chemical Industries). About 300 g of the placebo tablet was placed in a tablet coating apparatus HC-Labo (manufactured by Freund Corporation), and a pH-adjusted liquid was added to perform film coating to obtain a tablet containing saxagliptin in the film layer.
(分析方法)
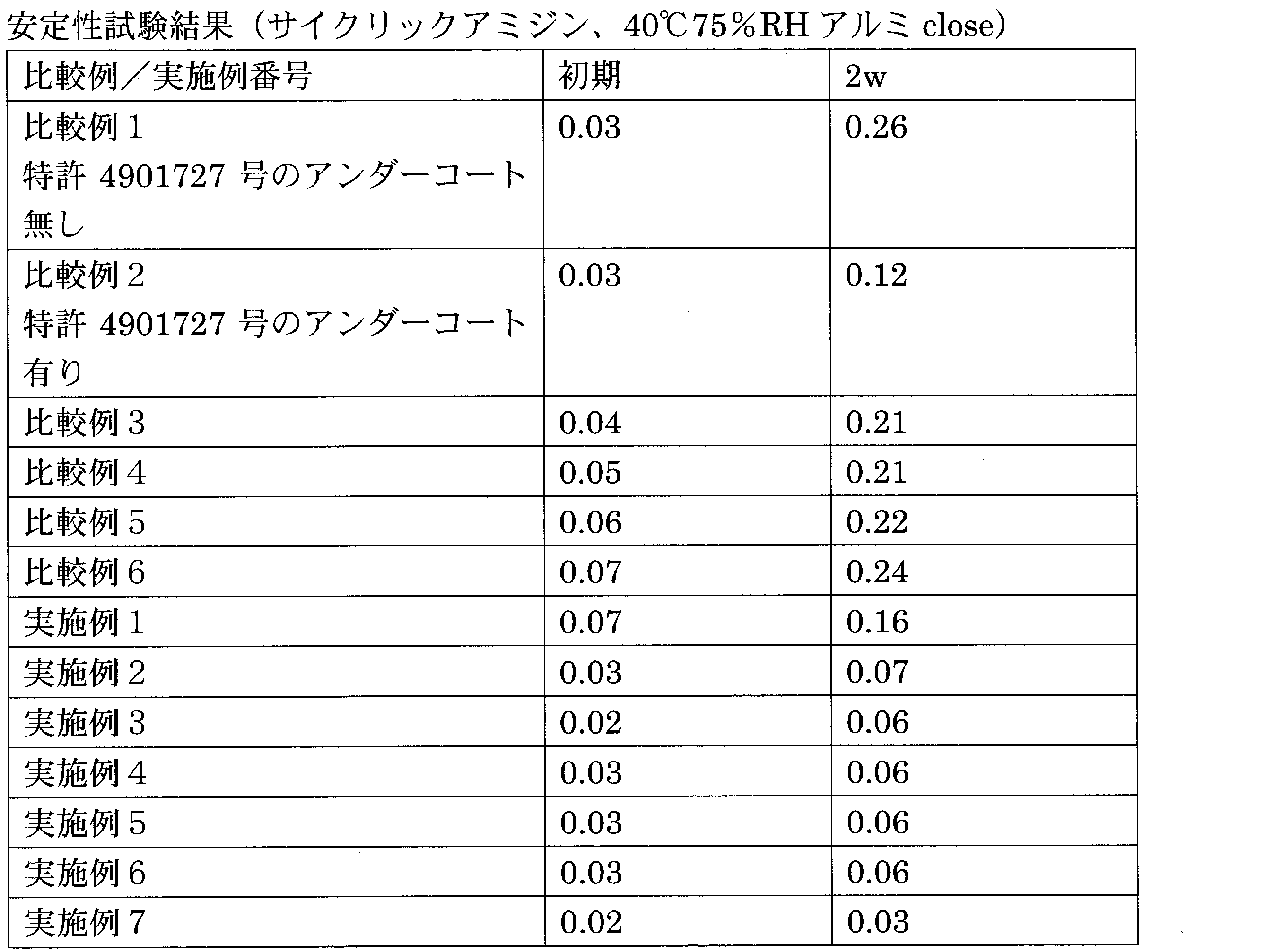
フィルムコート錠を、アルミ袋に入れてヒートシールをして、40℃、75%RH条件下に2週間保存した。保存前及び保存後に、液体クロマトグラフィーでサイクリックアミジン量を測定した。
液体クロマトグラフィーによる測定条件を以下に示す。
検出器:紫外吸光光度計(測定波長:210nm)
カラム:ACQUITY UPLC BEH C18 粒径1.7μm 2.1mm×100mm
カラム温度:30℃付近の一定温度
移動相A:Buffer/アセトニトリル混液(90:10)
移動相B:Buffer/アセトニトリル混液(60:40)
Buffer:リン酸二水素カリウム2.72gに1000mL水を加え、リン酸を用いてpH4.0に調整する。
移動相の送液:移動相A及び移動相Bの混合比を、下記の表1に示すように制御した。
流量:0.3mL/min
(analysis method)
The film-coated tablet was placed in an aluminum bag, heat-sealed, and stored under conditions of 40° C. and 75% RH for 2 weeks. Before and after storage, the amount of cyclic amidine was measured by liquid chromatography.
Measurement conditions by liquid chromatography are shown below.
Detector: UV absorption photometer (measurement wavelength: 210 nm)
Column: ACQUITY UPLC BEH C18 particle size 1.7 μm 2.1 mm × 100 mm
Column temperature: Constant temperature around 30°C Mobile phase A: Buffer/acetonitrile mixture (90:10)
Mobile phase B: Buffer/acetonitrile mixture (60:40)
Buffer: 1000 mL water is added to 2.72 g of potassium dihydrogen phosphate, and the pH is adjusted to 4.0 using phosphoric acid.
Transfer of mobile phase: The mixing ratio of mobile phase A and mobile phase B was controlled as shown in Table 1 below.
Flow rate: 0.3mL/min
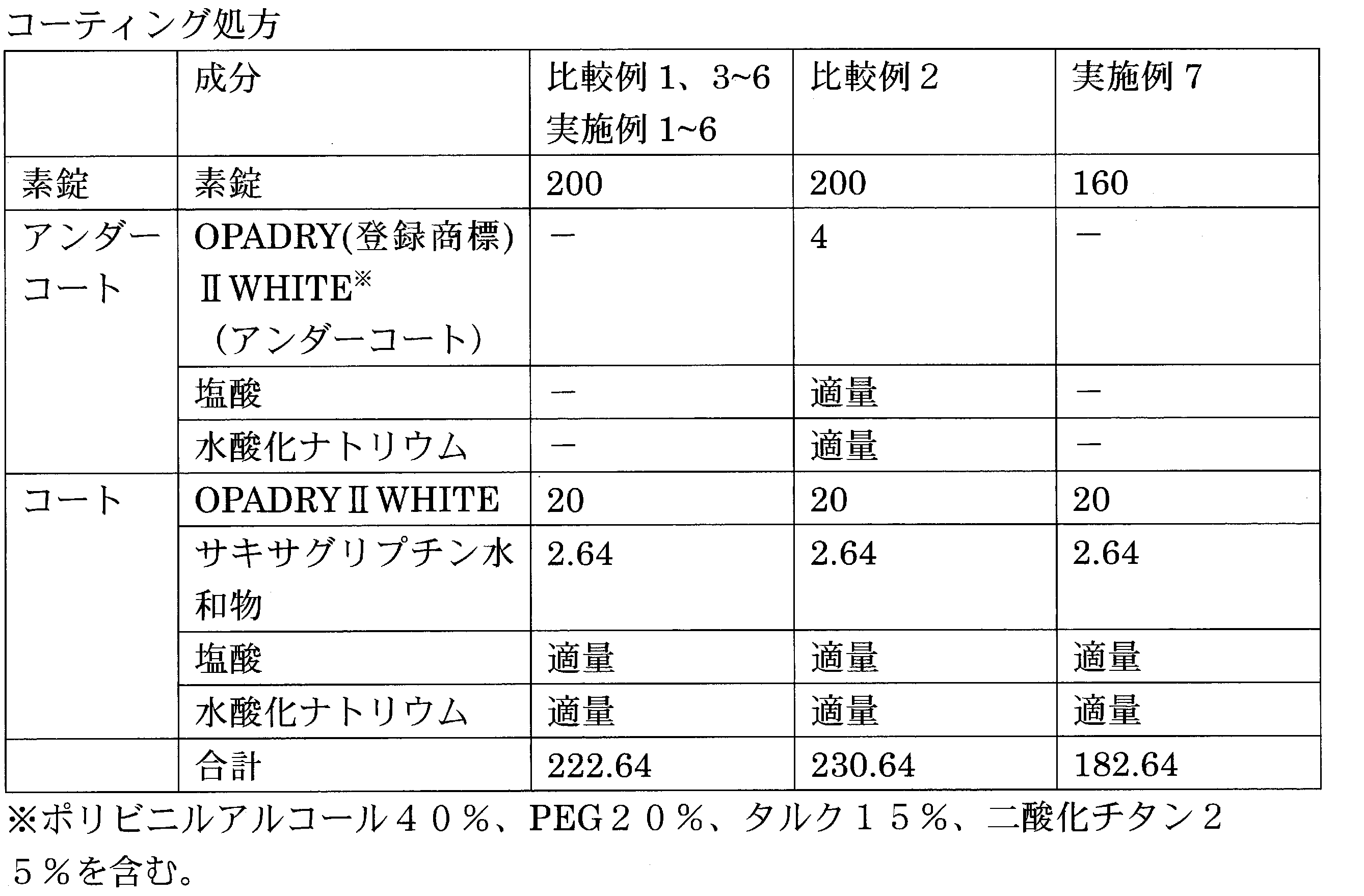
比較例1~6及び実施例1~6の素錠の処方を表2に示す。
実施例7の湿製錠については、フィルムコート錠を、アルミ袋に入れて開封状態で、40℃、75%RH条件下に2週間保存し、液体クロマトグラフィーでサイクリックアミジン量を測定した。
その結果、実施例7の湿製錠については、開放系保存においても、サイクリックアミジン量が0.05%であり、特に安定性に優れていることが判明した。
As for the wet tablet of Example 7, the film-coated tablet was placed in an aluminum bag and stored unsealed under conditions of 40° C. and 75% RH for 2 weeks, and the amount of cyclic amidine was measured by liquid chromatography.
As a result, it was found that the wet tablet of Example 7 had a cyclic amidine content of 0.05% even during storage in an open system, and was particularly excellent in stability.
Claims (4)
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2021034765A JP2022135147A (en) | 2021-03-04 | 2021-03-04 | Tablets containing saxagliptin |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2021034765A JP2022135147A (en) | 2021-03-04 | 2021-03-04 | Tablets containing saxagliptin |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2022135147A true JP2022135147A (en) | 2022-09-15 |
Family
ID=83232331
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021034765A Pending JP2022135147A (en) | 2021-03-04 | 2021-03-04 | Tablets containing saxagliptin |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2022135147A (en) |
Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS63104930A (en) * | 1986-10-20 | 1988-05-10 | ワーナー−ランバート・コンパニー | stabilized drug composition |
| JP2009525047A (en) * | 2006-02-02 | 2009-07-09 | ザ ユーエイビー リサーチ ファウンデイション | Non-coil-protected region of Streptococcus pneumoniae surface proteins PSPA and PSPC |
| JP4901727B2 (en) * | 2004-05-28 | 2012-03-21 | ブリストル−マイヤーズ スクイブ カンパニー | Coated tablet formulation and method |
| US20140072628A1 (en) * | 2012-09-12 | 2014-03-13 | Glenmark Generics Ltd. | Stable pharmaceutical composition of saxagliptin |
| WO2014096982A1 (en) * | 2012-12-21 | 2014-06-26 | Wockhardt Limited | Stable pharmaceutical compositions of saxagliptin or salts thereof |
| JP2020196705A (en) * | 2019-05-31 | 2020-12-10 | 沢井製薬株式会社 | Method of stabilizing saxagliptin and powder containing saxagliptin |
| JP2022003016A (en) * | 2020-06-23 | 2022-01-11 | 沢井製薬株式会社 | Saxagliptin-containing preparation and its manufacturing method |
-
2021
- 2021-03-04 JP JP2021034765A patent/JP2022135147A/en active Pending
Patent Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS63104930A (en) * | 1986-10-20 | 1988-05-10 | ワーナー−ランバート・コンパニー | stabilized drug composition |
| JP4901727B2 (en) * | 2004-05-28 | 2012-03-21 | ブリストル−マイヤーズ スクイブ カンパニー | Coated tablet formulation and method |
| JP2009525047A (en) * | 2006-02-02 | 2009-07-09 | ザ ユーエイビー リサーチ ファウンデイション | Non-coil-protected region of Streptococcus pneumoniae surface proteins PSPA and PSPC |
| US20140072628A1 (en) * | 2012-09-12 | 2014-03-13 | Glenmark Generics Ltd. | Stable pharmaceutical composition of saxagliptin |
| WO2014096982A1 (en) * | 2012-12-21 | 2014-06-26 | Wockhardt Limited | Stable pharmaceutical compositions of saxagliptin or salts thereof |
| JP2020196705A (en) * | 2019-05-31 | 2020-12-10 | 沢井製薬株式会社 | Method of stabilizing saxagliptin and powder containing saxagliptin |
| JP2022003016A (en) * | 2020-06-23 | 2022-01-11 | 沢井製薬株式会社 | Saxagliptin-containing preparation and its manufacturing method |
Non-Patent Citations (1)
| Title |
|---|
| 医薬品添加物事典2016, vol. 第1刷, JPN6024050935, 2016, pages 729 - 731, ISSN: 0005596502 * |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| TWI404534B (en) | Solid pharmaceutical composition comprising amlodipine and losartan with improved stability | |
| JP6730978B2 (en) | Solid formulation | |
| JP5827299B2 (en) | Pharmaceutical composition containing irbesartan and amlodipine or a salt thereof | |
| US20090208583A1 (en) | Tablets comprising candesartan cilexetil | |
| US11331273B2 (en) | Film-coated tablet having high chemical stability of active ingredient | |
| JP2011162531A (en) | Fexofenadine-including, film-coating oral pharmaceutical preparation | |
| JP4972563B2 (en) | New film-coated tablets | |
| JP2017048174A (en) | Orally disintegrable tablet containing chemically stable coated particles containing drug substance | |
| RU2651460C2 (en) | COMBINED COMPOSITION CONTAINING METFORMIN OF SUSTAINED RELEASE AND INHIBITOR HMG-CoA-REDUCTASE OF IMMEDIATE RELEASE | |
| KR102206104B1 (en) | Granule comprising silodosin, and pharmaceutical composition and formulation comprising the same | |
| EP3886817A1 (en) | Pharmaceutical composition comprising ramipril and indapamide | |
| JP2022135147A (en) | Tablets containing saxagliptin | |
| JP6816972B2 (en) | Ezetimibe-containing pharmaceutical composition and its production method, ezetimibe-containing pharmaceutical composition hardness reduction inhibitor and hardness reduction suppression method, and ezetimibe-containing pharmaceutical composition moisture absorption inhibitor and moisture absorption suppression method | |
| WO2020111089A1 (en) | Pharmaceutical composition | |
| JP2022012138A (en) | Pharmaceutical formulation containing linagliptin and photostabilizing ingredient | |
| JP2016155777A (en) | Composition comprising montelukast or salt thereof | |
| JP7206872B2 (en) | Pharmaceutical composition containing azilsartan and amlodipine and method for producing the same | |
| WO2022153330A1 (en) | Pharmaceutical compositions comprising acalabrutinib | |
| JP2022121165A (en) | Saxagliptin-containing tablet | |
| JP2009521518A (en) | Oral formulations of anhydrous olanzapine type I | |
| JP7518316B1 (en) | Teneligliptin-containing particles and formulations containing the same | |
| JP2021155359A (en) | Tablet containing levocarnitine as active ingredient | |
| JP7336241B2 (en) | Method for producing tablet containing vardenafil | |
| JP2019156844A (en) | Memantine hydrochloride-containing tablet | |
| JP2020147511A (en) | Pharmaceutical composition and pharmaceutical preparation containing levocetirizine hydrochloride, and method of stabilizing levocetirizine hydrochloride |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20240229 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20241217 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20241218 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20250520 |