JP2020534788A - アデノ随伴ウイルスカプシド変異体及びその使用方法 - Google Patents
アデノ随伴ウイルスカプシド変異体及びその使用方法 Download PDFInfo
- Publication number
- JP2020534788A JP2020534788A JP2019562303A JP2019562303A JP2020534788A JP 2020534788 A JP2020534788 A JP 2020534788A JP 2019562303 A JP2019562303 A JP 2019562303A JP 2019562303 A JP2019562303 A JP 2019562303A JP 2020534788 A JP2020534788 A JP 2020534788A
- Authority
- JP
- Japan
- Prior art keywords
- aav
- amino acids
- virion
- raav
- fold
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/005—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from viruses
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N7/00—Viruses; Bacteriophages; Compositions thereof; Preparation or purification thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/66—Microorganisms or materials therefrom
- A61K35/76—Viruses; Subviral particles; Bacteriophages
- A61K35/761—Adenovirus
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
- A61K48/0008—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy characterised by an aspect of the 'non-active' part of the composition delivered, e.g. wherein such 'non-active' part is not delivered simultaneously with the 'active' part of the composition
- A61K48/0025—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy characterised by an aspect of the 'non-active' part of the composition delivered, e.g. wherein such 'non-active' part is not delivered simultaneously with the 'active' part of the composition wherein the non-active part clearly interacts with the delivered nucleic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/79—Vectors or expression systems specially adapted for eukaryotic hosts
- C12N15/85—Vectors or expression systems specially adapted for eukaryotic hosts for animal cells
- C12N15/86—Viral vectors
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2227/00—Animals characterised by species
- A01K2227/10—Mammal
- A01K2227/105—Murine
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2267/00—Animals characterised by purpose
- A01K2267/03—Animal model, e.g. for test or diseases
- A01K2267/0393—Animal model comprising a reporter system for screening tests
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2750/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssDNA viruses
- C12N2750/00011—Details
- C12N2750/14011—Parvoviridae
- C12N2750/14111—Dependovirus, e.g. adenoassociated viruses
- C12N2750/14122—New viral proteins or individual genes, new structural or functional aspects of known viral proteins or genes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2750/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssDNA viruses
- C12N2750/00011—Details
- C12N2750/14011—Parvoviridae
- C12N2750/14111—Dependovirus, e.g. adenoassociated viruses
- C12N2750/14133—Use of viral protein as therapeutic agent other than vaccine, e.g. apoptosis inducing or anti-inflammatory
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2750/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssDNA viruses
- C12N2750/00011—Details
- C12N2750/14011—Parvoviridae
- C12N2750/14111—Dependovirus, e.g. adenoassociated viruses
- C12N2750/14141—Use of virus, viral particle or viral elements as a vector
- C12N2750/14143—Use of virus, viral particle or viral elements as a vector viral genome or elements thereof as genetic vector
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2750/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssDNA viruses
- C12N2750/00011—Details
- C12N2750/14011—Parvoviridae
- C12N2750/14111—Dependovirus, e.g. adenoassociated viruses
- C12N2750/14141—Use of virus, viral particle or viral elements as a vector
- C12N2750/14145—Special targeting system for viral vectors
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2800/00—Nucleic acids vectors
- C12N2800/30—Vector systems comprising sequences for excision in presence of a recombinase, e.g. loxP or FRT
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Genetics & Genomics (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Health & Medical Sciences (AREA)
- Virology (AREA)
- Biomedical Technology (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Biochemistry (AREA)
- Biotechnology (AREA)
- Medicinal Chemistry (AREA)
- General Engineering & Computer Science (AREA)
- Molecular Biology (AREA)
- Biophysics (AREA)
- Microbiology (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Physics & Mathematics (AREA)
- Plant Pathology (AREA)
- Gastroenterology & Hepatology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Neurosurgery (AREA)
- Neurology (AREA)
- Epidemiology (AREA)
- Immunology (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Mycology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Psychiatry (AREA)
- Hospice & Palliative Care (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
Description
本願は、その出願が参照によりその全体が本明細書に組み込まれる、2017年8月28日に出願された米国仮特許出願第62/551,133号の利益を主張するものである。
アデノ随伴ウイルス(AAV)は、パルボウイルス(Parvoviridae)科ディペンドウイルス属に属し、この属のメンバーは、複製を促進するためにアデノウイルスのようなヘルパーウイルスとの重複感染を必要とし、ヘルパーが存在しない場合、AAVは潜伏感染状態となる。ビリオンは、25nmの正二十面体のカプシドで構成され、カプシドは、2つのオープンリーディングフレーム、rep及びcapを有する4.7kbの一本鎖DNAゲノムを包含する。非構造rep遺伝子は、ウイルス複製に不可欠な4つの調節タンパク質をコードし、capは、集合して60−merカプシド殻を構成する3つの構造タンパク質(VP1〜VP3)をコードする。このウイルスカプシドは、AAVベクターがウイルス形質導入の生物学的障壁の多くを克服する能力、例えば、細胞表面受容体結合、エンドサイトーシス、細胞内輸送、及び核内での脱殻などを仲介する。
本開示は、変異カプシドタンパク質を有する組換え型アデノ随伴ウイルスビリオンを提供し、ここで、かかる組換え型AAV(rAAV)ビリオンは、対照AAVと比較して、神経細胞障壁を通過する高い能力、神経幹細胞への高い感染力、神経細胞への高い感染力、及び抗体による中和に対する低い感受性のうち1つ以上を示し、かつ、異種核酸を含む。本開示は、個体の神経幹細胞または神経細胞に遺伝子産物を送達する方法を提供する。本開示は、神経幹細胞内または神経細胞内に存在する標的核酸を修飾する方法も提供する。
本明細書で使用する場合、用語「神経幹細胞」(NSC)とは、増殖、自己複製をすることができ、脳の主要な成体神経細胞に分化することができる未分化の神経細胞を指す。NSCには、自己維持(自己複製)する能力があり、すなわち、各細胞分裂で1つの娘細胞もまた幹細胞となることを意味する。幹細胞ではないNSC子孫は神経前駆細胞と呼ばれる。1つの多能性NSCから発生した神経前駆細胞は、ニューロン、アストロサイト(I型及びII型)、及びオリゴデンドロサイトに分化する能力がある。したがって、NSCは、その子孫が神経細胞としての複数の運命を持っているため「多能性」である。このことから、NSCは、機能上、1)増殖する能力、2)自己複製する能力、及び3)中枢神経系に見られる3つの主要な細胞型、すなわち、ニューロン、アストロサイト及びオリゴデンドロサイトに分化することができる機能的子孫を産生する能力を有する細胞として定義され得る。NSCは一般に、成熟ニューロン、成熟グリア細胞、成熟オリゴデンドロサイト、及び成熟アストロサイトのマーカーに対して陰性である。
ミスマッチペナルティ:1.00、
ギャップペナルティ:1.00、
ギャップサイズペナルティ:0.33、
ジョイニングペナルティ:30.0。
本開示は、変異カプシドタンパク質を有する組換え型アデノ随伴ウイルスビリオンを提供し、ここで、かかる組換え型AAV(rAAV)ビリオンは、対照AAVと比較して、神経細胞障壁を通過する高い能力、神経幹細胞への高い感染力、神経細胞への高い感染力、及び抗体による中和に対する低い感受性のうち1つ以上を示し、かつ、異種核酸を含む。本開示は、個体の神経幹細胞、神経前駆細胞、または神経細胞に遺伝子産物を送達する方法を提供する。本開示は、神経幹細胞内または神経細胞内に存在する標的核酸を修飾する方法も提供する。本開示はさらに、神経疾患を治療する方法を提供する。
本開示は、(i)本開示の変異型AAVカプシドポリペプチドと、(ii)異種ポリペプチド(すなわち、非AAVポリペプチド)をコードするヌクレオチド配列を含む異種核酸とを含む感染性rAAVビリオンを提供する。場合によっては、変異AAVカプシドタンパク質は、少なくとも3つの異なるAAV血清型に由来する少なくとも5つのセグメントを含み、ここで、各セグメントは長さが約50アミノ酸〜約160アミノ酸である。変異カプシドタンパク質は、以下の特性のうち1つ以上を付与する:(i)対応する親AAVカプシドタンパク質を含む対照AAVビリオンによる神経幹細胞または神経前駆細胞への感染力と比較して、または野生型AAVビリオンと比較して、または野生型AAVカプシドを含む対照AAVビリオンと比較して、神経幹細胞または神経前駆細胞への感染力が高い、(ii)対応する親AAVカプシドタンパク質を含む対照AAVビリオンによる神経細胞への感染力と比較して、または野生型AAVビリオンと比較して、または野生型AAVカプシドを含む対照AAVビリオンと比較して、神経細胞への感染力が高い、(iii)対応する親AAVカプシドタンパク質を含む対照AAVビリオンが細胞障壁を通過する能力と比較して、または野生型AAVビリオンが細胞障壁を通過する能力と比較して、または野生型AAVカプシドを含む対照AAVビリオンと比較して、細胞障壁を通過する能力が高い、(iv)対応する親AAVカプシドタンパク質を含む対照AAVビリオンにより示される耐性と比較して、または野生型AAVビリオンと比較して、または野生型AAVカプシドを含む対照AAVビリオンと比較して、ヒトAAV中和抗体に対する耐性が高い。
本開示は、変異カプシドタンパク質を有するrAAVビリオンを提供し、かかるrAAVビリオンは、変異カプシドタンパク質を含まない対照親AAVが神経幹細胞(NSC)または神経前駆細胞を感染させる能力と比較して、または野生型AAVがNSCまたは神経前駆細胞を感染させる能力と比較して、または野生型AAVカプシドを含む対照AAVビリオンがNSCまたは神経前駆細胞を感染させる能力と比較して、NSCまたは神経前駆細胞への高い感染力を示し、かつ、かかるrAAVビリオンは異種核酸を含む。
上記のように、場合によっては、本開示のrAAVビリオンに存在する変異カプシドポリペプチドは、変異カプシドタンパク質を含まない対照親AAVまたは野生型AAVが神経細胞を感染させる能力と比較して、高い神経細胞への感染力をrAAVビリオンに付与する。
本開示は、変異カプシドタンパク質を有する組換え型アデノ随伴ウイルスビリオンを提供し、かかるrAAVビリオンは、細胞障壁、すなわち生理的障壁を通過する高い能力を示す。例えば、細胞障壁は、神経幹細胞が含まれない第1のコンパートメントと、神経幹細胞が含まれる第2のコンパートメントとの間にある細胞の層を含むことができる。そのような障壁には、例えば、側脳室の表面を覆う上衣細胞層、低細胞性層、アストロサイト細胞体層、血液脳関門、及び移行帯層が含まれる。したがって、本開示は、変異カプシドタンパク質を有するrAAVビリオンを提供し、かかるrAAVビリオンは、上衣細胞層、低細胞性層、アストロサイト細胞体層、及び移行帯層の1つ以上を通過する能力が、変異カプシドタンパク質を含まない対照AAVの層通過能力と比較して、または野生型AAVカプシドタンパク質を含む対照AAVの能力と比較して、少なくとも2倍、少なくとも5倍、少なくとも10倍、少なくとも15倍、少なくとも20倍、少なくとも25倍、少なくとも50倍、または50倍以上高いことを示し、かつ、かかるrAAVビリオンは、異種遺伝子産物をコードするヌクレオチド配列を含む異種核酸を含む。
上記のように、場合によっては、本開示のrAAVビリオンは、野生型AAVカプシドを含むAAVに対する中和抗体の結合と比較して、中和抗体への結合低下を示す。
場合によっては、本開示のrAAVビリオンは神経細胞を選択的に感染させ、例えば、本開示のrAAVビリオンは、神経細胞を、非神経細胞よりも10倍、15倍、20倍、25倍、50倍、または50倍以上特異的に感染させる。
上記のように、本開示のrAAVビリオンは変異AAVカプシドタンパク質を含む。場合によっては、本開示のrAAVビリオンに存在する変異AAVカプシドタンパク質は、少なくとも3つの異なるAAV血清型に由来する少なくとも5つのセグメントを含み、各セグメントは、長さが約50アミノ酸〜約160アミノ酸である。
場合によっては、本開示の変異カプシドポリペプチドは、1つ以上のさらなる変異(例えば、アミノ酸置換、1つ以上のアミノ酸の挿入、1つ以上のアミノ酸の欠失)を含む。
から選択されるアミノ酸配列を含む挿入を含む。場合によっては、ペプチド挿入はTGVMRSTNSGLN(配列番号153)である。場合によっては、ペプチド挿入はTGEVDLAGGGLS(配列番号154)である。場合によっては、ペプチド挿入はTSPYSGSSDGLS(配列番号155)である。場合によっては、ペプチド挿入はTGGHDSSLDGLS(配列番号156)である。場合によっては、ペプチド挿入はTGDGGTTMNGLS(配列番号157)である。場合によっては、ペプチド挿入はTGGHGSAPDGLS(配列番号158)である。場合によっては、ペプチド挿入はTGMHVTMMAGLN(配列番号159)である。場合によっては、ペプチド挿入はTGASYLDNSGLS(配列番号160)である。場合によっては、ペプチド挿入はTVVSTQAGIGLS(配列番号161)である。場合によっては、ペプチド挿入はTGVMHSQASGLS(配列番号162)である。場合によっては、ペプチド挿入はTGDGSPAAPGLS(配列番号163)である。場合によっては、ペプチド挿入はTGSDMAHGTGLS(配列番号164)である。場合によっては、ペプチド挿入はTGSDGTRDHGLSPVTWT(配列番号166)である。場合によっては、ペプチド挿入はNGAVADYTRGLSPATGT(配列番号167)である。場合によっては、ペプチド挿入はTGGDPTRGTGLSPVTGA(配列番号168)である。場合によっては、ペプチド挿入はLQKNARPASTESVNFQ(配列番号169)である。場合によっては、ペプチド挿入はLQRGVRIPSVLEVNGQ(配列番号170)である。場合によっては、ペプチド挿入はLQRGNRPVTTADVNTQ(配列番号171)である。場合によっては、ペプチド挿入はLQKADRQPGVVVVNCQ(配列番号172)である。
上記のように、本開示のrAAVビリオンは、1つ以上の遺伝子産物(1つ以上の異種遺伝子産物)をコードするヌクレオチド配列を含む異種核酸を含む。場合によっては、遺伝子産物はポリペプチドである。場合によっては、遺伝子産物はRNAである。場合によっては、本開示のrAAVビリオンは、異種核酸遺伝子産物及び異種ポリペプチド遺伝子産物の両方をコードする異種ヌクレオチド配列を含む。遺伝子産物がRNAである場合、場合によっては、RNA遺伝子産物はポリペプチドをコードする。遺伝子産物がRNAである場合、場合によっては、RNA遺伝子産物はポリペプチドをコードしない。場合によっては、本開示のrAAVビリオンは、単一の異種遺伝子産物をコードするヌクレオチド配列を含む単一異種核酸を含む。場合によっては、本開示のrAAVビリオンは、2つの異種遺伝子産物をコードするヌクレオチド配列を含む単一異種核酸を含む。単一異種核酸が2つの異種遺伝子産物をコードする場合、場合によっては、かかる2つの異種遺伝子産物をコードするヌクレオチド配列は同一プロモーターに機能的に連結される。単一異種核酸が2つの異種遺伝子産物をコードする場合、場合によっては、かかる2つの異種遺伝子産物をコードするヌクレオチド配列は2つの異なるプロモーターに機能的に連結される。場合によっては、本開示のrAAVビリオンは、3つの異種遺伝子産物をコードするヌクレオチド配列を含む単一異種核酸を含む。単一異種核酸が3つの異種遺伝子産物をコードする場合、場合によっては、かかる3つの異種遺伝子産物をコードするヌクレオチド配列は同一プロモーターに機能的に連結される。単一異種核酸が3つの異種遺伝子産物をコードする場合、場合によっては、かかる3つの異種遺伝子産物をコードするヌクレオチド配列は2つまたは3つの異なるプロモーターに機能的に連結される。場合によっては、本開示のrAAVビリオンは、各々が異種遺伝子産物をコードするヌクレオチド配列を含む2つの異種核酸を含む。
遺伝子産物が干渉RNA(RNAi)である場合、適切なRNAiには、細胞でのアポトーシス因子または血管新生因子レベルを低下させるRNAiが含まれる。例えば、RNAiは、細胞でのアポトーシスを誘導または促進する遺伝子産物のレベルを低下させる、shRNAまたはsiRNAであり得る。その遺伝子産物がアポトーシスを誘導または促進する遺伝子を本明細書では「アポトーシス促進遺伝子」と呼び、それらの遺伝子の産物(mRNA;タンパク質)を「アポトーシス促進遺伝子産物」と呼ぶ。アポトーシス促進遺伝子産物には、例えば、Bax、Bid、Bak、及びBadなどの遺伝子産物が含まれる。例えば、米国特許第7,846,730号を参照のこと。
遺伝子産物がポリペプチドである場合、場合によっては、ポリペプチドは、神経幹細胞、神経前駆細胞、または神経細胞の機能を高めるポリペプチドである。
場合によっては、目的遺伝子産物は、遺伝子機能を部位特異的にノックダウンさせる部位特異的エンドヌクレアーゼであり、例えば、その場合、かかるエンドヌクレアーゼは神経疾患に関連したアレルをノックアウトする。例えば、顕性アレルが、野生型では神経構造タンパク質である遺伝子についての欠陥コピーをコードする、及び/または正常な神経機能を提供するという場合、部位特異的エンドヌクレアーゼを欠陥アレルに指向させ、欠陥アレルをノックアウトすることができる。場合によっては、部位特異的エンドヌクレアーゼはRNA誘導型エンドヌクレアーゼである。
場合によっては、遺伝子産物はRNA誘導型エンドヌクレアーゼである。場合によっては、遺伝子産物は、RNA誘導型エンドヌクレアーゼをコードするヌクレオチド配列を含むRNAである。場合によっては、遺伝子産物はガイドRNA、例えば、シングルガイドRNAである。場合によっては、遺伝子産物は、1)ガイドRNA、及び2)RNA誘導型エンドヌクレアーゼである。ガイドRNAは、a)RNA誘導型エンドヌクレアーゼに結合するタンパク質結合領域、及びb)標的核酸に結合する領域を含むことができる。RNA誘導型エンドヌクレアーゼは本明細書では「ゲノム編集ヌクレアーゼ」とも呼ばれる。
RNA誘導型エンドヌクレアーゼは本明細書では「ゲノム編集ヌクレアーゼ」とも呼ばれる。適切なゲノム編集ヌクレアーゼの例は、CRISPR/Casエンドヌクレアーゼ(例えば、クラス2のCRISPR/Casエンドヌクレアーゼ、例えば、II型、V型、またはVI型のCRISPR/Casエンドヌクレアーゼなど)である。適切なゲノム編集ヌクレアーゼは、CRISPR/Casエンドヌクレアーゼ(例えば、クラス2のCRISPR/Casエンドヌクレアーゼ、例えば、II型、V型、またはVI型のCRISPR/Casエンドヌクレアーゼなど)である。場合によっては、適切なゲノム編集ヌクレアーゼはクラス2のCRISPR/Casエンドヌクレアーゼである。場合によっては、適切なゲノム編集ヌクレアーゼは、クラス2のII型CRISPR/Casエンドヌクレアーゼ(例えば、Cas9タンパク質)である。場合によっては、適切なゲノム編集ヌクレアーゼは、クラス2のV型CRISPR/Casエンドヌクレアーゼ(例えば、Cpf1タンパク質、C2c1タンパク質、またはC2c3タンパク質)である。場合によっては、適切なゲノム編集ヌクレアーゼは、クラス2のVI型CRISPR/Casエンドヌクレアーゼ(例えば、C2c2タンパク質;「Cas13a」タンパク質とも呼ばれる)である。また、CasXタンパク質も使用に好適である。また、CasYタンパク質も使用に好適である。
また、酵素活性が低いRNA誘導型エンドヌクレアーゼも使用に好適である。そのようなRNA誘導型エンドヌクレアーゼは「デッド(dead)」RNA誘導型エンドヌクレアーゼと呼ばれ、例えば、実質的にエンドヌクレアーゼ活性を全く示さないが、ガイドRNAと複合体を形成させた際に依然として標的核酸に結合するような特定のアミノ酸置換を含むCas9ポリペプチドは、「デッド」Cas9または「dCas9」と呼ばれる。場合によっては、「デッド」Cas9タンパク質は、標的二本鎖核酸の相補鎖及び非相補鎖の両方を切断する能力が低下している。例えば、「ヌクレアーゼ欠損」Cas9は、機能性RuvCドメインを欠き(すなわち、標的二本鎖DNAの非相補鎖を切断しない)、また機能性HNHドメインを欠く(すなわち、標的二本鎖DNAの相補鎖を切断しない)。非限定的な例として、場合によっては、ヌクレアーゼ欠損Cas9タンパク質は、かかるポリペプチドが、標的核酸の相補鎖及び非相補鎖の両方に対する切断能が低くなる(例えば、切断しない)よう、配列番号40の残基D10及びH840(またはCas9のホモログの対応残基)に対応するアミノ酸位置に変異を有する(例えば、D10A及びH840A)。そのようなCas9タンパク質は、標的核酸(例えば、一本鎖または二本鎖の標的核酸)を切断する能力は低くなっているが、標的核酸と結合する能力は保持されている。標的核酸を切断することができないCas9タンパク質(例えば、RuvCドメイン及びHNHドメインの触媒ドメインでの、例えば、1つ以上の変異のため)は、「ヌクレアーゼ欠損Cas9」、「デッドCas9」または単に「dCas9」と呼ばれる。他の残基を変異させて上記の効果を達成する(すなわち、ヌクレアーゼ部分のいずれか一方を不活性化させる)ことができる。非限定的な例として、化膿レンサ球菌Cas9の残基D10、G12、G17、E762、H840、N854、N863、H982、H983、A984、D986、及び/またはA987(またはCas9ホモログの対応するアミノ酸)を変化させる(すなわち、置換する)ことができる。場合によっては、化膿レンサ球菌Cas9のD10、E762、H840、N854、N863、及びD986の2つ以上(またはCas9ホモログの対応するアミノ酸)を置換する。場合によっては、化膿レンサ球菌Cas9のD10及びN863(またはCas9ホモログの対応するアミノ酸)は、Alaで置換する。また、アラニン置換以外の変異も適している。
クラス2のCRISPR/Casエンドヌクレアーゼ(例えば、Cas9タンパク質;V型またはVI型のCRISPR/Casタンパク質;Cpf1タンパク質等)に結合し、かかる複合体を標的核酸内の特定の位置に指向させる核酸を、本明細書では「ガイドRNA」または「CRISPR/Casガイド核酸」または「CRISPR/CasガイドRNA」と呼ぶ。ガイドRNAは、指向セグメントを含めることにより標的特異性を複合体(RNP複合体)に与え、かかるセグメントには、標的核酸の配列に相補的なヌクレオチド配列であるガイド配列(本明細書では標的指向配列とも呼ばれる)が含まれる。
本開示は、a)上記のような対象rAAVビリオンと、b)薬理学的に許容される担体、希釈剤、添加剤、または緩衝剤とを含む医薬組成物を提供する。場合によっては、薬理学的に許容される担体、希釈剤、添加剤、または緩衝剤はヒトでの使用に好適である。
遺伝子産物の送達方法
本開示は、個体の神経細胞に遺伝子産物を送達する方法を提供し、かかる方法は、上記のように個体に対象rAAVビリオンを投与することを含む。遺伝子産物は、上記のようなポリペプチドもしくは干渉RNA(例えば、shRNA、siRNA等)、アプタマー、または部位特異的エンドヌクレアーゼ(例えば、RNA誘導型エンドヌクレアーゼ)であり得る。神経細胞に遺伝子産物を送達することにより神経疾患の治療を提供することができる。
対象方法を使用して治療され得る神経性疾患には、中枢神経系(CNS)の神経性の疾患及び障害、ならびに末梢神経系(PNS)の神経性の疾患及び障害が含まれる。
本開示は、上記のような対象変異アデノ随伴ウイルス(AAV)カプシドタンパク質をコードするヌクレオチド配列を含む単離された核酸を提供する。
上記の本願主題の実施形態などの態様は、単独でも、または1つ以上の他の態様もしくは実施形態と組み合わせても有益であり得る。上述の記載を限定するものではないが、1〜65の番号を付した特定の非限定的な開示態様を以下に記載する。本開示を読むと当業者には明らかとなるように、個々別々に番号付けされた態様の各々を使用しても、またはそれより前もしくは後の個々別々に番号付けされた態様と組み合わせてもいずれでもよい。これは、態様のそのような組み合わせをすべて支持することを意図しており、下記で明示的に提供する態様の組み合わせに限定するものではない。
組換え型アデノ随伴ウイルス(rAAV)ビリオンであって、
a)少なくとも3つの異なるAAV血清型に由来する、各セグメントが約50アミノ酸長〜約160アミノ酸長の少なくとも5つのセグメントを含み、かつ、i)神経幹細胞への感染力が、対応する親AAVカプシドタンパク質を含むかまたは野生型AAVカプシドを含む対照AAVビリオンによる神経幹細胞への感染力と比較して高い、ii)ニューロンへの感染力が、対応する親AAVカプシドタンパク質を含むかまたは野生型AAVカプシドを含む対照AAVビリオンによるニューロンへの感染力と比較して高い、iii)ヒトAAV中和抗体に対する耐性が、対応する親AAVカプシドタンパク質を含むかまたは野生型AAVカプシドを含む対照AAVビリオンが示す耐性と比較して高い、という特性のうち1つ以上を付与する、変異AAVカプシドタンパク質、及び
b)異種遺伝子産物をコードするヌクレオチド配列を含む異種核酸
を含む、前記組換え型アデノ随伴ウイルスビリオン。
前記変異AAVカプシドタンパク質は、N末端からC末端に向かって順に、第1のAAV血清型のアミノ酸1〜アミノ酸160に由来する約50アミノ酸長〜約160アミノ酸長の第1のセグメント、第2のAAV血清型のアミノ酸51〜アミノ酸320に由来する約50アミノ酸長〜約160アミノ酸長の第2のセグメント、第3のAAV血清型のアミノ酸101〜アミノ酸480に由来する約50アミノ酸長〜約160アミノ酸長の第3のセグメント、前記第2のAAV血清型のアミノ酸151〜アミノ酸640に由来する約50アミノ酸長〜約160アミノ酸長の第4のセグメント、及び前記第2のAAV血清型のアミノ酸201からC末端までのアミノ酸に由来する約50アミノ酸長〜約160アミノ酸長の第5のセグメントを含む、態様1に記載のrAAVビリオン。
前記第1のAAV血清型はAAV6である、態様2に記載のrAAVビリオン。
前記第2のAAV血清型はAAV9である、態様2に記載のrAAVビリオン。
前記第3のAAV血清型はAAV8である、態様2に記載のrAAVビリオン。
前記変異AAVカプシドタンパク質は、N末端からC末端に向かって順に、第1のAAV血清型のアミノ酸1〜アミノ酸160に由来する約50アミノ酸長〜約160アミノ酸長の第1のセグメント、第2のAAV血清型のアミノ酸51〜アミノ酸320に由来する約50アミノ酸長〜約160アミノ酸長の第2のセグメント、第3のAAV血清型のアミノ酸101〜アミノ酸480に由来する約50アミノ酸長〜約160アミノ酸長の第3のセグメント、前記第2のAAV血清型のアミノ酸151〜アミノ酸640に由来する約50アミノ酸長〜約160アミノ酸長の第4のセグメント、及び第4のAAV血清型のアミノ酸201からC末端までのアミノ酸に由来する約50アミノ酸長〜約160アミノ酸長の第5のセグメントを含む、態様1に記載のrAAVビリオン。
前記第1のAAV血清型はAAV6である、態様6に記載のrAAVビリオン。
前記第2のAAV血清型はAAV9である、態様6に記載のrAAVビリオン。
前記第3のAAV血清型はAAV8である、態様6に記載のrAAVビリオン。
前記第4のAAV血清型はAAV2である、態様6に記載のrAAVビリオン。
前記変異AAVカプシドタンパク質は、N末端からC末端に向かって順に、第1のAAV血清型のアミノ酸1〜アミノ酸160に由来する約50アミノ酸長〜約160アミノ酸長の第1のセグメント、第2のAAV血清型の約50アミノ酸長〜約160アミノ酸長の第2のセグメント、第3のAAV血清型の約50アミノ酸長〜約160アミノ酸長の第3のセグメント、前記第2のAAV血清型に由来する約50アミノ酸長〜約160アミノ酸長の第4のセグメント、前記第2のAAV血清型に由来する約50アミノ酸長〜約160アミノ酸長の第5のセグメント、第4のAAV血清型に由来する約50アミノ酸長〜約160アミノ酸長の第6のセグメント、前記第2のAAV血清型に由来する約50アミノ酸長〜約160アミノ酸長の第7のセグメント、及び前記第2のAAV血清型に由来する約50アミノ酸長〜約160アミノ酸長の第8のセグメントを含む、態様1に記載のrAAVビリオン。
前記第1のAAV血清型はAAV6である、態様11に記載のrAAVビリオン。
前記第2のAAV血清型はAAV9である、態様11に記載のrAAVビリオン。
前記第3のAAV血清型はAAV8である、態様11に記載のrAAVビリオン。
前記第4のAAV血清型はAAV2である、態様11に記載のrAAVビリオン。
前記変異AAVカプシドタンパク質は、N末端からC末端に向かって順に、第1のAAV血清型に由来する約50アミノ酸長〜約160アミノ酸長の第1のセグメント、第2のAAV血清型に由来する約50アミノ酸長〜約160アミノ酸長の第2のセグメント、第3のAAV血清型に由来する約50アミノ酸長〜約160アミノ酸長の第3のセグメント、前記第2のAAV血清型に由来する約50アミノ酸長〜約160アミノ酸長の第4のセグメント、第4のAAV血清型に由来する約50アミノ酸長〜約160アミノ酸長の第5のセグメント、前記第4のAAV血清型に由来する約50アミノ酸長〜約160アミノ酸長の第6のセグメント、前記第2のAAV血清型に由来する約50アミノ酸長〜約160アミノ酸長の第7のセグメント、及び前記第2のAAV血清型に由来する約50アミノ酸長〜約160アミノ酸長の第8のセグメントを含む、態様1に記載のrAAVビリオン。
前記第1のAAV血清型はAAV6である、態様16に記載のrAAVビリオン。
前記第2のAAV血清型はAAV9である、態様16に記載のrAAVビリオン。
前記第3のAAV血清型はAAV8である、態様16に記載のrAAVビリオン。
前記第4のAAV血清型はAAV2である、態様16に記載のrAAVビリオン。
前記rAAVビリオンは、対応する親AAVカプシドタンパク質を含むかまたは野生型AAVカプシドを含む前記対照AAVビリオンによる神経幹細胞への感染力と比較して、少なくとも5倍高い神経幹細胞への感染力を示す、態様1に記載のrAAVビリオン。
前記対照AAVビリオンはAAV9である、態様21に記載のrAAVビリオン。
前記対照AAVビリオンはAAV2である、態様21に記載のrAAVビリオン。
前記rAAVビリオンは、対応する親AAVカプシドタンパク質を含むかまたは野生型AAVカプシドを含む前記対照AAVビリオンによる神経幹細胞への感染力と比較して、少なくとも10倍高い神経幹細胞への感染力を示す、態様1に記載のrAAVビリオン。
前記対照AAVビリオンはAAV9である、態様24に記載のrAAVビリオン。
前記対照AAVビリオンはAAV2である、態様24に記載のrAAVビリオン。
前記変異AAVカプシドタンパク質は、配列番号1に記載の(及び図8に示す)アミノ酸配列に対するアミノ酸配列同一性が少なくとも約90%であるアミノ酸配列を含む、態様1に記載のrAAVビリオン。
前記変異AAVカプシドタンパク質は、配列番号1に記載の(及び図8に示す)アミノ酸配列に対するアミノ酸配列同一性が少なくとも約95%であるアミノ酸配列を含む、態様1に記載のrAAVビリオン。
前記変異AAVカプシドタンパク質は、配列番号1に記載の(及び図8に示す)アミノ酸配列を含む、態様1に記載のrAAVビリオン。
前記変異AAVカプシドタンパク質は、配列番号2に記載の(及び図9に示す)アミノ酸配列に対するアミノ酸配列同一性が少なくとも約90%であるアミノ酸配列を含む、態様1に記載のrAAVビリオン。
前記変異AAVカプシドタンパク質は、配列番号2に記載の(及び図9に示す)アミノ酸配列に対するアミノ酸配列同一性が少なくとも約95%であるアミノ酸配列を含む、態様1に記載のrAAVビリオン。
前記変異AAVカプシドタンパク質は、配列番号2に記載の(及び図9に示す)アミノ酸配列を含む、態様1に記載のrAAVビリオン。
前記変異AAVカプシドタンパク質は、ヒトAAV中和抗体に対し、対応する親AAVカプシドタンパク質を含むかまたは野生型AAVカプシドを含む前記対照AAVビリオンが示す耐性と比較して高い耐性を示す、態様1に記載のrAAVビリオン。
前記対照AAVビリオンはAAV9である、態様34に記載のrAAVビリオン。
前記対照AAVビリオンはAAV2である、態様34に記載のrAAVビリオン。
前記変異AAVカプシドタンパク質は、ヒトAAV中和抗体に対し、対応する親AAVカプシドタンパク質を含むかまたは野生型AAVカプシドを含む前記対照AAVビリオンが示す耐性と比較して少なくとも約1.5倍高い耐性を示す、態様1に記載のrAAVビリオン。
前記変異AAVカプシドタンパク質は、ヒトAAV中和抗体に対し、対応する親AAVカプシドタンパク質を含むかまたは野生型AAVカプシドを含む前記対照AAVビリオンが示す耐性と比較して少なくとも約3倍高い耐性を示す、態様1に記載のrAAVビリオン。
前記変異AAVカプシドタンパク質は、ヒトAAV中和抗体に対し、対応する親AAVカプシドタンパク質を含むかまたは野生型AAVカプシドを含む前記対照AAVビリオンが示す耐性と比較して少なくとも約5倍高い耐性を示す、態様1に記載のrAAVビリオン。
前記変異AAVカプシドタンパク質は、ヒトAAV中和抗体に対し、対応する親AAVカプシドタンパク質を含むかまたは野生型AAVカプシドを含む前記対照AAVビリオンが示す耐性と比較して少なくとも約10倍高い耐性を示す、態様1に記載のrAAVビリオン。
前記神経幹細胞は脳室下帯由来である、態様1に記載のrAAVビリオン。
前記プルキンエ細胞は小脳由来である、態様1に記載のrAAVビリオン。
前記遺伝子産物は、干渉RNAまたはアプタマーである、態様1〜41のいずれか1態様に記載のrAAVビリオン。
前記遺伝子産物はポリペプチドである、態様1〜41のいずれか1態様に記載のrAAVビリオン。
前記ポリペプチドは、神経保護ポリペプチド、血管新生阻害ポリペプチド、神経幹細胞の分化を誘導するポリペプチド、または神経幹細胞の機能を高めるポリペプチドである、態様43に記載のrAAVビリオン。
前記ポリペプチドは、セレブロライシン、ラミニン−IKVAV、cripto、下垂体アデニル酸シクラーゼ活性化ポリペプチド、神経成長因子、脳由来神経栄養因子、グリア由来神経栄養因子、線維芽細胞増殖因子2、ニュールツリン、毛様体神経栄養因子、上皮成長因子、X連鎖アポトーシス抑制因子、またはソニック・ヘッジホッグである、態様43に記載のrAAVビリオン。
前記ポリペプチドはゲノム編集酵素である、態様43に記載のrAAVビリオン。
前記ゲノム編集酵素は、Cas9ポリペプチド、ジンクフィンガーヌクレアーゼ、TALEN、または酵素的に不活性なII型CRISPR/Casポリペプチドである、態様46に記載のrAAVビリオン。
前記ポリペプチドは、II型CRISPR/Casポリペプチド、V型CRISPR/Casポリペプチド、及びVI型CRISPR/Casポリペプチドから選択されるRNA誘導型エンドヌクレアーゼである、態様47に記載のrAAVビリオン。
前記遺伝子産物は、RNA誘導型エンドヌクレアーゼ及びガイドRNAである、態様1〜41のいずれか1態様に記載のrAAVビリオン。
a)態様1〜49のいずれか1態様に記載の組換え型アデノ随伴ウイルスビリオン、及びb)薬理学的に許容される添加剤を含む、医薬組成物。
個体の神経幹細胞に遺伝子産物を送達する方法であって、態様1〜49のいずれか1態様に記載の組換え型アデノ随伴ウイルス(rAAV)ビリオンまたは態様50に記載の組成物を前記個体に投与することを含む、前記方法。
前記投与は、頭蓋内注射、脳室内注射、髄腔内注射、大槽内注射、または静脈内注射による、態様51に記載の方法。
前記遺伝子産物は、短鎖干渉RNAまたはアプタマーである、態様51に記載の方法。
前記遺伝子産物はポリペプチドである、態様51に記載の方法。
前記ポリペプチドは、神経保護ポリペプチド、血管新生阻害ポリペプチド、または神経幹細胞の機能を高めるポリペプチドである、態様43に記載の方法。
前記ポリペプチドは、セレブロライシン、ラミニン−IKVAV、cripto、下垂体アデニル酸シクラーゼ活性化ポリペプチド、神経成長因子、脳由来神経栄養因子、グリア由来神経栄養因子、線維芽細胞増殖因子2、ニュールツリン、毛様体神経栄養因子、上皮成長因子、X連鎖アポトーシス抑制因子、芳香族L−アミノ酸脱炭酸酵素、グルタミン酸脱炭酸酵素、トリペプチジルペプチダーゼ、アスパルトアシクラーゼ(aspartoacylase)、またはソニック・ヘッジホッグである、態様44に記載のrAAVビリオン。
前記ポリペプチドはゲノム編集酵素である、態様54に記載の方法。
前記ゲノム編集酵素は、Cas9ポリペプチド、ジンクフィンガーヌクレアーゼ、TALEN、または酵素的に不活性なII型CRISPR/Casポリペプチドである、態様57に記載の方法。
前記ポリペプチドは、II型CRISPR/Casポリペプチド、V型CRISPR/Casポリペプチド、及びVI型CRISPR/Casポリペプチドから選択されるRNA誘導型エンドヌクレアーゼである、態様57に記載の方法。
前記遺伝子産物は、RNA誘導型エンドヌクレアーゼ及びガイドRNAである、態様51に記載の方法。
神経性障害を治療する方法であって、態様1〜49のいずれか1態様に記載の組換え型アデノ随伴ウイルス(rAAV)ビリオンまたは態様50に記載の組成物の有効量を、それを必要とする個体に投与することを含む、前記方法。
前記神経性障害は、脊髄小脳失調症、ハンチントン病、パーキンソン病、アルツハイマー病、リソソーム蓄積障害、フリードライヒ運動失調症、神経膠芽腫、レット症候群、前頭側頭型認知症、またはてんかんである、態様62に記載の方法。
変異アデノ随伴ウイルス(AAV)カプシドタンパク質をコードするヌクレオチド配列を含む単離された核酸であって、
前記変異AAVカプシドタンパク質は、少なくとも3つの異なるAAV血清型に由来する、各セグメントが約50アミノ酸長〜約160アミノ酸長の少なくとも5つのセグメントを含み、かつ、i)神経幹細胞への感染力が、対応する親AAVカプシドタンパク質を含むかまたは野生型AAVカプシドを含む対照AAVビリオンによる神経幹細胞への感染力と比較して高い、ii)ニューロンへの感染力が、対応する親AAVカプシドタンパク質を含むかまたは野生型AAVカプシドを含む対照AAVビリオンによるニューロンへの感染力と比較して高い、iii)ヒトAAV中和抗体に対する耐性が、対応する親AAVカプシドタンパク質を含むかまたは野生型AAVカプシドを含む前記対照AAVビリオンが示す耐性と比較して高い、という特性のうち1つ以上を付与する、前記核酸。
態様63に記載の核酸を含む、単離された遺伝子改変宿主細胞。
変異アデノ随伴ウイルス(AAV)カプシドタンパク質であって、少なくとも3つの異なるAAV血清型に由来する、各セグメントが約50アミノ酸長〜約160アミノ酸長の少なくとも5つのセグメントを含み、かつ、i)神経幹細胞への感染力が、対応する親AAVカプシドタンパク質を含むかまたは野生型AAVカプシドを含む対照AAVビリオンによる神経幹細胞への感染力と比較して高い、ii)ニューロンへの感染力が、対応する親AAVカプシドタンパク質を含むかまたは野生型AAVカプシドを含む対照AAVビリオンによるニューロンへの感染力と比較して高い、iii)ヒトAAV中和抗体に対する耐性が、対応する親AAVカプシドタンパク質を含むかまたは野生型AAVカプシドを含む対照AAVビリオンが示す耐性と比較して高い、という特性のうち1つ以上を付与する、前記変異アデノ随伴ウイルスカプシドタンパク質。
材料及び方法
特に記載がない限り、本明細書に記載の実施例で提示されている結果には一般に以下の材料及び方法が適用される。
キメラAAVのライブラリーは、複数の系統分岐群を表す(例えば、Gao et al.(2004)J.Virol.78を参照のこと)SCHEMAスコアリング関数及びRASPPアルゴリズム(例えば、Voigt et al.(2002)Nature Struct.Mol.Biol.6、及びEndelman et al.(2004)PEDS 17を参照のこと)を使用して設計されたが、これは、さまざまな受容体結合特性を有しており(例えば、Asokan et al.(2012)Mol.Ther.20を参照のこと)、臨床において多少の効果が享受された(例えば、Kotterman et al.(2015)Annu.Rev.Biomed.Eng.17を参照のこと)。MUSCLE(例えば、Edgar et al.(2004)Nucleic Acids Res.32を参照のこと)を使用してAAV2、4、5、6、8、及び9のアミノ酸配列を整列させ、親配列アラインメントを生成した。多量体AAVカプシドにおけるサブユニットアミノ酸内の接触及びサブユニットアミノ酸同士の接触の両方が考慮されるようSCHEMAを変更したが、ここで、一対の残基が接触しているのは、それらに水素以外の原子が4.5オングストローム以内に含有されている場合である。AAV2(1LP3)、AAV4(2G8G)、AAV5(3NTT)、AAV6(3OAH)、AAV8(2QA0)、及びAAV9(3UX1)の結晶構造を使用して、接触残基の位置を計算した。最終接触マップは、これらの6つの親構造の少なくとも50%で接触している残基対を含有した。ライブラリーの高い多様性を達成するため、6つの交差を含有するライブラリーをカプシドの結晶化領域内に設計するべきであり、7つ目の交差を、その位置での組換えが成功している先の例に基づき、位置128の非結晶化VP1領域(アミノ酸1〜アミノ酸216)に設計する。例えば、Excoffon et al.(2009)Proc.Natl.Acad.Sci.U.S.A.106を参照のこと。6種の親血清型由来のカプシドタンパク質ブロックを8つ含有するライブラリーから、理論上、160万(68)を越えるキメラ変異型というライブラリー多様性が得られる。キメラカプシドのSCHEMA破壊<E>は、親配列のいずれにも存在しない、アミノ酸の新しい組み合わせを含有する接触の数であった。キメラカプシドの<m>は、最も近い親配列からの変異の数であった。
RASPPアルゴリズムを使用して、平均構造破壊<E>と平均配列多様性<m>のバランスのとれたライブラリーを設計した。SCHEMAスコアリング関数をさらに変更して、ライブラリー構築のコンビナトリアルゴールデンゲートアセンブリの影響を受けやすい交差位置について検索したが、これには、すべてのAAV親配列を通じて保存されている4つのヌクレオチド領域を要した。可能な交差部位の数を増やして、より大きい配列空間をインシリコで探索するために、4つのヌクレオチド領域は、ライブラリーアセンブリ中はサイレント変異させて、すべての親配列で同一となるように含めた。ライブラリー設計では、最小許容配列ブロック長は20アミノ酸及び最大長さは250アミノ酸を検討した。最終ライブラリーは、その<E>が低いもの、その均一なブロックサイズ、及びカプシドの主要構造特徴の組み換えに基づいて選択した。
図2.
II型の制限酵素BsaIを用いたコンビナトリアルゴールデンゲートクローニングを容易に行うために、pBluescript SK(+)、AAV2、4、5、6、8、及び9に見られるBsaI認識部位をすべて、部位特異的変異導入のQuikChangeによりサイレント変異させた。
シャッフルしたブロックそれぞれに相当する48のDNA配列を、DNAアセンブリ設計オートメーションソフトウェアのj5で設計したPCRプライマーを使用して、親cap遺伝子からPCR増幅させた。例えば、Hillson et al.(2012)ACS Synth.Biol.1を参照のこと。
プライマーは、ブロック接合部にサイレント変異を組み込んでpBluescriptベクター骨格へのゴールデンゲートクローニングを促進するよう設計された。ゴールデンゲート反応物をエレクトロコンピテントなDH10B大腸菌に形質転換し、理論上の多様性である68クローンより大きなライブラリーサイズを達成した。その後、ライブラリーを、制限酵素HindIII及びNotIを使用してpBluescriptからAAVパッケージングプラスミドpSub2FloxCapにサブクローニングした。
構成体設計及びcap増幅に使用したPCRプライマーは図2に提示されている。pSub2RepKO及びpRepヘルパーを使用した。AAVパッケージングプラスミドpSub2でrepをノックアウトさせたpSub2RepKO(例えば、Maheshri et al.(2006)Nature Biotechnol.24を参照のこと)を、SgraI及びBamHIを用いた消化、クレノウ反応、及び平滑末端ライゲーションにより作製した。AAVパッケージングの際にRepをトランスで供給するために使用するpRepHelperを、PmeI及びBsmIを用いたpAAV2/rh10の連続消化、クレノウ反応、及び平滑末端ライゲーションにより創製した。lox66をcapの5’部位に挿入するため、プライマーBglIIFwd及びBglIIRevを使用した部位特異的変異導入により、pSub2RepKOに固有BglII部位を導入した。オリゴヌクレオチドLox66Fwd及びLox66Revをアニールし、pSub2RepKOのBglII部位及びHindIII部位に連結してpSub2Lox66を形成した。lox71をcapの3’部位に挿入するため、プライマーXhoIFwd/XhoIRev及びKpnIFwd/KpnIRevをそれぞれ用いた部位特異的変異導入により、固有XhoI部位及び固有KpnI部位をpSub2Lox66に導入した。オリゴヌクレオチドSOELox71Fwd及びSOELox71Revをオーバーラップエクステンションでスプライスして組み立て、Lox71Fwd及びLox71Revを用いて増幅した。得られる断片及びpSub2Lox66をXhoI及びKpnIで消化させ、連結してpSub2Floxを創製した。この選択で使用するpSub2Flox及びAAV capライブラリーをHindIII及びNotIで消化させ、連結してウイルスパッケージング用pSub2FloxCapライブラリーを産生した。
HEK293T細胞をAmerican Type Culture Collection(Manassas,VA)から入手し、10%ウシ胎児血清(Invitrogen)及び1%ペニシリン/ストレプトマイシン(Invitrogen)添加ダルベッコ改変イーグル培地(DMEM、Gibco)で37℃、5%CO2で培養した。先にKoerber et al.(2008)Mol.Ther.16、及びMaheshri et al.(2006)Nature Biotechnol.24に記載のように、サイトメガロウイルス初期エンハンサー/ニワトリベータアクチン(CAG)プロモーターの制御下で緑色蛍光タンパク質(GFP)もしくはCreリコンビナーゼの発現を誘導する、AAVライブラリーまたは自己相補的組換え型AAVベクターを、HEK293T細胞にパッケージングした。簡単に言えば、一過性トランスフェクション、イオジキサノールの密度勾配遠心分離による精製、及びAmiconでのろ過によるリン酸緩衝食塩水(PBS)へのバッファー交換を、3回繰り返してAAVベクターを作製した。DNase耐性ウイルスゲノム力価を、Biorad iCycler(Bio−Rad、Hercules,CA)を使用して定量的リアルタイムPCRで測定した。
7週齢のGFAP−Cre73.12(Jackson Laboratory Stock 012886)、C57BL/6J(Jackson Laboratory Stock000664)、またはAi9 tdTomatoマウス(Jackson Laboratory Stock 007909)をイソフルランで麻酔し、定位固定装置に置いた。切開を行って頭蓋骨を露出させ、ドリルで注入用の穴を作製した。ライブラリー選択では、先に記載の100のように、AAVライブラリーの等モル混合物(1×1010ウイルスゲノム/μl)5マイクロリットルを、GFAP−Creマウス(n=3)の右側脳室内、座標がブレグマより0.05mm後ろ、1.0mm側方、深さ2.5mmにハミルトンシリンジを使用して定位的に注入した。マウス脳アトラス(Franklin and Paxinos,2007)を使用して注入座標を選択し、0.1%FastGreen色素(Sigma)を用いて試験注入をしてから調整した。試験期間を通しての注入精度は、脈絡叢内及び対側の側脳室周辺のレポーター発現により確認された。注入から3週間後にマウスを屠殺し、脳組織を採取した。乳鉢及び乳棒を使用してドライアイス上で注射部位の対側半球を均質化した。プロテアーゼK(New England Biolabs)及びRNase A(ThermoFisher)を添加したHirt溶解バッファー中で均質化組織を55℃にて3時間消化させ、先のArad et al.(1998)BioTechniques 24に記載のようなHirt法を使用して染色体外DNAを単離した。PCRプライマーCap_ISF及びCap_Rを使用して逆位capを増幅させ、プライマーCap_NSF及びCap_Rで非逆位capを特異的に増幅させた。逆位capの増幅が困難な場合はネステッドPCRでプライマーInternal_Cap_ISF及びInternal_Cap_Rを使用してよい。選択を3ラウンド行った後、サンガー法による配列決定(UC Berkeley DNA Sequencing Facility)でカプシド配列を決定し、優性変異体をHindIII及びNotIで消化し、pXX2Notに連結して組換え型AAVパッケージングに供した。
マウスを、ケタミン100mg/kg及びキシラジン10mg/kgの腹腔内注射により麻酔し、0.9%生理食塩水で経心腔的灌流を行った後、4%パラホルムアルデヒドで経心腔的灌流を行った。脳を4%パラホルムアルデヒド中で4℃にて一晩、灌流後固定を行い、PBSで洗浄し、脳が沈んでくるまで30%ショ糖中で保存した。冠状断または矢状断での連続切片を、Series 8000スライディングミクロトーム(Bright)で厚さ40μmにカットして作製し、使用時まで凍結保護剤中で−20℃にて保存した。浮遊切片をPBS中で3回洗浄し、ブロッキング溶液(10%ロバ血清、1% Triton X−100含有PBS)と共に室温で2時間インキュベートし、一次抗体を用いてブロッキング溶液中で4℃にて72時間染色した。本試験では以下の一次抗体を使用した:マウス抗カルビンジン(1:2000;Abcam、ab82812)、ウサギ抗GFP(1:1000;Life Technologies、A−11122)、ヤギ抗GFAP(1:750;Abcam、ab53554)、モルモット抗DCX(1:1000、EMD Millipore、AB2253)、ラット抗VCAM1(1:50;EMD Millipore、MAB2627)、ニワトリ抗GFAP(1:750;Abcam、ab4674)、ラット抗BrdU(1:750;Abcam、ab6326)、及びウサギ抗tdTomato(1:750、Rockland、600−401−379)。PBS中で3回洗浄した後、切片を二次抗体と共に室温で2時間インキュベートし、DAPI(Thermo Fisher)で10分間染色した。染色した切片をPBS中で3回洗浄し、VectaShield HardSet Antifade Mounting Medium(Vector Laboratories)を使用してスライドガラス上に封入した。
Zeiss Axio Scan.Z1または共焦点Zeiss LSM 880 NLO AxioExaminer(UC Berkeley Molecular Imaging Center)を使用して画像を取得した。画像解析はすべて、同等の設定で取得した原画像で実施した。データは、平均±SEMとして提示され、統計的有意性は両側スチューデントのt検定により確証された。
特に断りのない限り、細胞株はすべて、10%ウシ胎児血清(Invitrogen)及び1%ペニシリン/ストレプトマイシン(Invitrogen)を添加したDMEM(Gibco)で37℃、5%CO2にて培養した。SCH9、SCH2、及び野生型AAV2のヘパリン親和性を、先のJang et al.(2011)Mol.Ther.19に記載のように決定した。1ml HiTrapヘパリンカラム(GE Healthcare Sciences)を、150mM NaCl及び50mM Tris、pH7.5で平衡化した。1×1011の精製ウイルスゲノム粒子をカラムに担持させ、50mMのNaClを最終濃度950mMまで段階的に増加させて溶出を行い、その後、1M NaClで洗浄した。各溶出画分を使用してHEK293T細胞を感染させ、感染から48時間後、Guava EasyCyte 6HTフローサイトメーター(EMD/Millipore)(UC Berkeley Stem Cell Center,Berkeley,CA)を使用してGFP陽性細胞の割合を定量化した。
6つの天然の血清型−AAV2、4、5、6、8、及び9を組み換えたキメラAAVライブラリーを設計した。
図1.
設計パラメータを指定した後、RASPPによる方法(最短経路問題としての組換え)(例えば、Endelman et al.(2004)PEDS 17を参照のこと)を適用して、変異レベルの範囲にわたり、最も破壊の少ない160のライブラリー設計(7つの交差位置からなる各種セット)を短時間で同定した。これらの設計それぞれについて、平均ライブラリー破壊スコア<E>及び最も近い親血清型に対する導入されたアミノ酸変異数<m>を計算し(図1A)、すべてのRASPP設計の交差位置を図1Bに提示した。いくつかの理由から、カプシドの結晶化領域のサブユニットあたりの平均破壊スコア<E>が59、平均変異数<m>が82である最終設計(図1A−C)を選択した。第1に、この設計は、<E>における極小を高レベルの変異で表すRASPPライブラリークラスター内にあった(図1A)。第2に、選択した設計では、表面露出ループ及び天然のAAV血清型の進化において最も可変な領域を表す超可変領域など、カプシドの主要な構造的特徴がシャッフルされていた(図1C)。接触に富むこれらの領域内での組換えにより大きな破壊がもたらされたが、新規かつ興味深い機能を有するAAVキメラを生じさせる可能性も高かった。例えば、ブロック5とブロック6を合わせることにより有意に低い破壊スコアの達成が可能と考えられたが、そのようにすることで、単一親配列由来の表面露出ループ領域を有するカプシドが生じることが考えられた。最終的に、ブロックサイズの分布が比較的均等に得られることから、このセットの交差位置を選択した。20〜250アミノ酸の許容ブロックサイズ範囲が考慮されるようRASPPをプログラムした。<E>が最も低い設計の大部分には2つの長ブロック(ブロック3及びブロック4で175アミノ酸超)、それに続く一連の短ブロック(ブロック5〜7で30アミノ酸未満)(図1B)が含有されていた。対照的に、選択された交差位置セット(図1C)では、ブロックサイズの分布がさらに均等に得られ、これにより、多様性に限界がある親配列の少数領域内に交差を限定する場合とは対照的に、カプシド全体のシャッフリングが保証された。
NSCを特異的に指向させるため、SVZのNSCを感染させたAAV変異体の陽性選択を誘導するよう、インビボのCre依存的指向進化及び選択法を設計した。本試験の期間中、概念上は似ているが別個のCre依存的システムが報告された。Deverman et al.(2016)Nature Biotechnol.34を参照のこと。
図6.
AAV cap遺伝子の選択的回収を仲介するよう、cap遺伝子を一対のloxP部位で挟むことによりCre発現の細胞型特異性を形成させた。Creを発現している細胞をAAVに感染させて2本目のAAVゲノムを合成させ、floxedになっていたcapの逆位を生じさせ、逆位になった遺伝子鋳型でのみフォワードプライマーとリバースプライマーの対として機能するPCRプライマーを使用して、Cre逆位cap遺伝子を脳組織から選択的に回収した(図6A、B)。変異loxP部位であるlox66及びlox71 40を用いて、Cre組換えの平衡を一方向性逆位に誘導した。最初、loxP部位をcapの3’UTRに挿入したが、その際、Cre依存的回収に使用するリバースプライマー用の標的配列を含有した短いスタッファー配列にloxP部位を隣接させた。図7に示すように、細菌プラスミドの増殖中、組換えは少量出現し、リコンビナーゼ欠損大腸菌のSure2でも低かった。インビボ選択の際、こうした望ましくない逆位cap回収がないようにするため、loxP部位がcapに隣接するよう位置を決め直し、ベクタープラスミドライブラリーの細菌増殖の際の人工的逆位が、ウイルスタンパク質をコードしない逆位cap配列を生じさせて、293細胞にそれ以上パッケージングが行われないようにしたが、これは、別の設計には含まれていない規定である。例えば、Deverman et al.(2016)Nature Biotechnol.34を参照のこと。loxP部位をcap遺伝子に隣接させて挿入したことにより、rep遺伝子の読み枠が変化したことに留意されたい。したがって、repの翻訳開始コドンを除去し、cap発現を誘導したウイルスプロモーターは維持した(図6A)が、その代わりに、repをコードする別個のヘルパーを一過性にトランスフェクションすることにより、ウイルスパッケージングにrepをトランスで供給した。ウイルスパッケージングプラスミドに対するこれらの修飾により、qPCRで定量化したAAVウイルスゲノムの収量は高かった(図6C)。
capのCre依存的回収を確認した後、6つのAAVライブラリーの等モル混合物を使用してインビボ選択を開始し、ライブラリーの各々は、106〜107の特有の変異体、すなわち、(i)新規SCHEMA AAV、(ii)エラーが起こりやすいAAV9、(iii)祖先AAV(例えば、Santiago−Ortiz et al.(2015)Gene Ther.22を参照のこと)、(iv)DNase Iにより消化し、AAV1、2、4、5、6、8、及び9を再構築することによる、シャッフルAAVの作製(例えば、Koerber et al.(2008)Mol.Ther.16を参照のこと)、(v)エラーが起こりやすいAAV2(例えば、Koerber et al.(2006)Nature Protoc.1を参照のこと)、及び(vi)アミノ酸588に7merペプチドの挿入があるAAV2(例えば、Muller et al.(2003)Nature Biotechnol.21を参照のこと)を含有した。ライブラリーiii〜viは、これまでの本発明者らの指向進化選択では高感染性クローンを与え、進化的なSCHEMAライブラリー競争をした。例えば、Dalkara et al.(2013)Sci.Transl.Med.5;Tervo et al.(2016)Neuron;Steines et al.(2016)JCI Insight 1;Koerber et al.(2008)Mol.Ther.16;及びSantiago−Ortiz et al.(2015)Gene Ther.22を参照のこと。ライブラリーを合わせて成体GFAP−Creマウス(n=3)の右側脳室内に脳室内投与で注入し、両半球のSVZ全体にわたりNSCに形質導入した。対照的に、SVZへの直接注入は局所組織に対しより破壊的であり、同量の組織体積を網羅するためには複数注入を要し得たであろう。
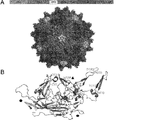
SCH9の3次元構造モデルにより、AAV9はカプシド表面のループVR−IVに、AAV2はループV〜ループVIIIに、AAV8は5回回転対称軸の細孔構造に示された。これらの興味深い特徴、及び選択プールに対するその優位性に基づき、SCH9のインビボ特性解析を行った。
SVZでのSCH9の形質導入特性を評価するため、自己相補的CAG−GFPカセットを保持するrAAVを首尾よくパッケージングし(組換え型AAVパッケージングの収量は図12に報告されている)、成体C57BL/6Jマウスの右側脳室に送達した。AAV9はCNSで広く使用されており、髄腔内注入後、脳脊髄液(CSF)から脳実質へ形質導入する能力があることから、AAV9を基準にSCH9を評価した。例えば、Samaranch et al.(2012)Hum.Gene Ther.23、及びSchuster et al.(2014)Front.Neuroanat.8を参照のこと。さらに、天然血清型のうち、AAV9がSCH9に最も近縁の配列である。
注入から4週間後に対側半球の形質導入を解析したところ、GFP発現は脳室周辺領域に主に関連しており、その強度は脳室下帯で最も強かった(図13A)。形質導入効率を、GFP発現強度、及びGFP陽性であったSVZの総体積の両方によって評価した。SCH9では、組込みGFPの蛍光強度は24倍高く、またGFPは、AAV9と比べて12倍大きいSVZ形質導入体積で発現した(図13B、C)。初回特性解析として、脳室下帯でGFP/GFAP/VCAM1陽性成体神経幹細胞にSCH9により形質導入した(図13D)。
標的細胞型の感染を高めるカプシド変異は脳の他の領域での形質導入を同時に改善することができる。
脳室内注入の後のSCH9による形質導入は主にSVZに関連しているが、脳脊髄液中を循環するベクターに直接接近可能な脳の領域である小脳のプルキンエ細胞において、レポーター発現の増加も観察された(図14A)。プルキンエ細胞は、脊髄小脳失調症など神経変性疾患に対する遺伝子治療の主要標的である。例えば、Orr et al.(2012)J.Cell Biol.197を参照のこと。CellProfilerで定量化したところ、SCH9−Creの送達によりtdTomatoレポーター発現はAAV9−Creよりも12.2倍強く活性化し、カルビンジン陽性領域は9.3倍広い領域を占めた(図14B、C)。
小脳への遺伝子送達に最も一般的に使用される血清型であるAAV1の形質導入パターンとSCH9の形質導入パターンを、右半球深部小脳核内への片側注入の後、比較した。両ベクターとも、同側半球の小脳全体にわたりプルキンエ細胞への強い形質導入を支持したことから、SCH9は逆方向に輸送され得ることが示された。
SCH9の感染特性が有望であることから、その複数の親血清型の受容体結合能を調節することによりSCH9に選択的長所を付与し得るか否かを決定するため、そのキメラとしての性質を次に調べた。SCH9のブロック6はAAV2カプシドのヘパリン結合ポケットを含有した。例えば、Kern et al.(2003)J.Virol.77を参照のこと。さらに、ブロック2及びブロック5は、AAV9のガラクトース結合残基D271、N272、N470、及びY446を含有し、ブロック6は残基W503を保存していた。例えば、Bell et al.(2012)J.Virol.86を参照のこと。対照的に、SCH2は、ブロック5でAAV9がAAV2で置換されたため主要ガラクトース結合残基を2つ欠いた。
両SCHEMA変異体のヘパリン親和性がAAV2に匹敵することを示すため、最初にクロマトグラフィーを利用し、これにより、ヘパリンポケット外側のキメラ配列構成は結合親和性に有意な影響を与えないことが示された(図16A)。次に、末端ガラクトース残基及びHSPGを細胞表面に発現するCHO−Lec2細胞を感染させ、ヘパラン硫酸プロテオグリカン(HSPG)とガラクトースとを二重に利用する可能性を評価した。先にShen et al.(2013)J.Biol.Chem.288に記載されるように、Erythrina cristagalliレクチン(ECL)を付加すると末端ガラクトースは遮断されたが、ウイルスを可溶性ヘパリンとインキュベーションすると、HSPGを細胞への進入に利用するAAV血清型を競合的に阻害した。予測通り、AAV2及びAAV9の対照ベクターはそれぞれ、HSPG及びガラクトースを利用した。興味深いことに、SCH2はもっぱらHSPG依存的であったが、SCH9はHSPG及びガラクトースの双方を使用することができたため、実際には、細胞へ形質導入しないよう双方を遮断する必要があった(図16B)。SCH2及びSCH9の異なるグリカン結合特性を特徴付けた後、天然のAAV血清型でAAV感染に重要な、新たに記載されたタンパク質受容体であるAAVRの利用を両変異体が保持したか否かを決定するため、これらの変異体を調べた。例えば、Pillay et al.(2016)Nature 530を参照のこと。
SCH2、SCH9、及びAAV2対照はいずれも、明らかにAAVRに依存していた。
Claims (65)
- 組換え型アデノ随伴ウイルス(rAAV)ビリオンであって、
(a)少なくとも3つの異なるAAV血清型に由来する、各セグメントが約50アミノ酸長〜約160アミノ酸長を有する少なくとも5つのセグメントを含み、かつ、
(i)野生型AAVビリオンを含む対照AAVビリオンによる神経幹細胞への感染力と比較して前記神経幹細胞への感染力が高い、
(ii)野生型AAVビリオンを含む対照AAVビリオンによる神経細胞への感染力と比較して前記神経細胞への感染力が高い、
(iii)野生型AAVカプシドを含む対照AAVビリオンが細胞障壁を通過する能力と比較して前記細胞障壁を通過する能力が高い、
(iv)ヒトAAV中和抗体に対する耐性が、野生型AAVカプシドを含む対照AAVビリオンが示す耐性と比較して高い、
という特性のうち1つ以上を付与する、変異AAVカプシドタンパク質、及び
(b)異種遺伝子産物をコードするヌクレオチド配列を含む異種核酸
を含む、前記組換え型アデノ随伴ウイルスビリオン。 - 前記変異AAVカプシドタンパク質は、N末端からC末端に向かって順に、
(a)第1のAAV血清型のアミノ酸1〜アミノ酸160に由来する約50アミノ酸長〜約160アミノ酸長を有する第1のセグメント、
(b)第2のAAV血清型のアミノ酸51〜アミノ酸320に由来する約50アミノ酸長〜約160アミノ酸長を有する第2のセグメント、
(c)第3のAAV血清型のアミノ酸101〜アミノ酸480に由来する約50アミノ酸長〜約160アミノ酸長を有する第3のセグメント、
(d)前記第2のAAV血清型のアミノ酸151〜アミノ酸640に由来する約50アミノ酸長〜約160アミノ酸長を有する第4のセグメント、及び
(e)前記第2のAAV血清型のアミノ酸201からC末端までのアミノ酸に由来する約50アミノ酸長〜約160アミノ酸長を有する第5のセグメント
を含む、請求項1に記載のrAAVビリオン。 - 前記第1のAAV血清型はAAV6である、請求項2に記載のrAAVビリオン。
- 前記第2のAAV血清型はAAV9である、請求項2に記載のrAAVビリオン。
- 前記第3のAAV血清型はAAV8である、請求項2に記載のrAAVビリオン。
- 前記変異AAVカプシドタンパク質は、N末端からC末端に向かって順に、
(a)第1のAAV血清型のアミノ酸1〜アミノ酸160に由来する約50アミノ酸長〜約160アミノ酸長を有する第1のセグメント、
(b)第2のAAV血清型のアミノ酸51〜アミノ酸320に由来する約50アミノ酸長〜約160アミノ酸長を有する第2のセグメント、
(c)第3のAAV血清型のアミノ酸101〜アミノ酸480に由来する約50アミノ酸長〜約160アミノ酸長を有する第3のセグメント、
(d)前記第2のAAV血清型のアミノ酸151〜アミノ酸640に由来する約50アミノ酸長〜約160アミノ酸長を有する第4のセグメント、及び
(e)第4のAAV血清型のアミノ酸201からC末端までのアミノ酸に由来する約50アミノ酸長〜約160アミノ酸長を有する第5のセグメント
を含む、請求項1に記載のrAAVビリオン。 - 前記第1のAAV血清型はAAV6である、請求項6に記載のrAAVビリオン。
- 前記第2のAAV血清型はAAV9である、請求項6に記載のrAAVビリオン。
- 前記第3のAAV血清型はAAV8である、請求項6に記載のrAAVビリオン。
- 前記第4のAAV血清型はAAV2である、請求項6に記載のrAAVビリオン。
- 前記変異AAVカプシドタンパク質は、N末端からC末端に向かって順に、
(a)第1のAAV血清型のアミノ酸1〜アミノ酸160に由来する約50アミノ酸長〜約160アミノ酸長を有する第1のセグメント、
(b)第2のAAV血清型のアミノ酸51〜アミノ酸320に由来する約50アミノ酸長〜約160アミノ酸長を有する第2のセグメント、
(c)第3のAAV血清型のアミノ酸101〜アミノ酸480に由来する約50アミノ酸長〜約160アミノ酸長を有する第3のセグメント、
(d)前記第2のAAV血清型のアミノ酸151〜アミノ酸640に由来する約50アミノ酸長〜約160アミノ酸長を有する第4のセグメント、及び
(e)第4のAAV血清型のアミノ酸201〜アミノ酸800に由来する約50アミノ酸長〜約160アミノ酸長を有する第5のセグメント、
(f)前記第4のAAV血清型のアミノ酸251〜アミノ酸960に由来する約50アミノ酸長〜約160アミノ酸長を有する第6のセグメント、
(g)前記第2のAAV血清型のアミノ酸301〜アミノ酸1120に由来する約50アミノ酸長〜約160アミノ酸長を有する第7のセグメント、及び
(h)前記第2のAAV血清型のアミノ酸351からC末端までのアミノ酸に由来する約50アミノ酸長〜約160アミノ酸長を有する第8のセグメント
を含む、請求項1に記載のrAAVビリオン。 - 前記第1のAAV血清型はAAV6である、請求項11に記載のrAAVビリオン。
- 前記第2のAAV血清型はAAV9である、請求項11に記載のrAAVビリオン。
- 前記第3のAAV血清型はAAV8である、請求項11に記載のrAAVビリオン。
- 前記第4のAAV血清型はAAV2である、請求項11に記載のrAAVビリオン。
- 前記変異AAVカプシドタンパク質は、N末端からC末端に向かって順に、
(a)第1のAAV血清型のアミノ酸1〜アミノ酸160に由来する約50アミノ酸長〜約160アミノ酸長を有する第1のセグメント、
(b)第2のAAV血清型のアミノ酸51〜アミノ酸320に由来する約50アミノ酸長〜約160アミノ酸長を有する第2のセグメント、
(c)第3のAAV血清型のアミノ酸101〜アミノ酸480に由来する約50アミノ酸長〜約160アミノ酸長を有する第3のセグメント、
(d)前記第2のAAV血清型のアミノ酸151〜アミノ酸640に由来する約50アミノ酸長〜約160アミノ酸長を有する第4のセグメント、及び
(e)第4のAAV血清型のアミノ酸201〜アミノ酸800に由来する約50アミノ酸長〜約160アミノ酸長を有する第5のセグメント、
(f)前記第4のAAV血清型のアミノ酸251〜アミノ酸960に由来する約50アミノ酸長〜約160アミノ酸長を有する第6のセグメント、
(g)前記第2のAAV血清型のアミノ酸301〜アミノ酸1120に由来する約50アミノ酸長〜約160アミノ酸長を有する第7のセグメント、及び
(h)前記第2のAAV血清型のアミノ酸351からC末端までのアミノ酸に由来する約50アミノ酸長〜約160アミノ酸長を有する第8のセグメント
を含む、請求項1に記載のrAAVビリオン。 - 前記第1のAAV血清型はAAV6である、請求項16に記載のrAAVビリオン。
- 前記第2のAAV血清型はAAV9である、請求項16に記載のrAAVビリオン。
- 前記第3のAAV血清型はAAV8である、請求項16に記載のrAAVビリオン。
- 前記第4のAAV血清型はAAV2である、請求項16に記載のrAAVビリオン。
- 前記rAAVビリオンは、対応する親AAVカプシドタンパク質を含む前記対照AAVビリオンによる神経幹細胞への感染力と比較して、少なくとも5倍高い前記神経幹細胞への感染力を示す、請求項1に記載のrAAVビリオン。
- 前記対照AAVビリオンはAAV9である、請求項21に記載のrAAVビリオン。
- 前記対照AAVビリオンはAAV2である、請求項21に記載のrAAVビリオン。
- 前記rAAVビリオンは、対応する親AAVカプシドタンパク質を含む前記対照AAVビリオンによる神経幹細胞への感染力と比較して、少なくとも10倍高い前記神経幹細胞への感染力を示す、請求項1に記載のrAAVビリオン。
- 前記対照AAVビリオンはAAV9である、請求項24に記載のrAAVビリオン。
- 前記対照AAVビリオンはAAV2である、請求項24に記載のrAAVビリオン。
- 前記変異AAVカプシドタンパク質は、図8に示すアミノ酸配列に対する少なくとも約90%のアミノ酸配列同一性を有するアミノ酸配列を含む、請求項1に記載のrAAVビリオン。
- 前記変異AAVカプシドタンパク質は、図8に示すアミノ酸配列に対する少なくとも約95%のアミノ酸配列同一性を有するアミノ酸配列を含む、請求項1に記載のrAAVビリオン。
- 前記変異AAVカプシドタンパク質は、図8に示すアミノ酸配列を含む、請求項1に記載のrAAVビリオン。
- 前記変異AAVカプシドタンパク質は、図9に示すアミノ酸配列に対する少なくとも約90%のアミノ酸配列同一性を有するアミノ酸配列を含む、請求項1に記載のrAAVビリオン。
- 前記変異AAVカプシドタンパク質は、図9に示すアミノ酸配列に対する少なくとも約95%のアミノ酸配列同一性を有するアミノ酸配列を含む、請求項1に記載のrAAVビリオン。
- 前記変異AAVカプシドタンパク質は、図9に示すアミノ酸配列を含む、請求項1に記載のrAAVビリオン。
- 前記変異AAVカプシドタンパク質は、ヒトAAV中和抗体に対し、野生型AAVカプシドタンパク質を含む対照AAVビリオンが示す耐性と比較して高い耐性を示す、請求項1に記載のrAAVビリオン。
- 前記対照AAVビリオンはAAV9である、請求項33に記載のrAAVビリオン。
- 前記対照AAVビリオンはAAV2である、請求項33に記載のrAAVビリオン。
- 前記変異AAVカプシドタンパク質は、ヒトAAV中和抗体に対し、野生型AAVカプシドを含む対照AAVビリオンが示す耐性と比較して少なくとも約1.5倍高い耐性を示す、請求項1に記載のrAAVビリオン。
- 前記変異AAVカプシドタンパク質は、ヒトAAV中和抗体に対し、野生型AAVカプシドを含む対照AAVビリオンが示す耐性と比較して少なくとも約3倍高い耐性を示す、請求項1に記載のrAAVビリオン。
- 前記変異AAVカプシドタンパク質は、ヒトAAV中和抗体に対し、野生型AAVカプシドを含む対照AAVビリオンが示す耐性と比較して少なくとも約5倍高い耐性を示す、請求項1に記載のrAAVビリオン。
- 前記変異AAVカプシドタンパク質は、ヒトAAV中和抗体に対し、野生型AAVカプシドを含む対照AAVビリオンが示す耐性と比較して少なくとも約10倍高い耐性を示す、請求項1に記載のrAAVビリオン。
- 前記神経幹細胞は脳室下帯由来である、請求項1に記載のrAAVビリオン。
- 前記神経幹細胞は小脳由来である、請求項1に記載のrAAVビリオン。
- 前記遺伝子産物は、干渉RNAまたはアプタマーである、請求項1〜41のいずれか1項に記載のrAAVビリオン。
- 前記遺伝子産物はポリペプチドである、請求項1〜41のいずれか1項に記載のrAAVビリオン。
- 前記ポリペプチドは、神経保護ポリペプチド、血管新生阻害ポリペプチド、神経幹細胞の分化を誘導するポリペプチド、または神経幹細胞の機能を高めるポリペプチドである、請求項43に記載のrAAVビリオン。
- 前記ポリペプチドは、セレブロライシン、ラミニン−IKVAV、cripto、下垂体アデニル酸シクラーゼ活性化ポリペプチド、神経成長因子、脳由来神経栄養因子、グリア由来神経栄養因子、線維芽細胞増殖因子2、ニュールツリン、毛様体神経栄養因子、上皮成長因子、X連鎖アポトーシス抑制因子、芳香族L−アミノ酸脱炭酸酵素、グルタミン酸脱炭酸酵素、トリペプチジルペプチダーゼ、アスパルトアシクラーゼ、またはソニック・ヘッジホッグである、請求項43に記載のrAAVビリオン。
- 前記ポリペプチドはゲノム編集酵素である、請求項43に記載のrAAVビリオン。
- 前記ゲノム編集酵素は、Cas9ポリペプチド、ジンクフィンガーヌクレアーゼ、TALEN、または酵素的に不活性なII型CRISPR/Casポリペプチドである、請求項46に記載のrAAVビリオン。
- 前記ポリペプチドは、II型CRISPR/Casポリペプチド、V型CRISPR/Casポリペプチド、及びVI型CRISPR/Casポリペプチドから選択されるRNA誘導型エンドヌクレアーゼである、請求項47に記載のrAAVビリオン。
- 前記遺伝子産物は、RNA誘導型エンドヌクレアーゼ及びガイドRNAである、請求項1〜41のいずれか1項に記載のrAAVビリオン。
- (a)請求項1〜49のいずれか1項に記載の組換え型アデノ随伴ウイルスビリオン、及び
(b)薬理学的に許容される添加剤
を含む、医薬組成物。 - 個体の神経幹細胞に遺伝子産物を送達する方法であって、
請求項1〜49のいずれか1項に記載の組換え型アデノ随伴ウイルス(rAAV)ビリオンまたは請求項50に記載の組成物を前記個体に投与することを含む、前記方法。 - 前記投与は、頭蓋内注射、脳室内注射、髄腔内注射、大槽内注射、または静脈内注射による、請求項51に記載の方法。
- 前記遺伝子産物は、短鎖干渉RNAまたはアプタマーである、請求項51に記載の方法。
- 前記遺伝子産物はポリペプチドである、請求項51に記載の方法。
- 前記ポリペプチドは、神経保護ポリペプチド、血管新生阻害ポリペプチド、神経幹細胞の分化を誘導するポリペプチド、または神経幹細胞の機能を高めるポリペプチドである、請求項54に記載の方法。
- 前記ポリペプチドは、セレブロライシン、ラミニン−IKVAV、cripto、下垂体アデニル酸シクラーゼ活性化ポリペプチド、神経成長因子、脳由来神経栄養因子、グリア由来神経栄養因子、線維芽細胞増殖因子2、ニュールツリン、毛様体神経栄養因子、上皮成長因子、X連鎖アポトーシス抑制因子、またはソニック・ヘッジホッグである、請求項54に記載の方法。
- 前記ポリペプチドはゲノム編集酵素である、請求項54に記載の方法。
- 前記ゲノム編集酵素は、Cas9ポリペプチド、ジンクフィンガーヌクレアーゼ、TALEN、または酵素的に不活性なII型CRISPR/Casポリペプチドである、請求項57に記載の方法。
- 前記ポリペプチドは、II型CRISPR/Casポリペプチド、V型CRISPR/Casポリペプチド、及びVI型CRISPR/Casポリペプチドから選択されるRNA誘導型エンドヌクレアーゼである、請求項57に記載の方法。
- 前記遺伝子産物は、RNA誘導型エンドヌクレアーゼ及びガイドRNAである、請求項51に記載の方法。
- 神経性障害を治療する方法であって、
請求項1〜49のいずれか1項に記載の組換え型アデノ随伴ウイルス(rAAV)ビリオンまたは請求項50に記載の組成物の有効量を、それを必要とする個体に投与することを含む、前記方法。 - 前記神経性障害は、脊髄小脳失調症、ハンチントン病、パーキンソン病、アルツハイマー病、リソソーム蓄積障害、フリードライヒ運動失調症、神経膠芽腫、レット症候群、前頭側頭型認知症、またはてんかんである、請求項61に記載の方法。
- 変異アデノ随伴ウイルス(AAV)カプシドタンパク質をコードするヌクレオチド配列を含む単離された核酸であって、
前記変異AAVカプシドタンパク質が、少なくとも3つの異なるAAV血清型に由来する、各セグメントが約50アミノ酸長〜約160アミノ酸長を有する少なくとも5つのセグメントを含み、かつ
前記変異カプシドタンパク質が、野生型AAVカプシドを含む対照AAVビリオンによる神経幹細胞への感染力と比較して、前記神経幹細胞への高い感染力を付与する、
前記核酸。 - 請求項63に記載の核酸を含む、単離された遺伝子改変宿主細胞。
- 変異アデノ随伴ウイルス(AAV)カプシドタンパク質であって、
少なくとも3つの異なるAAV血清型に由来する、各セグメントが約50アミノ酸長〜約160アミノ酸長を有する少なくとも5つのセグメントを含み、かつ
野生型AAVカプシドを含む対照AAVビリオンによる神経幹細胞への感染力と比較して、前記神経幹細胞への高い感染力を付与する、
前記変異アデノ随伴ウイルスカプシドタンパク質。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201762551133P | 2017-08-28 | 2017-08-28 | |
| US62/551,133 | 2017-08-28 | ||
| PCT/US2018/047561 WO2019046069A1 (en) | 2017-08-28 | 2018-08-22 | ADENO-ASSOCIATED VIRUS CAPSID VARIANTS AND METHODS OF USE |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2020534788A true JP2020534788A (ja) | 2020-12-03 |
| JP2020534788A5 JP2020534788A5 (ja) | 2021-09-30 |
Family
ID=65525930
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019562303A Withdrawn JP2020534788A (ja) | 2017-08-28 | 2018-08-22 | アデノ随伴ウイルスカプシド変異体及びその使用方法 |
Country Status (10)
| Country | Link |
|---|---|
| US (1) | US11680249B2 (ja) |
| EP (1) | EP3676373A4 (ja) |
| JP (1) | JP2020534788A (ja) |
| KR (1) | KR20200039617A (ja) |
| CN (1) | CN110709511A (ja) |
| AU (1) | AU2018324477A1 (ja) |
| BR (1) | BR112020003571A2 (ja) |
| CA (1) | CA3059995A1 (ja) |
| MX (1) | MX2020001997A (ja) |
| WO (1) | WO2019046069A1 (ja) |
Families Citing this family (32)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SI3693025T1 (sl) | 2011-04-22 | 2022-04-29 | The Regents Of The University Of California | Virioni adeno-povezanega virusa z varianto kapsida in postopki za njihovo uporabo |
| US11136557B2 (en) | 2013-05-31 | 2021-10-05 | The Regents Of The University Of California | Adeno-associated virus variants and methods of use thereof |
| CN106414474B (zh) | 2014-03-17 | 2021-01-15 | 阿德夫拉姆生物技术股份有限公司 | 用于视锥细胞中增强的基因表达的组合物和方法 |
| EP3151866B1 (en) | 2014-06-09 | 2023-03-08 | Voyager Therapeutics, Inc. | Chimeric capsids |
| EP3490531A4 (en) | 2016-07-29 | 2020-06-03 | The Regents of The University of California | ADENO ASSOCIATED VIRUS VIRIONS WITH VARIABLE CAPSIDE AND METHOD FOR USE THEREOF |
| AU2017345470B2 (en) | 2016-10-19 | 2023-08-03 | Adverum Biotechnologies, Inc. | Modified AAV capsids and uses thereof |
| BR112019019015A2 (pt) | 2017-06-30 | 2020-04-14 | Univ California | vírions de vírus adeno-associado com capsídeos variantes e seus métodos de uso |
| KR102850887B1 (ko) | 2017-08-03 | 2025-08-28 | 보이저 테라퓨틱스, 인크. | Aav의 전달을 위한 조성물 및 방법 |
| JP2020534788A (ja) | 2017-08-28 | 2020-12-03 | ザ リージェンツ オブ ザ ユニバーシティ オブ カリフォルニア | アデノ随伴ウイルスカプシド変異体及びその使用方法 |
| MX2020003042A (es) | 2017-09-29 | 2020-11-18 | Voyager Therapeutics Inc | Rescate del fenotipo neurológico central y periférico de la ataxia de friedreich mediante administración intravenosa. |
| US12054724B2 (en) | 2018-04-10 | 2024-08-06 | President And Fellows Of Harvard College | AAV vectors encoding clarin-1 or GJB2 and uses thereof |
| SG11202103102WA (en) | 2018-09-26 | 2021-04-29 | California Inst Of Techn | Adeno-associated virus compositions for targeted gene therapy |
| EP3856762A1 (en) | 2018-09-28 | 2021-08-04 | Voyager Therapeutics, Inc. | Frataxin expression constructs having engineered promoters and methods of use thereof |
| KR20210143869A (ko) * | 2019-03-28 | 2021-11-29 | 더 제너럴 하스피탈 코포레이션 | 트랜스진 발현을 위한 조작된 아데노-연관 (aav) 벡터 |
| TW202102526A (zh) * | 2019-04-04 | 2021-01-16 | 美商銳進科斯生物股份有限公司 | 重組腺相關病毒及其用途 |
| KR20220007056A (ko) * | 2019-04-11 | 2022-01-18 | 캘리포니아 인스티튜트 오브 테크놀로지 | 뇌에서 증진된 특이성을 갖는 바이러스 조성물 |
| MX2021013913A (es) * | 2019-05-14 | 2022-03-17 | Univ Duke | Composiciones y metodos para el tratamiento de enfermedades mediadas por atpasa. |
| US20230048732A1 (en) * | 2020-05-26 | 2023-02-16 | Shape Therapeutics Inc. | High throughput engineering of functional aav capsids |
| CA3179597A1 (en) * | 2020-05-29 | 2021-12-02 | John G. Flannery | Adeno-associated virus virions with variant capsids and methods of use thereof |
| US12129287B2 (en) | 2020-09-14 | 2024-10-29 | President And Fellows Of Harvard College | Recombinant adeno associated virus encoding clarin-1 and uses thereof |
| CN113717248B (zh) * | 2020-09-30 | 2022-07-08 | 广州派真生物技术有限公司 | 腺相关病毒突变体及其应用 |
| US20220154223A1 (en) | 2020-10-15 | 2022-05-19 | Hoffmann-La Roche Inc. | Nucleic acid constructs for simultaneous gene activation |
| CN113025658B (zh) * | 2021-03-10 | 2022-04-22 | 华侨大学 | 一种神经干细胞特异性基因的递送载体及其应用 |
| CN113121651B (zh) * | 2021-04-19 | 2023-11-17 | 信念医药科技(上海)有限公司 | 低中和抗体腺相关病毒衣壳蛋白 |
| US20240342311A1 (en) * | 2021-07-30 | 2024-10-17 | University Of Florida Research Foundation, Incorporated | Engineering aav vectors with improved cns targeting |
| CN114057840B (zh) * | 2021-10-14 | 2022-09-20 | 和元生物技术(上海)股份有限公司 | 包含变异的aav9衣壳蛋白的重组腺相关病毒颗粒 |
| US20250161486A1 (en) * | 2022-02-22 | 2025-05-22 | The University Of North Carolina At Chapel Hill | Chimeric neurotropic aav capsids |
| CN119894920A (zh) * | 2022-07-22 | 2025-04-25 | 上海天泽云泰生物医药有限公司 | 用于靶向神经系统的新型aav衣壳及其用途 |
| CN116789738B (zh) * | 2022-12-08 | 2023-12-19 | 广州派真生物技术有限公司 | 腺相关病毒突变体及其应用 |
| CN117012275A (zh) * | 2023-08-11 | 2023-11-07 | 瑞诺元(苏州)生物科技有限公司 | 一种腺相关病毒测序数据的分析方法及系统 |
| WO2025147741A1 (en) * | 2024-01-11 | 2025-07-17 | Children's Medical Research Institute | Aav capsids and vectors for transduction of cells |
| WO2026024045A1 (ko) * | 2024-07-22 | 2026-01-29 | 한국생명공학연구원 | 변이체 캡시드를 포함하는 아데노-연관 바이러스 및 이의 용도 |
Family Cites Families (84)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB9206016D0 (en) | 1992-03-19 | 1992-04-29 | Sandoz Ltd | Improvements in or relating to organic compounds |
| US6440425B1 (en) | 1995-05-01 | 2002-08-27 | Aventis Pasteur Limited | High molecular weight major outer membrane protein of moraxella |
| US6001650A (en) | 1995-08-03 | 1999-12-14 | Avigen, Inc. | High-efficiency wild-type-free AAV helper functions |
| US6096548A (en) | 1996-03-25 | 2000-08-01 | Maxygen, Inc. | Method for directing evolution of a virus |
| CA2251738A1 (en) | 1996-04-16 | 1997-10-23 | Immusol Incorporated | Targeted viral vectors |
| US6710036B2 (en) | 1997-07-25 | 2004-03-23 | Avigen, Inc. | Induction of immune response to antigens expressed by recombinant adeno-associated virus |
| AU9319198A (en) | 1997-09-19 | 1999-04-05 | Trustees Of The University Of Pennsylvania, The | Methods and vector constructs useful for production of recombinant aav |
| EP1030861A4 (en) | 1997-10-31 | 2001-09-05 | Maxygen Inc | MODIFICATION OF VIRUSTROPISMIUS AND THE ECONOMIC SPECTRUM BY VIRAL GENOM MIXING |
| US6410300B1 (en) | 1998-01-12 | 2002-06-25 | The University Of North Carolina At Chapel Hill | Methods and formulations for mediating adeno-associated virus (AAV) attachment and infection and methods for purifying AAV |
| US6551795B1 (en) | 1998-02-18 | 2003-04-22 | Genome Therapeutics Corporation | Nucleic acid and amino acid sequences relating to pseudomonas aeruginosa for diagnostics and therapeutics |
| DE19827457C1 (de) | 1998-06-19 | 2000-03-02 | Medigene Ag | Strukturprotein von AAV, seine Herstellung und Verwendung |
| US6451594B1 (en) | 1998-09-11 | 2002-09-17 | The Regents Of The University Of California | Recombinant adenovirus for tissue specific expression in heart |
| DE69941905D1 (de) | 1998-11-10 | 2010-02-25 | Univ North Carolina | Virusvektoren und verfahren für ihre herstellung und verabreichung. |
| US6943153B1 (en) | 1999-03-15 | 2005-09-13 | The Regents Of The University Of California | Use of recombinant gene delivery vectors for treating or preventing diseases of the eye |
| US6498244B1 (en) | 1999-05-28 | 2002-12-24 | Cell Genesys, Inc. | Adeno-associated virus capsid immunologic determinants |
| US7314912B1 (en) | 1999-06-21 | 2008-01-01 | Medigene Aktiengesellschaft | AAv scleroprotein, production and use thereof |
| DE19933288A1 (de) | 1999-07-15 | 2001-01-18 | Medigene Ag | Strukturprotein von Adeno-assoziiertem Virus mit veränderter Antigenität, seine Herstellung und Verwendung |
| DE19933719A1 (de) | 1999-07-19 | 2001-01-25 | Medigene Ag | Strukturprotein in Adeno-assoziiertem Virus mit veränderten chromatographischen Eigenschaften, seine Herstellung und Verwendung |
| US8232081B2 (en) | 1999-09-21 | 2012-07-31 | Basf Se | Methods and microorganisms for production of panto-compounds |
| US6855314B1 (en) | 2000-03-22 | 2005-02-15 | The United States Of America As Represented By The Department Of Health And Human Services | AAV5 vector for transducing brain cells and lung cells |
| US7749492B2 (en) | 2001-01-05 | 2010-07-06 | Nationwide Children's Hospital, Inc. | AAV vectors and methods |
| WO2002053703A2 (en) | 2001-01-05 | 2002-07-11 | Children's Hospital, Inc. | Aav2 vectors and methods |
| EP1386004A4 (en) | 2001-04-05 | 2005-02-16 | Ribozyme Pharm Inc | MODULATION OF GENE EXPRESSION ASSOCIATED WITH INFLAMMATORY PROLIFERATION AND GROWTH OF NEURITIES BY METHODS INVOLVING NUCLEIC ACID |
| US20030129203A1 (en) | 2001-08-27 | 2003-07-10 | Nautilus Biotech S.A. | Mutant recombinant adeno-associated viruses |
| US7647184B2 (en) | 2001-08-27 | 2010-01-12 | Hanall Pharmaceuticals, Co. Ltd | High throughput directed evolution by rational mutagenesis |
| JP4677187B2 (ja) * | 2001-11-13 | 2011-04-27 | ザ・トラステイーズ・オブ・ザ・ユニバーシテイ・オブ・ペンシルベニア | 新規なアデノ随伴ウイルス(aav)7配列、それを含むベクターおよびそれらの使用 |
| JP2005512569A (ja) | 2001-12-21 | 2005-05-12 | メディジーン・アクチェンゲゼルシャフト | 目的とする細胞指向性をもつウイルスクローンの同定に有用な修飾した構造遺伝子またはキャプシド修飾した粒子のライブラリー |
| US20060292117A1 (en) | 2002-04-17 | 2006-12-28 | Loiler Scott A | Improved rAAv vectors |
| AU2003223775A1 (en) | 2002-04-30 | 2003-11-17 | Duke University | Adeno-associated viral vectors and methods for their production from hybrid adenovirus and for their use |
| AU2003237159A1 (en) | 2002-04-30 | 2003-11-17 | University Of Florida | Treatment for phenylketonuria |
| US7071172B2 (en) | 2002-04-30 | 2006-07-04 | The University Of North Carolina At Chapel Hill | Secretion signal vectors |
| US7254489B2 (en) | 2002-05-31 | 2007-08-07 | Microsoft Corporation | Systems, methods and apparatus for reconstructing phylogentic trees |
| US7220577B2 (en) | 2002-08-28 | 2007-05-22 | University Of Florida Research Foundation, Inc. | Modified AAV |
| US20070172460A1 (en) | 2003-03-19 | 2007-07-26 | Jurgen Kleinschmidt | Random peptide library displayed on aav vectors |
| WO2004108922A2 (en) | 2003-04-25 | 2004-12-16 | The Trustees Of The University Of Pennsylvania | Use of aav comprising a capsid protein from aav7 or aav8 for the delivery of genes encoding apoprotein a or e genes to the liver |
| EP1486567A1 (en) | 2003-06-11 | 2004-12-15 | Deutsches Krebsforschungszentrum Stiftung des öffentlichen Rechts | Improved adeno-associated virus (AAV) vector for gene therapy |
| HUE034597T2 (en) | 2003-06-19 | 2018-02-28 | Genzyme Corp | Reduced immunoreactivity of AAV virions and their applications |
| EP1644038A2 (en) | 2003-06-23 | 2006-04-12 | A & G Pharmaceuticals, Inc. | Compositions and methods for restoring sensitivity of tumor cells to antitumor therapy and inducing apoptosis |
| US9233131B2 (en) | 2003-06-30 | 2016-01-12 | The Regents Of The University Of California | Mutant adeno-associated virus virions and methods of use thereof |
| US9441244B2 (en) | 2003-06-30 | 2016-09-13 | The Regents Of The University Of California | Mutant adeno-associated virus virions and methods of use thereof |
| US20050019927A1 (en) | 2003-07-13 | 2005-01-27 | Markus Hildinger | DECREASING GENE EXPRESSION IN A MAMMALIAN SUBJECT IN VIVO VIA AAV-MEDIATED RNAi EXPRESSION CASSETTE TRANSFER |
| EP1670897A4 (en) | 2003-09-24 | 2008-02-27 | Univ Leland Stanford Junior | IGF-1 FORM OF NERVOUS STEM CELLS OF THE CENTRAL NERVOUS SYSTEM ADULTS PLURIPOTENT TO AN OLIGODENDROGICAL LINE |
| NZ545628A (en) | 2003-09-30 | 2009-04-30 | Univ Pennsylvania | Adeno-associated virus (AAV) clades, sequences, vectors containing same, and uses therefor |
| US7427396B2 (en) | 2004-06-03 | 2008-09-23 | Genzyme Corporation | AAV vectors for gene delivery to the lung |
| ES2385837T3 (es) | 2004-12-15 | 2012-08-01 | The University Of North Carolina At Chapel Hill | Vectores quiméricos |
| WO2006101634A1 (en) | 2005-02-17 | 2006-09-28 | The Regents Of The University Of California | Müller cell specific gene therapy |
| EP2359866B1 (en) | 2005-04-07 | 2013-07-17 | The Trustees of The University of Pennsylvania | Modified AAV rh48 capsids, compositions containing same and uses thereof |
| WO2007089632A2 (en) | 2006-01-27 | 2007-08-09 | The University Of North Carolina At Chapel Hill | Heparin and heparan sulfate binding chimeric vectors |
| WO2007120542A2 (en) | 2006-03-30 | 2007-10-25 | The Board Of Trustees Of The Leland Stanford Junior University | Aav capsid library and aav capsid proteins |
| CA2685900A1 (en) | 2006-05-04 | 2007-11-15 | Wayne State University | Restoration of visual responses by in vivo delivery of rhodopsin nucleic acids |
| CN1966082B (zh) | 2006-11-03 | 2010-06-30 | 许瑞安 | 一种防治结直肠癌的基因药物及其制备方法和用途 |
| US9725485B2 (en) | 2012-05-15 | 2017-08-08 | University Of Florida Research Foundation, Inc. | AAV vectors with high transduction efficiency and uses thereof for gene therapy |
| CA2683443A1 (en) | 2007-04-13 | 2008-10-23 | Catalyst Biosciences, Inc. | Modified factor vii polypeptides and uses thereof |
| EP1985708B1 (en) | 2007-04-27 | 2015-04-15 | Universität Rostock | Selective targeting of viruses to neural precursor cells |
| WO2009137006A2 (en) | 2008-04-30 | 2009-11-12 | The University Of North Carolina At Chapel Hill | Directed evolution and in vivo panning of virus vectors |
| US20120093772A1 (en) | 2008-05-20 | 2012-04-19 | Alan Horsager | Vectors for delivery of light sensitive proteins and methods of use |
| EP2297185A1 (en) | 2008-06-17 | 2011-03-23 | Amsterdam Molecular Therapeutics (AMT) B.V. | Parvoviral capsid with incorporated gly-ala repeat region |
| EP2396343B1 (en) | 2009-02-11 | 2017-05-17 | The University of North Carolina At Chapel Hill | Modified virus vectors and methods of making and using the same |
| CN101532024A (zh) | 2009-04-30 | 2009-09-16 | 许瑞安 | 一种用于基因治疗的新型细胞特异性内含microRNA结合序列的基因HAAVmir |
| WO2010138263A2 (en) | 2009-05-28 | 2010-12-02 | University Of Massachusetts | Novel aav 's and uses thereof |
| WO2011117258A2 (en) | 2010-03-22 | 2011-09-29 | Association Institut De Myologie | Methods of increasing efficiency of vector penetration of target tissue |
| US8663624B2 (en) | 2010-10-06 | 2014-03-04 | The Regents Of The University Of California | Adeno-associated virus virions with variant capsid and methods of use thereof |
| SI3693025T1 (sl) | 2011-04-22 | 2022-04-29 | The Regents Of The University Of California | Virioni adeno-povezanega virusa z varianto kapsida in postopki za njihovo uporabo |
| WO2013029030A1 (en) * | 2011-08-24 | 2013-02-28 | The Board Of Trustees Of The Leland Stanford Junior University | New aav capsid proteins for nucleic acid transfer |
| WO2013170078A1 (en) | 2012-05-09 | 2013-11-14 | Oregon Health & Science University | Adeno associated virus plasmids and vectors |
| TWI698240B (zh) | 2012-05-15 | 2020-07-11 | 澳大利亞商艾佛蘭屈澳洲私營有限公司 | 使用腺相關病毒(aav)sflt-1治療老年性黃斑部退化(amd) |
| CN104937100B (zh) | 2012-12-25 | 2020-04-03 | 宝生物工程株式会社 | Aav 变体 |
| WO2014124282A1 (en) | 2013-02-08 | 2014-08-14 | The Trustees Of The University Of Pennsylvania | Enhanced aav-mediated gene transfer for retinal therapies |
| AU2014273085B2 (en) | 2013-05-29 | 2020-10-22 | Cellectis | New compact scaffold of Cas9 in the type II CRISPR system |
| US11136557B2 (en) | 2013-05-31 | 2021-10-05 | The Regents Of The University Of California | Adeno-associated virus variants and methods of use thereof |
| WO2014207190A1 (en) | 2013-06-28 | 2014-12-31 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Methods for expressing a polynucleotide of interest in the retina of a subject |
| EP3633041A3 (en) | 2013-09-26 | 2020-07-29 | University of Florida Research Foundation, Inc. | Synthetic combinatorial aav capsid library for targeted gene therapy |
| LT3459965T (lt) | 2013-10-11 | 2021-03-10 | Massachusetts Eye & Ear Infirmary | Viruso prototipo sekų ir jų panaudojimo prognozavimo metodai |
| GB201403684D0 (en) | 2014-03-03 | 2014-04-16 | King S College London | Vector |
| CN106414474B (zh) | 2014-03-17 | 2021-01-15 | 阿德夫拉姆生物技术股份有限公司 | 用于视锥细胞中增强的基因表达的组合物和方法 |
| PL3137497T5 (pl) | 2014-05-02 | 2025-06-09 | Genzyme Corporation | Wektory AAV do terapii genowej siatkówki i OUN |
| WO2015191693A2 (en) | 2014-06-10 | 2015-12-17 | Massachusetts Institute Of Technology | Method for gene editing |
| CN108347932B (zh) | 2015-02-20 | 2022-09-13 | 衣阿华大学研究基金会 | 用于治疗遗传性眼病的方法和组合物 |
| BR112017018846A2 (pt) | 2015-03-02 | 2018-07-31 | Adverum Biotechnologies, Inc. | composições e métodos para entrega intravítrea de polinucleotídeos a cones retinianos. |
| ES2806054T3 (es) | 2015-03-06 | 2021-02-16 | Massachusetts Eye & Ear Infirmary | Terapias de aumento génico de la degeneración retiniana causada por mutaciones en el gen PRPF31 |
| US20190000940A1 (en) * | 2015-07-31 | 2019-01-03 | Voyager Therapeutics, Inc. | Compositions and methods for the treatment of aadc deficiency |
| PT4206216T (pt) | 2016-05-13 | 2025-12-03 | 4D Molecular Therapeutics Inc | Cápsides variantes de vírus adeno-associado e métodos de utilização das mesmas |
| MA44546B1 (fr) | 2016-06-15 | 2021-03-31 | Univ California | Virus adéno-associés variants et procédés d'utilisation |
| JP2020534788A (ja) | 2017-08-28 | 2020-12-03 | ザ リージェンツ オブ ザ ユニバーシティ オブ カリフォルニア | アデノ随伴ウイルスカプシド変異体及びその使用方法 |
-
2018
- 2018-08-22 JP JP2019562303A patent/JP2020534788A/ja not_active Withdrawn
- 2018-08-22 MX MX2020001997A patent/MX2020001997A/es unknown
- 2018-08-22 CN CN201880035665.2A patent/CN110709511A/zh active Pending
- 2018-08-22 AU AU2018324477A patent/AU2018324477A1/en not_active Abandoned
- 2018-08-22 CA CA3059995A patent/CA3059995A1/en active Pending
- 2018-08-22 KR KR1020197035110A patent/KR20200039617A/ko not_active Withdrawn
- 2018-08-22 BR BR112020003571-8A patent/BR112020003571A2/pt not_active IP Right Cessation
- 2018-08-22 EP EP18850221.5A patent/EP3676373A4/en not_active Withdrawn
- 2018-08-22 WO PCT/US2018/047561 patent/WO2019046069A1/en not_active Ceased
- 2018-08-22 US US16/500,706 patent/US11680249B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| CA3059995A1 (en) | 2019-03-07 |
| EP3676373A4 (en) | 2021-06-09 |
| KR20200039617A (ko) | 2020-04-16 |
| CN110709511A (zh) | 2020-01-17 |
| US20200095559A1 (en) | 2020-03-26 |
| EP3676373A1 (en) | 2020-07-08 |
| US11680249B2 (en) | 2023-06-20 |
| WO2019046069A1 (en) | 2019-03-07 |
| MX2020001997A (es) | 2020-07-20 |
| AU2018324477A1 (en) | 2019-10-17 |
| BR112020003571A2 (pt) | 2020-08-25 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2020534788A (ja) | アデノ随伴ウイルスカプシド変異体及びその使用方法 | |
| JP7612767B2 (ja) | アデノ随伴ウイルスベクター | |
| JP7706582B2 (ja) | 変異カプシドを有するアデノ随伴ウイルスビリオン及びその使用方法 | |
| JP2023126919A (ja) | バリアントカプシドを有するアデノ随伴ウイルスビリオン及びその使用方法 | |
| Ojala et al. | In vivo selection of a computationally designed SCHEMA AAV library yields a novel variant for infection of adult neural stem cells in the SVZ | |
| CN115023242B (zh) | 腺相关病毒载体变体 | |
| Pignataro et al. | Adeno-associated viral vectors serotype 8 for cell-specific delivery of therapeutic genes in the central nervous system | |
| TW202039854A (zh) | 治療威爾遜氏病的組合物和方法 | |
| CN111718420A (zh) | 一种用于基因治疗的融合蛋白及其应用 | |
| US20220098254A1 (en) | NEUROD1 and DLX2 VECTOR | |
| Woodbury et al. | Gene delivery and gene therapy for Alzheimer’s disease | |
| WO2023184688A1 (zh) | 功能性β-半乳糖苷酶变体、AAV介导的人β-半乳糖苷酶表达载体及其用途 | |
| WO2024191877A2 (en) | Human central nervous system (cns) targeting aav variants | |
| JP2025508059A (ja) | 肺向性が改善されたアデノ随伴ウイルス変異体カプシドおよびその使用 | |
| CN120187407A (zh) | 重组aav载体及其用途 | |
| HK40019369A (en) | Adeno-associated virus vector | |
| Duan | Molecular characterization of adeno-associated virus for the gene therapy of submucosal gland in cystic fibrosis | |
| WO2020187272A1 (zh) | 一种用于基因治疗的融合蛋白及其应用 | |
| HK1226768B (zh) | 腺相关病毒载体 | |
| HK1226768A1 (zh) | 腺相關病毒載體 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200311 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20210617 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210819 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20210819 |
|
| A761 | Written withdrawal of application |
Free format text: JAPANESE INTERMEDIATE CODE: A761 Effective date: 20220721 |