JP2015512900A - Combination therapy to treat HCV infection in a special patient genotype subpopulation - Google Patents
Combination therapy to treat HCV infection in a special patient genotype subpopulation Download PDFInfo
- Publication number
- JP2015512900A JP2015512900A JP2015502107A JP2015502107A JP2015512900A JP 2015512900 A JP2015512900 A JP 2015512900A JP 2015502107 A JP2015502107 A JP 2015502107A JP 2015502107 A JP2015502107 A JP 2015502107A JP 2015512900 A JP2015512900 A JP 2015512900A
- Authority
- JP
- Japan
- Prior art keywords
- compound
- acceptable salt
- pharmaceutically acceptable
- interferon alpha
- ribavirin
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 208000015181 infectious disease Diseases 0.000 title claims abstract description 38
- 238000002648 combination therapy Methods 0.000 title description 13
- 150000001875 compounds Chemical class 0.000 claims abstract description 96
- IWUCXVSUMQZMFG-AFCXAGJDSA-N Ribavirin Chemical compound N1=C(C(=O)N)N=CN1[C@H]1[C@H](O)[C@H](O)[C@@H](CO)O1 IWUCXVSUMQZMFG-AFCXAGJDSA-N 0.000 claims abstract description 82
- 108010047761 Interferon-alpha Proteins 0.000 claims abstract description 72
- 102000006992 Interferon-alpha Human genes 0.000 claims abstract description 72
- 229960000329 ribavirin Drugs 0.000 claims abstract description 69
- HZCAHMRRMINHDJ-DBRKOABJSA-N ribavirin Natural products O[C@@H]1[C@H](O)[C@@H](CO)O[C@H]1N1N=CN=C1 HZCAHMRRMINHDJ-DBRKOABJSA-N 0.000 claims abstract description 69
- 150000003839 salts Chemical class 0.000 claims abstract description 67
- 230000001225 therapeutic effect Effects 0.000 claims abstract description 34
- 102210017790 rs12979860 Human genes 0.000 claims abstract description 33
- 102210007160 rs8099917 Human genes 0.000 claims abstract description 30
- 238000000034 method Methods 0.000 claims abstract description 27
- 208000024891 symptom Diseases 0.000 claims abstract description 9
- 241000711549 Hepacivirus C Species 0.000 claims description 93
- 238000011282 treatment Methods 0.000 claims description 64
- 102000014150 Interferons Human genes 0.000 claims description 53
- 108010050904 Interferons Proteins 0.000 claims description 53
- 229940079322 interferon Drugs 0.000 claims description 52
- 102100020992 Interferon lambda-3 Human genes 0.000 claims description 16
- 101710099621 Interferon lambda-3 Proteins 0.000 claims description 16
- 102100040018 Interferon alpha-2 Human genes 0.000 claims description 13
- 108010079944 Interferon-alpha2b Proteins 0.000 claims description 13
- 238000012423 maintenance Methods 0.000 claims description 9
- 239000008194 pharmaceutical composition Substances 0.000 claims description 9
- 239000003814 drug Substances 0.000 claims description 8
- 159000000000 sodium salts Chemical class 0.000 claims description 6
- 230000002829 reductive effect Effects 0.000 claims description 4
- 238000011260 co-administration Methods 0.000 claims description 2
- 108700026220 vif Genes Proteins 0.000 claims 1
- 101001002466 Homo sapiens Interferon lambda-3 Proteins 0.000 abstract description 26
- 239000003112 inhibitor Substances 0.000 abstract description 4
- 102000012479 Serine Proteases Human genes 0.000 abstract description 3
- 108010022999 Serine Proteases Proteins 0.000 abstract description 3
- 230000003389 potentiating effect Effects 0.000 abstract description 3
- 230000004077 genetic alteration Effects 0.000 abstract description 2
- 231100000118 genetic alteration Toxicity 0.000 abstract description 2
- 239000000203 mixture Substances 0.000 description 16
- 239000002202 Polyethylene glycol Substances 0.000 description 12
- 229920001223 polyethylene glycol Polymers 0.000 description 12
- 238000009472 formulation Methods 0.000 description 9
- 238000002560 therapeutic procedure Methods 0.000 description 9
- 230000001684 chronic effect Effects 0.000 description 7
- 238000003205 genotyping method Methods 0.000 description 7
- 230000003612 virological effect Effects 0.000 description 7
- -1 2-isopropylcarbamoyl-thiazol-4-yl Chemical group 0.000 description 6
- 239000002253 acid Substances 0.000 description 6
- 238000003556 assay Methods 0.000 description 6
- 230000000694 effects Effects 0.000 description 6
- 108010092851 peginterferon alfa-2b Proteins 0.000 description 6
- 101000959820 Homo sapiens Interferon alpha-1/13 Proteins 0.000 description 5
- 102100040019 Interferon alpha-1/13 Human genes 0.000 description 5
- 238000004458 analytical method Methods 0.000 description 5
- 229940047124 interferons Drugs 0.000 description 5
- 229920000642 polymer Polymers 0.000 description 5
- 108090000623 proteins and genes Proteins 0.000 description 5
- 230000004044 response Effects 0.000 description 5
- HZAXFHJVJLSVMW-UHFFFAOYSA-N 2-Aminoethan-1-ol Chemical compound NCCO HZAXFHJVJLSVMW-UHFFFAOYSA-N 0.000 description 4
- 229940122604 HCV protease inhibitor Drugs 0.000 description 4
- 208000005176 Hepatitis C Diseases 0.000 description 4
- 241000700605 Viruses Species 0.000 description 4
- 230000000840 anti-viral effect Effects 0.000 description 4
- 239000002585 base Substances 0.000 description 4
- RYYVLZVUVIJVGH-UHFFFAOYSA-N caffeine Chemical compound CN1C(=O)N(C)C(=O)C2=C1N=CN2C RYYVLZVUVIJVGH-UHFFFAOYSA-N 0.000 description 4
- 238000001514 detection method Methods 0.000 description 4
- 229940079593 drug Drugs 0.000 description 4
- 229950000038 interferon alfa Drugs 0.000 description 4
- 108010092853 peginterferon alfa-2a Proteins 0.000 description 4
- 238000011002 quantification Methods 0.000 description 4
- 238000012163 sequencing technique Methods 0.000 description 4
- 210000002966 serum Anatomy 0.000 description 4
- GETQZCLCWQTVFV-UHFFFAOYSA-N trimethylamine Chemical compound CN(C)C GETQZCLCWQTVFV-UHFFFAOYSA-N 0.000 description 4
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 4
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- XBPCUCUWBYBCDP-UHFFFAOYSA-N Dicyclohexylamine Chemical compound C1CCCCC1NC1CCCCC1 XBPCUCUWBYBCDP-UHFFFAOYSA-N 0.000 description 3
- SJRJJKPEHAURKC-UHFFFAOYSA-N N-Methylmorpholine Chemical compound CN1CCOCC1 SJRJJKPEHAURKC-UHFFFAOYSA-N 0.000 description 3
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 3
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 3
- 230000001154 acute effect Effects 0.000 description 3
- 239000002671 adjuvant Substances 0.000 description 3
- 230000002411 adverse Effects 0.000 description 3
- 125000003277 amino group Chemical group 0.000 description 3
- 239000002775 capsule Substances 0.000 description 3
- 208000020403 chronic hepatitis C virus infection Diseases 0.000 description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 3
- 238000011284 combination treatment Methods 0.000 description 3
- 239000002552 dosage form Substances 0.000 description 3
- 230000009240 extended rapid viral response Effects 0.000 description 3
- 108020001507 fusion proteins Proteins 0.000 description 3
- 102000037865 fusion proteins Human genes 0.000 description 3
- 230000002068 genetic effect Effects 0.000 description 3
- 239000005022 packaging material Substances 0.000 description 3
- 230000008569 process Effects 0.000 description 3
- PAMIQIKDUOTOBW-UHFFFAOYSA-N 1-methylpiperidine Chemical compound CN1CCCCC1 PAMIQIKDUOTOBW-UHFFFAOYSA-N 0.000 description 2
- XMIIGOLPHOKFCH-UHFFFAOYSA-N 3-phenylpropionic acid Chemical compound OC(=O)CCC1=CC=CC=C1 XMIIGOLPHOKFCH-UHFFFAOYSA-N 0.000 description 2
- HVBSAKJJOYLTQU-UHFFFAOYSA-N 4-aminobenzenesulfonic acid Chemical compound NC1=CC=C(S(O)(=O)=O)C=C1 HVBSAKJJOYLTQU-UHFFFAOYSA-N 0.000 description 2
- KDCGOANMDULRCW-UHFFFAOYSA-N 7H-purine Chemical compound N1=CNC2=NC=NC2=C1 KDCGOANMDULRCW-UHFFFAOYSA-N 0.000 description 2
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 2
- QGZKDVFQNNGYKY-UHFFFAOYSA-O Ammonium Chemical compound [NH4+] QGZKDVFQNNGYKY-UHFFFAOYSA-O 0.000 description 2
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 2
- FERIUCNNQQJTOY-UHFFFAOYSA-N Butyric acid Chemical compound CCCC(O)=O FERIUCNNQQJTOY-UHFFFAOYSA-N 0.000 description 2
- ROSDSFDQCJNGOL-UHFFFAOYSA-N Dimethylamine Chemical compound CNC ROSDSFDQCJNGOL-UHFFFAOYSA-N 0.000 description 2
- JOYRKODLDBILNP-UHFFFAOYSA-N Ethyl urethane Chemical compound CCOC(N)=O JOYRKODLDBILNP-UHFFFAOYSA-N 0.000 description 2
- QUSNBJAOOMFDIB-UHFFFAOYSA-N Ethylamine Chemical compound CCN QUSNBJAOOMFDIB-UHFFFAOYSA-N 0.000 description 2
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 2
- AEMRFAOFKBGASW-UHFFFAOYSA-N Glycolic acid Chemical compound OCC(O)=O AEMRFAOFKBGASW-UHFFFAOYSA-N 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 2
- CPELXLSAUQHCOX-UHFFFAOYSA-N Hydrogen bromide Chemical compound Br CPELXLSAUQHCOX-UHFFFAOYSA-N 0.000 description 2
- 108010078049 Interferon alpha-2 Proteins 0.000 description 2
- LPHGQDQBBGAPDZ-UHFFFAOYSA-N Isocaffeine Natural products CN1C(=O)N(C)C(=O)C2=C1N(C)C=N2 LPHGQDQBBGAPDZ-UHFFFAOYSA-N 0.000 description 2
- OFOBLEOULBTSOW-UHFFFAOYSA-N Malonic acid Chemical compound OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 2
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 2
- BAVYZALUXZFZLV-UHFFFAOYSA-N Methylamine Chemical compound NC BAVYZALUXZFZLV-UHFFFAOYSA-N 0.000 description 2
- JLTDJTHDQAWBAV-UHFFFAOYSA-N N,N-dimethylaniline Chemical compound CN(C)C1=CC=CC=C1 JLTDJTHDQAWBAV-UHFFFAOYSA-N 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- GLUUGHFHXGJENI-UHFFFAOYSA-N Piperazine Chemical compound C1CNCCN1 GLUUGHFHXGJENI-UHFFFAOYSA-N 0.000 description 2
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 2
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 2
- LCTONWCANYUPML-UHFFFAOYSA-N Pyruvic acid Chemical compound CC(=O)C(O)=O LCTONWCANYUPML-UHFFFAOYSA-N 0.000 description 2
- 238000013381 RNA quantification Methods 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 2
- WNLRTRBMVRJNCN-UHFFFAOYSA-N adipic acid Chemical compound OC(=O)CCCCC(O)=O WNLRTRBMVRJNCN-UHFFFAOYSA-N 0.000 description 2
- 150000001412 amines Chemical class 0.000 description 2
- 230000003321 amplification Effects 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 2
- 210000004369 blood Anatomy 0.000 description 2
- 239000008280 blood Substances 0.000 description 2
- 230000037396 body weight Effects 0.000 description 2
- 229960001948 caffeine Drugs 0.000 description 2
- VJEONQKOZGKCAK-UHFFFAOYSA-N caffeine Natural products CN1C(=O)N(C)C(=O)C2=C1C=CN2C VJEONQKOZGKCAK-UHFFFAOYSA-N 0.000 description 2
- OEYIOHPDSNJKLS-UHFFFAOYSA-N choline Chemical compound C[N+](C)(C)CCO OEYIOHPDSNJKLS-UHFFFAOYSA-N 0.000 description 2
- 229960001231 choline Drugs 0.000 description 2
- 229940055354 copegus Drugs 0.000 description 2
- HPNMFZURTQLUMO-UHFFFAOYSA-N diethylamine Chemical compound CCNCC HPNMFZURTQLUMO-UHFFFAOYSA-N 0.000 description 2
- XBDQKXXYIPTUBI-UHFFFAOYSA-N dimethylselenoniopropionate Natural products CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 description 2
- 230000029142 excretion Effects 0.000 description 2
- 102000054767 gene variant Human genes 0.000 description 2
- 238000011221 initial treatment Methods 0.000 description 2
- JJWLVOIRVHMVIS-UHFFFAOYSA-N isopropylamine Chemical compound CC(C)N JJWLVOIRVHMVIS-UHFFFAOYSA-N 0.000 description 2
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 2
- 150000002632 lipids Chemical class 0.000 description 2
- 208000019423 liver disease Diseases 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 2
- 231100000252 nontoxic Toxicity 0.000 description 2
- 230000003000 nontoxic effect Effects 0.000 description 2
- 238000003199 nucleic acid amplification method Methods 0.000 description 2
- 230000036961 partial effect Effects 0.000 description 2
- 229940002988 pegasys Drugs 0.000 description 2
- 229940106366 pegintron Drugs 0.000 description 2
- 229920000233 poly(alkylene oxides) Polymers 0.000 description 2
- 102000054765 polymorphisms of proteins Human genes 0.000 description 2
- 108090000765 processed proteins & peptides Proteins 0.000 description 2
- 235000018102 proteins Nutrition 0.000 description 2
- 102000004169 proteins and genes Human genes 0.000 description 2
- 229940053146 rebetol Drugs 0.000 description 2
- 230000009467 reduction Effects 0.000 description 2
- 239000011347 resin Substances 0.000 description 2
- 229920005989 resin Polymers 0.000 description 2
- YGSDEFSMJLZEOE-UHFFFAOYSA-N salicylic acid Chemical compound OC(=O)C1=CC=CC=C1O YGSDEFSMJLZEOE-UHFFFAOYSA-N 0.000 description 2
- 238000000926 separation method Methods 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- YAPQBXQYLJRXSA-UHFFFAOYSA-N theobromine Chemical compound CN1C(=O)NC(=O)C2=C1N=CN2C YAPQBXQYLJRXSA-UHFFFAOYSA-N 0.000 description 2
- 238000011295 triple combination therapy Methods 0.000 description 2
- ZDPHROOEEOARMN-UHFFFAOYSA-N undecanoic acid Chemical compound CCCCCCCCCCC(O)=O ZDPHROOEEOARMN-UHFFFAOYSA-N 0.000 description 2
- QBYIENPQHBMVBV-HFEGYEGKSA-N (2R)-2-hydroxy-2-phenylacetic acid Chemical compound O[C@@H](C(O)=O)c1ccccc1.O[C@@H](C(O)=O)c1ccccc1 QBYIENPQHBMVBV-HFEGYEGKSA-N 0.000 description 1
- MIOPJNTWMNEORI-GMSGAONNSA-N (S)-camphorsulfonic acid Chemical compound C1C[C@@]2(CS(O)(=O)=O)C(=O)C[C@@H]1C2(C)C MIOPJNTWMNEORI-GMSGAONNSA-N 0.000 description 1
- BJEPYKJPYRNKOW-REOHCLBHSA-N (S)-malic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O BJEPYKJPYRNKOW-REOHCLBHSA-N 0.000 description 1
- UWYVPFMHMJIBHE-OWOJBTEDSA-N (e)-2-hydroxybut-2-enedioic acid Chemical compound OC(=O)\C=C(\O)C(O)=O UWYVPFMHMJIBHE-OWOJBTEDSA-N 0.000 description 1
- WBYWAXJHAXSJNI-VOTSOKGWSA-M .beta-Phenylacrylic acid Natural products [O-]C(=O)\C=C\C1=CC=CC=C1 WBYWAXJHAXSJNI-VOTSOKGWSA-M 0.000 description 1
- IWUCXVSUMQZMFG-RGDLXGNYSA-N 1-[(2s,3s,4r,5s)-3,4-dihydroxy-5-(hydroxymethyl)oxolan-2-yl]-1,2,4-triazole-3-carboxamide Chemical compound N1=C(C(=O)N)N=CN1[C@@H]1[C@@H](O)[C@@H](O)[C@H](CO)O1 IWUCXVSUMQZMFG-RGDLXGNYSA-N 0.000 description 1
- LXFQSRIDYRFTJW-UHFFFAOYSA-N 2,4,6-trimethylbenzenesulfonic acid Chemical compound CC1=CC(C)=C(S(O)(=O)=O)C(C)=C1 LXFQSRIDYRFTJW-UHFFFAOYSA-N 0.000 description 1
- LBLYYCQCTBFVLH-UHFFFAOYSA-N 2-Methylbenzenesulfonic acid Chemical compound CC1=CC=CC=C1S(O)(=O)=O LBLYYCQCTBFVLH-UHFFFAOYSA-N 0.000 description 1
- MSWZFWKMSRAUBD-IVMDWMLBSA-N 2-amino-2-deoxy-D-glucopyranose Chemical compound N[C@H]1C(O)O[C@H](CO)[C@@H](O)[C@@H]1O MSWZFWKMSRAUBD-IVMDWMLBSA-N 0.000 description 1
- GRWKNBPOGBTZMN-UHFFFAOYSA-N 2-benzyl-3-phenylpropane-1,2-diamine Chemical class C=1C=CC=CC=1CC(N)(CN)CC1=CC=CC=C1 GRWKNBPOGBTZMN-UHFFFAOYSA-N 0.000 description 1
- BFSVOASYOCHEOV-UHFFFAOYSA-N 2-diethylaminoethanol Chemical compound CCN(CC)CCO BFSVOASYOCHEOV-UHFFFAOYSA-N 0.000 description 1
- 229940013085 2-diethylaminoethanol Drugs 0.000 description 1
- QKRMFCXDTFLKKT-UHFFFAOYSA-N 2-hydroxyethanesulfonic acid Chemical compound OCCS(O)(=O)=O.OCCS(O)(=O)=O QKRMFCXDTFLKKT-UHFFFAOYSA-N 0.000 description 1
- WLJVXDMOQOGPHL-PPJXEINESA-N 2-phenylacetic acid Chemical compound O[14C](=O)CC1=CC=CC=C1 WLJVXDMOQOGPHL-PPJXEINESA-N 0.000 description 1
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 1
- 102100036475 Alanine aminotransferase 1 Human genes 0.000 description 1
- 108010082126 Alanine transaminase Proteins 0.000 description 1
- 102100027211 Albumin Human genes 0.000 description 1
- 108010088751 Albumins Proteins 0.000 description 1
- 108700028369 Alleles Proteins 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- 239000005711 Benzoic acid Substances 0.000 description 1
- KWIUHFFTVRNATP-UHFFFAOYSA-N Betaine Natural products C[N+](C)(C)CC([O-])=O KWIUHFFTVRNATP-UHFFFAOYSA-N 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-M Bicarbonate Chemical class OC([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-M 0.000 description 1
- MLODIWMGYOVJHF-UHFFFAOYSA-N C(C1=CN=CC=C1)(=O)O.C1(=CC=CC2=CC=CC=C12)S(=O)(=O)O Chemical compound C(C1=CN=CC=C1)(=O)O.C1(=CC=CC2=CC=CC=C12)S(=O)(=O)O MLODIWMGYOVJHF-UHFFFAOYSA-N 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- BHPQYMZQTOCNFJ-UHFFFAOYSA-N Calcium cation Chemical compound [Ca+2] BHPQYMZQTOCNFJ-UHFFFAOYSA-N 0.000 description 1
- LSPHULWDVZXLIL-UHFFFAOYSA-N Camphoric acid Natural products CC1(C)C(C(O)=O)CCC1(C)C(O)=O LSPHULWDVZXLIL-UHFFFAOYSA-N 0.000 description 1
- WWZKQHOCKIZLMA-UHFFFAOYSA-N Caprylic acid Natural products CCCCCCCC(O)=O WWZKQHOCKIZLMA-UHFFFAOYSA-N 0.000 description 1
- 208000006154 Chronic hepatitis C Diseases 0.000 description 1
- WBYWAXJHAXSJNI-SREVYHEPSA-N Cinnamic acid Chemical compound OC(=O)\C=C/C1=CC=CC=C1 WBYWAXJHAXSJNI-SREVYHEPSA-N 0.000 description 1
- 206010010356 Congenital anomaly Diseases 0.000 description 1
- JPVYNHNXODAKFH-UHFFFAOYSA-N Cu2+ Chemical compound [Cu+2] JPVYNHNXODAKFH-UHFFFAOYSA-N 0.000 description 1
- 108020001019 DNA Primers Proteins 0.000 description 1
- 239000003155 DNA primer Substances 0.000 description 1
- 229920002307 Dextran Polymers 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- BWLUMTFWVZZZND-UHFFFAOYSA-N Dibenzylamine Chemical compound C=1C=CC=CC=1CNCC1=CC=CC=C1 BWLUMTFWVZZZND-UHFFFAOYSA-N 0.000 description 1
- PIICEJLVQHRZGT-UHFFFAOYSA-N Ethylenediamine Chemical compound NCCN PIICEJLVQHRZGT-UHFFFAOYSA-N 0.000 description 1
- 206010016654 Fibrosis Diseases 0.000 description 1
- 238000000729 Fisher's exact test Methods 0.000 description 1
- 101710107035 Gamma-glutamyltranspeptidase Proteins 0.000 description 1
- 206010064571 Gene mutation Diseases 0.000 description 1
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 description 1
- 101710173228 Glutathione hydrolase proenzyme Proteins 0.000 description 1
- 206010020751 Hypersensitivity Diseases 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- 102000003996 Interferon-beta Human genes 0.000 description 1
- 108090000467 Interferon-beta Proteins 0.000 description 1
- 108010074328 Interferon-gamma Proteins 0.000 description 1
- 102000008070 Interferon-gamma Human genes 0.000 description 1
- 102000015696 Interleukins Human genes 0.000 description 1
- 108010063738 Interleukins Proteins 0.000 description 1
- ODKSFYDXXFIFQN-BYPYZUCNSA-P L-argininium(2+) Chemical compound NC(=[NH2+])NCCC[C@H]([NH3+])C(O)=O ODKSFYDXXFIFQN-BYPYZUCNSA-P 0.000 description 1
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 1
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 1
- HNDVDQJCIGZPNO-YFKPBYRVSA-N L-histidine Chemical compound OC(=O)[C@@H](N)CC1=CN=CN1 HNDVDQJCIGZPNO-YFKPBYRVSA-N 0.000 description 1
- KDXKERNSBIXSRK-YFKPBYRVSA-N L-lysine Chemical compound NCCCC[C@H](N)C(O)=O KDXKERNSBIXSRK-YFKPBYRVSA-N 0.000 description 1
- HBBGRARXTFLTSG-UHFFFAOYSA-N Lithium ion Chemical compound [Li+] HBBGRARXTFLTSG-UHFFFAOYSA-N 0.000 description 1
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 1
- 239000004472 Lysine Substances 0.000 description 1
- JLVVSXFLKOJNIY-UHFFFAOYSA-N Magnesium ion Chemical compound [Mg+2] JLVVSXFLKOJNIY-UHFFFAOYSA-N 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- KWIUHFFTVRNATP-UHFFFAOYSA-O N,N,N-trimethylglycinium Chemical compound C[N+](C)(C)CC(O)=O KWIUHFFTVRNATP-UHFFFAOYSA-O 0.000 description 1
- UEEJHVSXFDXPFK-UHFFFAOYSA-N N-dimethylaminoethanol Chemical compound CN(C)CCO UEEJHVSXFDXPFK-UHFFFAOYSA-N 0.000 description 1
- HTLZVHNRZJPSMI-UHFFFAOYSA-N N-ethylpiperidine Chemical compound CCN1CCCCC1 HTLZVHNRZJPSMI-UHFFFAOYSA-N 0.000 description 1
- MBBZMMPHUWSWHV-BDVNFPICSA-N N-methylglucamine Chemical compound CNC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO MBBZMMPHUWSWHV-BDVNFPICSA-N 0.000 description 1
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 description 1
- 208000037581 Persistent Infection Diseases 0.000 description 1
- 239000004372 Polyvinyl alcohol Substances 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- 229940124158 Protease/peptidase inhibitor Drugs 0.000 description 1
- IWYDHOAUDWTVEP-UHFFFAOYSA-N R-2-phenyl-2-hydroxyacetic acid Natural products OC(=O)C(O)C1=CC=CC=C1 IWYDHOAUDWTVEP-UHFFFAOYSA-N 0.000 description 1
- 108020005719 Species specific proteins Proteins 0.000 description 1
- 102000007397 Species specific proteins Human genes 0.000 description 1
- 235000021355 Stearic acid Nutrition 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 1
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 1
- 108020000999 Viral RNA Proteins 0.000 description 1
- PTFCDOFLOPIGGS-UHFFFAOYSA-N Zinc dication Chemical compound [Zn+2] PTFCDOFLOPIGGS-UHFFFAOYSA-N 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 239000004480 active ingredient Substances 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 125000002015 acyclic group Chemical group 0.000 description 1
- 230000033289 adaptive immune response Effects 0.000 description 1
- 239000001361 adipic acid Substances 0.000 description 1
- 235000011037 adipic acid Nutrition 0.000 description 1
- 229960000250 adipic acid Drugs 0.000 description 1
- AWUCVROLDVIAJX-UHFFFAOYSA-N alpha-glycerophosphate Natural products OCC(O)COP(O)(O)=O AWUCVROLDVIAJX-UHFFFAOYSA-N 0.000 description 1
- BJEPYKJPYRNKOW-UHFFFAOYSA-N alpha-hydroxysuccinic acid Natural products OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 150000001413 amino acids Chemical group 0.000 description 1
- 229910021529 ammonia Inorganic materials 0.000 description 1
- 150000003868 ammonium compounds Chemical class 0.000 description 1
- 239000000427 antigen Substances 0.000 description 1
- 230000000890 antigenic effect Effects 0.000 description 1
- 108091007433 antigens Proteins 0.000 description 1
- 102000036639 antigens Human genes 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 235000010323 ascorbic acid Nutrition 0.000 description 1
- 239000011668 ascorbic acid Substances 0.000 description 1
- 229960005070 ascorbic acid Drugs 0.000 description 1
- 235000003704 aspartic acid Nutrition 0.000 description 1
- 229960005261 aspartic acid Drugs 0.000 description 1
- 210000003719 b-lymphocyte Anatomy 0.000 description 1
- SRSXLGNVWSONIS-UHFFFAOYSA-N benzenesulfonic acid Chemical compound OS(=O)(=O)C1=CC=CC=C1 SRSXLGNVWSONIS-UHFFFAOYSA-N 0.000 description 1
- 229940092714 benzenesulfonic acid Drugs 0.000 description 1
- 235000010233 benzoic acid Nutrition 0.000 description 1
- 229960004365 benzoic acid Drugs 0.000 description 1
- GONOPSZTUGRENK-UHFFFAOYSA-N benzyl(trichloro)silane Chemical compound Cl[Si](Cl)(Cl)CC1=CC=CC=C1 GONOPSZTUGRENK-UHFFFAOYSA-N 0.000 description 1
- MSWZFWKMSRAUBD-UHFFFAOYSA-N beta-D-galactosamine Natural products NC1C(O)OC(CO)C(O)C1O MSWZFWKMSRAUBD-UHFFFAOYSA-N 0.000 description 1
- OQFSQFPPLPISGP-UHFFFAOYSA-N beta-carboxyaspartic acid Natural products OC(=O)C(N)C(C(O)=O)C(O)=O OQFSQFPPLPISGP-UHFFFAOYSA-N 0.000 description 1
- 229960003237 betaine Drugs 0.000 description 1
- 229920001400 block copolymer Polymers 0.000 description 1
- 230000036765 blood level Effects 0.000 description 1
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 229910001424 calcium ion Inorganic materials 0.000 description 1
- LSPHULWDVZXLIL-QUBYGPBYSA-N camphoric acid Chemical compound CC1(C)[C@H](C(O)=O)CC[C@]1(C)C(O)=O LSPHULWDVZXLIL-QUBYGPBYSA-N 0.000 description 1
- 150000001720 carbohydrates Chemical class 0.000 description 1
- 150000004649 carbonic acid derivatives Chemical class 0.000 description 1
- 150000001768 cations Chemical class 0.000 description 1
- 230000004663 cell proliferation Effects 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 210000000349 chromosome Anatomy 0.000 description 1
- 235000013985 cinnamic acid Nutrition 0.000 description 1
- 229930016911 cinnamic acid Natural products 0.000 description 1
- 230000007882 cirrhosis Effects 0.000 description 1
- 208000019425 cirrhosis of liver Diseases 0.000 description 1
- 229940126523 co-drug Drugs 0.000 description 1
- 229940124301 concurrent medication Drugs 0.000 description 1
- 230000021615 conjugation Effects 0.000 description 1
- 238000011443 conventional therapy Methods 0.000 description 1
- 229920001577 copolymer Polymers 0.000 description 1
- 229910001431 copper ion Inorganic materials 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 230000037213 diet Effects 0.000 description 1
- 235000005911 diet Nutrition 0.000 description 1
- ZBCBWPMODOFKDW-UHFFFAOYSA-N diethanolamine Chemical compound OCCNCCO ZBCBWPMODOFKDW-UHFFFAOYSA-N 0.000 description 1
- 201000010099 disease Diseases 0.000 description 1
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 239000003937 drug carrier Substances 0.000 description 1
- 229940126534 drug product Drugs 0.000 description 1
- 229940088679 drug related substance Drugs 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- CCIVGXIOQKPBKL-UHFFFAOYSA-M ethanesulfonate Chemical compound CCS([O-])(=O)=O CCIVGXIOQKPBKL-UHFFFAOYSA-M 0.000 description 1
- 229940012017 ethylenediamine Drugs 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- 210000002950 fibroblast Anatomy 0.000 description 1
- 235000019253 formic acid Nutrition 0.000 description 1
- 239000012458 free base Substances 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- 102000006640 gamma-Glutamyltransferase Human genes 0.000 description 1
- 229940044627 gamma-interferon Drugs 0.000 description 1
- 108091008053 gene clusters Proteins 0.000 description 1
- 229960002442 glucosamine Drugs 0.000 description 1
- 235000013922 glutamic acid Nutrition 0.000 description 1
- 239000004220 glutamic acid Substances 0.000 description 1
- 229940093915 gynecological organic acid Drugs 0.000 description 1
- 230000035876 healing Effects 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 208000010710 hepatitis C virus infection Diseases 0.000 description 1
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 description 1
- 229920001519 homopolymer Polymers 0.000 description 1
- XGIHQYAWBCFNPY-AZOCGYLKSA-N hydrabamine Chemical compound C([C@@H]12)CC3=CC(C(C)C)=CC=C3[C@@]2(C)CCC[C@@]1(C)CNCCNC[C@@]1(C)[C@@H]2CCC3=CC(C(C)C)=CC=C3[C@@]2(C)CCC1 XGIHQYAWBCFNPY-AZOCGYLKSA-N 0.000 description 1
- 229910000042 hydrogen bromide Inorganic materials 0.000 description 1
- 150000004679 hydroxides Chemical class 0.000 description 1
- 230000028993 immune response Effects 0.000 description 1
- 229940090438 infergen Drugs 0.000 description 1
- 239000007972 injectable composition Substances 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 108010055511 interferon alfa-2c Proteins 0.000 description 1
- 108010006088 interferon alfa-n1 Proteins 0.000 description 1
- 108010010648 interferon alfacon-1 Proteins 0.000 description 1
- 238000005342 ion exchange Methods 0.000 description 1
- 229910052742 iron Inorganic materials 0.000 description 1
- XEEYBQQBJWHFJM-UHFFFAOYSA-N iron Substances [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 1
- 230000007794 irritation Effects 0.000 description 1
- 239000004310 lactic acid Substances 0.000 description 1
- 235000014655 lactic acid Nutrition 0.000 description 1
- 210000000265 leukocyte Anatomy 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 239000012669 liquid formulation Substances 0.000 description 1
- 229910001416 lithium ion Inorganic materials 0.000 description 1
- 238000012317 liver biopsy Methods 0.000 description 1
- 238000004020 luminiscence type Methods 0.000 description 1
- 239000008176 lyophilized powder Substances 0.000 description 1
- 125000003588 lysine group Chemical group [H]N([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])(N([H])[H])C(*)=O 0.000 description 1
- 229910001425 magnesium ion Inorganic materials 0.000 description 1
- 159000000003 magnesium salts Chemical class 0.000 description 1
- 239000001630 malic acid Substances 0.000 description 1
- 235000011090 malic acid Nutrition 0.000 description 1
- 229960002510 mandelic acid Drugs 0.000 description 1
- 229910001437 manganese ion Inorganic materials 0.000 description 1
- 230000004060 metabolic process Effects 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 150000002739 metals Chemical class 0.000 description 1
- 229940098779 methanesulfonic acid Drugs 0.000 description 1
- WBYWAXJHAXSJNI-UHFFFAOYSA-N methyl p-hydroxycinnamate Natural products OC(=O)C=CC1=CC=CC=C1 WBYWAXJHAXSJNI-UHFFFAOYSA-N 0.000 description 1
- 150000007522 mineralic acids Chemical class 0.000 description 1
- LNOPIUAQISRISI-UHFFFAOYSA-N n'-hydroxy-2-propan-2-ylsulfonylethanimidamide Chemical compound CC(C)S(=O)(=O)CC(N)=NO LNOPIUAQISRISI-UHFFFAOYSA-N 0.000 description 1
- UQEIFYRRSNJVDO-UHFFFAOYSA-N n,n-dibenzyl-2-phenylethanamine Chemical compound C=1C=CC=CC=1CN(CC=1C=CC=CC=1)CCC1=CC=CC=C1 UQEIFYRRSNJVDO-UHFFFAOYSA-N 0.000 description 1
- FUZZWVXGSFPDMH-UHFFFAOYSA-N n-hexanoic acid Natural products CCCCCC(O)=O FUZZWVXGSFPDMH-UHFFFAOYSA-N 0.000 description 1
- KVBGVZZKJNLNJU-UHFFFAOYSA-N naphthalene-2-sulfonic acid Chemical compound C1=CC=CC2=CC(S(=O)(=O)O)=CC=C21 KVBGVZZKJNLNJU-UHFFFAOYSA-N 0.000 description 1
- 229910017604 nitric acid Inorganic materials 0.000 description 1
- 108020004707 nucleic acids Proteins 0.000 description 1
- 150000007523 nucleic acids Chemical class 0.000 description 1
- 102000039446 nucleic acids Human genes 0.000 description 1
- 239000002773 nucleotide Substances 0.000 description 1
- 125000003729 nucleotide group Chemical group 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 1
- 229940100688 oral solution Drugs 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 235000006408 oxalic acid Nutrition 0.000 description 1
- 238000004806 packaging method and process Methods 0.000 description 1
- WLJNZVDCPSBLRP-UHFFFAOYSA-N pamoic acid Chemical compound C1=CC=C2C(CC=3C4=CC=CC=C4C=C(C=3O)C(=O)O)=C(O)C(C(O)=O)=CC2=C1 WLJNZVDCPSBLRP-UHFFFAOYSA-N 0.000 description 1
- FJKROLUGYXJWQN-UHFFFAOYSA-N papa-hydroxy-benzoic acid Natural products OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 1
- 229920003175 pectinic acid Polymers 0.000 description 1
- 239000000137 peptide hydrolase inhibitor Substances 0.000 description 1
- 239000011129 pharmaceutical packaging material Substances 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- IUGYQRQAERSCNH-UHFFFAOYSA-N pivalic acid Chemical compound CC(C)(C)C(O)=O IUGYQRQAERSCNH-UHFFFAOYSA-N 0.000 description 1
- 239000000902 placebo Substances 0.000 description 1
- 229940068196 placebo Drugs 0.000 description 1
- 229920002401 polyacrylamide Polymers 0.000 description 1
- 229920000768 polyamine Chemical class 0.000 description 1
- 229920005862 polyol Polymers 0.000 description 1
- 150000003077 polyols Chemical class 0.000 description 1
- 229920001451 polypropylene glycol Polymers 0.000 description 1
- 229920002451 polyvinyl alcohol Polymers 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 229910001414 potassium ion Inorganic materials 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 150000003141 primary amines Chemical class 0.000 description 1
- 102000004196 processed proteins & peptides Human genes 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 235000019260 propionic acid Nutrition 0.000 description 1
- 229940095574 propionic acid Drugs 0.000 description 1
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 1
- 229940107700 pyruvic acid Drugs 0.000 description 1
- IUVKMZGDUIUOCP-BTNSXGMBSA-N quinbolone Chemical compound O([C@H]1CC[C@H]2[C@H]3[C@@H]([C@]4(C=CC(=O)C=C4CC3)C)CC[C@@]21C)C1=CCCC1 IUVKMZGDUIUOCP-BTNSXGMBSA-N 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 230000004043 responsiveness Effects 0.000 description 1
- 238000012340 reverse transcriptase PCR Methods 0.000 description 1
- 229960004889 salicylic acid Drugs 0.000 description 1
- 239000000523 sample Substances 0.000 description 1
- 150000003335 secondary amines Chemical class 0.000 description 1
- 230000036332 sexual response Effects 0.000 description 1
- AWUCVROLDVIAJX-GSVOUGTGSA-N sn-glycerol 3-phosphate Chemical compound OC[C@@H](O)COP(O)(O)=O AWUCVROLDVIAJX-GSVOUGTGSA-N 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 229910001415 sodium ion Inorganic materials 0.000 description 1
- 238000001179 sorption measurement Methods 0.000 description 1
- 239000008117 stearic acid Substances 0.000 description 1
- 229960004274 stearic acid Drugs 0.000 description 1
- 229950000244 sulfanilic acid Drugs 0.000 description 1
- 230000002459 sustained effect Effects 0.000 description 1
- 239000003826 tablet Substances 0.000 description 1
- NHKZSTHOYNWEEZ-AFCXAGJDSA-N taribavirin Chemical compound N1=C(C(=N)N)N=CN1[C@H]1[C@H](O)[C@H](O)[C@@H](CO)O1 NHKZSTHOYNWEEZ-AFCXAGJDSA-N 0.000 description 1
- 229950006081 taribavirin Drugs 0.000 description 1
- 235000002906 tartaric acid Nutrition 0.000 description 1
- 239000011975 tartaric acid Substances 0.000 description 1
- 229960001367 tartaric acid Drugs 0.000 description 1
- 150000003512 tertiary amines Chemical class 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- CBXCPBUEXACCNR-UHFFFAOYSA-N tetraethylammonium Chemical class CC[N+](CC)(CC)CC CBXCPBUEXACCNR-UHFFFAOYSA-N 0.000 description 1
- 229960004559 theobromine Drugs 0.000 description 1
- 238000011285 therapeutic regimen Methods 0.000 description 1
- 230000004797 therapeutic response Effects 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 1
- 238000011269 treatment regimen Methods 0.000 description 1
- IMFACGCPASFAPR-UHFFFAOYSA-N tributylamine Chemical compound CCCCN(CCCC)CCCC IMFACGCPASFAPR-UHFFFAOYSA-N 0.000 description 1
- YFTHZRPMJXBUME-UHFFFAOYSA-N tripropylamine Chemical compound CCCN(CCC)CCC YFTHZRPMJXBUME-UHFFFAOYSA-N 0.000 description 1
- 230000029812 viral genome replication Effects 0.000 description 1
- 229920003169 water-soluble polymer Polymers 0.000 description 1
- 230000003442 weekly effect Effects 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/4709—Non-condensed quinolines and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7042—Compounds having saccharide radicals and heterocyclic rings
- A61K31/7052—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides
- A61K31/7056—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing five-membered rings with nitrogen as a ring hetero atom
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/19—Cytokines; Lymphokines; Interferons
- A61K38/21—Interferons [IFN]
- A61K38/212—IFN-alpha
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6876—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes
- C12Q1/6883—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for diseases caused by alterations of genetic material
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/106—Pharmacogenomics, i.e. genetic variability in individual responses to drugs and drug metabolism
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/156—Polymorphic or mutational markers
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Medicinal Chemistry (AREA)
- Organic Chemistry (AREA)
- Veterinary Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Engineering & Computer Science (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Zoology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Epidemiology (AREA)
- Molecular Biology (AREA)
- Genetics & Genomics (AREA)
- Immunology (AREA)
- General Chemical & Material Sciences (AREA)
- Gastroenterology & Hepatology (AREA)
- Analytical Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Virology (AREA)
- Wood Science & Technology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Microbiology (AREA)
- Biotechnology (AREA)
- Oncology (AREA)
- Biophysics (AREA)
- Communicable Diseases (AREA)
- Biochemistry (AREA)
- Physics & Mathematics (AREA)
- General Engineering & Computer Science (AREA)
- Pathology (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Peptides Or Proteins (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
Abstract
【課題】本発明はIL28B 遺伝子付近に位置する遺伝子変化(非CC遺伝子型を有するSNP rs12979860及び非TT遺伝子型を有するSNP rs8099917 を含む)を有する患者のHCV 感染症を治療し、又はその一種以上の症候を軽減するためのこのような治療上の組み合わせ及びその使用方法を提供する。【解決手段】本発明は(a) 本明細書に記載された、化合物 (1)、又はその医薬上許される塩、(b) インターフェロンアルファ及び(c) リバビリンを含む治療上の組み合わせに関する。化合物 (1)はHCV NS3 セリンプロテアーゼの選択的かつ強力な阻害薬である。【選択図】なしThe present invention treats HCV infection in patients with genetic alterations (including SNP rs12979860 having a non-CC genotype and SNP rs8099917 having a non-TT genotype) located near the IL28B gene, or one or more thereof Such therapeutic combinations and methods of use thereof are provided to alleviate the symptoms. The present invention relates to a therapeutic combination comprising (a) a compound (1), or a pharmaceutically acceptable salt thereof, (b) interferon alpha and (c) ribavirin as described herein. Compound (1) is a selective and potent inhibitor of HCV NS3 serine protease. [Selection figure] None
Description
本発明は本明細書に記載される化合物 (1)、インターフェロンアルファ及びリバビリンを含む治療上の組み合わせに関する。また、本発明は非CC遺伝子型を含むSNP rs12979860及び非TT遺伝子型を含むSNP rs8099917 を含む、IL28B 遺伝子付近に位置する遺伝子変化を有すると同定された患者のHCV 感染症を治療し、又はその一種以上の症候を軽減するためのこのような治療上の組み合わせの使用方法に関する。また、本発明は本発明の治療上の組み合わせを含むキットを提供する。 The present invention relates to a therapeutic combination comprising compound (1) described herein, interferon alpha and ribavirin. The present invention also treats an HCV infection in a patient identified as having a genetic alteration located near the IL28B gene, including SNP rs12979860 containing a non-CC genotype and SNP rs8099917 containing a non-TT genotype, or It relates to the use of such therapeutic combinations for alleviating one or more symptoms. The present invention also provides kits comprising the therapeutic combinations of the present invention.
化学名:1-{[4-[8-ブロモ-2-(2-イソプロピルカルバモイル-チアゾール-4-イル)-7-メトキシ-キノリン-4-イルオキシ]-1-(R)-(2-シクロペンチルオキシカルボニルアミノ-3,3-(S)-ジメチル-ブチリル)-ピロリジン-(S)-2-カルボニル]-アミノ}-2-(S)-ビニル-シクロプロパン-(R)-カルボン酸を有する下記の式の化合物 (1)は、HCV NS3 セリンプロテアーゼの選択的かつ強力な阻害薬として知られており、HCV 感染症の治療に有益である。 Chemical Name: 1-{[4- [8-Bromo-2- (2-isopropylcarbamoyl-thiazol-4-yl) -7-methoxy-quinolin-4-yloxy] -1- (R)-(2-cyclopentyl Oxycarbonylamino-3,3- (S) -dimethyl-butyryl) -pyrrolidine- (S) -2-carbonyl] -amino} -2- (S) -vinyl-cyclopropane- (R) -carboxylic acid Compound (1) of the following formula is known as a selective and potent inhibitor of HCV NS3 serine protease and is useful for the treatment of HCV infection.
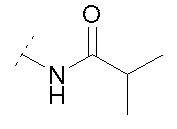
式中、Bは下記の基であり、
化合物 (1)は米国再発行特許第40,525号、米国特許第7,514,557 号及び同第7,585,845 号に開示されたHCV 阻害薬の非環式ペプチドシリーズの範囲内に入る。化合物 (1)は米国特許第7,585,845 号に化合物 # 1055 として、また米国特許第7,514,557 号に化合物 # 1008 として特別に開示されている。化合物 (1)、及びその医薬製剤は、先に引用された文献(これらの全てが本明細書に参考としてそのまま含まれる)に見られる一般操作に従って調製し得る。化合物 (1)の好ましい形態として、結晶性形態、特に結晶性ナトリウム塩形態が挙げられ、これは米国特許出願公開第2010/0093792号(また、参考として本明細書に含まれる)に記載されたように調製し得る。 Compound (1) falls within the acyclic peptide series of HCV inhibitors disclosed in US Reissued Patent No. 40,525, US Patent Nos. 7,514,557 and 7,585,845. Compound (1) is specifically disclosed as Compound # 1055 in US Pat. No. 7,585,845 and as Compound # 1008 in US Pat. No. 7,514,557. Compound (1), and pharmaceutical formulations thereof, can be prepared according to the general procedures found in the literature cited above, all of which are hereby incorporated by reference in their entirety. Preferred forms of compound (1) include crystalline forms, particularly crystalline sodium salt forms, which are described in US Patent Application Publication No. 2010/0093792 (also included herein by reference). Can be prepared as follows.
HCV NS3 セリンプロテアーゼの阻害薬としての化合物 (1)の活性及び患者のHCV 感染症の治療におけるその相当する実証された実用性を実証するデータが、米国特許第7,585,845 号だけでなく、化合物 (1)による予備臨床特性決定又は臨床試験結果を提示する多くの刊行物に見られる。例えば、Sulkowski MSら著, Hepatol (2009), 50巻, 2A頁, Abtract LB3;Sulkowski MSら著, J Hepatol (2010) 52巻, 補遺1, S462-S463頁, Abstract 1190; Berg ら著, Hepatol (2010), 52巻, 補遺S1, Abstract 804; 及びWhite PWら著, Antimicrob Agents Chemother (2010) 54(11):4611-4618を参照のこと。
HCV 感染症の治療のために化合物 (1)をインターフェロン−アルファ及びリバビリンとともに投与することに関する併用治療養生法が米国特許出願公開第2010/0068182号及び同第2011/0268700号に記載されている。
特別なHCV サブタイプ及び患者遺伝子亜型はHCV 治療に異なって応答し得ることが当業界で知られている。HCV 遺伝子型1aは遺伝子型1bよりも治療するのに従来困難であり、坑ウイルス治療に応答性ではない。例えば、Ghany, Marc ら著 “遺伝子型1慢性C型肝炎感染症の治療についてのアップデート: 肝臓疾患の研究のための米国協会による2011実務ガイドライン”, Hepatology, 54(4): 1433-44 (2011))を参照のこと。加えて、特にインターフェロンに基づく治療によれば、治療を受けている患者の、IL-28B (インターロイキン (IL) 28B 、またラムダインターフェロンと称される) の遺伝子クラスター内の染色体19の長いアームに位置する特別な単一ヌクレオチド多形 (SNP)が、坑ウイルス治療に対するその患者の応答性に直接影響し得る。特に、SNP rs12979860の非CC遺伝子型又はSNP rs8099917 の非TT遺伝子型を有する患者はCC又はTT遺伝子型を有する患者よりも治療するのに従来困難であり、持続ウイルス学的応答 (SVR)に関して応答性ではない。ゲノムワイド分析においてSVR と最も強く関連するSNP はrs12979860、続いてrs8099917 であった。例えば、Geら著, Nature, 461:399-401 (2009)及びBalagopal 著, Gastroenterology, 139:1865-1876 (2010)を参照のこと。或る研究は治療応答にほぼ7倍の差を示した。G.Cairns著, “C型肝炎治療を助ける遺伝子変異体がHIV 治療を阻害し得る”, 2011, at: http://www.bhiva.org/News.aspx?NewsID=a7503829-94b9-4d2f-bd91-1d2fbaad6e8dを参照のこと。
SVR 率のこの差及び疾患の治癒はNS3/4 HCV プロテアーゼ阻害薬 (テラプレバー) がペギル化(pegylated) インターフェロンアルファ及びリバビリン (PegIFN/RBV) による通常の養生法に加えられた場合に変化しなかったことが更に知られている。Akuta ら著, Hepatology, 52: 421-429 (2010)により示されたように、非CC又は非TT遺伝子型を有する患者はIL28B 付近に位置する、夫々、rs12979860又はrs8099917 中の遺伝子変化によりCC又はTT遺伝子型と較べて51.5 %又は56.2 %だけ強く異なるSVR 率を経験した。最後にIL28B 遺伝子型関連がまたHCV 患者の無インターフェロン治療中に早いウイルス動態で見られていた。Chu ら著, “慢性C型肝炎の患者の無インターフェロン治療中の早いウイルス動態についてのIL28B 遺伝子型の効果”, Gastroenterology (2012)(現在印刷中、オンラインで入手し得る, January 13, 2012)を参照のこと。
Data demonstrating the activity of compound (1) as an inhibitor of HCV NS3 serine protease and its corresponding demonstrated utility in the treatment of HCV infection in patients is not only U.S. Patent No. 7,585,845, but also compound (1 ) In many publications that present preliminary clinical characterization or clinical trial results. For example, Sulkowski MS et al., Hepatol (2009), 50, 2A, Abtract LB3; Sulkowski MS et al., J Hepatol (2010) 52, Addendum 1, S462-S463, Abstract 1190; Berg et al., Hepatol. (2010), 52, Addendum S1, Abstract 804; and White PW et al., Antimicrob Agents Chemother (2010) 54 (11): 4611-4618.
Combination therapy regimens involving the administration of compound (1) with interferon-alpha and ribavirin for the treatment of HCV infection are described in US 2010/0068182 and 2011/0268700.
It is known in the art that particular HCV subtypes and patient gene subtypes can respond differently to HCV treatment. HCV genotype 1a has traditionally been more difficult to treat than genotype 1b and is not responsive to antiviral treatment. For example, Ghany, Marc et al., “Updates on the Treatment of Genotype 1 Chronic Hepatitis C Infection: 2011 Practice Guidelines by the American Association for the Study of Liver Disease”, Hepatology, 54 (4): 1433-44 (2011 ))checking. In addition, especially with interferon-based therapy, the long arm of chromosome 19 within the IL-28B (interleukin (IL) 28B, also referred to as lambda interferon) gene cluster in patients undergoing treatment The particular single nucleotide polymorphism (SNP) located can directly affect the patient's responsiveness to antiviral therapy. In particular, patients with a non-CC genotype of SNP rs12979860 or a non-TT genotype of SNP rs8099917 are conventionally more difficult to treat than patients with CC or TT genotype and respond with respect to sustained virological response (SVR) Not sex. The SNP most strongly associated with SVR in genome-wide analysis was rs12979860, followed by rs8099917. See, for example, Ge et al., Nature, 461: 399-401 (2009) and Balagopal, Gastroenterology, 139: 1865-1876 (2010). One study showed a nearly 7-fold difference in treatment response. G. Cairns, “Gene variants that help treat hepatitis C can inhibit HIV treatment”, 2011, at: http://www.bhiva.org/News.aspx?NewsID=a7503829-94b9-4d2f- See bd91-1d2fbaad6e8d.
This difference in SVR rates and disease healing did not change when NS3 / 4 HCV protease inhibitor (Teraprever) was added to conventional regimens with pegylated interferon alfa and ribavirin (PegIFN / RBV) It is further known. As shown by Akuta et al., Hepatology, 52: 421-429 (2010), patients with non-CC or non-TT genotypes are located near IL28B, respectively, due to genetic changes in rs12979860 or rs8099917, or We experienced SVR rates that differed significantly by 51.5% or 56.2% compared to the TT genotype. Finally, an IL28B genotype association was also seen with early viral kinetics during interferon-free treatment in HCV patients. Chu et al., “Effect of IL28B genotype on early viral kinetics during interferon-free treatment in patients with chronic hepatitis C”, Gastroenterology (2012) (currently printed and available online, January 13, 2012) See
こうして、一層治療し難い患者分集団、特にHCV サブタイプ1aを示し、IL28B 遺伝子付近に位置するSNP rs12979860の非CC遺伝子型又はSNP rs8099917 の非TT遺伝子型を有する患者分集団に対してさえも有効である療法についての要望が当業界にある。 Thus, even more difficult to treat patient populations, particularly those with SNP rs12979860 non-CC genotypes or SNP rs8099917 non-TT genotypes that show HCV subtype 1a and are located near the IL28B gene There is a need in the industry for therapies that are.
化合物 (1)、又はその医薬上許される塩と、インターフェロンアルファ及びリバビリンの治療上の組み合わせは、HCV を治療するのに従来困難な患者分集団、特にSNP rs12979860の非CC遺伝子型又はSNP rs8099917 の非TT遺伝子型(両方ともIL28B 遺伝子の付近に位置する)を有するこれらの患者でさえも治療するのに良好な有効性を有することが今発見された。
PegIFN/RBV及びNS3/4 HCV プロテアーゼ阻害薬テラプレバーで治療された患者で観察されたSVR 率の予想されたIL28B-関連の差は本発明の治療上の組み合わせを使用する場合に広く消失すること、及び好ましくない遺伝子型非CCもしくはTT又は好ましくないHCV サブタイプ1a感染症を有する患者がSVR に関して一貫して高い治癒率に達したことは驚くべきことである。
The therapeutic combination of compound (1), or a pharmaceutically acceptable salt thereof, and interferon alfa and ribavirin, can be used in patient populations that are conventionally difficult to treat HCV, particularly non-CC genotypes of SNP rs12979860 or SNP rs8099917. It has now been discovered that even these patients with non-TT genotypes (both located near the IL28B gene) have good efficacy in treating them.
The expected IL28B-related differences in SVR rates observed in patients treated with the PegIFN / RBV and NS3 / 4 HCV protease inhibitor terrapreber are widely lost when using the therapeutic combinations of the present invention; And it is surprising that patients with unfavorable genotype non-CC or TT or unfavorable HCV subtype 1a infection have consistently achieved high cure rates for SVR.
本発明は患者に本明細書に特定されたインターフェロンアルファ及びリバビリンと一緒に、本明細書に特定された化合物 (1)又はその医薬上許される塩を含む治療上の組み合わせを投与する工程を含む患者のHCV 感染症を治療し、又はその一種以上の症候を軽減する方法を提供し、その患者はIL28B 遺伝子の付近に位置するSNP rs12979860の非CC遺伝子型又はSNP rs8099917 の非TT遺伝子型を有する。その組み合わせの3種の活性成分は養生法の一部として、同時又は別々に投与し得る。
更に、本発明は一種以上の用量の化合物 (1)、又はその医薬上許される塩、並びに(b) IL28B 遺伝子の付近に位置するSNP rs12979860の非CC遺伝子型又はSNP rs8099917 の非TT遺伝子型を有する患者のHCV 感染症の治療のための化合物 (1)、又はその医薬上許される塩、インターフェロンアルファ、及びリバビリンの同時投与に関する記述された指示を含むパッケージを含む包装された医薬組成物を提供する。
The invention includes the step of administering to a patient a therapeutic combination comprising a compound (1) identified herein or a pharmaceutically acceptable salt thereof together with interferon alpha and ribavirin identified herein. Provide a method of treating a patient's HCV infection or alleviating one or more symptoms thereof, wherein the patient has a non-CC genotype of SNP rs12979860 or a non-TT genotype of SNP rs8099917 located in the vicinity of the IL28B gene . The three active ingredients of the combination can be administered simultaneously or separately as part of the regimen.
Furthermore, the present invention relates to one or more doses of compound (1), or a pharmaceutically acceptable salt thereof, and (b) a non-CC genotype of SNP rs12979860 or a non-TT genotype of SNP rs8099917 located near the IL28B gene. Providing a packaged pharmaceutical composition comprising a package comprising written instructions for the simultaneous administration of compound (1), or a pharmaceutically acceptable salt thereof, interferon alfa and ribavirin, for the treatment of HCV infection in a patient having To do.
定義
“化合物 (1)”は先に定義されたとおりである。
本明細書に使用される“HCV 感染症”はサブタイプ1-6 を含む、C型肝炎ウイルスのあらゆるサブタイプによる感染症を意味し、急性及び慢性の両方のHCV 感染症を含む。
“インターフェロン”はウイルス複製及び細胞増殖を抑制し、免疫応答を変調する高度に相同の種特異性タンパク質のファミリーの員を意味する。ヒトインターフェロンはそれらの細胞起源及び抗原性に基づいて三つのクラス:α-インターフェロン (白血球), β-インターフェロン (繊維芽細胞) 及びγ-インターフェロン (B細胞) に分類される。夫々のグループの組換え形態が開発され、市販されている。夫々のグループ中のサブタイプは抗原/構造特性に基づく。異なるアミノ酸配列を有する少なくとも24のインターフェロンアルファ (サブタイプA〜Hに分類される) がこれらのペプチドをコードするDNA を単離し、配列決定することにより同定されていた。“α -インターフェロン”、“アルファ-インターフェロン”及び“インターフェロンアルファ”という用語はこの出願で互換可能に使用されてこのグループの員を記載する。コンセンサスインターフェロンを含む、天然産及び組換えの両方のアルファ-インターフェロンが、本発明の実施に使用されてもよい。
本発明に適したインターフェロン-アルファとして、組換えインターフェロンアルファ-2b、例えば、INTRON(登録商標)-A インターフェロン及びVIRAFERON(登録商標); 組換えインターフェロンアルファ-2a 、例えば、ROFERON(登録商標)インターフェロン; 組換えインターフェロンアルファ-2c 、例えば、BEROFOR(登録商標) アルファ 2 インターフェロン; インターフェロンアルファ-n1 、天然アルファインターフェロンの精製ブレンド、例えば、SUMIFERON (登録商標)又はWELLFERON (登録商標)インターフェロンアルファ-n1 (INS); 又はコンセンサスアルファインターフェロン、例えば、米国特許第4,897,471号及び同第4,695,623号に記載されたもの; 或いはインターフェロンアルファ-n3、天然アルファインターフェロンの混合物、例えば、ALFERON(登録商標)が挙げられるが、これらに限定されない。インターフェロンアルファ-2a 又はアルファ2bの使用が好ましい。インターフェロンアルファ2bの製造が米国特許第4,530,901 号に記載されている。
“インターフェロンアルファ”という用語は更にインターフェロンアルファ、好ましくはインターフェロンアルファ-2a 及び-2b のポリエチレングリコール変性コンジュゲートを意味するこれらの“ペギル化”類似体を含むことが意図されている。好ましいポリエチレン−グリコール−インターフェロンアルファ-2b コンジュゲートはPEG12000 -インターフェロンアルファ 2bである。本明細書に使用される“PEG12000-IFN アルファ”という用語は国際特許出願WO 95/13090の方法に従って調製されるようなコンジュゲートを意味し、インターフェロンアルファ-2a 又は-2b アミノ基の間にウレタン結合を含み、ポリエチレングリコールが12000 の平均分子量を有する。
The definition “compound (1)” is as defined above.
As used herein, “HCV infection” refers to an infection caused by any subtype of hepatitis C virus, including subtypes 1-6, and includes both acute and chronic HCV infections.
“Interferon” means a member of a family of highly homologous species-specific proteins that inhibit viral replication and cell proliferation and modulate the immune response. Human interferons are divided into three classes based on their cellular origin and antigenicity: α-interferon (leukocytes), β-interferon (fibroblasts) and γ-interferon (B cells). Recombinant forms of each group have been developed and are commercially available. The subtypes in each group are based on antigen / structural characteristics. At least 24 interferon alphas (classified as subtypes A to H) having different amino acid sequences have been identified by isolating and sequencing the DNA encoding these peptides. The terms “α-interferon”, “alpha-interferon” and “interferon alpha” are used interchangeably in this application to describe members of this group. Both naturally occurring and recombinant alpha-interferons, including consensus interferons, may be used in the practice of the present invention.
Interferon-alpha suitable for the present invention includes recombinant interferon alpha-2b, such as INTRON®-A interferon and VIRAFERON®; recombinant interferon alpha-2a, such as ROFERON® interferon; Recombinant interferon alpha-2c, eg, BEROFOR® alpha 2 interferon; interferon alpha-n1, a purified blend of natural alpha interferon, eg, SUMIFERON® or WELLFERON® interferon alpha-n1 (INS) Or a consensus alpha interferon, such as those described in US Pat. Nos. 4,897,471 and 4,695,623; or a mixture of interferon alpha-n3 and natural alpha interferon, such as ALFERON®. It is, but is not limited thereto. The use of interferon alpha-2a or alpha 2b is preferred. The manufacture of interferon alpha 2b is described in US Pat. No. 4,530,901.
The term “interferon alpha” is further intended to include these “pegylated” analogs which refer to polyethylene glycol modified conjugates of interferon alpha, preferably interferon alpha-2a and -2b. A preferred polyethylene-glycol-interferon alpha-2b conjugate is PEG 12000 -interferon alpha 2b. As used herein, the term “PEG 12000- IFN alpha” refers to a conjugate as prepared according to the method of International Patent Application WO 95/13090, between an interferon alpha-2a or −2b amino group. Contains urethane linkages and polyethylene glycol has an average molecular weight of 12000.
好ましいPEG12000-インターフェロンアルファ-2bはPEG ポリマーをIFN アルファ-2b 分子中のリシン残基のエプシロンアミノ基に結合することにより調製される。単一PEG12000分子がウレタン結合によりIFN アルファ-2b 分子の遊離アミノ基に複合される。このコンジュゲートは結合されたPEG12000の分子量により特性決定される。PEG12000-IFN アルファ-2bコンジュゲートは注射のための凍結乾燥粉末として製剤化される。PEG とのIFN アルファの複合の目的はその血漿半減期を有意に延長することによりタンパク質の送出を改良し、それによりIFN アルファの延長された活性を与えることである。
本発明に使用し得るインターフェロンアルファの特に好ましいコンジュゲートはペギル化アルファ-インターフェロン、例えば、ペギル化インターフェロンアルファ-2a、ペギル化インターフェロンアルファ-2b、ペギル化コンセンサスインターフェロン又はペギル化 精製インターフェロンアルファ生成物である。ペギル化インターフェロンアルファ-2a は、例えば、欧州特許第EP 0 593 868号に記載されており、例えば、商品名PEGASYS (登録商標)(Hoffmann-La Roche) として市販されている。ペギル化インターフェロンアルファ-2b は、例えば、米国特許第5,908,621 号及びWO 98/48840 に記載されており、例えば、商品名PEG-INTRON(登録商標) A (Schering Plough)として市販されている。ペギル化コンセンサスインターフェロンはWO 96/11953 に記載されている。好ましいペギル化アルファインターフェロンはペギル化インターフェロンアルファ-2a 及びペギル化インターフェロンアルファ-2b である。また、ペギル化コンセンサスインターフェロンが好ましい。
A preferred PEG 12000 -interferon alpha-2b is prepared by attaching a PEG polymer to the epsilon amino group of a lysine residue in the IFN alpha-2b molecule. A single PEG 12000 molecule is conjugated to the free amino group of the IFN alpha-2b molecule via a urethane linkage. This conjugate is characterized by the molecular weight of PEG 12000 attached. PEG 12000 -IFN alpha-2b conjugate is formulated as a lyophilized powder for injection. The purpose of IFN alpha conjugation with PEG is to improve protein delivery by significantly extending its plasma half-life, thereby providing extended activity of IFN alpha.
Particularly preferred conjugates of interferon alpha that can be used in the present invention are pegylated alpha-interferon, such as pegylated interferon alpha-2a, pegylated interferon alpha-2b, pegylated consensus interferon or pegylated purified interferon alpha product. . Pegylated interferon alpha-2a is described, for example, in European Patent No. EP 0 593 868, and is commercially available, for example, under the trade name PEGASYS® (Hoffmann-La Roche). Pegylated interferon alpha-2b is described, for example, in US Pat. No. 5,908,621 and WO 98/48840 and is commercially available, for example, under the trade name PEG-INTRON® A (Schering Plow). Pegylated consensus interferon is described in WO 96/11953. Preferred pegylated alpha interferons are pegylated interferon alpha-2a and pegylated interferon alpha-2b. Pegylated consensus interferon is also preferred.
“インターフェロンアルファ”という用語はインターフェロンアルファを水溶性ポリマーにカップリングすることにより調製し得るその他のインターフェロンアルファコンジュゲートを更に含む。このようなポリマーの非限定リストはその他のポリアルキレンオキサイドホモポリマー、例えば、ポリエチレングリコール (PEG)、ポリプロピレングリコール、ポリオキシエチレン化ポリオール、これらのコポリマー及びこれらのブロックコポリマーを含む。ポリアルキレンオキサイドをベースとするポリマーの代替物として、有効に非抗原性の物質、例えば、デキストラン、ポリビニルピロリドン、ポリアクリルアミド、ポリビニルアルコール、炭水化物をベースとするポリマー等が使用し得る。このようなインターフェロンアルファ−ポリマーコンジュゲートが米国特許第4,766,106 号、同第4,917,888 号、欧州特許出願第0 236 987 号、同第0510 356号、同第0 593 868 号及び同第0 809 996 号同第 (ペギル化インターフェロンアルファ-2a)並びに国際特許公開第WO 95/13090 号に記載されている。
“インターフェロンアルファ”という用語はインターフェロンアルファの融合タンパク質、例えば、インターフェロン-α-2a、インターフェロン- α-2b 、コンセンサスインターフェロン又は精製インターフェロン-α 生成物(これらのそれぞれが別のタンパク質と融合される)の融合タンパク質を更に含む。或る好ましい融合タンパク質は米国特許第6,972,322 号並びに国際特許公開WO2005/003296 及びWO2005/077042 に記載されたようなインターフェロン (例えば、インターフェロン-α-2b) 及びアルブミンを含む。また、コンセンサスインターフェロン、例えば、INFERGEN(登録商標)が含まれる。
“医薬上許される塩”という用語は、理にかなった医療判断の範囲内で、不当な毒性、刺激、アレルギー反応等を生じないでヒト及び下等動物の組織と接触しての使用に適し、妥当な利益/リスク比と釣り合い、一般に水溶性もしくは油溶性又は水分散性もしくは油分散性であり、それらの意図される使用に有効である式 (1)の化合物の塩を意味する。
その用語は医薬上許される酸付加塩及び医薬上許される塩基付加塩を含む。好適な塩のリストが、例えば、S.M.Birge ら著, J.Pharm.Sci., 1977, 66, 1-19頁に見られる。
“医薬上許される酸付加塩”という用語は遊離塩基の生物学的有効性及び性質を保持し、生物学的に、又はそれ以外に望ましくなくはなく、無機酸、例えば、塩酸、臭化水素酸、硫酸、スルファミン酸、硝酸、リン酸等、及び有機酸、例えば、酢酸、トリフルオロ酢酸、アジピン酸、アスコルビン酸、アスパラギン酸、ベンゼンスルホン酸、安息香酸、酪酸、ショウノウ酸、ショウノウスルホン酸、ケイ皮酸、クエン酸、ジグルコン酸、エタンスルホン酸、グルタミン酸、グリコール酸、グリセロリン酸、ヘミスルフィン酸、ヘキサン酸、ギ酸、フマル酸、2-ヒドロキシエタンスルホン酸(イセチオン酸)、乳酸、ヒドロキシマレイン酸、リンゴ酸、マロン酸、マンデル酸、メシチレンスルホン酸、メタンスルホン酸、ナフタレンスルホン酸、ニコチン酸、2-ナフタレンスルホン酸、シュウ酸、パモ酸、ペクチン酸、フェニル酢酸、3-フェニルプロピオン酸、ピバル酸、プロピオン酸、ピルビン酸、サリチル酸、ステアリン酸、コハク酸、スルファニル酸、酒石酸、p-トルエンスルホン酸、ウンデカン酸等で生成されるこれらの塩を意味する。
The term “interferon alpha” further includes other interferon alpha conjugates that can be prepared by coupling interferon alpha to a water soluble polymer. A non-limiting list of such polymers includes other polyalkylene oxide homopolymers such as polyethylene glycol (PEG), polypropylene glycol, polyoxyethylenated polyols, copolymers thereof and block copolymers thereof. As an alternative to polymers based on polyalkylene oxides, effectively non-antigenic substances such as dextran, polyvinylpyrrolidone, polyacrylamide, polyvinyl alcohol, carbohydrate based polymers and the like can be used. Such interferon alpha-polymer conjugates are described in U.S. Pat.Nos. 4,766,106, 4,917,888, European Patent Applications 0 236 987, 0510 356, 0 593 868 and 0 809 996. No. (Pegylated Interferon Alpha-2a) as well as International Patent Publication No. WO 95/13090.
The term “interferon alpha” refers to an interferon alpha fusion protein, eg, interferon-α-2a, interferon-α-2b, consensus interferon or purified interferon-α product, each of which is fused to another protein Further comprising a fusion protein. Some preferred fusion proteins include interferon (eg, interferon-α-2b) and albumin as described in US Pat. No. 6,972,322 and International Patent Publications WO2005 / 003296 and WO2005 / 077042. Also included are consensus interferons such as INFERGEN®.
The term "pharmaceutically acceptable salt" is suitable for use in contact with human and lower animal tissues without causing undue toxicity, irritation, allergic reactions, etc., within reasonable medical judgment. Means a salt of a compound of formula (1) that is commensurate with a reasonable benefit / risk ratio and generally water or oil soluble or water dispersible or oil dispersible and effective for their intended use.
The term includes pharmaceutically acceptable acid addition salts and pharmaceutically acceptable base addition salts. A list of suitable salts can be found, for example, in SMBirge et al., J. Pharm. Sci., 1977, 66, pages 1-19.
The term “pharmaceutically acceptable acid addition salt” retains the biological effectiveness and properties of the free base, and is not biologically or otherwise undesirable, and includes inorganic acids such as hydrochloric acid, hydrogen bromide. Acids, sulfuric acid, sulfamic acid, nitric acid, phosphoric acid, and organic acids such as acetic acid, trifluoroacetic acid, adipic acid, ascorbic acid, aspartic acid, benzenesulfonic acid, benzoic acid, butyric acid, camphoric acid, camphorsulfonic acid, Cinnamic acid, citric acid, digluconic acid, ethanesulfonic acid, glutamic acid, glycolic acid, glycerophosphoric acid, hemisulphinic acid, hexanoic acid, formic acid, fumaric acid, 2-hydroxyethanesulfonic acid (isethionic acid), lactic acid, hydroxymaleic acid, Malic acid, malonic acid, mandelic acid, mesitylenesulfonic acid, methanesulfonic acid, naphthalenesulfonic acid Nicotinic acid, 2-naphthalenesulfonic acid, oxalic acid, pamoic acid, pectinic acid, phenylacetic acid, 3-phenylpropionic acid, pivalic acid, propionic acid, pyruvic acid, salicylic acid, stearic acid, succinic acid, sulfanilic acid, tartaric acid, p -These salts produced with toluenesulfonic acid, undecanoic acid and the like are meant.
“医薬上許される塩基付加塩” という用語は遊離酸の生物学的有効性及び性質を保持し、生物学的に、又はそれ以外に望ましくなくはなく、無機塩気、例えば、アンモニア又はアンモニウムもしくは金属陽イオン、例えば、ナトリウムイオン、カリウムイオン、リチウムイオン、カルシウムイオン、マグネシウムイオン、鉄イオン、亜鉛イオン、銅イオン、マンガンイオン、アルミニウムイオン等の水酸化物、炭酸塩、もしくは重炭酸で生成されるこれらの塩を意味する。アンモニウム塩、カリウム塩、ナトリウム塩、カルシウム塩、及びマグネシウム塩が特に好ましい。医薬上許される有機無毒性塩基から誘導される塩として、一級アミン、二級アミン、及び三級アミン、四級アミン化合物、置換アミン(天然産置換アミンを含む)、環状アミン並びに塩基性イオン交換樹脂、例えば、メチルアミン、ジメチルアミン、トリメチルアミン、エチルアミン、ジエチルアミン、トリエチルアミン、イソプロピルアミン、トリプロピルアミン、トリブチルアミン、エタノールアミン、ジエタノールアミン、2-ジメチルアミノエタノール、2-ジエチルアミノエタノール、ジシクロヘキシルアミン、リシン、アルギニン、ヒスチジン、カフェイン、ヒドラバミン、コリン、ベタイン、エチレンジアミン、グルコサミン、メチルグルカミン、テオブロミン、プリン、ピペラジン、ピペリジン、N-エチルピペリジン、テトラメチルアンモニウム化合物、テトラエチルアンモニウム化合物、ピリジン、N,N-ジメチルアニリン、N-メチルピペリジン、N-メチルモルホリン、ジシクロヘキシルアミン、ジベンジルアミン、N,N-ジベンジルフェネチルアミン、1-エフェナミン、N,N’-ジベンジルエチレンジアミン、ポリアミン樹脂等の塩が挙げられる。特に好ましい有機無毒性塩基はイソプロピルアミン、ジエチルアミン、エタノールアミン、トリメチルアミン、ジシクロヘキシルアミン、コリン、及びカフェインである。 The term “pharmaceutically acceptable base addition salt” retains the biological effectiveness and properties of the free acid and is not biologically or otherwise undesirable, such as inorganic salts such as ammonia or ammonium or metals. Produced with cations such as hydroxides, carbonates or bicarbonates such as sodium ions, potassium ions, lithium ions, calcium ions, magnesium ions, iron ions, zinc ions, copper ions, manganese ions, aluminum ions, etc. These salts are meant. Particularly preferred are the ammonium, potassium, sodium, calcium, and magnesium salts. Salts derived from pharmaceutically acceptable organic non-toxic bases include primary amines, secondary amines, and tertiary amines, quaternary amine compounds, substituted amines (including naturally occurring substituted amines), cyclic amines, and basic ion exchange. Resins such as methylamine, dimethylamine, trimethylamine, ethylamine, diethylamine, triethylamine, isopropylamine, tripropylamine, tributylamine, ethanolamine, diethanolamine, 2-dimethylaminoethanol, 2-diethylaminoethanol, dicyclohexylamine, lysine, arginine , Histidine, caffeine, hydrabamine, choline, betaine, ethylenediamine, glucosamine, methylglucamine, theobromine, purine, piperazine, piperidine, N-ethylpiperidine, tetramethi Ammonium compounds, tetraethylammonium compounds, pyridine, N, N-dimethylaniline, N-methylpiperidine, N-methylmorpholine, dicyclohexylamine, dibenzylamine, N, N-dibenzylphenethylamine, 1-ephenamine, N, N'- Examples thereof include salts of dibenzylethylenediamine and polyamine resin. Particularly preferred organic non-toxic bases are isopropylamine, diethylamine, ethanolamine, trimethylamine, dicyclohexylamine, choline, and caffeine.
“リバビリン”はICN Pharmaceuticals 社(コスタ・メサ、カリフォルニア)から入手し得る、1-β-D-リボフラノシル-1H-1,2,4-トリアゾール-3-カルボキサミドを表し、Merck Index, 化合物No.8199, 第11編に記載されている。その製造及び製剤化が米国特許第4,211,771 号に記載されている。好ましい市販のリバビリン製品として、REBETOL (登録商標)及びCOPEGUS (登録商標)が挙げられる。更に、その用語はその誘導体又は類似体、例えば、米国特許第6,063,772 号、同第6,403,564 号及び同第6,277,830 号に記載されたものを含む。例えば、誘導体又は類似体として、変性リバビリン、例えば、5’-アミノエステル、リバビリンのICN PharmaceuticalのL-鏡像体 (ICN 17261)、リバビリンの2'-デオキシ誘導体及びリバビリンの3-カルボキシアミジン誘導体、ビラミジン (既にリバミジンとして知られている) 等が挙げられる。
本明細書に使用される“治療上の組み合わせ”という用語は一種以上の活性薬物物質、すなわち、治療実用性を有する化合物の組み合わせを意味する。典型的には、本発明の治療上の組み合わせ中のこのような夫々の化合物はその化合物及び医薬上許される担体を含む医薬組成物中に存在するであろう。本発明の治療上の組み合わせ中の化合物は、養生法の一部として、同時又は別々に投与されてもよい。
“Ribavirin” refers to 1-β-D-ribofuranosyl-1H-1,2,4-triazole-3-carboxamide, available from ICN Pharmaceuticals (Costa Mesa, Calif.), Merck Index, Compound No. 8199 , 11th edition. Its manufacture and formulation is described in US Pat. No. 4,211,771. Preferred commercially available ribavirin products include REBETOL® and COPEGUS®. Further, the term includes derivatives or analogs thereof, such as those described in US Pat. Nos. 6,063,772, 6,403,564 and 6,277,830. For example, derivatives or analogs such as modified ribavirin, such as 5′-aminoesters, ICN Pharmaceutical L-enantiomers of ribavirin (ICN 17261), 2′-deoxy derivatives of ribavirin and 3-carboxyamidine derivatives of ribavirin, viramidine (Already known as rivamidine) and the like.
As used herein, the term “therapeutic combination” means a combination of one or more active drug substances, ie, compounds having therapeutic utility. Typically, each such compound in the therapeutic combinations of the present invention will be in a pharmaceutical composition comprising that compound and a pharmaceutically acceptable carrier. The compounds in the therapeutic combinations of the present invention may be administered simultaneously or separately as part of a regimen.
本発明の実施態様
一般の実施態様によれば、本発明はインターフェロンアルファ及びリバビリンと一緒に、本明細書に特定された化合物 (1)、又はその医薬上許される塩を含む治療上の組み合わせを患者に投与する工程を含む患者のHCV 感染症を治療し、又はその一種以上の症候を軽減する方法を提供し、その患者はIL28B 遺伝子付近に位置するSNP rs12979860の非CC遺伝子型又はSNP rs8099917 の非TT遺伝子型を有する。別の実施態様において、本発明は患者のC型肝炎ウイルス (HCV)感染症を治療し、又はその一種以上の症候を軽減するための医薬キットの調製のための本明細書に特定された化合物 (1) 、又はその医薬上許される塩、インターフェロンアルファ、及びリバビリンの使用を教示し、その患者はIL28B 遺伝子付近に位置するSNP rs12979860の非CC遺伝子型又はSNP rs8099917 の非TT遺伝子型を有する。
本発明の治療上の組み合わせを投与する際に、夫々の活性薬剤が同時に一緒に、又は異なる時点で別々の投薬投与で別々に投与し得る。本発明は本明細書に特定された3種治療上の組み合わせを投与する場合の全てのこのような投薬養生法を意図し、これらを含む。
この併用療法は全ての遺伝子型に対して有効であると予想されるが、サブタイプ1a及び1bを含み、またIL28B 遺伝子付近に位置するSNP rs12979860の非CC遺伝子型又はSNP rs8099917 の非TT遺伝子型を有する、HCV 遺伝子型1 感染症を治療するのに特に有効であることが実証された。特別な実施態様は下記の患者分集団を含む。
(1)HCV サブタイプ 1a及び/又はSNP rs12979860のC/T 遺伝子型
(2)HCV サブタイプ 1a及び/又はSNP rs12979860のT/T 遺伝子型
(3)HCV サブタイプ 1b及び/又はSNP rs12979860のC/T 遺伝子型
(4)HCV サブタイプ 1b及び/又はSNP rs12979860のT/T 遺伝子型
(5)HCV サブタイプ 1a及び/又はSNP rs8099917 のG/T 遺伝子型
(6)HCV サブタイプ 1a及び/又はSNP rs8099917 のG/G 遺伝子型
(7)HCV サブタイプ 1b及び/又はSNP rs8099917 のG/T 遺伝子型
(8)HCV サブタイプ 1b及び/又はSNP rs8099917 のG/G 遺伝子型。
Embodiments of the Invention According to a general embodiment, the present invention provides a therapeutic combination comprising a compound (1) identified herein, or a pharmaceutically acceptable salt thereof, together with interferon alpha and ribavirin. A method of treating a patient's HCV infection or reducing one or more symptoms thereof comprising the step of administering to the patient, wherein the patient is a non-CC genotype of SNP rs12979860 or SNP rs8099917 located near the IL28B gene. Has a non-TT genotype. In another embodiment, the invention provides a compound identified herein for the preparation of a pharmaceutical kit for treating hepatitis C virus (HCV) infection in a patient or alleviating one or more symptoms thereof. (1) or the use of a pharmaceutically acceptable salt thereof, interferon alpha, and ribavirin, the patient having a non-CC genotype of SNP rs12979860 or a non-TT genotype of SNP rs8099917 located near the IL28B gene.
In administering the therapeutic combinations of the present invention, each active agent may be administered together at the same time or separately in separate dosages at different times. The present invention contemplates and includes all such dosing regimens when administering the three therapeutic combinations identified herein.
This combination therapy is expected to be effective for all genotypes, but includes subtypes 1a and 1b and is located near the IL28B gene, non-CC genotype of SNP rs12979860 or non-TT genotype of SNP rs8099917 Has been demonstrated to be particularly effective in treating HCV genotype 1 infections. Special embodiments include the following patient populations:
(1) HCV subtype 1a and / or C / T genotype of SNP rs12979860
(2) T / T genotype of HCV subtype 1a and / or SNP rs12979860
(3) C / T genotype of HCV subtype 1b and / or SNP rs12979860
(4) T / T genotype of HCV subtype 1b and / or SNP rs12979860
(5) G / T genotype of HCV subtype 1a and / or SNP rs8099917
(6) G / G genotype of HCV subtype 1a and / or SNP rs8099917
(7) HCV subtype 1b and / or SNP rs8099917 G / T genotype
(8) G / G genotype of HCV subtype 1b and / or SNP rs8099917.
好ましい実施態様はHCV サブタイプ 1a 及びIL28B 遺伝子付近に位置するSNP 12979860のC/T もしくはT/T 遺伝子型又はSNP rs8099917 のG/T もしくはG/G 遺伝子型を有する患者(これらは特に治療し難いHCV-感染患者集団に相当する)の治療に関する。
特別な好ましい下位の実施態様において、患者は本発明の治療上の組み合わせを投与する工程の前にIL28B 遺伝子付近に位置するSNP rs12979860の非CC遺伝子型又はSNP rs8099917 の非TT遺伝子型を有すると最初に同定されていた。このような遺伝子型の同定のための方法が本明細書に詳しく示される。
本発明の併用療法で治療される患者集団は“治療ナイーブ”患者、即ち、HCV 感染症についての先の治療を受けていなかったこれらの患者及び“治療経験”患者、即ち、HCV についての先の治療を受けていたこれらの患者に更に分類し得る。これらのクラスの患者のいずれもが本発明の併用療法で治療されてもよい。以下に提示される臨床データは治療ナイーブ患者のみに関する。それにもかかわらず、同様の効力結果が治療経験患者で見られるであろうという予想がある。治療されることが好ましい特別なクラスの患者は先のインターフェロン+リバビリン治療を受けていたが、前記治療に応答性ではないこれらの治療経験患者(本明細書中、“非応答者”)である。このような非応答者として、三つの異なるグループの患者:(1) インターフェロン+リバビリンによる治療中にHCV RNA レベルの< 1x log10 最大減少を経験した者 (“ゼロ応答者”), (2) インターフェロン+リバビリンによる治療中にHCV RNA レベルの≧ 1x log10 最大減少を経験したが、検出のレベルより下のHCV RNA レベルに達しない者 (“部分応答者”)、及び(3)インターフェロン+リバビリン治療中に検出できないHCV RNA レベルに達したが、治療が完結した後にウイルス負荷リバウンドを有した者 (“再発者”) が挙げられる。本発明の併用療法で治療される別の治療経験患者集団として、(ペギル化)インターフェロン+リバビリンで初期のウイルス学的応答に達したが、治療への非執着のため以外に治療中にウイルス負荷リバウンドを有した者が挙げられる。
別の実施態様によれば、本発明は本発明の治療上の組み合わせをこれを要する患者に投与する工程を含む、前記患者のHCV-RNA レベルを減少する方法を提供する。本発明の方法は患者のHCV-RNA レベルを定量の下限より下のレベル (又は“BLQ”)に減少することが好ましい。本発明に使用されるHCV RNA のBLQ レベルはWHO 国際規格による定量的、多サイクル逆転写酵素PCR 方法(Saladanha J, Lelie N及びHeath A 著, “HCV RNA についての核酸増幅技術 (NAT)アッセイについての最初の国際規格の確立” WHO 共同研究グループ Vox Sang 76:149-158,1999)により測定して患者の血清又は血漿1ml当り25国際単位(IU)より下のレベルを意味する。このような方法は当業界で公知である。好ましい実施態様において、本発明の方法は患者のHCV-RNA レベルを血清又は血漿1ml当り25IU未満に減少する。別の実施態様において、本発明の方法は患者のHCV-RNA レベルを検出可能なレベル未満に減少する。好ましい実施態様において、本発明の方法は患者のHCV-RNA レベルを血清1ml当り25IU未満、更に好ましくは血清1ml当り10IU未満に減少する。
Preferred embodiments include patients with a C / T or T / T genotype of SNP 12979860 or a G / T or G / G genotype of SNP rs8099917 located near the HCV subtype 1a and IL28B genes (these are particularly difficult to treat) (Corresponding to the HCV-infected patient population).
In a particularly preferred sub-embodiment, the patient initially has a non-CC genotype of SNP rs12979860 or a non-TT genotype of SNP rs8099917 located near the IL28B gene prior to administering the therapeutic combination of the invention. Have been identified. Methods for such genotype identification are detailed herein.
The patient population to be treated with the combination therapy of the present invention is the “treated naïve” patients, ie those patients who have not received prior treatment for HCV infection and the “treatment experienced” patients, ie those previously treated for HCV. They can be further categorized into those patients who were undergoing treatment. Any of these classes of patients may be treated with the combination therapy of the present invention. The clinical data presented below relate only to treated naïve patients. Nevertheless, there is an expectation that similar efficacy results will be seen in patients with treatment experience. A special class of patients that are preferably treated are those patients who have received prior interferon plus ribavirin treatment but are not responsive to the treatment (herein “non-responders”). . As such non-responders, three different groups of patients: (1) experienced <1x log 10 maximum reduction in HCV RNA levels during treatment with interferon plus ribavirin (“zero responders”), (2) Those who experienced a ≥1x log 10 maximum reduction in HCV RNA levels during treatment with interferon + ribavirin but did not reach HCV RNA levels below the level of detection (“partial responders”), and (3) interferon + ribavirin Those who have reached HCV RNA levels that cannot be detected during treatment but have had viral load rebound after treatment is complete ("relapsed"). As another treatment-experienced patient population treated with the combination therapy of the present invention, an initial virological response was reached with (pegylated) interferon + ribavirin, but during treatment other than due to non-adherence to treatment The person who has rebound is mentioned.
According to another embodiment, the present invention provides a method of reducing HCV-RNA levels in a patient comprising administering to the patient in need thereof the therapeutic combination of the present invention. The method of the invention preferably reduces the patient's HCV-RNA level to a level below the lower limit of quantification (or “BLQ”). The BLQ levels of HCV RNA used in the present invention are quantitative, multi-cycle reverse transcriptase PCR methods by WHO international standards (Saladanha J, Lelie N and Heath A, “Nucleic acid amplification technology (NAT) assay for HCV RNA). Establishing the first international standard of “WHO collaborative research group Vox Sang 76: 149-158, 1999) means a level below 25 international units (IU) per ml of patient serum or plasma. Such methods are well known in the art. In a preferred embodiment, the methods of the invention reduce a patient's HCV-RNA levels to less than 25 IU per ml of serum or plasma. In another embodiment, the methods of the invention reduce the patient's HCV-RNA levels below detectable levels. In a preferred embodiment, the method of the invention reduces the patient's HCV-RNA level to less than 25 IU per ml of serum, more preferably less than 10 IU per ml of serum.
別の実施態様において、本発明の方法は患者のHCV-RNA レベルを検出可能なレベルより下(検出の限界の下、BLD)に減少する。HCV 治療の期間についての治療決定はBLD 、及び初期治療中のその後の時点におけるBLQ とBLD HCV RNAの組み合わせに基づいてなし得る。典型的な時点は治療の開始後の4週、8週、及び12週におけるHCV RNA 測定を含み、結果が“応答ガイド治療”中の更なる治療を導くのに利用される。HCV RNA がHCV 治療の終了後12-24 週でBLD に留まるならば、HCV 感染症からの治癒が典型的に推定される。こうして、付加的な実施態様において、本発明の方法は全ての治療の終了後、12週、好ましくは24週で検出可能なレベル未満である患者のHCV-RNA レベルをもたらす。
通常のインターフェロン+リバビリン治療についての通常の治療の期間はHCV 遺伝子型1又は4による慢性HCV 感染症について少なくとも48週、かつ72週までであり、慢性HCV 遺伝子型2又は3感染症を有する患者の大半について48週である。慢性HCV 遺伝子型2及び3感染症を有する少数の患者は24週のインターフェロンアルファ及びリバビリンで治療されてもよい。しかしながら、本発明の3種の治療上の組み合わせ中の、化合物 (1)、又はその医薬上許される塩の添加により、治療の極めて短い期間を有することが可能であり得る。本発明の3種併用治療により、治療の意図される期間は少なくとも4週、好ましくは少なくとも12週、例えば、約12週から約24週までを含むが、48週まで、更には48週を超えての治療が同様に可能である。こうして、更なる実施態様は少なくとも24週、また少なくとも48週にわたっての治療を含む。慢性HCV 感染症の治療の期間は特別なHCV 遺伝子型に応じて変化してもよい。例えば、治療の典型的な期間は遺伝子型2及び3よりも、遺伝子型1及び4について長いであろう。加えて、治療期間は慢性感染症と較べて急性感染症の治療について短いであろう。また、本発明の3種併用治療による初期の治療養生法、続いてインターフェロン+リバビリン2種併用治療の継続が意図されている。こうして、初期の3種併用次いで2種併用治療についての可能なシナリオは、例えば、(1) 4週の3種併用治療、続いて8〜44週のインターフェロン+リバビリンのみの治療; (2) 12週の3種併用治療、続いて0〜36週のインターフェロン+リバビリンのみの治療; 及び(3) 24週の3種併用治療、続いて0〜24週のインターフェロン+リバビリンのみの治療を含む。
In another embodiment, the methods of the invention reduce the patient's HCV-RNA levels below detectable levels (under detection limits, BLD). Treatment decisions regarding the duration of HCV treatment can be based on BLD and the combination of BLQ and BLD HCV RNA at a later time during initial treatment. Typical time points include HCV RNA measurements at 4 weeks, 8 weeks, and 12 weeks after the start of treatment, and the results are used to guide further treatment during “response guided treatment”. If HCV RNA remains in BLD 12-24 weeks after the end of HCV treatment, cure from HCV infection is typically presumed. Thus, in an additional embodiment, the methods of the invention result in patient HCV-RNA levels that are below detectable levels at the end of all treatments at 12 weeks, preferably 24 weeks.
The duration of normal treatment for normal interferon plus ribavirin treatment is at least 48 weeks and up to 72 weeks for chronic HCV infection with HCV genotype 1 or 4, and for patients with chronic HCV genotype 2 or 3 infection The majority is 48 weeks. A small number of patients with chronic HCV genotype 2 and 3 infections may be treated with 24 weeks of interferon alpha and ribavirin. However, it may be possible to have a very short duration of treatment by the addition of compound (1), or a pharmaceutically acceptable salt thereof, in the three therapeutic combinations of the present invention. With the triple combination treatment of the present invention, the intended duration of treatment includes at least 4 weeks, preferably at least 12 weeks, eg, from about 12 weeks to about 24 weeks, but up to 48 weeks and even more than 48 weeks. All treatments are possible as well. Thus, further embodiments include treatment for at least 24 weeks and also for at least 48 weeks. The duration of treatment for chronic HCV infection may vary depending on the particular HCV genotype. For example, a typical period of treatment would be longer for genotypes 1 and 4 than for genotypes 2 and 3. In addition, the duration of treatment will be short for the treatment of acute infections compared to chronic infections. In addition, it is intended to continue the initial treatment regimen by the combination therapy of the present invention, followed by the combination therapy of interferon and ribavirin. Thus, possible scenarios for initial triple combination followed by double combination treatment are, for example: (1) 4 week triple combination therapy followed by 8 to 44 week interferon plus ribavirin only treatment; (2) 12 3 week combination therapy followed by 0-36 weeks interferon plus ribavirin alone treatment; and (3) 24 week triple combination treatment followed by 0-24 week interferon plus ribavirin alone treatment.
治療上の組み合わせの第一成分、即ち、化合物 (1)又はその医薬上許される塩は組成物中に含まれる。このような組成物は化合物 (1)、又はその医薬上許される塩、及び医薬上許されるアジュバント又は担体を含む。化合物 (1)、又はその医薬上許される塩について使用し得る典型的な医薬組成物は、米国特許第7,585,845 号、WO 2010/059667及びWO 2011/005646に記載されたとおりである。
一般に、化合物 (1)又はその医薬上許される塩は少なくとも40 mg/日 (単一用量又は分割用量) の維持量で投与し得る。投薬量及び範囲についての付加的な実施態様は以下を含んでもよい(単一用量又は分割用量):
(a) 少なくとも48 mg/日
(b) 少なくとも100mg/日
(c) 少なくとも120mg/日
(d) 少なくとも200mg/日
(e) 少なくとも240mg/日
(f) 少なくとも360mg/日
(g) 少なくとも480mg/日
(h) 約40 mg/日から約480mg/日まで
(i) 約48 mg/日から約240mg/日まで
(j) 約100mg/日から約300mg/日まで
(k) 約120mg/日から約300mg/日まで
(l) 約120mg/日から約240mg/日まで
(m) 約240mg/日から約480mg/日まで
(n) 約48 mg/日
(o) 約120mg/日
(p) 約240mg/日
(q) 約360mg/日
(r) 約480mg/日。
The first component of the therapeutic combination, ie, compound (1) or a pharmaceutically acceptable salt thereof is included in the composition. Such a composition comprises Compound (1), or a pharmaceutically acceptable salt thereof, and a pharmaceutically acceptable adjuvant or carrier. Exemplary pharmaceutical compositions that may be used for compound (1), or a pharmaceutically acceptable salt thereof, are as described in US Pat. No. 7,585,845, WO 2010/059667 and WO 2011/005646.
In general, compound (1) or a pharmaceutically acceptable salt thereof may be administered in a maintenance dose of at least 40 mg / day (single dose or divided dose). Additional embodiments for dosages and ranges may include the following (single dose or divided dose):
(a) At least 48 mg / day
(b) At least 100 mg / day
(c) at least 120 mg / day
(d) at least 200 mg / day
(e) at least 240 mg / day
(f) at least 360 mg / day
(g) At least 480 mg / day
(h) From about 40 mg / day to about 480 mg / day
(i) From about 48 mg / day to about 240 mg / day
(j) From about 100 mg / day to about 300 mg / day
(k) From about 120 mg / day to about 300 mg / day
(l) From about 120 mg / day to about 240 mg / day
(m) From about 240 mg / day to about 480 mg / day
(n) Approx. 48 mg / day
(o) About 120mg / day
(p) Approx. 240 mg / day
(q) About 360mg / day
(r) About 480 mg / day.
化合物 (1)又はその医薬上許される塩は毎日の単一用量又は分割用量で投与されてもよいが、毎日の用量の1日1回の投与(QD)が好ましい。しかしながら、当業者が認めるように、先に列挙された用量よりも低いか、又は高い用量が必要とされるかもしれない。特別な患者に特別な用量及び治療養生法は年齢、体重、全般の健康状態、性別、食事、投与の時期、排泄の速度、併用薬物(共薬物)、感染症の重度及び経過、感染症についての患者の素質及び治療医師の判断を含む、種々の因子に依存するであろう。投薬に影響する特別な因子として、例えば、化合物 (1)の吸着、分布、代謝及び排泄を変更する個々の患者因子; 特別なHCV 遺伝子型; 患者の特別なIL28B 遺伝子型; HCV に対する患者の先天性/適応性免疫応答; 急性vs慢性HCV 感染症; 並びにホスト因子に基づくリバビリンの性質が挙げられるかもしれない。一般に、化合物は有害又は危険な副作用を生じないで坑ウイルス有効結果を一般に与える濃度レベルで投与されることが最も望ましい。 Compound (1) or a pharmaceutically acceptable salt thereof may be administered in a single daily dose or in divided doses, but daily dose once daily (QD) is preferred. However, as those skilled in the art will appreciate, doses lower or higher than those listed above may be required. Special doses and treatment regimens for special patients include age, weight, general health, sex, diet, time of administration, rate of excretion, concomitant medication (co-drug), severity and course of infection, infection Will depend on various factors, including the patient's predisposition and the judgment of the treating physician. Special factors that influence medication include, for example, individual patient factors that alter the adsorption, distribution, metabolism and excretion of compound (1); special HCV genotypes; patient specific IL28B genotypes; patient congenitals for HCV Sexual / adaptive immune responses; acute vs chronic HCV infection; as well as the nature of ribavirin based on host factors. In general, the compound is most desirably administered at a concentration level that will generally provide antiviral efficacy results without causing adverse or dangerous side effects.
本発明の別の実施態様において、負荷投薬量の化合物 (1)が治療の最初の投与用量のために投与される。負荷投薬量は治療におけるその後の投与のために投与される投薬量(これらは維持量と称される)よりも高い。負荷投薬量は治療におけるその後の投与における量のほぼ2倍の量(質量基準)であることが好ましい。例えば、一実施態様において、化合物 (1)の最初の用量が約240 mgの負荷用量で投与され、化合物 (1)のその後の維持量が約120 mgの用量で投与される。別の実施態様において、化合物 (1)の最初の用量が約480 mgの負荷用量で投与され、化合物 (1)のその後の維持量が約240 mgの用量で投与される。
この負荷投薬概念を使用することにより、明らかな利点はそうしないと到達されるよりも早く患者の系中の活性薬物の定常状態レベルに到達することがそれにより可能であることである。一層高い血液レベルが負荷用量、好ましくは維持量の2倍を最初の服用時に使用することにより早く到達される。治療の早期に活性薬物の目標定常状態レベルに達することはまた耐性ウイルス株が出現する一層小さい機会を有するように治療の開始時に不十分な薬物暴露の可能性が少ないことを意味する。
治療上の組み合わせの第二成分、即ち、インターフェロン−アルファは、医薬組成物中に含まれる。典型的には、このような組成物はインターフェロン−アルファ及び医薬上許されるアジュバント又は担体を含む注射製剤であり、当業界で公知であり、幾つかの市販インターフェロン−アルファ製剤を含む。例えば、種々の市販インターフェロン−アルファ製品並びに先に引用されたインターフェロン−アルファに関する種々の特許及びその他の文献を参照のこと。
In another embodiment of the invention, the loading dose of compound (1) is administered for the first dose of treatment. The loading dosage is higher than the dosage administered for subsequent administration in therapy (these are referred to as maintenance doses). The loading dosage is preferably about twice the amount (mass basis) in subsequent administrations in the treatment. For example, in one embodiment, an initial dose of compound (1) is administered at a loading dose of about 240 mg and a subsequent maintenance dose of compound (1) is administered at a dose of about 120 mg. In another embodiment, the first dose of compound (1) is administered at a loading dose of about 480 mg and the subsequent maintenance dose of compound (1) is administered at a dose of about 240 mg.
By using this loading dosing concept, an obvious advantage is that it is thereby possible to reach a steady state level of the active drug in the patient's system earlier than would otherwise be achieved. Higher blood levels are reached early by using a loading dose, preferably twice the maintenance dose, at the first dose. Reaching the target steady state level of active drug early in treatment also means that there is less chance of inadequate drug exposure at the start of treatment so that resistant virus strains have a smaller chance of emergence.
The second component of the therapeutic combination, interferon-alpha, is included in the pharmaceutical composition. Typically such compositions are injectable formulations comprising interferon-alpha and a pharmaceutically acceptable adjuvant or carrier and are known in the art and include several commercially available interferon-alpha formulations. See, for example, various commercial interferon-alpha products and various patents and other literature relating to interferon-alpha cited above.
組み合わせ中に使用し得るインターフェロン−アルファの型は定義の節に先に概説されたとおりである。一つの好ましい実施態様において、インターフェロンアルファがペギル化インターフェロンアルファである。更なる実施態様において、インターフェロンアルファがペギル化インターフェロンアルファ-2a 又はペギル化インターフェロンアルファ-2b である。特に好ましい実施態様において、インターフェロンアルファがPEGASYS (登録商標)又はPEG-INTRON(登録商標)である。
既知の、市販インターフェロンアルファ製品を使用する場合、このような製品はHCV 感染症の治療のためのインターフェロン+リバビリン併用治療に指示されたそれらの標識用量レベルで投与し得る。勿論、本発明の3種併用治療により、一層低い用量のインターフェロンアルファ、例えば、現行の通常のインターフェロン+リバビリン治療に使用されるよりも有意に低い用量のインターフェロンアルファを使用することが可能であり得るとともに、このような治療と通常関連する副作用よりも少なくて現行の通常の治療と同じか、又はそれより良好な効力を発する。
一実施態様において、インターフェロンアルファが週当り1〜3回、好ましくは週1回又は2回非経口投与されてもよい。ペギル化インターフェロンアルファに関して、これらがペギル化インターフェロンアルファ-2b の場合には典型的には週当り1回投与され、合計の毎週の用量が、例えば、約0.5 μg/kg/週から約2 μg/kg/週までの範囲であり、またペギル化インターフェロンアルファ-2a に関して、用量がホストの体重とは独立であり、典型的には約90〜200 μg/週、更に好ましくは約160 〜約200 μg/週である。リバビリンを含む組み合わせでは、ペギル化インターフェロンアルファ-2b の通常の用量が約1.5 μg/kg/週であり、またペギル化インターフェロンアルファ-2a の通常の用量がリバビリン(これは体重に従って毎日1回又は2回で、約200 〜1800 mg/日、特に、800-1200 mg/日の経口リバビリンの毎日の合計用量で投薬されることが好ましい)と一緒に、約180μg/週である。
The types of interferon-alpha that can be used in the combination are as outlined above in the definitions section. In one preferred embodiment, the interferon alpha is pegylated interferon alpha. In further embodiments, the interferon alpha is pegylated interferon alpha-2a or pegylated interferon alpha-2b. In particularly preferred embodiments, the interferon alpha is PEGASYS® or PEG-INTRON®.
When using known, commercially available interferon alpha products, such products can be administered at their labeled dose levels indicated for interferon plus ribavirin combination therapy for the treatment of HCV infection. Of course, the triple therapy of the present invention may make it possible to use lower doses of interferon alpha, eg, significantly lower doses of interferon alpha than are used for current conventional interferon plus ribavirin treatment. At the same time, it produces the same or better efficacy than current normal treatments with fewer side effects usually associated with such treatments.
In one embodiment, interferon alpha may be administered parenterally 1 to 3 times per week, preferably once or twice a week. With respect to pegylated interferon alpha, these are typically administered once per week in the case of pegylated interferon alfa-2b, for a total weekly dose of, for example, about 0.5 μg / kg / week to about 2 μg / week. kg / week and for pegylated interferon alpha-2a, the dose is independent of the host body weight, typically about 90-200 μg / week, more preferably about 160-about 200 μg / Week. For combinations containing ribavirin, the usual dose of pegylated interferon alfa-2b is about 1.5 μg / kg / week, and the usual dose of pegylated interferon alfa-2a is ribavirin (this is once or twice daily depending on body weight). About 180 μg / week, preferably with a daily total dose of oral ribavirin of about 200-1800 mg / day, in particular 800-1200 mg / day.
更なる実施態様によれば、ペギル化インターフェロンアルファ-2b が下記の用量で投与し得る:
(a) 約0.5 μg/kg/週〜約2 μg/kg/週;
(b) 約1 μg/kg/週〜約2 μg/kg/週;
(c) 約1.5 μg/kg/週〜約2 μg/kg/週;
(d) 約1.5 μg/kg/週。
更なる実施態様によれば、ペギル化インターフェロンアルファ-2a が下記の用量で投与し得る:
(a) 約90から約200μg/週;
(b) 約160 〜約200μg/週;
(c) 約180 μg/週。
治療上の組み合わせの第三成分、即ち、リバビリンが、医薬組成物中に含まれる。典型的には、このような組成物がリバビリン及び医薬上許されるアジュバント又は担体を含み、当業界で公知であり、幾つかの市販のリバビリン製剤を含む。リバビリンを含む製剤がまた、例えば、米国特許第4,211,771 号に開示されている。
治療上の組み合わせ中に使用し得るリバビリンの型は定義の節に先に概説されたとおりである。一つの好ましい実施態様において、リバビリンがREBETOL (登録商標)又はCOPEGUS (登録商標)であり、それらがHCV 感染症の治療のためにインターフェロン+リバビリン併用治療に指示されたそれらの標識用量レベルで投与されてもよい。勿論、本発明の3種併用療法により、例えば、現行の通常のインターフェロン+リバビリン療法で使用されるよりも低い、リバビリンの一層低い用量を使用することが可能であり得るとともに、現行の通常の療法と同じ又は良好な効力をこのような療法と通常関連する少ない副作用で発する。
According to a further embodiment, pegylated interferon alpha-2b may be administered at the following dose:
(a) about 0.5 μg / kg / week to about 2 μg / kg / week;
(b) about 1 μg / kg / week to about 2 μg / kg / week;
(c) about 1.5 μg / kg / week to about 2 μg / kg / week;
(d) About 1.5 μg / kg / week.
According to a further embodiment, pegylated interferon alpha-2a may be administered at the following dose:
(a) about 90 to about 200 μg / week;
(b) about 160 to about 200 μg / week;
(c) About 180 μg / week.
A third component of the therapeutic combination, ribavirin, is included in the pharmaceutical composition. Typically, such compositions comprise ribavirin and a pharmaceutically acceptable adjuvant or carrier and are known in the art and comprise several commercially available ribavirin formulations. Formulations containing ribavirin are also disclosed, for example, in US Pat. No. 4,211,771.
The types of ribavirin that can be used in therapeutic combinations are as outlined above in the definitions section. In one preferred embodiment, ribavirin is REBETOL® or COPEGUS® and they are administered at their labeled dose levels indicated for interferon + ribavirin combination therapy for the treatment of HCV infection. May be. Of course, the triple combination therapy of the present invention may make it possible to use lower doses of ribavirin, for example, lower than that used in current normal interferon plus ribavirin therapy, as well as current conventional therapy. Produces the same or better efficacy with fewer side effects usually associated with such therapy.
種々の実施態様によれば、リバビリンが下記の用量(単一用量又は分割用量)で投与し得る:
(a) 200mg/日〜約1800 mg/日;
(b) 約800mg/日〜約1200mg/日;
(c) 約1000 mg/日〜約1200mg/日;
(d) 約1000 mg/日
(e) 約1200 mg/日
(f) 約300mg/日から約800mg/日まで
(g) 約300mg/日から約700mg/日まで
(h) 500mg/日から約700mg/日まで
(i) 400mg/日から約600mg/日まで
(j) 約400mg/日
(k) 約600 mg/日
(l) 約800 mg/日。
一実施態様によれば、リバビリン組成物が1日1回又は1日2回の投薬に適した製剤中にリバビリンを含む。例えば、治療上の組み合わせが約1000 mg/日の用量のリバビリンを含み、かつ1日2回の投薬が所望される場合、治療上の組み合わせは製剤、例えば、約200 mgのリバビリンを含む錠剤中に、600 mg (又は400 mg) の第一用量、続いて少なくとも6時間離れて400 mg (又は600 mg) の第二用量で、リバビリンを含むであろう。
本発明の化合物 (1)又はその医薬上許される塩+インターフェロンアルファ+リバビリン3種併用療法に関して、本発明は先に示された種々の好ましい実施態様及び下位の実施態様の全ての治療上の組み合わせを意図しており、これらを含む。
According to various embodiments, ribavirin may be administered at the following doses (single dose or divided dose):
(a) 200 mg / day to about 1800 mg / day;
(b) about 800 mg / day to about 1200 mg / day;
(c) about 1000 mg / day to about 1200 mg / day;
(d) Approximately 1000 mg / day
(e) Approx. 1200 mg / day
(f) From about 300 mg / day to about 800 mg / day
(g) From about 300 mg / day to about 700 mg / day
(h) From 500mg / day to about 700mg / day
(i) From 400mg / day to about 600mg / day
(j) About 400mg / day
(k) Approx. 600 mg / day
(l) About 800 mg / day.
According to one embodiment, the ribavirin composition comprises ribavirin in a formulation suitable for once daily or twice daily dosing. For example, if the therapeutic combination includes a dose of about 1000 mg / day ribavirin and dosing twice a day is desired, the therapeutic combination is in a formulation, eg, a tablet containing about 200 mg ribavirin. At a first dose of 600 mg (or 400 mg) followed by a second dose of 400 mg (or 600 mg) at least 6 hours apart.
With respect to the compound (1) of the present invention or a pharmaceutically acceptable salt thereof + interferon alpha + ribavirin triple therapy, the present invention provides all therapeutic combinations of the various preferred embodiments and subembodiments shown above. Including and including these.
例えば、一実施態様において、本発明はIL28B 遺伝子付近に位置するSNP rs12979860の非CC遺伝子型又はSNP rs8099917 の非TT遺伝子型を有する患者に
(a) 約40 mg /日〜約480 mg/日の用量の化合物 (1)又はその医薬上許される塩;
(b) 約160 〜約200μg/週の用量のペギル化インターフェロンアルファ -2a又は約0.5 μg/kg/週〜約2 μg/kg/週の用量のペギル化インターフェロンアルファ -2b;及び
(c) 約200mg/日〜約1800 mg/日の用量のリバビリン
を含む治療上の組み合わせを投与する工程を含む前記患者のC型肝炎ウイルス (HCV)感染症を治療し、又はその一種以上の症候を軽減する方法を意図している。
別の実施態様において、本発明はIL28B 遺伝子付近に位置するSNP rs12979860の非CC遺伝子型又はSNP rs8099917 の非TT遺伝子型を有する患者に
(a) 約120mg /日〜約240 mg/日の用量の化合物 (1)又はその医薬上許される塩;
(b) 約180μg/週の用量のペギル化インターフェロンアルファ -2a;及び
(c) 約1000 mg/日〜約1200 mg/日の用量のリバビリン
を含む治療上の組み合わせを投与する工程を含む前記患者のC型肝炎ウイルス (HCV)感染症を治療し、又はその一種以上の症候を軽減する方法を意図している。
別の実施態様において、本発明はIL28B 遺伝子付近に位置するSNP rs12979860の非CC遺伝子型又はSNP rs8099917 の非TT遺伝子型を有する患者に
(a) 約120mg /日〜約240 mg/日の用量の化合物 (1)又はその医薬上許される塩;
(b) 約1.5 μg/kg/週の用量のペギル化インターフェロンアルファ-2b;及び
(c) 約1000 mg/日〜約1200 mg/日の用量のリバビリン
を含む治療上の組み合わせを投与する工程を含む前記患者のC型肝炎ウイルス (HCV)感染症を治療し、又はその一種以上の症候を軽減する方法を意図している。
更なる実施態様は
(a) HCV 感染症が遺伝子型1、好ましくは遺伝子型1aであり、かつ患者が治療ナイーブ患者であり、又は
(b) HCV 感染症が遺伝子型1、好ましくは遺伝子型1aであり、かつ患者がインターフェロン+リバビリンの治療上の組み合わせに非応答性である治療経験患者である、上記実施態様のいずれかを含む。
For example, in one embodiment, the invention relates to a patient having a non-CC genotype of SNP rs12979860 or a non-TT genotype of SNP rs8099917 located near the IL28B gene.
(a) a dose of about 40 mg / day to about 480 mg / day of compound (1) or a pharmaceutically acceptable salt thereof;
(b) pegylated interferon alfa-2a at a dose of about 160 to about 200 μg / week or pegylated interferon alfa-2b at a dose of about 0.5 μg / kg / week to about 2 μg / kg / week; and
(c) treating the patient with a hepatitis C virus (HCV) infection comprising administering a therapeutic combination comprising ribavirin at a dose of about 200 mg / day to about 1800 mg / day, or one or more thereof Intended for ways to reduce symptoms.
In another embodiment, the present invention relates to a patient having a non-CC genotype of SNP rs12979860 or a non-TT genotype of SNP rs8099917 located near the IL28B gene.
(a) a dose of about 120 mg / day to about 240 mg / day of compound (1) or a pharmaceutically acceptable salt thereof;
(b) a pegylated interferon alpha-2a dose of about 180 μg / week; and
(c) treating hepatitis C virus (HCV) infection in said patient comprising administering a therapeutic combination comprising ribavirin at a dose of about 1000 mg / day to about 1200 mg / day, or one or more thereof Is intended to alleviate the symptoms.
In another embodiment, the present invention relates to a patient having a non-CC genotype of SNP rs12979860 or a non-TT genotype of SNP rs8099917 located near the IL28B gene.
(a) a dose of about 120 mg / day to about 240 mg / day of compound (1) or a pharmaceutically acceptable salt thereof;
(b) pegylated interferon alfa-2b at a dose of about 1.5 μg / kg / week; and
(c) treating hepatitis C virus (HCV) infection in said patient comprising administering a therapeutic combination comprising ribavirin at a dose of about 1000 mg / day to about 1200 mg / day, or one or more thereof Is intended to alleviate the symptoms.
Further embodiments are
(a) the HCV infection is genotype 1, preferably genotype 1a and the patient is a therapeutic naïve patient, or
(b) including any of the above embodiments, wherein the HCV infection is genotype 1, preferably genotype 1a, and the patient is a therapeutically experienced patient who is unresponsive to a therapeutic combination of interferon + ribavirin .
更なる実施態様において、患者が本発明の治療上の組み合わせを投与する工程の前にIL28B 遺伝子付近に位置するSNP rs12979860の非CC遺伝子型又はSNP rs8099917 の非TT遺伝子型を有すると最初に同定されていた。
更なる実施態様は化合物 (1)又はその医薬上許される塩が1日1回投与され、インターフェロンアルファが週1回投与され、かつリバビリンが1日2回投与される、上記実施態様のいずれかを含む。
本発明の3種の治療上の組み合わせに関して、本発明は本明細書に示された種々の好ましい実施態様及び下位の実施態様の全ての組み合わせを意図しており、これらを含む。
別の実施態様によれば、本発明の治療養生法が患者に少なくとも約4週、更に好ましくは少なくとも約12週又は少なくとも約24週にわたって
(i) 治療有効量の化合物 (1)又はその医薬上許される塩を1日1回;
(ii) 治療有効量のインターフェロンアルファを週1回; そして
(iii) 治療有効量のリバビリンを1日2回
投与することを含む。
付加的な実施態様はIL28B 遺伝子付近に位置するSNP rs12979860の非CC遺伝子型又はSNP rs8099917 の非TT遺伝子型を有すると同定されていた患者のHCV 感染症の治療のための化合物 (1)、インターフェロンアルファ及びリバビリンの同時投与に関する記述された指示と一緒に、化合物 (1)又はその医薬上許される塩、インターフェロンアルファ及びリバビリンの一種以上の用量を含むパッケージを含む包装された医薬組成物に関する。化合物 (1)又はその医薬上許される塩の個々の剤形は、通常の医薬剤形、例えば、錠剤、カプセルのいずれかの形態であってもよく、医薬包装材料(それら自体が紙/カードボードボックスの如き外部包装材料内に含まれてもよい)の通常の型、例えば、びん、ブリスター−パック等のいずれかの中に包装し得る。記述された指示は典型的には包装材料それ自体又は外部包装材料内に剤形と一緒に用意される別々の紙(所謂“パッケージインサート”)の上に用意されるであろう。全てのこのような包装実施態様及びこれらの変化が本発明により含まれる。
In a further embodiment, the patient is first identified as having a non-CC genotype of SNP rs12979860 or a non-TT genotype of SNP rs8099917 located near the IL28B gene prior to administering the therapeutic combination of the invention. It was.
A further embodiment is any of the above embodiments wherein compound (1) or a pharmaceutically acceptable salt thereof is administered once a day, interferon alpha is administered once a week, and ribavirin is administered twice a day. including.
With respect to the three therapeutic combinations of the present invention, the present invention contemplates and includes all combinations of the various preferred embodiments and sub-embodiments shown herein.
According to another embodiment, the therapeutic regimen of the present invention provides the patient with at least about 4 weeks, more preferably at least about 12 weeks or at least about 24 weeks.
(i) a therapeutically effective amount of compound (1) or a pharmaceutically acceptable salt thereof once a day;
(ii) a therapeutically effective amount of interferon alpha once a week; and
(iii) administration of a therapeutically effective amount of ribavirin twice daily.
An additional embodiment is a compound for the treatment of HCV infection in a patient identified as having a non-CC genotype of SNP rs12979860 or a non-TT genotype of SNP rs8099917 located near the IL28B gene (1), interferon It relates to a packaged pharmaceutical composition comprising a package comprising one or more doses of Compound (1) or a pharmaceutically acceptable salt thereof, interferon alfa and ribavirin, together with written instructions for co-administration of alpha and ribavirin. The individual dosage forms of compound (1) or pharmaceutically acceptable salts thereof may be in the form of conventional pharmaceutical dosage forms, such as tablets, capsules, or pharmaceutical packaging materials (paper / card themselves). It may be packaged in any conventional mold (e.g., bottles, blister packs, etc.) which may be contained within an external packaging material such as a board box. The described instructions will typically be provided on a separate paper (so-called “package insert”) that is provided with the dosage form in the packaging material itself or in the outer packaging material. All such packaging embodiments and variations thereof are encompassed by the present invention.
HCV サブタイプ及び遺伝子亜型の測定方法
HCV RNA 定量、HCV サブタイピング及びIL28B 遺伝子型判定に使用された特別な方法は以下に詳述されるとおりである。その他の方法が当業界で知られているかもしれず、また利用できるかもしれない程度まで、全てが本発明内に含まれると考えられ、それと関連して使用し得る。
HCV RNA 定量
約6 mlの血漿サンプルが患者から得られ、Roche COBAS (登録商標)TaqMan HCV/HPSアッセイを使用して処理される。そのアッセイは25 IU/mlの定量の下限及び10 IU/mlの検出の下限で25〜2000,000,000 IU/ml (2.0 E8 IU/ml) の線形範囲を有する。
HCV サブタイピング
HCV サブタイプがTRUGENE (登録商標)HCV 遺伝子型判定アッセイを使用することにより測定された。そのアッセイはウイルスを直接増幅し、配列決定し、2種の蛍光標識DNA プライマーを使用して2方向の配列を生じることによりウイルスのRNA の直接検査を可能にする。そのライブラリーは6種の主要なC型肝炎遺伝子型及び41のサブタイプの測定を可能にするためにウイルス分離物を含む。
IL28B の遺伝子型判定
遺伝子型分析が遺伝子変異体の分析のためのBeckman Coulter Genomics (Bernried, ドイツ) により確立されたTaqMan PCRをベースとする試験アッセイを使用することにより患者の血液サンプルから抽出されたDNA について行なわれた。遺伝子型分析のプロセスフローは血液サンプルからのゲノムDNA の抽出、特別な遺伝子標的部位を増幅するための確立された分子遺伝子技術の適用並びにその増幅プロセスで使用された蛍光TaqManプローブの発光データの検出及び分析からなっていた。3種の対照: a) DNA分離の前に含まれる一種の水対照、b) DNA分離の後に含まれる一種の水対照及びc) 一種の異型接合及び/又は一種の同型接合の (野生型又は変異体) 遺伝子型判定対照が夫々の産物について使用された。
Method for measuring HCV subtype and gene subtype
The specific methods used for HCV RNA quantification, HCV subtyping and IL28B genotyping are as detailed below. To the extent that other methods may be known in the art and may be available, all are considered to be included within the present invention and may be used in connection therewith.
HCV RNA quantification Approximately 6 ml plasma samples are obtained from patients and processed using the Roche COBAS® TaqMan HCV / HPS assay. The assay has a linear range of 25-2000,000,000 IU / ml (2.0 E8 IU / ml) with a lower limit of quantification of 25 IU / ml and a lower limit of detection of 10 IU / ml.
HCV subtyping
The HCV subtype was determined by using the TRUGENE® HCV genotyping assay. The assay allows direct examination of the viral RNA by directly amplifying and sequencing the virus and using two fluorescently labeled DNA primers to generate a bi-directional sequence. The library contains virus isolates to allow measurement of 6 major hepatitis C genotypes and 41 subtypes.
IL28B genotyping genotyping was extracted from patient blood samples using a TaqMan PCR-based test assay established by Beckman Coulter Genomics (Bernried, Germany) for analysis of genetic variants Done about DNA. The genotyping process flow includes the extraction of genomic DNA from blood samples, the application of established molecular genetic techniques to amplify special gene target sites, and the detection of luminescence data from fluorescent TaqMan probes used in the amplification process And analysis. Three controls: a) a water control included before DNA separation, b) a water control included after DNA separation, and c) a heterozygous and / or a homozygous (wild type or Mutant) A genotyping control was used for each product.
この研究に適用された対立遺伝子識別のためのTaqManをベースとする産物についてのプロセスフローが先の図に示される。全てのサンプル及び夫々のプロセシングバッチの全ての産物についての最終の遺伝子型結果がBeckman Coulter GenomicsソフトウェアSNPsuiteを使用して合わされた。結果は夫々の被験者の遺伝子型に関する情報を含む。 The process flow for TaqMan based products for allele discrimination applied to this study is shown in the previous figure. The final genotype results for all samples and all products of each processing batch were combined using Beckman Coulter Genomics software SNPsuite. The results contain information about the genotype of each subject.
I.化合物 (1)の調製方法
無定形化合物 (1)の調製方法は米国特許第6,323,180 号、同第7,514,557 号及び同第7,585,845 号(これらが参考として本明細書に含まれる)に見られる。化合物 (1)の付加的な形態、特に結晶性ナトリウム塩形態の調製方法が、米国特許出願公開第2010/0093792号に見られる。
II. 化合物 (1)の製剤
化合物 (1)の医薬製剤の一例として、WO 2010/059667に開示された経口溶液製剤が挙げられる。付加的な例として、WO 2011/005646に開示された、脂質をベースとする液体製剤を含むカプセルが挙げられる。
III.臨床結果
以下に記載される臨床試験について、化合物 (1)薬物製品を化合物 (1)ナトリウム塩を含む脂質をベースとする製剤で充填された軟質ゲルカプセルとして投与した。以下の臨床研究における“化合物 (1)”についての全ての言及はナトリウム塩形態である。
実施例6−治療ナイーブ患者による臨床研究
HCV プロテアーゼ阻害薬化合物 (1)による治療は高く、かつ一貫したSVR 率−異なるベースラインファクターにわたっての治療ナイーブ患者におけるSILEN-C1からの結果をもたらす。
背景及び目的:化合物 (1)は慢性HCV 遺伝子型-1 (GT1)感染症で強い坑ウイルス活性を有する1日1回(QD)与えられる高度に強力かつ特異的なHCV NS3/4Aプロテアーゼ阻害薬である。この研究は治療し難い患者のサブグループ分析を提示する。
方法:この二重盲検、ランダム化フェーズII試験では、429 HCV GT1 治療ナイーブ患者を偽薬又は化合物 (1)、120mg とともに3日リード−イン(lead-in) (LI)のペギル化インターフェロン-アルファ及びリバビリン (PR) (120mg QD/LI)、240mg QD/LI 又はLIを伴なわない240mg QD (240mg QD)に1:1:2:2にランダム化した。夫々のアームにおいて、化合物 (1)を24週又は48週にわたってのPRと一緒に24週にわたって与えた。ウイルス負荷(VL)をRoche TaqMan (定量の下限25 IU/mL) により測定し、サブタイプをNS3/4A配列決定により分析し、IL-28B 遺伝子型 (SNP rs12979860 から) を患者の約50% について回顧的に集めた。化合物 (1)の両方のLIグループにおけるわずかに減少された応答率に基づいて、240mg QD用量がフェーズIII 評価に選ばれた (120mg QDとともに) 。重要な患者特性にわたってPRとのこの用量の比較がここに提示される。
I. Method for Preparing Compound (1) A method for preparing amorphous compound (1) can be found in US Pat. Nos. 6,323,180, 7,514,557, and 7,585,845, which are hereby incorporated by reference. Additional forms of compound (1), particularly crystalline sodium salt forms, can be found in US Patent Application Publication No. 2010/0093792.
II. Formulation of Compound (1) An example of a pharmaceutical formulation of Compound (1) is the oral solution formulation disclosed in WO 2010/059667. Additional examples include capsules containing lipid-based liquid formulations disclosed in WO 2011/005646.
III. Clinical Results For the clinical trials described below, Compound (1) drug product was administered as a soft gel capsule filled with a lipid-based formulation containing Compound (1) sodium salt. All references to “compound (1)” in the following clinical studies are in the sodium salt form.
Example 6 Clinical Study with Treated Naive Patients
Treatment with the HCV protease inhibitor compound (1) is high and results in consistent SVR rates-treatment from SILEN-C1 in naïve patients across different baseline factors.
Background and Objective: Compound (1) is a highly potent and specific HCV NS3 / 4A protease inhibitor given once a day (QD) with strong antiviral activity in chronic HCV genotype-1 (GT1) infection It is. This study presents a subgroup analysis of patients who are difficult to treat.
Method: In this double-blind, randomized Phase II study, 429 HCV GT1-treated naïve patients were treated with placebo or compound (1), 120 mg with a 3-day lead-in (LI) pegylated interferon-alpha And Ribavirin (PR) (120 mg QD / LI), 240 mg QD / LI or 240 mg QD (240 mg QD) without LI were randomized 1: 1: 2: 2. In each arm, compound (1) was given over 24 weeks with PR over 24 or 48 weeks. Viral load (VL) was measured by Roche TaqMan (lower limit of quantification 25 IU / mL), subtypes were analyzed by NS3 / 4A sequencing, and IL-28B genotype (from SNP rs12979860) was determined in about 50% of patients Collected retrospectively. Based on the slightly reduced response rate in both LI groups of Compound (1), a 240 mg QD dose was chosen for Phase III evaluation (along with 120 mg QD). A comparison of this dose with PR across important patient characteristics is presented here.
主たる組み入れ基準
・年齢18〜65才
・GT-1慢性C型肝炎感染症
・インターフェロン及び/又はRBV に対しナイーブ
・HCV RNA ≧ 100,000 IU/mL
・肝硬変のない肝臓バイオプシー< 2 年
ベースラインファクターにわたっての部分解析
・Roche COBAS TaqMan(登録商標) (定量の下限: 25 IU/mL)により分析されたHCV RNA
・NS3/4A配列決定により分析されたサブタイプ
・患者の50% について回顧的に集められたIL28B 遺伝子型
結果:総合して、化合物 (1) 240mg QD で治療された患者の83.8% が、PR単独の患者の56.3% と較べて、SVR に達した (p<0.0001) 。SVR 率は広範囲の治癒し難いサブグループにわたって一貫して高かった(表を参照のこと)。注目すべきことに、サブタイプ1a患者についてのSVR 率は82.4% であった(PRについての46.9% と較べて、p=0.0013)。LIを伴なわないで24週の化合物 (1) 240mgを受けたSNP rs12979860のIL-28B 遺伝子型CCの全ての22の患者 (100%) がPR単独についての81.8% と較べて、SVR に達した (p = 0.1042) 。非CC (SNP rs12979860の) 患者のSVR はまたPR単独(41.4%, p = 0.0162) と較べて有意に高かった (70.8%)。24週の全治療期間にわたってeRVRに達し、こうして望ましい患者の%は87.3% であり、非CC患者を含む全てのサブグループにわたって一貫して高い比率であった。
Main inclusion criteria-Age 18-65-GT-1 chronic hepatitis C infection-Naive for interferon and / or RBV-HCV RNA ≥ 100,000 IU / mL
・ Partial analysis over liver biopsy <2 years baseline factor without cirrhosis ・ HCV RNA analyzed by Roche COBAS TaqMan® (lower limit of quantification: 25 IU / mL)
• Subtypes analyzed by NS3 / 4A sequencing • IL28B genotype results collected retrospectively for 50% of patients: Overall, 83.8% of patients treated with Compound (1) 240 mg QD were PR SVR was reached (p <0.0001) compared to 56.3% of single patients. SVR rates were consistently high across a wide range of refractory subgroups (see table). Of note, the SVR rate for subtype 1a patients was 82.4% (p = 0.0013 compared to 46.9% for PR). All 22 patients (100%) with IL-28B genotype CC of SNP rs12979860 who received 240 mg of compound (1) 240 mg without LI achieved SVR compared to 81.8% for PR alone (P = 0.1042). Non-CC (SNP rs12979860) patients' SVR was also significantly higher (70.8%) compared to PR alone (41.4%, p = 0.0162). The eRVR was reached over the entire treatment period of 24 weeks, thus the percentage of patients desired was 87.3%, a consistently high rate across all subgroups including non-CC patients.
^ eRVR=4週でHCV RNA <25 IU/mL そして8-20週で検出不能
ALT = アラニントランスアミナーゼ; GGT, ガンマ−グルタミルトランスペプチダーゼ; ULN, 正常の上限; BL VL = 基準線HCV RNA (IU/mL)
* SVR 率の同等についてのFisherの正確な試験
治療し難いHCV サブタイプの患者、例えば、ウイルスGT1a 又はIL-28B 非CC遺伝子変異体 (多形) の患者の大半がSVR に達したことは特に注目される。
・詳しくは、GT1bよりもおそらく治療に耐性であるウイルス型である、GT1a HCVの患者(n=51)の中で、82% がSVR に達し、一方、GT1b HCV患者(n=91)について、85% がSVR に達した。
・加えて、SVR はIL-28B遺伝子付近に位置するSNP rs12979860の非CC多形の患者(n=48)について71% であり、一方、CC多形の患者(n=22)は100% SVR に達し、またIL-28B 遺伝子型判定が欠失している患者(n=72)は88% SVR に達した。非CC多形を示す患者はPegIFN/RBV治療でSVR に達しそうにない。
^ eRVR = HCV RNA <25 IU / mL at 4 weeks and undetectable at 8-20 weeks
ALT = alanine transaminase; GGT, gamma-glutamyl transpeptidase; ULN, upper limit of normal; BL VL = baseline HCV RNA (IU / mL)
* Fisher's exact test for SVR rate equivalence. Particularly difficult to treat HCV subtype patients, for example, the majority of patients with viral GT1a or IL-28B non-CC gene variants (polymorphisms) reached SVR. Attention.
Specifically, among GT1a HCV patients (n = 51), a virus type that is probably more resistant to treatment than GT1b, 82% reached SVR, while GT1b HCV patients (n = 91) 85% reached SVR.
In addition, SVR was 71% for non-CC polymorphic patients with SNP rs12979860 (n = 48) located near the IL-28B gene, whereas patients with CC polymorphism (n = 22) were 100% SVR Patients with a loss of IL-28B genotyping (n = 72) reached 88% SVR. Patients who show non-CC polymorphism are unlikely to reach SVR with PegIFN / RBV treatment.
結論:治療ナイーブ患者で1日1回の化合物 (1) 240mgは、治癒し難い患者、例えば、GT1a及びIL28B 非CCでさえも、一貫して強く、かつ有意なeRVR率及びSVR 率に達した。GT1 HCV は治療するのに最も魅力的なHCV の遺伝子型であり (例えば、Ghany, Marc ら著“遺伝子型 1慢性C型肝炎ウイルス感染症の治療についてのアップデート:肝臓疾患についての米国協会による2011の実務ガイドライン”, Hepatology, 54(4): 1433-44 (2011) を参照のこと) 、IL-28B遺伝子付近に位置するSNP rs12979860の非CC遺伝子型又はSNP rs8099917 の非TT遺伝子型を有するものはCC又はTT多形を有するものよりもSVR に達しそうになく、幾つかの研究が治療応答にほぼ7倍の差を示している (G.Cairns著, “C型肝炎治療を助ける遺伝子変異体はHIV 治療を妨げ得る”, 2011年, http://www.bhiva.org/News.aspx?NewsID=a7503829-94b9-4d2f-bd91-1d2fbaad6e8dを参照のこと)。この技術水準を考慮すると、治療し難い患者集団(HCV GT 1a で感染された患者並びにIL-28B遺伝子付近に位置するSNP rs12979860の非CC遺伝子型を有する患者を含む)について本明細書で得られた結果はこの療法についての優れた結果を反映する。同様の優れた結果が本発明の併用療法を使用してIL-28B遺伝子付近に位置するSNP rs8099917 の非TT遺伝子型を有する患者で予想されるべきである。PegIFN/RBV及びNS3/4 HCV プロテアーゼ阻害薬テラプレバー (Akuta ら2010)の組み合わせで見られるようなこのような治療し難い患者集団におけるかなり低下された治療有効性に基づいて、PegIFN/RBV及びテラプレバーで治療された患者で観察されたSVR 率の予想されたIL28B 関連の差が本発明の併用療法で広く消失し、又は有意に減少されたこと及び不利な遺伝子型非CCもしくは非TT又は不利なHCV 遺伝子型 1a 感染症の患者がSVR に関して一貫して高い治癒率に達したことは驚くべきである。
1日1回の240mg の治療がフェーズIII 試験で120mg QDとともに現在試験されている。
CONCLUSION: Once a day in treated naive patients (1) 240 mg reached consistently strong and significant eRVR and SVR rates even in refractory patients, such as GT1a and IL28B non-CC . GT1 HCV is the most attractive genotype of HCV to treat (eg, Ghany, Marc et al., “Genotype 1 Update on Treatment of Chronic Hepatitis C Virus Infection: American Association for Liver Disease 2011” Practical guidelines for “,” Hepatology, 54 (4): 1433-44 (2011)), SNP rs12979860 non-CC genotype or SNP rs8099917 non-TT genotype located near IL-28B gene Are less likely to reach SVR than those with CC or TT polymorphisms, and some studies have shown almost a 7-fold difference in therapeutic response (G. Cairns, “Gene mutations that help treat hepatitis C” The body can interfere with HIV treatment ”, 2011, see http://www.bhiva.org/News.aspx?NewsID=a7503829-94b9-4d2f-bd91-1d2fbaad6e8d). Given this state of the art, it is obtained here for a population of patients who are difficult to treat, including patients infected with HCV GT 1a as well as patients with a non-CC genotype of SNP rs12979860 located near the IL-28B gene. The results reflect the excellent results for this therapy. Similar superior results should be expected in patients with a non-TT genotype of SNP rs8099917 located near the IL-28B gene using the combination therapy of the present invention. Based on the significantly reduced therapeutic efficacy in such intractable patient populations as seen with the combination of PegIFN / RBV and NS3 / 4 HCV protease inhibitor Teraprever (Akuta et al 2010), PegIFN / RBV and Teraprever Expected IL28B-related differences in SVR rates observed in treated patients were largely eliminated or significantly reduced with the combination therapy of the present invention and adverse genotype non-CC or non-TT or adverse HCV It is surprising that patients with genotype 1a infection have consistently achieved high cure rates for SVR.
A once-daily treatment of 240 mg is currently being tested with 120 mg QD in a Phase III study.
Claims (30)
(式中、Bは下記の基であり、
前記方法が患者に
(a) 式 (1)の化合物又はその医薬上許される塩、
(b) インターフェロンアルファ、及び
(c) リバビリン
を投与することを含むことを特徴とする前記化合物又はその医薬上許される塩。 Method of treating hepatitis C virus (HCV) infection in a patient having a non-CC genotype of SNP rs12979860 or a non-TT genotype of SNP rs8099917 located near the IL-28B gene, or reducing one or more symptoms thereof A compound of formula (1) below or a pharmaceutically acceptable salt thereof for use in:
(In the formula, B is the following group,
Said method to the patient
(a) a compound of formula (1) or a pharmaceutically acceptable salt thereof,
(b) interferon alpha, and
(c) The above compound or a pharmaceutically acceptable salt thereof, which comprises administering ribavirin.
(式中、Bは
(b) IL-28B遺伝子付近に位置するSNP rs12979860の非CC遺伝子型又はSNP rs8099917 の非TT遺伝子型を有する患者のHCV 感染症の治療のための化合物 (1)又はその医薬上許される塩、インターフェロンアルファ、及びリバビリンの同時投与に関する記述された指示を含むパッケージを含むことを特徴とする包装された医薬組成物。 (a) one or more doses of a compound of formula (1) below or a pharmaceutically acceptable salt thereof,
(Where B is
(b) Compound (1) or a pharmaceutically acceptable salt thereof for the treatment of HCV infection in a patient having a non-CC genotype of SNP rs12979860 or a non-TT genotype of SNP rs8099917 located near the IL-28B gene, A packaged pharmaceutical composition comprising a package comprising written instructions for co-administration of interferon alpha and ribavirin.
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| PCT/EP2012/055453 WO2013143581A1 (en) | 2012-03-28 | 2012-03-28 | Combination therapy for treating hcv infection in specific patient subgenotype sub-population |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2015512900A true JP2015512900A (en) | 2015-04-30 |
| JP2015512900A5 JP2015512900A5 (en) | 2015-06-18 |
Family
ID=48013997
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015502107A Pending JP2015512900A (en) | 2012-03-28 | 2012-03-28 | Combination therapy to treat HCV infection in a special patient genotype subpopulation |
Country Status (2)
| Country | Link |
|---|---|
| JP (1) | JP2015512900A (en) |
| WO (2) | WO2013143581A1 (en) |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2011053617A1 (en) * | 2009-10-30 | 2011-05-05 | Boehringer Ingelheim International Gmbh | Dosage regimens for hcv combination therapy comprising bi201335, interferon alpha and ribavirin |
| JP2012502999A (en) * | 2008-09-17 | 2012-02-02 | ベーリンガー インゲルハイム インターナショナル ゲゼルシャフト ミット ベシュレンクテル ハフツング | Combination of HCV NS3 protease inhibitors with interferon and ribavirin |
Family Cites Families (24)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4211771A (en) | 1971-06-01 | 1980-07-08 | Robins Ronald K | Treatment of human viral diseases with 1-B-D-ribofuranosyl-1,2,4-triazole-3-carboxamide |
| US4530901A (en) | 1980-01-08 | 1985-07-23 | Biogen N.V. | Recombinant DNA molecules and their use in producing human interferon-like polypeptides |
| US6936694B1 (en) | 1982-05-06 | 2005-08-30 | Intermune, Inc. | Manufacture and expression of large structural genes |
| US4766106A (en) | 1985-06-26 | 1988-08-23 | Cetus Corporation | Solubilization of proteins for pharmaceutical compositions using polymer conjugation |
| US4917888A (en) | 1985-06-26 | 1990-04-17 | Cetus Corporation | Solubilization of immunotoxins for pharmaceutical compositions using polymer conjugation |
| JP2514950B2 (en) | 1986-03-10 | 1996-07-10 | エフ・ホフマン―ラ ロシユ アーゲー | Chemically modified protein, its production method and intermediate |
| US5595732A (en) | 1991-03-25 | 1997-01-21 | Hoffmann-La Roche Inc. | Polyethylene-protein conjugates |
| FR2686899B1 (en) | 1992-01-31 | 1995-09-01 | Rhone Poulenc Rorer Sa | NOVEL BIOLOGICALLY ACTIVE POLYPEPTIDES, THEIR PREPARATION AND PHARMACEUTICAL COMPOSITIONS CONTAINING THEM. |
| US5382657A (en) | 1992-08-26 | 1995-01-17 | Hoffmann-La Roche Inc. | Peg-interferon conjugates |
| CA2176229C (en) | 1993-11-10 | 2003-05-27 | Carl W. Gilbert | Improved interferon polymer conjugates |
| US5824784A (en) | 1994-10-12 | 1998-10-20 | Amgen Inc. | N-terminally chemically modified protein compositions and methods |
| US5908621A (en) | 1995-11-02 | 1999-06-01 | Schering Corporation | Polyethylene glycol modified interferon therapy |
| US5767097A (en) | 1996-01-23 | 1998-06-16 | Icn Pharmaceuticals, Inc. | Specific modulation of Th1/Th2 cytokine expression by ribavirin in activated T-lymphocytes |
| TW517067B (en) | 1996-05-31 | 2003-01-11 | Hoffmann La Roche | Interferon conjugates |
| US6323180B1 (en) | 1998-08-10 | 2001-11-27 | Boehringer Ingelheim (Canada) Ltd | Hepatitis C inhibitor tri-peptides |
| US6277830B1 (en) | 1998-10-16 | 2001-08-21 | Schering Corporation | 5′-amino acid esters of ribavirin and the use of same to treat hepatitis C with interferon |
| US6403564B1 (en) | 1998-10-16 | 2002-06-11 | Schering Corporation | Ribavirin-interferon alfa combination therapy for eradicating detectable HCV-RNA in patients having chronic hepatitis C infection |
| EP1594530A4 (en) | 2003-01-22 | 2006-10-11 | Human Genome Sciences Inc | Albumin fusion proteins |
| ES2297424T3 (en) | 2003-05-21 | 2008-05-01 | Boehringer Ingelheim International Gmbh | INHIBITING COMPOUNDS OF HEPATITIS C. |
| CA2554089C (en) | 2004-02-09 | 2013-10-22 | Human Genome Sciences, Inc. | Albumin fusion proteins |
| US7514557B2 (en) | 2004-05-25 | 2009-04-07 | Boehringer Ingelheim International Gmbh | Process for preparing acyclic HCV protease inhibitors |
| PT2331538E (en) | 2008-09-16 | 2014-05-12 | Boehringer Ingelheim Int | Crystalline forms of a 2-thiazolyl- 4-quinolinyl-oxy derivative, a potent hcv inhibitor |
| KR20110087297A (en) | 2008-11-21 | 2011-08-02 | 베링거 인겔하임 인터내셔날 게엠베하 | Pharmaceutical Compositions of Potent HCC Inhibitors for Oral Administration |
| ME01718B (en) | 2009-07-07 | 2014-09-20 | Boehringer Ingelheim Int | Pharmaceutical composition for a hepatitis C viral protease inhibitor |
-
2012
- 2012-03-28 JP JP2015502107A patent/JP2015512900A/en active Pending
- 2012-03-28 WO PCT/EP2012/055453 patent/WO2013143581A1/en not_active Ceased
-
2013
- 2013-03-27 WO PCT/EP2013/056499 patent/WO2013144193A1/en not_active Ceased
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2012502999A (en) * | 2008-09-17 | 2012-02-02 | ベーリンガー インゲルハイム インターナショナル ゲゼルシャフト ミット ベシュレンクテル ハフツング | Combination of HCV NS3 protease inhibitors with interferon and ribavirin |
| WO2011053617A1 (en) * | 2009-10-30 | 2011-05-05 | Boehringer Ingelheim International Gmbh | Dosage regimens for hcv combination therapy comprising bi201335, interferon alpha and ribavirin |
Non-Patent Citations (6)
| Title |
|---|
| JPN6016001720; 'Press Release' [online] , 20111122, ベーリンガーインゲルハイムジャパン株式会社広報部 * |
| JPN6016001723; White PW, et al.: 'Preclinical characterization of BI 201335, a C-terminal carboxylic acid inhibitor of the hepatitis C' Antimicrobial Agents and Chemotherapy Vol.54, No.11, 201011, p.4611-4618 * |
| JPN6016001725; Lemke CT, et al.: 'Combined X-ray, NMR, and kinetic analyses reveal uncommon binding characteristics of the hepatitis C' The Journal of Biological Chemistry Vol.286, No.13, 20110401, p.11434-11443 * |
| JPN6016001729; 杉山 真也,溝上 雅史: 'ゲノミクスの手法に基づくHCV感染者のIFN治療効果の研究' ウイルス 第61巻,第1号, 2011, p.15-24 * |
| JPN6016001733; 渡邊 綱正,田中 靖人: 'IL28B:C型肝炎テーラーメイド治療の幕開け' Nagoya Medical Journal 第52巻,第1号, 2011, p.51-56 * |
| JPN6016001736; 松浦 健太郎, 田中 靖人: 'IL-28B遺伝子多型とC型肝炎' 医学のあゆみ 第239巻,第12-13号, 20111224, p.1183-1188 * |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2013143581A1 (en) | 2013-10-03 |
| WO2013144193A1 (en) | 2013-10-03 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5539363B2 (en) | Combination of HCV NS3 protease inhibitors with interferon and ribavirin | |
| EP2061513B1 (en) | Method of treating hepatitis c patients | |
| HUP0301444A2 (en) | The use of ribavirin-pegylated interferon alfa for the preparation of pharmaceutical compositions for the treatment of hcv infection | |
| US8822496B2 (en) | Dosage regimens for HCV combination therapy | |
| EP2776024A1 (en) | Methods and compositions for treating hepatitis c virus | |
| CN1635886A (en) | Method for treating diseases with omega interferon | |
| CN1368887A (en) | Mycophenolate Mofetil in association with PEG-IFN alpha | |
| US20010046957A1 (en) | Method for treating hepatitis C | |
| US20150273015A1 (en) | Treatments of hepatitis c virus infection | |
| US20150147295A1 (en) | Combination therapy for treating hcv infection in specific patient subgenotype sub-population | |
| JP2015512900A (en) | Combination therapy to treat HCV infection in a special patient genotype subpopulation | |
| JP2014509628A (en) | Alice polyvir for treating hepatitis C virus infection | |
| JP2015509980A (en) | Combination therapy to treat HCV infection in a population of HCV-HIV co-infected patients | |
| US20140335052A1 (en) | Combination therapy for treating hcv infection in an hcv-hiv coinfected patient population | |
| WO2014138374A1 (en) | Oral combination therapy for treating hcv infection in specific patient sub-population | |
| HK1129315B (en) | Method of treating hepatitis c patients | |
| HK1167609A (en) | A method of treating hepatitis c patients | |
| CN103732242A (en) | Treatment of chronic hepatitis C in a patient population with IFN-α5 in combination with IFN-α2b |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20150325 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20150325 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20160120 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20161005 |