JP2008537941A - Fc variants with optimized properties - Google Patents
Fc variants with optimized properties Download PDFInfo
- Publication number
- JP2008537941A JP2008537941A JP2008504389A JP2008504389A JP2008537941A JP 2008537941 A JP2008537941 A JP 2008537941A JP 2008504389 A JP2008504389 A JP 2008504389A JP 2008504389 A JP2008504389 A JP 2008504389A JP 2008537941 A JP2008537941 A JP 2008537941A
- Authority
- JP
- Japan
- Prior art keywords
- antibody
- variant
- positions
- variants
- polypeptide
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Landscapes
- Peptides Or Proteins (AREA)
Abstract
本発明は、最適化特性を有するFc変異体、それらの製造方法、最適化特性を有するFc変異体を含むFcポリペプチド、ならびに最適化特性を有するFc変異体の使用方法に関する。 The present invention relates to Fc variants with optimized properties, methods for their production, Fc polypeptides comprising Fc variants with optimized properties, and methods of using Fc variants with optimized properties.
Description
本発明は、2005年3月31日出願のUSSN60/667,197;2005年8月3日出願のUSSN60/705,378;2005年10月3日出願のUSSN60/723,294;および、2005年10月3日出願のUSSN60/723,335;ならびに、2005年5月5日出願のUSSN11/124,620の一部継続出願(全て、参照によりその全体が本明細書中に包含される。)に対し米国特許法119条(e)項の利益を請求する。2004年3月26日出願の米国特許出願番号第10/822,231号の開示内容はまた、参照によりその全体が明示的に包含される。 USSN 60 / 667,197 filed March 31, 2005; USSN 60 / 705,378 filed August 3, 2005; USSN 60 / 723,294 filed October 3, 2005; and 2005 USSN 60 / 723,335 filed Oct. 3, and USSN 11 / 124,620, filed May 5, 2005, all of which are hereby incorporated by reference in their entirety. Claim the benefit of Section 119 (e) of the US Patent Act. The disclosure of US patent application Ser. No. 10 / 822,231 filed Mar. 26, 2004 is also expressly incorporated by reference in its entirety.
発明の分野
本発明は、最適化特性を有するFc変異体ポリペプチド、それらの製造のための操作(engineering)方法、および特に治療目的でのそれらの適用に関する。
The present invention relates to Fc variant polypeptides with optimized properties, engineering methods for their production, and their application, particularly for therapeutic purposes.
発明の背景
抗体は、特定の抗原に結合する免疫学的タンパク質である。ヒトおよびマウスを含むほとんどの哺乳動物において、抗体は、一対の重鎖および軽鎖ポリペプチド鎖から構築される。各鎖は、個々の免疫グロブリン(Ig)ドメインから成り、故に、一般名である免疫グロブリンが、そのようなタンパク質に用いられる。各鎖は、可変領域(V領域)および定常領域と称される2個の異なる領域から成る。軽鎖可変領域(VL)および重鎖可変領域(VH)は、抗体間の顕著な配列多様性を示し、標的抗原への結合に関与する。定常領域は、配列多様性をあまり示さず、多くの天然タンパク質の結合に関与して重要な生化学的事象を引き起こす。ヒトでは、IgA(IgA1およびIgA2サブクラスを含む)、IgD、IgE、IgG(IgG1、IgG2、IgG3およびIgG4サブクラスを含む)、およびIgMを含む5種の異なる抗体クラスがある。これらの抗体クラス間の顕著な特徴は、それらの定常領域であるが、わずかな差異がV領域に存在し得る。免疫グロブリンの一般的な構造的特徴を記載する例として本明細書で用いる図1は、IgG1抗体を示す。IgG抗体は、2個の重鎖および2個の軽鎖からなる四量体タンパク質である。IgG重鎖は、N末端からC末端にVH−CH1−CH2−CH3(それぞれ、重鎖可変ドメイン、重鎖定常ドメイン1、重鎖定常ドメイン2、および重鎖定常ドメイン3を示す。)(また、VH−Cγ1−Cγ2−Cγ3(それぞれ、重鎖可変ドメイン、定常ガンマ1ドメイン、定常ガンマ2ドメイン、および定常ガンマ3ドメインを示す。)とも称される。)の順で連結する4個の免疫グロブリンドメインからなる。IgG軽鎖は、N末端からC末端にVL−CL(それぞれ、軽鎖可変ドメインおよび軽鎖定常ドメインを示す。)の順で連結した2個の免疫グロブリンドメインからなる。
BACKGROUND OF THE INVENTION Antibodies are immunological proteins that bind to a specific antigen. In most mammals, including humans and mice, antibodies are constructed from a pair of heavy and light chain polypeptide chains. Each chain consists of an individual immunoglobulin (Ig) domain, hence the generic name immunoglobulin is used for such proteins. Each chain consists of two different regions called the variable region (V region) and the constant region. The light chain variable region (VL) and heavy chain variable region (VH) exhibit significant sequence diversity between antibodies and are involved in binding to the target antigen. The constant region does not show much sequence diversity and is involved in the binding of many natural proteins, causing important biochemical events. In humans, there are five different antibody classes including IgA (including IgA1 and IgA2 subclasses), IgD, IgE, IgG (including IgG1, IgG2, IgG3 and IgG4 subclasses), and IgM. A striking feature between these antibody classes is their constant region, although slight differences may exist in the V region. FIG. 1, used herein as an example to describe the general structural characteristics of immunoglobulins, shows an IgG1 antibody. An IgG antibody is a tetrameric protein consisting of two heavy chains and two light chains. The IgG heavy chain represents V H -CH1-CH2-CH3 from the N-terminus to the C-terminus (representing heavy chain variable domain, heavy chain
抗体の可変領域は、分子の抗原結合決定基を含み、故に、その標的抗原に対する抗体の特異性を決定する。可変領域は、同じクラス内の他の抗体と配列が最も異なるため、そのように称される。配列多様性の大部分は、相補性決定領域(CDR)中に生じる。重鎖および軽鎖あたりそれぞれ3個の、VH CDR1、VH CDR2、VH CDR3、VL CDR1、VL CDR2、およびVL CDR3で示される、計6個のCDRがある。可変領域のうちCDR以外は、フレームワーク(FR)領域と称される。CDRほど多様ではないが、配列多様性が、異なる抗体間のFR領域中に生じる。概して、抗体のこの特徴的構造は、実質的な抗原結合の多様性(CDR)が免疫系により調査され、広範囲の抗原に対する特異性を得ることを可能にする、安定な骨格(FR領域)を提供する。多くの高分解能構造が、異なる生物由来の多様な可変領域断片(いくつかは抗原と非結合、およびいくつかは抗原との複合体)に利用可能である。抗体可変領域の配列および構造的特徴は、よく特徴付けられており(Morea et al., 1997, Biophys Chem 68:9−16;Morea et al., 2000, Methods 20:267−279、参照によりその全体が本明細書中に包含される)、抗体の保存的特徴は、多くの抗体操作技術の開発を可能にしている(Maynard et al., 2000, Annu Rev Biomed Eng 2:339−376、参照によりその全体が本明細書中に包含される)。例えば、ある抗体、例えばマウス抗体由来のCDRを、別の抗体、例えばヒト抗体のフレームワーク領域に移植することが可能である。この方法は、当技術分野で“ヒト化”と称され、非ヒト抗体由来の免疫原性の低い抗体治療剤の製造を可能とする。可変領域を含む断片は、抗体の他の領域を欠失して存在することができ、例えばVH−Cγ1およびVH−CLを含む抗原結合断片(Fab)、VHおよびVLを含む可変断片(Fv)、同じ鎖中で共に連結するVHおよびVLを含む単鎖可変断片(scFv)、ならびに多様な他の可変領域断片が含まれる(Little et al., 2000, Immunol Today 21:364−370、参照によりその全体が本明細書中に包含される)。 The variable region of an antibody contains the antigen-binding determinants of the molecule and thus determines the specificity of the antibody for its target antigen. Variable regions are so named because they are most different in sequence from other antibodies in the same class. Most of the sequence diversity occurs in the complementarity determining region (CDR). There are a total of 6 CDRs, denoted V H CDR1, V H CDR2, V H CDR3, V L CDR1, V L CDR2, and V L CDR3, each 3 per heavy and light chain. The variable region other than the CDR is called a framework (FR) region. Although not as diverse as CDRs, sequence diversity occurs in the FR regions between different antibodies. In general, this characteristic structure of an antibody provides a stable scaffold (FR region) that allows substantial antigen binding diversity (CDR) to be investigated by the immune system to obtain specificity for a wide range of antigens. provide. Many high resolution structures are available for various variable region fragments from different organisms, some unbound with antigen and some in complex with antigen. The sequence and structural characteristics of antibody variable regions are well characterized (Morea et al., 1997, Biophys Chem 68: 9-16; Morea et al., 2000, Methods 20: 267-279, with reference to Conserved features of antibodies, which are encompassed herein in their entirety, allow the development of many antibody engineering techniques (see Maynard et al., 2000, Annu Rev Biomed Eng 2: 339-376). Are incorporated herein in their entirety). For example, a CDR from one antibody, such as a mouse antibody, can be transplanted into the framework region of another antibody, such as a human antibody. This method is referred to in the art as “humanization” and allows the production of less immunogenic antibody therapeutics derived from non-human antibodies. Fragment containing the variable region can exist lacking other regions of the antibody, including for example, V H -Shiganma1 and V H -C antigen-binding fragments comprising an L (Fab), the V H and V L Variable fragments (Fv), single chain variable fragments (scFv) containing V H and V L linked together in the same chain, and a variety of other variable region fragments are included (Little et al., 2000, Immunol Today 21 : 364-370, which is incorporated herein by reference in its entirety).
抗体のFc領域は、多くのFc受容体およびリガンドと相互作用し、エフェクター機能と称される一連の重要な機能を与える。IgGに関して、図1に示す通り、Fc領域は、IgドメインCγ2およびCγ3、ならびにCγ2につながるN末端ヒンジを含む。IgGクラスに関して重要なFc受容体ファミリーは、Fcガンマ受容体(FcγR)である。これらの受容体は、抗体と細胞性免疫応答とのコミュニケーションを仲介する(Raghavan et al., 1996, Annu Rev Cell Dev Biol 12:181−220;Ravetch et al., 2001, Annu Rev Immunol 19:275−290、両方とも、参照によりその全体が本明細書中に包含される)。ヒトにおいて、このタンパク質ファミリーには、イソ型であるFcγRIa、FcγRIbおよびFcγRIcを含むFcγRI(CD64);イソ型であるFcγRIIa(アロタイプH131およびR131を含む)、FcγRIIb(FcγRIIb−1およびFcγRIIb−2を含む)およびFcγRIIcを含むFcγRII(CD32);ならびに、イソ型であるFcγRIIIa(アロタイプV158およびF158を含む)およびFcγRIIIb(アロタイプFcγRIIIb−NA1およびFcγRIIIb−NA2を含む)を含むFcγRIII(CD16)が含まれる(Jefferis et al., 2002, Immunol Lett 82:57−65、参照によりその全体が本明細書中に包含される)。これらの受容体は、典型的に、Fcとの結合を仲介する細胞外ドメイン、膜貫通領域、および細胞内のいくつかのシグナル伝達事象を仲介し得る細胞内ドメインを有する。これらの受容体は、単球、マクロファージ、好中球、樹状細胞、好酸球、マスト細胞、血小板、B細胞、大型顆粒リンパ球、ランゲルハンス細胞、ナチュラルキラー(NK)細胞、およびγγT細胞を含む、様々な免疫細胞において発現される。Fc/FcγR複合体の形成は、これらのエフェクター細胞を結合した抗原の部位に捕捉し、典型的に、細胞内のシグナル伝達事象ならびに、炎症メディエーターの放出、B細胞活性化、エンドサイトーシス、食作用、および細胞傷害性攻撃のようなその後の重要な免疫応答をもたらす。細胞傷害性および食作用エフェクター機能を仲介する能力は、抗体が標的細胞を破壊することによる可能性のある機序である。FcγRを発現する非特異的細胞傷害性細胞が、標的細胞への抗体の結合を認識し、次いで標的細胞の溶解をもたらす細胞により仲介される反応は、抗体依存性細胞介在性細胞傷害作用(ADCC)と称される(Raghavan et al., 1996, Annu Rev Cell Dev Biol 12:181−220;Ghetie et al., 2000, Annu Rev Immunol 18:739−766;Ravetch et al., 2001, Annu Rev Immunol 19:275−290、全て、参照によりその全体が本明細書中に包含される)。FcγRを発現する非特異的細胞傷害性細胞が、標的細胞への抗体の結合を認識し、次いで標的細胞の食作用をもたらす細胞により仲介される反応は、抗体依存性細胞介在性食作用(ADCP)と称される。FcγRIIa(pdb受託コード1H9V、参照によりその全体が本明細書中に包含される)(Sondermann et al., 2001, J Mol Biol 309:737−749、参照によりその全体が本明細書中に包含される)(pdb受託コード1FCG、参照によりその全体が本明細書中に包含される)(Maxwell et al., 1999, Nat Struct Biol 6:437−442、参照によりその全体が本明細書中に包含される)、FcγRIIb(pdb受託コード2FCB、参照によりその全体が本明細書中に包含される)(Sondermann et al., 1999, Embo J 18:1095−1103、参照によりその全体が本明細書中に包含される);および、FcγRIIIb(pdb受託コード1E4J、参照によりその全体が本明細書中に包含される)(Sondermann et al., 2000, Nature 406:267−273、参照によりその全体が本明細書中に包含される)を含むヒトFcγRの細胞外ドメインの多くの構造が、解明されている。全てのFcγRは、図2に示す通り、Cγ2ドメインおよび前記ヒンジのN末端でFc上の同じ領域に結合する。この相互作用は、構造的によく特徴付けられており(Sondermann et al., 2001, J Mol Biol 309:737−749、参照によりその全体が本明細書中に包含される)、ヒトFcγRIIIbの細胞外ドメインに結合するヒトFcのいくつかの構造(pdb受託コード1E4K、参照によりその全体が本明細書中に包含される)(Sondermann et al., 2000, Nature 406:267−273、参照によりその全体が本明細書中に包含される)(pdb受託コード1IISおよび1IIX、参照によりその全体が本明細書中に包含される)(Radaev et al., 2001, J Biol Chem 276:16469−16477、参照によりその全体が本明細書中に包含される)、ならびにヒトIgE Fc/FcεRIα複合体の構造(pdb受託コード1F6A、参照によりその全体が本明細書中に包含される)(Garman et al., 2000, Nature 406:259−266、参照によりその全体が本明細書中に包含される)は、解明されてきた。 The Fc region of an antibody interacts with many Fc receptors and ligands and provides a series of important functions called effector functions. For IgG, as shown in FIG. 1, the Fc region includes Ig domains Cγ2 and Cγ3, and an N-terminal hinge leading to Cγ2. An important Fc receptor family for the IgG class is the Fc gamma receptor (FcγR). These receptors mediate communication between antibodies and cellular immune responses (Raghavan et al., 1996, Annu Rev Cell Dev Biol 12: 181-220; Ravetch et al., 2001, Annu Rev Immunol 19: 275 -290, both of which are incorporated herein by reference in their entirety). In humans, this protein family includes FcγRIa (CD64) including isoforms FcγRIa, FcγRIb and FcγRIc; FcγRIIa (including allotypes H131 and R131), FcγRIIb (FcγRIIb-1 and FcγRIIb-2) And FcγRII (CD32) including FcγRIIIa (including allotypes FcγRIIIb-NA1 and FcγRIIIb-NA2) including FcγRIIIa (including allotypes V158 and F158) and FcγRIIIb (CD16), including FcγRIIc (Jefferis) et al., 2002, Immunol Lett 82: 57-65, which is incorporated herein in its entirety by reference). These receptors typically have an extracellular domain that mediates binding to Fc, a transmembrane region, and an intracellular domain that can mediate several signaling events within the cell. These receptors include monocytes, macrophages, neutrophils, dendritic cells, eosinophils, mast cells, platelets, B cells, large granular lymphocytes, Langerhans cells, natural killer (NK) cells, and γγ T cells. It is expressed in a variety of immune cells, including. The formation of the Fc / FcγR complex captures these effector cells at the site of the bound antigen and typically causes intracellular signaling events as well as release of inflammatory mediators, B cell activation, endocytosis, phagocytosis Effects and subsequent important immune responses such as cytotoxic attack. The ability to mediate cytotoxic and phagocytic effector functions is a possible mechanism by which antibodies destroy target cells. The reaction mediated by non-specific cytotoxic cells that express FcγR recognizes the binding of the antibody to the target cell and then results in the lysis of the target cell is an antibody-dependent cell-mediated cytotoxicity (ADCC). (Raghavan et al., 1996, Annu Rev Cell Dev Biol 12: 181-220; Ghetie et al., 2000, Annu Rev Immunol 18: 739-766; Ravetch et al., 2001, Annu Rev Immunol 19: 275-290, all of which are incorporated herein by reference in their entirety). The reaction mediated by non-specific cytotoxic cells expressing FcγR that recognize antibody binding to the target cell and then phagocytoses the target cell is antibody-dependent cell-mediated phagocytosis (ADCP). ). FcγRIIa (pdb accession code 1H9V, incorporated herein by reference in its entirety) (Sondermann et al., 2001, J Mol Biol 309: 737-749, incorporated herein by reference in its entirety. (Pdb accession code 1FCG, incorporated herein by reference in its entirety) (Maxwell et al., 1999, Nat Struct Biol 6: 437-442, incorporated herein by reference in its entirety. FcγRIIb (pdb accession code 2FCB, which is incorporated herein by reference in its entirety) (Sondermann et al., 1999, Embo J 18: 1095-1103, which is hereby incorporated by reference in its entirety. And FcγRIIIb (pdb accession code 1E4J, which is hereby incorporated in its entirety by reference) (Sondermann et al., 2000, Nature 406: 267-273, which is hereby incorporated by reference in its entirety. Included in the specification) Many structure of the extracellular domain of bets FcγR have been elucidated. All FcγRs bind to the same region on Fc at the N-terminus of the Cγ2 domain and the hinge, as shown in FIG. This interaction is structurally well characterized (Sondermann et al., 2001, J Mol Biol 309: 737-749, which is hereby incorporated by reference in its entirety) and is a cell of human FcγRIIIb Some structures of human Fc that bind to the outer domain (pdb accession code 1E4K, which is incorporated by reference in its entirety) (Sondermann et al., 2000, Nature 406: 267-273, (Incorporated herein in its entirety) (pdb accession codes 1IIS and 11IX, which is incorporated herein in its entirety by reference) (Radaev et al., 2001, J Biol Chem 276: 16469-16477, The entirety of which is hereby incorporated by reference), as well as the structure of the human IgE Fc / FcεRIα complex (pdb accession code 1F6A, which is hereby incorporated in its entirety by reference) (Garman et al. , 2000, Nature 406: 259-266 By reference in its entirety are incorporated herein) has been elucidated.
異なるIgGサブクラスは、FcγRに対して異なる親和性を有し、IgG1およびIgG3は典型的に、受容体に対してIgG2およびIgG4よりも実質的によく結合する(Jefferis et al., 2002, Immunol Lett 82:57−65、参照によりその全体が本明細書中に包含される)。全てのFcγRは、異なる親和性を有するが、IgG Fcの同じ領域に結合する:高親和性結合体であるFcγRIは、IgG1についてKd10−8M−1を有し、一方、低親和性受容体であるFcγRIIおよびFcγRIIIは、一般的に、それぞれ10−6および10−5で結合する。FcγRIIIaおよびFcγRIIIbの細胞外ドメインは、96%の同一性を有する;しかしながら、FcγRIIIbは、細胞内シグナル伝達ドメインを有さない。さらに、免疫受容体チロシン依存性活性化モチーフ(ITAM)を有する細胞内ドメインを有することにより特徴付けられるFcγRI、FcγRIIa/c、およびFcγRIIIaは、免疫複合体により誘発される活性化の正の調節因子であるが、FcγRIIbは、免疫受容体チロシン依存性阻害モチーフ(ITIM)を有し、故に阻害性である。故に、前者は、活性化受容体と称され、FcγRIIbは、阻害性受容体と称される。前記受容体はまた、様々な免疫細胞で発現パターンおよびレベルが異なる。さらに別の複雑度は、ヒトプロテオームにおける多くのFcγR多型の存在である。臨床的重要性を有する特に関連する多型は、V158/F158 FcγRIIIaである。ヒトIgG1は、F158アロタイプよりもV158アロタイプにより高い親和性で結合する。この親和性の差異、およびADCCおよび/またはADCPに対する推定上のその効果が、抗CD20抗体であるリツキシマブ(リツキサン(登録商標)、BiogenIdec)の効果の重要な決定因子であることが示されている。V158アロタイプを有する患者は、リツキシマブ処置に好都合に応答する;しかしながら、低親和性のF158アロタイプを有する患者は、ほとんど応答しない(Cartron et al., 2002, Blood 99:754−758、参照によりその全体が本明細書中に包含される)。ヒトの約10−20%が、V158/V158ホモ接合型であり、45%が、V158/F158ヘテロ接合型であり、そして35−45%が、F158/F158ホモ接合型である(Lehrnbecher et al., 1999, Blood 94:4220−4232;Cartron et al., 2002, Blood 99:754−758、両方とも、参照によりその全体が本明細書中に包含される)。故に、ヒトの80−90%がほとんど応答せず、例えば、彼らは、F158 FcγRIIIaの少なくとも一方のアレルを有する。 Different IgG subclasses have different affinities for FcγR, and IgG1 and IgG3 typically bind substantially better to the receptor than IgG2 and IgG4 (Jefferis et al., 2002, Immunol Lett 82: 57-65, which is hereby incorporated by reference in its entirety). All FcγRs have different affinities but bind to the same region of IgG Fc: the high affinity binder FcγRI has a Kd10 −8 M −1 for IgG1, while a low affinity receptor FcγRII and FcγRIII, which generally bind at 10 −6 and 10 −5 , respectively. The extracellular domains of FcγRIIIa and FcγRIIIb have 96% identity; however, FcγRIIIb does not have an intracellular signaling domain. Furthermore, FcγRI, FcγRIIa / c, and FcγRIIIa, characterized by having an intracellular domain with an immunoreceptor tyrosine-dependent activation motif (ITAM), are positive regulators of activation induced by immune complexes. However, FcγRIIb has an immunoreceptor tyrosine-dependent inhibition motif (ITIM) and is therefore inhibitory. Therefore, the former is called an activating receptor and FcγRIIb is called an inhibitory receptor. The receptors also differ in expression patterns and levels in various immune cells. Yet another complexity is the presence of many FcγR polymorphisms in the human proteome. A particularly relevant polymorphism with clinical significance is V158 / F158 FcγRIIIa. Human IgG1 binds with higher affinity to the V158 allotype than to the F158 allotype. This difference in affinity and its putative effect on ADCC and / or ADCP has been shown to be an important determinant of the effect of the anti-CD20 antibody rituximab (Rituxan®, BiogenIdec) . Patients with the V158 allotype respond favorably to rituximab treatment; however, patients with the low affinity F158 allotype rarely respond (Cartron et al., 2002, Blood 99: 754-758, in its entirety by reference). Is encompassed herein). About 10-20% of humans are V158 / V158 homozygous, 45% are V158 / F158 heterozygous, and 35-45% are F158 / F158 homozygous (Lehrnbecher et al ., 1999, Blood 94: 4220-4322; Cartron et al., 2002, Blood 99: 754-758, both of which are hereby incorporated by reference in their entirety). Thus, 80-90% of humans hardly respond, for example, they have at least one allele of F158 FcγRIIIa.
図1に示すFc上の重複しているが別個の部位は、補体タンパク質C1qのための接合部位として機能する。Fc/FcγR結合がADCCを仲介するのと同様に、Fc/C1q結合は、補体依存性細胞傷害作用(CDC)を仲介する。C1qは、セリンプロテアーゼであるC1rおよびC1sと複合体を形成し、C1複合体を形成する。C1qは、6個の抗体を結合し得るが、2個のIgGとの結合が、補体カスケードを活性化するのに十分である。FcとFcγRの相互作用と同様に、様々なIgGサブクラスが、C1qに対して異なる親和性を有し、典型的に、IgG1およびIgG3は、FcγRに対してIgG2およびIgG4よりも実質的に結合する(Jefferis et al., 2002, Immunol Lett 82:57−65、参照によりその全体が本明細書中に包含される)。現在、Fc/C1q複合体に利用可能な構造は存在しない;しかしながら、変異誘発実験は、C1qに対するヒトIgG上の結合部位を残基D270、K322、K326、P329、P331およびE333を含む領域にマッピングした(Idusogie et al., 2000, J Immunol 164:4178−4184; Idusogie et al., 2001, J Immunol 166:2571−2575、両方とも、参照によりその全体が本明細書中に包含される)。 The overlapping but distinct site on Fc shown in FIG. 1 functions as a junction site for complement protein C1q. Just as Fc / FcγR binding mediates ADCC, Fc / C1q binding mediates complement dependent cytotoxicity (CDC). C1q forms a complex with C1r and C1s, which are serine proteases, to form a C1 complex. C1q can bind 6 antibodies, but binding to 2 IgGs is sufficient to activate the complement cascade. Similar to the Fc and FcγR interaction, various IgG subclasses have different affinities for C1q, and typically IgG1 and IgG3 bind substantially more to FcγR than IgG2 and IgG4 (Jefferis et al., 2002, Immunol Lett 82: 57-65, which is hereby incorporated by reference in its entirety). Currently there is no structure available for the Fc / C1q complex; however, mutagenesis experiments map the binding site on human IgG to C1q to a region containing residues D270, K322, K326, P329, P331 and E333. (Idusogie et al., 2000, J Immunol 164: 4178-4184; Idusogie et al., 2001, J Immunol 166: 2571-2575, both of which are hereby incorporated by reference in their entirety).
図1に示すCγ2ドメインとCγ3ドメインの間のFc上の部位は、胎児性受容体(neonatal receptor:FcRn)との相互作用を仲介し、その結合は、エンドサイトーシスされた抗体をエンドソームから血流に戻して再利用する(Raghavan et al., 1996, Annu Rev Cell Dev Biol 12:181−220;Ghetie et al., 2000, Annu Rev Immunol 18:739−766、両方とも参照によりその全体が本明細書中に包含される)。この過程は、全長分子のサイズが大きいため腎臓ろ過による除去を伴い、結果として、1ないし3週間までの範囲の好都合な抗体の血清半減期をもたらす。FcのFcRnとの結合はまた、抗体輸送において重要な役割を果たす。FcRnのためのFc上の結合部位は、細菌プロテインAおよびGが結合する部位でもある。これらのタンパク質による強い結合は、典型的に、タンパク質精製中に、タンパク質Aまたはタンパク質G親和性クロマトグラフィーを用いることにより抗体を精製するための手段として用いられる。故に、Fc上のこの領域の適合度は、抗体の臨床的特徴およびそれらの精製の両方に重要である。ラットFc/FcRn複合体(Burmeister et al., 1994, Nature, 372:379−383;Martin et al., 2001, Mol Cell 7:867−877、両方とも参照によりその全体が本明細書中に包含される)、およびFcとタンパク質AおよびGとの複合体(Deisenhofer, 1981, Biochemistry 20:2361−2370;Sauer−Eriksson et al., 1995, Structure 3:265−278;Tashiro et al., 1995, Curr Opin Struct Biol 5:471−481、全て参照によりその全体が本明細書中に包含される)の利用可能な構造は、Fcとこれらのタンパク質の相互作用に関する理解を提供する。 The site on the Fc between the Cγ2 domain and the Cγ3 domain shown in FIG. 1 mediates interaction with the fetal receptor (neonatal receptor: FcRn), and the binding of the endocytic antibody from the endosome to the blood Recycled and reused (Raghavan et al., 1996, Annu Rev Cell Dev Biol 12: 181-220; Ghetie et al., 2000, Annu Rev Immunol 18: 739-766, both of which are incorporated by reference in their entirety. Included in the specification). This process involves removal by renal filtration due to the large size of the full-length molecule, resulting in a convenient antibody serum half-life ranging from 1 to 3 weeks. The binding of Fc to FcRn also plays an important role in antibody transport. The binding site on Fc for FcRn is also the site where bacterial proteins A and G bind. Strong binding by these proteins is typically used as a means to purify antibodies by using protein A or protein G affinity chromatography during protein purification. Therefore, the suitability of this region on Fc is important for both clinical features of antibodies and their purification. Rat Fc / FcRn complex (Burmeister et al., 1994, Nature, 372: 379-383; Martin et al., 2001, Mol Cell 7: 867-877, both of which are hereby incorporated by reference in their entirety. And a complex of Fc and proteins A and G (Deisenhofer, 1981, Biochemistry 20: 2361-2370; Sauer-Eriksson et al., 1995, Structure 3: 265-278; Tashiro et al., 1995, The available structure of Curr Opin Struct Biol 5: 471-481, all incorporated herein by reference in its entirety, provides an understanding of the interaction of Fc with these proteins.
Fc領域の1つの重要な特徴は、図1に示すN297に起こる保存されたN結合グリコシル化である。よく記載される通り、この炭水化物またはオリゴ糖は、抗体にとって重要な構造的かつ機能的役割を果たし、抗体を哺乳動物発現系を用いて製造しなければならない根本的理由の1つである。1つの理論に制限されることを望まないが、この炭水化物の構造的目的は、Fcを安定化または可溶化すること、Cγ3とCγ2ドメインの間の特定の角度またはフレキシビリティーレベルを決定すること、2個のCγ2ドメインを互いに中心軸を横切って凝集しないようにすること、またはこれらの組み合わせであり得ると考えられる。FcγRおよびC1qとの効率的なFc結合は、この修飾を必要とし、N297炭水化物の組成の変化またはその除去がこれらのタンパク質との結合に影響を与える(Umana et al., 1999, Nat Biotechnol 17:176−180; Davies et al., 2001, Biotechnol Bioeng 74:288−294; Mimura et al., 2001, J Biol Chem 276:45539−45547.; Radaev et al., 2001, J Biol Chem 276:16478−16483; Shields et al., 2001, J Biol Chem 276:6591−6604; Shields et al., 2002, J Biol Chem 277:26733−26740; Simmons et al., 2002, J Immunol Methods 263:133−147、全て参照によりその全体が本明細書中に包含される)。該炭水化物は、FcγRと何ら特定の結合を作製しないが(Radaev et al., 2001, J Biol Chem 276:16469−16477、参照によりその全体が本明細書中に包含される)、Fc/FcγR結合を仲介するN297炭水化物の機能的役割が、Fc立体構造を決定する構造的役割を果たし得ることが示される。このことは、4個の異なるFc糖型の結晶構造の収集により支持され、それは、オリゴ糖の組成が、Cγ2の立体構造に影響を与え、結果としてFc/FcγR結合をもたらすことを示す(Krapp et al., 2003, J Mol Biol 325:979−989、参照によりその全体が本明細書中に包含される)。 One important feature of the Fc region is the conserved N-linked glycosylation that occurs at N297 shown in FIG. As well described, this carbohydrate or oligosaccharide plays an important structural and functional role for antibodies, and is one of the fundamental reasons why antibodies must be produced using mammalian expression systems. Without wishing to be limited to one theory, the structural purpose of this carbohydrate is to stabilize or solubilize Fc, to determine a specific angle or flexibility level between the Cγ3 and Cγ2 domains It is believed that the two Cγ2 domains may not aggregate together across the central axis, or a combination thereof. Efficient Fc binding to FcγR and C1q requires this modification, and changes in the composition of N297 carbohydrates or their removal affects binding to these proteins (Umana et al., 1999, Nat Biotechnol 17: 176-180; Davies et al., 2001, Biotechnol Bioeng 74: 288-294; Mimura et al., 2001, J Biol Chem 276: 45539-45547 .; Radaev et al., 2001, J Biol Chem 276: 16478- 16483; Shields et al., 2001, J Biol Chem 276: 6591-6604; Shields et al., 2002, J Biol Chem 277: 26733-26740; Simmons et al., 2002, J Immunol Methods 263: 133-147, All of which are incorporated herein by reference in their entirety). The carbohydrate does not make any specific binding with FcγR (Radaev et al., 2001, J Biol Chem 276: 16469-16477, which is hereby incorporated by reference in its entirety), but with Fc / FcγR binding It is shown that the functional role of the N297 carbohydrate that mediates can play a structural role in determining Fc conformation. This is supported by the collection of crystal structures of four different Fc glycoforms, which shows that the composition of the oligosaccharide affects the Cγ2 conformation resulting in Fc / FcγR binding (Krapp et al., 2003, J Mol Biol 325: 979-989, which is incorporated herein by reference in its entirety).
上記の抗体の特徴−標的に対する特異性、免疫エフェクター機構を仲介する能力、および血清中の長い半減期−は、抗体を強力な治療薬にする。モノクローナル抗体は、癌、炎症性疾患および心疾患を含む様々な状態の処置のために治療的に用いられる。現在、10種以上の市販されている抗体製品および数百種の開発中の抗体製品が存在する。抗体に加えて、研究および治療に拡大する役割を見出されている抗体様タンパク質が、Fc融合体である(Chamow et al., 1996, Trends Biotechnol 14:52−60; Ashkenazi et al., 1997, Curr Opin Immunol 9:195−200、両方とも参照によりその全体が本明細書中に包含される)。Fc融合体は、1個以上のポリペプチドが、Fcに作動可能に連結するタンパク質である。Fc融合体は、受容体、リガンドまたはいくつかの他のタンパク質もしくはタンパク質ドメインの標的結合領域と抗体のFc領域を結合し、それにより、その好ましいエフェクター機能および薬物動態組み合わせる。後者の役割は、標的認識を仲介することであり、故に、それは抗体の可変領域に機能的に類似している。Fc融合体と抗体の構造的および機能的重複により、本発明の抗体に関する説明はFc融合体にも拡大される。 The characteristics of the antibodies described above—specificity for the target, ability to mediate immune effector mechanisms, and long half-life in serum—makes the antibody a powerful therapeutic agent. Monoclonal antibodies are used therapeutically for the treatment of various conditions including cancer, inflammatory diseases and heart diseases. Currently, there are more than 10 commercially available antibody products and hundreds of antibody products under development. In addition to antibodies, antibody-like proteins that have found an expanding role in research and therapy are Fc fusions (Chamow et al., 1996, Trends Biotechnol 14: 52-60; Ashkenazi et al., 1997 Curr Opin Immunol 9: 195-200, both of which are incorporated herein by reference in their entirety). An Fc fusion is a protein in which one or more polypeptides are operably linked to an Fc. An Fc fusion binds the target binding region of a receptor, ligand or some other protein or protein domain to the Fc region of an antibody, thereby combining its preferred effector function and pharmacokinetics. The latter role is to mediate target recognition, and therefore it is functionally similar to the variable region of an antibody. Due to the structural and functional overlap of Fc fusions and antibodies, the description of the antibodies of the invention extends to Fc fusions.
抗体は、腫瘍学における幅広い適用、特に細胞破壊を目的として、腫瘍細胞で選択的に発現される細胞抗原を標的化するための適用が見出されている。必要な増殖経路の阻止による抗増殖作用、アポトーシス、増強した下方制御および/または受容体のターンオーバーをもたらす細胞内シグナル伝達、CDC、ADCC、ADCP、および適応的免疫応答の促進を含む、抗体が腫瘍細胞を破壊する多くの可能性のある機構が存在する(Cragg et al., 1999, Curr Opin Immunol 11:541−547; Glennie et al., 2000, Immunol Today 21:403−410、両方とも参照によりその全体が本明細書中に包含される)。抗腫瘍効果は、これらの機構の組み合わせの結果であり、臨床治療におけるそれらの相対的重要性は、癌依存性であるように見える。これらの抗腫瘍手段を具備しているにもかかわらず、抗癌剤としての抗体の有効性は満足のいくものではなく、特にそれらは高コストである。患者の腫瘍応答データは、モノクローナル抗体が、通常の単剤の細胞傷害性化学療法剤よりも治療の成功にほんのわずかな改善しか提供しないことを示す。例えば、全ての再発した軽度の非ホジキンリンパ腫の患者の半数しか、抗CD20抗体であるリツキシマブに応答しない(McLaughlin et al., 1998, J Clin Oncol 16:2825−2833、参照によりその全体が本明細書中に包含される)。166名の臨床患者のうち、約12ヶ月の反応期間中央値で、6%が完全な応答を示し、42%が部分的な応答を示した。転移性乳癌の処置用の抗HER2/neu抗体であるトラスツズマブ(ハーセプチン(登録商標)、Genentech)は、効果がより少ない。222名の試験患者に関するトラスツズマブを用いる全体の反応率は、8名の完全な応答、および26名の部分的な応答を含む、わずか15%であって、9ないし13ヶ月の反応期間中央値および生存期間であった(Cobleigh et al., 1999, J Clin Oncol 17:2639−2648、参照によりその全体が本明細書中に包含される)。現在の抗癌治療においては、死亡率におけるどんな小さな改善も成功を定義する。故に、標的癌細胞を破壊するために抗体の能力を高めることがかなり必要とされる。 Antibodies have found wide application in oncology, particularly for targeting cellular antigens that are selectively expressed in tumor cells for the purpose of cell destruction. Antibodies comprising anti-proliferative effects by blocking the required proliferation pathways, apoptosis, enhanced down-regulation and / or intracellular signaling resulting in receptor turnover, CDC, ADCC, ADCP, and promotion of adaptive immune responses There are many possible mechanisms to destroy tumor cells (Cragg et al., 1999, Curr Opin Immunol 11: 541-547; Glennie et al., 2000, Immunol Today 21: 403-410, both see Are incorporated herein in their entirety). Antitumor effects are the result of a combination of these mechanisms, and their relative importance in clinical therapy appears to be cancer dependent. Despite having these anti-tumor means, the effectiveness of antibodies as anti-cancer agents is not satisfactory, especially they are expensive. Patient tumor response data indicates that monoclonal antibodies provide only a slight improvement in treatment success over conventional single agent cytotoxic chemotherapeutic agents. For example, only half of all recurrent mild non-Hodgkin lymphoma patients respond to the anti-CD20 antibody rituximab (McLaughlin et al., 1998, J Clin Oncol 16: 2825-2833, hereby incorporated by reference in its entirety. Included in the book). Of the 166 clinical patients, with a median response time of approximately 12 months, 6% showed a complete response and 42% showed a partial response. Trastuzumab (Herceptin®, Genentech), an anti-HER2 / neu antibody for the treatment of metastatic breast cancer, is less effective. The overall response rate with trastuzumab for 222 study patients was only 15%, including 8 complete responses and 26 partial responses, with a median response duration of 9 to 13 months and It was survival time (Cobleigh et al., 1999, J Clin Oncol 17: 2639-2648, which is hereby incorporated in its entirety by reference). In current anticancer therapies, any minor improvement in mortality defines success. Therefore, there is a considerable need to increase the ability of antibodies to destroy target cancer cells.
抗体の抗腫瘍効果を高める有望な手段は、ADCC、ADCPおよびCDCのような細胞傷害性エフェクター機能を仲介するそれらの能力を増強することによる。抗体の抗癌活性に関するFcγRにより仲介されるエフェクター機能の重要性は、マウスで立証されており(Clynes et al., 1998, Proc Natl Acad Sci U S A 95:652−656; Clynes et al., 2000, Nat Med 6:443−446、両方とも参照によりその全体が本明細書中に包含される)、Fcと任意のFcγRの相互作用の親和性は、細胞ベースのアッセイにおいて標的とする細胞傷害性と相関関係を有する(Shields et al., 2001, J Biol Chem 276:6591−6604; Presta et al., 2002, Biochem Soc Trans 30:487−490; Shields et al., 2002, J Biol Chem 277:26733−26740、全て参照によりその全体が本明細書中に包含される)。さらに、相関関係は、ヒトにおける臨床効果と、FcγRIIIaのアロタイプの高親和性多型(V158)または低親和性多型(F158)との間で観察されている(Cartron et al., 2002, Blood 99:754−758、参照によりその全体が本明細書中に包含される)。これらのデータを合わせると、任意のFcγRに結合するのに最適化される抗体が、エフェクター機能をより多く仲介し、それにより患者の癌細胞をより効果的に破壊することが示唆される。受容体の活性化と阻害のバランスは重要な検討事項であり、最適なエフェクター機能は、活性化受容体、例えばFcγRI、FcγRIIa/c、およびFcγRIIIaに対して増大した親和性を有するが、阻害性受容体FcγRIIbに対して減少した親和性を有する抗体によって生じ得る。さらに、FcγRが、抗原提示細胞による抗原の取り込みおよびプロセシングを仲介し得るため、最適化FcγR親和性はまた、適応的免疫応答を誘導する抗体治療薬の能力を高め得る(Dhodapkar & Dhodapkar, 2005, Proc Natl Acad Sci USA, 102, 6243−6244、参照によりその全体が本明細書中に包含される)。抗体の抗癌治療に対する補体仲介性エフェクター機能の重要性は、あまり特徴付けられていない。CDCに対して最適化された抗体は、抗体の臨床適用における補体の役割を調査する方法を提供し、抗体の殺腫瘍能力を改善するための可能性のある機構を提供し得る。 A promising means to enhance the anti-tumor effects of antibodies is by enhancing their ability to mediate cytotoxic effector functions such as ADCC, ADCP and CDC. The importance of FcγR-mediated effector function for the anticancer activity of antibodies has been demonstrated in mice (Clynes et al., 1998, Proc Natl Acad Sci USA 95: 652-656; Clynes et al., 2000, Nat Med 6: 443-446, both of which are hereby incorporated by reference in their entirety), the affinity of the interaction between Fc and any FcγR is determined by the cytotoxicity targeted in the cell-based assay. Correlated (Shields et al., 2001, J Biol Chem 276: 6591-6604; Presta et al., 2002, Biochem Soc Trans 30: 487-490; Shields et al., 2002, J Biol Chem 277: 26733 -26740, all incorporated herein by reference in its entirety). Furthermore, a correlation has been observed between clinical effects in humans and FcγRIIIa allotype high affinity polymorphism (V158) or low affinity polymorphism (F158) (Cartron et al., 2002, Blood 99: 754-758, which is incorporated herein in its entirety by reference). Taken together, these data suggest that an antibody that is optimized to bind to any FcγR mediates more effector function, thereby more effectively destroying the patient's cancer cells. The balance between receptor activation and inhibition is an important consideration, and optimal effector function has increased affinity for activating receptors such as FcγRI, FcγRIIa / c, and FcγRIIIa, but is inhibitory It can be generated by antibodies with reduced affinity for the receptor FcγRIIb. Furthermore, because FcγR can mediate antigen uptake and processing by antigen presenting cells, optimized FcγR affinity can also enhance the ability of antibody therapeutics to induce an adaptive immune response (Dhodapkar & Dhodapkar, 2005, Proc Natl Acad Sci USA, 102, 6243-6244, which is hereby incorporated by reference in its entirety). The importance of complement-mediated effector function for anti-cancer therapy of antibodies has not been well characterized. Antibodies optimized against CDC provide a way to investigate the role of complement in the clinical application of antibodies and may provide a potential mechanism for improving the tumoricidal ability of antibodies.
エフェクター機能が臨床効果に貢献する抗体治療および適用とは対照的に、いくつかの抗体および臨床適用に関して、1種以上のFcγRとの結合を減少するもしくは除去すること、または限定されないがADCC、ADCPおよび/またはCDCを含む、1種以上のFcγRまたは補体仲介性エフェクター機能を減少するもしくは除去することが、好適であり得る。このことはしばしば、その作用機序が、標的抗原を保持する細胞を殺すのではなく、阻止または抑制することを含む、治療抗体の場合に当てはまる。これらの場合において、標的細胞の減少は望ましくなく、副作用であると考えられ得る。例えば、T細胞上のCD4受容体を阻害する抗CD4抗体の能力は、それらを効果的な抗炎症薬にし、さらに、FcγR受容体を捕捉するそれらの能力はまた、標的細胞に対する免疫的攻撃を誘導し、結果としてT細胞の減少をもたらす(Reddy et al., 2000, J Immunol 164:1925−1933、参照によりその全体が本明細書中に包含される)。エフェクター機能はまた、放射性複合体と称される放射性標識抗体、および免疫毒素(immunotoxin)と称される毒素と複合体を形成した抗体にとって課題であり得る。これらの薬剤を、癌細胞を破壊するために用いることができるが、FcのFcγRとの相互作用による免疫細胞の捕捉は、健康な免疫細胞を有害なペイロード(放射線または毒素)の近接域にもたらし、結果として標的癌細胞と共に正常なリンパ系組織の減少をもたらす(Hutchins et al., 1995, Proc Natl Acad Sci U S A 92:11980−11984; White et al., 2001, Annu Rev Med 52:125−145、両方とも参照によりその全体が本明細書中に包含される)。補体またはエフェクター細胞の捕捉が不十分であるIgGイソ型、例えばIgG2およびIgG4は、この課題に取り組むために部分的に用いられ得る。Fcリガンド結合を減少または低下するFc変異体も当技術分野で公知である(Alegre et al., 1994, Transplantation 57:1537−1543; Hutchins et al., 1995, Proc Natl Acad Sci USA 92:11980−11984; Armour et al., 1999, Eur J Immunol 29:2613−2624; Reddy et al., 2000, J Immunol 164:1925−1933; Xu et al., 2000, Cell Immunol 200:16−26; Shields et al., 2001, J Biol Chem 276:6591−6604; Armour et al., 1999, Eur J Immunol 29:2613−2624; US6,194,551;US5,885,573;PCT WO99/58572;USSN10/267,286、全て参照によりその全体が本明細書中に包含される)。しかしながら、これらの変異体の完全なFcリガンド結合特性およびエフェクター機能の能力、およびWT IgGイソ型と比較したそれらの特性は明らかでない。全てのFcγR結合ならびにFcγRおよび補体仲介性エフェクター機能の完全な低下のための一般的かつ強固な手段が必要である。さらなる検討事項は、他の重要な抗体特性が不安定でないことである。Fc変異体は、FcγRおよび/またはC1qとの結合を低下するだけでなく、抗体の安定性、溶解性および構造的完全性、ならびにFcRnおよびプロテインAおよびプロテインGのような他の重要なFcリガンドと相互作用する能力を維持するように製造されるべきである。
In contrast to antibody therapies and applications where effector function contributes to clinical efficacy, for some antibodies and clinical applications, reducing or eliminating binding to one or more FcγRs, or without limitation, ADCC, ADCP It may be preferred to reduce or eliminate one or more FcγR or complement-mediated effector functions, including and / or CDC. This is often the case for therapeutic antibodies, whose mechanism of action involves blocking or suppressing rather than killing cells that carry the target antigen. In these cases, target cell reduction is undesirable and may be considered a side effect. For example, the ability of anti-CD4 antibodies to inhibit the CD4 receptor on T cells makes them effective anti-inflammatory drugs, and furthermore, their ability to capture FcγR receptors also prevents immune attack against target cells. Induces and results in T cell depletion (Reddy et al., 2000, J Immunol 164: 1925-1933, which is hereby incorporated by reference in its entirety). Effector function can also be a challenge for radiolabeled antibodies termed radioconjugates and antibodies complexed with toxins termed immunotoxins. Although these agents can be used to destroy cancer cells, the capture of immune cells by the interaction of Fc with FcγR brings healthy immune cells into close proximity to harmful payloads (radiation or toxins). Resulting in a reduction in normal lymphoid tissue with target cancer cells (Hutchins et al., 1995, Proc Natl Acad Sci USA 92: 11980-11984; White et al., 2001, Annu Rev Med 52: 125-145 , Both of which are incorporated herein by reference in their entirety). IgG isoforms that lack sufficient capture of complement or effector cells, such as IgG2 and IgG4, can be used in part to address this challenge. Fc variants that reduce or reduce Fc ligand binding are also known in the art (Alegre et al., 1994, Transplantation 57: 1537-1543; Hutchins et al., 1995, Proc Natl Acad Sci USA 92: 11980- 11984; Armor et al., 1999, Eur J Immunol 29: 2613-2624; Reddy et al., 2000, J Immunol 164: 1925-1933; Xu et al., 2000, Cell Immunol 200: 16-26; Shields et al., 2001, J Biol Chem 276: 6591-6604; Armor et al., 1999, Eur J Immunol 29: 2613-2624; US 6,194,551; US 5,885,573; PCT WO 99/58572;
最近の成功は、FcγRおよびC1qとの変化した結合を有するFc変異体を得ることを成し遂げ、いくつかの場合において、これらのFc変異体は、FcγRおよび補体仲介性エフェクター機能を仲介する能力について試験されている(2005年5月5日出願の、USSN10/672,280、USSN10/822,231、USSN11/124,620、および2005年10月21日出願のUSSN11/256,060、全て参照によりその全体が本明細書中に包含される)。これらの実験において得られたFc変異体は、FcγRとの選択的に改善した結合、増大したADCC、補体タンパク質C1qとの改善した結合、FcγRとの減少した結合、補体タンパク質C1qとの減少した結合、および他の最適化特性を含むFcリガンドおよびエフェクター機能特性の様々な最適な増強を、それらに限定されないが、提供する。本発明は、これらの実験から選択したFc変異体の特性をさらに特徴付けること、および最適化特性を有する新規の変異体を製造するためにそのデータを利用することを目的とする。
Recent successes have achieved obtaining Fc variants with altered binding to FcγR and C1q, and in some cases, these Fc variants have the ability to mediate FcγR and complement-mediated effector functions.
発明の概要
本発明は、最適化特性を有するFc変異体を提供する。該最適化特性には、親Fcポリペプチドと比較して、FcγRとの変化した結合、変化した抗体依存性細胞介在性細胞傷害作用、および変化した補体依存性細胞傷害作用が含まれる。
Summary of the Invention The present invention provides Fc variants with optimized properties. The optimized properties include altered binding to FcγR, altered antibody-dependent cell-mediated cytotoxicity, and altered complement-dependent cytotoxicity compared to the parent Fc polypeptide.
1つの態様において、本発明のFc変異体は、親Fcポリペプチドと比較して、1種以上のFcγRとの結合を改善する。別の態様において、本発明のFc変異体は、親Fcポリペプチドと比較して、抗体依存性細胞介在性細胞傷害作用を改善する。好ましい態様において、該Fc変異体は、227位、234位、235位、236位、239位、246位、255位、258位、260位、264位、267位、268位、272位、281位、282位、283位、284位、293位、295位、304位、324位、327位、328位、330位、332位および335位(ここで、番号は、EU Indexに従う。)からなる群から選択される1箇所以上でのアミノ酸修飾を含む。
In one embodiment, the Fc variants of the present invention improve binding to one or more FcγRs compared to the parent Fc polypeptide. In another embodiment, the Fc variants of the present invention improve antibody-dependent cell-mediated cytotoxicity compared to the parent Fc polypeptide. In a preferred embodiment, the Fc variant comprises
別の態様において、本発明のFc変異体は、親Fcポリペプチドと比較して補体依存性細胞傷害作用を改善する。好ましい態様において、該Fc変異体は、233位、234位、235位、239位、267位、268位、271位、272位、274位、276位、278位、281位、282位、284位、285位、293位、300位、320位、322位、324位、326位、327位、328位、330位、331位、332位、333位、334位および335位(ここで、番号は、EU Indexに従う。)からなる群から選択される1箇所以上でのアミノ酸修飾を含む。
In another embodiment, the Fc variants of the present invention improve complement dependent cytotoxicity compared to the parent Fc polypeptide. In a preferred embodiment, the Fc variant has
別の態様において、本発明のFc変異体は、親Fcポリペプチドと比較して1種以上のFcγRとの結合を減少する。別の態様において、本発明のFc変異体は、親Fcポリペプチドと比較して抗体依存性細胞介在性細胞傷害作用を減少する。別の態様において、本発明のFc変異体は、親Fcポリペプチドと比較して補体依存性細胞傷害作用を減少する。好ましい態様において、本発明のFc変異体は、親Fcポリペプチドと比較して、1種以上のFcγRとの結合を減少し、抗体依存性細胞介在性細胞傷害作用を減少し、補体依存性細胞傷害作用を減少する。最も好ましい態様において、該Fc変異体は、232位、234位、235位、236位、237位、238位、239位、265位、267位、269位、270位、297位、299位、325位、327位、328位、329位、330位および331位(ここで、番号は、EU Indexに従う。)からなる群から選択される位置での1個以上のアミノ酸修飾を含む。
In another embodiment, the Fc variants of the present invention reduce binding to one or more FcγRs as compared to a parent Fc polypeptide. In another embodiment, the Fc variants of the present invention reduce antibody-dependent cell-mediated cytotoxicity compared to the parent Fc polypeptide. In another embodiment, the Fc variants of the present invention reduce complement dependent cytotoxicity as compared to a parent Fc polypeptide. In a preferred embodiment, the Fc variants of the present invention reduce binding to one or more FcγRs, reduce antibody-dependent cell-mediated cytotoxicity and complement-dependent, compared to the parent Fc polypeptide. Reduces cytotoxic effects. In a most preferred embodiment, the Fc variant has
本発明は、最適化特性を有するFc変異体の製造方法を提供する。本発明のさらなる目的は、最適化したFc変異体を得るための実験的製造方法およびスクリーニング方法を提供することである。 The present invention provides a method for producing Fc variants having optimized properties. A further object of the present invention is to provide experimental production and screening methods to obtain optimized Fc variants.
本発明は、本明細書に記載のFc変異体をコードする単離した核酸を提供する。本発明は、所望により制御配列と作動可能に連結した該核酸を含むベクターを提供する。本発明は、該ベクターを含む宿主細胞、およびFc変異体の製造方法および所望によりFc変異体の回収方法を提供する。 The present invention provides isolated nucleic acids that encode the Fc variants described herein. The present invention provides a vector comprising the nucleic acid operably linked to a regulatory sequence as desired. The present invention provides a host cell containing the vector, and a method for producing an Fc variant and optionally a method for recovering the Fc variant.
本発明は、本明細書に記載のFc変異体を含む、抗体、Fc融合体、単離したFc、およびFc断片を含む新規のFcポリペプチドを提供する。該新規のFcポリペプチドは、治療用製品への使用を見出され得る。最も好ましい態様において、本発明のFcポリペプチドは抗体である。 The present invention provides novel Fc polypeptides comprising antibodies, Fc fusions, isolated Fc, and Fc fragments comprising the Fc variants described herein. The novel Fc polypeptides can find use in therapeutic products. In a most preferred embodiment, the Fc polypeptide of the present invention is an antibody.
本発明は、本明細書に記載のFc変異体を含むFcポリペプチド、および生理学的または薬学的に許容される担体または希釈剤を含む組成物を提供する。 The invention provides a composition comprising an Fc polypeptide comprising an Fc variant described herein and a physiologically or pharmaceutically acceptable carrier or diluent.
本発明は、本明細書に記載のFc変異体を含むFcポリペプチドの治療的および診断的使用を意図する。 The present invention contemplates therapeutic and diagnostic uses for Fc polypeptides comprising the Fc variants described herein.
図面の簡単な説明
図1。抗体の構造および機能。pdb受託コード1CE1からのヒト化Fab構造(James et al., 1999, J Mol Biol 289:293−301、参照によりその全体が本明細書中に包含される)およびpdb受託コード1DN2からのヒトIgG1Fc構造(DeLano et al., 2000, Science 287:1279−1283、参照によりその全体が本明細書中に包含される)を用いてモデル化された、全長ヒトIgG1抗体のモデルを示す。FabおよびFc領域を連結するフレキシブルヒンジは示さず。IgG1は、2個の軽鎖および2個の重鎖からなるヘテロ二量体のホモ二量体である。軽鎖のVLおよびCL、ならびに重鎖のVH、Cガンマ1(Cγ1)、Cガンマ2(Cγ2)、およびCガンマ3(Cγ3)を含む、抗体を含むIgドメインを示す。Fc領域を示す。可変領域中の抗原結合部位、ならびにFc領域中のFcγR、FcRn、C1qおよびプロテインAおよびGのための結合部位を含む、関連タンパク質の結合部位を示す。
BRIEF DESCRIPTION OF THE DRAWINGS FIG. Antibody structure and function. Humanized Fab structure from pdb accession code 1CE1 (James et al., 1999, J Mol Biol 289: 293-301, incorporated herein by reference in its entirety) and human IgG1Fc from pdb
図2。Fc/FcγRIIIb複合体構造1IIS。Fcを灰色リボンで示し、FcγRIIIbを黒色リボンで示す。N297炭水化物を黒色棒で示す。 FIG. Fc / FcγRIIIb complex structure 1IIS. Fc is shown as a gray ribbon and FcγRIIIb is shown as a black ribbon. N297 carbohydrate is shown as a black bar.
図3a−3b。ヒトIgG免疫グロブリンIgG1、IgG2、IgG3およびIgG4のアミノ酸配列のアライメント。図3aは、CH1(Cγ1)の配列およびヒンジドメインを提供し、図3bは、CH2(Cγ2)およびCH3(Cγ3)ドメインの配列を提供する。位置は、IgG1配列のEU Indexに従って番号付けられ、IgG1と他の免疫グロブリンIgG2、IgG3およびIgG4との差異を、灰色で示す。多型が多数の位置に存在し(Kim et al., 2001, J. Mol. Evol. 54:1−9、参照によりその全体が本明細書中に包含される)、故に、示した配列と従来の配列とにわずかな差異が存在し得る。Fc領域の可能性のある開始点が示され、EUの226位または230位のどちらかとして本明細書に記載される。
3a-3b. Alignment of amino acid sequences of human IgG immunoglobulins IgG1, IgG2, IgG3 and IgG4. FIG. 3a provides the sequence and hinge domain of CH1 (Cγ1), and FIG. 3b provides the sequence of CH2 (Cγ2) and CH3 (Cγ3) domains. The positions are numbered according to the EU index of the IgG1 sequence and the differences between IgG1 and other immunoglobulins IgG2, IgG3 and IgG4 are shown in gray. Polymorphisms are present at multiple positions (Kim et al., 2001, J. Mol. Evol. 54: 1-9, which is hereby incorporated by reference in its entirety), and thus the sequence shown There may be slight differences from conventional sequences. Possible starting points for the Fc region are indicated and are described herein as either
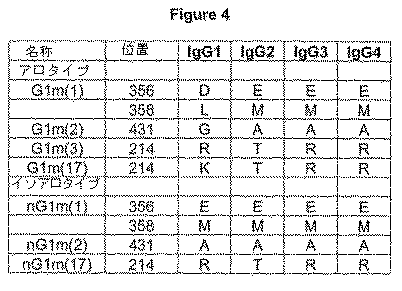
図4。ヒトIgG1のガンマ1鎖のアロタイプおよびイソアロタイプの位置および関連するアミノ酸置換を示す(Gorman & Clark, 1990, Semin Immunol 2(6):457−66、参照によりその全体が本明細書中に包含される)。比較のため、ヒトIgG2、IgG3およびIgG4ガンマ鎖における等価な位置に見出されるアミノ酸も示す。
FIG. The allotype and isoallotype positions of the
図5。Fc変異体およびFcγR結合データ。全てのFc変異体を、抗体PRO70769 IgG1に照らして構築した。倍数は、AlphaScreen競合アッセイにより測定される、ヒトV158およびF158 FcγRIIIaとの結合に関してWT PRO70769 IgG1と比較したIC50倍数を示す。 FIG. Fc variant and FcγR binding data. All Fc variants were constructed against the antibody PRO70769 IgG1. Fold indicates IC50 fold compared to WT PRO70769 IgG1 for binding to human V158 and F158 FcγRIIIa as measured by AlphaScreen competition assay.
図6。AlphaScreen競合アッセイにより決定される、選択したPRO70769 Fc変異体によるヒトV158 FcγRIIIa(図6a)およびF158 FcγRIIIa(図6b)との結合。競合抗体(Fc変異体またはWT)の存在において、特徴的阻害曲線が発光シグナルの減少として観察される。結合データを、低および高濃度の抗体それぞれにおけるベースラインにより供される、それぞれの特定の曲線についての最大および最小発光シグナルに対して標準化した。曲線は、非線形回帰を用いて、一部位競合モデルへのデータの適合を示す。 FIG. Binding of human V158 FcγRIIIa (FIG. 6a) and F158 FcγRIIIa (FIG. 6b) by selected PRO70769 Fc variants as determined by AlphaScreen competition assay. In the presence of a competing antibody (Fc variant or WT), a characteristic inhibition curve is observed as a decrease in luminescent signal. Binding data was normalized to the maximum and minimum luminescence signals for each particular curve provided by the baseline at low and high concentrations of antibody, respectively. The curve shows the fit of the data to a partial competition model using nonlinear regression.
図7。AlphaScreen競合アッセイにより測定される、PRO70769 Fc変異体によるヒトV158 FcγRIIIaおよびF158 FcγRIIIaとの結合。図7aは、選択した変異体についてのデータを示し、図7bは、WT PRO70769 IgG1と比較したIC50値および倍数を示す。 FIG. Binding of human V158 FcγRIIIa and F158 FcγRIIIa by PRO70769 Fc variants as measured by AlphaScreen competition assay. FIG. 7a shows data for selected mutants and FIG. 7b shows IC50 values and folds compared to WT PRO70769 IgG1.
図8。Fc変異体およびFcγR結合データ。全てのFc変異体を、可変領域PRO70769およびヒトIgG1またはIgG(1/2) ELLGGのどちらかに照らして構築した。図8aは、AlphaScreen競合アッセイにより測定される、ヒト活性化受容体V158およびF158 FcγRIIIa、および阻害性受容体FcγRIIbとの結合の、WT PRO70769 IgG1と比較したIC50値およびIC50倍数を示す。図8bは、選択した変異体のAlphaScreenデータを示す。 FIG. Fc variant and FcγR binding data. All Fc variants were constructed against the variable region PRO70769 and either human IgG1 or IgG (1/2) ELLGG. FIG. 8a shows IC50 values and IC50 fold compared to WT PRO70769 IgG1 for binding to human activated receptors V158 and F158 FcγRIIIa, and inhibitory receptor FcγRIIb as measured by AlphaScreen competition assay. FIG. 8b shows AlphaScreen data for selected mutants.
図9。ヒトV158 FcγRIIIaに対するトラスツズマブにおける、I332EおよびS239D/I332E変異体の結合親和性を測定する競合表面プラズモン共鳴(SPR)実験。図9aは、センサーグラム生データ(sensorgram raw data)を示し、図9bは、各濃度で得られた初期結合率に対する受容体濃度のログ値(対数値)のプロットを示し、そして図9cは、実施例1に記載の、これらのデータへの適合から得られた親和性を示す。 FIG. Competition surface plasmon resonance (SPR) experiment measuring the binding affinity of I332E and S239D / I332E mutants in trastuzumab against human V158 FcγRIIIa. FIG. 9a shows sensorgram raw data, FIG. 9b shows a plot of the log value (logarithmic value) of the receptor concentration against the initial binding rate obtained at each concentration, and FIG. The affinities obtained from the fit to these data as described in Example 1 are shown.
図10。抗CD20抗体 PRO70769における、選択したFc変異体の細胞ベースのADCCアッセイ。ADCCを、LDH細胞傷害性検出キット(Roche Diagnostic)を用いて、ラクトースデヒドロゲナーゼの放出により測定した。CD20+リンパ腫WIL2−S細胞を標的細胞として用い、ヒトPBMCをエフェクター細胞として用いた。低濃度および高濃度の抗体それぞれにおけるベースラインにより供される、それぞれの特定の曲線についての最小および最大蛍光シグナルに対して標準化した、所定の抗体の抗体濃度におけるADCCの用量依存性を示す。曲線は、非線形回帰を用いて、シグモイド型用量応答モデルへのデータの適合を示す。 FIG. Cell-based ADCC assay of selected Fc variants in anti-CD20 antibody PRO70769. ADCC was measured by the release of lactose dehydrogenase using the LDH cytotoxicity detection kit (Roche Diagnostic). CD20 + lymphoma WIL2-S cells were used as target cells and human PBMC was used as effector cells. FIG. 5 shows the dose dependence of ADCC at the antibody concentration of a given antibody, normalized to the minimum and maximum fluorescence signals for each particular curve provided by the baseline at low and high concentrations of antibody, respectively. The curve shows the fit of the data to a sigmoidal dose response model using non-linear regression.
図11。血清レベルのヒトIgGの不存在および存在下におけるPRO70769 IgG1における、選択したFc変異体の細胞ベースのADCCアッセイ。ADCCを、LDH細胞傷害性検出キット(Roche Diagnostic)を用いて、ラクトースデヒドロゲナーゼの放出により測定した。CD20+リンパ腫WIL2−S細胞を標的細胞として用い、ヒトPBMCをエフェクター細胞として用いた。 FIG. Cell-based ADCC assay of selected Fc variants in PRO70769 IgG1 in the absence and presence of serum levels of human IgG. ADCC was measured by the release of lactose dehydrogenase using the LDH cytotoxicity detection kit (Roche Diagnostic). CD20 + lymphoma WIL2-S cells were used as target cells and human PBMC was used as effector cells.
図12。CDCを増強するように設計されたFc変異体において変異した残基。ヒトIgG1Fc領域の構造(pdb受託コード1E4K、Sondermann et al., 2000, Nature 406:267−273、参照によりその全体が本明細書中に包含される)を示す。黒色の球および棒は、補体タンパク質C1qとの結合を仲介するのに重要であることが示されている残基D270、K322、P329およびP331を示し、灰色の棒は、CDCに影響を与える変異体を検討するために本発明において変異させた残基を示す。 FIG. Residues mutated in Fc variants designed to enhance CDC. 1 shows the structure of a human IgG1 Fc region (pdb accession code 1E4K, Sondermann et al., 2000, Nature 406: 267-273, which is hereby incorporated by reference in its entirety). Black spheres and bars indicate residues D270, K322, P329 and P331 which have been shown to be important in mediating binding to complement protein C1q, gray bars affect CDC The residues mutated in the present invention in order to examine the mutants are shown.
図13。補体仲介性細胞傷害作用(CDC)についてスクリーニングしたFc変異体およびCDCデータ。可変領域は、抗CD20抗体PRO70769のものであり、重鎖定常領域は、IgG1であり、特に他に記載のない限りIgG(1/2)ELLGGである。CDC倍数は、WT PRO70769 IgG1と比較した相対的CDC活性を示す。 FIG. Fc variants and CDC data screened for complement-mediated cytotoxicity (CDC). The variable region is that of the anti-CD20 antibody PRO70769, the heavy chain constant region is IgG1, and unless otherwise stated, is IgG (1/2) ELLGG. CDC fold indicates relative CDC activity compared to WT PRO70769 IgG1.
図14。Fc変異体 抗CD20抗体のCDCアッセイ。補体により仲介される溶解の抗体濃度の用量依存性を、CD20+WIL2−Sリンパ腫標的細胞に対する示したPRO70769抗体について示す。溶解を、アラマーブルー(Alamar Blue)の放出を用いて測定し、データを、低濃度および高濃度の抗体それぞれにおいてベースラインにより供される、それぞれの特定の曲線の最小および最大蛍光シグナルに対して標準化した。曲線は、非線形回帰を用いて、勾配変化のあるシグモイド型用量応答モデルへのデータの適合を示す。 FIG. Fc variant CDC assay of anti-CD20 antibody. The dose dependence of antibody concentration of complement-mediated lysis is shown for the indicated PRO70769 antibody against CD20 + WIL2-S lymphoma target cells. Lysis was measured using the release of Alamar Blue, and the data is relative to the minimum and maximum fluorescence signals for each specific curve provided by the baseline at low and high concentrations of antibody, respectively. And standardized. The curve shows the fit of the data to a sigmoidal dose response model with a slope change using non-linear regression.
図15。増大および減少したCDCを供するアミノ酸修飾、および増大/調節したCDCを供し得るように修飾され得る位置。位置は、EU indexに従い番号付けされる。 FIG. Amino acid modifications that provide increased and decreased CDC, and positions that can be modified to provide increased / regulated CDC. The positions are numbered according to the EU index.
図16。減少したFcγR親和性、FcγRにより仲介されるエフェクター機能、および補体により仲介されるエフェクター機能についてスクリーニングしたFc変異体。可変領域は、抗CD20抗体 PRO70769のものであり、重鎖定常領域はIgG1である。図は、ヒトV158 FcγRIIIaと結合するためのIC50倍数、およびWT PRO70769 IgG1と比較したCDC活性のEC50倍数を示す。 FIG. Fc variants screened for reduced FcγR affinity, effector function mediated by FcγR, and effector function mediated by complement. The variable region is that of the anti-CD20 antibody PRO70769, and the heavy chain constant region is IgG1. The figure shows the IC50 fold for binding to human V158 FcγRIIIa and the EC50 fold for CDC activity compared to WT PRO70769 IgG1.
図17。AlphaScreen競合アッセイにより決定される、PRO70769 Fc変異体の選択によるヒトV158 FcγRIIIaへの結合。 FIG. Binding to human V158 FcγRIIIa by selection of PRO70769 Fc variants as determined by AlphaScreen competition assay.
図18。CD20+WIL2−Sリンパ腫標的細胞に対する選択した抗CD20抗体 Fc変異体のCDCアッセイ。溶解をアラマーブルー放出により測定した。 FIG. CDC assay of selected anti-CD20 antibody Fc variants against CD20 + WIL2-S lymphoma target cells. Dissolution was measured by Alamar Blue release.
図19。CD20+リンパ腫WIL2−S細胞に対する選択した抗CD20抗体 Fc変異体の細胞ベースのADCC活性。ヒトPBMCをエフェクター細胞として用い、溶解をLDH放出により測定した。 FIG. Cell-based ADCC activity of selected anti-CD20 antibody Fc variants against CD20 + lymphoma WIL2-S cells. Human PBMC were used as effector cells and lysis was measured by LDH release.
図20。減少したFcγR親和性、FcγRにより仲介されるエフェクター機能、および補体仲介性エフェクター機能についてスクリーニングしたFc変異体。可変領域は、抗CD20抗体 PRO70769のものであり、重鎖定常領域はIgG1である。図は、2つの別個の試験による、WTと比較したヒトV158 FcγRIIIaとの結合についてのIC50倍数、WTと比較したヒトFcγRIとの結合についてのIC50倍数、およびWTと比較したCDC活性についてのEC50倍数を示す。 FIG. Fc variants screened for reduced FcγR affinity, FcγR-mediated effector function, and complement-mediated effector function. The variable region is that of the anti-CD20 antibody PRO70769, and the heavy chain constant region is IgG1. The figure shows the IC50 fold for binding to human V158 FcγRIIIa compared to WT, the IC50 fold for binding to human FcγRI compared to WT, and the EC50 fold for CDC activity compared to WT by two separate tests. Indicates.
図21。AlphaScreen競合アッセイにより決定される、選択したPRO70769Fc変異体による低親和性ヒト活性化受容体V158 FcγRIIIaおよび高親和性ヒト活性化受容体FcγRIとの結合。 FIG. Binding of the low affinity human activated receptor V158 FcγRIIIa and the high affinity human activated receptor FcγRI by selected PRO70769 Fc variants as determined by AlphaScreen competition assay.
図22。CD20+WIL2−Sリンパ腫標的細胞に対する選択したPRO70769Fc変異体のCDC活性。溶解をアラマーブルーの放出により測定した。 FIG. CDC activity of selected PRO70769Fc variants against CD20 + WIL2-S lymphoma target cells. Dissolution was measured by the release of alamar blue.
図23。Her2/neu+SkBr−3乳癌標的細胞に対する抗Her2 Fc変異体およびWT IgG抗体の細胞ベースのADCC活性。ヒトPBMCをエフェクター細胞として用い、溶解をLDH放出により測定した。 FIG. Cell-based ADCC activity of anti-Her2 Fc variants and WT IgG antibodies against Her2 / neu + SkBr-3 breast cancer target cells. Human PBMC were used as effector cells and lysis was measured by LDH release.
図24。PRO70769(図24aおよび24b)、トラスツズマブ(図24cおよび24d)、およびイピリムマブ(図24eおよび24f)を含む、本発明で用いた可変軽鎖(VL)および可変重鎖(VH)のアミノ酸配列。 FIG. Amino acid sequences of variable light chain (VL) and variable heavy chain (VH) used in the present invention, including PRO70769 (Figures 24a and 24b), trastuzumab (Figures 24c and 24d), and ipilimumab (Figures 24e and 24f).
図25。本発明で用いたヒト定常軽鎖カッパ(図25a)および定常重鎖(図25b−25f)のアミノ酸配列。 FIG. Amino acid sequences of human constant light chain kappa (FIG. 25a) and constant heavy chain (FIGS. 25b-25f) used in the present invention.
図26。減少したFcリガンド結合およびエフェクター機能特性を有する可能性のある定常重鎖配列(図26a)、および改良した抗CTLA−4抗体の配列(図26b−26d)を示す配列。図26aは、X1、X2、X3、X4、X5、X6、X7およびX8として強調して示す可変位置を含む、可能性のあるFc変異体定常重鎖配列を示す。配列の下の表は、WTアミノ酸およびこれらの位置において可能性のある置換基を示す。改良した抗体配列は、この可能性のある修飾基から選択される1個以上の非WTアミノ酸を含み得る。図26bは、抗CTLA−4抗体の軽鎖配列を示し、図26cおよび26dは、減少したFcリガンド結合およびFcにより仲介されるエフェクター機能を有する抗CTLA−4抗体の重鎖配列を示す。これらには、L235G/G236R IgG1重鎖(図26c)およびIgG2重鎖(図26d)が含まれる。位置は、Kabatに記載のEU indexに従って番号付けられ、故に、配列中の連続順に対応していない。 FIG. A sequence showing a constant heavy chain sequence that may have reduced Fc ligand binding and effector function properties (FIG. 26a) and an improved anti-CTLA-4 antibody sequence (FIGS. 26b-26d). FIG. 26a shows a possible Fc variant constant heavy chain sequence with variable positions shown highlighted as X1, X2, X3, X4, X5, X6, X7 and X8. The table below the sequence shows WT amino acids and possible substituents at these positions. Improved antibody sequences can include one or more non-WT amino acids selected from this potential modifying group. FIG. 26b shows the anti-CTLA-4 antibody light chain sequence, and FIGS. 26c and 26d show the anti-CTLA-4 antibody heavy chain sequence with reduced Fc ligand binding and Fc-mediated effector function. These include the L235G / G236R IgG1 heavy chain (FIG. 26c) and the IgG2 heavy chain (FIG. 26d). The positions are numbered according to the EU index described in Kabat and therefore do not correspond to the sequential order in the sequence.
発明の詳しい説明
本発明は、理解をより完全にし得るために、いくつかの定義を以下に記載する。かかる定義は、文法的同等物を包含することを意味する。
Detailed Description of the Invention In order that the present invention may be more fully understood, some definitions are set forth below. Such a definition is meant to encompass grammatical equivalents.
本明細書で記載の“ADCC”または“抗体依存性細胞介在性細胞傷害作用”は、標的細胞上に結合した抗体を認識し、次いで標的細胞の溶解をもたらすFcγRを発現する非特異的細胞傷害性細胞である細胞により仲介される反応を意味する。 As described herein, “ ADCC ” or “ antibody-dependent cell-mediated cytotoxicity ” refers to non-specific cytotoxicity that recognizes an antibody bound on a target cell and then expresses FcγR resulting in lysis of the target cell. It means a reaction mediated by cells that are sex cells.
本明細書で記載の“ADCP”または“抗体依存性細胞介在性食作用”は、標的細胞上に結合した抗体を認識し、次いで標的細胞の食作用を誘導するFcγRを発現する非特異的細胞傷害性細胞である細胞により仲介される反応を意味する。 “ ADCP ” or “ antibody-dependent cell-mediated phagocytosis ” as described herein is a non-specific cell that expresses FcγR that recognizes the antibody bound on the target cell and then induces phagocytosis of the target cell. It means a reaction mediated by cells that are damaging cells.
本明細書中、“アミノ酸修飾”は、ポリペプチド配列中の、アミノ酸置換、挿入、および/または欠失を意味する。本明細書中、“アミノ酸置換”または“置換”は、親ポリペプチド配列中、特定の位置での、あるアミノ酸の別のアミノ酸との置換を意味する。例えば、L328R置換は、この場合のFc変異体において、328位のロイシンをアルギニンに置換される変異体ポリペプチドを意味する。本明細書で用いる“アミノ酸挿入”または“挿入”は、親ポリペプチド配列中、特定の位置でのアミノ酸の付加を意味する。例えば、G>235−236挿入は、235および236位の間へのグリシンの挿入を意味する。本明細書で用いる“アミノ酸欠失”または“欠失”は、親ポリペプチド配列中、特定の位置でのアミノ酸の除去を意味する。例えば、G236−は、236位でのグリシンの欠失を意味する。本発明のアミノ酸はさらに、同位体または新規のどちらかとして分類され得る。
As used herein, “ amino acid modification ” means an amino acid substitution, insertion, and / or deletion in a polypeptide sequence. As used herein, “ amino acid substitution ” or “ substitution ” means a substitution of one amino acid for another at a particular position in the parent polypeptide sequence. For example, the L328R substitution means a mutant polypeptide in which leucine at
本明細書で記載の“CDC”または“補体依存性細胞傷害作用”は、1個以上の補体タンパク質成分が、標的細胞上に結合した抗体を認識し、次いで標的細胞の溶解をもたらす反応を意味する。 “ CDC ” or “ complement dependent cytotoxicity ”, as described herein, is a reaction in which one or more complement protein components recognize an antibody bound on a target cell and then result in lysis of the target cell. Means.
本明細書で記載の“同位体修飾”は、あるイソ型のあるアミノ酸を、対応する異なるアミノ酸(整列したイソ型)に変換するアミノ酸修飾を意味する。例えば、IgG1は、EU 296位にチロシンを有し、IgG2は、フェニルアラニンを有するため、IgG2におけるF296Y置換は、同位体修飾と見なされる。 As used herein, “ isotopic modification ” refers to an amino acid modification that converts one amino acid of one isoform to the corresponding different amino acid (aligned isoform). For example, IgG1 has a tyrosine at EU position 296 and IgG2 has phenylalanine, so F296Y substitution in IgG2 is considered an isotope modification.
本明細書で記載の“新規の修飾”は、イソ型ではないアミノ酸修飾を意味する。例えば、IgGは332位にグルタミン酸を有しないため、IgG1、IgG2、IgG3またはIgG4におけるI332E置換は、新規の修飾と見なされる。
As used herein, “ novel modifications ” refers to amino acid modifications that are not isoforms. For example, since IgG does not have a glutamic acid at
本明細書で記載の“アミノ酸”および“アミノ酸同一性”は、特定の定められた位置に存在し得る、20個の天然に存在するアミノ酸または何らかの天然に存在しない類似体のうち1つを意味する As used herein, “ amino acid ” and “ amino acid identity ” means one of the 20 naturally occurring amino acids or any non-naturally occurring analog that may be present in a particular defined position. Do
本明細書で記載の“エフェクター機能”は、抗体のFc領域と、Fc受容体またはリガンドとの相互作用によりもたらされる生化学的事象を意味する。エフェクター機能には、ADCCおよびADCPのようなFcγRにより仲介されるエフェクター機能、ならびにCDCのような補体仲介性エフェクター機能が含まれる。 As used herein, “ effector function ” refers to a biochemical event that results from the interaction of an Fc region of an antibody with an Fc receptor or ligand. Effector functions include effector functions mediated by FcγR such as ADCC and ADCP, and complement-mediated effector functions such as CDC.
本明細書で記載の“エフェクター細胞”は、1種以上のFc受容体を発現し、1個以上のエフェクター機能を仲介する免疫系の細胞を意味する。エフェクター細胞には、単球、マクロファージ、好中球、樹状細胞、好酸球、マスト細胞、血小板、B細胞、大型顆粒リンパ球、ランゲルハンス細胞、ナチュラルキラー(NK)細胞、およびγδT細胞が含まれるが、それらに限定されず、ヒト、マウス、ラット、ウサギおよびサルを含む何れかの生物を含むが、それらに限定されない生物由来であり得る。 As used herein, “ effector cells ” refers to cells of the immune system that express one or more Fc receptors and mediate one or more effector functions. Effector cells include monocytes, macrophages, neutrophils, dendritic cells, eosinophils, mast cells, platelets, B cells, large granular lymphocytes, Langerhans cells, natural killer (NK) cells, and γδT cells But can be from any organism including but not limited to humans, mice, rats, rabbits and monkeys.
本明細書で記載の“Fab”または“Fab領域”は、VH、CH1、VLおよびCL免疫グロブリンドメインを含むポリペプチドを意味する。Fabは、単独のこの領域、または全長抗体もしくは抗体断片中のこの領域を意味し得る。 "Fab" or "Fab region" as used herein refers to a polypeptide comprising a V H, CH1, V L and C L immunoglobulin domains. Fab can refer to this region alone or in a full-length antibody or antibody fragment.
本明細書で記載の“Fc”または“Fc領域”は、免疫グロブリンドメインの第一の定常領域を除く、抗体の定常領域を含むポリペプチドを意味する。故に、Fcは、IgA、IgD、およびIgGの免疫グロブリンドメインの残り2個の定常領域、ならびにIgEおよびIgMの免疫グロブリンドメインの残り3個の定常領域、ならびにこれらのドメインのN末端のフレキシブルヒンジを意味する。IgAおよびIgMに関して、Fcには、J鎖が含まれ得る。IgGに関して、図1に示す通り、Fcは、免疫グロブリンドメインCガンマ2およびCガンマ3(Cγ2およびCγ3)、ならびにCガンマ1(Cγ1)とCガンマ2(Cγ2)の間のヒンジを含む。Fc領域の境界は変化し得るが、ヒトIgG重鎖Fc領域は、通常、そのカルボキシル末端に残基C226またはP230を含むと定義され、ここで、番号は、Kabatに記載のEU indexに従う。Fcは、下記の通り、単離したこの領域か、またはFcポリペプチド中のこの領域を意味し得る。本明細書で記載の“Fcポリペプチド”は、Fc領域の全てまたは一部を含むポリペプチドを意味する。Fcポリペプチドは、抗体、Fc融合体、単離されたFc、およびFc断片を含む。 As used herein, “ Fc ” or “ Fc region ” refers to a polypeptide comprising the constant region of an antibody, excluding the first constant region of an immunoglobulin domain. Thus, Fc comprises the remaining two constant regions of the IgA, IgD, and IgG immunoglobulin domains, and the remaining three constant regions of the IgE and IgM immunoglobulin domains, as well as the N-terminal flexible hinge of these domains. means. For IgA and IgM, Fc can include the J chain. For IgG, as shown in FIG. 1, Fc includes immunoglobulin domains Cgamma2 and Cgamma3 (Cγ2 and Cγ3) and a hinge between Cgamma1 (Cγ1) and Cgamma2 (Cγ2). Although the boundaries of the Fc region can vary, a human IgG heavy chain Fc region is usually defined to include residues C226 or P230 at its carboxyl terminus, where the numbers follow the EU index described in Kabat. Fc may refer to this isolated region or this region in an Fc polypeptide as described below. As used herein, “Fc polypeptide” means a polypeptide comprising all or part of an Fc region. Fc polypeptides include antibodies, Fc fusions, isolated Fc, and Fc fragments.
本明細書で記載の“Fc融合体”は、1個以上のポリペプチドがFc領域に作動可能に連結されるタンパク質を意味する。本明細書中、Fc融合体は、従来技術(Chamow et al., 1996, Trends Biotechnol 14:52−60;Ashkenazi et al., 1997, Curr Opin Immunol 9:195−200、両方とも参照によりその全体が本明細書中に包含される)で用いられる通り、用語“免疫アドヘシン(immunoadhesin)”、“Ig融合体”、“Igキメラ”、および“受容体グロブリン”(ダッシュを付けることもある)と同義の意味である。Fc融合体は、一般的に、何れかのタンパク質、ポリペプチドまたは小分子であり得る“融合パートナー”を有する免疫グロブリンのFc領域を結合する。Fc融合体の非Fc部分、すなわち融合パートナーの役割は、標的結合を仲介することであり、故に、それは、抗体の可変領域と機能的に類似している。実際、何れかのタンパク質または小分子はFcと結合し、Fc融合体を作製し得る。タンパク質融合パートナーには、受容体の標的結合領域、接着分子、リガンド、酵素、サイトカイン、ケモカイン、または他のタンパク質もしくはタンパク質ドメインが含まれ得るが、それらに限定されない。小分子融合パートナーは、Fc融合体を治療標的に向ける何れかの治療剤を含み得る。かかる標的は、何れかの分子、好ましくは疾患に関与する細胞外受容体であり得る。 As used herein, an “ Fc fusion ” refers to a protein in which one or more polypeptides are operably linked to an Fc region. As used herein, Fc fusions are described in the prior art (Chamow et al., 1996, Trends Biotechnol 14: 52-60; Ashkenazi et al., 1997, Curr Opin Immunol 9: 195-200, both in their entirety by reference. As used herein) and the terms “immunoadhesin”, “Ig fusion”, “Ig chimera”, and “receptor globulin” (sometimes with dashes). It is synonymous. An Fc fusion generally binds an Fc region of an immunoglobulin with a “ fusion partner ” that can be any protein, polypeptide or small molecule. The role of the non-Fc portion of the Fc fusion, the fusion partner, is to mediate target binding, and thus it is functionally similar to the variable region of an antibody. In fact, any protein or small molecule can bind Fc and create an Fc fusion. Protein fusion partners can include, but are not limited to, a target binding region of a receptor, an adhesion molecule, a ligand, an enzyme, a cytokine, a chemokine, or other protein or protein domain. Small molecule fusion partners can include any therapeutic agent that directs the Fc fusion to a therapeutic target. Such a target can be any molecule, preferably an extracellular receptor involved in the disease.
本明細書で記載の“Fcガンマ受容体”または“FcγR”は、IgG抗体Fc領域に結合し、FcγR遺伝子により実質的にコードされる何れかのタンパク質ファミリーのメンバーを意味する。ヒトにおいて、このファミリーには、イソ型FcγRIa、FcγRIb、およびFcγRIcを含むFcγRI(CD64);イソ型FcγRIIa(アロタイプH131およびR131を含む)、FcγRIIb(FcγRIIb−1およびFcγRIIb−2を含む)、およびFcγRIIcを含むFcγRII(CD32);ならびに、イソ型FcγRIIIa(アロタイプV158およびF158を含む)およびFcγRIIIb(アロタイプFcγRIIIb−NA1およびFcγRIIIb−NA2を含む)を含むFcγRIII(CD16)(Jefferis et al., 2002, Immunol Lett 82:57−65、参照によりその全体が本明細書中に包含される)、ならびに何れかの未知のヒトFcγRまたはFcγRイソ型またはアロタイプが含まれるが、それらに限定されない。FcγRは、ヒト、マウス、ラット、ウサギ、およびサルを含むが、それらに限定されない何れかの生物由来であり得る。マウスFcγRには、FcγRI(CD64)、FcγRII(CD32)、FcγRIII(CD16)、およびFcγRIII−2(CD16−2)、ならびに何れかの未発見のマウスFcγRまたはFcγRイソ型もしくはアロタイプが含まれるが、それらに限定されない。 As used herein, “ Fc gamma receptor ” or “ FcγR ” refers to a member of any protein family that binds to the IgG antibody Fc region and is substantially encoded by the FcγR gene. In humans, this family includes FcγRI (CD64), including isoforms FcγRIa, FcγRIb, and FcγRIc; isoforms FcγRIIa (including allotypes H131 and R131), FcγRIIb (including FcγRIIb-1 and FcγRIIb-2), and FcγRIIc And FcγRIII (CD16), including isoforms FcγRIIIa (including allotypes V158 and F158) and FcγRIIIb (including allotypes FcγRIIIb-NA1 and FcγRIIIb-NA2) (Jefferis et al., 2002, Immunol Lett 82: 57-65, which is hereby incorporated by reference in its entirety), as well as any unknown human FcγR or FcγR isoform or allotype. Not. The FcγR can be from any organism, including but not limited to humans, mice, rats, rabbits, and monkeys. Mouse FcγR includes FcγRI (CD64), FcγRII (CD32), FcγRIII (CD16), and FcγRIII-2 (CD16-2), and any undiscovered mouse FcγR or FcγR isotype or allotype, It is not limited to them.
本明細書で記載の“Fcリガンド”は、抗体のFc領域と結合し、Fc/Fcリガンド複合体を形成する、何れかの生物由来の分子、好ましくはポリペプチドを意味する。Fcリガンドには、FcγR、FcγR、FcγR、FcRn、C1q、C3、マンナン結合レクチン、マンノース受容体、ブドウ球菌タンパク質A、ブドウ球菌タンパク質G、およびウイルスFcγRが含まれるが、それらに限定されない。Fcリガンドにはまた、FcγRと相同性のFc受容体ファミリーであるFc受容体相同体(FcRH)が含まれる(Davis et al., 2002, Immunological Reviews 190:123−136、参照によりその全体が本明細書中に包含される)。Fcリガンドは、Fcに結合する未知の分子を含み得る。 As used herein, “ Fc ligand ” refers to a molecule, preferably a polypeptide, from any organism that binds to the Fc region of an antibody to form an Fc / Fc ligand complex. Fc ligands include, but are not limited to, FcγR, FcγR, FcγR, FcRn, C1q, C3, mannan binding lectin, mannose receptor, staphylococcal protein A, staphylococcal protein G, and viral FcγR. Fc ligands also include the Fc receptor homologue (FcRH), a family of Fc receptors that are homologous to FcγR (Davis et al., 2002, Immunological Reviews 190: 123-136, which is hereby incorporated by reference in its entirety. Included in the specification). An Fc ligand may comprise an unknown molecule that binds to Fc.
本明細書で記載の“全長抗体”は、可変領域および定常領域を含む抗体の天然の生物学的形態を構成する構造を意味する。例えば、ヒトおよびマウスを含むほとんどの哺乳動物において、IgGイソ型の全長抗体は四量体であり、2個の免疫グロブリン鎖の2個の相同対であって、各対が、1個の軽鎖および1個の重鎖(各軽鎖は、免疫グロブリンドメインVLおよびCLを含む軽鎖を含み、各重鎖は、免疫グロブリンドメインVH、Cγ1、Cγ2およびCγ3を含む。)を有する相同対から構成される。ある哺乳動物、例えばラクダおよびラマにおいて、IgG抗体は、2個の重鎖(各重鎖は、Fc領域に結合した可変ドメインを含む。)のみから構成され得る。 As used herein, “ full-length antibody ” refers to the structure that constitutes the natural biological form of an antibody, including variable and constant regions. For example, in most mammals, including humans and mice, IgG isoform full-length antibodies are tetramers, two homologous pairs of two immunoglobulin chains, each pair having one light Chain and one heavy chain (each light chain comprises a light chain comprising immunoglobulin domains V L and C L , each heavy chain comprising immunoglobulin domains V H , Cγ1, Cγ2 and Cγ3). Consists of homologous pairs. In some mammals, such as camels and llamas, IgG antibodies can be composed of only two heavy chains, each heavy chain comprising a variable domain attached to an Fc region.
本明細書で記載の“IgG”は、認識される免疫グロブリンガンマ遺伝子により実質的にコードされる抗体のクラスに属するポリペプチドを意味する。ヒトにおいて、このIgGには、サブクラスまたはイソ型であるIgG1、IgG2、IgG3およびIgG4が含まれる。マウスにおいて、IgGには、IgG1、IgG2a、IgG2b、IgG3が含まれる。 As used herein, “ IgG ” refers to a polypeptide belonging to the class of antibodies substantially encoded by recognized immunoglobulin gamma genes. In humans, this IgG includes subclasses or isoforms IgG1, IgG2, IgG3 and IgG4. In mice, IgG includes IgG1, IgG2a, IgG2b, and IgG3.
本明細書中、“免疫グロブリン(Ig)“は、免疫グロブリン遺伝子により実質的にコードされる1個以上のポリペプチドからなるタンパク質を意味する。免疫グロブリンには、抗体が含まれるが、それに限定されない。免疫グロブリンは、全長抗体、抗体断片、および個々の免疫グロブリンドメインを含むが、これらに限定されない多くの構造形態を有し得る。 As used herein, “ immunoglobulin (Ig) ” means a protein consisting of one or more polypeptides substantially encoded by immunoglobulin genes. Immunoglobulins include but are not limited to antibodies. Immunoglobulins can have many structural forms, including but not limited to full length antibodies, antibody fragments, and individual immunoglobulin domains.
本明細書で記載の“免疫グロブリン(Ig)ドメイン“は、タンパク質構造分野の当業者により確認される異なる構造要素として存在する免疫グロブリンの領域を意味する。Igドメインは典型的に、特徴的なβ−サンドイッチフォールディングトポロジーを有する。抗体のIgGイソ型における既知のIgドメインは、VH、Cγ1、Cγ2、Cγ3、VLおよびCLである。 As used herein, an “ immunoglobulin (Ig) domain ” refers to a region of an immunoglobulin that exists as a different structural element identified by one skilled in the art of protein structure. Ig domains typically have a characteristic β-sandwich folding topology. Known Ig domains in IgG isotype antibodies, V H, Cγ1, Cγ2, Cγ3, a V L and C L.
本明細書で記載の“IgG”または“IgG免疫グロブリン”は、認識される免疫グロブリンガンマ遺伝子により実質的にコードされる抗体クラスに属するポリペプチドを意味する。ヒトにおいて、このクラスには、サブクラスまたはイソ型IgG1、IgG2、IgG3およびIgG4が含まれる。本明細書で用いる“イソ型”は、それらの定常領域の化学特性および抗原特性により定義される免疫グロブリンのサブクラスのいずれかを意味する。既知のヒト免疫グロブリンイソ型は、IgG1、IgG2、IgG3、IgG4、IgA1、IgA2、IgM、IgDおよびIgEである。 As used herein, “ IgG ” or “ IgG immunoglobulin ” refers to a polypeptide belonging to the antibody class substantially encoded by a recognized immunoglobulin gamma gene. In humans, this class includes subclasses or isoforms IgG1, IgG2, IgG3 and IgG4. As used herein, “ isoform ” refers to any of the immunoglobulin subclasses defined by the chemical and antigenic properties of their constant regions. Known human immunoglobulin isoforms are IgG1, IgG2, IgG3, IgG4, IgA1, IgA2, IgM, IgD and IgE.
本明細書で記載の“親ポリペプチド”、“親タンパク質”、“前駆体ポリペプチド”または“前駆体タンパク質”は、後に修飾されて変異体を作製する未修飾ポリペプチドを意味する。該親ポリペプチドは、天然に存在するポリペプチド、または天然に存在するポリペプチドの変異体もしくは改変型であり得る。親ポリペプチドは、そのポリペプチド自体、該親ポリペプチドまたはそれをコードするアミノ酸配列を含む組成物を意味し得る。従って、本明細書で記載の“親Fcポリペプチド”は、修飾されて変異体を作製するFcポリペプチドを意味し、本明細書で記載の“親抗体”は、修飾されて変異体抗体を作製する抗体を意味する。 As used herein, “ parent polypeptide ”, “ parent protein ”, “ precursor polypeptide ” or “ precursor protein ” refers to an unmodified polypeptide that is subsequently modified to create a variant. The parent polypeptide can be a naturally occurring polypeptide, or a variant or modified form of a naturally occurring polypeptide. A parent polypeptide can refer to the polypeptide itself, the parent polypeptide or a composition comprising the amino acid sequence that encodes it. Thus, a “ parent Fc polypeptide ” as used herein refers to an Fc polypeptide that is modified to create a variant, and a “ parent antibody ” as described herein is referred to as a modified antibody. It means the antibody to be produced.
本明細書で記載の“位置”は、タンパク質配列中の位置を意味する。位置は、連続して、または確立された形式、例えばKabatに記載のEU indexに従い、番号付けされ得る。例えば、297位は、ヒト抗体IgG1中の位置である。 As used herein, “ position ” means a position in a protein sequence. The positions can be numbered sequentially or according to an established format, for example the EU index described in Kabat. For example, position 297 is a position in human antibody IgG1.
本明細書で記載の“ポリペプチド”または“タンパク質”は、少なくとも2個の共有結合したアミノ酸を意味し、タンパク質、ポリペプチド、オリゴペプチドおよびペプチドが含まれる。 As used herein, “ polypeptide ” or “ protein ” refers to at least two covalently linked amino acids and includes proteins, polypeptides, oligopeptides and peptides.
本明細書で記載の“残基”は、タンパク質中の位置およびその関係するアミノ酸の特定を意味する。例えば、アスパラギン297(Asn297、またN297とも称する)は、ヒト抗体IgG1中の残基である。 As used herein, “ residue ” refers to the identification of a position in a protein and its associated amino acid. For example, asparagine 297 (Asn297, also referred to as N297) is a residue in the human antibody IgG1.
本明細書で記載の“標的抗原”は、所定の抗体の可変領域により特異的に結合される分子を意味する。標的抗原は、タンパク質、炭水化物、脂質、または他の化合物であり得る。 As used herein, “ target antigen ” refers to a molecule that is specifically bound by the variable region of a given antibody. The target antigen can be a protein, carbohydrate, lipid, or other compound.
本明細書で記載の“標的細胞”は、標的抗原を発現する細胞を意味する。 As used herein, “ target cell ” means a cell that expresses a target antigen.
本明細書で記載の“可変領域”は、カッパ、ラムダ、および重鎖免疫グロブリン遺伝子領域それぞれからなるVκ、Vλ、および/またはVH遺伝子の何れかにより実質的にコードされる1個以上のIgドメインを含む免疫グロブリンの領域を意味する。 As used herein, a “ variable region ” refers to one or more of the Vκ, Vλ, and / or V H genes that are substantially encoded by kappa, lambda, and heavy chain immunoglobulin gene regions, respectively. It refers to the region of an immunoglobulin that contains an Ig domain.
本明細書で記載の“変異体ポリペプチド”、“ポリペプチド変異体”または“変異体”は、少なくとも1個のアミノ酸修飾により親ポリペプチド配列と異なるポリペプチド配列を意味する。親ポリペプチドは、天然に存在するかまたは野生型(WT)ポリペプチドであり得るか、またはWTポリペプチドの改変型であり得る。変異体ポリペプチドは、ポリペプチド自体、該ポリペプチドまたはそれをコードするアミノ配列を含む組成物を意味し得る。好ましくは、変異体ポリペプチドは、親ポリペプチドと比較して、少なくとも1個のアミノ酸修飾を有し、例えば、親ポリペプチドと比較して約1個ないし約10個のアミノ酸修飾、好ましくは約1個ないし約5個のアミノ酸修飾を有する。本明細書中、変異体ポリペプチド配列は、好ましくは、親ポリペプチド配列と少なくとも約80%の相同性、最も好ましくは少なくとも約90%の相同性、より好ましくは少なくとも約95%の相同性を有し得る。従って、本明細書で記載の“Fc変異体”または“変異体Fc”は、少なくとも1個のアミノ酸修飾により親Fc配列とは異なるFc配列を意味する。Fc変異体は、Fc領域のみを含み得るか、または抗体、Fc融合体、単離されたFc、Fc断片、もしくはFcにより実質的にコードされる他のポリペプチドとして存在し得る。Fc変異体は、Fcポリペプチド自体、該Fc変異体ポリペプチドまたはそれをコードするアミノ酸配列を含む組成物を意味し得る。本明細書で記載の“Fcポリペプチド変異体”または“変異体Fcポリペプチド”は、少なくとも1個のアミノ酸修飾により親Fcポリペプチドと異なるFcポリペプチドを意味する。本明細書で記載の“タンパク質変異体”または“変異体タンパク質”は、少なくとも1個のアミノ酸修飾により親タンパク質と異なるタンパク質を意味する。本明細書で記載の“抗体変異体”または“変異体抗体”は、少なくとも1個のアミノ酸修飾により親抗体と異なる抗体を意味する。本明細書で記載の“IgG変異体”または“変異体IgG”は、少なくとも1個のアミノ酸修飾により親IgGと異なる抗体を意味する。本明細書で記載の“免疫グロブリン変異体”または“変異体免疫グロブリン”は、少なくとも1個のアミノ酸修飾により親免疫グロブリン配列とは異なる免疫グロブリン配列を意味する。 As used herein, a “ variant polypeptide ”, “ polypeptide variant ” or “ variant ” means a polypeptide sequence that differs from a parent polypeptide sequence by at least one amino acid modification. The parent polypeptide can be a naturally occurring or wild type (WT) polypeptide, or can be a modified version of a WT polypeptide. Variant polypeptide can refer to the polypeptide itself, a composition comprising the polypeptide or the amino sequence that encodes it. Preferably, the variant polypeptide has at least one amino acid modification compared to the parent polypeptide, eg, about 1 to about 10 amino acid modifications compared to the parent polypeptide, preferably about Has 1 to about 5 amino acid modifications. As used herein, a variant polypeptide sequence preferably has at least about 80% homology, most preferably at least about 90% homology, more preferably at least about 95% homology with the parent polypeptide sequence. Can have. Thus, as used herein, an “ Fc variant ” or “ variant Fc ” means an Fc sequence that differs from a parent Fc sequence by at least one amino acid modification. An Fc variant may comprise only the Fc region or may exist as an antibody, Fc fusion, isolated Fc, Fc fragment, or other polypeptide substantially encoded by Fc. Fc variant may refer to a composition comprising the Fc polypeptide itself, the Fc variant polypeptide or the amino acid sequence encoding it. As used herein, an “ Fc polypeptide variant ” or “ variant Fc polypeptide ” refers to an Fc polypeptide that differs from a parent Fc polypeptide by at least one amino acid modification. As used herein, a “ protein variant ” or “ variant protein ” refers to a protein that differs from a parent protein by at least one amino acid modification. As used herein, an “ antibody variant ” or “ variant antibody ” refers to an antibody that differs from a parent antibody by at least one amino acid modification. As used herein, an “ IgG variant ” or “ variant IgG ” refers to an antibody that differs from the parent IgG by at least one amino acid modification. As used herein, an “ immunoglobulin variant ” or “ variant immunoglobulin ” refers to an immunoglobulin sequence that differs from a parent immunoglobulin sequence by at least one amino acid modification.
本明細書中、“野生型またはWT”は、アレル変異体を含む、天然に見出されるアミノ酸配列またはヌクレオチド配列を意味する。WTタンパク質、ポリペプチド、抗体、免疫グロブリン、IgGなどは、意図的に改変されていないアミノ酸配列またはヌクレオチド配列を有する。 As used herein, “ wild type or WT ” means an amino acid sequence or nucleotide sequence found in nature, including allelic variants. A WT protein, polypeptide, antibody, immunoglobulin, IgG, etc. has an amino acid sequence or nucleotide sequence that has not been intentionally modified.
抗体
従って、本発明は、変異体抗体を提供する。
Antibodies Accordingly, the present invention provides variant antibodies.
古典的抗体構造単位には、典型的に、四量体が含まれる。各四量体は、典型的に、ポリペプチド鎖の2個の相同対(各対は、1個の“軽”鎖(典型的に、約25kDaの分子量を有する。)および1個の“重”鎖(典型的に、約50−70kDaの分子量を有する。)を有する。)からなる。ヒト軽鎖は、カッパおよびラムダ軽鎖に分類される。重鎖は、ミュー、デルタ、ガンマ、アルファ、またはイプシロンに分類され、それぞれIgM、IgD、IgG、IgA、およびIgEとして抗体のイソ型を定義する。IgGは、IgG1、IgG2、IgG3およびIgG4を含むが、それらに限定されない、いくつかのサブクラスを有する。IgMは、IgM1およびIgM2を含むが、これに限定されないサブクラスを有する。故に、本明細書で記載の“イソ型”は、それらの定常領域の化学特性および抗原特性により定義される免疫グロブリンのサブクラスのいずれかを意味する。既知のヒト免疫グロブリンイソ型は、IgG1、IgG2、IgG3、IgG4、IgA1、IgA2、IgM1、IgM2、IgDおよびIgEである。 Classical antibody structural units typically include tetramers. Each tetramer typically has two homologous pairs of polypeptide chains (each pair has one “light” chain (typically having a molecular weight of about 25 kDa) and one “heavy”. "Having a chain (typically having a molecular weight of about 50-70 kDa)." Human light chains are classified as kappa and lambda light chains. Heavy chains are classified as mu, delta, gamma, alpha, or epsilon, and define the antibody's isotype as IgM, IgD, IgG, IgA, and IgE, respectively. IgG has several subclasses, including but not limited to IgG1, IgG2, IgG3 and IgG4. IgM has subclasses including but not limited to IgM1 and IgM2. Thus, as used herein, “isoform” refers to any of the immunoglobulin subclasses defined by the chemical and antigenic properties of their constant regions. Known human immunoglobulin isoforms are IgG1, IgG2, IgG3, IgG4, IgA1, IgA2, IgM1, IgM2, IgD and IgE.
各鎖のアミノ末端部位には、抗原認識に主要な役割を果たす、約100ないし110またはそれ以上のアミノ酸の可変領域が含まれる。可変領域中、3つのループが、重鎖および軽鎖の各Vドメインに集合し、抗原結合部位を形成する。各ループは、相補性決定領域(以降、“CDR”と称する)と称され、そこでのアミノ酸配列中の変異は、最も重要である。 The amino terminal site of each chain includes a variable region of about 100 to 110 or more amino acids that plays a major role in antigen recognition. In the variable region, three loops assemble into each heavy and light chain V domain to form an antigen binding site. Each loop is referred to as a complementarity determining region (hereinafter referred to as “CDR”), where mutations in the amino acid sequence are most important.
各鎖のカルボキシ末端部位は、エフェクター機能に主要な役割を果たす定常領域を定義する。Kabatらは、重鎖および軽鎖の可変領域の多数の主要配列を集めた。該配列の保存の程度に基づき、彼らは、CDRおよびフレームワークに個々の主要配列を分類し、そのリストを作成した(SEQUENCES OF IMMUNOLOGICAL INTEREST, 5th edition, NIH publication, No. 91−3242, E.A. Kabat et alを参照のこと)。 The carboxy terminal site of each chain defines a constant region that plays a major role in effector function. Kabat et al. Collected a number of major sequences of the variable regions of the heavy and light chains. Based on the degree of conservation of the sequences, they classified individual major sequences into CDRs and frameworks and created a list (SEQUENCES OF IMMUNOLOGICAL INTEREST, 5th edition, NIH publication, No. 91-3242, EA Kabat see et al).
免疫グロブリンのIgGサブクラスにおいて、重鎖には、いくつかの免疫グロブリンドメインが存在する。本明細書中、“免疫グロブリン(Ig)ドメイン”とは、異なる三次元構造を有する免疫グロブリンの領域を意味する。本発明において興味があるのは、重鎖定常(CH)ドメインおよびヒンジドメインを含む重鎖ドメインである。IgG抗体において、IgGイソ型はそれぞれ、3個のCH領域を有する。従って、IgGにおける“CH”ドメインは、下記である:“CH1”は、Kabatに記載のEU indexに従い、118−220位を示す。“CH2”は、Kabatに記載のEU indexに従い、237−340位を示し、“CH3”は、Kabatに記載のEU indexに従い、341−447位を示す。 In the IgG subclass of immunoglobulins, there are several immunoglobulin domains in the heavy chain. As used herein, “ immunoglobulin (Ig) domain ” means a region of an immunoglobulin having a different three-dimensional structure. Of interest in the present invention are heavy chain domains comprising a heavy chain constant (CH) domain and a hinge domain. In IgG antibodies, each IgG isoform has 3 CH regions. Thus, the “CH” domain in IgG is: “CH1” indicates positions 118-220 according to the EU index described in Kabat. “CH2” indicates positions 237-340 according to the EU index described in Kabat, and “CH3” indicates positions 341-447 according to the EU index described in Kabat.
重鎖のIgドメインの別のタイプは、ヒンジ領域である。本明細書中、“ヒンジ”もしくは“ヒンジ領域”または“抗体ヒンジ領域”もしくは“免疫グロブリンヒンジ領域”は、抗体の第一および第二定常ドメイン間のアミノ酸を含むフレキシブルポリペプチドを意味する。構造的には、IgG CH1ドメインは、EU 220位で終わり、IgG CH2ドメインは、EU 237位の残基で始まる。故に、IgGに関して、抗体ヒンジは、本明細書中、221位(IgG1にてD221)ないし236位(IgG1にてG236)を含むと定義され、ここで、番号は、Kabatに記載のEU indexに従う。いくつかの態様において、例えばFc領域において、一般的に226位または230位に当たる“下流側ヒンジ(lower hinge)”が包含される。
Another type of heavy chain Ig domain is the hinge region. As used herein, “hinge” or “hinge region” or “antibody hinge region” or “immunoglobulin hinge region” refers to a flexible polypeptide comprising amino acids between the first and second constant domains of an antibody. Structurally, the IgG CH1 domain ends at
本発明において特に興味があるのは、Fc領域である。本明細書で用いる“Fc”または“Fc領域”は、免疫グロブリンドメインの第一の定常領域、いくつかの場合に、ヒンジの一部を除く、抗体の定常領域を含むポリペプチドを意味する。故に、Fcは、免疫グロブリンドメインIgA、IgD、およびIgGの残り2個の定常領域、ならびに免疫グロブリンドメインIgEおよびIgMの残り3個の定常領域、ならびにこれらのドメインのN末端のフレキシブルヒンジを意味する。IgAおよびIgMに関して、Fcには、J鎖が含まれ得る。IgGに関して、図1に示す通り、Fcは、免疫グロブリンドメインCガンマ2およびCガンマ3(Cg2およびCg3)、ならびにCガンマ1(Cg1)とCガンマ2(Cg2)の間の下流側ヒンジ領域を含む。Fc領域の境界は変化し得るが、ヒトIgG重鎖Fc領域は、通常、そのカルボキシル末端に残基C226またはP230を含むと定義され、ここで、番号は、Kabatに記載のEU indexに従う。Fcは、下記に記載の通り、単離したこの領域か、またはFcポリペプチド中のこの領域を意味し得る。本明細書で記載の“Fcポリペプチド”は、Fc領域の全てまたは一部を含むポリペプチドを意味する。Fcポリペプチドは、抗体、Fc融合体、単離されたFc、およびFc断片を含む。 Of particular interest in the present invention is the Fc region. As used herein, “Fc” or “Fc region” refers to a polypeptide that comprises the first constant region of an immunoglobulin domain, in some cases the constant region of the antibody, excluding part of the hinge. Thus, Fc means the remaining two constant regions of immunoglobulin domains IgA, IgD, and IgG, and the remaining three constant regions of immunoglobulin domains IgE and IgM, and the N-terminal flexible hinge of these domains . For IgA and IgM, Fc can include the J chain. With respect to IgG, as shown in FIG. 1, Fc comprises immunoglobulin domains Cgamma2 and Cgamma3 (Cg2 and Cg3) and a downstream hinge region between Cgamma1 (Cg1) and Cgamma2 (Cg2). Including. Although the boundaries of the Fc region can vary, a human IgG heavy chain Fc region is usually defined to include residues C226 or P230 at its carboxyl terminus, where the numbers follow the EU index described in Kabat. Fc can refer to this isolated region or this region in an Fc polypeptide, as described below. As used herein, “Fc polypeptide” means a polypeptide comprising all or part of an Fc region. Fc polypeptides include antibodies, Fc fusions, isolated Fc, and Fc fragments.
いくつかの態様において、抗体は全長である。本明細書中、“全長抗体”とは、本明細書に記載の通り、1個以上の修飾を含む可変領域および定常領域を含む抗体の天然の生物学的形態を構成する構造を意味する。 In some embodiments, the antibody is full length. As used herein, “full-length antibody” means a structure that constitutes the natural biological form of an antibody, including variable and constant regions containing one or more modifications, as described herein.
あるいは、抗体は、それぞれ、抗体断片、モノクローナル抗体、二重特異的抗体、ミニボディ、ドメイン抗体、合成抗体(本明細書中、“抗体模倣体”と称されることもある。)、キメラ抗体、ヒト化抗体、抗体融合体(本明細書中、“抗体複合体”と称されることもある。)、および各断片を含むが、それらに限定されない、多様な構造であり得る。 Alternatively, the antibodies are antibody fragments, monoclonal antibodies, bispecific antibodies, minibodies, domain antibodies, synthetic antibodies (sometimes referred to herein as “antibody mimics”), chimeric antibodies, respectively. , Humanized antibodies, antibody fusions (sometimes referred to herein as “antibody complexes”), and various structures, including but not limited to fragments.
抗体断片
1つの態様において、抗体は抗体断片である。特に興味があるのは、Fc領域、Fc融合体および重鎖の定常領域(CH1−ヒンジ−CH2−CH3)を含み、さらにまた、重鎖定常領域融合体を含む、抗体である。
Antibody Fragment In one embodiment, the antibody is an antibody fragment. Of particular interest are antibodies comprising an Fc region, an Fc fusion and a heavy chain constant region (CH1-hinge-CH2-CH3), and also comprising a heavy chain constant region fusion.
特定の抗体断片には、(i)VL、VH、CLおよびCH1ドメインからなるFab断片、(ii)VHおよびCH1ドメインからなるFd断片、(iii)単一抗体のVLおよびVHドメインからなるFv断片;(iv)単一の可変領域からなるdAb断片(Ward et al., 1989, Nature 341:544−546)、(v)単離されたCDR領域、(vi)F(ab’)2断片、2つの結合したFab断片を含む二価断片、(vii)一本鎖Fv分子(scFv)(ここで、VHドメインおよびVLドメインは、2個のドメインを結合させ、抗原結合部位を形成させるペプチドリンカーにより連結される(Bird et al., 1988, Science 242:423−426, Huston et al., 1988, Proc. Natl. Acad. Sci. U.S.A. 85:5879−5883)、(viii)二重特異的一本鎖Fv二量体(PCT/US92/09965)、ならびに(ix)“二重抗体(diabody)”または“三重抗体(triabody)”、遺伝子融合により構築される多価または多特異的断片(Tomlinson et. al., 2000, Methods Enzymol. 326:461−479;WO94/13804;Holliger et al., 1993, Proc. Natl. Acad. Sci. U.S.A. 90:6444−6448)が含まれるが、それらに限定されない。該抗体断片は、修飾され得る。例えば、分子は、VHおよびVLドメインを連結するジスルフィド架橋の組込みにより安定化され得る(Reiter et al., 1996, Nature Biotech. 14:1239−1245)。 Specific antibody fragments include (i) a Fab fragment consisting of VL, VH, CL and CH1 domains, (ii) an Fd fragment consisting of VH and CH1 domains, (iii) an Fv fragment consisting of VL and VH domains of a single antibody (Iv) a dAb fragment consisting of a single variable region (Ward et al., 1989, Nature 341: 544-546), (v) an isolated CDR region, (vi) an F (ab ′) 2 fragment, A bivalent fragment comprising two linked Fab fragments, (vii) a single chain Fv molecule (scFv), where the VH and VL domains are peptide linkers that bind the two domains and form an antigen binding site (Bird et al., 1988, Science 242: 423-426, Huston et al., 1988, Proc. Natl. Acad. Sci. USA 85: 5879-5883), (viii) bispecific mono This chain Fv dimer (PCT / US92 / 0996 ), And (ix) “diabodies” or “triabodies”, multivalent or multispecific fragments constructed by gene fusion (Tomlinson et. Al., 2000, Methods Enzymol. 326: WO94 / 13804; Holliger et al., 1993, Proc. Natl. Acad. Sci. USA 90: 6444-6448), etc. The antibody fragment may be modified, for example. The molecule can be stabilized by the incorporation of disulfide bridges that link the VH and VL domains (Reiter et al., 1996, Nature Biotech. 14: 1239-1245).
キメラ抗体およびヒト化抗体
いくつかの態様において、骨格成分は、異なる種由来の混合物であり得る。そういうものとして、問題の抗体がそのような抗体であるとき、かかる抗体は、キメラ抗体および/またはヒト化抗体であり得る。一般的に、“キメラ抗体”および“ヒト化抗体”は両方とも、2種以上由来の領域を組み合わせた抗体を意味する。例えば、“キメラ抗体”には、伝統的に、マウス(またはいくつかの場合に、ラット)由来の可変領域(複数可)およびヒト由来の定常領域(複数可)が含まれる。“ヒト化抗体”は、一般的に、ヒト抗体中に見出される配列に置換した可変ドメインフレームワーク領域を有している非ヒト抗体を意味する。一般的に、ヒト化抗体において、CDRを除く抗体全体は、ヒト起源のポリヌクレオチドによりコードされるか、またはそのCDR内を除いてそのような抗体と同一である。そのいくつかまたは全てが非ヒト生物に由来する核酸によりコードされるCDRは、ヒト抗体可変領域のベータ−シートフレームワークに移植され、抗体を作製し、その特異性は、移植したCDRにより決定される。そのような抗体の作製は、例えば、WO92/11018、Jones, 1986, Nature 321:522−525, Verhoeyen et al., 1988, Science 239:1534−1536に記載される。対応するドナー残基への選択したアクセプターフレームワーク残基の“復帰突然変異(Backmutation)”は、しばしば、初期の移植したコンストラクトで欠失している親和性を再び得るのに必要である(US5530101;US5585089;US5693761;US5693762;US6180370;US5859205;US5821337;US6054297;US6407213)。ヒト化抗体はまた、最適には、免疫グロブリン定常領域、典型的にはヒト免疫グロブリンの少なくとも一部を含み、故に、ヒトFc領域を典型的に含むだろう。ヒト化抗体はまた、遺伝子組み換えされた免疫系を有するマウスを用いて作製され得る(Roque et al., 2004, Biotechnol. Prog. 20:639−654)。非ヒト抗体のヒト化および再形成のための様々な技術および方法は、当技術分野でよく知られている(Tsurushita & Vasquez, 2004, Humanization of Monoclonal Antibodies, Molecular Biology of B Cells, 533−545, Elsevier Science(USA)およびそこで引用される文献)。ヒト化方法には、Jones et al., 1986, Nature 321:522−525;Riechmann et al.,1988;Nature 332:323−329;Verhoeyen et al., 1988, Science, 239:1534−1536;Queen et al., 1989, Proc Natl Acad Sci, USA 86:10029−33;He et al., 1998, J. Immunol. 160: 1029−1035;Carter et al., 1992, Proc Natl Acad Sci USA 89:4285−9, Presta et al., 1997, Cancer Res.57(20):4593−9;Gorman et al., 1991, Proc. Natl. Acad. Sci. USA 88:4181−4185;O’Connor et al., 1998, Protein Eng 11:321−8に記載の方法が含まれるが、それらに限定されない。非ヒト抗体可変領域の免疫原性を減じるヒト化または他の方法には、例えば、Roguska et al., 1994, Proc. Natl. Acad. Sci. USA 91:969−973に記載の表面再形成(resurfacing)方法が含まれ得る。1つの態様において、親抗体は、当技術分野で公知の通り、成熟した親和性を有する。構造に基づく方法は、例えばUSSN11/004,590に記載のヒト化および親和性成熟に用いられ得る。選択に基づく方法は、Wu et al., 1999, J. Mol. Biol. 294:151−162;Baca et al., 1997, J. Biol. Chem. 272(16):10678−10684;Rosok et al., 1996, J. Biol. Chem. 271(37): 22611−22618;Rader et al., 1998, Proc. Natl. Acad. Sci. USA 95: 8910−8915;Krauss et al., 2003, Protein Engineering 16(10):753−759に記載の方法を含むが、これらに限定されない、抗体可変領域のヒト化および/または親和性成熟に用いられ得る。他のヒト化方法は、USSN09/810,502;Tan et al., 2002, J. Immunol. 169:1119−1125;De Pascalis et al., 2002, J. Immunol. 169:3076−3084に記載の方法を含むが、これらに限定されない、CDRの一部のみの移植を伴い得る。
Chimeric and humanized antibodies In some embodiments, the backbone component can be a mixture from different species. As such, when the antibody in question is such an antibody, such antibody can be a chimeric antibody and / or a humanized antibody. In general, both “chimeric antibodies” and “humanized antibodies” refer to antibodies that combine regions from two or more species. For example, “chimeric antibodies” traditionally include variable region (s) from mouse (or in some cases, rat) and constant region (s) from human. “Humanized antibody” generally refers to non-human antibodies having variable domain framework regions substituted for sequences found in human antibodies. In general, in a humanized antibody, the entire antibody, except the CDRs, is encoded by a polynucleotide of human origin or is identical to such an antibody except within its CDRs. CDRs, some or all of which are encoded by nucleic acids derived from non-human organisms, are grafted into the beta-sheet framework of the human antibody variable region to produce antibodies, the specificity of which is determined by the grafted CDRs. The The production of such antibodies is described, for example, in WO 92/11018, Jones, 1986, Nature 321: 522-525, Verhoeyen et al., 1988, Science 239: 1534-1536. “Backmutation” of selected acceptor framework residues to the corresponding donor residues is often necessary to regain the affinity missing in the initial grafted construct ( US5530101; US5585089; US5693761; US5693762; US6180370; US5859205; US5821337; US6054297; US6407213). A humanized antibody will also optimally comprise an immunoglobulin constant region, typically at least a portion of a human immunoglobulin, and thus will typically comprise a human Fc region. Humanized antibodies can also be generated using mice with a genetically engineered immune system (Roque et al., 2004, Biotechnol. Prog. 20: 639-654). Various techniques and methods for humanization and remodeling of non-human antibodies are well known in the art (Tsurushita & Vasquez, 2004, Humanization of Monoclonal Antibodies, Molecular Biology of B Cells, 533-545, Elsevier Science (USA) and references cited therein). Humanization methods include Jones et al., 1986, Nature 321: 522-525; Riechmann et al., 1988; Nature 332: 323-329; Verhoeyen et al., 1988, Science, 239: 1534-1536; Queen et al., 1989, Proc Natl Acad Sci, USA 86: 10029-33; He et al., 1998, J. Immunol. 160: 1029-1035; Carter et al., 1992, Proc Natl Acad Sci USA 89: 4285 -9, Presta et al., 1997, Cancer Res. 57 (20): 4593-9; Gorman et al., 1991, Proc. Natl. Acad. Sci. USA 88: 4181-4185; O'Connor et al. 1998, Protein Eng 11: 321-8, but is not limited thereto. Humanization or other methods for reducing the immunogenicity of non-human antibody variable regions include, for example, surface remodeling as described in Roguska et al., 1994, Proc. Natl. Acad. Sci. USA 91: 969-973 ( resurfacing) method may be included. In one embodiment, the parent antibody has mature affinity, as is known in the art. Structure-based methods can be used for humanization and affinity maturation as described, for example, in
二重特異的抗体
1つの態様において、本発明の多特異的抗体、特に二重特異的抗体はまた、“二重抗体”と称されることもある。これらは、2個(またはそれ以上)の異なる抗原に結合する抗体である。二重抗体は、当技術分野で公知の様々な方法で製造することができ(Holliger and Winter, 1993, Current Opinion Biotechnol. 4:446−449)、例えば化学的に、またはハイブリッド・ハイブリドーマ(hybrid hybridoma)から製造することができる。
Bispecific Antibodies In one embodiment, multispecific antibodies, particularly bispecific antibodies, of the present invention may also be referred to as “biantibodies”. These are antibodies that bind to two (or more) different antigens. Double antibodies can be produced by various methods known in the art (Holliger and Winter, 1993, Current Opinion Biotechnol. 4: 446-449), eg chemically or hybrid hybridoma. ).
ミニボディ
1つの態様において、抗体はミニボディである。ミニボディは、CH3ドメインに結合したscFvを含む最小化抗体様タンパク質である(Hu et al., 1996, Cancer Res. 56:3055−3061)。いくつかの場合に、scFvは、Fc領域と結合することができ、ヒンジ領域のいくつかまたは全てを包含し得る。
Minibodies In one embodiment, the antibody is a minibody. A minibody is a minimized antibody-like protein that contains an scFv bound to a CH3 domain (Hu et al., 1996, Cancer Res. 56: 3055-3061). In some cases, the scFv can bind to the Fc region and can include some or all of the hinge region.
ヒト抗体
1つの態様において、抗体は、本明細書に記載の通り、少なくとも1個の修飾を有する全長ヒト抗体である。“全長ヒト抗体”または“完全ヒト抗体”は、本明細書に記載の修飾を有するヒト染色体に由来する抗体の遺伝子配列を有するヒト抗体を意味する。
Human antibodies In one embodiment, the antibody is a full-length human antibody having at least one modification as described herein. “Full-length human antibody” or “fully human antibody” means a human antibody having the gene sequence of an antibody derived from a human chromosome having the modifications described herein.
抗体融合体
1つの態様において、本発明の抗体は、抗体融合タンパク質(本明細書中、“抗体複合体”と称されることもある)である。抗体融合体の1つのタイプは、結合パートナーを有するFc領域を連結するFc融合体を含む。本明細書で記載の“Fc融合体”は、1個以上のポリペプチドが、Fc領域に作動可能に連結されるタンパク質を意味する。本明細書中、Fc融合体は、従来技術(Chamow et al., 1996, Trends Biotechnol 14:52−60;Ashkenazi et al., 1997, Curr Opin Immunol 9:195−200)で用いる通り、用語“免疫アドヘシン(immunoadhesin)”、“Ig融合体”、“Igキメラ”、および“受容体グロブリン”(ダッシュを付けることもある)と同義の意味である。Fc融合体は、一般的に、何れかのタンパク質または小分子であり得る融合パートナーを有する免疫グロブリンのFc領域を結合する。実際、何れかのタンパク質または小分子はFcと結合し、Fc融合体を作製し得る。タンパク質融合パートナーには、何れかの抗体の可変領域、受容体の標的結合領域、接着分子、リガンド、酵素、サイトカイン、ケモカイン、または他のタンパク質もしくはタンパク質ドメインが含まれ得るが、それらに限定されない。小分子融合パートナーは、Fc融合体を治療標的に向ける何れかの治療剤を含み得る。かかる標的は、疾患に関与する何れかの分子、好ましくは細胞外受容体であり得る。
Antibody Fusion In one embodiment, an antibody of the invention is an antibody fusion protein (sometimes referred to herein as an “antibody complex”). One type of antibody fusion includes an Fc fusion that links Fc regions with binding partners. As used herein, an “ Fc fusion ” refers to a protein in which one or more polypeptides are operably linked to an Fc region. In this specification, Fc fusion is the term “as used in the prior art (Chamow et al., 1996, Trends Biotechnol 14: 52-60; Ashkenazi et al., 1997, Curr Opin Immunol 9: 195-200). Synonymous with “immunoadhesin”, “Ig fusion”, “Ig chimera”, and “receptor globulin” (sometimes with dashes). Fc fusions generally bind the Fc region of an immunoglobulin with a fusion partner that can be any protein or small molecule. In fact, any protein or small molecule can bind Fc and create an Fc fusion. Protein fusion partners can include, but are not limited to, the variable region of any antibody, the target binding region of a receptor, an adhesion molecule, a ligand, an enzyme, a cytokine, a chemokine, or other protein or protein domain. Small molecule fusion partners can include any therapeutic agent that directs the Fc fusion to a therapeutic target. Such a target may be any molecule involved in the disease, preferably an extracellular receptor.
Fc融合体に加えて、抗体融合体は、重鎖の定常領域と、1個以上の融合パートナー(何れかの抗体の可変領域をさらに含む)の融合を含むが、一方、他の抗体融合体は、融合パートナーを有する実質的または完全な全長抗体である。1つの態様において、融合パートナーの役割は標的結合を仲介することであり、故に、それは、抗体の可変領域に機能的に類似する(そして、実際抗体可変領域であり得る)。実際、何れかのタンパク質または小分子は、Fcと結合してFc融合体(または抗体融合体)を作製し得る。タンパク質融合パートナーは、受容体の標的結合領域、接着分子、リガンド、酵素、サイトカイン、ケモカインまたはいくつかの他のタンパク質またはタンパク質ドメインを含み得るが、それらに限定されない。小分子融合パートナーは、Fc融合体を治療標的に向ける何れかの治療剤を含み得る。かかる標的は、疾患に関与する何れかの分子、好ましくは細胞外受容体であり得る。 In addition to Fc fusions, antibody fusions comprise a fusion of the constant region of the heavy chain and one or more fusion partners (further including the variable region of any antibody), while other antibody fusions. Is a substantial or complete full-length antibody with a fusion partner. In one embodiment, the role of the fusion partner is to mediate target binding, and thus it is functionally similar to the variable region of an antibody (and may actually be an antibody variable region). In fact, any protein or small molecule can bind to Fc to create an Fc fusion (or antibody fusion). A protein fusion partner can include, but is not limited to, a target binding region of a receptor, an adhesion molecule, a ligand, an enzyme, a cytokine, a chemokine or some other protein or protein domain. Small molecule fusion partners can include any therapeutic agent that directs the Fc fusion to a therapeutic target. Such a target may be any molecule involved in the disease, preferably an extracellular receptor.
結合パートナーは、タンパク性または非タンパク性であり得る;後者は、一般的に、抗体および結合パートナー上の官能基を用いて作製される。例えばリンカーは、当技術分野で公知である;例えば、ホモ−またはヘテロ−二官能性リンカーが、よく知られている(1994 Pierce Chemical Company catalog, technical section on cross−linkers, pages 155−200を参照のこと、参照により本明細書中に包含される)。 Binding partners can be proteinaceous or non-proteinaceous; the latter is generally made using functional groups on the antibody and binding partner. For example, linkers are known in the art; for example, homo- or hetero-bifunctional linkers are well known (see 1994 Pierce Chemical Company catalog, technical section on cross-linkers, pages 155-200). Which is incorporated herein by reference).
適する複合体には、下記の標識、薬剤、ならびに細胞毒性剤(例えば、化学療法剤)または毒物またはかかる毒物の活性断片を含むが、これらに限定されない細胞毒性物質が含まれるが、それらに限定されない。適する毒物およびそれらの対応する断片には、ジフテリアA鎖、エクソトキシンA鎖、リシンA鎖、アブリンA鎖、クルシン、クロチン、フェノマイシン、エノマイシンなどが含まれる。細胞毒性物質にはまた、放射性同位体と抗体を結合すること、または放射性核種と抗体に共有結合しているキレート剤を結合することにより作製される放射性化学物質が含まれる。さらなる態様が、カリケミシン、オーリスタチン(auristatin)、ゲルダナマイシン、マイタンシン、ならびにデュオカルマイシンおよび類似体を利用する;後者に関して、U.S.2003/0050331を参照のこと、参照によりその全体が本明細書中に包含される。
Suitable conjugates include, but are not limited to, the following labels, agents, and cytotoxic agents (eg, chemotherapeutic agents) or cytotoxic agents, or cytotoxic agents such as, but not limited to: Not. Suitable toxicants and their corresponding fragments include diphtheria A chain, exotoxin A chain, ricin A chain, abrin A chain, cursin, crotin, phenomycin, enomycin and the like. Cytotoxic agents also include radiochemicals made by linking a radioisotope and an antibody, or by binding a radionuclide and a chelator that is covalently bound to the antibody. Further embodiments utilize calichemicin, auristatin, geldanamycin, maytansine, and duocarmycin and analogs;
抗体の共有結合修飾(Covalent modification)
抗体の共有結合修飾は、本発明の範囲内に包含され、常にではないが一般的に、翻訳後に行われる。例えば、抗体の共有結合修飾のいくつかのタイプは、抗体の特定のアミノ酸残基を、選択した側鎖またはN−もしくはC−末端残基と反応し得る有機誘導体化剤と反応させることにより分子内に導入される。
Covalent modification of antibodies
Covalent modifications of antibodies are encompassed within the scope of the invention and are generally, but not always, post-translational. For example, some types of covalent modification of an antibody can be performed by reacting specific amino acid residues of an antibody with an organic derivatizing agent that can react with a selected side chain or N- or C-terminal residue. Introduced in.
システイニル残基は、最も一般的に、α−ハロ酢酸(および対応するアミン)、例えばクロロ酢酸またはクロロアセトアミドと反応し、カルボキシメチルまたはカルボキシアミドメチル誘導体を生じる。システイニル残基はまた、ブロモトリフルオロアセトン、α−ブロモ−β−(5−イミドゾイル)プロピオン酸、リン酸クロロアセチル、N−アルキルマレイミド、3−ニトロ−2−ピリジルジスルフィド、メチル−2−ピリジルジスルフィド、p−クロロ水銀ベンゾエート、2−クロロ水銀−4−ニトロフェノールまたはクロロ−7−ニトロベンゾ−2−オキサ−1,3−ジアゾールとの反応により誘導される。 Cysteinyl residues most commonly react with α-haloacetic acids (and corresponding amines) such as chloroacetic acid or chloroacetamide to give carboxymethyl or carboxyamidomethyl derivatives. Cysteinyl residues also include bromotrifluoroacetone, α-bromo-β- (5-imidozoyl) propionic acid, chloroacetyl phosphate, N-alkylmaleimide, 3-nitro-2-pyridyl disulfide, methyl-2-pyridyl disulfide , P-chloromercury benzoate, 2-chloromercury-4-nitrophenol or chloro-7-nitrobenzo-2-oxa-1,3-diazole.
ヒスチジル残基は、ヒスチジル側鎖と比較的特異的に反応するピロ炭酸ジエチルとのpH5.5−7.0での反応により誘導される。臭化パラフェンアシルブロミドも有用である;反応は、好ましくは0.1Mカコジル酸ナトリウム中、pH6.0にて行われる。 Histidyl residues are derived by reaction at pH 5.5-7.0 with diethyl pyrocarbonate which reacts relatively specifically with histidyl side chains. Paraphenacyl bromide bromide is also useful; the reaction is preferably carried out in 0.1 M sodium cacodylate at pH 6.0.
リシニル(Lysinyl)およびアミノ末端残基を、無水コハク酸または他のカルボン酸無水物と反応させる。これらの物質を用いる誘導体化は、リシニル残基の荷電を逆にする効果を有する。アルファ−アミノ含有残基を誘導体化するのに適する他の反応剤には、メチルピコリンイミダート;ピリドキサルリン酸;ピリドキサール;クロロボロハイドライド;トリニトロベンゼンスルホン酸;O−メチルイソウレア;2,4−ペンタンジオンのようなイミドエステル、ならびにグリオキシル酸とのトランスアミナーゼ触媒反応が含まれる。 Lysinyl and the amino terminal residue are reacted with succinic anhydride or other carboxylic anhydride. Derivatization using these substances has the effect of reversing the charge of the ricinyl residue. Other reagents suitable for derivatizing alpha-amino containing residues include methylpicoline imidate; pyridoxal phosphate; pyridoxal; chloroborohydride; trinitrobenzene sulfonic acid; O-methylisourea; Included are imidoesters such as diones, as well as transaminase catalyzed reactions with glyoxylic acid.
アルギニル残基は、1個またはいくつかの常套反応剤(とりわけ、フェニルグリオキサール、2,3−ブタンジオン、1,2−シクロヘキサンジオンおよびニンヒドリン)との反応により修飾される。アルギニン残基の誘導体化は、グアニジン官能基が高pKaであるためにアルカリ性条件で行うことが必要である。さらに、これらの反応剤は、リシンの複数の基ならびにアルギニン イプシロン−アミノ基と反応し得る。 Arginyl residues are modified by reaction with one or several conventional reactants (especially phenylglyoxal, 2,3-butanedione, 1,2-cyclohexanedione and ninhydrin). Derivatization of arginine residues must be performed under alkaline conditions because the guanidine functional group has a high pKa. In addition, these reactants can react with multiple groups of lysine as well as the arginine epsilon-amino group.
チロシル残基の特異的修飾を、特に関心を持って、芳香族性ジアゾニウム化合物またはテトラニトロメタンとの反応によりチロシル残基中にスペクトル標識を導入することにより作製することができる。最も一般的には、N−アセチルイミジゾール(acetylimidizole)およびテトラニトロメタンを、それぞれO−アセチルチロシル種および3−ニトロ誘導体を形成するために用いる。チロシル酸基を、ラジオイムノアッセイである、適する上記のクロラミンT法に用いるための標識したタンパク質を調製するために125Iまたは131Iを用いてヨウ素化する。 Specific modifications of tyrosyl residues can be made with particular interest by introducing spectral labels into tyrosyl residues by reaction with aromatic diazonium compounds or tetranitromethane. Most commonly, N-acetylimidizole and tetranitromethane are used to form O-acetyl tyrosyl species and 3-nitro derivatives, respectively. The tyrosyl acid group is iodinated with 125I or 131I to prepare a labeled protein for use in a suitable chloramine T method as described above, a radioimmunoassay.
カルボキシル側基(アスパルチルまたはグルタミル)は、カルボジイミド(R’N=C=N――R’)(式中、RおよびR’は、所望により、1−シクロヘキシル−3−(2−モルホリニル−4−エチル)カルボジイミドまたは1−エチル−3−(4−アゾニア−4,4−ジメチルペンチル)カルボジイミドのような異なるアルキル基であり得る。)との反応により選択的に修飾される。さらに、アスパルチルおよびグルタミル残基は、アンモニウムイオンとの反応によりアスパラギニルおよびグルタミニル残基に変換される。 The carboxyl side group (aspartyl or glutamyl) is carbodiimide (R′N═C═N—R ′) where R and R ′ are optionally 1-cyclohexyl-3- (2-morpholinyl-4- Can be different alkyl groups such as ethyl) carbodiimide or 1-ethyl-3- (4-azonia-4,4-dimethylpentyl) carbodiimide). Furthermore, aspartyl and glutamyl residues are converted to asparaginyl and glutaminyl residues by reaction with ammonium ions.
二官能性物質を用いる誘導体化は、下記の方法に加えて、様々な方法での使用のために抗体を不水溶性支持マトリックスまたは表面に架橋させるのに有用である。常用される架橋剤には、例えば、1,1−ビス(ジアゾアセチル)−2−フェニルエタン、グルタルアルデヒド、N−ヒドロキシスクシンイミドエステル、例えば、4−アジドサリチル酸とのエステル、3,3’−ジチオビス(サクシンイミジルプロピオネート)のようなジサクシンイミジルエステルを含むホモ二官能性イミドエステル、およびビス−N−マレイミド−1,8−オクタンのような二官能性マレイミドが含まれる。メチル−3−[(p−アジドフェニル)ジチオ]プロピオイミデートのような誘導体化剤は、光の存在下で架橋を形成し得る光活性化中間体を生じる。あるいは、臭化シアン活性化炭水化物のような反応性不水溶性マトリックスおよび米国特許番号第3,969,287号;同第3,691,016号;同第4,195,128号;同第4,247,642号;同第4,229,537号;および、同第4,330,440号に記載の反応基質を、タンパク質固定化に用いる。 Derivatization with bifunctional materials is useful for cross-linking antibodies to a water-insoluble support matrix or surface for use in various methods in addition to the methods described below. Commonly used crosslinking agents include, for example, 1,1-bis (diazoacetyl) -2-phenylethane, glutaraldehyde, N-hydroxysuccinimide esters such as esters with 4-azidosalicylic acid, 3,3′-dithiobis Included are homobifunctional imide esters, including disuccinimidyl esters such as (succinimidyl propionate), and bifunctional maleimides such as bis-N-maleimide-1,8-octane. Derivatizing agents such as methyl-3-[(p-azidophenyl) dithio] propioimidate yield photo-activated intermediates that can form crosslinks in the presence of light. Alternatively, a reactive water-insoluble matrix such as cyanogen bromide activated carbohydrate and US Pat. Nos. 3,969,287; 3,691,016; 4,195,128; 247,642; 4,229,537; and 4,330,440 are used for protein immobilization.
グルタミニルおよびアスパラギニル残基は、しばしば、それぞれ対応するグルタミルおよびアスパルチル残基に脱アミド化される。あるいは、これらの残基は、弱酸性条件下で脱アミド化される。これらの残基の形態はどちらも、本発明の範囲内である。 Glutaminyl and asparaginyl residues are often deamidated to the corresponding glutamyl and aspartyl residues, respectively. Alternatively, these residues are deamidated under mildly acidic conditions. Both forms of these residues are within the scope of the present invention.
他の修飾には、プロリンおよびリシンのヒドロキシル化、セリルまたはトレオニル残基のヒドロキシル基のリン酸化、リシン、アルギニンおよびヒスチジン側鎖のα−アミノ基のメチル化(T. E. Creighton, Proteins: Structure and Molecular Properties, W. H. Freeman & Co., San Francisco, pp. 79−86 [1983])、N末端アミンのアセチル化、ならびに何れかのC末端カルボキシル基のアミド化が含まれる。 Other modifications include hydroxylation of proline and lysine, phosphorylation of the hydroxyl group of seryl or threonyl residues, methylation of α-amino groups of lysine, arginine and histidine side chains (TE Creighton, Proteins: Structure and Molecular Properties , WH Freeman & Co., San Francisco, pp. 79-86 [1983]), acetylation of N-terminal amines, and amidation of any C-terminal carboxyl group.
グリコシル化
共有結合修飾の別のタイプは、グリコシル化である。他の態様において、本明細書に記載のIgG変異体は、1個以上の改変された糖鎖(engineered glycoform)を含むように修飾され得る。本明細書で用いる“改変された糖鎖”は、IgGと共有結合する炭水化物組成物を意味し、ここで該炭水化物組成物は、親IgGのそれと化学的に異なる。改変された糖鎖は、エフェクター機能を増強するかまたは減少することを含むが、これらに限定されない様々な目的に有用であり得る。改変された糖鎖は、当技術分野で公知の様々な方法により作製され得る(Umana et al., 1999, Nat Biotechnol 17:176−180;Davies et al., 2001, Biotechnol Bioeng 74:288−294;Shields et al., 2002, J Biol Chem 277:26733−26740;Shinkawa et al., 2003, J Biol Chem 278:3466−3473;US6,602,684;USSN10/277,370;USSN10/113,929;PCT WO00/61739A1;PCT WO01/29246A1;PCT WO02/31140A1;PCT WO02/30954A1;PotelligentTM technology [Biowa, Inc., Princeton, NJ];GlycoMAb(登録商標)glycosylation engineering technology [Glycart Biotechnology AG, Zuerich, Switzerland])。多くのこれらの技術は、例えば、様々な生物、または遺伝子組み換えもしくは他の方法の細胞株(例えば、Lec−13 CHO細胞またはラットハイブリドーマYB2/0細胞)中でIgGを発現させることによるか、またはグリコシル化経路に関与する酵素(例えば、FUT8[α1,6−フコシルトランスフェラーゼ]および/またはβ1−4−N−アセチルグルコサミニルトランスフェラーゼIII[GnTIII])を調節することによるか、またはIgGが発現された後、炭水化物(複数可)を修飾することにより、Fc領域に共有結合するオリゴ糖のフコシル化レベルを制御すること、および/またはそれを2つに切断することに基づく。改変された糖鎖は、典型的に、異なる炭水化物またはオリゴ糖を意味する;故に、IgG変異体、例えば抗体またはFc融合体は、改変された糖鎖に包含され得る。あるいは、改変された糖鎖は、異なる炭水化物またはオリゴ糖を含むIgG変異体を意味し得る。当技術分野で公知の通り、グリコシル化パターンは、タンパク質の配列(例えば、下記の特定のグリコシル化アミノ酸残基の存在または不存在)、または該タンパク質を産生する宿主細胞もしくは生物に依存し得る。特定の発現系を以下に記載する。
Glycosylation Another type of covalent modification is glycosylation. In other embodiments, the IgG variants described herein can be modified to include one or more engineered glycoforms. As used herein, “modified sugar chain” refers to a carbohydrate composition that is covalently linked to IgG, where the carbohydrate composition is chemically different from that of the parent IgG. Modified sugar chains may be useful for a variety of purposes including, but not limited to, enhancing or decreasing effector function. Modified sugar chains can be made by various methods known in the art (Umana et al., 1999, Nat Biotechnol 17: 176-180; Davies et al., 2001, Biotechnol Bioeng 74: 288-294 Shields et al., 2002, J Biol Chem 277: 26733-26740; Shinkawa et al., 2003, J Biol Chem 278: 3466-3473; US 6,602,684;
ポリペプチドのグリコシル化は、典型的に、N結合またはO結合のいずれかである。N結合は、アスパラギン残基の側鎖への炭水化物部分の付加を意味する。トリペプチド配列であるアスパラギン−X−セリンおよびアスパラギン−X−トレオニン(式中、Xは、プロリンを除く任意のアミノ酸である。)は、アスパラギン側鎖への炭水化物部分の酵素的結合のための認識配列である。故に、ポリペプチド中のこれらのトリペプチド配列の何れかの存在は、可能性のあるグリコシル化部位をもたらす。O結合グリコシル化は、ヒドロキシアミノ酸(最も一般的にはセリンまたはトレオニンであるが、5−ヒドロキシプロリンまたは5−ヒドロキシリシンも使用可能である。)への糖の一種(N−アセチルガラクトサミン、ガラクトース、またはキシロース)の付加を意味する。 Glycosylation of polypeptides is typically either N-linked or O-linked. N-linked refers to the addition of a carbohydrate moiety to the side chain of an asparagine residue. The tripeptide sequences asparagine-X-serine and asparagine-X-threonine, where X is any amino acid except proline, are recognized for enzymatic attachment of the carbohydrate moiety to the asparagine side chain. Is an array. Thus, the presence of any of these tripeptide sequences in the polypeptide provides a potential glycosylation site. O-linked glycosylation is a type of sugar (N-acetylgalactosamine, galactose, to hydroxyamino acids (most commonly serine or threonine, but 5-hydroxyproline or 5-hydroxylysine can also be used). Or addition of xylose).
抗体へのグリコシル化部位の付加は、(N結合グリコシル化部位のために)1個以上の上記トリペプチド配列を含むようにアミノ酸配列を改変することにより都合よく達成される。該改変はまた、(O結合グリコシル化部位のために)出発配列への1個以上のセリンまたはトレオニン残基の付加または置換により成され得る。簡単には、抗体のアミノ酸配列を、好ましくはDNAレベルでの変化により、特に、コドンが所望のアミノ酸に翻訳され得るように作製されるように予め選択された塩基にて、標的ポリペプチドをコードするDNAを変異させることにより、改変する。 Addition of glycosylation sites to the antibody is conveniently accomplished by altering the amino acid sequence to include one or more of the above tripeptide sequences (for N-linked glycosylation sites). The modification can also be made by addition or substitution of one or more serine or threonine residues to the starting sequence (for O-linked glycosylation sites). Briefly, the amino acid sequence of an antibody is encoded by a target polypeptide, preferably at a pre-selected base such that a change at the DNA level, in particular a codon can be translated into the desired amino acid. It is modified by mutating the DNA to be mutated.
抗体上の炭水化物部分の数を増加する他の手段は、タンパク質へのグリコシドの化学的または酵素的カップリングによる。これらの方法は、NおよびO結合グリコシル化のためのグリコシル化能を有する宿主細胞におけるタンパク質の産生を必要としない点で有利である。用いるカップリング法に依存して、糖(糖類)を、(a)アルギニンおよびヒスチジン、(b)遊離カルボキシル基、(c)システインの一部のような遊離スルフヒドリル基、(d)セリン、トレオニンまたはヒドロキシプロリンの一部のような遊離ヒドロキシル基、(e)フェニルアラニン、チロシン、またはトリプトランの一部のような芳香族性残基、または(f)グルタミンのアミド基に結合させることができる。これらの方法は、1987年9月11日刊行のWO87/05330およびAplin and Wriston, 1981, CRC Crit. Rev. Biochem., pp. 259−306に記載される。 Another means of increasing the number of carbohydrate moieties on the antibody is by chemical or enzymatic coupling of glycosides to the protein. These methods are advantageous in that they do not require production of the protein in a host cell that has glycosylation capabilities for N- and O-linked glycosylation. Depending on the coupling method used, the sugar (sugar) can be converted to (a) arginine and histidine, (b) a free carboxyl group, (c) a free sulfhydryl group such as part of cysteine, (d) serine, threonine or It can be attached to a free hydroxyl group such as part of hydroxyproline, (e) an aromatic residue such as phenylalanine, tyrosine, or part of triptolan, or (f) the amide group of glutamine. These methods are described in WO 87/05330 published September 11, 1987 and Aplin and Wriston, 1981, CRC Crit. Rev. Biochem., Pp. 259-306.
出発抗体上に存在する炭水化物部分の除去を、化学的または酵素的に達成することができる。化学的脱グリコシル化は、トリフルオロメタンスルホン酸化合物、または等価化合物へのタンパク質の暴露を必要とする。この処理により、結果として、架橋している糖(N−アセチルグルコサミンまたはN−アセチルガラクトサミン)を除くほとんどまたは全ての糖鎖が切断されるが、一方、ポリペプチドは無傷のままである。化学的脱グリコシル化は、Hakimuddin et al., 1987, Arch. Biochem. Biophys. 259:52、およびEdge et al., 1981, Anal. Biochem. 118:131に記載される。ポリペプチド上の炭水化物部分の酵素的切断は、Thotakura et al., 1987, Meth. Enzymol. 138:350に記載の通り、様々なエンド−およびエキソ−グリコシダーゼの使用により達成され得る。可能性のあるグリコシル化部位でのグリコシル化は、Duskin et al., 1982, J. Biol. Chem. 257:3105に記載の通り、ツニカマイシン化合物の使用により阻止することができる。ツニカマイシンは、タンパク質−N−グリコシド結合の形成を妨げる。 Removal of carbohydrate moieties present on the starting antibody can be accomplished chemically or enzymatically. Chemical deglycosylation requires exposure of the protein to a trifluoromethanesulfonic acid compound, or equivalent compound. This treatment results in the cleavage of most or all sugar chains except the cross-linked sugar (N-acetylglucosamine or N-acetylgalactosamine), while the polypeptide remains intact. Chemical deglycosylation is described in Hakimuddin et al., 1987, Arch. Biochem. Biophys. 259: 52, and Edge et al., 1981, Anal. Biochem. 118: 131. Enzymatic cleavage of the carbohydrate moiety on the polypeptide can be accomplished by the use of various endo- and exo-glycosidases as described in Thotakura et al., 1987, Meth. Enzymol. 138: 350. Glycosylation at potential glycosylation sites can be blocked by the use of tunicamycin compounds as described in Duskin et al., 1982, J. Biol. Chem. 257: 3105. Tunicamycin prevents the formation of protein-N-glycoside bonds.
抗体の共有結合修飾の他のタイプは、米国特許第4,640,835号;同第4,496,689号;同第4,301,144号;同第4,670,417号;同第4,791,192号または同第4,179,337号に記載の方法で、抗体を、ポリエチレングリコール、ポリプロピレングリコールまたはポリオキシアルキレンのような様々なポリオールを含むが、これらに限定されない様々な非タンパク性ポリマーに結合することを含む。さらに、当技術分野で公知の通り、アミノ酸置換を、PEGのようなポリマーの付加を促進するために抗体内の様々な部位に行うことができる。例えば、米国特許公開番号2005/0114037(参照によりその全体が本明細書中に包含される)を参照のこと。 Other types of covalent modification of antibodies are described in US Pat. Nos. 4,640,835; 4,496,689; 4,301,144; 4,670,417; In the method described in US Pat. No. 4,791,192 or US Pat. No. 4,179,337, the antibody can be prepared in various non-limiting ways including, but not limited to, various polyols such as polyethylene glycol, polypropylene glycol or polyoxyalkylene. Including binding to a proteinaceous polymer. In addition, as is known in the art, amino acid substitutions can be made at various sites within the antibody to facilitate the addition of polymers such as PEG. See, eg, US Patent Publication No. 2005/0114037, which is hereby incorporated by reference in its entirety.
標識抗体
いくつかの態様において、本発明の抗体の共有結合修飾は、1個以上の標識の付加を含む。いくつかの場合において、これらは、抗体融合体と見なされる。
Labeled antibodies In some embodiments, the covalent modification of the antibodies of the invention involves the addition of one or more labels. In some cases, these are considered antibody fusions.
用語“標識基”は、何れかの検出可能な標識を意味する。いくつかの態様において、標識基を、可能性のある立体障害を減じるために様々な長さのスペーサーアームを介して抗体と結合させる。タンパク質を標識するための多様な方法が、当技術分野で公知であり、本発明の実施に用いられ得る。 The term “labeling group” means any detectable label. In some embodiments, a labeling group is attached to the antibody via spacer arms of various lengths to reduce potential steric hindrance. Various methods for labeling proteins are known in the art and can be used in the practice of the present invention.
一般的に、標識は、それらが検出される分析に依存して様々なクラスに分類される:a)放射性同位体または重同位体であり得るアイソトープ標識;b)磁気標識(例えば、磁性粒子);c)レドックス活性部分;d)光学色素;酵素群(例えば、西洋わさびペルオキシダーゼ、β−ガラクトシダーゼ、ルシフェラーゼ、アルカリホスファターゼ);e)ビオチン化基;および、f)二次レポーターにより認識される所定のポリペプチドエピトープ(例えば、ロイシンジッパー塩基対配列、二次抗体の結合部位、金属結合ドメイン、エピトープタグなど)。いくつかの態様において、標識基を、可能性のある立体障害を減じるために様々な長さのスペーサーアームを介して抗体と結合させる。タンパク質を標識するための多様な方法が、当技術分野で公知であり、本発明の実施において用いられ得る。 In general, labels are classified into various classes depending on the analysis in which they are detected: a) isotope labels that can be radioisotopes or heavy isotopes; b) magnetic labels (eg, magnetic particles) C) a redox active moiety; d) an optical dye; an enzyme group (eg, horseradish peroxidase, β-galactosidase, luciferase, alkaline phosphatase); e) a biotinylated group; and f) a predetermined reporter recognized by a secondary reporter. Polypeptide epitopes (eg, leucine zipper base pair sequences, secondary antibody binding sites, metal binding domains, epitope tags, etc.). In some embodiments, a labeling group is attached to the antibody via spacer arms of various lengths to reduce potential steric hindrance. A variety of methods for labeling proteins are known in the art and can be used in the practice of the invention.
特定の標識は、発色団、蛍光体およびフルオロフォアを含むが、これらに限定されない光学色素を含み、多くの例において特に後者である。フルオロフォアは、“小分子”蛍光物質、またはタンパク性蛍光物質のどちらかであり得る。 Particular labels include optical dyes, including but not limited to chromophores, fluorophores and fluorophores, and in many instances are the latter in particular. Fluorophores can be either “small molecule” phosphors or proteinaceous phosphors.
“蛍光標識”は、その固有の蛍光特性により検出され得る何れかの分子を意味する。適する蛍光標識には、フルオレセイン、ローダミン、テトラメチルローダミン、エオシン、エリスロシン、クマリン、メチル−クマリン、ピレン、マラカイトグリーン(Malacite green)、スチルベン、黄色蛍光色素(Lucifer Yellow)、Cascade BlueJ、テキサスレッド、IAEDANS、EDANS、BODIPY FL、LC Red 640、Cy5、Cy5.5、LC Red 705、Oregon green、Alexa−Fluor色素(Alexa Fluor 350、Alexa Fluor 430、Alexa Fluor 488、Alexa Fluor 546、Alexa Fluor 568、Alexa Fluor 594、Alexa Fluor 633、Alexa Fluor 660、Alexa Fluor 680)、Cascade Blue、Cascade YellowおよびR−フィコエリトリン(PE)(Molecular Probes, Eugene, OR)、FITC、ローダミン、およびテキサスレッド(Pierce, Rockford, IL)、Cy5、Cy5.5、Cy7(Amersham Life Science, Pittsburgh, PA)が含まれるが、それらに限定されない。適するフルオロフォアを含む光学色素は、Richard P. HauglandのMolecular Probes Handbook(参照により本明細書中に明示的に包含される)に記載される。
“Fluorescent label” means any molecule that can be detected by its inherent fluorescent properties. Suitable fluorescent labels include fluorescein, rhodamine, tetramethylrhodamine, eosin, erythrosine, coumarin, methyl-coumarin, pyrene, malacite green, stilbene, yellow fluorescent dye (Lucifer Yellow), Cascade BlueJ, Texas Red, IAEDANS , EDANS, BODIPY FL, LC Red 640, Cy5, Cy5.5, LC Red 705, Oregon green, Alexa-Fluor dye (
適するタンパク性蛍光標識にはまた、ウミシイタケ(Renilla)種、ウミエラ(Ptilosarcus)種、またはオワンクラゲ(Aequorea)種のGFPを含む緑色蛍光タンパク質(Chalfie et al., 1994, Science 263:802−805)、EGFP(Clontech Laboratories, Inc., Genbank受託番号U55762)、青色蛍光タンパク質(BFP、Quantum Biotechnologies, Inc. 1801 de Maisonneuve Blvd. West, 8th Floor, Montreal, Quebec, Canada H3H 1J9;Stauber, 1998, Biotechniques 24:462−471;Heim et al., 1996, Curr. Biol. 6:178−182)、増強黄色蛍光タンパク質(EYFP、Clontech Laboratories, Inc.)、ルシフェラーゼ(Ichiki et al., 1993, J. Immunol. 150:5408−5417)、β−ガラクトシダーゼ(Nolan et al., 1988, Proc. Natl. Acad. Sci. U.S.A. 85:2603−2607)およびウミシイタケ(WO92/15673、WO95/07463、WO98/14605、WO98/26277、WO99/49019、米国特許番号第5292658号、同第5418155号、同第5683888号、同第5741668号、同第5777079号、同第5804387号、同第5874304号、同第5876995号、同第5925558号)が含まれるが、それらに限定されない。上記の引用文献は全て、参照により本明細書中に明示的に包含される。 Suitable proteinaceous fluorescent labels also include green fluorescent proteins (Chalfie et al., 1994, Science 263: 802-805), including Renilla, Ptilosarcus, or Aequorea GFP. EGFP (Clontech Laboratories, Inc., Genbank accession number U55762), blue fluorescent protein (BFP, Quantum Biotechnologies, Inc. 1801 de Maisonneuve Blvd. West, 8th Floor, Montreal, Quebec, Canada H3H 1J9; Stauber, 1998, Biotechniques 24: 462-471; Heim et al., 1996, Curr. Biol. 6: 178-182), enhanced yellow fluorescent protein (EYFP, Clontech Laboratories, Inc.), luciferase (Ichiki et al., 1993, J. Immunol. 150). : 5408-5417), β-galactosidase (Nolan et al., 1988, Proc. Natl. Acad. Sci. USA 85: 2603-2607) and Renilla (WO92 / 15673, WO95 / 07463, WO98 / 14605, WO 98/26277, WO 99/49019, U.S. Pat.Nos. 5,292,658, 5,418,155, 5,683,888, 5,741,668, 5,777,079, 5,804,387, 5,874,304, 5,876,995, No. 5925558), but is not limited thereto. All of the above cited references are expressly incorporated herein by reference.
任意の変異体において、抗体とは、認識された免疫グロブリン遺伝子の全てまたは一部により実質的にコードされる1個以上のポリペプチドからなるタンパク質を意味し得る。例えばヒトにおいて認識された免疫グロブリン遺伝子には、無数の可変領域遺伝子、ならびに定常領域遺伝子である、IgM、IgD、IgG(IgG1、IgG2、IgG3およびIgG4)、IgE、およびIgA(IgA1およびIgA2)イソ型それぞれによりコードされるミュー(μ)、デルタ(δ)、ガンマ(γ)、シグマ(σ)およびアルファ(α)を共に含む、カッパ(κ)、ラムダ(λ)および重鎖遺伝子領域が含まれる。本明細書中、抗体は、全長抗体および抗体断片を含むことを意味し、何れかの生物由来の天然抗体、改変された抗体、または実験目的、治療目的または他の目的で組み換え的に作製された抗体を意味し得る。 In any variant, an antibody can refer to a protein consisting of one or more polypeptides substantially encoded by all or part of a recognized immunoglobulin gene. For example, immunoglobulin genes recognized in humans include the myriad variable region genes and constant region genes, IgM, IgD, IgG (IgG1, IgG2, IgG3 and IgG4), IgE, and IgA (IgA1 and IgA2) isoforms. Includes kappa (κ), lambda (λ) and heavy chain gene regions, including mu (μ), delta (δ), gamma (γ), sigma (σ) and alpha (α) encoded by each type It is. As used herein, antibody is meant to include full-length antibodies and antibody fragments, natural antibodies from any organism, modified antibodies, or recombinantly produced for experimental, therapeutic or other purposes. Antibody may mean.
Fc変異体は、親Fcポリペプチドと比較して1個以上のアミノ酸修飾を含み、ここで、該アミノ酸修飾(複数可)は、1個以上の最適化特性を提供する。本発明のFc変異体は、少なくとも1個のアミノ酸修飾によりその親IgGと異なるアミノ酸配列である。故に、本発明のFc変異体は、親Fcポリペプチドと比較して少なくとも1個のアミノ酸修飾を有する。あるいは、本発明のFc変異体は、親Fcポリペプチドと比較して2個以上のアミノ酸修飾、例えば約1個ないし5個のアミノ酸修飾、好ましくは約1個ないし10個のアミノ酸修飾、最も好ましくは約1個ないし約5個のアミノ酸修飾を有し得る。故に、Fc変異体の配列および親Fcポリペプチドの配列は、実質的に相同性である。例えば、本明細書中、変異体Fcの変異体配列は、親Fc変異体配列と約80%の相同性、好ましくは少なくとも約90%の相同性、最も好ましくは少なくとも約95%の相同性を有し得る。修飾を、分子生物学を用いて遺伝子組み換え的に行うか、または酵素的または化学的に行うことができる。 Fc variants contain one or more amino acid modifications compared to the parent Fc polypeptide, wherein the amino acid modification (s) provide one or more optimization properties. The Fc variants of the present invention are amino acid sequences that differ from their parent IgG by at least one amino acid modification. Thus, the Fc variants of the present invention have at least one amino acid modification compared to the parent Fc polypeptide. Alternatively, the Fc variants of the present invention have 2 or more amino acid modifications, such as about 1 to 5 amino acid modifications, preferably about 1 to 10 amino acid modifications, most preferably compared to the parent Fc polypeptide. Can have from about 1 to about 5 amino acid modifications. Thus, the sequence of the Fc variant and the sequence of the parent Fc polypeptide are substantially homologous. For example, herein, a variant Fc variant sequence has about 80% homology with the parent Fc variant sequence, preferably at least about 90% homology, most preferably at least about 95% homology. Can have. Modifications can be made genetically using molecular biology, or enzymatically or chemically.
本発明のFc変異体は、それらを構成するアミノ酸修飾に従って定義される。故に、例えばI332Eは、親Fcポリペプチドと比較してI332E置換を含むFc変異体である。同様に、S239D/A330L/I332Eは、親Fcポリペプチドと比較してS239D、A330LおよびI332E置換を含むFc変異体を定義する。置換が供される順序は任意であり、すなわち、例えば、S239D/A330L/I332Eは、S239D/I332E/A330Lなどと同じFc変異体であることが特記される。本発明で検討する全ての位置について、番号付けは、EU indexまたはEU番号付けスキームに従う(Kabat et al., 1991, Sequences of Proteins of Immunological Interest, 5th Ed., United States Public Health Service, National Institutes of Health, Bethesda、参照によりその全体が本明細書中に包含される)。EU indexまたはKabatに記載のEU indexまたはEU番号付けスキームとは、EU抗体の番号付けを意味する(Edelman et al., 1969, Proc Natl Acad Sci USA 63:78−85、参照によりその全体が本明細書中に包含される)。 The Fc variants of the present invention are defined according to the amino acid modifications that constitute them. Thus, for example, I332E is an Fc variant containing an I332E substitution compared to the parent Fc polypeptide. Similarly, S239D / A330L / I332E defines Fc variants that contain S239D, A330L and I332E substitutions compared to the parent Fc polypeptide. It is noted that the order in which substitutions are provided is arbitrary, ie, for example, S239D / A330L / I332E is the same Fc variant as S239D / I332E / A330L and the like. For all positions considered in the present invention, the numbering follows the EU index or EU numbering scheme (Kabat et al., 1991, Sequences of Proteins of Immunological Interest, 5th Ed., United States Public Health Service, National Institutes of Health, Bethesda, which is hereby incorporated in its entirety by reference). EU index or EU numbering scheme as described in EU index or Kabat means EU antibody numbering (Edelman et al., 1969, Proc Natl Acad Sci USA 63: 78-85, which is incorporated herein by reference in its entirety. Included in the specification).
本発明のFc変異体は、何らかの生物、好ましくはヒトを含むがそれに限定されない哺乳動物、マウスおよびラットを含むがそれらに限定されないげっ歯動物、ウサギおよび野ウサギを含むがそれらに限定されないウサギ目(lagomorpha)、ラクダ、ラマおよびヒトコブラクダを含むがそれらに限定されないラクダ科(camelidae)、ならびに原猿(Prosimian)、広猿類(Platyrrhini)(新世界サル)、オナガザル上科(Cercopithecoidea)(旧世界サル)、ならびにギボンズおよび小型および大型類人猿を含むヒト上科を含むがそれらに限定されない非ヒト霊長動物由来の遺伝子により実質的にコードされ得る。最も好ましい態様において、本発明のFc変異体は、実質的にヒトのものである。 Fc variants of the present invention include Rabbits including but not limited to rodents, rabbits and hares including but not limited to any organism, preferably including mammals, mice and rats, including but not limited to humans ( lagomorpha), including but not limited to camels, llamas and dromedaries, as well as Prosimian, Platyrrhini (New World monkey), Cercopithecoidea (Old World monkey) And can be substantially encoded by genes derived from non-human primates including but not limited to Gibbons and human superfamily including small and large apes. In the most preferred embodiments, the Fc variants of the present invention are substantially human.
親Fcポリペプチドは、抗体であり得る。親抗体は、例えば遺伝子組み換えマウス(Bruggemann et al., 1997, Curr Opin Biotechnol 8:455−458、参照によりその全体が本明細書中に包含される)または選択方法と一体となったヒト抗体ライブラリー(Griffiths et al., 1998, Curr Opin Biotechnol 9:102−108、参照によりその全体が本明細書中に包含される)を用いて得られる、完全長ヒト抗体であり得る。親抗体は、天然に存在する必要はない。例えば、親抗体は、キメラ抗体およびヒト化抗体(Clark, 2000, Immunol Today 21:397−402、参照によりその全体が本明細書中に包含される)を含むがそれらに限定されない遺伝子組み換えにより作製された抗体であり得る。親抗体は、1個以上の天然抗体遺伝子によって実質的にコードされる遺伝子組み換え的に作製された抗体変異体であり得る。1つの態様において、親抗体は、当技術分野で公知の通り、成熟した親和性を有する。あるいは、抗体は、いくつかの他の方法で、例えば2003年3月3日出願のUSSN10/339788(参照によりその全体が本明細書中に包含される)に記載の通りに修飾されている。
The parent Fc polypeptide can be an antibody. The parent antibody can be, for example, a transgenic mouse (Bruggemann et al., 1997, Curr Opin Biotechnol 8: 455-458, which is hereby incorporated by reference in its entirety) or a human antibody live integrated with a selection method. It can be a full-length human antibody obtained using a rally (Griffiths et al., 1998, Curr Opin Biotechnol 9: 102-108, which is hereby incorporated by reference in its entirety). The parent antibody need not be naturally occurring. For example, parent antibodies are produced by genetic recombination, including but not limited to chimeric antibodies and humanized antibodies (Clark, 2000, Immunol Today 21: 397-402, which is hereby incorporated by reference in its entirety). Antibody. The parent antibody can be a genetically engineered antibody variant substantially encoded by one or more natural antibody genes. In one embodiment, the parent antibody has mature affinity, as is known in the art. Alternatively, the antibody has been modified in several other ways, for example as described in
本発明のFc変異体は、何れかの抗体クラスに属する免疫グロブリン遺伝子により実質的にコードされ得る。好ましい態様において、本発明のFc変異体を、IgG1、IgG2、IgG3またはIgG4を含む抗体のIgGクラスに属する配列を含む抗体またはFc融合体に使用する。図3は、これらのヒトIgG配列のアライメントを提供する。別の態様において、本発明のFc変異体を、IgA(IgA1およびIgA2サブクラスを含む)、IgD、IgE、IgGまたはIgMの抗体クラスに属する配列を含む抗体またはFc融合体に使用する。本発明のFc変異体は、2個以上のタンパク質鎖を含み得る。すなわち、本発明を、モノマー、またはホモ−もしくはヘテロ−オリゴマーを含むオリゴマーである抗体またはFc融合体に用い得る。 The Fc variants of the present invention can be substantially encoded by immunoglobulin genes belonging to any antibody class. In a preferred embodiment, the Fc variants of the present invention are used for antibodies or Fc fusions comprising sequences belonging to the IgG class of antibodies, including IgG1, IgG2, IgG3 or IgG4. FIG. 3 provides an alignment of these human IgG sequences. In another embodiment, the Fc variants of the invention are used in antibodies or Fc fusions comprising sequences belonging to the IgA (including IgA1 and IgA2 subclass), IgD, IgE, IgG or IgM antibody classes. The Fc variants of the present invention may contain more than one protein chain. That is, the present invention may be used with antibodies or Fc fusions that are monomers or oligomers including homo- or hetero-oligomers.
当技術分野でよく知られている通り、ヒト集団には免疫グロブリン多型が存在する。Gm多型は、ヒトIgG1、IgG2およびIgG3分子のマーカーのためのG1m、G2mおよびG3mアロタイプ(Gmアロタイプは、ガンマ4鎖上に見出されていない)と称されるアロタイプ抗原決定基をコードするアレルを有するIGHG1、IGHG2およびIGHG3遺伝子により決定される。マーカーは、‘アロタイプ’および‘イソアロタイプ’に分類され得る。これらは、イソ型間の強い配列相同性に依存して異なる血清学的塩基に区別される。アロタイプは、Ig遺伝子のアレル形態により特定される抗原決定基である。アロタイプは、異なる個々の重鎖または軽鎖のアミノ酸配列中にわずかな差異を示す。単一のアミノ酸差異でも、アロタイプ決定基を形成し得るが、多くの場合、いくつかのアミノ酸置換が起こっている。アロタイプは、血清がアレルの差異のみを認識する、サブクラスのアレル間の配列の差異である。イソアロタイプは、1個以上の他のイソ型の非多型相同性領域と共有されるエピトープを生じる1個のイソ型におけるアレルであり、このため、血清は、関連アロタイプおよび関連相同性イソ型の両方と反応し得る(Clark, 1997, IgG effector mechanisms, Chem Immunol. 65:88−110; Gorman & Clark, 1990, Semin Immunol 2(6):457−66、両方とも参照によりその全体が本明細書中に包含される)。
As is well known in the art, immunoglobulin polymorphisms exist in the human population. The Gm polymorphism encodes an allotype antigenic determinant called G1m, G2m and G3m allotypes (Gm allotypes are not found on the
ヒト免疫グロブリンのアレル形態は、よく特徴付けられている(WHO Review of the notation for the allotypic and related markers of human immunoglobulins. J Immunogen 1976, 3: 357−362; WHO Review of the notation for the allotypic and related markers of human immunoglobulins. 1976, Eur. J. Immunol. 6, 599−601; Loghem E van, 1986, Allotypic markers, Monogr Allergy 19: 40−51、全て参照によりその全体が本明細書中に包含される)。さらに、他の多型が特徴付けられている(Kim et al., 2001, J. Mol. Evol. 54:1−9、参照によりその全体が本明細書中に包含される)。現在、18個のGmアロタイプが知られている:G1m(1、2、3、17)またはG1m(a、x、f、z)、G2m(23)またはG2m(n)、G3m(5、6、10、11、13、14、15、16、21、24、26、27、28)またはG3m(b1、c3、b5、b0、b3、b4、s、t、g1、c5、u、v、g5)(Lefranc, et al., The human IgG subclasses: molecular analysis of structure, function and regulation. Pergamon, Oxford, pp. 43−78 (1990); Lefranc, G. et al., 1979, Hum. Genet.: 50, 199−211、両方とも参照によりその全体が本明細書中に包含される)。固定された組み合わせで遺伝するアロタイプは、Gmハプロタイプと称される。 The allelic form of human immunoglobulin is well characterized (WHO Review of the notation for the allotypic and related markers of human immunoglobulins. J Immunogen 1976, 3: 357-362; WHO Review of the notation for the allotypic and related 1976, Eur. J. Immunol. 6, 599-601; Loghem E van, 1986, Allotypic markers, Monogr Allergy 19: 40-51, all incorporated herein by reference in their entirety. ). In addition, other polymorphisms have been characterized (Kim et al., 2001, J. Mol. Evol. 54: 1-9, which is hereby incorporated by reference in its entirety). Currently, 18 Gm allotypes are known: G1m (1, 2, 3, 17) or G1m (a, x, f, z), G2m (23) or G2m (n), G3m (5, 6 10, 11, 13, 14, 15, 16, 21, 24, 26, 27, 28) or G3m (b1, c3, b5, b0, b3, b4, s, t, g1, c5, u, v, g5) (Lefranc, et al., The human IgG subclasses: molecular analysis of structure, function and regulation. Pergamon, Oxford, pp. 43-78 (1990); Lefranc, G. et al., 1979, Hum. Genet. : 50, 199-211, both of which are incorporated herein by reference in their entirety). Allotypes inherited in a fixed combination are called Gm haplotypes.
図4は、位置および関連アミノ酸置換を示すヒトIgG1のガンマ1鎖のアロタイプおよびイソアロタイプを示す(Gorman & Clark, 1990, Semin Immunol 2(6):457−66、参照によりその全体が本明細書中に包含される)。比較のため、ヒトIgG2、IgG3およびIgG4ガンマ鎖中の等価な位置に見出されるアミノ酸も示す。
FIG. 4 shows allotypes and isoallotypes of the
本発明のFc変異体は、何れかの免疫グロブリン遺伝子の何れかのアロタイプまたはイソアロタイプにより実質的にコードされ得る。好ましい態様において、本発明のFc変異体は、G1m(1)、G1m(2)、G1m(3)、G1m(17)、nG1m(1)、nG1m(2)、および/またはnG1m(17)に分類されるIgG1配列を含む抗体またはFc融合体に用いられる。故に、IgG1イソ型において、本発明のFc変異体には、214位にLys(G1m(17))またはArg(G1m(3))、431位にAsp356/Leu358(G1m(1))もしくはGlu356/Met358(nG1m(1))、および/またはGly(G1m(2))もしくはAla(nG1m(2))が含まれる。
The Fc variants of the present invention can be substantially encoded by any allotype or isoallotype of any immunoglobulin gene. In a preferred embodiment, the Fc variants of the present invention are G1m (1), G1m (2), G1m (3), G1m (17), nG1m (1), nG1m (2), and / or nG1m (17). Used for antibodies or Fc fusions containing IgG1 sequences to be classified. Therefore, in the IgG1 isoform, the Fc variants of the present invention include Lys (G1m (17)) or Arg (G1 m (3)) at
最も好ましい態様において、本発明のFc変異体は、ヒトIgG配列に基づき、そのためヒトIgG配列は、他の配列が比較される、他の生物、例えばげっ歯動物および霊長類由来の配列を含むが、それらに限定されない“ベース”配列として用いられる。Fc変異体はまた、IgA、IgE、IgD、IgMなどのような他の免疫グロブリンクラス由来の配列を含み得る。本発明のFc変異体は、ある親IgGに照らして製造されるが、該変異体は、別の、第二の親IgGに照らして製造または“変換”され得ることが考慮される。これは、一般的に、第一と第二のIgG配列間の配列または構造同一性に基づき、第一と第二のIgG間の“等価”または“対応する”残基および置換基を決定することにより行われる。相同性を確立するために、本明細書に概説する第一のIgGのアミノ酸配列を、第二のIgGの配列と直接比較する。アライメントを維持するために必要な挿入および欠失を考慮し(すなわち、任意の欠失および挿入による保存残基の除去を避けて)、当技術分野で公知の1個以上の相同性アライメントプログラムを用いて(例えば、種間で保存された残基を用いて)配列をアライメント後、第一のFc変異体の初めの配列において特定のアミノ酸と等価の残基が定義される。保存残基のアライメントは、好ましくはかかる残基の100%を保存すべきである。しかしながら、保存残基の75%以上またはわずか50%程度のアライメントも、等価残基を定義するのに適する。等価残基はまた、構造が決定されているIgGの三次構造レベルで、第一と第二のIgG間の構造的相同性を決定することにより定義され得る。この場合に、等価残基は、親または前駆体の特定のアミノ酸残基の2個以上の主鎖原子(NとN、CAとCA、CとCおよびOとO)の原子座標が、アライメント後、約0.13nm以内、好ましくは約0.1nmであると定義される。アライメントは、ベストモデルが、タンパク質の非水素タンパク質原子の原子座標の最大重複を与えるように方向および位置付けされた後、達成される。等価または対応残基をどのように決定するかに関わらず、かつIgGが作製される親IgGの同一性に関わらず、伝えられるべきであるとされていることは、本発明により見出されたFc変異体を、重要な配列またはFc変異体と構造的相同性を有する何れかの第二の親IgGに改変することができることである。故に、例えば、変異体抗体を、上記の方法または等価残基を決定するための他の方法を用いることにより作製するとき(ここで、親抗体はヒトIgG1である。)、変異体抗体は、異なる抗原を結合する別のIgG1親抗体、ヒトIgG2親抗体、ヒトIgA親抗体、マウスIgG2aまたはIgG2b親抗体などに改変され得る。さらに、上記の通り、親Fc変異体においては、本発明のFc変異体を他の親IgGに転換する能力に影響しない。 In a most preferred embodiment, the Fc variants of the present invention are based on human IgG sequences, so that human IgG sequences include sequences from other organisms, such as rodents and primates, to which other sequences are compared. , But not limited to, used as a “base” sequence. Fc variants may also include sequences from other immunoglobulin classes such as IgA, IgE, IgD, IgM and the like. It is contemplated that the Fc variants of the present invention are produced in the context of one parent IgG, but the variant may be produced or “converted” in the context of another, second parent IgG. This generally determines the “equivalent” or “corresponding” residues and substituents between the first and second IgG based on the sequence or structural identity between the first and second IgG sequences. Is done. In order to establish homology, the amino acid sequence of the first IgG outlined herein is directly compared to the sequence of the second IgG. One or more homology alignment programs known in the art, taking into account the insertions and deletions necessary to maintain alignment (ie, avoiding removal of conserved residues by any deletions and insertions) Using (eg, using residues conserved between species), after aligning the sequence, residues equivalent to a particular amino acid are defined in the first sequence of the first Fc variant. Conserved residue alignments should preferably conserve 100% of such residues. However, alignments of more than 75% or as little as 50% of conserved residues are also suitable for defining equivalent residues. Equivalent residues can also be defined by determining the structural homology between the first and second IgG at the tertiary structure level of the IgG whose structure has been determined. In this case, the equivalent residues are those in which the atomic coordinates of two or more main chain atoms (N and N, CA and CA, C and C, and O and O) of a specific amino acid residue of the parent or precursor are aligned. Later, it is defined to be within about 0.13 nm, preferably about 0.1 nm. Alignment is achieved after the best model is oriented and positioned to give maximum overlap of atomic coordinates of non-hydrogen protein atoms of the protein. It has been found by the present invention that it should be conveyed regardless of how equivalent or corresponding residues are determined and regardless of the identity of the parent IgG from which the IgG is made. The Fc variant can be modified to any second parent IgG that has structural homology with the critical sequence or Fc variant. Thus, for example, when a variant antibody is made by using the methods described above or other methods for determining equivalent residues (where the parent antibody is human IgG1), the variant antibody is: It can be modified to another IgG1 parent antibody that binds a different antigen, a human IgG2 parent antibody, a human IgA parent antibody, a mouse IgG2a or IgG2b parent antibody, and the like. Furthermore, as described above, the parent Fc variant does not affect the ability to convert the Fc variant of the present invention into another parent IgG.
実質的には、下記の標的リストに属するタンパク質、サブユニット、ドメイン、モチーフおよび/またはエピトープが含まれるが、それらに限定されない全ての抗原は、本発明のFc変異体により標的とされ得る:17−IA、4−1BB、4Dc、6−ケト−PGF1a、8−イソ−PGF2a、8−オキソ−dG、A1 アデノシン受容体、A33、ACE、ACE−2、アクチビン、アクチビンA、アクチビンAB、アクチビンB、アクチビンC、アクチビンRIA、アクチビンRIA ALK−2、アクチビンRIB ALK−4、アクチビンRIIA、アクチビンRIIB、ADAM、ADAM10、ADAM12、ADAM15、ADAM17/TACE、ADAM8、ADAM9、ADAMTS、ADAMTS4、ADAMTS5、アドレシン、aFGF、ALCAM、ALK、ALK−1、ALK−7、アルファ−1−アンチトリプシン、アルファ−V/ベータ−1アンタゴニスト、ANG、Ang、APAF−1、APE、APJ、APP、APRIL、AR、ARC、ART、アルテミン、抗Id、ASPARTIC、心房性ナトリウム利尿因子、av/b3インテグリン、Axl、b2M、B7−1、B7−2、B7−H、B−リンパ球刺激因子(BlyS)、BACE、BACE−1、Bad、BAFF、BAFF−R、Bag−1、BAK、Bax、BCA−1、BCAM、Bcl、BCMA、BDNF、b−ECGF、bFGF、BID、Bik、BIM、BLC、BL−CAM、BLK、BMP、BMP−2 BMP−2a、BMP−3 オステオゲニン(Osteogenin)、BMP−4 BMP−2b、BMP−5、BMP−6 Vgr−1、BMP−7(OP−1)、BMP−8(BMP−8a、OP−2)、BMPR、BMPR−IA(ALK−3)、BMPR−IB(ALK−6)、BRK−2、RPK−1、BMPR−II(BRK−3)、BMP、b−NGF、BOK、ボンベシン、骨由来神経栄養因子、BPDE、BPDE−DNA、BTC、補体因子3(C3)、C3a、C4、C5、C5a、C10、CA125、CAD−8、カルシトニン、cAMP、癌胎児性抗原(CEA)、癌関連抗原、カテプシンA、カテプシンB、カテプシンC/DPPI、カテプシンD、カテプシンE、カテプシンH、カテプシンL、カテプシンO、カテプシンS、カテプシンV、カテプシンX/Z/P、CBL、CCI、CCK2、CCL、CCL1、CCL11、CCL12、CCL13、CCL14、CCL15、CCL16、CCL17、CCL18、CCL19、CCL2、CCL20、CCL21、CCL22、CCL23、CCL24、CCL25、CCL26、CCL27、CCL28、CCL3、CCL4、CCL5、CCL6、CCL7、CCL8、CCL9/10、CCR、CCR1、CCR10、CCR10、CCR2、CCR3、CCR4、CCR5、CCR6、CCR7、CCR8、CCR9、CD1、CD2、CD3、CD3E、CD4、CD5、CD6、CD7、CD8、CD10、CD11a、CD11b、CD11c、CD13、CD14、CD15、CD16、CD18、CD19、CD20、CD21、CD22、CD23、CD25、CD27L、CD28、CD29、CD30、CD30L、CD32、CD33(p67タンパク質)、CD34、CD38、CD40、 Virtually all antigens, including but not limited to proteins, subunits, domains, motifs and / or epitopes belonging to the following target list can be targeted by the Fc variants of the present invention: 17 -IA, 4-1BB, 4Dc, 6-keto-PGF1a, 8-iso-PGF2a, 8-oxo-dG, A1 adenosine receptor, A33, ACE, ACE-2, activin, activin A, activin AB, activin B , Activin C, Activin RIA, Activin RIA ALK-2, Activin RIB ALK-4, Activin RIIA, Activin RIIB, ADAM, ADAM10, ADAM12, ADAM15, ADAM17 / TACE, ADAM8, ADAM9, ADAMTS, ADAMTS4, ADAMTS5 Adressin, aFGF, ALCAM, ALK, ALK-1, ALK-7, alpha-1-antitrypsin, alpha-V / beta-1 antagonist, ANG, Ang, APAF-1, APE, APJ, APP, APRIL, AR, ARC, ART, Artemin, anti-Id, ASPARTIC, atrial natriuretic factor, av / b3 integrin, Axl, b2M, B7-1, B7-2, B7-H, B-lymphocyte stimulating factor (BlyS), BACE, BACE-1, Bad, BAFF, BAFF-R, Bag-1, BAK, Bax, BCA-1, BCAM, Bcl, BCMA, BDNF, b-ECGF, bFGF, BID, Bik, BIM, BLC, BL-CAM, BLK, BMP, BMP-2 BMP-2a, BMP-3 osteogenin ( Osteogenin), BMP-4 BMP-2b, BMP-5, BMP-6 Vgr-1, BMP-7 (OP-1), BMP-8 (BMP-8a, OP-2), BMPR, BMPR-IA (ALK) -3), BMPR-IB (ALK-6), BRK-2, RPK-1, BMPR-II (BRK-3), BMP, b-NGF, BOK, bombesin, bone-derived neurotrophic factor, BPDE, BPDE- DNA, BTC, complement factor 3 (C3), C3a, C4, C5, C5a, C10, CA125, CAD-8, calcitonin, cAMP, carcinoembryonic antigen (CEA), cancer-associated antigen, cathepsin A, cathepsin B, Cathepsin C / DPPI, Cathepsin D, Cathepsin E, Cathepsin H, Cathepsin L, Cathepsin O, Cathepsin S, Cathepsin V, Cathepsin X / Z / P, C L, CCI, CCK2, CCL, CCL1, CCL11, CCL12, CCL13, CCL14, CCL15, CCL16, CCL17, CCL18, CCL19, CCL2, CCL20, CCL21, CCL22, CCL23, CCL24, CCL25, CCL26, CCL27, CCL28, CCL3 CCL4, CCL5, CCL6, CCL7, CCL8, CCL9 / 10, CCR, CCR1, CCR10, CCR10, CCR2, CCR3, CCR4, CCR5, CCR6, CCR7, CCR8, CCR9, CD1, CD2, CD3, CD3E, CD4, CD5, CD6, CD7, CD8, CD10, CD11a, CD11b, CD11c, CD13, CD14, CD15, CD16, CD18, CD19, CD20, CD21, D22, CD23, CD25, CD27L, CD28, CD29, CD30, CD30L, CD32, CD33 (p67 protein), CD34, CD38, CD40,
CD40L、CD44、CD45、CD46、CD49a、CD52、CD54、CD55、CD56、CD61、CD64、CD66e、CD74、CD80(B7−1)、CD89、CD95、CD123、CD137、CD138、CD140a、CD146、CD147、CD148、CD152、CD164、CEACAM5、CFTR、cGMP、CINC、ボツリヌス菌毒素、ウェルシュ菌毒素、CKb8−1、CLC、CMV、CMV UL、CNTF、CNTN−1、COX、C−Ret、CRG−2、CT−1、CTACK、CTGF、CTLA−4、CX3CL1、CX3CR1、CXCL、CXCL1、CXCL2、CXCL3、CXCL4、CXCL5、CXCL6、CXCL7、CXCL8、CXCL9、CXCL10、CXCL11、CXCL12、CXCL13、CXCL14、CXCL15、CXCL16、CXCR、CXCR1、CXCR2、CXCR3、CXCR4、CXCR5、CXCR6、サイトケラチン腫瘍関連抗原、DAN、DCC、DcR3、DC−SIGN、補体制御因子(Decay accelerating factor)、des(1−3)−IGF−I(脳IGF−1)、Dhh、ジゴキシン、DNAM−1、Dnase、Dpp、DPPIV/CD26、Dtk、ECAD、EDA、EDA−A1、EDA−A2、EDAR、EGF、EGFR(ErbB−1)、EMA、EMMPRIN、ENA、エンドセリン受容体、エンケファリナーゼ、eNOS、Eot、エオタキシン1、EpCAM、エフリンB2/EphB4、EPO、ERCC、E−セレクチン、ET−1、ファクターIIa、ファクターVII、ファクターVIIIc、ファクターIX、線維芽細胞活性化タンパク質(FAP)、Fas、FcR1、FEN−1、フェリチン、FGF、FGF−19、FGF−2、FGF3、FGF−8、FGFR、FGFR−3、フィブリン、FL、FLIP、Flt−3、Flt−4、卵胞刺激ホルモン、フラクタルカイン、FZD1、FZD2、FZD3、FZD4、FZD5、FZD6、FZD7、FZD8、FZD9、FZD10、G250、Gas6、GCP−2、GCSF、GD2、GD3、GDF、GDF−1、GDF−3(Vgr−2)、GDF−5(BMP−14、CDMP−1)、GDF−6(BMP−13、CDMP−2)、GDF−7(BMP−12、CDMP−3)、GDF−8(ミオスタチン)、GDF−9、GDF−15(MIC−1)、GDNF、GDNF、GFAP、GFRa−1、GFR−アルファ1、GFR−アルファ2、GFR−アルファ3、GITR、グルカゴン、Glut4、糖タンパク質IIb/IIIa(GPIIb/IIIa)、GM−CSF、gp130、gp72、GRO、成長ホルモン放出因子、ハプテン(NP−capまたはNIP−cap)、 CD40L, CD44, CD45, CD46, CD49a, CD52, CD54, CD55, CD56, CD61, CD64, CD66e, CD74, CD80 (B7-1), CD89, CD95, CD123, CD137, CD138, CD140a, CD146, CD147, CD148 CD152, CD164, CEACAM5, CFTR, cGMP, CINC, Clostridium botulinum toxin, Clostridium perfringens toxin, CKb8-1, CLC, CMV, CMV UL, CNTF, CNTN-1, COX, C-Ret, CRG-2, CT- 1, CTACK, CTGF, CTLA-4, CX3CL1, CX3CR1, CXCL, CXCL1, CXCL2, CXCL3, CXCL4, CXCL5, CXCL6, CXCL7, CXCL8, CXCL9, CXC L10, CXCL11, CXCL12, CXCL13, CXCL14, CXCL15, CXCL16, CXCR, CXCR1, CXCR2, CXCR3, CXCR4, CXCR5, CXCR6, cytokeratin tumor-related antigen, DAN, DCC, DcR3, DC-SIGN, complement control factor accelerating factor), des (1-3) -IGF-I (brain IGF-1), Dhh, digoxin, DNAM-1, Dnase, Dpp, DPPIV / CD26, Dtk, ECAD, EDA, EDA-A1, EDA-A2 , EDAR, EGF, EGFR (ErbB-1), EMA, EMMPRIN, ENA, endothelin receptor, enkephalinase, eNOS, Eot, eotaxin 1, EpCAM, ephrin B2 / EphB4, EPO, ERCC, E-se Lectin, ET-1, factor IIa, factor VII, factor VIIIc, factor IX, fibroblast activation protein (FAP), Fas, FcR1, FEN-1, ferritin, FGF, FGF-19, FGF-2, FGF3, FGF-8, FGFR, FGFR-3, fibrin, FL, FLIP, Flt-3, Flt-4, follicle stimulating hormone, fractalkine, FZD1, FZD2, FZD3, FZD4, FZD5, FZD6, FZD7, FZD8, FZD9, FZD10 G250, Gas6, GCP-2, GCSF, GD2, GD3, GDF, GDF-1, GDF-3 (Vgr-2), GDF-5 (BMP-14, CDMP-1), GDF-6 (BMP-13) CDMP-2), GDF-7 (BMP-12, CDMP) 3), GDF-8 (myostatin), GDF-9, GDF-15 (MIC-1), GDNF, GDNF, GFAP, GFRa-1, GFR-alpha1, GFR-alpha2, GFR-alpha3, GITR, Glucagon, Glut4, glycoprotein IIb / IIIa (GPIIb / IIIa), GM-CSF, gp130, gp72, GRO, growth hormone releasing factor, hapten (NP-cap or NIP-cap),
HB−EGF、HCC、HCMV gBエンベロープ糖タンパク質、HCMV gHエンベロープ糖タンパク質、HCMV UL、造血成長因子(HGF)、Hep B gp120、ヘパラナーゼ、Her2、Her2/neu(ErbB−2)、Her3(ErbB−3)、Her4(ErbB−4)、単純ヘルペスウイルス(HSV) gB糖タンパク質、HSV gD糖タンパク質、HGFA、高分子量黒色腫関連抗原(HMW−MAA)、HIV gp120、HIV IIIB gp 120 V3ループ、HLA、HLA−DR、HM1.24、HMFG PEM、HRG、Hrk、ヒト心臓ミオシン、ヒトサイトメガロウイルス(HCMV)、ヒト成長ホルモン(HGH)、HVEM、I−309、IAP、ICAM、ICAM−1、ICAM−3、ICE、ICOS、IFNg、Ig、IgA受容体、IgE、IGF、IGF結合タンパク質、IGF−1R、IGFBP、IGF−I、IGF−II、IL、IL−1、IL−1R、IL−2、IL−2R、IL−4、IL−4R、IL−5、IL−5R、IL−6、IL−6R、IL−8、IL−9、IL−10、IL−12、IL−13、IL−15、IL−18、IL−18R、IL−23、インターフェロン(INF)−アルファ、INF−ベータ、INF−ガンマ、インヒビン、iNOS、インスリンA鎖、インスリンB鎖、インスリン様増殖因子1、インテグリンアルファ2、インテグリンアルファ3、インテグリンアルファ4、インテグリンアルファ4/ベータ1、インテグリンアルファ4/ベータ7、インテグリンアルファ5(アルファV)、インテグリンアルファ5/ベータ1、インテグリンアルファ5/ベータ3、インテグリンアルファ6、インテグリンベータ1、インテグリンベータ2、インターフェロンガンマ、IP−10、I−TAC、JE、カリクレイン2、カリクレイン5、カリクレイン6、カリクレイン11、カリクレイン12、カリクレイン14、カリクレイン15、カリクレインL1、カリクレインL2、カリクレインL3、カリクレインL4、KC、KDR、ケラチノサイト増殖因子(KGF)、ラミニン5、LAMP、LAP、LAP(TGF−1)、潜在的TGF−1、潜在的TGF−1 bp1、LBP、LDGF、LECT2、レフティ、ルイス−Y抗原、ルイス−Y関連抗原、LFA−1、LFA−3、Lfo、LIF、LIGHT、リポタンパク質、LIX、LKN、Lptn、L−セレクチン、LT−a、LT−b、LTB4、LTBP−1、肺表面、黄体形成ホルモン、リンホトキシンベータ受容体、Mac−1、MAdCAM、MAG、MAP2、MARC、MCAM、MCAM、MCK−2、MCP、M−CSF、MDC、Mer、METALLOPROTEASES、MGDF受容体、MGMT、MHC(HLA−DR)、MIF、MIG、MIP、MIP−1−アルファ、MK、MMAC1、MMP、MMP−1、MMP−10、MMP−11、MMP−12、MMP−13、 HB-EGF, HCC, HCMV gB envelope glycoprotein, HCMV gH envelope glycoprotein, HCMV UL, hematopoietic growth factor (HGF), Hep B gp120, heparanase, Her2, Her2 / neu (ErbB-2), Her3 (ErbB-3) ), Her4 (ErbB-4), herpes simplex virus (HSV) gB glycoprotein, HSV gD glycoprotein, HGFA, high molecular weight melanoma associated antigen (HMW-MAA), HIV gp120, HIV IIIB gp 120 V3 loop, HLA, HLA-DR, HM1.24, HMFG PEM, HRG, Hrk, human heart myosin, human cytomegalovirus (HCMV), human growth hormone (HGH), HVEM, I-309, IAP, ICAM, ICAM-1, ICAM -3, ICE, ICOS, IFNg, Ig, IgA receptor, IgE, IGF, IGF binding protein, IGF-1R, IGFBP, IGF-I, IGF-II, IL, IL-1, IL-1R, IL-2 IL-2R, IL-4, IL-4R, IL-5, IL-5R, IL-6, IL-6R, IL-8, IL-9, IL-10, IL-12, IL-13, IL -15, IL-18, IL-18R, IL-23, interferon (INF) -alpha, INF-beta, INF-gamma, inhibin, iNOS, insulin A chain, insulin B chain, insulin-like growth factor 1, integrin alpha 2, integrin alpha 3, integrin alpha 4, integrin alpha 4 / beta 1, integrin alpha 4 / beta 7, integrin Rufa 5 (alpha V), integrin alpha 5 / beta 1, integrin alpha 5 / beta 3, integrin alpha 6, integrin beta 1, integrin beta 2, interferon gamma, IP-10, I-TAC, JE, kallikrein 2, kallikrein 5, kallikrein 6, kallikrein 11, kallikrein 14, kallikrein 14, kallikrein L, kallikrein L2, kallikrein L3, kallikrein L4, KC, KDR, keratinocyte growth factor (KGF), laminin 5, LAMP, LAP, LAP (TGF) -1), potential TGF-1, potential TGF-1 bp1, LBP, LDGF, LECT2, lefti, Lewis-Y antigen, Lewis-Y related antigen, LFA-1, LFA-3, Lfo, LIF, IGHT, lipoprotein, LIX, LKN, Lptn, L-selectin, LT-a, LT-b, LTB4, LTBP-1, lung surface, luteinizing hormone, lymphotoxin beta receptor, Mac-1, MAdCAM, MAG , MAP2, MARC, MCAM, MCAM, MCK-2, MCP, M-CSF, MDC, Mer, METALLOPROTEASES, MGDF receptor, MGMT, MHC (HLA-DR), MIF, MIG, MIP, MIP-1-alpha, MK, MMAC1, MMP, MMP-1, MMP-10, MMP-11, MMP-12, MMP-13,
MMP−14、MMP−15、MMP−2、MMP−24、MMP−3、MMP−7、MMP−8、MMP−9、MPIF、Mpo、MSK、MSP、ムチン(Muc1)、MUC18、ミュラー管抑制物質、Mug、MuSK、NAIP、NAP、NCAD、N−カドヘリン、NCA 90、NCAM、NCAM、ネプリライシン、ニューロトロフィン−3,−4、または−6、ニュールツリン、神経成長因子(NGF)、NGFR、NGF−ベータ、nNOS、NO、NOS、Npn、NRG−3、NT、NTN、OB、OGG1、OPG、OPN、OSM、OX40L、OX40R、p150、p95、PADPr、副甲状腺ホルモン、PARC、PARP、PBR、PBSF、PCAD、P−Cadherin、PCNA、PDGF、PDGF、PDK−1、PECAM、PEM、PF4、PGE、PGF、PGI2、PGJ2、PIN、PLA2、胎盤性アルカリホスファターゼ(PLAP)、PlGF、PLP、PP14、プロインスリン、プロレラキシン、プロテインC、PS、PSA、PSCA、前立腺特異的膜抗原(PSMA)、PTEN、PTHrp、Ptk、PTN、R51、RANK、RANKL、RANTES、RANTES、レラキシンA鎖、レラキシンB鎖、レニン、呼吸器多核体ウイルス(RSV)F、RSV Fgp、Ret、リウマイド因子、RLIP76、RPA2、RSK、S100、SCF/KL、SDF−1、SERINE、血清アルブミン、sFRP−3、Shh、SIGIRR、SK−1、SLAM、SLPI、SMAC、SMDF、SMOH、SOD、SPARC、Stat、STEAP、STEAP−II、TACE、TACI、TAG−72(腫瘍関連糖タンパク質−72)、TARC、TCA−3、T細胞受容体(例えば、T細胞受容体アルファ/ベータ)、TdT、TECK、TEM1、TEM5、TEM7、TEM8、TERT、睾丸PLAP様アルカリホスファターゼ、TfR、TGF、TGF−アルファ、TGF−ベータ、TGF−ベータ Pan 特異的、TGF−ベータRI(ALK−5)、TGF−ベータRII、TGF−ベータRIIb、TGF−ベータRIII、TGF−ベータ1、TGF−ベータ2、TGF−ベータ3、TGF−ベータ4、TGF−ベータ5、トロンビン、胸腺Ck−1、甲状腺刺激ホルモン、Tie、TIMP、TIQ、組織因子、TMEFF2、Tmpo、TMPRSS2、TNF、TNF−アルファ、TNF−アルファベータ、TNF−ベータ2、TNFc、TNF−RI、TNF−RII、TNFRSF10A(TRAIL R1 Apo−2、DR4)、 MMP-14, MMP-15, MMP-2, MMP-24, MMP-3, MMP-7, MMP-8, MMP-9, MPIF, Mpo, MSK, MSP, mucin (Muc1), MUC18, Mueller tube suppression Substance, Mug, MuSK, NAIP, NAP, NCAD, N-cadherin, NCA 90, NCAM, NCAM, neprilysin, neurotrophin-3, -4, or -6, neurturin, nerve growth factor (NGF), NGFR, NGF -Beta, nNOS, NO, NOS, Npn, NRG-3, NT, NTN, OB, OGG1, OPG, OPN, OSM, OX40L, OX40R, p150, p95, PADPr, parathyroid hormone, PARC, PARP, PBR, PBSF , PCAD, P-Cadherin, PCNA, PDGF, PDGF, PDK-1, PECAM, PEM, PF4, PGE, PGF, PGI2, PGJ2, PIN, PLA2, placental alkaline phosphatase (PLAP), PlGF, PLP, PP14, proinsulin, prorelaxin, protein C, PS, PSA, PSCA, prostate specific membrane antigen (PSMA), PTEN, PTHrp, Ptk, PTN, R51, RANK, RANKL, RANTES, RANTES, relaxin A chain, relaxin B chain, renin, respiratory multinuclear virus (RSV) F, RSV Fgp, Ret, Riumide factor, RLIP76, RPA2, RSK, S100, SCF / KL, SDF-1, SERINE, serum albumin, sFRP-3, Shh, SIGIRR, SK-1, SLAM, SLPI, SMAC, SMDF , SMOH, SOD, SPARC, Stat, STEAP, STEAP-II, TACE, TACI, TAG-72 (tumor-associated glycoprotein-72), TARC, TCA-3, T cell receptor (eg, T cell receptor alpha / Beta), TdT, TECK, TEM1, TEM5, TEM7, TEM8, TERT, testicular PLAP-like alkaline phosphatase, TfR, TGF, TGF-alpha, TGF-beta, TGF-beta Pan specific, TGF-beta RI (ALK-5) ), TGF-beta RII, TGF-beta RIIb, TGF-beta RIII, TGF-beta 1, TGF-beta 2, TGF-beta 3, TGF-beta 4, TGF-beta 5, thrombin, thymus Ck-1, thyroid Stimulating hormone, Tie, TIMP, TIQ, group Factor, TMEFF2, Tmpo, TMPRSS2, TNF, TNF- alpha, TNF- alpha beta, TNF- beta 2, TNFc, TNF-RI, TNF-RII, TNFRSF10A (TRAIL R1 Apo-2, DR4),
TNFRSF10B(TRAIL R2 DR5、KILLER、TRICK−2A、TRICK−B)、TNFRSF10C(TRAIL R3 DcR1、LIT、TRID)、TNFRSF10D(TRAIL R4 DcR2、TRUNDD)、TNFRSF11A(RANK ODF R、TRANCE R)、TNFRSF11B(OPG OCIF、TR1)、TNFRSF12(TWEAK R FN14)、TNFRSF13B(TACI)、TNFRSF13C(BAFF R)、TNFRSF14(HVEM ATAR、HveA、LIGHT R、TR2)、TNFRSF16(NGFR p75NTR)、TNFRSF17(BCMA)、TNFRSF18(GITR AITR)、TNFRSF19(TROY TAJ、TRADE)、TNFRSF19L(RELT)、TNFRSF1A(TNF RI CD120a、p55−60)、TNFRSF1B(TNF RII CD120b、p75−80)、TNFRSF26(TNFRH3)、TNFRSF3(LTbR TNF RIII、TNFC R)、TNFRSF4(OX40 ACT35、TXGP1 R)、TNFRSF5(CD40 p50)、TNFRSF6(Fas Apo−1、APT1、CD95)、TNFRSF6B(DcR3 M68、TR6)、TNFRSF7(CD27)、TNFRSF8(CD30)、TNFRSF9(4−1BB CD137、ILA)、TNFRSF21(DR6)、TNFRSF22(DcTRAIL R2 TNFRH2)、TNFRST23(DcTRAIL R1 TNFRH1)、TNFRSF25(DR3 Apo−3、LARD、TR−3、TRAMP、WSL−1)、TNFSF10(TRAIL Apo−2リガンド、TL2)、TNFSF11(TRANCE/RANKリガンド ODF、OPGリガンド)、TNFSF12(TWEAK Apo−3リガンド、DR3リガンド)、TNFSF13(APRIL TALL2)、TNFSF13B(BAFF BLYS、TALL1、THANK、TNFSF20)、TNFSF14(LIGHT HVEMリガンド、LTg)、TNFSF15(TL1A/VEGI)、TNFSF18(GITRリガンド AITRリガンド、TL6)、TNFSF1A(TNF−a コネクチン、DIF、TNFSF2)、TNFSF1B(TNF−b LTa、TNFSF1)、TNFSF3(LTb TNFC、p33)、TNFSF4(OX40リガンド gp34、TXGP1)、TNFSF5(CD40リガンド CD154、gp39、HIGM1、IMD3、TRAP)、TNFSF6(Fasリガンド Apo−1リガンド、APT1リガンド)、TNFSF7(CD27リガンド CD70)、TNFSF8(CD30リガンド CD153)、TNFSF9(4−1BBリガンド CD137リガンド)、TP−1、t−PA、Tpo、TRAIL、TRAIL R、TRAIL−R1、TRAIL−R2、TRANCE、トランスフェリン受容体、TRF、Trk、TROP−2、TSG、TSLP、腫瘍関連抗原CA125、腫瘍関連抗原発現ルイスY関連炭水化物、TWEAK、TXB2、Ung、uPAR、uPAR−1、ウロキナーゼ、VCAM、VCAM−1、VECAD、VE−Cadherin、VE−cadherin−2、VEFGR−1(flt−1)、VEGF、VEGFR、VEGFR−3(flt−4)、VEGI、VIM、ウイルス抗原、VLA、VLA−1、VLA−4、VNRインテグリン、フォン・ヴィレブランド因子、WIF−1、WNT1、WNT2、WNT2B/13、WNT3、WNT3A、WNT4、WNT5A、WNT5B、WNT6、WNT7A、WNT7B、WNT8A、WNT8B、WNT9A、WNT9A、WNT9B、WNT10A、WNT10B、WNT11、WNT16、XCL1、XCL2、XCR1、XCR1、XEDAR、XIAP、XPD、ならびにホルモンおよび成長因子のための受容体。 TNFRSF10B (TRAIL R2 DR5, KILLER, TRICK-2A, TRICK-B), TNFRSF10C (TRAIL R3 DcR1, LIT, TRID), TNFRSF10D (TRAIL R4 DcR2, TRUNDD), TNFRSF11A (TNKSF11RS (TNKSF11A) OCIF, TR1), TNFRSF12 (TWEAK R FN14), TNFRSF13B (TACI), TNFRSF13C (BAFF R), TNFRSF14 (HVEM ATAR, HveA, LIGHT R, TR2), TNFRSF16 (NGFR T75RSR18F) AITR), TNFRSF19 (TROY TAJ, TRADE), NFRSF19L (RELT), TNFRSF1A (TNF RI CD120a, p55-60), TNFRSF1B (TNF RII CD120b, p75-80), TNFRSF26 (TNFRH3), TNFRSF3 (LTbR TNF4, TNF RIII, TNF RIII, TNFC4) , TNFRSF5 (CD40 p50), TNFRSF6 (Fas Apo-1, APT1, CD95), TNFRSF6B (DcR3 M68, TR6), TNFRSF7 (CD27), TNFRSF8 (CD30), TNFRSF9 (4-1RSDR6, IL1F6137R ), TNFRSF22 (DcTRAIL R2 TNFRH2), TNFRRST23 (DcTRAIL R1 TNFRH1) ), TNFRSF25 (DR3 Apo-3, LARD, TR-3, TRAMP, WSL-1), TNFSF10 (TRAIL Apo-2 ligand, TL2), TNFSF11 (TRANCE / RANK ligand ODF, OPG ligand), TNFSF12 (TWEAK Apo-) 3 ligands, DR3 ligands), TNFSF13 (APRIL TALL2), TNFSF13B (BAFF BLYS, TALL1, THANK, TNFSF20), TNFSF14 (LIGHT HVEM ligand, LTg), TNFSF15 (TL1A / VEGIT) , TNFSF1A (TNF-a connectin, DIF, TNFSF2), TNFSF1B (TNF-b LTa, TNFSF1), TNFSF3 (LTb TNFC, p33), TNFSF4 (OX40 ligand gp34, TXGP1), TNFSF5 (CD40 ligand CD154, gp39, HIGM1, IMD3, TRAP), TNFSF6 (Fas ligand Apo-1 ligand, APT1CD7, APT1CD7, APT1CD7) ), TNFSF8 (CD30 ligand CD153), TNFSF9 (4-1BB ligand CD137 ligand), TP-1, t-PA, Tpo, TRAIL, TRAIL R, TRAIL-R1, TRAIL-R2, TRANCE, transferrin receptor, TRF, Trk, TROP-2, TSG, TSLP, tumor associated antigen CA125, tumor associated antigen expressing Lewis Y related carbohydrate, TWEAK, TXB2, Ung, uP R, uPAR-1, urokinase, VCAM, VCAM-1, VECAD, VE-cadherin, VE-cadherin-2, VEFGR-1 (flt-1), VEGF, VEGFR, VEGFR-3 (flt-4), VEGI, VIM, viral antigen, VLA, VLA-1, VLA-4, VNR integrin, von Willebrand factor, WIF-1, WNT1, WNT2, WNT2B / 13, WNT3, WNT3A, WNT4, WNT5A, WNT5B, WNT6, WNT7A, WNT7B, WNT8A, WNT8B, WNT9A, WNT9A, WNT9B, WNT10A, WNT10B, WNT11, WNT16, XCL1, XCL2, XCR1, XCR1, XEDAR, XIAP, XPD, and hormones and growth factors Receptor for.
本発明は、様々な治療的に関連のある特性について最適化されるFc変異体を提供する。1個以上の最適化特性を示すように組み込まれるまたは予測されるFc変異体は、本明細書中、“最適化Fc変異体”と称される。最適化され得る特性には、FcγRに対する増大または減少した親和性が含まれるが、これらに限定されない。好ましい態様において、本発明のFc変異体は、ヒト活性化FcγR、好ましくはFcγRI、FcγRIIa、FcγRIIc、FcγRIIIaおよびFcγRIIIb、最も好ましくはFcγRIIIaに対して増加した親和性を有するように最適化される。別の好ましい態様において、Fc変異体は、ヒト阻害性受容体 FcγRIIbに対して減少した親和性を有するように最適化される。これらの好ましい態様は、例えばヒトにおける増大した治療特性を有するIgGポリペプチドを提供することが予想される。別の態様において、本発明のFc変異体は、FcγRI、FcγRIIa、FcγRIIb、FcγRIIc、FcγRIIIa、およびFcγRIIIbを含むが、これらに限定されないヒトFcγRに対する減少または低下した親和性を有するように最適化される。これらの態様は、ヒトにおける増強された治療特性、例えば減少したエフェクター機能および減少した毒性を有するIgGポリペプチドを提供することが予定される。他の態様において、本発明のFc変異体は、1種以上のFcγRに対して増大した親和性を提供するが、1個以上の他のFcγRに対して減少した親和性を提供する。例えば、本発明のFc変異体は、FcγRIIIaに対して増大した結合を有し得るが、FcγRIIbに対して減少した結合を有し得る。あるいは、本発明のFc変異体は、FcγRIIaおよびFcγRIに対して増大した結合を有し得るが、FcγRIIbに対して減少した結合を有し得る。さらに別の態様において、本発明のFc変異体は、FcγRIIbに対して増大した親和性を有し得るが、1個以上の活性化FcγRに対して減少した親和性を有し得る。 The present invention provides Fc variants that are optimized for a variety of therapeutically relevant properties. An Fc variant that is incorporated or predicted to exhibit one or more optimization properties is referred to herein as an “ optimized Fc variant ”. Properties that can be optimized include, but are not limited to, increased or decreased affinity for FcγR. In a preferred embodiment, the Fc variants of the invention are optimized to have increased affinity for human activated FcγR, preferably FcγRI, FcγRIIa, FcγRIIc, FcγRIIIa and FcγRIIIb, most preferably FcγRIIIa. In another preferred embodiment, the Fc variant is optimized to have reduced affinity for the human inhibitory receptor FcγRIIb. These preferred embodiments are expected to provide IgG polypeptides with increased therapeutic properties, for example in humans. In another aspect, the Fc variants of the present invention are optimized to have reduced or reduced affinity for human FcγR, including but not limited to FcγRI, FcγRIIa, FcγRIIb, FcγRIIc, FcγRIIIa, and FcγRIIIb. . These aspects are intended to provide IgG polypeptides with enhanced therapeutic properties in humans, such as reduced effector function and reduced toxicity. In other embodiments, the Fc variants of the present invention provide increased affinity for one or more FcγRs but decreased affinity for one or more other FcγRs. For example, the Fc variants of the present invention may have increased binding to FcγRIIIa but decreased binding to FcγRIIb. Alternatively, the Fc variants of the invention may have increased binding to FcγRIIa and FcγRI, but decreased binding to FcγRIIb. In yet another aspect, the Fc variants of the present invention may have increased affinity for FcγRIIb, but may have decreased affinity for one or more activated FcγRs.
好ましい態様には、ヒトFcγRとの結合の最適化が含まれるが、別の態様において、本発明のFc変異体は、げっ歯動物および非ヒト霊長動物を含むが、これらに限定されない非ヒト生物由来のFcγRに対して増大または減少した親和性を有する。非ヒトFcγRとの結合を最適化されるFc変異体は、実験で使用され得る。例えば、マウスモデルは、所定の薬剤候補についての効果、毒性、および薬物動態のような特性の検査を可能にする様々な疾患に利用可能である。当技術分野で公知の通り、異種移植と称される方法である、癌細胞を、ヒト癌を模倣するためにマウスに移植または注入することができる。1個以上のマウスFcγRに対して最適化されるFc変異体を含むFc変異体の試験は、タンパク質の有効性、その作用機序などに関する有益な情報を提供し得る。本発明のFc変異体はまた、グリコシル化形態の機能性および/または溶解特性を増大するために最適化され得る。好ましい態様において、本発明のグリコシル化Fc変異体は、親Fc変異体のグリコシル化形態よりも強い親和性でFcリガンドを結合する。該Fcリガンドには、FcγR、C1q、FcRn、ならびにプロテインAおよびGが含まれるが、これらに限定されず、ヒト、マウス、ラット、ウサギまたはサルを含むが、これらに限定されない何れかの起源由来、好ましくはヒト由来であり得る。別の好ましい態様において、Fc変異体は、親Fc変異体のグリコシル化形態よりも安定および/または溶解性になるように最適化される。 Preferred embodiments include optimization of binding to human FcγR, but in another embodiment, the Fc variants of the present invention include non-human organisms, including but not limited to rodents and non-human primates. Has increased or decreased affinity for the derived FcγR. Fc variants that are optimized for binding to non-human FcγR can be used in experiments. For example, mouse models are available for various diseases that allow examination of properties such as effects, toxicity, and pharmacokinetics for a given drug candidate. As is known in the art, cancer cells, a method called xenotransplantation, can be transplanted or injected into mice to mimic human cancer. Testing Fc variants, including Fc variants that are optimized for one or more mouse FcγRs, may provide useful information regarding the effectiveness of the protein, its mechanism of action, and the like. The Fc variants of the present invention can also be optimized to increase the functionality and / or solubility properties of glycosylated forms. In preferred embodiments, the glycosylated Fc variants of the present invention bind Fc ligands with a stronger affinity than the glycosylated form of the parent Fc variant. The Fc ligands include FcγR, C1q, FcRn, and proteins A and G, but are not limited to any origin, including but not limited to human, mouse, rat, rabbit or monkey Preferably, it may be derived from a human. In another preferred embodiment, the Fc variant is optimized to be more stable and / or soluble than the glycosylated form of the parent Fc variant.
本発明のFc変異体は、補体タンパク質、FcRn、およびFc受容体相同体(FcRH)を含むが、これらに限定されないFcγR以外のFcリガンドと相互作用するように調節される修飾体を含み得る。FcRHには、FcRH1、FcRH2、FcRH3、FcRH4、FcRH5、およびFcRH6が含まれるが、これらに限定されない(Davis et al., 2002, Immunol. Reviews 190:123−136、参照によりその全体が本明細書中に包含される)。 The Fc variants of the present invention may include modifications that are regulated to interact with Fc ligands other than FcγR, including but not limited to complement proteins, FcRn, and Fc receptor homologs (FcRH). . FcRH includes, but is not limited to, FcRH1, FcRH2, FcRH3, FcRH4, FcRH5, and FcRH6 (Davis et al., 2002, Immunol. Reviews 190: 123-136, hereby incorporated by reference in its entirety. Included).
好ましくは、本発明のFc変異体のFcリガンド特異性は、その治療的有用性を決定し得る。治療目的のための所定のFc変異体の有用性は、標的抗原のエピトープまたは形態ならびに処置される疾患または適応症に依存して変わり得る。いくつかの標的および適応症について、増強したFcγRにより仲介されるエフェクター機能が、好ましい。このことは、抗癌性Fc変異体にとって特に好ましい。故に、活性化FcγRに対する増大した親和性および/または阻害性FcγRに対する減少した親和性を提供するFc変異体を含むFc変異体が、用いられ得る。いくつかの標的および適応症について、異なる活性化FcγRに対する異なる選択性を提供するFc変異体を利用することは、さらに有益であり得る;例えば、いくつかの場合に、FcγRIIaおよびFcγRIIIaとの増加した結合が望ましいが、FcγRIには望ましくなく、一方、他の場合において、FcγRIIaのみとの増加した結合が好ましい。任意の標的および適応症について、FcγRおよび補体により仲介されるエフェクター機能の両方を増強するFc変異体を利用することが好ましいが、一方、他の場合について、FcγRまたは補体により仲介されるエフェクター機能のどちらかを増大するFc変異体を利用するのが都合よい。いくつかの標的または癌適応症について、1個以上のエフェクター機能を、例えばC1q、1種以上のFcγR、FcRn、または1個以上の他のFcリガンドとの結合をなくすことにより減少または低下することは都合よい。他の標的および適応症について、活性化FcγRとのWTレベルの、減少したまたは低下した結合であるが、阻害性FcγRIIbとの増大した結合を提供するFc変異体を利用することが好ましい。このことは、例えば、Fc変異体の目的が、炎症疾患または自己免疫疾患を阻止すること、またはいくつかの方法で免疫系を調節することであるとき、特に有用であり得る。 Preferably, the Fc ligand specificity of the Fc variants of the present invention can determine its therapeutic utility. The usefulness of a given Fc variant for therapeutic purposes can vary depending on the epitope or form of the target antigen and the disease or indication being treated. For some targets and indications, enhanced FcγR-mediated effector function is preferred. This is particularly preferred for anticancer Fc variants. Thus, Fc variants can be used, including Fc variants that provide increased affinity for activated FcγR and / or reduced affinity for inhibitory FcγR. Utilizing Fc variants that provide different selectivity for different activated FcγRs for some targets and indications may be further beneficial; for example, in some cases increased with FcγRIIa and FcγRIIIa Although binding is desirable, it is not desirable for FcγRI, while in other cases, increased binding only with FcγRIIa is preferred. For any target and indication, it is preferred to utilize Fc variants that enhance both FcγR and complement-mediated effector functions, whereas in other cases, FcγR or complement-mediated effectors It is convenient to utilize Fc variants that increase either function. For some targets or cancer indications, one or more effector functions are reduced or reduced, eg, by eliminating binding to C1q, one or more FcγR, FcRn, or one or more other Fc ligands. Is convenient. For other targets and indications, it is preferred to utilize Fc variants that provide increased or decreased binding of inhibitory FcγRIIb, but decreased or decreased binding of WT levels to activated FcγR. This can be particularly useful, for example, when the purpose of the Fc variant is to prevent inflammatory or autoimmune diseases, or to modulate the immune system in several ways.
所定の疾患を処置するための所定のFc変異体の最も有益な選択性を決定する明らかに重要なパラメーターは、Fc変異体であり、例えばどのタイプFc変異体が用いられるかである。故に、所定のFc変異体のFcリガンド選択性または特異性は、それが、抗体、Fc融合体、または結合した融合体もしくは複合体パートナーを有するFc変異体を含むかどうかに依存して異なる特性を提供し得る。例えば、毒物、放射性核種、または他の複合体は、それらを含むFc変異体が、1種以上のFcリガンドとの結合を減少または低下したならば、正常細胞に対して毒性が少ない。別の例として、炎症性疾患または自己免疫疾患を阻止するため、活性化FcγRと結合し、それらの活性化を阻害するような、活性化FcγRに対する増大した親和性を有するFc変異体を利用することが好ましい。反対に、増大したFcγRIIb親和性を有する2個以上のFc領域を含むFc変異体は、免疫細胞の表面上でこの受容体と共結合し、それによりこれらの細胞の増殖を阻止し得る。いくつかの場合において、Fc変異体は、1つの細胞タイプ上のその標的抗原と結合し、さらに標的抗原とは別の細胞上のFcγRと結合し得るが、他の場合において、それは、標的抗原として同じ細胞の表面上のFcγRとの結合に都合よい。例えば、抗体が、1種以上のFcγRを発現する細胞上の抗原を標的とするならば、その細胞の表面上のFcγRとの結合を増大または減少するFc変異体を利用するのが有益であり得る。このことは、例えば、Fc変異体が抗癌剤として用いられるとき可能であり、同じ細胞の表面上の標的抗原およびFcγRの共結合は、増殖阻害、アポトーシス、または他の抗増殖性効果をもたらす細胞内のシグナル伝達事象を促進する。あるいは、同じ細胞上の抗原およびFcγRの共結合は、Fc変異体が、いくつかの方法で免疫系を調節するために使用されるとき都合よく、ここで、標的抗原およびFcγRの共結合は、いくつかの増殖性または抗増殖性効果を提供する。同様に、2個以上のFc領域を含むFc変異体は、FcγR選択性または特異性を調節して同じ細胞の表面上のFcγRを共結合するFc変異体により有益であり得る。 A clearly important parameter that determines the most beneficial selectivity of a given Fc variant for treating a given disease is the Fc variant, for example which type Fc variant is used. Thus, the Fc ligand selectivity or specificity of a given Fc variant varies depending on whether it comprises an antibody, Fc fusion, or Fc variant with a bound fusion or complex partner. Can provide. For example, toxicants, radionuclides, or other complexes are less toxic to normal cells if the Fc variant that contains them reduces or reduces binding to one or more Fc ligands. As another example, use Fc variants with increased affinity for activated FcγRs that bind to and inhibit activated FcγRs to block inflammatory or autoimmune diseases It is preferable. Conversely, Fc variants that contain two or more Fc regions with increased FcγRIIb affinity can co-associate with this receptor on the surface of immune cells, thereby preventing the growth of these cells. In some cases, an Fc variant can bind its target antigen on one cell type and further bind to an FcγR on a cell other than the target antigen, while in other cases it As convenient for binding to FcγR on the same cell surface. For example, if an antibody targets an antigen on a cell that expresses one or more FcγRs, it may be beneficial to utilize an Fc variant that increases or decreases binding to FcγR on the surface of the cell. obtain. This is possible, for example, when Fc variants are used as anticancer agents, where the co-binding of target antigen and FcγR on the same cell surface results in intracellular inhibition leading to growth inhibition, apoptosis, or other antiproliferative effects. Promotes signal transduction events. Alternatively, co-binding of antigen and FcγR on the same cell is convenient when Fc variants are used to modulate the immune system in several ways, where the co-binding of target antigen and FcγR is Provides several proliferative or antiproliferative effects. Similarly, an Fc variant comprising two or more Fc regions may be beneficial to an Fc variant that modulates FcγR selectivity or specificity and co-binds FcγRs on the same cell surface.
FcγRの異なる多型形態の存在は、本発明のFc変異体の治療的利用性に影響を与えるさらに別のパラメーターを提供する。FcγRの異なるクラスに対する所定のFc変異体の特異性および選択性は、所定の疾患の処置のために所定の抗原を標的とするFc変異体の能力に顕著な影響を与えるが、これらの受容体の異なる多型に対するFc変異体の特異性または選択性は、調査または前臨床実験が、試験に適当であり得るかどうか、最終的に患者集団が、処置に応答し得るかまたは応答し得ないかを一部決定することができる。故に、本発明のFc変異体の、FcγR、C1q、FcRnおよびFcRH多型を含むが、これらに限定されないFcリガンド多型に対する特異性または選択性を、有効な調査および前臨床実験、臨床試験計画、患者の選択、用量依存性、および/または他の臨床試験に関する局面の選択を導くために用いることができる。 The presence of different polymorphic forms of FcγR provides yet another parameter that affects the therapeutic availability of the Fc variants of the present invention. Although the specificity and selectivity of a given Fc variant for a different class of FcγR significantly influences the ability of an Fc variant to target a given antigen for treatment of a given disease, these receptors The specificity or selectivity of Fc variants for different polymorphisms of whether or not a study or preclinical experiment may be appropriate for the study, and ultimately the patient population may or may not respond to treatment You can decide in part. Thus, the specificity or selectivity of the Fc variants of the present invention for Fc ligand polymorphisms, including but not limited to FcγR, C1q, FcRn and FcRH polymorphisms, can be effectively investigated and preclinical experiments, clinical trial plans. Can be used to guide selection of aspects related to patient selection, dose dependence, and / or other clinical trials.
修飾は、IgG安定性、溶解性、機能性または臨床的用途を改善するために行われ得る。好ましい態様において、本発明のFc変異体は、ヒトにおける免疫原性を減少するための修飾を含み得る。最も好ましい態様において、本発明のFc変異体の免疫原性を、2004年12月3日出願のUSSN11/004,590(参照によりその全体が本明細書中に包含される)に記載の方法を用いて減少させる。別の態様において、本発明のFc変異体は、ヒト化される(Clark, 2000, Immunol Today 21:397−402、参照によりその全体が本明細書中に包含される)。本明細書で記載の“ヒト化”抗体は、ヒトフレームワーク領域(FR)および非ヒト(通常、マウスまたはラット)抗体由来の1個以上の相補性決定領域(CDR)を含む抗体を意味する。CDRを提示する非ヒト抗体は、“ドナー”と称され、フレームワークを提示するヒト免疫グロブリンは、“アクセプター”と称される。ヒト化は、主に、アクセプター(ヒト)VLおよびVHフレームワーク上へのドナーCDRの移植による(例えば、Winter et al, US 5225539、参照によりその全体が本明細書中に包含される)。このストラテジーは、“CDR移植”と称される。選択したアクセプターフレームワーク残基の対応するドナー残基への“逆変異(Backmutation)”は、しばしば、最初に移植されたコンストラクトが欠く親和性を取り戻すのに必要である(US5530101;US5585089;US5693761;US5693762;US6180370;US5859205;US5821337;US6054297;および、US6407213、全て参照によりその全体が本明細書中に包含される)。ヒト化抗体はまた、最適には、免疫グロブリン定常領域の少なくとも一部分、典型的にヒト免疫グロブリンの少なくとも一部分を含み、故に、典型的に、ヒトFc領域を含み得る。非ヒト抗体のヒト化および再形成のための様々な技術および方法は、当技術分野でよく知られている(Tsurushita & Vasquez, 2004, Humanization of Monoclonal Antibodies, Molecular Biology of B Cells, 533−545, Elsevier Science (USA)、およびそこに引用される文献を参照のこと、全て、参照によりその全体が本明細書中に包含される)。ヒト化方法には、Jones et al., 1986, Nature 321:522−525; Riechmann et al.,1988; Nature 332:323−329; Verhoeyen et al., 1988, Science, 239:1534−1536; Queen et al., 1989, Proc Natl Acad Sci, USA 86:10029−33; He et al., 1998, J. Immunol. 160: 1029−1035; Carter et al., 1992, Proc Natl Acad Sci USA 89:4285−9, Presta et al., 1997, Cancer Res.57(20):4593−9; Gorman et al., 1991, Proc. Natl. Acad. Sci. USA 88:4181−4185; O’Connor et al., 1998, Protein Eng 11:321−8(全て、参照によりその全体が本明細書中に包含される)に記載の方法が含まれるが、それらに限定されない。非ヒト抗体可変領域の免疫原性を減じるヒト化方法または他の方法には、例えば、Roguska et al., 1994, Proc. Natl. Acad. Sci. USA 91:969−973(参照によりその全体が本明細書中に包含される)に記載のような、表面再形成法が含まれ得る。1つの態様において、親抗体は、当技術分野でよく知られている通り、成熟した親和性を有する。構造に基づく方法は、例えばUSSN11/004,590(参照によりその全体が本明細書中に包含される)に記載のヒト化および親和性成熟に用いられ得る。選択に基づく方法は、Wu et al., 1999, J. Mol. Biol. 294:151−162;Baca et al., 1997, J. Biol. Chem. 272(16):10678−10684;Rosok et al., 1996, J. Biol. Chem. 271(37): 22611−22618;Rader et al., 1998, Proc. Natl. Acad. Sci. USA 95: 8910−8915;Krauss et al., 2003, Protein Engineering 16(10):753−759(全て、参照によりその全体が本明細書中に包含される。)に記載の方法を含むが、これらに限定されない抗体可変領域のヒト化および/または親和性成熟に用いられ得る。他のヒト化方法は、USSN09/810,510;Tan et al., 2002, J. Immunol. 169:1119−1125;De Pascalis et al., 2002, J. Immunol. 169:3076−3084(全て、参照によりその全体が本明細書中に包含される。)に記載の方法を含むが、これらに限定されない、CDRの一部のみの移植を伴い得る。
Modifications can be made to improve IgG stability, solubility, functionality or clinical use. In preferred embodiments, the Fc variants of the present invention may include modifications to reduce immunogenicity in humans. In a most preferred embodiment, the immunogenicity of the Fc variants of the present invention is determined by the method described in
免疫原性を減少する修飾には、親配列由来の処理ペプチドのMHCタンパク質への結合を減少する修飾が含まれ得る。例えば、アミノ酸修飾は、どんな一般的なMHCアレルにも高親和性で結合することが予測される免疫エピトープがないかまたはそれが最小数となるように、作製され得る。タンパク質配列中のMHC結合エピトープを同定するいくつかの方法が、当技術分野で公知であり、本発明のFc変異体中のエピトープを数えるために用い得る。例えば、WO98/52976;WO02/079232;WO00/3317;USSN09/903,378;USSN10/039,170;USSN60/222,697;USSN10/754,296;PCT WO 01/21823;および、PCT WO 02/00165;Mallios, 1999, Bioinformatics 15: 432−439;Mallios, 2001, Bioinformatics 17: 942−948;Sturniolo et al., 1999, Nature Biotech. 17: 555−561;WO98/59244;WO02/069232;WO02/77187;Marshall et al., 1995, J. Immunol. 154: 5927−5933;and Hammer et al., 1994, J. Exp. Med. 180: 2353−2358(全て、参照によりその全体が本明細書中に包含される)を参照のこと。配列に基づく情報は、所定のペプチド−MHC相互作用の結合スコアを決定するために用い得る(例えば、Mallios, 1999, Bioinformatics 15: 432−439;Mallios, 2001, Bioinformatics 17: p942−948;Sturniolo et. al., 1999, Nature Biotech. 17: 555−561を参照のこと、全て参照によりその全体が本明細書中に包含される)。
Modifications that reduce immunogenicity can include modifications that reduce binding of the processing peptide from the parent sequence to the MHC protein. For example, amino acid modifications can be made such that there are no or a minimal number of immune epitopes that are predicted to bind with high affinity to any common MHC allele. Several methods for identifying MHC binding epitopes in protein sequences are known in the art and can be used to count epitopes in the Fc variants of the present invention. For example, WO 98/52976; WO 02/079232; WO 00/3317;
1つの態様において、本発明のFc変異体は、1個以上の改変された糖鎖(engineered glycoform)を含む。本明細書で用いる“改変された糖鎖”は、IgGと共有結合する炭水化物組成物を意味し、ここで該炭水化物組成物は、親IgGのそれと化学的に異なる。改変された糖鎖は、エフェクター機能を増強するかまたは減少することを含むが、これらに限定されない様々な目的に有用であり得る。改変された糖鎖は、当技術分野で公知の様々な方法により作製され得る(Umana et al., 1999, Nat Biotechnol 17:176−180;Davies et al., 2001, Biotechnol Bioeng 74:288−294;Shields et al., 2002, J Biol Chem 277:26733−26740;Shinkawa et al., 2003, J Biol Chem 278:3466−3473);(US6,602,684;USSN10/277,370;USSN10/113,929;PCT WO00/61739A1;PCT WO01/29246A1;PCT WO02/31140A1;PCT WO02/30954A1);(PotelligentTM technology [Biowa, Inc., Princeton, NJ];GlycoMAb(登録商標)glycosylation engineering technology [GLYCART Biotechnology AG, Zuerich, Switzerland])(全て参照によりその全体が本明細書中に包含される)。多くのこれらの技術は、例えば遺伝子組み換えまたは他の様々な生物または細胞株(例えば、Lec−13 CHO細胞またはラットハイブリドーマYB2/0細胞)でIgGを発現することによるか、またはグリコシル化経路に関与する酵素(例えば、FUT8[α1,6−フコシルトランスフェラーゼ]および/またはβ1−4−N−アセチルグルコサミニルトランスフェラーゼIII[GnTIII])を調節することによるか、またはIgGが発現された後、炭水化物(複数可)を修飾することにより、Fc領域に共有結合するオリゴ糖のフコシル化レベルを制御すること、および/またはそれを2つに切断することに基づく。改変された糖鎖は、典型的に、異なる炭水化物またはオリゴ糖と称される;故に、Fc変異体、例えば抗体またはFc融合体は、改変された糖鎖を含み得る。あるいは、改変された糖鎖は、異なる炭水化物またはオリゴ糖を含むFc変異体と称され得る。
In one embodiment, the Fc variants of the present invention comprise one or more engineered glycoforms. As used herein, “ modified sugar chain ” refers to a carbohydrate composition that is covalently linked to IgG, where the carbohydrate composition is chemically different from that of the parent IgG. Modified sugar chains may be useful for a variety of purposes including, but not limited to, enhancing or decreasing effector function. Modified sugar chains can be made by various methods known in the art (Umana et al., 1999, Nat Biotechnol 17: 176-180; Davies et al., 2001, Biotechnol Bioeng 74: 288-294 Shields et al., 2002, J Biol Chem 277: 26733-26740; Shinkawa et al., 2003, J Biol Chem 278: 3466-3473); (US 6,602,684;
別の態様において、本発明のFc変異体は、別の治療化合物と結合されるか、または作動可能に連結される。該治療化合物は、細胞毒性剤、化学療法剤、毒物、放射性同位体、サイトカイン、または他の治療的活性剤であり得る。IgGは、様々な非タンパク性ポリマーのうち1つ、例えば、ポリエチレングリコール、ポリプロピレングリコール、ポリオキシアルキレン、またはポリエチレングリコールおよびポリプロピレングリコールのコポリマーと結合し得る。 In another embodiment, the Fc variants of the present invention are bound to or operably linked to another therapeutic compound. The therapeutic compound can be a cytotoxic agent, chemotherapeutic agent, toxicant, radioisotope, cytokine, or other therapeutically active agent. IgG can bind to one of a variety of non-proteinaceous polymers, such as polyethylene glycol, polypropylene glycol, polyoxyalkylene, or a copolymer of polyethylene glycol and polypropylene glycol.
本発明は、Fc変異体を製造、産生およびスクリーニングするための方法を提供する。記載の方法は、本発明が、何れかの特定の用途または操作理論にとらわれることを意味しない。むしろ、提供される方法は、一般的に、1種以上のFc変異体が、最適化されたエフェクター機能を有するFc変異体を実験的に得るために、製造、産生、およびスクリーニングされ得ることを説明することを意図する。様々な方法が、抗体の設計、産生、および試験、ならびにタンパク質変異体について、USSN10/672,280、USSN10/822,231、USSN11/124,620、およびUSSN11/256,060(全て、参照によりその全体が本明細書中に包含される)に記載される。
The present invention provides methods for producing, producing and screening Fc variants. The described method does not imply that the present invention is bound by any particular application or theory of operation. Rather, the provided methods generally indicate that one or more Fc variants can be manufactured, produced, and screened to experimentally obtain Fc variants with optimized effector functions. Intended to explain. Various methods are available for antibody design, production, and testing, and protein variants,
様々なタンパク質製造方法が、最適化したエフェクター機能を有するFc変異体を設計するために用いられ得る。1つの態様において、構造に基づく製造方法を用いることができ、ここで利用可能な構造情報を、置換を誘導するために用いる。配列のアライメントを、表示の位置での置換を誘導するために用いることができる。あるいは、無作為的または半無作為的変異誘導法を、所望の位置にアミノ酸修飾を製造するために用いることができる。 Various protein production methods can be used to design Fc variants with optimized effector functions. In one embodiment, a structure-based manufacturing method can be used, where the structural information available is used to induce substitution. Sequence alignment can be used to induce substitution at the indicated position. Alternatively, random or semi-random mutagenesis methods can be used to produce amino acid modifications at the desired positions.
Fc変異体の製造方法およびスクリーニング方法は、当技術分野でよく知られている。抗体分子生物学、発現、精製、およびスクリーニングのための一般的方法は、Antibody Engineering、Duebel & Kontermann編集, Springer−Verlag, Heidelberg, 2001;および、Hayhurst & Georgiou, 2001, Curr Opin Chem Biol 5:683−689;Maynard & Georgiou, 2000, Annu Rev Biomed Eng 2:339−76(全て、参照によりその全体が本明細書中に包含される)に記載される。また、USSN10/672,280、USSN10/822,231、USSN11/124,620、およびUSSN11/256,060(全て、参照によりその全体が本明細書中に包含される)に記載の方法を参照のこと。
Methods for producing and screening Fc variants are well known in the art. General methods for antibody molecular biology, expression, purification, and screening are described by Antibody Engineering, Duebel & Kontermann, Springer-Verlag, Heidelberg, 2001; and Hayhurst & Georgiou, 2001, Curr Opin Chem Biol 5: 683. -689; Maynard & Georgiou, 2000, Annu Rev Biomed Eng 2: 339-76, all of which are incorporated herein by reference in their entirety. See also the methods described in
本発明の1つの態様において、Fc変異体配列を、メンバー配列をコードし、故に、宿主細胞中にクローニングされ、要すれば発現され、かつ分析され得る核酸を製造するために用いる。これらの実施を、公知の方法、およびMolecular Cloning−A Laboratory Manual, 3rd Ed.(Maniatis, Cold Spring Harbor Laboratory Press, New York, 2001)、およびCurrent Protocols in Molecular Biology(John Wiley & Sons)(両方とも、参照によりその全体が本明細書中に包含される)に記載の、本発明において使用され得る様々な方法を用いて行う。本発明のFc変異体を、タンパク質の発現を誘導または引き起こすのに適当な条件下で、Fc変異体をコードする核酸を含む、核酸、好ましくは発現ベクターで形質転換した宿主細胞を培養することにより作製することができる。哺乳動物細胞、細菌、昆虫細胞および酵母を含むが、これらに限定されない多様な適当な宿主細胞を、用いることができる。例えば、本発明において使用され得る様々な細胞系は、ATCC細胞系カタログ(American Type Culture Collectionにより利用可能)に記載される。宿主細胞中に外来の核酸を導入する方法は、当技術分野で公知であり、用いる宿主細胞により異なり得る。 In one embodiment of the invention, the Fc variant sequence is used to produce a nucleic acid that encodes a member sequence and thus can be cloned, optionally expressed, and analyzed in a host cell. These embodiments, known methods, and Molecular Cloning-A Laboratory Manual, 3 rd Ed. (Maniatis, Cold Spring Harbor Laboratory Press, New York, 2001), and Current Protocols in Molecular Biology (John Wiley & Sons) ( both Both are performed using a variety of methods that may be used in the present invention, as described in their entirety herein by reference. By culturing a host cell transformed with a nucleic acid, preferably an expression vector, comprising a nucleic acid encoding the Fc variant under conditions suitable to induce or cause expression of the protein of the Fc variant of the invention. Can be produced. A variety of suitable host cells can be used, including but not limited to mammalian cells, bacteria, insect cells and yeast. For example, various cell lines that can be used in the present invention are described in the ATCC cell line catalog (available through the American Type Culture Collection). Methods for introducing foreign nucleic acids into host cells are known in the art and may vary depending on the host cell used.
好ましい態様において、Fc変異体を発現後に精製または単離する。抗体を、当業者に公知の多様な方法で単離または精製することができる。標準的精製方法には、クロマトグラフ法、電気泳動法、免疫学的方法、沈殿法、透析法、ろ過法、濃縮法およびクロマト分画技術が含まれる。当技術分野で公知の通り、様々な天然タンパク質、例えば細菌プロテインA、G、およびLが抗体に結合し、これらのタンパク質は、精製用に本発明で使用され得る。しばしば、精製は、特定の融合パートナーにより可能であり得る。例えば、タンパク質を、GST融合が用いられるときグルタチオン樹脂を用いて、Hisタグが用いられるときNi+2親和性クロマトグラフィーを用いて、またはフラグタグが用いられるとき固定化抗フラグ抗体を用いて精製することができる。適する精製技術における一般的ガイダンスについては、Antibody Purification: Principles and Practice, 3rd Ed., Scopes, Springer−Verlag, NY, 1994(参照によりその全体が本明細書中に包含される)を参照のこと。 In a preferred embodiment, the Fc variant is purified or isolated after expression. Antibodies can be isolated or purified by a variety of methods known to those skilled in the art. Standard purification methods include chromatographic, electrophoretic, immunological, precipitation, dialysis, filtration, concentration, and chromatographic fractionation techniques. As is known in the art, a variety of natural proteins such as bacterial proteins A, G, and L bind to antibodies and these proteins can be used in the present invention for purification. Often, purification may be possible with a particular fusion partner. For example, purifying proteins using glutathione resin when GST fusion is used, Ni +2 affinity chromatography when His tag is used, or using immobilized anti-flag antibody when flag tag is used. Can do. For general guidance in suitable purification techniques, Antibody Purification:. Principles and Practice , 3 rd Ed, Scopes, Springer-Verlag, NY, 1994 ( by reference in its entirety is being incorporated herein) see .
Fc変異体を、インビトロ分析、インビボおよび細胞に基づくアッセイ、ならびに選択技術に用いる方法を含むが、これらに限定されない様々な方法を用いてスクリーニングすることができる。自動化高性能スクリーニング技術を、スクリーニング方法に利用することができる。スクリーニングには、融合パートナーまたは標識、例えば免疫標識、同位体標識、または蛍光もしくは比色色素のような小分子標識の使用を用いることができる。 Fc variants can be screened using a variety of methods including, but not limited to, methods used in in vitro analysis, in vivo and cell-based assays, and selection techniques. Automated high performance screening techniques can be used for screening methods. Screening can employ the use of fusion partners or labels, such as immunolabels, isotope labels, or small molecule labels such as fluorescent or colorimetric dyes.
好ましい態様において、Fc変異体の機能的および/または生物物理的特徴を、インビトロ分析においてスクリーニングする。好ましい態様において、タンパク質を、機能性、例えばその反応を触媒する能力またはその標的に対するその結合親和性についてスクリーニングする。 In preferred embodiments, the functional and / or biophysical characteristics of the Fc variants are screened in in vitro analyses. In a preferred embodiment, the protein is screened for functionality, such as its ability to catalyze the reaction or its binding affinity to its target.
当技術分野で公知の通り、スクリーニング法の一部には、ライブラリーの好ましいメンバーを選択する方法が含まれる。該方法は、本明細書中、“選択方法”と称され、これらの方法は、本発明においてFc変異体のスクリーニングに使用される。タンパク質ライブラリーを、選択方法を用いてスクリーニングするとき、増殖され、単離され、および/または観察されるライブラリーのメンバーのみが、いくつかの選択基準を満たすとして好ましい。本発明においてタンパク質ライブラリーのスクリーニングに使用され得る様々な選択方法が、当技術分野で公知である。本発明において使用され得る他の選択方法には、インビボ方法のような提示によらない方法が含まれる。“定向進化(directed evolution)”法と称される選択方法の一部は、時折新規の変異の挿入を含む、選択中の好ましい配列のメイティング(mating)またはブレッディング(breading)を含む方法である。 As is known in the art, some screening methods include methods for selecting preferred members of a library. The methods are referred to herein as “ selection methods ” and these methods are used in the present invention to screen for Fc variants. When screening protein libraries using selection methods, only those library members that are grown, isolated and / or observed are preferred as meeting some selection criteria. Various selection methods that can be used for screening protein libraries in the present invention are known in the art. Other selection methods that can be used in the present invention include non-presentation methods such as in vivo methods. Some of the selection methods, referred to as “directed evolution” methods, include preferred sequence mating or breading during selection, sometimes including the insertion of new mutations. is there.
好ましい態様において、Fc変異体を、1個以上の細胞に基づくアッセイまたはインビボアッセイを用いてスクリーニングする。そのような分析のために、精製または非精製タンパク質が典型的に、細胞が個々の変異体またはライブラリーに属する変異体の集合に暴露されるように、細胞外に添加される。これらの分析は、常にではないが一般的に、Fcポリペプチドの機能に基づく;すなわち、その標的に結合し、いくつかの生化学的事象、例えばエフェクター機能、リガンド/受容体結合阻害、アポトーシスなどを仲介するFcポリペプチドの能力に基づく。かかる分析はしばしば、IgGに対する細胞の応答、例えば細胞生存、細胞死、細胞形態の変化、または天然遺伝子もしくはレポーター遺伝子の細胞発現のような転写活性化を観察することを含む。例えば、かかる分析は、ADCC、ADCP、またはCDCを誘導するFc変異体の能力を測定することができる。いくつかの分析に関して、標的細胞に加えて、さらなる細胞または成分、例えば血清補体、または末梢血単球(PBMC)、NK細胞、マクロファージなどのエフェクター細胞を添加する必要があり得る。かかる添加細胞は、何れかの生物、好ましくはヒト、マウス、ラット、ウサギおよびサル由来であり得る。抗体は、標的を発現する任意の細胞系のアポトーシスを引き起こし得るか、またはその分析に添加された免疫細胞による標的細胞への攻撃を仲介し得る。細胞死または細胞生存を観察するための方法は、当技術分野で公知であり、それらには、色素、免疫化学的反応剤、細胞化学的反応剤、および放射性反応剤の使用が包含される。転写活性化は、細胞に基づくアッセイにおいて機能を分析するための方法にもなり得る。あるいは、細胞に基づくスクリーニングを、変異体をコードする核酸で形質転換またはトランスフェクトした細胞を用いて行う。すなわち、Fc変異体を、細胞に対して細胞外に添加しない。 In preferred embodiments, Fc variants are screened using one or more cell based assays or in vivo assays. For such analysis, purified or unpurified protein is typically added extracellularly so that the cells are exposed to individual mutants or a collection of mutants belonging to a library. These analyzes are generally, but not always, based on the function of the Fc polypeptide; that is, it binds to its target and several biochemical events such as effector function, ligand / receptor binding inhibition, apoptosis, etc. Based on the ability of Fc polypeptides to mediate. Such analysis often involves observing cellular responses to IgG, eg, cell survival, cell death, changes in cell morphology, or transcriptional activation such as cellular expression of a native or reporter gene. For example, such an assay can measure the ability of an Fc variant to induce ADCC, ADCP, or CDC. For some analyses, it may be necessary to add additional cells or components, such as serum complement, or effector cells such as peripheral blood monocytes (PBMC), NK cells, macrophages, in addition to the target cells. Such added cells can be from any organism, preferably humans, mice, rats, rabbits and monkeys. The antibody can cause apoptosis of any cell line that expresses the target or can mediate attack on the target cell by immune cells added to the analysis. Methods for observing cell death or cell survival are known in the art and include the use of dyes, immunochemical reactive agents, cytochemical reactive agents, and radioactive reactive agents. Transcriptional activation can also be a method for analyzing function in cell-based assays. Alternatively, cell-based screening is performed using cells transformed or transfected with a nucleic acid encoding the variant. That is, the Fc variant is not added extracellularly to the cells.
好ましい態様において、Fc変異体の免疫原性を、1個以上の細胞に基づくアッセイ法を用いて実験的に決定する。いくつかの方法を、エピトープの実験的確認に用いることができる。 In a preferred embodiment, the immunogenicity of the Fc variant is determined experimentally using one or more cell based assays. Several methods can be used for experimental confirmation of epitopes.
本発明のFc変異体の生物学的特徴を、細胞、組織および生物全体の実験において特徴付けることができる。当技術分野で公知の通り、薬剤をしばしば、疾患または疾患モデルに対する処置のための薬剤の効果を測定するため、または薬剤の薬物動態、毒性および他の特性を測定するために、マウス、ラット、ウサギ、イヌ、ネコ、ブタおよびサルを含むが、これらに限定されない動物において試験する。該動物は、疾患モデルと称され得る。治療剤をしばしば、ヌードマウス、SCIDマウス、異種移植マウス、および遺伝子組み換えマウス(ノックインおよびノックアウトを含む)を含むが、それらに限定されないマウスにおいて試験する。かかる実験は、治療剤として用いられるタンパク質の可能性を決定するための意味のあるデータを提供することができる。何れかの生物、好ましくは哺乳動物を試験に用いることができる。例えばヒトに遺伝的に類似するため、サルを適する治療モデルとすることができ、故に、本発明のIgGの効果、毒性、薬物動態、または他の特性を試験するために用いることができる。ヒトにおける試験が、薬剤としての承認のために最終的に必要であり、故に、もちろんこれらの実験が意図される。従って、本発明のIgGをヒトにおいて試験し、その治療効果、毒性、免疫原性、薬物動態、および/または他の臨床特性を決定することができる。 The biological characteristics of the Fc variants of the present invention can be characterized in cell, tissue and whole organism experiments. As is known in the art, drugs are often used to measure the effects of drugs for treatment on a disease or disease model, or to measure the pharmacokinetics, toxicity and other properties of drugs, Test in animals including but not limited to rabbits, dogs, cats, pigs and monkeys. The animal can be referred to as a disease model. Therapeutic agents are often tested in mice including, but not limited to, nude mice, SCID mice, xenograft mice, and transgenic mice (including knock-in and knock-out). Such experiments can provide meaningful data for determining the potential of proteins used as therapeutic agents. Any organism, preferably a mammal, can be used for the test. For example, because it is genetically similar to humans, monkeys can be a suitable therapeutic model and can therefore be used to test the effects, toxicity, pharmacokinetics, or other properties of the IgGs of the invention. Tests in humans are ultimately needed for drug approval and, of course, these experiments are contemplated. Thus, IgGs of the invention can be tested in humans to determine their therapeutic efficacy, toxicity, immunogenicity, pharmacokinetics, and / or other clinical properties.
本発明のFc変異体は、様々な製品に用いられ得る。1つの態様において、本発明のFc変異体は、治療剤、診断剤、または実験反応剤であり、好ましくは治療剤である。Fc変異体は、モノクローナルまたはポリクローナルである抗体組成物に用いられ得る。好ましい態様において、本発明のFc変異体を、標的抗原を有する標的細胞、例えば癌細胞を殺すために使用する。別の態様において、本発明のFc変異体を、標的抗原を阻止、アンタゴナイズまたはアゴナイズするため、例えばサイトカインまたはサイトカイン受容体をアンタゴナイズするために用いる。別の好ましい態様において、本発明のFc変異体を、標的抗原を阻止、アンタゴナイズまたはアゴナイズするため、および標的抗原を有する標的細胞を殺すために用いる。 The Fc variants of the present invention can be used in a variety of products. In one embodiment, the Fc variant of the present invention is a therapeutic agent, diagnostic agent, or experimental reaction agent, preferably a therapeutic agent. Fc variants can be used in antibody compositions that are monoclonal or polyclonal. In a preferred embodiment, the Fc variants of the present invention are used to kill target cells having a target antigen, such as cancer cells. In another embodiment, the Fc variants of the present invention are used to block, antagonize or agonize a target antigen, for example to antagonize a cytokine or cytokine receptor. In another preferred embodiment, the Fc variants of the present invention are used to block, antagonize or agonize the target antigen, and kill target cells with the target antigen.
本発明のFc変異体を、様々な治療目的に用いることができる。好ましい態様において、Fc変異体を含む抗体を、抗体関連疾患を処置するために患者に投与する。本目的に関して“患者”には、ヒトおよび他の動物、好ましくは哺乳動物が含まれ、最も好ましくはヒトである。本明細書中、“抗体関連疾患”または“抗体応答性疾患”または“状態”または“疾患”は、本発明のFc変異体を含む医薬組成物の投与により緩和され得る疾患を意味する。抗体関連疾患には、自己免疫疾患、免疫学的疾患、感染症、炎症性疾患、神経疾患、疼痛、肺疾患、血液学的状態、線維性状態、ならびに癌を含む腫瘍性および新生物性疾患が含まれるが、これらに限定されない。本明細書中、“癌”および“癌性”は、制御されない細胞増殖により典型的に特徴付けられる哺乳動物における生理的状態を意味するか、または記載する。癌の例には、癌腫、リンパ腫、芽細胞腫、肉腫(脂肪肉腫を含む)、神経内分泌腫瘍、中皮種、神経鞘腫(schwanoma)、髄膜腫、腺癌、黒色腫、ならびに白血病およびリンパ性悪性腫瘍が含まれるが、それらに限定されない。処置され得る他の状態には、リウマチ性関節炎、若年性リウマチ性関節炎、クローン病、潰瘍性大腸炎、シェーグレン症候群(Sjorgren's disease)、多発性硬化症、強直性脊椎炎、喘息、アレルギーおよびアレルギー状態、移植片対宿主疾患などが含まれるが、これらに限定されない。本明細書で用いる用語“処置”は、治療的処置、ならびに疾患、状態もしくは障害の予防的、または抑制的手段を含むことを意味する。故に、例えば、疾患の発症前の、本発明のFc変異体を含む医薬組成物の成功裏の投与は、結果として疾患の“処置”をもたらす。別の例として、疾患の症状に対抗するための疾患の臨床症状後の、本発明のFc変異体を含む医薬組成物の成功裏の投与は、疾患の“処置”に含まれる。“処置”はまた、疾患を根絶するための、疾患の出現後の本発明のFc変異体を含む医薬組成物の投与を含む。臨床症状の排除可能性および疾患の改善可能性を有する、発症後および臨床症状の発生後の本発明のFc変異体を含む医薬組成物の成功裏の投与は、疾患の“処置”に含まれる。本明細書で用いる用語“処置を必要とする”ものには、予防されるべき疾患または障害を含む該疾患または障害を既に有する哺乳動物、ならびに該疾患または障害を有する傾向のある哺乳動物が含まれる。 The Fc variants of the present invention can be used for various therapeutic purposes. In a preferred embodiment, an antibody comprising an Fc variant is administered to a patient to treat an antibody related disease. “ Patient ” for this purpose includes humans and other animals, preferably mammals, most preferably humans. As used herein, “ antibody-related disease ” or “ antibody- responsive disease ” or “ condition ” or “ disease ” means a disease that can be alleviated by administration of a pharmaceutical composition comprising an Fc variant of the present invention. Antibody-related diseases include autoimmune diseases, immunological diseases, infectious diseases, inflammatory diseases, neurological diseases, pain, lung diseases, hematological conditions, fibrotic conditions, and neoplastic and neoplastic diseases including cancer Is included, but is not limited thereto. As used herein, “ cancer ” and “ cancerous ” refer to or describe the physiological condition in mammals that is typically characterized by unregulated cell growth. Examples of cancer include carcinoma, lymphoma, blastoma, sarcoma (including liposarcoma), neuroendocrine tumors, mesothelioma, schwanoma, meningioma, adenocarcinoma, melanoma, and leukemia and This includes but is not limited to lymphoid malignancies. Other conditions that can be treated include rheumatoid arthritis, juvenile rheumatoid arthritis, Crohn's disease, ulcerative colitis, Sjorgren's disease, multiple sclerosis, ankylosing spondylitis, asthma, allergies and allergic conditions Including, but not limited to, graft versus host disease. The term “ treatment ” as used herein is meant to include therapeutic treatment as well as prophylactic or inhibitory means of the disease, condition or disorder. Thus, for example, successful administration of a pharmaceutical composition comprising an Fc variant of the present invention prior to the onset of the disease results in a “treatment” of the disease. As another example, successful administration of a pharmaceutical composition comprising an Fc variant of the present invention after a clinical symptom of the disease to combat the symptom of the disease is included in the “treatment” of the disease. “Treatment” also includes administration of a pharmaceutical composition comprising an Fc variant of the present invention after the appearance of the disease to eradicate the disease. Successful administration of a pharmaceutical composition comprising an Fc variant of the present invention after onset and after the onset of clinical symptoms, with the possibility of elimination of clinical symptoms and the amelioration of the disease, is included in the “treatment” of the disease . As used herein, the term “ in need of treatment ” includes mammals already having the disease or disorder including the disease or disorder to be prevented, as well as mammals prone to have the disease or disorder It is.
1つの態様において、本発明のFc変異体は、患者に投与される唯一の治療的活性剤である。あるいは、本発明のFc変異体を、細胞毒性薬、化学療法剤、サイトカイン、増殖阻害剤、抗ホルモン剤、キナーゼ阻害剤、血管形成阻害剤、心臓保護剤、または他の治療剤を含むが、それらに限定されない1個以上の他の治療剤と併用して、ならびに外科手術の前または後に投与する。IgG変異体を、1個以上の他の治療レジメンと併用して投与し得る。例えば、本発明のFc変異体を、外科手術、化学療法、放射線治療、または外科手術、化学療法および放射線治療のいずれかもしくは全てと併用して、患者に投与し得る。1つの態様において、本発明のFc変異体を、本発明のFc変異体を含み得るかまたは含み得ない1個以上の抗体と併用投与することができる。本発明の別の態様に従い、本発明のFc変異体および1個以上の他の抗癌治療剤を、エクスビボで癌細胞の処置に用いる。かかるエクスビボ処置は、骨髄移植および特に、自家骨髄移植に有用であり得ると考えられる。もちろん、本発明のFc変異体は、外科手術のような、さらに他の治療技術と組み合わせて用いることができると考えられる。 In one embodiment, the Fc variant of the present invention is the only therapeutically active agent administered to a patient. Alternatively, Fc variants of the present invention include cytotoxic agents, chemotherapeutic agents, cytokines, growth inhibitors, antihormonal agents, kinase inhibitors, angiogenesis inhibitors, cardioprotectants, or other therapeutic agents, It is administered in combination with one or more other therapeutic agents that are not so limited, as well as before or after surgery. IgG variants can be administered in combination with one or more other treatment regimens. For example, the Fc variants of the present invention may be administered to a patient in combination with surgery, chemotherapy, radiation therapy, or any or all of surgery, chemotherapy and radiation therapy. In one embodiment, the Fc variants of the present invention can be co-administered with one or more antibodies that may or may not include the Fc variants of the present invention. In accordance with another aspect of the present invention, the Fc variants of the present invention and one or more other anti-cancer therapeutic agents are used for the treatment of cancer cells ex vivo. It is believed that such ex vivo treatment may be useful for bone marrow transplantation and particularly autologous bone marrow transplantation. Of course, it is contemplated that the Fc variants of the present invention can be used in combination with other therapeutic techniques, such as surgery.
様々な他の治療剤が、本発明のFc変異体との併用投与に使用され得る。1つの態様において、IgGを、血管形成阻害剤と併用投与する。本明細書で用いる“血管形成阻害剤”は、血管の形成を阻止、またはある程度妨げる化合物を意味する。血管形成阻害因子は、例えば、血管形成の促進に関与する増殖因子または増殖因子受容体と結合する、小分子またはタンパク質、例えば抗体、Fc融合体もしくはサイトカインであり得る。本明細書中、好ましい血管形成阻害因子は、血管内皮増殖因子(VEGF)と結合する抗体である。別の態様において、IgGを、適応的免疫応答を誘導または増大する治療剤、例えばCTLA−4を標的とする抗体と共に投与する。別の態様において、IgGを、チロシンキナーゼ阻害剤と共に投与する。本明細書で用いる“チロシンキナーゼ阻害剤”は、チロシンキナーゼのチロシンキナーゼ活性をある程度阻害する分子を意味する。別の態様において、本発明のFc変異体を、サイトカインと共に投与する。本明細書で用いる“サイトカイン”は、細胞間メディエーターとして別の細胞に作用する、ある細胞集団により放出されるタンパク質の一般名を意味する。 A variety of other therapeutic agents can be used for co-administration with the Fc variants of the present invention. In one embodiment, IgG is administered in combination with an angiogenesis inhibitor. As used herein, “ angiogenesis inhibitor ” means a compound that inhibits or prevents some formation of blood vessels. Angiogenesis inhibitors can be, for example, small molecules or proteins that bind to growth factors or growth factor receptors involved in promoting angiogenesis, such as antibodies, Fc fusions or cytokines. A preferred angiogenesis inhibitor herein is an antibody that binds to vascular endothelial growth factor (VEGF). In another embodiment, IgG is administered with a therapeutic agent that induces or augments an adaptive immune response, such as an antibody that targets CTLA-4. In another embodiment, IgG is administered with a tyrosine kinase inhibitor. As used herein, “ tyrosine kinase inhibitor ” means a molecule that inhibits to some extent the tyrosine kinase activity of a tyrosine kinase. In another embodiment, the Fc variants of the present invention are administered with a cytokine. As used herein, “cytokine” refers to the generic name of a protein released by a cell population that acts on another cell as an intercellular mediator.
医薬組成物とは、本発明のFc変異体および1個以上の治療的活性剤が、製剤されることを意図する。本発明のFc変異体の製剤は、所望の純度を有するIgGを、所望により薬学的に許容される担体、賦形剤または安定化剤(Remington’s Pharmaceutical Sciences 16th edition, Osol, A. Ed., 1980、参照によりその全体が本明細書中に包含される)と共に混合することにより、凍結乾燥製剤または水溶液の形態に保存用に調製される。インビボ投与用に使用される製剤を、好ましくは滅菌する。これは、滅菌ろ過膜を通すろ過または他の方法により容易に達成される。本明細書に記載のFc変異体および他の治療的活性剤は、免疫リポソーム、および/またはマイクロカプセル封入としても製剤され得る。 By pharmaceutical composition is intended that the Fc variants of the invention and one or more therapeutically active agents are formulated. The Fc variant formulations of the present invention may comprise IgG of desired purity, optionally pharmaceutically acceptable carriers, excipients or stabilizers (Remington's Pharmaceutical Sciences 16th edition, Osol, A. Ed., 1980). , Which is incorporated herein by reference in its entirety) and is prepared for storage in the form of a lyophilized formulation or an aqueous solution. The formulation used for in vivo administration is preferably sterilized. This is easily accomplished by filtration through sterile filtration membranes or other methods. The Fc variants and other therapeutically active agents described herein can also be formulated as immunoliposomes and / or microencapsulations.
製剤中の治療的に活性なFc変異体の濃度は、約0.001ないし100重量%で変化し得る。好ましい態様において、IgGの濃度は、0.003ないし1.0モルの範囲内である。患者を処置するために、本発明のFc変異体の治療的有効用量を投与することができる。本明細書中、“治療的有効用量”とは、それが投与されて効果を生じる用量を意味する。正確な用量は、処置の目的に依存して変化し、公知の技術を用いて当業者により確認され得る。投与量は、体重1kg当たり0.001ないし100mgまたはそれ以上、例えば体重1kg当たり0.1、1、10、または50mgの範囲であり、1ないし10mg/kgが好ましい。当技術分野で公知の通り、タンパク質分解、全身的対局所送達、および新しいタンパク質合成の速度、ならびに年齢、体重、一般的健康状態、性別、食事、投与の時間、薬剤の相互作用および状態の重症度に関する調整が必要であり、当業者により常套的実験にて確認され得る。 The concentration of therapeutically active Fc variant in the formulation can vary from about 0.001 to 100% by weight. In a preferred embodiment, the concentration of IgG is in the range of 0.003 to 1.0 mole. In order to treat a patient, a therapeutically effective dose of the Fc variants of the present invention can be administered. As used herein, “ therapeutically effective dose ” means the dose with which it is administered to produce an effect. The exact dose will vary depending on the purpose of the treatment, and will be ascertainable by one skilled in the art using known techniques. The dosage is in the range of 0.001 to 100 mg or more per kg body weight, for example 0.1, 1, 10, or 50 mg per kg body weight, with 1 to 10 mg / kg being preferred. As is known in the art, the rate of proteolysis, systemic versus local delivery, and new protein synthesis, as well as age, weight, general health, sex, diet, time of administration, severity of drug interactions and conditions Adjustment for the degree is necessary and can be ascertained by one skilled in the art through routine experimentation.
好ましくは滅菌水溶液の形態の、本発明のFc変異体を含む医薬組成物の投与を、経口、皮下、静脈内、経鼻的、耳内(intraotically)、経皮的、局所的(例えば、ジェル、軟膏、ローション、クリームなど)、腹腔内、筋肉内、肺内(例えば、Aradigmにより市販されるAERx(登録商標)吸入可能技術、またはInhale Therapeuticsにより市販されるInhance(登録商標)肺送達システムなど)、経膣的、非経腸的、経直腸的、または眼内(intraocularly)を含むが、それらに限定されない様々な方法で行うことができる。本明細書に記載の治療剤を、他の治療剤と併用して投与することができる。 Administration of a pharmaceutical composition comprising an Fc variant of the present invention, preferably in the form of a sterile aqueous solution, can be administered orally, subcutaneously, intravenously, nasally, intraotically, transdermally, topically (eg, gel , Ointments, lotions, creams, etc.), intraperitoneal, intramuscular, intrapulmonary (eg AERx® inhalable technology marketed by Aradigm, or Inance® pulmonary delivery system marketed by Inhale Therapeutics, etc. ), Vaginal, parenteral, rectal, or intraocularly, can be performed in a variety of ways. The therapeutic agents described herein can be administered in combination with other therapeutic agents.
実施例
下記の実施例を、本発明を説明するために提供する。これらの実施例は、どんな特定の適用または操作理論にも本発明を制限することを意味しない。
Examples The following examples are provided to illustrate the present invention. These examples are not meant to limit the invention to any particular application or theory of operation.
実施例1.増大したFcγRにより仲介されるエフェクター機能を有するFc変異体
USSN10/672,280、USSN10/822,231、USSN11/124,620およびUSSN11/256,060(全て、参照によりその全体が本明細書中に包含される)に記載の方法を用いて、さらなるFc変異体を、Fcリガンドとの結合を増大し、エフェクター機能を最適化するため、ならびにFcγR結合およびエフェクター機能を減少または低下させるために設計した。該変異体を、細胞に基づくアッセイにおいて測定可能なCDCおよびADCCを仲介することが知られる、抗CD20抗体であるPRO70769(PCT/US2003/040426、参照によりその全体が本明細書中に包含される)に照らして構築した。既に特徴付けられた変異体もまた、それらの特性をさらに特徴付け、現在の一連の新しい変異体の比較物(comparator)を提供するために、PRO70769中にコンストラクトした。図5は、これらのFc変異体のリストを提供する。とりわけ、この変異体セットには、多くの挿入が含まれる。例えば、“インサート L>235−236/I332E”は、I332E置換および残基235と236位の間へのロイシンの挿入を含む二重変異体を意味する。
Example 1. Fc variants USSN 10 / 672,280,
PRO70769の可変領域の遺伝子(図24aおよび24b)を、リカーシブ(recursive)PCRを用いてコンストラクトし、全長軽鎖カッパ(Cκ)および重鎖IgG1定常領域を含む哺乳動物発現ベクターであるpcDNA3.1Zeo(Invitrogen)中にサブクローニングした。変異体を、quick−change変異誘発技術(Stratagene)を用いて、pcDNA3.1Zeoベクター中の抗体の可変領域中にコンストラクトし、293T細胞中で発現させた。DNAを、配列の忠実度を確認するために配列決定した。重鎖遺伝子(VH−CH1−CH2−CH3)(野生型または変異体)を含むプラスミドを、軽鎖遺伝子(VL−Cκ)を含むプラスミドと共に、293T細胞中に共トランスフェクトした。培地をトランスフェクションの5日後に集め、抗体をプロテインA親和性クロマトグラフィー(Pierce)を用いて上清から精製した。選択したFc変異体は、アレムツズマブにおいても発現した。 The variable region gene of PRO70769 (FIGS. 24a and 24b) was constructed using recursive PCR and pcDNA3.1Zeo, a mammalian expression vector containing a full length light chain kappa (Cκ) and heavy chain IgG1 constant region. Invitrogen). Mutants were constructed into variable regions of antibodies in pcDNA3.1Zeo vector using quick-change mutagenesis technology (Stratagene) and expressed in 293T cells. DNA was sequenced to confirm sequence fidelity. A plasmid containing the heavy chain gene (VH-CH1-CH2-CH3) (wild type or mutant) was co-transfected into a 293T cell with a plasmid containing the light chain gene (VL-Cκ). The medium was collected 5 days after transfection and the antibody was purified from the supernatant using protein A affinity chromatography (Pierce). Selected Fc variants were also expressed in alemtuzumab.
IgG抗体によるヒトFcγRに対する結合親和性を、AlphaScreenTM競合分析を用いて測定した。AlphaScreenは、ビーズに基づく発光近接分析である。ドナービーズのレーザー励起は、酸素を励起し、アクセプタービーズとの接近が十分なとき、化学発光事象のカスケードを生じ、最終的に520−620nmでの蛍光放出をもたらし得る。AlphaScreenを、抗体をスクリーニングするための競合分析として用いた。野生型IgG1抗体を、ストレプトアビジン ドナービーズへの標準的結合方法によりビオチン化し、タグ付きFcγRを、グルタチオンキレート アクセプタービーズに結合させた。競合するFcポリペプチドの不存在において、野生型抗体およびFcγRが相互作用し、520−620nmでのシグナルを生じる。タグの付いていない抗体の添加は、野生型Fc/FcγR相互作用と競合し、蛍光を定量的に減少させて相対的結合親和性の決定を可能にする。 Binding affinity for human FcγR by IgG antibodies was measured using AlphaScreen ™ competition analysis. AlphaScreen is a bead-based luminescent proximity analysis. Laser excitation of the donor beads can excite oxygen and, when sufficient access to the acceptor beads, results in a cascade of chemiluminescent events, ultimately leading to fluorescence emission at 520-620 nm. AlphaScreen was used as a competition analysis to screen for antibodies. Wild-type IgG1 antibody was biotinylated by standard binding methods to streptavidin donor beads and tagged FcγR was bound to glutathione chelate acceptor beads. In the absence of competing Fc polypeptides, wild-type antibody and FcγR interact to produce a signal at 520-620 nm. The addition of untagged antibody competes with the wild type Fc / FcγR interaction and quantitatively reduces fluorescence to allow determination of relative binding affinity.
図6は、ヒト活性化受容体V158 FcγRIIIa(図6a)およびF158 FcγRIIIa(図6b)に対する選択したPRO70769Fc変異体の結合についてのAlphaScreen競合データを提供する。該データを、非線形回帰を用いて一部位競合モデルに適合させ、これらの適合を、図中曲線で示す。これらの適合は、各抗体についての50%の阻害濃度(IC50)(すなわち、50%阻害に必要な濃度)を提供し、故に、WTと比較した相対的結合親和性を決定することができる。図5は、これらの結合曲線への適合についての、WTと比較したIC50およびIC50倍数を提供する。 FIG. 6 provides AlphaScreen competition data for binding of selected PRO70769Fc variants to human activated receptors V158 FcγRIIIa (FIG. 6a) and F158 FcγRIIIa (FIG. 6b). The data was fitted to partial competition models using nonlinear regression and these fits are shown as curves in the figure. These fits provide a 50% inhibitory concentration (IC50) for each antibody (ie, the concentration required for 50% inhibition), and therefore the relative binding affinity compared to WT can be determined. FIG. 5 provides IC50 and IC50 multiples compared to WT for fitting to these binding curves.
選択したFc変異体を再発現させ、ヒトV158 FcγRIIIaおよびF158 FcγRIIIaとの結合についてAlphaScreen競合アッセイを用いて再試験した(図7)。図7aは、これらの変異体の結合データを示し、図7bは、これらの結合曲線への適合についての、WTと比較したIC50およびIC50倍数を提供する。 Selected Fc variants were re-expressed and retested using the AlphaScreen competition assay for binding to human V158 FcγRIIIa and F158 FcγRIIIa (FIG. 7). FIG. 7a shows the binding data for these variants and FIG. 7b provides the IC50 and IC50 fold compared to WT for fitting to these binding curves.
これらのデータに基づき、多くのさらなるFc変異体を、PRO70769 IgG1に照らしてコンストラクトした。さらに、いくつかのFc変異体を、2005年10月21日出願のUSSN11/256,060(参照によりその全体が本明細書中に包含される)に記載の新規IgG分子であるIgG(1/2)ELLGGに照らしてコンストラクトした。これらの変異体を、上記の通りにコンストラクトし、多くの既に特徴付けられたFc変異体と共に発現させ精製した。これらの変異体を図8aに列記する。ヒト活性化受容体V158 FcγRIIIaおよびF158 FcγRIIIa、ならびに阻害性受容体FcγRIIbとの該変異体の結合を、AlphaScreen競合アッセイを用いて測定した。図8bは、選択した変異体のこれらの受容体との結合データを示し、図8aは、この一連のFc変異体全てについての、WT PRO70769 IgG1と比較したIC50およびIC50倍数を提供する。
Based on these data, a number of additional Fc variants were constructed against PRO70769 IgG1. In addition, some Fc variants have been identified as IgG (1/1), a novel IgG molecule described in
該アッセイの高反応性性質のため、AlphaScreenは、相対的親和性のみ提供する。正確な結合定数を、抗体/FcγR平衡における非結合抗体をFcγRIIIa表面に捕捉した、競合SPR装置(Nieba et al., 1996, Anal Biochem 234:155−65、参照によりその全体が本明細書中に包含される)を用いて得た。この実験を、上記でコンストラクトされ特徴付けられたトラスツズマブ IgG1に照らして、I332EおよびS239D/I332E変異体を用いて行った(USSN10/672,280、USSN10/822,231、およびUSSN11/124,620、全て参照によりその全体が本明細書中に包含される)。WTおよび変異体トラスツズマブ抗体を、上記の通りに発現させ精製した。この実験に関して、データをBIAcore 3000装置(BIAcore)で得た。V158 FcγRIIIa−His−GSTを、固定化抗GST抗体を用いて捕捉し、組み換えGSTを用いてブロッキングし、抗体/受容体への結合競合分析物を測定した。抗GST抗体を、BIAcore GSTキャプチャーキットを用いてCM5センサーに共有結合させた。各センサーチップに1個のフローセルを、非特異的結合の対照としてエタノールアミンと結合させ、バルク屈折率変化をオンラインで減算した。泳動バッファーは、HBS−EP(0.01M HEPES pH7.4、0.15M NaCl、3mM EDTA、0.005%v/v界面活性剤P20、BIAcore)であり、チップ再生バッファーは、グリシン1.5(10mMグリシン−HCl、pH1.5、BIAcore)であった。1μM V158 FcγRIIIa−His−GSTを、1μl/分にて5分間、HBS−EP中で抗GST CM5チップに結合させた。表面を、1μl/分にて2分間、5μMの組み換えGST(Sigma)を注入してブロッキングした。100nMの野生型または変異体トラスツズマブ抗体を、4ないし1000nMの間の連続希釈のV158 FcγRIIIa−His−GSTと合わせ、室温で少なくとも2時間インキュベートした。該競合結合物を、50μl/分にて、HBS−EP中、30秒間の結合のために、V158 FcγRIIIa−His−GST/組み換えGST表面上に注入した。抗体を含むが競合受容体を含まない1サイクルが、ベースライン応答を提供した。
Due to the highly reactive nature of the assay, AlphaScreen provides only relative affinity. Accurate binding constants were determined by competing SPR devices (Nieba et al., 1996, Anal Biochem 234: 155-65, which are incorporated herein by reference in their entirety), with unbound antibody in the antibody / FcγR equilibrium captured on the FcγRIIIa surface. Included). This experiment was performed with the I332E and S239D / I332E mutants (
上記の“競合BIAcore”法を用いて、動力学的曲線を結合率を導くために適合させた(Nieba et al., 1996, Anal Biochem 234:155−65、参照によりその全体が本明細書中に包含される)。本発明者らは、動力学的曲線から得られる結合率が用いた抗体濃度に非線形相関を示したため、この方法があまり信頼性のないことを見出した。本研究に用いた分析は、初期結合率Rの遊離抗体濃度との比例に基づく(Holwill et al., 1996, Process Control and Quality 8:133−145; Edwards & Leatherbarrow, 1997, Anal Biochem 246:1−6、全て参照によりその全体が本明細書中に包含される)。応答単位データを、BIA評価ソフトウェア(BIAcore)を用いて出力し、Xlfitバージョン3.0.5のマイクロソフトExcel(IDBS)を用いて分析した。(シグナル増加の)初期結合率値を、傾きのExcel式を用いて各センサーグラムの生データから決定した。平衡解離結合定数(KD)を、各濃度で得られた初期結合率に対するFcγRIIIa濃度のlog値をプロットすることにより決定した。GraphPad Prism(GraphPad Software)を用いて、下記の式にデータを合わせた: Using the “competitive BIAcore” method described above, the kinetic curve was adapted to derive binding rates (Nieba et al., 1996, Anal Biochem 234: 155-65, which is hereby incorporated by reference in its entirety. Included). The inventors have found that this method is not very reliable because the binding rate obtained from the kinetic curve showed a non-linear correlation with the antibody concentration used. The analysis used in this study is based on the proportion of initial binding rate R to free antibody concentration (Holwill et al., 1996, Process Control and Quality 8: 133-145; Edwards & Leatherbarrow, 1997, Anal Biochem 246: 1 -6, all incorporated herein by reference in their entirety). Response unit data was output using BIA evaluation software (BIAcore) and analyzed using Microsoft Excel (IDBS) with Xlfit version 3.0.5. Initial binding values (for signal increase) were determined from the raw data for each sensorgram using the Excel formula of the slope. The equilibrium dissociation binding constant (K D ) was determined by plotting the log value of the FcγRIIIa concentration against the initial binding rate obtained at each concentration. Using GraphPad Prism (GraphPad Software), the data was fit to the following formula:
〔式中、
[A0]=抗体濃度
R0=競合する受容体の不存在下での、抗体濃度A0での初期結合率
X=log[L0](ここで、[L0]=インプット受容体濃度である。)
KD=平衡解離定数である。〕。
R0は、抗体と固定化受容体との結合率を示し(競合する受容体の不存在下での)、それらの異なる受容体親和性のため、それを、WT、I332E、およびS239D/I332E抗体について別個に計算した。
[Where,
[A 0 ] = antibody concentration R 0 = initial binding rate at antibody concentration A 0 in the absence of competing receptors X = log [L 0 ] (where [L 0 ] = input receptor concentration .)
K D = equilibrium dissociation constant. ].
R 0 indicates the binding rate of the antibody to the immobilized receptor (in the absence of competing receptors) and due to their different receptor affinities it is expressed as WT, I332E, and S239D / I332E. Calculated separately for antibodies.
初期結合率Rについての式は、単一の結合部位についてのKD:
で示される定義、および質量保存式
〔式中:
[L]=遊離受容体の濃度である。〕
から導かれる。
The formula for the initial binding rate R, K D for a single binding site:
Definitions indicated by and mass conservation formulas
[In the formula:
[L] = concentration of free receptor. ]
Derived from.
初期結合率を、センサーグラムの生データから決定し(図9a)、KD値を、各濃度で得られる初期結合率に対する受容体濃度のlog値をプロットすることにより計算した(図9b、9c)(Edwards & Leatherbarrow, 1997, Anal Biochem 246:1−6、参照によりその全体が本明細書中に包含される)。WT KD(252nM)は、公表されたデータとよく一致する(SPRからの208nM、熱量測定からの535nM)(Okazaki et al., 2004 J Mol Biol 336:1239−49、参照によりその全体が本明細書中に包含される)。I332E(30nM)およびS239D/I332E(2nM)変異体のKD値は、V158 FcγRIIIaに対してそれぞれおよそ10倍および100倍値(1-および2-logs)の強い親和性を示す。 The initial binding rate was determined from the raw data of sensorgrams (Fig. 9a), the K D values were calculated by plotting the log value of the receptor concentration for the initial binding rate obtained at each concentration (Fig. 9b, 9c (Edwards & Leatherbarrow, 1997, Anal Biochem 246: 1-6, which is hereby incorporated by reference in its entirety). WT K D (252 nM) is in good agreement with published data (208 nM from SPR, 535 nM from calorimetry) (Okazaki et al., 2004 J Mol Biol 336: 1239-49, which is entirely incorporated by reference. Included in the specification). I332E (30 nM) and the K D value of S239D / I332E (2nM) mutants show a strong affinity respectively about 10 times and 100 times values for V158 Fc [gamma] RIIIa (1-and 2-logs).
本発明のFc変異体を含む抗体の、FcγRにより仲介されるエフェクター機能を発揮するための能力を調査するために、インビトロでの細胞ベースのADCCアッセイを、エフェクター細胞としてヒトPBMCを用いて行った。ADCCを、LDH細胞傷害性検出キット(Roche Diagnostic)を用いてラクトースデヒドロゲナーゼの放出により測定した。ヒトPBMCを、フィコール・グラディエント(ficoll gradient)法を用いてleukopackから精製し、CD20+標的リンパ腫細胞株WIL2−SをATCCから得た。標的細胞を、96ウェルプレートに10,000細胞/ウェルで播種し、Fc変異体またはWT抗体を示した最終濃度で用いてオプソニン化した。トライトンX100およびPBMCのみを、対照として用いた。エフェクター細胞を、PBMC:標的細胞を25:1で添加し、プレートを、37℃で4時間インキュベートした。細胞を、LDH反応混合物と共にインキュベートし、蛍光を、FusionTMAlpha−FP(Perkin Elmer)を用いて測定した。データを、最大溶解(トライトン)および最小溶解(PBMCのみ)に標準化し、シグモイド型用量応答モデルに合わせた。図10は、可変領域PRO70769およびIgG1またはIgG(1/2)ELLGGのどちらかにおける選択したFc変異体抗体についてのこれらのデータを提供する。Fc変異体は、WT PRO70769 IgG1抗体と比較して、FcγRにより仲介されるCD20+標的細胞溶解における明確な増大を提供する。 In order to investigate the ability of antibodies comprising Fc variants of the present invention to exert FcγR-mediated effector functions, an in vitro cell-based ADCC assay was performed using human PBMC as effector cells. . ADCC was measured by the release of lactose dehydrogenase using an LDH cytotoxicity detection kit (Roche Diagnostic). Human PBMC was purified from leukopack using the ficoll gradient method and the CD20 + target lymphoma cell line WIL2-S was obtained from ATCC. Target cells were seeded at 10,000 cells / well in 96 well plates and opsonized with Fc variants or WT antibodies at the final concentrations indicated. Only Triton X100 and PBMC were used as controls. Effector cells were added PBMC: target cells at 25: 1 and the plates were incubated at 37 ° C. for 4 hours. Cells were incubated with the LDH reaction mixture and fluorescence was measured using Fusion ™ Alpha-FP (Perkin Elmer). Data were normalized to maximal lysis (Triton) and minimal lysis (PBMC only) and fit to a sigmoidal dose response model. FIG. 10 provides these data for variable region PRO70769 and selected Fc variant antibodies in either IgG1 or IgG (1/2) ELLGG. Fc variants provide a distinct increase in CD20 + target cell lysis mediated by FcγR compared to WT PRO70769 IgG1 antibody.
これらのインビトロ分析は、本発明のFc変異体が、臨床設定における増強した効力および/または有効性を提供し得ることを示唆する。インビボ性能は、これらのインビトロ実験で検討されないいくつかの因子を含む多くの因子の影響を受け得る。1つのそのようなパラメーターは、抗体の臨床効力に影響を与えることが示されている、血清中非特異的IgGの高濃度である(Vugmeyster & Howell, 2004, Int Immunopharmacol 4:1117−24; Preithner et al., 2005, Mol Immunol, 43(8):1183−93、全て参照によりその全体が本明細書中に包含される)。本発明のFc変異が、インビボ生物学により酷似した溶液中でどのように起こるのかを調べるため、ADCCアッセイを、生物学的に関連する濃度(1mg/ml)のヒト血清から精製したIgG(Jackson Immunoresearch Lab, Inc.により市販されている)の存在下で繰り返した。これらのデータを、図11に示す。WT 抗CD20抗体の有効性は、血清レベルのIgGの存在下で減少するだけでなく、完全になくなる。対照的に、Fc変異体抗体は、顕著に減少するが、依然、標的細胞系を殺すのを仲介する実質的な能力を示す。 These in vitro analyzes suggest that the Fc variants of the present invention may provide enhanced efficacy and / or efficacy in a clinical setting. In vivo performance can be affected by many factors, including several factors not considered in these in vitro experiments. One such parameter is the high concentration of non-specific IgG in serum that has been shown to affect the clinical efficacy of antibodies (Vugmeyster & Howell, 2004, Int Immunopharmacol 4: 1117-24; Preithner et al., 2005, Mol Immunol, 43 (8): 1183-93, all of which are hereby incorporated by reference in their entirety). To investigate how the Fc mutations of the present invention occur in solutions that more closely resemble in vivo biology, ADCC assays were performed using IgG purified from biologically relevant concentrations (1 mg / ml) of human serum (Jackson In the presence of (commercially available from Immunoresearch Lab, Inc.). These data are shown in FIG. The efficacy of the WT anti-CD20 antibody is not only reduced in the presence of serum levels of IgG, but is completely eliminated. In contrast, Fc variant antibodies are significantly reduced but still show substantial ability to mediate killing of the target cell line.
実施例2.増大した補体により仲介されるエフェクター機能を有するFc変異体
多くの変異体を、補体依存性細胞傷害作用(CDC)を増強するのを目的として設計した。Fc/FcγR結合がADCCを仲介するのと同じ方法で、Fc/C1q結合は、補体依存性細胞傷害作用(CDC)を仲介する。現在、Fc/C1q複合体に利用可能な構造は存在しない;しかしながら、変異誘発研究は、残基D270、K322、P329およびP331を中心とする領域にC1qのためのヒトIgG上の結合部位をマッピングした(Idusogie et al., 2000, J Immunol 164:4178−4184; Idusogie et al., 2001, J Immunol 166:2571−2575、両方とも参照によりその全体が本明細書中に包含される)。図12は、このマッピングされた中心点を含むヒトIgG1Fc領域の構造を示す。これらの4個の残基に構造的に近いUSSN10/672,280、USSN10/822,231、USSN11/124,620、およびUSSN11/256,060(全て参照によりその全体が本明細書中に包含される)に開示される選択したアミノ酸修飾を、C1qに対する増加した親和性を仲介し、および/または増加したCDCを提供し得る変異体を探索するために調査した。増加したFcγR親和性およびFcγRにより仲介されるエフェクター機能を既に示した変異体には、この一連の変異体が含まれ、それらの相補的特性を特徴付けた。この変異体ライブラリーを、図13に示す。
Example 2 Fc variants with effector function mediated by increased complement A number of variants were designed with the goal of enhancing complement-dependent cytotoxicity (CDC). In the same way that Fc / FcγR binding mediates ADCC, Fc / C1q binding mediates complement dependent cytotoxicity (CDC). There is currently no structure available for the Fc / C1q complex; however, mutagenesis studies have mapped the binding site on human IgG for C1q to a region centered on residues D270, K322, P329 and P331 (Idusogie et al., 2000, J Immunol 164: 4178-4184; Idusogie et al., 2001, J Immunol 166: 2571-2575, both of which are hereby incorporated by reference in their entirety). FIG. 12 shows the structure of the human IgG1 Fc region containing this mapped center point.
該変異体を、抗CD20抗体 PRO70769(可変領域)および重鎖定常領域としてIgG1またはIgG(1/2)ELLGGのどちらかに照らして、上記の通りにコンストラクトした。変異体を、上記の通りに発現させて精製した。細胞ベースの分析を、Fc変異体がCDCを仲介する能力を測定するために用いた。溶解を、Fc変異体およびWT PRO70769によりオプソニン化したWIL2−Sリンパ腫細胞の溶解をヒト血清補体によりモニターするために、アラマーブルーの放出を用いて測定した。標的細胞を、10%FBS培地で遠心および再懸濁して3回洗浄し、WTまたは変異体リツキシマブ抗体を、示した最終濃度で添加した。ヒト血清補体(Quidel)を、培地を用いて50%に希釈し、抗体によりオプソニン化した標的細胞に添加した。補体の最終濃度は、原液の1/6であった。プレートを37℃で2時間インキュベートし、アラマーブルーを添加し、細胞を2日間インキュベートし、蛍光を測定した。この分析の代表的なデータを図14に示す。結合データを、低濃度および高濃度の抗体それぞれでのベースラインにより、それぞれの特定の曲線について最大および最小発光シグナルに標準化した。データを、非線形回帰を用いて傾き変化モデル(variable slope model)を含むシグモイド型用量応答に適合させ、これらの適合を、図に曲線で示す。これらの適合は、Fc変異体の相対的結合親和性を定量的に決定するのを可能にする、各抗体についての50%有効濃度(EC50)(すなわち、50%応答に必要な濃度)を提供する。各変異体のEC50をWT PRO70769のEC50で割ることにより、WT PRO70769(WT倍数)と比較した増加倍数または減少倍数を得た。これらの値を、図13に示す。ここで、1を超える倍数は、WT PRO70769と比較してCDC EC50の増大を示し、1より小さい倍数は、CDC EC50の減少を示す。 The mutants were constructed as described above in the light of anti-CD20 antibody PRO70769 (variable region) and either IgG1 or IgG (1/2) ELLGG as the heavy chain constant region. Mutants were expressed and purified as described above. Cell based analysis was used to determine the ability of Fc variants to mediate CDC. Lysis was measured using Alamar Blue release to monitor lysis of WIL2-S lymphoma cells opsonized with Fc variants and WT PRO70769 by human serum complement. Target cells were washed 3 times by centrifugation and resuspension in 10% FBS medium and WT or mutant rituximab antibody was added at the indicated final concentrations. Human serum complement (Quidel) was diluted to 50% using media and added to target cells opsonized with antibody. The final concentration of complement was 1/6 of the stock solution. Plates were incubated for 2 hours at 37 ° C., alamar blue was added, cells were incubated for 2 days, and fluorescence was measured. Representative data for this analysis is shown in FIG. Binding data was normalized to maximum and minimum luminescence signals for each particular curve by baseline at low and high concentrations of antibody, respectively. The data was fitted to a sigmoidal dose response including a variable slope model using non-linear regression, and these fits are shown as curves in the figure. These fits provide a 50% effective concentration (EC50) for each antibody (ie, the concentration required for a 50% response) that allows quantitative determination of the relative binding affinity of the Fc variants. To do. Dividing the EC50 of each mutant by the EC50 of WT PRO70769 yielded an fold increase or decrease fold compared to WT PRO70769 (WT fold). These values are shown in FIG. Here, multiples greater than 1 indicate an increase in CDC EC50 compared to WT PRO70769, and multiples less than 1 indicate a decrease in CDC EC50.
図13および14のデータは、WT PRO70769 IgG1と比較して増大したCDCを提供することを示す。例えば、2倍以上のCDCの増大が、修飾239D、267D、267Q、268D、268E、268F、268G、272I、276D、276L、276S、278R、282G、284T、285Y、293R、300T、324I、324T、324V、326E、326T、326W、327D、330H、330S、332E、333F、334Tおよび335Dで観察される(図15)。さらに、データは、多くの修飾体が、WT PRO70769 IgG1と比較して減少したCDCを提供することを示す。例えば、0.5倍以下の相対的CDCを示す修飾には、235D、239D、284D、322H、322T、322Y、327R、330E、330I、330L、330N、330V、331D、331Lおよび332Eが含まれる(図15)。これらの修飾は、増大したCDCのための変異体のさらなる設計を導くために用いられ得るさらなる有益な構造活性相関(SAR)情報を提供する。同時に、データは、235位、239位、267位、268位、272位、276位、278位、282位、284位、285位、293位、300位、322位、324位、326位、327位、330位、331位、332位、333位、334位および335位(図15)での修飾が、親Fcポリペプチドと比較して、増大したCDCを提供し得ることを示唆する。
The data in FIGS. 13 and 14 show that it provides increased CDC compared to WT PRO70769 IgG1. For example, a CDC increase of 2 or more is indicated by
実施例3.減少したFcγRおよび補体により仲介されるエフェクター機能を有するFc変異体
上記の通り、エフェクター機能が臨床効果に貢献する抗体治療および適応とは対照的に、いくつかの抗体および臨床適用に関して、1種以上のFcγRとの結合を減少するもしくは除去するか、またはADCC、ADCPおよび/またはCDCを含むが、これらに限定されない1個以上のFcγRまたは補体により仲介されるエフェクター機能を減少するもしくは除去するのが、好ましい。これはしばしば、その作用機序が標的抗原を有する細胞の死ではなく、その阻止または拮抗作用を伴う治療抗体の場合である。これらの場合において、標的細胞の減少は望ましくなく、副作用と見なされ得る。エフェクター機能はまた、放射性複合体と称される放射性標識抗体、および免疫毒素と称される毒素と複合体形成した抗体についての課題でもあり得る。これらの薬物を、癌細胞を破壊するために用いることができるが、FcとFcγRとの相互作用による免疫細胞の捕捉は、有害なペイロード(放射物または毒素)の近接域に健康な免疫細胞をもたらし、結果として標的癌細胞と共に正常なリンパ系組織の減少をもたらす。
Example 3 Fc variants with reduced FcγR and complement-mediated effector functions As described above, one type of antibody and clinical application, as opposed to antibody therapy and indications where effector function contributes to clinical efficacy Reduce or eliminate the above binding to FcγR, or reduce or eliminate effector function mediated by one or more FcγR or complement, including but not limited to ADCC, ADCP and / or CDC Is preferred. This is often the case for therapeutic antibodies whose mechanism of action is not the death of cells with the target antigen, but with its blocking or antagonism. In these cases, target cell reduction is undesirable and can be considered a side effect. Effector function may also be a challenge for radiolabeled antibodies called radioconjugates and antibodies complexed with toxins called immunotoxins. Although these drugs can be used to destroy cancer cells, the capture of immune cells by the interaction of Fc and FcγR can result in healthy immune cells in close proximity to harmful payloads (radioactive substances or toxins). Resulting in a decrease in normal lymphoid tissue with the target cancer cells.
低下したFcγR結合および補体結合の従来考慮されていなかった利点は、エフェクター機能が必要ない場合に、FcγRおよび補体との結合が、薬物の活性濃度を効果的に低下し得ることである。Fcリガンドとの結合は、抗体またはFc融合体、または血清タンパク質が遊離の(複合体を形成していない)ときと比較して活性が低いかまたは不活性である血清タンパク質との複合体を細胞表面に局在化させ得る。これは、抗体が所望される結合部位での低下した有効濃度のためか、または恐らく、Fcリガンド結合が、Fcポリペプチドを、非結合であった場合より活性が低い立体構造にし得るためである。さらなる考察は、FcγR受容体が、抗体のターンオーバーの1つ機序であり得ること、ならびに樹状細胞およびマクロファージのような抗原提示細胞による取り込みおよびプロセシングを仲介し得ることである。これは、抗体またはFc融合体の薬物動態(または、インビボ半減期)およびその免疫原性(両方とも、臨床パフォーマンスの重要なパラメーターである。)に影響を与え得る。 A previously unconsidered advantage of reduced FcγR binding and complement binding is that FcγR and complement binding can effectively reduce the active concentration of the drug when effector function is not required. Binding to the Fc ligand can be achieved by binding the antibody or Fc fusion, or a complex with a serum protein that is less active or inactive compared to when the serum protein is free (not complexed). Can be localized to the surface. This is because the antibody is at a reduced effective concentration at the desired binding site, or perhaps because Fc ligand binding can render the Fc polypeptide a less active conformation than if unbound. . A further consideration is that FcγR receptors may be one mechanism of antibody turnover and mediate uptake and processing by antigen presenting cells such as dendritic cells and macrophages. This can affect the pharmacokinetics (or in vivo half-life) of the antibody or Fc fusion and its immunogenicity (both are important parameters of clinical performance).
Fc/FcγR構造(図2)および上記のFc/C1q接合部位(図12)の外観図、ならびに上記およびUSSN10/672,280、USSN10/822,231、USSN11/124,620、およびUSSN11/256,060(全て参照によりその全体が本明細書中に包含される)のデータを、FcγRに対する減少した親和性、および減少したCDCを有する変異体をスクリーニングするためのライブラリーの設計の指針に用いた。この変異体ライブラリーを図16に示す。変異体を、PRO70769 IgG1に照らしてコンストラクトし、上記の通り発現させ精製した。相対的FcγR親和性を、上記の通りに、AlphaScreen競合アッセイを用いて測定した。図17は、選択したFc変異体のヒトV158 FcγRIIIaとの結合についてのAlphaScreenデータを示し、図16は、WT PRO70769 IgG1と比較したそのIC50倍数を示す。変異体を、上記のCDCアッセイを用いて、CD20+WIL2−Sリンパ腫標的細胞に対する補体仲介性溶解を仲介するその能力についても調べた。図18は、選択したFc変異体のCDCデータを示し、図16は、WT PRO70769 IgG1と比較したEC50倍数を示す。これらの実験の結果に基づき、選択したFc変異体を、FcγRにより仲介されるエフェクター機能を仲介するその能力について特徴付けた。ヒトPBMCをエフェクター細胞として、およびWIL2−Sリンパ腫細胞を標的細胞として用いるADCCアッセイを、上記の通りに行った。図19は、選択した変異体についてのこれらのADCCデータを示す。
Appearance of the Fc / FcγR structure (FIG. 2) and the Fc / C1q junction (FIG. 12), and the above and
データは、多くの位置での修飾が、減少または低下したFcγR親和性、減少したFcγRにより仲介されるエフェクター機能、および減少した補体により仲介されるエフェクター機能を提供することを示す。さらに、235および330位を含むがこれらに限定されないいくつかの位置での修飾は、減少したCDCを提供するが、FcγR親和性はWTレベルであり得る。例えば、235D、330L、330Nおよび330Rは、そのような作用を示す。あるいは、236位および299位を含むがこれらに限定されないいくつかの位置における修飾は、減少したFcγR親和性を提供するが、CDCはWTレベルであり得る。例えば、236Iおよび299Aは、これらの特性を示す。
The data indicate that modifications at many positions provide reduced or reduced FcγR affinity, reduced FcγR-mediated effector function, and reduced complement-mediated effector function. Furthermore, modifications at several positions, including but not limited to
これらの実験の結果に基づき、FcγR親和性およびCDCを同時に低下する多くの修飾を、完全に低下したFcγR親和性、FcγRにより仲介されるエフェクター機能、および補体により仲介されるエフェクター機能を有する変異体をスクリーニングするために設計されたFc変異体の新しいライブラリー中の多数の変異を有する変異体に組み合わせた。これらの変異体は、234位、235位、236位、267位、269位、325位および328位での修飾を含み、図20に示す。WT IgG1抗体、ならびにIgG2およびIgG4抗体変異体、グリコシル化変異体N297S、および減少したエフェクター機能を有することが既に特徴付けられた2つの変異体:L234A/L235A(Xu et al., 2000, Cellular Immunology 200:16−26;USSN10/267,286、参照によりその全体が本明細書中に包含される)、およびE233P/L234V/L235A/G236−(Armour et al., 1999, Eur J Immunol 29:2613−2624、参照によりその全体が本明細書中に包含される)が、包含される。
Based on the results of these experiments, many modifications that simultaneously reduce FcγR affinity and CDC can be achieved by mutations with fully reduced FcγR affinity, effector function mediated by FcγR, and effector function mediated by complement. Combined with variants with multiple mutations in a new library of Fc variants designed to screen the body. These variants include modifications at
これらの変異体を、IgG2およびIgG4抗体以外の重鎖定常領域であるIgG1を含み、抗CD20抗体 PRO70769に照らしてコンストラクトした。抗体を、上記の通りに発現させ精製した。AlphaScreen競合アッセイを、Fc変異体の相対的FcγR親和性を測定するために、上記の通りに用いた。図21は、選択した変異体の、低親和性のヒト活性化受容体V158 FcγRIIIa、ならびに高親和性のヒト活性化受容体FcγRIとの結合についてのAlphaScreenデータを示す。WTと比較したIC50倍数を、図20に示す。Fc領域に対するそのより大きな結合親和性のため、FcγRIは、変異体のよりストリンジェントな試験を提供する。図20および21のデータはこれを支持し、変異体は、FcγRIIIaに対する親和性を実質的に減少し得るかまたは完全に低下し得るが、FcγRI結合にはあまり影響しないことを示す。Fc変異体はまた、上記のCDCアッセイを用いて、CD20+WIL2−S細胞に対して補体仲介性溶解を仲介するそれらの能力を試験した。図22は、選択したFc変異体についてのCDCデータを示し、図20は、WT PRO70769 IgG1と比較したEC50倍数を示す。 These variants contained IgG1, which is a heavy chain constant region other than IgG2 and IgG4 antibodies, and were constructed against the anti-CD20 antibody PRO70769. The antibody was expressed and purified as described above. The AlphaScreen competition assay was used as described above to determine the relative FcγR affinity of Fc variants. FIG. 21 shows AlphaScreen data for binding of selected variants to the low affinity human activated receptor V158 FcγRIIIa as well as the high affinity human activated receptor FcγRI. FIG. 20 shows the IC multiple of 50 compared with WT. Due to its greater binding affinity for the Fc region, FcγRI provides a more stringent test of variants. The data in FIGS. 20 and 21 support this and show that the mutant can substantially reduce or completely reduce the affinity for FcγRIIIa but has little effect on FcγRI binding. Fc variants were also tested for their ability to mediate complement-mediated lysis against CD20 + WIL2-S cells using the CDC assay described above. FIG. 22 shows CDC data for selected Fc variants and FIG. 20 shows EC50 fold compared to WT PRO70769 IgG1.
Fc変異体がADCCを仲介する能力を調べるため、選択した変異体を、抗Her2/neu抗体であるトラスツズマブ(可変領域配列を、図24cおよび24dに示す)中にサブクローニングした。トラスツズマブは、Her2+発現細胞系に対してADCCアッセイにおいて実質的なシグナルを確実に提供し、故に、エフェクター機能を減少/低下するFc変異体の厳しい検査を提供する。Fc変異体L235G、G236R、G237K、N325L、N325A、L328R、L235G/G236R、G236R/G237K、G236R/N325L、G236R/L328R、G237K/N325L、L235G/G236R/G237KおよびG236R/G237K/L328Rを、トラスツズマブIgG1に照らしてコンストラクトした。WT IgG1、WT IgG2およびWT IgG4抗体変異体を、同様にコンストラクトした。ADCCアッセイを、Her2+乳癌細胞系SkBr−3を標的細胞として用いた以外、上記の通りに行った。図23は、ADCC実験の結果を示す。データは、いくつかの変異体が、ADCCを完全に低下することを示す。さらに、IgG2はまた、ADCCを仲介しないことが明らかであるが、IgG4は、かなりのレベルのADCCを示す。 To examine the ability of Fc variants to mediate ADCC, selected variants were subcloned into trastuzumab, an anti-Her2 / neu antibody (variable region sequences are shown in FIGS. 24c and 24d). Trastuzumab reliably provides a substantial signal in the ADCC assay to the Her2 + expressing cell line and thus provides a rigorous examination of Fc variants that reduce / reduce effector function. Fc variants L235G, G236R, G237K, N325L, N325A, L328R, L235G / G236R, G236R / G237K, G236R / N325L, G236R / L328R, G237K / N325L, L235G / G236R / G236K / G236R / G236K Constructed in the light of WT IgG1, WT IgG2 and WT IgG4 antibody variants were similarly constructed. The ADCC assay was performed as described above except that Her2 + breast cancer cell line SkBr-3 was used as the target cell. FIG. 23 shows the results of the ADCC experiment. The data shows that some variants completely reduce ADCC. Furthermore, IgG2 also appears to not mediate ADCC, whereas IgG4 exhibits a significant level of ADCC.
結果は、232位、234位、235位、236位、237位、238位、239位、265位、267位、269位、270位、297位、299位、325位、327位、328位、329位、330位および331位を含むが、これらに限定されない多くの位置でのアミノ酸修飾が、FcγR結合、FcγRにより仲介されるエフェクター機能、および/または補体仲介性エフェクター機能が所望されない、抗体およびFc融合体の臨床特性を改善するための有望な候補を提供することを示す。例えば、アミノ酸修飾232G、234G、234H、235D、235G、235H、236I、236N、236P、236R、237K、237L、237N、237P、238K、239R、265G、267R、269R、270H、297S、299A、299I、299V、325A、325L、327R、328R、329K、330I、330L、330N、330P、330R、330Sおよび331Lは、顕著に減少したFcリガンド結合特性および/またはエフェクター機能を提供する。Fcリガンドとの結合およびエフェクター機能を減少するのに特に有効なのは、変異体236R/237K、236R/325L、236R/328R、237K/325L、237K/328R、325L/328R、235G/236R、267R/269R、234G/235G、236R/237K/325L、236R/325L/328R、235G/236R/237K、および237K/325L/328Rである。特に、234G、235G、236R、237K、267R、269R、325L、および328Rを含むこれらの変異体を含むアミノ酸修飾は、FcγRIIIaおよびFcγRIの両方との結合を減少し、10倍以上CDCを減少させ得る。さらに、データは、ヒトIgG2が、ヒトIgG4と比較して、顕著に減少したFcγR親和性、FcγRにより仲介されるエフェクター機能、および補体により仲介されるエフェクター機能を有することを示す。
Results are 232, 234, 235, 236, 237, 238, 239, 265, 267, 269, 270, 297, 299, 325, 327, 328 Amino acid modifications at a number of positions, including but not limited to
上記の通り、減少したFcγR親和性および/またはエフェクター機能は、Fcリガンド結合またはエフェクター機能が毒性および/または減少した効果をもたらすFcポリペプチドに最適であり得る。例えば、CTLA4を標的とする抗体がT細胞活性化の阻害を阻止し、抗腫瘍免疫応答を促進するのに有効であるが、抗体により仲介されるエフェクター機能によるT細胞の破壊は、作用機序および/または潜在的な毒性に逆効果となり得る。実際の毒性は、抗CTLA4抗体であるイピリムマブの臨床適用で観察した(Maker et al., 2005, Ann Surg Oncol 12:1005−16、参照によりその全体が本明細書中に包含される)。US6,984,720の配列番号7(VL、図24e)および配列番号17(VH、図24f)(参照により本明細書中にその全体が包含される)から抜粋した、抗CTLA4抗体であるイピリムマブ(Mab 10D.1、MDX010)の配列を、図24に示す。説明を目的として、本発明の多くのFc変異体を、CTLA4を標的とする抗体の配列中に組み込む。本発明のFc変異体の組み合わせが、典型的に、相加的または相乗的結合調節、それによるエフェクター機能の相加的または相乗的調節をもたらしたため、本発明で供されるFc変異体の未だ明らかになっていない組み合わせ、または他の既報の修飾との組み合わせがまた、好ましい結果を提供し得ることが、予想される。可能性のあるFc変異体を図26aに示す。最適化した抗体配列には、X1、X2、X3、X4、X5、X6、X7、およびX8からなる群から選択される少なくとも1個の非WTアミノ酸が含まれる。例えば、IgG1定常領域中L235GおよびG236R修飾を含む改良された抗CTLA−4抗体配列を、図26bおよび26cに示す。あるいは、本発明が示す通り、IgG2およびIgG4を、Fcリガンド結合およびFcにより仲介されるエフェクター機能を減少するためにも用い得る。図26bおよび26dは、改良した抗CTLA4 IgG2抗体配列の配列を提供する。本明細書中、抗CTLA4の使用は、単なる一例であり、Fc変異体の適用をこの抗体または何れか他の特定のFcポリペプチドに制限することを意味しない。減少したFcリガンド結合および/またはエフェクター機能の他の例示的適用には、例えばインフリキシマブおよびアダリムマブを含む抗TNFα抗体、例えばベバシツマブを含む抗VEGF抗体、例えばナタリズマブを含む抗α4−インテグリン抗体、および例えばUSSN10/643,857(参照により本明細書中にその全体が包含される)に記載のものを含む抗CD32b抗体が含まれるが、これらに限定されない。 As noted above, decreased FcγR affinity and / or effector function may be optimal for Fc polypeptides where Fc ligand binding or effector function results in toxic and / or reduced effects. For example, antibodies targeting CTLA4 are effective in preventing inhibition of T cell activation and promoting an anti-tumor immune response, but destruction of T cells by effector functions mediated by antibodies is And / or adverse effects on potential toxicity. Actual toxicity was observed in clinical application of ipilimumab, an anti-CTLA4 antibody (Maker et al., 2005, Ann Surg Oncol 12: 1005-16, which is hereby incorporated by reference in its entirety). Ipilimumab, an anti-CTLA4 antibody, extracted from SEQ ID NO: 7 (VL, FIG. 24e) and SEQ ID NO: 17 (VH, FIG. 24f) of US 6,984,720 (incorporated herein in its entirety by reference) The sequence of (Mab 10D.1, MDX010) is shown in FIG. For purposes of illustration, many Fc variants of the present invention are incorporated into the sequence of antibodies that target CTLA4. Since the combination of Fc variants of the present invention typically resulted in additive or synergistic binding modulation and thereby additive or synergistic modulation of effector function, the Fc variants provided in the present invention are still It is expected that combinations that have not been elucidated or in combination with other previously reported modifications may also provide favorable results. A possible Fc variant is shown in Figure 26a. The optimized antibody sequence includes at least one non-WT amino acid selected from the group consisting of X 1 , X 2 , X 3 , X 4 , X 5 , X 6 , X 7 , and X 8 . For example, improved anti-CTLA-4 antibody sequences comprising L235G and G236R modifications in the IgG1 constant region are shown in FIGS. 26b and 26c. Alternatively, as the present invention shows, IgG2 and IgG4 can also be used to reduce Fc ligand binding and Fc-mediated effector functions. Figures 26b and 26d provide the sequence of the improved anti-CTLA4 IgG2 antibody sequence. Herein, the use of anti-CTLA4 is only an example and does not imply that the application of the Fc variant is limited to this antibody or any other specific Fc polypeptide. Other exemplary applications of reduced Fc ligand binding and / or effector function include anti-TNFα antibodies including, for example, infliximab and adalimumab, anti-VEGF antibodies including, for example, bevacizumab, anti-α4-integrin antibodies including, for example, natalizumab, and USSN10 Anti-CD32b antibodies, including but not limited to those described in US Pat. No. 6,643,857, which is hereby incorporated by reference in its entirety.
好ましいFc変異体のこのリストは、本発明を制限することを意味しない。実際に、供される何れかのFc変異体の全ての組み合わせが、本発明の態様を提供する。さらに、本発明の何れかのFc変異体と他の発見されたまたは未発見のFc変異体との組み合わせも、好ましい特性を提供することができ、これらの組み合わせはまた、本発明の態様として意図される。最後に、これらの結果から、本発明において変異した位置での他の置換が、好ましい結合増大および特異性も提供し得ること、故に、本明細書に記載の全ての位置での置換が考慮されることが予想される。 This list of preferred Fc variants is not meant to limit the invention. Indeed, all combinations of any Fc variants provided provide aspects of the invention. Furthermore, combinations of any Fc variants of the present invention with other discovered or undiscovered Fc variants can also provide favorable properties, and these combinations are also contemplated as aspects of the present invention. Is done. Finally, from these results, other substitutions at mutated positions in the present invention may also provide favorable binding enhancement and specificity, and therefore substitutions at all positions described herein are considered. Is expected.
全ての引用される文献は、参照により本明細書中にその全体が明示的に包含される。 All cited references are expressly incorporated herein in their entirety by reference.
本発明の特定の態様は、説明を目的として上記されるが、多数の変形が、添付の特許請求の範囲に記載の通り、本発明から逸脱しない範囲で製造され得ることは、当業者に認められるだろう。 While particular embodiments of the present invention have been described above for purposes of illustration, those skilled in the art will recognize that numerous modifications can be made without departing from the present invention as set forth in the appended claims. Will be.
Claims (18)
Applications Claiming Priority (6)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US66719705P | 2005-03-31 | 2005-03-31 | |
| US11/124,620 US8188231B2 (en) | 2002-09-27 | 2005-05-05 | Optimized FC variants |
| US70537805P | 2005-08-03 | 2005-08-03 | |
| US72329405P | 2005-10-03 | 2005-10-03 | |
| US72333505P | 2005-10-03 | 2005-10-03 | |
| PCT/US2006/011752 WO2006105338A2 (en) | 2005-03-31 | 2006-03-31 | Fc VARIANTS WITH OPTIMIZED PROPERTIES |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2008537941A true JP2008537941A (en) | 2008-10-02 |
Family
ID=39916248
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008504389A Pending JP2008537941A (en) | 2005-03-31 | 2006-03-31 | Fc variants with optimized properties |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2008537941A (en) |
Cited By (22)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPWO2010126137A1 (en) * | 2009-05-01 | 2012-11-01 | 国立大学法人 東京大学 | Anti-cadherin antibody |
| JP2013515472A (en) * | 2009-12-23 | 2013-05-09 | シュニムネ ゲーエムベーハー | Anti-FLT3 antibody and method of use thereof |
| JP2013529908A (en) * | 2010-05-27 | 2013-07-25 | メルク・シャープ・エンド・ドーム・コーポレイション | Method for producing antibodies having improved properties |
| JP2015532278A (en) * | 2012-09-27 | 2015-11-09 | メルス・ベー・フェー | Bispecific IgG antibody as a T cell engager |
| JP2015533490A (en) * | 2012-09-12 | 2015-11-26 | ジェンザイム・コーポレーション | Fc-containing polypeptides with altered glycosylation and reduced effector function |
| JP2016512425A (en) * | 2013-03-11 | 2016-04-28 | ジェンザイム・コーポレーション | Highly glycosylated binding polypeptide |
| JP2018515072A (en) * | 2015-05-04 | 2018-06-14 | アポジェニックス アーゲー | Single chain CD40 receptor agonist protein |
| US10064952B2 (en) | 2014-10-09 | 2018-09-04 | Genzyme Corporation | Glycoengineered antibody drug conjugates |
| JP2018533948A (en) * | 2015-10-23 | 2018-11-22 | アポジェニックス アーゲー | Single chain LIGHT receptor agonist protein |
| JP2018533947A (en) * | 2015-10-23 | 2018-11-22 | アポジェニックス アーゲー | Single chain CD27 receptor agonist protein |
| JP2019500850A (en) * | 2015-10-23 | 2019-01-17 | アポジェニックス アーゲー | Single-chain CD137 receptor agonist protein |
| WO2020204152A1 (en) * | 2019-04-04 | 2020-10-08 | 小野薬品工業株式会社 | Bispecific antibody |
| US10836813B2 (en) | 2012-09-12 | 2020-11-17 | Genzyme Corporation | Fc containing polypeptides with altered glycosylation and reduced effector function |
| JP2021501575A (en) * | 2017-11-02 | 2021-01-21 | システィミューン, インク.Systimmune, Inc. | Bispecific antibody and its production method and usage method |
| JP2021019632A (en) * | 2011-12-23 | 2021-02-18 | ファイザー・インク | Engineered antibody constant regions for site-specific conjugation and methods and uses therefor |
| US11186638B2 (en) | 2011-09-12 | 2021-11-30 | Genzyme Corporation | Anti-αβTCR antibody |
| JP2022513653A (en) * | 2018-11-28 | 2022-02-09 | ブリストル-マイヤーズ スクイブ カンパニー | Antibodies containing modified heavy chain constant regions |
| JP2022060182A (en) * | 2020-10-02 | 2022-04-14 | 小野薬品工業株式会社 | Pharmaceutical composition comprising bispecific antibody as active ingredient |
| JP2022534498A (en) * | 2019-05-29 | 2022-08-01 | オービス ヘルス ソリューションズ エルエルシー | Delivery vectors and particles for expressing chimeric receptors and methods of use thereof |
| US11697690B2 (en) | 2014-03-19 | 2023-07-11 | Genzyme Corporation | Site-specific glycoengineering of targeting moieties |
| JP2024515014A (en) * | 2021-03-19 | 2024-04-04 | ユニヴェルシテ・トゥールーズ・トロワ-ポール・サバティエ | Hybrid molecules comprising an antibody Fc fragment and at least one fibrin-derived citrullinated peptide and uses thereof - Patents.com |
| US12365734B2 (en) | 2019-04-03 | 2025-07-22 | Genzyme Corporation | Anti-alpha beta TCR binding polypeptides with reduced fragmentation |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2004029207A2 (en) * | 2002-09-27 | 2004-04-08 | Xencor Inc. | Optimized fc variants and methods for their generation |
| WO2004099249A2 (en) * | 2003-05-02 | 2004-11-18 | Xencor, Inc. | Optimized fc variants and methods for their generation |
-
2006
- 2006-03-31 JP JP2008504389A patent/JP2008537941A/en active Pending
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2004029207A2 (en) * | 2002-09-27 | 2004-04-08 | Xencor Inc. | Optimized fc variants and methods for their generation |
| WO2004099249A2 (en) * | 2003-05-02 | 2004-11-18 | Xencor, Inc. | Optimized fc variants and methods for their generation |
Cited By (46)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9017683B2 (en) | 2009-05-01 | 2015-04-28 | The University Of Tokyo | Highly effective anti-cadherin antibody for induction of antibody-dependent cellular cytotoxicity in vivo |
| JPWO2010126137A1 (en) * | 2009-05-01 | 2012-11-01 | 国立大学法人 東京大学 | Anti-cadherin antibody |
| JP2013515472A (en) * | 2009-12-23 | 2013-05-09 | シュニムネ ゲーエムベーハー | Anti-FLT3 antibody and method of use thereof |
| US11959118B2 (en) | 2010-05-27 | 2024-04-16 | Merck Sharp & Dohme Llc | Fc-containing polypeptides having improved properties and comprising mutations at positions 243 and 264 of the Fc-region |
| JP2013529908A (en) * | 2010-05-27 | 2013-07-25 | メルク・シャープ・エンド・ドーム・コーポレイション | Method for producing antibodies having improved properties |
| US10858686B2 (en) | 2010-05-27 | 2020-12-08 | Merck Sharp & Dohme Corp. | Method for preparing antibodies having improved properties |
| US11186638B2 (en) | 2011-09-12 | 2021-11-30 | Genzyme Corporation | Anti-αβTCR antibody |
| JP7165175B2 (en) | 2011-12-23 | 2022-11-02 | ファイザー・インク | Engineered Antibody Constant Regions for Site-Specific Conjugation, and Methods and Uses Therefor |
| JP2021019632A (en) * | 2011-12-23 | 2021-02-18 | ファイザー・インク | Engineered antibody constant regions for site-specific conjugation and methods and uses therefor |
| US12503498B2 (en) | 2012-09-12 | 2025-12-23 | Genzyme Corporation | Fc containing polypeptides with altered glycosylation and reduced effector function |
| JP2015533490A (en) * | 2012-09-12 | 2015-11-26 | ジェンザイム・コーポレーション | Fc-containing polypeptides with altered glycosylation and reduced effector function |
| US10836813B2 (en) | 2012-09-12 | 2020-11-17 | Genzyme Corporation | Fc containing polypeptides with altered glycosylation and reduced effector function |
| JP2019068803A (en) * | 2012-09-27 | 2019-05-09 | メルス ナムローゼ フェンノートシャップ | Bispecific IgG antibodies as T cell engagers |
| JP2015532278A (en) * | 2012-09-27 | 2015-11-09 | メルス・ベー・フェー | Bispecific IgG antibody as a T cell engager |
| JP2023099146A (en) * | 2013-03-11 | 2023-07-11 | ジェンザイム・コーポレーション | Highly glycosylated binding polypeptide |
| JP2019103514A (en) * | 2013-03-11 | 2019-06-27 | ジェンザイム・コーポレーション | Hyperglycosylated binding polypeptides |
| US10494439B2 (en) | 2013-03-11 | 2019-12-03 | Genzyme Corporation | Hyperglycosylated binding polypeptides |
| JP2016512425A (en) * | 2013-03-11 | 2016-04-28 | ジェンザイム・コーポレーション | Highly glycosylated binding polypeptide |
| US10214589B2 (en) | 2013-03-11 | 2019-02-26 | Genzyme Corporation | Site-specific antibody-drug conjugation through glycoengineering |
| JP7321206B2 (en) | 2013-03-11 | 2023-08-04 | ジェンザイム・コーポレーション | Highly glycosylated binding polypeptide |
| US12110338B2 (en) | 2013-03-11 | 2024-10-08 | Genzyme Corporation | Site-specific antibody-drug conjugation through glycoengineering |
| US11807690B2 (en) | 2013-03-11 | 2023-11-07 | Genzyme Corporation | Hyperglycosylated binding polypeptides |
| JP2021106600A (en) * | 2013-03-11 | 2021-07-29 | ジェンザイム・コーポレーション | Hyperglycosylated binding polypeptide |
| US11130816B2 (en) | 2013-03-11 | 2021-09-28 | Genzyme Corporation | Site-specific antibody-drug conjugation through glycoengineering |
| JP7121675B2 (en) | 2013-03-11 | 2022-08-18 | ジェンザイム・コーポレーション | Highly glycosylated binding polypeptide |
| JP2016512426A (en) * | 2013-03-11 | 2016-04-28 | ジェンザイム・コーポレーション | Site-specific antibody-drug conjugation by saccharide engineering |
| US11697690B2 (en) | 2014-03-19 | 2023-07-11 | Genzyme Corporation | Site-specific glycoengineering of targeting moieties |
| US11160874B2 (en) | 2014-10-09 | 2021-11-02 | Genzyme Corporation | Glycoengineered antibody drug conjugates |
| US10064952B2 (en) | 2014-10-09 | 2018-09-04 | Genzyme Corporation | Glycoengineered antibody drug conjugates |
| JP2018515072A (en) * | 2015-05-04 | 2018-06-14 | アポジェニックス アーゲー | Single chain CD40 receptor agonist protein |
| JP2019500850A (en) * | 2015-10-23 | 2019-01-17 | アポジェニックス アーゲー | Single-chain CD137 receptor agonist protein |
| JP7033062B2 (en) | 2015-10-23 | 2022-03-09 | アポジェニックス アーゲー | Single-stranded CD137 receptor agonist protein |
| JP2018533948A (en) * | 2015-10-23 | 2018-11-22 | アポジェニックス アーゲー | Single chain LIGHT receptor agonist protein |
| JP2018533947A (en) * | 2015-10-23 | 2018-11-22 | アポジェニックス アーゲー | Single chain CD27 receptor agonist protein |
| JP7418326B2 (en) | 2017-11-02 | 2024-01-19 | システィミューン, インク. | Bispecific antibodies and their production and use methods |
| JP2021501575A (en) * | 2017-11-02 | 2021-01-21 | システィミューン, インク.Systimmune, Inc. | Bispecific antibody and its production method and usage method |
| JP2022513653A (en) * | 2018-11-28 | 2022-02-09 | ブリストル-マイヤーズ スクイブ カンパニー | Antibodies containing modified heavy chain constant regions |
| US12365734B2 (en) | 2019-04-03 | 2025-07-22 | Genzyme Corporation | Anti-alpha beta TCR binding polypeptides with reduced fragmentation |
| JP2024009224A (en) * | 2019-04-04 | 2024-01-19 | 小野薬品工業株式会社 | bispecific antibody |
| JP7688805B2 (en) | 2019-04-04 | 2025-06-05 | 小野薬品工業株式会社 | bispecific antibody |
| US12325746B2 (en) | 2019-04-04 | 2025-06-10 | Ono Pharmaceutical Co., Ltd. | Bispecific antibody |
| WO2020204152A1 (en) * | 2019-04-04 | 2020-10-08 | 小野薬品工業株式会社 | Bispecific antibody |
| JP2022534498A (en) * | 2019-05-29 | 2022-08-01 | オービス ヘルス ソリューションズ エルエルシー | Delivery vectors and particles for expressing chimeric receptors and methods of use thereof |
| JP2022060182A (en) * | 2020-10-02 | 2022-04-14 | 小野薬品工業株式会社 | Pharmaceutical composition comprising bispecific antibody as active ingredient |
| JP7714992B2 (en) | 2020-10-02 | 2025-07-30 | 小野薬品工業株式会社 | Pharmaceutical composition containing a bispecific antibody as an active ingredient |
| JP2024515014A (en) * | 2021-03-19 | 2024-04-04 | ユニヴェルシテ・トゥールーズ・トロワ-ポール・サバティエ | Hybrid molecules comprising an antibody Fc fragment and at least one fibrin-derived citrullinated peptide and uses thereof - Patents.com |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| AU2006230413B2 (en) | Fc variants with optimized properties | |
| US9040041B2 (en) | Modified FC molecules | |
| US20060235208A1 (en) | Fc variants with optimized properties | |
| AU2016234983B2 (en) | Fc variants with altered binding to FcRn | |
| KR101573883B1 (en) | Fc VARIANTS WITH ALTERED BINDING TO FcRn | |
| JP4652414B2 (en) | Fc variants with altered binding to FcRn | |
| US20060134105A1 (en) | IgG immunoglobulin variants with optimized effector function | |
| US20100093979A1 (en) | Fc Polypeptides With Novel Fc Ligand Binding Sites | |
| JP2018088938A (en) | Methods for purifying antibodies | |
| WO2006047350A2 (en) | IgG IMMUNOGLOBULIN VARIANTS WITH OPTIMIZED EFFECTOR FUNCTION | |
| CN101098890B (en) | Fc variants with altered binding to fcrn | |
| JP2008537941A (en) | Fc variants with optimized properties | |
| US20070275460A1 (en) | Fc Variants With Optimized Fc Receptor Binding Properties | |
| AU2016203334A1 (en) | Fc variants with altered binding to FcRn |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20101101 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20110201 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20110208 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20110905 |