JP2008260689A - Pharmaceutical composition containing peptide derived from HLA-A24 molecule binding parathyroid hormone related protein - Google Patents
Pharmaceutical composition containing peptide derived from HLA-A24 molecule binding parathyroid hormone related protein Download PDFInfo
- Publication number
- JP2008260689A JP2008260689A JP2005221399A JP2005221399A JP2008260689A JP 2008260689 A JP2008260689 A JP 2008260689A JP 2005221399 A JP2005221399 A JP 2005221399A JP 2005221399 A JP2005221399 A JP 2005221399A JP 2008260689 A JP2008260689 A JP 2008260689A
- Authority
- JP
- Japan
- Prior art keywords
- cancer
- peptide
- hla
- molecule
- cells
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/22—Hormones
- A61K38/29—Parathyroid hormone, i.e. parathormone; Parathyroid hormone-related peptides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/04—Antineoplastic agents specific for metastasis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Chemical & Material Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Endocrinology (AREA)
- Zoology (AREA)
- Gastroenterology & Hepatology (AREA)
- Immunology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Epidemiology (AREA)
- Oncology (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
Abstract
Description
本発明は、HLA-A24分子結合性副甲状腺ホルモン関連蛋白由来ペプチドを含有する、癌、特に胃癌、腎癌、大腸癌または子宮頸癌を処置または予防するための医薬組成物に関する。 The present invention relates to a pharmaceutical composition for treating or preventing cancer, particularly gastric cancer, renal cancer, colon cancer or cervical cancer, comprising a peptide derived from HLA-A24 molecule-binding parathyroid hormone-related protein.
初期段階の癌患者の多くにとって外科的切除と化学療法は有効な治療方法である。しかしながら現在利用可能な治療方法は、再発時や進行期の癌にはそれほど有効ではない。遠隔転移を有する癌患者の予後は非常に悪く、そのような患者のための新しい治療方法の提供が急務である。現在検討されている方法の1つが特異的免疫療法であり、なかでもペプチド基盤ワクチンは、癌に対する全身性免疫のための簡便かつ魅力的な方法を提供すると考えられる。 Surgical excision and chemotherapy are effective treatments for many early stage cancer patients. However, currently available treatment methods are not very effective for recurrent or advanced stage cancer. The prognosis for cancer patients with distant metastases is very poor, and it is urgent to provide new treatment methods for such patients. One of the methods currently under investigation is specific immunotherapy, and peptide-based vaccines are considered to provide a convenient and attractive method for systemic immunity against cancer.
副甲状腺ホルモン関連蛋白 (PTH-rP)は、副甲状腺ホルモン (PTH)と構造的に類似することからそのように名付けられた (非特許文献1)。PTH-rPは、悪性高カルシウム血症に関与すると考えられている (非特許文献2)。さらにPTH-rPは、初期前立腺癌の90%に発現し、かつ骨転移の発症に重要な分子であることが知られている (非特許文献3、4)。それゆえこの分子は、骨転移を有する癌患者に対する免疫療法的治療において有望な標的分子と考えられている(非特許文献3)。本発明者らは、HLA-A24またはHLA-A2分子陽性前立腺癌患者に対するペプチド基盤免疫療法に利用可能なPTH-rP由来ペプチドを同定している(非特許文献5、6)。
本発明は、前立腺癌だけでなく、骨転移を有する各種癌タイプの癌患者に対するペプチド基盤免疫療法を可能とする医薬組成物を提供することを目的とする。 An object of the present invention is to provide a pharmaceutical composition that enables peptide-based immunotherapy not only for prostate cancer but also for cancer patients of various cancer types having bone metastasis.
本発明者らは、PTH-rPが様々な癌タイプの患者に対する特異的免疫療法において共通の標的分子と成りうるかについて検討した。はじめに、各種腫瘍細胞株のPTH-rPのmRNAおよびタンパク質レベルでの発現を、RT-PCR、フローサイトメトリーおよび免疫細胞化学によって検討した。PTH-rP mRNAは、胃癌、腎癌、大腸癌、子宮頸癌、肺癌および乳癌細胞株の大部分に発現しており、フローサイトメトリーおよび免疫細胞化学によりタンパク質レベルでの発現も確認できた。次に、HLA-A24分子陽性の胃癌、腎癌、大腸癌および子宮頸癌患者の末梢血単核細胞(PBMC)を2種類のPTH-rPペプチド(PTH-rP102-111およびPTH-rP110-119ペプチド)でin vitro刺激し、癌反応性の細胞傷害性Tリンパ球(CTL)を誘導できるかについて検討した。これらペプチドは、各種癌タイプのHLA-A24分子陽性患者のPBMCからPTH-rPペプチド特異的癌反応性CTLを誘導することができた。以上の結果に基づき本発明が完成した。 The present inventors examined whether PTH-rP could be a common target molecule in specific immunotherapy for patients with various cancer types. First, the expression of PTH-rP at various mRNA and protein levels in various tumor cell lines was examined by RT-PCR, flow cytometry and immunocytochemistry. PTH-rP mRNA was expressed in most of gastric cancer, renal cancer, colon cancer, cervical cancer, lung cancer and breast cancer cell lines, and expression at the protein level could be confirmed by flow cytometry and immunocytochemistry. Next, peripheral blood mononuclear cells (PBMCs) of HLA-A24 molecule positive gastric cancer, renal cancer, colon cancer and cervical cancer patients were treated with two types of PTH-rP peptides (PTH-rP102-111 and PTH-rP110-119). Peptides) in vitro to examine whether cancer-reactive cytotoxic T lymphocytes (CTL) can be induced. These peptides were able to induce PTH-rP peptide-specific cancer-reactive CTLs from PBMCs of HLA-A24 molecule positive patients of various cancer types. The present invention has been completed based on the above results.
本発明は、以下のものを提供する:
(1)HLA-A24分子結合性副甲状腺ホルモン関連蛋白由来ペプチドまたは機能的に同等の性質を有するその誘導体を含む、癌(但し前立腺癌を除く)を処置または予防するための医薬組成物;
(2)癌が胃癌、腎癌、大腸癌および子宮頸癌よりなる群から選択される、(1)記載の医薬組成物;
(3)癌が骨転移性である、(1)または(2)記載の医薬組成物;
(4)ペプチドが配列番号1または2に示すアミノ酸配列を有する、(1)から(3)までのいずれかに記載の医薬組成物;
(5)癌の転移性骨病変を処置または予防するためのものである、(1)から(4)までのいずれかに記載の医薬組成物;
(6)HLA-A24分子結合性副甲状腺ホルモン関連蛋白由来ペプチドまたは機能的に同等の性質を有するその誘導体を発現するベクターを含む、癌(但し前立腺癌を除く)を処置または予防するための医薬組成物;
(7)HLA-A24分子結合性副甲状腺ホルモン関連蛋白由来ペプチドまたは機能的に同等の性質を有するその誘導体とHLA-A24分子陽性癌患者(但し前立腺癌患者を除く)より採取された末梢血単核細胞とを接触させることを含む、癌反応性細胞傷害性T細胞を誘導する方法;
(8)HLA-A24分子結合性副甲状腺ホルモン関連蛋白由来ペプチドまたは機能的に同等の性質を有するその誘導体を含む、癌(但し前立腺癌を除く)反応性細胞傷害性T細胞を誘導するためのキット;
(9)HLA-A24分子結合性副甲状腺ホルモン関連蛋白由来ペプチドまたは機能的に同等の性質を有するその誘導体をHLA-A24分子陽性癌患者(但し前立腺癌患者を除く)に由来する抗原提示能を有する細胞に取り込ませることを含む、癌反応性細胞傷害性T細胞を誘導可能な抗原提示細胞を調製する方法;
(10)HLA-A24分子結合性副甲状腺ホルモン関連蛋白由来ペプチドもしくは機能的に同等の性質を有するその誘導体または該ペプチドもしくは誘導体を発現するベクターを含む、癌(但し前立腺癌を除く)反応性細胞傷害性T細胞を誘導可能な抗原提示細胞を調製するためのキット。
The present invention provides the following:
(1) A pharmaceutical composition for treating or preventing cancer (excluding prostate cancer), comprising a peptide derived from HLA-A24 molecule-binding parathyroid hormone-related protein or a derivative thereof having functionally equivalent properties;
(2) The pharmaceutical composition according to (1), wherein the cancer is selected from the group consisting of stomach cancer, renal cancer, colon cancer and cervical cancer;
(3) The pharmaceutical composition according to (1) or (2), wherein the cancer is bone metastatic.
(4) The pharmaceutical composition according to any one of (1) to (3), wherein the peptide has the amino acid sequence shown in SEQ ID NO: 1 or 2;
(5) The pharmaceutical composition according to any one of (1) to (4), which is for treating or preventing metastatic bone lesions of cancer;
(6) A medicament for treating or preventing cancer (excluding prostate cancer), comprising a vector expressing a peptide derived from an HLA-A24 molecule-binding parathyroid hormone-related protein or a derivative having functionally equivalent properties. Composition;
(7) HLA-A24 molecule-binding parathyroid hormone-related protein-derived peptide or its derivatives having functionally equivalent properties and peripheral blood samples collected from HLA-A24 molecule-positive cancer patients (excluding prostate cancer patients) A method of inducing cancer reactive cytotoxic T cells comprising contacting with a nuclear cell;
(8) For inducing cancer (but excluding prostate cancer) reactive cytotoxic T cells comprising a peptide derived from HLA-A24 molecule-binding parathyroid hormone-related protein or a derivative thereof having functionally equivalent properties kit;
(9) HLA-A24 molecule-binding parathyroid hormone-related protein-derived peptide or its derivative having functionally equivalent properties is capable of presenting antigens derived from HLA-A24 molecule-positive cancer patients (excluding prostate cancer patients). A method for preparing an antigen-presenting cell capable of inducing a cancer-reactive cytotoxic T cell, the method comprising incorporating the cell into a cell having cancer;
(10) HLA-A24 molecule-binding parathyroid hormone-related protein-derived peptide or a derivative thereof having functionally equivalent properties or a vector expressing the peptide or derivative, but a cancer-reactive cell (excluding prostate cancer) A kit for preparing an antigen-presenting cell capable of inducing a cytotoxic T cell.
本発明により、各種癌タイプのHLA-A24分子陽性癌患者においてPTH-rPペプチド特異的癌反応性CTLを誘導することにより癌を処置または予防しうる医薬組成物が提供された。HLA-A24アレルは日本人の60%、コーカサス人の20%およびアフリカ人の12%に見られる(Imanishi, T., Akazawa, T., Kimura, A., K. Tokunaga, and T. Gojobori, Allele and haplotype frewuencies for HLA and completment loci in various ethnic groups. In HLA1991, Tsuji, K., Aizawa, M., Sasazuki, T. (eds). Oxford: Oxford Scientific Publications 1992; Vol. 1: 1065-220)。したがって本発明は、多くの癌患者に対するペプチド基盤免疫療法を可能とする。 The present invention provides a pharmaceutical composition capable of treating or preventing cancer by inducing PTH-rP peptide-specific cancer-reactive CTL in patients with HLA-A24 molecule-positive cancer of various cancer types. The HLA-A24 allele is found in 60% of Japanese, 20% of Caucasians and 12% of Africans (Imanishi, T., Akazawa, T., Kimura, A., K. Tokunaga, and T. Gojobori, Allele and haplotype frewuencies for HLA and completment loci in various ethnic groups.In HLA1991, Tsuji, K., Aizawa, M., Sasazuki, T. (eds). Oxford: Oxford Scientific Publications 1992; Vol. 1: 1065-220) . The present invention thus enables peptide-based immunotherapy for many cancer patients.
本発明において「副甲状腺ホルモン関連蛋白由来ペプチド」、「PTH-rP由来ペプチド」または「PTH-rPペプチド」とは、副甲状腺ホルモン関連蛋白(PTH-rP)の一部より成り、HLA-A24拘束性にペプチド特異的CTLを誘導可能なペプチドである。そのようなペプチドは、例えば前述の非特許文献5に記載の方法によって同定することができる。説明すると、まずPTH-rPのアミノ酸配列に基づきHLA-A24分子結合モチーフを有するペプチドを合成し、そのペプチドでHLA-A24分子陽性癌患者から採取したPBMCを刺激する。そして、ペプチド刺激PBMCが対応ペプチドをパルスした抗原提示細胞に応答してIFN-γのようなサイトカインを産生するか否かをELISA法等により測定して、CTL誘導能を判断する。誘導されたCTLの細胞傷害活性は、51Cr放出測定法等により確認することができる。副甲状腺ホルモン関連蛋白由来ペプチドは、アミノ酸残基数が8〜14個の範囲内であることが好ましく、より好ましくは8〜11個、特に好ましくは9または10個である。本発明では、配列番号1または2に示すアミノ酸配列を有するペプチドが好適に用いられる。
In the present invention, “parathyroid hormone-related protein-derived peptide”, “PTH-rP-derived peptide” or “PTH-rP peptide” comprises a part of parathyroid hormone-related protein (PTH-rP) and is restricted by HLA-A24. It is a peptide that can induce peptide-specific CTLs. Such a peptide can be identified by, for example, the method described in Non-Patent
本発明において「ペプチドの誘導体」とは、ペプチドのアミノ酸配列に1または2個の置換、欠失および/または付加を導入したペプチドをいう。「機能的に同等の性質を有する」とは、HLA-A24拘束性に特異的CTLを誘導可能な性質を備えることを意味する。「機能的に同等の性質を有する」か否かは、前記方法に従い判断することができる。 In the present invention, a “peptide derivative” refers to a peptide having 1 or 2 substitutions, deletions and / or additions introduced into the amino acid sequence of the peptide. “Having a functionally equivalent property” means having a property capable of inducing a specific CTL in an HLA-A24-restricted manner. Whether or not “having functionally equivalent properties” can be determined according to the above method.
アミノ酸の置換、欠失および/または付加は、HLA分子結合モチーフ上許容されるものが好ましい。他のアミノ酸による置換または付加を含む場合、他のアミノ酸は天然のアミノ酸またはアミノ酸アナログであってよく、アミノ酸アナログとしては、アミノ酸のN-アシル化物、O-アシル化物、エステル化物、酸アミド化物、アルキル化物等が挙げられる。ペプチドの性質を変化させない観点から、同族アミノ酸(極性アミノ酸、非極性アミノ酸、疎水性アミノ酸、親水性アミノ酸、陽性荷電アミノ酸、陰性荷電アミノおよび芳香族アミノ酸等)の間での置換が好ましい。 Amino acid substitutions, deletions and / or additions are preferably allowed on the HLA molecule binding motif. When including substitution or addition by other amino acids, the other amino acids may be natural amino acids or amino acid analogs, and examples of amino acid analogs include N-acylated products, O-acylated products, esterified products, acid amidated products of amino acids, Examples include alkylated products. From the viewpoint of not changing the properties of the peptide, substitution between homologous amino acids (polar amino acids, nonpolar amino acids, hydrophobic amino acids, hydrophilic amino acids, positively charged amino acids, negatively charged amino acids, aromatic amino acids and the like) is preferable.
本発明におけるペプチドおよび誘導体は、機能を著しく損なわない限りにおいてその構成アミノ酸またはカルボキシル基などが修飾されていてもよい。修飾は、N末端や遊離のアミノ基にホルミル基、アセチル基、t-ブトキシカルボニル基等を結合するものや、C末端や遊離のカルボキシル基にメチル基、エチル基、t-ブチル基、ベンジル基等を結合するものが挙げられる。 The peptides and derivatives in the present invention may be modified in their constituent amino acids or carboxyl groups as long as the functions are not significantly impaired. Modifications include N-terminal and free amino groups bound to formyl, acetyl, t-butoxycarbonyl, etc., and C-terminal and free carboxyl groups to methyl, ethyl, t-butyl, and benzyl groups. And the like.
本発明におけるペプチドおよび誘導体は、通常のペプチド合成により製造することができる。そのような方法として、例えば、Peptide Synthesis, Interscience, New York,1966; The Proteins, Vol2, Academic Press Inc.,New York, 1976;ペプチド合成、丸善(株)、1975;ペプチド合成の基礎と実験、丸善(株)、1985;医薬品の開発続 第十四巻・ペプチド合成、広川書店、1991)などに記載されている方法が挙げられる。 The peptides and derivatives in the present invention can be produced by ordinary peptide synthesis. Examples of such methods include Peptide Synthesis, Interscience, New York, 1966; The Proteins, Vol2, Academic Press Inc., New York, 1976; Peptide Synthesis, Maruzen Co., 1975; Maruzen Co., Ltd., 1985; continued development of pharmaceuticals, Volume 14, Peptide Synthesis, Hirokawa Shoten, 1991).
本発明は、PTH-rP由来ペプチドまたはその誘導体のアミノ酸配列を含み、細胞内で断片化されて前記ペプチドまたは誘導体をHLA分子との複合体として提供することができるペプチドを含む医薬組成物をも包含する。PTH-rP由来ペプチドまたはその誘導体を提供できる限り、ペプチドのアミノ酸残基数およびアミノ酸配列は任意である。 The present invention also includes a pharmaceutical composition comprising an amino acid sequence of a peptide derived from PTH-rP or a derivative thereof, and a peptide that can be fragmented in a cell to provide the peptide or derivative as a complex with an HLA molecule. Includes. As long as a PTH-rP-derived peptide or a derivative thereof can be provided, the number of amino acid residues and the amino acid sequence of the peptide are arbitrary.
本発明の医薬組成物は、1種類のペプチドまたは誘導体を含むものであってもよく、2種類以上のペプチドおよび/または誘導体を組み合わせて含んでも良い。癌患者のCTLは相異なる癌抗原ペプチドを認識する細胞の集合体なので、複数種類のペプチドおよび/また誘導体を組み合わせて使用するとさらに効果的である。本発明で使用するペプチド以外の癌抗原ペプチドと組み合わせても良い。 The pharmaceutical composition of the present invention may contain one kind of peptide or derivative, or may contain two or more kinds of peptides and / or derivatives in combination. Since CTLs of cancer patients are a collection of cells that recognize different cancer antigen peptides, it is more effective to use a combination of a plurality of types of peptides and / or derivatives. You may combine with cancer antigen peptides other than the peptide used by this invention.
本発明の医薬組成物は、ペプチドまたは誘導体に加えて、製薬的に許容される担体などを含むことができる。担体としては、セルロース、重合アミノ酸、アルブミン等が使用できる。リポソーム製剤、直径数μmのビーズに結合させた粒子状の製剤、リピッドを結合させた製剤などにしてもよい。また、免疫応答が効果的に成立するように従来からワクチン投与に用いられることが知られているアジュバントとともに投与することもできる。投与方法は、例えば皮内投与または皮下投与などである。 The pharmaceutical composition of the present invention may contain a pharmaceutically acceptable carrier in addition to the peptide or derivative. As the carrier, cellulose, polymerized amino acid, albumin and the like can be used. A liposome preparation, a particulate preparation bound to beads having a diameter of several μm, a preparation bound to lipid, and the like may be used. Moreover, it can also administer with the adjuvant conventionally known to be used for vaccine administration so that an immune response may be effective. The administration method is, for example, intradermal administration or subcutaneous administration.
本発明の医薬組成物は、癌ワクチンとして使用可能である。投与量は、疾患の状態、個々の患者の年齢、体重等により適宜調整することができるが、通常医薬組成物中のペプチドまたは誘導体の量として0.0001mg〜1000mg、好ましくは0.0001mg〜100mg、より好ましくは0.001mg〜10mg、0.01〜10mg、0.1〜5mgまたは0.5〜3mgである。これを数日、数週または数ヶ月に1回、1〜3年間継続して投与することが好ましい。 The pharmaceutical composition of the present invention can be used as a cancer vaccine. The dose can be appropriately adjusted depending on the disease state, the age, weight, etc. of the individual patient, but is usually 0.0001 mg to 1000 mg, preferably 0.0001 mg to 100 mg as the amount of the peptide or derivative in the pharmaceutical composition. More preferably 0.001 mg to 10 mg, 0.01 to 10 mg, 0.1 to 5 mg or 0.5 to 3 mg. It is preferable to administer this once every several days, weeks or months for 1 to 3 years.
本発明の医薬組成物は、PTH-rP発現癌細胞を特異的に傷害するCTLを効率的に増殖させ、癌を処置または予防することができる。本発明の医薬組成物は、癌が、胃癌、腎癌、大腸癌、子宮頸癌、肺癌および乳癌よりなる群、特に胃癌、腎癌、大腸癌および子宮頸癌よりなる群から選択される場合に好適である。PTH-rPは、骨芽細胞の受容体に結合して骨の形成と再吸収を刺激する因子である。癌細胞が産生したPTH-rPは、癌に伴う高カルシウム血症や転移性骨病変に関与すると考えられている。それゆえ本発明の医薬組成物は、骨転移を伴う癌に特に有用である。本発明の医薬組成物は、骨転移の予防にも有効である。 The pharmaceutical composition of the present invention can efficiently proliferate CTLs that specifically damage PTH-rP-expressing cancer cells to treat or prevent cancer. In the pharmaceutical composition of the present invention, the cancer is selected from the group consisting of stomach cancer, kidney cancer, colon cancer, cervical cancer, lung cancer and breast cancer, in particular, the group consisting of stomach cancer, kidney cancer, colon cancer and cervical cancer. It is suitable for. PTH-rP is a factor that binds to osteoblast receptors and stimulates bone formation and resorption. PTH-rP produced by cancer cells is thought to be involved in hypercalcemia associated with cancer and metastatic bone lesions. Therefore, the pharmaceutical composition of the present invention is particularly useful for cancer with bone metastasis. The pharmaceutical composition of the present invention is also effective in preventing bone metastasis.
本発明の医薬組成物は、癌の転移性骨病変を処置または予防するためにも用いうる。「転移性骨病変」とは、癌細胞の骨への転移により骨に生じる破壊的または増殖的変化を意味する。本発明の医薬組成物は、PTH-rP発現癌細胞の傷害を促進することにより、癌細胞の骨への転移を予防し、転移性骨病変の形成および進行を抑制する。 The pharmaceutical composition of the present invention can also be used to treat or prevent metastatic bone lesions of cancer. By “metastatic bone lesion” is meant a destructive or proliferative change that occurs in bone due to the metastasis of cancer cells to the bone. The pharmaceutical composition of the present invention promotes the injury of PTH-rP-expressing cancer cells, thereby preventing metastasis of cancer cells to bone and suppressing the formation and progression of metastatic bone lesions.
本発明はまた、HLA-A24分子結合性PTH-rP由来ペプチドまたは機能的に同等の性質を有するその誘導体を発現するベクターを含む、癌を処置または予防するための医薬組成物を提供する。前記ベクターが抗原提示細胞内で発現すると、HLA-A24拘束性に特異的CTLを誘導可能なPTH-rP由来ペプチドまたは誘導体がHLA-A24分子と複合体を形成して細胞表面に提示される。この抗原提示細胞は、PTH-rP発現癌細胞に反応するCTLを効率的に増殖させることができる。当該医薬組成物は、癌の転移性骨病変を処置または予防するために使用することもできる。当該医薬組成物は、胃癌、腎癌、大腸癌、子宮頸癌、肺癌および乳癌よりなる群、特に胃癌、腎癌、大腸癌および子宮頸癌よりなる群から選択される癌に好適に用いられる。ペプチドは、配列番号1または2に示すアミノ酸配列を有するものが好適である。 The present invention also provides a pharmaceutical composition for treating or preventing cancer comprising a vector that expresses an HLA-A24 molecule-binding PTH-rP derived peptide or a derivative thereof having functionally equivalent properties. When the vector is expressed in antigen-presenting cells, a PTH-rP-derived peptide or derivative capable of inducing specific CTLs restricted to HLA-A24 forms a complex with the HLA-A24 molecule and is presented on the cell surface. This antigen-presenting cell can efficiently proliferate CTLs that react with PTH-rP-expressing cancer cells. The pharmaceutical composition can also be used to treat or prevent metastatic bone lesions of cancer. The pharmaceutical composition is suitably used for a cancer selected from the group consisting of stomach cancer, renal cancer, colon cancer, cervical cancer, lung cancer and breast cancer, particularly from the group consisting of stomach cancer, kidney cancer, colon cancer and cervical cancer. . The peptide having the amino acid sequence shown in SEQ ID NO: 1 or 2 is preferable.
ベクターとしては、各種プラスミドおよびウィルスベクター、例えばアデノウィルス、アデノ関連ウィルス、レトロウィルス、ワクシニアウィルス等が挙げられる(Liu M, Acres B, Balloul JM, Bizouarne N, Paul S, Slos P, Squiban P. Gene-based vaccines and immunotherapeutics. Proc Natl Acad Sci U S A 101 Suppl, 14567-71, 2004)。ベクターの調製方法は当業界にて周知である(Molecular Cloning: A laboraroy manual, 2nd edn. New York, Cold Spring Harbor Laboratory)。
Examples of the vector include various plasmids and viral vectors such as adenovirus, adeno-associated virus, retrovirus, vaccinia virus (Liu M, Acres B, Balloul JM, Bizouarne N, Paul S, Slos P, Squiban P. Gene- based vaccines and immunotherapeutics. Proc Natl
前記ベクターを含む本発明の医薬組成物は、患者体内の抗原提示細胞において前記ペプチドまたは誘導体を発現させるため患者に投与してもよく、あるいは体外で適当な細胞、例えば患者由来の樹状細胞、において前記ペプチドまたは誘導体を発現させるために使用しても良い。これらの方法は当業界において周知である(Hrouda D, Dalgleish AG. Gene therapy for prostate cancer. Gene Ther 3: 845-52, 1996)。 The pharmaceutical composition of the present invention comprising the vector may be administered to a patient to express the peptide or derivative in antigen-presenting cells in the patient, or suitable cells outside the body, such as dendritic cells derived from the patient, May be used to express said peptide or derivative. These methods are well known in the art (Hrouda D, Dalgleish AG. Gene therapy for prostate cancer. Gene Ther 3: 845-52, 1996).
投与量は、疾患の状態、個々の患者の年齢、体重等により変化するが、DNA含量として0.1μg〜100mg、好ましくは1μg〜50mgである。投与方法には、静脈注射、皮下投与、皮内投与等が挙げられる。 The dose varies depending on the disease state, the age and weight of each individual patient, and the DNA content is 0.1 μg to 100 mg, preferably 1 μg to 50 mg. Examples of the administration method include intravenous injection, subcutaneous administration, intradermal administration and the like.
本発明のCTL誘導方法は、PTH-rPを発現するHLA-A24分子陽性癌細胞を特異的に傷害するCTLを提供するものである。本発明において「癌反応性」とは、癌細胞上のPTH-rP由来ペプチドとHLA-A24分子との複合体を認識し、その細胞を傷害しうる性質を有することを意味する。好ましい態様として、癌は、胃癌、腎癌、大腸癌、子宮頸癌、肺癌および乳癌よりなる群、特に胃癌、腎癌、大腸癌および子宮頸癌よりなる群から選択される。本発明のCTL誘導方法は、例えば、HLA-A24拘束性にペプチド特異的CTLを誘導可能なPTH-rP由来ペプチドの存在下、in vitroでHLA-A24分子陽性癌患者から採取されたPBMCを培養することにより行う。本方法は、PBMCを採取した患者体内に誘導したCTLを戻して癌細胞を傷害する養子免疫療法に有用である。 The CTL induction method of the present invention provides a CTL that specifically injures HLA-A24 molecule-positive cancer cells that express PTH-rP. In the present invention, “cancer reactivity” means that it has a property of recognizing a complex of a PTH-rP-derived peptide and an HLA-A24 molecule on a cancer cell and damaging the cell. In a preferred embodiment, the cancer is selected from the group consisting of stomach cancer, kidney cancer, colon cancer, cervical cancer, lung cancer and breast cancer, in particular, the group consisting of stomach cancer, kidney cancer, colon cancer and cervical cancer. The CTL induction method of the present invention includes, for example, culturing PBMCs collected from HLA-A24 molecule-positive cancer patients in vitro in the presence of a PTH-rP-derived peptide capable of inducing peptide-specific CTLs restricted to HLA-A24. To do. This method is useful for adoptive immunotherapy in which cancer cells are damaged by returning CTLs induced in the body of a patient from whom PBMCs have been collected.
本発明のCTL誘導キットは、前記CTL誘導方法を実施するために用いられる。本発明のキットは、HLA-A24拘束性にペプチド特異的CTLを誘導可能なPTH-rP由来ペプチドまたはその誘導体を1または2種類以上含み、さらに適当な緩衝液や培地などを含むこともできる。 The CTL induction kit of the present invention is used for carrying out the CTL induction method. The kit of the present invention contains one or more PTH-rP-derived peptides or derivatives thereof capable of inducing peptide-specific CTLs restricted to HLA-A24, and may further contain an appropriate buffer or medium.
本発明の抗原提示細胞調製方法は、PTH-rPを発現するHLA-A24分子陽性癌細胞を傷害するCTLを誘導するための抗原提示細胞を提供するものである。本方法は、癌が胃癌、腎癌、大腸癌、子宮頸癌、肺癌および乳癌よりなる群、特に胃癌、腎癌、大腸癌および子宮頸癌よりなる群から選択される場合に好適である。本発明の抗原提示細胞調製方法は、例えば、HLA-A24拘束性にペプチド特異的CTLを誘導可能なPTH-rP由来ペプチドを、HLA-A24分子陽性癌患者由来の抗原提示能を有する細胞にパルスすることより行う。あるいはそのようなペプチドを発現可能なベクターを、前記細胞に導入し発現させてもよい。ペプチドは、配列番号1または2に示すアミノ酸配列を有するものが好適である。抗原提示能を有する細胞は例えば樹状細胞であり、患者より採取したPBMCから培養プレート接着細胞を分離し、IL-4およびGM-CSFの存在下で約1週間培養することにより調製することができる。本発明の方法により調製された抗原提示細胞は、その細胞表面に提示するペプチドまたは誘導体とHLA分子との複合体を特異的に認識するCTLを誘導することができ、患者に投与されると患者体内でPTH-rPを発現するHLA-A24分子陽性癌細胞を傷害するCTLの誘導を促進することができる。 The antigen-presenting cell preparation method of the present invention provides an antigen-presenting cell for inducing CTL that damages an HLA-A24 molecule-positive cancer cell that expresses PTH-rP. This method is suitable when the cancer is selected from the group consisting of stomach cancer, renal cancer, colon cancer, cervical cancer, lung cancer and breast cancer, particularly from the group consisting of stomach cancer, kidney cancer, colon cancer and cervical cancer. The method for preparing an antigen-presenting cell of the present invention comprises, for example, pulsing a PTH-rP-derived peptide capable of inducing peptide-specific CTL in a HLA-A24-restricted manner into a cell having an antigen-presenting ability derived from an HLA-A24 molecule-positive cancer patient. Do more than you do. Alternatively, a vector capable of expressing such a peptide may be introduced into the cell and expressed. The peptide having the amino acid sequence shown in SEQ ID NO: 1 or 2 is preferable. Cells having antigen-presenting ability are, for example, dendritic cells, and can be prepared by separating cultured plate-adhered cells from PBMC collected from a patient and culturing them in the presence of IL-4 and GM-CSF for about 1 week. it can. Antigen-presenting cells prepared by the method of the present invention can induce CTL that specifically recognizes a complex of a peptide or derivative presented on the cell surface and an HLA molecule, and when administered to a patient Induction of CTLs that damage HLA-A24 molecule-positive cancer cells that express PTH-rP in the body can be promoted.
本発明の抗原提示細胞調製キットは、前記抗原提示細胞調製方法を行うために用いられる。本発明のキットは、HLA-A24拘束性にペプチド特異的CTLを誘導可能なPTH-rP由来ペプチドまたはその誘導体を1または2種類以上含み、さらに適当な緩衝液や培地などを含むこともできる。 The antigen-presenting cell preparation kit of the present invention is used for performing the antigen-presenting cell preparation method. The kit of the present invention contains one or more PTH-rP-derived peptides or derivatives thereof capable of inducing peptide-specific CTLs restricted to HLA-A24, and may further contain an appropriate buffer or medium.
本発明はさらに、治療上有効量のHLA-A24分子結合性PTH-rP由来ペプチドまたは機能的に同等の性質を有するその誘導体を患者に投与することを含む、癌(但し前立腺癌を除く)を処置または予防する方法を提供する。また、本発明は、HLA-A24分子結合性PTH-rP由来ペプチドまたは機能的に同等の性質を有するその誘導体の、癌(但し前立腺癌を除く)を処置または予防するための医薬組成物を製造するための使用を提供する。 The present invention further includes cancer (except for prostate cancer), comprising administering to a patient a therapeutically effective amount of an HLA-A24 molecule-binding PTH-rP derived peptide or a derivative thereof having functionally equivalent properties. Provide a method of treating or preventing. The present invention also provides a pharmaceutical composition for treating or preventing cancer (excluding prostate cancer) of an HLA-A24 molecule-binding PTH-rP-derived peptide or a derivative thereof having functionally equivalent properties. Provide use to do.
本発明を以下の実施例によりさらに詳細に説明するが、本発明はいかなる意味においてもこれら実施例により制限されるものではない。
I.材料と方法
細胞株
MKN-7、MKN-28およびMKN-45 (胃腺癌); RERF-LC-AIおよびQG56 (肺扁平上皮癌); 11-18、1-87、LK87およびLC-1 (肺腺癌); R-27およびCRL1500 (乳癌); KUR-11、RC30-14、Caki-1、MAMIYAおよびVMRC-RCW (腎細胞癌);およびCOLO201、COLO205、COLO320およびSW480 (大腸腺癌)細胞は、10% FCS含有RPMI-1640にて培養した。MDA-MB-231 (乳癌); HCT116 (大腸腺癌); SKG-I、SKG-II、OMC-1およびSKG-IIIb (子宮頸部扁平上皮癌); SKG-IIIaおよび OMC-4 (子宮頸部腺癌); およびOMC-3 (卵巣癌)細胞は、10% FCS含有DMEMにて培養した。KWS (胃腺癌)、MCF-7およびYMB-1-E (乳癌)およびSW620 (大腸腺癌)細胞は、10% FCS 含有EMEMにて、37℃、5% CO2加湿環境下で培養した。
The present invention will be described in more detail by the following examples, but the present invention is not limited by these examples in any way.
I. Materials and methods Cell lines
MKN-7, MKN-28 and MKN-45 (gastric adenocarcinoma); RERF-LC-AI and QG56 (lung squamous cell carcinoma); 11-18, 1-87, LK87 and LC-1 (lung adenocarcinoma); R -27 and CRL1500 (breast cancer); KUR-11, RC30-14, Caki-1, MAMIYA and VMRC-RCW (renal cell carcinoma); and COLO201, COLO205, COLO320 and SW480 (colon adenocarcinoma) cells, 10% FCS Incubated with RPMI-1640. MDA-MB-231 (breast cancer); HCT116 (colon adenocarcinoma); SKG-I, SKG-II, OMC-1 and SKG-IIIb (cervical squamous cell carcinoma); SKG-IIIa and OMC-4 (cervical cervix) Adenocarcinoma); and OMC-3 (ovarian cancer) cells were cultured in DMEM containing 10% FCS. KWS (gastric adenocarcinoma), MCF-7 and YMB-1-E (breast cancer) and SW620 (colon adenocarcinoma) cells were cultured in EMEM containing 10% FCS in a 37 ° C., 5% CO 2 humidified environment.
RT-PCR
RNAzolTM B (Tel-Test Inc., Friendswood, TX, USA)を用いて、癌細胞株からトータルRNA(Total RNA)を単離した。SuperScriptTM Preamplification System for First Strand cDNA Synthesis (Invitrogen)を用いてcDNAを調製し、それをPTH-rP については 5’-TCTTCCTTCACCATCTGATCG-3’(センス) および 5’-TGTCCTTGGAAGGTCTCTGC-3’(アンチセンス)を、β-アクチンについては 5’-CTTCGCGGGCGACGATGC-3’(センス)および5’-CGTACATGGCTGGGGTGTTG-3’(アンチセンス)をプライマーとして用いて増幅した。Taq DNA ポリメラーゼを使用し、DNAサーマルサイクラー(iCycler, Bio-Rad Laboratories, Hercules, CA, USA)で、95℃1分、60℃1分、72℃1分、30サイクル、のPCRを行った。PCR産物は、2%アガロースゲルにおける電気泳動により分離した。β-アクチン mRNAについてのRT-PCRは、解析に使用したRNAの質を評価するために行った。
RT-PCR
Total RNA was isolated from cancer cell lines using RNAzol ™ B (Tel-Test Inc., Friendswood, TX, USA). CDNA was prepared using SuperScript TM Preamplification System for First Strand cDNA Synthesis (Invitrogen), it 5'-TCTTCCTTCACCATCTGATCG-3 for PTH-rP '(sense) and 5'-TGTCCTTGGAAGGTCTCTGC-3' (the antisense) Β-actin was amplified using 5′-CTTCGCGGGCGACGATGC-3 ′ (sense) and 5′-CGTACATGGCTGGGGTGTTG-3 ′ (antisense) as primers. Taq DNA polymerase was used to perform PCR at 95 ° C. for 1 minute, 60 ° C. for 1 minute, 72 ° C. for 1 minute, 30 cycles with a DNA thermal cycler (iCycler, Bio-Rad Laboratories, Hercules, Calif., USA). PCR products were separated by electrophoresis on a 2% agarose gel. RT-PCR for β-actin mRNA was performed to assess the quality of the RNA used in the analysis.
免疫蛍光顕微鏡解析
35-mm 培養ディッシュ上の細胞をTBS (10 mM Tris, pH 7.4, 100 mM NaCl)ですすぎ、3.7 % ホルムアルデヒドを室温で5分間処置して固定し、TBSで洗浄し、その後3% BSAを15分間処置してブロックした。マウス抗PTH-rPモノクローナル抗体(mAb) (1:100希釈, Ab-1; Oncogene Research Products)を室温で1時間処置して細胞を染色した。TBSで洗浄した後、フルオレセインイソチオシアネート(FITC)結合抗マウスイムノグロブリンG(IgG) (1:200希釈; Molecular Probes)で細胞を染色し、ヨードプロピジウム (PI)で対比染色した。染色細胞に1, 4-ジアザビシクロ-[2, 2, 2]-オクタン/グリセロールをのせ、共焦点レーザー走査顕微鏡(Fluoview; Olympus)により観察した。
Immunofluorescence microscopy analysis
Cells on 35-mm culture dishes are rinsed with TBS (10 mM Tris, pH 7.4, 100 mM NaCl), fixed with 3.7% formaldehyde for 5 minutes at room temperature, washed with TBS, then 15% BSA with 15% Treated for minutes and blocked. Mouse anti-PTH-rP monoclonal antibody (mAb) (1: 100 dilution, Ab-1; Oncogene Research Products) was treated for 1 hour at room temperature to stain the cells. After washing with TBS, cells were stained with fluorescein isothiocyanate (FITC) -conjugated anti-mouse immunoglobulin G (IgG) (1: 200 dilution; Molecular Probes) and counterstained with iodopropidium (PI). 1,4-Diazabicyclo- [2, 2, 2] -octane / glycerol was placed on the stained cells and observed with a confocal laser scanning microscope (Fluoview; Olympus).
フローサイトメトリー解析
PTH-rPタンパク質の発現を調べるため、トリプシン処理して細胞を回収し、10% FCS-RPMIで再懸濁し、次いで3% ホルムアルデヒド中で固定した。固定後、細胞をPBSで3回洗浄し、2.5 μg/mlのウサギポリクローナル抗PTH-rP抗体(1:75希釈, H-137; Santa Cruz, CA, USA)と室温で1時間インキュベートした。ウサギ免疫前血清を対照として使用した。PBSで洗浄した後、FITC結合抗ウサギIgG (1:150希釈; Molecular Probes)を室温で1時間処置して細胞を染色した。フローサイトメトリーはEPICSフローサイトメーターにより行い、データはEXPO32解析ソフトウェア(Beckman Coulter)により解析した。
Flow cytometry analysis
To examine PTH-rP protein expression, cells were harvested by trypsinization, resuspended in 10% FCS-RPMI and then fixed in 3% formaldehyde. After fixation, the cells were washed 3 times with PBS and incubated with 2.5 μg / ml rabbit polyclonal anti-PTH-rP antibody (1:75 dilution, H-137; Santa Cruz, CA, USA) for 1 hour at room temperature. Rabbit preimmune serum was used as a control. After washing with PBS, cells were stained with FITC-conjugated anti-rabbit IgG (1: 150 dilution; Molecular Probes) for 1 hour at room temperature. Flow cytometry was performed with an EPICS flow cytometer, and data was analyzed with EXPO32 analysis software (Beckman Coulter).
患者由来PBMCの調製
本試験開始前に試験に参加した18人の癌患者から書面による同意を得た。これら患者はいずれもヒト免疫不全ウィルス (HIV)には感染していなかった。各被験者から末梢血20mlを採取し、Ficoll-Conray密度勾配遠心法によりPBMCを調製した。癌患者および健常人のPBMC上のHLA-A24分子の発現はフローサイトメトリーにより測定した。
Preparation of patient-derived PBMC
Written consent was obtained from 18 cancer patients who participated in the study before the start of the study. None of these patients were infected with human immunodeficiency virus (HIV). 20 ml of peripheral blood was collected from each subject, and PBMCs were prepared by Ficoll-Conray density gradient centrifugation. The expression of HLA-A24 molecule on PBMC of cancer patients and healthy people was measured by flow cytometry.
ペプチド
ペプチドは全て純度90%を超えるものであり、Biologica Co.(名古屋)より購入した。HLA-A24結合モチーフを有する、PTH-rP由来ペプチド(102-111: RYLTQETNKV および110-119: KVETYKEQPL)、インフルエンザ(Flu)ウィルス由来ペプチド(RFYIQMCYEL)、EBV由来ペプチド(TYGPVFMCL)およびHIV由来ペプチド(RYLRQQLLGI)を使用した。ペプチドは全てDMSOにて用量10 mg/ml に溶解した
Peptides All peptides have a purity exceeding 90% and were purchased from Biologica Co. (Nagoya). PTH-rP derived peptides (102-111: RYLTQETNKV and 110-119: KVETYKEQPL), influenza (Flu) virus derived peptides (RFYIQMCYEL), EBV derived peptides (TYGPVFMCL) and HIV derived peptides (RYLRQQLLGI) with HLA-A24 binding motif )It was used. All peptides were dissolved in DMSO at a dose of 10 mg / ml
PBMC中のペプチド反応性CTLの検出
PBMC中のペプチド反応性CTLを検出は、既報の方法に従い行った(非特許文献7)。説明すると、U底96ウェルマイクロカルチャープレート(Nunc, Roskilde, Denmark)にて培養培地200μlの容量でPBMC (1 X 105 細胞/ウェル)を各ペプチド10 μg/mlとともにインキュベートした。培養培地は、45 % RPMI-1640、45 % AIM-V 培地(Gibco BRL) 、10 % FCS、100 U/ml インターロイキン(IL)-2および0.1 mM MEM非必須アミノ酸溶液 (Gibco, BRL)より構成された。3日毎に培養培地の半分を除去し、対応ペプチド(20 μg/ml)を含有する新しい培地と置き換えた。培養15日目に培養細胞を4ウェルに分け、そのうち2ウェルはPTH-rPペプチドをパルスしたC1R-A24細胞 (Dr. M. Takiguchi, Kumamoto University, Japan)に対して、他の2ウェルはHIVペプチドをパルスしたC1R-A24細胞に対して使用した。18時間インキュベートした後、上清を回収し、IFN-γのレベルをELISAにより測定した。
Detection of peptide-reactive CTL in PBMC
Detection of peptide-reactive CTL in PBMC was performed according to a previously reported method (Non-patent Document 7). To explain, PBMC (1 × 10 5 cells / well) were incubated with 10 μg / ml of each peptide in a volume of 200 μl of culture medium in a U-bottom 96-well microculture plate (Nunc, Roskilde, Denmark). The culture medium is 45% RPMI-1640, 45% AIM-V medium (Gibco BRL), 10% FCS, 100 U / ml interleukin (IL) -2 and 0.1 mM MEM non-essential amino acid solution (Gibco, BRL) Configured. Every 3 days, half of the culture medium was removed and replaced with fresh medium containing the corresponding peptide (20 μg / ml). On
細胞傷害性試験
細胞傷害性試験を行うのに充分な数の細胞を得るため、PTH-rPペプチドでin vitro刺激をしたPBMCを、96ウェル丸底ウェルプレートにて100 U/ml IL-2 とともにさらに約10日間培養した。細胞傷害性試験の直前に、CD8 Positive Isolation Kit (Dynal, Oslo, Norway)を用いてCD8陽性T細胞を単離した。そして、6時間51Cr放出試験により、精製CD8陽性T細胞を腫瘍細胞に対する細胞傷害活性について試験した。96丸底ウェルプレートにおいて、各ウェルにつき2000個の51Cr-標識細胞を各種エフェクター細胞/標的細胞の比率で培養した。抗体による阻害実験では、試験開始時に抗HLAクラスI (W6/32: マウス IgG2a)、抗HLAクラスII(HLA-DR) (L243: マウス IgG2a)、または抗CD14 (H14: マウス IgG2a) mAbを 20 μg/mlの用量にて添加した。
Cytotoxicity test To obtain a sufficient number of cells to perform the cytotoxicity test, PBMC stimulated in vitro with PTH-rP peptide were combined with 100 U / ml IL-2 in a 96-well round bottom well plate. The culture was further continued for about 10 days. Immediately before the cytotoxicity test, CD8 positive T cells were isolated using a CD8 Positive Isolation Kit (Dynal, Oslo, Norway). The purified CD8 positive T cells were then tested for cytotoxic activity against tumor cells by a 6 hour 51 Cr release test. In a 96 round bottom well plate, 2000 51 Cr-labeled cells per well were cultured at various effector / target cell ratios. For antibody inhibition experiments, anti-HLA class I (W6 / 32: mouse IgG2a), anti-HLA class II (HLA-DR) (L243: mouse IgG2a), or anti-CD14 (H14: mouse IgG2a) mAb at the start of the study. Added at a dose of μg / ml.
コールド標的細胞阻害試験
PTH-rPペプチド反応性CTLの特異性は、コールド標的細胞阻害試験により確認した。説明すると、96丸底ウェルプレートにおいて、51Cr-標識標的細胞(2 X 103 細胞/ウェル)とCTL (4 X 104 細胞/ウェル)とを、2 X 104 細胞のコールド標的細胞とともに培養した。HIVペプチドまたは対応PTH-rPペプチドのいずれかを前もってパルスしたC1R-A24細胞をコールド標的細胞として使用した。51Cr-標識標的細胞には、癌タイプを合わせた癌細胞株を使用した。
Cold target cell inhibition test
The specificity of PTH-rP peptide-reactive CTL was confirmed by a cold target cell inhibition test. For example, 51 Cr-labeled target cells (2 x 10 3 cells / well) and CTL (4 x 10 4 cells / well) were cultured in 96 round bottom well plates with cold target cells of 2 x 10 4 cells did. C1R-A24 cells pre-pulsed with either HIV peptide or the corresponding PTH-rP peptide were used as cold target cells. As the 51 Cr-labeled target cells, cancer cell lines combined with cancer types were used.
統計
データの統計学的有意差は両側Student's t 検定により検討した。0.05未満のP値(*)を統計学的に有意であると判断した。
Statistical significance of statistical data was examined by two-sided Student's t test. P values (*) less than 0.05 were considered statistically significant.
II.結果
1.各種癌細胞株におけるPTH-rPの発現
はじめに、胃癌、腎癌、大腸癌、子宮頸癌、肺癌および乳癌細胞株におけるPTH-rPのmRNA発現レベルを半定量的RT-PCR解析により調べた(図1)。細胞株によって発現レベルは異なるものの、試験したほとんどの癌細胞株においてPTH-rP mRNAが発現していることがわかった。いくつかの細胞株においては、陽性対照(PC)として使用した前立腺癌細胞株であるLNCaPよりも発現が高かった。
次に、PTH-rPタンパク質の発現を確認するため免疫細胞化学的解析を行った(図2A)。PTH-rPは、SKG-I (子宮頸部扁平上皮癌)(図2A−a)、QG56 (肺扁平上皮癌)(図2A−b)およびMAMIYA (腎細胞癌)(図2A−d)細胞においては細胞質全体に点状に発現していた。一方、RT-PCR解析でPTH-rP mRNAの発現が弱かったR-27 (乳癌)細胞(図1−d)においては発現レベルが非常に低かった(図2A−c)。
さらに、細胞内染色のフローサイトメトリー解析によってPTH-rPタンパク質の発現を調べた(図2B)。PTH-rPタンパク質の発現は、MKN-45 (胃腺癌)(図2B−a)、SKG-I (子宮頸部扁平上皮癌)(図2B−b)、QG56 (肺扁平上皮癌)(図2B−c)、およびKUR-11並びにMAMIYA (腎細胞癌) (図2B−eおよびf)細胞においては高かった。しかしながら、R-27 (乳癌)(図2B−d)およびCOLO201 (大腸腺癌)(図2B−g)細胞は、ほんの低いレベルでしかPTH-rP発現を示さないか、あるいはPTH-rP発現が陰性であった。
これらタンパク質発現解析によって得られた結果は、PT-PCR解析によって得られた結果と一致する。
II.
Next, immunocytochemical analysis was performed to confirm the expression of PTH-rP protein (FIG. 2A). PTH-rP is expressed by SKG-I (cervical squamous cell carcinoma) (FIG. 2A-a), QG56 (squamous cell lung carcinoma) (FIG. 2A-b) and MAMIYA (renal cell carcinoma) (FIG. 2A-d) cells. In, it was expressed in punctate throughout the cytoplasm. On the other hand, the expression level was very low in R-27 (breast cancer) cells (FIG. 1-d) in which the expression of PTH-rP mRNA was weak in RT-PCR analysis (FIGS. 2A-c).
Furthermore, the expression of PTH-rP protein was examined by flow cytometric analysis of intracellular staining (FIG. 2B). The expression of PTH-rP protein is MKN-45 (gastric adenocarcinoma) (Fig. 2B-a), SKG-I (cervical squamous cell carcinoma) (Fig. 2B-b), QG56 (pulmonary squamous cell carcinoma) (Fig. 2B). -C), and KUR-11 and MAMIYA (renal cell carcinoma) (FIGS. 2B-e and f) higher in cells. However, R-27 (breast cancer) (FIG. 2B-d) and COLO201 (colon adenocarcinoma) (FIG. 2B-g) cells show PTH-rP expression only at very low levels or PTH-rP expression. Negative.
The results obtained by these protein expression analyzes are consistent with the results obtained by PT-PCR analysis.
2.各種癌タイプのHLA-A24分子陽性患者に由来するPTH-rPペプチド反応性CTLの誘導
本発明者らは以前、HLA-A24分子陽性前立腺癌患者のPBMCからペプチド特異的な前立腺癌反応性CTLを誘導することができる2種類のPTH-rP由来ペプチド、PTH-rP102-111およびPTH-rP110-119を同定した (非特許文献5)。これらペプチドが各種癌タイプの患者においてPTH-rPペプチド特異的CTLが誘導できるか否かについて検討するため、患者のPBMCをin vitro においていずれかのPTH-rPペプチドで刺激し、次いでそのペプチド刺激PBMCが対応PTH-rPペプチドまたはHIVペプチドを前もってパルスしたC1R-A24細胞に応答してIFN-γを産生するかについて調べた(表1)。本実験では、FluおよびEBV由来ペプチドを対照として使用した。HIVペプチドに応答し産生されたIFN-γをバックグラウンドとして差し引き、最良の応答が見られた結果を示す(表1)。ペプチド特異的CTLの誘導の成功は、有意な値(P<0.05、両側Student's t 検定による)が観察された場合に陽性であると判断した。
以上の結果は、これらPTH-rPペプチドが、様々な癌タイプの患者のPBMCからペプチド反応性CTLを誘導できることを示している。
2. Induction of PTH-rP peptide-reactive CTL derived from HLA-A24 molecule-positive patients of various cancer types We have previously obtained peptide-specific prostate cancer-reactive CTL from PBMC of HLA-A24 molecule-positive prostate cancer patients Two types of PTH-rP-derived peptides, PTH-rP102-111 and PTH-rP110-119, that can be induced were identified (Non-patent Document 5). To examine whether these peptides can induce PTH-rP peptide-specific CTLs in patients with various cancer types, the patient's PBMCs were stimulated in vitro with any of the PTH-rP peptides and then the peptide-stimulated PBMCs Were examined to produce IFN-γ in response to C1R-A24 cells pre-pulsed with the corresponding PTH-rP peptide or HIV peptide (Table 1). In this experiment, Flu and EBV derived peptides were used as controls. The results obtained by subtracting the IFN-γ produced in response to the HIV peptide as a background and showing the best response are shown (Table 1). Successful induction of peptide-specific CTL was judged positive when significant values (P <0.05, by two-sided Student's t test) were observed.
The above results indicate that these PTH-rP peptides can induce peptide-reactive CTLs from PBMCs of patients with various cancer types.
3.癌患者由来PTH-rPペプチド反応性CTLの癌細胞に対する細胞傷害活性
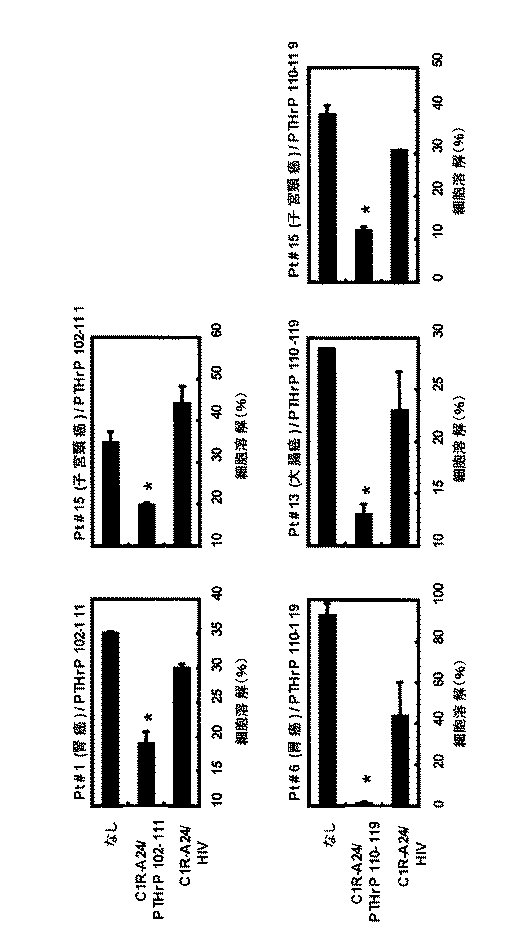
次に、癌患者から誘導されたPTH-rPペプチド反応性CTLが、癌細胞に対して細胞傷害活性を示し得るかについて検討した。RT-PCRの結果(図1)に基づき、以下の癌細胞株を細胞傷害活性試験の標的細胞として使用した: KUR-11およびRC30-14 (腎細胞癌);MKN-45およびMKN-28 (胃腺癌) ;COLO320およびCOLO205 (大腸腺癌) ; SKG-I並およびOMC-1 (子宮頸部扁平上皮癌)。以下の細胞株はHLA-A24分子の表面発現が陽性であった: KUR-11、MKN-45、COLO320およびSKG-I; 一方以下の細胞株はHLA-A24分子の表面発現は陰性であった: RC30-14、MKN-28、COLO205およびOMC-1 (データ非提示)。上記2で顕著なレベルのIFN-γを産生した5人の患者由来のPBMC (表1、Pt #1(胃癌)、Pt #6(腎癌)、Pt #12(大腸癌)、Pt #13(大腸癌)およびPt #15(子宮頸癌))を、前述の培養プロトコールに従い示したPTH-rPペプチドで繰り返し刺激した。そして、試験の直前にこれら細胞からCD8陽性T細胞を単離した。
PTH-rP102-111 ペプチドまたはPTH-rP110-119 ペプチド刺激CD8陽性T細胞は、PTH-rP陽性/HLA-A24分子陽性癌細胞(KUR-11、MKN-45、COLO320およびSKG-I)に対して、PTH-rP陽性/HLA-A24陰性癌細胞(RC30-14、MKN-28、COLO205およびOMC-1)およびPTH-rP陰性/HLA-A24分子陽性PHA誘導T芽球化細胞に対してよりも、高いレベルの細胞傷害活性を示した(図3)。
PTH-rP陽性/HLA-A24分子陽性癌細胞に対する細胞傷害活性は抗HLAクラスI mAbの添加によって有意に抑制されたが、抗HLAクラスII mAbまたは対照として使用した抗CD14 mAbの添加によっては抑制されなかった(図4A)。
さらに、PTH-rP陽性/HLA-A24分子陽性癌細胞に対する細胞傷害活性は、対応PTH-rPペプチドをパルスしたC1R-A24細胞をコールド標的細胞として添加すると有意に抑制されたが、この抑制はHIVペプチドパルスC1R-A24細胞の添加によっては観察されなかった(図4B)。
以上の結果は、これらPTH-rPペプチドで刺激した各種癌患者由来PBMCが対応する癌細胞を傷害しうることを示す。また、本実験で観察された細胞傷害活性は主にHLAクラスI拘束性PTH-rPペプチド特異的CD8陽性T細胞によることを示す。
4.まとめ
以上より、PTH-rP102-111 ペプチドおよびPTH-rP110-119 ペプチドが、各種癌タイプの癌患者に対するペプチド基盤免疫療法において有用であることが示された。
3. Cytotoxic activity of cancer patient-derived PTH-rP peptide-reactive CTLs against cancer cells Next, we examined whether PTH-rP peptide-reactive CTLs derived from cancer patients could show cytotoxic activity against cancer cells. . Based on RT-PCR results (Figure 1), the following cancer cell lines were used as target cells for cytotoxic activity studies: KUR-11 and RC30-14 (renal cell carcinoma); MKN-45 and MKN-28 ( Gastric adenocarcinoma); COLO320 and COLO205 (colon adenocarcinoma); SKG-I and OMC-1 (cervical squamous cell carcinoma). The following cell lines were positive for HLA-A24 molecule surface expression: KUR-11, MKN-45, COLO320 and SKG-I; whereas the following cell lines were negative for HLA-A24 molecule surface expression: : RC30-14, MKN-28, COLO205 and OMC-1 (data not shown). PBMCs from 5 patients who produced significant levels of IFN-γ in 2 above (Table 1, Pt # 1 (stomach cancer), Pt # 6 (kidney cancer), Pt # 12 (colon cancer), Pt # 13 (Colorectal cancer) and Pt # 15 (cervical cancer)) were repeatedly stimulated with the PTH-rP peptide indicated according to the culture protocol described above. Then, CD8 positive T cells were isolated from these cells immediately before the test.
PTH-rP102-111 peptide or PTH-rP110-119 peptide-stimulated CD8 positive T cells against PTH-rP positive / HLA-A24 molecule positive cancer cells (KUR-11, MKN-45, COLO320 and SKG-I) Than for PTH-rP positive / HLA-A24 negative cancer cells (RC30-14, MKN-28, COLO205 and OMC-1) and PTH-rP negative / HLA-A24 molecule positive PHA-induced T blasts Showed a high level of cytotoxic activity (FIG. 3).
Cytotoxic activity against PTH-rP positive / HLA-A24 molecule positive cancer cells was significantly suppressed by the addition of anti-HLA class I mAb, but was suppressed by addition of anti-HLA class II mAb or anti-CD14 mAb used as a control Not (FIG. 4A).
Furthermore, the cytotoxic activity against PTH-rP positive / HLA-A24 molecule positive cancer cells was significantly suppressed when C1R-A24 cells pulsed with the corresponding PTH-rP peptide were added as cold target cells. It was not observed by the addition of peptide pulsed C1R-A24 cells (FIG. 4B).
The above results indicate that PBMCs derived from various cancer patients stimulated with these PTH-rP peptides can damage the corresponding cancer cells. Moreover, it is shown that the cytotoxic activity observed in this experiment is mainly due to HLA class I-restricted PTH-rP peptide-specific CD8-positive T cells.
4). Summary From the above, it was shown that PTH-rP102-111 peptide and PTH-rP110-119 peptide are useful in peptide-based immunotherapy for cancer patients of various cancer types.
Claims (10)
HLA-A24 molecule-binding parathyroid hormone-related protein-derived peptide or a derivative thereof having functionally equivalent properties or a vector expressing the peptide or derivative reactive cancer (except for prostate cancer) reactive cytotoxicity T A kit for preparing an antigen-presenting cell capable of inducing a cell.
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2005221399A JP2008260689A (en) | 2005-07-29 | 2005-07-29 | Pharmaceutical composition containing peptide derived from HLA-A24 molecule binding parathyroid hormone related protein |
| PCT/JP2006/314412 WO2007013352A1 (en) | 2005-07-29 | 2006-07-20 | Medicinal composition containing hla-a24 molecule-binding peptide originating in parathyroid hormone-related protein |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2005221399A JP2008260689A (en) | 2005-07-29 | 2005-07-29 | Pharmaceutical composition containing peptide derived from HLA-A24 molecule binding parathyroid hormone related protein |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2008260689A true JP2008260689A (en) | 2008-10-30 |
Family
ID=37683253
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2005221399A Pending JP2008260689A (en) | 2005-07-29 | 2005-07-29 | Pharmaceutical composition containing peptide derived from HLA-A24 molecule binding parathyroid hormone related protein |
Country Status (2)
| Country | Link |
|---|---|
| JP (1) | JP2008260689A (en) |
| WO (1) | WO2007013352A1 (en) |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2000080100A (en) * | 1998-06-17 | 2000-03-21 | Japan Tobacco Inc | Human monoclonal antibody against parathyroid hormone-related protein |
| JP2003021631A (en) * | 2001-05-10 | 2003-01-24 | Chugai Pharmaceut Co Ltd | Screening method for bone metastasis inhibitor |
-
2005
- 2005-07-29 JP JP2005221399A patent/JP2008260689A/en active Pending
-
2006
- 2006-07-20 WO PCT/JP2006/314412 patent/WO2007013352A1/en not_active Ceased
Also Published As
| Publication number | Publication date |
|---|---|
| WO2007013352A1 (en) | 2007-02-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4764874B2 (en) | Tumor associated peptides that bind MHC molecules | |
| Maraskovsky et al. | NY-ESO-1 protein formulated in ISCOMATRIX adjuvant is a potent anticancer vaccine inducing both humoral and CD8+ t-cell-mediated immunity and protection against NY-ESO-1+ tumors | |
| JP5393144B2 (en) | HLA-A * 3303 restricted WT1 peptide and pharmaceutical composition comprising the same | |
| CN101835892B (en) | CDCA1 peptide and pharmaceutical agent comprising the same | |
| JP5114403B2 (en) | SART3-derived peptides useful for cancer vaccine therapy for HLA-A3 supertype allele positive prostate cancer patients | |
| JP5065273B2 (en) | HLA-A24 molecule binding peptide derived from KIF | |
| Yang et al. | Generated SecPen_NY-ESO-1_ubiquitin-pulsed dendritic cell cancer vaccine elicits stronger and specific T cell immune responses | |
| CN109970846A (en) | A kind of tumor associated antigen XAGE-1b nonapeptide and its application | |
| JP4972691B2 (en) | Lck-derived peptide useful for cancer vaccine therapy for HLA-A3 supertype allele positive cancer patients | |
| WO2020145222A1 (en) | Novel neoantigens and cancer immunotherapy using same | |
| Bright et al. | SV40 Tag-specific cytotoxic T lymphocytes generated from the peripheral blood of malignant pleural mesothelioma patients | |
| CN107875376A (en) | Microvesicle, preparation method and the usage comprising NY ESO 1 | |
| CN105163754A (en) | Prostate-specific tumor antigen and uses thereof | |
| JP4945444B2 (en) | Prostate-related protein-derived peptide that is a cancer vaccine candidate for HLA-A3 supertype allele molecule positive prostate cancer patients | |
| WO2017086354A1 (en) | Hla-a11 restrictive cytotoxic t cell epitope peptide | |
| JP7103571B2 (en) | Immunogenic peptide composition | |
| WO2015005479A1 (en) | Tumor antigen peptide | |
| EP1930427B1 (en) | Squamous cell carcinoma antigen-derived peptide binding to hla-a24 molecule | |
| JP2003522195A (en) | Methods and compositions for the treatment of hepatocellular carcinoma | |
| JP2008260689A (en) | Pharmaceutical composition containing peptide derived from HLA-A24 molecule binding parathyroid hormone related protein | |
| Tüting et al. | DNA vaccines targeting dendritic cells for the immunotherapy of cancer | |
| JP6918333B2 (en) | Peptides recognized by cell-mediated immunity and pharmaceuticals using them | |
| JP4925033B2 (en) | Stress-induced anti-apoptotic molecule (IEX-1) derived peptide | |
| JP6900610B2 (en) | HIF-1α-derived peptide that can bind to HLA-A24 molecule and is recognized by cell-mediated immunity, and renal cell carcinoma vaccine containing it | |
| JP6784964B2 (en) | EZH2-derived peptide useful for cancer vaccine therapy for HLA-A3 supertype allele-positive prostate cancer patients |