JP2004166702A - Method for detecting Paget's disease of bone - Google Patents
Method for detecting Paget's disease of bone Download PDFInfo
- Publication number
- JP2004166702A JP2004166702A JP2003379085A JP2003379085A JP2004166702A JP 2004166702 A JP2004166702 A JP 2004166702A JP 2003379085 A JP2003379085 A JP 2003379085A JP 2003379085 A JP2003379085 A JP 2003379085A JP 2004166702 A JP2004166702 A JP 2004166702A
- Authority
- JP
- Japan
- Prior art keywords
- seq
- chondroitin
- disease
- bone
- paget
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Landscapes
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
Abstract
Description
本発明は、骨パジェット病の検出方法に関連し、より詳細にはコンドロイチン/コンドロイチン硫酸の合成に関与する酵素の遺伝子の変異又は発現量と、骨パジェット病とを関連づける骨パジェット病の検出方法に関する。 The present invention relates to a method for detecting Paget's disease of bone, and more particularly, to a method for detecting Paget's disease of bone that associates mutation or expression level of a gene of an enzyme involved in the synthesis of chondroitin / chondroitin sulfate with bone Paget disease. .
骨パジェット病は破骨細胞と骨芽細胞とが共に増加し、骨吸収とそれに伴う二次的な骨形成が局所的に異常に亢進し、骨の変形や肥厚を来す疾病である。この疾病はウイルス感染症が引き金となって発症するという説が有力であり、患者の末梢血液と骨髄の単核球から抽出したRNAを使用して逆転写ポリメラーゼチェインリアクション法(RT-PCR法)で麻疹ウイルスを検出できたことが非特許文献1には記載されている。しかし、麻疹ウイルスが直接骨パジェット病を引き起こすことは示されておらず、骨パジェット病の病態を引き起こす原因は不明である。この疾病の患者は我が国に於いては希であるが、欧米には多くの患者がおり、高齢となるほど高い発症率となること、女性よりも男性で発症率が高いことが非特許文献2には記載されている。
Bone Paget's disease is a disease in which both osteoclasts and osteoblasts increase, and bone resorption and secondary bone formation associated therewith are abnormally enhanced locally, resulting in bone deformation and thickening. The prevailing theory is that the disease is triggered by a viral infection, and reverse transcription polymerase chain reaction (RT-PCR) using RNA extracted from the patient's peripheral blood and bone marrow mononuclear cells. Non-Patent Document 1 describes that measles virus could be detected by the method described above. However, it has not been shown that the measles virus causes bone Paget's disease directly, and the cause of the pathology of bone Paget's disease is unknown.
また、骨パジェット病の原因となる変異遺伝子座は既に公知で非特許文献3に記載されているが、この遺伝子座にはいくつもの遺伝子が存在し、何れの遺伝子に変異を来した場合に骨パジェット病となるのかは知られていなかった。従って、簡便な方法で骨パジェット病の診断を行うためには、何れの遺伝子に変異を来した場合に当該疾病が発症するのかを解明する必要があった。 In addition, a mutant locus causing bone Paget's disease is already known and described in Non-Patent Document 3, but there are many genes at this locus, and when any of the genes is mutated, bone It was not known if Paget's disease would occur. Therefore, in order to diagnose Paget's disease of bone by a simple method, it is necessary to clarify which gene is mutated to cause the disease.
骨パジェット病の病態を引き起こす原因遺伝子を解明し、骨パジェット病の簡便な検出方法に対する期待が高まっていた。 Expectations for a simple method for detecting Paget's disease of bone have been elucidated by elucidating the causative genes that cause the pathology of Paget's disease of bone.
本発明者等は上記課題を解決するために鋭意検討した結果、骨パジェット病の遺伝子変異が何れもコンドロイチン/コンドロイチン硫酸の合成に関与するDNAの遺伝子座に起こっていることを発見し、これを骨パジェット病の検出に応用して本発明を完成した。 The present inventors have conducted intensive studies in order to solve the above-mentioned problems, and as a result, have found that all of the gene mutations in Paget's disease of bone have occurred at loci of DNA involved in the synthesis of chondroitin / chondroitin sulfate. The present invention has been completed by applying it to the detection of Paget's disease of bone.
すなわち、本発明の要旨はコンドロイチン合成酵素をコードする遺伝子の変異又は発現量と、骨パジェット病とを関連づけることを特徴とする骨パジェット病の検出方法である。 That is, the gist of the present invention is a method for detecting Paget's disease of bone, wherein the mutation or expression level of a gene encoding chondroitin synthase is associated with Paget's disease of bone.
本発明により、骨パジェット病の新たな検出方法、及び骨パジェット病の病態動物が提供される。 According to the present invention, a novel method for detecting Paget's disease of bone and a pathological animal having Paget's disease of bone are provided.
本発明検出方法は、コンドロイチン合成酵素遺伝子の変異又は発現量と、骨パジェット病とを関連づけることを特徴とする骨パジェット病の検出方法である。 The detection method of the present invention is a method for detecting Paget's disease of bone, wherein the mutation or expression level of a chondroitin synthase gene is associated with Paget's disease of bone.
本発明検出方法に於ける「コンドロイチン合成酵素」とは、コンドロイチン又はコンドロイチン硫酸の合成に関与する酵素である限りに於いて特に限定はされない。つまりコンドロイチンやコンドロイチン硫酸は通常はプロテオグリカンとして生体内で合成されるので、コンドロイチン/コンドロイチン硫酸の基本骨格の伸長に関与する酵素のみならず、例えばプロテオグリカンのタンパク質とグリコサミノグリカンの連結部分を合成する酵素等も包含する。このような酵素が変異を起こしたり、発現がなされないとコンドロイチン/コンドロイチン硫酸の合成がなされない。 The “chondroitin synthase” in the detection method of the present invention is not particularly limited as long as it is an enzyme involved in the synthesis of chondroitin or chondroitin sulfate. In other words, chondroitin and chondroitin sulfate are usually synthesized in vivo as proteoglycans, so they synthesize not only enzymes involved in elongation of the basic skeleton of chondroitin / chondroitin sulfate, but also, for example, a linking portion between proteoglycan protein and glycosaminoglycan. Enzymes and the like are also included. If such an enzyme is mutated or not expressed, chondroitin / chondroitin sulfate is not synthesized.
このような本発明検出方法における「コンドロイチン合成酵素」は、「コンドロイチン/コンドロイチン硫酸の非還元末端の糖残基に対してD-グルクロン酸残基又はN-アセチル-D-ガラクトサミン残基を転移する活性を有する糖転移酵素」(便宜上、以下「糖転移酵素1」とも記載する)又は「『アミノ酸残基に結合したキシロース残基』にD-ガラクトースをβ1,4グリコシド結合で結合させる糖転移酵素」(便宜上、以下「糖転移酵素2」とも記載する)であることが好ましい。
The “chondroitin synthase” in the detection method of the present invention transfers “D-glucuronic acid residue or N-acetyl-D-galactosamine residue to the non-reducing terminal sugar residue of chondroitin / chondroitin sulfate. Glycosyltransferase having D-galactose bound to β- and 4-glycosidic bonds to “xylose residue linked to amino acid residue” (hereinafter also referred to as “glycosyltransferase 1” for convenience) (Hereinafter also referred to as “
上述の「糖転移酵素1」とは、「コンドロイチン/コンドロイチン硫酸の非還元末端の糖残基に対してD-グルクロン酸(以下単に「GlcUA」とも記載する)残基又はN-アセチル-D-ガラクトサミン(以下単に「N-アセチルガラクトサミン」又は「GalNAc」とも記載する)残基を転移する活性」を有する限りにおいて特に限定はされない。このような糖転移酵素1はコンドロイチン/コンドロイチン硫酸の伸長に関与しており、このような酵素に変異又は発現の抑制が起こると正常なコンドロイチン/コンドロイチン硫酸の生合成が妨げられ、骨形成に異常を来す骨パジェット病に繋がると考えられる。 The above-mentioned “glycosyltransferase 1” refers to “D-glucuronic acid (hereinafter also simply referred to as“ GlcUA ”) residue or N-acetyl-D- residue relative to the sugar residue at the non-reducing end of chondroitin / chondroitin sulfate. There is no particular limitation as long as it has an activity of transferring a galactosamine (hereinafter, also simply referred to as “N-acetylgalactosamine” or “GalNAc”) residue. Such glycosyltransferase 1 is involved in elongation of chondroitin / chondroitin sulfate, and when mutation or suppression of expression occurs in such an enzyme, normal biosynthesis of chondroitin / chondroitin sulfate is hindered and bone formation is abnormal. Is thought to lead to Paget's disease of bone.
上記「糖転移酵素1」における「コンドロイチン」とは、ウロン酸(以下単に「UA」とも記載する)残基とGalNAc残基とが1,3グリコシド結合で結合した二糖が、β1,4グリコシド結合で繰り返して結合してなる基本骨格(すなわち-[4UA1-3GalNAcβ1-]n:nは2以上の整数を示す)を有するグリコサミノグリカンの一種である。「コンドロイチン」はこの基本骨格に硫酸基が結合していないが、「コンドロイチン硫酸」はGalNAc残基の2位、4位、又は6位、又はウロン酸残基の2位の炭素原子が硫酸化されている。 The “chondroitin” in the above “glycosyltransferase 1” refers to a disaccharide in which a uronic acid (hereinafter, also simply referred to as “UA”) residue and a GalNAc residue are linked by a 1,3 glycosidic bond to β1,4 glycoside. It is a kind of glycosaminoglycan having a basic skeleton (ie,-[4UA1-3GalNAcβ1-] n : n is an integer of 2 or more) formed by bonding repeatedly. Chondroitin does not have a sulfate group attached to this basic skeleton, but chondroitin sulfate has a sulfated carbon atom at the 2-, 4-, or 6-position of a GalNAc residue, or the 2-position of a uronic acid residue. Have been.
「コンドロイチン/コンドロイチン硫酸の非還元末端の糖残基」とは、コンドロイチン/コンドロイチン硫酸の基本骨格を構成するGalNAc残基及びUA残基の何れかであり、「糖転移酵素1」は、上記糖残基がGalNAc残基の場合はUAを転移し、上記糖残基がUA残基の場合はGalNAcを転移するが、何れか一方の転移活性を少なくとも有している酵素である。 The “sugar residue at the non-reducing terminal of chondroitin / chondroitin sulfate” is any one of a GalNAc residue and a UA residue constituting the basic skeleton of chondroitin / chondroitin sulfate, and “glycotransferase 1” is When the residue is a GalNAc residue, it transfers UA, and when the sugar residue is a UA residue, it transfers GalNAc, but this enzyme has at least one transfer activity.
このような「糖転移酵素1」の具体例としては、「配列番号2記載のアミノ酸番号1乃至882からなるアミノ酸配列からなるタンパク質を含むコンドロイチン合成酵素」が挙げられる。 Specific examples of such “glycosyltransferase 1” include “chondroitin synthase containing a protein having an amino acid sequence consisting of amino acids 1 to 882 of SEQ ID NO: 2”.
当該酵素は下記式1で示される構造を含むGalNAc受容体にGalNAc供与体基質(例えばUDP-GalNAc)からGalNAc残基を転移し、下記式2で示される構造を含む化合物を合成する活性を有すると共に、下記式3で示される構造を含むGlcUA受容体にGlcUA供与体基質(例えばUDP-GlcUA)からGlcUA残基を転移し、下記式4で示される構造を含む化合物を合成する活性を有する(本明細書中参考例2参照)。
The enzyme has an activity of transferring a GalNAc residue from a GalNAc donor substrate (eg, UDP-GalNAc) to a GalNAc acceptor having a structure represented by the following formula 1, and synthesizing a compound having a structure represented by the following
GlcUAβ1−(3GalNAcβ1−4GlcUAβ1)k−(3GalNAc)l (1)
GalNAcβ1−4GlcUAβ1-(3GalNAcβ1-4GlcUAβ1)k−(3GalNAc)l (2)
GalNAcβ1−(4GlcUAβ1−3GalNAcβ1)m−(4GlcUA)n (3)
GlcUAβ1−3GalNAcβ1−(4GlcUAβ1−3GalNAcβ1)m−(4GlcUA)n (4)
式1乃至4中、「−」はグリコシド結合を示し、数字は前記グリコシド結合が存在する糖環の炭素位置を示す。また「α」及び「β」は糖環1位の前記グリコシド結合のアノマーを示し、5位CH2OH又はCOOHとの位置関係がトランスのものを「α」、シスのものを「β」で示す。k及びmは1以上の整数を示し、l及びnは1又は0を示す。
GlcUAβ1- (3GalNAcβ1-4GlcUAβ1) k- (3GalNAc) l (1)
GalNAcβ1-4GlcUAβ1- (3GalNAcβ1-4GlcUAβ1) k − (3GalNAc) l (2)
GalNAcβ1- (4GlcUAβ1-3GalNAcβ1) m- (4GlcUA) n (3)
GlcUAβ1-3GalNAcβ1- (4GlcUAβ1-3GalNAcβ1) m − (4GlcUA) n (4)
In the formulas 1 to 4, “-” indicates a glycosidic bond, and a number indicates a carbon position of the sugar ring where the glycosidic bond is present. “Α” and “β” denote the anomers of the glycosidic bond at the 1-position of the sugar ring, wherein the trans-position relative to the 5-position CH 2 OH or COOH is “α”, and the cis-position is “β”. Show. k and m each represent an integer of 1 or more, and l and n each represent 1 or 0.
塩基配列(配列番号1)からなる当該酵素遺伝子はOMIM(Online Mendelian Inheritance in Man)を使用して遺伝子座を調べると5q31.1に存在することが明かとなった(参考例1参照)。 Examination of the locus of the enzyme gene consisting of the nucleotide sequence (SEQ ID NO: 1) using OMIM (Online Mendelian Inheritance in Man) revealed that it was present at 5q31.1 (see Reference Example 1).
また「糖転移酵素1」の他の例としては、例えば「配列番号4記載のアミノ酸番号1乃至755からなるアミノ酸配列からなるタンパク質を含むコンドロイチン合成酵素」が挙げられる。 Another example of “glycosyltransferase 1” is “chondroitin synthase containing a protein consisting of an amino acid sequence consisting of amino acids 1 to 755 of SEQ ID NO: 4”.
当該酵素は前記式1で示される構造を含むGalNAc受容体にGalNAc供与体(例えばUDP-GalNAc)からGalNAc残基を転移し、前記式2で示される構造を含む化合物を合成する活性を有すると共に、前記式3で示される構造を含むGlcUA受容体にGlcUA供与体(例えばUDP-GlcUA)からGlcUA残基を転移し、前記式4で示される構造を含む化合物を合成する活性を有する(本明細書中参考例4参照)。
The enzyme has an activity of transferring a GalNAc residue from a GalNAc donor (for example, UDP-GalNAc) to a GalNAc acceptor having the structure represented by the above formula 1, and synthesizing a compound having the structure represented by the
塩基配列(配列番号3)からなる当該酵素遺伝子はOMIMを使用して遺伝子座を調べると遺伝子座を調べると2q36.3に存在することが明かとなった(本明細書中参考例3参照)。 Examination of the gene locus using OMIM revealed that the enzyme gene consisting of the base sequence (SEQ ID NO: 3) was present at 2q36.3 (see Reference Example 3 in this specification). .
なお、「コンドロイチンの非還元末端の糖残基に対してGlcUA残基又はGalNAc残基を転移する活性」は、例えば放射能などで標識したGlcUA供与体基質又はGalNAc供与体基質と、放射能で標識していないコンドロイチン/コンドロイチン硫酸(これらを低分子化して得られる低分子コンドロイチン/低分子コンドロイチン硫酸(20糖以下の糖鎖)も含む)の受容体基質とを用いて、酵素反応させた後、反応生成物についてゲル濾過とオートラジオグラフやシンチレーションカウンターなどを用いることで容易に検出することができる。上記GlcUA供与体基質としては、GlcUAを有する糖ヌクレオチドであることが好ましく、例えばアデノシン二リン酸-D-グルクロン酸(ADP-GlcUA)、ウリジン二リン酸-D-グルクロン酸(UDP-GlcUA)、グアノシン二リン酸-D-グルクロン酸(GDP-GlcUA)、シチジン二リン酸-D-グルクロン酸(CDP-GlcUA)等が例示され、UDP-GlcUAが最も好ましい。生体内ではUDP-GlcUAがGlcUA供与体基質として働いているからである。 The `` activity of transferring a GlcUA residue or a GalNAc residue to a sugar residue at the non-reducing end of chondroitin '' is, for example, a GlcUA donor substrate or a GalNAc donor substrate labeled with radioactivity, and the like. After an enzymatic reaction using an unlabeled chondroitin / chondroitin sulfate (including low-molecular-weight chondroitin / low-molecular-weight chondroitin sulfate (including sugar chains of 20 sugars or less) obtained by reducing the molecular weight thereof) with an acceptor substrate The reaction product can be easily detected by using gel filtration and an autoradiograph or a scintillation counter. The GlcUA donor substrate is preferably a sugar nucleotide having GlcUA, for example, adenosine diphosphate-D-glucuronic acid (ADP-GlcUA), uridine diphosphate-D-glucuronic acid (UDP-GlcUA), Examples include guanosine diphosphate-D-glucuronic acid (GDP-GlcUA) and cytidine diphosphate-D-glucuronic acid (CDP-GlcUA), with UDP-GlcUA being most preferred. This is because UDP-GlcUA works as a GlcUA donor substrate in a living body.
また、上記GalNAc供与体基質としては、GalNAcを有する糖ヌクレオチドであることが好ましく、例えばアデノシン二リン酸-N-アセチル-D-ガラクトサミン(ADP-GalNAc)、ウリジン二リン酸-N-アセチル-D-ガラクトサミン(UDP-GalNAc)、グアノシン二リン酸-N-アセチル-D-ガラクトサミン(GDP-GalNAc)、シチジン二リン酸-N-アセチル-D-ガラクトサミン(CDP-GalNAc)等が例示され、UDP-GalNAcが最も好ましい。生体内ではUDP-GalNAcがGalNAc供与体基質として働いているからである。 Further, the GalNAc donor substrate is preferably a sugar nucleotide having GalNAc, for example, adenosine diphosphate-N-acetyl-D-galactosamine (ADP-GalNAc), uridine diphosphate-N-acetyl-D -Galactosamine (UDP-GalNAc), guanosine diphosphate-N-acetyl-D-galactosamine (GDP-GalNAc), cytidine diphosphate-N-acetyl-D-galactosamine (CDP-GalNAc), and UDP- GalNAc is most preferred. This is because UDP-GalNAc works as a GalNAc donor substrate in the living body.
上記「糖転移酵素2」は「『アミノ酸残基に結合したキシロース残基』にD-ガラクトース(以下単に「ガラクトース」又は「Gal」とも記載する)をβ1,4グリコシド結合で転移する働きを有する糖転移酵素」である限りに於いて特に限定はされない。このような糖転移酵素2はコンドロイチン/コンドロイチン硫酸の生成初期の段階に関与しており、このような酵素に変異が起こると正常なコンドロイチン/コンドロイチン硫酸の生合成が妨げられるため、骨形成に異常を来す骨パジェット病に繋がると考えられる。
The above “
上記「糖転移酵素2」に於ける「アミノ酸残基」とは、ペプチド(タンパク質)を形成するアミノ酸であることが好ましく、特に生体内に存在するコンドロイチン/コンドロイチン硫酸プロテオグリカンの構造中、ペプチド(タンパク質)とコンドロイチン/コンドロイチン硫酸との結合部分に存在する特徴的四糖構造(GlcUAβ1−3Galβ1−3Galβ1−4Xyl:以下「リンケージ四糖」と記載する)の還元末端に存在するキシロースが結合しているアミノ酸が最も好ましい。このようなアミノ酸として最も好ましくはL-セリンが例示される。
The “amino acid residue” in the above “
すなわち「糖転移酵素2」は下記式5で示される構造を含むGal受容体にGal供与体基質(例えばUDP-Gal)からGal残基を転移し、下記式6で示される構造を含む化合物を合成する活性を有する(本明細書中参考例5参照)。
That is, “
Xylβ1−Ser (5)
Galβ1−4Xylβ1−Ser (6)
上記式5及び6において、「Ser」は上記「Xyl」で示されるキシロース残基がその側鎖に結合したセリン残基(ペプチド鎖中の場合を含む)を示し、「Xyl」は前記「Ser」で示されるセリン残基の側鎖に結合したキシロース残基を示し、「−」、「β」、数字は前記式1乃至4と同じである。
Xylβ1-Ser (5)
Galβ1-4Xylβ1-Ser (6)
In the above formulas 5 and 6, “Ser” represents a serine residue (including the case in a peptide chain) in which the xylose residue represented by the above “Xyl” is bonded to its side chain, and “Xyl” is the above “Ser” "Represents a xylose residue bonded to the side chain of the serine residue, and"-"," β ", and the numbers are the same as in the above formulas 1 to 4.
塩基配列(配列番号5)からなる当該酵素遺伝子はOMIMを使用して遺伝子座を調べると5q35に存在することが明かとなった(本明細書中参考例5参照)。 Examination of the gene locus using OMIM revealed that the enzyme gene consisting of the nucleotide sequence (SEQ ID NO: 5) was present at 5q35 (see Reference Example 5 in this specification).
なお、「『アミノ酸残基に結合したキシロース残基』にGalをβ1,4グリコシド結合で転移する活性」は、例えば放射能などで標識したGal供与体基質と、放射能で標識していないキシロース結合ペプチド(例えば配列番号15:第9番目のアミノ酸残基であるセリン残基に側鎖としてキシロースが結合しているビクニンのN-末端配列:ペプチド研究所製)とを用いて反応させた後、反応生成物についてゲル濾過とオートラジオグラフやシンチレーションカウンターなどを用いることで容易に検出することができる。なお、上記Gal供与体基質としては、Galを有する糖ヌクレオチドであることが好ましく、例えばアデノシン二リン酸-D-ガラクトース(ADP-Gal)、ウリジン二リン酸-D-ガラクトース(UDP-Gal)、グアノシン二リン酸-D-ガラクトース(GDP-Gal)、シチジン二リン酸-D-ガラクトース(CDP-Gal)等が例示され、UDP-Galが最も好ましい。生体内ではUDP-GalがGal供与体基質として働いているからである。 The “activity of transferring Gal to a“ xylose residue linked to an amino acid residue ”by β1,4 glycosidic bond” is, for example, a Gal donor substrate labeled with radioactivity or the like, and a xylose not labeled with radioactivity. After reacting with a binding peptide (for example, SEQ ID NO: 15: N-terminal sequence of bikunin in which xylose is bonded as a side chain to a serine residue at the ninth amino acid residue: manufactured by Peptide Institute) The reaction product can be easily detected by using gel filtration and an autoradiograph or a scintillation counter. The Gal donor substrate is preferably a sugar nucleotide having Gal, for example, adenosine diphosphate-D-galactose (ADP-Gal), uridine diphosphate-D-galactose (UDP-Gal), Examples include guanosine diphosphate-D-galactose (GDP-Gal) and cytidine diphosphate-D-galactose (CDP-Gal), with UDP-Gal being most preferred. This is because UDP-Gal works as a Gal donor substrate in vivo.
骨パジェット病に於ける遺伝子の変異としては、例えば亜種であるPDB2においては18q22.1、PDB3においては5q35、PDB4においては5q31に変異が起こっていることが知られており(OMIM #602080)、また家族性の骨パジェット病に於ける遺伝子の変異として、2q36、10q13、及び5q35に変異が起こっていることが知られている(Am. J. Hum. Genet. 69(2001), pp.1055-1061)。このような既知の変異部位には数個乃至十数個の遺伝子がコードされているが、上述した各コンドロイチン合成酵素遺伝子の存在位置は配列番号1(K3)が5q31.1、配列番号3(K11)が2q36.3、そして配列番号5(β4GalT7)は5q35であり、上記変異の存在する位置と各々完全に一致している。このようにコンドロイチン/コンドロイチン硫酸の合成に関わるこれらの酵素の遺伝子が全て骨パジェット病の遺伝子変異部位と重複することから、これらの遺伝子の変異は、コンドロイチン/コンドロイチン硫酸の生合成に障害を起こして骨パジェット病の発症に繋がっている蓋然性が極めて高い。 As a gene mutation in Paget's disease of bone, for example, it is known that a mutation occurs in 18q22.1 in PDB2, 5q35 in PDB3, and 5q31 in PDB4 (OMIM # 602080). It is known that mutations occur in 2q36, 10q13, and 5q35 as genes in familial bone Paget's disease (Am. J. Hum. Genet. 69 (2001), pp. 1055-1061). Several to a dozen or so genes are encoded in such known mutation sites, and the location of each of the above-mentioned chondroitin synthase genes is 5q31.1 in SEQ ID NO: 1 (K3) and 3 K11) is 2q36.3, and SEQ ID NO: 5 (β4GalT7) is 5q35, which is completely identical to the position where the above mutation exists. As described above, since the genes of these enzymes involved in the synthesis of chondroitin / chondroitin sulfate all overlap with the gene mutation sites in Paget's disease of bone, mutations in these genes cause disorders in the biosynthesis of chondroitin / chondroitin sulfate. The probability of causing Paget's disease of bone is extremely high.
本明細書において使用する用語「コンドロイチン合成酵素遺伝子の変異又は発現量と、骨パジェット病とを関連づける」とは、コンドロイチン合成酵素遺伝子の変異が検出された場合、又は該遺伝子の発現量が健常人と比べて低下した場合に骨パジェット病であると判断することをいう。 As used herein, the term "associating the mutation or expression level of the chondroitin synthase gene with the Paget's disease of the bone" means that a mutation in the chondroitin synthase gene is detected, or that the expression level of the gene is healthy. It means that it is determined to be a Paget's disease of bone when it is lower than that of.
本明細書において使用する用語「遺伝子の変異」とは、遺伝子の構造変化をいい、「変異」には、点突然変異、逆位、欠失、挿入、重複、転座等が含まれる。また、「変異遺伝子」とは、配列番号1、配列番号3、配列番号5、配列番号65、配列番号67、又は配列番号69に示される塩基配列において、1若しくは複数個のヌクレオチドが置換し若しくは欠失し、又は該塩基配列に1若しくは複数個のヌクレオチドが挿入され若しくは付加された塩基配列を意味する。ここで、「複数個」とは、好ましくは2個以上、より好ましくは4個以上、さらにより好ましくは6個以上、最も好ましくは10個以上である。 As used herein, the term “gene mutation” refers to a structural change in a gene, and the “mutation” includes point mutation, inversion, deletion, insertion, duplication, translocation and the like. Further, the “mutant gene” refers to a nucleotide sequence represented by SEQ ID NO: 1, SEQ ID NO: 3, SEQ ID NO: 5, SEQ ID NO: 65, SEQ ID NO: 67, or SEQ ID NO: 69, in which one or more nucleotides are substituted or It means a nucleotide sequence that has been deleted, or one or more nucleotides have been inserted or added to the nucleotide sequence. Here, the “plurality” is preferably 2 or more, more preferably 4 or more, still more preferably 6 or more, and most preferably 10 or more.
コンドロイチン合成酵素遺伝子の変異の態様は、好ましくは点突然変異、欠失、挿入、逆位、重複、転座、より好ましくは、点突然変異、欠失、挿入、逆位、転座、さらに好ましくは、点突然変異、欠失、挿入、転座、最も好ましくは点突然変異、欠失、挿入である。 Aspects of the mutation of the chondroitin synthase gene are preferably point mutation, deletion, insertion, inversion, duplication, translocation, more preferably point mutation, deletion, insertion, inversion, translocation, and still more preferably. Are point mutations, deletions, insertions, translocations, most preferably point mutations, deletions, insertions.
本明細書において使用する用語「遺伝子の発現」とは、典型的には、DNA又はその一部からRNAへの転写、又は該RNA又はその一部からタンパク質への翻訳をいう。従って、「遺伝子の発現量」というときは、遺伝子から転写されるRNAの量、又は該RNAから翻訳されるタンパク質の量をいう。 As used herein, the term "gene expression" typically refers to the transcription of DNA or a portion thereof into RNA, or the translation of the RNA or a portion thereof into a protein. Therefore, the term “gene expression level” refers to the amount of RNA transcribed from the gene or the amount of protein translated from the RNA.
RNAの発現量は、例えば、後述する実施例1に記載した表1のプライマーを使用したPCR法を用いて定量することができる。PCR法では、定量的PCR法の使用が好ましく、キネティックス分析のためのRT−PCR法、定量的リアルタイムPCR法が例示される。本発明によれば、RNAの定量は、これらに限定されるものではなく、ノーザンブロット、ドットブロット、DNAマイクロアレイ等を使用することも可能である。一方、同一組織等に広く一般的に存在する遺伝子の核酸、例えばグリセルアルデヒド−3リン酸−脱水素酵素(GAPDH)、β−アクチンをコードする核酸を対照として利用することができる。また、タンパク質の発現量は、例えば、ELISA法、ウェスタンブロットを用いて定量することができる。 The expression level of RNA can be quantified using, for example, a PCR method using the primers in Table 1 described in Example 1 described below. In the PCR method, the use of a quantitative PCR method is preferable, and an RT-PCR method for kinetic analysis and a quantitative real-time PCR method are exemplified. According to the present invention, the quantification of RNA is not limited to these, and Northern blots, dot blots, DNA microarrays and the like can also be used. On the other hand, nucleic acids of genes widely present in the same tissue or the like, for example, nucleic acids encoding glyceraldehyde-3-phosphate-dehydrogenase (GAPDH) and β-actin can be used as controls. The expression level of the protein can be quantified using, for example, an ELISA method or a Western blot.
本発明検出方法は具体的には以下の様にして行うことができる。 The detection method of the present invention can be specifically performed as follows.
すなわち、例えば遺伝子を含む検体(例えば上皮組織、結合組織等、好ましくは結合組織が挙げられ、採取が極めて容易で、且つ得られた検体が新鮮であることから特に好ましくは血液が挙げられる)から、例えば既存のRNA調製キット(例えばRNA Extraction Kit:アマシャムバイオサイエンス株式会社製など)を用いて全RNAを抽出・精製することができる。抽出・精製された全RNAを用いてK3、K11、及びβ4Gal-T7の発現量を既存のキット(例えばSUPERSCRIPT First-Strand Synthesis System for RT-PCR(インビトロジェン社製)等)を用いてRT-PCR法などの方法で定量することができる。使用する5'プライマー、3'プライマー、及びプローブの組み合わせの例としては、K3の発現量を定量する場合は配列番号56、配列番号57、配列番号58、K11の発現量を定量する場合は配列番号59、配列番号60、配列番号61、β4Gal-T7の発現量を定量する場合は配列番号62、配列番号63、配列番号64の組み合わせが挙げられるが、当業者であれば定量の目的に応じて適宜選択して調製することが可能である。 That is, for example, from a sample containing a gene (e.g., epithelial tissue, connective tissue, etc., preferably connective tissue is mentioned, and it is very easy to collect, and blood is particularly preferable because the obtained sample is fresh). For example, total RNA can be extracted and purified using an existing RNA preparation kit (for example, RNA Extraction Kit: manufactured by Amersham Bioscience). Using the extracted and purified total RNA, the expression levels of K3, K11, and β4Gal-T7 were determined by RT-PCR using an existing kit (eg, SUPERSCRIPT First-Strand Synthesis System for RT-PCR (manufactured by Invitrogen)). It can be quantified by a method such as a method. Examples of the combination of the 5 ′ primer, 3 ′ primer, and probe used include SEQ ID NO: 56 when quantifying the expression level of K3, SEQ ID NO: 57, SEQ ID NO: 58, and sequence when quantifying the expression level of K11. When quantifying the expression level of SEQ ID NO: 59, SEQ ID NO: 60, SEQ ID NO: 61, β4Gal-T7, a combination of SEQ ID NO: 62, SEQ ID NO: 63, SEQ ID NO: 64 can be mentioned. It is possible to select and prepare as appropriate.
そして、例えばこれらの定量の結果、K3、K11及びβ4GalT7の何れかの遺伝子の発現が一部又は完全に抑制されている患者を骨パジェット病の危険性が高い患者とすることができる。また、上記定量は上記で例示したようにK3、K11及びβ4Gal-T7の遺伝子の転写量をRNA量から定量して行うこともできるが、例えば常法に従って調製したK3、K11又はβ4Gal-T7の抗体などを使用してK3、K11又はβ4Gal-T7のタンパク質量を直接定量して行うことも可能であり、また検体中の上記酵素の活性を直接測定して酵素量を定量して骨パジェット病と関連づけることも可能である。 Then, for example, as a result of these quantifications, a patient in which the expression of any of K3, K11 and β4GalT7 gene is partially or completely suppressed can be regarded as a patient at high risk of bone Paget disease. In addition, the quantification can be performed by quantifying the amount of transcription of the K3, K11 and β4Gal-T7 genes from the RNA amount as exemplified above, for example, K3, K11 or β4Gal-T7 prepared according to a conventional method. It is also possible to directly determine the amount of K3, K11 or β4Gal-T7 protein using an antibody or the like. It is also possible to associate with.
より具体的には、後述する実施例2に記載されているように、骨パジェット病の患者の末梢血単核球と正常な末梢血単核球でのコンドロイチン合成酵素遺伝子の発現量の比を定量PCRによって測定することによって骨パジェット病と判断することができる。本発明によれば、骨パジェット病であると判断できる発現量の比は、1/2以下、好ましくは1/5以下、さらにより好ましくは1/10以下である。なお、本明細書において使用される用語「測定」には、検出、増幅、定量、及び半定量のいずれもが包含される。 More specifically, as described in Example 2 below, the ratio of the expression level of the chondroitin synthase gene in peripheral blood mononuclear cells of a patient with bone Paget disease and normal peripheral blood mononuclear cells was determined. Bone Paget disease can be determined by measuring by quantitative PCR. According to the present invention, the ratio of the expression level that can be determined to be bone Paget's disease is 1/2 or less, preferably 1/5 or less, and still more preferably 1/10 or less. The term “measurement” as used herein includes any of detection, amplification, quantification, and semi-quantification.
本発明によれば、コンドロイチン合成酵素遺伝子の変異の存在を確認することによって骨パジェット病を検出することができる。即ち、骨パジェット病の患者の末梢血単核球から抽出したコンドロイチン合成酵素遺伝子の塩基配列と正常な末梢血単核球から抽出したコンドロイチン合成酵素遺伝子の塩基配列とを比較し、変異の存在を検出することによって骨パジェット病であると判断することができる。より具体的には、後述する実施例1に記載されているように、本明細書配列表に記載されたK3、K11及びβ4Gal-T7の塩基配列を元に適宜調製したプライマーを用いてゲノムのDNAから直接K3、K11又はβ4Gal-T7の遺伝子をPCR法などの手法を用いて増幅し、公知の塩基配列決定法に従って塩基配列を解析し、これらの遺伝子に変異が存在する場合に骨パジェット病であると結論づけることが可能である。 According to the present invention, Paget's disease of bone can be detected by confirming the presence of a mutation in the chondroitin synthase gene. That is, the nucleotide sequence of the chondroitin synthase gene extracted from peripheral blood mononuclear cells of a patient with bone Paget disease is compared with the nucleotide sequence of the chondroitin synthase gene extracted from normal peripheral blood mononuclear cells, and the presence of the mutation is determined. By detecting, it can be determined that there is bone Paget disease. More specifically, as described in Example 1 described below, the genome of the genome was prepared using primers appropriately prepared based on the base sequences of K3, K11 and β4Gal-T7 described in the sequence listing of the present specification. The K3, K11 or β4Gal-T7 gene is directly amplified from DNA using a method such as PCR, and the nucleotide sequence is analyzed according to a known nucleotide sequencing method. It is possible to conclude that
骨パジェット病であると判断できる変異したヌクレオチドの数は、1以上、好ましくは4以上、さらにより好ましくは6以上、最も好ましくは10以上である。 The number of mutated nucleotides that can be determined to be a Paget disease of bone is 1 or more, preferably 4 or more, still more preferably 6 or more, and most preferably 10 or more.
コンドロイチン合成酵素遺伝子の変異の態様は、好ましくは点突然変異、欠失、挿入、逆位、重複、転座、より好ましくは、点突然変異、欠失、挿入、逆位、転座、さらに好ましくは、点突然変異、欠失、挿入、転座、最も好ましくは点突然変異、欠失、挿入である。 Aspects of the mutation of the chondroitin synthase gene are preferably point mutation, deletion, insertion, inversion, duplication, translocation, more preferably point mutation, deletion, insertion, inversion, translocation, and still more preferably. Are point mutations, deletions, insertions, translocations, most preferably point mutations, deletions, insertions.
また、本発明によりK3、K11及びβ4Gal-T7が骨パジェット病に関連していることが明かとなったので、実験動物において、これらの遺伝子の発現を一部又は完全に抑制することによって骨パジェット病の病態を示すノックアウト動物を調製することも可能である。ノックアウト動物としては、例えば、マウス、ラット、ウサギ、イヌ、ネコ、サルなどの哺乳動物が好ましく、ノックアウト動物調製の手法がある程度確立していることから、マウス又はラットが最も好ましいが、これに限定はされない。 In addition, the present invention has revealed that K3, K11 and β4Gal-T7 are related to bone Paget's disease. It is also possible to prepare knockout animals that exhibit the pathology of the disease. As the knockout animal, for example, mammals such as mice, rats, rabbits, dogs, cats, and monkeys are preferable, and mice or rats are most preferable since knockout animal preparation techniques have been established to some extent. Is not done.
例えば骨パジェット病の病態を示すノックアウトマウス(病態マウス)は例えばジーンターゲティングの最新技術(八木健編集 羊土社)、ジーンターゲティング(野田哲生監訳 メディカル・サイエンス・インターナショナル社)などの記載に従って行うことができる。 For example, knockout mice (pathological mice) showing the pathology of Paget's disease of bone can be performed according to the description of, for example, the latest technology of gene targeting (Ken Yagi edited by Yodosha) and gene targeting (translated by Tetsuo Noda, Medical Science International). it can.
例えば、ノックアウトしたいマウスの遺伝子(K3(mK3:配列番号65)、K11(mK11:配列番号67)又はβ4Gal-T7(mβ4Gal-T7:配列番号69))の活性化ドメインを含むexon(mK3の場合にはORF部分の3番目のexon(1560 bp)を含む断片、mK11の場合にはORF全長に相当する4598bpを含む断片、mβ4Gal-T7の場合にはORFの2から6番目のexonを含む断片)を中心とした染色体断片(約10kb)を挿入した直鎖状ターゲティングベクター80μgをES細胞(E14/129Svマウス由来)にエレクトロポレーション法などの公知の方法により導入し、G418耐性のコロニーを選択し、このG418耐性コロニーを24ウェルプレートに移して培養を行うことができる。細胞の一部を凍結保存した後、残りのES細胞からDNAを抽出し、公知の塩基配列解析方法により組換が起こっているクローンを120コロニー程度選択する。さらに、サザンブロッティング法などの方法を用いて組換が予定通り起こっている確認を行い、最終的に組換体を10クローン程度選択し、そのうちの2クローン程度のES細胞をC57BL/6マウスの胚盤胞内に注入する。このようにしてES細胞を注入したマウス胚を仮親マウスの子宮内へ移植してキメラマウスを誕生させることができる。キメラマウスをジャームトランスミッションによりヘテロノックアウトマウスを得ることができる。 For example, exon (in the case of mK3) containing the activation domain of the mouse gene (K3 (mK3: SEQ ID NO: 65), K11 (mK11: SEQ ID NO: 67) or β4Gal-T7 (mβ4Gal-T7: SEQ ID NO: 69)) to be knocked out The fragment containing the third exon (1560 bp) of the ORF portion, the fragment containing 4598 bp corresponding to the full length of the ORF in the case of mK11, and the fragment containing the second to sixth exon of the ORF in the case of mβ4Gal-T7 ) Into the ES cells (derived from E14 / 129Sv mouse) by a known method such as electroporation, and select G418-resistant colonies. Then, the G418-resistant colony can be transferred to a 24-well plate and cultured. After a portion of the cells is cryopreserved, DNA is extracted from the remaining ES cells, and about 120 colonies in which recombination has occurred are selected by a known nucleotide sequence analysis method. Furthermore, it was confirmed that the recombination had occurred as planned using a method such as Southern blotting, and finally about 10 recombinants were selected, and about 2 clones of the ES cells were transferred to C57BL / 6 mouse embryos. Inject into the blastocyst. In this way, the mouse embryo into which the ES cells have been injected can be transplanted into the uterus of a foster parent mouse to generate a chimeric mouse. Hetero knockout mice can be obtained from chimeric mice by germ transmission.
また、small interfering RNA法(T.R. Brummelkamp et al., Science, 296, 550-553 (2002))などの「遺伝子発現を抑制する方法」でもノックアウトマウスを作製することができる。 Knockout mice can also be prepared by a “method of suppressing gene expression” such as the small interfering RNA method (T.R. Brummelkamp et al., Science, 296, 550-553 (2002)).
より具体的には、後述する実施例3に記載されているように、ノックアウトマウスは、コンドロイチン合成酵素遺伝子をES細胞に導入し、目的とする相同組換えを起こしたクローンを用いて生殖細胞系列に入るマウス系列を樹立することにより作製することができる。 More specifically, as described in Example 3 below, a knockout mouse was prepared by introducing a chondroitin synthase gene into an ES cell, and using a clone in which the desired homologous recombination had occurred to obtain a germ line. Can be produced by establishing a mouse line.
以下、実施例により本発明をより具体的に説明する。
参考例1:コンドロイチン硫酸合成酵素(K3)の調製
(1)cDNAのクローニングと発現ベクターの構築
β1,4ガラクトース転移酵素(β4Gal-T)のアミノ酸配列(GenBank accession No.D29805がコードするアミノ酸配列)をクエリーとして、BLAST検索を行った。その結果、Expression Sequence Tag(EST:GenBank accession No. AC0004219) が見つかった。しかし、この配列は不完全であったため、ゲノムデータベースから、GenScan(米国スタンフォード大学)によりORFを調べた。その結果、配列番号1記載の塩基配列(コードされるアミノ酸配列は配列番号2)を発見した。配列番号1記載の塩基配列からなる遺伝子は、少なくともヒト脳で発現していることをMarathon-Ready cDNA(クロンテック社製)を鋳型としたRT-PCR法によって確認した(PCR用のプライマーとしては配列番号9及び配列番号10、並びに配列番号11及び配列番号12の5'プライマーと3'プライマーとの組み合わせを使用した)。この遺伝子の膜貫通領域を含む領域(配列番号2のアミノ酸番号1乃至129からなる領域)を除く可溶性領域をクローニングするため、配列番号7及び配列番号8の2種のプライマーを用いて常法に従ってPCRを行った。使用した鋳型cDNAはMarathon-Ready cDNA human brain(クロンテック社製)を使用した。増幅された約2.3kbのバンドを常法に従ってHindIIIとXbaIとで消化し、ほ乳類細胞用の発現ベクターpFLAG-CMV-1(シグマ社製)のHindIIIとXbaI部位に常法に従って挿入して発現ベクター(K3-FLAG-CMV1)を得た。得られた発現ベクターの塩基配列を確認したところ、配列番号1記載の塩基配列の塩基番号388乃至2649の塩基配列からなるDNA断片が挿入されていることを確認した。この塩基配列を有するDNAのゲノム上の位置を、OMIMを使用して確認したところ、5q31.1に存在することが明かとなった。
(2)K3の調製
K3-FLAG-CMV1 15μgをTransFast(プロメガ社製)を用い、プロトコールに従って、100 mm培養皿に70%コンフルエントになるように培養したCOS7細胞に遺伝子を導入した。3日間培養した上清を回収し、0.22μmのフィルターで濾過後、その上清10mlにAnti-FLAG M2-Agarose Affinity Gel (シグマ社製)100μlを加え、4℃で一晩、転倒混和した。反応後、ゲルを50mM Tris-HCl、pH7.4/20%グリセロールで3回洗浄後、27Gの注射針をつけたシリンジを用い余分な洗浄液を除いた。このゲルを50mmol/L Tris-HCl、pH7.4(20%グリセロール、10mmol/L フェニルメチルスルホニルフルオライド、1μg/ml leupeptin、1μg/ml pepstatin)に50%(v/v)となるように懸濁し、これを遠心分離した後に上清を取り除いて酵素吸着ゲル懸濁液とした。
参考例2
K3を用いたコンドロイチン骨格の伸長
(1)コンドロイチン/コンドロイチン硫酸奇数糖の調製
コンドロイチン(サメ軟骨由来コンドロイチン硫酸を化学的に脱硫酸化したもの:生化学工業株式会社製)及びコンドロイチン硫酸(サメ軟骨由来:生化学工業株式会社製:コンドロイチン硫酸Cとも呼ばれている)をウシ睾丸ヒアルロニダーゼ(シグマ社製)で限定消化後、反応液を10分間100℃で保ち、酵素を加熱失活させた。この反応液をSuperdex 30カラム(60 x 1.6cm: アマシャムバイオサイエンス株式会社製、クロマトグラフィー条件;移動相:0.2mol/L NH4HCO3、流速:2ml/分)にかけ、溶出液を225nmの吸光度でモニターしながら2ml毎に分画し、10糖相当画分をプールした。画分をPD10カラム(アマシャムバイオサイエンス株式会社製)により脱塩後、常法に従ってカルバゾール硫酸法によりウロン酸定量を行い、凍結乾燥した。凍結乾燥物を1mMとなるように蒸留水に溶解し、偶数オリゴ糖サンプルとした(コンドロイチン由来の10糖を「CH10」、コンドロイチン硫酸由来の10糖を「CS10」と記載する)。
Hereinafter, the present invention will be described more specifically with reference to examples.
Reference Example 1: Preparation of chondroitin sulfate synthase (K3) (1) Cloning of cDNA and construction of expression vector Amino acid sequence of β1,4 galactose transferase (β4Gal-T) (amino acid sequence encoded by GenBank accession No. D29805) Was used as a query to perform a BLAST search. As a result, Expression Sequence Tag (EST: GenBank accession No. AC0004219) was found. However, since this sequence was incomplete, the ORF was examined from the genome database by GenScan (Stanford University, USA). As a result, the nucleotide sequence described in SEQ ID NO: 1 (the encoded amino acid sequence is SEQ ID NO: 2) was discovered. The gene consisting of the nucleotide sequence shown in SEQ ID NO: 1 was confirmed to be expressed in at least human brain by RT-PCR using Marathon-Ready cDNA (Clontech) as a template. No. 9 and SEQ ID No. 10, and combinations of 5 ′ and 3 ′ primers of SEQ ID Nos. 11 and 12 were used). In order to clone a soluble region excluding a region containing a transmembrane region of this gene (a region consisting of amino acid numbers 1 to 129 of SEQ ID NO: 2), two primers of SEQ ID NO: 7 and SEQ ID NO: 8 are used in accordance with a conventional method. PCR was performed. As the template cDNA used, Marathon-Ready cDNA human brain (Clontech) was used. The amplified band of about 2.3 kb is digested with HindIII and XbaI according to a conventional method, and inserted into a HindIII and XbaI site of a mammalian cell expression vector pFLAG-CMV-1 (manufactured by Sigma) according to a conventional method. (K3-FLAG-CMV1) was obtained. When the base sequence of the obtained expression vector was confirmed, it was confirmed that a DNA fragment consisting of the base sequence of base numbers 388 to 2649 of the base sequence described in SEQ ID NO: 1 was inserted. When the position of the DNA having this nucleotide sequence on the genome was confirmed using OMIM, it was revealed that the DNA was present at 5q31.1.
(2) Preparation of K3
15 μg of K3-FLAG-CMV1 was transfected into COS7 cells cultured in a 100-mm culture dish so as to be 70% confluent using TransFast (promega) according to the protocol. The supernatant cultured for 3 days was collected, filtered through a 0.22 μm filter, and 10 μl of the supernatant was added with 100 μl of Anti-FLAG M2-Agarose Affinity Gel (manufactured by Sigma) and mixed by inversion at 4 ° C. overnight. After the reaction, the gel was washed three times with 50 mM Tris-HCl, pH 7.4 / 20% glycerol, and an excess washing solution was removed using a syringe fitted with a 27G injection needle. This gel was suspended in 50 mmol / L Tris-HCl, pH 7.4 (20% glycerol, 10 mmol / L phenylmethylsulfonyl fluoride, 1 μg / ml leupeptin, 1 μg / ml pepstatin) so as to be 50% (v / v). The suspension was turbid, and after centrifugation, the supernatant was removed to obtain an enzyme-adsorbed gel suspension.
Reference Example 2
Elongation of chondroitin skeleton using K3 (1) Preparation of chondroitin / chondroitin sulfate odd-numbered sugar Chondroitin (chemically desulfated chondroitin sulfate derived from shark cartilage: manufactured by Seikagaku Corporation) and chondroitin sulfate (derived from shark cartilage: After limited digestion of bovine testicular hyaluronidase (manufactured by Seikagaku Corporation; also known as chondroitin sulfate C), the reaction solution was kept at 100 ° C. for 10 minutes to inactivate the enzyme by heating. The reaction solution is applied to a Superdex 30 column (60 × 1.6 cm, manufactured by Amersham Bioscience, chromatography conditions; mobile phase: 0.2 mol / L NH 4 HCO 3 , flow rate: 2 ml / min), and the eluate is subjected to absorbance at 225 nm. While monitoring with, fractionation was performed every 2 ml, and fractions corresponding to 10 sugars were pooled. The fraction was desalted with a PD10 column (manufactured by Amersham Bioscience), and uronic acid was quantified by a carbazole sulfate method according to a conventional method, followed by freeze-drying. The lyophilized product was dissolved in distilled water so as to have a concentration of 1 mM, and used as an even-numbered oligosaccharide sample (a decasaccharide derived from chondroitin was described as “CH10”, and a decasaccharide derived from chondroitin sulfate was described as “CS10”).
10nmol/LのMnCl2、171μmol/LのATPナトリウム塩を含む50mmol/L MES緩衝液(pH6.5)に酵素吸着ゲル懸濁液10μl、被検物質(コンドロイチン(CHEL)、コンドロイチン硫酸(CSEL)、CH10又はCS10)を1nmol、[3H]UDP-GalNAcを0.036nmol添加して全量を30μlとした。酵素反応は37℃で1時間行い、その後反応液を100℃で1分間保って酵素を失活させて反応を停止させた。 10 μl of enzyme-adsorbed gel suspension in 50 mmol / L MES buffer (pH 6.5) containing 10 nmol / L MnCl 2 and 171 μmol / L ATP sodium salt, test substances (chondroitin (CHEL), chondroitin sulfate (CSEL)) , CH10 or CS10) and 0.036 nmol of [ 3 H] UDP-GalNAc to make a total volume of 30 μl. The enzyme reaction was performed at 37 ° C. for 1 hour, and then the reaction solution was kept at 100 ° C. for 1 minute to inactivate the enzyme and stop the reaction.
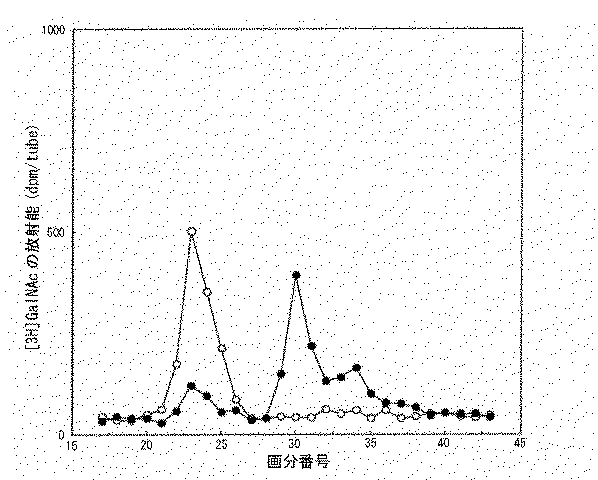
各々の反応液を孔径0.22μmのマイクロフィルター(ミリポア社製)で濾過した後、Superdex peptideカラム(30 x 1.0cm:アマシャムバイオサイエンス株式会社製、クロマトグラフィー条件;移動相:0.2mol/L NaCl、流速1.0ml/分)で分離し、溶出液を0.5mlの画分毎に分取して、シンチレーションカウンターで放射能を測定した(図1)。その結果、強いGalNAc転移活性がCHEL(17乃至18画分)、CH10(23画分)及びCS10(23画分)をGalNAc受容体基質とした場合に観察され、CSELに対してはGalNAc転移活性は観察されなかった(16画分)。CH10及びCS10から得られた反応生成物の23画分は11糖が溶出する分子量を示す画分だった。CH10から得られた11糖を「CH11(K3)」、CS10から得られた11糖を「CS11(K3)」と記載する。 After filtering each reaction solution with a micro filter (manufactured by Millipore) having a pore size of 0.22 μm, a Superdex peptide column (30 × 1.0 cm: manufactured by Amersham Biosciences Inc., chromatography conditions; mobile phase: 0.2 mol / L NaCl, (The flow rate was 1.0 ml / min), and the eluate was collected for each 0.5 ml fraction, and the radioactivity was measured with a scintillation counter (FIG. 1). As a result, strong GalNAc transfer activity was observed when CHEL (fractions 17 to 18), CH10 (fraction 23) and CS10 (fraction 23) were used as the GalNAc receptor substrate, and GalNAc transfer activity against CSEL was observed. Was not observed (16 fractions). 23 fractions of the reaction product obtained from CH10 and CS10 were fractions showing the molecular weight at which 11 sugars eluted. The 11 saccharide obtained from CH10 is referred to as “CH11 (K3)”, and the 11 saccharide obtained from CS10 is referred to as “CS11 (K3)”.
CS11(K3)の21〜25画分を回収してプールし、PD10カラムにより脱塩した。このようにして得られたサンプルを二等分して凍結乾燥した。二分した一方を30mMの酢酸ナトリウムを含む0.1mol/LのTrisHCl緩衝液(pH7.4)100μlに溶解し(CS11(K3)A)、他方をコンドロイチナーゼACIIで消化した(100mUのコンドロイチナーゼACII(生化学工業株式会社製)を100μlのCS11(K3)画分に溶解し、37℃で10時間酵素消化し、加熱して酵素を失活させた:CS11(K3)B)。 Fractions 21-25 of CS11 (K3) were collected, pooled and desalted on a PD10 column. The sample thus obtained was bisected and freeze-dried. One half was dissolved in 100 μl of 0.1 mol / L TrisHCl buffer (pH 7.4) containing 30 mM sodium acetate (CS11 (K3) A), and the other was digested with chondroitinase ACII (100 mU chondroitinase). ACII (manufactured by Seikagaku Corporation) was dissolved in 100 μl of the CS11 (K3) fraction, digested with enzyme at 37 ° C. for 10 hours, and heated to inactivate the enzyme: CS11 (K3) B).
CS11(K3)AとCS11(K3)Bとを孔径0.22μmのマイクロフィルター(ミリポア社製)で濾過した後、Superdex peptideカラム(30 x 10mm:アマシャムバイオサイエンス株式会社製、クロマトグラフィー条件;移動相:0.2mol/L NaCl、流速0.5ml/分)で分離し、溶出液を0.5mlの画分毎に分取して、シンチレーションカウンターで放射能を測定したところ、CS11(K3)Bにおいて単糖画分に放射能ピークがシフトした(図2)。この結果から、K3はコンドロイチン硫酸由来の10糖の非還元末端のGlcUAに対してGalNAcをβ1,4結合で転移し、11糖を調製することができることが明かとなった。
(2)コンドロイチン/コンドロイチン硫酸偶数糖の調製
コンドロイチン(サメ軟骨由来コンドロイチン硫酸を化学的に脱硫酸化:生化学工業株式会社製)及びコンドロイチン硫酸(サメ軟骨由来:生化学工業株式会社製:コンドロイチン硫酸Cとも呼ばれている)をウシ睾丸ヒアルロニダーゼ(シグマ社製)で限定消化後、反応液を10分間100℃で保ち、酵素を加熱失活させた。この反応液を10,000 x gで10分間遠心処理し、上清を回収して更にウシ肝臓由来βグルクロニダーゼ(シグマ社製)で消化した。酵素反応は反応液を10分間100℃で保って停止させた。この反応液をSuperdex 30カラム(60 x 1.6cm: アマシャムバイオサイエンス株式会社製、クロマトグラフィー条件;移動相:0.2mol/L NH4HCO3、流速:2ml/分)にかけ溶出液を225nmの吸光度でモニターしながら、2ml毎に分画し、11糖相当画分をプールした。各画分をPD10カラム(アマシャムバイオサイエンス株式会社製)により脱塩後、常法に従ってカルバゾール硫酸法によりウロン酸定量を行い、凍結乾燥した。凍結乾燥物を1mmol/Lとなるように蒸留水に溶解し、奇数オリゴ糖サンプルとした(コンドロイチン由来の11糖:「CH11」、コンドロイチン硫酸由来の11糖:「CS11」)。
After CS11 (K3) A and CS11 (K3) B were filtered through a 0.22 μm pore size microfilter (manufactured by Millipore), a Superdex peptide column (30 × 10 mm: manufactured by Amersham Biosciences, chromatography conditions; mobile phase) : 0.2 mol / L NaCl, flow rate 0.5 ml / min), and the eluate was collected for each 0.5 ml fraction, and the radioactivity was measured with a scintillation counter. As a result, the monosaccharide was detected in CS11 (K3) B. The radioactivity peak shifted to the fraction (FIG. 2). From these results, it was revealed that K3 can transfer GalNAc to GlcUA at the non-reducing terminal of chondroitin sulfate-derived decasaccharide by β1,4 bond to prepare 11-sugar.
(2) Preparation of chondroitin / chondroitin sulfate even sugar Chondroitin (chemically desulfating chondroitin sulfate derived from shark cartilage: manufactured by Seikagaku Corporation) and chondroitin sulfate (derived from shark cartilage: manufactured by Seikagaku Corporation: chondroitin sulfate C) Was digested with bovine testicular hyaluronidase (manufactured by Sigma), and the reaction solution was kept at 100 ° C. for 10 minutes to inactivate the enzyme. The reaction solution was centrifuged at 10,000 × g for 10 minutes, and the supernatant was recovered and further digested with bovine liver-derived β-glucuronidase (manufactured by Sigma). The enzyme reaction was stopped by keeping the reaction solution at 100 ° C. for 10 minutes. This reaction solution is applied to a Superdex 30 column (60 × 1.6 cm, manufactured by Amersham Biosciences, chromatography conditions; mobile phase: 0.2 mol / L NH 4 HCO 3 , flow rate: 2 ml / min), and the eluate is measured at an absorbance of 225 nm. While monitoring, fractionation was performed every 2 ml, and fractions corresponding to 11 sugars were pooled. Each fraction was desalted using a PD10 column (manufactured by Amersham Bioscience), and uronic acid was quantified by a carbazole sulfate method according to a conventional method, followed by freeze-drying. The lyophilized product was dissolved in distilled water so as to have a concentration of 1 mmol / L, and used as an odd-numbered oligosaccharide sample (11-saccharide derived from chondroitin: “CH11”, 11-saccharide derived from chondroitin sulfate: “CS11”).
またコンドロイチン(サメ軟骨由来コンドロイチン硫酸を化学的に脱硫酸化:生化学工業株式会社製)及びコンドロイチン硫酸(サメ軟骨由来:生化学工業株式社製:コンドロイチン硫酸Cとも呼ばれている)をウシ肝臓由来βグルクロニダーゼ(シグマ社製)で消化してサンプルとした(各々「CHOL」及び「CSOL」と記載する)。 Also, chondroitin (chemically desulfating chondroitin sulfate derived from shark cartilage: manufactured by Seikagaku Corporation) and chondroitin sulfate (derived from shark cartilage: manufactured by Seikagaku Corporation: also called chondroitin sulfate C) are derived from bovine liver. Samples were digested with β-glucuronidase (manufactured by Sigma) (described as “CHOL” and “CSOL”, respectively).
10mmol/LのMnCl2、50mmol/L 酢酸緩衝液(pH5.6)に酵素吸着ゲル懸濁液10μl、被検物質(CHOL、CSOL、CH11又はCS11)を1nmol、[14C]UDP-GlcUAを0.432nmol添加して全量を30μlとした。酵素反応は37℃で1時間行い、その後反応液を100℃で1分間保って酵素を失活させて反応を停止させた。
10 μl of the enzyme-adsorbed gel suspension in 10 mmol / L MnCl 2 , 50 mmol / L acetate buffer (pH 5.6), 1 nmol of the test substance (CHOL, CSOL, CH11 or CS11), and [ 14 C] UDP-GlcUA 0.432 nmol was added to make the
各々の反応液を孔径0.22μmのマイクロフィルター(ミリポア社製)で濾過した後、Superdex peptideカラム(30 x 1.0cm:アマシャムバイオサイエンス株式会社製、クロマトグラフィー条件;移動相:0.2mol/L NaCl、流速0.5ml/分)で分離し、溶出液を0.5mlの画分毎に分取して、シンチレーションカウンターで放射能を測定した(図3)。その結果、強いGlcUA転移活性がCHOL(17乃至18画分)、CH11(23画分)及びCS11(23画分)をGlcUA受容体基質とした場合に観察され、CSOLに対してはGlcUA転移活性が観察されなかった(16画分)。CH11及びCS11から得られた反応生成物の22〜23画分は12糖が溶出する分子量を示す画分だった。CH11から得られた12糖を「CH12(K3)」、CS11から得られた12糖を「CS12(K3)」と記載する。 After filtering each reaction solution with a micro filter (manufactured by Millipore) having a pore size of 0.22 μm, a Superdex peptide column (30 × 1.0 cm: manufactured by Amersham Biosciences Inc., chromatography conditions; mobile phase: 0.2 mol / L NaCl, The eluate was collected for each 0.5 ml fraction, and the radioactivity was measured with a scintillation counter (FIG. 3). As a result, strong GlcUA transfer activity was observed when CHOL (fractions 17 to 18), CH11 (fraction 23) and CS11 (fraction 23) were used as GlcUA receptor substrates, and GlcUA transfer activity against CSOL was observed. Was not observed (16 fractions). The 22 to 23 fractions of the reaction product obtained from CH11 and CS11 were fractions showing the molecular weight at which 12 sugars eluted. The dodecasaccharide obtained from CH11 is referred to as “CH12 (K3)”, and the dodecasaccharide obtained from CS11 is referred to as “CS12 (K3)”.
CS12(K3)の21乃至25画分を回収してプールし、PD10カラムにより脱塩した。このようにして得られたサンプルを二等分して凍結乾燥した。二分した一方を30mmol/Lの酢酸ナトリウムを含む0.1mol/LのTrisHCl緩衝液(pH7.4)100μlに溶解し(CS12(K3)A)、他方をコンドロイチナーゼACIIで消化した(100mユニットのコンドロイチナーゼACII(生化学工業株式会社製)を100μlのCS11(K3)画分に溶解し、37℃で10時間酵素消化し、加熱して酵素を失活させた:CS12(K3)B)。 Fractions 21 to 25 of CS12 (K3) were collected, pooled, and desalted on a PD10 column. The sample thus obtained was bisected and freeze-dried. One half was dissolved in 100 μl of 0.1 mol / L TrisHCl buffer (pH 7.4) containing 30 mmol / L sodium acetate (CS12 (K3) A), and the other was digested with chondroitinase ACII (100 m units). Chondroitinase ACII (manufactured by Seikagaku Corporation) was dissolved in 100 μl of the CS11 (K3) fraction, digested with enzyme at 37 ° C. for 10 hours, and heated to inactivate the enzyme: CS12 (K3) B). .
CS12(K3)AとCS12(K3)Bとを孔径0.22μmのマイクロフィルター(ミリポア社製)で濾過した後、Superdex peptideカラム(30 x 1.0cm:アマシャムバイオサイエンス株式会社製、クロマトグラフィー条件;移動相:0.2mol/L NaCl、流速0.5ml/分)で分離し、溶出液を0.5mlの画分毎に分取して、シンチレーションカウンターで放射能を測定したところ、CS12(K3)Bにおいて二糖画分に放射能ピークがシフトした(図4)。この結果から、K3はコンドロイチン硫酸由来の11糖に対してGlcUAをβ1,3結合で転移し、12糖を調製することができることが明かとなった。
参考例3
コンドロイチン硫酸合成酵素(K11)の調製
(1)cDNAのクローニングと発現ベクターの構築
コンドロイチン硫酸グルクロン酸転移酵素(CSGlcA-T)のアミノ酸配列(GenBank accession No.AB037823がコードするアミノ酸配列)をクエリーとして、BLAST検索を行った。その結果、EST (GenBank accession No. NM_018590) が見つかった。しかし、この配列は不完全であったため、ゲノムデータベースから、GenScan(米国スタンフォード大学)によりORFを調べた。その結果、配列番号3記載の塩基配列(コードされるアミノ酸配列は配列番号4)を発見した。配列番号3記載の塩基配列からなる遺伝子は、少なくともヒト脳で発現していることをMarathon-Ready cDNA(クロンテック社製)を鋳型としたRT-PCR法によって確認した。この遺伝子の膜貫通領域を含む領域(配列番号4のアミノ酸番号1乃至96からなる領域)を除く可溶性領域をクローニングするため、配列番号13及び配列番号14の2種のプライマーを用いて常法に従ってPCRを行った。使用した鋳型cDNAはMarathon-Ready cDNA human brain(クロンテック社製)を使用した。増幅された約2kbのバンドを常法に従ってEcoRIとBamHIで消化し、ほ乳類細胞用の発現ベクターpFLAG-CMV-1(シグマ社製)のEcoRIとBamHI部位に常法に従って挿入してK11-FLAG-CMV1を得た。得られたベクターの塩基配列を確認したところ、配列番号3記載の塩基配列の塩基番号287乃至2328の塩基配列からなるDNA断片が挿入されていることを確認した。この塩基配列を有するDNAのゲノム上の位置を、OMIMを使用して確認したところ、2q36.3に存在することが明かとなった。
(2)K11の調製
K11-FLAG-CMV1 15mgをTransFast(プロメガ社製)を用い、プロトコールに従って100 mm培養皿に70%コンフルエントになるように培養したCOS7細胞に遺伝子を導入した。3日間培養した上清を回収し、0.22μmのフィルターで濾過後、その上清10mlにAnti-FLAG M2-Agarose Affinity Gel (シグマ社製)100μlを加え、4℃で一晩、転倒混和した。反応後、ゲルを50mmol/L Tris-HCl、pH7.4(20%グリセロール)3回洗浄後、27Gの注射針をつけたシリンジを用い余分な洗浄液を除いた。このゲルを50mmol/L pH7.4のTrisHCl緩衝液、(20%グリセロール、10mmol/L フェニルメチルスルホニルフルオライド、1μg/ml leupeptin、1μg/ml pepstatin)に50%(v/v)となるように懸濁し、これを遠心分離した後に上清を取り除いて酵素 吸着ゲル懸濁液とした。
参考例4
K11を用いたコンドロイチン骨格の伸長
(1)コンドロイチン/コンドロイチン硫酸奇数糖の調製
10nmol/LのMnCl2、171μmol/LのATPナトリウム塩を含む50mmol/L MES緩衝液(pH6.5)に酵素吸着ゲル懸濁液10μl、被検物質(CHEL、CSEL、CH10又はCS10)を1nmol、[3H]UDP-GalNAcを0.036nmol添加して全量を30μlとした。酵素反応は37℃で1時間行い、その後反応液を100℃で1分間保って酵素を失活させて反応を停止させた。
After filtering CS12 (K3) A and CS12 (K3) B through a micro filter (manufactured by Millipore) having a pore size of 0.22 μm, a Superdex peptide column (30 × 1.0 cm: manufactured by Amersham Biosciences, chromatography conditions; migration) Phase: 0.2 mol / L NaCl, flow rate 0.5 ml / min). The eluate was fractionated into 0.5 ml fractions, and the radioactivity was measured with a scintillation counter. The radioactivity peak shifted to the sugar fraction (FIG. 4). From these results, it was revealed that K3 can transfer GlcUA to 11 sugars derived from chondroitin sulfate by β1,3 bond to prepare dodecasaccharide.
Reference Example 3
Preparation of chondroitin sulfate synthase (K11)
(1) Cloning of cDNA and Construction of Expression Vector A BLAST search was performed using the amino acid sequence of chondroitin sulfate glucuronyltransferase (CSGlcA-T) (the amino acid sequence encoded by GenBank accession No. AB037823) as a query. As a result, EST (GenBank accession No. NM_018590) was found. However, since this sequence was incomplete, the ORF was examined from the genome database by GenScan (Stanford University, USA). As a result, the nucleotide sequence described in SEQ ID NO: 3 (the encoded amino acid sequence was SEQ ID NO: 4) was discovered. The gene consisting of the nucleotide sequence of SEQ ID NO: 3 was confirmed to be expressed in at least human brain by RT-PCR using Marathon-Ready cDNA (Clontech) as a template. In order to clone a soluble region excluding a region containing a transmembrane region of this gene (a region consisting of amino acids 1 to 96 of SEQ ID NO: 4), two types of primers of SEQ ID NO: 13 and SEQ ID NO: 14 are used in accordance with a conventional method. PCR was performed. As the template cDNA used, Marathon-Ready cDNA human brain (Clontech) was used. The amplified band of about 2 kb was digested with EcoRI and BamHI according to a conventional method, and inserted into the EcoRI and BamHI sites of an expression vector for mammalian cells pFLAG-CMV-1 (manufactured by Sigma) according to a conventional method to obtain K11-FLAG-. CMV1 was obtained. When the base sequence of the obtained vector was confirmed, it was confirmed that a DNA fragment consisting of the base sequence of base numbers 287 to 2328 of the base sequence described in SEQ ID NO: 3 was inserted. The position of the DNA having this nucleotide sequence on the genome was confirmed using OMIM, and it was revealed that the DNA was present at 2q36.3.
(2) Preparation of K11
Using TransFast (promega), 15 mg of K11-FLAG-CMV1 was used to introduce the gene into COS7 cells cultured in a 100 mm culture dish so as to be 70% confluent according to the protocol. The supernatant cultured for 3 days was collected and filtered through a 0.22 μm filter, and 100 μl of Anti-FLAG M2-Agarose Affinity Gel (manufactured by Sigma) was added to 10 ml of the supernatant, and the mixture was inverted and mixed at 4 ° C. overnight. After the reaction, the gel was washed three times with 50 mmol / L Tris-HCl, pH 7.4 (20% glycerol), and excess washing solution was removed using a syringe fitted with a 27G injection needle. This gel was adjusted to 50% (v / v) in 50 mmol / L TrisHCl buffer, pH 7.4, (20% glycerol, 10 mmol / L phenylmethylsulfonyl fluoride, 1 μg / ml leupeptin, 1 μg / ml pepstatin). After suspending and centrifuging the suspension, the supernatant was removed to obtain an enzyme-adsorbed gel suspension.
Reference example 4
Extension of chondroitin skeleton using K11
(1) Preparation of chondroitin / chondroitin sulfate odd-numbered sugar
10 μl of enzyme-adsorbed gel suspension in 50 mmol / L MES buffer (pH 6.5) containing 10 nmol / L MnCl 2 and 171 μmol / L ATP sodium salt, 1 nmol of test substance (CHEL, CSEL, CH10 or CS10) Then, 0.036 nmol of [ 3 H] UDP-GalNAc was added to make the
各々の反応液を孔径0.22μmのマイクロフィルター(ミリポア社製)で濾過した後、Superdex peptideカラム(30 x 1.0cm:アマシャムバイオサイエンス株式会社製、クロマトグラフィー条件;移動相:0.2mol/L NaCl、流速0.5ml/分)で分離し、溶出液を0.5mlの画分毎に分取して、シンチレーションカウンターで放射能を測定した(図5)。その結果、強いGalNAc転移活性がCHEL(18画分)、CH10(23画分)及びCS10(23画分)をGalNAc受容体基質とした場合に観察され、CSELに対しては弱いGalNAc転移活性が観察された(16画分)。CH10及びCS10から得られた反応生成物の22〜23画分は11糖が溶出する分子量を示す画分だった。CH10から得られた11糖を「CH11(K11)」、CS10から得られた11糖を「CS11(K11)」と記載する。 After filtering each reaction solution with a micro filter (manufactured by Millipore) having a pore size of 0.22 μm, a Superdex peptide column (30 × 1.0 cm: manufactured by Amersham Biosciences Inc., chromatography conditions; mobile phase: 0.2 mol / L NaCl, The eluate was collected for each 0.5 ml fraction, and the radioactivity was measured with a scintillation counter (FIG. 5). As a result, strong GalNAc transfer activity was observed when CHEL (fraction 18), CH10 (fraction 23) and CS10 (fraction 23) were used as GalNAc receptor substrates, and weak GalNAc transfer activity was observed for CSEL. Observed (16 fractions). The 22 to 23 fractions of the reaction product obtained from CH10 and CS10 were fractions showing the molecular weight at which 11 sugars eluted. The 11 saccharide obtained from CH10 is referred to as “CH11 (K11)”, and the 11 saccharide obtained from CS10 is referred to as “CS11 (K11)”.
CS11(K11)の21〜25画分を回収してプールし、PD10カラムにより脱塩した。このようにして得られたサンプルを二等分して凍結乾燥した。二分した一方を30mMの酢酸ナトリウムを含む0.1mol/LのTrisHCl緩衝液(pH7.4)100μlに溶解し(CS11(K11)A)、他方をコンドロイチナーゼACIIで消化した(100mユニットのコンドロイチナーゼACII(生化学工業株式会社製)を100μlのCS11画分に溶解し、37℃で10時間酵素消化し、加熱して酵素を失活させた:CS11(K11)B)。 Fractions 21-25 of CS11 (K11) were collected, pooled and desalted on a PD10 column. The sample thus obtained was bisected and freeze-dried. One half was dissolved in 100 μl of 0.1 mol / L TrisHCl buffer (pH 7.4) containing 30 mM sodium acetate (CS11 (K11) A), and the other was digested with chondroitinase ACII (100 m chondroitin). Nase ACII (manufactured by Seikagaku Corporation) was dissolved in 100 μl of the CS11 fraction, subjected to enzyme digestion at 37 ° C. for 10 hours, and heated to inactivate the enzyme: CS11 (K11) B).
CS11(K11)AとCS11(K11)Bとを孔径0.22μmのマイクロフィルター(ミリポア社製)で濾過した後、Superdex peptideカラム(30 x 10mm:アマシャムバイオサイエンス株式会社製、クロマトグラフィー条件;移動相:0.2mol/L NaCl、流速0.5ml/分)で分離し、溶出液を0.5mlの画分毎に分取して、シンチレーションカウンターで放射能を測定したところ、CS11(K11)Bにおいて三糖画分に放射能ピークがシフトした(図6)。この結果から、K11はコンドロイチン硫酸由来の10糖の非還元末端のGlcUAに対してGalNAcをβ1,4結合で転移し、11糖を調製することができることが推測された。
(2)コンドロイチン/コンドロイチン硫酸偶数糖の調製
10nmol/LのMnCl2、50mmol/L 酢酸緩衝液(pH5.6)に酵素吸着ゲル懸濁液10μl、被検物質(CHOL、CSOL、CH11又はCS11)を1nmol、[14C]UDP-GlcUAを0.432nmol添加して全量を30μlとした。酵素反応は37℃で1時間行い、その後反応液を100℃で1分間保って酵素を失活させて反応を停止させた。
After CS11 (K11) A and CS11 (K11) B were filtered through a microfilter (manufactured by Millipore) having a pore size of 0.22 μm, a Superdex peptide column (30 × 10 mm: manufactured by Amersham Biosciences, chromatography conditions; mobile phase) : 0.2 mol / L NaCl, flow rate 0.5 ml / min). The eluate was fractionated for each 0.5 ml fraction, and the radioactivity was measured with a scintillation counter. The radioactivity peak shifted to the fraction (FIG. 6). These results suggest that K11 can transfer GalNAc to GlcUA at the non-reducing end of chondroitin sulfate-derived decasaccharide by β1,4 bond to prepare the decasaccharide.
(2) Preparation of chondroitin / chondroitin sulfate even sugar
10 nmol / L MnCl 2 , 10 μl of the enzyme-adsorbed gel suspension in 50 mmol / L acetate buffer (pH 5.6), 1 nmol of the test substance (CHOL, CSOL, CH11 or CS11), and [ 14 C] UDP-GlcUA 0.432 nmol was added to make the
各々の反応液を孔径0.22μmのマイクロフィルター(ミリポア社製)で濾過した後、Superdex peptideカラム(30 x 1.0cm:アマシャムバイオサイエンス株式会社製、クロマトグラフィー条件;移動相:0.2mol/L NaCl、流速0.5ml/分)で分離し、溶出液を0.5mlの画分毎に分取して、シンチレーションカウンターで放射能を測定した(図3)。その結果、強いGlcUA転移活性がCHOL(18画分)、CH11(23画分)及びCS11(22画分)をGlcUA受容体基質とした場合に観察され、CSOLに対してはGlcUA転移活性が観察されなかった。CH11及びCS11から得られた反応生成物の22乃至23画分は12糖が溶出する分子量を示す画分だった。CH11から得られた12糖を「CH12(K11)」、CS11から得られた12糖を「CS12(K11)」と記載する。 After filtering each reaction solution with a micro filter (manufactured by Millipore) having a pore size of 0.22 μm, a Superdex peptide column (30 × 1.0 cm: manufactured by Amersham Biosciences Inc., chromatography conditions; mobile phase: 0.2 mol / L NaCl, The eluate was collected for each 0.5 ml fraction, and the radioactivity was measured with a scintillation counter (FIG. 3). As a result, strong GlcUA transfer activity was observed when CHOL (fraction 18), CH11 (fraction 23) and CS11 (fraction 22) were used as GlcUA receptor substrates, and GlcUA transfer activity was observed for CSOL. Was not done. The 22 to 23 fractions of the reaction products obtained from CH11 and CS11 were fractions showing the molecular weight at which 12 sugars eluted. The dodecasaccharide obtained from CH11 is referred to as “CH12 (K11)”, and the dodecasaccharide obtained from CS11 is referred to as “CS12 (K11)”.
CS12(K11)の21乃至25画分を回収してプールし、PD10カラムにより脱塩した。このようにして得られたサンプルを二等分して凍結乾燥した。二分した一方を30mmol/Lの酢酸ナトリウムを含む0.1mol/LのTrisHCl緩衝液(pH7.4)100μlに溶解し(CS12(K11)A)、他方をコンドロイチナーゼACIIで消化した(100mユニットのコンドロイチナーゼACII(生化学工業株式会社製)を100μlのCS11(K11)画分に溶解し、37℃で10時間酵素消化し、加熱して酵素を失活させた:CS12(K11)B)。 Fractions 21 to 25 of CS12 (K11) were collected, pooled, and desalted on a PD10 column. The sample thus obtained was bisected and freeze-dried. One half was dissolved in 100 μl of 0.1 mol / L TrisHCl buffer (pH 7.4) containing 30 mmol / L sodium acetate (CS12 (K11) A), and the other was digested with chondroitinase ACII (100 m units). Chondroitinase ACII (manufactured by Seikagaku Corporation) was dissolved in 100 μl of the CS11 (K11) fraction, digested with enzyme at 37 ° C. for 10 hours, and heated to inactivate the enzyme: CS12 (K11) B). .
CS12(K11)AとCS12(K11)Bとを孔径0.22μmのマイクロフィルター(ミリポア社製)で濾過した後、Superdex peptideカラム(30 x 1.0cm:アマシャムバイオサイエンス株式会社製、クロマトグラフィー条件;移動相:0.2mol/L NaCl、流速0.5ml/分)で分離し、溶出液を0.5mlの画分毎に分取して、シンチレーションカウンターで放射能を測定したところ、CS12(K11)Bにおいて二糖画分に放射能ピークがシフトした(図4)。この結果から、本発明酵素はコンドロイチン硫酸由来の11糖に対してGlcUAをβ1,3結合で転移し、12糖を調製することができることが明かとなった。
参考例5
コンドロイチン硫酸合成酵素(β4Gal-T7)の調製と活性の確認
Almeidaらの方法(J. Biol. Chem.,274, 37, 26165-26171(1999)のEXPERIMENTAL PROCEDURESの記載)に従ってβ4Gal-T7のクローニングを行なった。得られたクローンの塩基配列を常法に従って確認したところ、配列番号5記載の塩基配列からなることが明かとなった。この塩基配列を有するDNAのゲノム上の位置を、OMIMを使用して確認したところ、5q35に存在することが明かとなった。
After filtering CS12 (K11) A and CS12 (K11) B through a micro filter (manufactured by Millipore) having a pore size of 0.22 μm, a Superdex peptide column (30 × 1.0 cm: manufactured by Amersham Biosciences, chromatography conditions; migration) Phase: 0.2 mol / L NaCl, flow rate 0.5 ml / min). The eluate was fractionated into 0.5 ml fractions, and the radioactivity was measured with a scintillation counter. The radioactivity peak shifted to the sugar fraction (FIG. 4). From these results, it was revealed that the enzyme of the present invention can transfer GlcUA to 11 sugars derived from chondroitin sulfate by β1,3 bond to prepare 12 sugars.
Reference example 5
Preparation of chondroitin sulfate synthase (β4Gal-T7) and confirmation of its activity
Β4Gal-T7 was cloned according to the method of Almeida et al. (Described in EXPERIMENTAL PROCEDURES in J. Biol. Chem., 274, 37, 26165-26171 (1999)). When the nucleotide sequence of the obtained clone was confirmed according to a conventional method, it was revealed that the clone consisted of the nucleotide sequence of SEQ ID NO: 5. The location of the DNA having this nucleotide sequence on the genome was confirmed using OMIM, and it was revealed that the DNA was present at 5q35.
更に、Gotohらの方法(J. Biol. Chem.,277, 41, 38189-38196(2002)に従ってβ4Gal-T7の発現を行なってβ4Gal-T7が結合したアフィニティー担体の懸濁液を得た後、ゲル10μl、受容体基質(キシロース結合ペプチド(配列番号15:第9番目のアミノ酸残基であるセリンに側鎖としてキシロースが結合しているビクニンのN-末端配列):ペプチド研究所製)6.25mg、171μmolのアデノシン三リン酸(ATP)ナトリウム塩、0.036molの[3H]UDP-Galを10nmol/LのMnCl2を含む50mmolのMES緩衝液(pH6.5)に加えて全量を30μlとし、37℃で1時間反応を行なった。その後反応液を100℃で1分間保って酵素を失活させて反応を停止させた。
Further, expression of β4Gal-T7 was performed according to the method of Gotoh et al. (J. Biol. Chem., 277, 41, 38189-38196 (2002) to obtain a suspension of an affinity carrier to which β4Gal-T7 was bound.
反応液を孔径0.22μmのマイクロフィルター(ミリポア社製)で濾過した後、Superdex peptideカラム(30 x 1.0cm:アマシャム バイオサイエンス株式会社製、クロマトグラフィー条件;移動相:0.2mol/L NaCl、流速1.0ml/分)で分離し、溶出液を0.5mlの画分毎に分取して、シンチレーションカウンターで放射能を測定した。その結果、[3H]UDP-Galの溶出画分とは別の高分子の画分に強い放射能が観察された。このことから、β4Gal-T7が受容体基質にガラクトースを結合させていることが裏付けられた。 After the reaction solution was filtered through a microfilter (manufactured by Millipore) having a pore size of 0.22 μm, a Superdex peptide column (30 × 1.0 cm; manufactured by Amersham Biosciences, Inc., chromatography conditions; mobile phase: 0.2 mol / L NaCl, flow rate 1.0) The eluate was collected for each 0.5 ml fraction, and the radioactivity was measured with a scintillation counter. As a result, strong radioactivity was observed in a fraction of a polymer different from the fraction eluted with [ 3 H] UDP-Gal. This confirmed that β4Gal-T7 binds galactose to the receptor substrate.
実施例1 血液サンプルからのDNA抽出と塩基配列解析
1mlの血液からGFX Genomic Blood DNA Purification Kit(アマシャム バイオサイエンス社製)を用いてDNAを抽出した。得られる14〜16μgのDNAのうち、250ngを鋳型として、各種プライマー(下記表1参照)によりコンドロイチン硫酸合成酵素(K3、K11、β4Gal-T7)遺伝子のエクソンを増幅した。このようにして得られる断片を鋳型にして、常法により塩基配列を解析し、それを健常な各コンドロイチン合成酵素の遺伝子の塩基配列を対比することで、変異や一塩基多型の有無を容易に調べることができる。
Example 1 DNA extraction from blood sample and nucleotide sequence analysis
DNA was extracted from 1 ml of blood using a GFX Genomic Blood DNA Purification Kit (manufactured by Amersham Bioscience). The exon of the chondroitin sulfate synthase (K3, K11, β4Gal-T7) gene was amplified by various primers (see Table 1 below) using 250 ng of the obtained 14 to 16 μg of DNA as a template. Using the fragment obtained in this way as a template, the nucleotide sequence is analyzed by a conventional method, and the nucleotide sequence of each healthy chondroitin synthase gene is compared with the nucleotide sequence to easily determine the presence or absence of a mutation or single nucleotide polymorphism. You can find out.
実施例2 血液サンプルからのRNA抽出と発現量解析
10mlの血液を3,000rpmで10分間遠心分離し、中間層を分取する。さらに、Lympho Prep(Nycomed社)を用いて遠心分離し中間層を分取する。この操作により末梢血中の単核球(PBMC)9x107細胞を得る。全量のPBMCからRNA Extraction Kit(アマシャム バイオサイエンス社製)を用いて総RNAを調製することができる。総RNA 10ngからSUPERSCRIPT First-Strand Synthesis System for RT-PCR(インビトロジェン社製)により1st strand cDNAを合成した。このcDNAを鋳型にして、real-time PCR法により各遺伝子の発現量を定量することができる。使用するプライマー及びプローブを表2に示す。
Example 2 RNA extraction from blood sample and expression level analysis
10 ml of blood is centrifuged at 3,000 rpm for 10 minutes, and the intermediate layer is separated. Furthermore, centrifugation is performed using Lympho Prep (Nycomed) to separate the intermediate layer. By this operation, 9 × 10 7 mononuclear cells (PBMC) in peripheral blood are obtained. Total RNA can be prepared from the entire amount of PBMC using an RNA Extraction Kit (Amersham Bioscience). A 1st strand cDNA was synthesized from 10 ng of the total RNA by a SUPERSCRIPT First-Strand Synthesis System for RT-PCR (manufactured by Invitrogen). Using this cDNA as a template, the expression level of each gene can be quantified by real-time PCR. The primers and probes used are shown in Table 2.
実施例3 病態モデルマウスの調製
ノックアウトマウスはマウスのK3(mK3:配列番号65)、K11(mK11:配列番号67)あるいはβ4Gal-T7(mβ4Gal-T7:配列番号69)の活性化ドメインを含むexon(mK3の場合にはORF部分の3番目のexon(1560bp)を含む約10kb断片、mK11の場合にはORF全長に相当する4598bpを含む約10 kb断片、mβ4Gal-T7の場合にはORFの2から6番目のexonを含む約10 kb断片)を中心とした染色体断片(約10 kb)を挿入した直鎖状ターゲティングベクター80 μgをES細胞(E14 / 129Svマウス由来)にトランスフェクション(エレクトロポレーション)し、G418耐性のコロニーを選択した。G418耐性コロニーを24ウェルプレートに移し、培養を行った。細胞の一部を凍結保存した後、残りのES細胞からDNAを抽出し、PCRにより組み換えが起こっているクローンを120コロニー程度選択した。さらに、サザンブロッティングにより組換が予定通り起こっていることを確認し、最終的に組換体を10クローン程度選択した。選択したうちの2クローンのES細胞をC57BL/6マウスの胚盤胞内に注入した。ES細胞を注入したマウス胚を仮親マウスの子宮内へ移植してキメラマウスを誕生させた。 その後、ジャームトランスミッションによりヘテロノックアウトマウスを得た。
Example 3 Preparation of Disease Model Mouse Knockout mouse is an exon containing an activation domain of mouse K3 (mK3: SEQ ID NO: 65), K11 (mK11: SEQ ID NO: 67) or β4Gal-T7 (mβ4Gal-T7: SEQ ID NO: 69) (In the case of mK3, an approximately 10 kb fragment containing the third exon (1560 bp) of the ORF portion, in the case of mK11, an approximately 10 kb fragment containing 4598 bp corresponding to the full length of the ORF, and in the case of mβ4Gal-T7, the
本発明は、骨パジェット病の検出及び骨パジェット病の病態動物の産生等に利用できる。 INDUSTRIAL APPLICABILITY The present invention can be used for the detection of Paget's disease of bone and the production of a diseased animal of Paget's disease of bone.
Claims (5)
SEQ ID NO: 2, SEQ ID NO: 4, SEQ ID NO: 6, SEQ ID NO: 66, SEQ ID NO: 68, or SEQ ID NO: 70, or a glycosyltransferase gene comprising an amino acid sequence having homology thereto A knockout animal, the expression of which is partially or completely suppressed.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2003379085A JP2004166702A (en) | 2002-11-07 | 2003-11-07 | Method for detecting Paget's disease of bone |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2002323438 | 2002-11-07 | ||
| JP2003379085A JP2004166702A (en) | 2002-11-07 | 2003-11-07 | Method for detecting Paget's disease of bone |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2004166702A true JP2004166702A (en) | 2004-06-17 |
Family
ID=32716017
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2003379085A Pending JP2004166702A (en) | 2002-11-07 | 2003-11-07 | Method for detecting Paget's disease of bone |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2004166702A (en) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8129148B2 (en) | 2005-08-24 | 2012-03-06 | Seikagaku Corporation | Process for preparation of chondroitin fraction |
-
2003
- 2003-11-07 JP JP2003379085A patent/JP2004166702A/en active Pending
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8129148B2 (en) | 2005-08-24 | 2012-03-06 | Seikagaku Corporation | Process for preparation of chondroitin fraction |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP3131322B2 (en) | Novel α2 → 3 sialyltransferase | |
| AU706747B2 (en) | Antibody specific for beta1->6N- acetylglucosamininyltransferase | |
| JP2002507409A (en) | Glycosyl sulfotransferase-3 | |
| Yamada et al. | Embryonic fibroblasts with a gene trap mutation in Ext1 produce short heparan sulfate chains | |
| US20050042738A1 (en) | Carbohydrate-associated proteins | |
| JP4333880B2 (en) | Chondroitin synthase and DNA encoding the enzyme | |
| JP2003047467A (en) | Chondroitin synthetase | |
| JP4791676B2 (en) | Sulfate transferase and DNA encoding the enzyme | |
| JP3170369B2 (en) | β1,3-galactosyltransferase | |
| Habuchi et al. | Biosynthesis of heparan sulfate and heparin how are the multifunctional glycosaminoglycans built up? | |
| JP2004166702A (en) | Method for detecting Paget's disease of bone | |
| JP4338038B2 (en) | Chondroitin synthase and nucleic acid encoding the enzyme | |
| JP4226693B2 (en) | Sulfate transferase and DNA encoding the same | |
| US20060141463A1 (en) | Method of detecting bone paget's disease | |
| AU718472B2 (en) | DNA sequence coding for a mammalian glucuronyl C5-epimerase and a process for its production | |
| JPWO2002000889A1 (en) | Sulfotransferase and DNA encoding said enzyme | |
| JP4571242B2 (en) | Glycosaminoglycan sulfotransferase polypeptide derived from human and DNA encoding the same | |
| EP0745668A2 (en) | DNA coding for sulfotransferase | |
| JP3969469B2 (en) | N-acetylglucosamine transferase and DNA encoding the same | |
| JP4590434B2 (en) | Sulfate transfer agent containing human glycosaminoglycan sulfotransferase | |
| JP4514708B2 (en) | Identification and utilization of chondroitin polymerization factor | |
| JP4377987B2 (en) | Galactose transferase and DNA encoding the same | |
| EP0845533B1 (en) | Keratan sulfate 6-sulfotransferase and DNA coding for the same | |
| JP4288327B2 (en) | Sulfyltransferase, polypeptide thereof and DNA encoding the same | |
| EP1135472B1 (en) | UDP-N- ACETYL GLUCOSAMINE: GALACTOSE-BETA1, 3-N- ACETYL GALACTOSAMINE-ALPHA-R/ N- ACETYL GLUCOSAMINE -BETA1, 3-N- ACETYL GALACTOSAMINE- ALPHA-R (GlcNAc TO GalNAc) BETA1, 6-N- ACETYL GLUCOSAMINYL TRANSFERASE, C2/4GnT |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20061003 |
|
| A131 | Notification of reasons for refusal |
Effective date: 20090903 Free format text: JAPANESE INTERMEDIATE CODE: A131 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20100104 |