ES2940890T3 - Combinaciones farmacéuticas para el tratamiento del cáncer - Google Patents
Combinaciones farmacéuticas para el tratamiento del cáncer Download PDFInfo
- Publication number
- ES2940890T3 ES2940890T3 ES14859220T ES14859220T ES2940890T3 ES 2940890 T3 ES2940890 T3 ES 2940890T3 ES 14859220 T ES14859220 T ES 14859220T ES 14859220 T ES14859220 T ES 14859220T ES 2940890 T3 ES2940890 T3 ES 2940890T3
- Authority
- ES
- Spain
- Prior art keywords
- cancer
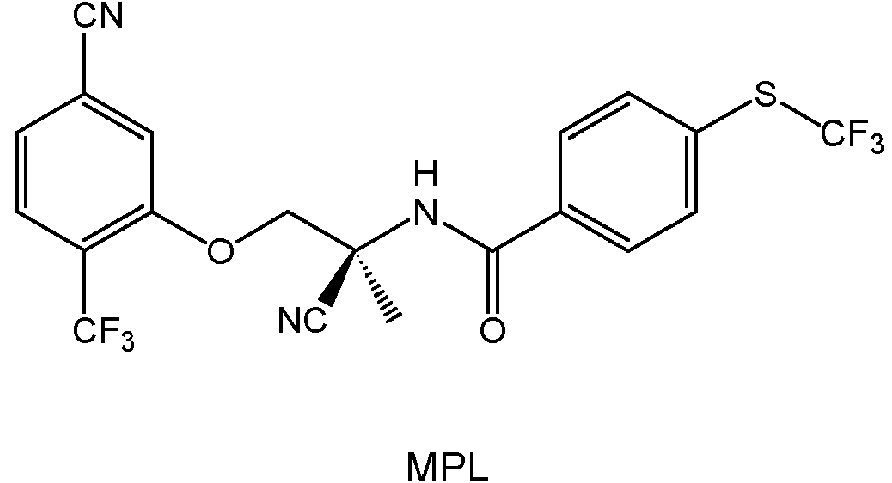
- mpl
- compound
- cells
- doxorubicin
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 238000011282 treatment Methods 0.000 title claims abstract description 84
- 206010028980 Neoplasm Diseases 0.000 title claims abstract description 78
- 201000011510 cancer Diseases 0.000 title claims abstract description 66
- 150000001875 compounds Chemical class 0.000 claims abstract description 113
- 230000001093 anti-cancer Effects 0.000 claims abstract description 78
- 150000008361 aminoacetonitriles Chemical class 0.000 claims abstract description 24
- WTERNLDOAPYGJD-SFHVURJKSA-N monepantel Chemical compound C([C@@](C)(NC(=O)C=1C=CC(SC(F)(F)F)=CC=1)C#N)OC1=CC(C#N)=CC=C1C(F)(F)F WTERNLDOAPYGJD-SFHVURJKSA-N 0.000 claims description 245
- AOJJSUZBOXZQNB-TZSSRYMLSA-N Doxorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(=O)CO)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 AOJJSUZBOXZQNB-TZSSRYMLSA-N 0.000 claims description 143
- 239000003814 drug Substances 0.000 claims description 79
- 229960004679 doxorubicin Drugs 0.000 claims description 71
- 229960005277 gemcitabine Drugs 0.000 claims description 62
- SDUQYLNIPVEERB-QPPQHZFASA-N gemcitabine Chemical compound O=C1N=C(N)C=CN1[C@H]1C(F)(F)[C@H](O)[C@@H](CO)O1 SDUQYLNIPVEERB-QPPQHZFASA-N 0.000 claims description 62
- GHASVSINZRGABV-UHFFFAOYSA-N Fluorouracil Chemical compound FC1=CNC(=O)NC1=O GHASVSINZRGABV-UHFFFAOYSA-N 0.000 claims description 61
- 229960002949 fluorouracil Drugs 0.000 claims description 57
- NKANXQFJJICGDU-QPLCGJKRSA-N Tamoxifen Chemical compound C=1C=CC=CC=1C(/CC)=C(C=1C=CC(OCCN(C)C)=CC=1)/C1=CC=CC=C1 NKANXQFJJICGDU-QPLCGJKRSA-N 0.000 claims description 47
- DYKFCLLONBREIL-KVUCHLLUSA-N minocycline Chemical compound C([C@H]1C2)C3=C(N(C)C)C=CC(O)=C3C(=O)C1=C(O)[C@@]1(O)[C@@H]2[C@H](N(C)C)C(O)=C(C(N)=O)C1=O DYKFCLLONBREIL-KVUCHLLUSA-N 0.000 claims description 46
- 229930012538 Paclitaxel Natural products 0.000 claims description 45
- 229960001592 paclitaxel Drugs 0.000 claims description 45
- RCINICONZNJXQF-MZXODVADSA-N taxol Chemical compound O([C@@H]1[C@@]2(C[C@@H](C(C)=C(C2(C)C)[C@H](C([C@]2(C)[C@@H](O)C[C@H]3OC[C@]3([C@H]21)OC(C)=O)=O)OC(=O)C)OC(=O)[C@H](O)[C@@H](NC(=O)C=1C=CC=CC=1)C=1C=CC=CC=1)O)C(=O)C1=CC=CC=C1 RCINICONZNJXQF-MZXODVADSA-N 0.000 claims description 45
- 230000000694 effects Effects 0.000 claims description 43
- 229960004023 minocycline Drugs 0.000 claims description 34
- 150000003839 salts Chemical class 0.000 claims description 34
- 229960001756 oxaliplatin Drugs 0.000 claims description 32
- DWAFYCQODLXJNR-BNTLRKBRSA-L oxaliplatin Chemical compound O1C(=O)C(=O)O[Pt]11N[C@@H]2CCCC[C@H]2N1 DWAFYCQODLXJNR-BNTLRKBRSA-L 0.000 claims description 32
- 239000012453 solvate Substances 0.000 claims description 29
- IAKHMKGGTNLKSZ-INIZCTEOSA-N (S)-colchicine Chemical compound C1([C@@H](NC(C)=O)CC2)=CC(=O)C(OC)=CC=C1C1=C2C=C(OC)C(OC)=C1OC IAKHMKGGTNLKSZ-INIZCTEOSA-N 0.000 claims description 24
- 229960001603 tamoxifen Drugs 0.000 claims description 24
- 230000001225 therapeutic effect Effects 0.000 claims description 24
- 239000002246 antineoplastic agent Substances 0.000 claims description 20
- 239000008194 pharmaceutical composition Substances 0.000 claims description 17
- 208000005017 glioblastoma Diseases 0.000 claims description 16
- KTUFNOKKBVMGRW-UHFFFAOYSA-N imatinib Chemical compound C1CN(C)CCN1CC1=CC=C(C(=O)NC=2C=C(NC=3N=C(C=CN=3)C=3C=NC=CC=3)C(C)=CC=2)C=C1 KTUFNOKKBVMGRW-UHFFFAOYSA-N 0.000 claims description 16
- 239000005517 L01XE01 - Imatinib Substances 0.000 claims description 15
- 206010033128 Ovarian cancer Diseases 0.000 claims description 14
- 229960002074 flutamide Drugs 0.000 claims description 14
- MKXKFYHWDHIYRV-UHFFFAOYSA-N flutamide Chemical compound CC(C)C(=O)NC1=CC=C([N+]([O-])=O)C(C(F)(F)F)=C1 MKXKFYHWDHIYRV-UHFFFAOYSA-N 0.000 claims description 14
- 229960002411 imatinib Drugs 0.000 claims description 13
- 229960001338 colchicine Drugs 0.000 claims description 12
- 206010027406 Mesothelioma Diseases 0.000 claims description 11
- 206010009944 Colon cancer Diseases 0.000 claims description 10
- 208000001333 Colorectal Neoplasms Diseases 0.000 claims description 10
- AZSNMRSAGSSBNP-UHFFFAOYSA-N 22,23-dihydroavermectin B1a Natural products C1CC(C)C(C(C)CC)OC21OC(CC=C(C)C(OC1OC(C)C(OC3OC(C)C(O)C(OC)C3)C(OC)C1)C(C)C=CC=C1C3(C(C(=O)O4)C=C(C)C(O)C3OC1)O)CC4C2 AZSNMRSAGSSBNP-UHFFFAOYSA-N 0.000 claims description 9
- SPBDXSGPUHCETR-JFUDTMANSA-N 8883yp2r6d Chemical compound O1[C@@H](C)[C@H](O)[C@@H](OC)C[C@@H]1O[C@@H]1[C@@H](OC)C[C@H](O[C@@H]2C(=C/C[C@@H]3C[C@@H](C[C@@]4(O[C@@H]([C@@H](C)CC4)C(C)C)O3)OC(=O)[C@@H]3C=C(C)[C@@H](O)[C@H]4OC\C([C@@]34O)=C/C=C/[C@@H]2C)/C)O[C@H]1C.C1C[C@H](C)[C@@H]([C@@H](C)CC)O[C@@]21O[C@H](C\C=C(C)\[C@@H](O[C@@H]1O[C@@H](C)[C@H](O[C@@H]3O[C@@H](C)[C@H](O)[C@@H](OC)C3)[C@@H](OC)C1)[C@@H](C)\C=C\C=C/1[C@]3([C@H](C(=O)O4)C=C(C)[C@@H](O)[C@H]3OC\1)O)C[C@H]4C2 SPBDXSGPUHCETR-JFUDTMANSA-N 0.000 claims description 9
- 229960002669 albendazole Drugs 0.000 claims description 9
- HXHWSAZORRCQMX-UHFFFAOYSA-N albendazole Chemical compound CCCSC1=CC=C2NC(NC(=O)OC)=NC2=C1 HXHWSAZORRCQMX-UHFFFAOYSA-N 0.000 claims description 9
- 229960002418 ivermectin Drugs 0.000 claims description 9
- 230000002829 reductive effect Effects 0.000 claims description 8
- 206010061535 Ovarian neoplasm Diseases 0.000 claims description 7
- 206010060862 Prostate cancer Diseases 0.000 claims description 7
- 208000000236 Prostatic Neoplasms Diseases 0.000 claims description 7
- 206010061902 Pancreatic neoplasm Diseases 0.000 claims description 6
- 208000015486 malignant pancreatic neoplasm Diseases 0.000 claims description 6
- 201000002528 pancreatic cancer Diseases 0.000 claims description 6
- 208000008443 pancreatic carcinoma Diseases 0.000 claims description 6
- ZAHRKKWIAAJSAO-UHFFFAOYSA-N rapamycin Natural products COCC(O)C(=C/C(C)C(=O)CC(OC(=O)C1CCCCN1C(=O)C(=O)C2(O)OC(CC(OC)C(=CC=CC=CC(C)CC(C)C(=O)C)C)CCC2C)C(C)CC3CCC(O)C(C3)OC)C ZAHRKKWIAAJSAO-UHFFFAOYSA-N 0.000 claims description 6
- 229960002930 sirolimus Drugs 0.000 claims description 6
- QFJCIRLUMZQUOT-HPLJOQBZSA-N sirolimus Chemical compound C1C[C@@H](O)[C@H](OC)C[C@@H]1C[C@@H](C)[C@H]1OC(=O)[C@@H]2CCCCN2C(=O)C(=O)[C@](O)(O2)[C@H](C)CC[C@H]2C[C@H](OC)/C(C)=C/C=C/C=C/[C@@H](C)C[C@@H](C)C(=O)[C@H](OC)[C@H](O)/C(C)=C/[C@@H](C)C(=O)C1 QFJCIRLUMZQUOT-HPLJOQBZSA-N 0.000 claims description 6
- 239000011885 synergistic combination Substances 0.000 claims description 6
- 229940124597 therapeutic agent Drugs 0.000 claims description 5
- 201000007270 liver cancer Diseases 0.000 claims description 4
- 208000014018 liver neoplasm Diseases 0.000 claims description 4
- GXJABQQUPOEUTA-RDJZCZTQSA-N bortezomib Chemical compound C([C@@H](C(=O)N[C@@H](CC(C)C)B(O)O)NC(=O)C=1N=CC=NC=1)C1=CC=CC=C1 GXJABQQUPOEUTA-RDJZCZTQSA-N 0.000 claims description 3
- 229960001467 bortezomib Drugs 0.000 claims description 3
- 210000004027 cell Anatomy 0.000 description 253
- 229950003439 monepantel Drugs 0.000 description 241
- 230000003211 malignant effect Effects 0.000 description 62
- 230000001472 cytotoxic effect Effects 0.000 description 42
- 230000002195 synergetic effect Effects 0.000 description 42
- 231100000433 cytotoxic Toxicity 0.000 description 40
- 239000000203 mixture Substances 0.000 description 40
- 229940079593 drug Drugs 0.000 description 38
- 238000002474 experimental method Methods 0.000 description 33
- 230000003013 cytotoxicity Effects 0.000 description 30
- 231100000135 cytotoxicity Toxicity 0.000 description 30
- 239000003795 chemical substances by application Substances 0.000 description 28
- 238000000034 method Methods 0.000 description 26
- -1 England) Substances 0.000 description 25
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 25
- 230000009044 synergistic interaction Effects 0.000 description 25
- 230000004083 survival effect Effects 0.000 description 24
- 231100000338 sulforhodamine B assay Toxicity 0.000 description 21
- 238000003210 sulforhodamine B staining Methods 0.000 description 21
- 231100000337 synergistic cytotoxicity Toxicity 0.000 description 21
- 238000002512 chemotherapy Methods 0.000 description 19
- DQLATGHUWYMOKM-UHFFFAOYSA-L cisplatin Chemical compound N[Pt](N)(Cl)Cl DQLATGHUWYMOKM-UHFFFAOYSA-L 0.000 description 19
- 229960004316 cisplatin Drugs 0.000 description 19
- 241000282414 Homo sapiens Species 0.000 description 17
- 125000003118 aryl group Chemical group 0.000 description 16
- 230000037396 body weight Effects 0.000 description 16
- 238000002560 therapeutic procedure Methods 0.000 description 16
- 239000002671 adjuvant Substances 0.000 description 15
- 201000010099 disease Diseases 0.000 description 15
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 15
- 229940002612 prodrug Drugs 0.000 description 15
- 239000000651 prodrug Substances 0.000 description 15
- DNIAPMSPPWPWGF-UHFFFAOYSA-N propylene glycol Substances CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 15
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 14
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 13
- 230000005764 inhibitory process Effects 0.000 description 13
- 230000002611 ovarian Effects 0.000 description 13
- 125000000217 alkyl group Chemical group 0.000 description 12
- 125000001072 heteroaryl group Chemical group 0.000 description 12
- 206010061289 metastatic neoplasm Diseases 0.000 description 12
- 206010073071 hepatocellular carcinoma Diseases 0.000 description 11
- 230000001965 increasing effect Effects 0.000 description 11
- 206010024627 liposarcoma Diseases 0.000 description 11
- 239000000243 solution Substances 0.000 description 11
- 238000001356 surgical procedure Methods 0.000 description 11
- HLFSDGLLUJUHTE-SNVBAGLBSA-N Levamisole Chemical compound C1([C@H]2CN3CCSC3=N2)=CC=CC=C1 HLFSDGLLUJUHTE-SNVBAGLBSA-N 0.000 description 10
- 238000003556 assay Methods 0.000 description 10
- 229940044683 chemotherapy drug Drugs 0.000 description 10
- 230000034994 death Effects 0.000 description 10
- 231100000517 death Toxicity 0.000 description 10
- 239000003085 diluting agent Substances 0.000 description 10
- 229960001614 levamisole Drugs 0.000 description 10
- 239000007788 liquid Substances 0.000 description 10
- 239000002207 metabolite Substances 0.000 description 10
- 230000035945 sensitivity Effects 0.000 description 10
- 125000004432 carbon atom Chemical group C* 0.000 description 9
- 230000003993 interaction Effects 0.000 description 9
- 230000001394 metastastic effect Effects 0.000 description 9
- 238000002360 preparation method Methods 0.000 description 9
- 238000001959 radiotherapy Methods 0.000 description 9
- 125000001424 substituent group Chemical group 0.000 description 9
- 230000001988 toxicity Effects 0.000 description 9
- 231100000419 toxicity Toxicity 0.000 description 9
- IOOMXAQUNPWDLL-UHFFFAOYSA-N 2-[6-(diethylamino)-3-(diethyliminiumyl)-3h-xanthen-9-yl]-5-sulfobenzene-1-sulfonate Chemical compound C=12C=CC(=[N+](CC)CC)C=C2OC2=CC(N(CC)CC)=CC=C2C=1C1=CC=C(S(O)(=O)=O)C=C1S([O-])(=O)=O IOOMXAQUNPWDLL-UHFFFAOYSA-N 0.000 description 8
- NWIBSHFKIJFRCO-WUDYKRTCSA-N Mytomycin Chemical compound C1N2C(C(C(C)=C(N)C3=O)=O)=C3[C@@H](COC(N)=O)[C@@]2(OC)[C@@H]2[C@H]1N2 NWIBSHFKIJFRCO-WUDYKRTCSA-N 0.000 description 8
- 206010039491 Sarcoma Diseases 0.000 description 8
- 239000000890 drug combination Substances 0.000 description 8
- 230000009977 dual effect Effects 0.000 description 8
- 231100000844 hepatocellular carcinoma Toxicity 0.000 description 8
- 238000000338 in vitro Methods 0.000 description 8
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 8
- 239000000725 suspension Substances 0.000 description 8
- 210000001519 tissue Anatomy 0.000 description 8
- HNDVDQJCIGZPNO-UHFFFAOYSA-N Histidine Chemical compound OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 description 7
- 235000019483 Peanut oil Nutrition 0.000 description 7
- BPEGJWRSRHCHSN-UHFFFAOYSA-N Temozolomide Chemical compound O=C1N(C)N=NC2=C(C(N)=O)N=CN21 BPEGJWRSRHCHSN-UHFFFAOYSA-N 0.000 description 7
- 238000004113 cell culture Methods 0.000 description 7
- 229940127089 cytotoxic agent Drugs 0.000 description 7
- 239000003937 drug carrier Substances 0.000 description 7
- 230000006872 improvement Effects 0.000 description 7
- 239000000312 peanut oil Substances 0.000 description 7
- 239000007787 solid Substances 0.000 description 7
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 6
- 206010006187 Breast cancer Diseases 0.000 description 6
- 208000026310 Breast neoplasm Diseases 0.000 description 6
- 108020004414 DNA Proteins 0.000 description 6
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 6
- 208000007571 Ovarian Epithelial Carcinoma Diseases 0.000 description 6
- 239000004480 active ingredient Substances 0.000 description 6
- 239000000969 carrier Substances 0.000 description 6
- 239000006210 lotion Substances 0.000 description 6
- 238000004519 manufacturing process Methods 0.000 description 6
- 229910052760 oxygen Inorganic materials 0.000 description 6
- 229960004964 temozolomide Drugs 0.000 description 6
- 239000003981 vehicle Substances 0.000 description 6
- VBICKXHEKHSIBG-UHFFFAOYSA-N 1-monostearoylglycerol Chemical compound CCCCCCCCCCCCCCCCCC(=O)OCC(O)CO VBICKXHEKHSIBG-UHFFFAOYSA-N 0.000 description 5
- HNDVDQJCIGZPNO-YFKPBYRVSA-N L-histidine Chemical compound OC(=O)[C@@H](N)CC1=CN=CN1 HNDVDQJCIGZPNO-YFKPBYRVSA-N 0.000 description 5
- 241000244206 Nematoda Species 0.000 description 5
- 229940041181 antineoplastic drug Drugs 0.000 description 5
- 210000001130 astrocyte Anatomy 0.000 description 5
- 239000002775 capsule Substances 0.000 description 5
- 229910052799 carbon Inorganic materials 0.000 description 5
- 239000001768 carboxy methyl cellulose Substances 0.000 description 5
- 230000004663 cell proliferation Effects 0.000 description 5
- 238000011161 development Methods 0.000 description 5
- 230000018109 developmental process Effects 0.000 description 5
- 238000003745 diagnosis Methods 0.000 description 5
- 239000000839 emulsion Substances 0.000 description 5
- VJJPUSNTGOMMGY-MRVIYFEKSA-N etoposide Chemical compound COC1=C(O)C(OC)=CC([C@@H]2C3=CC=4OCOC=4C=C3[C@@H](O[C@H]3[C@@H]([C@@H](O)[C@@H]4O[C@H](C)OC[C@H]4O3)O)[C@@H]3[C@@H]2C(OC3)=O)=C1 VJJPUSNTGOMMGY-MRVIYFEKSA-N 0.000 description 5
- 230000001605 fetal effect Effects 0.000 description 5
- 235000011187 glycerol Nutrition 0.000 description 5
- 230000002401 inhibitory effect Effects 0.000 description 5
- 229960004857 mitomycin Drugs 0.000 description 5
- 229910052757 nitrogen Inorganic materials 0.000 description 5
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 5
- 239000004006 olive oil Substances 0.000 description 5
- 235000008390 olive oil Nutrition 0.000 description 5
- 239000000546 pharmaceutical excipient Substances 0.000 description 5
- 230000035755 proliferation Effects 0.000 description 5
- 238000002271 resection Methods 0.000 description 5
- 229910052717 sulfur Inorganic materials 0.000 description 5
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 4
- 206010055113 Breast cancer metastatic Diseases 0.000 description 4
- 206010008342 Cervix carcinoma Diseases 0.000 description 4
- 206010059866 Drug resistance Diseases 0.000 description 4
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 4
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 4
- 241000124008 Mammalia Species 0.000 description 4
- 102000029749 Microtubule Human genes 0.000 description 4
- 108091022875 Microtubule Proteins 0.000 description 4
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 4
- 229920001615 Tragacanth Polymers 0.000 description 4
- 208000006105 Uterine Cervical Neoplasms Diseases 0.000 description 4
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 description 4
- 125000003545 alkoxy group Chemical group 0.000 description 4
- 230000000844 anti-bacterial effect Effects 0.000 description 4
- 230000006907 apoptotic process Effects 0.000 description 4
- 239000003899 bactericide agent Substances 0.000 description 4
- 229960000397 bevacizumab Drugs 0.000 description 4
- RYYVLZVUVIJVGH-UHFFFAOYSA-N caffeine Chemical compound CN1C(=O)N(C)C(=O)C2=C1N=CN2C RYYVLZVUVIJVGH-UHFFFAOYSA-N 0.000 description 4
- 201000010881 cervical cancer Diseases 0.000 description 4
- 230000000295 complement effect Effects 0.000 description 4
- 239000006071 cream Substances 0.000 description 4
- 125000004122 cyclic group Chemical group 0.000 description 4
- 239000006196 drop Substances 0.000 description 4
- 102000015694 estrogen receptors Human genes 0.000 description 4
- 108010038795 estrogen receptors Proteins 0.000 description 4
- 229960005420 etoposide Drugs 0.000 description 4
- 239000000796 flavoring agent Substances 0.000 description 4
- 238000009472 formulation Methods 0.000 description 4
- 229910052736 halogen Inorganic materials 0.000 description 4
- 150000002367 halogens Chemical class 0.000 description 4
- 125000005842 heteroatom Chemical group 0.000 description 4
- 239000004615 ingredient Substances 0.000 description 4
- GURKHSYORGJETM-WAQYZQTGSA-N irinotecan hydrochloride (anhydrous) Chemical compound Cl.C1=C2C(CC)=C3CN(C(C4=C([C@@](C(=O)OC4)(O)CC)C=4)=O)C=4C3=NC2=CC=C1OC(=O)N(CC1)CCC1N1CCCCC1 GURKHSYORGJETM-WAQYZQTGSA-N 0.000 description 4
- 229940057995 liquid paraffin Drugs 0.000 description 4
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 4
- 239000000463 material Substances 0.000 description 4
- 229920000609 methyl cellulose Polymers 0.000 description 4
- 235000010981 methylcellulose Nutrition 0.000 description 4
- 239000001923 methylcellulose Substances 0.000 description 4
- 210000004688 microtubule Anatomy 0.000 description 4
- 229940035032 monophosphoryl lipid a Drugs 0.000 description 4
- 231100000252 nontoxic Toxicity 0.000 description 4
- 230000003000 nontoxic effect Effects 0.000 description 4
- 239000003921 oil Substances 0.000 description 4
- 235000019198 oils Nutrition 0.000 description 4
- 230000036470 plasma concentration Effects 0.000 description 4
- 229910052697 platinum Inorganic materials 0.000 description 4
- 239000000843 powder Substances 0.000 description 4
- 239000003755 preservative agent Substances 0.000 description 4
- 235000019812 sodium carboxymethyl cellulose Nutrition 0.000 description 4
- 239000003826 tablet Substances 0.000 description 4
- 229960004528 vincristine Drugs 0.000 description 4
- OGWKCGZFUXNPDA-XQKSVPLYSA-N vincristine Chemical compound C([N@]1C[C@@H](C[C@]2(C(=O)OC)C=3C(=CC4=C([C@]56[C@H]([C@@]([C@H](OC(C)=O)[C@]7(CC)C=CCN([C@H]67)CC5)(O)C(=O)OC)N4C=O)C=3)OC)C[C@@](C1)(O)CC)CC1=C2NC2=CC=CC=C12 OGWKCGZFUXNPDA-XQKSVPLYSA-N 0.000 description 4
- OGWKCGZFUXNPDA-UHFFFAOYSA-N vincristine Natural products C1C(CC)(O)CC(CC2(C(=O)OC)C=3C(=CC4=C(C56C(C(C(OC(C)=O)C7(CC)C=CCN(C67)CC5)(O)C(=O)OC)N4C=O)C=3)OC)CN1CCC1=C2NC2=CC=CC=C12 OGWKCGZFUXNPDA-UHFFFAOYSA-N 0.000 description 4
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 4
- LNAZSHAWQACDHT-XIYTZBAFSA-N (2r,3r,4s,5r,6s)-4,5-dimethoxy-2-(methoxymethyl)-3-[(2s,3r,4s,5r,6r)-3,4,5-trimethoxy-6-(methoxymethyl)oxan-2-yl]oxy-6-[(2r,3r,4s,5r,6r)-4,5,6-trimethoxy-2-(methoxymethyl)oxan-3-yl]oxyoxane Chemical compound CO[C@@H]1[C@@H](OC)[C@H](OC)[C@@H](COC)O[C@H]1O[C@H]1[C@H](OC)[C@@H](OC)[C@H](O[C@H]2[C@@H]([C@@H](OC)[C@H](OC)O[C@@H]2COC)OC)O[C@@H]1COC LNAZSHAWQACDHT-XIYTZBAFSA-N 0.000 description 3
- IXPNQXFRVYWDDI-UHFFFAOYSA-N 1-methyl-2,4-dioxo-1,3-diazinane-5-carboximidamide Chemical compound CN1CC(C(N)=N)C(=O)NC1=O IXPNQXFRVYWDDI-UHFFFAOYSA-N 0.000 description 3
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 3
- 206010052747 Adenocarcinoma pancreas Diseases 0.000 description 3
- 241000416162 Astragalus gummifer Species 0.000 description 3
- MLDQJTXFUGDVEO-UHFFFAOYSA-N BAY-43-9006 Chemical compound C1=NC(C(=O)NC)=CC(OC=2C=CC(NC(=O)NC=3C=C(C(Cl)=CC=3)C(F)(F)F)=CC=2)=C1 MLDQJTXFUGDVEO-UHFFFAOYSA-N 0.000 description 3
- CMSMOCZEIVJLDB-UHFFFAOYSA-N Cyclophosphamide Chemical compound ClCCN(CCCl)P1(=O)NCCCO1 CMSMOCZEIVJLDB-UHFFFAOYSA-N 0.000 description 3
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 3
- 201000008808 Fibrosarcoma Diseases 0.000 description 3
- 206010018338 Glioma Diseases 0.000 description 3
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 3
- 108010017213 Granulocyte-Macrophage Colony-Stimulating Factor Proteins 0.000 description 3
- 102100039620 Granulocyte-macrophage colony-stimulating factor Human genes 0.000 description 3
- 241000282412 Homo Species 0.000 description 3
- 239000005511 L01XE05 - Sorafenib Substances 0.000 description 3
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 3
- 240000007472 Leucaena leucocephala Species 0.000 description 3
- 235000010643 Leucaena leucocephala Nutrition 0.000 description 3
- 206010027476 Metastases Diseases 0.000 description 3
- ZDZOTLJHXYCWBA-VCVYQWHSSA-N N-debenzoyl-N-(tert-butoxycarbonyl)-10-deacetyltaxol Chemical compound O([C@H]1[C@H]2[C@@](C([C@H](O)C3=C(C)[C@@H](OC(=O)[C@H](O)[C@@H](NC(=O)OC(C)(C)C)C=4C=CC=CC=4)C[C@]1(O)C3(C)C)=O)(C)[C@@H](O)C[C@H]1OC[C@]12OC(=O)C)C(=O)C1=CC=CC=C1 ZDZOTLJHXYCWBA-VCVYQWHSSA-N 0.000 description 3
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 3
- 229920003171 Poly (ethylene oxide) Chemical class 0.000 description 3
- 239000002202 Polyethylene glycol Substances 0.000 description 3
- 235000019485 Safflower oil Nutrition 0.000 description 3
- 235000021355 Stearic acid Nutrition 0.000 description 3
- 229940123237 Taxane Drugs 0.000 description 3
- 108010022394 Threonine synthase Proteins 0.000 description 3
- 102000005497 Thymidylate Synthase Human genes 0.000 description 3
- GLNADSQYFUSGOU-GPTZEZBUSA-J Trypan blue Chemical compound [Na+].[Na+].[Na+].[Na+].C1=C(S([O-])(=O)=O)C=C2C=C(S([O-])(=O)=O)C(/N=N/C3=CC=C(C=C3C)C=3C=C(C(=CC=3)\N=N\C=3C(=CC4=CC(=CC(N)=C4C=3O)S([O-])(=O)=O)S([O-])(=O)=O)C)=C(O)C2=C1N GLNADSQYFUSGOU-GPTZEZBUSA-J 0.000 description 3
- 102000004243 Tubulin Human genes 0.000 description 3
- 108090000704 Tubulin Proteins 0.000 description 3
- 238000010162 Tukey test Methods 0.000 description 3
- 230000009471 action Effects 0.000 description 3
- 230000000996 additive effect Effects 0.000 description 3
- 230000002411 adverse Effects 0.000 description 3
- 239000000443 aerosol Substances 0.000 description 3
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 3
- 229910052782 aluminium Inorganic materials 0.000 description 3
- 239000003098 androgen Substances 0.000 description 3
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 3
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 3
- 238000001516 cell proliferation assay Methods 0.000 description 3
- 230000003833 cell viability Effects 0.000 description 3
- 229920002678 cellulose Polymers 0.000 description 3
- 239000001913 cellulose Substances 0.000 description 3
- 235000010980 cellulose Nutrition 0.000 description 3
- 229960005395 cetuximab Drugs 0.000 description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 3
- 230000002301 combined effect Effects 0.000 description 3
- 239000000470 constituent Substances 0.000 description 3
- 235000005687 corn oil Nutrition 0.000 description 3
- 239000002285 corn oil Substances 0.000 description 3
- 125000000753 cycloalkyl group Chemical group 0.000 description 3
- 238000002784 cytotoxicity assay Methods 0.000 description 3
- 231100000263 cytotoxicity test Toxicity 0.000 description 3
- GYOZYWVXFNDGLU-XLPZGREQSA-N dTMP Chemical compound O=C1NC(=O)C(C)=CN1[C@@H]1O[C@H](COP(O)(O)=O)[C@@H](O)C1 GYOZYWVXFNDGLU-XLPZGREQSA-N 0.000 description 3
- 238000001514 detection method Methods 0.000 description 3
- 235000014113 dietary fatty acids Nutrition 0.000 description 3
- 239000002270 dispersing agent Substances 0.000 description 3
- 239000003995 emulsifying agent Substances 0.000 description 3
- 230000002708 enhancing effect Effects 0.000 description 3
- 210000001508 eye Anatomy 0.000 description 3
- 239000000194 fatty acid Substances 0.000 description 3
- 229930195729 fatty acid Natural products 0.000 description 3
- 235000003599 food sweetener Nutrition 0.000 description 3
- 229960001031 glucose Drugs 0.000 description 3
- 229960002885 histidine Drugs 0.000 description 3
- 238000001727 in vivo Methods 0.000 description 3
- 229960004768 irinotecan Drugs 0.000 description 3
- 239000008101 lactose Substances 0.000 description 3
- 230000004060 metabolic process Effects 0.000 description 3
- 230000009401 metastasis Effects 0.000 description 3
- 239000001788 mono and diglycerides of fatty acids Substances 0.000 description 3
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 3
- 239000002674 ointment Substances 0.000 description 3
- 238000011275 oncology therapy Methods 0.000 description 3
- 239000001301 oxygen Substances 0.000 description 3
- 201000002094 pancreatic adenocarcinoma Diseases 0.000 description 3
- 238000011518 platinum-based chemotherapy Methods 0.000 description 3
- 229920001223 polyethylene glycol Polymers 0.000 description 3
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 3
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 3
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 3
- 230000003389 potentiating effect Effects 0.000 description 3
- 102000003998 progesterone receptors Human genes 0.000 description 3
- 108090000468 progesterone receptors Proteins 0.000 description 3
- 239000003528 protein farnesyltransferase inhibitor Substances 0.000 description 3
- 125000004076 pyridyl group Chemical group 0.000 description 3
- 230000009467 reduction Effects 0.000 description 3
- 238000011160 research Methods 0.000 description 3
- 125000006413 ring segment Chemical group 0.000 description 3
- 102200082402 rs751610198 Human genes 0.000 description 3
- 235000005713 safflower oil Nutrition 0.000 description 3
- 239000003813 safflower oil Substances 0.000 description 3
- 239000008159 sesame oil Substances 0.000 description 3
- 235000011803 sesame oil Nutrition 0.000 description 3
- 230000019491 signal transduction Effects 0.000 description 3
- 235000010413 sodium alginate Nutrition 0.000 description 3
- 239000000661 sodium alginate Substances 0.000 description 3
- 229940005550 sodium alginate Drugs 0.000 description 3
- 229920001027 sodium carboxymethylcellulose Polymers 0.000 description 3
- 229960003787 sorafenib Drugs 0.000 description 3
- 239000000600 sorbitol Substances 0.000 description 3
- 235000010356 sorbitol Nutrition 0.000 description 3
- 239000008117 stearic acid Substances 0.000 description 3
- 238000006467 substitution reaction Methods 0.000 description 3
- 239000000375 suspending agent Substances 0.000 description 3
- 239000003765 sweetening agent Substances 0.000 description 3
- 208000024891 symptom Diseases 0.000 description 3
- 210000004881 tumor cell Anatomy 0.000 description 3
- PUPZLCDOIYMWBV-UHFFFAOYSA-N (+/-)-1,3-Butanediol Chemical compound CC(O)CCO PUPZLCDOIYMWBV-UHFFFAOYSA-N 0.000 description 2
- YXTKHLHCVFUPPT-YYFJYKOTSA-N (2s)-2-[[4-[(2-amino-5-formyl-4-oxo-1,6,7,8-tetrahydropteridin-6-yl)methylamino]benzoyl]amino]pentanedioic acid;(1r,2r)-1,2-dimethanidylcyclohexane;5-fluoro-1h-pyrimidine-2,4-dione;oxalic acid;platinum(2+) Chemical compound [Pt+2].OC(=O)C(O)=O.[CH2-][C@@H]1CCCC[C@H]1[CH2-].FC1=CNC(=O)NC1=O.C1NC=2NC(N)=NC(=O)C=2N(C=O)C1CNC1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 YXTKHLHCVFUPPT-YYFJYKOTSA-N 0.000 description 2
- GVJHHUAWPYXKBD-UHFFFAOYSA-N (±)-α-Tocopherol Chemical compound OC1=C(C)C(C)=C2OC(CCCC(C)CCCC(C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-UHFFFAOYSA-N 0.000 description 2
- IIZPXYDJLKNOIY-JXPKJXOSSA-N 1-palmitoyl-2-arachidonoyl-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCC\C=C/C\C=C/C\C=C/C\C=C/CCCCC IIZPXYDJLKNOIY-JXPKJXOSSA-N 0.000 description 2
- DGHHQBMTXTWTJV-BQAIUKQQSA-N 119413-54-6 Chemical compound Cl.C1=C(O)C(CN(C)C)=C2C=C(CN3C4=CC5=C(C3=O)COC(=O)[C@]5(O)CC)C4=NC2=C1 DGHHQBMTXTWTJV-BQAIUKQQSA-N 0.000 description 2
- IZHVBANLECCAGF-UHFFFAOYSA-N 2-hydroxy-3-(octadecanoyloxy)propyl octadecanoate Chemical compound CCCCCCCCCCCCCCCCCC(=O)OCC(O)COC(=O)CCCCCCCCCCCCCCCCC IZHVBANLECCAGF-UHFFFAOYSA-N 0.000 description 2
- VVIAGPKUTFNRDU-UHFFFAOYSA-N 6S-folinic acid Natural products C1NC=2NC(N)=NC(=O)C=2N(C=O)C1CNC1=CC=C(C(=O)NC(CCC(O)=O)C(O)=O)C=C1 VVIAGPKUTFNRDU-UHFFFAOYSA-N 0.000 description 2
- 108010042708 Acetylmuramyl-Alanyl-Isoglutamine Proteins 0.000 description 2
- 229920001817 Agar Polymers 0.000 description 2
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 2
- 244000105624 Arachis hypogaea Species 0.000 description 2
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 2
- 206010003571 Astrocytoma Diseases 0.000 description 2
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 description 2
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 2
- 102000009016 Cholera Toxin Human genes 0.000 description 2
- 108010049048 Cholera Toxin Proteins 0.000 description 2
- 229920002261 Corn starch Polymers 0.000 description 2
- 239000004971 Cross linker Substances 0.000 description 2
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 2
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 2
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 2
- 102000004190 Enzymes Human genes 0.000 description 2
- 108090000790 Enzymes Proteins 0.000 description 2
- MPJKWIXIYCLVCU-UHFFFAOYSA-N Folinic acid Natural products NC1=NC2=C(N(C=O)C(CNc3ccc(cc3)C(=O)NC(CCC(=O)O)CC(=O)O)CN2)C(=O)N1 MPJKWIXIYCLVCU-UHFFFAOYSA-N 0.000 description 2
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 2
- 108010010803 Gelatin Proteins 0.000 description 2
- 239000004471 Glycine Substances 0.000 description 2
- 229920002907 Guar gum Polymers 0.000 description 2
- 229920000084 Gum arabic Polymers 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 2
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 2
- LPHGQDQBBGAPDZ-UHFFFAOYSA-N Isocaffeine Natural products CN1C(=O)N(C)C(=O)C2=C1N(C)C=N2 LPHGQDQBBGAPDZ-UHFFFAOYSA-N 0.000 description 2
- 229930195725 Mannitol Natural products 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 2
- 229930192392 Mitomycin Natural products 0.000 description 2
- 206010073137 Myxoid liposarcoma Diseases 0.000 description 2
- 208000020258 Myxoid/round cell liposarcoma Diseases 0.000 description 2
- HSHXDCVZWHOWCS-UHFFFAOYSA-N N'-hexadecylthiophene-2-carbohydrazide Chemical compound CCCCCCCCCCCCCCCCNNC(=O)c1cccs1 HSHXDCVZWHOWCS-UHFFFAOYSA-N 0.000 description 2
- 102000038030 PI3Ks Human genes 0.000 description 2
- 108091007960 PI3Ks Proteins 0.000 description 2
- 241001494479 Pecora Species 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- 241000725643 Respiratory syncytial virus Species 0.000 description 2
- 229930006000 Sucrose Natural products 0.000 description 2
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 2
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- IQFYYKKMVGJFEH-XLPZGREQSA-N Thymidine Chemical compound O=C1NC(=O)C(C)=CN1[C@@H]1O[C@H](CO)[C@@H](O)C1 IQFYYKKMVGJFEH-XLPZGREQSA-N 0.000 description 2
- 239000007983 Tris buffer Substances 0.000 description 2
- 238000002835 absorbance Methods 0.000 description 2
- 239000000205 acacia gum Substances 0.000 description 2
- 239000002253 acid Substances 0.000 description 2
- 239000008272 agar Substances 0.000 description 2
- 235000010419 agar Nutrition 0.000 description 2
- 239000000556 agonist Substances 0.000 description 2
- 238000007605 air drying Methods 0.000 description 2
- 239000004411 aluminium Substances 0.000 description 2
- ILRRQNADMUWWFW-UHFFFAOYSA-K aluminium phosphate Chemical compound O1[Al]2OP1(=O)O2 ILRRQNADMUWWFW-UHFFFAOYSA-K 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- 238000010171 animal model Methods 0.000 description 2
- 239000005557 antagonist Substances 0.000 description 2
- 229940046836 anti-estrogen Drugs 0.000 description 2
- 230000001833 anti-estrogenic effect Effects 0.000 description 2
- 230000000340 anti-metabolite Effects 0.000 description 2
- 229940100197 antimetabolite Drugs 0.000 description 2
- 239000002256 antimetabolite Substances 0.000 description 2
- 239000007864 aqueous solution Substances 0.000 description 2
- VSRXQHXAPYXROS-UHFFFAOYSA-N azanide;cyclobutane-1,1-dicarboxylic acid;platinum(2+) Chemical compound [NH2-].[NH2-].[Pt+2].OC(=O)C1(C(O)=O)CCC1 VSRXQHXAPYXROS-UHFFFAOYSA-N 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- 239000011230 binding agent Substances 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 230000006406 biphasic response Effects 0.000 description 2
- 210000000481 breast Anatomy 0.000 description 2
- VJEONQKOZGKCAK-UHFFFAOYSA-N caffeine Natural products CN1C(=O)N(C)C(=O)C2=C1C=CN2C VJEONQKOZGKCAK-UHFFFAOYSA-N 0.000 description 2
- 229960001948 caffeine Drugs 0.000 description 2
- 230000005907 cancer growth Effects 0.000 description 2
- 229960004562 carboplatin Drugs 0.000 description 2
- 239000004359 castor oil Substances 0.000 description 2
- 235000019438 castor oil Nutrition 0.000 description 2
- 239000006143 cell culture medium Substances 0.000 description 2
- 210000003169 central nervous system Anatomy 0.000 description 2
- 125000001309 chloro group Chemical group Cl* 0.000 description 2
- CCGSUNCLSOWKJO-UHFFFAOYSA-N cimetidine Chemical compound N#CNC(=N/C)\NCCSCC1=NC=N[C]1C CCGSUNCLSOWKJO-UHFFFAOYSA-N 0.000 description 2
- 229960001380 cimetidine Drugs 0.000 description 2
- 239000011248 coating agent Substances 0.000 description 2
- 239000003240 coconut oil Substances 0.000 description 2
- 235000019864 coconut oil Nutrition 0.000 description 2
- 208000029742 colonic neoplasm Diseases 0.000 description 2
- 201000010989 colorectal carcinoma Diseases 0.000 description 2
- 229940000425 combination drug Drugs 0.000 description 2
- 238000011284 combination treatment Methods 0.000 description 2
- 230000000052 comparative effect Effects 0.000 description 2
- 239000008120 corn starch Substances 0.000 description 2
- 235000012343 cottonseed oil Nutrition 0.000 description 2
- 239000002385 cottonseed oil Substances 0.000 description 2
- 229960004397 cyclophosphamide Drugs 0.000 description 2
- 239000002254 cytotoxic agent Substances 0.000 description 2
- 231100000599 cytotoxic agent Toxicity 0.000 description 2
- JSRLJPSBLDHEIO-SHYZEUOFSA-N dUMP Chemical compound O1[C@H](COP(O)(O)=O)[C@@H](O)C[C@@H]1N1C(=O)NC(=O)C=C1 JSRLJPSBLDHEIO-SHYZEUOFSA-N 0.000 description 2
- 239000008121 dextrose Substances 0.000 description 2
- 229960003668 docetaxel Drugs 0.000 description 2
- POULHZVOKOAJMA-UHFFFAOYSA-M dodecanoate Chemical compound CCCCCCCCCCCC([O-])=O POULHZVOKOAJMA-UHFFFAOYSA-M 0.000 description 2
- 239000002552 dosage form Substances 0.000 description 2
- 238000009510 drug design Methods 0.000 description 2
- 239000002158 endotoxin Substances 0.000 description 2
- 102000052116 epidermal growth factor receptor activity proteins Human genes 0.000 description 2
- 108700015053 epidermal growth factor receptor activity proteins Proteins 0.000 description 2
- 150000002148 esters Chemical class 0.000 description 2
- 239000000328 estrogen antagonist Substances 0.000 description 2
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 2
- 235000019197 fats Nutrition 0.000 description 2
- 150000004665 fatty acids Chemical class 0.000 description 2
- 150000002191 fatty alcohols Chemical class 0.000 description 2
- 238000001914 filtration Methods 0.000 description 2
- 125000001153 fluoro group Chemical group F* 0.000 description 2
- VVIAGPKUTFNRDU-ABLWVSNPSA-N folinic acid Chemical compound C1NC=2NC(N)=NC(=O)C=2N(C=O)C1CNC1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 VVIAGPKUTFNRDU-ABLWVSNPSA-N 0.000 description 2
- 235000008191 folinic acid Nutrition 0.000 description 2
- 239000011672 folinic acid Substances 0.000 description 2
- 235000013355 food flavoring agent Nutrition 0.000 description 2
- 239000000417 fungicide Substances 0.000 description 2
- 239000008273 gelatin Substances 0.000 description 2
- 229920000159 gelatin Polymers 0.000 description 2
- 235000019322 gelatine Nutrition 0.000 description 2
- 235000011852 gelatine desserts Nutrition 0.000 description 2
- 229940080856 gleevec Drugs 0.000 description 2
- 230000002518 glial effect Effects 0.000 description 2
- 229940075507 glyceryl monostearate Drugs 0.000 description 2
- 229960002449 glycine Drugs 0.000 description 2
- 235000010417 guar gum Nutrition 0.000 description 2
- 239000000665 guar gum Substances 0.000 description 2
- 229960002154 guar gum Drugs 0.000 description 2
- 235000010979 hydroxypropyl methyl cellulose Nutrition 0.000 description 2
- 239000001866 hydroxypropyl methyl cellulose Substances 0.000 description 2
- 229920003088 hydroxypropyl methyl cellulose Polymers 0.000 description 2
- 125000002883 imidazolyl group Chemical group 0.000 description 2
- 239000003112 inhibitor Substances 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- 239000000543 intermediate Substances 0.000 description 2
- 238000007918 intramuscular administration Methods 0.000 description 2
- 230000002147 killing effect Effects 0.000 description 2
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 2
- 229940070765 laurate Drugs 0.000 description 2
- 235000010445 lecithin Nutrition 0.000 description 2
- 239000000787 lecithin Substances 0.000 description 2
- 229940067606 lecithin Drugs 0.000 description 2
- 229960001691 leucovorin Drugs 0.000 description 2
- 230000000670 limiting effect Effects 0.000 description 2
- 239000000865 liniment Substances 0.000 description 2
- 229920006008 lipopolysaccharide Polymers 0.000 description 2
- 239000002502 liposome Substances 0.000 description 2
- 210000004185 liver Anatomy 0.000 description 2
- 244000144972 livestock Species 0.000 description 2
- DHMTURDWPRKSOA-RUZDIDTESA-N lonafarnib Chemical compound C1CN(C(=O)N)CCC1CC(=O)N1CCC([C@@H]2C3=C(Br)C=C(Cl)C=C3CCC3=CC(Br)=CN=C32)CC1 DHMTURDWPRKSOA-RUZDIDTESA-N 0.000 description 2
- 239000000314 lubricant Substances 0.000 description 2
- 235000019359 magnesium stearate Nutrition 0.000 description 2
- 230000036210 malignancy Effects 0.000 description 2
- 239000000594 mannitol Substances 0.000 description 2
- 235000010355 mannitol Nutrition 0.000 description 2
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 2
- LXCFILQKKLGQFO-UHFFFAOYSA-N methylparaben Chemical compound COC(=O)C1=CC=C(O)C=C1 LXCFILQKKLGQFO-UHFFFAOYSA-N 0.000 description 2
- VKHAHZOOUSRJNA-GCNJZUOMSA-N mifepristone Chemical compound C1([C@@H]2C3=C4CCC(=O)C=C4CC[C@H]3[C@@H]3CC[C@@]([C@]3(C2)C)(O)C#CC)=CC=C(N(C)C)C=C1 VKHAHZOOUSRJNA-GCNJZUOMSA-N 0.000 description 2
- 229960003248 mifepristone Drugs 0.000 description 2
- 150000007522 mineralic acids Chemical class 0.000 description 2
- 238000002156 mixing Methods 0.000 description 2
- BSOQXXWZTUDTEL-ZUYCGGNHSA-N muramyl dipeptide Chemical compound OC(=O)CC[C@H](C(N)=O)NC(=O)[C@H](C)NC(=O)[C@@H](C)O[C@H]1[C@H](O)[C@@H](CO)O[C@@H](O)[C@@H]1NC(C)=O BSOQXXWZTUDTEL-ZUYCGGNHSA-N 0.000 description 2
- YOHYSYJDKVYCJI-UHFFFAOYSA-N n-[3-[[6-[3-(trifluoromethyl)anilino]pyrimidin-4-yl]amino]phenyl]cyclopropanecarboxamide Chemical compound FC(F)(F)C1=CC=CC(NC=2N=CN=C(NC=3C=C(NC(=O)C4CC4)C=CC=3)C=2)=C1 YOHYSYJDKVYCJI-UHFFFAOYSA-N 0.000 description 2
- 229920001206 natural gum Polymers 0.000 description 2
- 210000004498 neuroglial cell Anatomy 0.000 description 2
- 231100000956 nontoxicity Toxicity 0.000 description 2
- 239000002777 nucleoside Substances 0.000 description 2
- 238000001543 one-way ANOVA Methods 0.000 description 2
- 150000007524 organic acids Chemical class 0.000 description 2
- 229960001972 panitumumab Drugs 0.000 description 2
- 238000007911 parenteral administration Methods 0.000 description 2
- 239000006072 paste Substances 0.000 description 2
- 230000000144 pharmacologic effect Effects 0.000 description 2
- 239000002953 phosphate buffered saline Substances 0.000 description 2
- 150000003057 platinum Chemical class 0.000 description 2
- 229920001296 polysiloxane Polymers 0.000 description 2
- 230000000069 prophylactic effect Effects 0.000 description 2
- QELSKZZBTMNZEB-UHFFFAOYSA-N propylparaben Chemical compound CCCOC(=O)C1=CC=C(O)C=C1 QELSKZZBTMNZEB-UHFFFAOYSA-N 0.000 description 2
- 210000005267 prostate cell Anatomy 0.000 description 2
- 125000003226 pyrazolyl group Chemical group 0.000 description 2
- 125000000714 pyrimidinyl group Chemical group 0.000 description 2
- 230000003439 radiotherapeutic effect Effects 0.000 description 2
- 230000004044 response Effects 0.000 description 2
- YGSDEFSMJLZEOE-UHFFFAOYSA-N salicylic acid Chemical compound OC(=O)C1=CC=CC=C1O YGSDEFSMJLZEOE-UHFFFAOYSA-N 0.000 description 2
- QZAYGJVTTNCVMB-UHFFFAOYSA-N serotonin Chemical compound C1=C(O)C=C2C(CCN)=CNC2=C1 QZAYGJVTTNCVMB-UHFFFAOYSA-N 0.000 description 2
- 241000894007 species Species 0.000 description 2
- PRAKJMSDJKAYCZ-UHFFFAOYSA-N squalane Chemical compound CC(C)CCCC(C)CCCC(C)CCCCC(C)CCCC(C)CCCC(C)C PRAKJMSDJKAYCZ-UHFFFAOYSA-N 0.000 description 2
- 238000007920 subcutaneous administration Methods 0.000 description 2
- 239000005720 sucrose Substances 0.000 description 2
- 235000000346 sugar Nutrition 0.000 description 2
- 239000011593 sulfur Substances 0.000 description 2
- 239000004094 surface-active agent Substances 0.000 description 2
- 238000003786 synthesis reaction Methods 0.000 description 2
- 239000000454 talc Substances 0.000 description 2
- 229910052623 talc Inorganic materials 0.000 description 2
- 235000012222 talc Nutrition 0.000 description 2
- WGTYBPLFGIVFAS-UHFFFAOYSA-M tetramethylammonium hydroxide Chemical compound [OH-].C[N+](C)(C)C WGTYBPLFGIVFAS-UHFFFAOYSA-M 0.000 description 2
- 238000011287 therapeutic dose Methods 0.000 description 2
- 231100001274 therapeutic index Toxicity 0.000 description 2
- 125000000335 thiazolyl group Chemical group 0.000 description 2
- RWQNBRDOKXIBIV-UHFFFAOYSA-N thymine Chemical compound CC1=CNC(=O)NC1=O RWQNBRDOKXIBIV-UHFFFAOYSA-N 0.000 description 2
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 2
- 238000011200 topical administration Methods 0.000 description 2
- 229960000303 topotecan Drugs 0.000 description 2
- 231100000331 toxic Toxicity 0.000 description 2
- 230000002588 toxic effect Effects 0.000 description 2
- 238000011269 treatment regimen Methods 0.000 description 2
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 2
- 229940121358 tyrosine kinase inhibitor Drugs 0.000 description 2
- 239000005483 tyrosine kinase inhibitor Substances 0.000 description 2
- 230000035899 viability Effects 0.000 description 2
- 238000003026 viability measurement method Methods 0.000 description 2
- GVJHHUAWPYXKBD-IEOSBIPESA-N α-tocopherol Chemical compound OC1=C(C)C(C)=C2O[C@@](CCC[C@H](C)CCC[C@H](C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-IEOSBIPESA-N 0.000 description 2
- JNYAEWCLZODPBN-JGWLITMVSA-N (2r,3r,4s)-2-[(1r)-1,2-dihydroxyethyl]oxolane-3,4-diol Chemical class OC[C@@H](O)[C@H]1OC[C@H](O)[C@H]1O JNYAEWCLZODPBN-JGWLITMVSA-N 0.000 description 1
- PAORVUMOXXAMPL-SECBINFHSA-N (2s)-3,3,3-trifluoro-2-methoxy-2-phenylpropanoyl chloride Chemical compound CO[C@](C(Cl)=O)(C(F)(F)F)C1=CC=CC=C1 PAORVUMOXXAMPL-SECBINFHSA-N 0.000 description 1
- WRIDQFICGBMAFQ-UHFFFAOYSA-N (E)-8-Octadecenoic acid Natural products CCCCCCCCCC=CCCCCCCC(O)=O WRIDQFICGBMAFQ-UHFFFAOYSA-N 0.000 description 1
- BJEPYKJPYRNKOW-REOHCLBHSA-N (S)-malic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O BJEPYKJPYRNKOW-REOHCLBHSA-N 0.000 description 1
- FTNJQNQLEGKTGD-UHFFFAOYSA-N 1,3-benzodioxole Chemical compound C1=CC=C2OCOC2=C1 FTNJQNQLEGKTGD-UHFFFAOYSA-N 0.000 description 1
- 229940058015 1,3-butylene glycol Drugs 0.000 description 1
- BHFLSZOGGDDWQM-UHFFFAOYSA-N 1h-benzimidazole;carbamic acid Chemical compound NC(O)=O.C1=CC=C2NC=NC2=C1 BHFLSZOGGDDWQM-UHFFFAOYSA-N 0.000 description 1
- SMZOUWXMTYCWNB-UHFFFAOYSA-N 2-(2-methoxy-5-methylphenyl)ethanamine Chemical compound COC1=CC=C(C)C=C1CCN SMZOUWXMTYCWNB-UHFFFAOYSA-N 0.000 description 1
- NIXOWILDQLNWCW-UHFFFAOYSA-N 2-Propenoic acid Natural products OC(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 1
- IVLXQGJVBGMLRR-UHFFFAOYSA-N 2-aminoacetic acid;hydron;chloride Chemical compound Cl.NCC(O)=O IVLXQGJVBGMLRR-UHFFFAOYSA-N 0.000 description 1
- LQJBNNIYVWPHFW-UHFFFAOYSA-N 20:1omega9c fatty acid Natural products CCCCCCCCCCC=CCCCCCCCC(O)=O LQJBNNIYVWPHFW-UHFFFAOYSA-N 0.000 description 1
- WEVYNIUIFUYDGI-UHFFFAOYSA-N 3-[6-[4-(trifluoromethoxy)anilino]-4-pyrimidinyl]benzamide Chemical compound NC(=O)C1=CC=CC(C=2N=CN=C(NC=3C=CC(OC(F)(F)F)=CC=3)C=2)=C1 WEVYNIUIFUYDGI-UHFFFAOYSA-N 0.000 description 1
- BMYNFMYTOJXKLE-UHFFFAOYSA-N 3-azaniumyl-2-hydroxypropanoate Chemical compound NCC(O)C(O)=O BMYNFMYTOJXKLE-UHFFFAOYSA-N 0.000 description 1
- HIQIXEFWDLTDED-UHFFFAOYSA-N 4-hydroxy-1-piperidin-4-ylpyrrolidin-2-one Chemical compound O=C1CC(O)CN1C1CCNCC1 HIQIXEFWDLTDED-UHFFFAOYSA-N 0.000 description 1
- 108010068327 4-hydroxyphenylpyruvate dioxygenase Proteins 0.000 description 1
- STQGQHZAVUOBTE-UHFFFAOYSA-N 7-Cyan-hept-2t-en-4,6-diinsaeure Natural products C1=2C(O)=C3C(=O)C=4C(OC)=CC=CC=4C(=O)C3=C(O)C=2CC(O)(C(C)=O)CC1OC1CC(N)C(O)C(C)O1 STQGQHZAVUOBTE-UHFFFAOYSA-N 0.000 description 1
- QSBYPNXLFMSGKH-UHFFFAOYSA-N 9-Heptadecensaeure Natural products CCCCCCCC=CCCCCCCCC(O)=O QSBYPNXLFMSGKH-UHFFFAOYSA-N 0.000 description 1
- 244000215068 Acacia senegal Species 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- 208000030090 Acute Disease Diseases 0.000 description 1
- 208000036832 Adenocarcinoma of ovary Diseases 0.000 description 1
- 235000019489 Almond oil Nutrition 0.000 description 1
- 201000004384 Alopecia Diseases 0.000 description 1
- 239000005995 Aluminium silicate Substances 0.000 description 1
- QGZKDVFQNNGYKY-UHFFFAOYSA-O Ammonium Chemical compound [NH4+] QGZKDVFQNNGYKY-UHFFFAOYSA-O 0.000 description 1
- 244000144725 Amygdalus communis Species 0.000 description 1
- 235000017060 Arachis glabrata Nutrition 0.000 description 1
- 235000010777 Arachis hypogaea Nutrition 0.000 description 1
- 235000018262 Arachis monticola Nutrition 0.000 description 1
- 102000014654 Aromatase Human genes 0.000 description 1
- 108010078554 Aromatase Proteins 0.000 description 1
- 206010003445 Ascites Diseases 0.000 description 1
- 108010011485 Aspartame Proteins 0.000 description 1
- 208000032791 BCR-ABL1 positive chronic myelogenous leukemia Diseases 0.000 description 1
- OLCWFLWEHWLBTO-HSZRJFAPSA-N BMS-214662 Chemical compound C=1C=CSC=1S(=O)(=O)N([C@@H](C1)CC=2C=CC=CC=2)CC2=CC(C#N)=CC=C2N1CC1=CN=CN1 OLCWFLWEHWLBTO-HSZRJFAPSA-N 0.000 description 1
- 241000894006 Bacteria Species 0.000 description 1
- DWRXFEITVBNRMK-UHFFFAOYSA-N Beta-D-1-Arabinofuranosylthymine Natural products O=C1NC(=O)C(C)=CN1C1C(O)C(O)C(CO)O1 DWRXFEITVBNRMK-UHFFFAOYSA-N 0.000 description 1
- 206010065553 Bone marrow failure Diseases 0.000 description 1
- 241000167854 Bourreria succulenta Species 0.000 description 1
- 206010006895 Cachexia Diseases 0.000 description 1
- 208000034598 Caecitis Diseases 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- 201000009030 Carcinoma Diseases 0.000 description 1
- 206010048610 Cardiotoxicity Diseases 0.000 description 1
- 201000003883 Cystic fibrosis Diseases 0.000 description 1
- UHDGCWIWMRVCDJ-CCXZUQQUSA-N Cytarabine Chemical compound O=C1N=C(N)C=CN1[C@H]1[C@@H](O)[C@H](O)[C@@H](CO)O1 UHDGCWIWMRVCDJ-CCXZUQQUSA-N 0.000 description 1
- 102000004127 Cytokines Human genes 0.000 description 1
- 108090000695 Cytokines Proteins 0.000 description 1
- 230000000970 DNA cross-linking effect Effects 0.000 description 1
- 230000004543 DNA replication Effects 0.000 description 1
- 230000006820 DNA synthesis Effects 0.000 description 1
- 229940123780 DNA topoisomerase I inhibitor Drugs 0.000 description 1
- 229940124087 DNA topoisomerase II inhibitor Drugs 0.000 description 1
- WEAHRLBPCANXCN-UHFFFAOYSA-N Daunomycin Natural products CCC1(O)CC(OC2CC(N)C(O)C(C)O2)c3cc4C(=O)c5c(OC)cccc5C(=O)c4c(O)c3C1 WEAHRLBPCANXCN-UHFFFAOYSA-N 0.000 description 1
- 235000019739 Dicalciumphosphate Nutrition 0.000 description 1
- 206010061818 Disease progression Diseases 0.000 description 1
- 208000037162 Ductal Breast Carcinoma Diseases 0.000 description 1
- LVGKNOAMLMIIKO-UHFFFAOYSA-N Elaidinsaeure-aethylester Natural products CCCCCCCCC=CCCCCCCCC(=O)OCC LVGKNOAMLMIIKO-UHFFFAOYSA-N 0.000 description 1
- 101710146739 Enterotoxin Proteins 0.000 description 1
- 229940102550 Estrogen receptor antagonist Drugs 0.000 description 1
- 239000001856 Ethyl cellulose Substances 0.000 description 1
- ZZSNKZQZMQGXPY-UHFFFAOYSA-N Ethyl cellulose Chemical compound CCOCC1OC(OC)C(OCC)C(OCC)C1OC1C(O)C(O)C(OC)C(CO)O1 ZZSNKZQZMQGXPY-UHFFFAOYSA-N 0.000 description 1
- 206010063599 Exposure to chemical pollution Diseases 0.000 description 1
- 241000282326 Felis catus Species 0.000 description 1
- 208000010412 Glaucoma Diseases 0.000 description 1
- 208000032612 Glial tumor Diseases 0.000 description 1
- 206010068601 Glioneuronal tumour Diseases 0.000 description 1
- 108010068370 Glutens Proteins 0.000 description 1
- 244000148687 Glycosmis pentaphylla Species 0.000 description 1
- UYTPUPDQBNUYGX-UHFFFAOYSA-N Guanine Natural products O=C1NC(N)=NC2=C1N=CN2 UYTPUPDQBNUYGX-UHFFFAOYSA-N 0.000 description 1
- 238000010268 HPLC based assay Methods 0.000 description 1
- 241000243974 Haemonchus contortus Species 0.000 description 1
- 208000002250 Hematologic Neoplasms Diseases 0.000 description 1
- 101001012157 Homo sapiens Receptor tyrosine-protein kinase erbB-2 Proteins 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- 206010062016 Immunosuppression Diseases 0.000 description 1
- 108010050904 Interferons Proteins 0.000 description 1
- 102000014150 Interferons Human genes 0.000 description 1
- 102000013462 Interleukin-12 Human genes 0.000 description 1
- 108010065805 Interleukin-12 Proteins 0.000 description 1
- 102000000588 Interleukin-2 Human genes 0.000 description 1
- 108010002350 Interleukin-2 Proteins 0.000 description 1
- 102000000704 Interleukin-7 Human genes 0.000 description 1
- 108010002586 Interleukin-7 Proteins 0.000 description 1
- FBOZXECLQNJBKD-ZDUSSCGKSA-N L-methotrexate Chemical compound C=1N=C2N=C(N)N=C(N)C2=NC=1CN(C)C1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 FBOZXECLQNJBKD-ZDUSSCGKSA-N 0.000 description 1
- 239000005411 L01XE02 - Gefitinib Substances 0.000 description 1
- 239000005551 L01XE03 - Erlotinib Substances 0.000 description 1
- 239000004166 Lanolin Substances 0.000 description 1
- CERQOIWHTDAKMF-UHFFFAOYSA-N Methacrylic acid Chemical compound CC(=C)C(O)=O CERQOIWHTDAKMF-UHFFFAOYSA-N 0.000 description 1
- 229940121849 Mitotic inhibitor Drugs 0.000 description 1
- 229920000715 Mucilage Polymers 0.000 description 1
- 238000007126 N-alkylation reaction Methods 0.000 description 1
- 150000001204 N-oxides Chemical class 0.000 description 1
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 description 1
- 239000005642 Oleic acid Substances 0.000 description 1
- ZQPPMHVWECSIRJ-UHFFFAOYSA-N Oleic acid Natural products CCCCCCCCC=CCCCCCCCC(O)=O ZQPPMHVWECSIRJ-UHFFFAOYSA-N 0.000 description 1
- 201000010133 Oligodendroglioma Diseases 0.000 description 1
- 206010061328 Ovarian epithelial cancer Diseases 0.000 description 1
- 108091000080 Phosphotransferase Proteins 0.000 description 1
- 229920000776 Poly(Adenosine diphosphate-ribose) polymerase Polymers 0.000 description 1
- 229920001214 Polysorbate 60 Polymers 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- 102000004022 Protein-Tyrosine Kinases Human genes 0.000 description 1
- 108090000412 Protein-Tyrosine Kinases Proteins 0.000 description 1
- CZPWVGJYEJSRLH-UHFFFAOYSA-N Pyrimidine Chemical compound C1=CN=CN=C1 CZPWVGJYEJSRLH-UHFFFAOYSA-N 0.000 description 1
- 102100030086 Receptor tyrosine-protein kinase erbB-2 Human genes 0.000 description 1
- 229940123934 Reductase inhibitor Drugs 0.000 description 1
- 240000007651 Rubus glaucus Species 0.000 description 1
- 235000011034 Rubus glaucus Nutrition 0.000 description 1
- 235000009122 Rubus idaeus Nutrition 0.000 description 1
- 241000282849 Ruminantia Species 0.000 description 1
- 229920001800 Shellac Polymers 0.000 description 1
- DWAQJAXMDSEUJJ-UHFFFAOYSA-M Sodium bisulfite Chemical compound [Na+].OS([O-])=O DWAQJAXMDSEUJJ-UHFFFAOYSA-M 0.000 description 1
- BCKXLBQYZLBQEK-KVVVOXFISA-M Sodium oleate Chemical compound [Na+].CCCCCCCC\C=C/CCCCCCCC([O-])=O BCKXLBQYZLBQEK-KVVVOXFISA-M 0.000 description 1
- 206010068771 Soft tissue neoplasm Diseases 0.000 description 1
- 208000021712 Soft tissue sarcoma Diseases 0.000 description 1
- 238000007059 Strecker synthesis reaction Methods 0.000 description 1
- 101710172711 Structural protein Proteins 0.000 description 1
- 238000003639 Student–Newman–Keuls (SNK) method Methods 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 1
- 235000019486 Sunflower oil Nutrition 0.000 description 1
- 206010043275 Teratogenicity Diseases 0.000 description 1
- 102000002689 Toll-like receptor Human genes 0.000 description 1
- 108020000411 Toll-like receptor Proteins 0.000 description 1
- IVTVGDXNLFLDRM-HNNXBMFYSA-N Tomudex Chemical compound C=1C=C2NC(C)=NC(=O)C2=CC=1CN(C)C1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)S1 IVTVGDXNLFLDRM-HNNXBMFYSA-N 0.000 description 1
- 239000000365 Topoisomerase I Inhibitor Substances 0.000 description 1
- 239000000317 Topoisomerase II Inhibitor Substances 0.000 description 1
- 206010045170 Tumour lysis syndrome Diseases 0.000 description 1
- 102000007537 Type II DNA Topoisomerases Human genes 0.000 description 1
- 108010046308 Type II DNA Topoisomerases Proteins 0.000 description 1
- 208000004387 Typhlitis Diseases 0.000 description 1
- 229940122803 Vinca alkaloid Drugs 0.000 description 1
- 229930003427 Vitamin E Natural products 0.000 description 1
- 206010047700 Vomiting Diseases 0.000 description 1
- 240000008042 Zea mays Species 0.000 description 1
- 229920002494 Zein Polymers 0.000 description 1
- UZQJVUCHXGYFLQ-AYDHOLPZSA-N [(2s,3r,4s,5r,6r)-4-[(2s,3r,4s,5r,6r)-4-[(2r,3r,4s,5r,6r)-4-[(2s,3r,4s,5r,6r)-3,5-dihydroxy-6-(hydroxymethyl)-4-[(2s,3r,4s,5s,6r)-3,4,5-trihydroxy-6-(hydroxymethyl)oxan-2-yl]oxyoxan-2-yl]oxy-3,5-dihydroxy-6-(hydroxymethyl)oxan-2-yl]oxy-3,5-dihydroxy-6-(hy Chemical compound O([C@H]1[C@H](O)[C@@H](CO)O[C@H]([C@@H]1O)O[C@H]1[C@H](O)[C@@H](CO)O[C@H]([C@@H]1O)O[C@H]1CC[C@]2(C)[C@H]3CC=C4[C@@]([C@@]3(CC[C@H]2[C@@]1(C=O)C)C)(C)CC(O)[C@]1(CCC(CC14)(C)C)C(=O)O[C@H]1[C@@H]([C@@H](O[C@H]2[C@@H]([C@@H](O[C@H]3[C@@H]([C@@H](O[C@H]4[C@@H]([C@@H](O[C@H]5[C@@H]([C@@H](O)[C@H](O)[C@@H](CO)O5)O)[C@H](O)[C@@H](CO)O4)O)[C@H](O)[C@@H](CO)O3)O)[C@H](O)[C@@H](CO)O2)O)[C@H](O)[C@@H](CO)O1)O)[C@@H]1O[C@H](CO)[C@@H](O)[C@H](O)[C@H]1O UZQJVUCHXGYFLQ-AYDHOLPZSA-N 0.000 description 1
- 206010000059 abdominal discomfort Diseases 0.000 description 1
- GZOSMCIZMLWJML-VJLLXTKPSA-N abiraterone Chemical compound C([C@H]1[C@H]2[C@@H]([C@]3(CC[C@H](O)CC3=CC2)C)CC[C@@]11C)C=C1C1=CC=CN=C1 GZOSMCIZMLWJML-VJLLXTKPSA-N 0.000 description 1
- 229960000853 abiraterone Drugs 0.000 description 1
- 235000010489 acacia gum Nutrition 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 230000010933 acylation Effects 0.000 description 1
- 238000005917 acylation reaction Methods 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 208000009956 adenocarcinoma Diseases 0.000 description 1
- 239000000853 adhesive Substances 0.000 description 1
- 238000009098 adjuvant therapy Methods 0.000 description 1
- 229940009456 adriamycin Drugs 0.000 description 1
- 201000007348 adult fibrosarcoma Diseases 0.000 description 1
- TXUZVZSFRXZGTL-QPLCGJKRSA-N afimoxifene Chemical compound C=1C=CC=CC=1C(/CC)=C(C=1C=CC(OCCN(C)C)=CC=1)/C1=CC=C(O)C=C1 TXUZVZSFRXZGTL-QPLCGJKRSA-N 0.000 description 1
- 229940023476 agar Drugs 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 239000000783 alginic acid Substances 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 229960001126 alginic acid Drugs 0.000 description 1
- 150000004781 alginic acids Chemical class 0.000 description 1
- 125000001931 aliphatic group Chemical group 0.000 description 1
- 125000004414 alkyl thio group Chemical group 0.000 description 1
- 229940100198 alkylating agent Drugs 0.000 description 1
- 239000002168 alkylating agent Substances 0.000 description 1
- 230000029936 alkylation Effects 0.000 description 1
- 238000005804 alkylation reaction Methods 0.000 description 1
- 239000008168 almond oil Substances 0.000 description 1
- 229940087168 alpha tocopherol Drugs 0.000 description 1
- BJEPYKJPYRNKOW-UHFFFAOYSA-N alpha-hydroxysuccinic acid Natural products OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 1
- 229940037003 alum Drugs 0.000 description 1
- AZDRQVAHHNSJOQ-UHFFFAOYSA-N alumane Chemical class [AlH3] AZDRQVAHHNSJOQ-UHFFFAOYSA-N 0.000 description 1
- WNROFYMDJYEPJX-UHFFFAOYSA-K aluminium hydroxide Chemical compound [OH-].[OH-].[OH-].[Al+3] WNROFYMDJYEPJX-UHFFFAOYSA-K 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 235000012211 aluminium silicate Nutrition 0.000 description 1
- 229940024545 aluminum hydroxide Drugs 0.000 description 1
- 229940024546 aluminum hydroxide gel Drugs 0.000 description 1
- SMYKVLBUSSNXMV-UHFFFAOYSA-K aluminum;trihydroxide;hydrate Chemical compound O.[OH-].[OH-].[OH-].[Al+3] SMYKVLBUSSNXMV-UHFFFAOYSA-K 0.000 description 1
- 150000001408 amides Chemical group 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 235000011114 ammonium hydroxide Nutrition 0.000 description 1
- 238000009167 androgen deprivation therapy Methods 0.000 description 1
- 208000007502 anemia Diseases 0.000 description 1
- 125000000129 anionic group Chemical group 0.000 description 1
- 239000003945 anionic surfactant Substances 0.000 description 1
- 230000000507 anthelmentic effect Effects 0.000 description 1
- 229940124339 anthelmintic agent Drugs 0.000 description 1
- 239000000921 anthelmintic agent Substances 0.000 description 1
- 239000003817 anthracycline antibiotic agent Substances 0.000 description 1
- 229940045799 anthracyclines and related substance Drugs 0.000 description 1
- 230000002280 anti-androgenic effect Effects 0.000 description 1
- 230000003527 anti-angiogenesis Effects 0.000 description 1
- 230000001028 anti-proliverative effect Effects 0.000 description 1
- 239000000051 antiandrogen Substances 0.000 description 1
- 238000011319 anticancer therapy Methods 0.000 description 1
- 238000011394 anticancer treatment Methods 0.000 description 1
- 229940045719 antineoplastic alkylating agent nitrosoureas Drugs 0.000 description 1
- 238000003782 apoptosis assay Methods 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 239000010425 asbestos Substances 0.000 description 1
- 235000010323 ascorbic acid Nutrition 0.000 description 1
- 229960005070 ascorbic acid Drugs 0.000 description 1
- 239000011668 ascorbic acid Substances 0.000 description 1
- IAOZJIPTCAWIRG-QWRGUYRKSA-N aspartame Chemical compound OC(=O)C[C@H](N)C(=O)N[C@H](C(=O)OC)CC1=CC=CC=C1 IAOZJIPTCAWIRG-QWRGUYRKSA-N 0.000 description 1
- 239000000605 aspartame Substances 0.000 description 1
- 235000010357 aspartame Nutrition 0.000 description 1
- 229960003438 aspartame Drugs 0.000 description 1
- 239000000305 astragalus gummifer gum Substances 0.000 description 1
- 125000004429 atom Chemical group 0.000 description 1
- 102000004441 bcr-abl Fusion Proteins Human genes 0.000 description 1
- 108010056708 bcr-abl Fusion Proteins Proteins 0.000 description 1
- 235000013871 bee wax Nutrition 0.000 description 1
- 239000012166 beeswax Substances 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 239000000440 bentonite Substances 0.000 description 1
- 229910000278 bentonite Inorganic materials 0.000 description 1
- 229940092782 bentonite Drugs 0.000 description 1
- 235000012216 bentonite Nutrition 0.000 description 1
- SVPXDRXYRYOSEX-UHFFFAOYSA-N bentoquatam Chemical compound O.O=[Si]=O.O=[Al]O[Al]=O SVPXDRXYRYOSEX-UHFFFAOYSA-N 0.000 description 1
- 229960000686 benzalkonium chloride Drugs 0.000 description 1
- 125000003785 benzimidazolyl group Chemical group N1=C(NC2=C1C=CC=C2)* 0.000 description 1
- 125000000499 benzofuranyl group Chemical group O1C(=CC2=C1C=CC=C2)* 0.000 description 1
- 125000004601 benzofurazanyl group Chemical group N1=C2C(=NO1)C(=CC=C2)* 0.000 description 1
- 125000001164 benzothiazolyl group Chemical group S1C(=NC2=C1C=CC=C2)* 0.000 description 1
- 125000004541 benzoxazolyl group Chemical group O1C(=NC2=C1C=CC=C2)* 0.000 description 1
- 125000004599 benzpyrazolyl group Chemical group N1N=C(C2=C1C=CC=C2)* 0.000 description 1
- CADWTSSKOVRVJC-UHFFFAOYSA-N benzyl(dimethyl)azanium;chloride Chemical compound [Cl-].C[NH+](C)CC1=CC=CC=C1 CADWTSSKOVRVJC-UHFFFAOYSA-N 0.000 description 1
- IQFYYKKMVGJFEH-UHFFFAOYSA-N beta-L-thymidine Natural products O=C1NC(=O)C(C)=CN1C1OC(CO)C(O)C1 IQFYYKKMVGJFEH-UHFFFAOYSA-N 0.000 description 1
- 238000004166 bioassay Methods 0.000 description 1
- 239000000090 biomarker Substances 0.000 description 1
- 230000000903 blocking effect Effects 0.000 description 1
- 210000001185 bone marrow Anatomy 0.000 description 1
- 210000004556 brain Anatomy 0.000 description 1
- 210000005013 brain tissue Anatomy 0.000 description 1
- 201000008275 breast carcinoma Diseases 0.000 description 1
- 125000001246 bromo group Chemical group Br* 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 239000006172 buffering agent Substances 0.000 description 1
- 235000019437 butane-1,3-diol Nutrition 0.000 description 1
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 229910000019 calcium carbonate Inorganic materials 0.000 description 1
- 235000010216 calcium carbonate Nutrition 0.000 description 1
- 239000001506 calcium phosphate Substances 0.000 description 1
- 239000000378 calcium silicate Substances 0.000 description 1
- 229910052918 calcium silicate Inorganic materials 0.000 description 1
- 235000012241 calcium silicate Nutrition 0.000 description 1
- OYACROKNLOSFPA-UHFFFAOYSA-N calcium;dioxido(oxo)silane Chemical compound [Ca+2].[O-][Si]([O-])=O OYACROKNLOSFPA-UHFFFAOYSA-N 0.000 description 1
- 239000012830 cancer therapeutic Substances 0.000 description 1
- 239000007894 caplet Substances 0.000 description 1
- 125000000609 carbazolyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3NC12)* 0.000 description 1
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 description 1
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 1
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 1
- 239000008112 carboxymethyl-cellulose Substances 0.000 description 1
- 229940105329 carboxymethylcellulose Drugs 0.000 description 1
- 231100000504 carcinogenesis Toxicity 0.000 description 1
- 231100000259 cardiotoxicity Toxicity 0.000 description 1
- 125000002091 cationic group Chemical group 0.000 description 1
- 239000003093 cationic surfactant Substances 0.000 description 1
- 230000012820 cell cycle checkpoint Effects 0.000 description 1
- 230000030833 cell death Effects 0.000 description 1
- 238000003570 cell viability assay Methods 0.000 description 1
- 210000003679 cervix uteri Anatomy 0.000 description 1
- 238000001311 chemical methods and process Methods 0.000 description 1
- 238000007385 chemical modification Methods 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 239000012829 chemotherapy agent Substances 0.000 description 1
- 235000019693 cherries Nutrition 0.000 description 1
- 238000004296 chiral HPLC Methods 0.000 description 1
- 229960002152 chlorhexidine acetate Drugs 0.000 description 1
- BULLHNJGPPOUOX-UHFFFAOYSA-N chloroacetone Chemical compound CC(=O)CCl BULLHNJGPPOUOX-UHFFFAOYSA-N 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- 125000004230 chromenyl group Chemical group O1C(C=CC2=CC=CC=C12)* 0.000 description 1
- 230000001684 chronic effect Effects 0.000 description 1
- 125000000259 cinnolinyl group Chemical group N1=NC(=CC2=CC=CC=C12)* 0.000 description 1
- 235000015165 citric acid Nutrition 0.000 description 1
- 201000010897 colon adenocarcinoma Diseases 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 238000002648 combination therapy Methods 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 229920001577 copolymer Polymers 0.000 description 1
- 238000007821 culture assay Methods 0.000 description 1
- 230000001120 cytoprotective effect Effects 0.000 description 1
- 210000004292 cytoskeleton Anatomy 0.000 description 1
- 239000000824 cytostatic agent Substances 0.000 description 1
- 238000011393 cytotoxic chemotherapy Methods 0.000 description 1
- VUIKXKJIWVOSMF-GHTOIXBYSA-N d(CG)12 Chemical group O=C1N=C(N)C=CN1[C@@H]1O[C@H](CO)[C@@H](OP(O)(=O)OC[C@@H]2[C@H](C[C@@H](O2)N2C3=C(C(NC(N)=N3)=O)N=C2)OP(O)(=O)OC[C@@H]2[C@H](C[C@@H](O2)N2C(N=C(N)C=C2)=O)OP(O)(=O)OC[C@@H]2[C@H](C[C@@H](O2)N2C3=C(C(NC(N)=N3)=O)N=C2)OP(O)(=O)OC[C@@H]2[C@H](C[C@@H](O2)N2C(N=C(N)C=C2)=O)OP(O)(=O)OC[C@@H]2[C@H](C[C@@H](O2)N2C3=C(C(NC(N)=N3)=O)N=C2)OP(O)(=O)OC[C@@H]2[C@H](C[C@@H](O2)N2C(N=C(N)C=C2)=O)OP(O)(=O)OC[C@@H]2[C@H](C[C@@H](O2)N2C3=C(C(NC(N)=N3)=O)N=C2)OP(O)(=O)OC[C@@H]2[C@H](C[C@@H](O2)N2C(N=C(N)C=C2)=O)OP(O)(=O)OC[C@@H]2[C@H](C[C@@H](O2)N2C3=C(C(NC(N)=N3)=O)N=C2)OP(O)(=O)OC[C@@H]2[C@H](C[C@@H](O2)N2C(N=C(N)C=C2)=O)OP(O)(=O)OC[C@@H]2[C@H](C[C@@H](O2)N2C3=C(C(NC(N)=N3)=O)N=C2)OP(O)(=O)OC[C@@H]2[C@H](C[C@@H](O2)N2C(N=C(N)C=C2)=O)OP(O)(=O)OC[C@@H]2[C@H](C[C@@H](O2)N2C3=C(C(NC(N)=N3)=O)N=C2)OP(O)(=O)OC[C@@H]2[C@H](C[C@@H](O2)N2C(N=C(N)C=C2)=O)OP(O)(=O)OC[C@@H]2[C@H](C[C@@H](O2)N2C3=C(C(NC(N)=N3)=O)N=C2)OP(O)(=O)OC[C@@H]2[C@H](C[C@@H](O2)N2C(N=C(N)C=C2)=O)OP(O)(=O)OC[C@@H]2[C@H](C[C@@H](O2)N2C3=C(C(NC(N)=N3)=O)N=C2)OP(O)(=O)OC[C@@H]2[C@H](C[C@@H](O2)N2C(N=C(N)C=C2)=O)OP(O)(=O)OC[C@@H]2[C@H](C[C@@H](O2)N2C3=C(C(NC(N)=N3)=O)N=C2)OP(O)(=O)OC[C@@H]2[C@H](C[C@@H](O2)N2C(N=C(N)C=C2)=O)OP(O)(=O)OC[C@@H]2[C@H](C[C@@H](O2)N2C3=C(C(NC(N)=N3)=O)N=C2)OP(O)(=O)OC[C@@H]2[C@H](C[C@@H](O2)N2C(N=C(N)C=C2)=O)OP(O)(=O)OC[C@@H]2[C@H](C[C@@H](O2)N2C3=C(C(NC(N)=N3)=O)N=C2)O)C1 VUIKXKJIWVOSMF-GHTOIXBYSA-N 0.000 description 1
- STQGQHZAVUOBTE-VGBVRHCVSA-N daunorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(C)=O)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 STQGQHZAVUOBTE-VGBVRHCVSA-N 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 230000007547 defect Effects 0.000 description 1
- 230000003111 delayed effect Effects 0.000 description 1
- 230000002939 deleterious effect Effects 0.000 description 1
- 238000001212 derivatisation Methods 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 238000002405 diagnostic procedure Methods 0.000 description 1
- NEFBYIFKOOEVPA-UHFFFAOYSA-K dicalcium phosphate Chemical compound [Ca+2].[Ca+2].[O-]P([O-])([O-])=O NEFBYIFKOOEVPA-UHFFFAOYSA-K 0.000 description 1
- 229940038472 dicalcium phosphate Drugs 0.000 description 1
- 229910000390 dicalcium phosphate Inorganic materials 0.000 description 1
- 230000004069 differentiation Effects 0.000 description 1
- 239000000539 dimer Substances 0.000 description 1
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 1
- 230000005750 disease progression Effects 0.000 description 1
- 238000002224 dissection Methods 0.000 description 1
- 239000012153 distilled water Substances 0.000 description 1
- 229940115080 doxil Drugs 0.000 description 1
- 229960003722 doxycycline Drugs 0.000 description 1
- XQTWDDCIUJNLTR-CVHRZJFOSA-N doxycycline monohydrate Chemical compound O.O=C1C2=C(O)C=CC=C2[C@H](C)[C@@H]2C1=C(O)[C@]1(O)C(=O)C(C(N)=O)=C(O)[C@@H](N(C)C)[C@@H]1[C@H]2O XQTWDDCIUJNLTR-CVHRZJFOSA-N 0.000 description 1
- 238000012377 drug delivery Methods 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 210000005069 ears Anatomy 0.000 description 1
- 230000008030 elimination Effects 0.000 description 1
- 238000003379 elimination reaction Methods 0.000 description 1
- 239000003974 emollient agent Substances 0.000 description 1
- 230000002124 endocrine Effects 0.000 description 1
- 210000004696 endometrium Anatomy 0.000 description 1
- 210000002889 endothelial cell Anatomy 0.000 description 1
- 230000003511 endothelial effect Effects 0.000 description 1
- 239000000147 enterotoxin Substances 0.000 description 1
- 231100000655 enterotoxin Toxicity 0.000 description 1
- 210000002919 epithelial cell Anatomy 0.000 description 1
- 229930013356 epothilone Natural products 0.000 description 1
- HESCAJZNRMSMJG-KKQRBIROSA-N epothilone A Chemical class C/C([C@@H]1C[C@@H]2O[C@@H]2CCC[C@@H]([C@@H]([C@@H](C)C(=O)C(C)(C)[C@@H](O)CC(=O)O1)O)C)=C\C1=CSC(C)=N1 HESCAJZNRMSMJG-KKQRBIROSA-N 0.000 description 1
- AAKJLRGGTJKAMG-UHFFFAOYSA-N erlotinib Chemical compound C=12C=C(OCCOC)C(OCCOC)=CC2=NC=NC=1NC1=CC=CC(C#C)=C1 AAKJLRGGTJKAMG-UHFFFAOYSA-N 0.000 description 1
- 229940011871 estrogen Drugs 0.000 description 1
- 239000000262 estrogen Substances 0.000 description 1
- 235000019325 ethyl cellulose Nutrition 0.000 description 1
- 229920001249 ethyl cellulose Polymers 0.000 description 1
- LVGKNOAMLMIIKO-QXMHVHEDSA-N ethyl oleate Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OCC LVGKNOAMLMIIKO-QXMHVHEDSA-N 0.000 description 1
- 229940093471 ethyl oleate Drugs 0.000 description 1
- 239000003889 eye drop Substances 0.000 description 1
- 229940012356 eye drops Drugs 0.000 description 1
- 235000013861 fat-free Nutrition 0.000 description 1
- 201000010255 female reproductive organ cancer Diseases 0.000 description 1
- 235000019634 flavors Nutrition 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- 238000001640 fractional crystallisation Methods 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- 235000011087 fumaric acid Nutrition 0.000 description 1
- 125000002541 furyl group Chemical group 0.000 description 1
- WIGCFUFOHFEKBI-UHFFFAOYSA-N gamma-tocopherol Natural products CC(C)CCCC(C)CCCC(C)CCCC1CCC2C(C)C(O)C(C)C(C)C2O1 WIGCFUFOHFEKBI-UHFFFAOYSA-N 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 230000002496 gastric effect Effects 0.000 description 1
- 244000000050 gastrointestinal parasite Species 0.000 description 1
- XGALLCVXEZPNRQ-UHFFFAOYSA-N gefitinib Chemical compound C=12C=C(OCCCN3CCOCC3)C(OC)=CC2=NC=NC=1NC1=CC=C(F)C(Cl)=C1 XGALLCVXEZPNRQ-UHFFFAOYSA-N 0.000 description 1
- 208000002409 gliosarcoma Diseases 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 235000001727 glucose Nutrition 0.000 description 1
- 235000021312 gluten Nutrition 0.000 description 1
- ZEMPKEQAKRGZGQ-XOQCFJPHSA-N glycerol triricinoleate Natural products CCCCCC[C@@H](O)CC=CCCCCCCCC(=O)OC[C@@H](COC(=O)CCCCCCCC=CC[C@@H](O)CCCCCC)OC(=O)CCCCCCCC=CC[C@H](O)CCCCCC ZEMPKEQAKRGZGQ-XOQCFJPHSA-N 0.000 description 1
- 229940074045 glyceryl distearate Drugs 0.000 description 1
- 229940075529 glyceryl stearate Drugs 0.000 description 1
- 229960001269 glycine hydrochloride Drugs 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 239000003102 growth factor Substances 0.000 description 1
- 239000001963 growth medium Substances 0.000 description 1
- 229940093915 gynecological organic acid Drugs 0.000 description 1
- 208000024963 hair loss Diseases 0.000 description 1
- 230000003676 hair loss Effects 0.000 description 1
- 125000005843 halogen group Chemical group 0.000 description 1
- 230000003862 health status Effects 0.000 description 1
- 208000019622 heart disease Diseases 0.000 description 1
- 230000002440 hepatic effect Effects 0.000 description 1
- 208000002672 hepatitis B Diseases 0.000 description 1
- 229940022353 herceptin Drugs 0.000 description 1
- 125000000623 heterocyclic group Chemical group 0.000 description 1
- 230000002962 histologic effect Effects 0.000 description 1
- 229940125697 hormonal agent Drugs 0.000 description 1
- 208000027706 hormone receptor-positive breast cancer Diseases 0.000 description 1
- 238000001794 hormone therapy Methods 0.000 description 1
- 210000005260 human cell Anatomy 0.000 description 1
- 239000003906 humectant Substances 0.000 description 1
- 229930195733 hydrocarbon Natural products 0.000 description 1
- 150000002430 hydrocarbons Chemical class 0.000 description 1
- 229910052739 hydrogen Inorganic materials 0.000 description 1
- XMBWDFGMSWQBCA-UHFFFAOYSA-N hydrogen iodide Chemical compound I XMBWDFGMSWQBCA-UHFFFAOYSA-N 0.000 description 1
- 229940071870 hydroiodic acid Drugs 0.000 description 1
- 230000003301 hydrolyzing effect Effects 0.000 description 1
- HOMGKSMUEGBAAB-UHFFFAOYSA-N ifosfamide Chemical compound ClCCNP1(=O)OCCCN1CCCl HOMGKSMUEGBAAB-UHFFFAOYSA-N 0.000 description 1
- YLMAHDNUQAMNNX-UHFFFAOYSA-N imatinib methanesulfonate Chemical compound CS(O)(=O)=O.C1CN(C)CCN1CC1=CC=C(C(=O)NC=2C=C(NC=3N=C(C=CN=3)C=3C=NC=CC=3)C(C)=CC=2)C=C1 YLMAHDNUQAMNNX-UHFFFAOYSA-N 0.000 description 1
- 230000002163 immunogen Effects 0.000 description 1
- 239000000367 immunologic factor Substances 0.000 description 1
- 230000001506 immunosuppresive effect Effects 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 125000003392 indanyl group Chemical group C1(CCC2=CC=CC=C12)* 0.000 description 1
- 125000003453 indazolyl group Chemical group N1N=C(C2=C1C=CC=C2)* 0.000 description 1
- 125000003387 indolinyl group Chemical group N1(CCC2=CC=CC=C12)* 0.000 description 1
- 125000001041 indolyl group Chemical group 0.000 description 1
- 208000000509 infertility Diseases 0.000 description 1
- 230000036512 infertility Effects 0.000 description 1
- 231100000535 infertility Toxicity 0.000 description 1
- 229940102223 injectable solution Drugs 0.000 description 1
- 229940102213 injectable suspension Drugs 0.000 description 1
- 150000007529 inorganic bases Chemical class 0.000 description 1
- 229910010272 inorganic material Inorganic materials 0.000 description 1
- 239000011147 inorganic material Substances 0.000 description 1
- 229940047124 interferons Drugs 0.000 description 1
- 210000004347 intestinal mucosa Anatomy 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 238000010253 intravenous injection Methods 0.000 description 1
- 238000011835 investigation Methods 0.000 description 1
- 125000002346 iodo group Chemical group I* 0.000 description 1
- 229940084651 iressa Drugs 0.000 description 1
- 229910052742 iron Inorganic materials 0.000 description 1
- 230000002427 irreversible effect Effects 0.000 description 1
- 125000001977 isobenzofuranyl group Chemical group C=1(OC=C2C=CC=CC12)* 0.000 description 1
- 125000000904 isoindolyl group Chemical group C=1(NC=C2C=CC=CC12)* 0.000 description 1
- QXJSBBXBKPUZAA-UHFFFAOYSA-N isooleic acid Natural products CCCCCCCC=CCCCCCCCCC(O)=O QXJSBBXBKPUZAA-UHFFFAOYSA-N 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- XUGNVMKQXJXZCD-UHFFFAOYSA-N isopropyl palmitate Chemical compound CCCCCCCCCCCCCCCC(=O)OC(C)C XUGNVMKQXJXZCD-UHFFFAOYSA-N 0.000 description 1
- 125000005956 isoquinolyl group Chemical group 0.000 description 1
- 125000001786 isothiazolyl group Chemical group 0.000 description 1
- 125000000842 isoxazolyl group Chemical group 0.000 description 1
- NLYAJNPCOHFWQQ-UHFFFAOYSA-N kaolin Chemical compound O.O.O=[Al]O[Si](=O)O[Si](=O)O[Al]=O NLYAJNPCOHFWQQ-UHFFFAOYSA-N 0.000 description 1
- 229940043355 kinase inhibitor Drugs 0.000 description 1
- 239000004310 lactic acid Substances 0.000 description 1
- 235000014655 lactic acid Nutrition 0.000 description 1
- 229960001375 lactose Drugs 0.000 description 1
- 235000019388 lanolin Nutrition 0.000 description 1
- 229940039717 lanolin Drugs 0.000 description 1
- 230000003902 lesion Effects 0.000 description 1
- 231100000636 lethal dose Toxicity 0.000 description 1
- 239000003446 ligand Substances 0.000 description 1
- 210000005228 liver tissue Anatomy 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 231100000053 low toxicity Toxicity 0.000 description 1
- 210000004072 lung Anatomy 0.000 description 1
- ZLNQQNXFFQJAID-UHFFFAOYSA-L magnesium carbonate Chemical compound [Mg+2].[O-]C([O-])=O ZLNQQNXFFQJAID-UHFFFAOYSA-L 0.000 description 1
- 239000001095 magnesium carbonate Substances 0.000 description 1
- 229910000021 magnesium carbonate Inorganic materials 0.000 description 1
- 235000014380 magnesium carbonate Nutrition 0.000 description 1
- 239000001630 malic acid Substances 0.000 description 1
- 235000011090 malic acid Nutrition 0.000 description 1
- 208000006178 malignant mesothelioma Diseases 0.000 description 1
- 201000005282 malignant pleural mesothelioma Diseases 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 230000010534 mechanism of action Effects 0.000 description 1
- 230000001404 mediated effect Effects 0.000 description 1
- 239000001525 mentha piperita l. herb oil Substances 0.000 description 1
- 201000008806 mesenchymal cell neoplasm Diseases 0.000 description 1
- 230000002503 metabolic effect Effects 0.000 description 1
- 230000031864 metaphase Effects 0.000 description 1
- 229940098779 methanesulfonic acid Drugs 0.000 description 1
- 229960000485 methotrexate Drugs 0.000 description 1
- 239000004292 methyl p-hydroxybenzoate Substances 0.000 description 1
- 235000010270 methyl p-hydroxybenzoate Nutrition 0.000 description 1
- OSWPMRLSEDHDFF-UHFFFAOYSA-N methyl salicylate Chemical compound COC(=O)C1=CC=CC=C1O OSWPMRLSEDHDFF-UHFFFAOYSA-N 0.000 description 1
- 229960002216 methylparaben Drugs 0.000 description 1
- 239000004005 microsphere Substances 0.000 description 1
- 239000002480 mineral oil Substances 0.000 description 1
- 230000011278 mitosis Effects 0.000 description 1
- 230000000394 mitotic effect Effects 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- LNOPIUAQISRISI-UHFFFAOYSA-N n'-hydroxy-2-propan-2-ylsulfonylethanimidamide Chemical compound CC(C)S(=O)(=O)CC(N)=NO LNOPIUAQISRISI-UHFFFAOYSA-N 0.000 description 1
- JXTPJDDICSTXJX-UHFFFAOYSA-N n-Triacontane Natural products CCCCCCCCCCCCCCCCCCCCCCCCCCCCCC JXTPJDDICSTXJX-UHFFFAOYSA-N 0.000 description 1
- WTERNLDOAPYGJD-GOSISDBHSA-N n-[(2r)-2-cyano-1-[5-cyano-2-(trifluoromethyl)phenoxy]propan-2-yl]-4-(trifluoromethylsulfanyl)benzamide Chemical compound C([C@](C)(NC(=O)C=1C=CC(SC(F)(F)F)=CC=1)C#N)OC1=CC(C#N)=CC=C1C(F)(F)F WTERNLDOAPYGJD-GOSISDBHSA-N 0.000 description 1
- 125000006606 n-butoxy group Chemical group 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000001624 naphthyl group Chemical group 0.000 description 1
- 229930014626 natural product Natural products 0.000 description 1
- 230000001069 nematicidal effect Effects 0.000 description 1
- 239000005645 nematicide Substances 0.000 description 1
- 208000027831 neuroepithelial neoplasm Diseases 0.000 description 1
- 230000000926 neurological effect Effects 0.000 description 1
- 229910017604 nitric acid Inorganic materials 0.000 description 1
- 239000002736 nonionic surfactant Substances 0.000 description 1
- 210000001331 nose Anatomy 0.000 description 1
- 150000003833 nucleoside derivatives Chemical class 0.000 description 1
- 239000002773 nucleotide Substances 0.000 description 1
- 125000003729 nucleotide group Chemical group 0.000 description 1
- ZQPPMHVWECSIRJ-KTKRTIGZSA-N oleic acid Chemical compound CCCCCCCC\C=C/CCCCCCCC(O)=O ZQPPMHVWECSIRJ-KTKRTIGZSA-N 0.000 description 1
- 239000003605 opacifier Substances 0.000 description 1
- 238000005457 optimization Methods 0.000 description 1
- 210000000056 organ Anatomy 0.000 description 1
- 230000008816 organ damage Effects 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 150000007530 organic bases Chemical class 0.000 description 1
- 208000013371 ovarian adenocarcinoma Diseases 0.000 description 1
- 201000006588 ovary adenocarcinoma Diseases 0.000 description 1
- 125000001715 oxadiazolyl group Chemical group 0.000 description 1
- 235000006408 oxalic acid Nutrition 0.000 description 1
- 125000002971 oxazolyl group Chemical group 0.000 description 1
- 201000008129 pancreatic ductal adenocarcinoma Diseases 0.000 description 1
- FJKROLUGYXJWQN-UHFFFAOYSA-N papa-hydroxy-benzoic acid Natural products OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 1
- 239000012188 paraffin wax Substances 0.000 description 1
- 244000045947 parasite Species 0.000 description 1
- 244000052769 pathogen Species 0.000 description 1
- 230000001717 pathogenic effect Effects 0.000 description 1
- 230000001575 pathological effect Effects 0.000 description 1
- 230000037361 pathway Effects 0.000 description 1
- 235000020232 peanut Nutrition 0.000 description 1
- 108010092851 peginterferon alfa-2b Proteins 0.000 description 1
- 229940106366 pegintron Drugs 0.000 description 1
- 229960005079 pemetrexed Drugs 0.000 description 1
- QOFFJEBXNKRSPX-ZDUSSCGKSA-N pemetrexed Chemical compound C1=N[C]2NC(N)=NC(=O)C2=C1CCC1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 QOFFJEBXNKRSPX-ZDUSSCGKSA-N 0.000 description 1
- 230000035515 penetration Effects 0.000 description 1
- 235000019477 peppermint oil Nutrition 0.000 description 1
- 230000000737 periodic effect Effects 0.000 description 1
- 150000002989 phenols Chemical class 0.000 description 1
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 1
- PDTFCHSETJBPTR-UHFFFAOYSA-N phenylmercuric nitrate Chemical compound [O-][N+](=O)O[Hg]C1=CC=CC=C1 PDTFCHSETJBPTR-UHFFFAOYSA-N 0.000 description 1
- 210000004214 philadelphia chromosome Anatomy 0.000 description 1
- 229910052698 phosphorus Inorganic materials 0.000 description 1
- 230000000865 phosphorylative effect Effects 0.000 description 1
- 102000020233 phosphotransferase Human genes 0.000 description 1
- 239000003757 phosphotransferase inhibitor Substances 0.000 description 1
- 229940068196 placebo Drugs 0.000 description 1
- 239000000902 placebo Substances 0.000 description 1
- 229920002627 poly(phosphazenes) Polymers 0.000 description 1
- 229920001515 polyalkylene glycol Polymers 0.000 description 1
- 125000003367 polycyclic group Chemical group 0.000 description 1
- 229920000728 polyester Polymers 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 229920001451 polypropylene glycol Polymers 0.000 description 1
- 229920001282 polysaccharide Polymers 0.000 description 1
- 239000005017 polysaccharide Substances 0.000 description 1
- 150000004804 polysaccharides Chemical class 0.000 description 1
- 238000010149 post-hoc-test Methods 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 230000002335 preservative effect Effects 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- 230000037452 priming Effects 0.000 description 1
- 238000004393 prognosis Methods 0.000 description 1
- 230000005522 programmed cell death Effects 0.000 description 1
- ALDITMKAAPLVJK-UHFFFAOYSA-N prop-1-ene;hydrate Chemical group O.CC=C ALDITMKAAPLVJK-UHFFFAOYSA-N 0.000 description 1
- BDERNNFJNOPAEC-UHFFFAOYSA-N propan-1-ol Chemical compound CCCO BDERNNFJNOPAEC-UHFFFAOYSA-N 0.000 description 1
- 238000011321 prophylaxis Methods 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 239000004405 propyl p-hydroxybenzoate Substances 0.000 description 1
- 235000010232 propyl p-hydroxybenzoate Nutrition 0.000 description 1
- MCSINKKTEDDPNK-UHFFFAOYSA-N propyl propionate Chemical compound CCCOC(=O)CC MCSINKKTEDDPNK-UHFFFAOYSA-N 0.000 description 1
- 235000013772 propylene glycol Nutrition 0.000 description 1
- 229960003415 propylparaben Drugs 0.000 description 1
- 210000002307 prostate Anatomy 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 235000018102 proteins Nutrition 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 108090000623 proteins and genes Proteins 0.000 description 1
- 125000004309 pyranyl group Chemical group O1C(C=CC=C1)* 0.000 description 1
- 125000003373 pyrazinyl group Chemical group 0.000 description 1
- 125000002098 pyridazinyl group Chemical group 0.000 description 1
- 125000000168 pyrrolyl group Chemical group 0.000 description 1
- 125000001453 quaternary ammonium group Chemical group 0.000 description 1
- 125000005493 quinolyl group Chemical group 0.000 description 1
- 125000001567 quinoxalinyl group Chemical group N1=C(C=NC2=CC=CC=C12)* 0.000 description 1
- 238000007674 radiofrequency ablation Methods 0.000 description 1
- 229960004432 raltitrexed Drugs 0.000 description 1
- 229940044551 receptor antagonist Drugs 0.000 description 1
- 239000002464 receptor antagonist Substances 0.000 description 1
- 230000000306 recurrent effect Effects 0.000 description 1
- 208000016691 refractory malignant neoplasm Diseases 0.000 description 1
- 239000003340 retarding agent Substances 0.000 description 1
- 238000012770 revaccination Methods 0.000 description 1
- 229910052895 riebeckite Inorganic materials 0.000 description 1
- CVHZOJJKTDOEJC-UHFFFAOYSA-N saccharin Chemical compound C1=CC=C2C(=O)NS(=O)(=O)C2=C1 CVHZOJJKTDOEJC-UHFFFAOYSA-N 0.000 description 1
- 235000019204 saccharin Nutrition 0.000 description 1
- 229940081974 saccharin Drugs 0.000 description 1
- 239000000901 saccharin and its Na,K and Ca salt Substances 0.000 description 1
- 229960004889 salicylic acid Drugs 0.000 description 1
- 229910052594 sapphire Inorganic materials 0.000 description 1
- 239000010980 sapphire Substances 0.000 description 1
- 238000009094 second-line therapy Methods 0.000 description 1
- 208000011581 secondary neoplasm Diseases 0.000 description 1
- 229940076279 serotonin Drugs 0.000 description 1
- 208000004548 serous cystadenocarcinoma Diseases 0.000 description 1
- 239000004208 shellac Substances 0.000 description 1
- 229940113147 shellac Drugs 0.000 description 1
- 235000013874 shellac Nutrition 0.000 description 1
- ZLGIYFNHBLSMPS-ATJNOEHPSA-N shellac Chemical compound OCCCCCC(O)C(O)CCCCCCCC(O)=O.C1C23[C@H](C(O)=O)CCC2[C@](C)(CO)[C@@H]1C(C(O)=O)=C[C@@H]3O ZLGIYFNHBLSMPS-ATJNOEHPSA-N 0.000 description 1
- 230000011664 signaling Effects 0.000 description 1
- 229920002545 silicone oil Polymers 0.000 description 1
- 238000009097 single-agent therapy Methods 0.000 description 1
- 239000000344 soap Substances 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- WXMKPNITSTVMEF-UHFFFAOYSA-M sodium benzoate Chemical compound [Na+].[O-]C(=O)C1=CC=CC=C1 WXMKPNITSTVMEF-UHFFFAOYSA-M 0.000 description 1
- 239000004299 sodium benzoate Substances 0.000 description 1
- 235000010234 sodium benzoate Nutrition 0.000 description 1
- 229960003885 sodium benzoate Drugs 0.000 description 1
- 229940001607 sodium bisulfite Drugs 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 235000010267 sodium hydrogen sulphite Nutrition 0.000 description 1
- 210000004872 soft tissue Anatomy 0.000 description 1
- 239000007909 solid dosage form Substances 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 229940032094 squalane Drugs 0.000 description 1
- 238000011301 standard therapy Methods 0.000 description 1
- 238000011272 standard treatment Methods 0.000 description 1
- 230000001954 sterilising effect Effects 0.000 description 1
- 238000004659 sterilization and disinfection Methods 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 125000000547 substituted alkyl group Chemical group 0.000 description 1
- 229960004793 sucrose Drugs 0.000 description 1
- 150000008163 sugars Chemical class 0.000 description 1
- 239000002600 sunflower oil Substances 0.000 description 1
- 239000000829 suppository Substances 0.000 description 1
- 238000007910 systemic administration Methods 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 229940120982 tarceva Drugs 0.000 description 1
- 238000002626 targeted therapy Methods 0.000 description 1
- 229940063683 taxotere Drugs 0.000 description 1
- 229940061353 temodar Drugs 0.000 description 1
- 231100000211 teratogenicity Toxicity 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 125000003831 tetrazolyl group Chemical group 0.000 description 1
- 229940126585 therapeutic drug Drugs 0.000 description 1
- 125000001113 thiadiazolyl group Chemical group 0.000 description 1
- 239000002562 thickening agent Substances 0.000 description 1
- 125000001544 thienyl group Chemical group 0.000 description 1
- 229940104230 thymidine Drugs 0.000 description 1
- 239000003734 thymidylate synthase inhibitor Substances 0.000 description 1
- 229940113082 thymine Drugs 0.000 description 1
- 229960000984 tocofersolan Drugs 0.000 description 1
- 230000000699 topical effect Effects 0.000 description 1
- 239000012049 topical pharmaceutical composition Substances 0.000 description 1
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- 238000002054 transplantation Methods 0.000 description 1
- 229960000575 trastuzumab Drugs 0.000 description 1
- 229960001612 trastuzumab emtansine Drugs 0.000 description 1
- 150000003626 triacylglycerols Chemical class 0.000 description 1
- 125000004306 triazinyl group Chemical group 0.000 description 1
- 125000001425 triazolyl group Chemical group 0.000 description 1
- 231100000164 trypan blue assay Toxicity 0.000 description 1
- 208000010380 tumor lysis syndrome Diseases 0.000 description 1
- 150000004917 tyrosine kinase inhibitor derivatives Chemical class 0.000 description 1
- 150000003668 tyrosines Chemical class 0.000 description 1
- 210000003606 umbilical vein Anatomy 0.000 description 1
- 210000005166 vasculature Anatomy 0.000 description 1
- 229940099259 vaseline Drugs 0.000 description 1
- 235000013311 vegetables Nutrition 0.000 description 1
- 231100000747 viability assay Toxicity 0.000 description 1
- 229940046009 vitamin E Drugs 0.000 description 1
- 235000019165 vitamin E Nutrition 0.000 description 1
- 239000011709 vitamin E Substances 0.000 description 1
- 239000001993 wax Substances 0.000 description 1
- 208000016261 weight loss Diseases 0.000 description 1
- 230000004580 weight loss Effects 0.000 description 1
- 239000009637 wintergreen oil Substances 0.000 description 1
- 210000002268 wool Anatomy 0.000 description 1
- QDLHCMPXEPAAMD-UHFFFAOYSA-N wortmannin Natural products COCC1OC(=O)C2=COC(C3=O)=C2C1(C)C1=C3C2CCC(=O)C2(C)CC1OC(C)=O QDLHCMPXEPAAMD-UHFFFAOYSA-N 0.000 description 1
- QDLHCMPXEPAAMD-QAIWCSMKSA-N wortmannin Chemical compound C1([C@]2(C)C3=C(C4=O)OC=C3C(=O)O[C@@H]2COC)=C4[C@@H]2CCC(=O)[C@@]2(C)C[C@H]1OC(C)=O QDLHCMPXEPAAMD-QAIWCSMKSA-N 0.000 description 1
- 229920001285 xanthan gum Polymers 0.000 description 1
- 235000010493 xanthan gum Nutrition 0.000 description 1
- 239000000230 xanthan gum Substances 0.000 description 1
- 229940082509 xanthan gum Drugs 0.000 description 1
- 239000005019 zein Substances 0.000 description 1
- 229940093612 zein Drugs 0.000 description 1
- 150000003751 zinc Chemical class 0.000 description 1
- 239000002076 α-tocopherol Substances 0.000 description 1
- 235000004835 α-tocopherol Nutrition 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/275—Nitriles; Isonitriles
- A61K31/277—Nitriles; Isonitriles having a ring, e.g. verapamil
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/13—Amines
- A61K31/135—Amines having aromatic rings, e.g. ketamine, nortriptyline
- A61K31/138—Aryloxyalkylamines, e.g. propranolol, tamoxifen, phenoxybenzamine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/16—Amides, e.g. hydroxamic acids
- A61K31/165—Amides, e.g. hydroxamic acids having aromatic rings, e.g. colchicine, atenolol, progabide
- A61K31/167—Amides, e.g. hydroxamic acids having aromatic rings, e.g. colchicine, atenolol, progabide having the nitrogen of a carboxamide group directly attached to the aromatic ring, e.g. lidocaine, paracetamol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/16—Amides, e.g. hydroxamic acids
- A61K31/17—Amides, e.g. hydroxamic acids having the group >N—C(O)—N< or >N—C(S)—N<, e.g. urea, thiourea, carmustine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/335—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin
- A61K31/337—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin having four-membered rings, e.g. taxol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
- A61K31/403—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil condensed with carbocyclic rings, e.g. carbazole
- A61K31/404—Indoles, e.g. pindolol
- A61K31/4045—Indole-alkylamines; Amides thereof, e.g. serotonin, melatonin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/4164—1,3-Diazoles
- A61K31/4184—1,3-Diazoles condensed with carbocyclic rings, e.g. benzimidazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/425—Thiazoles
- A61K31/429—Thiazoles condensed with heterocyclic ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/4965—Non-condensed pyrazines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/513—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim having oxo groups directly attached to the heterocyclic ring, e.g. cytosine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/54—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one sulfur as the ring hetero atoms, e.g. sulthiame
- A61K31/5415—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one sulfur as the ring hetero atoms, e.g. sulthiame ortho- or peri-condensed with carbocyclic ring systems, e.g. phenothiazine, chlorpromazine, piroxicam
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/55—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having seven-membered rings, e.g. azelastine, pentylenetetrazole
- A61K31/551—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having seven-membered rings, e.g. azelastine, pentylenetetrazole having two nitrogen atoms, e.g. dilazep
- A61K31/5513—1,4-Benzodiazepines, e.g. diazepam or clozapine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/56—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids
- A61K31/565—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids not substituted in position 17 beta by a carbon atom, e.g. estrane, estradiol
- A61K31/567—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids not substituted in position 17 beta by a carbon atom, e.g. estrane, estradiol substituted in position 17 alpha, e.g. mestranol, norethandrolone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/56—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids
- A61K31/58—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids containing heterocyclic rings, e.g. danazol, stanozolol, pancuronium or digitogenin
- A61K31/585—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids containing heterocyclic rings, e.g. danazol, stanozolol, pancuronium or digitogenin containing lactone rings, e.g. oxandrolone, bufalin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/65—Tetracyclines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7028—Compounds having saccharide radicals attached to non-saccharide compounds by glycosidic linkages
- A61K31/7034—Compounds having saccharide radicals attached to non-saccharide compounds by glycosidic linkages attached to a carbocyclic compound, e.g. phloridzin
- A61K31/704—Compounds having saccharide radicals attached to non-saccharide compounds by glycosidic linkages attached to a carbocyclic compound, e.g. phloridzin attached to a condensed carbocyclic ring system, e.g. sennosides, thiocolchicosides, escin, daunorubicin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7042—Compounds having saccharide radicals and heterocyclic rings
- A61K31/7052—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides
- A61K31/706—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom
- A61K31/7064—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom containing condensed or non-condensed pyrimidines
- A61K31/7068—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom containing condensed or non-condensed pyrimidines having oxo groups directly attached to the pyrimidine ring, e.g. cytidine, cytidylic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/18—Drugs for disorders of the alimentary tract or the digestive system for pancreatic disorders, e.g. pancreatic enzymes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/08—Drugs for disorders of the urinary system of the prostate
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P15/00—Drugs for genital or sexual disorders; Contraceptives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/275—Nitriles; Isonitriles
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C255/00—Carboxylic acid nitriles
- C07C255/01—Carboxylic acid nitriles having cyano groups bound to acyclic carbon atoms
- C07C255/24—Carboxylic acid nitriles having cyano groups bound to acyclic carbon atoms containing cyano groups and singly-bound nitrogen atoms, not being further bound to other hetero atoms, bound to the same saturated acyclic carbon skeleton
- C07C255/29—Carboxylic acid nitriles having cyano groups bound to acyclic carbon atoms containing cyano groups and singly-bound nitrogen atoms, not being further bound to other hetero atoms, bound to the same saturated acyclic carbon skeleton containing cyano groups and acylated amino groups bound to the carbon skeleton
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C317/00—Sulfones; Sulfoxides
- C07C317/44—Sulfones; Sulfoxides having sulfone or sulfoxide groups and carboxyl groups bound to the same carbon skeleton
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C323/00—Thiols, sulfides, hydropolysulfides or polysulfides substituted by halogen, oxygen or nitrogen atoms, or by sulfur atoms not being part of thio groups
- C07C323/50—Thiols, sulfides, hydropolysulfides or polysulfides substituted by halogen, oxygen or nitrogen atoms, or by sulfur atoms not being part of thio groups containing thio groups and carboxyl groups bound to the same carbon skeleton
- C07C323/62—Thiols, sulfides, hydropolysulfides or polysulfides substituted by halogen, oxygen or nitrogen atoms, or by sulfur atoms not being part of thio groups containing thio groups and carboxyl groups bound to the same carbon skeleton having the sulfur atom of at least one of the thio groups bound to a carbon atom of a six-membered aromatic ring of the carbon skeleton
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Epidemiology (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Molecular Biology (AREA)
- Pain & Pain Management (AREA)
- Reproductive Health (AREA)
- Endocrinology (AREA)
- Gastroenterology & Hepatology (AREA)
- Biomedical Technology (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Hematology (AREA)
- Oncology (AREA)
- Urology & Nephrology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
La presente invención se refiere a combinaciones farmacéuticas que comprenden derivados de aminoacetonitrilo y compuestos anticancerígenos. Además, la presente invención se refiere a estas combinaciones farmacéuticas para uso en el tratamiento del cáncer. (Traducción automática con Google Translate, sin valor legal)
Description
DESCRIPCIÓN
Combinaciones farmacéuticas para el tratamiento del cáncer
Campo
La presente invención se refiere a combinaciones farmacéuticas que comprenden derivados de aminoacetonitrilo y a compuestos anticancerosos. Además, la presente invención se refiere a estas combinaciones farmacéuticas para su uso en el tratamiento del cáncer.
Antecedentes
Los derivados de aminoacetonitrilo (AAD) son una clase de antihelmínticos efectivos contra los nematodos resistentes a los fármacos. Los nematodos, o lombrices intestinales, comprenden un gran número de patógenos del hombre y de los animales domésticos. Los nematodos gastrointestinales, tales como Haemonchus contortus, son los principales parásitos de los rumiantes que causan pérdidas económicas sustanciales a la producción ganadera en todo el mundo. El monepantel (MPL) (N-[(1 S)-1 -ciano-2-(5-ciano-2-trifluorometil-fenoxi)-1 -metil-etil]-4-trifluorometil-sulfanilbenzamida) es un ejemplo de dicho AAD y ha sido aprobado como nematocida para el tratamiento de parásitos gastrointestinales en ovejas.
Se ha mostrado que el MPL es eficaz contra varias especies de nematodos patógenos del ganado. La solicitud de patente internacional WO2013138863 de Newsouth Innovations Pty Limited describe métodos para el tratamiento de uno o más cánceres que comprenden administrar una cantidad terapéuticamente efectiva de un compuesto AAD tal como MPL.
Sorprendentemente, ahora se ha encontrado que la combinación de derivados de aminoacetonitrilo (AAD) y otros compuestos anticancerosos mejora drásticamente la eficacia de los compuestos anticancerosos en el tratamiento del cáncer.
Resumen de la invención
La presente invención es tal como se define en las reivindicaciones adjuntas. Las referencias a métodos de tratamiento por terapia o cirugía o métodos de diagnóstico in vivo en los párrafos posteriores o ejemplos de esta descripción deben interpretarse como referencias a los compuestos, composiciones farmacéuticas y medicamentos de la presente invención reivindicada para su uso en esos métodos.
Según un primer aspecto, se proporciona una composición farmacéutica que comprende una combinación sinérgica de al menos un derivado de aminoacetonitrilo, una sal farmacéuticamente aceptable, o solvato del mismo, y al menos un compuesto anticanceroso, sal farmacéuticamente aceptable, o solvato del mismo.
Según un segundo aspecto, se proporciona una composición farmacéutica según el primer aspecto de la invención para el tratamiento del cáncer.
Según un tercer aspecto que no forma parte de la presente invención, se proporciona un método para el tratamiento del cáncer, comprendiendo el método administrar una cantidad terapéuticamente efectiva de la composición farmacéutica según el primer aspecto de la invención a un paciente que lo necesita.
Según un cuarto aspecto, se proporciona el uso de la composición farmacéutica según el primer aspecto de la invención para la fabricación de un medicamento para el tratamiento del cáncer.
Según un quinto aspecto, se proporciona el uso de al menos un derivado de aminoacetonitrilo, sal farmacéuticamente aceptable, o solvato del mismo, para mejorar la eficacia terapéutica de un compuesto anticanceroso en un régimen anticanceroso.
Según un sexto aspecto, se proporciona el uso de al menos un derivado de aminoacetonitrilo, sal farmacéuticamente aceptable, o solvato del mismo, para reducir la dosis de un compuesto anticanceroso en un régimen anticanceroso.
Según un séptimo aspecto, se proporciona el uso de al menos un derivado de aminoacetonitrilo, sal farmacéuticamente aceptable, o solvato del mismo, para reducir los efectos secundarios de un compuesto anticanceroso en un régimen anticanceroso.
Según un octavo aspecto que no forma parte de la presente invención, se proporciona un método para mejorar la eficacia terapéutica de un compuesto anticanceroso en un régimen anticanceroso, que comprende administrar una cantidad terapéuticamente efectiva de al menos un derivado de aminoacetonitrilo, sal farmacéuticamente aceptable. o solvato del mismo.
Según un noveno aspecto, se proporciona un método para reducir la dosis de un compuesto anticanceroso en un régimen anticanceroso, que comprende administrar una cantidad terapéuticamente efectiva de al menos un derivado de aminoacetonitrilo, sal farmacéuticamente aceptable, o solvato del mismo.
Según un décimo aspecto, se proporciona un método para reducir los efectos secundarios de un compuesto anticanceroso en un régimen anticanceroso, que comprende administrar una cantidad terapéuticamente efectiva de al menos un derivado de aminoacetonitrilo, sal farmacéuticamente aceptable, o solvato del mismo.
Según un undécimo aspecto, se proporciona el uso de al menos un derivado de aminoacetonitrilo, sal farmacéuticamente aceptable, o solvato del mismo, en la fabricación de un medicamento para mejorar la eficacia terapéutica de un compuesto anticanceroso en un régimen anticanceroso.
Según un duodécimo aspecto, se proporciona el uso de al menos un derivado de aminoacetonitrilo, sal farmacéuticamente aceptable, o solvato del mismo, en la fabricación de un medicamento para reducir la dosis de un compuesto anticanceroso en un régimen anticanceroso.
Según un decimotercer aspecto, se proporciona el uso de al menos un derivado de aminoacetonitrilo, sal farmacéuticamente aceptable, o solvato del mismo, en la fabricación de un medicamento para reducir los efectos secundarios de un compuesto anticanceroso en un régimen anticanceroso.
Breve descripción de los dibujos
La Figura 1 muestra el efecto combinado de doxorrubicina y MPL sobre la proliferación celular en células A2780. La adición de MPL 5 pM al programa de tratamiento con doxiciclina redujo el valor CI50 de 500 a 1 nM (valores aproximados). La doxorrubicina (10 nM) en presencia de MPL (5 pM) es equivalente a la doxorrubicina a 1.000 nM en ausencia de MPL.
La Figura 2 muestra un ensayo SRB del tratamiento de células A2780 durante 72 horas con MPL y cisplatino. La Figura 3 muestra un ensayo SRB del tratamiento de células A2780 durante 72 horas con MPL y etopósido. La Figura 4 muestra un ensayo SRB del tratamiento de células A2780 durante 72 horas con MPL y cimetidina. La Figura 5 muestra un ensayo SRB del tratamiento de células A2780 durante 72 horas con MPL y mifepristona. La Figura 6 muestra un ensayo SRB del tratamiento de células A2780 durante 72 horas con MPL e imatinib. La Figura 7 muestra un ensayo SRB del tratamiento de células OVCAR-3 durante 72 horas con MPL y cafeína. La Figura 8 muestra un ensayo SRB del tratamiento de células OVCAR-3 durante 72 horas con MPL y L-histidina. La Figura 9 muestra un ensayo SRB del tratamiento de células OVCAR-3 durante 72 horas con MPL y DL-histidina. La Figura 10 muestra un ensayo SRB del tratamiento de células OVCAR-3 durante 72 horas con MPL e hidrocloruro de glicina.
La Figura 11 muestra un ensayo SRB del tratamiento de células A2780 durante 72 horas con MPL y mitomicina. La Figura 12 muestra un ensayo SRB del tratamiento de células A2780 durante 72 horas con MPL y vincristina. La Figura 13 muestra un ensayo SRB del tratamiento de células A2780 durante 72 horas con MPL y paclitaxel. La Figura 14 muestra células A2780 (tratamiento de 72 horas) con MPL y albendazol (ABZ).
La Figura 15 muestra células A2780 (tratamiento de 72 horas) con MPL e ivermectina.
La Figura 16 muestra OVCAR-3 (tratamiento de 72 horas) con MPL y levamisol.
La Figura 17 muestra un ensayo SRB del tratamiento de células A2780 (tratamiento de 72 horas) con MPL y rapamicina.
La Figura 18 muestra un ensayo SRB del tratamiento de células A2780 (tratamiento de 72 horas) con MPL y everilimus.
La Figura 19 muestra células A2780 (tratamiento de 72 horas) con MPL e imatinib.
La Figura 20 muestra interacciones de MPL y flutamida sobre células malignas LNCAP-1 y células no malignas HOSE.
La Figura 21 muestra interacciones de MPL y doxorrubicina o gemcitabina sobre células malignas LN18 y U87. La Figura 22 muestra las interacciones de MPL y doxorrubicina, fluorouracilo, gemcitabina, oxaliplatino o paclitaxel sobre células malignas A2780 y OVCAR-3 y células no malignas HOSE.
La Figura 23 muestra las interacciones de MPL y doxorrubicina, fluorouracilo o gemcitabina, sobre células malignas AsPC-1 y CFPAC-1.
La Figura 24 muestra las interacciones de MPL y cisplatino, doxorrubicina, fluorouracilo, gemcitabina, oxaliplatino o paclitaxel sobre células malignas Hep3B y células no malignas HOSE.
La Figura 25 muestra las interacciones de MPL y doxorrubicina o gemcitabina sobre células malignas PET, REN y YOU.
La Figura 26 muestra las interacciones de MPL y bortezimib, colchicina, levamisol o tamoxifeno sobre células malignas A2780 y OVCAR-3 y células no malignas HOSE.
La Figura 27 muestra las interacciones de MPL combinado con fluorouracilo, gemcitabina o ambos, fluorouracilo y gemcitabina, y MPL combinado con fluorouracilo, oxaliplatino o ambos, fluorouracilo y oxaliplatino, sobre células malignas C170 y HT29.
La Figura 28 muestra las interacciones de MPL combinado con minociclina, doxorrubicina o ambas, minociclina y doxorrubicina, y MPL combinado con minociclina, paclitaxel o ambos, minociclina y paclitaxel, sobre células malignas OVCAR-3 y SKOV-1 y células no malignas HOSE.
Descripción de realizaciones
Los derivados del aminoacetonitrilo (AAD) tienen la siguiente estructura:
R1 es -CN, H o halógeno. R2 es H o halógeno. R3 es -CF3 o halógeno. R4 es -SCF3 , -SOCF3 , -SO2CF3 , -OCF3 o -CF3. R5 es H. R6 es alquilo. X es O. n es 1 a 15, 1 a 10, 1 a 5, 1 a 2 o 1. R4 está dispuesto en para del resto amida.
El compuesto de fórmula (I) puede ser el enantiómero (R) o (S) o el racemato.
El compuesto de fórmula (I) de la invención reivindicada es:
El compuesto de fórmula (I) puede ser:
Otros ejemplos de compuestos de fórmula (I) que no están dentro del alcance de las reivindicaciones incluyen:
AAD 907;
en donde cada uno de los compuestos anteriores es el enantiómero (R) o (S), o el racemato, o un metabolito, sal farmacéuticamente aceptable, solvato o profármaco del mismo.
Preferiblemente, el compuesto de fórmula (I) es MPL (N-[(1 S)-1 -ciano-2-(5-ciano-2-trifluorometil-fenoxi)-1 -metil-etil]-4-trifluorometilsulfanil-benzamida):
o sal farmacéuticamente aceptable, o solvato del mismo.
Los compuestos AAD anteriores de fórmula (I) se pueden resumir según la Tabla 1 y la fórmula (Ia):
Tabla 1 : Derivados de amino-acetonitrilo (AAD) según la fórmula (la)
"MPL-(R)" se refiere a N-[(1R)-1-ciano-2-(5-ciano-2-trifluorometil-fenoxi)-1-metil-etil]-4-trifluorometilsulfanilbenzamida, y "MPL-(S)" se refiere a N-[(1S)-1-ciano-2-(5-ciano-2-trifluorometil-fenoxi)-1-metil-etil]-4-trifluorometilsulfanil-benzamida.
La combinación farmacéutica de la presente invención comprende al menos un compuesto anticanceroso. Por ejemplo, los compuestos anticancerosos son típicamente cualquier fármaco que modifica o ralentiza la proliferación de células cancerosas e incluyen compuestos del grupo que incluye agentes citostáticos, agentes citotóxicos (tales como, por ejemplo, pero no limitado a, agentes que interaccionan con el ADN (tales como cisplatino o doxorrubicina)); taxanos (p. ej., taxotere, taxol); inhibidores de la topoisomerasa II (tales como etopósido); inhibidores de la topoisomerasa I (tales como irinotecán (o CPT-11), camptostar o topotecán); agentes que interaccionan con la tubulina (tales como paclitaxel, docetaxel o las epotilonas); agentes hormonales (tales como tamoxifeno); inhibidores de timidilato sintasa (tales como 5-fluorouracilo); antimetabolitos (tales como metotrexato); agentes alquilantes (tales como temozolomida (TEMODAR(TM) de Schering-Plough Corporation, Kenilworth, Nueva Yersey), ciclofosfamida); inhibidores de la farnesil proteína transferasa (tales como SARASAR(TM)(4~ [2-[4-[(11 R)-3,10-dibromo-8-cloro-6,11-dihidro-5H-benzo[5,6 ]ciclohepta[1,2- b]piridin-11 -il-]-1 -piperidinil]-2-oxoetil]-1 -piperidinacarboxamida, o SCH 66336 de Schering-Plough Corporation, Kenilworth, Nueva Yersey), tipifamib (Zamestra® o R115777 de Janssen Pharmaceuticals), L778.123 (un inhibidor de la farnesil proteína transferasa de Merck & Company, Whitehouse Station, Nueva Yersey), BMS 214662 (un inhibidor de la farnesil proteína transferasa de Bristol-Myers Squibb Pharmaceuticals, Princeton, Nueva Yersey); inhibidores de la transducción de señales (tales como Iressa (de Astra Zeneca Pharmaceuticals, Inglaterra), Tarceva (inhibidores de la EGFR quinasa), anticuerpos contra EGFR (p. ej., C225), GLEEVEC(TM) (inhibidor de la C-abl quinasa de Novartis Pharmaceuticals, East Hanover, Nueva Yersey); interferones tales como, por ejemplo, intron (de Schering-Plough Corporation), Peg-Intron (de Schering-Plough Corporation); combinaciones de terapia hormonal; combinaciones de aromatasa; ara-C, adriamicina, Cytoxan, gemcitabina y las nitrosoureas .
El compuesto anticanceroso se selecciona de uno cualquiera o más de doxorrubicina, albendazol, imatinib, ivermectina, fluorouracilo, gemcitabina, oxaliplatino, paclitaxel, bortezomib, colchicina, tamoxifeno, minociclina, rapamicina, minociclina combinada con paclitaxel y minociclina combinada con doxorrubicina, cuando el cáncer a tratar es el cáncer de ovario.
El compuesto anticanceroso se selecciona de uno cualquiera o más de fluorouracilo (5FU) y gemcitabina, cuando el cáncer a tratar es cáncer colorrectal.
El compuesto anticanceroso se selecciona de uno cualquiera o más de doxorrubicina y gemcitabina, cuando el cáncer a tratar es glioblastoma.
El compuesto anticanceroso es flutamida, cuando el cáncer a tratar es cáncer de próstata, el compuesto anticanceroso es doxorrubicina, cuando el cáncer a tratar es mesotelioma, el compuesto anticanceroso se selecciona de uno cualquiera o más de doxorrubicina y paclitaxel, cuando el cáncer a tratar es cáncer de hígado, y el compuesto anticanceroso se selecciona de uno cualquiera o más de fluorouracilo (5FU) y gemcitabina, cuando el cáncer a tratar es cáncer pancreático.
Según la invención, el cáncer a tratar se selecciona entre cáncer de los ovarios, cáncer de próstata o mesotelioma, cáncer colorrectal, glioblastoma, cáncer de hígado y cáncer pancreático.
La doxorrubicina (nombre comercial Doxil; también conocida como hidroxidaunorrubicina) es un fármaco que se usa en la quimioterapia contra el cáncer. Es un antibiótico de antraciclina, estrechamente relacionado con el producto natural daunomicina. Se usa comúnmente en el tratamiento de una amplia gama de cánceres, incluidas las
malignidades hematológicas, muchos tipos de carcinoma y sarcomas de tejidos blandos.
El cisplatino (cisplatino o cis-diaminodicloroplatino(ll)) es un fármaco de quimioterapia. Fue el primer miembro de una clase de fármacos anticancerosos que contienen platino, que ahora también incluye carboplatino y oxaliplatino. Estos complejos de platino reaccionan in vivo, uniéndose a y causando la reticulación del ADN, lo que finalmente desencadena la apoptosis (muerte celular programada).
El fluorouracilo (o 5-FU) es un agente de quimioterapia, que actúa principalmente como inhibidor de la timidilato sintasa. La interrupción de la acción de esta enzima bloquea la síntesis de la pirimidina timidina, que es un nucleósido necesario para la replicación del ADN. La timidilato sintasa metila el monofosfato de desoxiuridina (dUMP) en monofosfato de timidina (dTMP). La administración de 5-FU provoca una escasez de dTMP, por lo que las células cancerosas que se dividen rápidamente sufren muerte celular por muerte sin timina.
El etopósido forma un complejo ternario con el ADN y la enzima topoisomerasa II (que ayuda a desenrollar el ADN), previene la religación de las cadenas de ADN y, al hacerlo, hace que las cadenas de ADN se rompan. Las células cancerosas dependen de esta enzima más que las células sanas, ya que se dividen más rápidamente. Por lo tanto, esto provoca errores en la síntesis del ADN y promueve la apoptosis de la célula cancerosa.
El imatinib (comercializado por Novartis como Gleevec (EE. UU.) o Glivec (Europa/Australia/América Latina), y a veces denominado por su nombre de investigación STI-571, es un inhibidor de la tirosina quinasa que se usa en el tratamiento de múltiples cánceres, en particular la leucemia mielógena crónica (CML) con cromosoma Filadelfia positivo (Ph+). Al igual que todos los inhibidores de tirosina quinasa, el imatinib actúa impidiendo que una enzima tirosina quinasa, en este caso BCR-Abl, fosforile las proteínas subsiguientes e inicie la cascada de señalización necesaria para el desarrollo del cáncer, previniendo así el crecimiento de células cancerosas y provocando su muerte por apoptosis. Como la enzima tirosina quinasa BCR-Abl existe solo en las células cancerosas y no en las células sanas, el imatinib funciona como una forma de terapia dirigida; solo las células cancerosas se eliminan a través de la acción del fármaco. En este sentido, el imatinib fue una de las primeras terapias contra el cáncer en mostrar el potencial para tal acción dirigida, y a menudo se cita como un paradigma para la investigación en agentes terapéuticos contra el cáncer.
La mitomicina (o mitomicina C) es un agente quimioterapéutico en la cirugía del glaucoma. También es un potente reticulante del ADN. Se ha demostrado que una sola reticulación por genoma es efectiva para matar bacterias. Esto se logra mediante la activación reductora seguida de dos N-alquilaciones. Ambas alquilaciones son específicas de secuencia para un nucleósido de guanina en la secuencia 5'-CpG-3'.
La tubulina es una proteína estructural que se polimeriza en microtúbulos. El citoesqueleto celular y el huso mitótico, entre otras cosas, están formados por microtúbulos. La vincristina se une a los dímeros de tubulina, inhibiendo el ensamblaje de las estructuras de los microtúbulos. La interrupción de los microtúbulos detiene la mitosis en la metafase. Por lo tanto, los alcaloides de la vinca afectan a todos los tipos de células que se dividen rápidamente, incluidas las células cancerosas, pero también a las del epitelio intestinal y la médula ósea.
El paclitaxel es un inhibidor mitótico usado en la quimioterapia contra el cáncer.
El tamoxifeno es un antagonista del receptor de estrógeno en el tejido mamario a través de su metabolito activo, el hidroxitamoxifeno. En otros tejidos, tales como el endometrio, se comporta como un agonista y, por lo tanto, puede caracterizarse como un agonista/antagonista mixto. El tamoxifeno es la terapia endocrina habitual (antiestrógeno) para el cáncer de mama positivo para receptores hormonales en mujeres premenopáusicas, y también es un estándar en mujeres posmenopáusicas.
En la presente invención, la citotoxicidad de ciertos compuestos anticancerosos se potencia mediante la adición de derivados de aminoacetonitrilo, tales como MPL. Esto es importante porque:
• si se puede reducir la dosis de un fármaco anticanceroso, puede ser más seguro y más beneficioso para el paciente y dar lugar a una reducción de los efectos secundarios de la quimioterapia (por ejemplo, la mejora de la actividad de la doxorrubicina sin la toxicidad cardíaca asociada);
• el MPL no tiene toxicidad, por lo que la mejora es muy diferente a la que se puede ver al mezclar dos fármacos anticancerosos;
• puede ser posible administrar MPL o el fármaco de forma selectiva a los tumores a través de la vasculatura de los órganos para maximizar la potenciación de la citotoxicidad de manera localizada (particularmente relevante en tejido cerebral o hepático); y
• el uso de MPL puede ser particularmente relevante en situaciones en las que se ha desarrollado resistencia a los fármacos y normalmente no se puede aumentar la dosis de la quimioterapia.
Uno de los mayores desafíos de la medicina durante los últimos 50 años ha sido la identificación de fármacos que puedan matar eficazmente las células tumorales sin dañar los tejidos normales. El perfil de efectos secundarios de casi todas las clases conocidas de fármacos anticancerosos es fundamental para limitar la capacidad del médico para
tratar al paciente con cáncer, especialmente en los últimos estadios cuando a menudo se desarrolla resistencia al fármaco. En tales casos de resistencia a fármacos, la opción de aumentar la dosis de quimioterapia citotóxica está limitada por la toxicidad en los tejidos normales. Al potenciar la actividad específica de agentes quimioterapéuticos conocidos hasta 100 veces mediante el uso de AAD como se describe en la presente invención, esto proporciona al médico la opción de aumentar la quimioterapia sin efectos secundarios asociados. En otras palabras, la composición farmacéutica de la presente invención aumenta la actividad del compuesto anticanceroso hasta 100 veces, sin aumentar la toxicidad del compuesto anticanceroso en el mismo grado.
Por consiguiente, la presente invención reduce los eventos adversos asociados con la quimioterapia al potenciar selectivamente la actividad anticancerosa de los agentes quimioterapéuticos y no afectar la actividad citotóxica en los tejidos normales. Dichos efectos adversos incluyen:
• Inmunosupresión y mielosupresión
• Tiflitis
• Malestar gastrointestinal
• Anemia
• Fatiga
• Náuseas y vómitos inducidos por quimioterapia
• Perdida de cabello
• Neoplasma secundario
• Infertilidad
• Teratogenicidad
• Efectos adversos neurológicos
• Síndrome de lisis tumoral
• Daño a órganos
• Caquexia
• Pérdida de peso
• Cardiotoxicidad
La citotoxicidad mejorada que ofrecen los AAD no se limita a los fármacos anticancerosos usados convencionalmente en la quimioterapia. Se ha mostrado aquí que otros fármacos que interfieren con el metabolismo también se benefician de una mejora significativa.
El grado de mejora observado depende de la naturaleza y el mecanismo de acción del compuesto anticanceroso. El uso de combinaciones de AAD y compuestos anticancerosos puede lograrse mediante la administración de una mezcla de los dos fármacos o mediante la administración secuencial individual.
Aunque los AAD pueden mejorar drásticamente las actividades citotóxicas de los fármacos quimioterapéuticos en las células cancerosas, esta mejora de la citotoxicidad no se observa en las células normales. Como tal, la presente invención se presta a los tratamientos del cáncer, cánceres resistentes a fármacos y en la reducción de los efectos secundarios de la quimioterapia. Por lo tanto, al mantener la citotoxicidad de un agente quimioterapéutico contra el cáncer a una dosis mucho más baja que la prescrita normalmente sin aumentar la toxicidad para las células normales, se permite la eliminación de los efectos secundarios mediados por fármacos en la terapia del cáncer.
Según la presente invención, puede desarrollarse un régimen de tratamiento mediante el cual se puede lograr el índice terapéutico óptimo en el tratamiento del cáncer con quimioterapia o fármacos que interfieren con el metabolismo de las células cancerosas. Además, puede desarrollarse un régimen de tratamiento que optimice la cronología del tratamiento con los AAD y un fármaco para el tratamiento del cáncer.
Definiciones
"Halógeno" significa flúor, cloro, bromo o yodo, preferiblemente flúor o cloro.
"Alquilo" significa un grupo hidrocarburo alifático que puede ser lineal o ramificado y que comprende de aproximadamente 1 a aproximadamente 20 átomos de carbono en la cadena. Los grupos alquilo preferidos contienen de aproximadamente 1 a aproximadamente 12 átomos de carbono en la cadena. Los grupos alquilo más preferidos contienen de aproximadamente 1 a aproximadamente 6 átomos de carbono en la cadena. Ramificado significa que uno o más grupos alquilo inferior, tales como metilo, etilo o propilo, están unidos a una cadena de alquilo lineal. "Alquilo inferior" significa un grupo que tiene de aproximadamente 1 a aproximadamente 6 átomos de carbono en la cadena que puede ser lineal o ramificada. "Alquilo" puede estar sin sustituir u opcionalmente sustituido con uno o más sustituyentes que pueden ser iguales o diferentes, seleccionándose cada sustituyente independientemente del grupo que consiste en halo, alquilo, arilo, cicloalquilo, ciano, hidroxi, alcoxi, alquiltio, amino, -NH(alquilo), - NH(cicloalquilo), -N(alquilo)2, carboxi y -C(O)O-alquilo. Los ejemplos no limitantes de grupos alquilo adecuados incluyen metilo, etilo, n-propilo, isopropilo y t-butilo.
"Arilo" por sí mismo o como parte de otro sustituyente, significa un radical hidrocarburo cíclico aromático. Los grupos arilo preferidos tienen de seis a diez átomos de carbono. El término "arilo" incluye sistemas de anillos múltiples, así como sistemas de un solo anillo. Los grupos arilo preferidos para usar en la invención incluyen fenilo y naftilo. El término "arilo" también incluye anillos hidrocarburos cíclicos condensados que son parcialmente aromáticos (es decir, uno de los anillos condensados es aromático y el otro no es aromático). Un grupo arilo ejemplar que es parcialmente aromático es indanilo.
"Heteroarilo", por sí mismo o como parte de otro sustituyente, significa un grupo cíclico o policíclico que tiene de cinco a doce átomos en el anillo seleccionados entre C, N, O y S, en donde al menos un heteroátomo en el anillo es O, N o S, y en donde al menos uno de los anillos constituyentes es aromático. Los grupos heteroarilo ejemplares para uso en la invención incluyen carbazolilo, carbolinlilo, cromenilo, cinolinilo, furanilo, benzofuranilo, benzofurazanilo, isobenzofuranilo, imidazolilo, bencimidazolilo, bencimidazolonilo, indazolilo, indolilo, isoindolilo, indolinilo, indolazinilo, indinilo, oxadiazolilo, oxazolilo, benzoxazolilo, isoxazolilo, piranilo, pirazinilo, pirazolilo, benzopirazolilo, piridazinilo, piridilo, pirimidinilo, pirrolilo, quinolilo, isoquinolilo, tetrazolilo, tiazolilo, isotiazolilo, tiadiazolilo, tienilo, benzotioenilo, benzotiazolilo, quinoxalinilo, triazinilo y triazolilo, y N-óxidos de los mismos.
Un subgrupo de grupos heteroarilo tiene 5 átomos en el anillo. Los grupos heteroarilo ejemplares en esta realización son pirazolilo, piridilo, tiazolilo e imidazolilo.
Otro subgrupo de grupos heteroarilo tiene 6 átomos en el anillo. Los grupos heteroarilo ejemplares en esta realización son piridinilo y pirimidinilo.
El término "heteroarilo" también incluye anillos heterocíclicos cíclicos condensados que son parcialmente aromáticos (es decir, uno de los anillos condensados es aromático y el otro no es aromático). Un grupo heteroarilo ejemplar que es parcialmente aromático es benzodioxol.
Cuando se sustituye un grupo heteroarilo como se define en la presente memoria, el sustituyente puede estar unido a un átomo de carbono del anillo del grupo heteroarilo, o en un heteroátomo del anillo (es decir, un nitrógeno, oxígeno o azufre), que tiene una valencia que permite la sustitución. Preferiblemente, el sustituyente está unido a un átomo de carbono del anillo. De manera similar, cuando un grupo heteroarilo se define en la presente memoria como un sustituyente, el punto de unión puede estar en un átomo de carbono del anillo del grupo heteroarilo, o en un heteroátomo del anillo (es decir, un nitrógeno, oxígeno o azufre), que tiene una valencia que permite la unión. Preferiblemente, la unión está en un átomo de carbono del anillo.
"Heteroátomo" significa un átomo seleccionado de N, O, P y S. Cuando sea necesario, cualquier valencia no designada se selecciona independientemente de H, OH, carbonilo, n-alquilo o alcoxi.
"n" puede ser de 1 a 20, preferiblemente de 1 a 10, más preferiblemente de 1 a 6 y lo más preferiblemente de 1 a 4.
"Alcoxi" significa un grupo alquil-O- en el que el grupo alquilo es como se ha descrito anteriormente. Los ejemplos no limitativos de grupos alcoxi adecuados incluyen metoxi, etoxi, n-propoxi, isopropoxi y n-butoxi. El enlace con el resto parental es a través del oxígeno del éter.
"Sal farmacéuticamente aceptable" se refiere a sales de adición de ácido o sales de adición de base convencionales que retienen la eficacia biológica y las propiedades de los compuestos de la presente invención y se forman a partir de ácidos orgánicos o inorgánicos o bases orgánicas o inorgánicas no tóxicos adecuados. Las sales de adición de ácido de muestra incluyen las derivadas de ácidos inorgánicos tales como ácido clorhídrico, ácido bromhídrico, ácido yodhídrico, ácido sulfúrico, ácido sulfámico, ácido fosfórico y ácido nítrico, y las derivadas de ácidos orgánicos tales como ácido p-toluenosulfónico, ácido salicílico, ácido metanosulfónico, ácido oxálico, ácido succínico, ácido cítrico, ácido málico, ácido láctico, ácido fumárico y similares. Las sales de adición de bases de muestra incluyen las derivadas de hidróxidos de amonio, potasio, sodio y amonio cuaternario, tales como, por ejemplo, hidróxido de tetrametilamonio. La modificación química de un compuesto farmacéutico (es decir, un fármaco) en una sal es una técnica bien conocida por los químicos farmacéuticos para obtener estabilidad física y química, higroscopicidad, fluidez y solubilidad mejoradas de los compuestos. Véase, p. ej., H.Ansel et. al., Pharmaceutical Dosage Forms and Drug Delivery Systems (6a Ed. 1995) en las p. 196 y 1456-1457.
"Farmacéuticamente aceptable", tal como vehículo, excipiente, etc. farmacéuticamente aceptable, significa farmacológicamente aceptable y sustancialmente no tóxico para el sujeto al que se administra el compuesto particular.
"Sustituido", como en alquilo sustituido, significa que la sustitución puede ocurrir en una o más posiciones y, a no ser que se indique otra cosa, los sustituyentes en cada sitio de sustitución se seleccionan independientemente de las opciones especificadas, lo que significa que puede haber más de un sustituyente presente simultáneamente en varios sitios.
También se contemplan en la presente memoria los "profármacos" y "solvatos" de los compuestos de la invención. Una discusión de los profármacos se proporciona en T. Higuchi y V. Stella, Pro-drugs as Novel Delivery Systems (1987) 14 de la A.C.S. Symposium Series, y en Bioreversible Carriers in Drug Design, (1987) Edward B. Roche, ed., American Pharmaceutical Association y Pergamon Press. El término "profármaco" significa un compuesto (p. ej., un precursor de un fármaco) que se transforma in vivo para producir un compuesto de la presente invención o un metabolito, sal farmacéuticamente aceptable o solvato del compuesto. La transformación puede ocurrir por varios mecanismos (p. ej., por procesos metabólicos o químicos). Una discusión sobre el uso de profármacos se proporciona en T. Higuchi y W. Stella, "Prodrugs as Novel Delivery Systems", Vol. 14 de la A.C.S. Symposium Series, y en Bioreversible Carriers in Drug Design, ed. Edward B. Roche, American Pharmaceutical Association y Pergamon Press, 1987.
Los "metabolitos" de los compuestos de la invención se refieren a los intermedios y productos del metabolismo.
Los compuestos de fórmula (I) pueden contener centros asimétricos o quirales y, por lo tanto, existen en diferentes formas estereoisoméricas. Se pretende que todas las formas estereoisoméricas de los compuestos de fórmula (I), así como mezclas de las mismas, incluidas las mezclas, formen parte de la presente invención. Además, la presente invención abarca todos los isómeros geométricos y posicionales. Las mezclas diastereoméricas pueden separarse en sus diastereómeros individuales sobre la base de sus diferencias físico-químicas por métodos bien conocidos por los expertos en la técnica, tales como, por ejemplo, por cromatografía y/o cristalización fraccionada. Los enantiómeros se pueden separar convirtiendo la mezcla enantiomérica en una mezcla diastereomérica por reacción con un compuesto ópticamente activo apropiado (p. ej., un auxiliar quiral tal como un alcohol quiral o cloruro de ácido de Mosher), separando los diastereómeros y convirtiendo (p. ej., hidrolizando) los diastereómeros individuales en los correspondientes enantiómeros puros. Los enantiómeros también se pueden separar mediante el uso de una columna de HPLC quiral. Los centros quirales de la presente invención pueden tener la configuración S o R como se define por la IUPAC 1974.
El uso de los términos "sal", "solvato" o "profármaco" y similares, pretende aplicarse igualmente a la sal, solvato y profármaco de enantiómeros, estereoisómeros, rotámeros, tautómeros, isómeros posicionales, racematos o profármacos de los compuestos inventivos.
Los términos "sinergia", "sinérgico", "efecto sinérgico" y "combinación sinérgica" tal y como se usan en la presente memoria se refieren a una mezcla de dos o más agentes discretos que, cuando se combinan, muestran un grado de actividad anticancerosa, tal como actividad antiproliferativa. o citotoxicidad, etc., que es mayor que el efecto aditivo esperado de dichos agentes. Los términos también se refieren al efecto combinado de administrar una cantidad de un agente terapéutico que, cuando se administra solo, no produce una respuesta significativa, pero, cuando se administra en combinación con otro compuesto terapéutico, produce una respuesta general que es significativamente mayor que la producida por el segundo compuesto solo.
El término "anticanceroso", tal y como se usa en la presente memoria, se refiere a la actividad de suprimir la formación o el crecimiento de células cancerosas, matar células cancerosas o inhibir o bloquear la metástasis de células cancerosas, abarcando el significado de inhibición de la metástasis de células cancerosas, así como la profilaxis y el tratamiento del cáncer.
Tal y como se usa en esta solicitud, la forma singular "un", "un" y "el" incluyen referencias en plural a no ser que el contexto dicte claramente otra cosa.
Tal y como se usa en la presente memoria, el término "que comprende" significa "que incluye". Las variaciones de la palabra "que comprende", tales como "comprenden" y "comprende", tienen significados correspondientemente variados. Así, por ejemplo, una composición farmacéutica "que comprende" un compuesto de fórmula (I) puede consistir exclusivamente en ese compuesto o puede incluir uno o más componentes adicionales (p. ej., un vehículo, excipiente y/o diluyente farmacéuticamente aceptable).
Tal y como se usa en la presente memoria, el término "pluralidad" significa más de uno. En ciertos aspectos o realizaciones específicas, una pluralidad puede significar 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21,22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41,42, 43, 44, 45, 46, 47, 48, 49, 50, 51 o más, y cualquier número entero que se pueda derivar de él, y cualquier rango que se pueda derivar de él.
"Cantidad terapéuticamente efectiva" significa una cantidad de al menos un compuesto de la presente invención, o un metabolito, sal farmacéuticamente aceptable, solvato o profármaco del mismo, que inhibe sustancialmente la proliferación y/o previene la diferenciación de una célula tumoral humana, incluyendo líneas de células tumorales humanas. El término "cantidad terapéuticamente efectiva", tal y como se usa en la presente memoria, incluye dentro de su significado una cantidad no tóxica pero suficiente de un agente o composición para usar en la presente invención para proporcionar el efecto terapéutico deseado. La cantidad exacta requerida variará de un sujeto a otro dependiendo
de factores tales como la especie que se está tratando, la edad y el estado general del sujeto, la gravedad de la afección que se está tratando, el agente particular que se está administrando, el modo de administración, etc. Por lo tanto, no es posible especificar una "cantidad efectiva" exacta aplicable a todas las realizaciones. Sin embargo, para cualquier caso dado, un experto en la técnica puede determinar una "cantidad efectiva" apropiada usando sólo experimentación de rutina.
Descripción detallada
Los AAD (p. ej., fórmula (I)) son una clase de compuestos que pueden sintetizarse usando el conocimiento ordinario de la metodología de síntesis orgánica. Por ejemplo, los AAD pueden sintetizarse mediante derivatización de fenoles con cloroacetona, reacción de Strecker y acilación de la amina resultante con cloruros de aroilo (como se muestra en el Esquema 1). Cuando sea necesario, se puede obtener un enantiómero particular, por ejemplo, por resolución quiral (como se muestra en el Esquema 2).
Esquema 1:
La presente invención proporciona composiciones farmacéuticas que comprenden al menos un derivado de aminoacetonitrilo como se define en las reivindicaciones adjuntas o una sal farmacéuticamente aceptable, solvato del mismo y al menos un compuesto anticanceroso adicional o una sal farmacéuticamente aceptable, solvato del mismo, y al menos un vehículo farmacéuticamente aceptable. Para preparar composiciones farmacéuticas a partir de los compuestos descritos por esta invención, los vehículos inertes farmacéuticamente aceptables pueden ser sólidos o líquidos. Las preparaciones en forma sólida incluyen polvos, comprimidos, gránulos dispersables, cápsulas, sellos y supositorios. Los polvos y comprimidos pueden estar compuestos por de aproximadamente un 5 a aproximadamente un 95 por ciento de ingrediente activo. Los vehículos sólidos adecuados son conocidos en la técnica, p. ej., carbonato de magnesio, estearato de magnesio, talco, azúcar o lactosa. Los comprimidos, polvos, sellos y cápsulas se pueden usar como formas de dosificación sólidas adecuadas para la administración oral. Se pueden encontrar ejemplos de vehículos farmacéuticamente aceptables y métodos de fabricación para diversas composiciones en A. Gennaro (ed.), Remington's Pharmaceutical Sciences, 18a Edición, (1990), Mack Publishing Co., Easton, Pensilvania.
Las composiciones y medicamentos de la presente invención pueden estar en una forma adecuada para la administración por inyección (p. ej., para la administración parenteral, incluida la inyección subcutánea, intramuscular, intraperitoneal o intravenosa), por administración oral (tales como cápsulas, comprimidos, comprimidos oblongos y elixires, por ejemplo), por administración tópica (p. ej., en forma de ungüento, crema o loción, o una forma adecuada para administrarse como colirio), o por inhalación intranasal (p. ej., en forma de aerosoles).
Las preparaciones en forma líquida incluyen soluciones, suspensiones y emulsiones, por ejemplo, soluciones en agua o agua-propilenglicol para inyección parenteral o adición de edulcorantes y opacificantes para soluciones orales, suspensiones y emulsiones. Las preparaciones en forma líquida también pueden incluir soluciones para administración intranasal.
Las preparaciones en aerosol adecuadas para la inhalación pueden incluir soluciones y sólidos en forma de polvo, que pueden combinarse con un vehículo farmacéuticamente aceptable, tal como un gas comprimido inerte, p. ej., nitrógeno. También se incluyen preparaciones en forma sólida que están destinadas a convertirse, poco antes de su uso, en preparaciones en forma líquida para administración oral o parenteral. Dichas formas líquidas incluyen soluciones, suspensiones y emulsiones.
Las combinaciones farmacéuticas de la invención también se pueden administrar por vía transdérmica. Las composiciones transdérmicas pueden tomar la forma de cremas, lociones, aerosoles y/o emulsiones y pueden incluirse en un parche transdérmico del tipo matriz o depósito como son convencionales en la técnica para este propósito.
Las combinaciones farmacéuticas de esta invención también pueden administrarse por vía subcutánea.
En una realización, las combinaciones farmacéuticas de la presente invención se administran en el cuerpo por vía intraperitoneal.
Las composiciones y medicamentos de la presente invención pueden comprender un vehículo, adyuvante, excipiente y/o diluyente farmacéuticamente aceptable. Los vehículos, diluyentes, excipientes y adyuvantes deben ser "aceptables" en términos de ser compatibles con los demás ingredientes de la composición o medicamento, y generalmente no son perjudiciales para el receptor de los mismos. Los ejemplos no limitativos de vehículos o diluyentes farmacéuticamente aceptables son agua desmineralizada o destilada; solución salina; aceites de base vegetal tales como aceite de cacahuete, aceite de cártamo, aceite de oliva, aceite de semilla de algodón, aceite de maíz; aceites de sésamo tales como aceite de cacahuete, aceite de cártamo, aceite de oliva, aceite de semilla de algodón, aceite de maíz, aceite de sésamo, aceite de cacahuete o aceite de coco; aceites de silicona, incluidos polisiloxanos, tales como metilpolisiloxano, fenilpolisiloxano y metilfenilpolisolpoxano; siliconas volátiles; aceites minerales tales como parafina líquida, parafina blanda o escualano; derivados de celulosa tales como metilcelulosa, etilcelulosa, carboximetilcelulosa, carboximetilcelulosa sódica o hidroxipropilmetilcelulosa; alcanoles inferiores, por ejemplo, etanol o isopropanol; aralcanoles inferiores; polialquilenglicoles inferiores o alquilenglicoles inferiores, por ejemplo, polietilenglicol, polipropilenglicol, etilenglicol, propilenglicol, 1,3-butilenglicol o glicerina; ésteres de ácidos grasos tales como palmitato de isopropilo, miristato de isopropilo u oleato de etilo; polivinilpirrolidona; agar; goma tragacanto o goma arábiga, y vaselina. Típicamente, el vehículo o vehículos formarán de aproximadamente el 10 % a aproximadamente el 99,9 % en peso de la composición o medicamento.
Para la administración como solución o suspensión inyectable, los diluyentes o vehículos parenteralmente aceptables no tóxicos pueden incluir solución de Ringer, solución salina isotónica, solución salina tamponada con fosfato, etanol y 1,2 propilenglicol. Los métodos para preparar composiciones y medicamentos administrables por vía parenteral son evidentes para los expertos en la técnica y se describen con más detalle, por ejemplo, en Remington's Pharmaceutical Science, 15a ed., Mack Publishing Company, Easton, Pa.
Para la administración oral, algunos ejemplos de vehículos, diluyentes, excipientes y adyuvantes adecuados incluyen aceite de cacahuete, parafina líquida, carboximetilcelulosa sódica, metilcelulosa, alginato sódico, goma arábiga, goma tragacanto, dextrosa, sacarosa, sorbitol, manitol, gelatina y lecitina. Además, estas formulaciones orales pueden contener agentes saporíferos y colorantes adecuados. Cuando se usan en forma de cápsula, las cápsulas pueden recubrirse con compuestos tales como monoestearato de glicerilo o estearato de glicerilo con disgregación retrasada. Los adyuvantes incluyen típicamente emolientes, emulsionantes, agentes espesantes, conservantes, bactericidas y agentes tamponadores.
Las formas sólidas para administración oral pueden contener aglutinantes aceptables en la práctica farmacéutica humana y veterinaria, edulcorantes, agentes disgregantes, diluyentes, saporíferos, agentes de recubrimiento, conservantes, lubricantes y/o agentes retardadores de tiempo. Los aglutinantes adecuados incluyen goma arábiga, gelatina, almidón de maíz, goma de tragacanto, alginato de sodio, carboximetilcelulosa o polietilenglicol. Los edulcorantes adecuados incluyen sacarosa, lactosa, glucosa, aspartamo o sacarina. Los agentes disgregantes adecuados incluyen almidón de maíz, metilcelulosa, polivinilpirrolidona, goma guar, goma xantana, bentonita, ácido algínico o agar. Los diluyentes adecuados incluyen lactosa, sorbitol, manitol, dextrosa, caolín, celulosa, carbonato de calcio, silicato de calcio o fosfato dicálcico. Los agentes saporíferos adecuados incluyen aceite de menta, aceite de gaulteria, sabor de cereza, naranja o frambuesa. Los agentes de recubrimiento adecuados incluyen polímeros o copolímeros de ácido acrílico y/o ácido metacrílico y/o sus ésteres, ceras, alcoholes grasos, zeína, goma laca o gluten.
Los conservantes adecuados incluyen benzoato de sodio, vitamina E, alfa-tocoferol, ácido ascórbico, metilparabeno, propilparabeno o bisulfito de sodio. Los lubricantes adecuados incluyen estearato de magnesio, ácido esteárico, oleato de sodio, cloruro de sodio o talco. Los agentes retardadores de tiempo adecuados incluyen monoestearato de glicerilo o diestearato de glicerilo.
Las formas líquidas para administración oral pueden contener, además de los agentes anteriores, un vehículo líquido. Los vehículos líquidos adecuados incluyen agua, aceites tales como aceite de oliva, aceite de cacahuete, aceite de sésamo, aceite de girasol, aceite de cártamo, aceite de cacahuete, aceite de coco, parafina líquida, etilenglicol, propilenglicol, polietilenglicol, etanol, propanol, isopropanol, glicerol, alcoholes grasos, triglicéridos o mezclas de los mismos.
Las suspensiones para administración oral pueden comprender además agentes dispersantes y/o agentes de suspensión. Los agentes de suspensión adecuados incluyen carboximetilcelulosa de sodio, metilcelulosa, hidroxipropilmetilcelulosa, polivinilpirrolidona, alginato de sodio o alcohol acetílico. Los agentes dispersantes adecuados incluyen lecitina, polioxietilen ésteres de ácidos grasos tales como ácido esteárico, mono o dioleato, estearato o laurato de polioxietilen sorbitol, mono o dioleato, estearato o laurato de polioxietilen sorbitán, y similares.
Las formulaciones para administración oral pueden comprender uno o más agentes emulsionantes. Los agentes emulsionantes adecuados incluyen agentes dispersantes como los ejemplificados anteriormente o gomas naturales tales como goma guar, goma arábiga o goma tragacanto.
Las formulaciones tópicas de la presente invención pueden comprender un ingrediente activo junto con uno o más vehículos aceptables y, opcionalmente, cualquier otro ingrediente terapéutico. Las formulaciones adecuadas para la administración tópica incluyen preparaciones líquidas o semilíquidas adecuadas para la penetración a través de la piel hasta el sitio donde se requiere el tratamiento, tales como linimentos, lociones, cremas, ungüentos o pastas, y gotas adecuadas para la administración en los ojos, los oídos o la nariz.
Las gotas según la presente invención pueden comprender soluciones o suspensiones acuosas u oleosas estériles. Estas pueden prepararse disolviendo el ingrediente activo en una solución acuosa de un agente bactericida y/o fungicida y/o cualquier otro conservante adecuado, y opcionalmente incluyendo un agente tensioactivo. A continuación, la solución resultante puede clarificarse por filtración, transferirse a un recipiente adecuado y esterilizarse. La esterilización puede lograrse en autoclave o manteniéndola a 90 °C-100 °C durante media hora, o por filtración, seguida de transferencia a un recipiente mediante una técnica aséptica. Los ejemplos de agentes bactericidas y fungicidas adecuados para su inclusión en las gotas son nitrato o acetato fenilmercúrico (0,002 %), cloruro de benzalconio (0,01 %) y acetato de clorhexidina (0,01 %). Los disolventes adecuados para la preparación de una solución oleosa incluyen glicerol, alcohol diluido y propilenglicol.
Las lociones según la presente invención incluyen las adecuadas para su aplicación en la piel o los ojos. Una loción para los ojos puede comprender una solución acuosa estéril que contiene opcionalmente un bactericida y puede prepararse mediante métodos similares a los descritos anteriormente en relación con la preparación de gotas. Las lociones o linimentos para aplicar sobre la piel también pueden incluir un agente para acelerar el secado y enfriar la piel, tal como un alcohol o acetona, y/o un humectante tal como glicerol, o un aceite tal como aceite de ricino o aceite de cacahuete.
Las cremas, ungüentos o pastas según la presente invención son formulaciones semisólidas del ingrediente activo para aplicación externa. Pueden prepararse mezclando el ingrediente activo en forma finamente dividida o en polvo, solo o en solución o suspensión en un fluido acuoso o no acuoso, con una base grasa o no grasa. La base puede comprender hidrocarburos tales como parafina dura, blanda o líquida, glicerol, cera de abejas, un jabón metálico; un mucílago; un aceite de origen natural tal como aceite de almendras, maíz, cacahuete, ricino u oliva, grasa de lana o sus derivados, o un ácido graso tal como ácido esteárico u oleico junto con un alcohol tal como propilenglicol o macrogoles.
Las composiciones y medicamentos de la presente invención pueden incorporar cualquier tensioactivo adecuado, tal como un tensioactivo aniónico, catiónico o no iónico, tal como ésteres de sorbitán o derivados de polioxietileno de los mismos. También se pueden incluir agentes de suspensión tales como gomas naturales, derivados de celulosa o materiales inorgánicos tales como sílices salicáceas y otros ingredientes tales como lanolina.
Las composiciones y medicamentos de la presente invención se pueden administrar en forma de liposomas. Se conocen en la técnica métodos adecuados para formar liposomas, y en relación con este asunto específico se hace referencia a Prescott, (Ed), (1976), "Methods in Cell Biology", Volumen XIV, Academic Press, Nueva York, N.Y. p.33 y siguientes.
También se pueden incorporar a las composiciones y medicamentos de la presente invención ingredientes activos suplementarios tales como adyuvantes o modificadores de la respuesta biológica.
Puede incluirse cualquier adyuvante adecuado en las composiciones y medicamentos de la presente invención. Por ejemplo, se puede utilizar un adyuvante basado en aluminio. Los adyuvantes basados en aluminio adecuados incluyen, pero no se limitan a, hidróxido de aluminio, fosfato de aluminio y combinaciones de los mismos. Otros ejemplos específicos de adyuvantes basados en aluminio que pueden utilizarse se describen en la Patente Europea No.
1216053 y Patente de EE. UU. No. 6.372.223. Otros adyuvantes adecuados incluyen el adyuvante incompleto y el adyuvante completo de Freund (Difco Laboratories, Detroit, Mich.); Adyuvante 65 de Merck (Merck and Company, Inc., Rahway, N.J.); AS-2 (SmithKline Beecham, Filadelfia, Pa.); sales de aluminio tales como gel de hidróxido de aluminio (alumbre) o fosfato de aluminio; sales de calcio, hierro o zinc; una suspensión insoluble de tirosina acilada; azúcares acilados; polisacáridos derivatizados catiónicamente o aniónicamente; polifosfacenos; microesferas biodegradables; monofosforil lípido A y quil A; emulsiones de aceite en agua, incluidas las descritas en la Patente Europea No.0399843, Patente de e E. UU. No. 7.029.678 y Publicación PCT No. WO 2007/006939; y/o citoquinas adicionales, tales como GM-CSF o interleuquina-2, 7 o 12, factor estimulante de colonias de granulocitos y macrófagos (GM-CSF), monofosforil lípido A (MPL), toxina del cólera (CT) o su subunidad constituyente, enterotoxina termolábil (LT) o su subunidad constituyente, adyuvantes de ligandos de receptores tipo toll tales como lipopolisacáridos (LPS) y derivados de los mismos (p. ej., monofosforil lípido A y monofosforil lípido A 3-desacetilado), muramil dipéptido (MDP) y Proteína F del Virus Sincitial Respiratorio (RSV).
Otro aspecto que no forma parte de la invención reivindicada es un kit que comprende una cantidad terapéuticamente efectiva de al menos un derivado de aminoacetonitrilo, o un metabolito, sal, solvato o profármaco farmacéuticamente aceptable de dicho compuesto, al menos un compuesto anticanceroso, o un metabolito, sal, solvato o profármaco farmacéuticamente aceptable de dicho compuesto, y un portador, vehículo o diluyente farmacéuticamente aceptable.
Otro aspecto que no forma parte de la invención reivindicada es un kit que comprende una cantidad de al menos un derivado de aminoacetonitrilo, o un metabolito, sal, solvato o profármaco farmacéuticamente aceptable de dicho compuesto, al menos un compuesto anticanceroso, o un metabolito, sal, solvato o profármaco farmacéuticamente aceptable de dicho compuesto, y una cantidad de al menos una terapia anticancerosa listada anteriormente, en donde las cantidades de los dos o más ingredientes dan como resultado el efecto terapéutico deseado.
Los kits que no forman parte de la invención actualmente reivindicada pueden comprender componentes para ayudar a realizar los métodos de la presente invención tales como, por ejemplo, dispositivo(s) de administración, tampón(es) y/o diluyente(s). Los kits pueden incluir recipientes para albergar los diversos componentes e instrucciones para usar los componentes del kit en los métodos de la presente invención.
En ciertas realizaciones, los kits pueden ser kits combinados.
En otras realizaciones, los kits pueden ser kits fragmentados.
Dosificación y vías de administración
Los agentes, composiciones y medicamentos pueden administrarse a un receptor por vías estándar, incluidas, pero no limitadas a, la vía parenteral (p. ej., intravenosa, intraespinal, subcutánea o intramuscular), oral, tópica o mucosal (p. ej., intranasal). En algunas realizaciones, pueden administrarse a un receptor de forma aislada o en combinación con otro(s) agente(s) terapéutico(s) adicional(es). En dichas realizaciones, la administración puede ser simultánea o secuencial.
En general, los agentes, composiciones y medicamentos pueden administrarse de manera compatible con la vía de administración y las características físicas del receptor (incluido el estado de salud) y de tal manera que se induzcan el o los efectos deseados (es decir, terapéuticamente efectivo, inmunogénico y/o protector). Por ejemplo, la dosificación apropiada puede depender de una variedad de factores que incluyen, pero no se limitan a, las características físicas del sujeto (p. ej., edad, peso, sexo), si el agente, la composición o el medicamento se usa como agente único o terapia adyuvante, la progresión (es decir, el estado patológico) del cáncer que se está tratando, y otros factores fácilmente evidentes para los expertos en la técnica.
Varias consideraciones generales al determinar una dosificación apropiada de los agentes, composiciones y medicamentos se describen, por ejemplo, en Gennaro et al. (Eds), (1990), "Remington’s Pharmaceutical Sciences", Mack Publishing Co., Easton, Pensilvania, EE. UU.; y Gilman et al., (Eds), (1990), "Goodman and Gilman's: The Pharmacological Bases of Therapeutics", Pergamon Press.
Los compuestos de fórmula (I) generalmente reflejan una baja toxicidad. Por ejemplo, MPL tiene una toxicidad de dosis única superior a 2.000 mg por kg de peso corporal.
Además, existe una tolerancia clínica generalmente alta de los compuestos de fórmula (I) para el tratamiento del cáncer. Por ejemplo, los mamíferos toleran bien una dosificación de 1.000 mg de MPL por kg de peso corporal en 24 horas.
En general, se espera que una dosificación efectiva esté en el rango de aproximadamente 0,0001 mg a aproximadamente 1.000 mg de componente(s) activo(s) por kg de peso corporal en 24 horas; típicamente, aproximadamente 0,001 mg a aproximadamente 750 mg por kg de peso corporal en 24 horas; aproximadamente 0,01 mg a aproximadamente 500 mg por kg de peso corporal en 24 horas; aproximadamente 0,1 mg a aproximadamente 500 mg por kg de peso corporal en 24 horas; aproximadamente 0,1 mg a aproximadamente 250 mg por kg de peso corporal en 24 horas; o aproximadamente 1,0 mg a aproximadamente 250 mg por kg de peso corporal en 24 horas. Más típicamente, se espera que un rango de dosificación efectiva esté en el rango de aproximadamente 1,0 mg a aproximadamente 200 mg por kg de peso corporal en 24 horas; aproximadamente 1,0 mg a aproximadamente 100 mg por kg de peso corporal en 24 horas; aproximadamente 1,0 mg a aproximadamente
50 mg por kg de peso corporal en 24 horas; aproximadamente 1,0 mg a aproximadamente 25 mg por kg de peso corporal en 24 horas; aproximadamente 5,0 mg a aproximadamente 50 mg por kg de peso corporal por 24 horas; aproximadamente 5,0 mg a aproximadamente 20 mg por kg de peso corporal en 24 horas; o aproximadamente 5,0 mg a aproximadamente 15 mg por kg de peso corporal en 24 horas.
Por ejemplo, una dosificación preferida puede ser de aproximadamente 1 - 100 mg, 50 mg, 2,5 - 10 mg o una dosis o rango terapéutico estándar del compuesto de fórmula (I) por kg de peso corporal en 24 horas. Las dosis terapéuticas adoptadas de compuestos anticancerosos usados actualmente en la terapia del cáncer pueden variar ampliamente dependiendo del cáncer y del fármaco terapéutico. Los médicos pueden determinar la optimización de la dosis del compuesto anticanceroso en presencia del AAD caso por caso.
Típicamente, en aplicaciones de tratamiento, el tratamiento puede ser durante la duración del cáncer. Además, será evidente para un experto en la técnica que la cantidad y el espaciamiento óptimos de las dosificaciones individuales pueden determinarse por la naturaleza y el alcance del estado de enfermedad o afección que se está tratando, la forma, la vía y el lugar de administración, y la naturaleza del sujeto particular que se está tratando. Las dosificaciones óptimas se pueden determinar usando técnicas convencionales.
Se pretende que los compuestos anticancerosos se usen para tratar los tipos de cáncer para los que normalmente se utilizan, p. ej., fármacos estándar de atención de primera y segunda línea. En una realización, los compuestos anticancerosos se proporcionan o administran en sus dosis normales, en cuyo caso la provisión o administración de un AAD descrito en la presente memoria mejora principalmente la eficacia terapéutica del agente.
En una realización, la eficacia terapéutica de un compuesto anticanceroso puede mejorarse en aproximadamente un 10 % a aproximadamente un 2.000 %. En una realización, el efecto terapéutico puede mejorarse en aproximadamente un 10 %, 20 %, 30 %, 40 %, 50 %, 60 %, 70 %, 80 %, 90 %, 100 %, 150 %, 200 %, 250 %, 300 %, 350 %, 400 %, 450 %, 500 %, 550 %, 600 %, 650 %, 700 %, 750 %, 800 %, 850 %, 900 %, 950 %, 1.000 %, 1.050 %, 1.100 %, 1.150 %, 1.200 %, 1.250 %, 1.300 %, 1.350 %, 1.400 %, 1.450 %, 1.500 %, 1.550 %, 1.600 %, 1.650 %, 1.700 %, 1.750 %, 1.800 %, 1.850 %, 1.900 %, 1.950 % o aproximadamente un 2.000 %.
Puede mejorarse la eficacia terapéutica de al menos uno de doxorrubicina, 5-fluorouracilo, imatinib, paclitaxel, tamoxifeno, minociclina, albendazol, flutamida, tamoxifeno, oxaliplatino, bortezimib, gemcitabina, ivermectina, colchicina y rapamicina.
La dosis de un compuesto anticanceroso se puede proporcionar o administrar a una dosis reducida cuando se combina con un AAD. Dicha reducción de dosis o mejora de la eficacia terapéutica del compuesto anticanceroso Dicha mejora puede permitir el uso de un compuesto anticanceroso particular para tratar un cáncer para el cual el agente no es actualmente una terapia estándar. La reducción de la dosis de un compuesto anticanceroso en una combinación sinérgica con un AAD también puede reducir los efectos secundarios del compuesto anticanceroso.
En una realización, la dosis de un compuesto anticanceroso presente en una combinación sinérgica de la invención o usado en un régimen anticanceroso puede reducirse aproximadamente 2 veces a aproximadamente 100 veces. En una realización, la reducción de la dosis es de aproximadamente 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60, 70, 80, 90 o aproximadamente 100 veces.
En una realización preferida, se puede reducir la dosis de al menos una de doxorrubicina, 5-fluorouracilo, imatinib, paclitaxel, tamoxifeno, minociclina, albendazol, flutamida, tamoxifeno, oxaliplatino, bortezimib, gemcitabina, ivermectina, colchicina y rapamicina.
En muchos casos (p. ej., aplicaciones preventivas), puede ser deseable tener varias o múltiples administraciones de un agente, composición o medicamento de la presente invención que puede, por ejemplo, administrarse 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 o más veces. Las administraciones pueden ser de intervalos de aproximadamente una a aproximadamente doce semanas, y en ciertas realizaciones intervalos de aproximadamente una a aproximadamente cuatro semanas. También se contempla la readministración periódica.
También será evidente para un experto en la técnica que el curso óptimo de administración se puede determinar usando ensayos convencionales de determinación del curso del tratamiento.
Cuando dos o más entidades (p. ej., agentes o medicamentos) se administran a un sujeto "en conjunto", se pueden administrar en una sola composición al mismo tiempo, o en composiciones separadas al mismo tiempo, o en composiciones separadas, separadas en el tiempo.
Ciertas realizaciones de la presente invención implican la administración de los agentes, composiciones o medicamentos en múltiples dosis separadas. Por consiguiente, los métodos para el tratamiento profiláctico y terapéutico descritos en la presente memoria abarcan la administración de múltiples dosis separadas a un sujeto, por ejemplo, durante un período de tiempo definido. Por consiguiente, en algunas realizaciones, los métodos incluyen la administración de una dosis de cebado, que puede ir seguida de una dosis de refuerzo. El refuerzo puede ser para el propósito de una revacunación. En diversas realizaciones, el agente, composición o medicamento se administra al menos una, dos, tres veces o más.
Los agentes, composiciones y medicamentos generalmente pueden administrarse en una cantidad efectiva para lograr un propósito previsto. Más específicamente, pueden administrarse en una cantidad terapéuticamente efectiva, lo que significa una cantidad efectiva para prevenir el desarrollo de, o para aliviar los síntomas existentes de, una enfermedad o afección diana. La determinación de las cantidades efectivas está dentro de la capacidad de los expertos en la técnica. Por ejemplo, una dosis terapéuticamente efectiva de los agentes, composiciones y medicamentos puede estimarse inicialmente a partir de ensayos de cultivos celulares. Por ejemplo, se puede formular una dosis en modelos animales para lograr un rango de concentración circulante que incluya la CI50 determinada en cultivo celular. Dicha información se puede usar para determinar con mayor precisión las dosis útiles en seres humanos y otros sujetos mamíferos.
Una dosis terapéuticamente efectiva se refiere a la cantidad del agente, composición o medicamento para prevenir el desarrollo de síntomas, mejorar los síntomas y/o prolongar la supervivencia del sujeto bajo tratamiento. La toxicidad y la eficacia terapéutica de los agentes, composiciones y medicamentos pueden determinarse mediante ensayos farmacéuticos estándar en cultivos celulares y/o animales de experimentación (p. ej., mediante la determinación de la DL50 (la dosis letal para el 50 % de la población) y la DE50 (la dosis terapéuticamente efectiva en el 50% de la población)). La relación de dosis entre efectos tóxicos y terapéuticos es el índice terapéutico que se puede expresar como la relación entre DL50 y DE50. Se prefieren los agentes, composiciones y medicamentos que exhiben altos índices terapéuticos. Los datos obtenidos de dichos ensayos de cultivos celulares y/o estudios en animales pueden usarse para formular un rango de dosificación para uso en seres humanos u otros mamíferos. La dosificación de dichos compuestos se encuentra preferiblemente dentro de un rango de concentraciones circulantes que incluyen la DE50 con poca o ninguna toxicidad. La dosificación puede variar dentro de este rango dependiendo de la forma de dosificación empleada y la vía de administración utilizada. La fórmula exacta, la vía de administración y la dosificación pueden seleccionarse sin dificultad por un médico individual en vista de la condición del sujeto (véase, por ejemplo, Fingl et al., (1975), en "The Pharmacological Basis of Therapeutics", Cap. 1 p. 1). La cantidad de dosificación y el intervalo pueden ajustarse individualmente para proporcionar niveles plasmáticos del agente activo suficientes para lograr y mantener el o los efectos terapéuticos deseados y/o una concentración efectiva mínima (MEC). Las dosificaciones necesarias para lograr la MEC dependerán de la vía de administración y otras características individuales. Pueden usarse bioensayos y/o ensayos de HPLC para determinar las concentraciones plasmáticas.
Los intervalos de dosificación también pueden determinarse usando el valor MEC. En general, los agentes, composiciones y medicamentos pueden administrarse usando un régimen que mantiene los niveles plasmáticos por encima de la MEC durante entre aproximadamente el 10 %-90 % del tiempo, preferiblemente entre el 30 %-90 % y más preferiblemente entre aproximadamente el 50 %-90 %. En las realizaciones en las que se utiliza la administración local o la captación selectiva, la concentración local efectiva del fármaco puede no estar relacionada con la concentración plasmática.
La combinación de la invención también puede ser útil en combinación con uno o más tratamientos anticancerosos tales como la radioterapia (administrados juntos o secuencialmente).
Sujetos
Los métodos profilácticos y terapéuticos de la presente invención se pueden aplicar a cualquier sujeto adecuado. En algunas realizaciones, el sujeto es un sujeto mamífero. Por ejemplo, el sujeto puede ser un ratón, rata, perro, gato, vaca, oveja, caballo o cualquier otro mamífero de importancia social, económica o de investigación. Por lo tanto, el sujeto puede ser un mamífero tal como, por ejemplo, un mamífero humano o no humano.
Los expertos en la técnica apreciarán que se pueden realizar numerosas variaciones y/o modificaciones a la presente invención, tal como se divulga en las realizaciones específicas, sin apartarse del alcance de la presente invención reivindicada, tal como se describe en términos generales. Las presentes realizaciones, por lo tanto, deben considerarse en todos los aspectos como ilustrativas y no restrictivas.
La presente invención se describirá ahora con referencia a ejemplos específicos, que no deben considerarse como limitativos de ningún modo.
Ejemplos
Ejemplo 1. Efectos de monepantel (MPL) en varias líneas celulares malignas y no malignas
Materiales y Métodos
Líneas celulares y cultivo celular
Todas las líneas celulares descritas en la presente memoria se adquirieron en la ATCC. Las células se cultivaron según las instrucciones del fabricante en los medios enumerados en la Tabla 2 (a continuación) y en FBS al 5 %. Las células se sembraron en placas de 96 pocillos (2.000-3.000 células/pocillo) y se cultivaron durante la noche antes del tratamiento con MPL. Los cultivos de control se trataron con etanol solo.
Tabla 2. Medios de cultivo de células tisulares
Cultivo y ensayo de citotoxicidad
La citotoxicidad se evaluó usando el ensayo de sulforodamina B (SRB) y se informó como la mitad de la concentración inhibitoria máxima (CI50; Tabla 3). Las células se sembraron en placas de 96 pocillos (2.000-3.000 células/pocillo), se trataron con el o los compuestos indicados durante 72 h, se fijaron, lavaron y tiñeron con 100 |ul de SRB al 0,4 % (p/v) disuelto en ácido acético al 1 %. El colorante no unido se eliminó mediante cinco lavados con ácido acético al 1 % antes del secado al aire. La SRB unida se solubilizó con 100 |ul de base Tris 10 mM (pH 10,5) y se leyó la absorbancia a 570 nm.
Resultados
Los Inventores han ensayado la adición de MPL (0, 5, 10, 25, 50 y 100 pmoles/L) a cultivos de poblaciones celulares: (i) 28 malignas, (ii) cuatro inmortalizadas y (iii) tres de subcultivo temprano o primario no malignas y sanas, y se evaluó la citotoxicidad usando el ensayo SRB, como se describe anteriormente. La citotoxicidad correspondiente del metabolito principal MPL-SO2 también se ha ensayado donde se indica. Las líneas celulares malignas incluyeron: (i) mama [MCF-7, MdA-MB-231, T47-D], (ii) cuello uterino [HeLa], (iii) colorrectal [C170, HCT-116, HT-29, HT-295m11], (iv) glial [LN-18, T98G, U87, U251], (v) hepática [Hep3B], (vi) mesenquimal (sarcoma): fibrosarcoma y liposarcoma [HT-1080, SW-876] (vii) mesotelial [PET, YOU], (viii) ovárica [1A9, A2780, IGROV-1, OVCAR-3, SKOV-3], (ix) pancreática [AsPC-1, CFPAC-1] y (x) prostática [DU-145, LNCaP, PC-3]. Las líneas celulares inmortalizadas incluyeron: (i) epidérmica [HaCat], (ii) mesenquimal [3T3] (iii) nefrítica [HEK] y (iv) ovárica [CHO]. Los tipos de células no malignas de subcultivo temprano/primario incluyeron: (i) endotelial [célula endotelial de la vena umbilical humana; HUVEC], (ii) glial [astrocitos fetales humanos], y (iii) ovárica [epitelial de la superficie del ovario humano; HOSE]. Lascélulas HUVEC, astrocitos fetales humanos y HOSE son poblaciones de células no transformadas, no inmortalizadas y no malignas, recién aisladas/de bajo número de subcultivos, de tejido aparentemente sano y no enfermo. Estas poblaciones de células sanas se incluyeron en la serie experimental como controles de toxicidad no específica. Tanto MPL como MPL-SO2 se suspendieron en etanol y se aplicaron en concentraciones finales de etanol del 0,5 al 1 % en los respectivos medios de cultivo.
Tabla 3. La concentración inhibidora mitad de la máxima (CI50) de MPL y MPLSO2 para diversas líneas celulares malignas, inmortalizadas y no malignas.
MPL mostró un efecto citotóxico selectivo y relativamente alto en las 28 líneas celulares malignas ensayadas, con la excepción de la línea celular CFPAC-1 pancreática y la línea celular SKOV-3 de ovario quimiorresistente y mutante p53 que fueron ligeramente menos sensibles (2 pM < proliferación CI50 < 25 pM, Tabla 3). Todas las líneas celulares inmortalizadas y las líneas celulares CFPAC-1 y SKOV-3 mostraron una sensibilidad intermedia a MPL (12 pM < proliferación Cl50 < 35 pM; Tabla 3). Por el contrario, las tres poblaciones de células de subcultivo temprano/primario: HUVEC, astrocitos fetales humanos y células HOSE, mostraron una sensibilidad relativamente baja a MPL (proliferación CI50 > 85 pM; Tabla 3). La citotoxicidad de MPL-SO2 para todas las líneas celulares y células ensayadas en esta serie de experimentos fue generalmente comparable al compuesto parental, MPL.
Ejemplo 2. Efectos de la combinación farmacéutica de monepantel (MPL) y otros compuestos anticancerosos en líneas celulares de cáncer de ovario
Materiales y métodos
Líneas celulares
Las líneas celulares de cáncer de ovario humano OVCAR-3 y A2780, y la línea celular epitelial de superficie de ovario humano normal no maligna (HOSE), se obtuvieron todas de la American Type Culture Collection (ATCC) y se mantuvieron según sus instrucciones.
Ensayos de viabilidad y proliferación
Con el fin de evaluar el efecto de MPL sobre la eficacia in vitro de un fármaco establecido, se evaluó usando ensayos de viabilidad celular y proliferación celular. La viabilidad celular se realizó según el método estándar de Azul de Tripán. La proliferación celular se evaluó usando el ensayo de sulforodamina B (SRB). Para los experimentos de viabilidad, las células se sembraron en placas de 6 pocillos, mientras que, para los ensayos de proliferación, las células se cultivaron en placas de 96 pocillos. Después de adherencia durante la noche, las células se trataron con el fármaco deseado en varias concentraciones bien solo o en combinación con monepantel (MPL) durante 72 h. Paralelamente a esto, las células tratadas con MPL solo también se usaron con fines comparativos. Después de la incubación durante 72 h en una incubadora de cultivo celular estándar, se evaluó el efecto de los tratamientos farmacológicos mono y combinados sobre la viabilidad celular y/o la proliferación celular mediante el uso de ensayos de Azul de tripán o SRB, respectivamente.
Para el ensayo de viabilidad, al final del período de tratamiento, las células se lavaron con PBS, se tripsinizaron y se contaron usando Azul de tripán y hemocitómetro. Para el ensayo de SRB, las células se fijaron, lavaron y tiñeron con 100 pl de SRB al 0,4 % (p/v) disuelto en ácido acético al 1 %. El colorante no unido se eliminó mediante cinco lavados con ácido acético al 1 % antes del secado al aire. La SRB unida se solubilizó con 100 pl de base Tris 10 mM (pH 10,5) y se leyó la absorbancia a 570 nm. El monepantel (obsequio de Novartis, Basilea, Suiza) se disolvió en etanol al 100 % y luego se diluyó con el medio de cultivo celular. Otros agentes empleados en el estudio se compraron en Sigma Australia o Sapphire Australia, se prepararon y conservaron para su uso en cultivos celulares según las instrucciones del proveedor.
Análisis estadístico
Todos los datos se informan como la media ± errores estándar (S.E.M.) de al menos dos experimentos independientes. Las diferencias en la proliferación celular entre el grupo tratado con MPL frente al grupo de control se analizaron usando ANOVA de una vía con la prueba de comparación múltiple de Tukey.
Resultados
Tabla 4: Combinación farmacéutica de monepantel (MPL) y otros compuestos anticancerosos en células OVCAR-3
Tabla 5: Combinación farmacéutica de monepantel (MPL) y otros compuestos en células OVCAR-3 - Ejemplos Comparativos
Los datos de la doxorrubicina son particularmente Impresionantes con una citotoxicidad mejorada 100 veces.
Las Figuras 1 y 22 muestran que existe sinergia entre MPL y doxorrubicina, y especialmente a concentraciones más bajas de doxorrubicina. Esto es importante debido a que la toxicidad de la doxorrubicina en el hombre limita la dosificación. La Figura 2 muestra cierto aumento del efecto del cisplatino mediante la adición de una dosis muy baja de MPL (el reticulante de ADN produce apoptosis).
La Figura 22 también muestra un aumento significativo en el efecto de 5FU con MPL (antimetabolito, inhibición irreversible de timidilato sintasa), así como para la combinación de tamoxifeno/MPL. A dosis bajas de gemcitabina, la combinación de MPL/gemcitabina muestra un aumento notable en la eficacia de la gemcitabina (la gemcitabina es un inhibidor de la nucleótido reductasa y se usa para tratar el cáncer pancreático, de pulmón y otros).
La Figura 3 muestra algún efecto sinérgico entre etopósido y MPL.
Las Figuras 4 a 6 muestran un efecto sinérgico de combinación significativo de cimetidina con MPL, mifepristona con MPL e imatinib con MPL.
La Figura 11 muestra que la combinación de mitomicina C con MPL da lugar a un aumento efectivo de la actividad de la mitomicina C.
La Figura 12 muestra que la combinación de vincristina/MPL muestra un efecto sinérgico.
La Figura 14 muestra que la combinación de albendazol/MPL muestra un buen efecto sinérgico (el albendazol es un carbamato de bencimidazol que ha mostrado tener una variedad de efectos anticancerosos).
La Figura 15 muestra que la combinación de ivermectina/MPL mostró un efecto sinérgico. Aunque los efectos de la ivermectina en el tratamiento del cáncer son en gran parte desconocidos, la ivermectina inhibió A2780 (ovárico). La Figura 16 muestra un efecto sinérgico significativo de MPL con levamisol en células OVCAR-3.
La Figura 26 muestra un efecto sinérgico de MPL con colchicina.
El MPL no tiene efecto sobre la actividad de la glicina, L-histidina o DL-histidina. Las Figuras 7 a 10 muestran que las combinaciones de cafeína/MPL, histidina/MP, DL histidina/MPL y glicina/MPL no muestran ningún efecto sinérgico. La Figura 13 muestra que la combinación de paclitaxel/MPL no muestra ningún efecto sinérgico cuando se administra a células A2780. Sin embargo, como se muestra en la Figura 22, se observó una inhibición sinérgica tanto para OVCAR-3 como para células HOSE no malignas.
Ejemplo 3. Efectos de la combinación farmacéutica de monepantel (MPL) en combinación doble con varios fármacos quimioterapéuticos de cuidado estándar de primera y segunda línea
Los inventores han ensayado MPL en combinación doble con varios fármacos quimioterapéuticos de cuidado estándar de primera y segunda línea para determinar la interacción sinérgica sobre la citotoxicidad en células malignas usando el ensayo SRB.
Materiales y métodos
Todas las líneas celulares se obtuvieron de la American Type Culture Collection (ATCC) y se mantuvieron como se describe en el Ejemplo 1 anterior. Los ensayos de citotoxicidad también se realizaron como se describe en el Ejemplo 1 anterior.
Análisis estadístico
Todos los datos se informan como la media ± errores estándar (S.E.M.) de al menos dos experimentos independientes. Las diferencias en la proliferación celular entre el grupo tratado con MPL frente al grupo de control se analizaron usando ANOVA de una vía con la prueba de comparación múltiple de Tukey.
Resultados
Los inventores han ensayado la adición de ocho fármacos en un rango de concentraciones en combinación con MPL, incluidos: cisplatino, doxorrubicina, fluorouracilo, flutamida, gemcitabina, minociclina, oxaliplatino y paclitaxel. Las líneas celulares malignas ensayadas hasta la fecha incluyen las líneas celulares humanas malignas derivadas de: glioblastoma LN18 y U87; hepatoma Hep3B; mesotelioma PET, REN y YOU; adenocarcinoma pancreático AsPC-1 y CFPAC-1; carcinoma y adenocarcinoma de ovario A2780 y OVCAR-3, respectivamente; y próstata LNCaP. Se considera que cualquier aplicación clínica futura de MPL implicaría la administración sistémica y, teniendo esto en cuenta, se han incluido células HOSE sanas y no malignas como control de citotoxicidad para cada una de estas combinaciones. Los datos complementarios obtenidos usando minociclina y tamoxifeno en ensayos más restringidos (rangos de concentración menos completos) se describen en el Ejemplo 4, a continuación. Las células colorrectales C170 y HT29 y las células ováricas SKOV-1 también se evaluaron en ensayos más restringidos (rangos de concentración de fármaco menos completos) y también se describen en el Ejemplo 4, a continuación.
Líneas celulares/nombre usadas frente a la combinación de fármacos. El tratamiento fue con MPL 5 |uM y la combinación de fármacos durante 72 h, excepto con células Hep3B, en las que el tratamiento fue de 48 h. Los tiempos de tratamiento de HOSE 48 h correspondientes se indican en la Figura 24. En las columnas de "Fármaco Combinado", una J indica inhibición sinérgica, mientras que una x indica que no hay efecto sinérgico). 1 x = número de eventos, X = número de experimentos. 2 En un experimento (Oxaliplatino), una prueba post-hoc de Tukey dio p>0,05, pero una prueba post-hoc de Newman-Keuls dio p<0,05. 3 Las células de control HOSE fueron generalmente insensibles a la administración de MPL, sin embargo, en dos experimentos se registró citotoxicidad a niveles bajos: 5 y 3 %, respectivamente (experimentos con oxaliplatino y flutamida, véanse las Figuras 21 y 22, a continuación). 4 Se observó sinergia en células HOSE solo a altas concentraciones de MPL (véase la Figura 22 a continuación). 5 La sinergia sobre las células HOSE dio lugar a una modesta disminución en la supervivencia de las células HOSE (véase la Figura 22 a continuación). 6 No se observó ningún efecto sinérgico sobre las células HOSE después de 48 de tratamiento: la citotoxicidad observada después de este tiempo solo se podía atribuir a los efectos del Fármaco Combinado (véase la Figura 23 a continuación).
En la Figura 20, MPL y flutamida muestran una interacción sinérgica sobre las células LNCAP-1, pero no sobre las células HOSE a las concentraciones ensayadas. * indica la dosis más efectiva de todas las dosis ensayadas, ya sea con el fármaco usado solo o en combinación. La dosis más efectiva proporcionó el efecto citotóxico más alto a la concentración de fármaco más baja ensayada. ** indica sinergia.
En la Figura 21, MPL y doxorrubicina muestran una interacción sinérgica sobre las células gliales LN18 y U87. MPL y gemcitabina muestran una interacción sinérgica sobre las células LN18. * indica la dosis más efectiva, ** indica sinergia.
En la Figura 22, MPL y doxorrubicina muestran una interacción sinérgica sobre las células A2780 y OVCAR a bajas concentraciones de doxorrubicina, y las células de control A2780, OVCAR y HOSE a altas concentraciones de doxorrubicina. MPL y fluorouracilo muestran una interacción sinérgica sobre las células A2780 malignas y de control HOSE. Gemcitabina y MPL muestran una fuerte interacción sinérgica sobre las células A2780 y no muestran la misma interacción sinérgica sobre las células de control HOSE. MPL y oxaliplatino muestran una fuerte interacción sinérgica sobre las células A2780 y una interacción relativamente pequeña pero sinérgica sobre las células de control HOSE. MPL y paclitaxel muestran una interacción sinérgica sobre las células OVCAR-3 y HOSE. MPL solo muestra un efecto citotóxico pequeño pero significativo sobre las células HOSE en las Filas 2 (fluorouracilo) y 5 (paclitaxel) (no indicado). * indica la dosis más efectiva, ** indica sinergia, A indica un efecto citoprotector.
En la Figura 23, MPL y doxorrubicina no muestran una interacción sinérgica sobre las células AsPC-1. MPL y gemcitabina muestran una fuerte interacción sinérgica sobre las células AsPC-1 y no muestran una interacción sinérgica sobre las células de control HOSE a estas concentraciones (véase la Figura 22: la citotoxicidad frente a las células HOSE es atribuible solo al uso de gemcitabina). De manera similar, MPL combinado con fluorouracilo o gemcitabina muestra una interacción sinérgica sobre las células CFPAC-1. No se observa sinergia para bajas concentraciones de 5-FU sobre células HOSE, pero sí para altas concentraciones (véase la Figura 22). * indica la dosis más efectiva, ** indica sinergia.
En la Figura 24, MPL solo a 2,5 |uM no muestra un efecto citotóxico sobre las células Hep3B después de 48 horas de tratamiento. MPL solo a 5 |uM muestra un efecto citotóxico significativo sobre las células Hep3B después de 48 horas de tratamiento en 5 de 5 ensayos. MPL a 5 |uM muestra una citotoxicidad sinérgica sobre las células Hep3B en combinación con doxorrubicina o paclitaxel después de 48 horas de tratamiento. MPL a 5 |uM no muestra una citotoxicidad sinérgica sobre las células HOSE en combinación con cisplatino, doxorrubicina, oxaliplatino o paclitaxel después de 48 h de tratamiento. * indica la dosis más efectiva, ** indica sinergia.
En la Figura 25, MPL y doxorrubicina muestran una interacción sinérgica sobre las células de mesotelioma PET, REN y YOU. MPL y gemcitabina no muestran una interacción sinérgica sobre las células de mesotelioma PET, REN y YOU. * indica la dosis más efectiva, ** indica sinergia.
Los inventores han mostrado que después de 72 h de tratamiento, los efectos sobre tasas de supervivencia de líneas celulares malignas de MPL en combinación con: (i) flutamida, inhibe sinérgicamente LNCaP prostática, y (ii) gemcitabina, inhibe sinérgicamente LN18 de glioblastoma, A2780 ovárica y AsPC-1 pancreática, sin mostrar una interacción sinérgica a las mismas concentraciones sobre células de control HOSE no malignas (Tabla 6; LNCAP-1 -Figura 20; LN18 - Figura 21; A2780 y HOSE - Figura 22; y AsPC1 y C - Figura 23). Además, y después de 48 h de tratamiento y en combinación con doxorrubicina o paclitaxel, MPL inhibe sinérgicamente las tasas de supervivencia de las células Hep3B, sin mostrar una interacción sinérgica a las mismas concentraciones sobre las células de control sanas y no malignas HOSE (Tabla 6; Figura 24). En cada caso, la citotoxicidad observada en células HOSE fue atribuible únicamente a la presencia de doxorrubicina, flutamida, gemcitabina o paclitaxel y no a MPL. Después de 72 h y en combinación con concentraciones relativamente bajas de doxorrubicina, MPL muestra una inhibición sinérgica sobre las tasas de supervivencia de: (i) LN18 y U87 de glioblastoma; (ii) líneas celulares malignas de ovario A2780 y OVCAR-3, y (iii) PET, REN y YOU de mesotelioma; pero no de células HOSE no malignas (Tabla 6; LN18 -Figura 21; A2780, Ov Ca R-3 y HOSE - Figura 22; PET, REN y YOU - Figura 25). Es decir, a estas bajas concentraciones de doxorrubicina, la citotoxicidad observada en las células HOSE es atribuible únicamente a la presencia de doxorrubicina. En combinación con concentraciones relativamente bajas de oxaliplatino, MPL muestra una inhibición sinérgica sobre las tasas de supervivencia de las líneas celulares malignas A2780, pero no sobre las
células HOSE no malignas. En combinación con: (i) fluorouracilo y (ii) paclitaxel, MPL muestra una inhibición sinérgica sobre (i) A2780 ovárica y (ii) líneas celulares malignas de ovario OVCAR-3, respectivamente, así como las tasas de supervivencia de células HOSE no malignas. Si el efecto combinado de MPL con fluorouracilo y paclitaxel puede ser significativo a un nivel preclínico requiere más investigación.
La disección adicional de los efectos de las combinaciones de fármacos de MPL sobre las células Hep3B después de 48 h de tratamiento demuestra un potente efecto de MPL 5 gM solo, independientemente de la combinación de fármacos combinatoria (12 de 12 experimentos). Como se describió anteriormente, MPL 5 gM en combinación con doxorrubicina o paclitaxel muestra una citotoxicidad sinérgica sobre las tasas de supervivencia de las células Hep3B, y en estos experimentos, MPL solo muestra un fuerte efecto citotóxico. Sin embargo, en combinación con cisplatino, gemcitabina u oxaliplatino, no se observa sinergia debido a la alta citotoxicidad de MPL 5 gM solo. Además, y en cada caso, MPL 5 gM no ejerce ningún efecto citotóxico aditivo sobre las células HOSE cuando se combina con: cisplatino, doxorrubicina, oxaliplatino o paclitaxel, a las concentraciones ensayadas y después de 48h de tratamiento. MPL (2,5 gM) no ejerce un efecto citotóxico sobre las células Hep3B en los experimentos descritos aquí (6 de 6 experimentos).
Además de los fármacos citotóxicos enumerados anteriormente, se han ensayado otros cuatro (4) fármacos citotóxicos separados con los controles HOSE correspondientes (véase la Tabla 7, Figura 26).
Tabla 7. Citotoxicidad sinérgica incitada entre MPL y fármacos citotóxicos seleccionados en líneas celulares malignas in vitro.
En la tabla 7, Líneas celulares/nombre usado frente a la combinación de fármacos. El tratamiento fue con MPL 5 gM y la combinación de fármacos durante 72h. En las columnas de "Fármaco Combinado", un y indica inhibición sinérgica, mientras que una x indica que no hay efecto sinérgico). 1 x = número de eventos, X = número de experimentos.
2 Bortezimib mostró una respuesta bifásica, siendo sinérgico con MPL 5 gM a 0,01,2,5, 5 y 10 nM, pero no a 0,05, 0,1 o 0,5 nM (dos experimentos separados). 3 Este experimento se repitió. 4 En el experimento con tamoxifeno, se usó MPL 2,5 gM. No se determinó la dosis más eficiente. La sinergia en células HOSE no se ensayó con bortezimib 2,5, 5, 10 y 20 nM. (Bort = Bortezimib; Col = Colchicina, Lev = levamisol, Tam - tamoxifeno).
En la Figura 26, todos los tiempos de tratamiento son de 72 h. MPL solo a 5 gM muestra un efecto citotóxico significativo sobre todas las células malignas ensayadas. MPL a 5 gM muestra una citotoxicidad sinérgica sobre las células A2780 en combinación con: Bortezimib o colchicina. MPL a 5 gM no muestra aquí una citotoxicidad sinérgica sobre las células A2780 en combinación con levamisol, pero lo hace contra las células OVCAR-3 usando levamisol (10 gM) y MPL (5 o 10 gM). Véase la Figura 16 y Tablas 4 y 7). El tamoxifeno muestra aquí una citotoxicidad sinérgica con MPL sobre las células OVCAR-3. En combinación con MPL, Bortezimib y tamoxifeno ejercen una citotoxicidad sinérgica sobre las células HOSE, pero aquí no en combinación con colchicina o levamisol. Obsérvese que en combinación con tamoxifeno sobre células HOSE, se usó MPL 2,5 gM y no 5 gM. * indica la dosis más efectiva, ** indica sinergia. Se podría aumentar la dosis de levamisol.
Bortezimib muestra una respuesta bifásica aparente en las células A2780, siendo sinérgico con MPL 5 gM a 0,01,2,5, 5 y 10 nM, pero no a 0,05, 0,1 o 0,5 nM (dos experimentos separados). Las células HOSE tratadas con MPL 5 gM a 0,01,0,05, 0,1 y 0,5 nM de Bortezimib mostraron una citotoxicidad sinérgica a 0,01 y 0,05, pero no a 0,1 o 0,5 nM de Bortezimib. No se ensayaron concentraciones más altas de Bortezimib en células HOSE. La colchicina en combinación con MPL mostró un efecto citotóxico sobre las células malignas A2780, pero no sobre las células HOSE no malignas a las concentraciones ensayadas. El levamisol combinado con MPL no mostró aquí un efecto sinérgico sobre las células A2780; sin embargo, se predice que el levamisol en concentraciones más altas y en combinación con MPL puede ejercer un efecto citotóxico sinérgico sobre las células A2780. MPL y tamoxifeno mostraron un efecto sinérgico sobre las células OVCAR-3 en todas las concentraciones ensayadas. De manera similar, MPL y tamoxifeno mostraron un efecto sinérgico sobre las células HOSE, pero a la mitad de la concentración de MPL ensayada para las células OVCAR-3. Se han ensayado otros 18 fármacos citotóxicos separados en combinación doble con MPL en otros ensayos más restringidos que carecían de controles HOSE equivalentes a las mismas concentraciones (véase la Tabla 8 a continuación). Todos, menos uno, mostraron una interacción sinérgica con MPL sobre las líneas celulares ensayadas y en las concentraciones ensayadas.
Tabla 8. Citotoxicidad sinérgica incitada entre MPL y fármacos citotóxicos seleccionados en líneas celulares malignas in vitro.
En la tabla 8, Líneas celulares/nombre usado frente a la combinación de fármacos. El tratamiento fue con MPL 5 o 10 gM y la combinación de fármacos durante 72 h. En las columnas de "Fármaco Combinado", un y indica inhibición sinérgica, mientras que una x indica que no hay efecto sinérgico). 1 x = número de eventos, X = número de experimentos. 2 MPL solo se usó como control para serotonina y wortmanina en el mismo experimento.
Ejemplo 4. Efectos de la combinación farmacéutica de monepantel (MPL) en combinación triple con varios fármacos quimioterapéuticos de cuidado estándar de primera y segunda línea
Los inventores han ensayado MPL en combinación triple con varios fármacos quimioterapéuticos de cuidado estándar de primera y segunda línea para determinar la interacción sinérgica sobre la citotoxicidad de células malignas usando el ensayo SRB.
Materiales y métodos
Todas las líneas celulares se obtuvieron de la American Type Culture Collection (ATCC) y se mantuvieron como se describe en el Ejemplo 1 anterior. Los ensayos de citotoxicidad también se realizaron como se describe en el Ejemplo 1 anterior. Se aplicaron MPL (5 gM) y fármacos combinados durante 72 h a no ser que se indique otra cosa.
Resultados
Células de pancreatoma CFPAC-1: MPL, Gemcitabina y Fluorouracilo
Las células CFPAC-1 representan una línea celular de adenocarcinoma ductal pancreático aislada del hígado de un paciente con fibrosis quística después de metástasis. La citotoxicidad de CFPAC-1 se evaluó mediante el ensayo SRB después del tratamiento con MPL 5 gM solo y en combinación doble con gemcitabina o fluorouracilo (véanse las Tablas 3, 6; Figura 22). MPL (5 gM) solo ejerció un efecto citotóxico significativo sobre las células CFPAC-1 en 1 de 10 experimentos. En combinación doble con gemcitabina y fluorouracilo, MPL ejerció sinérgicamente un efecto citotóxico sobre las células CFPAC-1 a bajas concentraciones. Por lo tanto, se ensayó adicionalmente MPL a concentraciones más altas (10 gM) y en combinaciones dobles y triples con gemcitabina y fluorouracilo a esta concentración más alta. MPL (10 gM) solo y a las 72 h de tratamiento ejerció un efecto citotóxico sobre las células CFPAC-1 en 4 de 9 experimentos (datos no mostrados). En combinación con gemcitabina o fluorouracilo, MPL 10 gM ejerció sinérgicamente un efecto citotóxico sobre las células CFPAC-1 a bajas concentraciones, como se observó anteriormente (datos no mostrados, véase la Figura 23). No se observó más sinergia sobre la citotoxicidad de CFPAC-1 a partir de la combinación triple de MPL, gemcitabina y fluorouracilo.
Células de Hepatoma Hep3B: MPL, Minociclina, Oxaliplatino y Gemcitabina
Las células Hep3B son una línea celular de carcinoma hepatocelular que contiene hepatitis B. La citotoxicidad de Hep3B se evaluó mediante el ensayo SRB después del tratamiento con MPL 5 gM solo y en combinación doble con cisplatino, doxorrubicina, gemcitabina, oxaliplatino y paclitaxel o (véanse las Tablas 3, 6; Figura 24). MPL (5 gM) solo ejerció un efecto citotóxico significativo sobre las células Hep3B en 12 de 12 experimentos (Tabla 6). MPL en combinación con doxorrubicina y paclitaxel fue sinérgicamente citotóxico para las células Hep3B (Figura 24). No se observó sinergia en combinación con cisplatino, gemcitabina u oxaliplatino: el efecto citotóxico de MPL solo fue tan fuerte como el efecto citotóxico en combinación.
MPL (5 pM) en combinación doble con minociclina (5 pM) ejerció una citotoxicidad sinérgica sobre las células Hep3B después de 48 h de cultivo en uno (1) de dos (2) experimentos. La combinación triple de MPL con: (i) minociclina (5 pM) y oxaliplatino (1 pM), o (ii) minociclina (5 pM) y gemcitabina (0,01 pM), no resultó en una citotoxicidad mayor a la observada con MPL solo o en combinación doble de fármacos, respectivamente (datos no mostrados).
Células de Carcinoma Colorrectal C170 y HT29: MPL, Fluorouracilo, Oxaliplatino y Gemcitabina
C170
La línea celular C170 es una línea celular colorrectal derivada de un tumor primario. MPL (5 pM) solo indujo un efecto citotóxico significativo sobre las células C170 en uno de dos experimentos (Figura 27 y datos no mostrados). En combinación doble con 5-FU (20 pM; n = 2) o gemcitabina (0,5 pM; n = 1), MPL (5 pM) ejerció una citotoxicidad sinérgica sobre las células C170 (Figura 27). No se observó ningún efecto sinérgico en combinación doble con oxaliplatino (1 pM; n=1; Figura 27). En combinación triple con 5-FU (20 pM) y gemcitabina (0,5 pM), MPL (5 pM) ejerció una citotoxicidad sinérgica adicional sobre las células C170 (Figura 27). No se observó citotoxicidad sinérgica adicional de MPL (5 pM) en células C170 en combinación triple con 5-FU (20 pM) y oxaliplatino (1 pM).
HT29
La línea celular HT29 es una línea celular colorrectal derivada de un tumor primario. MPL (5 pM) solo no indujo un efecto citotóxico significativo sobre las células HT29 en dos experimentos (Figura 27 y datos no mostrados). En combinación doble con 5-FU (20 pM; n = 1/2) o gemcitabina (0,5 pM; n = 1), MPL (5 pM) ejerció una citotoxicidad sinérgica sobre las células HT29 (Figura 27). No se observó ningún efecto sinérgico en combinación doble con oxaliplatino (1 pM; n=1; Figura 27). En combinación triple con 5-FU (20 pM) y gemcitabina (0,5 pM), MPL (5 pM) ejerció una citotoxicidad sinérgica adicional sobre las células HT29 (Figura 27). No se observó citotoxicidad sinérgica adicional de MPL (5 pM) sobre las células HT29 en combinación triple con 5-FU (20 pM) y oxaliplatino (1 pM).
En la Figura 27, no se determinó la dosis más efectiva para las combinaciones de MPL, 5-FU y oxaliplatino. * indica la dosis más efectiva, ** indica sinergia.
Células Ováricas Malignas OVCAR-3 y SKOV-1 y no malignas HOSE: MPL, Minociclina, Tamoxifeno, Paclitaxel y Doxorrubicina
Tabla 9. Citotoxicidad sinérgica incitada entre MPL y fármacos citotóxicos seleccionados en células malignas A2780 y OVCAR-3 y no malignas HOSE in vitro.
El tratamiento con MPL y la combinación de fármacos fue durante 72h. Un y indica inhibición sinérgica, mientras que un x indica que no hay efecto sinérgico. El número de y o de x por célula corresponde al número de experimentos realizados usando esa combinación de fármacos en particular.
OVCAR-3
MPL, 5 gM solo (6/6 experimentos), pero no 2,5 gM solo (1/1 experimentos), induce un efecto citotóxico significativo sobre las células OVCAR-3 (Tabla 9; Figura 28). MPL en combinación doble con minociclina, tamoxifeno, taxol (paclitaxel) y doxorrubicina puede ejercer un efecto citotóxico sinérgico sobre las células OVCAR-3 (Tabla 9; Figura 28). Una combinación triple de MPL con: (i) minociclina y paclitaxel, o (ii) minociclina y doxorrubicina puede ejercer un efecto tóxico sinérgico sobre las células OVCAR-3 (Tabla 9; Figura 28).
Células SKOV-1
MPL, 5 gM solo (3/3 experimentos), indujo un efecto citotóxico significativo sobre las células SKOV-1 (Tabla 9; Figura 28). MPL en combinación doble con minociclina (1/3 experimentos) y tamoxifeno (1/1 experimentos) puede ejercer un efecto citotóxico sinérgico sobre las células SKOV-1 (Tabla 9; Figura 28). No se observó citotoxicidad sinérgica sobre las células SKOV-3 en los tratamientos de combinación triple de MPL estudiados aquí (Tabla 9; Figura 28).
Células HOSE
MPL, 5 gM solo (3/3 experimentos) y 2,5 gM solo (1/1 experimentos), no indujo aquí un efecto citotóxico significativo sobre las células HOSE (Tabla 9; Figura 28). MPL en combinación doble con minociclina y doxorrubicina puede ejercer un efecto citotóxico sinérgico sobre las células HOSE (Tabla 9; Figura 28). No se observó citotoxicidad sinérgica sobre las células HOSE en los tratamientos de combinación triple de MPL estudiados aquí (Tabla 9; Figura 28).
En la Figura 28, MPL (5 gM) combinado con: (i) minociclina o (ii) doxorrubicina muestra una interacción sinérgica sobre las células OVCAR-3, pero no sobre las células SKOV-1. MPL (5 gM) combinado con minociclina, pero no con doxorrubicina muestra una interacción sinérgica sobre las células HOSE. MPL (2,5 gM) combinado con: (i) minociclina o (ii) paclitaxel muestra una interacción sinérgica sobre las células OVCAR-3, pero no sobre las células HOSE. El MPL combinada tanto con minociclina como (i) doxorrubicina o (ii) paclitaxel muestra una interacción sinérgica sobre las células OVCAR-3, pero no sobre las células HOSE. No se determinó la dosis más efectiva para las combinaciones de MPL, monociclina y doxorrubicina sobre células SKOV-1. ** indica sinergia.
Discusión
El MPL in vitro y solo mostró un efecto inhibidor y selectivo sobre las 28 líneas malignas ensayadas (véase el Ejemplo 1). HOSE control, los astrocitos fetales humanos y las células HUVEC fueron relativamente insensibles a la citotoxicidad inducida por MPL. MPL in vitro y en combinación doble con fármacos quimioterapéuticos conocidos mostró una inhibición sinérgica sobre las tasas de supervivencia de todas las líneas celulares malignas ensayadas (véase el Ejemplo 3). Las células HOSE de control fueron insensibles a MPL en combinación con las concentraciones de colchicina, flutamida y gemcitabina ensayadas y bajas concentraciones de doxorrubicina y oxaliplatino. MPL in vitro y en combinación triple con fármacos quimioterapéuticos conocidos mostró una inhibición sinérgica sobre las tasas de supervivencia de las líneas celulares malignas C170 y HT29 colorrectales (MPL/fluorouracilo/gemcitabina) y OVCAR-3 pancreática (MPL/minociclina/paclitaxel y MPL/minociclina/doxorrubicina) (véase el Ejemplo 4). Estos datos son significativos para los tipos de células malignas individuales estudiados hasta la fecha por muchas razones, como se expone a continuación.
Cáncer de Mama: MCF-7, MDA-MB-231 y T47-D
El cáncer de mama es el cáncer diagnosticado con mayor frecuencia (aproximadamente 1,7 millones en 2012) y la principal causa de muerte por cáncer en mujeres en todo el mundo. El tratamiento más efectivo es la detección temprana con radioterapia y quimioterapia combinadas para reducir el tamaño del tumor antes de la cirugía. A pesar de las mejoras en el tratamiento del cáncer de mama en estadio temprano, muchas mujeres finalmente desarrollan cáncer de mama metastásico (MBC). El MBC es esencialmente una enfermedad incurable y el pronóstico ha cambiado poco en la última década, con la mayoría de los pacientes sucumbiendo a su enfermedad en los dos años posteriores al diagnóstico. Los fármacos quimioterapéuticos dirigidos para el cáncer de mama incluyen: tamoxifeno (un antagonista del receptor de estrógeno [ER]) y trastuzumab, ado-trastuzumab emtansina, perstuzumab y lapitinib (Herceptina; antagonistas del receptor del factor de crecimiento epitelial [EGF] HER-2). La mayoría de los regímenes modernos también pueden englobar antraciclinas y taxanos, a menudo aplicados en un diseño secuencial. El hecho de que el MBC siga siendo esencialmente una enfermedad incurable demuestra que se requieren nuevas clases de agentes terapéuticos.
MCF-7 y T47-D son líneas de carcinoma ductal mamario que responden a antiestrógenos, positivas para ER, positivas para receptor de progesterona [PR] y negativas para HER-2. MDA-MB-231 es una línea celular de carcinoma mamario basal-B negativa triple para ER/PR/HER-2 que es relativamente refractaria a los quimioterapéuticos conocidos. Las tres líneas celulares de cáncer de mama ensayadas fueron relativamente sensibles a la administración de MPL con CI50 de 15,5, 23,8 y 5,3 |j M, respectivamente (véase la Tabla 3). Los tumores triple negativos son responsables del 15-25 % de todos los cánceres de mama y tienen una tasa de recidiva considerablemente alta. La demostración de que MDA-MB-231 muestra una alta sensibilidad a la administración de MPL sugiere que MPL es un buen candidato como alternativa terapéutica de línea posterior para dichos tumores representativos triple negativos quimiorresistentes. La demostración de una sensibilidad particularmente alta de las líneas MCF-7 y T47-D sugiere de manera similar que MPL puede proporcionar un complemento viable o una terapia alternativa posterior para dichos tumores sensibles a los estrógenos.
Cáncer de Cuello Uterino: HeLa
El cáncer de cuello uterino es el tercer cáncer ginecológico más común, con 500.000 nuevos diagnósticos cada año y representa el 1,2 % de todas las muertes por cáncer en mujeres. Las tasas de supervivencia a cinco años para pacientes con cáncer de cuello uterino localmente avanzado se han mantenido en aproximadamente el 70 % durante los últimos 20-30 años y faltan nuevas clases de agentes terapéuticos. La adición de quimioterapia basada en platino a la radioterapia ha mejorado los resultados en comparación con la radioterapia sola; sin embargo, entre el 30 % y el 50 % de todos los pacientes no responden al tratamiento o desarrollan enfermedad recurrente. No existen opciones de tratamiento estándar para estos pacientes, aunque la quimioterapia basada en platino se usa con frecuencia y los ensayos están en curso.
Las células de cáncer de cuello uterino de adenocarcinoma HeLa fueron relativamente sensibles a la administración de MPL con una CI50 de 15,8 |jM, lo que sugiere que MPL puede representar una opción terapéutica complementaria o alternativa viable.
Cáncer Colorrectal: C170, HCT116, HT29 y HT-295m11
El cáncer colorrectal (CRC) es el segundo cáncer más común informado, con aproximadamente 1,4 millones de casos en todo el mundo en 2012, y una progresión metastásica asociada (mCRC) en el 50 % de todos los pacientes con el tiempo. Entre 1995 y 2006, las opciones terapéuticas para el mCRC avanzaron desde la resección y la terapia basada en 5-FU hasta la inclusión de tratamientos con irinotecán, ácido folínico, oxaliplatino, bevacizumab, cetuximab y panitumumab. La combinación triple de 5-FU, ácido folínico y oxaliplatino (FOLFOX) se ha convertido en un estándar de cuidado adyuvante en pacientes con cáncer de colon en estadio III. La inclusión de dichas opciones ha significado que la mediana de supervivencia global desde el diagnóstico ha aumentado, pero solo de un máximo aproximado de 9 meses a 20 meses, sin cura, según los ensayos publicados. Como resultado de estos desarrollos, el mCRC ahora se clasifica como una enfermedad crónica en lugar de aguda y, con la excepción de los ensayos prospectivos de biomarcadores de Kras en asociación con el tratamiento con cetuximab, la rentabilidad y la utilidad de estos tratamientos siguen siendo subóptimas o cuestionables. El caso de los tratamientos rentables que mejoran significativamente el tiempo de supervivencia del paciente con efectos secundarios mínimos es claro.
HT29 y HT-29 5m11 son líneas celulares de adenocarcinoma de colon de tipo salvaje, mientras que HCT116 es un carcinoma colorrectal mutante en Kras. Cada línea celular fue relativamente muy sensible a MPL con CL50 de 5,9, 10,4 y 10,5 |j M, respectivamente. Dado que cetuximab y panitumumab muestran poco efecto sobre los tumores colorrectales de Kras y en los casos en que Folfox, irinotecán y bevacizumab no han tenido un efecto suficiente, MPL puede, por lo tanto, proporcionar una línea de terapia viable adicional.
Glioblastoma: LN18, T98G, U87 y U251
Los gliomas son tumores neuroepiteliales que se originan en las células gliales de soporte del sistema nervioso central (SNC) con una incidencia de aproximadamente 2 o 3 casos por cada 100.000 personas. Los ejemplos de tumores gliales incluyen: astrocitomas, oligodendrogliomas, tumores oligoastrocíticos mixtos y glioneuronales mixtos. El
glioblastoma (GBM) multiforme, un astrocitoma, es la malignidad más frecuente y agresiva del cerebro, representa el 60-70 % de todos los gliomas y tiene dos variantes: GBM de células gigantes y gliosarcoma. Sin tratamiento, la mediana del tiempo de supervivencia tras el diagnóstico de GBM multiforme es de 4,5 meses. Con radioterapia y quimioterapia con temozolomida (TMZ) como estándar de cuidado, la mediana de supervivencia es de 14,6 meses; y con cirugía y radioterapia solas, la mediana de supervivencia es de 12,1 meses. En general, los estudios de combinación de TMZ actualmente no sugieren que un régimen de combinación de quimioterapia en particular ofrezca una mediana de supervivencia mayor que la administración de TMZ solo. La recurrencia del tumor ocurre en el 90 % de los casos en el sitio primario después de la cirugía y actualmente faltan clases terapéuticas alternativas.
Las líneas celulares de GBM U87 y U251 son sensibles a TPZ, mientras que las líneas celulares de GBM LN18 y T98G son relativamente insensibles a TPZ. Sin embargo, independientemente de la sensibilidad a TPZ, las cuatro líneas de GBM ensayadas mostraron una sensibilidad a MPL relativamente alta, mientras que las células control no malignas HOSE, astrocitos fetales humanos y HUVEC fueron relativamente insensibles a MPL. Además, MPL combinado con los fármacos quimioterapéuticos de cuidado estándar de la segunda ronda, doxorrubicina y gemcitabina, tuvo un efecto citotóxico sinérgico sobre las líneas celulares de GBM LN18 y U87, mientras que tuvo un umbral más alto para el efecto o ningún efecto, respectivamente, sobre las células HOSE. Estos datos sugieren que MPL puede ofrecer una terapia para GMB independiente o combinada viable cuando TMZ puede haber fallado.
Hepatoma: Hep3B
El carcinoma hepatocelular (HCC) es el quinto tumor más frecuente en el mundo, provoca entre 250.000 y un millón de muertes al año en todo el mundo y tiene una incidencia creciente. La resección o el trasplante de hígado son tratamientos de primera línea para el HCC, con la ablación por radiofrecuencia también como una opción, y una mediana de supervivencia global (OS) de 49 meses, pero altas tasas de recurrencia local. Sorafenib es el único tratamiento autorizado para el HCC metastásico o localmente incontrolable y aumenta la mediana de OS de 7,9 a 10,7 meses en comparación con el placebo.
Hep3B es un carcinoma hepatocelular humano sensible a sorafenib maligno mutante en p53 que, al igual que el HCC, es relativamente resistente a los agentes quimioterapéuticos convencionales tales como 5-FU, cisplatino y paclitaxel. Las células Hep3B mostraron una sensibilidad relativamente alta al tratamiento con MPL solo y se observaron efectos citotóxicos sinérgicos cuando MPL se combinó con doxorrubicina, minociclina y paclitaxel. Se requieren estudios en curso para determinar con mayor precisión la citotoxicidad de la terapia combinada con MPL en tejidos sanos, pero estos datos sugieren que MPL puede ofrecer una alternativa viable o una terapia complementaria al Sorafenib para ciertos casos de HCC.
Tumores Mesenquimales de Tejidos Blandos: Fibrosarcomas y Liposarcomas: HT-1080 y SW-872
Los sarcomas de tejidos blandos (STS) son un grupo de tumores malignos raros y heterogéneos que se originan a partir de un amplio rango de células mesenquimales en todo el cuerpo. La cirugía representa la única posibilidad de curación, ya que la enfermedad metastásica e irresecable localmente avanzada se considera generalmente incurable. La doxorrubicina y isosfamida sistémicas han sido los quimioterapéuticos estándar de primera línea para los tumores metastásicos en estadio avanzado durante más de 30 años y ofrecen una OS de aproximadamente 12-16 meses. Existe una necesidad urgente de nuevos tratamientos que mejoren la supervivencia en pacientes con enfermedad avanzada.
El fibrosarcoma del adulto es un sarcoma de tejido blando raro y agresivo, que se estima representa menos del 1 % de todos los tumores de tejido blando. La resección quirúrgica y la radioterapia proporcionan una tasa de supervivencia a los 5 años del 50 % al 80 %; sin embargo, la quimioterapia para células residuales o metastásicas no está establecida debido a la alta tasa de resistencia contra los agentes citotóxicos. Los liposarcomas son los sarcomas de tejidos blandos más comunes con una estimación de 2.600 personas diagnosticadas en los EE. UU. en 2009 y representan el 20-25 % de todos los sarcomas en adultos. Los liposarcomas están representados por tres tipos principales: liposarcomas bien diferenciados/desdiferenciados (WD/DDLPS), liposarcomas mixoides/de células redondas (MLPS) y liposarcomas pleomórficos de alto grado indiferenciados (PLPS). Los PLPS representan el 5 % de los liposarcomas y tienen una alta propensión metastásica. Existen pocas opciones terapéuticas disponibles además de la detección temprana, la extirpación quirúrgica y la radioterapia de las lesiones locales. No existe ningún predictor clínico o patológico actual del resultado.
Las líneas celulares de fibrosarcoma HT-1080 y liposarcoma SW-872 son líneas celulares sensibles a doxorrubicina, cisplatino y vincristina. Tanto las células HT-1080 como las SW-872 fueron sensibles al tratamiento con MPL, con CE50 de 17,2 pM y 14,7 pM, respectivamente. Estos datos sugieren que MPL puede tener un efecto clínicamente significativo sobre los sarcomas de tejidos blandos.
5.7 Mesotelioma: PET, REN y YOU
En los EE. UU., se notifican anualmente 3.300 casos de mesotelioma pleural maligno y más de 2.500 muertes relacionadas. Esta enfermedad está asociada con un período de latencia de progresión de la enfermedad de aproximadamente 20 a 40 años después de la exposición al asbesto. El ataque terrorista del 9/11 depositó 400.000 toneladas de asbesto en Nueva York y se espera que la incidencia de mesotelioma aumente correspondientemente. La mejor opción actual para la curación es la cirugía de escisión extensa. La mayoría de los casos (aproximadamente
el 80 %), sin embargo, se presentan en estadio tardío y no son candidatos para la curación quirúrgica. Las opciones quimioterapéuticas siguen siendo subóptimas con la terapia de cuidado estándar de cisplatino y pemetrexed/raltitrexed de primera línea que ofrece regresión en el 15-20 % de los pacientes, recidivas frecuentes y mediana de supervivencia de solo 12 meses; la terapia de segunda línea es decepcionante.
La sensibilidad relativa de las líneas de mesotelioma PET, REN y YOU a MPL y el efecto citotóxico sinérgico observado de MPL y doxorrubicina sugieren que MPL solo o en combinación puede ofrecer un efecto clínicamente importante en una enfermedad relativamente rara pero devastadora.
Cáncer de Ovario: 1A9, A2780, IGROV-1, OVCAR-3 y SKOV-3
El cáncer epitelial de ovario (EOC) es la segunda malignidad ginecológica más común y es la principal causa de muerte ginecológica en mujeres, con 20.000 muertes al año solo en los EE. UU. La cirugía y la quimioterapia basada en platino pueden ser curativas en los primeros estadios de la enfermedad; sin embargo, solo el 40-50 % de los pacientes sobreviven cinco años después del diagnóstico con EOC avanzado y la mayoría sucumbirá a la enfermedad. Aproximadamente el 70-75 % de los pacientes con EOC son diagnosticados en estadio avanzado y responden al tratamiento con cirugía y quimioterapia que comprende: carboplatino/cisplatino y paclitaxel/docetaxel. La combinación de terapias basadas en platino y taxanos ofrece un aumento de la OS de 36 meses en comparación con la OS de 24 meses que ofrecen las terapias basadas en platino solas. La doxorrubicina liposomal, el topotecán, la gemcitabina, la ciclofosfamida y el etopósido también se pueden usar dependiendo de: insensibilidad al platino, historial del paciente, toxicidad, costo y/o recurrencia. Sin embargo, la mayoría de los pacientes desarrollan resistencia a los fármacos y los pacientes resistentes al platino no responden bien a las terapias posteriores, con una mediana de OS de menos de 12 meses. El uso de Bevacizumab en cuatro ensayos cruciales de fase III y las estrategias de inhibición de PARP y antiangiogénesis han mostrado una mayor supervivencia libre de progresión (PFS), pero con menos frecuencia mejoras significativas en la mediana de la OS [p. ej., 28,8 frente a 36,6 meses con Bevacizumab]. Como tal, existe una clara necesidad de nuevas clases de agentes terapéuticos efectivos para EOC.
Las líneas celulares malignas A2780 e IGROV-1 sensibles al cisplatino, así como las líneas celulares malignas 1A29 y OVCAR-3 insensibles al cisplatino, todas mostraron una sensibilidad relativamente alta a MPL. La línea celular SKOV3 mutante en p53 sensible a taxol e insensible a cisplatino y 5-FU mostró una resistencia relativamente mayor a la citotoxicidad inducida por MPL, sin embargo, aún era considerablemente más sensible que las células de control no malignas. La combinación de MPL con: (i) doxorrubicina, fluorouracilo, gemcitabina y oxaliplatino, y (ii) doxorrubicina y paclitaxel, demostró un efecto citotóxico sinérgico sobre las células A2780 y OVCAR-3, respectivamente. Las combinaciones adicionales de MPL con 17 fármacos citotóxicos conocidos diferentes demostraron un efecto citotóxico sinérgico sobre las células A2780 y OVCAR-3 (véase la Tabla 8). Estos datos sugieren que MPL puede ofrecer una alternativa viable o una terapia complementaria a otras clases de terapias menos efectivas.
Es de interés que el carcinoma seroso de alto grado (HGSC) es el subtipo histológico más común de EOC y las vías potencialmente moduladas por fármacos incluyen: (i) el punto de control del ciclo celular G1 y (ii) la señalización de PI3K, que están alteradas en el 67 % y 45 % de casos, respectivamente. MPL se dirige a la vía de señalización de PI3K y, como tal, esta clase de defecto puede proporcionar un candidato para un futuro enfoque dirigido molecularmente para el desarrollo terapéutico.
Cáncer Pancreático: AsPC-1
El cáncer pancreático en estadio temprano generalmente es asintomático y, por lo tanto, el diagnóstico ocurre principalmente en estadios localmente avanzados o metastásicos. La resección completa es el único tratamiento potencial de supervivencia a largo plazo. Desde 1997, la quimioterapia basada en fluorouracilo y/o gemcitabina después de la resección ha representado el estándar de cuidado de los agentes quimioterapéuticos y ha aumentado la mediana de OS de cuatro a siete meses. Sin embargo, desde su introducción, no se han producido avances reales en los resultados de OS.
AsPC-1 se deriva de la ascitis de un adenocarcinoma pancreático humano metastásico resistente a la quimioterapia. Las células AsPC-1 son altamente sensibles a MPL in vitro y muestran una sensibilidad aún mayor y una citotoxicidad sinérgica en comparación con el tratamiento estándar de primera línea con gemcitabina. Las células de control HOSE fueron sensibles a la gemcitabina, pero MPL se sumó a la citotoxicidad incitada por la gemcitabina. Estos datos sugieren que MPL puede ofrecer una alternativa viable o un tratamiento complementario a la gemcitabina para el adenocarcinoma pancreático metastásico refractario, y puede hacerlo sin causar ninguna citotoxicidad adicional, incluso en presencia de una terapia con gemcitabina existente.
Cáncer de Próstata: DU-145, LNCaP, PC-3
Debido a la introducción del ensayo de PSA rutinario para la detección temprana y la mejora del tratamiento quirúrgico y radioterapéutico de la enfermedad localizada, la tasa de mortalidad por cáncer de próstata ha disminuido significativamente desde 1994. Sin embargo, el 30 % de los diagnósticos tempranos serán recurrentes a pesar de la cirugía y la radioterapia y sigue existiendo una incapacidad para tratar aproximadamente el 80 % de los casos con enfermedad metastásica. Como tal, el cáncer de próstata sigue siendo responsable del 10 % de todas las muertes por cáncer en los hombres y se prevé que siga siendo responsable de 30.000 muertes en los EE. UU. en 2014.
La terapia de privación de andrógenos generalmente se proporciona para la enfermedad refractiva quirúrgica y radioterapéutica y es efectiva durante 2-3 años, después de lo cual se puede usar quimioterapia con abiraterona y supuleucel-T para proporcionar ventajas de supervivencia de aproximadamente cuatro meses. DU145 PC3 y son líneas celulares de próstata malignas metastásicas independientes de andrógenos, mientras que la línea celular LNCaP es una línea celular de próstata maligna metastásica que responde a andrógenos
Tanto las células PC3 como las DU145 son sensibles a MPL solo, mientras que las células LNCaP son relativamente muy sensibles a MPL solo. En combinación con el antiandrógeno flutamida, MPL ejerce un fuerte efecto citotóxico sinérgico, mientras que, de forma notable, no tiene ningún efecto aditivo sobre la citotoxicidad de las células HOSE causada por la flutamida. MPL, por lo tanto, puede representar una alternativa viable o una terapia complementaria para el tratamiento de enfermedades sensibles e incluso insensibles a los andrógenos.
Claims (8)
1. Una composición farmacéutica que comprende una combinación sinérgica de al menos un derivado de aminoacetonitrilo, o una sal o solvato farmacéuticamente aceptable del mismo, y al menos un compuesto anticanceroso, o una sale o solvato farmacéuticamente aceptable del mismo para su uso en el tratamiento del cáncer; en donde el derivado de aminoacetonitrilo es un compuesto farmacéutico de fórmula (I):
en donde,
el compuesto de fórmula (I) es
y
en donde el compuesto anticanceroso se selecciona de uno cualquiera o más de doxorrubicina, albendazol, imatinib, ivermectina, fluorouracilo, gemcitabina, oxaliplatino, paclitaxel, bortezomib, colchicina, tamoxifeno, minociclina, rapamicina, minociclina combinada con paclitaxel y minociclina combinada con doxorrubicina, cuando el cáncer a tratar es el cáncer de ovario,
en donde el compuesto anticanceroso se selecciona de uno cualquiera o más de fluorouracilo (5FU) y gemcitabina, cuando el cáncer a tratar es cáncer colorrectal,
en donde el compuesto anticanceroso se selecciona de uno cualquiera o más de doxorrubicina y gemcitabina, cuando el cáncer a tratar es glioblastoma,
en donde el compuesto anticanceroso es flutamida, cuando el cáncer a tratar es cáncer de próstata, en donde el compuesto anticanceroso es doxorrubicina, cuando el cáncer a tratar es mesotelioma, en donde el compuesto anticanceroso se selecciona de uno cualquiera o más de doxorrubicina y paclitaxel, cuando el cáncer a tratar es cáncer de hígado,
y en donde el compuesto anticanceroso se selecciona de uno cualquiera o más de Fluorouracilo (5FU) y gemcitabina, cuando el cáncer a tratar es cáncer pancreático.
2. Una composición farmacéutica que comprende al menos un derivado de aminoacetonitrilo, o una sal o solvato farmacéuticamente aceptable del mismo, para su uso en el tratamiento del cáncer, en donde dicho uso es conjuntamente con al menos un compuesto anticanceroso; en donde el derivado de aminoacetonitrilo es un compuesto farmacéutico de fórmula (I):
en donde el compuesto de fórmula (I) es
y
en donde el compuesto anticanceroso se selecciona de uno cualquiera o más de doxorrubicina, albendazol, imatinib, ivermectina, fluorouracilo, gemcitabina, oxaliplatino, paclitaxel, bortezomib, colchicina, tamoxifeno, minociclina, rapamicina, minociclina combinada con paclitaxel y minociclina combinada con doxorrubicina, cuando el cáncer a tratar es el cáncer de ovario,
en donde el compuesto anticanceroso se selecciona de uno cualquiera o más de fluorouracilo (5FU) y gemcitabina, cuando el cáncer a tratar es cáncer colorrectal,
en donde el compuesto anticanceroso se selecciona de uno cualquiera o más de doxorrubicina y gemcitabina, cuando el cáncer a tratar es glioblastoma,
en donde el compuesto anticanceroso es flutamida, cuando el cáncer a tratar es cáncer de próstata,
en donde el compuesto anticanceroso es doxorrubicina, cuando el cáncer a tratar es mesotelioma,
en donde el compuesto anticanceroso se selecciona de uno cualquiera o más de doxorrubicina y paclitaxel, cuando el cáncer a tratar es cáncer de hígado,
y en donde el compuesto anticanceroso se selecciona de uno cualquiera o más de Fluorouracilo (5FU) y gemcitabina, cuando el cáncer a tratar es cáncer pancreático.
3. La composición farmacéutica para su uso según la reivindicación 1 o 2, en donde el compuesto de fórmula (I) es el enantiómero (R) y/o (S) o el racemato, preferiblemente el enantiómero (S).
6. La composición farmacéutica para su uso según una cualquiera de las reivindicaciones 2 a 5, en donde en dicho uso el agente anticanceroso y el compuesto de fórmula (I) se administran a un sujeto al mismo tiempo.
7. La composición farmacéutica para su uso según una cualquiera de las reivindicaciones 2 a 6, en donde en dicho uso, a) se potencia la eficacia terapéutica del compuesto anticanceroso, b) se reduce la dosis del compuesto anticanceroso en un régimen anticanceroso, o c) se reduce un efecto secundario del compuesto anticanceroso.
8. La composición farmacéutica para su uso según una cualquiera de las reivindicaciones 1 a 7, en donde dicho uso es conjuntamente con al menos uno o más agentes terapéuticos adicionales.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| AU2013904239A AU2013904239A0 (en) | 2013-11-01 | Pharmaceutical combinations for the treatment of cancer | |
| PCT/AU2014/001017 WO2015061832A1 (en) | 2013-11-01 | 2014-10-31 | Pharmaceutical combinations for the treatment of cancer |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2940890T3 true ES2940890T3 (es) | 2023-05-12 |
Family
ID=53002997
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES14859220T Active ES2940890T3 (es) | 2013-11-01 | 2014-10-31 | Combinaciones farmacéuticas para el tratamiento del cáncer |
Country Status (11)
| Country | Link |
|---|---|
| US (1) | US9833431B2 (es) |
| EP (1) | EP3062790B1 (es) |
| JP (2) | JP2016535014A (es) |
| KR (1) | KR102271848B1 (es) |
| CN (1) | CN105792823B (es) |
| AU (1) | AU2014344789B2 (es) |
| CA (1) | CA2922575C (es) |
| ES (1) | ES2940890T3 (es) |
| NZ (1) | NZ716765A (es) |
| PL (1) | PL3062790T3 (es) |
| WO (1) | WO2015061832A1 (es) |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR102124392B1 (ko) * | 2012-08-06 | 2020-06-19 | 피트니 파마슈티컬스 피티와이 리미티드 | mTOR 경로 관련 질병 치료를 위한 화합물 |
| EP3612177A4 (en) * | 2017-04-21 | 2021-01-13 | Lunella Biotech, Inc. | TARGETING HYPOXIC CARCINOUS STEM CELLS (SCC) USING DOXYCYCLINE: IMPLICATIONS FOR IMPROVING ANTI-ANGIOGENIC THERAPY |
| CN108078987B (zh) * | 2018-01-29 | 2019-02-15 | 中国人民解放军第四军医大学 | 阿苯达唑在制备治疗胶质母细胞瘤的药物中的用途 |
| KR102185544B1 (ko) * | 2019-04-18 | 2020-12-02 | 한림대학교 산학협력단 | 에보디아민과 화학치료제를 포함하는 갑상선암 치료용 조성물 |
| CN110075303A (zh) * | 2019-05-08 | 2019-08-02 | 长治医学院 | Na+-H+交换泵抑制剂联合顺铂促卵巢癌耐药细胞凋亡的方法 |
| EP4149454A4 (en) * | 2020-05-11 | 2024-10-16 | Pitney Pharmaceuticals Pty Limited | Use of aminoacetonitrile compounds for the treatment of infection and disease |
| WO2022033465A1 (zh) * | 2020-08-10 | 2022-02-17 | 萧乃文 | 具有协同抗癌功效的氯硝柳胺和双硫仑医药组合物及其用途 |
| CN115531398A (zh) * | 2022-10-09 | 2022-12-30 | 无锡紫杉药业股份有限公司 | 一种紫杉醇和抑制剂联合应用在抗肿瘤药物中的用途 |
| WO2024242538A1 (ko) * | 2023-05-19 | 2024-11-28 | 국립암센터 | 이버멕틴 및 항암제를 포함하는 암 예방 또는 치료용 조성물 |
Family Cites Families (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0655066A1 (en) * | 1992-08-12 | 1995-05-31 | PHARMACIA & UPJOHN COMPANY | Protein kinase inhibitors and related compounds combined with taxol |
| DK0862622T3 (da) * | 1995-11-16 | 2004-12-20 | Novartis Ag | Fremgangsmåde til identifikation af forbindelser, der vekselvirker med RAC-proteinkinase |
| US5961969A (en) * | 1996-05-14 | 1999-10-05 | Maxim Pharmaceuticals, Inc. | Stable circulating histamine levels |
| US6811788B2 (en) * | 2000-01-19 | 2004-11-02 | Baofa Yu | Combinations and methods for treating neoplasms |
| IL139975A0 (en) * | 2000-11-29 | 2002-02-10 | Univ Ramot | Anti proliferative drugs |
| WO2003013536A2 (en) * | 2001-07-23 | 2003-02-20 | Epidauros Biotechnologie Ag | Methods for treatment of cancer using irinotecan based on ugt1a1 |
| GB0402677D0 (en) * | 2003-11-06 | 2004-03-10 | Novartis Ag | Organic compounds |
| ES2528363T3 (es) * | 2004-12-06 | 2015-02-09 | Pitney Pharmaceuticals Pty Limited | Tratamiento para el cáncer |
| JP2009542623A (ja) * | 2006-07-07 | 2009-12-03 | ティルタン ファーマ リミテッド | H2遮断薬、少なくとも1つの抗炎症薬剤および細胞毒性薬剤を含む抗がん治療 |
| US20090274698A1 (en) * | 2007-07-06 | 2009-11-05 | Shripad Bhagwat | Combination anti-cancer therapy |
| CN101675930B (zh) * | 2008-09-16 | 2012-04-25 | 江苏恒瑞医药股份有限公司 | 用于治疗增生性疾病的药物组合物 |
| FR2939314A1 (fr) * | 2008-12-04 | 2010-06-11 | Univ Victor Segalen Bordeaux 2 | Nouvelles compositions et methodes pour la potentialisation des signaux d'apoptose dans les cellules tumorales |
| AU2011329638C1 (en) * | 2010-11-18 | 2017-04-27 | The General Hospital Corporation | Novel compositions and uses of anti-hypertension agents for cancer therapy |
| BR112014008203A2 (pt) * | 2011-10-04 | 2017-04-18 | Invivis Pharmaceuticals Inc | métodos e sistemas para identificação e tratamento de tumores sensíveis á antiprogestina |
| EP2822558B1 (en) * | 2012-03-06 | 2020-02-19 | The Board of Trustees of the University of Illionis | Procaspase 3 activation by combination therapy |
| KR102055176B1 (ko) | 2012-03-23 | 2019-12-12 | 피트니 파마슈티컬스 피티와이 리미티드 | 암 치료용 키나제 저해제 |
| KR102124392B1 (ko) * | 2012-08-06 | 2020-06-19 | 피트니 파마슈티컬스 피티와이 리미티드 | mTOR 경로 관련 질병 치료를 위한 화합물 |
-
2014
- 2014-10-31 ES ES14859220T patent/ES2940890T3/es active Active
- 2014-10-31 NZ NZ716765A patent/NZ716765A/en unknown
- 2014-10-31 EP EP14859220.7A patent/EP3062790B1/en active Active
- 2014-10-31 CN CN201480052310.6A patent/CN105792823B/zh active Active
- 2014-10-31 JP JP2016524588A patent/JP2016535014A/ja active Pending
- 2014-10-31 WO PCT/AU2014/001017 patent/WO2015061832A1/en not_active Ceased
- 2014-10-31 PL PL14859220.7T patent/PL3062790T3/pl unknown
- 2014-10-31 AU AU2014344789A patent/AU2014344789B2/en active Active
- 2014-10-31 US US15/021,217 patent/US9833431B2/en active Active
- 2014-10-31 CA CA2922575A patent/CA2922575C/en active Active
- 2014-10-31 KR KR1020167008078A patent/KR102271848B1/ko active Active
-
2019
- 2019-03-12 JP JP2019044801A patent/JP6666494B2/ja not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| JP2019094351A (ja) | 2019-06-20 |
| KR20160106042A (ko) | 2016-09-09 |
| AU2014344789B2 (en) | 2019-10-03 |
| JP6666494B2 (ja) | 2020-03-13 |
| WO2015061832A1 (en) | 2015-05-07 |
| CN105792823B (zh) | 2019-11-12 |
| JP2016535014A (ja) | 2016-11-10 |
| KR102271848B1 (ko) | 2021-07-01 |
| HK1222548A1 (en) | 2017-07-07 |
| US9833431B2 (en) | 2017-12-05 |
| EP3062790B1 (en) | 2023-03-08 |
| US20160228399A1 (en) | 2016-08-11 |
| CA2922575C (en) | 2022-10-11 |
| NZ716765A (en) | 2020-02-28 |
| EP3062790A4 (en) | 2017-05-24 |
| CA2922575A1 (en) | 2015-05-07 |
| AU2014344789A1 (en) | 2016-03-03 |
| CN105792823A (zh) | 2016-07-20 |
| PL3062790T3 (pl) | 2023-05-15 |
| EP3062790A1 (en) | 2016-09-07 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2940890T3 (es) | Combinaciones farmacéuticas para el tratamiento del cáncer | |
| ES2727686T3 (es) | Tratamiento de enfermedades que implican mucina | |
| AU2016204389B2 (en) | Kinase inhibitors for the treatment of cancer | |
| WO2015153814A1 (en) | Sigma-2 receptor ligand drug conjugates as antitumor compounds, methods of synthesis and uses thereof | |
| HK1222548B (en) | Pharmaceutical combinations for the treatment of cancer | |
| HK1205500B (en) | Kinase inhibitors for the treatment of cancer | |
| GB2504550A (en) | Diarylurea compound PQ401 for inhibiting the growth and/or proliferation of cancer stem cells |