DE69837975T2 - Diagnostic imaging method - Google Patents
Diagnostic imaging method Download PDFInfo
- Publication number
- DE69837975T2 DE69837975T2 DE69837975T DE69837975T DE69837975T2 DE 69837975 T2 DE69837975 T2 DE 69837975T2 DE 69837975 T DE69837975 T DE 69837975T DE 69837975 T DE69837975 T DE 69837975T DE 69837975 T2 DE69837975 T2 DE 69837975T2
- Authority
- DE
- Germany
- Prior art keywords
- vector
- groups
- linker
- angiogenesis
- und
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
- 238000000034 method Methods 0.000 title claims abstract description 47
- 238000002059 diagnostic imaging Methods 0.000 title description 10
- 239000013598 vector Substances 0.000 claims abstract description 128
- 125000005647 linker group Chemical group 0.000 claims abstract description 108
- 230000033115 angiogenesis Effects 0.000 claims abstract description 45
- 239000002872 contrast media Substances 0.000 claims abstract description 37
- 239000000203 mixture Substances 0.000 claims abstract description 24
- 241000894007 species Species 0.000 claims abstract description 16
- 210000002889 endothelial cell Anatomy 0.000 claims abstract description 13
- 125000000962 organic group Chemical group 0.000 claims abstract description 9
- 238000011503 in vivo imaging Methods 0.000 claims abstract description 5
- -1 N-hydroxyamino Chemical group 0.000 claims description 69
- 229910052751 metal Chemical group 0.000 claims description 49
- 239000002184 metal Chemical group 0.000 claims description 49
- 102000005962 receptors Human genes 0.000 claims description 35
- 108020003175 receptors Proteins 0.000 claims description 35
- 239000000463 material Substances 0.000 claims description 20
- 239000003814 drug Substances 0.000 claims description 19
- 229940079593 drug Drugs 0.000 claims description 15
- QPCDCPDFJACHGM-UHFFFAOYSA-N N,N-bis{2-[bis(carboxymethyl)amino]ethyl}glycine Chemical class OC(=O)CN(CC(O)=O)CCN(CC(=O)O)CCN(CC(O)=O)CC(O)=O QPCDCPDFJACHGM-UHFFFAOYSA-N 0.000 claims description 12
- 229910052740 iodine Inorganic materials 0.000 claims description 11
- 230000000694 effects Effects 0.000 claims description 10
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical group [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 claims description 9
- 238000001514 detection method Methods 0.000 claims description 9
- 108010044426 integrins Proteins 0.000 claims description 9
- 102000006495 integrins Human genes 0.000 claims description 9
- 239000011630 iodine Substances 0.000 claims description 9
- 108091008605 VEGF receptors Proteins 0.000 claims description 4
- 102000009484 Vascular Endothelial Growth Factor Receptors Human genes 0.000 claims description 4
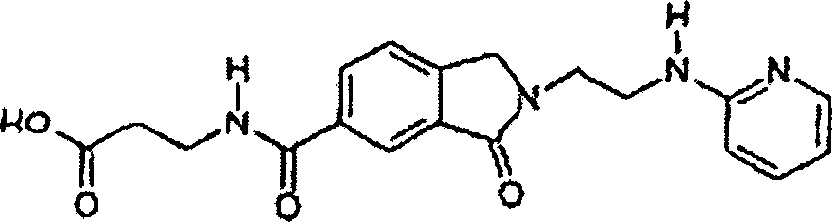
- KKTHJRWWAOTKEI-UHFFFAOYSA-N n-[3-(2-aminoethylamino)-3-oxopropyl]-3-oxo-2-[2-(pyridin-2-ylamino)ethyl]-1h-isoindole-5-carboxamide Chemical compound O=C1C2=CC(C(=O)NCCC(=O)NCCN)=CC=C2CN1CCNC1=CC=CC=N1 KKTHJRWWAOTKEI-UHFFFAOYSA-N 0.000 claims description 3
- 108010042918 Integrin alpha5beta1 Proteins 0.000 claims description 2
- 238000012544 monitoring process Methods 0.000 claims description 2
- 102000004504 Urokinase Plasminogen Activator Receptors Human genes 0.000 claims 2
- 108010042352 Urokinase Plasminogen Activator Receptors Proteins 0.000 claims 2
- 229960005190 phenylalanine Drugs 0.000 claims 2
- 125000000143 2-carboxyethyl group Chemical group [H]OC(=O)C([H])([H])C([H])([H])* 0.000 claims 1
- COLNVLDHVKWLRT-QMMMGPOBSA-N L-phenylalanine Chemical compound OC(=O)[C@@H](N)CC1=CC=CC=C1 COLNVLDHVKWLRT-QMMMGPOBSA-N 0.000 claims 1
- HIRIQFSERGCJCF-UHFFFAOYSA-N n-(6-aminohexyl)-2-[4-[(6,7-dimethoxyquinazolin-4-yl)amino]phenyl]acetamide;hydrochloride Chemical compound Cl.C=12C=C(OC)C(OC)=CC2=NC=NC=1NC1=CC=C(CC(=O)NCCCCCCN)C=C1 HIRIQFSERGCJCF-UHFFFAOYSA-N 0.000 claims 1
- COLNVLDHVKWLRT-UHFFFAOYSA-N phenylalanine Natural products OC(=O)C(N)CC1=CC=CC=C1 COLNVLDHVKWLRT-UHFFFAOYSA-N 0.000 claims 1
- FUXJMHXHGDAHPD-UHFFFAOYSA-N pyrimidine-2-carboxamide Chemical compound NC(=O)C1=NC=CC=N1 FUXJMHXHGDAHPD-UHFFFAOYSA-N 0.000 claims 1
- 150000001875 compounds Chemical class 0.000 description 76
- 239000000975 dye Substances 0.000 description 71
- PXHVJJICTQNCMI-UHFFFAOYSA-N nickel Substances [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 49
- 239000002245 particle Substances 0.000 description 41
- 239000003795 chemical substances by application Substances 0.000 description 35
- 239000000243 solution Substances 0.000 description 34
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 33
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 30
- 239000002738 chelating agent Substances 0.000 description 28
- 238000006243 chemical reaction Methods 0.000 description 28
- XEEYBQQBJWHFJM-UHFFFAOYSA-N iron Substances [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 28
- 108090000623 proteins and genes Proteins 0.000 description 28
- 229910021645 metal ion Inorganic materials 0.000 description 27
- 235000018102 proteins Nutrition 0.000 description 27
- 102000004169 proteins and genes Human genes 0.000 description 27
- 150000002148 esters Chemical class 0.000 description 26
- 238000003384 imaging method Methods 0.000 description 22
- 229920000642 polymer Polymers 0.000 description 22
- 239000000126 substance Substances 0.000 description 22
- 230000027455 binding Effects 0.000 description 21
- 239000010949 copper Substances 0.000 description 21
- 229920001223 polyethylene glycol Polymers 0.000 description 21
- 239000000047 product Substances 0.000 description 21
- 229910052717 sulfur Inorganic materials 0.000 description 21
- 230000015572 biosynthetic process Effects 0.000 description 20
- 229910052688 Gadolinium Inorganic materials 0.000 description 19
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 19
- 239000003153 chemical reaction reagent Substances 0.000 description 18
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 16
- 239000013522 chelant Substances 0.000 description 16
- GUTLYIVDDKVIGB-UHFFFAOYSA-N cobalt atom Chemical compound [Co] GUTLYIVDDKVIGB-UHFFFAOYSA-N 0.000 description 16
- 229920001577 copolymer Polymers 0.000 description 16
- 229910052759 nickel Inorganic materials 0.000 description 16
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical group CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 15
- 125000006850 spacer group Chemical group 0.000 description 15
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 14
- 206010028980 Neoplasm Diseases 0.000 description 14
- 239000002253 acid Substances 0.000 description 14
- 150000001412 amines Chemical class 0.000 description 14
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 14
- UIWYJDYFSGRHKR-UHFFFAOYSA-N gadolinium atom Chemical compound [Gd] UIWYJDYFSGRHKR-UHFFFAOYSA-N 0.000 description 14
- 230000005298 paramagnetic effect Effects 0.000 description 14
- 230000008685 targeting Effects 0.000 description 14
- 210000004027 cell Anatomy 0.000 description 13
- 239000003112 inhibitor Substances 0.000 description 13
- 239000003446 ligand Substances 0.000 description 13
- 229960003330 pentetic acid Drugs 0.000 description 13
- 238000003786 synthesis reaction Methods 0.000 description 13
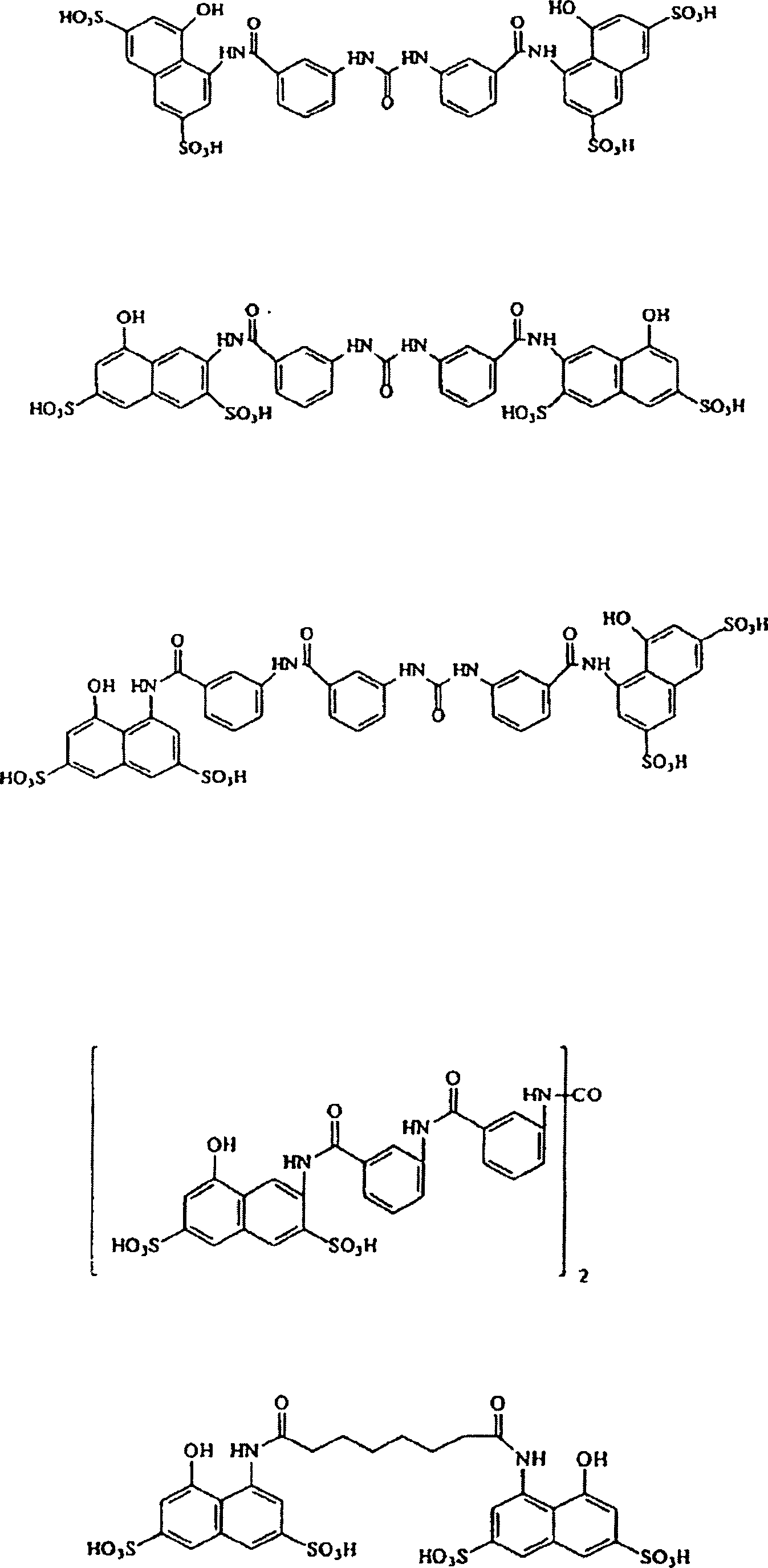
- 0 C*(C(CC1O)=Cc2c1c(*C(c1cc(*)ccc1)=O)cc(*)c2)O Chemical compound C*(C(CC1O)=Cc2c1c(*C(c1cc(*)ccc1)=O)cc(*)c2)O 0.000 description 12
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 12
- 125000003277 amino group Chemical group 0.000 description 12
- 125000003396 thiol group Chemical group [H]S* 0.000 description 12
- 239000000460 chlorine Substances 0.000 description 11
- 229910052802 copper Inorganic materials 0.000 description 11
- RTZKZFJDLAIYFH-UHFFFAOYSA-N ether Substances CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 11
- 125000000524 functional group Chemical group 0.000 description 11
- 229910052757 nitrogen Inorganic materials 0.000 description 11
- 239000002904 solvent Substances 0.000 description 11
- DTQVDTLACAAQTR-UHFFFAOYSA-N trifluoroacetic acid Substances OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 11
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 10
- 229910052742 iron Inorganic materials 0.000 description 10
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 10
- 238000002360 preparation method Methods 0.000 description 10
- 239000011541 reaction mixture Substances 0.000 description 10
- 230000001225 therapeutic effect Effects 0.000 description 10
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 9
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 9
- 239000004037 angiogenesis inhibitor Substances 0.000 description 9
- 229940121369 angiogenesis inhibitor Drugs 0.000 description 9
- 125000004429 atom Chemical group 0.000 description 9
- 201000010099 disease Diseases 0.000 description 9
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 9
- 238000001727 in vivo Methods 0.000 description 9
- 150000002500 ions Chemical class 0.000 description 9
- 239000011159 matrix material Substances 0.000 description 9
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 9
- 229910052760 oxygen Inorganic materials 0.000 description 9
- 108090000765 processed proteins & peptides Proteins 0.000 description 9
- 150000003839 salts Chemical class 0.000 description 9
- 239000000377 silicon dioxide Substances 0.000 description 9
- 229910052720 vanadium Inorganic materials 0.000 description 9
- 102000004190 Enzymes Human genes 0.000 description 8
- 108090000790 Enzymes Proteins 0.000 description 8
- 108091034117 Oligonucleotide Proteins 0.000 description 8
- 150000001299 aldehydes Chemical class 0.000 description 8
- 125000000217 alkyl group Chemical group 0.000 description 8
- 150000001413 amino acids Chemical class 0.000 description 8
- 150000001720 carbohydrates Chemical class 0.000 description 8
- 235000014633 carbohydrates Nutrition 0.000 description 8
- 229910017052 cobalt Inorganic materials 0.000 description 8
- 239000010941 cobalt Substances 0.000 description 8
- 230000008878 coupling Effects 0.000 description 8
- 238000010168 coupling process Methods 0.000 description 8
- 238000005859 coupling reaction Methods 0.000 description 8
- 239000003431 cross linking reagent Substances 0.000 description 8
- 229940088598 enzyme Drugs 0.000 description 8
- 238000003818 flash chromatography Methods 0.000 description 8
- 239000012634 fragment Substances 0.000 description 8
- 230000006870 function Effects 0.000 description 8
- 150000004676 glycans Chemical class 0.000 description 8
- 239000011133 lead Substances 0.000 description 8
- 239000011777 magnesium Substances 0.000 description 8
- 238000004949 mass spectrometry Methods 0.000 description 8
- 238000000816 matrix-assisted laser desorption--ionisation Methods 0.000 description 8
- 229920001282 polysaccharide Polymers 0.000 description 8
- 239000005017 polysaccharide Substances 0.000 description 8
- 229940002612 prodrug Drugs 0.000 description 8
- 239000000651 prodrug Substances 0.000 description 8
- 150000003573 thiols Chemical class 0.000 description 8
- PNWSHHILERSSLF-UHFFFAOYSA-N 4-methylbenzene-1,3-dicarboxylic acid Chemical compound CC1=CC=C(C(O)=O)C=C1C(O)=O PNWSHHILERSSLF-UHFFFAOYSA-N 0.000 description 7
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 7
- 238000005481 NMR spectroscopy Methods 0.000 description 7
- 201000011510 cancer Diseases 0.000 description 7
- 238000004587 chromatography analysis Methods 0.000 description 7
- 239000002502 liposome Substances 0.000 description 7
- 230000005291 magnetic effect Effects 0.000 description 7
- 239000012528 membrane Substances 0.000 description 7
- 210000004379 membrane Anatomy 0.000 description 7
- 230000009257 reactivity Effects 0.000 description 7
- YBJHBAHKTGYVGT-ZKWXMUAHSA-N (+)-Biotin Chemical compound N1C(=O)N[C@@H]2[C@H](CCCCC(=O)O)SC[C@@H]21 YBJHBAHKTGYVGT-ZKWXMUAHSA-N 0.000 description 6
- RBAFCMJBDZWZIV-UHFFFAOYSA-N (2,5-dioxopyrrolidin-1-yl) 4-azido-2-hydroxybenzoate Chemical compound OC1=CC(N=[N+]=[N-])=CC=C1C(=O)ON1C(=O)CCC1=O RBAFCMJBDZWZIV-UHFFFAOYSA-N 0.000 description 6
- LMDZBCPBFSXMTL-UHFFFAOYSA-N 1-ethyl-3-(3-dimethylaminopropyl)carbodiimide Chemical compound CCN=C=NCCCN(C)C LMDZBCPBFSXMTL-UHFFFAOYSA-N 0.000 description 6
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 6
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 6
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 6
- 108010073929 Vascular Endothelial Growth Factor A Proteins 0.000 description 6
- 102100039037 Vascular endothelial growth factor A Human genes 0.000 description 6
- 150000001408 amides Chemical class 0.000 description 6
- 235000001014 amino acid Nutrition 0.000 description 6
- 239000002870 angiogenesis inducing agent Substances 0.000 description 6
- 239000007864 aqueous solution Substances 0.000 description 6
- 239000000987 azo dye Substances 0.000 description 6
- 239000012620 biological material Substances 0.000 description 6
- 210000004204 blood vessel Anatomy 0.000 description 6
- 150000001718 carbodiimides Chemical class 0.000 description 6
- 230000009920 chelation Effects 0.000 description 6
- 235000019439 ethyl acetate Nutrition 0.000 description 6
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 6
- 230000003993 interaction Effects 0.000 description 6
- 229910052755 nonmetal Inorganic materials 0.000 description 6
- 102000004196 processed proteins & peptides Human genes 0.000 description 6
- 238000011160 research Methods 0.000 description 6
- 239000011734 sodium Substances 0.000 description 6
- 239000000725 suspension Substances 0.000 description 6
- VEEGZPWAAPPXRB-BJMVGYQFSA-N (3e)-3-(1h-imidazol-5-ylmethylidene)-1h-indol-2-one Chemical group O=C1NC2=CC=CC=C2\C1=C/C1=CN=CN1 VEEGZPWAAPPXRB-BJMVGYQFSA-N 0.000 description 5
- 108090001008 Avidin Proteins 0.000 description 5
- QOSSAOTZNIDXMA-UHFFFAOYSA-N Dicylcohexylcarbodiimide Chemical compound C1CCCCC1N=C=NC1CCCCC1 QOSSAOTZNIDXMA-UHFFFAOYSA-N 0.000 description 5
- 108090000379 Fibroblast growth factor 2 Proteins 0.000 description 5
- 102000003974 Fibroblast growth factor 2 Human genes 0.000 description 5
- 102100031000 Hepatoma-derived growth factor Human genes 0.000 description 5
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 5
- 208000007766 Kaposi sarcoma Diseases 0.000 description 5
- 238000010976 amide bond formation reaction Methods 0.000 description 5
- 238000004458 analytical method Methods 0.000 description 5
- 125000003118 aryl group Chemical group 0.000 description 5
- 239000002585 base Substances 0.000 description 5
- 230000037396 body weight Effects 0.000 description 5
- 238000012512 characterization method Methods 0.000 description 5
- 229940125782 compound 2 Drugs 0.000 description 5
- 238000004132 cross linking Methods 0.000 description 5
- 239000006185 dispersion Substances 0.000 description 5
- 238000001914 filtration Methods 0.000 description 5
- 108010052188 hepatoma-derived growth factor Proteins 0.000 description 5
- 238000004128 high performance liquid chromatography Methods 0.000 description 5
- 238000005304 joining Methods 0.000 description 5
- 150000002739 metals Chemical class 0.000 description 5
- 210000000056 organ Anatomy 0.000 description 5
- 230000008569 process Effects 0.000 description 5
- 238000000746 purification Methods 0.000 description 5
- 230000002285 radioactive effect Effects 0.000 description 5
- 229910052711 selenium Inorganic materials 0.000 description 5
- 229910052708 sodium Inorganic materials 0.000 description 5
- LPXPTNMVRIOKMN-UHFFFAOYSA-M sodium nitrite Chemical compound [Na+].[O-]N=O LPXPTNMVRIOKMN-UHFFFAOYSA-M 0.000 description 5
- 239000007787 solid Substances 0.000 description 5
- 229910052727 yttrium Inorganic materials 0.000 description 5
- HHLZCENAOIROSL-UHFFFAOYSA-N 2-[4,7-bis(carboxymethyl)-1,4,7,10-tetrazacyclododec-1-yl]acetic acid Chemical compound OC(=O)CN1CCNCCN(CC(O)=O)CCN(CC(O)=O)CC1 HHLZCENAOIROSL-UHFFFAOYSA-N 0.000 description 4
- RZESKRXOCXWCFX-UHFFFAOYSA-N 2-[bis[2-[carboxymethyl-[2-(methylamino)-2-oxoethyl]amino]ethyl]amino]acetic acid Chemical compound CNC(=O)CN(CC(O)=O)CCN(CC(O)=O)CCN(CC(O)=O)CC(=O)NC RZESKRXOCXWCFX-UHFFFAOYSA-N 0.000 description 4
- UKZVGXXDKKIPFF-UHFFFAOYSA-N 3-[[3-oxo-2-[2-(pyridin-2-ylamino)ethyl]-1h-isoindole-5-carbonyl]amino]propanoic acid Chemical compound O=C1C2=CC(C(=O)NCCC(=O)O)=CC=C2CN1CCNC1=CC=CC=N1 UKZVGXXDKKIPFF-UHFFFAOYSA-N 0.000 description 4
- HTTJABKRGRZYRN-UHFFFAOYSA-N Heparin Chemical compound OC1C(NC(=O)C)C(O)OC(COS(O)(=O)=O)C1OC1C(OS(O)(=O)=O)C(O)C(OC2C(C(OS(O)(=O)=O)C(OC3C(C(O)C(O)C(O3)C(O)=O)OS(O)(=O)=O)C(CO)O2)NS(O)(=O)=O)C(C(O)=O)O1 HTTJABKRGRZYRN-UHFFFAOYSA-N 0.000 description 4
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 4
- 101000686934 Mus musculus Prolactin-7D1 Proteins 0.000 description 4
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 4
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 4
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 4
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 4
- 229910052782 aluminium Inorganic materials 0.000 description 4
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 4
- 210000002469 basement membrane Anatomy 0.000 description 4
- 230000001588 bifunctional effect Effects 0.000 description 4
- 229920001222 biopolymer Polymers 0.000 description 4
- 239000007767 bonding agent Substances 0.000 description 4
- 229910052793 cadmium Inorganic materials 0.000 description 4
- BDOSMKKIYDKNTQ-UHFFFAOYSA-N cadmium atom Chemical compound [Cd] BDOSMKKIYDKNTQ-UHFFFAOYSA-N 0.000 description 4
- 125000004432 carbon atom Chemical group C* 0.000 description 4
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 description 4
- 229910052801 chlorine Inorganic materials 0.000 description 4
- 230000005293 ferrimagnetic effect Effects 0.000 description 4
- 230000005294 ferromagnetic effect Effects 0.000 description 4
- 239000003102 growth factor Substances 0.000 description 4
- 229910001385 heavy metal Inorganic materials 0.000 description 4
- 239000005556 hormone Substances 0.000 description 4
- 229940088597 hormone Drugs 0.000 description 4
- 150000004698 iron complex Chemical class 0.000 description 4
- 150000002576 ketones Chemical class 0.000 description 4
- 229910052749 magnesium Inorganic materials 0.000 description 4
- 229910052748 manganese Inorganic materials 0.000 description 4
- 239000011572 manganese Substances 0.000 description 4
- 238000004519 manufacturing process Methods 0.000 description 4
- 239000002609 medium Substances 0.000 description 4
- 239000003068 molecular probe Substances 0.000 description 4
- 150000002843 nonmetals Chemical class 0.000 description 4
- 238000009206 nuclear medicine Methods 0.000 description 4
- 239000000546 pharmaceutical excipient Substances 0.000 description 4
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N phenol group Chemical group C1(=CC=CC=C1)O ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 4
- 229920002635 polyurethane Polymers 0.000 description 4
- 239000004814 polyurethane Substances 0.000 description 4
- 239000002243 precursor Substances 0.000 description 4
- 238000002953 preparative HPLC Methods 0.000 description 4
- 230000009467 reduction Effects 0.000 description 4
- 238000006722 reduction reaction Methods 0.000 description 4
- 125000001424 substituent group Chemical group 0.000 description 4
- 125000004434 sulfur atom Chemical group 0.000 description 4
- VZGDMQKNWNREIO-UHFFFAOYSA-N tetrachloromethane Chemical compound ClC(Cl)(Cl)Cl VZGDMQKNWNREIO-UHFFFAOYSA-N 0.000 description 4
- FYSNRJHAOHDILO-UHFFFAOYSA-N thionyl chloride Chemical compound ClS(Cl)=O FYSNRJHAOHDILO-UHFFFAOYSA-N 0.000 description 4
- 210000001519 tissue Anatomy 0.000 description 4
- 229910052721 tungsten Inorganic materials 0.000 description 4
- GPPXJZIENCGNKB-UHFFFAOYSA-N vanadium Chemical compound [V]#[V] GPPXJZIENCGNKB-UHFFFAOYSA-N 0.000 description 4
- AFVLVVWMAFSXCK-UHFFFAOYSA-N α-cyano-4-hydroxycinnamic acid Chemical compound OC(=O)C(C#N)=CC1=CC=C(O)C=C1 AFVLVVWMAFSXCK-UHFFFAOYSA-N 0.000 description 4
- JRNVQLOKVMWBFR-UHFFFAOYSA-N 1,2-benzenedithiol Chemical class SC1=CC=CC=C1S JRNVQLOKVMWBFR-UHFFFAOYSA-N 0.000 description 3
- BYVHWRKMSXVVAM-UHFFFAOYSA-N 2,3-dihydro-1h-isoindol-2-ium-5-carboxylate Chemical compound OC(=O)C1=CC=C2CNCC2=C1 BYVHWRKMSXVVAM-UHFFFAOYSA-N 0.000 description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 3
- NOWKCMXCCJGMRR-UHFFFAOYSA-N Aziridine Chemical compound C1CN1 NOWKCMXCCJGMRR-UHFFFAOYSA-N 0.000 description 3
- 229910020366 ClO 4 Inorganic materials 0.000 description 3
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 3
- 229910052692 Dysprosium Inorganic materials 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- 101000582950 Homo sapiens Platelet factor 4 Proteins 0.000 description 3
- UQSXHKLRYXJYBZ-UHFFFAOYSA-N Iron oxide Chemical compound [Fe]=O UQSXHKLRYXJYBZ-UHFFFAOYSA-N 0.000 description 3
- 125000003412 L-alanyl group Chemical group [H]N([H])[C@@](C([H])([H])[H])(C(=O)[*])[H] 0.000 description 3
- KDXKERNSBIXSRK-YFKPBYRVSA-N L-lysine Chemical compound NCCCC[C@H](N)C(O)=O KDXKERNSBIXSRK-YFKPBYRVSA-N 0.000 description 3
- 102000007330 LDL Lipoproteins Human genes 0.000 description 3
- 108010007622 LDL Lipoproteins Proteins 0.000 description 3
- 108010085895 Laminin Proteins 0.000 description 3
- 102000007547 Laminin Human genes 0.000 description 3
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 3
- 239000004472 Lysine Substances 0.000 description 3
- 108010038807 Oligopeptides Proteins 0.000 description 3
- 102000015636 Oligopeptides Human genes 0.000 description 3
- 229910019142 PO4 Inorganic materials 0.000 description 3
- 102000013566 Plasminogen Human genes 0.000 description 3
- 108010051456 Plasminogen Proteins 0.000 description 3
- 108010001014 Plasminogen Activators Proteins 0.000 description 3
- 102000001938 Plasminogen Activators Human genes 0.000 description 3
- 229920002732 Polyanhydride Polymers 0.000 description 3
- 229910005965 SO 2 Inorganic materials 0.000 description 3
- 229910052772 Samarium Inorganic materials 0.000 description 3
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 3
- 102000002938 Thrombospondin Human genes 0.000 description 3
- 108060008245 Thrombospondin Proteins 0.000 description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 3
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Chemical compound NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 description 3
- 108010019530 Vascular Endothelial Growth Factors Proteins 0.000 description 3
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 3
- JLCPHMBAVCMARE-UHFFFAOYSA-N [3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-hydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methyl [5-(6-aminopurin-9-yl)-2-(hydroxymethyl)oxolan-3-yl] hydrogen phosphate Polymers Cc1cn(C2CC(OP(O)(=O)OCC3OC(CC3OP(O)(=O)OCC3OC(CC3O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c3nc(N)[nH]c4=O)C(COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3CO)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cc(C)c(=O)[nH]c3=O)n3cc(C)c(=O)[nH]c3=O)n3ccc(N)nc3=O)n3cc(C)c(=O)[nH]c3=O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)O2)c(=O)[nH]c1=O JLCPHMBAVCMARE-UHFFFAOYSA-N 0.000 description 3
- 238000010521 absorption reaction Methods 0.000 description 3
- 239000005557 antagonist Substances 0.000 description 3
- 239000000427 antigen Substances 0.000 description 3
- 230000000890 antigenic effect Effects 0.000 description 3
- 102000036639 antigens Human genes 0.000 description 3
- 108091007433 antigens Proteins 0.000 description 3
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 3
- 239000011616 biotin Substances 0.000 description 3
- 229960002685 biotin Drugs 0.000 description 3
- 235000020958 biotin Nutrition 0.000 description 3
- 229920001400 block copolymer Polymers 0.000 description 3
- 210000004369 blood Anatomy 0.000 description 3
- 239000008280 blood Substances 0.000 description 3
- 229910052796 boron Inorganic materials 0.000 description 3
- 229910052794 bromium Inorganic materials 0.000 description 3
- PFKFTWBEEFSNDU-UHFFFAOYSA-N carbonyldiimidazole Chemical class C1=CN=CN1C(=O)N1C=CN=C1 PFKFTWBEEFSNDU-UHFFFAOYSA-N 0.000 description 3
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 3
- 150000001735 carboxylic acids Chemical class 0.000 description 3
- 229910001914 chlorine tetroxide Inorganic materials 0.000 description 3
- 229910052804 chromium Inorganic materials 0.000 description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 3
- 238000003776 cleavage reaction Methods 0.000 description 3
- 239000012568 clinical material Substances 0.000 description 3
- 229940125904 compound 1 Drugs 0.000 description 3
- 229940126214 compound 3 Drugs 0.000 description 3
- 238000001816 cooling Methods 0.000 description 3
- 239000013078 crystal Substances 0.000 description 3
- 125000004122 cyclic group Chemical group 0.000 description 3
- 125000002704 decyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 3
- 150000002367 halogens Chemical class 0.000 description 3
- 229920000669 heparin Polymers 0.000 description 3
- 229960002897 heparin Drugs 0.000 description 3
- 229910052739 hydrogen Inorganic materials 0.000 description 3
- 230000004054 inflammatory process Effects 0.000 description 3
- 239000010954 inorganic particle Substances 0.000 description 3
- 229920000831 ionic polymer Polymers 0.000 description 3
- WTFXARWRTYJXII-UHFFFAOYSA-N iron(2+);iron(3+);oxygen(2-) Chemical compound [O-2].[O-2].[O-2].[O-2].[Fe+2].[Fe+3].[Fe+3] WTFXARWRTYJXII-UHFFFAOYSA-N 0.000 description 3
- 125000000654 isopropylidene group Chemical group C(C)(C)=* 0.000 description 3
- 229910052747 lanthanoid Inorganic materials 0.000 description 3
- 235000018977 lysine Nutrition 0.000 description 3
- 230000014759 maintenance of location Effects 0.000 description 3
- 239000003550 marker Substances 0.000 description 3
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 3
- 239000003607 modifier Substances 0.000 description 3
- 210000000865 mononuclear phagocyte system Anatomy 0.000 description 3
- 125000001624 naphthyl group Chemical group 0.000 description 3
- 125000003729 nucleotide group Chemical group 0.000 description 3
- 239000003921 oil Substances 0.000 description 3
- 239000012074 organic phase Substances 0.000 description 3
- 239000001301 oxygen Substances 0.000 description 3
- 238000010647 peptide synthesis reaction Methods 0.000 description 3
- VLTRZXGMWDSKGL-UHFFFAOYSA-M perchlorate Chemical group [O-]Cl(=O)(=O)=O VLTRZXGMWDSKGL-UHFFFAOYSA-M 0.000 description 3
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 3
- 239000010452 phosphate Substances 0.000 description 3
- 150000003904 phospholipids Chemical class 0.000 description 3
- 229920001308 poly(aminoacid) Polymers 0.000 description 3
- 229920002627 poly(phosphazenes) Polymers 0.000 description 3
- 229920000728 polyester Polymers 0.000 description 3
- 239000005020 polyethylene terephthalate Substances 0.000 description 3
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 3
- 239000013014 purified material Substances 0.000 description 3
- 229920013730 reactive polymer Polymers 0.000 description 3
- 108091008598 receptor tyrosine kinases Proteins 0.000 description 3
- 102000027426 receptor tyrosine kinases Human genes 0.000 description 3
- 238000010992 reflux Methods 0.000 description 3
- 125000006853 reporter group Chemical group 0.000 description 3
- 230000007017 scission Effects 0.000 description 3
- 229910052710 silicon Inorganic materials 0.000 description 3
- 239000011780 sodium chloride Substances 0.000 description 3
- 239000011343 solid material Substances 0.000 description 3
- 125000000020 sulfo group Chemical group O=S(=O)([*])O[H] 0.000 description 3
- 239000011593 sulfur Substances 0.000 description 3
- FIAFUQMPZJWCLV-UHFFFAOYSA-N suramin Chemical compound OS(=O)(=O)C1=CC(S(O)(=O)=O)=C2C(NC(=O)C3=CC=C(C(=C3)NC(=O)C=3C=C(NC(=O)NC=4C=C(C=CC=4)C(=O)NC=4C(=CC=C(C=4)C(=O)NC=4C5=C(C=C(C=C5C(=CC=4)S(O)(=O)=O)S(O)(=O)=O)S(O)(=O)=O)C)C=CC=3)C)=CC=C(S(O)(=O)=O)C2=C1 FIAFUQMPZJWCLV-UHFFFAOYSA-N 0.000 description 3
- 229920001059 synthetic polymer Polymers 0.000 description 3
- 229940124597 therapeutic agent Drugs 0.000 description 3
- 150000003568 thioethers Chemical group 0.000 description 3
- CNHYKKNIIGEXAY-UHFFFAOYSA-N thiolan-2-imine Chemical compound N=C1CCCS1 CNHYKKNIIGEXAY-UHFFFAOYSA-N 0.000 description 3
- 238000012546 transfer Methods 0.000 description 3
- 229910052725 zinc Inorganic materials 0.000 description 3
- 239000011701 zinc Substances 0.000 description 3
- LWAVGNJLLQSNNN-UHFFFAOYSA-N (2,5-dioxopyrrolidin-1-yl) 4-azidobenzoate Chemical compound C1=CC(N=[N+]=[N-])=CC=C1C(=O)ON1C(=O)CCC1=O LWAVGNJLLQSNNN-UHFFFAOYSA-N 0.000 description 2
- NMWKYTGJWUAZPZ-WWHBDHEGSA-N (4S)-4-[[(4R,7S,10S,16S,19S,25S,28S,31R)-31-[[(2S)-2-[[(1R,6R,9S,12S,18S,21S,24S,27S,30S,33S,36S,39S,42R,47R,53S,56S,59S,62S,65S,68S,71S,76S,79S,85S)-47-[[(2S)-2-[[(2S)-4-amino-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-amino-3-methylbutanoyl]amino]-3-methylbutanoyl]amino]-3-hydroxypropanoyl]amino]-3-(1H-imidazol-4-yl)propanoyl]amino]-3-phenylpropanoyl]amino]-4-oxobutanoyl]amino]-3-carboxypropanoyl]amino]-18-(4-aminobutyl)-27,68-bis(3-amino-3-oxopropyl)-36,71,76-tribenzyl-39-(3-carbamimidamidopropyl)-24-(2-carboxyethyl)-21,56-bis(carboxymethyl)-65,85-bis[(1R)-1-hydroxyethyl]-59-(hydroxymethyl)-62,79-bis(1H-imidazol-4-ylmethyl)-9-methyl-33-(2-methylpropyl)-8,11,17,20,23,26,29,32,35,38,41,48,54,57,60,63,66,69,72,74,77,80,83,86-tetracosaoxo-30-propan-2-yl-3,4,44,45-tetrathia-7,10,16,19,22,25,28,31,34,37,40,49,55,58,61,64,67,70,73,75,78,81,84,87-tetracosazatetracyclo[40.31.14.012,16.049,53]heptaoctacontane-6-carbonyl]amino]-3-methylbutanoyl]amino]-7-(3-carbamimidamidopropyl)-25-(hydroxymethyl)-19-[(4-hydroxyphenyl)methyl]-28-(1H-imidazol-4-ylmethyl)-10-methyl-6,9,12,15,18,21,24,27,30-nonaoxo-16-propan-2-yl-1,2-dithia-5,8,11,14,17,20,23,26,29-nonazacyclodotriacontane-4-carbonyl]amino]-5-[[(2S)-1-[[(2S)-1-[[(2S)-3-carboxy-1-[[(2S)-1-[[(2S)-1-[[(1S)-1-carboxyethyl]amino]-4-methyl-1-oxopentan-2-yl]amino]-4-methyl-1-oxopentan-2-yl]amino]-1-oxopropan-2-yl]amino]-1-oxopropan-2-yl]amino]-3-(1H-imidazol-4-yl)-1-oxopropan-2-yl]amino]-5-oxopentanoic acid Chemical compound CC(C)C[C@H](NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](C)NC(=O)[C@H](Cc1c[nH]cn1)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@@H]1CSSC[C@H](NC(=O)[C@@H](NC(=O)[C@@H]2CSSC[C@@H]3NC(=O)[C@H](Cc4ccccc4)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](NC(=O)[C@H](Cc4c[nH]cn4)NC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@@H]4CCCN4C(=O)[C@H](CSSC[C@H](NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](Cc4c[nH]cn4)NC(=O)[C@H](Cc4ccccc4)NC3=O)[C@@H](C)O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](Cc3ccccc3)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CCCCN)C(=O)N3CCC[C@H]3C(=O)N[C@@H](C)C(=O)N2)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](Cc2ccccc2)NC(=O)[C@H](Cc2c[nH]cn2)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@@H](N)C(C)C)C(C)C)[C@@H](C)O)C(C)C)C(=O)N[C@@H](Cc2c[nH]cn2)C(=O)N[C@@H](CO)C(=O)NCC(=O)N[C@@H](Cc2ccc(O)cc2)C(=O)N[C@@H](C(C)C)C(=O)NCC(=O)N[C@@H](C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N1)C(=O)N[C@@H](C)C(O)=O NMWKYTGJWUAZPZ-WWHBDHEGSA-N 0.000 description 2
- MTZUIIAIAKMWLI-UHFFFAOYSA-N 1,2-diisocyanatobenzene Chemical compound O=C=NC1=CC=CC=C1N=C=O MTZUIIAIAKMWLI-UHFFFAOYSA-N 0.000 description 2
- JIHQDMXYYFUGFV-UHFFFAOYSA-N 1,3,5-triazine Chemical class C1=NC=NC=N1 JIHQDMXYYFUGFV-UHFFFAOYSA-N 0.000 description 2
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 2
- FBMQNRKSAWNXBT-UHFFFAOYSA-N 1,4-diaminoanthracene-9,10-dione Chemical compound O=C1C2=CC=CC=C2C(=O)C2=C1C(N)=CC=C2N FBMQNRKSAWNXBT-UHFFFAOYSA-N 0.000 description 2
- RKDVKSZUMVYZHH-UHFFFAOYSA-N 1,4-dioxane-2,5-dione Chemical group O=C1COC(=O)CO1 RKDVKSZUMVYZHH-UHFFFAOYSA-N 0.000 description 2
- 125000001140 1,4-phenylene group Chemical group [H]C1=C([H])C([*:2])=C([H])C([H])=C1[*:1] 0.000 description 2
- MEZJQXVOMGUAMP-UHFFFAOYSA-N 1-(2-methylnaphthalen-1-yl)pyrrole-2,5-dione Chemical class CC1=CC=C2C=CC=CC2=C1N1C(=O)C=CC1=O MEZJQXVOMGUAMP-UHFFFAOYSA-N 0.000 description 2
- CULQNACJHGHAER-UHFFFAOYSA-N 1-[4-[(2-iodoacetyl)amino]benzoyl]oxy-2,5-dioxopyrrolidine-3-sulfonic acid Chemical compound O=C1C(S(=O)(=O)O)CC(=O)N1OC(=O)C1=CC=C(NC(=O)CI)C=C1 CULQNACJHGHAER-UHFFFAOYSA-N 0.000 description 2
- YOSZEPWSVKKQOV-UHFFFAOYSA-N 12h-benzo[a]phenoxazine Chemical compound C1=CC=CC2=C3NC4=CC=CC=C4OC3=CC=C21 YOSZEPWSVKKQOV-UHFFFAOYSA-N 0.000 description 2
- XTBAPWCYTNCZTO-UHFFFAOYSA-N 1H-isoindolone Natural products C1=CC=C2C(=O)N=CC2=C1 XTBAPWCYTNCZTO-UHFFFAOYSA-N 0.000 description 2
- UEJJHQNACJXSKW-UHFFFAOYSA-N 2-(2,6-dioxopiperidin-3-yl)-1H-isoindole-1,3(2H)-dione Chemical compound O=C1C2=CC=CC=C2C(=O)N1C1CCC(=O)NC1=O UEJJHQNACJXSKW-UHFFFAOYSA-N 0.000 description 2
- WOXFMYVTSLAQMO-UHFFFAOYSA-N 2-Pyridinemethanamine Chemical compound NCC1=CC=CC=N1 WOXFMYVTSLAQMO-UHFFFAOYSA-N 0.000 description 2
- SQKUFYLUXROIFM-UHFFFAOYSA-N 2-[2-[carboxymethyl-[[3-hydroxy-2-methyl-5-(phosphonooxymethyl)pyridin-4-yl]methyl]amino]ethyl-[[3-hydroxy-2-methyl-5-(phosphonooxymethyl)pyridin-4-yl]methyl]amino]acetic acid Chemical compound CC1=NC=C(COP(O)(O)=O)C(CN(CCN(CC(O)=O)CC=2C(=C(C)N=CC=2COP(O)(O)=O)O)CC(O)=O)=C1O SQKUFYLUXROIFM-UHFFFAOYSA-N 0.000 description 2
- RAZLJUXJEOEYAM-UHFFFAOYSA-N 2-[bis[2-(2,6-dioxomorpholin-4-yl)ethyl]azaniumyl]acetate Chemical compound C1C(=O)OC(=O)CN1CCN(CC(=O)O)CCN1CC(=O)OC(=O)C1 RAZLJUXJEOEYAM-UHFFFAOYSA-N 0.000 description 2
- HJVAVGOPTDJYOJ-UHFFFAOYSA-N 2-amino-4,5-dimethoxybenzoic acid Chemical compound COC1=CC(N)=C(C(O)=O)C=C1OC HJVAVGOPTDJYOJ-UHFFFAOYSA-N 0.000 description 2
- IJVRPNIWWODHHA-UHFFFAOYSA-N 2-cyanoprop-2-enoic acid Chemical compound OC(=O)C(=C)C#N IJVRPNIWWODHHA-UHFFFAOYSA-N 0.000 description 2
- 125000000175 2-thienyl group Chemical group S1C([*])=C([H])C([H])=C1[H] 0.000 description 2
- KIUMMUBSPKGMOY-UHFFFAOYSA-N 3,3'-Dithiobis(6-nitrobenzoic acid) Chemical compound C1=C([N+]([O-])=O)C(C(=O)O)=CC(SSC=2C=C(C(=CC=2)[N+]([O-])=O)C(O)=O)=C1 KIUMMUBSPKGMOY-UHFFFAOYSA-N 0.000 description 2
- FZPBXNLCWHEGFO-UHFFFAOYSA-N 4-[2-(4-carboxyphenoxy)propan-2-yloxy]benzoic acid Chemical compound C(=O)(O)C1=CC=C(OC(C)(C)OC2=CC=C(C=C2)C(=O)O)C=C1 FZPBXNLCWHEGFO-UHFFFAOYSA-N 0.000 description 2
- NGSWKAQJJWESNS-UHFFFAOYSA-N 4-coumaric acid Chemical compound OC(=O)C=CC1=CC=C(O)C=C1 NGSWKAQJJWESNS-UHFFFAOYSA-N 0.000 description 2
- YYROPELSRYBVMQ-UHFFFAOYSA-N 4-toluenesulfonyl chloride Chemical compound CC1=CC=C(S(Cl)(=O)=O)C=C1 YYROPELSRYBVMQ-UHFFFAOYSA-N 0.000 description 2
- 102400000068 Angiostatin Human genes 0.000 description 2
- 108010079709 Angiostatins Proteins 0.000 description 2
- 201000001320 Atherosclerosis Diseases 0.000 description 2
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 2
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 2
- 102000000844 Cell Surface Receptors Human genes 0.000 description 2
- 108010001857 Cell Surface Receptors Proteins 0.000 description 2
- 229910052684 Cerium Inorganic materials 0.000 description 2
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 2
- 239000004971 Cross linker Substances 0.000 description 2
- 229920001651 Cyanoacrylate Polymers 0.000 description 2
- RGHNJXZEOKUKBD-SQOUGZDYSA-N D-gluconic acid Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C(O)=O RGHNJXZEOKUKBD-SQOUGZDYSA-N 0.000 description 2
- BWGNESOTFCXPMA-UHFFFAOYSA-N Dihydrogen disulfide Chemical compound SS BWGNESOTFCXPMA-UHFFFAOYSA-N 0.000 description 2
- 108010024212 E-Selectin Proteins 0.000 description 2
- 102100023471 E-selectin Human genes 0.000 description 2
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 2
- 102000012085 Endoglin Human genes 0.000 description 2
- 108010036395 Endoglin Proteins 0.000 description 2
- 102100038083 Endosialin Human genes 0.000 description 2
- 101710144543 Endosialin Proteins 0.000 description 2
- 108010079505 Endostatins Proteins 0.000 description 2
- BRLQWZUYTZBJKN-UHFFFAOYSA-N Epichlorohydrin Chemical compound ClCC1CO1 BRLQWZUYTZBJKN-UHFFFAOYSA-N 0.000 description 2
- 102400001368 Epidermal growth factor Human genes 0.000 description 2
- 101800003838 Epidermal growth factor Proteins 0.000 description 2
- 229910052691 Erbium Inorganic materials 0.000 description 2
- PIICEJLVQHRZGT-UHFFFAOYSA-N Ethylenediamine Chemical compound NCCN PIICEJLVQHRZGT-UHFFFAOYSA-N 0.000 description 2
- 229910052693 Europium Inorganic materials 0.000 description 2
- 101800003778 Fibrinopeptide B Proteins 0.000 description 2
- 102000018233 Fibroblast Growth Factor Human genes 0.000 description 2
- 108050007372 Fibroblast Growth Factor Proteins 0.000 description 2
- 108090000378 Fibroblast growth factor 3 Proteins 0.000 description 2
- 102100028043 Fibroblast growth factor 3 Human genes 0.000 description 2
- 108090000368 Fibroblast growth factor 8 Proteins 0.000 description 2
- 102100037362 Fibronectin Human genes 0.000 description 2
- 108010067306 Fibronectins Proteins 0.000 description 2
- ZHNUHDYFZUAESO-UHFFFAOYSA-N Formamide Chemical compound NC=O ZHNUHDYFZUAESO-UHFFFAOYSA-N 0.000 description 2
- 229910003317 GdCl3 Inorganic materials 0.000 description 2
- 206010018338 Glioma Diseases 0.000 description 2
- 229920002683 Glycosaminoglycan Polymers 0.000 description 2
- IQUHNCOJRJBMSU-UHFFFAOYSA-N H3HP-DO3A Chemical compound CC(O)CN1CCN(CC(O)=O)CCN(CC(O)=O)CCN(CC(O)=O)CC1 IQUHNCOJRJBMSU-UHFFFAOYSA-N 0.000 description 2
- 108090000100 Hepatocyte Growth Factor Proteins 0.000 description 2
- 102100021866 Hepatocyte growth factor Human genes 0.000 description 2
- 229910052689 Holmium Inorganic materials 0.000 description 2
- 101000595923 Homo sapiens Placenta growth factor Proteins 0.000 description 2
- 206010061218 Inflammation Diseases 0.000 description 2
- 102000006992 Interferon-alpha Human genes 0.000 description 2
- 108010047761 Interferon-alpha Proteins 0.000 description 2
- 108010063738 Interleukins Proteins 0.000 description 2
- 102000015696 Interleukins Human genes 0.000 description 2
- 229910052765 Lutetium Inorganic materials 0.000 description 2
- PWHULOQIROXLJO-UHFFFAOYSA-N Manganese Chemical compound [Mn] PWHULOQIROXLJO-UHFFFAOYSA-N 0.000 description 2
- 206010027476 Metastases Diseases 0.000 description 2
- CERQOIWHTDAKMF-UHFFFAOYSA-N Methacrylic acid Chemical compound CC(=C)C(O)=O CERQOIWHTDAKMF-UHFFFAOYSA-N 0.000 description 2
- VVQNEPGJFQJSBK-UHFFFAOYSA-N Methyl methacrylate Chemical compound COC(=O)C(C)=C VVQNEPGJFQJSBK-UHFFFAOYSA-N 0.000 description 2
- 125000001429 N-terminal alpha-amino-acid group Chemical group 0.000 description 2
- 229930192627 Naphthoquinone Natural products 0.000 description 2
- 229910052779 Neodymium Inorganic materials 0.000 description 2
- 206010061902 Pancreatic neoplasm Diseases 0.000 description 2
- 102000007079 Peptide Fragments Human genes 0.000 description 2
- 108010033276 Peptide Fragments Proteins 0.000 description 2
- 102100035194 Placenta growth factor Human genes 0.000 description 2
- 102000004211 Platelet factor 4 Human genes 0.000 description 2
- 108090000778 Platelet factor 4 Proteins 0.000 description 2
- 108010038512 Platelet-Derived Growth Factor Proteins 0.000 description 2
- 102000010780 Platelet-Derived Growth Factor Human genes 0.000 description 2
- 108010039918 Polylysine Proteins 0.000 description 2
- 229920000388 Polyphosphate Polymers 0.000 description 2
- 229910052777 Praseodymium Inorganic materials 0.000 description 2
- 208000000236 Prostatic Neoplasms Diseases 0.000 description 2
- 241000700159 Rattus Species 0.000 description 2
- 239000008156 Ringer's lactate solution Substances 0.000 description 2
- 239000002262 Schiff base Substances 0.000 description 2
- 150000004753 Schiff bases Chemical class 0.000 description 2
- 102000003800 Selectins Human genes 0.000 description 2
- 108090000184 Selectins Proteins 0.000 description 2
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 2
- 102000013275 Somatomedins Human genes 0.000 description 2
- 229920002472 Starch Polymers 0.000 description 2
- 108010090804 Streptavidin Proteins 0.000 description 2
- 229910052771 Terbium Inorganic materials 0.000 description 2
- KKEYFWRCBNTPAC-UHFFFAOYSA-N Terephthalic acid Chemical group OC(=O)C1=CC=C(C(O)=O)C=C1 KKEYFWRCBNTPAC-UHFFFAOYSA-N 0.000 description 2
- 108090000190 Thrombin Proteins 0.000 description 2
- 229910052775 Thulium Inorganic materials 0.000 description 2
- 102100031372 Thymidine phosphorylase Human genes 0.000 description 2
- 108700023160 Thymidine phosphorylases Proteins 0.000 description 2
- 102000005354 Tissue Inhibitor of Metalloproteinase-2 Human genes 0.000 description 2
- 108010031372 Tissue Inhibitor of Metalloproteinase-2 Proteins 0.000 description 2
- 102000005876 Tissue Inhibitor of Metalloproteinases Human genes 0.000 description 2
- 108010005246 Tissue Inhibitor of Metalloproteinases Proteins 0.000 description 2
- GYDJEQRTZSCIOI-UHFFFAOYSA-N Tranexamic acid Chemical compound NCC1CCC(C(O)=O)CC1 GYDJEQRTZSCIOI-UHFFFAOYSA-N 0.000 description 2
- 102400001320 Transforming growth factor alpha Human genes 0.000 description 2
- 101800004564 Transforming growth factor alpha Proteins 0.000 description 2
- 108060008682 Tumor Necrosis Factor Proteins 0.000 description 2
- 102000000852 Tumor Necrosis Factor-alpha Human genes 0.000 description 2
- 102000016548 Vascular Endothelial Growth Factor Receptor-1 Human genes 0.000 description 2
- 108010053096 Vascular Endothelial Growth Factor Receptor-1 Proteins 0.000 description 2
- 108010031318 Vitronectin Proteins 0.000 description 2
- 102100035140 Vitronectin Human genes 0.000 description 2
- 229910052769 Ytterbium Inorganic materials 0.000 description 2
- VRGWBRLULZUWAJ-XFFXIZSCSA-N [(2s)-2-[(1r,3z,5s,8z,12z,15s)-5,17-dihydroxy-4,8,12,15-tetramethyl-16-oxo-18-bicyclo[13.3.0]octadeca-3,8,12,17-tetraenyl]propyl] acetate Chemical compound C1\C=C(C)/CC\C=C(C)/CC[C@H](O)\C(C)=C/C[C@@H]2C([C@@H](COC(C)=O)C)=C(O)C(=O)[C@]21C VRGWBRLULZUWAJ-XFFXIZSCSA-N 0.000 description 2
- 125000000738 acetamido group Chemical group [H]C([H])([H])C(=O)N([H])[*] 0.000 description 2
- YRKCREAYFQTBPV-UHFFFAOYSA-N acetylacetone Chemical compound CC(=O)CC(C)=O YRKCREAYFQTBPV-UHFFFAOYSA-N 0.000 description 2
- 150000007513 acids Chemical class 0.000 description 2
- 230000003213 activating effect Effects 0.000 description 2
- 230000002411 adverse Effects 0.000 description 2
- 150000001298 alcohols Chemical class 0.000 description 2
- 150000001350 alkyl halides Chemical class 0.000 description 2
- 239000002168 alkylating agent Substances 0.000 description 2
- 229940100198 alkylating agent Drugs 0.000 description 2
- 239000004411 aluminium Substances 0.000 description 2
- 150000001409 amidines Chemical class 0.000 description 2
- 239000012491 analyte Substances 0.000 description 2
- 239000001000 anthraquinone dye Substances 0.000 description 2
- 230000000259 anti-tumor effect Effects 0.000 description 2
- 239000003963 antioxidant agent Substances 0.000 description 2
- 238000000149 argon plasma sintering Methods 0.000 description 2
- FZCSTZYAHCUGEM-UHFFFAOYSA-N aspergillomarasmine B Natural products OC(=O)CNC(C(O)=O)CNC(C(O)=O)CC(O)=O FZCSTZYAHCUGEM-UHFFFAOYSA-N 0.000 description 2
- 125000005605 benzo group Chemical group 0.000 description 2
- NRIMHVFWRMABGJ-UHFFFAOYSA-N bicyclo[2.2.1]hepta-2,5-diene-2,3-dicarboxylic acid Chemical compound C1C2C(C(=O)O)=C(C(O)=O)C1C=C2 NRIMHVFWRMABGJ-UHFFFAOYSA-N 0.000 description 2
- 238000006065 biodegradation reaction Methods 0.000 description 2
- 230000004071 biological effect Effects 0.000 description 2
- 238000006664 bond formation reaction Methods 0.000 description 2
- 210000004556 brain Anatomy 0.000 description 2
- 239000012267 brine Substances 0.000 description 2
- 239000000872 buffer Substances 0.000 description 2
- 239000000337 buffer salt Substances 0.000 description 2
- WERYXYBDKMZEQL-UHFFFAOYSA-N butane-1,4-diol Chemical compound OCCCCO WERYXYBDKMZEQL-UHFFFAOYSA-N 0.000 description 2
- 229910052799 carbon Inorganic materials 0.000 description 2
- 235000011089 carbon dioxide Nutrition 0.000 description 2
- 150000007942 carboxylates Chemical class 0.000 description 2
- 125000002057 carboxymethyl group Chemical group [H]OC(=O)C([H])([H])[*] 0.000 description 2
- 230000015556 catabolic process Effects 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- 125000003636 chemical group Chemical group 0.000 description 2
- 239000011651 chromium Substances 0.000 description 2
- 230000000295 complement effect Effects 0.000 description 2
- 229940125773 compound 10 Drugs 0.000 description 2
- 230000021615 conjugation Effects 0.000 description 2
- 229940039231 contrast media Drugs 0.000 description 2
- 238000013270 controlled release Methods 0.000 description 2
- 230000001276 controlling effect Effects 0.000 description 2
- 239000006071 cream Substances 0.000 description 2
- 238000000354 decomposition reaction Methods 0.000 description 2
- 238000006731 degradation reaction Methods 0.000 description 2
- 239000000412 dendrimer Substances 0.000 description 2
- 229920000736 dendritic polymer Polymers 0.000 description 2
- 238000003745 diagnosis Methods 0.000 description 2
- 150000004985 diamines Chemical class 0.000 description 2
- 150000002009 diols Chemical group 0.000 description 2
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N diphenyl Chemical group C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 description 2
- 238000001647 drug administration Methods 0.000 description 2
- 238000002593 electrical impedance tomography Methods 0.000 description 2
- 238000005516 engineering process Methods 0.000 description 2
- 229940116977 epidermal growth factor Drugs 0.000 description 2
- HKASNZKRIQURIX-BZDVOYDHSA-N ethyl (2r)-2-[2-[[(2r)-1-ethoxy-1-oxo-3-sulfanylpropan-2-yl]amino]ethylamino]-3-sulfanylpropanoate;dihydrochloride Chemical compound Cl.Cl.CCOC(=O)[C@H](CS)NCCN[C@@H](CS)C(=O)OCC HKASNZKRIQURIX-BZDVOYDHSA-N 0.000 description 2
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 2
- 230000005284 excitation Effects 0.000 description 2
- 229940126864 fibroblast growth factor Drugs 0.000 description 2
- GNBHRKFJIUUOQI-UHFFFAOYSA-N fluorescein Chemical compound O1C(=O)C2=CC=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 GNBHRKFJIUUOQI-UHFFFAOYSA-N 0.000 description 2
- 239000007850 fluorescent dye Substances 0.000 description 2
- NGGMYCMLYOUNGM-CSDLUJIJSA-N fumagillin Chemical class C([C@H]([C@H]([C@@H]1[C@]2(C)[C@H](O2)CC=C(C)C)OC)OC(=O)\C=C\C=C\C=C\C=C\C(O)=O)C[C@@]21CO2 NGGMYCMLYOUNGM-CSDLUJIJSA-N 0.000 description 2
- VRGWBRLULZUWAJ-UHFFFAOYSA-N fusaproliferin Natural products C1C=C(C)CCC=C(C)CCC(O)C(C)=CCC2C(C(COC(C)=O)C)=C(O)C(=O)C21C VRGWBRLULZUWAJ-UHFFFAOYSA-N 0.000 description 2
- 229940075613 gadolinium oxide Drugs 0.000 description 2
- 229910001938 gadolinium oxide Inorganic materials 0.000 description 2
- MEANOSLIBWSCIT-UHFFFAOYSA-K gadolinium trichloride Chemical compound Cl[Gd](Cl)Cl MEANOSLIBWSCIT-UHFFFAOYSA-K 0.000 description 2
- CMIHHWBVHJVIGI-UHFFFAOYSA-N gadolinium(iii) oxide Chemical compound [O-2].[O-2].[O-2].[Gd+3].[Gd+3] CMIHHWBVHJVIGI-UHFFFAOYSA-N 0.000 description 2
- 239000007789 gas Substances 0.000 description 2
- 230000012010 growth Effects 0.000 description 2
- 229910052736 halogen Inorganic materials 0.000 description 2
- 125000005843 halogen group Chemical group 0.000 description 2
- 230000036541 health Effects 0.000 description 2
- 238000010438 heat treatment Methods 0.000 description 2
- 125000000623 heterocyclic group Chemical group 0.000 description 2
- 102000052196 human PF4 Human genes 0.000 description 2
- 229920002674 hyaluronan Polymers 0.000 description 2
- KIUKXJAPPMFGSW-MNSSHETKSA-N hyaluronan Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)C1O[C@H]1[C@H](O)[C@@H](O)[C@H](O[C@H]2[C@@H](C(O[C@H]3[C@@H]([C@@H](O)[C@H](O)[C@H](O3)C(O)=O)O)[C@H](O)[C@@H](CO)O2)NC(C)=O)[C@@H](C(O)=O)O1 KIUKXJAPPMFGSW-MNSSHETKSA-N 0.000 description 2
- 229940099552 hyaluronan Drugs 0.000 description 2
- 239000001257 hydrogen Substances 0.000 description 2
- 150000002463 imidates Chemical class 0.000 description 2
- 125000002883 imidazolyl group Chemical group 0.000 description 2
- 238000010348 incorporation Methods 0.000 description 2
- 230000002401 inhibitory effect Effects 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- 229940047122 interleukins Drugs 0.000 description 2
- 125000003010 ionic group Chemical group 0.000 description 2
- 235000013980 iron oxide Nutrition 0.000 description 2
- 239000012948 isocyanate Substances 0.000 description 2
- 150000002513 isocyanates Chemical class 0.000 description 2
- 150000002540 isothiocyanates Chemical class 0.000 description 2
- ZLVXBBHTMQJRSX-VMGNSXQWSA-N jdtic Chemical compound C1([C@]2(C)CCN(C[C@@H]2C)C[C@H](C(C)C)NC(=O)[C@@H]2NCC3=CC(O)=CC=C3C2)=CC=CC(O)=C1 ZLVXBBHTMQJRSX-VMGNSXQWSA-N 0.000 description 2
- JJTUDXZGHPGLLC-UHFFFAOYSA-N lactide Chemical compound CC1OC(=O)C(C)OC1=O JJTUDXZGHPGLLC-UHFFFAOYSA-N 0.000 description 2
- 150000002602 lanthanoids Chemical class 0.000 description 2
- 229910052746 lanthanum Inorganic materials 0.000 description 2
- WABPQHHGFIMREM-UHFFFAOYSA-N lead(0) Chemical compound [Pb] WABPQHHGFIMREM-UHFFFAOYSA-N 0.000 description 2
- 208000032839 leukemia Diseases 0.000 description 2
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 2
- 208000020816 lung neoplasm Diseases 0.000 description 2
- 239000006249 magnetic particle Substances 0.000 description 2
- 230000003211 malignant effect Effects 0.000 description 2
- 238000001906 matrix-assisted laser desorption--ionisation mass spectrometry Methods 0.000 description 2
- 230000007246 mechanism Effects 0.000 description 2
- 201000001441 melanoma Diseases 0.000 description 2
- 239000003475 metalloproteinase inhibitor Substances 0.000 description 2
- XJRBAMWJDBPFIM-UHFFFAOYSA-N methyl vinyl ether Chemical compound COC=C XJRBAMWJDBPFIM-UHFFFAOYSA-N 0.000 description 2
- 239000000693 micelle Substances 0.000 description 2
- 229910052750 molybdenum Inorganic materials 0.000 description 2
- 210000004165 myocardium Anatomy 0.000 description 2
- LKKPNUDVOYAOBB-UHFFFAOYSA-N naphthalocyanine Chemical compound N1C(N=C2C3=CC4=CC=CC=C4C=C3C(N=C3C4=CC5=CC=CC=C5C=C4C(=N4)N3)=N2)=C(C=C2C(C=CC=C2)=C2)C2=C1N=C1C2=CC3=CC=CC=C3C=C2C4=N1 LKKPNUDVOYAOBB-UHFFFAOYSA-N 0.000 description 2
- 150000002791 naphthoquinones Chemical class 0.000 description 2
- 230000007935 neutral effect Effects 0.000 description 2
- 239000012299 nitrogen atmosphere Substances 0.000 description 2
- 125000004433 nitrogen atom Chemical group N* 0.000 description 2
- 108020004707 nucleic acids Proteins 0.000 description 2
- 150000007523 nucleic acids Chemical class 0.000 description 2
- 102000039446 nucleic acids Human genes 0.000 description 2
- 239000012038 nucleophile Substances 0.000 description 2
- 239000002773 nucleotide Substances 0.000 description 2
- 229920001542 oligosaccharide Polymers 0.000 description 2
- 150000002482 oligosaccharides Chemical class 0.000 description 2
- 125000004430 oxygen atom Chemical group O* 0.000 description 2
- 125000003854 p-chlorophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C([H])=C1Cl 0.000 description 2
- 239000003182 parenteral nutrition solution Substances 0.000 description 2
- 239000008363 phosphate buffer Substances 0.000 description 2
- XHXFXVLFKHQFAL-UHFFFAOYSA-N phosphoryl trichloride Chemical compound ClP(Cl)(Cl)=O XHXFXVLFKHQFAL-UHFFFAOYSA-N 0.000 description 2
- IEQIEDJGQAUEQZ-UHFFFAOYSA-N phthalocyanine Chemical compound N1C(N=C2C3=CC=CC=C3C(N=C3C4=CC=CC=C4C(=N4)N3)=N2)=C(C=CC=C2)C2=C1N=C1C2=CC=CC=C2C4=N1 IEQIEDJGQAUEQZ-UHFFFAOYSA-N 0.000 description 2
- 239000001007 phthalocyanine dye Substances 0.000 description 2
- 230000003169 placental effect Effects 0.000 description 2
- 229940127126 plasminogen activator Drugs 0.000 description 2
- 102000005162 pleiotrophin Human genes 0.000 description 2
- 229920000768 polyamine Polymers 0.000 description 2
- 229920000570 polyether Polymers 0.000 description 2
- 229920000139 polyethylene terephthalate Polymers 0.000 description 2
- 229920000656 polylysine Polymers 0.000 description 2
- 229920001184 polypeptide Polymers 0.000 description 2
- 239000001205 polyphosphate Substances 0.000 description 2
- 235000011176 polyphosphates Nutrition 0.000 description 2
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 2
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 2
- 229930185346 proliferin Natural products 0.000 description 2
- 230000009145 protein modification Effects 0.000 description 2
- 230000017854 proteolysis Effects 0.000 description 2
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 2
- WVIICGIFSIBFOG-UHFFFAOYSA-N pyrylium Chemical compound C1=CC=[O+]C=C1 WVIICGIFSIBFOG-UHFFFAOYSA-N 0.000 description 2
- 230000002829 reductive effect Effects 0.000 description 2
- 229910052702 rhenium Inorganic materials 0.000 description 2
- 206010039073 rheumatoid arthritis Diseases 0.000 description 2
- SMQUZDBALVYZAC-UHFFFAOYSA-N salicylaldehyde Chemical compound OC1=CC=CC=C1C=O SMQUZDBALVYZAC-UHFFFAOYSA-N 0.000 description 2
- 238000012216 screening Methods 0.000 description 2
- 239000010703 silicon Substances 0.000 description 2
- 238000002603 single-photon emission computed tomography Methods 0.000 description 2
- 235000010288 sodium nitrite Nutrition 0.000 description 2
- VUFNRPJNRFOTGK-UHFFFAOYSA-M sodium;1-[4-[(2,5-dioxopyrrol-1-yl)methyl]cyclohexanecarbonyl]oxy-2,5-dioxopyrrolidine-3-sulfonate Chemical compound [Na+].O=C1C(S(=O)(=O)[O-])CC(=O)N1OC(=O)C1CCC(CN2C(C=CC2=O)=O)CC1 VUFNRPJNRFOTGK-UHFFFAOYSA-M 0.000 description 2
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 2
- 238000001228 spectrum Methods 0.000 description 2
- 208000035736 spondylodysplastic type Ehlers-Danlos syndrome Diseases 0.000 description 2
- 239000003381 stabilizer Substances 0.000 description 2
- 235000019698 starch Nutrition 0.000 description 2
- 239000008107 starch Substances 0.000 description 2
- 239000007858 starting material Substances 0.000 description 2
- 125000000472 sulfonyl group Chemical group *S(*)(=O)=O 0.000 description 2
- YBBRCQOCSYXUOC-UHFFFAOYSA-N sulfuryl dichloride Chemical compound ClS(Cl)(=O)=O YBBRCQOCSYXUOC-UHFFFAOYSA-N 0.000 description 2
- 229960005314 suramin Drugs 0.000 description 2
- 229910052714 tellurium Inorganic materials 0.000 description 2
- NTGJTYUHTCIKHI-UHFFFAOYSA-N tert-butyl 3-[[3-oxo-2-[2-(pyridin-2-ylamino)ethyl]-1h-isoindole-5-carbonyl]amino]propanoate Chemical compound O=C1C2=CC(C(=O)NCCC(=O)OC(C)(C)C)=CC=C2CN1CCNC1=CC=CC=N1 NTGJTYUHTCIKHI-UHFFFAOYSA-N 0.000 description 2
- 125000003698 tetramethyl group Chemical group [H]C([H])([H])* 0.000 description 2
- 229960003433 thalidomide Drugs 0.000 description 2
- 238000002560 therapeutic procedure Methods 0.000 description 2
- 150000007970 thio esters Chemical group 0.000 description 2
- CWERGRDVMFNCDR-UHFFFAOYSA-N thioglycolic acid Chemical compound OC(=O)CS CWERGRDVMFNCDR-UHFFFAOYSA-N 0.000 description 2
- UMGDCJDMYOKAJW-UHFFFAOYSA-N thiourea Chemical compound NC(N)=S UMGDCJDMYOKAJW-UHFFFAOYSA-N 0.000 description 2
- 229910052723 transition metal Inorganic materials 0.000 description 2
- 150000003624 transition metals Chemical class 0.000 description 2
- 238000000101 transmission high energy electron diffraction Methods 0.000 description 2
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 description 2
- QVWDCTQRORVHHT-UHFFFAOYSA-N tropone Chemical compound O=C1C=CC=CC=C1 QVWDCTQRORVHHT-UHFFFAOYSA-N 0.000 description 2
- 230000004614 tumor growth Effects 0.000 description 2
- VBEQCZHXXJYVRD-GACYYNSASA-N uroanthelone Chemical compound C([C@@H](C(=O)N[C@H](C(=O)N[C@@H](CS)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CS)C(=O)N[C@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)NCC(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H](CO)C(=O)NCC(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CS)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(O)=O)C(C)C)[C@@H](C)O)NC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@@H](NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H](CCSC)NC(=O)[C@H](CS)NC(=O)[C@@H](NC(=O)CNC(=O)CNC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CS)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)CNC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CS)NC(=O)CNC(=O)[C@H]1N(CCC1)C(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC(N)=O)C(C)C)[C@@H](C)CC)C1=CC=C(O)C=C1 VBEQCZHXXJYVRD-GACYYNSASA-N 0.000 description 2
- 239000003981 vehicle Substances 0.000 description 2
- DGVVWUTYPXICAM-UHFFFAOYSA-N β‐Mercaptoethanol Chemical compound OCCS DGVVWUTYPXICAM-UHFFFAOYSA-N 0.000 description 2
- NGGMYCMLYOUNGM-UHFFFAOYSA-N (-)-fumagillin Natural products O1C(CC=C(C)C)C1(C)C1C(OC)C(OC(=O)C=CC=CC=CC=CC(O)=O)CCC21CO2 NGGMYCMLYOUNGM-UHFFFAOYSA-N 0.000 description 1
- ILKQVTIMOGNSAS-UHFFFAOYSA-N (2,5-dioxopyrrolidin-1-yl) 2-(7-amino-4-methyl-2-oxochromen-3-yl)acetate Chemical compound O=C1OC=2C=C(N)C=CC=2C(C)=C1CC(=O)ON1C(=O)CCC1=O ILKQVTIMOGNSAS-UHFFFAOYSA-N 0.000 description 1
- FLCQLSRLQIPNLM-UHFFFAOYSA-N (2,5-dioxopyrrolidin-1-yl) 2-acetylsulfanylacetate Chemical compound CC(=O)SCC(=O)ON1C(=O)CCC1=O FLCQLSRLQIPNLM-UHFFFAOYSA-N 0.000 description 1
- JWDFQMWEFLOOED-UHFFFAOYSA-N (2,5-dioxopyrrolidin-1-yl) 3-(pyridin-2-yldisulfanyl)propanoate Chemical compound O=C1CCC(=O)N1OC(=O)CCSSC1=CC=CC=N1 JWDFQMWEFLOOED-UHFFFAOYSA-N 0.000 description 1
- PVGATNRYUYNBHO-UHFFFAOYSA-N (2,5-dioxopyrrolidin-1-yl) 4-(2,5-dioxopyrrol-1-yl)butanoate Chemical compound O=C1CCC(=O)N1OC(=O)CCCN1C(=O)C=CC1=O PVGATNRYUYNBHO-UHFFFAOYSA-N 0.000 description 1
- BQWBEDSJTMWJAE-UHFFFAOYSA-N (2,5-dioxopyrrolidin-1-yl) 4-[(2-iodoacetyl)amino]benzoate Chemical compound C1=CC(NC(=O)CI)=CC=C1C(=O)ON1C(=O)CCC1=O BQWBEDSJTMWJAE-UHFFFAOYSA-N 0.000 description 1
- PMJWDPGOWBRILU-UHFFFAOYSA-N (2,5-dioxopyrrolidin-1-yl) 4-[4-(2,5-dioxopyrrol-1-yl)phenyl]butanoate Chemical compound O=C1CCC(=O)N1OC(=O)CCCC(C=C1)=CC=C1N1C(=O)C=CC1=O PMJWDPGOWBRILU-UHFFFAOYSA-N 0.000 description 1
- FUOJEDZPVVDXHI-UHFFFAOYSA-N (2,5-dioxopyrrolidin-1-yl) 5-azido-2-nitrobenzoate Chemical compound [O-][N+](=O)C1=CC=C(N=[N+]=[N-])C=C1C(=O)ON1C(=O)CCC1=O FUOJEDZPVVDXHI-UHFFFAOYSA-N 0.000 description 1
- NGXDNMNOQDVTRL-UHFFFAOYSA-N (2,5-dioxopyrrolidin-1-yl) 6-(4-azido-2-nitroanilino)hexanoate Chemical compound [O-][N+](=O)C1=CC(N=[N+]=[N-])=CC=C1NCCCCCC(=O)ON1C(=O)CCC1=O NGXDNMNOQDVTRL-UHFFFAOYSA-N 0.000 description 1
- BAERPNBPLZWCES-UHFFFAOYSA-N (2-hydroxy-1-phosphonoethyl)phosphonic acid Chemical compound OCC(P(O)(O)=O)P(O)(O)=O BAERPNBPLZWCES-UHFFFAOYSA-N 0.000 description 1
- QDZOEBFLNHCSSF-PFFBOGFISA-N (2S)-2-[[(2R)-2-[[(2S)-1-[(2S)-6-amino-2-[[(2S)-1-[(2R)-2-amino-5-carbamimidamidopentanoyl]pyrrolidine-2-carbonyl]amino]hexanoyl]pyrrolidine-2-carbonyl]amino]-3-(1H-indol-3-yl)propanoyl]amino]-N-[(2R)-1-[[(2S)-1-[[(2R)-1-[[(2S)-1-[[(2S)-1-amino-4-methyl-1-oxopentan-2-yl]amino]-4-methyl-1-oxopentan-2-yl]amino]-3-(1H-indol-3-yl)-1-oxopropan-2-yl]amino]-1-oxo-3-phenylpropan-2-yl]amino]-3-(1H-indol-3-yl)-1-oxopropan-2-yl]pentanediamide Chemical compound C([C@@H](C(=O)N[C@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(N)=O)NC(=O)[C@@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CCCCN)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](N)CCCNC(N)=N)C1=CC=CC=C1 QDZOEBFLNHCSSF-PFFBOGFISA-N 0.000 description 1
- WWTBZEKOSBFBEM-SPWPXUSOSA-N (2s)-2-[[2-benzyl-3-[hydroxy-[(1r)-2-phenyl-1-(phenylmethoxycarbonylamino)ethyl]phosphoryl]propanoyl]amino]-3-(1h-indol-3-yl)propanoic acid Chemical compound N([C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)O)C(=O)C(CP(O)(=O)[C@H](CC=1C=CC=CC=1)NC(=O)OCC=1C=CC=CC=1)CC1=CC=CC=C1 WWTBZEKOSBFBEM-SPWPXUSOSA-N 0.000 description 1
- GDIYMWAMJKRXRE-UHFFFAOYSA-N (2z)-2-[(2e)-2-[2-chloro-3-[(z)-2-(1,3,3-trimethylindol-1-ium-2-yl)ethenyl]cyclohex-2-en-1-ylidene]ethylidene]-1,3,3-trimethylindole Chemical compound CC1(C)C2=CC=CC=C2N(C)C1=CC=C1C(Cl)=C(C=CC=2C(C3=CC=CC=C3[N+]=2C)(C)C)CCC1 GDIYMWAMJKRXRE-UHFFFAOYSA-N 0.000 description 1
- QFLWZFQWSBQYPS-AWRAUJHKSA-N (3S)-3-[[(2S)-2-[[(2S)-2-[5-[(3aS,6aR)-2-oxo-1,3,3a,4,6,6a-hexahydrothieno[3,4-d]imidazol-4-yl]pentanoylamino]-3-methylbutanoyl]amino]-3-(4-hydroxyphenyl)propanoyl]amino]-4-[1-bis(4-chlorophenoxy)phosphorylbutylamino]-4-oxobutanoic acid Chemical compound CCCC(NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](Cc1ccc(O)cc1)NC(=O)[C@@H](NC(=O)CCCCC1SC[C@@H]2NC(=O)N[C@H]12)C(C)C)P(=O)(Oc1ccc(Cl)cc1)Oc1ccc(Cl)cc1 QFLWZFQWSBQYPS-AWRAUJHKSA-N 0.000 description 1
- CUKWUWBLQQDQAC-VEQWQPCFSA-N (3s)-3-amino-4-[[(2s)-1-[[(2s)-1-[[(2s)-1-[[(2s,3s)-1-[[(2s)-1-[(2s)-2-[[(1s)-1-carboxyethyl]carbamoyl]pyrrolidin-1-yl]-3-(1h-imidazol-5-yl)-1-oxopropan-2-yl]amino]-3-methyl-1-oxopentan-2-yl]amino]-3-(4-hydroxyphenyl)-1-oxopropan-2-yl]amino]-3-methyl-1-ox Chemical compound C([C@@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CC=1NC=NC=1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](C)C(O)=O)NC(=O)[C@@H](NC(=O)[C@H](CCCN=C(N)N)NC(=O)[C@@H](N)CC(O)=O)C(C)C)C1=CC=C(O)C=C1 CUKWUWBLQQDQAC-VEQWQPCFSA-N 0.000 description 1
- NXLNNXIXOYSCMB-UHFFFAOYSA-N (4-nitrophenyl) carbonochloridate Chemical compound [O-][N+](=O)C1=CC=C(OC(Cl)=O)C=C1 NXLNNXIXOYSCMB-UHFFFAOYSA-N 0.000 description 1
- QGKMIGUHVLGJBR-UHFFFAOYSA-M (4z)-1-(3-methylbutyl)-4-[[1-(3-methylbutyl)quinolin-1-ium-4-yl]methylidene]quinoline;iodide Chemical compound [I-].C12=CC=CC=C2N(CCC(C)C)C=CC1=CC1=CC=[N+](CCC(C)C)C2=CC=CC=C12 QGKMIGUHVLGJBR-UHFFFAOYSA-M 0.000 description 1
- SHXHPUAKLCCLDV-UHFFFAOYSA-N 1,1,1-trifluoropentane-2,4-dione Chemical compound CC(=O)CC(=O)C(F)(F)F SHXHPUAKLCCLDV-UHFFFAOYSA-N 0.000 description 1
- NKIJBSVPDYIEAT-UHFFFAOYSA-N 1,4,7,10-tetrazacyclododec-10-ene Chemical compound C1CNCCN=CCNCCN1 NKIJBSVPDYIEAT-UHFFFAOYSA-N 0.000 description 1
- VPVXHAANQNHFSF-UHFFFAOYSA-N 1,4-dioxan-2-one Chemical class O=C1COCCO1 VPVXHAANQNHFSF-UHFFFAOYSA-N 0.000 description 1
- UOFGSWVZMUXXIY-UHFFFAOYSA-N 1,5-Diphenyl-3-thiocarbazone Chemical compound C=1C=CC=CC=1N=NC(=S)NNC1=CC=CC=C1 UOFGSWVZMUXXIY-UHFFFAOYSA-N 0.000 description 1
- VILFTWLXLYIEMV-UHFFFAOYSA-N 1,5-difluoro-2,4-dinitrobenzene Chemical compound [O-][N+](=O)C1=CC([N+]([O-])=O)=C(F)C=C1F VILFTWLXLYIEMV-UHFFFAOYSA-N 0.000 description 1
- ASOKPJOREAFHNY-UHFFFAOYSA-N 1-Hydroxybenzotriazole Chemical compound C1=CC=C2N(O)N=NC2=C1 ASOKPJOREAFHNY-UHFFFAOYSA-N 0.000 description 1
- ONBQEOIKXPHGMB-VBSBHUPXSA-N 1-[2-[(2s,3r,4s,5r)-3,4-dihydroxy-5-(hydroxymethyl)oxolan-2-yl]oxy-4,6-dihydroxyphenyl]-3-(4-hydroxyphenyl)propan-1-one Chemical compound O[C@@H]1[C@H](O)[C@@H](CO)O[C@H]1OC1=CC(O)=CC(O)=C1C(=O)CCC1=CC=C(O)C=C1 ONBQEOIKXPHGMB-VBSBHUPXSA-N 0.000 description 1
- DIYPCWKHSODVAP-UHFFFAOYSA-N 1-[3-(2,5-dioxopyrrol-1-yl)benzoyl]oxy-2,5-dioxopyrrolidine-3-sulfonic acid Chemical compound O=C1C(S(=O)(=O)O)CC(=O)N1OC(=O)C1=CC=CC(N2C(C=CC2=O)=O)=C1 DIYPCWKHSODVAP-UHFFFAOYSA-N 0.000 description 1
- XKSOTQXTPALQMY-UHFFFAOYSA-N 1-[3-[(4-azidophenyl)disulfanyl]propanoyloxy]-2,5-dioxopyrrolidine-3-sulfonic acid Chemical compound O=C1C(S(=O)(=O)O)CC(=O)N1OC(=O)CCSSC1=CC=C(N=[N+]=[N-])C=C1 XKSOTQXTPALQMY-UHFFFAOYSA-N 0.000 description 1
- XKQYCEFPFNDDSJ-UHFFFAOYSA-N 1-[3-[2-[(4-azido-2-hydroxybenzoyl)amino]ethyldisulfanyl]propanoyloxy]-2,5-dioxopyrrolidine-3-sulfonic acid Chemical compound OC1=CC(N=[N+]=[N-])=CC=C1C(=O)NCCSSCCC(=O)ON1C(=O)C(S(O)(=O)=O)CC1=O XKQYCEFPFNDDSJ-UHFFFAOYSA-N 0.000 description 1
- VOTJUWBJENROFB-UHFFFAOYSA-N 1-[3-[[3-(2,5-dioxo-3-sulfopyrrolidin-1-yl)oxy-3-oxopropyl]disulfanyl]propanoyloxy]-2,5-dioxopyrrolidine-3-sulfonic acid Chemical compound O=C1C(S(=O)(=O)O)CC(=O)N1OC(=O)CCSSCCC(=O)ON1C(=O)C(S(O)(=O)=O)CC1=O VOTJUWBJENROFB-UHFFFAOYSA-N 0.000 description 1
- WQQBUTMELIQJNY-UHFFFAOYSA-N 1-[4-(2,5-dioxo-3-sulfopyrrolidin-1-yl)oxy-2,3-dihydroxy-4-oxobutanoyl]oxy-2,5-dioxopyrrolidine-3-sulfonic acid Chemical compound O=C1CC(S(O)(=O)=O)C(=O)N1OC(=O)C(O)C(O)C(=O)ON1C(=O)CC(S(O)(=O)=O)C1=O WQQBUTMELIQJNY-UHFFFAOYSA-N 0.000 description 1
- FPKVOQKZMBDBKP-UHFFFAOYSA-N 1-[4-[(2,5-dioxopyrrol-1-yl)methyl]cyclohexanecarbonyl]oxy-2,5-dioxopyrrolidine-3-sulfonic acid Chemical compound O=C1C(S(=O)(=O)O)CC(=O)N1OC(=O)C1CCC(CN2C(C=CC2=O)=O)CC1 FPKVOQKZMBDBKP-UHFFFAOYSA-N 0.000 description 1
- VHYRLCJMMJQUBY-UHFFFAOYSA-N 1-[4-[4-(2,5-dioxopyrrol-1-yl)phenyl]butanoyloxy]-2,5-dioxopyrrolidine-3-sulfonic acid Chemical compound O=C1C(S(=O)(=O)O)CC(=O)N1OC(=O)CCCC1=CC=C(N2C(C=CC2=O)=O)C=C1 VHYRLCJMMJQUBY-UHFFFAOYSA-N 0.000 description 1
- UPNUQQDXHCUWSG-UHFFFAOYSA-N 1-[6-(4-azido-2-nitroanilino)hexanoyloxy]-2,5-dioxopyrrolidine-3-sulfonic acid Chemical compound O=C1C(S(=O)(=O)O)CC(=O)N1OC(=O)CCCCCNC1=CC=C(N=[N+]=[N-])C=C1[N+]([O-])=O UPNUQQDXHCUWSG-UHFFFAOYSA-N 0.000 description 1
- NQTSTBMCCAVWOS-UHFFFAOYSA-N 1-dimethoxyphosphoryl-3-phenoxypropan-2-one Chemical compound COP(=O)(OC)CC(=O)COC1=CC=CC=C1 NQTSTBMCCAVWOS-UHFFFAOYSA-N 0.000 description 1
- RILYGJMAUXOTGJ-UHFFFAOYSA-N 1-oxa-4,7,10-triazacyclododec-11-ene Chemical compound C1CNCCOC=CNCCN1 RILYGJMAUXOTGJ-UHFFFAOYSA-N 0.000 description 1
- COSJCAMRRQYRRD-UHFFFAOYSA-N 1-pyridin-2-ylethane-1,2-diamine Chemical compound NCC(N)C1=CC=CC=N1 COSJCAMRRQYRRD-UHFFFAOYSA-N 0.000 description 1
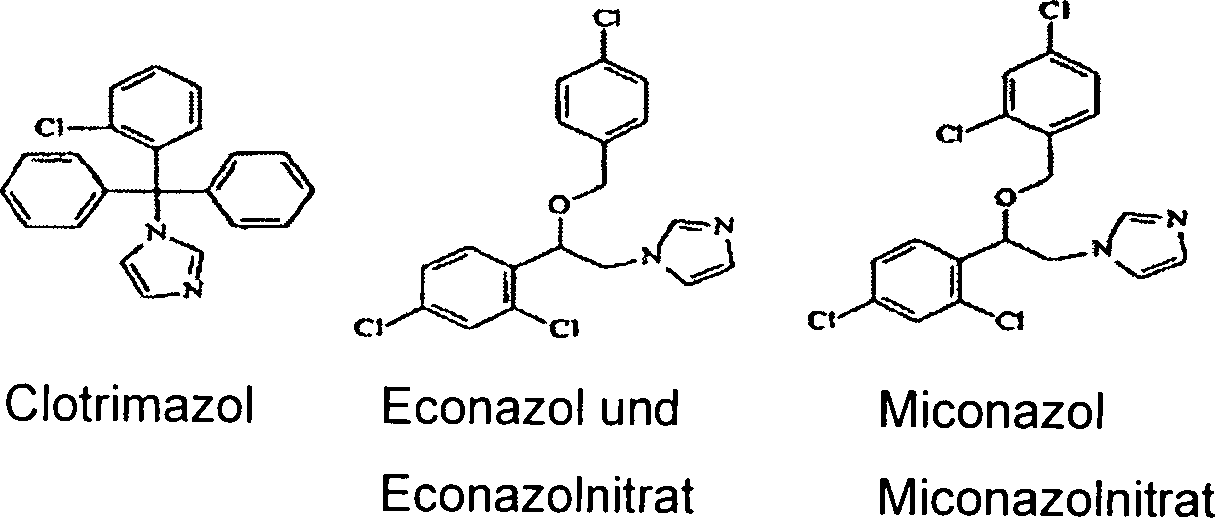
- LEZWWPYKPKIXLL-UHFFFAOYSA-N 1-{2-(4-chlorobenzyloxy)-2-(2,4-dichlorophenyl)ethyl}imidazole Chemical compound C1=CC(Cl)=CC=C1COC(C=1C(=CC(Cl)=CC=1)Cl)CN1C=NC=C1 LEZWWPYKPKIXLL-UHFFFAOYSA-N 0.000 description 1
- WJFKNYWRSNBZNX-UHFFFAOYSA-N 10H-phenothiazine Chemical compound C1=CC=C2NC3=CC=CC=C3SC2=C1 WJFKNYWRSNBZNX-UHFFFAOYSA-N 0.000 description 1
- PGIGZWJIJSINOD-UHFFFAOYSA-N 12h-benzo[a]phenothiazine Chemical compound C1=CC=CC2=C3NC4=CC=CC=C4SC3=CC=C21 PGIGZWJIJSINOD-UHFFFAOYSA-N 0.000 description 1
- 238000001644 13C nuclear magnetic resonance spectroscopy Methods 0.000 description 1
- XEZNGIUYQVAUSS-UHFFFAOYSA-N 18-crown-6 Chemical compound C1COCCOCCOCCOCCOCCO1 XEZNGIUYQVAUSS-UHFFFAOYSA-N 0.000 description 1
- 238000005160 1H NMR spectroscopy Methods 0.000 description 1
- HKAVADYDPYUPRD-UHFFFAOYSA-N 1h-pyrazine-2-thione Chemical compound SC1=CN=CC=N1 HKAVADYDPYUPRD-UHFFFAOYSA-N 0.000 description 1
- VILCJCGEZXAXTO-UHFFFAOYSA-N 2,2,2-tetramine Chemical compound NCCNCCNCCN VILCJCGEZXAXTO-UHFFFAOYSA-N 0.000 description 1
- JFJNVIPVOCESGZ-UHFFFAOYSA-N 2,3-dipyridin-2-ylpyridine Chemical compound N1=CC=CC=C1C1=CC=CN=C1C1=CC=CC=N1 JFJNVIPVOCESGZ-UHFFFAOYSA-N 0.000 description 1
- IEJPPSMHUUQABK-UHFFFAOYSA-N 2,4-diphenyl-4h-1,3-oxazol-5-one Chemical compound O=C1OC(C=2C=CC=CC=2)=NC1C1=CC=CC=C1 IEJPPSMHUUQABK-UHFFFAOYSA-N 0.000 description 1
- ASNTZYQMIUCEBV-UHFFFAOYSA-N 2,5-dioxo-1-[6-[3-(pyridin-2-yldisulfanyl)propanoylamino]hexanoyloxy]pyrrolidine-3-sulfonic acid Chemical compound O=C1C(S(=O)(=O)O)CC(=O)N1OC(=O)CCCCCNC(=O)CCSSC1=CC=CC=N1 ASNTZYQMIUCEBV-UHFFFAOYSA-N 0.000 description 1
- CSEWAUGPAQPMDC-UHFFFAOYSA-N 2-(4-aminophenyl)acetic acid Chemical compound NC1=CC=C(CC(O)=O)C=C1 CSEWAUGPAQPMDC-UHFFFAOYSA-N 0.000 description 1
- TXLHNFOLHRXMAU-UHFFFAOYSA-N 2-(4-benzylphenoxy)-n,n-diethylethanamine;hydron;chloride Chemical compound Cl.C1=CC(OCCN(CC)CC)=CC=C1CC1=CC=CC=C1 TXLHNFOLHRXMAU-UHFFFAOYSA-N 0.000 description 1
- DTCYNRIBBFRFNN-UHFFFAOYSA-N 2-(4-oxaldehydoylphenyl)-2-oxoacetaldehyde Chemical compound O=CC(=O)C1=CC=C(C(=O)C=O)C=C1 DTCYNRIBBFRFNN-UHFFFAOYSA-N 0.000 description 1
- JJJBMWFBWHJKTG-UHFFFAOYSA-N 2-(methyldisulfanyl)-3-nitropyridine Chemical compound CSSC1=NC=CC=C1[N+]([O-])=O JJJBMWFBWHJKTG-UHFFFAOYSA-N 0.000 description 1
- BHANCCMWYDZQOR-UHFFFAOYSA-N 2-(methyldisulfanyl)pyridine Chemical compound CSSC1=CC=CC=N1 BHANCCMWYDZQOR-UHFFFAOYSA-N 0.000 description 1
- HVAUUPRFYPCOCA-AREMUKBSSA-N 2-O-acetyl-1-O-hexadecyl-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCCCCOC[C@@H](OC(C)=O)COP([O-])(=O)OCC[N+](C)(C)C HVAUUPRFYPCOCA-AREMUKBSSA-N 0.000 description 1
- RHPJLBAMJXHCEC-UHFFFAOYSA-N 2-[3-[2-[(4-chlorophenyl)methoxy]-2-(2,4-dichlorophenyl)ethyl]-2h-imidazol-1-yl]acetic acid Chemical compound C1=CN(CC(=O)O)CN1CC(C=1C(=CC(Cl)=CC=1)Cl)OCC1=CC=C(Cl)C=C1 RHPJLBAMJXHCEC-UHFFFAOYSA-N 0.000 description 1
- JHALWMSZGCVVEM-UHFFFAOYSA-N 2-[4,7-bis(carboxymethyl)-1,4,7-triazonan-1-yl]acetic acid Chemical compound OC(=O)CN1CCN(CC(O)=O)CCN(CC(O)=O)CC1 JHALWMSZGCVVEM-UHFFFAOYSA-N 0.000 description 1
- YAWTYNUYRZWXPV-UHFFFAOYSA-N 2-[4-[(6,7-dimethoxyquinazolin-4-yl)amino]phenyl]acetic acid Chemical compound C=12C=C(OC)C(OC)=CC2=NC=NC=1NC1=CC=C(CC(O)=O)C=C1 YAWTYNUYRZWXPV-UHFFFAOYSA-N 0.000 description 1
- OTLLEIBWKHEHGU-UHFFFAOYSA-N 2-[5-[[5-(6-aminopurin-9-yl)-3,4-dihydroxyoxolan-2-yl]methoxy]-3,4-dihydroxy-6-(hydroxymethyl)oxan-2-yl]oxy-3,5-dihydroxy-4-phosphonooxyhexanedioic acid Chemical compound C1=NC=2C(N)=NC=NC=2N1C(C(C1O)O)OC1COC1C(CO)OC(OC(C(O)C(OP(O)(O)=O)C(O)C(O)=O)C(O)=O)C(O)C1O OTLLEIBWKHEHGU-UHFFFAOYSA-N 0.000 description 1
- GOJUJUVQIVIZAV-UHFFFAOYSA-N 2-amino-4,6-dichloropyrimidine-5-carbaldehyde Chemical group NC1=NC(Cl)=C(C=O)C(Cl)=N1 GOJUJUVQIVIZAV-UHFFFAOYSA-N 0.000 description 1
- CDAWCLOXVUBKRW-UHFFFAOYSA-N 2-aminophenol Chemical class NC1=CC=CC=C1O CDAWCLOXVUBKRW-UHFFFAOYSA-N 0.000 description 1
- IZQAUUVBKYXMET-UHFFFAOYSA-N 2-bromoethanamine Chemical compound NCCBr IZQAUUVBKYXMET-UHFFFAOYSA-N 0.000 description 1
- IMRWILPUOVGIMU-UHFFFAOYSA-N 2-bromopyridine Chemical compound BrC1=CC=CC=N1 IMRWILPUOVGIMU-UHFFFAOYSA-N 0.000 description 1
- GTQFGAJYMBBUSO-UHFFFAOYSA-N 2-diazoacetamide Chemical class NC(=O)C=[N+]=[N-] GTQFGAJYMBBUSO-UHFFFAOYSA-N 0.000 description 1
- NEAQRZUHTPSBBM-UHFFFAOYSA-N 2-hydroxy-3,3-dimethyl-7-nitro-4h-isoquinolin-1-one Chemical compound C1=C([N+]([O-])=O)C=C2C(=O)N(O)C(C)(C)CC2=C1 NEAQRZUHTPSBBM-UHFFFAOYSA-N 0.000 description 1
- 125000000954 2-hydroxyethyl group Chemical group [H]C([*])([H])C([H])([H])O[H] 0.000 description 1
- OFLNEVYCAMVQJS-UHFFFAOYSA-N 2-n,2-n-diethylethane-1,1,1,2-tetramine Chemical compound CCN(CC)CC(N)(N)N OFLNEVYCAMVQJS-UHFFFAOYSA-N 0.000 description 1
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 1
- AUFVJZSDSXXFOI-UHFFFAOYSA-N 2.2.2-cryptand Chemical compound C1COCCOCCN2CCOCCOCCN1CCOCCOCC2 AUFVJZSDSXXFOI-UHFFFAOYSA-N 0.000 description 1
- BCHZICNRHXRCHY-UHFFFAOYSA-N 2h-oxazine Chemical compound N1OC=CC=C1 BCHZICNRHXRCHY-UHFFFAOYSA-N 0.000 description 1
- DFSFLZCLKYZYRD-UHFFFAOYSA-N 3,4-diethoxycyclobut-3-ene-1,2-dione Chemical compound CCOC1=C(OCC)C(=O)C1=O DFSFLZCLKYZYRD-UHFFFAOYSA-N 0.000 description 1
- CJAZCKUGLFWINJ-UHFFFAOYSA-N 3,4-dihydroxybenzene-1,2-disulfonic acid Chemical compound OC1=CC=C(S(O)(=O)=O)C(S(O)(=O)=O)=C1O CJAZCKUGLFWINJ-UHFFFAOYSA-N 0.000 description 1
- MWOOKDULMBMMPN-UHFFFAOYSA-N 3-(2-ethyl-1,2-oxazol-2-ium-5-yl)benzenesulfonate Chemical compound O1[N+](CC)=CC=C1C1=CC=CC(S([O-])(=O)=O)=C1 MWOOKDULMBMMPN-UHFFFAOYSA-N 0.000 description 1
- FPQQSJJWHUJYPU-UHFFFAOYSA-N 3-(dimethylamino)propyliminomethylidene-ethylazanium;chloride Chemical compound Cl.CCN=C=NCCCN(C)C FPQQSJJWHUJYPU-UHFFFAOYSA-N 0.000 description 1
- JMUAKWNHKQBPGJ-UHFFFAOYSA-N 3-(pyridin-2-yldisulfanyl)-n-[4-[3-(pyridin-2-yldisulfanyl)propanoylamino]butyl]propanamide Chemical compound C=1C=CC=NC=1SSCCC(=O)NCCCCNC(=O)CCSSC1=CC=CC=N1 JMUAKWNHKQBPGJ-UHFFFAOYSA-N 0.000 description 1
- NITXODYAMWZEJY-UHFFFAOYSA-N 3-(pyridin-2-yldisulfanyl)propanehydrazide Chemical compound NNC(=O)CCSSC1=CC=CC=N1 NITXODYAMWZEJY-UHFFFAOYSA-N 0.000 description 1
- TVZRAEYQIKYCPH-UHFFFAOYSA-N 3-(trimethylsilyl)propane-1-sulfonic acid Chemical compound C[Si](C)(C)CCCS(O)(=O)=O TVZRAEYQIKYCPH-UHFFFAOYSA-N 0.000 description 1
- XATIUUHFLMDNJN-UHFFFAOYSA-N 3-[2-[(4-octylphenyl)carbamoyl]-6,7-dihydro-5h-[1,3]thiazolo[3,2-a]pyrimidin-3-yl]propanoic acid Chemical compound C1=CC(CCCCCCCC)=CC=C1NC(=O)C(S1)=C(CCC(O)=O)N2C1=NCCC2 XATIUUHFLMDNJN-UHFFFAOYSA-N 0.000 description 1
- ZFJOMUKPDWNRFI-UHFFFAOYSA-N 3-bromo-4-methylbenzoic acid Chemical compound CC1=CC=C(C(O)=O)C=C1Br ZFJOMUKPDWNRFI-UHFFFAOYSA-N 0.000 description 1
- UHBAPGWWRFVTFS-UHFFFAOYSA-N 4,4'-dipyridyl disulfide Chemical compound C=1C=NC=CC=1SSC1=CC=NC=C1 UHBAPGWWRFVTFS-UHFFFAOYSA-N 0.000 description 1
- IBOFVQJTBBUKMU-UHFFFAOYSA-N 4,4'-methylene-bis-(2-chloroaniline) Chemical compound C1=C(Cl)C(N)=CC=C1CC1=CC=C(N)C(Cl)=C1 IBOFVQJTBBUKMU-UHFFFAOYSA-N 0.000 description 1
- ZMRMMAOBSFSXLN-UHFFFAOYSA-N 4-[4-(2,5-dioxopyrrol-1-yl)phenyl]butanehydrazide Chemical compound C1=CC(CCCC(=O)NN)=CC=C1N1C(=O)C=CC1=O ZMRMMAOBSFSXLN-UHFFFAOYSA-N 0.000 description 1
- LLLHRNQLGUOJHP-UHFFFAOYSA-N 4-chloro-6,7-dimethoxyquinazoline Chemical compound C1=NC(Cl)=C2C=C(OC)C(OC)=CC2=N1 LLLHRNQLGUOJHP-UHFFFAOYSA-N 0.000 description 1
- SGOOQMRIPALTEL-UHFFFAOYSA-N 4-hydroxy-N,1-dimethyl-2-oxo-N-phenyl-3-quinolinecarboxamide Chemical compound OC=1C2=CC=CC=C2N(C)C(=O)C=1C(=O)N(C)C1=CC=CC=C1 SGOOQMRIPALTEL-UHFFFAOYSA-N 0.000 description 1
- PZNQZSRPDOEBMS-QMMMGPOBSA-N 4-iodo-L-phenylalanine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(I)C=C1 PZNQZSRPDOEBMS-QMMMGPOBSA-N 0.000 description 1
- JJTUDXZGHPGLLC-IMJSIDKUSA-N 4511-42-6 Chemical compound C[C@@H]1OC(=O)[C@H](C)OC1=O JJTUDXZGHPGLLC-IMJSIDKUSA-N 0.000 description 1
- DEQPBRIACBATHE-FXQIFTODSA-N 5-[(3as,4s,6ar)-2-oxo-1,3,3a,4,6,6a-hexahydrothieno[3,4-d]imidazol-4-yl]-2-iminopentanoic acid Chemical compound N1C(=O)N[C@@H]2[C@H](CCCC(=N)C(=O)O)SC[C@@H]21 DEQPBRIACBATHE-FXQIFTODSA-N 0.000 description 1
- IJJWOSAXNHWBPR-HUBLWGQQSA-N 5-[(3as,4s,6ar)-2-oxo-1,3,3a,4,6,6a-hexahydrothieno[3,4-d]imidazol-4-yl]-n-(6-hydrazinyl-6-oxohexyl)pentanamide Chemical compound N1C(=O)N[C@@H]2[C@H](CCCCC(=O)NCCCCCC(=O)NN)SC[C@@H]21 IJJWOSAXNHWBPR-HUBLWGQQSA-N 0.000 description 1
- DNXDWMHPTVQBIP-ZQIUZPCESA-N 5-[(3as,4s,6ar)-2-oxo-1,3,3a,4,6,6a-hexahydrothieno[3,4-d]imidazol-4-yl]-n-[6-[(2-iodoacetyl)amino]hexyl]pentanamide Chemical compound N1C(=O)N[C@@H]2[C@H](CCCCC(=O)NCCCCCCNC(=O)CI)SC[C@@H]21 DNXDWMHPTVQBIP-ZQIUZPCESA-N 0.000 description 1
- QLPHBNRMJLFRGO-YDHSSHFGSA-N 5-[(3as,4s,6ar)-2-oxo-1,3,3a,4,6,6a-hexahydrothieno[3,4-d]imidazol-4-yl]-n-[6-[3-(pyridin-2-yldisulfanyl)propanoylamino]hexyl]pentanamide Chemical compound C([C@H]1[C@H]2NC(=O)N[C@H]2CS1)CCCC(=O)NCCCCCCNC(=O)CCSSC1=CC=CC=N1 QLPHBNRMJLFRGO-YDHSSHFGSA-N 0.000 description 1
- YCPXWRQRBFJBPZ-UHFFFAOYSA-N 5-sulfosalicylic acid Chemical compound OC(=O)C1=CC(S(O)(=O)=O)=CC=C1O YCPXWRQRBFJBPZ-UHFFFAOYSA-N 0.000 description 1
- DMSRMHGCZUXCMJ-UHFFFAOYSA-N 6,7-dimethoxy-1h-quinazolin-4-one Chemical compound C1=NC(O)=C2C=C(OC)C(OC)=CC2=N1 DMSRMHGCZUXCMJ-UHFFFAOYSA-N 0.000 description 1
- JSBWQIZQJOQPFN-UHFFFAOYSA-N 6-[(2-methylpropan-2-yl)oxycarbonylamino]hexylazanium;chloride Chemical compound Cl.CC(C)(C)OC(=O)NCCCCCCN JSBWQIZQJOQPFN-UHFFFAOYSA-N 0.000 description 1
- DDGMDTGNGDOUPX-UHFFFAOYSA-N 7-methyliminophenothiazin-3-amine;hydrochloride Chemical compound [Cl-].C1=C(N)C=C2SC3=CC(=[NH+]C)C=CC3=NC2=C1 DDGMDTGNGDOUPX-UHFFFAOYSA-N 0.000 description 1
- 239000005725 8-Hydroxyquinoline Substances 0.000 description 1
- OYJCVIGKMXUVKB-GARJFASQSA-N Ala-Leu-Pro Chemical compound C[C@@H](C(=O)N[C@@H](CC(C)C)C(=O)N1CCC[C@@H]1C(=O)O)N OYJCVIGKMXUVKB-GARJFASQSA-N 0.000 description 1
- 102000009840 Angiopoietins Human genes 0.000 description 1
- 108010009906 Angiopoietins Proteins 0.000 description 1
- 102400000345 Angiotensin-2 Human genes 0.000 description 1
- 101800000733 Angiotensin-2 Proteins 0.000 description 1
- 208000022211 Arteriovenous Malformations Diseases 0.000 description 1
- 206010003571 Astrocytoma Diseases 0.000 description 1
- OMPJBNCRMGITSC-UHFFFAOYSA-N Benzoylperoxide Chemical compound C=1C=CC=CC=1C(=O)OOC(=O)C1=CC=CC=C1 OMPJBNCRMGITSC-UHFFFAOYSA-N 0.000 description 1
- 102000004954 Biglycan Human genes 0.000 description 1
- 108090001138 Biglycan Proteins 0.000 description 1
- 102000015081 Blood Coagulation Factors Human genes 0.000 description 1
- 108010039209 Blood Coagulation Factors Proteins 0.000 description 1
- 102000004506 Blood Proteins Human genes 0.000 description 1
- 108010017384 Blood Proteins Proteins 0.000 description 1
- BTBUEUYNUDRHOZ-UHFFFAOYSA-N Borate Chemical compound [O-]B([O-])[O-] BTBUEUYNUDRHOZ-UHFFFAOYSA-N 0.000 description 1
- 208000003174 Brain Neoplasms Diseases 0.000 description 1
- 206010006187 Breast cancer Diseases 0.000 description 1
- 208000026310 Breast neoplasm Diseases 0.000 description 1
- CANKXBUUHBQWHA-UHFFFAOYSA-N C(C)(=O)O.C(C)(=O)O.C(C)(=O)O.O1CCNCCNCCNCC1 Chemical compound C(C)(=O)O.C(C)(=O)O.C(C)(=O)O.O1CCNCCNCCNCC1 CANKXBUUHBQWHA-UHFFFAOYSA-N 0.000 description 1
- FRBYJCORNHQJTG-UHFFFAOYSA-N C(CN(C(C1=CC=CC=C1)C(=O)O)O)N(C(C1=CC=CC=C1)C(=O)O)O Chemical compound C(CN(C(C1=CC=CC=C1)C(=O)O)O)N(C(C1=CC=CC=C1)C(=O)O)O FRBYJCORNHQJTG-UHFFFAOYSA-N 0.000 description 1
- CLDZYSUDOQXJOU-UHFFFAOYSA-M C5-oxacyanine Chemical compound [I-].O1C2=CC=CC=C2[N+](CC)=C1C=CC=CC=C1N(CC)C2=CC=CC=C2O1 CLDZYSUDOQXJOU-UHFFFAOYSA-M 0.000 description 1
- UZLDSPSTABQEQP-UHFFFAOYSA-M C7-oxacyanine Chemical compound [I-].O1C2=CC=CC=C2[N+](CC)=C1C=CC=CC=CC=C1N(CC)C2=CC=CC=C2O1 UZLDSPSTABQEQP-UHFFFAOYSA-M 0.000 description 1
- 102000053028 CD36 Antigens Human genes 0.000 description 1
- 108010045374 CD36 Antigens Proteins 0.000 description 1
- 101100381481 Caenorhabditis elegans baz-2 gene Proteins 0.000 description 1
- 229940127291 Calcium channel antagonist Drugs 0.000 description 1
- KXDHJXZQYSOELW-UHFFFAOYSA-N Carbamic acid Chemical class NC(O)=O KXDHJXZQYSOELW-UHFFFAOYSA-N 0.000 description 1
- 229920001661 Chitosan Polymers 0.000 description 1
- 208000006332 Choriocarcinoma Diseases 0.000 description 1
- KRKNYBCHXYNGOX-UHFFFAOYSA-K Citrate Chemical compound [O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O KRKNYBCHXYNGOX-UHFFFAOYSA-K 0.000 description 1
- SSLUSTSKXIHHMJ-UHFFFAOYSA-N Cl.C(C)(=O)NC1=CC=C(C=C1)N(CCCCCCN)C1=NC=NC2=CC(=C(C=C12)OC)OC Chemical compound Cl.C(C)(=O)NC1=CC=C(C=C1)N(CCCCCCN)C1=NC=NC2=CC(=C(C=C12)OC)OC SSLUSTSKXIHHMJ-UHFFFAOYSA-N 0.000 description 1
- 206010009900 Colitis ulcerative Diseases 0.000 description 1
- 108010035532 Collagen Proteins 0.000 description 1
- 102000008186 Collagen Human genes 0.000 description 1
- 102000012422 Collagen Type I Human genes 0.000 description 1
- 108010022452 Collagen Type I Proteins 0.000 description 1
- 206010009944 Colon cancer Diseases 0.000 description 1
- 208000001333 Colorectal Neoplasms Diseases 0.000 description 1
- 239000011665 D-biotin Substances 0.000 description 1
- RGHNJXZEOKUKBD-UHFFFAOYSA-N D-gluconic acid Natural products OCC(O)C(O)C(O)C(O)C(O)=O RGHNJXZEOKUKBD-UHFFFAOYSA-N 0.000 description 1
- 229920004934 Dacron® Polymers 0.000 description 1
- 102000004237 Decorin Human genes 0.000 description 1
- 108090000738 Decorin Proteins 0.000 description 1
- 229920000045 Dermatan sulfate Polymers 0.000 description 1
- 229920002307 Dextran Polymers 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- RPNUMPOLZDHAAY-UHFFFAOYSA-N Diethylenetriamine Chemical compound NCCNCCN RPNUMPOLZDHAAY-UHFFFAOYSA-N 0.000 description 1
- 241000551547 Dione <red algae> Species 0.000 description 1
- QXNVGIXVLWOKEQ-UHFFFAOYSA-N Disodium Chemical compound [Na][Na] QXNVGIXVLWOKEQ-UHFFFAOYSA-N 0.000 description 1
- GKQLYSROISKDLL-UHFFFAOYSA-N EEDQ Chemical compound C1=CC=C2N(C(=O)OCC)C(OCC)C=CC2=C1 GKQLYSROISKDLL-UHFFFAOYSA-N 0.000 description 1
- 102000012545 EGF-like domains Human genes 0.000 description 1
- 108050002150 EGF-like domains Proteins 0.000 description 1
- 108010044063 Endocrine-Gland-Derived Vascular Endothelial Growth Factor Proteins 0.000 description 1
- 102000006402 Endocrine-Gland-Derived Vascular Endothelial Growth Factor Human genes 0.000 description 1
- 208000004145 Endometritis Diseases 0.000 description 1
- 102400001047 Endostatin Human genes 0.000 description 1
- 102000002045 Endothelin Human genes 0.000 description 1
- 108050009340 Endothelin Proteins 0.000 description 1
- 239000004593 Epoxy Substances 0.000 description 1
- 108090000371 Esterases Proteins 0.000 description 1
- IAYPIBMASNFSPL-UHFFFAOYSA-N Ethylene oxide Chemical group C1CO1 IAYPIBMASNFSPL-UHFFFAOYSA-N 0.000 description 1
- BWGVNKXGVNDBDI-UHFFFAOYSA-N Fibrin monomer Chemical group CNC(=O)CNC(=O)CN BWGVNKXGVNDBDI-UHFFFAOYSA-N 0.000 description 1
- 108010049003 Fibrinogen Proteins 0.000 description 1
- 102000008946 Fibrinogen Human genes 0.000 description 1
- KRHYYFGTRYWZRS-UHFFFAOYSA-M Fluoride anion Chemical compound [F-] KRHYYFGTRYWZRS-UHFFFAOYSA-M 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- 208000032612 Glial tumor Diseases 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 description 1
- 229920002527 Glycogen Polymers 0.000 description 1
- 102000003886 Glycoproteins Human genes 0.000 description 1
- 108090000288 Glycoproteins Proteins 0.000 description 1
- 102000002812 Heat-Shock Proteins Human genes 0.000 description 1
- 108010004889 Heat-Shock Proteins Proteins 0.000 description 1
- 102100031573 Hematopoietic progenitor cell antigen CD34 Human genes 0.000 description 1
- 108010054147 Hemoglobins Proteins 0.000 description 1
- 102000001554 Hemoglobins Human genes 0.000 description 1
- 229920002971 Heparan sulfate Polymers 0.000 description 1
- 229920001499 Heparinoid Polymers 0.000 description 1
- 206010019695 Hepatic neoplasm Diseases 0.000 description 1
- 102000007625 Hirudins Human genes 0.000 description 1
- 108010007267 Hirudins Proteins 0.000 description 1
- 101000945318 Homo sapiens Calponin-1 Proteins 0.000 description 1
- 101000777663 Homo sapiens Hematopoietic progenitor cell antigen CD34 Proteins 0.000 description 1
- 101000652736 Homo sapiens Transgelin Proteins 0.000 description 1
- 206010062904 Hormone-refractory prostate cancer Diseases 0.000 description 1
- 206010021143 Hypoxia Diseases 0.000 description 1
- 108010031792 IGF Type 2 Receptor Proteins 0.000 description 1
- 108060003951 Immunoglobulin Proteins 0.000 description 1
- 102000001706 Immunoglobulin Fab Fragments Human genes 0.000 description 1
- 108010054477 Immunoglobulin Fab Fragments Proteins 0.000 description 1
- 102000008394 Immunoglobulin Fragments Human genes 0.000 description 1
- 108010021625 Immunoglobulin Fragments Proteins 0.000 description 1
- 206010061216 Infarction Diseases 0.000 description 1
- 108090000723 Insulin-Like Growth Factor I Proteins 0.000 description 1
- 108090001007 Interleukin-8 Proteins 0.000 description 1
- 206010022998 Irritability Diseases 0.000 description 1
- 208000008839 Kidney Neoplasms Diseases 0.000 description 1
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 1
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 1
- 125000003440 L-leucyl group Chemical group O=C([*])[C@](N([H])[H])([H])C([H])([H])C(C([H])([H])[H])([H])C([H])([H])[H] 0.000 description 1
- QIVBCDIJIAJPQS-VIFPVBQESA-N L-tryptophane Chemical compound C1=CC=C2C(C[C@H](N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-VIFPVBQESA-N 0.000 description 1
- 108010000851 Laminin Receptors Proteins 0.000 description 1
- 102000002297 Laminin Receptors Human genes 0.000 description 1
- 102000004856 Lectins Human genes 0.000 description 1
- 108090001090 Lectins Proteins 0.000 description 1
- VTJUNIYRYIAIHF-IUCAKERBSA-N Leu-Pro Chemical compound CC(C)C[C@H](N)C(=O)N1CCC[C@H]1C(O)=O VTJUNIYRYIAIHF-IUCAKERBSA-N 0.000 description 1
- 108010028921 Lipopeptides Proteins 0.000 description 1
- 102000004895 Lipoproteins Human genes 0.000 description 1
- 108090001030 Lipoproteins Proteins 0.000 description 1
- 206010058467 Lung neoplasm malignant Diseases 0.000 description 1
- 108091054438 MHC class II family Proteins 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 102000019218 Mannose-6-phosphate receptors Human genes 0.000 description 1
- 102000000424 Matrix Metalloproteinase 2 Human genes 0.000 description 1
- 108010016165 Matrix Metalloproteinase 2 Proteins 0.000 description 1
- 102000018697 Membrane Proteins Human genes 0.000 description 1
- 108010052285 Membrane Proteins Proteins 0.000 description 1
- 102000005741 Metalloproteases Human genes 0.000 description 1
- 108010006035 Metalloproteases Proteins 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- MWCLLHOVUTZFKS-UHFFFAOYSA-N Methyl cyanoacrylate Chemical compound COC(=O)C(=C)C#N MWCLLHOVUTZFKS-UHFFFAOYSA-N 0.000 description 1
- MSFSPUZXLOGKHJ-UHFFFAOYSA-N Muraminsaeure Natural products OC(=O)C(C)OC1C(N)C(O)OC(CO)C1O MSFSPUZXLOGKHJ-UHFFFAOYSA-N 0.000 description 1
- 101100059320 Mus musculus Ccdc85b gene Proteins 0.000 description 1
- FSVCELGFZIQNCK-UHFFFAOYSA-N N,N-bis(2-hydroxyethyl)glycine Chemical compound OCCN(CCO)CC(O)=O FSVCELGFZIQNCK-UHFFFAOYSA-N 0.000 description 1
- NRFJZTXWLKPZAV-UHFFFAOYSA-N N-(2-oxo-3-thiolanyl)acetamide Chemical compound CC(=O)NC1CCSC1=O NRFJZTXWLKPZAV-UHFFFAOYSA-N 0.000 description 1
- MZRVEZGGRBJDDB-UHFFFAOYSA-N N-Butyllithium Chemical compound [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 description 1
- PCLIMKBDDGJMGD-UHFFFAOYSA-N N-bromosuccinimide Chemical compound BrN1C(=O)CCC1=O PCLIMKBDDGJMGD-UHFFFAOYSA-N 0.000 description 1
- GHAZCVNUKKZTLG-UHFFFAOYSA-N N-ethyl-succinimide Natural products CCN1C(=O)CCC1=O GHAZCVNUKKZTLG-UHFFFAOYSA-N 0.000 description 1
- HDFGOPSGAURCEO-UHFFFAOYSA-N N-ethylmaleimide Chemical compound CCN1C(=O)C=CC1=O HDFGOPSGAURCEO-UHFFFAOYSA-N 0.000 description 1
- OPFJDXRVMFKJJO-ZHHKINOHSA-N N-{[3-(2-benzamido-4-methyl-1,3-thiazol-5-yl)-pyrazol-5-yl]carbonyl}-G-dR-G-dD-dD-dD-NH2 Chemical compound S1C(C=2NN=C(C=2)C(=O)NCC(=O)N[C@H](CCCN=C(N)N)C(=O)NCC(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC(O)=O)C(N)=O)=C(C)N=C1NC(=O)C1=CC=CC=C1 OPFJDXRVMFKJJO-ZHHKINOHSA-N 0.000 description 1
- 206010029113 Neovascularisation Diseases 0.000 description 1
- 206010029260 Neuroblastoma Diseases 0.000 description 1
- 102000003797 Neuropeptides Human genes 0.000 description 1
- 108090000189 Neuropeptides Proteins 0.000 description 1
- 101100330292 Neurospora crassa (strain ATCC 24698 / 74-OR23-1A / CBS 708.71 / DSM 1257 / FGSC 987) cys-12 gene Proteins 0.000 description 1
- MSHZHSPISPJWHW-PVDLLORBSA-N O-(chloroacetylcarbamoyl)fumagillol Chemical compound C([C@H]([C@H]([C@@H]1[C@]2(C)[C@H](O2)CC=C(C)C)OC)OC(=O)NC(=O)CCl)C[C@@]21CO2 MSHZHSPISPJWHW-PVDLLORBSA-N 0.000 description 1
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 1
- BXEFQPCKQSTMKA-UHFFFAOYSA-N OC(=O)C=[N+]=[N-] Chemical class OC(=O)C=[N+]=[N-] BXEFQPCKQSTMKA-UHFFFAOYSA-N 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 206010061535 Ovarian neoplasm Diseases 0.000 description 1
- 108091008606 PDGF receptors Proteins 0.000 description 1
- SJEYSFABYSGQBG-UHFFFAOYSA-M Patent blue Chemical compound [Na+].C1=CC(N(CC)CC)=CC=C1C(C=1C(=CC(=CC=1)S([O-])(=O)=O)S([O-])(=O)=O)=C1C=CC(=[N+](CC)CC)C=C1 SJEYSFABYSGQBG-UHFFFAOYSA-M 0.000 description 1
- 208000031481 Pathologic Constriction Diseases 0.000 description 1
- 229920002230 Pectic acid Polymers 0.000 description 1
- 101000882917 Penaeus paulensis Hemolymph clottable protein Proteins 0.000 description 1
- 102000035195 Peptidases Human genes 0.000 description 1
- 108091005804 Peptidases Proteins 0.000 description 1
- 108010013639 Peptidoglycan Proteins 0.000 description 1
- 102000003992 Peroxidases Human genes 0.000 description 1
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 1
- 108010022233 Plasminogen Activator Inhibitor 1 Proteins 0.000 description 1
- 102100039418 Plasminogen activator inhibitor 1 Human genes 0.000 description 1
- 108010003541 Platelet Activating Factor Proteins 0.000 description 1
- 102100030304 Platelet factor 4 Human genes 0.000 description 1
- 102000011653 Platelet-Derived Growth Factor Receptors Human genes 0.000 description 1
- 229920001244 Poly(D,L-lactide) Polymers 0.000 description 1
- 239000004952 Polyamide Substances 0.000 description 1
- 229920000805 Polyaspartic acid Polymers 0.000 description 1
- 229920001710 Polyorthoester Polymers 0.000 description 1
- 239000004743 Polypropylene Substances 0.000 description 1
- 240000009305 Pometia pinnata Species 0.000 description 1
- 235000017284 Pometia pinnata Nutrition 0.000 description 1
- 206010060862 Prostate cancer Diseases 0.000 description 1
- 102000004022 Protein-Tyrosine Kinases Human genes 0.000 description 1
- 108090000412 Protein-Tyrosine Kinases Proteins 0.000 description 1
- 102000008022 Proto-Oncogene Proteins c-met Human genes 0.000 description 1
- 108010089836 Proto-Oncogene Proteins c-met Proteins 0.000 description 1
- 201000004681 Psoriasis Diseases 0.000 description 1
- 101100372762 Rattus norvegicus Flt1 gene Proteins 0.000 description 1
- 206010038389 Renal cancer Diseases 0.000 description 1
- 208000006265 Renal cell carcinoma Diseases 0.000 description 1
- 208000017442 Retinal disease Diseases 0.000 description 1
- 206010038923 Retinopathy Diseases 0.000 description 1
- 206010039710 Scleroderma Diseases 0.000 description 1
- 201000010208 Seminoma Diseases 0.000 description 1
- 206010040047 Sepsis Diseases 0.000 description 1
- 241000270295 Serpentes Species 0.000 description 1
- 108010071390 Serum Albumin Proteins 0.000 description 1
- 102000007562 Serum Albumin Human genes 0.000 description 1
- 208000000453 Skin Neoplasms Diseases 0.000 description 1
- VMHLLURERBWHNL-UHFFFAOYSA-M Sodium acetate Chemical compound [Na+].CC([O-])=O VMHLLURERBWHNL-UHFFFAOYSA-M 0.000 description 1
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical class [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 1
- 101710104074 Spermidine/putrescine-binding periplasmic protein Proteins 0.000 description 1
- 102400000096 Substance P Human genes 0.000 description 1
- 101800003906 Substance P Proteins 0.000 description 1
- 102000005450 TIE receptors Human genes 0.000 description 1
- 108010006830 TIE receptors Proteins 0.000 description 1
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 1
- WDLRUFUQRNWCPK-UHFFFAOYSA-N Tetraxetan Chemical compound OC(=O)CN1CCN(CC(O)=O)CCN(CC(O)=O)CCN(CC(O)=O)CC1 WDLRUFUQRNWCPK-UHFFFAOYSA-N 0.000 description 1
- 108090000166 Thrombin receptors Proteins 0.000 description 1
- 102000003790 Thrombin receptors Human genes 0.000 description 1
- 108010000499 Thromboplastin Proteins 0.000 description 1
- 102000002262 Thromboplastin Human genes 0.000 description 1
- 102100033142 Transcription factor 20 Human genes 0.000 description 1
- 108010009583 Transforming Growth Factors Proteins 0.000 description 1
- 102000009618 Transforming Growth Factors Human genes 0.000 description 1
- 102100031013 Transgelin Human genes 0.000 description 1
- 108060008539 Transglutaminase Proteins 0.000 description 1
- GSEJCLTVZPLZKY-UHFFFAOYSA-N Triethanolamine Chemical compound OCCN(CCO)CCO GSEJCLTVZPLZKY-UHFFFAOYSA-N 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- YZCKVEUIGOORGS-NJFSPNSNSA-N Tritium Chemical compound [3H] YZCKVEUIGOORGS-NJFSPNSNSA-N 0.000 description 1
- QIVBCDIJIAJPQS-UHFFFAOYSA-N Tryptophan Natural products C1=CC=C2C(CC(N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-UHFFFAOYSA-N 0.000 description 1
- 201000006704 Ulcerative Colitis Diseases 0.000 description 1
- 108010073923 Vascular Endothelial Growth Factor C Proteins 0.000 description 1
- 102000016663 Vascular Endothelial Growth Factor Receptor-3 Human genes 0.000 description 1
- 108010053100 Vascular Endothelial Growth Factor Receptor-3 Proteins 0.000 description 1
- 102100038232 Vascular endothelial growth factor C Human genes 0.000 description 1
- 102100033220 Xanthine oxidase Human genes 0.000 description 1
- 108010093894 Xanthine oxidase Proteins 0.000 description 1
- DGEZNRSVGBDHLK-UHFFFAOYSA-N [1,10]phenanthroline Chemical compound C1=CN=C2C3=NC=CC=C3C=CC2=C1 DGEZNRSVGBDHLK-UHFFFAOYSA-N 0.000 description 1
- AHWXCYJGJOLNFA-UHFFFAOYSA-N [1,4]benzoxazino[2,3-b]phenoxazine Chemical compound O1C2=CC=CC=C2N=C2C1=CC1=NC3=CC=CC=C3OC1=C2 AHWXCYJGJOLNFA-UHFFFAOYSA-N 0.000 description 1
- YDONNITUKPKTIG-UHFFFAOYSA-N [Nitrilotris(methylene)]trisphosphonic acid Chemical compound OP(O)(=O)CN(CP(O)(O)=O)CP(O)(O)=O YDONNITUKPKTIG-UHFFFAOYSA-N 0.000 description 1
- AFCIMSXHQSIHQW-UHFFFAOYSA-N [O].[P] Chemical compound [O].[P] AFCIMSXHQSIHQW-UHFFFAOYSA-N 0.000 description 1
- 239000006096 absorbing agent Substances 0.000 description 1
- 230000035508 accumulation Effects 0.000 description 1
- 238000009825 accumulation Methods 0.000 description 1
- DHKHKXVYLBGOIT-UHFFFAOYSA-N acetaldehyde Diethyl Acetal Natural products CCOC(C)OCC DHKHKXVYLBGOIT-UHFFFAOYSA-N 0.000 description 1
- 150000001241 acetals Chemical class 0.000 description 1
- CYJYKTMBMMYRHR-UHFFFAOYSA-N acetic acid;1,4,7-triazonane Chemical compound CC(O)=O.CC(O)=O.CC(O)=O.C1CNCCNCCN1 CYJYKTMBMMYRHR-UHFFFAOYSA-N 0.000 description 1
- OLEDZQHKPUSANJ-UHFFFAOYSA-N acetic acid;1,4,8,11-tetrazacyclotetradecane Chemical compound CC(O)=O.CC(O)=O.CC(O)=O.CC(O)=O.C1CNCCNCCCNCCNC1 OLEDZQHKPUSANJ-UHFFFAOYSA-N 0.000 description 1
- 150000008065 acid anhydrides Chemical class 0.000 description 1
- 239000000980 acid dye Substances 0.000 description 1
- 239000003929 acidic solution Substances 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 125000002252 acyl group Chemical group 0.000 description 1
- 230000010933 acylation Effects 0.000 description 1
- 238000005917 acylation reaction Methods 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 230000002776 aggregation Effects 0.000 description 1
- 238000004220 aggregation Methods 0.000 description 1
- 125000003172 aldehyde group Chemical group 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 125000001931 aliphatic group Chemical group 0.000 description 1
- 125000004183 alkoxy alkyl group Chemical group 0.000 description 1
- 125000003545 alkoxy group Chemical group 0.000 description 1
- 125000003282 alkyl amino group Chemical group 0.000 description 1
- 125000002877 alkyl aryl group Chemical group 0.000 description 1
- 230000002152 alkylating effect Effects 0.000 description 1
- 102000003801 alpha-2-Antiplasmin Human genes 0.000 description 1
- 108090000183 alpha-2-Antiplasmin Proteins 0.000 description 1
- AVJBPWGFOQAPRH-FWMKGIEWSA-N alpha-L-IdopA-(1->3)-beta-D-GalpNAc4S Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@H](OS(O)(=O)=O)[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@H](O)[C@H](C(O)=O)O1 AVJBPWGFOQAPRH-FWMKGIEWSA-N 0.000 description 1
- AFVLVVWMAFSXCK-VMPITWQZSA-N alpha-cyano-4-hydroxycinnamic acid Chemical group OC(=O)C(\C#N)=C\C1=CC=C(O)C=C1 AFVLVVWMAFSXCK-VMPITWQZSA-N 0.000 description 1
- 238000010640 amide synthesis reaction Methods 0.000 description 1
- 150000003862 amino acid derivatives Chemical class 0.000 description 1
- 150000001414 amino alcohols Chemical class 0.000 description 1
- LHIJANUOQQMGNT-UHFFFAOYSA-N aminoethylethanolamine Chemical compound NCCNCCO LHIJANUOQQMGNT-UHFFFAOYSA-N 0.000 description 1
- 230000002491 angiogenic effect Effects 0.000 description 1
- 229950006323 angiotensin ii Drugs 0.000 description 1
- 150000008064 anhydrides Chemical class 0.000 description 1
- 125000000129 anionic group Chemical group 0.000 description 1
- 150000004056 anthraquinones Chemical class 0.000 description 1
- 239000004599 antimicrobial Substances 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 239000012736 aqueous medium Substances 0.000 description 1
- 150000004984 aromatic diamines Chemical group 0.000 description 1
- 125000006615 aromatic heterocyclic group Chemical group 0.000 description 1
- 230000005744 arteriovenous malformation Effects 0.000 description 1
- 125000001769 aryl amino group Chemical group 0.000 description 1
- 150000001502 aryl halides Chemical class 0.000 description 1
- 108010044715 asialofetuin Proteins 0.000 description 1
- 235000003704 aspartic acid Nutrition 0.000 description 1
- 238000003556 assay Methods 0.000 description 1
- 230000003143 atherosclerotic effect Effects 0.000 description 1
- IVRMZWNICZWHMI-UHFFFAOYSA-N azide group Chemical group [N-]=[N+]=[N-] IVRMZWNICZWHMI-UHFFFAOYSA-N 0.000 description 1
- 150000001541 aziridines Chemical class 0.000 description 1
- 125000000751 azo group Chemical group [*]N=N[*] 0.000 description 1
- DMLAVOWQYNRWNQ-UHFFFAOYSA-N azobenzene Chemical compound C1=CC=CC=C1N=NC1=CC=CC=C1 DMLAVOWQYNRWNQ-UHFFFAOYSA-N 0.000 description 1
- PGWTYMLATMNCCZ-UHFFFAOYSA-M azure A Chemical compound [Cl-].C1=CC(N)=CC2=[S+]C3=CC(N(C)C)=CC=C3N=C21 PGWTYMLATMNCCZ-UHFFFAOYSA-M 0.000 description 1
- KFZNPGQYVZZSNV-UHFFFAOYSA-M azure B Chemical compound [Cl-].C1=CC(N(C)C)=CC2=[S+]C3=CC(NC)=CC=C3N=C21 KFZNPGQYVZZSNV-UHFFFAOYSA-M 0.000 description 1
- 229940125717 barbiturate Drugs 0.000 description 1
- 239000000981 basic dye Substances 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 125000000043 benzamido group Chemical group [H]N([*])C(=O)C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- ZYGHJZDHTFUPRJ-UHFFFAOYSA-N benzo-alpha-pyrone Natural products C1=CC=C2OC(=O)C=CC2=C1 ZYGHJZDHTFUPRJ-UHFFFAOYSA-N 0.000 description 1
- 235000019400 benzoyl peroxide Nutrition 0.000 description 1
- KGNDCEVUMONOKF-UGPLYTSKSA-N benzyl n-[(2r)-1-[(2s,4r)-2-[[(2s)-6-amino-1-(1,3-benzoxazol-2-yl)-1,1-dihydroxyhexan-2-yl]carbamoyl]-4-[(4-methylphenyl)methoxy]pyrrolidin-1-yl]-1-oxo-4-phenylbutan-2-yl]carbamate Chemical compound C1=CC(C)=CC=C1CO[C@H]1CN(C(=O)[C@@H](CCC=2C=CC=CC=2)NC(=O)OCC=2C=CC=CC=2)[C@H](C(=O)N[C@@H](CCCCN)C(O)(O)C=2OC3=CC=CC=C3N=2)C1 KGNDCEVUMONOKF-UGPLYTSKSA-N 0.000 description 1
- OQFSQFPPLPISGP-UHFFFAOYSA-N beta-carboxyaspartic acid Natural products OC(=O)C(N)C(C(O)=O)C(O)=O OQFSQFPPLPISGP-UHFFFAOYSA-N 0.000 description 1
- 229920000229 biodegradable polyester Polymers 0.000 description 1
- 239000004622 biodegradable polyester Substances 0.000 description 1
- 229920002988 biodegradable polymer Polymers 0.000 description 1
- 239000004621 biodegradable polymer Substances 0.000 description 1
- 230000006287 biotinylation Effects 0.000 description 1
- 238000007413 biotinylation Methods 0.000 description 1
- 230000023555 blood coagulation Effects 0.000 description 1
- 239000003114 blood coagulation factor Substances 0.000 description 1
- 239000000480 calcium channel blocker Substances 0.000 description 1
- BPKIGYQJPYCAOW-FFJTTWKXSA-I calcium;potassium;disodium;(2s)-2-hydroxypropanoate;dichloride;dihydroxide;hydrate Chemical compound O.[OH-].[OH-].[Na+].[Na+].[Cl-].[Cl-].[K+].[Ca+2].C[C@H](O)C([O-])=O BPKIGYQJPYCAOW-FFJTTWKXSA-I 0.000 description 1
- BMLSTPRTEKLIPM-UHFFFAOYSA-I calcium;potassium;disodium;hydrogen carbonate;dichloride;dihydroxide;hydrate Chemical compound O.[OH-].[OH-].[Na+].[Na+].[Cl-].[Cl-].[K+].[Ca+2].OC([O-])=O BMLSTPRTEKLIPM-UHFFFAOYSA-I 0.000 description 1
- DHZBEENLJMYSHQ-XCVPVQRUSA-N cantharidin Chemical compound C([C@@H]1O2)C[C@@H]2[C@]2(C)[C@@]1(C)C(=O)OC2=O DHZBEENLJMYSHQ-XCVPVQRUSA-N 0.000 description 1
- 239000004202 carbamide Substances 0.000 description 1
- 125000000837 carbohydrate group Chemical group 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-N carbonic acid Chemical class OC(O)=O BVKZGUZCCUSVTD-UHFFFAOYSA-N 0.000 description 1
- 125000004181 carboxyalkyl group Chemical group 0.000 description 1
- 125000005026 carboxyaryl group Chemical group 0.000 description 1
- 229920001525 carrageenan Polymers 0.000 description 1
- 235000010418 carrageenan Nutrition 0.000 description 1
- 210000000845 cartilage Anatomy 0.000 description 1
- 239000003054 catalyst Substances 0.000 description 1
- 125000002091 cationic group Chemical group 0.000 description 1
- 230000015861 cell surface binding Effects 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 150000001793 charged compounds Polymers 0.000 description 1
- 238000012412 chemical coupling Methods 0.000 description 1
- 239000013626 chemical specie Substances 0.000 description 1
- AOGYCOYQMAVAFD-UHFFFAOYSA-N chlorocarbonic acid Chemical class OC(Cl)=O AOGYCOYQMAVAFD-UHFFFAOYSA-N 0.000 description 1
- HLVXFWDLRHCZEI-UHFFFAOYSA-N chromotropic acid Chemical compound OS(=O)(=O)C1=CC(O)=C2C(O)=CC(S(O)(=O)=O)=CC2=C1 HLVXFWDLRHCZEI-UHFFFAOYSA-N 0.000 description 1
- 230000001684 chronic effect Effects 0.000 description 1
- 229960004753 citiolone Drugs 0.000 description 1
- 235000015165 citric acid Nutrition 0.000 description 1
- 238000004140 cleaning Methods 0.000 description 1
- 229920001436 collagen Polymers 0.000 description 1
- 229940096422 collagen type i Drugs 0.000 description 1
- 208000029742 colonic neoplasm Diseases 0.000 description 1
- 238000004440 column chromatography Methods 0.000 description 1
- 230000002301 combined effect Effects 0.000 description 1
- 239000002131 composite material Substances 0.000 description 1
- 229940126142 compound 16 Drugs 0.000 description 1
- 229940125810 compound 20 Drugs 0.000 description 1
- 229940126086 compound 21 Drugs 0.000 description 1
- 229940126208 compound 22 Drugs 0.000 description 1
- 229940125833 compound 23 Drugs 0.000 description 1
- 229940125898 compound 5 Drugs 0.000 description 1
- 239000012141 concentrate Substances 0.000 description 1
- 235000001671 coumarin Nutrition 0.000 description 1
- 150000004775 coumarins Chemical class 0.000 description 1
- 239000007822 coupling agent Substances 0.000 description 1
- AMHIJMKZPBMCKI-PKLGAXGESA-N ctds Chemical compound O[C@@H]1[C@@H](OS(O)(=O)=O)[C@@H]2O[C@H](COS(O)(=O)=O)[C@H]1O[C@H]([C@@H]([C@H]1OS(O)(=O)=O)OS(O)(=O)=O)O[C@H](CO)[C@H]1O[C@@H](O[C@@H]1CO)[C@H](OS(O)(=O)=O)[C@@H](OS(O)(=O)=O)[C@@H]1O[C@@H](O[C@@H]1CO)[C@H](OS(O)(=O)=O)[C@@H](OS(O)(=O)=O)[C@@H]1O[C@@H](O[C@@H]1CO)[C@H](OS(O)(=O)=O)[C@@H](OS(O)(=O)=O)[C@@H]1O[C@@H](O[C@@H]1CO)[C@H](OS(O)(=O)=O)[C@@H](OS(O)(=O)=O)[C@@H]1O[C@@H](O[C@@H]1CO)[C@H](OS(O)(=O)=O)[C@@H](OS(O)(=O)=O)[C@@H]1O2 AMHIJMKZPBMCKI-PKLGAXGESA-N 0.000 description 1
- 208000035250 cutaneous malignant susceptibility to 1 melanoma Diseases 0.000 description 1
- NLCKLZIHJQEMCU-UHFFFAOYSA-N cyano prop-2-enoate Chemical class C=CC(=O)OC#N NLCKLZIHJQEMCU-UHFFFAOYSA-N 0.000 description 1
- 108010045325 cyclic arginine-glycine-aspartic acid peptide Proteins 0.000 description 1
- 125000000151 cysteine group Chemical group N[C@@H](CS)C(=O)* 0.000 description 1
- 229940127089 cytotoxic agent Drugs 0.000 description 1
- 239000002254 cytotoxic agent Substances 0.000 description 1
- 231100000599 cytotoxic agent Toxicity 0.000 description 1
- 230000006378 damage Effects 0.000 description 1
- 125000001295 dansyl group Chemical group [H]C1=C([H])C(N(C([H])([H])[H])C([H])([H])[H])=C2C([H])=C([H])C([H])=C(C2=C1[H])S(*)(=O)=O 0.000 description 1
- BELUJIRQWUXEKA-UHFFFAOYSA-N decanedioic acid;octanedioic acid Chemical compound OC(=O)CCCCCCC(O)=O.OC(=O)CCCCCCCCC(O)=O BELUJIRQWUXEKA-UHFFFAOYSA-N 0.000 description 1
- GHVNFZFCNZKVNT-UHFFFAOYSA-N decanoic acid Chemical class CCCCCCCCCC(O)=O GHVNFZFCNZKVNT-UHFFFAOYSA-N 0.000 description 1
- TVMUHOAONWHJBV-UHFFFAOYSA-N dehydroglycine Chemical compound OC(=O)C=N TVMUHOAONWHJBV-UHFFFAOYSA-N 0.000 description 1
- 238000001212 derivatisation Methods 0.000 description 1
- 229940051593 dermatan sulfate Drugs 0.000 description 1
- 108010040063 dermatan sulfate proteoglycan Proteins 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 239000008356 dextrose and sodium chloride injection Substances 0.000 description 1
- 239000008355 dextrose injection Substances 0.000 description 1
- LSXWFXONGKSEMY-UHFFFAOYSA-N di-tert-butyl peroxide Chemical compound CC(C)(C)OOC(C)(C)C LSXWFXONGKSEMY-UHFFFAOYSA-N 0.000 description 1
- 239000012969 di-tertiary-butyl peroxide Substances 0.000 description 1
- 206010012601 diabetes mellitus Diseases 0.000 description 1
- 125000004420 diamide group Chemical group 0.000 description 1
- 150000008049 diazo compounds Chemical class 0.000 description 1
- 239000012954 diazonium Substances 0.000 description 1
- 150000001989 diazonium salts Chemical class 0.000 description 1
- 235000014113 dietary fatty acids Nutrition 0.000 description 1
- IRDLUHRVLVEUHA-UHFFFAOYSA-N diethyl dithiophosphate Chemical compound CCOP(S)(=S)OCC IRDLUHRVLVEUHA-UHFFFAOYSA-N 0.000 description 1
- LMBWSYZSUOEYSN-UHFFFAOYSA-N diethyldithiocarbamic acid Chemical compound CCN(CC)C(S)=S LMBWSYZSUOEYSN-UHFFFAOYSA-N 0.000 description 1
- UAOMVDZJSHZZME-UHFFFAOYSA-N diisopropylamine Chemical compound CC(C)NC(C)C UAOMVDZJSHZZME-UHFFFAOYSA-N 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- WQABCVAJNWAXTE-UHFFFAOYSA-N dimercaprol Chemical compound OCC(S)CS WQABCVAJNWAXTE-UHFFFAOYSA-N 0.000 description 1
- JGUQDUKBUKFFRO-CIIODKQPSA-N dimethylglyoxime Chemical compound O/N=C(/C)\C(\C)=N\O JGUQDUKBUKFFRO-CIIODKQPSA-N 0.000 description 1
- NALBLJLOBICXRH-UHFFFAOYSA-N dinitrogen monohydride Chemical group N=[N] NALBLJLOBICXRH-UHFFFAOYSA-N 0.000 description 1
- 239000000982 direct dye Substances 0.000 description 1
- 125000002228 disulfide group Chemical group 0.000 description 1
- MNQDKWZEUULFPX-UHFFFAOYSA-M dithiazanine iodide Chemical compound [I-].S1C2=CC=CC=C2[N+](CC)=C1C=CC=CC=C1N(CC)C2=CC=CC=C2S1 MNQDKWZEUULFPX-UHFFFAOYSA-M 0.000 description 1
- 150000004662 dithiols Chemical class 0.000 description 1
- 229950004394 ditiocarb Drugs 0.000 description 1
- NFDRPXJGHKJRLJ-UHFFFAOYSA-N edtmp Chemical compound OP(O)(=O)CN(CP(O)(O)=O)CCN(CP(O)(O)=O)CP(O)(O)=O NFDRPXJGHKJRLJ-UHFFFAOYSA-N 0.000 description 1
- 230000005672 electromagnetic field Effects 0.000 description 1
- 238000007336 electrophilic substitution reaction Methods 0.000 description 1
- 230000009881 electrostatic interaction Effects 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 230000012202 endocytosis Effects 0.000 description 1
- 230000003511 endothelial effect Effects 0.000 description 1
- ZUBDGKVDJUIMQQ-UBFCDGJISA-N endothelin-1 Chemical compound C([C@@H](C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(O)=O)NC(=O)[C@H]1NC(=O)[C@H](CC=2C=CC=CC=2)NC(=O)[C@@H](CC=2C=CC(O)=CC=2)NC(=O)[C@H](C(C)C)NC(=O)[C@H]2CSSC[C@@H](C(N[C@H](CO)C(=O)N[C@@H](CO)C(=O)N[C@H](CC(C)C)C(=O)N[C@@H](CCSC)C(=O)N[C@H](CC(O)=O)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCC(O)=O)C(=O)N2)=O)NC(=O)[C@@H](CO)NC(=O)[C@H](N)CSSC1)C1=CNC=N1 ZUBDGKVDJUIMQQ-UBFCDGJISA-N 0.000 description 1
- 230000002255 enzymatic effect Effects 0.000 description 1
- 210000003743 erythrocyte Anatomy 0.000 description 1
- 125000004185 ester group Chemical group 0.000 description 1
- 229940011871 estrogen Drugs 0.000 description 1
- 239000000262 estrogen Substances 0.000 description 1
- 150000002170 ethers Chemical class 0.000 description 1
- 125000004494 ethyl ester group Chemical group 0.000 description 1
- 125000004672 ethylcarbonyl group Chemical group [H]C([H])([H])C([H])([H])C(*)=O 0.000 description 1
- IYBKWXQWKPSYDT-UHFFFAOYSA-L ethylene glycol disuccinate bis(sulfo-N-succinimidyl) ester sodium salt Chemical compound [Na+].[Na+].O=C1C(S(=O)(=O)[O-])CC(=O)N1OC(=O)CCC(=O)OCCOC(=O)CCC(=O)ON1C(=O)C(S([O-])(=O)=O)CC1=O IYBKWXQWKPSYDT-UHFFFAOYSA-L 0.000 description 1
- OUDSFQBUEBFSPS-UHFFFAOYSA-N ethylenediaminetriacetic acid Chemical compound OC(=O)CNCCN(CC(O)=O)CC(O)=O OUDSFQBUEBFSPS-UHFFFAOYSA-N 0.000 description 1
- 125000006125 ethylsulfonyl group Chemical group 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 230000008020 evaporation Effects 0.000 description 1
- 239000002095 exotoxin Substances 0.000 description 1
- 231100000776 exotoxin Toxicity 0.000 description 1
- 239000000194 fatty acid Substances 0.000 description 1
- 229930195729 fatty acid Natural products 0.000 description 1
- 230000005308 ferrimagnetism Effects 0.000 description 1
- 230000005307 ferromagnetism Effects 0.000 description 1
- 239000000208 fibrin degradation product Substances 0.000 description 1
- 108010068611 fibrin fragment E-2 Proteins 0.000 description 1
- 108010020275 fibrin receptor Proteins 0.000 description 1
- 229940012952 fibrinogen Drugs 0.000 description 1
- 239000003527 fibrinolytic agent Substances 0.000 description 1
- 230000003480 fibrinolytic effect Effects 0.000 description 1
- 239000012467 final product Substances 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- 238000001917 fluorescence detection Methods 0.000 description 1
- 239000006260 foam Substances 0.000 description 1
- 125000002485 formyl group Chemical group [H]C(*)=O 0.000 description 1
- 238000013467 fragmentation Methods 0.000 description 1
- 238000006062 fragmentation reaction Methods 0.000 description 1
- 238000004108 freeze drying Methods 0.000 description 1
- 229960000936 fumagillin Drugs 0.000 description 1
- 238000007306 functionalization reaction Methods 0.000 description 1
- HZHFFEYYPYZMNU-UHFFFAOYSA-K gadodiamide Chemical compound [Gd+3].CNC(=O)CN(CC([O-])=O)CCN(CC([O-])=O)CCN(CC([O-])=O)CC(=O)NC HZHFFEYYPYZMNU-UHFFFAOYSA-K 0.000 description 1
- 150000008275 galactosamines Chemical class 0.000 description 1
- 108010003460 galactosyl-neoglycoalbumin Proteins 0.000 description 1
- 210000001035 gastrointestinal tract Anatomy 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 239000003349 gelling agent Substances 0.000 description 1
- 238000007429 general method Methods 0.000 description 1
- 208000007565 gingivitis Diseases 0.000 description 1
- 208000005017 glioblastoma Diseases 0.000 description 1
- 239000000174 gluconic acid Substances 0.000 description 1
- 235000012208 gluconic acid Nutrition 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 235000013922 glutamic acid Nutrition 0.000 description 1
- 239000004220 glutamic acid Substances 0.000 description 1
- 229940096919 glycogen Drugs 0.000 description 1
- 125000003827 glycol group Chemical group 0.000 description 1
- 229930182470 glycoside Natural products 0.000 description 1
- JAXFJECJQZDFJS-XHEPKHHKSA-N gtpl8555 Chemical compound OC(=O)C[C@H](N)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](C(C)C)C(=O)N1CCC[C@@H]1C(=O)N[C@H](B1O[C@@]2(C)[C@H]3C[C@H](C3(C)C)C[C@H]2O1)CCC1=CC=C(F)C=C1 JAXFJECJQZDFJS-XHEPKHHKSA-N 0.000 description 1
- 150000004820 halides Chemical class 0.000 description 1
- 208000019622 heart disease Diseases 0.000 description 1
- 201000011066 hemangioma Diseases 0.000 description 1
- 239000002554 heparinoid Substances 0.000 description 1
- 229940025770 heparinoids Drugs 0.000 description 1
- 206010073071 hepatocellular carcinoma Diseases 0.000 description 1
- GNOIPBMMFNIUFM-UHFFFAOYSA-N hexamethylphosphoric triamide Chemical compound CN(C)P(=O)(N(C)C)N(C)C GNOIPBMMFNIUFM-UHFFFAOYSA-N 0.000 description 1
- WQPDUTSPKFMPDP-OUMQNGNKSA-N hirudin Chemical compound C([C@@H](C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC=1C=CC(OS(O)(=O)=O)=CC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(O)=O)NC(=O)[C@H](CC(O)=O)NC(=O)CNC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CCCCN)NC(=O)[C@H]1N(CCC1)C(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)CNC(=O)[C@@H](NC(=O)[C@@H](NC(=O)[C@H]1NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CCC(O)=O)NC(=O)CNC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)CNC(=O)[C@H](CC(C)C)NC(=O)[C@H]([C@@H](C)CC)NC(=O)[C@@H]2CSSC[C@@H](C(=O)N[C@@H](CCC(O)=O)C(=O)NCC(=O)N[C@@H](CO)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@H](C(=O)N[C@H](C(NCC(=O)N[C@@H](CCC(N)=O)C(=O)NCC(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCCCN)C(=O)N2)=O)CSSC1)C(C)C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H]1NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)CNC(=O)[C@H](CO)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@@H](NC(=O)[C@H](CC=2C=CC(O)=CC=2)NC(=O)[C@@H](NC(=O)[C@@H](N)C(C)C)C(C)C)[C@@H](C)O)CSSC1)C(C)C)[C@@H](C)O)[C@@H](C)O)C1=CC=CC=C1 WQPDUTSPKFMPDP-OUMQNGNKSA-N 0.000 description 1
- 229940006607 hirudin Drugs 0.000 description 1
- 125000000717 hydrazino group Chemical group [H]N([*])N([H])[H] 0.000 description 1
- 150000002431 hydrogen Chemical class 0.000 description 1
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 1
- 230000007062 hydrolysis Effects 0.000 description 1
- 238000006460 hydrolysis reaction Methods 0.000 description 1
- 230000002209 hydrophobic effect Effects 0.000 description 1
- WGCNASOHLSPBMP-UHFFFAOYSA-N hydroxyacetaldehyde Natural products OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 description 1
- 206010020718 hyperplasia Diseases 0.000 description 1
- 230000002390 hyperplastic effect Effects 0.000 description 1
- 230000007954 hypoxia Effects 0.000 description 1
- 150000002460 imidazoles Chemical class 0.000 description 1
- NBZBKCUXIYYUSX-UHFFFAOYSA-N iminodiacetic acid Chemical compound OC(=O)CNCC(O)=O NBZBKCUXIYYUSX-UHFFFAOYSA-N 0.000 description 1
- 230000002163 immunogen Effects 0.000 description 1
- 102000018358 immunoglobulin Human genes 0.000 description 1
- 229940072221 immunoglobulins Drugs 0.000 description 1
- 239000007943 implant Substances 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 235000019239 indanthrene blue RS Nutrition 0.000 description 1
- UHOKSCJSTAHBSO-UHFFFAOYSA-N indanthrone blue Chemical compound C1=CC=C2C(=O)C3=CC=C4NC5=C6C(=O)C7=CC=CC=C7C(=O)C6=CC=C5NC4=C3C(=O)C2=C1 UHOKSCJSTAHBSO-UHFFFAOYSA-N 0.000 description 1
- 229960004657 indocyanine green Drugs 0.000 description 1
- MOFVSTNWEDAEEK-UHFFFAOYSA-M indocyanine green Chemical compound [Na+].[O-]S(=O)(=O)CCCCN1C2=CC=C3C=CC=CC3=C2C(C)(C)C1=CC=CC=CC=CC1=[N+](CCCCS([O-])(=O)=O)C2=CC=C(C=CC=C3)C3=C2C1(C)C MOFVSTNWEDAEEK-UHFFFAOYSA-M 0.000 description 1
- 230000007574 infarction Effects 0.000 description 1
- 230000002757 inflammatory effect Effects 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 229920000592 inorganic polymer Polymers 0.000 description 1
- 238000009434 installation Methods 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- VBMVTYDPPZVILR-UHFFFAOYSA-N iron(2+);oxygen(2-) Chemical class [O-2].[Fe+2] VBMVTYDPPZVILR-UHFFFAOYSA-N 0.000 description 1
- 230000007794 irritation Effects 0.000 description 1
- 230000000302 ischemic effect Effects 0.000 description 1
- CTAPFRYPJLPFDF-UHFFFAOYSA-N isoxazole Chemical class C=1C=NOC=1 CTAPFRYPJLPFDF-UHFFFAOYSA-N 0.000 description 1
- 210000003734 kidney Anatomy 0.000 description 1
- 201000010982 kidney cancer Diseases 0.000 description 1
- FZLIPJUXYLNCLC-UHFFFAOYSA-N lanthanum atom Chemical compound [La] FZLIPJUXYLNCLC-UHFFFAOYSA-N 0.000 description 1
- 229910052745 lead Inorganic materials 0.000 description 1
- 239000002523 lectin Substances 0.000 description 1
- 230000003902 lesion Effects 0.000 description 1
- 108010057821 leucylproline Proteins 0.000 description 1
- DJQJFMSHHYAZJD-UHFFFAOYSA-N lidofenin Chemical compound CC1=CC=CC(C)=C1NC(=O)CN(CC(O)=O)CC(O)=O DJQJFMSHHYAZJD-UHFFFAOYSA-N 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 239000012035 limiting reagent Substances 0.000 description 1
- 150000002632 lipids Chemical class 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 239000007791 liquid phase Substances 0.000 description 1
- 210000004185 liver Anatomy 0.000 description 1
- 208000014018 liver neoplasm Diseases 0.000 description 1
- 210000004072 lung Anatomy 0.000 description 1
- 201000005202 lung cancer Diseases 0.000 description 1
- 210000004698 lymphocyte Anatomy 0.000 description 1
- 150000002678 macrocyclic compounds Chemical class 0.000 description 1
- 210000002540 macrophage Anatomy 0.000 description 1
- 208000002780 macular degeneration Diseases 0.000 description 1
- NXPHGHWWQRMDIA-UHFFFAOYSA-M magnesium;carbanide;bromide Chemical compound [CH3-].[Mg+2].[Br-] NXPHGHWWQRMDIA-UHFFFAOYSA-M 0.000 description 1
- FPYJFEHAWHCUMM-UHFFFAOYSA-N maleic anhydride Chemical compound O=C1OC(=O)C=C1 FPYJFEHAWHCUMM-UHFFFAOYSA-N 0.000 description 1
- 208000015486 malignant pancreatic neoplasm Diseases 0.000 description 1
- OCSMOTCMPXTDND-OUAUKWLOSA-N marimastat Chemical compound CNC(=O)[C@H](C(C)(C)C)NC(=O)[C@H](CC(C)C)[C@H](O)C(=O)NO OCSMOTCMPXTDND-OUAUKWLOSA-N 0.000 description 1
- 229950008959 marimastat Drugs 0.000 description 1
- 230000001404 mediated effect Effects 0.000 description 1
- DZVCFNFOPIZQKX-LTHRDKTGSA-M merocyanine Chemical compound [Na+].O=C1N(CCCC)C(=O)N(CCCC)C(=O)C1=C\C=C\C=C/1N(CCCS([O-])(=O)=O)C2=CC=CC=C2O\1 DZVCFNFOPIZQKX-LTHRDKTGSA-M 0.000 description 1
- 230000002503 metabolic effect Effects 0.000 description 1
- 150000002736 metal compounds Chemical class 0.000 description 1
- NYGZLYXAPMMJTE-UHFFFAOYSA-M metanil yellow Chemical group [Na+].[O-]S(=O)(=O)C1=CC=CC(N=NC=2C=CC(NC=3C=CC=CC=3)=CC=2)=C1 NYGZLYXAPMMJTE-UHFFFAOYSA-M 0.000 description 1
- 230000009401 metastasis Effects 0.000 description 1
- 230000001394 metastastic effect Effects 0.000 description 1
- 206010061289 metastatic neoplasm Diseases 0.000 description 1
- CXKWCBBOMKCUKX-UHFFFAOYSA-M methylene blue Chemical compound [Cl-].C1=CC(N(C)C)=CC2=[S+]C3=CC(N(C)C)=CC=C3N=C21 CXKWCBBOMKCUKX-UHFFFAOYSA-M 0.000 description 1
- 125000000325 methylidene group Chemical group [H]C([H])=* 0.000 description 1
- 229960000907 methylthioninium chloride Drugs 0.000 description 1
- 230000005012 migration Effects 0.000 description 1
- 238000013508 migration Methods 0.000 description 1
- 239000003226 mitogen Substances 0.000 description 1
- 230000011278 mitosis Effects 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 239000002808 molecular sieve Substances 0.000 description 1
- 239000000983 mordant dye Substances 0.000 description 1
- VMGAPWLDMVPYIA-HIDZBRGKSA-N n'-amino-n-iminomethanimidamide Chemical compound N\N=C\N=N VMGAPWLDMVPYIA-HIDZBRGKSA-N 0.000 description 1
- ZIUHHBKFKCYYJD-UHFFFAOYSA-N n,n'-methylenebisacrylamide Chemical compound C=CC(=O)NCNC(=O)C=C ZIUHHBKFKCYYJD-UHFFFAOYSA-N 0.000 description 1
- OKPYIWASQZGASP-UHFFFAOYSA-N n-(2-hydroxypropyl)-2-methylprop-2-enamide Chemical compound CC(O)CNC(=O)C(C)=C OKPYIWASQZGASP-UHFFFAOYSA-N 0.000 description 1
- GHGCFJGBPOQLPE-UHFFFAOYSA-N n-(6-aminohexyl)-2-[3-[2-[(4-chlorophenyl)methoxy]-2-(2,4-dichlorophenyl)ethyl]-2h-imidazol-1-yl]acetamide Chemical compound C1=CN(CC(=O)NCCCCCCN)CN1CC(C=1C(=CC(Cl)=CC=1)Cl)OCC1=CC=C(Cl)C=C1 GHGCFJGBPOQLPE-UHFFFAOYSA-N 0.000 description 1
- 239000002105 nanoparticle Substances 0.000 description 1
- 230000014399 negative regulation of angiogenesis Effects 0.000 description 1
- 150000002815 nickel Chemical class 0.000 description 1
- MGFYIUFZLHCRTH-UHFFFAOYSA-N nitrilotriacetic acid Chemical compound OC(=O)CN(CC(O)=O)CC(O)=O MGFYIUFZLHCRTH-UHFFFAOYSA-N 0.000 description 1
- 125000006501 nitrophenyl group Chemical group 0.000 description 1
- 231100000252 nontoxic Toxicity 0.000 description 1
- 230000003000 nontoxic effect Effects 0.000 description 1
- SJYNFBVQFBRSIB-UHFFFAOYSA-N norbornadiene Chemical compound C1=CC2C=CC1C2 SJYNFBVQFBRSIB-UHFFFAOYSA-N 0.000 description 1
- 238000012633 nuclear imaging Methods 0.000 description 1
- 230000000269 nucleophilic effect Effects 0.000 description 1
- 235000015097 nutrients Nutrition 0.000 description 1
- 230000014207 opsonization Effects 0.000 description 1
- 239000011368 organic material Substances 0.000 description 1
- 239000011146 organic particle Substances 0.000 description 1
- 125000002092 orthoester group Chemical group 0.000 description 1
- 201000008482 osteoarthritis Diseases 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 150000002923 oximes Chemical class 0.000 description 1
- 150000002924 oxiranes Chemical class 0.000 description 1
- 229960003540 oxyquinoline Drugs 0.000 description 1
- 239000003002 pH adjusting agent Substances 0.000 description 1
- 230000000242 pagocytic effect Effects 0.000 description 1
- 201000002528 pancreatic cancer Diseases 0.000 description 1
- 208000008443 pancreatic carcinoma Diseases 0.000 description 1
- 238000007911 parenteral administration Methods 0.000 description 1
- 239000011236 particulate material Substances 0.000 description 1
- 230000007170 pathology Effects 0.000 description 1
- 230000001175 peptic effect Effects 0.000 description 1
- 229940124633 peptidic drug Drugs 0.000 description 1
- 208000030613 peripheral artery disease Diseases 0.000 description 1
- 108040007629 peroxidase activity proteins Proteins 0.000 description 1
- 150000002989 phenols Chemical class 0.000 description 1
- 229950000688 phenothiazine Drugs 0.000 description 1
- UEZVMMHDMIWARA-UHFFFAOYSA-M phosphonate Chemical compound [O-]P(=O)=O UEZVMMHDMIWARA-UHFFFAOYSA-M 0.000 description 1
- 150000003009 phosphonic acids Chemical class 0.000 description 1
- 150000008300 phosphoramidites Chemical class 0.000 description 1
- 229910052698 phosphorus Inorganic materials 0.000 description 1
- 239000011574 phosphorus Substances 0.000 description 1
- LFGREXWGYUGZLY-UHFFFAOYSA-N phosphoryl Chemical group [P]=O LFGREXWGYUGZLY-UHFFFAOYSA-N 0.000 description 1
- 239000000049 pigment Substances 0.000 description 1
- 125000000587 piperidin-1-yl group Chemical group [H]C1([H])N(*)C([H])([H])C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 229920001432 poly(L-lactide) Polymers 0.000 description 1
- 229920000233 poly(alkylene oxides) Polymers 0.000 description 1
- 239000002745 poly(ortho ester) Substances 0.000 description 1
- 229920001281 polyalkylene Polymers 0.000 description 1
- 229920002647 polyamide Polymers 0.000 description 1
- 108010064470 polyaspartate Proteins 0.000 description 1
- 239000004632 polycaprolactone Substances 0.000 description 1
- 125000003367 polycyclic group Polymers 0.000 description 1
- 108010077051 polycysteine Proteins 0.000 description 1
- 229920000867 polyelectrolyte Polymers 0.000 description 1
- 239000004848 polyfunctional curative Substances 0.000 description 1
- 239000010318 polygalacturonic acid Substances 0.000 description 1
- 229920002704 polyhistidine Polymers 0.000 description 1
- 229920000193 polymethacrylate Polymers 0.000 description 1
- 229920005862 polyol Polymers 0.000 description 1
- 150000003077 polyols Chemical class 0.000 description 1
- 229920001155 polypropylene Polymers 0.000 description 1
- 229920001451 polypropylene glycol Polymers 0.000 description 1
- 229920002451 polyvinyl alcohol Polymers 0.000 description 1
- 235000019422 polyvinyl alcohol Nutrition 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 150000004032 porphyrins Chemical class 0.000 description 1
- JCBJVAJGLKENNC-UHFFFAOYSA-M potassium ethyl xanthate Chemical compound [K+].CCOC([S-])=S JCBJVAJGLKENNC-UHFFFAOYSA-M 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 230000002062 proliferating effect Effects 0.000 description 1
- 230000035755 proliferation Effects 0.000 description 1
- 108010029020 prolylglycine Proteins 0.000 description 1
- 229940024999 proteolytic enzymes for treatment of wounds and ulcers Drugs 0.000 description 1
- 125000002112 pyrrolidino group Chemical group [*]N1C([H])([H])C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 150000003246 quinazolines Chemical class 0.000 description 1
- MCJGNVYPOGVAJF-UHFFFAOYSA-N quinolin-8-ol Chemical compound C1=CN=C2C(O)=CC=CC2=C1 MCJGNVYPOGVAJF-UHFFFAOYSA-N 0.000 description 1
- IZMJMCDDWKSTTK-UHFFFAOYSA-N quinoline yellow Chemical compound C1=CC=CC2=NC(C3C(C4=CC=CC=C4C3=O)=O)=CC=C21 IZMJMCDDWKSTTK-UHFFFAOYSA-N 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 150000003254 radicals Chemical class 0.000 description 1
- 230000005258 radioactive decay Effects 0.000 description 1
- 238000000163 radioactive labelling Methods 0.000 description 1
- 239000012217 radiopharmaceutical Substances 0.000 description 1
- 229940121896 radiopharmaceutical Drugs 0.000 description 1
- 230000002799 radiopharmaceutical effect Effects 0.000 description 1
- 230000003439 radiotherapeutic effect Effects 0.000 description 1
- GZUITABIAKMVPG-UHFFFAOYSA-N raloxifene Chemical compound C1=CC(O)=CC=C1C1=C(C(=O)C=2C=CC(OCCN3CCCCC3)=CC=2)C2=CC=C(O)C=C2S1 GZUITABIAKMVPG-UHFFFAOYSA-N 0.000 description 1
- 229960004622 raloxifene Drugs 0.000 description 1
- 239000000376 reactant Substances 0.000 description 1
- 230000035484 reaction time Effects 0.000 description 1
- 238000001953 recrystallisation Methods 0.000 description 1
- 238000006268 reductive amination reaction Methods 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 238000007634 remodeling Methods 0.000 description 1
- BOLDJAUMGUJJKM-LSDHHAIUSA-N renifolin D Natural products CC(=C)[C@@H]1Cc2c(O)c(O)ccc2[C@H]1CC(=O)c3ccc(O)cc3O BOLDJAUMGUJJKM-LSDHHAIUSA-N 0.000 description 1
- 230000000250 revascularization Effects 0.000 description 1
- 230000002441 reversible effect Effects 0.000 description 1
- WUAPFZMCVAUBPE-UHFFFAOYSA-N rhenium atom Chemical compound [Re] WUAPFZMCVAUBPE-UHFFFAOYSA-N 0.000 description 1
- PYWVYCXTNDRMGF-UHFFFAOYSA-N rhodamine B Chemical class [Cl-].C=12C=CC(=[N+](CC)CC)C=C2OC2=CC(N(CC)CC)=CC=C2C=1C1=CC=CC=C1C(O)=O PYWVYCXTNDRMGF-UHFFFAOYSA-N 0.000 description 1
- 238000007142 ring opening reaction Methods 0.000 description 1
- 229960003522 roquinimex Drugs 0.000 description 1
- 229910052707 ruthenium Inorganic materials 0.000 description 1
- AHTFMWCHTGEJHA-UHFFFAOYSA-N s-(2,5-dioxooxolan-3-yl) ethanethioate Chemical compound CC(=O)SC1CC(=O)OC1=O AHTFMWCHTGEJHA-UHFFFAOYSA-N 0.000 description 1
- ORIHZIZPTZTNCU-YVMONPNESA-N salicylaldoxime Chemical compound O\N=C/C1=CC=CC=C1O ORIHZIZPTZTNCU-YVMONPNESA-N 0.000 description 1
- 239000000523 sample Substances 0.000 description 1
- 239000004576 sand Substances 0.000 description 1
- BBIKPGRUAMIMIA-UHFFFAOYSA-N sapb Chemical compound C1SCC(C(=O)NC(CC(N)=O)C(O)=O)NC(=O)C(C(C)O)NC(=O)C(C(C)O)NC(=O)C(C(C)CC)NC(=O)C(=C)NC(=O)C(CC(C)C)NC(=O)C(CO)NC(=O)C1NC(=O)C(CC(O)=O)NC(=O)CNC(=O)C1NC(=O)C(CC(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC(C)C)NC(=O)C(=C)NC(=O)C(C)NC(=O)C(CCCNC(N)=N)NC(=O)C(NC(=O)CNC(=O)C(N)C(C)O)CSC1 BBIKPGRUAMIMIA-UHFFFAOYSA-N 0.000 description 1
- 229920006395 saturated elastomer Polymers 0.000 description 1
- 230000003248 secreting effect Effects 0.000 description 1
- 230000028327 secretion Effects 0.000 description 1
- 125000001439 semicarbazido group Chemical group [H]N([H])C(=O)N([H])N([H])* 0.000 description 1
- 210000002966 serum Anatomy 0.000 description 1
- 230000035939 shock Effects 0.000 description 1
- 229940074386 skatole Drugs 0.000 description 1
- 239000001632 sodium acetate Substances 0.000 description 1
- 235000017281 sodium acetate Nutrition 0.000 description 1
- URGAHOPLAPQHLN-UHFFFAOYSA-N sodium aluminosilicate Chemical compound [Na+].[Al+3].[O-][Si]([O-])=O.[O-][Si]([O-])=O URGAHOPLAPQHLN-UHFFFAOYSA-N 0.000 description 1
- 229910000029 sodium carbonate Inorganic materials 0.000 description 1
- 239000008354 sodium chloride injection Substances 0.000 description 1
- BAZAXWOYCMUHIX-UHFFFAOYSA-M sodium perchlorate Chemical compound [Na+].[O-]Cl(=O)(=O)=O BAZAXWOYCMUHIX-UHFFFAOYSA-M 0.000 description 1
- 229910001488 sodium perchlorate Inorganic materials 0.000 description 1
- 235000019832 sodium triphosphate Nutrition 0.000 description 1
- ULARYIUTHAWJMU-UHFFFAOYSA-M sodium;1-[4-(2,5-dioxopyrrol-1-yl)butanoyloxy]-2,5-dioxopyrrolidine-3-sulfonate Chemical compound [Na+].O=C1C(S(=O)(=O)[O-])CC(=O)N1OC(=O)CCCN1C(=O)C=CC1=O ULARYIUTHAWJMU-UHFFFAOYSA-M 0.000 description 1
- HHSGWIABCIVPJT-UHFFFAOYSA-M sodium;1-[4-[(2-iodoacetyl)amino]benzoyl]oxy-2,5-dioxopyrrolidine-3-sulfonate Chemical compound [Na+].O=C1C(S(=O)(=O)[O-])CC(=O)N1OC(=O)C1=CC=C(NC(=O)CI)C=C1 HHSGWIABCIVPJT-UHFFFAOYSA-M 0.000 description 1
- JJGWLCLUQNFDIS-GTSONSFRSA-M sodium;1-[6-[5-[(3as,4s,6ar)-2-oxo-1,3,3a,4,6,6a-hexahydrothieno[3,4-d]imidazol-4-yl]pentanoylamino]hexanoyloxy]-2,5-dioxopyrrolidine-3-sulfonate Chemical compound [Na+].O=C1C(S(=O)(=O)[O-])CC(=O)N1OC(=O)CCCCCNC(=O)CCCC[C@H]1[C@H]2NC(=O)N[C@H]2CS1 JJGWLCLUQNFDIS-GTSONSFRSA-M 0.000 description 1
- 239000007790 solid phase Substances 0.000 description 1
- 238000001179 sorption measurement Methods 0.000 description 1
- 230000036262 stenosis Effects 0.000 description 1
- 208000037804 stenosis Diseases 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 229910052712 strontium Inorganic materials 0.000 description 1
- 125000005504 styryl group Chemical group 0.000 description 1
- ACTRVOBWPAIOHC-XIXRPRMCSA-N succimer Chemical compound OC(=O)[C@@H](S)[C@@H](S)C(O)=O ACTRVOBWPAIOHC-XIXRPRMCSA-N 0.000 description 1
- 229960005346 succimer Drugs 0.000 description 1
- JJAHTWIKCUJRDK-UHFFFAOYSA-N succinimidyl 4-(N-maleimidomethyl)cyclohexane-1-carboxylate Chemical compound C1CC(CN2C(C=CC2=O)=O)CCC1C(=O)ON1C(=O)CCC1=O JJAHTWIKCUJRDK-UHFFFAOYSA-N 0.000 description 1
- 235000000346 sugar Nutrition 0.000 description 1
- 239000003774 sulfhydryl reagent Substances 0.000 description 1
- 125000000565 sulfonamide group Chemical group 0.000 description 1
- BDHFUVZGWQCTTF-UHFFFAOYSA-M sulfonate Chemical compound [O-]S(=O)=O BDHFUVZGWQCTTF-UHFFFAOYSA-M 0.000 description 1
- 150000003457 sulfones Chemical group 0.000 description 1
- 150000003464 sulfur compounds Chemical class 0.000 description 1
- 239000011975 tartaric acid Substances 0.000 description 1
- 235000002906 tartaric acid Nutrition 0.000 description 1
- 229910052713 technetium Inorganic materials 0.000 description 1
- GKLVYJBZJHMRIY-UHFFFAOYSA-N technetium atom Chemical compound [Tc] GKLVYJBZJHMRIY-UHFFFAOYSA-N 0.000 description 1
- 238000005287 template synthesis Methods 0.000 description 1
- BNWCETAHAJSBFG-UHFFFAOYSA-N tert-butyl 2-bromoacetate Chemical compound CC(C)(C)OC(=O)CBr BNWCETAHAJSBFG-UHFFFAOYSA-N 0.000 description 1
- ZJXHVYSDMUKUCA-UHFFFAOYSA-N tert-butyl 3-aminopropanoate Chemical compound CC(C)(C)OC(=O)CCN ZJXHVYSDMUKUCA-UHFFFAOYSA-N 0.000 description 1
- RIYPCUVFZLHLRZ-UHFFFAOYSA-N tert-butyl n-[6-[[2-[3-[2-[(4-chlorophenyl)methoxy]-2-(2,4-dichlorophenyl)ethyl]-2h-imidazol-1-yl]acetyl]amino]hexyl]carbamate Chemical compound C1=CN(CC(=O)NCCCCCCNC(=O)OC(C)(C)C)CN1CC(C=1C(=CC(Cl)=CC=1)Cl)OCC1=CC=C(Cl)C=C1 RIYPCUVFZLHLRZ-UHFFFAOYSA-N 0.000 description 1
- YNHJECZULSZAQK-UHFFFAOYSA-N tetraphenylporphyrin Chemical compound C1=CC(C(=C2C=CC(N2)=C(C=2C=CC=CC=2)C=2C=CC(N=2)=C(C=2C=CC=CC=2)C2=CC=C3N2)C=2C=CC=CC=2)=NC1=C3C1=CC=CC=C1 YNHJECZULSZAQK-UHFFFAOYSA-N 0.000 description 1
- 150000004905 tetrazines Chemical class 0.000 description 1
- 229910052716 thallium Inorganic materials 0.000 description 1
- TXBBUSUXYMIVOS-UHFFFAOYSA-N thenoyltrifluoroacetone Chemical compound FC(F)(F)C(=O)CC(=O)C1=CC=CS1 TXBBUSUXYMIVOS-UHFFFAOYSA-N 0.000 description 1
- 229940126585 therapeutic drug Drugs 0.000 description 1
- 239000001016 thiazine dye Substances 0.000 description 1
- 125000001984 thiazolidinyl group Chemical group 0.000 description 1
- DUYAAUVXQSMXQP-UHFFFAOYSA-M thioacetate Chemical compound CC([S-])=O DUYAAUVXQSMXQP-UHFFFAOYSA-M 0.000 description 1
- 125000002813 thiocarbonyl group Chemical group *C(*)=S 0.000 description 1
- ATGUDZODTABURZ-UHFFFAOYSA-N thiolan-2-ylideneazanium;chloride Chemical compound Cl.N=C1CCCS1 ATGUDZODTABURZ-UHFFFAOYSA-N 0.000 description 1
- 150000003585 thioureas Chemical class 0.000 description 1
- 210000000115 thoracic cavity Anatomy 0.000 description 1
- 229960004072 thrombin Drugs 0.000 description 1
- 229910052718 tin Inorganic materials 0.000 description 1
- 238000003325 tomography Methods 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 238000005809 transesterification reaction Methods 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- 238000000844 transformation Methods 0.000 description 1
- 102000003601 transglutaminase Human genes 0.000 description 1
- 230000007704 transition Effects 0.000 description 1
- 102000027257 transmembrane receptors Human genes 0.000 description 1
- 108091008578 transmembrane receptors Proteins 0.000 description 1
- 238000006478 transmetalation reaction Methods 0.000 description 1
- 125000005627 triarylcarbonium group Chemical group 0.000 description 1
- 150000003852 triazoles Chemical class 0.000 description 1
- 229910052722 tritium Inorganic materials 0.000 description 1
- 125000000430 tryptophan group Chemical group [H]N([H])C(C(=O)O*)C([H])([H])C1=C([H])N([H])C2=C([H])C([H])=C([H])C([H])=C12 0.000 description 1
- 238000002604 ultrasonography Methods 0.000 description 1
- 238000012285 ultrasound imaging Methods 0.000 description 1
- 230000002792 vascular Effects 0.000 description 1
- 210000005166 vasculature Anatomy 0.000 description 1
- 230000004862 vasculogenesis Effects 0.000 description 1
- 108010047303 von Willebrand Factor Proteins 0.000 description 1
- 102100036537 von Willebrand factor Human genes 0.000 description 1
- 229960001134 von willebrand factor Drugs 0.000 description 1
- 238000010792 warming Methods 0.000 description 1
- 239000008215 water for injection Substances 0.000 description 1
- 238000009736 wetting Methods 0.000 description 1
- 230000029663 wound healing Effects 0.000 description 1
- 239000001018 xanthene dye Substances 0.000 description 1
- 239000008096 xylene Substances 0.000 description 1
- NLIVDORGVGAOOJ-MAHBNPEESA-M xylene cyanol Chemical compound [Na+].C1=C(C)C(NCC)=CC=C1C(\C=1C(=CC(OS([O-])=O)=CC=1)OS([O-])=O)=C\1C=C(C)\C(=[NH+]/CC)\C=C/1 NLIVDORGVGAOOJ-MAHBNPEESA-M 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K51/00—Preparations containing radioactive substances for use in therapy or testing in vivo
- A61K51/12—Preparations containing radioactive substances for use in therapy or testing in vivo characterised by a special physical form, e.g. emulsion, microcapsules, liposomes, characterized by a special physical form, e.g. emulsions, dispersions, microcapsules
- A61K51/1241—Preparations containing radioactive substances for use in therapy or testing in vivo characterised by a special physical form, e.g. emulsion, microcapsules, liposomes, characterized by a special physical form, e.g. emulsions, dispersions, microcapsules particles, powders, lyophilizates, adsorbates, e.g. polymers or resins for adsorption or ion-exchange resins
- A61K51/1255—Granulates, agglomerates, microspheres
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K49/00—Preparations for testing in vivo
- A61K49/0002—General or multifunctional contrast agents, e.g. chelated agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K49/00—Preparations for testing in vivo
- A61K49/001—Preparation for luminescence or biological staining
- A61K49/0013—Luminescence
- A61K49/0017—Fluorescence in vivo
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K49/00—Preparations for testing in vivo
- A61K49/001—Preparation for luminescence or biological staining
- A61K49/0063—Preparation for luminescence or biological staining characterised by a special physical or galenical form, e.g. emulsions, microspheres
- A61K49/0069—Preparation for luminescence or biological staining characterised by a special physical or galenical form, e.g. emulsions, microspheres the agent being in a particular physical galenical form
- A61K49/0089—Particulate, powder, adsorbate, bead, sphere
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K49/00—Preparations for testing in vivo
- A61K49/06—Nuclear magnetic resonance [NMR] contrast preparations; Magnetic resonance imaging [MRI] contrast preparations
- A61K49/08—Nuclear magnetic resonance [NMR] contrast preparations; Magnetic resonance imaging [MRI] contrast preparations characterised by the carrier
- A61K49/085—Nuclear magnetic resonance [NMR] contrast preparations; Magnetic resonance imaging [MRI] contrast preparations characterised by the carrier conjugated systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K49/00—Preparations for testing in vivo
- A61K49/06—Nuclear magnetic resonance [NMR] contrast preparations; Magnetic resonance imaging [MRI] contrast preparations
- A61K49/08—Nuclear magnetic resonance [NMR] contrast preparations; Magnetic resonance imaging [MRI] contrast preparations characterised by the carrier
- A61K49/10—Organic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K51/00—Preparations containing radioactive substances for use in therapy or testing in vivo
- A61K51/02—Preparations containing radioactive substances for use in therapy or testing in vivo characterised by the carrier, i.e. characterised by the agent or material covalently linked or complexing the radioactive nucleus
- A61K51/04—Organic compounds
- A61K51/041—Heterocyclic compounds
- A61K51/044—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine, rifamycins
- A61K51/0459—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine, rifamycins having six-membered rings with two nitrogen atoms as the only ring hetero atoms, e.g. piperazine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K51/00—Preparations containing radioactive substances for use in therapy or testing in vivo
- A61K51/02—Preparations containing radioactive substances for use in therapy or testing in vivo characterised by the carrier, i.e. characterised by the agent or material covalently linked or complexing the radioactive nucleus
- A61K51/04—Organic compounds
- A61K51/0497—Organic compounds conjugates with a carrier being an organic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K51/00—Preparations containing radioactive substances for use in therapy or testing in vivo
- A61K51/02—Preparations containing radioactive substances for use in therapy or testing in vivo characterised by the carrier, i.e. characterised by the agent or material covalently linked or complexing the radioactive nucleus
- A61K51/04—Organic compounds
- A61K51/08—Peptides, e.g. proteins, carriers being peptides, polyamino acids, proteins
- A61K51/088—Peptides, e.g. proteins, carriers being peptides, polyamino acids, proteins conjugates with carriers being peptides, polyamino acids or proteins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K51/00—Preparations containing radioactive substances for use in therapy or testing in vivo
- A61K51/12—Preparations containing radioactive substances for use in therapy or testing in vivo characterised by a special physical form, e.g. emulsion, microcapsules, liposomes, characterized by a special physical form, e.g. emulsions, dispersions, microcapsules
- A61K51/1241—Preparations containing radioactive substances for use in therapy or testing in vivo characterised by a special physical form, e.g. emulsion, microcapsules, liposomes, characterized by a special physical form, e.g. emulsions, dispersions, microcapsules particles, powders, lyophilizates, adsorbates, e.g. polymers or resins for adsorption or ion-exchange resins
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Optics & Photonics (AREA)
- Physics & Mathematics (AREA)
- Pharmacology & Pharmacy (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Radiology & Medical Imaging (AREA)
- Engineering & Computer Science (AREA)
- Dispersion Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Biomedical Technology (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Peptides Or Proteins (AREA)
- Magnetic Resonance Imaging Apparatus (AREA)
- Ultra Sonic Daignosis Equipment (AREA)
- Steroid Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
- Apparatus For Radiation Diagnosis (AREA)
Abstract
Description
Diese Erfindung bezieht sich auf diagnostische Bilderzeugungstechniken, mit denen ein Krankheitszustand unter Verwenden eines Zielkontrastmittels abgebildet werden kann. Insbesondere bezieht sich die Erfindung auf die Verwendung derartiger Kontrastmittel, bei denen der Targetingvektor an Rezeptoren bindet, die mit Angiogenese assoziiert sind. Derartige Kontrastmittel können daher für die Diagnose von beispielsweise malignen Krankheiten, Herzkrankheiten, entzündungs-bezogenen Krankheiten, rheumatoider Arthritis und Kaposi-Sarkom verwendet werden.These This invention relates to diagnostic imaging techniques, with which a disease state using a target contrast agent can be displayed. In particular, the invention relates to the use of such contrast agents in which the targeting vector binds to receptors associated with angiogenesis. such Contrast agents can therefore for the diagnosis of, for example, malignant diseases, heart disease, inflammation-related Diseases, rheumatoid arthritis and Kaposi's sarcoma become.
Neue
Blutgefäße können durch
zwei verschiedene Mechanismen gebildet werden:
Vaskulogenese
oder Angiogenese. Angiogenese ist die Bildung neuer Blutgefäße durch
Abzweigung von existierenden Gefäßen. Der
primäre
Stimulus für
diesen Prozess kann eine unangemessene Versorgung von Zellen in
einem Gewebe mit Nährstoffen
und Sauerstoff (Hypoxia) sein. Die Zellen können durch Absondern von angiogenen
Faktoren reagieren, von denen es viele gibt; ein Beispiel, auf das
häufig
Bezug genommen wird, ist der vaskuläre endotheliale Wachstumsfaktor
(VEGF). Diese Faktoren initiieren die Sekretion von proteolytischen
Enzymen, die die Proteine der Basalmembran zerlegen, wie auch Inhibitoren,
die die Wirkung dieser möglicherweise
schädlichen
Enzyme beschränken.
Die andere herausragende Wirkung von angiogenen Faktoren ist es,
endotheliale Zellen zu veranlassen, dass sie wandern und sich teilen.
Endotheliale Zellen, die an die Basalmembran gebunden sind, die
ein kontinuierliches Stück
um Blutgefäße auf der
kontraluminalen Seite bildet, durchlaufen keine Mitose. Die kombinierte
Wirkung des Verlustes der Bindung und der Signale von den Rezeptoren
für angiogene
Faktoren ist, dass die endothelialen Zellen veranlasst werden, sich
zu bewegen, zu vervielfachen und sich selbst wieder anzuordnen,
und schließlich
eine Basalmembran um die neuen Gefäße zu synthetisieren.New blood vessels can be formed by two different mechanisms:
Vasculogenesis or angiogenesis. Angiogenesis is the formation of new blood vessels by diversion of existing vessels. The primary stimulus to this process may be inadequate supply of cells in a tissue containing nutrients and oxygen (hypoxia). The cells can respond by secreting angiogenic factors, of which there are many; One example that is frequently referred to is vascular endothelial growth factor (VEGF). These factors initiate the secretion of proteolytic enzymes that break down the proteins of the basement membrane, as well as inhibitors that limit the action of these potentially harmful enzymes. The other prominent effect of angiogenic factors is to cause endothelial cells to migrate and divide. Endothelial cells bound to the basement membrane, which forms a continuous piece around blood vessels on the contraluminal side, do not undergo mitosis. The combined effect of the loss of binding and the signals from the angiogenic factor receptors is that the endothelial cells are caused to move, multiply, and rearrange themselves, and eventually synthesize a basement membrane around the new vessels.
Angiogenese ist herausragend beim Wachstum und der Remodellierung von Geweben, einschließlich der Wundheilung und entzündlicher Prozesse. Tumore müssen Angiogenese initiieren, wenn sie eine Millimetergröße erreichen, um ihre Wachstumsgeschwindigkeit aufrechtzuerhalten. Da die Angiogenese von charakteristischen Änderungen in den endothelialen Zellen und ihrer Umgebung begleitet ist, ist dieser Prozess ein vielversprechendes Ziel für die therapeutische Intervention. Die Inhibierung von Angiogenese wird auch als eine vielversprechende Strategie für eine Antitumortherapie betrachtet. Die Transformationen, die Angiogenese begleiten, sind auch sehr vielversprechend für die Diagnose, ein offensichtliches Beispiel ist die maligne Krankheit, aber das Konzept berechtigt auch zu großen Hoffnungen bei einer Entzündung und einer Vielzahl von entzündungs-bezogenen Krankheiten, einschließlich Atherosklerose, wobei die Makrophagen von frühen atherosklerotischen Läsionen mögliche Quellen von angiogenen Faktoren sind. Diese Faktoren können auch in die Revaskularisation von Teilen des Myokards, die von einen Infarkt betroffen sind, involviert sein, was auftritt, falls eine Stenose innerhalb kurzer Zeit gelöst wird.angiogenesis is outstanding in the growth and remodeling of tissues, including the Wound healing and inflammatory Processes. Tumors need Initiate angiogenesis when they reach a millimeter size, to maintain their growth rate. Because angiogenesis of characteristic changes is accompanied in the endothelial cells and their environment is this process is a promising target for therapeutic intervention. The inhibition of angiogenesis is also considered to be a promising one Strategy for Considered an anti-tumor therapy. The transformations, the angiogenesis are also very promising for the diagnosis, an obvious one Example is the malignant disease, but the concept is justified too big Hopes of inflammation and a variety of inflammatory-related diseases, including Atherosclerosis, wherein the macrophages of early atherosclerotic lesions are possible sources of angiogenic factors. These factors can also affect the revascularization of parts of the myocardium affected by an infarct be what happens if a stenosis is resolved within a short time.
Bei der Angiogenese sind Rezeptoren involviert, die für endotheliale Zellen einmalig sind. Die Oberfläche dieser Zellen wird bei der Vorbereitung für die Migration remodelliert und verborgene Strukturen werden freigelegt, wo die Basalmembran abgebaut wird, zusätzlich zu der Vielzahl von Proteinen, die beim Bewirken und Kontrollieren der Proteolyse involviert sind.at angiogenesis are receptors involved in endothelial Cells are unique. The surface These cells are remodeled in preparation for the migration and hidden structures are exposed where the basement membrane is mined, in addition to the variety of proteins involved in creating and controlling proteolysis are involved.
Eine
Anzahl bekannter Rezeptoren/Targets, die mit Angiogenese assoziiert
sind, sind unten in Tabelle 1 aufgelistet. Im Falle von Tumoren
ist das resultierende Netzwerk von Blutgefäßen üblicherweise disorganisiert
mit der Bildung von scharfen Knicken und auch arteriovenösen Shunts.
Unter Verwenden der Targetingprinzipien, die in der vorliegenden
Offenbarung beschrieben werden, kann Angiogenese durch die Mehrzahl der
Bilderzeugungsmodalitäten,
die in der Medizin verwendet werden, detektiert werden. Tabelle
1 Rezeptoren/Targets, assoziiert mit Angiogenese
- Anmerkung: Viele Hormone, Wachstumsfaktoren und andere Verbindungen, die an Zelloberflächenrezeptoren binden, können als Vektoren wirken durch Binden an ihre Rezeptoren, oder, wenn sie bereits an die Zelloberfläche gebunden sind, sind sie Targets für Vektoren, die an sie binden, z.B. Antikörper.
- Note: Many hormones, growth factors and other compounds that bind to cell surface receptors can act as vectors by binding to their receptors or, if already attached to the cell surface, are targets for vectors that bind to them, eg antibodies.
Wie
oben erläutert
sind viele unerwünschte
Zustände
mit Neovaskularisation oder Angiogenese, der Entwicklung oder Proliferation
neuer Blutgefäße assoziiert.
Beispiele für
derartige Zustände
sind unten in Tabelle 2 aufgelistet. Tabelle
2 – Krankheiten
und Indikationen, assoziiert mit Angiogenese
Die
Oberflächenzellen,
endothelialen Zellen, von derartigen neuen Blutgefäßen haben
Konzentrationen verschiedener Oberflächen- oder Transmembranrezeptoren,
die größer sind
als normal, wie beispielsweise Rezeptortyrosinkinasen (RTK), und
es wurde vorgeschlagen, radiomarkierte oder Chromophor-markierte Antikörper gegen
derartige Rezeptoren zu verwenden, oder auf ähnliche Weise markierte Analoga
von natürlichen
Proteinliganden für
derartige Rezeptoren, als ein Mittel zum Detektieren der Zentren
von Angiogenese (siehe z.B.
Peptidische Liganden haben jedoch relativ wenig Bindungsstellen für detektierbare Marker (Reporter) und die Bindung von Reportern an viele Stellen auf derartigen peptidischen Liganden wird die Konformationen beeinflussen, die der Ligand annehmen kann. Ein weiteres Problem mit Peptiden ist, dass sie in vivo oft instabil sind.peptidic However, ligands have relatively few binding sites for detectable Markers (reporters) and the binding of reporters in many places on such peptidic ligands will affect the conformations, which the ligand can accept. Another problem with peptides is that they are often unstable in vivo.
Es gibt deshalb immer noch eine Notwendigkeit für Verfahren, die Bilder erzeugen, in denen wirksame zielausgerichtete Kontrastmittel mit Affinitäten für mit Angiogenese assozierte Rezeptoren verwendet werden.It Therefore, there is still a need for methods that produce images, in which are effective targeted contrast media with affinities for angiogenesis Associated receptors are used.
Daher
stellt die Erfindung, ausgehend von einem Aspekt, ein Verfahren
zum Erzeugen eines Bildes eines lebenden menschlichen oder nicht-menschlichen
tierischen Subjektes bereit, dem zuvor ein Kontrastmittel verabreicht
worden ist, umfassend Erzeugen eines Bildes mindestens eines Teils
des Subjekts, dadurch gekennzeichnet, dass das Kontrastmittel eine
Zusammensetzung eines Materials der Formel (I) ist,
Wo R eine makromolekulare oder teilchenförmige Spezies ist, die eine Vielzahl von Markern bereitstellt, können diese Marker sein, die individuell detektierbar sind (z.B. paramagnetische oder radioaktive Spezien) oder sie können Wechselwirken, um ein detektierbares Material zu erzeugen, z.B. mittels eines kooperativen magnetischen Phänomens. Beispiele derartiger Multireporter umfassen Polychelate und polyionische Spezien und ferromagnetische, ferrimagnetische und superparamagnetische Teilchen.Where R is a macromolecular or particulate species having a Providing variety of markers can be those markers that individually detectable (e.g., paramagnetic or radioactive Species) or they can Interacting to produce a detectable material, e.g. by means of a cooperative magnetic phenomenon. Examples of such Multireporter include polychelates and polyionic species and ferromagnetic, ferrimagnetic and superparamagnetic particles.
In vielen Fällen wird die Stoffzusammensetzung der Formel I eine charakterisierbare Verbindung sein. In anderen kann sie eine Kombination von Verbindungen sein, die gebunden oder andernfalls miteinander assoziiert, z.B. konjugiert sind. Der Einfachheit halber wird die Stoffzusammensetzung im Folgenden als ein Mittel bezeichnet.In many cases the substance composition of the formula I becomes a characterizable Be connected. In others, it can be a combination of compounds be that bound or otherwise associated with each other, e.g. are conjugated. For the sake of simplicity, the composition of matter hereinafter referred to as a means.
Kontrastmittel,
umfassend Gas-enthaltende Reporter, sind beschrieben in unserer
parallel anhängigen Internationalen
Patenanmeldung Nr.
In einem Aspekt stellt die Erfindung bereit ein Verfahren zur Erzeugung eines Bildes eines lebendigen menschlichen oder nicht-menschlichen (bevorzugt Säuger oder Vogel) tierischen Subjektes, dem zuvor ein Kontrastmittel verabreicht worden war, z.B. in das vaskuläre System oder den Gi-Trakt, und zur Erzeugung eines Bildes mindestens eines Teils des Subjektes, an das das Kontrastmittel verabreicht wurde, z.B. durch Röntgenstrahlung, MR, Ultraschall, Szintigraphie, PET, SPECT, Electrical Impedance, licht- oder magnetometrische Bilderzeugungsmodalitäten, dadurch gekennzeichnet, dass als das Kontrastmittel ein Mittel der Formel I verwendet wird.In In one aspect, the invention provides a method of production a picture of a living human or non-human (preferably mammal or bird) animal subject previously administered a contrast agent had been, e.g. into the vascular System or the Gi tract, and to create an image at least a part of the subject to whom the contrast agent is administered was, e.g. by X-radiation, MR, Ultrasound, Scintigraphy, PET, SPECT, Electrical Impedance, light or magnetometric imaging modalities, thereby in that, as the contrast agent, an agent of the formula I is used.
Von
einem weiteren Aspekt aus gesehen stellt die Erfindung bereit ein
Verfahren zum Überwachen
des Effekts einer Behandlung eines menschlichen oder nicht-menschlichen tierischen
Subjekts mit einem Arzneimittel, um einen mit Angiogenese verbundenen
Zustand zu bekämpfen
z.B. ein zytotoxisches Mittel, wobei das Verfahren umfasst Detektieren
der Aufnahme einer zuvor verabreichten Zusammensetzung der Formel
I
Die Mittel der Formel I haben drei charakteristische Komponenten: einen Vektor (V); einen Linker (L); und einen Reporter (R). Der Vektor muss die Fähigkeit haben, die Verbindung in einen Bereich der Angiogenese ins Ziel zu bringen, der Reporter muss in einer in vivo-Diagnosebilderzeugungsprozedur detektierbar sein; und der Linker muss den Vektor an den Reporter koppeln, zumindest bis der Reporter an den Bereich der Angiogenese geliefert wurde, und bevorzugt bis die Bilderzeugungsprozedur abgeschlossen ist.The Agents of formula I have three characteristic components: one Vector (V); a linker (L); and a reporter (R). The vector must have the ability have the connection in one area of angiogenesis to the target To bring the reporter into an in vivo diagnostic imaging procedure be detectable; and the linker needs the vector to the reporter couple, at least until the reporter to the field of angiogenesis and preferably until the image-forming procedure is completed is.
Vektorenvectors
Als der Vektor kann eine beliebige peptidische oder bevorzugter nicht-peptidische Verbindung mit einer Affinität für Rezeptoren, assoziiert mit Angiogenese, verwendet werden.When the vector may be any peptide or more preferably non-peptidic Connection with an affinity for receptors, associated with angiogenesis.
Nicht-peptidische Verbindungen werden bevorzugt verwendet, da peptidische Vektoren im Allgemeinen eine schlechte biologische Stabilität besitzen werden und unerwünschte Reaktionen des Körpers provozieren können.Non-peptidic Compounds are preferably used because peptidic vectors generally have poor biological stability become and unwanted Reactions of the body can provoke.
Bevorzugt ist der Vektor eine Verbindung, die keinerlei nicht akzeptable biologische Reaktion auslöst, insbesondere eine Verbindung, die tatsächlich nicht Angiogenese fördert.Prefers the vector is a compound that does not contain any unacceptable biological Reaction triggers, in particular a connection that actually does not promote angiogenesis.
Besonders bevorzugt ist der Vektor ein Angiogeneseinhibitor, insbesondere bevorzugt ein nicht-peptidischer Angiogeneseinhibitor.Especially Preferably, the vector is an angiogenesis inhibitor, in particular preferably a non-peptidic angiogenesis inhibitor.
Beispiele
von nicht-peptidischen Angiogeneseinhibitoren werden in
Beispiele
von peptidischen Angiogeneseinhibitoren werden in
Besondere
Angiogeneseinhibitoren in Entwicklung umfassen jene, die unten in
Tabelle 3 aufgelistet sind: Tabelle 3 – Angiogeneseinhibitoren
Andere
bekannte Verbindungen, die des Targetings von Bereichen der Angiogenese
fähig sind,
sind unten in Tabelle 4 aufgelistet. Tabelle
4 – Vektormoleküle mit bekannter
Affinität
für Rezeptoren,
assoziiert mit Angiogenese
Auf ähnliche
Weise können
die Verbindungen, die in
Besondere
Beispiele von Vektorverbindungen, die in einigen der oben erwähnten Patentveröffentlichungen
erwähnt
werden, sind wie folgt:
Ar1 und Ar2 aromatische
Gruppen sind und verschieden oder dieselben sein können; und
X eine verbindende Gruppe ist, z.B. o, S, SO2,
CO, CHCN, Alkyl, Alkoxy oder Alkoxyalkyl, und wobei
A für N oder
CH steht; R1 für H, -CONH, -CONHR5,
COOH, -COOR5, SO2NH2 steht; R2 für H, NH2, NHCOPh, -NHCOR5,
-NHCHO, -NHR5, -N(R5)2 steht; und R5 ein
Alkyl mit 1-6 Kohlenstoffatomen ist, z.B.Specific examples of vector compounds mentioned in some of the above-mentioned patent publications are as follows:
Ar 1 and Ar 2 are aromatic groups and may be different or the same; and X is a linking group, for example, O, S, SO 2 , CO, CHCN, alkyl, alkoxy or alkoxyalkyl, and in which
A is N or CH; R 1 is H, -CONH, -CONHR 5 , COOH, -COOR 5 , SO 2 NH 2 ; R 2 is H, NH 2 , NHCOPh, -NHCOR 5 , -NHCHO, -NHR 5 , -N (R 5 ) 2 ; and R 5 is an alkyl of 1-6 carbon atoms, eg
X
für O,
COO steht; und M ein Übergangsmetall
ist; und wobei
X1 und X2 substituierte
oder unsubstituierte Phenyl- oder Naphthylgruppen sind; Y1 und Y2 Halogenatome,
Aminogruppen oder mono- oder di-substituierte Aminogruppen sind;
und Z für
NHC2H4NH steht oder
ein substituierter oder unsubstituierter aromatischer Diaminrest
ist, z.B.
X is O, COO; and M is a transition metal; and in which
X 1 and X 2 are substituted or unsubstituted phenyl or naphthyl groups; Y 1 and Y 2 are halogen atoms, amino groups or mono- or di-substituted amino groups; and Z is NHC 2 H 4 NH or is a substituted or unsubstituted aromatic diamine residue, eg
leu-pro-ala-leu-pro-glu-asp-gly-gly-xx-gly-ala-phe-pro-pro-gly
(xx
= unidentifizierte Aminosäureeinheit).
leu-pro-ala-leu-pro-glu-asp-gly-gly-xx-gly-ala-phe-pro-pro-gly
(xx = unidentified amino acid unit).
Ein
HDGF-Peptidfragment ist auch offenbart, das eine N-terminale Aminosäureextensionssequenz besitzt,
die umfasst:
(ala/ser)-(leu/arg)-pro-(ala/gly)-(leu/pro)-ala-gly-thr-met-ala-(ala)-gly-ser-(isoleu)-thr-thr-leu An HDGF peptide fragment is also disclosed having an N-terminal amino acid extension sequence comprising:
(Ala / ser) - (leu / arg) -Pro- (ala / gly) - (leu / pro) -ala-gly-thr-met-ala- (ala) -Gly-Ser (isoleu) -Thr- thr-leu
R1 und
R3 für
H, Me, -C(O)(C1-C6 Alkyl),
-C(O)Ar stehen; Ar optional substituiertes Phenyl ist; und R2 Pyrrolidino oder Piperidino ist, z.B.
R 1 and R 3 are H, Me, -C (O) (C 1 -C 6 alkyl), -C (O) Ar; Ar is optionally substituted phenyl; and R 2 is pyrrolidino or piperidino is, for example
MPF-4MPF-4
- NH2-Ser-Gln-Val-Arg-Pro-Arg-His-Ile-Thr-Ser-Leu-Glu-Val-Ile-Lys-Ala-Gly-Pro-His-Cys-Pro-Thr-Ala-Gln-Leu-Ile-Ala-Thr-Leu-Lys-Asn-Gly-Arg-Lys-Ile-Cys-Leu-Asp-Leu-Gln-Ala-Pro-Leu-Tyr-Lys-Lys-Ile-Ile-Lys-Lys-Leu-Leu-Glu-Ser-COOHNH 2 -Ser-Gln-Val-Arg-Pro-Arg-His-Ile-Thr-Ser-Leu-Glu-Val-Ile-Lys-Ala-Gly-Pro-His-Cys-Pro-Thr-Ala-Gln -Leu-Ile-Ala-Thr-Leu-Lys-Asn-Gly-Arg-Lys-Ile-Cys-Leu-Asp-Leu-Gln-Ala-Pro-Leu-Tyr-Lys-Lys-Ile-Ile-Lys -Lys-Leu-Leu-Glu-Ser-COOH
CPF-4CPF-4
- NH2-Ser-Gln-Val-Arg-Pro-Arg-His-Ile-Thr-Ser-Leu-Glu-Val-Ile-Lys-Ala-Gly-Pro-His-Cys-Pro-Thr-Ala-Gln-Leu-Ile-Ala-Thr-Leu-Lys-Asn-Gly-Arg-Lys-Ile-Cys-Leu-Asp-Leu-Gln-Ala-Pro-Leu-Tyr-Lys-Ile-Ile-Lys-Lys-Leu-Leu-Glu-Ser-COOH-disulfid, gebunden an ein zweites Protein mit der Aminosäuresequenz NH2-Glu-Ala-Glu-Glu-Asp-Gly- Asp-Leu-Gln-Cys-Leu-Cys-Val-Lys-Thr-Thr-COOH. Es gibt Disulfidbrücken zwischen Cys-20 von MPF-4 und Cys-10 des genannten zweiten Proteins und zwischen Cys-36 von MPF-4 und Cys-12 des genannten zweiten Proteins.NH 2 -Ser-Gln-Val-Arg-Pro-Arg-His-Ile-Thr-Ser-Leu-Glu-Val-Ile-Lys-Ala-Gly-Pro-His-Cys-Pro-Thr-Ala-Gln -Leu-Ile-Ala-Thr-Leu-Lys-Asn-Gly-Arg-Lys-Ile-Cys-Leu-Asp-Leu-Gln-Ala-Pro-Leu-Tyr-Lys-Ile-Ile-Lys-Lys Leu-Leu-Glu-Ser-COOH disulfide bound to a second protein having the amino acid sequence NH 2 -Glu-Ala-Glu-Glu-Asp-Gly-Asp-Leu-Gln-Cys-Leu-Cys-Val Lys-Thr-Thr-COOH. There are disulfide bonds between Cys-20 of MPF-4 and Cys-10 of said second protein and Cys-36 of MPF-4 and Cys-12 of said second protein.
R1 bis
R4 jeweils unabhängig für eines oder mehrere von -X,
N3, -NO2, Halo,
Trifluormethyl, R5, OR5,
-CH2OR6, -OCOR5, -CH2COOR5, -NHCOR5, -CH2NHCOR5, -NR5R6, -CH2NR5R6, -CH2NO2, CONR5R6, CH2CONR5R6, -COOR5, -CH3COOR5, -CHO und CH2CHO
steht und -X unabhängig
für -SO3R5, -CH2PO3R5R6,
-CH2O3R5, -OSO3R5, -CH2OSO3R5, -NHSO3R5, -CH2NHSO3R5, OPO3R5R6, -CH2OPO3R5R6 und
-PO3R5R6 steht,
wobei R5 und R6 unabhängig aus
-H und Niederalkyl ausgewählt
sind und wobei A eine chemische Gruppe ist, die mindestens 5 bis
nicht mehr als 30 Bindungen umfasst, die die Naphthylgruppen direkt
verbinden, vorausgesetzt, dass (i) die Verbindung nicht Suramin
ist und (ii) wenn A nicht ist, wobei
m
und n unabhängig
0, 1 oder 2 sind, dann mindestens eine von R1 bis
R4 für
-OH oder eine saure Gruppe steht; und der pharmazeutisch annehmbaren
Salze, Ester, Salze derartiger Ester oder Amide derartiger Verbindungen.
R 1 to R 4 are each independently one or more of -X, N 3 , -NO 2 , halo, trifluoromethyl, R 5 , OR 5 , -CH 2 OR 6 , -OCOR 5 , -CH 2 COOR 5 , -NHCOR 5 , -CH 2 NHCOR 5 , -NR 5 R 6 , -CH 2 NR 5 R 6 , -CH 2 NO 2 , CONR 5 R 6 , CH 2 CONR 5 R 6 , -COOR 5 , -CH 3 COOR 5 , -CHO and CH 2 CHO and -X independently represent -SO 3 R 5 , -CH 2 PO 3 R 5 R 6 , -CH 2 O 3 R 5 , -OSO 3 R 5 , -CH 2 OSO 3 R 5 , -NHSO 3 R 5 , -CH 2 NHSO 3 R 5 , OPO 3 R 5 R 6 , -CH 2 OPO 3 R 5 R 6 and -PO 3 R 5 R 6 , where R 5 and R 6 are independently -H and lower alkyl and wherein A is a chemical group comprising at least 5 to not more than 30 bonds connecting the naphthyl groups directly, provided that (i) the compound is not suramin and (ii) when A is not is, where
m and n are independently 0, 1 or 2, then at least one of R 1 to R 4 is -OH or an acidic group; and the pharmaceutically acceptable salts, esters, salts of such esters or amides of such compounds.
Es werden auch Verbindungen beschrieben, in denen die Verbindung von A zum Naphthylring über eine Amid- oder Sulfonamidgruppe stattfindet. Außerdem kann A in einigen Fällen eine Gruppe der Formel II sein. A kann auch von geradkettigen oder verzweigten Alkylgruppen, Arylgruppen, Alkylarylgruppen, aliphatischen Dicarbonsäuren, Polgenen und Derivaten davon und Polyolen und Derivaten davon ausgewählt sein. Einige weitere Verbindungen besitzen die Formeln: Compounds are also described in which the connection of A to the naphthyl ring takes place via an amide or sulfonamide group. In addition, A may in some cases be a group of formula II. A may also be selected from straight chain or branched alkyl groups, aryl groups, alkylaryl groups, aliphatic dicarboxylic acids, polynes and derivatives thereof, and polyols and derivatives thereof. Some other compounds have the formulas:
X für -CONHOH
oder COOH steht, in erster Linie gekennzeichnet durch das Vorhandensein
einer Gruppe der Formel (II) im Substituenten R3 und/oder
R4 z.B.
X is -CONHOH or COOH, characterized primarily by the presence of a group of the formula (II) in the substituent R 3 and / or R 4 eg
Besonders
bevorzugte Vektoren umfassen Aminosäurederivate, wie in
CAM-D und andere in Frage kommenden Identifikations- und Evaluationstechniken wie oben erwähnt können auch verwendet werden, um weitere in Frage kommende peptidische und nicht-peptidische Vektoren zu finden oder zu bewerten.CAM-D and other eligible identification and evaluation techniques as mentioned above can also used to further eligible peptidic and non-peptidic Find or rate vectors.
Daher ist es auch möglich, Moleküle zu erhalten, die speziell an mit Angiogenese assoziierte Rezeptoren binden, durch direktes Screenen molekularer Bibliotheken. Screening peptidischer Bibliotheken kann auch verwendet werden, um allgemein wirksame peptidische Strukturen zu identifizieren, von denen nicht-peptidische Analoga durch herkömmliche oder kombinatorische Chemie erzeugt werden können. Bindungseinheiten, die auf diese Weise identifiziert sind, können an ein Linkermolekül gekoppelt werden, was ein allgemeines Werkzeug zum Binden eines beliebigen Vektormoleküls (oder -moleküle) an den Reporter bildet.Therefore it is also possible molecules specifically to angiogenesis-associated receptors bind, by directly screening molecular libraries. screening Peptidic libraries can also be used to generalize to identify effective peptidic structures, of which non-peptidic Analogues by conventional or combinatorial chemistry can be generated. Bonding units, the Identified in this way can be coupled to a linker molecule become what a common tool for tying any vector molecule (or molecules) to the reporter.
Vektormoleküle können aus kombinatorischen Bibliotheken erzeugt werden, ohne notwendigerweise das genaue molekulare Target zu kennen, durch funktionelles Selektieren (in vitro, ex vivo oder in vivo) von Molekülen, die an den Bereich/die Struktur, die abgebildet werden soll, binden.Vector molecules can out combinatorial libraries are generated, without necessarily the to know the exact molecular target by functional selection (in vitro, ex vivo or in vivo) of molecules attached to the region (s) Structure to be imaged bind.
Wie
oben erwähnt,
umfassen die Mittel der Formel I Vektor-, Linker- und Reportereinheiten.
Eine Linkereinheit kann dazu dienen, einen Vektor mit einem Reporter
zu verbinden; alternativ kann sie mehr als einen Vektor und/oder
mehr als einen Reporter miteinander verbinden. Auf ähnliche
Weise kann ein Reporter oder ein Vektor mit mehr als einem Linker
verbunden werden. Die Verwendung einer Mehrzahl von Reportern auf diese
Weise (z.B. mehrere Linker-Reportereinheiten, gebunden an einen
Vektor oder mehrere Reporter, gebunden an einen Linker, der selbst
an einen Vektor gebunden ist) kann ermöglichen, dass die Detektierbarkeit des
Kontrastmittels vergrößert wird
(z.B. durch Vergrößern der
Strahlenundurchlässigkeit,
der Echogenität oder
der Relaxivity) oder kann ermöglichen,
dass es in mehr als einer Bilderzeugungsmodalität detektiert wird. Eine Verwendung
einer Mehrzahl von Vektoren auf diese Weise kann die Targetingeffizienz
des Kontrastmittels vergrößern oder
kann das Kontrastmittel befähigen,
auf mehr als eine Stelle, z.B. verschiedene Rezeptoren für ein Mittel,
das eine Rezeptorheterogenität
hat, zu zielen. Daher kann zum Beispiel das Mittel der Formel I Vektoreinheiten
mit Affinitätsstellen
umfassen, die andere sind als mit Angiogenese assoziierte Rezeptoren, z.B.
mit Affinitäten
für Zeltoberflächen auf
Körperduktuswandoberflächen. Demgemäß kann das
Mittel Vektoren umfassen, wie Antikörperfragmente und Oligopeptide,
z.B. RGD oder analoge Zelloberflächenbindungspeptidmotife
(z.B. wie in
Es ist besonders bevorzugt, dass derartige zusätzliche Vektoren derart binden sollten, dass sie die Bewegung des Mittels im Blutstrom verlangsamen, aber sie nicht verhindern, und es am Ort verankern, wenn es an eine Rezeptorstelle assoziiert mit Angiogenese gebunden wird.It it is particularly preferred that such additional vectors bind in such a way should slow down the movement of the agent in the blood stream, but do not prevent it, and anchor it in place when it is at one Receptor site associated with angiogenesis is bound.
Funktionelle Gruppen (z.B. Aminogruppen, Hydroxylgruppen, Carboxygruppen, Thiolgruppen, etc.) auf der Vektorverbindung können zum Binden des Vektors an die Linkereinheit oder direkt an die Reportereinheit verwendet werden, z.B. unter Verwenden konventioneller chemischer Kopplungstechniken.functional Groups (e.g., amino groups, hydroxyl groups, carboxy groups, thiol groups, etc.) on the vector compound for binding the vector to the linker unit or directly to the reporter unit can be used, e.g. using conventional chemical Coupling techniques.
Wo der Vektor eine peptidische Verbindung ist, ist der Reporter ein Multireporter, z.B. ein metallierter Polychelatbildner (bevorzugt ein dendrimerer Polychelatbildner), ein magnetisches (bevorzugt superparamagnetisches) Teilchen, ein Vesikel, das konstratwirksame Teilchen oder eine Lösung eines kontrastwirksamen Moleküls enthält, eine polyionische Spezies (z.B. ein Polymer, das eine Vielzahl ionischer Gruppen, bevorzugt anionischer Gruppen trägt, z.B. ein Carboxylat, Phosphat oder Sulfonatpolymer).Where the vector is a peptidic compound, the reporter is one Multireporter, e.g. a metalated polychelant (preferred a dendrimeric polychelant), a magnetic (preferred superparamagnetic) particle, a vesicle, the Particles or a solution a contrasting molecule contains a polyionic species (e.g., a polymer containing a variety of ionic Groups, preferably anionic groups, e.g. a carboxylate, phosphate or sulfonate polymer).
Wo der Vektor nicht-peptidisch ist, kann der Reporter ein Multireporter sein oder alternativ einen oder eine kleine Anzahl (z.B. bis zu 10) detektierbarer Marker aufweisen, z.B. chelatierte paramagnetische Metallionen, kovalent gebundene oder chelatierte Radioisotope und Chromophore (oder Fluorophore, etc.). Wo der Reporter ein kovalent gebundenes Radionuklid ist oder aufweist, ist dies ein lodradionuklid bevorzugt gegenüber einem Tritium- oder 13C-Atom.Where the vector is nonpeptidic, the reporter may be a multireporter or alternatively have one or a small number (eg, up to 10) detectable markers, eg, chelated paramagnetic metal ions, covalently bound or chelated radioisotopes, and chromophores (or fluorophores, etc.). , Where the reporter is or has a covalently bound radionuclide, this is an iodine radionuclide preferred over a tritium or 13 C atom.
Linkerleft
Eine breite Vielzahl von Linkern kann verwendet werden, einschließlich bioabbaubare Linker und Biopolymere.A Wide variety of linkers can be used, including biodegradable ones Linker and biopolymers.
Die Linkerkomponente des Kontrastmittels ist am einfachsten eine Bindung zwischen dem Vektor und Reportereinheiten. Allgemeiner wird der Linker jedoch ein mono- oder multimolekulares Skelett bereitstellen, das kovalent oder nicht-kovalent einen oder mehrerer Vektoren mit einem oder mehreren Reportern verbindet, z.B. ein lineares, cyclisches, verzweigtes oder vernetztes molekulares Skelett, oder ein molekulares Aggregat, mit eingebauten oder seitlichen Gruppen, die kovalent oder nicht-kovalent, z.B. koordinativ, an die Vektor- und Reportereinheiten binden oder die derartige Einheiten einkapseln, einfangen oder verankern.The Linker component of the contrast agent is most easily a bond between the vector and reporters units. More general is the Left, however, a mono- or to provide a multimolecular skeleton that is covalent or non-covalent associates one or more vectors with one or more reporters, e.g. a linear, cyclic, branched or crosslinked molecular Skeleton, or a molecular aggregate, with built-in or lateral Groups which are covalently or non-covalently, e.g. coordinative, to the vector and reporter units bind or such units encapsulate, capture or anchor.
Daher kann das Verbinden einer Reportereinheit mit einem erwünschten Vektor durch kovalente oder nicht-kovalente Mittel erreicht werden, wobei üblicherweise eine Wechselwirkung mit einer oder mehreren funktionellen Gruppen angeordnet auf dem Reporter und/oder Vektor involviert ist. Beispiele von chemisch reaktiven funktionellen Gruppen, die für diesen Zweck eingesetzt werden können, umfassen Amino-, Hydroxyl-, Sulfhydryl-, Carboxyl- und Carbonylgruppen, wie auch Kohlenhydratgruppen, vicinale Diole, Thioether, 2-Aminoalkohole, 2-Aminothiole, Guanidinyl-, Imidazolyl- und Phenolgruppen.Therefore, joining a reporter moiety to a desired vector can be accomplished by covalent or non-covalent means, usually involving interaction with one or more functional groups arranged on the reporter and / or vector is involved. Examples of chemically reactive functional groups that can be used for this purpose include amino, hydroxyl, sulfhydryl, carboxyl and carbonyl groups, as well as carbohydrate groups, vicinal diols, thioethers, 2-amino alcohols, 2-aminothiols, guanidinyl, Imidazolyl and phenolic groups.
Kovalentes Koppeln von Reporter und Vektor kann daher bewirkt werden unter Verwenden von verbindenden Mitteln, die reaktive Einheiten enthalten, die der Reaktion mit der derartigen funktionellen Gruppen fähig sind. Beispiele von reaktiven Einheiten, die der Reaktion mit Sulfhydrylgruppen fähig sind, umfassen α-Haloacetylverbindungen des Typs X-CH2CO-(wobei X = Br, Cl oder I), die eine besondere Reaktivität für Sulfhydrylgruppen zeigen, die aber auch verwendet werden können, um Imidazolyl-, Thioether-, Phenol- und Aminogruppen zu modifizieren, wie von Gurd, F.R.N. in Methods Enzymol. (1967) 11, 532 beschrieben. N- Maleimidderivate können auch als selektiv gegenüber Sulfhydrylgruppen angesehen werden, können aber auch beim Koppeln an Aminogruppen unter bestimmten Bedingungen nützlich sein. Reagenzien, wie 2-Iminothiolan, z.B. wie beschrieben von Traut, R. et al. in Biochemistry (1973) 12, 3266, die eine Thiolgruppe durch Umwandlung einer Aminogruppe einführen, können als Sulfhydrylreagenzien angesehen werden, falls Verbinden durch die Bildung von Disulfidbrücken vorkommt. Daher können Reagenzien, die reaktive Disulfidbindungen in entweder den Reporter oder den Vektor einführen, nützlich sein, da das Verbinden durch Disulfidaustausch zwischen dem Vektor und dem Reporter herbeigeführt werden kann; Beispiele derartiger Reagenzien umfassen Ellman-Reagens (DTNB), 4,4'-Dithiodipyridin, Methyl-3-nitro-2-pyridyldisulfid und Methyl-2-pyridyldisulfid (beschrieben von Kimura, T. et al. in Analyt. Biochem. (1982) 122, 271).Covalent coupling of reporter and vector can therefore be effected using linking agents containing reactive moieties capable of reaction with such functional groups. Examples of reactive moieties capable of reaction with sulfhydryl groups include alpha-haloacetyl compounds of the type X-CH 2 CO- (where X = Br, Cl or I), which exhibit particular reactivity for sulfhydryl groups, but which may also be used to modify imidazolyl, thioether, phenol and amino groups as described by Gurd, FRN in Methods Enzymol. (1967) 11, 532. N-maleimide derivatives may also be considered selective to sulfhydryl groups, but may also be useful in coupling to amino groups under certain conditions. Reagents such as 2-iminothiolane, eg as described by Traut, R. et al. in Biochemistry (1973) 12, 3266, which introduce a thiol group by conversion of an amino group can be considered as sulfhydryl reagents, if joining occurs through the formation of disulfide bridges. Thus, reagents that introduce reactive disulfide bonds into either the reporter or the vector may be useful, as the joining can be induced by disulfide interchange between the vector and the reporter; Examples of such reagents include Ellman's reagent (DTNB), 4,4'-dithiodipyridine, methyl 3-nitro-2-pyridyl disulfide, and methyl 2-pyridyl disulfide (described by Kimura, T., et al., Analyt. Biochem ) 122, 271).
Beispiele reaktiver Einheiten, die der Reaktion mit Aminogruppen fähig sind, umfassen alkylierende und acylierende Mittel. Repräsentative alkylierende Mittel umfassen:
- i) α-Haloacetylverbindungen, die eine Spezifität gegenüber Aminogruppen in Abwesenheit reaktiver Thiolgruppen zeigen und vom Typ X-CH2CO- sind (wobei X=Cl, Br oder I), z.B. wie beschrieben von Wong, Y-H.H. in Biochemistry (1979) 24, 5337;
- ii) N-Maleimidderivate, die mit Aminogruppen entweder über eine Reaktion des Michael-Typs oder über Acylierung durch Addition an die Ringcarbonylgruppe reagieren können, wie von Smyth, D.G. et al. in J. Am. Chem. Soc. (1960) 82, 4600 und Biocher. J. (1964) 91, 589, beschrieben;
- iii) Arylhalogenide, wie reaktive nitrohaloaromatische Verbindungen;
- iv) Alkylhalogenide, wie von McKenzie, J.A. et al. in J. Protein Chem. (1988) 7, 581 beschrieben;
- v) Aldehyde und Ketone, die der Schiff-Basenbildung mit Aminogruppen fähig sind, wobei die gebildeten Addukte üblicherweise über eine Reduktion stabilisiert werden, um ein stabiles Amin zu ergeben;
- vi) Epoxidderivate, wie Epichlorohydrin und Bisoxirane, die mit Amino-, Sulfhydryl- oder Phenolhydroxylgruppen reagieren können;
- vii) Chlor enthaltende Derivate von s-Triazinen, die gegenüber Nukleophilen, wie Amino-, Sulfhydryl- und Hydroxygruppen, sehr reaktiv sind; viii) Aziridine, die auf oben im Detail angegebenen s-Triazinverbindungen basieren, z.B. wie beschrieben von Ross, W.C.J. in Adv. Cancer Res. (1954) 2, 1, die mit Nukleophilen, wie Aminogruppen, durch Ringöffnung reagieren;
- ix) Quadratsäurediethylester, wie von Tietze, L.F. in Chem. Ber. (1991) 124, 1215 beschrieben; und
- x) α-Haloalkylether, die reaktivere Alkylierungsmittel als normale Alkylhalogenide sind wegen der Aktivierung, die durch das Ethersauerstoffatom verursacht sind, z.B. wie beschrieben von Benneche, T. et al. in Eur. J. Med. Chem. (1993) 28, 463.
- i) α-haloacetyl compounds which exhibit specificity to amino groups in the absence of reactive thiol groups and are of the X-CH 2 CO- type (where X = Cl, Br or I), for example as described by Wong, YH.H. in Biochemistry (1979) 24, 5337;
- ii) N-maleimide derivatives which can react with amino groups either via a Michael-type reaction or via acylation by addition to the ring carbonyl group as described by Smyth, DG et al. in J. Am. Chem. Soc. (1960) 82, 4600 and Biocher. J. (1964) 91, 589;
- iii) aryl halides, such as reactive nitrohaloaromatic compounds;
- iv) alkyl halides as described by McKenzie, JA et al. in J. Protein Chem. (1988) 7, 581;
- v) aldehydes and ketones capable of Schiff base formation with amino groups, the adducts formed usually being stabilized via reduction to give a stable amine;
- vi) epoxide derivatives such as epichlorohydrin and bisoxiranes capable of reacting with amino, sulfhydryl or phenolic hydroxyl groups;
- vii) chlorine-containing derivatives of s-triazines which are highly reactive towards nucleophiles such as amino, sulfhydryl and hydroxy groups; viii) aziridines based on s-triazine compounds detailed above, eg as described by Ross, WCJ in Adv. Cancer Res. (1954) 2,1, which react with nucleophiles such as amino groups by ring opening;
- ix) diethyl squarate, as described by Tietze, LF in Chem. Ber. (1991) 124, 1215; and
- x) α-haloalkyl ethers which are more reactive alkylating agents than normal alkyl halides because of activation caused by the ether oxygen atom, eg as described by Benneche, T. et al. in Eur. J. Med. Chem. (1993) 28, 463.
Repräsentative aminoreaktive Acylierungsmittel umfassen:
- i) Isocyanate und Isothiocyanate, insbesondere aromatische Derivate, die stabile Harnstoff- bzw. Thioharnstoffderivate bilden und für die Proteinvernetzung verwendet wurden, wie von Schick, A.F. et al. in J. Biol. Chem. (1961) 236, 2477 beschrieben;
- ii) Sulfonylchloride, die von Herzig, D.J. et al. in Biopolymers (1964) 2, 349 beschrieben wurden, und die für die Einführung einer fluoreszierenden Reportergruppe in den Linker nützlich sein können,
- iii) Säurehalogenide;
- iv) aktive Ester, wie Nitrophenylester oder N-Hydroxysuccinimidylester;
- v) Säureanhydride, wie gemischte, symmetrische oder N-Carboxyanhydride;
- vi) andere nützliche Reagenzien für die Amidbindungsbildung, wie von Bodansky, M. et al. in "Principles of Peptide Synthesis" (1984) Springer-Verlag beschrieben;
- vii) Acylazide, z.B. in denen die Azidgruppe aus einem vorgebildeten Hydrazidderivat unter Verwenden von Natriumnitrit erzeugt wird, z.B. wie beschrieben von Wetz, K. et al. in Anal. Biochem. (1974) 58, 347;
- viii) Azlactone, gebunden an Polymere, wie Bisacrylamid, z.B. wie von Rasmussen, J.K. in Reactive Polymers (1991) 16, 199 beschrieben; und
- ix) Imidoester, die stabile Amidine bei der Reaktion mit Aminogruppen bilden, z.B. wie beschrieben von Hunter, M.J. und Ludwig, M.L. in J. Am. Chem. Soc. (1962) 84, 3491.
- i) isocyanates and isothiocyanates, in particular aromatic derivatives which form stable urea or thiourea derivatives and were used for protein crosslinking, as described by Schick, AF et al. in J. Biol. Chem. (1961) 236, 2477;
- ii) sulfonyl chlorides described by Herzig, DJ et al. in Biopolymers (1964) 2, 349, and which may be useful for the introduction of a fluorescent reporter group into the linker,
- iii) acid halides;
- iv) active esters, such as nitrophenyl esters or N-hydroxysuccinimidyl esters;
- v) acid anhydrides, such as mixed, symmetrical or N-carboxyanhydrides;
- vi) other useful reagents for amide bond formation as described by Bodansky, M. et al. in "Principles of Peptide Synthesis" (1984) Springer-Verlag;
- vii) acylazides, eg in which the azide group is generated from a preformed hydrazide derivative using sodium nitrite, eg as described by Wetz, K. et al. in anal. Biochem. (1974) 58, 347;
- viii) azlactones bonded to polymers such as bisacrylamide, for example as described by Rasmussen, JK in Reactive Polymers (1991) 16, 199; and
- ix) Imidoesters which form stable amidines in the reaction with amino groups, for example as described by Hunter, MJ and Ludwig, ML in J. Am. Chem. Soc. (1962) 84, 3491.
Carbonylgruppen, wie Aldehydfunktionen, können mit schwachen Proteinbasen bei einem derartigen pH zur Reaktion gebracht werden, dass die nukleophilen Proteinseitenkettenfunktionen protoniert werden. Schwache Basen umfassen 1,2-Aminothiole, wie jene, die in N-terminalen Cysteinresten gefunden werden, die selektiv stabile 5-gliedrige Thiazolidinringe mit Aldehydgruppen bilden, z.B. wie beschrieben von Ratner, S. et al. in J. Am. Chem. Soc. (1937) 59, 200. Andere schwache Basen, wie Phenylhydrazone können verwendet werden, z.B. wie beschrieben von Heitzman, J. et al. in Proc. Natl. Acad. Sci. USA (1974) 71, 3537.carbonyl groups, like aldehyde functions, can with weak protein bases at such a pH for reaction be brought that the nucleophilic protein side chain functions be protonated. Weak bases include 1,2-aminothiols, such as those in N-terminal ones Cysteine residues are found that selectively stably 5-membered Forming thiazolidine rings with aldehyde groups, e.g. as described by Ratner, S. et al. in J. Am. Chem. Soc. (1937) 59, 200. Others weak bases such as phenylhydrazones may be used, e.g. as described by Heitzman, J. et al. in proc. Natl. Acad. Sci. USA (1974) 71, 3537.
Aldehyde und Ketone können auch mit Aminen zur Reaktion gebracht werden, um Schiff-Basen zu bilden, die vorteilhafterweise über reduktive Aminierung stabilisiert werden können. Alkoxylaminoeinheiten reagieren leicht mit Ketonen und Aldehyden, um stabile Alkoxamine zu produzieren, z.B. wie von Webb, R. et al. in Bioconjugate Chem. (1990) 1, 96 beschrieben.aldehydes and ketones can can also be reacted with amines to ship bases form that advantageously over reductive amination can be stabilized. Alkoxylaminoeinheiten react easily with ketones and aldehydes to form stable alkoxamines to produce, e.g. as reported by Webb, R. et al. in Bioconjugate Chem. (1990) 1, 96.
Beispiele reaktiver Einheiten, die der Reaktion mit Carboxylgruppen fähig sind, umfassen Diazoverbindungen, wie Diazoacetatester und Diazoacetamide, die mit hoher Spezifität reagieren, um Estergruppen zu erzeugen, z.B. wie von Herriot R.M. in Adv. Protein Chem. (1947) 3, 169 beschrieben. Carbonsäure modifizierende Reagenzien, wie Carbodiimide, die über O-Acylharnstoffbildung, gefolgt von Amidbindungsbildung reagieren, können auch nützlich verwendet werden; das Verbinden kann vereinfacht werden durch die Zugabe eines Amins oder kann zu einer direkten Vektor-Rezeptorkopplung führen. Nützliche wasserlösliche Carbodiimide umfassen 1-Cyclohexyl-3-(2-morpholinyl-4-ethyl)carbodiimid (CMC) und 1-Ethyl-3-(3-dimethylaminopropyl)carbodiimid (EDC), z.B. wie von Zot, H.G. und Puett, D. in J. Biol. Chem. (1989) 264, 15552 beschrieben. Andere nützliche Carbonsäure modifizierende Reagenzien umfassen Isoxazoliumderivate, wie Woodwards-Reagenz K; Chloroformiate, wie p-Nitrophenylchloroformiat, Carbonyldiimidazole, wie 1,1'-Carbonyldiimidazol; und N-Carbalkoxydihydrochinoline, wie N-(Ethoxycarbonyl)-2-ethoxy-1,2-dihydrochinolin.Examples reactive moieties capable of reaction with carboxyl groups, include diazo compounds such as diazoacetate esters and diazoacetamides, those with high specificity react to produce ester groups, e.g. as described by Herriot R.M. in Adv. Protein Chem. (1947) 3, 169. Carboxylic acid modifying Reagents, such as carbodiimides, which undergo O-acyl urea formation, followed by amide bond formation can also be usefully used; the Joining can be simplified by adding an amine or can lead to a direct vector receptor coupling. Useful water-soluble carbodiimides include 1-cyclohexyl-3- (2-morpholinyl-4-ethyl) carbodiimide (CMC) and 1-ethyl-3- (3-dimethylaminopropyl) carbodiimide (EDC), e.g. as by Zot, H.G. and Puett, D. in J. Biol. Chem. (1989) 264, 15552 described. Other useful carboxylic acid Modifying reagents include isoxazolium derivatives, such as Woodward's reagent K; Chloroformates, such as p-nitrophenyl chloroformate, carbonyldiimidazoles, such as 1,1'-carbonyldiimidazole; and N-carbalkoxydihydroquinolines such as N- (ethoxycarbonyl) -2-ethoxy-1,2-dihydroquinoline.
Andere möglicherweise nützliche reaktive Einheiten umfassen vicinale Dione, wie p-Phenylendiglyoxal, die verwendet werden können, um mit Guanidinylgruppen zu reagieren, z.B. wie von Wagner et al. in Nucleic acid Res. (1978) 5, 4065 beschrieben; und Diazoniumsalze, die elektrophilen Substitutionsreaktionen unterzogen werden können, z.B. wie von Ishizaka, K. und Ishizaka, T. in J. Immunol. (1960) 85, 163 beschrieben. Bis-Diazoniumverbindungen können leicht durch Behandlung von Aryldiaminen mit Natriumnitrit in sauren Lösungen hergestellt werden. Es wird anerkannt werden, dass funktionelle Gruppen in dem Reporter und/oder Vektor, falls es erwünscht ist, zu anderen funktionellen Gruppen vor der Reaktion umgewandelt werden können, z.B. um eine zusätzliche Reaktivität oder Selektivität zu verleihen. Beispiele von Verfahren, die für diesen Zweck nützlich sind, umfassen die Umwandlung von Aminen zu Carbonsäuren unter Verwendung von Reagenzien, wie Dicarbonsäureanhydride; die Umwandlung von Aminen zu Thiolen unter Verwendung von Reagenzien, wie N-Acetylhomocysteinthiolacton, S-Acetylmercaptobernsteinsäureanhydrid, 2-Iminothiolan oder Thiol enthaltende Succinimidylderivate; die Umwandlung von Thiolen zu Carbonsäuren unter Verwenden von Reagenzien, wie α-Haloacetate; die Umwandlung von Thiolen zu Aminen unter Verwenden von Reagenzien, wie Ethylenimin oder 2-Bromethylamin; die Umwandlung von Carbonsäuren zu Aminen unter Verwenden von Reagenzien, wie Carbodiimide, gefolgt von Diaminen; und die Umwandlung von Alkoholen zu Thiolen unter Verwenden von Reagenzien, wie Tosylchlorid, gefolgt von Umesterung mit Thioacetat und Hydrolyse zum Thiol mit Natriumacetat.Other possibly useful reactive moieties include vicinal diones such as p-phenylene diglyoxal, which can be used to react with guanidinyl groups, e.g. as described by Wagner et al. in Nucleic Acid Res. (1978) 5, 4065; and diazonium salts, which can be subjected to electrophilic substitution reactions, e.g. as reported by Ishizaka, K. and Ishizaka, T. in J. Immunol. (1960) 85, 163 described. Bis-diazonium compounds can easily be treated of aryl diamines with sodium nitrite in acidic solutions. It will be recognized that functional groups in the reporter and / or vector, if desired is converted to other functional groups before the reaction can be e.g. for an additional Reactivity or selectivity to rent. Examples of methods that are useful for this purpose include the conversion of amines to carboxylic acids using reagents, such as dicarboxylic anhydrides; the conversion of amines to thiols using reagents, such as N-acetyl homocysteine thiolactone, S-acetylmercaptosuccinic anhydride, 2-iminothiolane or thiol-containing succinimidyl derivatives; the Conversion of thiols to carboxylic acids using reagents, such as α-haloacetates; the conversion of thiols to amines using reagents such as Ethyleneimine or 2-bromoethylamine; the conversion of carboxylic acids too Amines are followed using reagents such as carbodiimides of diamines; and converting alcohols to thiols using of reagents such as tosyl chloride, followed by transesterification with thioacetate and hydrolysis to the thiol with sodium acetate.
Die Vektor-Reporter-Kopplung kann auch bewirkt werden unter Verwenden von Enzymen wie Zero-Length-Vernetzungsmitteln; daher, wurden, z.B. Transglutaminase, Peroxidase und Xanthinoxidase verwendet, um vernetzte Produkte zu erzeugen. Reverse Proteolyse kann auch verwendet zum Vernetzen über Amidbindungsbildung.The Vector reporter coupling can also be effected using enzymes such as zero-length crosslinkers; therefore, e.g. Transglutaminase, peroxidase and xanthine oxidase are used to make crosslinked products to create. Reverse proteolysis can also be used to crosslink via amide bond formation.
Nicht-kovalente Vektor-Reporter-Kopplung kann zum Beispiel durch elektrostatische Ladungswechselwirkungen bewirkt werden, über Chelatbildung in der Form stabiler Metallkomplexe oder über Hochaffinitätsbindungswechselwirkung.Non-covalent Vector reporter coupling can be done, for example, by electrostatic Charge interactions are effected via chelation in the mold stable metal complexes or over High affinity binding interaction.
Ein Vektor, der an einen Peptid-, Lipo-Oligosaccharid- oder Lipopeptid-Linker gekoppelt ist, der ein Element enthält, das fähig ist, eine Membraneinlagerung zu vermitteln, kann auch nützlich sein. Ein Beispiel wird von Leenhouts, J.M. et al. in Febs Letters (1995) 370(3), 189-192 beschrieben.One Vector attached to a peptide, lipo-oligosaccharide or lipopeptide linker which contains an element capable of incorporating a membrane can also be useful be. An example is given by Leenhouts, J.M. et al. in Feb's Letters (1995) 370 (3), 189-192.
Die Kopplung kann auch bewirkt werden, unter Verwenden von Avidin oder Streptavidin, die vier Hochaffinitätsbindungsstellen für Biotin besitzen. Avidin kann deshalb verwendet werden, um einen Vektor mit einem Reporter zu konjugieren, falls sowohl der Vektor, als auch der Reporter biotinyliert sind. Beispiele werden von Bayer, E.A. und Wilchek, M. in Methods Biochem. Anal. (1980) 26, 1 beschrieben. Dieses Verfahren kann auch erweitert werden, um das Verbinden des Reporters mit einem Reporter einzuschließen, ein Prozess, der die Assoziierung des Mittels und eine folgende möglicherweise erhöhte Wirksamkeit fördert. Alternativ kann Avidin oder Streptavidin direkt an die Oberfläche von Reporterteilchen gebunden werden.The coupling can also be effected using avidin or streptavidin, which have four high affinity binding sites for biotin. Avidin can therefore be used to conjugate a vector to a reporter if both the vector and the reporter are biotinylated. Examples will be by Bayer, EA and Wilchek, M. in Methods Biochem. Anal. (1980) 26, 1. This method can also be extended to include linking the reporter to a reporter, a process that promotes association of the agent and consequent increased potency. Alternatively, avidin or streptavidin can be bound directly to the surface of reporter particles.
Nicht-kovalente Kopplung kann auch die bifunktionelle Natur von bispezifischen Immunoglobulinen nutzen. Diese Moleküle können spezifisch zwei Antigene binden, und sie so zu verbinden. Zum Beispiel können entweder bispezifische IgG- oder chemisch erzeugte bispezifische F(ab)'2-Fragmente als Verbindungsmittel verwendet werden. Es wurde auch von heterobifunktionellen, bispezifischen Antikörpern zum Verbinden zweier verschiedener Antigene berichtet, z.B. wie beschrieben von Bode, C. et al. in J. Bio. Chem. (1989) 264, 944 und von Staerz, U.D. et al. in Proc. Natl. Acad. Sci. USA (1986) 83, 1453. Auf ähnliche Weise kann ein beliebiger Reporter und/oder Vektor, der zwei oder mehr antigene Determinanten besitzt (z.B. wie von Chen, Aa et al. in Am. J. Pathol. (1988) 130, 216 beschrieben), durch Antikörpermoleküle vernetzt werden und zur Bildung von vernetzten Ansammlungen von Mitteln der Formel I einer möglicherweise erhöhten Wirksamkeit führen.Noncovalent coupling may also exploit the bifunctional nature of bispecific immunoglobulins. These molecules can specifically bind two antigens and bind them together. For example, either bispecific IgG or chemically generated bispecific F (ab) ' 2 fragments may be used as the linking agent. Heterobifunctional bispecific antibodies have also been reported for joining two different antigens, eg as described by Bode, C. et al. in J. Bio. Chem. (1989) 264, 944 and by Staerz, UD et al. in proc. Natl. Acad. Sci. USA (1986) 83, 1453. Similarly, any reporter and / or vector possessing two or more antigenic determinants (eg as described by Chen, Aa et al., Am. J. Pathol. (1988) 130, 216 be crosslinked by antibody molecules and lead to the formation of crosslinked accumulations of agents of the formula I of a possibly increased efficacy.
Sogenannte Zero-Length-Verbindungsmittel, die eine direkte kovalente Verbindung zweier reaktiver chemischer Gruppen ohne die Einführung von zusätzlichem verbindendem Material induzieren (z.B. wie in der Amidbindungsbildung, die unter Verwenden von Carbodiimiden oder enzymatisch induziert wird), können, falls erwünscht, in Übereinstimmung mit der Erfindung verwendet werden, wie auch viele Mittel, wie Biotin/Avidin-Systeme, die eine nicht-kovalente Reporter-Vektorverbindung induzieren und Mittel, die elektrostatische Wechselwirkungen induzieren.So-called Zero-length bonding agent, which is a direct covalent bond two reactive chemical groups without the introduction of additional induce binding (e.g., as in amide bond formation, which induced using carbodiimides or enzymatically will), if desired, in accordance used with the invention, as well as many agents, such as biotin / avidin systems, which induce a non-covalent reporter vector compound and agents, induce electrostatic interactions.
Im allgemeinsten Falle wird das Verbindungsmittel jedoch zwei oder mehr reaktive Einheiten aufweisen, z.B. wie oben beschrieben, verbunden durch ein Spacerelement. Die Anwesenheit eines derartigen Spacers erlaubt bifunktionellen Linkern, mit spezifischen funktionellen Gruppen innerhalb eines Moleküls oder zwischen zwei verschiedenen Molekülen zu reagieren, was zu einer Bindung zwischen diesen zwei Komponenten und Einführen von extrinsischem, vom Linker erhaltenem Material in das Reporter-Vektor-Konjugat führt. Die reaktiven Einheiten in einem Verbindungsmittel können dieselben (homobifunktionelle Mittel) oder verschiedene (heterobifunktionelle Mittel oder, wo mehrere unähnliche reaktive Einheiten vorhanden sind, heteromultifunktionelle Mittel) sein, was zu einer Vielfalt möglicher Reagenzien führt, die eine kovalente Bindung zwischen beliebigen chemischen Spezien entweder intramolekular oder intermolekuar herbeiführen können.in the However, in the most general case, the connecting means becomes two or more have more reactive units, e.g. as described above through a spacer element. The presence of such a spacer allows bifunctional linkers, with specific functional Groups within a molecule or to react between two different molecules, resulting in one Binding between these two components and inserting extrinsic linker-derived material into the reporter-vector conjugate. The reactive moieties in a linking agent may be the same (homobifunctional Means) or various (heterobifunctional agents or where several dissimilar reactive units are present, heteromultifunctional agents) be, leading to a variety of possible Leads reagents, the one covalent bond between any chemical species either intramolecular or intermolecular can cause.
Die Natur extrinsischen Materials, das durch das Verbindungsmittel eingeführt wird, kann von kritischem Belang für die Targetingfähigkeit und allgemeine Stabilität des Endproduktes sein. Daher kann es erwünscht sein, labile Verbindungen einzuführen, z.B. die Spacerarme enthalten, welche bioabbaubar oder chemisch empfindlich sind, oder die enzymatische Spaltungsstellen eingebaut haben. Alternativ kann der Spacer polymere Komponenten umfassen, z.B. um als oberflächenaktive Mittel zu wirken und die Stabilität des Mittels zu verbessern. Der Spacer kann auch reaktive Einheiten enthalten, z.B. wie oben beschrieben, um die Oberflächenvernetzung zu verbessern.The Nature of extrinsic material introduced by the bonding agent, may be of critical concern to the targeting ability and general stability be the final product. Therefore, it may be desirable to have labile compounds introduce, e.g. contain the spacer arms, which biodegradable or chemical sensitive, or the enzymatic cleavage sites incorporated to have. Alternatively, the spacer may comprise polymeric components, e.g. as a surface-active To act agents and to improve the stability of the agent. The spacer may also contain reactive moieties, e.g. as above described the surface crosslinking to improve.
Spacerelemente können tpyischerweise aus aliphatischen Ketten bestehen, die die reaktiven Einheiten des Linkers über Distanzen zwischen 5 und 30 Å trennen. Sie können auch makromolekulare Strukturen, wie Poly(ethylen)glykole enthalten. Derartige polymere Strukturen, die im Folgenden als PEGs bezeichnet werden, sind einfache, neutrale Polyether, denen in biotechnischen und biomedizinischen Anwendungen große Aufmerksamkeit zuteil wurde (siehe z.B. Milton Harris, J. (Hrsg.) "Poly(ethylene glycol) chemistry, biotechnical and biomedical applications", Plenum Press, New York, 1992). PEGs sind in den meisten Lösemitteln einschließlich Wasser löslich und werden in wässrigen Umgebungen stark hydratisiert, wobei zwei oder drei Wassermoleküle an jedes Ethylenglykolsegment gebunden werden; dies hat die Wirkung des Verhinderns einer Adsorption entweder von anderen Polymeren oder von Proteinen an die PEG-modifizierten Oberflächen. PEGs sind dafür bekannt, dass sie nichttoxisch sind und aktive Proteine oder Zellen nicht schädigen, während kovalent gebundene PEGs dafür bekannt sind, dass sie nicht immunogen und nicht antigen sind. Außerdem können PEGs leicht modifiziert und an andere Moleküle mit nur einer geringen Wirkung auf ihre Chemie gebunden werden. Ihre vorteilhafte Löslichkeit und biologischen Eigenschaften sind von den vielen möglichen Verwendungen von PEGs und den zugehörigen Copolymeren, einschließlich Blockcopolymeren, wie PEG-Polyurethane und PEG-Polypropylene offenbar.spacer elements can typically consist of aliphatic chains containing the reactive Units of the linker over Separate distances between 5 and 30 Å. You can also contain macromolecular structures, such as poly (ethylene) glycols. Such polymeric structures, hereinafter referred to as PEGs, are simple, neutral polyethers used in biotechnical and biomedical Applications great Attention has been paid (see, e.g., Milton Harris, J. (ed.)) "Poly (ethylene glycol)" chemistry, biotechnical and biomedical applications ", Plenum Press, New York, 1992). PEGs are in most solvents including water soluble and are in watery Environments strongly hydrated, with two or three water molecules attached to each Be bound ethylene glycol segment; this has the effect of preventing it adsorption of either other polymers or proteins to the PEG-modified surfaces. PEGs are for it known to be non-toxic and active proteins or cells do not harm while covalent bound PEGs for it are known to be non-immunogenic and non-antigenic. In addition, PEGs slightly modified and to other molecules with little effect be tied to their chemistry. Your beneficial solubility and biological properties are among the many possible uses of PEGs and the associated ones Copolymers, including Block copolymers, such as PEG polyurethanes and PEG polypropylenes apparently.
Geeignete Molekulargewichte für PEG-Spacer, die in Übereinstimmung mit der Erfindung verwendet werden, können beispielsweise zwischen 120 Daltons und 20 kDaltons liegen.suitable Molecular weights for PEG spacers in agreement can be used with the invention, for example, between 120 Daltons and 20 kDaltons lie.
Der Hauptmechanismus für die Aufnahme von Teilchen durch die Zellen des Retikuloendothelialen Systems (RES) ist die Opsonisierung durch Plasmaproteine im Blut; diese markieren Fremdteilchen, welche dann von dem RES aufgenommen werden. Die biologischen Eigenschaften von PEG-Spacerelementen, die in Übereinstimmung mit der Erfindung verwendet werden, können dazu dienen, die Zirkulationszeit des Mittels auf eine ähnliche Weise zu erhöhen, wie jene, die für PEGylierte Liposomen beobachtet wurde (siehe z.B. Klibanov, A.L. et al. in FEBS Letters (1990) 268, 235-237 und Blume, G. und Cevc, G. in Biochim. Biophys. Acta (1990) 1029, 91-97). Eine vergrößerte Kopplungseffizienz an Gebiete von Interesse kann auch unter Verwenden von Antikörpern erreicht werden, die an die Termini von PEG-Spacern gebunden sind (siehe z.B. Maruyama, K. et al. in Biochim. Biophys. Acta (1995) 1234, 74-80 und Hansen, C.B. et al. in Biochim. Biophys. Acta (1995) 1239, 133-144).Of the Main mechanism for the uptake of particles by the cells of the reticuloendothelial system (RES) is the opsonization by plasma proteins in the blood; these mark foreign particles, which are then taken up by the RES. The biological properties of PEG spacer elements in agreement can be used with the invention can serve the circulation time of the agent on a similar one Way to increase like those for PEGylated liposomes was observed (see, e.g., Klibanov, A.L. et al. in FEBS Letters (1990) 268, 235-237 and Blume, G. and Cevc, G. in Biochim. Biophys. Acta (1990) 1029, 91-97). An increased coupling efficiency Areas of interest can also be achieved using antibodies which are attached to the termini of PEG spacers (see e.g. Maruyama, K. et al. in Biochim. Biophys. Acta (1995) 1234, 74-80 and Hansen, C.B. et al. in Biochim. Biophys. Acta (1995) 1239, 133-144).
Andere repräsentative Spacerelemente umfassen Polysaccharide des Strukturtyps, wie Polygalacturonsäure, Glykosaminoglycane, Heparinoide, Cellulose und marine Polysaccharide, wie Alginate, Chitosane und Carrageeenans; Polysaccharide des Speichertyps, wie Stärke, Glykogen, Dextran und Aminodextrane, Polyaminosäuren und Methyl- und Ethylester davon, wie in Homo- und Copolymeren von Lysin, Glutaminsäure und Asparaginsäure; und Polypeptide, Oligosaccharide und Oligonukleotide, die Enzymspaltungsstellen enthalten können oder nicht.Other representative Spacer elements include structure-type polysaccharides such as polygalacturonic acid, glycosaminoglycans, Heparinoids, cellulose and marine polysaccharides, such as alginates, Chitosans and carrageenans; Memory type polysaccharides, such as Strength, Glycogen, dextran and aminodextrans, polyamino acids and methyl and ethyl esters of which, as in homo- and copolymers of lysine, glutamic acid and aspartic acid; and polypeptides, oligosaccharides and oligonucleotides, the enzyme cleavage sites can contain or not.
Im
Allgemeinen können
Spacerelemente spaltbare Gruppen enthalten wie vicinale Glykol-,
Azo-, Sulfon-, Ester-, Thioester- oder Disulfidgruppen. Spacer,
die bioabbaubare Methylendiester oder Diamidgruppen der Formel
Poly[N-(2-Hydroxyethyl)methacrylamide] sind möglicherweise nützliche Spacermaterialien dank ihres niedrigen Grads an Wechselwirkung mit Zellen und Geweben (siehe z.B. Volfová, I., Rihová, B. und V.R., und Vetvicka, P. in J. Bioact. Comp. Polymers (1992) 7, 175-190). Eine Arbeit über ein ähnliches Polymer, das hauptsächlich aus dem nahe verwandten 2-Hydroxypropylderivat bestand, zeigte, dass es durch das mononukleare Phagocytensystem nur in einem ziemlich geringen Ausmaß durch Endocytose aufgenommen wurde (siehe Goddard, P., Willamson, I., Bron, J., Hutchkinson, L.E., Nicholls, J. und Petrak, K. in J. Bioct. Compat. Polym. (1991) 6, 4-24).Poly [N- (2-hydroxyethyl) methacrylamides] may be useful Spacer materials thanks to their low degree of interaction with Cells and tissues (see, e.g., Volfová, I., Rihová, B. and V. R., and Vetvicka, P. in J. Bioact. Comp. Polymers (1992) 7, 175-190). A work about a similar Polymer, mainly from the closely related 2-hydroxypropyl derivative, that it is only in a fairly wide range due to the mononuclear phagocytic system small extent Endocytosis was recorded (see Goddard, P., Willamson, I., Bron, J., Hutchkinson, L.E., Nicholls, J. and Petrak, K. in J. Bioct. Compat. Polym. (1991) 6, 4-24).
Andere möglicherweise nützliche Polymerspacermaterialien umfassen:
- i) Copolymere von Methylmethacrylat mit Methacrylsäure; diese können erodierbar sein (siehe Lee, P.I. in Pharm. Res. (1993) 10, 980) und die Carboxylatsubstituenten können einen höheren Grad an Ausdehnung als mit neutralen Polymeren verursachen;
- ii) Blockcopolymere von Polymethacrylaten mit bioabbaubaren Polyestern (siehe z.B. San Roman, J. und Guillen-Garcia, P. in Biomaterials (1991) 12, 236-241);
- iii) Cyanoacrylate, d.h. Polymere von Estern von 2-Cyanoacrylsäure – diese sind bioabbaubar und wurden in der Form von Nanoteilchen für selektive Arzneimittelverabreichung verwendet (siehe Forestier, F., Gerrier, P., Chaumard, C., Quero, A.M., Couvreur, P. und Labarre, C. in J. Antimicrob. Chemoter. (1992) 30, 173-179);
- iv) Polyvinylalkohole, die wasserlöslich sind und allgemein als biokompatibel angesehen werden (siehe z.B. Langer, R. in J. Control. Release (1991) 16, 53-60);
- v) Copolymere von Vinylmethylether mit Maleinsäureanhydrid, von denen festgestellt wurde, dass sie bioerodierbar sind (siehe Finne, U., Hannus, M. und Urtti, A., in Int. J. Pharm. (1992) 78, 237-241);
- vi) Polyvinylpyrrolidone, z.B. mit einem Molekulargewicht, das geringer als ungefähr 25.000 ist, die schnell durch die Nieren gefiltert werden (siehe Hespe, W., Meier, A. M. und Blankwater, Y.M. in Arzheim.-Forsch./Drug Res. (1977) 27, 1158-1162);
- vii) Polymere und Copolymere von kurzkettigen aliphatischen Hydroxysäuren, wie Glykol-, Milch-, Butter-, Valerian- und Capronsäuren (siehe z.B. Carli, F. in Chim. Ind. (Milan) (1993) 75, 494-9), einschließlich Copolymere, die aromatische Hydroxysäuren einbauen, um ihre Abbaugeschwindigkeit zu erhöhen (siehe Imasaki, K., Yoshida, M., Fukuzaki, H., Asano, M., Kumakura, M., Mashimo, T., Yamanaka, H. und Nagai. T. in Int. J Pharm. (1992) 81, 31-38);
- viii) Polyester, die aus alternierenden Einheiten von Ethylenglykol und Terephthalsäure bestehen, z.B. DacronR, die nicht abbaubar sind, aber hoch biokompatibel;
- ix) Blockcopolymere, die bioabbaubare Segmente von aliphatischen Hydroxysäurepolymeren umfassen (siehe Younes, H., Nataf, P.R., Cohn, D., Appelbaum, Y.J., Pizov, G. und Uretzky, G. in Biomater. Artif Cells Artif. Organs (1988) 16, 705-719), beispielsweise in Zusammenhang mit Polyurethanen (siehe Kobayashi, H., Hyon, S.H. und Ikada, Y. in "Watercurable and biodegradable prepolymers" – J. Biomed. Mater. Res. (1991) 25, 1481-1494);
- x) Polyurethane, die als gut toleriert in Implantaten bekannt sind und die kombiniert werden können mit flexiblen "weichen" Segmenten, z.B. die Poly(tetramethylenglykol), Poly(propylenglykol) oder Poly(ethylenglykol) umfassen, und aromatischen "harten" Segmenten, z.B. die 4,4'-Methylenbis(phenylenisocyanat) umfassen (siehe z.B. Ratner, B.D., Johnston, A.B. und Lenk, T.J. in J. Biomed. Mater. Res: Applied Biomaterials (1987) 21, 59-90; Sa Da Costa, V. et al. in J. Coll. Interface Sci. (1981) 80, 445-452 und Affrossman, S. et al. in Clinical Materials (1991) 8, 25-31);
- xi) Poly(1,4-dioxan-2-one), die als bioabbaubare Ester angesichts ihrer hydrolysierbaren Esterverbindungen betrachtet werden können (siehe z.B. Song, C. X., Cui, X.M., und Schindler, A. in Med. Biol. Eng. Comput. (1993) 31, S147-150), und Glycolideinheiten umfassen können, um ihre Absorptionsfähigheit zu verbessern (siehe Bezwada, R.S., Shalaby, S.W. und Newman, H.D.J. in Agricultural and synthetic polymers: Biodegradability and utilization (1990) (Hrsg. Glass, J.E. und Swift, G.), 167-174 – ACS Symposium Series, #433, Washington D.C., U.S.A. – American Chemical Society);
- xii) Polyanhydride, wie Copolymere von Sebacinsäure (Octandisäure) mit bis(4-Carboxyphenoxy)propan, für die in Studien mit Kaninchen (siehe Brem, H., Kader, A., Epstein, J.I., Tamargo, R.J., Domb, A. Langer, R. und Leong, K.W. in Sel. Cancer Ther. (1989) 5, 55-65) und Studien mit Ratten (siehe Tamargo, R.J., Epstein, J.I. Reinhard, C.S., Chasin, M. und Brem, H. in J. Biomed. Mater. Res. (1989) 23, 253-266) gezeigt wurde, dass sie für die kontrollierte Freisetzung von Arzneimitteln im Gehirn ohne evidente toxische Wirkungen nützlich sind; xiii) bioabbaubare Polymere, die Orthoestergruppen enthalten, welche für die kontrollierte Freisetzung in vivo eingesetzt wurden (siehe Maa, Y.F. und Heller, J. in J. Control Release (1990) 14, 21-28); und
- xiv) Polyphosphazene, welche anorganische Polymere sind, die aus alternierenden Phosphor- und Stickstoffatomen bestehen (siehe Crommen, J.H., Vandorpe, J. und Schacht, E.H. in J. Control. Release (1993) 24, 167-180).
- i) copolymers of methyl methacrylate with methacrylic acid; these may be erodible (see Lee, PI in Pharm. Res. (1993) 10, 980) and the carboxylate substituents may cause a higher degree of expansion than with neutral polymers;
- ii) block copolymers of polymethacrylates with biodegradable polyesters (see, eg, San Roman, J. and Guillen-Garcia, P. in Biomaterials (1991) 12, 236-241);
- iii) cyanoacrylates, ie polymers of esters of 2-cyanoacrylic acid - these are biodegradable and have been used in the form of nanoparticles for selective drug administration (see Forestier, F., Gerrier, P., Chaumard, C., Quero, AM, Couvreur, P. and Labarre, C. in J. Antimicrob. Chemoter. (1992) 30, 173-179);
- iv) polyvinyl alcohols which are water-soluble and generally considered to be biocompatible (see eg Langer, R. in J. Control, Release (1991) 16, 53-60);
- v) Copolymers of vinyl methyl ether with maleic anhydride found to be bioerodible (see Finne, U., Hannus, M., and Urtti, A., Int. J. Pharm. (1992) 78, 237-241) ;
- vi) polyvinylpyrrolidones, eg having a molecular weight less than about 25,000, which are rapidly filtered by the kidneys (see Hespe, W., Meier, AM and Blankwater, YM in Arzheim. - Research / Drug Res. (1977) 27, 1158-1162);
- vii) Polymers and copolymers of short chain aliphatic hydroxy acids such as glycolic, lactic, butyric, valeric and capric acids (see eg Carli, F. in Chim. Ind. (Milan) (1993) 75, 494-9), including Copolymers that incorporate aromatic hydroxy acids to increase their rate of degradation (see Imasaki, K., Yoshida, M., Fukuzaki, H., Asano, M., Kumakura, M., Mashimo, T., Yamanaka, H., and Nagai T. in Int J J Pharm. (1992) 81, 31-38);
- viii) polyesters consisting of alternating units of ethylene glycol and terephthalic acid, eg Da cron R , which are not degradable, but highly biocompatible;
- ix) block copolymers comprising biodegradable segments of aliphatic hydroxy acid polymers (see Younes, H., Nataf, PR, Cohn, D., Appelbaum, YJ, Pizov, G. and Uretzky, G. in Biomater Artif Cells Artif ) 16, 705-719), for example in connection with polyurethanes (see Kobayashi, H., Hyon, SH and Ikada, Y. in "Watercurable and Biodegradable prepolymers" - J. Biomed. Mater. Res. (1991) 25, 1481 -1494);
- x) polyurethanes which are well tolerated in implants and which can be combined with flexible "soft" segments, eg poly (tetramethylene glycol), poly (propylene glycol) or poly (ethylene glycol), and aromatic "hard" segments, eg 4,4'-methylenebis (phenylene isocyanate) (see, for example, Ratner, BD, Johnston, AB and Lenk, TJ in J. Biomed., Mater Res: Applied Biomaterials (1987) 21, 59-90, Sa Da Costa, V in J. Coll., Interface Sci. (1981) 80, 445-452 and Affrossman, S. et al., Clinical Materials (1991) 8, 25-31);
- xi) poly (1,4-dioxan-2-ones) which may be considered biodegradable esters in view of their hydrolyzable ester compounds (see, eg, Song, CX, Cui, XM, and Schindler, A. in Med. Biol. Eng. Comput (1993) 31, S147-150), and may include glycolide units to improve their absorbency (see Bezwada, RS, Shalaby, SW and Newman, HDJ in Agricultural and Synthetic Polymers: Biodegradability and Utilization (1990) (Ed. Glass , JE and Swift, G.), 167-174 - ACS Symposium Series, # 433, Washington DC, USA - American Chemical Society);
- xii) Polyanhydrides, such as copolymers of sebacic acid (octanedioic acid) with bis (4-carboxyphenoxy) propane, for use in studies with rabbits (see Brem, H., Kader, A., Epstein, JI, Tamargo, RJ, Domb, A. Langer, R. and Leong, KW in Sel. Cancer Ther. (1989) 5, 55-65) and rat studies (see Tamargo, RJ, Epstein, JI Reinhard, CS, Chasin, M. and Brem, H. in J. Biomed. Mater. Res. (1989) 23, 253-266) has been shown to be useful for the controlled release of drugs in the brain without evident toxic effects; xiii) biodegradable polymers containing orthoester groups used for controlled release in vivo (see Maa, YF and Heller, J. in J. Control Release (1990) 14, 21-28); and
- xiv) polyphosphazenes which are inorganic polymers consisting of alternating phosphorus and nitrogen atoms (see Crommen, JH, Vandorpe, J. and Schacht, EH in J. Control, Release (1993) 24, 167-180).
Die
folgenden Tabellen listen Verbindungsmittel auf, die in targetingfähigen Mitteln
in Übereinstimmung
mit der Erfindung nützlich
sein können. Heterobifunktionelle Verbindungsmittel
Zusätzlich zu den bereits in Betracht gezogenen geradkettigen und verzweigten PEG-ähnlichen Linkern (z.B. Polyethylenglykole und andere, die 2 bis 100 sich wiederholende Einheiten von Ethylenoxid enthalten), können Linker im VLR-System unabhängig eine chemische Bindung oder der Rest einer verbindenden Gruppe sein. Der Ausdruck "Rest einer verbindenden Gruppe" wie hier verwendet, bezieht sich auf eine Einheit, die bleibt, resultiert oder erhalten wird aus der Reaktion einer vektorreaktiven Gruppe mit einer reaktiven Stelle auf einem Vektor. Der Ausdruck "vektorreaktive Gruppe" wie hier verwendet, bezieht sich auf eine beliebige Gruppe, die mit funktionellen Gruppen reagieren kann, die typischerweise auf Vektoren gefunden werden, deren Derivatisierung die Fähigkeit des Vektors, an seinen Rezeptor zu binden, nur minimal beeinflusst. Jedoch wird besonders in Betracht gezogen, dass derartige vektorreaktive Gruppen auch mit funktionellen Gruppen reagieren können, die typischerweise auf relevanten Proteinmolekülen gefunden werden. Daher werden in einem Aspekt die Linker, die in der Ausführung dieser Erfindung nützlich sind, von jenen Gruppen erhalten, die mit beliebigen relevanten Molekülen reagieren können, die einen Vektor wie oben beschrieben aufweisen, der eine reaktive Gruppe enthält, ob solch ein relevantes Molekül ein Protein ist oder nicht, um eine verbindende Gruppe zu bilden.In addition to the straight and branched PEG-like linkers already contemplated (eg, polyethylene glycols and others containing from 2 to 100 repeating units of ethylene oxide), linkers in the VLR system may independently be a chemical bond or the residue of a linking group. The term "linking group moiety" as used herein refers to a moiety that remains, results or is obtained from the reaction of a vector reactive group with a reactive site on a vector. The term "vector reactive group" as used herein refers to a belie a group which can react with functional groups typically found on vectors whose derivatization only minimally affects the ability of the vector to bind to its receptor. However, it is especially contemplated that such vector reactive groups can also react with functional groups typically found on relevant protein molecules. Thus, in one aspect, the linkers useful in the practice of this invention are obtained from those groups which can react with any relevant molecules having a vector as described above containing a reactive group, whether such a relevant molecule Protein is or not to form a linking group.
Bevorzugte
verbindende Gruppen werden von vektorreaktiven Gruppen erhalten,
die ausgewählt
sind aus, aber nicht beschränkt
sind auf:
eine Gruppe, die direkt mit Carboxy, Aldehyd, Amin
(NHR), Alkoholen, Sulfhydrylgruppen, aktivierten Methylenen und
dergleichen auf dem Vektor reagieren, zum Beispiel aktives Halogen
enthaltende Gruppen einschließlich
beispielsweise Chlormethylphenylgruppen und Chloracetyl-[ClCH2C(=O)-]-Gruppen, aktivierte 2-(Austrittsgruppen
substituierte)-Ethylsulfonyl- und Ethylcarbonylgruppen, wie 2-Chlorethylsulfonyl
und 2-Chlorethylcarbonyl; Vinylsulfonyl; Vinylcarbonyl; Epoxy; Isocyanato,
Isothiocyanato; Aldehyd; Aziridin; Succinimidoxycarbonyl; aktivierte
Acylgruppen, wie Carboxylsäurehalogenide;
gemischte Anyhdride und dergleichen.Preferred linking groups are obtained from vector reactive groups selected from, but not limited to:
a group that reacts directly with carboxy, aldehyde, amine (NHR), alcohols, sulfhydryl groups, activated methylenes, and the like on the vector, for example, active halogen-containing groups including, for example, chloromethylphenyl groups and chloroacetyl- [ClCH 2 C (= O) -] Groups activated 2- (leaving group substituted) ethylsulfonyl and ethylcarbonyl groups such as 2-chloroethylsulfonyl and 2-chloroethylcarbonyl; vinylsulfonyl; vinylcarbonyl; epoxy; Isocyanato, isothiocyanato; Aldehyde; aziridine; succinimidoxycarbonyl; activated acyl groups, such as carboxylic acid halides; mixed Anyhdride and the like.
Eine
Gruppe, die leicht mit modifizierten Vektormolekülen reagieren kann, die eine
vektorreaktive Gruppe enthalten, z.B. Vektoren, die eine reaktive
Gruppe enthalten, die modifiziert ist, um reaktive Gruppen wie jene
in den oben angegebenen Tabellen erwähnt zu enthalten, zum Beispiel
durch Oxidiation des Vektors zu einem Aldehyd oder einer Carbonsäure, wobei
in diesem Fall die "verbindende
Gruppe" von reaktiven
Gruppen erhalten werden kann, die ausgewählt sind aus Amino, Alkylamino,
Arylamino, Hydrazino, Alkylhadrazino, Arylhydrazino, Carbazido,
Semicarbazido, Thiocarbazido, Thiosemicarbazido, Sulfhydryl, Sulfhydrylalkyl, Sulfhydrylaryl,
Hydroxy, Carboxy, Carboxyalkyl und Carboxyaryl. Die Alkylteile der
genannten verbindenden Gruppen können
1 bis ungefähr
20 Kohlenstoffatome enthalten. Die Arylteile der genannten verbindenden
Gruppen können
ungefähr
6 bis ungefähr
20 Kohlenstoffatome enthalten; und eine Gruppe, die mit dem Vektor,
der eine reaktive Gruppe enthält,
oder mit dem wie oben angegebenen modifizierten Vektor durch Verwenden
eines Vernetzungsmittels verbunden werden kann. Die Reste bestimmter
nützlicher
Vernetzungsmittel, wie z.B. homobifunktionelle und heterobifunktionelle
Gelatinehärtungsmittel,
Bisepoxide und Bisisocyanate können
ein Teil einer verbindenden Gruppe während der Vernetzungsreaktion
werden. Andere nützliche
Vernetzungsmittel können
jedoch das Vernetzen vereinfachen, zum Beispiel wie konsumierbare
Katalysatoren, und sind nicht in dem Endkonjugat vorhanden. Beispiele
derartiger Vernetzungsmittel sind Carbodiimid- und Carbamoylonium-Vernetzungsmittel,
wie in
Bevorzugte
nützliche
Verbindungsgruppen werden von verschiedenen heterobifunktionellen
Vernetzungsreagenzien erhalten, wie jene, die in Pierce Chemical
Company Immunotechnology Catalog – Protein Modification Section
(1995 und 1996) aufgelistet sind. Nützliche nicht beschränkende Beispiele
derartiger Reagenzien umfassen:
Sulfo-SMCC Sulfosuccinimidyl-4-(N-maleimidomethyl)cyclohexan-1-carboxylat
Sulfo-SIAB
Sulfosuccinimidyl-(4-iodacetyl)aminobenzoat
Sulfo-SMPB Sulfosuccinimidyl-4-(p-maleimidophenyl)butyrat
2-IT
2-Iminothiolan
SATA N-Succinimidyl-S-acetylthioacetat.Preferred useful linking groups are obtained from various heterobifunctional crosslinking reagents, such as those listed in Pierce Chemical Company Immunotechnology Catalog - Protein Modification Section (1995 and 1996). Useful non-limiting examples of such reagents include:
Sulfo-SMCC sulfosuccinimidyl-4- (N-maleimidomethyl) cyclohexane-1-carboxylate
Sulfo-SIAB sulfosuccinimidyl (4-iodoacetyl) aminobenzoate
Sulfo-SMPB sulfosuccinimidyl-4- (p-maleimidophenyl) butyrate
2-IT 2-iminothiolane
SATA N-succinimidyl-S-acetylthioacetate.
Zusätzlich zu der vorstehenden Beschreibung können die verbindenden Gruppen ganz oder teilweise auch aus komplementären Sequenzen von Nukleotiden und Resten von Nukleotiden bestehen und davon erhalten werden, die beide natürlich auftreten und modifiziert sind, bevorzugt nicht selbst assoziierende Oligonukleotidsequenzen. Besonders nützliche, nicht beschränkende Reagenzien für den Einbau von modifizierten Nukleotideinheiten, die reaktive funktionelle Gruppen enthalten, wie Amin- und Sulfhydrylgruppen, in eine Oligonukleotidsequenz sind kommerziell erhältlich von beispielsweise Clontech Laborstories Inc. (Palo Alto California) und umfassen Uni-Link AminoModifier (Catalog # 5190), Biotin-ON Phosphoramidit (Catalog # 5191), N-MNT-C6-AminoModifier (Catalog # 5202), AminoModifier II (Catalog # 5203), DMT-C6-3'Amin-ON (Catalog # 5222), C6-ThiolModifier (Catalog # 5211) und dergleichen. In einem Aspekt werden die verbindenden Gruppen dieser Erfindung aus der Reaktion einer reaktiven funktionellen Gruppe, wie beispielsweise einer Amin- oder Sulfhydrylgruppe, wie sie in den oben genannten Clontech Reagenzien zur Verfügung stehen, erhalten, von denen eine oder mehrere in eine Oligonukleotidsequenz eingebaut wurden, mit beispielsweise einer oder mehrerer der zuvor beschriebenen vektorreaktiven Gruppen, wie eine heterobifunktionelle Gruppe auf dem Vektor.In addition to the above description, all or part of the linking groups may also consist of and be obtained from complementary sequences of nucleotides and residues of nucleotides, both naturally occurring and modified, preferably non-self-associating oligonucleotide sequences. Particularly useful, non-limiting reagents for the incorporation of modified nucleotide units containing reactive functional groups, such as amine and sulfhydryl groups, in an oligonucleotide sequence are commercially available from, for example, Clontech Laboratories Inc. (Palo Alto California) and include Uni-Link AminoModifier (Catalog # 5190), biotin-ON phosphoramidite (Catalog # 5191), N-MNT-C6 Amino Modifier (Catalog # 5202), AminoModifier II (Catalog # 5203), DMT-C6-3 Amine-ON (Catalog # 5222), C6 Thiol Modifier (Catalog # 5211), and the like. In one aspect, the linking groups of this invention are obtained from the reaction of a reactive functional group, such as an amine or sulfhydryl group, as available in the Clontech reagents listed above, one or more of which have been incorporated into an oligonucleotide sequence, with, for example, one or more of the vector reactive groups described above, such as a heterobifunctional group on the vector.
Durch Binden zweier komplementärer Oligonukleotidsequenzen, eine davon an den Vektor und die andere an den Reporter, weist das resultierende doppelsträngige hybridisierte Oligonukleotid dann die verbindende Gruppe zwischen dem Vektor und dem Reporter auf.By Binding two complementary Oligonucleotide sequences, one to the vector and the other to the reporter, assigns the resulting double-stranded hybridized Oligonucleotide then the linking group between the vector and the reporter.
Andere
Polymersysteme, die als Linker dienen, umfassen:
Poly(L- oder
D- oder DL-Aminosäuren)
= Proteine und Peptide; natürlich
auftretend oder synthetisch
Pseudo-Poly(aminosäuren) =
(Aminosäuren,
die durch Nichtamidbindungen verbunden sind);
Poly (L- oder
D- oder DL-Lactid) und die Copolymere, z.B. Poly (L-Lactid/DL-Lactid)
Poly(glycolid)
L-Lactid/Glycolidcopolymere
Poly-Caprolacton
und seine Copolymere
Polyanhydride
Poly(orthoester)
Polyphosphazene
Langkettige,
gerade oder verzweigte Lipide (& Phospholipide)
Zucker
und Kohlenhydrate
Oligonukleotide (siehe oben)
wie auch
Mischungen der oben genannten.Other polymer systems that serve as linkers include:
Poly (L or D or DL amino acids) = proteins and peptides; naturally occurring or synthetic
Pseudo-poly (amino acids) = (amino acids linked by non-amide bonds);
Poly (L- or D- or DL-lactide) and the copolymers, eg poly (L-lactide / DL-lactide)
Poly (glycolide)
L-lactide / glycolide copolymers
Poly-caprolactone and its copolymers
polyanhydrides
Poly (orthoester)
polyphosphazenes
Long-chain, straight or branched lipids (& phospholipids)
Sugar and carbohydrates
Oligonucleotides (see above)
as well as mixtures of the above.
Verbindungsmittel, die gemäß der Erfindung verwendet werden, werden im Allgemeinen ein Verbinden des Vektors mit dem Reporter oder des Reporters mit dem Reporter mit einigem Grad an Spezifität herbeiführen, und können auch verwendet werden, um ein oder mehrere therapeutisch wirksame Mittel zu binden.Connecting means those according to the invention are used, generally connecting the vector with the reporter or the reporter with the reporter with some Degree of specificity bring, and can also be used to one or more therapeutically effective Means to bind.
Die vorliegende Erfindung stellt demgemäß ein Werkzeug zur therapeutischen Arzneimittelverabreichung in Kombination mit vektorvermitteltem Leiten des Produktes an die erwünschte Stelle bereit. Mit "therapeutisch" oder "Arzneimittel" ist ein Mittel gemeint, das eine günstige Wirkung auf eine spezielle Krankheit in einem lebenden Menschen oder nicht-menschlichen Tier besitzt.The The present invention accordingly provides a tool for therapeutic Drug administration in combination with vector-mediated Direct the product to the desired one Get ready. By "therapeutic" or "medicinal" is meant a means the cheap one Effect on a specific disease in a living human or non-human animal possesses.
Therapeutische Verbindungen können im Inneren eines molekularen Aggregats oder teilchenförmigen Linkers eingekapselt werden oder an die einkapselnden Wände eines vesikulären Linkers gebunden oder darin eingebaut werden. Daher kann die therapeutische Verbindung an einen Teil der Oberfläche gebunden werden, zum Beispiel durch kovalente oder ionische Bindungen, oder kann physikalisch in ein einkapselndes Material gemischt werden, insbesondere, falls das Arzneimittel eine Polarität oder Löslichkeit ähnlich zu dem Material besitzt, um es so davon abzuhalten, aus dem Produkt zu entweichen, bevor beabsichtigt ist, dass es im Körper wirkt. Die Freisetzung des Arzneimittels kann lediglich durch benetzenden Kontakt mit Blut auf die Verabreichung folgend oder als eine Folge anderer interner oder externer Einflüsse initiiert werden, z.B. Auflösungsprozesse, die durch Enzyme katalysiert werden, oder die Verwendung von magnetischem Heizen, wo der Reporter ein magnetisches Teilchen ist.therapeutic Connections can inside a molecular aggregate or particulate linker encapsulated or to the encapsulating walls of a vesicular linker bound or incorporated therein. Therefore, the therapeutic Be bound to a part of the surface, for example by covalent or ionic bonds, or may be physical be mixed in an encapsulating material, especially if the drug is a polarity or solubility similar to the material possesses, so as to keep it from the product to escape before it is intended to work in the body. The release of the drug can only by wetting Contact with blood following administration or as a result other internal or external influences, e.g. Resolution processes, which are catalyzed by enzymes, or the use of magnetic Heating, where the reporter is a magnetic particle.
Die therapeutische Substanz kann kovalent an die einkapselnde Membranoberfläche eines vesikulären Linkers gebunden werden unter Verwenden eines geeigneten Verbindungsmittels, z.B. wie hier beschrieben. Daher kann man beispielsweise anfänglich ein Phospholipidderivat herstellen, an das das Arzneimittel durch eine bioabbaubare Bindung oder Linker gebunden wird, und dann dieses Derivat in das Material, das zum Herstellen der Vesikelmembran verwendet wurde, einbauen, wie oben beschrieben.The Therapeutic substance may be covalently attached to the encapsulating membrane surface of a vesicular Linkers are bound using a suitable coupling agent, e.g. as described here. Therefore, you can, for example, initially Phospholipidderivat produce, to which the drug by a biodegradable bond or linker is bound, and then this Derivative in the material used to make the vesicle membrane was installed as described above.
Alternativ kann das Mittel anfänglich ohne das Therapeutikum hergestellt werden, das dann an teilchenförmige (z.B. vesikuläre) Mittel vor der Verwendung gekoppelt wird oder darauf aufgebracht wird. Daher könnte zum Beispiel ein Therapeutikum zu einer Suspension von Liposomen in wässrigem Medium gegeben werden und geschüttelt werden, um das Therapeutikum an die Liposomen zu binden oder daran haften zu lassen.alternative The agent may be initial without the therapeutic agent, which is then added to particulate (e.g. vesicular) Agent is coupled before use or applied to it becomes. Therefore could for example, a therapeutic to a suspension of liposomes in watery Be given medium and shaken to bind the therapeutic to the liposomes or to it to be held liable.
Das Therapeutikum kann beispielsweise ein Arzneimittel oder ein Prodrug sein, das für die Verwendung zur Bekämpfung von Angiogenese oder Tumoren bekannt ist.The therapeutic agent may be, for example, a drug or a prodrug suitable for use known to combat angiogenesis or tumors.
Durch Targeting (Zielausrichten) eines Mittels, das ein Prodrug aktivierendes Enzym enthält, in Gebiete der Pathologie kann man das Targeting des Enzyms abbilden, was es möglich macht zu visualisieren, wenn das Mittel genau ins Ziel gebracht wird und wenn das Mittel von Nichtzielgebieten verschwunden ist. Auf diese Weise kann man die optimale Zeit für die Injektion des Prodrugs in individuelle Patienten bestimmen.By Targeting of an agent that activates a prodrug Contains enzyme, in areas of pathology, one can map the targeting of the enzyme, what is possible makes visualize when the agent finishes the target and if the means of non-target areas disappeared. In this way you can get the optimal time for the injection of the prodrug in individual patients.
Eine andere Alternative ist es, ein Prodrug, ein Prodrug aktivierendes Enzym und einen Vektor in denselben teilchenförmigen Linkerreporter auf eine derartige Weise einzubauen, dass das Prodrug nur nach einem externen Stimulus aktiviert werden wird. Ein derartiger Stimulus kann beispielsweise die Lichtstimulierung eines chromophoren Reporters oder das magnetische Heizen eines superparamagnetischen Reporters sein, nachdem das gewünschte Targeting erreicht wurde.A Another alternative is to activate a prodrug, a prodrug Enzyme and a vector in the same particulate linker reporter on a incorporate such a way that the prodrug only after an external Stimulus will be activated. Such a stimulus can be, for example the light stimulation of a chromophore reporter or the magnetic Heating a superparamagnetic reporter after the desired targeting was achieved.
Sogenannte Prodrugs können auch in Mitteln gemäß der Erfindung verwendet werden. Daher können Arzneimittel derivatisiert werden, um ihre physikochemischen Eigenschaften zu ändern und das Mittel der Erfindung zu adaptieren; derartige derivatisierte Arzneimittel können als Prodrugs betrachtet werden und sind üblicherweise inaktiv, bis eine Spaltung der derivatisierenden Gruppe die aktive Form des Arzneimittels regeneriert.So-called Prodrugs can also in agents according to the invention be used. Therefore, drugs can be derivatized to change their physicochemical properties and to adapt the means of the invention; such derivatized Medicines can are considered to be prodrugs and are usually inactive until one Cleavage of the derivatizing group the active form of the drug regenerated.
Therapeutika können auf einfache Weise an Stellen von Angiogenese geliefert werden.therapeutics can be easily delivered to sites of angiogenesis.
Zum Beispiel wo der Reporter eine chelatierte Metallspezies ist (zum Beispiel ein paramagnetisches Metallion oder ein Metallradionuklid), kann der Linker eine Kette umfassen, die an eine Metall chelatierende Gruppe gebunden ist, eine polymere Kette mit einer Mehrzahl von Metall chelatierenden Gruppen, die seitlich am molekularen Rückgrat oder in das molekulare Rückgrat eingebaut sind, ein verzweigtes Polymer mit Metall chelatierenden Gruppen an Verzweigungstermini (z.B. ein dendrimerer Polychelatbildner), etc. Was für den Linker erforderlich ist, ist einfach, dass er die Vektor- und Reportereinheiten miteinander für eine angemessene Zeitdauer verbindet. Mit angemessener Zeitdauer ist eine Zeitdauer gemeint, die für das Kontrastmittel ausreichend ist, um seine erwünschten Wirkungen auszuüben, z.B. den Kontrast in vivo während einer diagnostischen Bilderzeugungsprozedur zu verbessern.To the Example where the reporter is a chelated metal species (for Example, a paramagnetic metal ion or a metal radionuclide), For example, the linker may comprise a chain attached to a metal chelating group is bound, a polymeric chain with a plurality of metal chelating groups attached laterally to the molecular backbone or into the molecular backbone are incorporated, a branched polymer with metal chelating Groups at branch termini (e.g., a dendrimeric polychelant), etc. What for The linker required is simply that he is the vector and Reporters units together for a reasonable amount of time. With reasonable time is meant a period of time sufficient for the contrast agent is to his desired To exert effects e.g. during in vivo contrast to improve a diagnostic imaging procedure.
Daher kann es unter bestimmten Umständen erwünscht sein, dass der Linker nach der Verabreichung biologisch abgebaut wird. Durch Auswählen eines geeigneten bioabbaubaren Linkers ist es möglich, die Biodistributions- und Bioeliminationsmuster für den Vektor und/oder Reporter zu modifizieren. Wo der Vektor und/oder der Reporter biologisch aktiv sind oder fähig sind, unerwünschte Wirkungen auszuüben, falls er zurückbehalten wird nachdem die Bilderzeugungsprozedur vorüber ist, kann es erwünscht sein, eine Linker-Bioabbaubarkeit einzuplanen, die eine geeignete Bioelimination oder eine metabolische Zersetzung der Vektor- und/oder Reportereinheiten sichert. Daher kann ein Linker eine bioabbaubare Funktion enthalten, die beim Zersetzen Zersetzungsprodukte mit modifizierten Biodistributionsmustern ergibt, die aus der Freisetzung des Reporters von dem Vektor oder aus der Fragmentierung einer makromolekularen Struktur resultieren. Beispielsweise ist es für Linker, die chelatierte Metallionenreporter tragen, möglich, dass der Linker eine bioabbaubare Funktion eingebaut hat, die beim Zersetzen eine ausscheidbare Chelatverbindung freisetzt, die den Reporter enthält.Therefore It can be under certain circumstances he wishes be that the linker biodegraded after administration becomes. By selecting a suitable biodegradable linker, it is possible to reconcile the biodistribution and bioelimination patterns for to modify the vector and / or reporter. Where the vector and / or the reporters are biologically active or capable of causing adverse effects exercise, if he withheld after the imaging process is over, it may be desirable to a linker biodegradability plan to have a suitable bioelimination or a metabolic Decomposition of the vector and / or reporter units ensures. Therefore For example, a linker may contain a biodegradable function when decomposing Gives decomposition products with modified biodistribution patterns, from the release of the reporter from the vector or from the Fragmentation of a macromolecular structure result. For example is it for Linkers carrying chelated metal ion reporters, possible that the linker has incorporated a biodegradable function that decomposes releases a precipitable chelate compound, which is the reporter contains.
Demgemäß können bioabbaubare Funktionen, falls erwünscht, innerhalb der Linkerstruktur eingebaut sein, bevorzugt an Stellen, die (a) Verzweigungsstellen, (b) an oder nahe von Bindungsstellen für Vektoren oder Reporter, oder (c) derart sind, dass der biologische Abbau physiologisch tolerierbare oder schnell ausscheidbare Fragmente ergibt.Accordingly, biodegradable Functions, if desired, be incorporated within the linker structure, preferably at sites the (a) branching sites, (b) at or near binding sites for vectors or Reporters, or (c) are such that biodegradation is physiological tolerable or rapidly excreted fragments.
Beispiele von geeigneten bioabbaubaren Funktionen umfassen Ester-, Amid-, Doppelester-, Phosphoester-, Ether-, Thioether-, Guanidyl-, Acetal- und Ketalfunktionen.Examples suitable biodegradable functions include ester, amide, Double ester, phosphoester, ether, thioether, guanidyl, acetal and ketal functions.
Wie oben diskutiert kann die Linkergruppe, falls erwünscht, in ihrem molekularen Rückgrat Gruppen eingebaut haben, die die Biodistribution des Kontrastmittels beeinflussen oder die eine geeignete räumliche Konformation für das Kontrastmittel sicherstellen, z.B. um Wasser Zugang zu chelatierten paramagnetischen Metallionenreportern zu ermöglichen. Beispielsweise kann das Linkerrückgrat teilweise oder im Wesentlichen ganz aus einer oder mehreren Polyalkylenoxidketten bestehen.As discussed above, the linker group, if desired, in its molecular backbone Groups have incorporated the biodistribution of the contrast agent affect or provide a suitable spatial conformation for the contrast agent ensure, e.g. water access to chelated paramagnetic metal ion reporters to enable. For example, the linker backbone partially or substantially all of one or more polyalkylene oxide chains consist.
Daher kann der Linker als ein Verbund aus optional bioabbaubaren Vektorbindungs(Vb)- und Reporterbindungs-(Rb)-Gruppen, verbunden über Linkerrückgrat-(Lb)-Gruppen, angesehen werden, wobei die Linkergrückgrat-Gruppen Linkerseitenketten-(Lsc)-Gruppen tragen können, um die Biodistribution etc. zu modifizieren, und können selbst bioabbaubare Funktionen einbauen. Die Rb- und Vb-Bindungsgruppen können seitlich am Linkerrückgrat oder können an Linkerrückgrattermini sein, zum Beispiel mit einer Rb- oder Vb-Gruppe an einem Lb-Terminus, wobei Rb- oder Vb-Gruppen zwei Lb-Termini verbinden oder ein Lb-Terminus zwei oder mehrere Rb- oder Vb-Gruppen trägt. Die Lb- und LSC-Gruppen werden günstigerweise oligomere oder polymere Strukturen sein (z.B. Polyester, Polyamide, Polyether, Polyamine, Oligopeptide, Polypeptide, Oligo- und Polysaccharide, Oligonukleotide, etc.), bevorzugt Strukturen, die mindestens teilweise eine hydrophile oder lipophile Natur besitzen, z.B. hydrophile, amphiphile oder lipophile Strukturen.Thus, the linker can be viewed as a composite of optionally biodegradable vector binding (V b ) and reporter binding (R b ) groups linked via linker backbone (L b ) groups, where the lin Kerf-backbone groups may carry linker side chain (L sc ) groups to modify biodistribution, etc., and may incorporate biodegradable functions themselves. The R b and V b bonding groups may be on the side of the linker backbone or may be on link backbone minima, for example with an R b or V b group on a L b terminus, where R b or V b groups are two L b Connect termini or a L b termini bears two or more R b or V b groups. The L b and L SC groups will desirably be oligomeric or polymeric structures (eg, polyesters, polyamides, polyethers, polyamines, oligopeptides, polypeptides, oligo- and polysaccharides, oligonucleotides, etc.), preferably structures which are at least partially hydrophilic or polymeric possess lipophilic nature, such as hydrophilic, amphiphilic or lipophilic structures.
Der Linker kann ein niedriges, mittleres oder hohes Molekulargewicht besitzen, z.B. bis zu 2 MD. Im Allgemeinen werden Linker eines höheren Molekulargewichts bevorzugt werden, falls sie mit einer Vielzahl von Vektoren oder Reportern beladen werden sollen oder falls es nötig ist, den Vektor und den Reporter räumlich zu trennen, oder falls der Linker selbst dazu dient, eine Rolle bei der Modifikation der Biodistribution anzubieten. Im Allgemeinen werden jedoch Linker ein Molekulargewicht von 100 bis 100.000 D, insbesondere 120 D bis 20 kD besitzen.Of the Linker may have a low, medium or high molecular weight own, e.g. up to 2 MD. Generally, linkers are of higher molecular weight if preferred with a variety of vectors or Reporters should be loaded or, if necessary, the vector and the Spatially separating reporters, or if the linker itself serves a role in the modification to offer the biodistribution. In general, however, linkers a molecular weight of 100 to 100,000 D, in particular 120 D to 20 kD own.
Die Konjugation des Linkers mit dem Vektor und des Linkers mit dem Reporter kann durch eine beliebige geeignete chemische Konjugationstechnik ausgeführt werden, z.B. kovalentes Binden (z.B. Ester- oder Amidbildung), Metall-Chelatierung oder eine andere Metall-koordinative oder ionische Bindung, wieder wie oben beschrieben.The Conjugation of the linker with the vector and the linker with the reporter may be by any suitable chemical conjugation technique accomplished be, e.g. covalent bonding (e.g., ester or amide formation), metal chelation or another metal-coordinative or ionic bond, again as described above.
Beispiele
von geeigneten Linkersystemen umfassen die Magnifier-Polychelatbildnerstrukturen
von
Wo
der Reporter ein chelatiertes Metallion ist, wird die Linkergruppe
im Allgemeinen die Chelatbildnereinheit einbauen. Alternativ kann
das chelatierte Metall auf oder in einem teilchenförmigen Reporter
getragen werden. Es können
in jedem Fall konventionelle Metall chelatierende Gruppen, wie sie
in den Gebieten der Radiopharmazeutika und MRI-Kontrastmedien bekannt
sind, verwendet werden, z.B. lineare, cyclische und verzweigte Polyamino-Polycarbonsäuren und
Phosphorsauerstoffsäuren-Äquivalente,
und andere Schwefel- und/oder Stickstoffliganden, die in der Technik
bekannt sind, z.B. DTPA, DTPA-BMA, EDTA, DO3A, TMT (siehe beispielsweise
Reporterreporter
Die Reportereinheiten in den Kontrastmitteln der Erfindung können eine beliebige Einheit sein, die der Definition entweder direkt oder indirekt in einer in vivo diagnostischen Bilderzeugungsprozedur zugänglich sind, z.B. Einheiten, die eine detektierbare Strahlung emittieren oder veranlasst werden können, diese zu emittieren (z.B. durch radioaktiven Zerfall, Fluoreszenzanregung, Spinresonanzanregung, etc.), Einheiten, die lokale elektromagnetische Felder beeinflussen (z.B. paramagnetische, superparamagnetische, ferrimagnetische oder ferromagnetische Spezien), Einheiten, die Strahlungsenergie absorbieren oder streuen (z.B. Chromophore und Fluorophore), Teilchen (einschließlich Flüssigkeit enthaltende Vesikel), schwere Elemente und Verbindungen davon und Einheiten, die eine detektierbare Substanz erzeugen, etc.The Reporter units in the contrast agents of the invention may have a be any unit that is the definition either direct or indirectly in an in vivo diagnostic imaging procedure are accessible, e.g. Units that emit detectable radiation or can be arranged to emit them (e.g., by radioactive decay, fluorescence excitation, Spin resonance excitation, etc.), units that are local electromagnetic Fields (e.g., paramagnetic, superparamagnetic, ferrimagnetic or ferromagnetic species), units which Absorb or scatter radiant energy (e.g., chromophores and Fluorophores), particles (including fluid-containing vesicles), heavy elements and compounds thereof and units having a generate detectable substance, etc.
Ein sehr weiter Bereich von Materialien, die durch diagnostische Bilderzeugungsmodalitäten detektierbar sind, ist aus der Technik bekannt, und der Reporter wird gemäß der zu verwendenden Bilderzeugungsmodalität ausgewählt werden. Daher wird zum Beispiel für Ultraschallbilderzeugung ein echogenes Material oder ein Material, das fähig ist ein echogenes Material zu erzeugen, normalerweise ausgewählt werden, für Röntgenstrahlungsbilderzeugung wird der Reporter im Allgemeinen ein schweres Atom sein oder es enthalten (z.B. eines Atomgewichts von 38 oder mehr), für MR-Bilderzeugung wird der Reporter entweder ein Nicht-Null-Kernspinisotop sein (wie beispielsweise 19F) oder ein Material, das ungepaarte Elektronenspins und daher paramagnetische, superparamagnetische, ferrimagnetische oder ferromagnetische Eigenschaften besitzt, für eine Lichtbilderzeugung wird der Reporter ein Lichtstreuer sein (z.B. ein gefärbtes oder nicht gefärbtes Teilchen), ein Lichtabsorber oder ein Lichtemitter, für magnetometrische Bilderzeugung wird der Reporter detektierbare magnetische Eigenschaften besitzen, für Electrical Impedance Imaging wird der Reporter die elektrische Impedanz beeinflussen und für die Szintigraphie, SPECT, PET, etc. wird der Reporter ein Radionuklid sein.A very wide range of materials detectable by diagnostic imaging modalities is known in the art, and the reporter will be selected according to the imaging modality to be used. Thus, for example, for ultrasound imaging, an echogenic material or a material capable of producing an echogenic material will normally be selected; for X-ray imaging, the reporter will generally be or contain a heavy atom (eg for MR imaging, the reporter will either be a non-zero nuclear spin isotope (such as 19 F) or a material that has unpaired electron spins and therefore paramagnetic, superparamagnetic, ferrimagnetic or ferromagnetic properties for a For light imaging, the reporter will be a light scatterer (eg, a colored or uncolored particle), a light absorber or a light emitter, for magnetometric imaging the reporter will have detectable magnetic properties, for electrical impedance imaging the reporter will affect the electrical impedance and for scintigraphy, SPECT, PET, etc. the reporter will be a radionuclide.
Beispiele
von geeigneten Reportern sind aus der Literatur der diagnostischen
Bilderzeugung weit bekannt, z.B. magnetische Eisenoxidteilchen,
Röntgenstrahlungskontrastmittel
enthaltende Vesikel, chelatierte paramagnetische Metalle (z.B. Gd,
Dy, Mn, Fe, etc.). Siehe beispielsweise
Als Reporter besonders bevorzugt sind: chelatierte paramagnetische Metallionen, wie Gd, Dy, Fe und Mn, insbesondere, wenn sie durch makrocyclische chelatbildende Gruppen chelatiert sind (z.B. Tetraazacyclododecan-Chelatbildner, wie DOTA, DO3A, HP-DO3A und Analoga davon) oder durch chelatbildende Linkergruppen wie DTPA, DTPA-BMA, EDTA, DPDP, etc; Metallradionuklide, wie 90Y, 99mTc, 111In, 47Sc, 67/Ga, 51Cr, 177mSn, 67Cu, 167Tm, 97Ru, 188Re, 177Lu, 199Au 203Pb und 141Ce; superparamagnetische Eisenoxidkristalle; Chromophore und Fluorophore mit Absorptions- und/oder Emissionsmaxima im Bereich von 300 bis 1400 nm, insbesondere 600 nm bis 1200 nm, insbesondere 650 bis 1000 nm; chelatierte Schwermetallclusterionen (z.B. W- oder Mo-Polyoxoanionen oder die Schwefel- oder gemischten Sauerstoff/Schwefelanaloga); kovalent gebundene Nichtmetallatome, die entweder eine hohe Atomnummer besitzen (z.B. Iod) oder radioaktiv sind, z.B. 123I, 131I, etc., -atome; iodierte Verbindung enthaltende Vesikel; etc.Particularly preferred reporters are: chelated paramagnetic metal ions such as Gd, Dy, Fe and Mn, especially when chelated by macrocyclic chelating groups (eg tetraazacyclododecane chelating agents such as DOTA, DO3A, HP-DO3A and analogs thereof) or by chelating Linker groups such as DTPA, DTPA-BMA, EDTA, DPDP, etc .; Metal radionuclides such as 90 Y, 99m Tc, 111 In, 47 Sc, 67 / Ga, 51 Cr, 177m Sn, 67 Cu, 167 Tm, 97 Ru, 188 Re, 177 Lu, 199 Au 203 Pb, and 141 Ce; superparamagnetic iron oxide crystals; Chromophores and fluorophores with absorption and / or emission maxima in the range from 300 to 1400 nm, in particular 600 nm to 1200 nm, in particular 650 to 1000 nm; chelated heavy metal cluster ions (eg, W or Mo polyoxoanions or the sulfur or mixed oxygen / sulfur analogs); covalently bonded non-metal atoms which either have a high atomic number (eg iodine) or are radioactive, eg 123 I, 131 I, etc., atoms; iodinated compound-containing vesicles; Etc.
Allgemein gesagt kann der Reporter (1) ein chelatierbares Metall oder ein polyatomares Metall enthaltendes Ion sein (z.B. TcO, etc.), wobei das Metall ein Metall einer hohen Atomnummer ist (z.B. einer Atomnummer größer als 37), eine paramagnetische Spezies (z.B. ein Übergangsmetall oder Lanthanid), oder ein radioaktives Isotop, (2) eine kovalent gebundene nicht-metallische Spezies, die eine ungepaarte Elektronenstelle besitzt (z.B. ein Sauerstoff oder Kohlenstoff in einem stabilen freien Radikal), ein Nicht-Metall einer hohen Atomnummer oder ein Radioisotop, (3) ein polyatomarer Cluster oder Kristall, der Atome hoher Atomnummer enthält, und der ein kooperatives magnetisches Verhalten zeigt (z.B. Suparamagnetismus, Ferrimagnetismus oder Ferromagnetismus) oder Radionuklide enthält, (4) ein Chromophor (wobei mit diesem Ausdruck Spezien eingeschlossen sind, die fluoreszierend oder phosphoreszierend sind), z.B. eine anorganische oder organische Struktur, insbesondere ein komplexiertes Metallion oder eine organische Gruppe mit einem ausgedehnten delokalisierten Elektronensystem, oder (5) eine Struktur oder eine Gruppe mit variierenden Eigenschaften der elektrischen Impedanz, z.B. aufgrund eines ausgedehnten delokalisierten Elektronensystems.Generally said reporter (1) can be a chelatable metal or a polyatomic metal-containing ion (e.g., TcO, etc.), wherein the metal is a high atomic number metal (e.g., an atomic number greater than 37), a paramagnetic species (e.g., a transition metal or lanthanide), or a radioactive isotope, (2) a covalently bonded non-metallic Species having an unpaired electron site (e.g., a Oxygen or carbon in a stable free radical) Non-metal of a high atomic number or a radioisotope, (3) a polyatomic cluster or crystal containing atoms of high atomic number, and showing cooperative magnetic behavior (e.g., supra-magnetism, Ferrimagnetism or ferromagnetism) or radionuclides, (4) a chromophore (including species with this term are fluorescent or phosphorescent), e.g. a inorganic or organic structure, in particular a complexed Metal ion or an organic group with an extended delocalized Electron system, or (5) a structure or a group with varying Properties of electrical impedance, e.g. due to an extended delocalized electron system.
Beispiele
besonderer bevorzugter Reportergruppen werden unten detaillierter
beschrieben:
Chelatierte Metallreporter: Metallradionuklide,
paramagnetische Metallionen, fluoreszierende Metallionen, Schwermetallionen
und ClusterionenExamples of particular preferred reporter groups are described in more detail below:
Chelated metal reporters: metal radionuclides, paramagnetic metal ions, fluorescent metal ions, heavy metal ions and cluster ions
Bevorzugte Metallradionuklide umfassen 90Y, 99mTc, 111In, 47Sc, 67Ga, 51Cr, 177mSn, 67Cu, 167Tm, 97Ru, 188Re, 177Lu, 199Au, 203Pb und 141Ce.Preferred metal radionuclides include 90 Y, 99m Tc, 111 In, 47 Sc, 67 Ga, 51 Cr, 177m Sn, 67 Cu, 167 Tm, 97 Ru, 188 Re, 177 Lu, 199 Au, 203 Pb and 141 Ce.
Bevorzugte paramagnetische Metallionen umfassen Ionen von Übergangs- und Lanthanidmetallen (z.B. Metallen mit Atomnummern von 6 bis 9, 21-29, 42, 43, 44 oder 57-71), insbesondere Ionen von Cr, V, Mn, Fe, Co, Ni, Cu, La, Ce, Pr, Nd, Pm, Sm, Eu, Gd, Tb, Dy, Ho, Er, Tm, Yb und Lu, insbesondere von Mn, Cr, Fe, Gd und Dy, mehr insbesondere Gd.preferred paramagnetic metal ions include ions of transition and lanthanide metals (e.g. Metals with atomic numbers of 6 to 9, 21-29, 42, 43, 44 or 57-71), in particular ions of Cr, V, Mn, Fe, Co, Ni, Cu, La, Ce, Pr, Nd, Pm, Sm, Eu, Gd, Tb, Dy, Ho, Er, Tm, Yb and Lu, in particular of Mn, Cr, Fe, Gd and Dy, more especially Gd.
Bevorzugte fluoreszierende Metallionen umfassen Lanthanide, insbesondere La, Ce, Pr, Nd, Pm, Sm, Eu, Gd, Tb, Dy, Ho, Er, Tm, Yb und Lu. Eu ist besonders bevorzugt.preferred fluorescent metal ions include lanthanides, especially La, Ce, Pr, Nd, Pm, Sm, Eu, Gd, Tb, Dy, Ho, Er, Tm, Yb and Lu. Eu is particularly preferred.
Bevorzugte
Schwermetall enthaltende Reporter können Atome von Mo, Bi, Si und
W enthalten, und insbesondere können
sie polyatomare Clusterionen sein (z.B. Bi-Verbindungen und W- und Mo-Oxide), wie
in
Die
Metallionen werden erwünschterweise
durch chelatbildende Gruppen an der Linkereinheit oder in oder auf
einem Teilchen chelatiert (z.B. ein Vesikel oder ein poröser oder
nichtporöser
anorganischer oder organischer Feststoff) insbesondere lineare,
makrocyclische, Terpyridin- und N2S2-Chelatbildner, wie beispielsweise DTPA,
DTPA-BMA, EDTA, DO3A, TMT. Weitere Beispiele von geeigneten chelatbildenden
Gruppen sind in
Die Linkereinheit oder das Teilchen können eine oder mehrere derartige chelatbildende Gruppen enthalten, falls erwünscht, metalliert durch eine oder mehrere Metallspezien (z.B. um Reporter zu ergeben, die in unterschiedlichen Bilderzeugungsmodalitäten detektierbar sind).The Linker unit or the particle may have one or more such Chelating groups contain, if desired, metalated by a or multiple metal species (e.g., to yield reporters present in different Imaging modalities are detectable).
Insbesondere wo das Metall nicht radioaktiv ist, ist es bevorzugt, dass ein polychelatbildender Linker oder ein teilchenförmiger Reporter verwendet werden.Especially where the metal is not radioactive, it is preferred that a polychelant Left or a particulate Reporters are used.
Eine chelatbildende oder chelatierende Gruppe wie hier erwähnt kann den Rest einer oder mehrerer einer breiten Vielzahl von chelatierenden Mitteln umfassen, die ein Metallion oder ein polyatomares Ion komplexieren können (z.B. TcO).A chelating or chelating group as mentioned herein the remainder of one or more of a wide variety of chelating Comprise agents that complex a metal ion or a polyatomic ion can (e.g., TcO).
Wie gut bekannt ist, ist ein chelatierendes Mittel eine Verbindung, die Donoratome enthält, die sich durch koordinative Bindung mit einem Metallion kombinieren können, um eine cyclische Struktur zu bilden, die ein Chelationkomplex oder ein Chelat genannt wird. Diese Klasse von Verbindungen ist in der Kirk-Othmer Encyclopedia of Chemical Technology, Band 5, 339-368 beschrieben.As well known, a chelating agent is a compound, contains the donor atoms, which combine by coordinative bonding with a metal ion can, to form a cyclic structure containing a chelation complex or a chelate is called. This class of compounds is in the Kirk-Othmer Encyclopedia of Chemical Technology, Vol. 5, 339-368 described.
Der Rest eines geeigneten chelatierenden Mittels kann ausgewählt werden aus Polyphosphaten, wie Natriumtripolyphosphat und Hexametaphosphorsäure; Aminocarbonsäuren, wie Ethylendiamintetraessigsäure, N-(2-Hydroxy)ethlendiamintriessigsäure, Nitrilotriessigsäure, N,N-Di(2-Hydroxyethyl)glycin, Ethylenbis(hydroxyphenylglycin) und Diethylentriaminpentaessigsäure; 1,3-Diketone, wie Acetylaceton, Trifluoracetylaceton und Thenoyltrifluoraceton; Hydroxycarbonsäuren, wie Weinsäure, Zitronensäure, Gluconsäure und 5-Sulfosalicylsäure; Polyamine, wie Ethylendiamin, Diethylentriamin, Triethylentetraamin und Triaminotriethylamin; Aminoalkohole, wie Triethanolamin und N-(2-Hydroxyethyl)ethylendiamin, aromatische heterocyclische Basen, wie 2,2'-Diimidazol, Picolinamin, Dipicolinamin und 1,10-Phenanthrolin; Phenole, wie Salicylaldehyd, Disulfopyrocatechol und Chromotropsäure; Aminophenole, wie 8-Hydroxychinolin und Oximsulfonsäure, Oxime, wie Dimethylglyoxim und Salicylaldoxim; Peptide, die eine proximale chelatierende Funktionalität enthalten, wie Polycystein, Polyhistidin, Polyasparaginsäure, Polyglutarsäure oder Kombinationen derartiger Aminosäuren; Schiff-Basen, wie Disalicylaldehyd-1,2-propylendiimin; Tetrapyrrole, wie Tetraphenylporphin und Phthalocyanin; Schwefelverbindungen, wie Toluoldithiol, meso-2,3-Dimercaptobernsteinsäure, Dimercaptopropanol, Thioglykolsäure, Kaliumethylxanthat, Natriumdiethyldithiocarbamat, Dithizon, Diethyldithiophosphorsäure und Thioharnstoff; synthetische makrocyclische Verbindungen, wie Dibenzo[18]-Krone-6, (CH3)6-[14]-4,11]-dien-N4 und (2.2.2-Cryptat), Phosphonsäuren, wie Nitrilotrimethylenphosphonsäure, Ethylendiamintetra(methylenphosphonsäure) und Hydroxyethylidendiphosphonsäure oder Kombinationen zweier oder mehrerer der oben genannten Mittel. Der Rest von geeigneten chelatierenden Mitteln umfasst bevorzugt eine Polycarbonsäuregruppe und bevorzugte Beispiele umfassen: Ethylendiamin-N,N,N',N'-Tetraessigsäure (EDTA); N,N,N',N'',N''-Diethylentriaminpentaessigsäure (DTPA); 1,4,7,10-Tetraazacyclododecan-N,N',N'',N''-tetraessigsäure (DOTA); 1,4,7,10-Tetraazacyclodeodecan-N,N',N''-triessigsäure (DO3A); 1-Oxa-4,7,10-triazacyclododecan-N,N',N''-triessigsäure (OTTA); trans(1,2)-Cyclohexandiethylentriaminpentaessigsäure (CDTPA).The balance of a suitable chelating agent may be selected from polyphosphates such as sodium tripolyphosphate and hexametaphosphoric acid; Aminocarboxylic acids such as ethylenediaminetetraacetic acid, N- (2-hydroxy) ethylenediaminetriacetic acid, nitrilotriacetic acid, N, N-di (2-hydroxyethyl) glycine, ethylenebis (hydroxyphenylglycine) and diethylenetriaminepentaacetic acid; 1,3-diketones such as acetylacetone, trifluoroacetylacetone and thenoyltrifluoroacetone; Hydroxycarboxylic acids such as tartaric acid, citric acid, gluconic acid and 5-sulfosalicylic acid; Polyamines such as ethylenediamine, diethylenetriamine, triethylenetetraamine and triaminotriethylamine; Amino alcohols such as triethanolamine and N- (2-hydroxyethyl) ethylenediamine, aromatic heterocyclic bases such as 2,2'-diimidazole, picolinamine, dipicolinamine and 1,10-phenanthroline; Phenols such as salicylaldehyde, disulfopyrocatechol and chromotropic acid; Aminophenols such as 8-hydroxyquinoline and oximesulfonic acid, oximes such as dimethylglyoxime and salicylaldoxime; Peptides containing proximal chelating functionality, such as polycysteine, polyhistidine, polyaspartic acid, polyglutaric acid, or combinations of such amino acids; Schiff bases such as disalicylaldehyde-1,2-propylenediimine; Tetrapyrroles such as tetraphenylporphine and phthalocyanine; Sulfur compounds such as toluenedithiol, meso-2,3-dimercaptosuccinic acid, dimercaptopropanol, thioglycolic acid, potassium ethylxanthate, sodium diethyldithiocarbamate, dithizone, diethyldithiophosphoric acid and thiourea; synthetic macrocyclic compounds such as dibenzo [18] crown-6, (CH 3 ) 6 - [14] -4,11] -diene-N 4 and (2,2,2-cryptate), phosphonic acids such as nitrilotrimethylenephosphonic acid, ethylenediaminetetra (methylenephosphonic acid ) and hydroxyethylidenediphosphonic acid or combinations of two or more of the above mentioned agents. The remainder of suitable chelating agents preferably comprise a polycarboxylic acid group and preferred examples include: ethylenediamine-N, N, N ', N'-tetraacetic acid (EDTA); N, N, N ', N ", N" -diethylenetriamine pentaacetic acid (DTPA); 1,4,7,10-tetraazacyclododecane-N, N ', N ", N" -tetraacetic acid (DOTA); 1,4,7,10-tetraazacyclodeodecane-N, N ', N "-triacetic acid (DO3A); 1-oxa-4,7,10-triazacyclododecane-N, N ', N "-triacetic acid (OTTA); trans (1,2) -cyclohexanediethylenetriamine pentaacetic acid (CDTPA).
Andere
geeignete Reste von chelatierenden Mitteln umfassen Proteine, die
für die
Chelatierung von Metallen, wie Technetium und Rhenium modifiziert
sind, wie in
Geeignete
Reste von chelatierenden Mitteln können auch von N3S und N2S2
enthaltenden Verbindungen erhalten werden, wie beispielsweise jene,
die in
Andere
geeignete Reste von chelatierenden Mitteln sind in
Bevorzugte chelatierende Gruppen sind aus der Gruppe ausgewählt, die besteht aus 2-Aminomethylpyridin, Iminoessigsäure, Iminodiessigsäure, Ethylendiamintetraessigsäure (EDTA), Diethylentriaminpentaessigsäure (DTPA), 1,4,7,10-Tetraazacyclododecan-1,4,7,10-Tetraessigsäure (DOTA), Carbonyliminodiessigsäure, Methyleniminoessigsäure, Methyleniminodiessigsäure, Ethylenthioethyleniminoessigsäure, Ethylenthioethyleniminodiessigsäure, TMT, eine Terpyridinylgruppe, ein chelatierendes Mittel mit einer Terpyridylgruppe und einer Carboxymethylaminogruppe, oder ein Salz einer beliebigen der vorstehenden Säuren. Besonders bevorzugte chelatierende Gruppen sind DTPA, DTPA-BMA, DPDP, TMT, DOTA und HPDO3A.preferred chelating groups are selected from the group consisting of 2-aminomethylpyridine, imino acetic acid, iminodiacetic acid, ethylenediaminetetraacetic (EDTA), diethylenetriamine pentaacetic acid (DTPA), 1,4,7,10-tetraazacyclododecane-1,4,7,10-tetraacetic acid (DOTA), carbonyliminodiacetic acid, Methyleniminoessigsäure, methyleneiminodiacetic, Ethylenthioethyleniminoessigsäure, Ethylenthioethyleniminodiessigsäure, TMT, a terpyridinyl group, a chelating agent with a Terpyridyl group and a carboxymethylamino group, or a salt any of the foregoing acids. Especially preferred chelating groups are DTPA, DTPA-BMA, DPDP, TMT, DOTA and HPDO3A.
Repräsentative
chelatierende Gruppen sind auch beschrieben in
Verfahren zum Metallieren beliebiger vorliegender chelatierender Mittel liegen innerhalb des Niveaus des Fachwissens. Metalle können in eine chelatbildende Einheit durch ein beliebiges von drei allgemeinen Verfahren eingebaut werden: direkter Einbau, Templatsynthese und/oder Transmetallierung. Direkter Einbau ist bevorzugt.method for metalating any of the present chelating agents within the level of expertise. Metals can turn into a chelating Unit incorporated by any of three general methods are: direct incorporation, template synthesis and / or transmetalation. Direct installation is preferred.
Daher ist es erwünscht, dass das Metallion leicht an das chelatierende Mittel komplexiert wird, zum Beispiel durch lediglich Aussetzen oder Mischen einer wässrigen Lösung der das chelatierende Mittel enthaltenden Einheit mit einem Metallsalz in einer wässrigen Lösung, die bevorzugt einen pH im Bereich von ungefähr 4 bis ungefähr 11 besitzt. Das Salz kann ein beliebiges Salz sein, aber bevorzugt ist das Salz ein wasserlösliches Salz des Metalls, wie ein Halogensalz, und bevorzugter sind solche Salze so ausgewählt, dass sie nicht mit dem Binden des Metallions an das chelatierende Mittel interferieren. Die das chelatierende Mittel enthaltende Einheit befindet sich bevorzugt in einer wässrigen Lösung bei einem pH zwischen ungefähr 5 und ungefähr 9, bevorzugter einem pH zwischen ungefähr 6 bis ungefähr 8. Die das chelatierende Mittel enthaltende Einheit kann mit Puffersalzen, wie Citrat, Acetat, Phosphat und Borat gemischt werden, um den optimalen pH zu erzeugen. Bevorzugt sind die Puffersalze so ausgewählt, dass sie nicht mit dem nachfolgenden Binden des Metallions an das chelatierende Mittel interferieren.Therefore is it desirable that the metal ion readily complexes with the chelating agent is, for example, merely by suspending or mixing one aqueous solution the moiety containing the chelating agent with a metal salt in an aqueous Solution, which preferably has a pH in the range of about 4 to about 11. The salt may be any salt, but preferred is the salt a water-soluble Salt of the metal, such as a halide salt, and more preferred are those Salts so selected that they do not interfere with the binding of the metal ion to the chelating Intermediate means. The unit containing the chelating agent is preferably in an aqueous solution at a pH between approximately 5 and about 9, more preferably pH between about 6 to about 8. The the chelant-containing moiety can be reacted with buffer salts, As citrate, acetate, phosphate and borate are mixed to the optimum pH to create. Preferably, the buffer salts are selected so that do not interfere with the subsequent binding of the metal ion to the chelating one Intermediate means.
Bei der diagnostischen Bilderzeugung enthält das Vektor-Linker-Reporter-(VLR)-Konstrukt bevorzugt ein Verhältnis von Metallradionuklidion zu chelatierendem Mittel, das in derartigen diagnostischen Bilderzeugungsanwendungen wirksam ist. In bevorzugten Ausführungsformen reicht das Molverhältnis von Metallion pro chelatierendem Mittel von ungefähr 1:1000 bis ungefähr 1:1.at diagnostic imaging preferably includes the vector linker reporter (VLR) construct relationship from metal radionuclide ion to chelating agent used in such diagnostic imaging applications. In preferred embodiments the molar ratio is sufficient of metal ion per chelating agent of about 1: 1000 until about 1: 1.
In radiotherapeutischen Anwendungen enthält das VLR bevorzugt ein Verhältnis von Metallradionuklidion zu chelatierendem Mittel, das in derartigen therapeutischen Anwendungen wirksam ist. In bevorzugten Ausführungsformen reicht das Molverhältnis von Metallion pro chelatierendem Mittel von ungefähr 1:100 bis ungefähr 1:1. Das Radionuklid kann ausgewählt werden beispielsweise von Radioisotopen von Sc, Fe, Pb, Ga, Y, Bi, Mn, Cu, Cr, Zn, Ge, Mo, Ru, Sn, Sr, Sm, Lu, Sb, W, Re, Po, Ta und Tl. Bevorzugte Radionuklide umfassen 44Sc, 64Cu, 67Cu, 212Pb, 68Ga, 90Y, 153Sm, 212Bi, 186Re und 188Re. Von diesen ist 90Y besonders bevorzugt. Diese Radioisotope können atomar oder bevorzugt ionisch sein.In radiotherapeutic applications, the VLR preferably contains a ratio of metal radionuclide ion to chelating agent that is effective in such therapeutic applications. In preferred embodiments, the mole ratio of metal ion per chelating agent ranges from about 1: 100 to about 1: 1. The radionuclide can be selected, for example, from radioisotopes of Sc, Fe, Pb, Ga, Y, Bi, Mn, Cu, Cr, Zn, Ge, Mo, Ru, Sn, Sr, Sm, Lu, Sb, W, Re, Po , Ta and Tl. Preferred radionuclides include 44 Sc, 64 Cu, 67 Cu, 212 Pb, 68 Ga, 90 Y, 153 Sm, 212 Bi, 186 Re and 188 Re. Of these, 90 Y is particularly preferred. These radioisotopes may be atomic or preferably ionic.
Die folgenden Isotope oder Isotopenpaare können sowohl für die Bilderzeugung als auch für die Therapie verwendet werden, ohne dass die Radiomarkierungsmethode oder der Chelator gewechselt werden muss: 47Sc21; 141Ce58; 188Re75; 177Lu71; 199Au79; 47SC21; 131I53; 67CU29; 131I53 und 123I53; 188R75 und 99mTc43; 90Y39 und 87Y39; 47Sc21 und 44Sc21; 90Y39 und 123I53; 146Sm62 und 153Sm62; und 90Y39 und 111In49 Wo die Linkereinheit einen einzelnen Chelatbildner enthält, kann der Chelatbildner direkt an die Vektoreinheit gebunden werden, z.B. über eine der Metallkoordinationsgruppen des Chelatbildners, die eine Ester-, Amid-, Thioester- oder Thioamidbindung mit einer Amin-, Thiol- oder Hydroxygruppe auf dem Vektor bilden kann. Alternativ können der Vektor und der Chelatbildner direkt über eine Funktionalität an das Chelatbildnerrückgrat gebunden sein, z.B. eine CH2-Phenyl-NCS-Gruppe, gebunden an einen Ringkohlenstoff von DOTA, wie vorgeschlagen wie Meares et al. in JACS 110:6266-6267 (1988), oder indirekt über einen homo- oder heterobifunktionellen Linker, z.B. ein Bisamin, Bisepoxid, Diol, Diacid, difunktionalisiertes PEG, etc. In diesem Fall wird der bifunktionelle Linker günstigerweise eine Kette von 1 bis 200, bevorzugt 3 bis 30 Atomen zwischen dem Vektor und dem chelatbildenden Rest bereitstellen.The following isotopes or isotope pairs can be used for both imaging and therapy without having to change the radiolabeling method or chelator: 47 Sc 21 ; 141 Ce 58 ; 188 Re 75 ; 177 Lu 71 ; 199 Au 79 ; 47 SC 21 ; 131 I 53 ; 67 CU 29 ; 131 I 53 and 123 I 53 ; 188 R 75 and 99m Tc 43 ; 90 Y 39 and 87 Y 39 ; 47 sc 21 and 44 sc 21 ; 90 Y 39 and 123 I 53 ; 146 Sm 62 and 153 Sm 62 ; and 90 Y 39 and 111 In 49 Where the linker moiety contains a single chelating agent, the chelant may be attached directly to the vector moiety, eg via one of the metal coordination groups of the chelating agent having an ester, amide, thioester or thioamide bond with an amine moiety. , Thiol or hydroxy group on the vector. Alternatively, the vector and chelant may be directly attached to the chelant backbone via functionality, eg, a CH 2 -phenyl NCS group attached to a ring carbon of DOTA as suggested as Meares et al. in JACS 110: 6266-6267 (1988), or indirectly via a homo- or heterobifunctional linker, eg, a bisamine, bis-epoxide, diol, diacid, difunctionalized PEG, etc. In this case, the bifunctional linker desirably becomes a chain of 1 to 200 , preferably 3 to 30 atoms between the vector and the chelating moiety.
Wo
die Linkereinheit eine Mehrzahl von chelatbildenden Gruppen enthält, ist
oder enthält
der Linker bevorzugt Teile der Formeln wobei Ch eine chelatbildende
Einheit und Li eine Linkerrückgratkomponente
ist, d.h. der Linker besitzt bevorzugt seitliche Chelatbildner,
Chelatbildner im Rückgrat
oder terminale Chelatbildner oder eine Kombination davon. Die seitlichen
und im Rückgrat
befindlichen polymeren Strukturen können verzweigt sein oder sind
bevorzugter linear und die Wiederholungseinheiten (LiCh) oder andere
Wiederholungseinheiten im Polymer können im Rückgrat befindliche oder seitliche
biodistributionsmodifizierende Gruppen besitzen, z.B. Polyalkylengruppen,
wie in
Die
chelatbildenden Einheiten innerhalb des polychelatbildenden Linkers
können über Rückgratfunktionalisierung
des Chelatbildners oder durch Nutzen einer oder mehrerer der Metall
koordinierenden Gruppen des Chelatbildners oder durch eine Amid-
oder Etherbindungsbildung zwischen dem Säurechelatbildner und einem
ein Amin oder Hydroxyl tragenden Linkerrückgrat gebunden werden, z.B.
wie in Polylysin-polyDTPA, Polylysin-polyDOTA und in den sogenannten
Magnifierpolychelatbildnern von
Wo
die chelatierte Spezies von einem teilchenförmigen (oder Molekularaggregat-,
z.B. vesikulären) Linker
getragen wird, kann das Chelat zum Beispiel ein nichtgebundenes
Mono- oder Polychelat (wie Gd DTPA-BMA oder Gd HP-DO3A), eingeschlossen
innerhalb des Teilchens, sein oder es kann ein Mono- oder Polychelat
sein, das mit dem Teilchen entweder durch kovalente Bindung oder
durch Wechselwirkung einer Ankergruppe (z.B. einer lipophilen Gruppe)
auf dem Mono/Polychelat mit der Membran eines Vesikels konjugiert ist
(siehe z.B.
NichtmetallatomreporterNon-metal atomic reporter
Bevorzugte Nichtmetallatomreporter umfassen Radioisotope wie 123I und 131I, wie auch Nicht-Null-Kernspinatome wie 19F und schwere Atome wie I.Preferred non-metal atomic reporters include radioisotopes such as 123 I and 131 I as well as non-zero nuclear spin atoms such as 19 F and heavy atoms such as I.
Derartige Reporter, bevorzugt eine Mehrzahl davon, z.B. 2 bis 200, können kovalent an ein Linkerrückgrat gebunden werden, entweder unter direktem Verwenden konventioneller chemischer Synthesetechniken oder über eine Trägergruppe, z.B. eine Triiodphenylgruppe.such Reporter, preferably a plurality thereof, e.g. 2 to 200, can be covalent to a linker backbone be bound, either directly using conventional chemical synthesis techniques or via a support group, e.g. a triiodophenyl group.
In einer Ausführungsform dieser Erfindung wird die Verwendung von Radioisotopen von Iod besonders in Betracht gezogen. Zum Beispiel, falls der Vektor oder Linker aus Substituenten besteht, die durch Iod in einer Kovalentbindungsbildungsreaktion chemisch substituiert werden können, wie beispielsweise Substituenten, die eine Hydrophenylfunktionalität enthalten, können derartige Substituenten durch Verfahren, die in der Technik gut bekannt sind, mit einem Radioisotop von Iod markiert werden. Die Iodspezien können in therapeutischen und diagnostischen Bilderzeugungsanwendungen verwendet werden. Während zur gleichen Zeit ein Metall in einem chelatierenden Mittel auf demselben Vektor-Linker auch in entweder therapeutischen oder diagnostischen Bilderzeugungsanwendungen verwendet werden kann.In an embodiment This invention will be particularly useful in the use of radioisotopes of iodine Considered. For example, if the vector or linker off Substituents formed by iodine in a covalent bond forming reaction can be chemically substituted, such as substituents containing a hydrophenyl functionality, can such substituents by methods well-known in the art are known to be labeled with a radioisotope of iodine. The Iodine species can in therapeutic and diagnostic imaging applications be used. While at the same time a metal in a chelating agent the same vector linker also in either therapeutic or diagnostic Image forming applications can be used.
Wie
mit den oben diskutierten Metallchelatbildnern, können derartige
Metallatomreporter an den Linker gebunden sein oder in oder auf
einem teilchenförmigen
Linker getragen werden, z.B. in einem Vesikel (siehe
Linker des oben in Zusammenhang mit den Metallreportern beschriebenen Typs können für Nichtmetallatomreporter verwendet werden, wobei der Nichtmetallatomreporter oder Gruppen, die derartige Reporter tragen, die Stelle einer oder aller chelatbildenden Gruppen einnehmen.left of the type described above in connection with the metal reporters can for non-metal atom reporters using the non-metal atom reporter or groups, which carry such reporters, the site of one or all chelating Take groups.
Organische chromophore oder fluorophore ReporterOrganic chromophores or fluorophore reporter
Bevorzugte
organische chromopore und fluorophore Reporter umfassen Gruppen
mit einem ausgedehnten delokalisierten Elektronensystem, z.B. Cyanine,
Merocyanine, Phthalocyanine, Naphthalocyanine, Triphenylmethine,
Porphyrine, Pyryliumfarbstoffe, Thiapyryliumfarbstoffe, Squaryliumfarbstoffe,
Croconiumfarbsroffe, Azuleniumfarbstoffe, Indoaniline, Benzophenoxaziniumfarbstoffe,
Benzothiaphenothiaziniumfarbstoffe, Anthrachinone, Naphthochinone,
Indathrene, Phthaloylacridone, Trisphenochinone, Azofarbstoffe,
intramolekulare und intermolekulare Charge-Transfer-Farbstoffe und
-Farbstoffkomplexe, Tropone, Tetrazine, Bis(dithiolen)komplexe,
Bis(benzoldithiolat)komplexe, Iodanilinfarbstoffe, Bis(S,O-dithiolen)komplexe,
etc. Beispiele von geeigneten organischen oder metallierten organischen
Chromophoren können
gefunden werden in "Topics
in Applied Chemistry: Infrared absorbing dyes" Hrsg. M. Matsuoka, Plenum, NY 1990, "Topics in Applied
Chemistry: The Chemistry and Application of Dyes", Waring et al., Plenum, NY, 1990, "Handbook of Fluorescent
Probes and Research Chemicals" Haugland,
Molecular Probes Inc., 1996,
Besonders bevorzugt sind Gruppen, die Absorptionsmaxima zwischen 600 und 1000 nm besitzen, um Interferenz mit Hämoglobinabsorption zu vermeiden (z.B. Xylencyanole).Especially preferred are groups, the absorption maxima between 600 and 1000 nm to avoid interference with hemoglobin absorption (e.g., xylene cyanols).
Weitere derartige Beispiele umfassen: Cyaninfarbstoffe: wie Heptamethincyaninfarbstoffe, z.B. Verbindungen 4a bis 4g Tabelle II auf Seite 26 von Matsuoka (supra)
- 4a: wobei Y=S, X=I, R=Et
- 4b: wobei Y=S, X=ClO4, R=Et
- 4c: wobei Y=CMe2, X=1, R=Me
- 4d: wobei Y=CMe2, X=ClO4, R=Me
- 4e: wobei Y=CH=CH, X=I, R=Et
- 4f: wobei Y=CH=CH, X=Br, R=Et
- 4g: wobei Y=CH=CH, X=ClO4, R=Et
wobei Y=CMe2, X=I, R=Me
wobei Y=S, X=Br, R=Et
Chalcogenpyrylomethinfarbstoffe, z.B. Verbindungen 12 auf Seite 31 von Matsuoka (supra), d.h. wobei Y = Te, Se, O or NR;
Monochalcogenpyrylomethinfarbstoffe, z.B. Verbindungen 13 auf Seite 31 von Matsuoka (supra), d.h. wobei n = 1 oder 2;
Pyryliumfarbstoffe, z.B. Verbindungen 14 (X=O) auf Seite 32 von Matsuoka (supra), d.h. wobei X = O, S oder Se;
Thiapyryliumfarbstoffe, z.B. Verbindungen 15 auf Seite 32 und Verbindung I auf Seite 167 von Matsuoka (supra), d.h. wobei n = 1 oder 2;
Squaryliumfarbstoffe, z.B. Verbindung 10 und Tabelle IV auf Seite 30 von Matsuoka (supra), d.h. wobei X = CH=CH, Y = H und R = Et,
X=S, Y=H und R=Et und
X = CMe2, Y = H und R = Me,
und Verbindung 6, Seite 26 von Matsuoka (supra), d.h. wobei X = CH=CH, Y = H und R=Et;
Croconiumfarbstoffe, z.B. Verbindung 9 und Tabelle IV auf Seite 30 von Matsuoka (supra), d.h. wobei X = CH=CH, Y = H und R = Et,
X = S, Y = H und R = Et
X = CMe2, Y = H und R = Me
und Verbindung 7, Seite 26 von Matsuoka (supra), d.h. wobei X = CH=CH, Y = H und R = Et;
Azuleniumfarbstoffe, d.h. Verbindung 8 auf Seite 27 von Matsuoka (supra), d.h. Merocyaninfarbstoffe, z.B. Verbindung 16, R = Me, auf Seite 32 von Matsuoka (supra), d.h. Indoanilinfarbstoffe, wie Kupfer- und Nickelkomplexe von Indoanilinfarbstoffen, z.B. Verbindung 6 auf Seite 63 von Matsuoka (supra), d.h. wobei R = Et, R = Me, M = Cu,
R = Et, R' = Me, M = Ni
R = Me, R' = H, M = Cu oder
R = Me, R' = H, M = Ni,
Benzo[a]phenoxaziniumfarbstoffe und Benzo[a]phenothiaziniumfarbstoffe, z.B. wie auf Seite 201 von Matsuoka (supra) gezeigt, d.h. wobei X = O oder S;
1,4-Diaminoanthrachinon(N-alkyl)-3'-thioxo-2,3-dicarboximide, z.B. Verbindung 20 auf Seite 41 von Matsuoka (supra) Indanthrenpigmente, z.B. siehe Verbindung 21 auf Seite 41 von Matsuoka (supra);
2-Arylamino-3,4-phthaloylacridonfarbstoffe, z.B. Verbindung 22 auf Seite 41 von Matsuoka (supra) Trisphenochinonfarbstoffe, z.B. Verbindung 23 auf Seite 41 von Matsuoka (supra) Azofarbstoffe, z.B. der Monoazofarbstoff, Verbindung 2 auf Seite 90 von Matsuoka (supra), d.h. wobei X = CH=C(CN)2, R1 = R2 = Et, R3 = R4 = H,
X = C(CN)=C(CN)2, R1 = R2 = Et, R3 = R4 = H oder
X= und Y = C=O, R1 = R2 = Et, R3 = R4 = H,
oder Y = SO2, R1 = H, R2 = CH (Me) nBu, R3 = OMe und R4 = NHAc;
Azofarbstoffe, z.B. der Polyazofarbstoff, Verbindung 5 auf Seite 91 von Matsuoka (supra), d.h. Intramolekular-Charge-Transfer-Donor-Akzeptor-Infrarotfarbstoffe, z.B. Verbindungen 6 und 7 auf Seite 91 von Matsuoka (supra), d.h. und nichtbenzoide aromatische Farbstoffe, z.B. Verbindung 8, ein Tropon, auf Seite 92 von Matsuoka (supra), d.h. Tetrazinradikalfarbstoffe, z.B. Verbindung 9 auf Seite 92 von Matsuoka (supra), d.h. worin, X = p-Phenylen oder
X = p-Terphenylen, wie auch Verbindung 10 auf Seite 92 von Matsuoka (supra), d.h. worin X = p-Biphenyl;
kationische Salze von Tetrazinradikalfarbstoffen, z.B. Verbindung 11 auf Seite 92 von Matsuoka (supra) worin X = p-Phenylen;
Donor-Akzeptor-Intramolekular-Charge-Transfer-Farbstoffe, z.B. CT-Komplexe von Verbindungen 13b und 14a bis 14c auf Seite 93 von Matsuoka (supra), d.h. wobei X = CH=N-N(Ph)2 im Donor und
- a) Y = CN, Z = NO2
- b) Y = CN, Z = H oder
- c) Y = Cl, Z = NO2 in dem Akzeptor;
Naphthochinonfarbstoffe, z.B. Verbindungen 2, 3 und 4 auf Seite 37 von Matsuoka (supra), d.h. und metallierte Azofarbstoffe, wie Azofarbstoffe, die Nickel, Kobalt, Kupfer, Eisen und Mangan enthalten; Phthalocyaninfarbstoffe, z.B. Verbindung 1 in Tabelle II auf Seite 51 von Matsuoka (supra), z.B. Naphthalocyaninfarbstoffe, z.B. Verbindung 3 in Tabelle II auf Seite 51 von Matsuoka (supra), z.B. Metallphthalocyanine, wie Phthalocyanine, die Aluminium, Silicium, Nickel, Zink, Blei, Cadmium, Magnesium, Vanadium, Kobalt, Kupfer und Eisen enthalten, z.B. Verbindung 1 in Tabelle III auf Seite 52 von Matsuoka (supra), z.B. worin beispielsweise M = Mg;
Metallnaphthocyanine, wie Naphthalocyanine, die Aluminium, Zink, Kobalt, Magnesium, Cadmium, Silicium, Nickel, Vanadium, Blei, Kupfer und Eisen enthalten, siehe Verbindung 3 in Tabelle III auf Seite 52 von Matsuoka (supra), z.B. worin beispielsweise M = Mg;
Bis(dithiolen)metallkomplexe, die ein Metallion wie Nickel, Kobalt, Kupfer und Eisen koordiniert an vier Schwefelatome in einem Bis(S,S'-bidentat)ligandkomplex aufweisen, z.B. siehe Tabelle I auf Seite 59 von Matsuoka (supra) wobei
R1 = R2 = CF3, M = Ni
R1 = R2 = Phenyl, M = Pd,
R1 = R2 = Phenyl, M = Pt,
R1 = C4 bis C10 Alkyl, R2 = H, M = Ni,
R1 = C4 bis C10 Alkyl, R2 = H, M = Pd,
R1 = C4 bis C10 Alkyl, R2 = H, M = Pt,
R1 = R2 = Phenyl, M = Ni,
R1 = R2 = p-CH3-Phenyl, M = Ni,
R1 = R2 = p-CH3O-Phenyl, M = Ni,
R1 = R2 = p-Cl-Phenyl, M = Ni,
R1 = R2 = p-CF3-Phenyl, M = Ni,
R1 = R2 = 3,4-diCl-Phenyl, M = Ni,
R1 = R2 = o-Cl-Phenyl, M = Ni,
R1 = R2 = o-Br-Phenyl, M = Ni,
R1 = R2 = 3,4-diCl-Phenyl, M = Ni,
R1 = R2 = p-CH3, M = Ni,
R1 = R2 = 2-Thienyl, M = Ni,
R1 = p-(CH3)2 N-Phenyl, R2 = Phenyl, M = Ni, und
R1 = p-(CH3)2 N-Phenyl, R2 = p-H2N-Phenyl, M = Ni;
Bis(benzoldithiolat)metallkomplexe, die ein Metallion aufweisen, wie Nickel, Kobalt, Kupfer und Eisen, koordiniert an vier Schwefelatome in einem Ligandkomplex, z.B. siehe Tabelle III auf Seite 62 von Matsuoka (supra), d.h. wobei
X = Tetramethyl, M = Ni,
X = 4,5-Dimethyl, M = Ni,
X = 4-Methyl, M = Ni,
X = Tetrachlor, M = Ni,
X = H, M = Ni,
X = 4-Methyl, M = Co,
X = 4-Methyl, M = Cu, und
X = 4-Methyl, M = Fe;
N,O-Bidentatindoanilinfarbstoffe, die ein Metallion aufweisen, wie Nickel, Kobalt, Kupfer und Eisen koordiniert an zwei Stickstoff- und zwei Sauerstoffatome von zwei N,O-Bidentatindoanilinliganden, z.B. Verbindung 6 in Tabelle IV auf Seite 63 von Matsuoka (supra), z.B. wobei R = Et, R' = Me, M = Cu,
R = Et, R' = Me, M = Ni,
R = Me, R' = H, M = Cu, und
R = Me, R' = H, M = Ni,
bis(S,O-Dithiolen)metallkomplexe, die ein Metallion aufweisen, wie Nickel, Kobalt, Kupfer und Eisen koordiniert an zwei Schwefelatome und zwei Sauerstoffatome in einem Bis(S,O-bidentat)ligandkomplex, z.B. siehe
tris-(a-Diimin)komplexe, die ein Metallion aufweisen, das mit sechs Stickstoffatomen in einem Triligandkomplex koordiniert ist, z.B. siehe Tabelle II auf Seite 180 von Matsuoka (supra), letzte Verbindung (siehe auch
- 4a: where Y = S, X = I, R = Et
- 4b: where Y = S, X = ClO 4 , R = Et
- 4c: where Y = CMe 2 , X = 1, R = Me
- 4d: where Y = CMe 2 , X = ClO 4 , R = Me
- 4e: where Y = CH = CH, X = I, R = Et
- 4f: where Y = CH = CH, X = Br, R = Et
- 4g: where Y = CH = CH, X = ClO 4 , R = Et
where Y = CMe 2 , X = I, R = Me
where Y = S, X = Br, R = Et
Chalcogenpyrylomethine dyes, eg compounds 12 on page 31 of Matsuoka (supra), ie where Y = Te, Se, O or NR;
Monochalcogenpyrylomethine dyes, eg compounds 13 on page 31 of Matsuoka (supra), ie where n = 1 or 2;
Pyrylium dyes, eg compounds 14 (X = O) on page 32 of Matsuoka (supra), ie where X = O, S or Se;
Thiapyrylium dyes, eg compounds 15 on page 32 and compound I on page 167 of Matsuoka (supra), ie where n = 1 or 2;
Squarylium dyes, eg Compound 10 and Table IV on page 30 of Matsuoka (supra), ie where X = CH = CH, Y = H and R = Et,
X = S, Y = H and R = Et and
X = CMe 2 , Y = H and R = Me,
and Compound 6, page 26 of Matsuoka (supra), ie where X = CH = CH, Y = H and R = Et;
Croconium dyes, eg Compound 9 and Table IV on page 30 of Matsuoka (supra), ie where X = CH = CH, Y = H and R = Et,
X = S, Y = H and R = Et
X = CMe 2 , Y = H and R = Me
and Compound 7, page 26 of Matsuoka (supra), ie where X = CH = CH, Y = H and R = Et;
Azulenium dyes, ie compound 8 on page 27 of Matsuoka (supra), ie Merocyanine dyes, eg Compound 16, R = Me, on page 32 of Matsuoka (supra), ie Indoaniline dyes, such as copper and nickel complexes of indoaniline dyes, eg Compound 6 on page 63 of Matsuoka (supra), ie where R = Et, R = Me, M = Cu,
R = Et, R '= Me, M = Ni
R = Me, R '= H, M = Cu or
R = Me, R '= H, M = Ni,
Benzo [a] phenoxazinium dyes and benzo [a] phenothiazinium dyes, eg as shown on page 201 of Matsuoka (supra), ie where X = O or S;
1,4-diaminoanthraquinone (N-alkyl) -3'-thioxo-2,3-dicarboximides, eg Compound 20 on page 41 of Matsuoka (supra) Indanthrene pigments, eg see compound 21 on page 41 of Matsuoka (supra);
2-arylamino-3,4-phthaloylacridone dyes, eg Compound 22 on page 41 of Matsuoka (supra) Trisphenoquinone dyes, eg Compound 23 on page 41 of Matsuoka (supra) Azo dyes, for example the monoazo dye, Compound 2 on page 90 of Matsuoka (supra), ie where X = CH = C (CN) 2 , R 1 = R 2 = Et, R 3 = R 4 = H,
X = C (CN) = C (CN) 2 , R 1 = R 2 = Et, R 3 = R 4 = H or
X = and Y = C = O, R 1 = R 2 = Et, R 3 = R 4 = H,
or Y = SO 2 , R 1 = H, R 2 = CH (Me) n Bu, R 3 = OMe and R 4 = NHAc;
Azo dyes, eg the polyazo dye, Compound 5 on page 91 of Matsuoka (supra), ie Intramolecular charge-transfer donor-acceptor infrared dyes, eg compounds 6 and 7 on page 91 of Matsuoka (supra), ie and non-benzoic aromatic dyes, eg Compound 8, a tropon, at page 92 of Matsuoka (supra), ie Tetrazinradikalfarbstoffe, eg, compound 9 on page 92 of Matsuoka (supra), ie wherein, X = p-phenylene or
X = p-terphenylene, as well as compound 10 on page 92 of Matsuoka (supra), ie wherein X = p-biphenyl;
cationic salts of tetrazine radical dyes, eg Compound 11 on page 92 of Matsuoka (supra) wherein X = p-phenylene;
Donor Acceptor Intramolecular Charge Transfer Dyes, eg CT Complexes of Compounds 13b and 14a to 14c on page 93 of Matsuoka (supra), ie where X = CH = NN (Ph) 2 in the donor and
- a) Y = CN, Z = NO 2
- b) Y = CN, Z = H or
- c) Y = Cl, Z = NO 2 in the acceptor;
Naphthoquinone dyes, eg compounds 2, 3 and 4 on page 37 of Matsuoka (supra), ie and metallated azo dyes, such as azo dyes containing nickel, cobalt, copper, iron and manganese; Phthalocyanine dyes, eg Compound 1 in Table II on page 51 of Matsuoka (supra), eg Naphthalocyanine dyes, eg Compound 3 in Table II on page 51 of Matsuoka (supra), eg Metal phthalocyanines such as phthalocyanines containing aluminum, silicon, nickel, zinc, lead, cadmium, magnesium, vanadium, cobalt, copper and iron, eg Compound 1 in Table III on page 52 of Matsuoka (supra), eg wherein, for example, M = Mg;
Metal naphthocyanines such as naphthalocyanines containing aluminum, zinc, cobalt, magnesium, cadmium, silicon, nickel, vanadium, lead, copper and iron, see compound 3 in Table III on page 52 of Matsuoka (supra), eg wherein, for example, M = Mg;
Bis (dithiolene) metal complexes having a metal ion such as nickel, cobalt, copper and iron coordinated to four sulfur atoms in a bis (S, S'-bidentate) ligand complex, eg see Table I on page 59 of Matsuoka (supra) in which
R 1 = R 2 = CF 3 , M = Ni
R 1 = R 2 = phenyl, M = Pd,
R 1 = R 2 = phenyl, M = Pt,
R 1 = C 4 to C 10 alkyl, R 2 = H, M = Ni,
R 1 = C 4 to C 10 alkyl, R 2 = H, M = Pd,
R 1 = C 4 to C 10 alkyl, R 2 = H, M = Pt,
R 1 = R 2 = phenyl, M = Ni,
R 1 = R 2 = p-CH 3 -phenyl, M = Ni,
R 1 = R 2 = p-CH 3 O-phenyl, M = Ni,
R 1 = R 2 = p-Cl-phenyl, M = Ni,
R 1 = R 2 = p-CF 3 -phenyl, M = Ni,
R 1 = R 2 = 3,4-diCl-phenyl, M = Ni,
R 1 = R 2 = o-Cl-phenyl, M = Ni,
R 1 = R 2 = o-Br-phenyl, M = Ni,
R 1 = R 2 = 3,4-diCl-phenyl, M = Ni,
R 1 = R 2 = p-CH 3 , M = Ni,
R 1 = R 2 = 2-thienyl, M = Ni,
R 1 = p- (CH 3 ) 2 N-phenyl, R 2 = phenyl, M = Ni, and
R 1 = p- (CH 3 ) 2 N -phenyl, R 2 = pH 2 N-phenyl, M = Ni;
Bis (benzenedithiolate) metal complexes having a metal ion, such as nickel, cobalt, copper and iron, coordinated to four sulfur atoms in a ligand complex, eg see Table III on page 62 of Matsuoka (supra), ie in which
X = tetramethyl, M = Ni,
X = 4,5-dimethyl, M = Ni,
X = 4-methyl, M = Ni,
X = tetrachloro, M = Ni,
X = H, M = Ni,
X = 4-methyl, M = Co,
X = 4-methyl, M = Cu, and
X = 4-methyl, M = Fe;
N, O-bidentate indoaniline dyes having a metal ion such as nickel, cobalt, copper and iron coordinated to two nitrogen and two oxygen atoms of two N, O-bidentate indoaniline ligands, eg Compound 6 in Table IV on page 63 of Matsuoka (supra), eg where R = Et, R '= Me, M = Cu,
R = Et, R '= Me, M = Ni,
R = Me, R '= H, M = Cu, and
R = Me, R '= H, M = Ni,
bis (S, O-dithiols) metal complexes having a metal ion such as nickel, cobalt, copper and iron coordinated to two sulfur atoms and two oxygen atoms in a bis (S, O-bidentate) ligand complex, eg see
tris (a-diimine) complexes having a metal ion coordinated to six nitrogen atoms in a triligand complex, eg, see Table II on page 180 of Matsuoka (supra), final compound (see also
Repräsentative Beispiele von sichtbaren Farbstoffen umfassen Fluoresceinderivate, Rhodaminderivate, Cumarine, Azofarbstoffe, metallierbare Farbstoffe, Anthrachinonfarbstoffe, Benzodifuranonfarbstoffe, polycyclische aromatische Carbonylfarbstoffe, indigoide Farbstoffe, Polymethinfarbstoffe, Azacarbocyaninfarbstoffe, Hemicyaninfarbstoffe, Barbiturate, Diazahemicyaninfarbstoffe, Styrylfarbstoffe, Diarylcarboniumfarbstoffe, Triarylcarboniumfarbstoffe, Phthalocyaninfarbstoffe, Quinophthalonfarbstoffe, Triphenodioxazinfarbstoffe, Formazanfarbstoffe, Phenothiazinfarbstoffe, wie Methylenblau, Azur A, Azur B und Azur C, Oxazinfarbstoffe, Thiazinfarbstoffe, Naptholactamfarbstoffe, Diazahemicyaninfarbstoffe, Azopyridonfarbstoffe, Azobenzolfarbstoffe, Beizenfarbstoffe, saure Farbstoffe, basische Farbstoffe, metallisierte und vormetallisierte Farbstoffe, Xanthenfarbstoffe, Direktfarbstoffe, Leukofarbstoffe, die oxidiert werden können, um Farbstoffe zu erzeugen, die bathochrom verschoben von denjenigen der Precursor-Leukofarbstoffe getönt sind, und andere Farbstoffe, wie jene, die aufgelistet wurden von Waring, D.R. und Hallas, G. in "The Chemistry and Application von Dyes", Topcis in Applied Chemistry, Plenum Press, New York, N.Y., 1990. Zusätzliche Farbstoffe können gefunden werden aufgelistet in Haugland, R.P., "Handbook of Fluorscent Probes and Research Chemicals", 6. Ausgabe, Molecular Probes, Inc., Eugene OR, 1996.Representative examples of visible dyes include fluorescein derivatives, rhodamine derivatives, coumarins, azo dyes, metalatable dyes, anthraquinone dyes, benzodifuranone dyes, poly cyclic aromatic carbonyl dyes, indigoid dyes, polymethine dyes, azacarbocyanine dyes, hemicyanine dyes, barbiturates, diazahemicyanine dyes, styryl dyes, diaryl carbonium dyes, triaryl carbonium dyes, phthalocyanine dyes, quinophthalone dyes, triphenodioxazine dyes, formazan dyes, phenothiazine dyes such as methylene blue, azure A, azure B and azure C, oxazine dyes, thiazine dyes, naptholactam dyes , Diazahemicyanine dyes, azopyridone dyes, azobenzene dyes, mordant dyes, acid dyes, basic dyes, metallized and premetallized dyes, xanthene dyes, direct dyes, leuco dyes that can be oxidized to form dyes that are bathochromically shifted from those of the precursor leuco dyes, and others Dyes, such as those listed by Waring, DR and Hallas, G. in "The Chemistry and Application of Dyes", Topcis in Applied Chemist Additional dyes can be found listed in Haugland, RP, "Handbook of Fluoride Probes and Research Chemicals", 6th Edition, Molecular Probes, Inc., Eugene OR, 1996.
Derartige Chromophore und Fluorophore können entweder direkt an den Vektor oder innerhalb einer Linkerstruktur kovalent gebunden sein. Wieder können Linker des oben zusammen mit den Metallreportern beschriebenen Typs für organische Chromophore oder Fluorophore verwendet werden, wobei die Choromophore/Fluorophore den Platz von einigen oder allen chelatbildenden Gruppen einnehmen.such Chromophores and fluorophores can either directly to the vector or within a linker structure be covalently bound. Again you can Linker of the type described above together with the metal reporters for organic Chromophores or fluorophores are used, with the choromophore / fluorophores take the place of some or all chelating groups.
Wie mit den oben diskutierten Metallchelatbildnern können Chromophore/Fluorophore in oder auf teilchenförmigen Linkereinheiten getragen werden, z.B. in oder auf einem Vesikel, oder können kovalent an inerte Matrixteilchen gebunden sein, die auch als ein Lichtstreuungsreporter dienen können.As Chromophors / fluorophores can be used with the metal chelators discussed above in or on particulate Linker units are worn, e.g. in or on a vesicle, or can covalently bound to inert matrix particles, also called a Light scattering reporters can serve.
Teilchenförmige Reporter oder Linker-ReporterParticulate reporter or linker reporter
Die teilchenförmigen Reporter und die Linker-Reporter fallen im Allgemeinen in zwei Kategorien – jene, bei denen das Teilchen eine Matrix oder Schale aufweist, die den Reporter trägt oder enthält, und jene, bei denen die Teilchenmatrix selbst der Reporter ist. Beispiele der ersten Kategorie sind: Vesikel (z.B. Micellen und Liposomen), die eine flüssige oder feste Phase enthalten, die den kontrastwirksamen Reporter enthält, z.B. ein chelatiertes paramagnetisches Metall oder Radionuklid, oder ein wasserlösliches iodiertes Röntgenstrahlungskonstrastmittel; poröse Teilchen, die mit dem Reporter beladen sind, z.B. mit paramagnetischem Metall beladene Teilchen eines Molekularsiebes; und feste Teilchen, z.B. ein inertes biotolerables Polymer, auf dem der Reporter gebunden oder aufgebracht ist, z.B. mit Farbstoff beladene Polymerteilchen.The particulate Reporters and the linker reporters generally fall into two categories - those where the particle has a matrix or shell containing the Reporter carries or contains, and those where the particle matrix itself is the reporter. Examples of the first category are: vesicles (e.g., micelles and liposomes), the one liquid or solid phase containing the contrast-effective reporter, e.g. a chelated paramagnetic metal or radionuclide, or a water-soluble iodinated X-ray contrast agent; porous Particles loaded with the reporter, e.g. with paramagnetic Metal-loaded particles of a molecular sieve; and solid particles, e.g. an inert biotolerable polymer to which the reporter is bound or applied, e.g. dye particles loaded with polymer.
Beispiele der zweiten Kategorie sind: lichtstreuende organische oder anorganische Teilchen, magnetische Teilchen (z.B. superparamagnetische, ferromagnetische oder ferrimagnetische Teilchen); und Farbstoffteilchen.Examples the second category are: light-scattering organic or inorganic Particles, magnetic particles (e.g., superparamagnetic, ferromagnetic or ferrimagnetic particles); and dye particles.
Bevorzugte
teilchenförmige
Reporter oder Reporter-Linker umfassen superparamagnetische Teilchen (siehe
Die
teilchenförmigen
Reporter können
einen oder mehrere Vektoren besitzen, die direkt oder indirekt an
ihre Oberflächen
gebunden sind. Im Allgemeinen wird es bevorzugt werden, eine Mehrzahl
(z.B. 2 bis 50) von Vektoreinheiten pro Teilchen zu binden. Besonders
günstig
wird man, neben dem erwünschten
Targetingvektor, auch flussverlangsamende Vektoren an die Teilchen
binden, d.h. Vektoren, die eine Affinität für das Kapillarlumen oder andere
Organoberflächen
besitzen, die ausreichend ist, um die Passage des Kontrastmittels durch
die Kapillaren oder das Zielorgan zu verringern, aber nicht selbst
ausreicht, um das Kontrastmittel zu immobilisieren. Derartige flussverlangsamende
Vektoren (z.B. beschrieben in
Das Mittel, durch das die Vektor-an-Teilchen-Bindung erreicht wird, wird von der Natur der Teilchenoberfläche abhängen. Für anorganische Teilchen kann die Verbindung mit dem Teilchen beispielsweise mittels einer Wechselwirkung zwischen einer Metallbindungsgruppe (z.B. einer Phosphat-, Phosphonat- oder Oligo- oder Polyphosphatgruppe) auf dem Vektor oder auf einem Linker gebunden an den Vektor ausgeführt werden. Für organische (z.B. polymere) Teilchen kann die Vektorbindung mittels direkter kovalenter Bindung zwischen Gruppen auf der Teilchenoberfläche und reaktiven Gruppen im Vektor, z.B. Amid- oder Esterbindung, oder durch kovalente Bindung des Vektors und des Teilchens an einen Linker ausgeführt werden. Linker des oben zusammen mit chelatierten Metallreportern diskutierten Typs können verwendet werden, obwohl im Allgemeinen die Linker nicht verwendet werden, um Teilchen miteinander zu koppeln.The Means by which vector-to-particle binding is achieved will depend on the nature of the particle surface. For inorganic particles can the connection with the particle, for example by means of an interaction between a metal linking group (e.g., a phosphate, phosphonate, or oligo- or polyphosphate group) on the vector or on one Linker bound to the vector. For organic (e.g., polymeric) particles can be used to direct vector binding covalent bond between groups on the particle surface and reactive groups in the vector, e.g. Amide or ester bond, or by covalent attachment of the vector and the particle to a linker accomplished become. Linker of the above together with chelated metal reporters of the type discussed although generally the linker is not used be used to couple particles together.
Für nicht-feste
Teilchen, z.B. Tröpfchen
(z.B. von wasserunlöslichen
iodierten Flüssigkeiten,
wie in
Außer den
Vektoren können
andere Gruppen an die Teilchenoberfläche gebunden werden, z.B. Stabilisatoren
(um eine Aggregration zu verhindern) und Biodistributionsmodifizierer,
wie PEG. Derartige Gruppen werden beispielsweise in
Bevorzugt
werden die V-L-R-Mittel der Erfindung die Rezeptortargetingvektoren
direkt oder indirekt an einen Reporter gekoppelt haben, z.B. mit
kovalent gebundenen Iodradioisotopen, mit Metallchelaten, die direkt oder über eine
organische Linkergruppe gebunden sind, oder gekoppelt an einen teilchenförmigen Reporter oder
Linker-Reporter, z.B. superparamagnetische Kristalle (optional beschichtet,
z.B. wie in
Kurz
gesagt können
für die
Bilderzeugungsmodalitäten
MRI, Röntgenstrahlung,
Lichtbilderzeugung, Nuklearbilderzeugung, Magnetotomographie und
Electrical Impedance Tomography die favorisierten Reporter folgende
sein:
Die Mittel der Erfindung können an Patienten zur Bilderzeugung in Mengen verabreicht werden, die ausreichen, um den erwünschten Kontrast mit der bestimmten Bilderzeugungstechnik zu ergeben. Wo der Reporter ein Metall ist, sind im Allgemeinen Dosierungen von ungefähr 0,001 bis 5,0 mmol chelatiertes Bilderzeugungsmetallion pro Kilogramm des Patientenkörpergewichts wirksam, um angemessene Kontrastverbesserungen zu erhalten. Für die meisten MRI-Anwendungen werden die bevorzugten Dosierungen an bilderzeugendem Metallion im Bereich von 0,02 bis 1,2 mmol/kg Körpergewicht liegen, während für Röntgenstrahlungsanwendungen Dosierungen von 0,05 bis 2,0 mmol/kg im Allgemeinen wirksam sind, um eine Röntgenstrahlungsabschwächung zu erreichen. Bevorzugte Dosierungen für die meisten Röntgenstrahlungsanwendungen sind 0,1 bis 1,2 mmol der Lanthandien- oder Schwermetallverbindung/kg Körpergewicht.The Means of the invention can administered to patients for imaging purposes in amounts sufficient around the desired Contrast with the particular imaging technique. Where The reporter is a metal, are generally dosages of approximately 0.001 to 5.0 mmoles of chelated imaging metal ion per kilogram of the patient's body weight effective to obtain adequate contrast enhancements. For the most MRI applications become the preferred dosages of imaging metal ion in the range of 0.02 to 1.2 mmol / kg body weight while for X-ray applications Doses of 0.05 to 2.0 mmol / kg are generally effective, about an X-ray attenuation too to reach. Preferred dosages for most X-ray applications are 0.1 to 1.2 mmol of the lanthanum or heavy metal compound / kg Body weight.
Wo der Reporter ein Radionuklid ist, werden Dosierungen von 0,01 bis 100 mCi, bevorzugt 0,1 bis 50 mCi normalerweise pro 70 kg Körpergewicht ausreichen. Wo der Reporter ein superparamagnetisches Teilchen ist, wird die Dosierung normalerweise zwischen 0,5 bis 30 mg Fe/kg Körpergewicht sein.Where The reporter is a radionuclide, dosages are from 0.01 to 100 mCi, preferably 0.1 to 50 mCi normally per 70 kg body weight suffice. Where the reporter is a superparamagnetic particle, the dosage is normally between 0.5 to 30 mg Fe / kg body weight be.
Die Verbindungen der vorliegenden Erfindung können mit konventionellen pharmazeutischen oder veterinärmedizinischen Hilfsstoffen formuliert werden, zum Beispiel Emulgatoren, Fettsäureester, Geliermittel, Stabilisatoren, Antioxidanzien, die Osmolalität einstellende Mittel, Puffer, den pH einstellende Mittel, etc., und können in einer Form vorliegen, die für die parenterale Verabreichung, beispielsweise Injektion oder Infusion oder die Verabreichung direkt in die Vaskulatur geeignet ist. Daher können die Verbindungen der vorliegenden Erfindung in konventionellen pharmazeutischen Verabreichungsformen vorliegen, wie beispielsweise Lösungen, Suspensionen und Dispersionen in physiologisch annehmbaren Trägermedien, zum Beispiel Wasser für Injektionen.The Compounds of the present invention can be treated with conventional pharmaceutical or veterinary Excipients, for example emulsifiers, fatty acid esters, Gelling agents, stabilizers, antioxidants, osmolality adjusting Agents, buffers, pH adjusting agents, etc., and can be used in in a form suitable for parenteral administration, for example, injection or infusion or the administration is suitable directly into the vasculature. Therefore, the Compounds of the present invention in conventional pharmaceutical Administration forms, such as solutions, Suspensions and dispersions in physiologically acceptable carrier media, for example, water for injections.
Die Verbindungen gemäß der Erfindung können deshalb für die Verabreichung unter Verwenden physiologisch annehmbarer Träger oder Exzipienten in einer Weise formuliert werden, die voll innerhalb des Fachwissens liegt. Beispielsweise können die Verbindungen, optional mit der Zugabe von pharmazeutisch annehmbaren Exzipienten, in einem wässrigen Medium suspendiert oder aufgelöst werden, wobei die resultierende Lösung oder Suspension dann sterilisiert wird.The compounds according to the invention may therefore be suitable for administration using phy siologically acceptable carrier or excipient may be formulated in a manner that is fully within the skill of the art. For example, the compounds, optionally with the addition of pharmaceutically acceptable excipients, may be suspended or dissolved in an aqueous medium, the resulting solution or suspension then being sterilized.
Parenteral verabreichbare Formen, z.B. intravenöse Lösungen, sollten steril und frei von physiologisch nicht annehmbaren Mitteln sein, und sollten eine niedrige Osmolalität besitzen, um eine Irritation oder andere nachteilige Wirkungen bei der Verabreichung zu minimieren, und daher sollte das Kontrastmedium bevorzugt isotonisch oder leicht hypertonisch sein. Geeignete Vehikel umfassen wässrige Vehikel, die üblicherweise für die Verabreichung parenteraler Lösungen verwendet werden, wie Natriumchloridinjektion, Ringers-Injektion, Dextroseinjektion, Dextrose- und Natriumchloridinjektion, Laktierte Ringers-Injektion und andere Lösungen, wie in Remington's Pharmaceutical Sciences, 15. Ausgabe, Easton: Mack Publishing Co., S. 1405-1412 und 1461-1487 (1975) und The National Formulary XIV, 14. Ausgabe, Washington: American Pharmaceutical Association (1975) beschrieben. Die Lösungen können Konservierungsstoffe, antimikrobielle Mittel, Puffer und Antioxidanzien, die üblicherweise für parenterale Lösungen verwendet werden, Exzipienten und andere Additive enthalten, die mit den Chelaten kompatibel sind und die nicht mit der Herstellung, Lagerung oder der Verwendung von Produkten interferieren.parenterally administrable forms, e.g. intravenous solutions, should be sterile and free from physiologically unacceptable agents, and should a low osmolality to contribute to irritation or other adverse effects to minimize administration, and therefore the contrast medium should preferably isotonic or slightly hypertonic. Suitable vehicles include watery Vehicles, usually for the Administration of parenteral solutions such as sodium chloride injection, Ringer's injection, dextrose injection, Dextrose and sodium chloride injection, Lactated Ringer's injection and other solutions, as in Remington's Pharmaceutical Sciences, 15th Edition, Easton: Mack Publishing Co., pp. 1405-1412 and 1461-1487 (1975) and The National Formulary XIV, 14th Edition, Washington: American Pharmaceutical Association (1975). The solutions can Preservatives, antimicrobials, buffers and antioxidants, the usual for parenteral solutions used, excipients and other additives that contain compatible with the chelates and not with the production, Storage or use of products.
Die vorliegende Erfindung wird nun weiter veranschaulicht mittels der folgenden Beispiele. Wenn nicht anders bezeichnet, sind alle Prozentsätze in Gewichtsprozent angegeben.The The present invention will now be further illustrated by means of following examples. Unless otherwise indicated, all percentages are in weight percent specified.
Beispiel 1example 1
Kontrastmittel für MR-Bilderzeugung von AngiogeneseContrast agent for MR imaging of angiogenesis
Verbindung 1Connection 1
Lysin
(0,1 g, 0,7 mmol) wird zu einer Lösung von N2-[3S-Hydroxy-4-(N-hydroxyamino)2R-isobutylsuccinyl]-L-(4-oxymethylcarboxy)phenylalanin-N1-methylamid
(hergestellt gemäß
Die Dispersion wird über Nacht bei +4°C belassen. Die Dispersion wird gefiltert und das Lösemittel wird am Rotationsverdampfer verdampft, bevor die Substanz durch Chromatographie gereinigt wird.The Dispersion is over Night at + 4 ° C leave. The dispersion is filtered and the solvent becomes evaporated on a rotary evaporator before the substance by chromatography is cleaned.
Verbindung 2Connection 2
Diethylentriaminpentaessigsäuredieanhydrid (17,9 g, 50 mmol) wird in trockenem DMF aufgelöst und die Verbindung 1 (0,3 g, 0,5 mmol), aufgelöst in trockenem DMF, wird zugegeben. Die Reaktionsmischung wird bei erhöhter Temperatur unter Stickstoffatmosphäre gerührt. Der Reaktion folgt eine TLC. Das Lösemittel wird am Rotationsverdampfer verdampft und die Substanz durch Chromatographie gereinigt.Diethylentriaminpentaessigsäuredieanhydrid (17.9 g, 50 mmol) is dissolved in dry DMF and compound 1 (0.3 g, 0.5 mmol) in dry DMF is added. The reaction mixture is at increased Temperature stirred under nitrogen atmosphere. The reaction is followed by a TLC. The solvent is evaporated on a rotary evaporator and the substance by chromatography cleaned.
Gd(III)-Chelat der Verbindung 2Gd (III) chelate of compound 2
Zu einer Lösung der Verbindung 2 (0,4 g, 0,4 mmol) in Wasser wird Gadoliniumoxid Gd2O3 (0,1 g, 0,2 mmol) zugegeben und die Mischung wird bei 95°C erwärmt. Nach der Filtration wird die Lösung verdampft und in vacuo bei 50°C getrocknet.To a solution of Compound 2 (0.4 g, 0.4 mmol) in water is added gadolinium oxide Gd 2 O 3 (0.1 g, 0.2 mmol) and the mixture is heated at 95 ° C. After filtration, the solution is evaporated and dried in vacuo at 50 ° C.
Beispiel 2Example 2
Kontrastmittel für MR-Bilderzeugung von AngiogeneseContrast agent for MR imaging of angiogenesis
Verbindung 3Connection 3
Lysin
(0,1 g, 0,7 mmol) wird zu einer Lösung von N-(4-Octylphenyl)-3-(2-carboxyethyl)-6,7-dihydro-5H-thiazolo[3,2-a]pyrimidin-2-carboxamid
(hergestellt gemäß
Verbindung 4Connection 4
Diethylentriaminpentaessigsäuredianhydrid (17,9 g, 50 mmol) wird in trockenem DMF aufgelöst und die Verbindung 3 (0,3 g, 0,5 mmol), aufgelöst in trockenem DMF, wird zugegeben. Die Reaktionsmischung wird bei erhöhter Temperatur unter Stickstoffatmosphäre gerührt. Der Reaktion folgt TLC. Das Lösemittel wird am Rotationsverdampfer verdampft und die Substanz wird durch Chromatographie gereinigt.diethylenetriaminepentaacetic (17.9 g, 50 mmol) is dissolved in dry DMF and compound 3 (0.3 g, 0.5 mmol) in dry DMF is added. The reaction mixture is at increased Temperature stirred under nitrogen atmosphere. The reaction is followed by TLC. The solvent is evaporated on a rotary evaporator and the substance is passed through Purified by chromatography.
GD(III)-Chelat der Verbindung 4GD (III) chelate of compound 4
Zu einer Lösung der Verbindung 4 (0,4 g, 0,4 mmol) in Wasser wird Gadoliniumoxid Gd2O3 (0,1 g, 0,2 mmol) gegeben und die Mischung wird bei 95°C erwärmt. Nach der Filtration wird die Lösung verdampft und in vacuo bei 50°C getrocknet.To a solution of compound 4 (0.4 g, 0.4 mmol) in water is added gadolinium oxide Gd 2 O 3 (0.1 g, 0.2 mmol) and the mixture is heated at 95 ° C. After filtration, the solution is evaporated and dried in vacuo at 50 ° C.
Beispiel 3Example 3
Kontrastmittel für Nuklearmedizin zur Erfassung von Angiogenesecontrast agents for nuclear medicine for the detection of angiogenesis
99mTc-Chelat der Verbindung 2 99m Tc-chelate of compound 2
Die Verbindung 2 von Beispiel 1 (1 mg) wird in 0,1 N NaOH aufgelöst. SnCl2·2H2O (100 μg), aufgelöst in 0,05 N HCl und eine Lösung von 10-100 mCi 99mTc in der Form von Natriumpertechnetat in Salzlösung wird zugegeben. Der pH der Lösung wird auf pH 7-8 durch Zugabe von 0,5 M Phosphatpuffer (pH 5) nach weniger als einer Minute eingestellt. Der Reaktion folgt TLC und die Substanz wird durch Chromatographie gereinigt.Compound 2 of Example 1 (1 mg) is dissolved in 0.1 N NaOH. SnCl 2 · 2H 2 O (100 ug) dissolved in 0.05 N HCl and a solution of 10-100 mCi 99m Tc in the form of sodium pertechnetate in saline is added. The pH of the solution is adjusted to pH 7-8 by adding 0.5 M phosphate buffer (pH 5) in less than one minute. The reaction is followed by TLC and the substance is purified by chromatography.
Beispiel 4Example 4
Kontrastmittel für Nuklearmedizin zur Erfassung von AngiogeneseContrast agent for nuclear medicine for detection of angiogenesis
99mTc-Chelat Verbindung 4 99m Tc-chelate compound 4
Die Verbindung 4 von Beispiel 2 (1 mg) wird in 0,1 N NaOH aufgelöst. SnCl2·2H2O (100 μg), aufgelöst in 0,05 N HCl und eine Lösung von 10-100 mCi 99mTc in der Form von Natriumpertechnetat in Salzlösung wird zugegeben. Der pH der Lösung wird auf pH 7-8 durch Zugabe von 0,5 M Phosphatpuffer (pH 5) nach weniger als einer Minute eingestellt. Der Reaktion folgt TLC und die Substanz wird durch Chromatographie gereinigt.Compound 4 of Example 2 (1 mg) is dissolved in 0.1 N NaOH. SnCl 2 · 2H 2 O (100 ug) dissolved in 0.05 N HCl and a solution of 10-100 mCi 99m Tc in the form of sodium pertechnetate in saline is added. The pH of the solution is adjusted to pH 7-8 by adding 0.5 M phosphate buffer (pH 5) in less than one minute. The reaction is followed by TLC and the substance is purified by chromatography.
Beispiel 5Example 5
Kontrastmittel für Nuklearmedizin zur Erfassung von AngiogeneseContrast agent for nuclear medicine for detection of angiogenesis
Eine
wässrige
Lösung
von 131I2 (2 Äquivalente)
und Natriumperchlorat (1 Äquivalent)
wird zu einer wässrigen
Lösung
von N2-[3S-Hydroxy-4-hydroxyamino)-2R-isobutylsuccinyl]-L-phenylalanin-N1-methylamid (hergestellt gemäß
Beispiel 6Example 6
Herstellung von DTPA-Monoamidgadoliniumkomplex umfassend einen Vektor zum Targeting eines VEGF-Rezeptors für MR-Erfassung von Angiogenese Preparation of DTPA-monoamide-gadolinium complex comprising a vector for targeting a VEGF receptor for MR detection of angiogenesis
a) Synthese von 6,7-Dimethoxy-3H-Chinazolin-4-ona) Synthesis of 6,7-dimethoxy-3H-quinazolin-4-one
Eine Mischung von 2-Amino-4,5-dimethoxybenzoesäure (9,9 mg, 0,050 mmol) und Formamid (5 ml) wurde bei 190°C 6 Stunden lang erwärmt. Die Mischung wurde auf 80°C gekühlt und auf Wasser gegossen (25 ml). Präzipitiertes Material wurde abgefiltert, mit Wasser gewaschen und in vacuo betrocknet. Ausbeute 1,54 g (15 %), braunes Pulver. Die Struktur wurde durch 1H (500 MHz)- und 13C-NMR (125 MHz)-Analyse bestätigt.A mixture of 2-amino-4,5-dimethoxybenzoic acid (9.9 mg, 0.050 mmol) and formamide (5 mL) was heated at 190 ° C for 6 hours. The mixture was cooled to 80 ° C and poured onto water (25 ml). Precipitated material was filtered off, washed with water and dried in vacuo. yield 1.54 g (15%), brown powder. The structure was confirmed by 1 H (500 MHz) and 13 C NMR (125 MHz) analysis.
b) Synthese von 4-Chlor-6,7-dimethoxychinazolinb) Synthesis of 4-chloro-6,7-dimethoxyquinazoline
Eine Suspension der Verbindung von a) (1,03 g, 5,00 mmol) in Phosphoroxychlorid (20 ml) wurde 3 Stunden unter Rückfluss gekocht. Die dunkle Lösung wurde konzentriert und der Rückstand wurde in Ethylacetat aufgenommen. Die organische Phase wurde mit gesättigter Natriumbicarbonatlösung gewaschen und getrocknet (MgSO4). Die Lösung wurde durch eine kurze Silicasäule gefiltert und konzentriert, um 392 mg (35 %) eines cremefarbenen Materials zu ergeben. 1H-NMR (300 MHz)- und 13C-NMR (75 MHz)-Spektren waren in Übereinstimmung mit der Struktur.A suspension of the compound of a) (1.03 g, 5.00 mmol) in phosphorus oxychloride (20 ml) was refluxed for 3 hours. The dark solution was concentrated and the residue was taken up in ethyl acetate. The organic phase was washed with saturated sodium bicarbonate solution and dried (MgSO 4 ). The solution was filtered through a short silica column and concentrated to give 392 mg (35%) of a cream colored material. 1 H NMR (300 MHz) and 13 C NMR (75 MHz) spectra were in agreement with the structure.
c) Synthese von [4-(6,7-Dimethoxychinazolin-4-ylamino)-phenyl]essigsäurec) Synthesis of [4- (6,7-dimethoxyquinazolin-4-ylamino) -phenyl] acetic acid
Eine Mischung der Verbindung von b) (112 mg, 0,500 mmol) und 4-Aminophenylessigsäure (76 mg, 0,50 mmol) in 2-Propanol (8 ml) wurde 3 Stunden lang unter Rückfluss gekocht. Die Reaktionsmischung wurde gekühlt und präzipitiertes Material wurde isoliert, mit 2-Propanol gewaschen und in vacuo getrocknet. Ausbeute 183 mg (97 %), blassgelbes festes Material. Die Struktur wurde mit 1H-NMR (500 MHz)- und 13C-NMR (125 MHz)-Analyse verifiziert. Weitere Charakterisierung wurde unter Verwenden von MALDI-Massenspektrometrie (α-Cyano-4-Hydroxyzimtsäurematrix) ausgeführt, was m/z für [MH]+ bei 341 ergab, erwartet 340.A mixture of the compound of b) (112 mg, 0.500 mmol) and 4-aminophenylacetic acid (76 mg, 0.50 mmol) in 2-propanol (8 ml) was refluxed for 3 hours. The reaction mixture was cooled and precipitated material was isolated, washed with 2-propanol and dried in vacuo. Yield 183 mg (97%), pale yellow solid material. The structure was verified by 1 H-NMR (500 MHz) and 13 C-NMR (125 MHz) analysis. Further characterization was performed using MALDI mass spectrometry (α-cyano-4-hydroxycinnamic acid matrix), giving m / z for [MH] + at 341, expecting 340.
d) Synthese von t-Butyl-(6-{2-[4-(6,7-dimethoxychinazolin-4-ylamino)phenyl]acetylamino}hexyl)carbamatd) Synthesis of t-butyl (6- {2- [4- (6,7-dimethoxyquinazolin-4-ylamino) phenyl] acetylamino} hexyl) carbamate
Zu einer Suspension der Verbindung von c) (38 mg, 0,10 mmol) und N-Boc-1,6-diaminohexanhydrochlorid (25 mg, 0,10 mmol) in DMF (2,0 ml) wurde N,N-Diisopropylethylamin (34 ml, 0,20 mmol) gegeben. Zu der klaren Lösung wurde N-(3-Dimethylaminopropyl)-N'-ethylcarbodiimidhydrochlorid (19 mg, 0,10 mmol) und 1-Hydroxybenzotriazol (15 mg, 0,10 mmol) gegeben. Die Reaktionsmischung wurde bei Raumtemperatur über Nacht gerührt und dann auf 25 ml Wasser gegossen, das Natriumcarbonat (2,5 g) und Natriumchlorid (4,0 g) enthielt. Organisches Material wurde in Chloroform extrahiert und die organische Phase wurde mit Wasser gewaschen und getrocknet (Na2SO4). Die Lösung wurde gefiltert und konzentriert. Das Produkt wurde durch Säulenchromatographie (Silica, Chloroform/Methanol/Essigsäure 85:10:5) gereinigt und schließlich aus Essigsäure lyophilisiert. Ausbeute 54 mg ( 90 %), gelb-weißes festes Material (Acetat). Das Produkt wurde durch MALDI-Massenspektrometrie (α-Cyano-4-Hydroxyzimtsäurematrix) charakterisiert, was m/z für [MH]+ bei 539 wie erwartet ergab.To a suspension of the compound of c) (38 mg, 0.10 mmol) and N-Boc-1,6-diaminohexane hydrochloride (25 mg, 0.10 mmol) in DMF (2.0 mL) was N, N-diisopropylethylamine (34 mL, 0.20 mmol). To the clear solution was added N- (3-dimethylaminopropyl) -N'-ethylcarbodiimide hydrochloride (19 mg, 0.10 mmol) and 1-hydroxybenzotriazole (15 mg, 0.10 mmol). The reaction mixture was stirred at room temperature overnight and then poured into 25 ml of water containing sodium carbonate (2.5 g) and sodium chloride (4.0 g). Organic material was extracted into chloroform and the organic phase was washed with water and dried (Na 2 SO 4 ). The solution was filtered and concentrated. The product was purified by column chromatography (silica, chloroform / methanol / acetic acid 85: 10: 5) and finally lyophilized from acetic acid. Yield 54 mg (90%), yellow-white solid material (acetate). The product was characterized by MALDI mass spectrometry (α-cyano-4-hydroxycinnamic acid matrix), giving m / z for [MH] + at 539 as expected.
Eine weitere Charakterisierung wurde ausgeführt unter Verwenden von 1H (500 MHz)- und 13C (125 MHz)-NMR-Spektroskopie.Further characterization was performed using 1 H (500 MHz) and 13 C (125 MHz) NMR spectroscopy.
e) Synthese von N-(6-Aminohexyl)-[4-(6,7-dimethoxychinazolin-4-ylamino)phenyl]acetamidhydrochloride) Synthesis of N- (6-aminohexyl) - [4- (6,7-dimethoxyquinazolin-4-ylamino) phenyl] acetamide hydrochloride
Die Verbindung von d) (27 mg, 0,050 mmol) wurde in Dioxan (3 ml) durch sanftes Erwärmen aufgelöst. Zu der Lösung wurde 4 N HCl in Dioxan (0,5 ml) gegeben. Die Reaktionsmischung wurde über Nacht gerührt und in vacuo konzentriert, um eine quantitative Ausbeute der Titelverbindung zu ergeben. Eine Charakterisierung wurde ausgeführt unter Verwenden der MALDI-Massenspektrometrie (α-Cyano-4-Hydroxyzimtsäurematrix), was m/z für [MH]+ bei 439 wie erwartet ergab. Eine weitere Charakterisierung wurde ausgeführt unter Verwenden von analytischem HPLC (Säule Vydac 218TP54, Gradient 12 bis 24 % B über 20 Minuten, A = Wasser/0,1 % TFA, B = Acetonitril/0,1 % TFA, Flussgeschwindigkeit 1,0 ml/min), was einen einzelnen Produktpeak mit einer Retentionszeit von 13,0 min, detektiert bei 340 nm ergab. Eine Charakterisierung wurde auch ausgeführt mittels NMR-Spektroskopie, was 1H (500 MHz)- und 13C (125 MHz)-Spektren in Übereinstimmung mit der Struktur ergab.The compound of d) (27 mg, 0.050 mmol) was dissolved in dioxane (3 mL) by gentle warming. To the solution was added 4N HCl in dioxane (0.5 ml). The reaction mixture was stirred overnight and concentrated in vacuo to give a quantitative yield of the title compound. Characterization was carried out using MALDI mass spectrometry (α-cyano-4-hydroxycinnamic acid matrix), giving m / z for [MH] + at 439 as expected. Further characterization was performed using analytical HPLC (Vydac 218TP54 column, gradient 12 to 24% B over 20 minutes, A = water / 0.1% TFA, B = acetonitrile / 0.1% TFA, flow rate 1.0 ml / min), giving a single product peak with a retention time of 13.0 minutes detected at 340 nm. Characterization was also carried out by NMR spectroscopy, giving 1 H (500 MHz) and 13 C (125 MHz) spectra in accordance with the structure.
f) Synthese eines DTPA-Monoamidderivats für Gadoliniumchelatierung (Struktur oben gezeigt)f) Synthesis of a DTPA monoamide derivative for gadolinium chelation (Structure shown above)
N,N-Diisopropylethylamin (17 μl, 0,10 mmol) wurde zu einer Suspension der Verbindung von e) (0,05 mmol) und DTPA-Anhydrid (179 mg, 0,500 mmol) in DMF (5 ml) gegeben. Die Mischung wurde bei Raumtemperatur 2 Stunden lang gerührt und in vacuo konzentriert. HPLC-Analyse (Säule Vydac 218TP54, Gradient 16-28 % B über 20 Minuten, A = Wasser/0,1 % TFA, B = Acetonitril/0,1 % TFA, Flussgeschwindigkeit 1,0 ml/min) ergab einen Produktpeak bei 7,9 min für die durch LC-MS (ESI) gezeigt wurde, dass sie der Titelverbindung (m/z für [MH]+ bei 813, erwartet 814) entsprach. Das Produkt wurde durch präparative HPLC gereinigt (Säule Vydac 218TP1022, Gradient 16-28 % B über 60 Minuten, A = Wasser/0,1 % TFA, B = Acetonitril/0,1 % TFA, Flussgeschwindigkeit 10,0 ml/min, Erfassung bei 254 nm), was eine Ausbeute von 6,7 mg an gereinigtem Material ergab. Analyse des gereinigten Materials durch analytische HPLC zeigte eine Verschiebung in der Retentionszeit auf 5,6 min (analytische Bedingungen wie oben beschrieben), wofür durch MALDI-Massenspektrometrie gezeigt wurde, dass es dem Eisenkomplex entsprach, was m/z bei 870 für den Komplex und 816 für den freien Ligand ergab.N, N-Diisopropylethylamine (17 μl, 0.10 mmol) was added to a suspension of the compound of e) (0.05 mmol) and DTPA anhydride (179 mg, 0.500 mmol) in DMF (5 ml). The mixture was stirred at room temperature for 2 hours and concentrated in vacuo. HPLC analysis (Vydac 218TP54 column, gradient 16-28% B over 20 minutes, A = water / 0.1% TFA, B = acetonitrile / 0.1% TFA, flow rate 1.0 mL / min) gave a product peak 7.9 min, which was shown by LC-MS (ESI) to correspond to the title compound (m / z for [MH] + at 813, expected 814). The product was purified by preparative HPLC (Vydac 218TP1022 column, gradient 16-28% B over 60 minutes, A = water / 0.1% TFA, B = acetonitrile / 0.1%. TFA, flow rate 10.0 ml / min, detection at 254 nm), giving a yield of 6.7 mg of purified material. Analysis of the purified material by analytical HPLC showed a shift in retention time to 5.6 min (analytical conditions as described above), which was shown by MALDI mass spectrometry to correspond to the iron complex, giving m / z at 870 for the complex and 816 for the free ligand.
g) Herstellung das Gadoliniumkomplexes der Verbindung von f)g) Preparation of the Gadolinium Complex the compound of f)
Die Verbindung von f) (0,1 mg) wurde in einer wässrigen Lösung von Gadoliniumtrichlorid (Konz. 2 mg/ml, 0,1 ml) aufgelöst. Die Mischung wurde über Nacht gerührt. Die quantitative Umwandlung zum Gadoliniumkomplex wurde durch MALDI-Massenspektrometrie (α-Cyano-4-Hydroxyzimtsäurematrix) verifiziert, was m/z-Peaks bei 970, 992 und 1014 für den Gadoliniumkomplex (Gadolinium, Gadolinium/Natrium bzw. Gadolinium/Dinatrium) und bei 816/838 entsprechend dem freien Liganden/Natriumkomplex ergab. Keine Spur des Eisenkomplexes konnte detektiert werden.The Compound of f) (0.1 mg) was dissolved in an aqueous solution of gadolinium trichloride (Conc. 2 mg / ml, 0.1 ml). The mixture was over Night stirred. The quantitative conversion to the gadolinium complex was determined by MALDI mass spectrometry (Α-cyano-4-hydroxycinnamic acid matrix) verified what m / z peaks at 970, 992 and 1014 for the gadolinium complex (Gadolinium, gadolinium / sodium or gadolinium / disodium) and at 816/838 corresponding to the free ligand / sodium complex. None Trace of the iron complex could be detected.
Beispiel 7Example 7
Herstellung eines DTPA-Bisamidgadoliniumkomplexes umfassend einen Vektor zum Targeting eines VEGF-Rezeptors für die MR-Erfassung von Angiogenese Preparation of a DTPA-bisamide gadolinium complex comprising a vector for targeting a VEGF receptor for MR detection of angiogenesis
a) Synthese eines DTPA-Bisamidderivats für Gadoliniumchelatierung (Struktur oben gezeigt)a) Synthesis of a DTPA bisamide derivative for gadolinium chelation (Structure shown above)
Die analytische HPLC der Reaktionsmischung in Beispiel 6f) ergab auch einen Peak bei 16,8 min, für das durch LC-MS (EIS)-Analyse gezeigt wurde, dass er dem oben gezeigten DTPA-Bisamid entsprach, was m/z bei 1233 für [MH]+ wie erwartet und 616,6 wie erwartet für [MH2]2+ ergab. Das Produkt wude durch präparative HPLC (Bedingungen wie in Beispiel 6f beschrieben) gereinigt, um 14 mg des reinen Materials nach der Lyophilisierung zu ergeben. Eine Analyse des gereinigten Materials durch analytische HPLC zeigte eine Verschiebung in der Retentionszeit von 16,8 min (in der rohen Mischung) auf 11,1 min aufgrund der Bildung des Eisenkomplexes währed der Reinigung, wie verifiziert durch MALDI-Massenspektrometrie (α-Cyano-4-Hydroxyzimtsäurematrix), was m/z bei 1291 für den Eisenkomplex und 1237 für den freien Ligand ergab.Analytical HPLC of the reaction mixture in Example 6f) also gave a peak at 16.8 min, which was shown by LC-MS (EIS) analysis to be equal to the DTPA-bisamide shown above, m / z at 1233 for [MH] + as expected and yielded 616.6 as expected for [MH 2 ] 2+ . The product was purified by preparative HPLC (conditions as described in Example 6f) to give 14 mg of the pure material after lyophilization. Analysis of the purified material by analytical HPLC showed a shift in retention time from 16.8 minutes (in the crude mixture) to 11.1 minutes due to formation of the iron complex during purification, as verified by MALDI mass spectrometry (α-cyano). 4-hydroxycinnamic acid matrix), giving m / z at 1291 for the iron complex and 1237 for the free ligand.
b) Herstellung des Gadoliniumkomplexes der Verbindung von a)b) Preparation of the Gadolinium Complex the compound of a)
Die Verbindung von a) wurde mit Gadoliniumtrichlorid wie in Beispiel 6g) beschrieben behandelt. Nach 2 Stunden Reaktionszeit zeigte MALDI-Massenspektrometrie eine Umwandlung zu dem Gadoliniumkomplex, was m/z bei 1391 für den Gadoliniumkomplex und 1235 für den freien Ligand ergab.The Compound of a) was treated with gadolinium trichloride as in Example 6g). After 2 hours reaction time showed MALDI mass spectrometry a conversion to the gadolinium complex, which is m / z at 1391 for the gadolinium complex and 1235 for revealed the free ligand.
Beispiel 8Example 8
Carboxymethyl-[2-(carboxymethyl-{2-[carboxymethyl-({2-[3-({3-oxo-2-[2-(pyridin-2-ylamino)-ethyl]-2,3-dihydro-1H-isoindol-5-carbonyl}-amino)propionylamino]-ethylcarbamoyl}-methyl)-amino]-ethyl}-amino)-ethyl]-amino}essigsäure (12) Carboxymethyl- [2- (carboxymethyl {2- [carboxymethyl - ({2- [3 - ({3-oxo-2- [2- (pyridin-2-ylamino) -ethyl] -2,3-dihydro-1 H -isoindole-5-carbonyl} amino) propionylamino] ethylcarbamoyl} methyl) amino] ethyl} amino) ethyl] amino} acetic acid (12)
a) 4-Methylisophthalsäure (2)a) 4-methylisophthalic acid (2)
Zu einer THF (130 ml)-Lösung von 3-Brom-4-methylbenzoesäure (5,0 g, 23,25 mmol) unter Stickstoff und gekühlt auf -78°C (Trockeneis/Methanol) wurde MeMgBr in Ether (3,0 M, 8,5 ml, 25,57 mmol) in einer derartigen Geschwindigkeit gegeben, dass die Temperatur nicht -75°C überschritt. Man ließ die Temperatur dann auf -60°C ansteigen und nachdem die Gasentwicklung aufgehört hatte, wurde die Lösung wieder auf -78°C gekühlt. BuLi in Hexan (1,6 M, 29,06 ml, 46,50 mmol) wurde dann tropfenweise derart zugegeben, dass die Temperatur nicht über -75°C anstieg. Die Mischung wurde dann bei dieser Temperatur 15 Minuten lang gerührt, bevor zerstoßenes Trockeneis (4,4 g, 100 mmol) zugegeben wurde. Das Präzipitat wurde heftig gerührt, während man die Temperatur frei auf Umgebungstemperatur ansteigen ließ. Die Mischung wurde unter Verwendung von 6 N HCl sauer gemacht und das feste Material wurde durch Filtrieren gesammelt, mit Diethylether gewaschen und getrocknet. Die Umkristallisation aus Wasser ergab die cremefarbene reine Verbindung (81 %) Smp. 296-298°C (sublimiert). NMR bestätigt die erwartete Struktur.To a THF (130 ml) solution of 3-bromo-4-methylbenzoic acid (5.0 g, 23.25 mmol) under nitrogen and cooled to -78 ° C (dry ice / methanol) MeMgBr in ether (3.0 M, 8.5 mL, 25.57 mmol) in such Given speed that the temperature did not exceed -75 ° C. They left the Temperature then to -60 ° C increase and after the evolution of gas had ceased, the solution became again cooled to -78 ° C. BuLi in hexane (1.6M, 29.06mL, 46.50mmol) was then added dropwise admitted that the temperature did not rise above -75 ° C. The mixture was then stirred at this temperature for 15 minutes before crushed dry ice (4.4 g, 100 mmol) was added. The precipitate was stirred vigorously while stirring the temperature was allowed to rise freely to ambient temperature. The mixture was acidified using 6N HCl and the solid material was collected by filtration, washed with diethyl ether and dried. Recrystallization from water gave the cream-colored pure compound (81%) mp 296-298 ° C (sublimed). NMR confirms the expected structure.
b) 4-Methylisophthalmethylester (4)b) 4-methylisophthalmethyl ester (4)
Eine Mischung der Verbindung (2) (2,83 g, 15,71 mmol), Thionylchlorid (50 ml) und DMF (3 Tropfen) wurde 2 Stunden lang unter Rückfluss erwärmt. Nach dem Kühlen auf Raumtemperatur wurde überschüssiges Thionylchlorid unter reduziertem Druck (Rotationsverdampfer) entfernt. Das dunkle Öl, das erhalten wurde, wurde in Kohlenstofftetrachlorid (30 ml) aufgelöst, mit Pyridin (1 ml, 12,43 mmol) und Methanol (20 ml) behandelt und bei Umgebungstemperatur 2 Stunden lang gerührt. Die Lösemittel wurden verdampft und der Rückstand wurde durch Flashchromatographie: Silica, Hexan/EtOAc (9:1) gereinigt.A Mixture of compound (2) (2.83 g, 15.71 mmol), thionyl chloride (50 ml) and DMF (3 drops) was refluxed for 2 hours heated. After cooling to room temperature was excess thionyl chloride removed under reduced pressure (rotary evaporator). The dark oil that received was dissolved in carbon tetrachloride (30 ml) Pyridine (1 ml, 12.43 mmol) and methanol (20 ml) and treated at Stirred ambient temperature for 2 hours. The solvents were evaporated and the residue was purified by flash chromatography: silica, hexane / EtOAc (9: 1).
c) 4-Bromethylisophthalsäuredimethylester (5)c) 4-Bromethylisophthalsäuredimethylester (5)
Eine Mischung von (4) (0,96 g, 4,61 mmol), Dibenzoylperoxid (56 mg, 0,23 mmol) und N-Bromsuccinimid (NBS) (0,82 g, 4,61 mmol) in Kohlenstofftetrachlorid (20 ml) wurde 20 Stunden lang unter Rückfluss erwärmt. Nach dem Kühlen auf Raumtemperatur und Filtrieren wurde das Lösemittel verdampft, um ein gelbes Öl zu ergeben. Flashchromatographie: Silica, Hexan/EtOAc (7:3) ergab die reine Verbindung.A Mixture of (4) (0.96 g, 4.61 mmol), dibenzoyl peroxide (56 mg, 0.23 mmol) and N-bromosuccinimide (NBS) (0.82 g, 4.61 mmol) in carbon tetrachloride (20 ml) was heated at reflux for 20 hours. After cooling up Room temperature and filtration, the solvent was evaporated to a yellow oil to surrender. Flash chromatography: silica, hexane / EtOAc (7: 3) the pure connection.
d) 3-Oxo-2-[2-(pyridin-2-ylamino)-ethyl]2,3-dihydro-1H-isoindol-5-carbonsäuremethylester (6)d) Methyl 3-oxo-2- [2- (pyridin-2-ylamino) ethyl] 2,3-dihydro-1H-isoindole-5-carboxylate (6)
Eine Lösung von (5) (511 mg, 1,78 mmol) in Toluol (10 ml) wurde mit Et3N (744 μl, 5,33 mmol) behandelt und N1-Pyridin-2-yl-ethan-1,2-diamin (244 mg, 1,78 mmol) [hergestellt durch Behandlung von 2-Brompyridin mit überschüssigem Ethylendiamin und Pyridin] behandelt und die Mischung wurde 6 Stunden lang unter Rückfluss gekocht. Nach dem Kühlen auf Raumtemperatur und Verdampfen des Lösemittels wurde der Rückstand durch Flashchromatographie: Silica, CH2Cl2/Aceton (3:2) gereinigt.A solution of (5) (511 mg, 1.78 mmol) in toluene (10 mL) was treated with Et 3 N (744 μL, 5.33 mmol) and N, 1-pyridin-2-yl-ethane-1,2 -diamine (244 mg, 1.78 mmol) [prepared by treating 2-bromopyridine with excess ethylenediamine and pyridine] and refluxing the mixture for 6 hours. After cooling to room temperature and evaporation of the solvent, the residue was purified by flash chromatography: silica, CH 2 Cl 2 / acetone (3: 2).
e) 3-Oxo-2-[2-pyridin-2-ylamino)-ethyl]2,3-dihydro-1H-isoindol-5-carbonsäure (7)e) 3-Oxo-2- [2-pyridin-2-ylamino) -ethyl] 2,3-dihydro-1H-isoindole-5-carboxylic acid (7)
Eine Methanollösung (6 ml) von (6) (301 mg, 0,97 mmol) und 1 N NaOH (3 ml) wurde bei Umgebungstemperatur 24 Stunden lang gerührt. Die Lösung wurde unter Verwenden von 1 M NaHSO4-Lösung sauer gemacht und das präzipitierte Produkt wurde durch Filtrieren gesammelt, gründlich mit Wasser gewaschen und über P2O5/Bluegel 24 Stunden lang getrocknet.A methanol solution (6 ml) of (6) (301 mg, 0.97 mmol) and 1 N NaOH (3 ml) was stirred at ambient temperature for 24 hours. The solution was acidified using 1 M NaHSO 4 solution and the precipitated product was collected by filtration, washed thoroughly with water and dried over P 2 O 5 / Bluegel for 24 hours.
f) 3-({3-Oxo-2-[2-(pyridin-2-ylamino)-ethyl]2,3-dihydro-1H-isoindol-5-carbonyl}amino)-propionsäure-tert-butylester (8)f) 3 - ({3-Oxo-2- [2- (pyridin-2-ylamino) ethyl] 2,3-dihydro-1H-isoindole-5-carbonyl} amino) -propionic acid tert-butyl ester (8th)
Eine Lösung von (7) (166 mg, 0,56 mmol), N-Methylmorfolin (185 μl, 1,68 mmol), BOP (322 mg, 0,73 mmol) und H-β-ala-OtBu (152 mg, 0,84 mmol) in DMF (5 ml) wurde bei Umgebungstemperatur 20 Stunden lang gerührt. Die Mischung wurde mit Ethylactet (10 ml) verdünnt und dann jeweils einmal mit H2O, NaHCO3, 10 % KHSO4 und Salzlauge (5 ml) gewaschen, getrocknet (MgSO4) und konzentriert. Flashchromatographie (Silica, EtOAc) ergab das Ester (8) als einen weißen Festkörper.A solution of (7) (166 mg, 0.56 mmol), N-methylmorfolin (185 μl, 1.68 mmol), BOP (322 mg, 0.73 mmol) and H-β-ala-OtBu (152 mg , 0.84 mmol) in DMF (5 ml) was stirred at ambient temperature for 20 hours. The mixture was diluted with ethyl acetate (10 ml) and then washed once each with H 2 O, NaHCO 3 , 10% KHSO 4 and brine (5 ml), dried (MgSO 4 ) and concentrated. Flash chromatography (silica, EtOAc) gave the ester (8) as a white solid.
g) 3-({3-Oxo-2-[2-(pyridin-2-ylamino)-ethyl]2,3-dihydro-1H-isoindol-5-carbonyl}amino)-propionsäure (9)g) 3 - ({3-Oxo-2- [2- (pyridin-2-ylamino) ethyl] 2,3-dihydro-1H-isoindole-5-carbonyl} amino) -propionic acid (9)
Eine Lösung des Esters (8) (252 mg, 0,60 mmol), TFA (4 ml) und CH2Cl2 (8 ml) wurde bei Umgebungstemperatur 3 Stunden lang gerührt. Die Mischung wurde bis zum Trocknen verdampft und der Rückstand durch Flashchromatographie (Silica, EtOH/NH4OH 19:1) gereinigt, um (9) als cremefarbenen Schaum zu ergeben. NMR bestätigt die Struktur.A solution of ester (8) (252 mg, 0.60 mmol), TFA (4 mL) and CH 2 Cl 2 (8 mL) was stirred at ambient temperature for 3 hours. The mixture was evaporated to dryness and the residue was purified by flash chromatography (silica, EtOH / NH 4 OH 19: 1) to give (9) as a cream foam. NMR confirms the structure.
h) {2-[3-({3-Oxo-2-[2-(pyridin-2-ylamino)-ethyl]-2,3-dihydro-1H-isoindol-5-carbonylamino)-propionylaminol-ethyl}-carbaminsäure-tert-butylester (10)h) {2- [3 - ({3-Oxo-2- [2- (pyridin-2-ylamino) ethyl] -2,3-dihydro-1H-isoindole-5-carbonylamino) -propionylaminol-ethyl} - carbamic acid tert-butyl ester (10)
Zu einer Lösung der Säure (9) (20 mg, 0,054 mmol) in DMF (2 ml) wurde N-Methylmorfolin (NMM) (16,40 mg, 0,162 mmol), BOP (Castro's-Reagens) 31,05 mg, 0,070 mmol) und das BOC-geschützte Diamin (13 mg, 0,081 mmol) gegeben und die Mischung wurde bei Umgebungstemperatur 20 Stunden lang gerührt. Nach der Verdünnung mit EtOAc (5 ml) wurde die Lösung einmal jeweils mit H2O, gesätt. NaHCO3, 10 % KHSO4 und Salzlauge gewaschen. Die organische Phase wurde getrocknet (MgSO4) und konzentriert. Flashchromatographie (Silica, 1:1 CH2Cl2/Aceton). MALDI-MS; 510,59.To a solution of the acid (9) (20 mg, 0.054 mmol) in DMF (2 mL) was N-methylmorfolin (NMM) (16.40 mg, 0.162 mmol), BOP (Castro's reagent) 31.05 mg, 0.070 mmol) and the BOC-protected diamine (13 mg, 0.081 mmol) and the mixture was stirred at ambient temperature for 20 hours. After dilution with EtOAc (5 ml), the solution was washed once with H 2 O, sat. NaHCO 3 , 10% KHSO 4 and brine. The organic phase was dried (MgSO 4 ) and concentrated. Flash chromatography (silica, 1: 1 CH 2 Cl 2 / acetone). MALDI-MS; 510.59.
i) 3-Oxo-2-[2-(pyridin-2-ylamino)-ethyl]-2,3-dihydro-1H-isoindol-5-carbonsäure[2-(2-aminoethylcarbamoyl)-ethyl]-amid (11)i) 3-Oxo-2- [2- (pyridin-2-ylamino) -ethyl] -2,3-dihydro-1H-isoindole-5-carboxylic acid [2- (2-aminoethylcarbamoyl) -ethyl] -amide (11)
Eine CH2Cl2-Lösung (3 ml) von (10) (20 mg, 0,039 mmol) und TFA (2 ml) wurde unter Umgebungsbedingungen 4 Stunden lang gerührt. Die Reaktionsmischung wurde konzentriert und der Rückstand durch Flashchromatographie (Silica, 19:1, CH2Cl2/Aceton) gereinigt, um (4) als einen weißen Feststoff zu ergeben. MALDI-MS; 410,48.A CH 2 Cl 2 solution (3 mL) of (10) (20 mg, 0.039 mmol) and TFA (2 mL) was stirred under ambient conditions for 4 hours. The reaction mixture was concentrated and the residue was purified by flash chromatography (silica, 19: 1, CH 2 Cl 2 / acetone) to give (4) as a white solid. MALDI-MS; 410.48.
j) Carboxymethyl-[2-(carboxymethyl-{2-[carboxymethyl-f{2-[3-[{3-oxo-2-[2-[pyridin-2-ylamino)-ethyl]-2,3-dihydro-1H-isoindol-5-carbonyl}-amino)-propionylaminolethylcarbamoyl}-methyl)-amino]-ethyl}-amino)-ethyl]-amino}-essigsäure (12)j) Carboxymethyl [2- (carboxymethyl) {2- [carboxymethyl-f {2- [3 - [{3-oxo-2- [2- [pyridin-2-ylamino) ethyl] -2,3-dihydro -1H-isoindole-5-carbonyl} -amino) -propionylaminolethylcarbamoyl} -methyl) -amino] -ethyl} -amino) -ethyl] -amino} -acetic acid (12)
Eine Lösung von (11) (15 mg, 0,36 mmol), N,N-Diisopropylamin (17 μl, 0,10 mmol) und DTPA-Anhydrid (129 mg„ 0,36 mmol) in DMF (2 ml) wurde bei Umgebungstemperatur 3 Stunden lang gerührt und in vacuo konzentriert. Der Rückstand wurde durch präparative HPLC (Acetonitril/0,1 % TFA in Wasser) gereinigt.A solution of (11) (15 mg, 0.36 mmol), N, N-diisopropylamine (17 μl, 0.10 mmol) and DTPA anhydride (129 mg "0.36 mmol) in DMF (2 ml) at ambient temperature for 3 hours touched and concentrated in vacuo. The residue was by preparative HPLC (acetonitrile / 0.1% TFA in water).
Beispiel 9Example 9
Herstellung eines DTPA-Monoamidgadoliniumkomplexes umfassend einen Vektor zum Targeting eines bFGF-Rezeptors für die MR-Erfassung von Angiogenese Preparation of a DTPA monoamide gadolinium complex comprising a vector for targeting a bFGF receptor for MR detection of angiogenesis
a) Synthese von: {3-[2-(4-Chlorbenzyloxy)-2-(2,4-dichlorphenyl)-ethyl]-3H-imidazol-1-yl}-essigsäure-tert-butylestera) Synthesis of tert-butyl {3- [2- (4-chlorobenzyloxy) -2- (2,4-dichlorophenyl) ethyl] -3H-imidazol-1-yl} acetic acid
1-[2-(4-Chlorbenzyloxy)-2-(2,4-dichlorphenyl)-ethyl]-1H-imidazol (1 g, 2,25 mmol) und tert-Butylbromacetat (1 ml, 6,8 mmol) wurden in 15 ml Acetonitril aufgelöst und über Nacht unter Rückfluss erwärmt. TLC zeigte eine volle Umwandlung des Ausgangsmaterials. Das Lösemittel wurde gekühlt, in vacuo verdampft und das Rückstandsöl wurde in Chloroform aufgelöst und mit Ether verrieben. Das Produkt wurde durch MALDI-Massenspektrometrie identifiziert und in dem nächsten Schritt ohne weitere Reinigung verwendet.1- [2- (4-chlorobenzyloxy) -2- (2,4-dichlorophenyl) -ethyl] -1H-imidazole (1g, 2.25mmol) and tert -butyl bromoacetate (1mL, 6.8mmol) dissolved in 15 ml of acetonitrile and over Night under reflux heated. TLC showed a full conversion of the starting material. The solvent was cooled, evaporated in vacuo and the residual oil was dissolved in chloroform and triturated with ether. The product was analyzed by MALDI mass spectrometry identified and in the next Step used without further purification.
b) Synthese von: {3-[2-(4-Chlorbenzyloxy)-2-(2,4-dichlorphenyl)-ethyl]-3H-imidazol-1-yl}-essigsäureb) Synthesis of: {3- [2- (4-Chlorobenzyloxy) -2- (2,4-dichlorophenyl) ethyl] -3H-imidazol-1-yl} acetic acid
Die Verbindung von a) (500 mg, 1 mmol) wurde in 2 ml Dichlormethan aufgelöst und in einem Eisbad gekühlt. 2 ml Trifluoressigsäure wurde zugegeben, das Eisbad wurde entfernt und die Reaktionsmischung wurde 1 Stunde lang gerührt. TLC zeigte eine volle Umwandlung des Ausgangsmaterials. Das Lösemittel wurde in vacuo entfernt und das Produkt im nächsten Schritt ohne weitere Reinigung verwendet.The Compound of a) (500 mg, 1 mmol) was dissolved in 2 ml of dichloromethane and dissolved in cooled in an ice bath. 2 ml of trifluoroacetic acid was added, the ice bath was removed and the reaction mixture was stirred for 1 hour. TLC showed a full conversion of the starting material. The solvent was removed in vacuo and the product in the next step without further Cleaning used.
c) Synthese von: [6-(2-{3-[2-(4-Chlorbenzyloxy)-2-(2,4-dichlorphenyl)-ethyl]-3H-imidazol-1-yl}-acetylamino)-hexyl]-carbaminsäure-tert-butylesterc) Synthesis of: [6- (2- {3- [2- (4-Chlorobenzyloxy) -2- (2,4-dichlorophenyl) ethyl] -3 H -imidazol-1-yl} -acetylamino) -hexyl] -carbamic acid tert-butyl ester
Das Produkt von b) wurde zu c) durch die für Beispiel 6d) beschriebene Prozedur umgewandelt, und das Produkt wurde durch Flashchromatographie gereinigt.The Product of b) became c) by that described for Example 6d) Procedure was converted, and the product was purified by flash chromatography cleaned.
d) Synthese von: N-(6-Aminohexyl)-2-{3-[2-(4-chlorbenzyloxy)-2-(2,4-dichlorphenyl)ethyl]-3H-imidazol-1-yl}-acetamidd) Synthesis of: N- (6-aminohexyl) -2- {3- [2- (4-chlorobenzyloxy) -2- (2,4-dichlorophenyl) ethyl] -3H-imidazol-1-yl} -acetamide
Das Produkt von c) wurde zu d) durch die für Beispiel 6e) beschriebene Prozedur umgewandelt. Das Produkt wurde ohne weitere Reinigung verwendet.The Product of c) became d) by that described for example 6e) Procedure converted. The product was used without further purification.
e) Synthese von: ((2-{[2-(Bis-carboxymethvlamino)-ethyl]-carboxymethylamino}ethyl)-{[6-(2-{3-[2-(4-chlorbenzyloxy)-2-(2,4-dichlorphenyl)-ethyl]-3H-imidazol-1-yl}acetylamino)-hexylcarbamoyl]-methyl}-amino)-essigsäuree) Synthesis of: ((2 - {[2- (Bis-carboxymethylamino) -ethyl] -carboxymethylamino} ethyl) - {[6- (2- {3- [2- (4-chlorobenzyloxy) -2- (2 , 4-dichlorophenyl) -ethyl] -3H-imidazol-1-yl} acetylamino) -hexylcarbamoyl] -methyl} -amino) -acetic acid
Das Produkt von d) wurde zu e) durch die für Beispiel 6f) beschriebene Prozedur umgewandelt. Eine Reinigung wurde durch präparative HPLC wie in Beispiel 6f) beschrieben ausgeführt.
- f) Die Herstellung des Gadoliniumkomplexes der Verbindung e) wurde durch die in Beispiel 6g) beschriebene Prozedur ausgeführt.
- f) The preparation of the gadolinium complex of compound e) was carried out by the procedure described in Example 6g).
LITERATURSTELLEN, ZITIERT IN DER BESCHREIBUNGLITERATURE STATIONS, QUOTED IN DESCRIPTION
Diese Liste von Literaturstellen, die vom Anmelder zitiert sind, ist nur als Annehmlichkeit für den Leser gedacht. Sie bildet nicht Teil der europäischen Patentschrift. Sogar obwohl große Sorgfalt unternommen wurde, die Literaturstellen zusammenzustellen, können Irrtümer oder Unterlassungen nicht ausgeschlossen werden, und das EPA erkennt keinerlei Haftung in dieser Hinsicht an.These List of references cited by the Applicant is only as a convenience for thought the reader. It does not form part of the European patent specification. Even though big Care has been taken to compile the references, can errors or omissions are not excluded, and the EPO recognizes no liability in this regard.
Patent-Dokumente, zitiert in der BeschreibungPatent documents cited in the description
-
•
WO 9526364 A WO 9526364 A -
•
WO 9630046 A WO 9630046 A -
•
WO 9512414 A WO 95/1414 A -
•
GB 9702958 W GB 9702958 W -
•
WO 9417084 A WO 9417084 A -
•
EP 618208 A EP 618208 A -
•
WO 9413277 A WO 9413277 A -
•
WO 9506473 A WO 9506473 A -
•
WO 9421612 A WO 9421612 A -
•
WO 9737655 A WO 9737655 A -
•
WO 9730035 A WO 9730035 A -
•
EP 678296 A EP 678296 A -
•
WO 9418967 A WO 9418967 A -
•
WO 9508327 A WO 9508327 A -
•
US 4590201 A US 4590201 A -
•
EP 652000 A EP 652000 A -
•
WO 9402446 A WO 9402446 A -
•
WO 9402447 A WO 9402447 A -
•
WO 9421625 A WO 9421625 A -
•
WO 9424140 A WO 9424140 A -
•
WO 9504033 A WO 9504033 A -
•
EP 589719 A EP 589719 A -
•
US 5399667 A US 5399667 A -
•
EP 241830 A EP 241830 A -
•
WO 9738009 A WO 9738009 A -
•
WO 9424149 A WO 9424149 A -
•
EP 422937 A EP 422937 A -
•
EP 422938 A EP 422938 A -
•
GB 9700699 A GB 9700699 A -
•
WO 9217436 A WO 9217436 A -
•
US 4421847 A US 4421847 A -
•
US 4877724 A US 4877724 A -
•
US 5364613 A US 5364613 A -
•
EP 9000565 W EP 9000565 W -
•
WO 9306868 A WO 9306868 A -
•
WO 9408629 A WO 9408629 A -
•
WO 9409056 A WO 9409056 A -
•
WO 9626754 A WO 9626754 A -
•
US 5367080 A US 5367080 A -
•
US 4647447 A US 4647447 A -
•
EP 71564 A EP 71564 A -
•
US 4687659 A US 4687659 A -
•
WO 8900557 A WO 8900557 A -
•
US 4885363 A US 4885363 A -
•
EP 232751 A EP 232751 A -
•
GB 9700067 W GB 9700067 W -
•
US 4863715 A US 4863715 A -
•
US 4770183 A US 4770183 A -
•
WO 9609840 A WO 9609840 A -
•
WO 8502772 A WO 8502772 A -
•
WO 9217212 A WO 9217212 A -
•
GB 9700459 W GB 9700459 W -
•
EP 554213 A EP 554213 A -
•
US 5228446 A US 5228446 A -
•
WO 9115243 A WO 9115243 A -
•
WO 9305818 A WO 9305818 A -
•
WO 9623524 A WO 9623524 A -
•
WO 9617628 A WO 9617628 A -
•
US 5387080 A US 5387080 A -
•
WO 9526205 A WO 9526205 A -
•
GB 9624918 A GB 9624918 A -
•
WO 9114460 A WO 9114460 A -
•
WO 9217215 A WO 9217215 A -
•
WO 9640287 A WO 9640287 A -
•
WO 9622914 A WO 96/2914 A -
•
US 5078985 A US 5078985 A -
•
US 4444690 A US 4444690 A -
•
US 4670545 A US 4670545 A -
•
US 4673562 A US 4673562 A -
•
US 4897255 A US 4897255 A -
•
US 4965392 A US 4965392 A -
•
US 4980417 A US 4980417 A -
•
US 4988496 A US 4988496 A -
•
US 5021556 A US 5021556 A -
•
US 5075099 A US 5075099 A -
•
US 9108253 W US 9108253 W -
•
US 5559214 A US 5559214 A -
•
WO 9526754 A WO 9526754 A -
•
WO 9408624 A WO 9408624 A -
•
WO 9429333 A WO 94/23333 A -
•
WO 9408629 A1 WO 9408629 A1 -
•
WO 9413327 A1 WO 9413327 A1 -
•
WO 9412216 A1 WO 9412216 A1 -
•
WO 9620754 A WO 9620754 A -
•
WO 9528966 A WO 9528966 A -
•
EP 9600565 W EP 9600565 W -
•
GB 9502378 A GB 9502378 A -
•
DE 4445065 A DE 4445065 A -
•
DE 4326466 A DE 4326466 A -
•
JP 3228046 A JP 3228046 A -
•
WO 9623525 A WO 9623525 A -
•
US 3806462 A US Pat. No. 3,804,662 A -
•
JP 62039682 A JP 62039682 A -
•
JP 63126889 A JP 63126889 A -
•
JP 63139303 A JP 63139303 A -
•
JP 61020002 A JP 61020002 A -
•
JP 61073902 A JP 61073902 A -
•
US 5318767 US 5318767 -
•
US 5451393 A US 5451393 A -
•
US 5352459 A US 5352459 A -
•
US 5569448 A US 5569448 A -
•
GB 9622368 A GB 9622368 A -
•
EP 284549 A EP 284549 A -
•
US 4904479 A US 4904479 A -
•
WO 94024470 A WO 94024470 A
Nicht-Patent-Literatur, zitiert in der BeschreibungNon-patent literature cited in the description
- • KOHN et al. Proc. Nat. Acad. Sci. USA, 1995 Band 92, 1307-1311 [0024]• KOHN et al. Proc. Nat. Acad. Sci. USA, 1995 Vol. 92, 1307-1311 [0024]
- • J. CIin. Oncol, 1997, Band 15, 1985-1993 [0024]• J. CIin. Oncol, 1997, Vol. 15, 1985-1993 [0024]
- • VERA et al. Radiology, 1984, Band 151, 191 [0046]• VERA et al. Radiology, 1984, Vol. 151, 191 [0046]
- • DUNCAN et al. Biochim. Biophys. Acta, 1986, Band 880, 62 [0046]• DUNCAN et al. Biochim. Biophys. Acta, 1986, Vol. 880, 62 [0046]
- • WONG et al. Carbo. Res., 1987, Band 170, 27 [0046]• WONG et al. Carbo. Res., 1987, Vol. 170, 27 [0046]
- • OLEXA et al. J. Biol. Chem., 1979, Band 254, 4926 [0046]• OLEXA et al. J. Biol. Chem., 1979, Vol. 254, 4926 [0046]
- • DE BEER et al. J. Immunol. Methods, 1982, Band 50, 17 [0046]• DE BEER et al. J. Immunol. Methods, 1982, Vol. 50, 17 [0046]
- • GURD, F.R.N. Methods Enzymol., 1967, Band 11, 532 [0054]• GURD, F.R.N. Methods Enzymol., 1967, Vol. 11, 532 [0054]
- • TRAUT, R et al. Biochemistry, 1973, Band 12, 3266 [0054]• TRAUT, R et al. Biochemistry, 1973, Vol. 12, 3266 [0054]
- • KIMURA, T et al. Analyt. Biochem., 1982, Band 122, 271 [0054]• KIMURA, T et al. Analyte. Biochem., 1982, Vol. 122, 271 [0054]
- • WONG, Y-H.H. Biochemistry, 1979, Band 4, 5337 [0055]• WONG, Y-H.H. Biochemistry, 1979, Vol. 4, 5337 [0055]
- • SMYTH, D.G. et al. J. Am. Chem. Soc., 1960, Band 82, 4600 [0055]• SMYTH, D. G. et al. J. Am. Chem. Soc., 1960, Vol. 82, 4600 [0055]
- • Biochem. J., 1964, Band 91, 589 [0055]• Biochem. J., 1964, Vol. 91, 589 [0055]
- • MCKENZIE, J.A et al. J. Protein Chem, 1988, Band 7, 581 [0055]• MCKENZIA, J.A. et al. J. Protein Chem, 1988, Vol. 7, 581 [0055]
- • TIETZE, L.F. Chem. Ber., 1991, Band 124, 1215 [0055]• TIES, L. F. Chem. Ber., 1991, Vol. 124, 1215 [0055]
- • BENNECHE, T et al. Eur. J. Med. Chem., 1993, Band 28, 463 [0055]• BENNECHE, T et al. Eur. J. Med. Chem., 1993, Vol. 28, 463 [0055]
- • SCHICK, A.F. et al. J. Bio. Chem., 1961, Band 236, 2477 [0056]• FANCY, A. F. et al. J. Bio. Chem., 1961, Vol. 236, 2477 [0056]
- • HERZIG, D.J. et al. Biopolymers, 1964, Band 2, 349 [0056]• HEARTY, D.J. et al. Biopolymers, 1964, Volume 2, 349 [0056]
- • BODANSKY, M et al. Principles of Peptide Synthesis. Springer-Verlag, 1984 [0056]• BODANSKY, M et al. Principles of Peptide Synthesis. Springer-Verlag, 1984 [0056]
- • WETZ, K et al. Anal. Biochem., 1974, Band 58, 347 [0056]• WETZ, K et al. Anal. Biochem., 1974, Vol. 58, 347 [0056]
- • RASMUSSEN, J.K. Reactive Polymers, 1991, Band 16, 199 [0056]• RASMUSSEN, J.K. Reactive Polymers, 1991, Vol. 16, 199 [0056]
- • HUNTER, M.J.; LUDWIG, M.L. J. Am. Chem. Soc., 1962, Band 84, 3491 [0056]• HUNTER, M.J. .; LUDWIG, M.L. J. Am. Chem. Soc., 1962, Vol. 84, 3491 [0056]
- • RATNER, S. et al. J. Am. Chem. Soc., 1937, Band 59, 200 [0057]• RATNER, S. et al. J. Am. Chem. Soc., 1937, Vol. 59, 200 [0057]
- • HEITZMAN, H et al. Proc. Natl. Acad. Sci. USA, 1974, Band 71, 3537 [0057]• HEITZMAN, H et al. Proc. Natl. Acad. Sci. USA, 1974, Volume 71, 3537 [0057]
- • WEBB, R et al. Bioconjugate Chem, 1990, Band 1, 96 [0058]• WEBB, R et al. Bioconjugate Chem, 1990, Vol. 1, 96 [0058]
- • HERRIOT R.M. Adv. Protein Chem, 1947, Band 3, 169 [0059]• HERRIOT R.M. Adv. Protein Chem, 1947, Vol. 3, 169 [0059]
- • ZOT, H.G.; PUETT, D.J. Biol. Chem., 1989, Band 264, 15552 [0059]• ZOT, h.g .; PUETT, D.J. Biol. Chem., 1989, Vol. 264, 15552 [0059]
- • WAGNER et al. Nuceic acid Res., 1978, Band 5, 4065 [0060]• WAGNER et al. Nuceic acid Res., 1978, Vol. 5, 4065 [0060]
- • ISHIZAKA, K; ISHIZAKA T. J. Immunol., 1960, Band 85, 163 [0060]• ISHIZAKA, K; ISHIZAKA T.J. Immunol., 1960, Vol. 85, 163 [0060]
- • LEENHOUTS, J.M et al. Febs Letters, 1995, Band 370 (3), 189-192 [0063]• LEENHOUTS, J.M et al. Febs Letters, 1995, Vol. 370 (3), 189-192 [0063]
- • BAYER, E.A; WILCHEK, M. Methods Biochem. Anal, 1980, Band 26 (1 [0064]• BAYER, E.A; WILCHEK, M. Methods Biochem. Anal, 1980, Vol. 26 (1) [0064]
- • BODE, C et al. J. Biol. Chem., 1989, Band 264, 944 [0065]• BODE, C et al. J. Biol. Chem., 1989, Vol. 264, 944 [0065]
- • STAERZ, U.D et al. Proc. Natl. Acad. Sci. USA, 1986, Band 83, 1453 [0065]• STAERZ, U.D et al. Proc. Natl. Acad. Sci. USA, 1986, Volume 83, 1453 [0065]
- • CHEN, AA et al. Am. J. Pathol, 1988, Band 130, 216 [0065]• CHEN, AA et al. At the. J. Pathol, 1988, Vol. 130, 216 [0065]
- • Poly(ethylen glycol) chemistry, biotechnical and biomedical applications. Plenum Press, 1992 [0069]• poly (ethylene glycol) chemistry, biotechnical and biomedical applications. plenum Press, 1992 [0069]
- • KLIBANOV, A.L. et al. FEBS Letters, 1990, Band 268, 235-237 [0071]• KLIBANOV, A.L. et al. FEBS Letters, 1990, Vol. 268, 235-237 [0071]
- • BLUME, G; CEVC, G. Biochim. Biophys. Acata, 1990, Band 1029, 91-97 [0071]• FLOWER, G; CEVC, G. Biochim. Biophys. Acata, 1990, Vol. 1029, 91-97 [0071]
- • MARUYAMA, K et al. Biochim. Biophys. Acta, 1995, Band 1234, 74-80 [0071]• MARUYAMA, K et al. Biochim. Biophys. Acta, 1995, Vol. 1234, 74-80 [0071]
- • HANSEN, C.B et al. Biochim. Biophys, Acta, 1995, Band 1239, 133-144 [0071]• HANSEN, C.B et al. Biochim. Biophys, Acta, 1995, Vol. 1239, 133-144 [0071]
- • VOLFOVÁ, I; RÍHOVÁ, B; V.R. AND VETVICKA, P. J. Bioact. Comp. Polymers, 1992, Band 7, 175-190 [0074]• VOLFOVA, I; RÍHOVÁ, B; V.R. AND VETVICKA, P.J. Bioact. Comp. Polymers, 1992, Vol. 7, 175-190 [0074]
- • GODDARD, P; WILLIAMSON, I; BRON, J; HUTCHKINSON, L.E; NICHOLLS, J; PETRAK, K. J. Bioct. Compat. Polym, 1991, Band 6, 4-24 [0074]• GODDARD, P; WILLIAMSON, I; BRON, J; HUTCHKINSON, L.E .; NICHOLLS, J; Petrak, K.J. Bioct. Compat. Polym, 1991, Vol. 6, 4-24 [0074]
- • LEE, P.I. Pharm res., 1993, Band 10, 980 [0075]• LEE, PI. Pharmres., 1993, Vol. 10, 980 [0075]
- • SAN ROMAN, J; GUILLEN-GARCIA, P. Biomaterials, 1991, Band 12, 236-241 [0075]• SAN ROMAN, J; GUILLEN-GARCIA, P. Biomaterials, 1991, Vol. 12, 236-241 [0075]
- • FORRESTIER, F; GERRIER, P; CHAUMARD, C; QUERO, A.M; COUVREUR, P; LABARRE, C. J. Antimicrob. Chemoter, 1992, Band 30, 173-179 [0075]• FOREST, F; GERRIER, P; CHAUMARD, C; QUERO, A.M .; COUVREUR, P; Labarre, C. J. Antimicrob. Chemoter, 1992, Vol. 30, 173-179 [0075]
- • LANGER, R. J. Control. Release, 1991, Band 16, 53-60 [0075]• LONGER, R.J. Control. Release, 1991, Vol. 16, 53-60 [0075]
- • FINNE, U; HANNUS, M; URITTI, A Int. J. Pharm, 1992, Band 78, 237-24 [0075]• FIN, U; HANNUS, M; URITTI, A Int. J. Pharm, 1992, Vol. 78, 237-24 [0075]
- • HESPE, W; MEIER, A.M; BLANKWATER, Y.M. Arzeim-Forsch./Drug Res, 1977, Band 27, 1158-1162 [0075]• HESPE, W; MEIER, A.M .; BLANKWATER, Y.M. Arzeim Research / Drug Res, 1977, vol 27, 1158-1162 [0075]
- • CARLI, F. Chim. Indm 1993, Band 75, 494-9 [0075]• CARLI, F. Chim. Indm 1993, Vol. 75, 494-9 [0075]
- • IMASAKI, K; YOSHIDA, M; FUKUZAKI, H; ASANO, M; KUMAKURA, M; MASHIMO, T; YAMANAKA, H; NAGAI.T. Int. J. Pharm, 1992, Band 81, 31-38 [0075]• IMASAKI, K; YOSHIDA, M; FUKUZAKI, H; ASANO, M; KUMAKURA, M; MASHIMO, T; YAMANAKA, H; NAGAI.T. Int. J. Pharm, 1992, Vol. 81, 31-38 [0075]
- • YOUNES, H; NATAF, P.R; COHN, D; APPELBAUM, Y.J; PIZOV, G; URETZKY, G. Biomater. Artif. Cells Artif. Organs, 1988, Band 16, 705-719 [0075]• YOUNES, H; NATAF, P.R .; COHN, D; APPELBAUM, Y.J; PIZOV, G; URETZKY, G. Biomater. Artif. Cells Artif. Organs, 1988, Vol. 16, 705-719 [0075]
- • KOBAYASHI, H; HYON, S.H.; IKADA, Y. Water-curable and biodegradable prepolymers. J. Biomed. Mater. Res, 1991, Band 25, 1481-1494 [0075]• KOBAYASHI, H; HYON, S.H .; IKADA, Y. Water-curable and biodegradable prepolymers. J. Biomed. Mater. Res, 1991, Vol. 25, 1481-1494 [0075]
- • RATNER, B.D; JOHNSTON, A.B; LENK, T.J. J. Biomed. Mater. Res: Applied Biomaterials, 1987, Band 21, 59-90 [0075]• RATNER, b, d; JOHNSTON, A.B .; LENK, T.J. J. Biomed. Mater. Res: Applied Biomaterials, 1987, Vol. 21, 59-90 [0075]
- • SA DA COSTA, V et al. J. Coll. Interface Sci, 1981, Band 80, 445-452 [0075]• SA DA COSTA, V et al. J. Coll. Interface Sci, 1981, Vol. 80, 445-452 [0075]
- • AFFROSSMAN, S et al. Clinical Materials, 1991, Band 8, 25-31 [0075]• AFFROSSMAN, S et al. Clinical Materials, 1991, Vol. 8, 25-31 [0075]
- • SONG, C.X; CUI, X.M; SCHINDLER, A. Med. Biol. Eng. Comput, 1993, Band 31, 147-150 [0075]• SONG, C.X; CUI, X.M; SCHINDLER, A. Med. Biol. Eng. Comput, 1993, volume 31, 147-150 [0075]
- • Agricultural and synthetic polymers: Biodergradability and utilization. BEZWADA, R.S.; SHALABY, S.W; NEWMAN, H.D.J ACS symposium Series. American Chemical Society, 1990 [0075]• Agricultural and synthetic polymers: Biodegradability and utilization. Bezwada, R, S .; SHALABY, S.W .; NEWMAN, H.D.J ACS Symposium Series. American Chemical Society, 1990 [0075]
- • BREM, H; KADER, A; EPSTEIN, J.I.; TAMARGO, R.J; DOMB, A; LANGER, R; LEONG, K.W Sel. Cancer Ther., 1989, Band 5, 55-65 [0075]• BREM, H; KADER, A; EPSTEIN, J.I .; TAMARGO, R.J .; DOMB, A; LANGER, R; LEONG, K.W Sel. Cancer Ther., 1989, Vol. 5, 55-65 [0075]
- • TAMARGO, R.J; EPSTEIN, J.I; REINHARD, C.S; CHASIN, M; BREM, H. Biomed. Mater. Res. 1989, Band 23, 253-266 [0075]• TAMARGO, R. J; EPSTEIN, J.I; REINHARD, C.S. CHASINE, M; BREM, H. Biomed. Mater. Res. 1989, Vol. 23, 253-266 [0075]
- • MAA, Y.F.; HELLER, J. J. Control. Release, 1990, Band 14, 21-28 [0075]• MAA, Y.F .; HELLER, J.J. Control. Release, 1990, Vol. 14, 21-28 [0075]
- • CROMMEN, J.H; VANDORPE, J.; SCHACHT, E.H. J. Control.Release, 1993 Band 24, 167-180 [0075]• CROMMEN, J.H; VANDORPE, J .; SCHACHT, E.H. J. Control. Release, 1993 Volume 24, 167-180 [0075]
- • TOMALIA et al. Angew. Chem. Int. Engl., 1990, Band 29, 138-175 [0105]• TOMALIA et al. Angew. Chem. Int. Engl., 1990, Vol. 29, 138-175 [0105]
- • OHMONO et al. J. med. Chem., 1992, Band 35, 157-162 [0106]• OHMONO et al. J. med. Chem., 1992, Vol. 35, 157-162 [0106]
- • KUNG et al. J. Nucl. Med., 1984, Band 25, 326-332 [0106]• KUNG et al. J. Nucl. Med., 1984, Vol. 25, 326-332 [0106]
- • JURISSON et al. Chem. Rev., 1993, Band 93, 1137-1156 [0106]• JURISSON et al. Chem. Rev., 1993, vol. 93, 1137-1156 [0106]
- • MEARES et al. JACS, 1988, Band 110, 6266-6267 [0134]• MEARES et al. JACS, 1988, Vol. 110, 6266-6267 [0134]
- • Topics in Applied Chemistry: Infrared absorbing dyes. Topics in Applied Chemistry: The Chemistry and Application of Dyes. Plenum, 1990 [0142]• Topics in Applied Chemistry: Infrared absorbing dyes. Topics in Applied Chemistry: The Chemistry and Application of Dyes. Plenum, 1990 [0142]
- • WARING et al. Handbook of Fluorescent Probes and Research Chemicals. Molecular Probes Inc, 1990 [0142]• WARING et al. Handbook of Fluorescent Probes and Research Chemicals. Molecular Probes Inc, 1990 [0142]
- • NARAYANAN et al. J. Org. Chem., 1995, Band 60, 2391-2395 [0142]• NARAYANAN et al. J. Org. Chem., 1995, Vol. 60, 2391-2395 [0142]
- • LIPOWSKA et al. Heterocyclic Comm, 1995, Band 1, 427-430 [0142]• LIPOWSKA et al. Heterocyclic Comm, 1995, Vol. 1, 427-430 [0142]
- • FABIAN et al. Chem. Rev., 1992, Band 92, 1197 [0142]• FABIAN et al. Chem. Rev., 1992, Vol. 92, 1197 [0142]
- • STREKOWSKA et al. J. Org. Chem., 1992, Band 57, 4578-4580 [0142]• STREKOWSKA et al. J. Org. Chem., 1992, Vol. 57, 4578-4580 [0142]
- • The Chemistry and Application of Dyes. WARING, D.R; HALLAS, G. Topics in Applied Chemistry. Plenum Press, 1990 [0146]• The Chemistry and Application of Dyes. WARING, D.R .; HALLAS, G. Topics in Applied Chemistry. Plenary Press, 1990 [0146]
- • HAUGLAND, R.P. Handbook of Fluorescent Probes and Research Chemicals. Molecular Probes, Inc, 1996 [0146]• HAUGLAND, R.P. Handbook of Fluorescent Probes and Research Chemicals. Molecular Probes, Inc, 1996 [0146]
- • Remington's Pharmaceutical Sciences. Mack Publishing Co, 1975 [0161]• Remington's Pharmaceutical Sciences. Mack Publishing Co., 1975 [0161]
Claims (10)
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GBGB9708265.5A GB9708265D0 (en) | 1997-04-24 | 1997-04-24 | Contrast agents |
| GB9708265 | 1997-04-24 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| DE69837975D1 DE69837975D1 (en) | 2007-08-02 |
| DE69837975T2 true DE69837975T2 (en) | 2008-02-28 |
Family
ID=10811256
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE69837975T Expired - Lifetime DE69837975T2 (en) | 1997-04-24 | 1998-04-24 | Diagnostic imaging method |
| DE69824842T Expired - Lifetime DE69824842T2 (en) | 1997-04-24 | 1998-04-24 | CONTRASTING AGENTS AIMING AT ANGIOGENESIS RECEPTORS |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE69824842T Expired - Lifetime DE69824842T2 (en) | 1997-04-24 | 1998-04-24 | CONTRASTING AGENTS AIMING AT ANGIOGENESIS RECEPTORS |
Country Status (10)
| Country | Link |
|---|---|
| US (2) | US6610269B1 (en) |
| EP (2) | EP0977600B1 (en) |
| JP (1) | JP4993419B2 (en) |
| AT (2) | ATE270116T1 (en) |
| AU (1) | AU7068798A (en) |
| DE (2) | DE69837975T2 (en) |
| DK (1) | DK1442751T3 (en) |
| ES (2) | ES2287599T3 (en) |
| GB (1) | GB9708265D0 (en) |
| WO (1) | WO1998047541A1 (en) |
Families Citing this family (110)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB9708265D0 (en) * | 1997-04-24 | 1997-06-18 | Nycomed Imaging As | Contrast agents |
| US6245318B1 (en) | 1997-05-27 | 2001-06-12 | Mallinckrodt Inc. | Selectively binding ultrasound contrast agents |
| JP4487019B2 (en) | 1998-03-31 | 2010-06-23 | ランサス メディカル イメージング インコーポレイテッド | Drugs for imaging angiogenic diseases |
| US6537520B1 (en) | 1998-03-31 | 2003-03-25 | Bristol-Myers Squibb Pharma Company | Pharmaceuticals for the imaging of angiogenic disorders |
| US6524553B2 (en) | 1998-03-31 | 2003-02-25 | Bristol-Myers Squibb Pharma Company | Quinolone vitronectin receptor antagonist pharmaceuticals |
| US6548663B1 (en) | 1998-03-31 | 2003-04-15 | Bristol-Myers Squibb Pharma Company | Benzodiazepine vitronectin receptor antagonist pharmaceuticals |
| DE19845798A1 (en) * | 1998-09-29 | 2000-04-13 | Schering Ag | Use of neoangiogenesis markers for diagnosis and therapy of tumors, agents containing them, and methods for their production |
| US6299860B1 (en) | 1998-10-15 | 2001-10-09 | Fluoro Probe, Inc. | Method for viewing diseased tissue located within a body cavity |
| US6652836B2 (en) | 1998-10-15 | 2003-11-25 | Fluoroprobe, Inc. | Method for viewing tumor tissue located within a body cavity |
| US6284223B1 (en) | 1998-10-15 | 2001-09-04 | Fluoroprobe, Inc. | Method for viewing tumor tissue located within a body cavity |
| US6569402B1 (en) | 1998-12-18 | 2003-05-27 | Bristol-Myers Squibb Pharma Company | Vitronectin receptor antagonist pharmaceuticals |
| US6794518B1 (en) | 1998-12-18 | 2004-09-21 | Bristol-Myers Squibb Pharma Company | Vitronectin receptor antagonist pharmaceuticals |
| JP2002532440A (en) | 1998-12-18 | 2002-10-02 | デュポン ファーマシューティカルズ カンパニー | Vitronectin receptor antagonist drug |
| TR200101757T2 (en) | 1998-12-18 | 2001-12-21 | Dupont Pharmaceuticais Company | Vitronectin receptor antagonist pharmaceuticals |
| US6511649B1 (en) | 1998-12-18 | 2003-01-28 | Thomas D. Harris | Vitronectin receptor antagonist pharmaceuticals |
| CA2356532A1 (en) | 1999-01-15 | 2000-07-20 | Light Sciences Corporation | Noninvasive vascular therapy |
| US6454789B1 (en) | 1999-01-15 | 2002-09-24 | Light Science Corporation | Patient portable device for photodynamic therapy |
| US6602274B1 (en) | 1999-01-15 | 2003-08-05 | Light Sciences Corporation | Targeted transcutaneous cancer therapy |
| DE19924138A1 (en) | 1999-05-26 | 2000-11-30 | Henkel Kgaa | Detachable adhesive connections |
| GB9922173D0 (en) * | 1999-09-21 | 1999-11-17 | Zeneca Ltd | Chemical compounds |
| AU785505B2 (en) * | 1999-10-15 | 2009-02-26 | Mayo Foundation For Medical Education And Research | Cobalamin conjugates useful as imaging and therapeutic agents |
| DE19951599A1 (en) * | 1999-10-27 | 2001-05-23 | Henkel Kgaa | Process for adhesive separation of adhesive bonds |
| EP1267935A2 (en) | 2000-01-12 | 2003-01-02 | Light Sciences Corporation | Novel treatment for eye disease |
| US6989139B2 (en) * | 2000-02-15 | 2006-01-24 | Bristol-Myers Squibb Pharma Company | Matrix metalloproteinase inhibitors |
| US6656448B1 (en) | 2000-02-15 | 2003-12-02 | Bristol-Myers Squibb Pharma Company | Matrix metalloproteinase inhibitors |
| JP5043271B2 (en) | 2000-04-12 | 2012-10-10 | ジーイー・ヘルスケア・アクスイェ・セルスカプ | Peptide-based compounds |
| CA2410887C (en) | 2000-06-02 | 2012-07-24 | Bracco Research Usa | Compounds for targeting endothelial cells, compositions containing the same and methods for their use |
| US8263739B2 (en) | 2000-06-02 | 2012-09-11 | Bracco Suisse Sa | Compounds for targeting endothelial cells, compositions containing the same and methods for their use |
| ES2518926T3 (en) | 2000-06-02 | 2014-11-05 | Board Of Regents, The University Of Texas System | Ethylenedicysteine conjugates and a glucose analogue |
| AU7002501A (en) * | 2000-06-21 | 2002-01-02 | Du Pont Pharm Co | Vitronectin receptor antagonist pharmaceuticals for use in combination therapy |
| DE10037884A1 (en) * | 2000-08-03 | 2002-02-21 | Henkel Kgaa | Accelerated curing process |
| NO20004795D0 (en) | 2000-09-26 | 2000-09-26 | Nycomed Imaging As | Peptide-based compounds |
| CA2452923C (en) | 2001-07-10 | 2012-02-07 | Amersham Health As | Peptide-based compounds for targeting integrin receptors |
| US7087212B2 (en) * | 2001-08-17 | 2006-08-08 | Mallinckrodt, Inc | Multicomponent assemblies having enhanced binding properties for diagnosis and therapy |
| US20030100830A1 (en) * | 2001-11-27 | 2003-05-29 | Sheng-Ping Zhong | Implantable or insertable medical devices visible under magnetic resonance imaging |
| US7261876B2 (en) | 2002-03-01 | 2007-08-28 | Bracco International Bv | Multivalent constructs for therapeutic and diagnostic applications |
| US7211240B2 (en) | 2002-03-01 | 2007-05-01 | Bracco International B.V. | Multivalent constructs for therapeutic and diagnostic applications |
| US8623822B2 (en) | 2002-03-01 | 2014-01-07 | Bracco Suisse Sa | KDR and VEGF/KDR binding peptides and their use in diagnosis and therapy |
| US7666979B2 (en) | 2002-03-01 | 2010-02-23 | Bracco International B.V. | Methods for preparing multivalent constructs for therapeutic and diagnostic applications and methods of preparing the same |
| US7794693B2 (en) * | 2002-03-01 | 2010-09-14 | Bracco International B.V. | Targeting vector-phospholipid conjugates |
| WO2004065621A1 (en) | 2002-03-01 | 2004-08-05 | Dyax Corp. | Kdr and vegf/kdr binding peptides and their use in diagnosis and therapy |
| US20050250700A1 (en) * | 2002-03-01 | 2005-11-10 | Sato Aaron K | KDR and VEGF/KDR binding peptides |
| US7985402B2 (en) * | 2002-03-01 | 2011-07-26 | Bracco Suisse Sa | Targeting vector-phospholipid conjugates |
| EP1369134A1 (en) * | 2002-06-05 | 2003-12-10 | Bracco Imaging S.p.A. | New agents for magnetic imaging method |
| JP2004138397A (en) * | 2002-10-15 | 2004-05-13 | Kyowa Hakko Kogyo Co Ltd | Screening method for compounds accumulating at specific sites |
| ES2557286T3 (en) | 2003-03-03 | 2016-01-25 | Dyax Corp. | Uses of peptides that specifically bind to the HGF receptor (cMet) |
| WO2004112840A2 (en) * | 2003-06-25 | 2004-12-29 | Guerbet | Peptide conjugate for magnetic resonance imaging |
| FR2856689A1 (en) * | 2003-06-25 | 2004-12-31 | Guerbet Sa | New targeted diagnostic agents, used especially for detecting cardiovascular, cancerous or inflammatory disorders, comprise high relaxivity signal moiety bonded via linker to biovector |
| NO20034350D0 (en) * | 2003-09-29 | 2003-09-29 | Amersham Health As | Optical imaging of colorectal cancer |
| US9695251B2 (en) | 2003-10-31 | 2017-07-04 | The Regents Of The University Of California | Activatable cell penetrating peptides with quenched fluorophores |
| US7985401B2 (en) * | 2003-10-31 | 2011-07-26 | The Regents Of The University Of California | Peptides whose uptake by cells is controllable |
| US7431915B2 (en) * | 2003-10-31 | 2008-10-07 | The Regents Of The University Of California | Peptides whose uptake by cells is controllable |
| US9050378B2 (en) * | 2003-12-10 | 2015-06-09 | Board Of Regents, The University Of Texas System | N2S2 chelate-targeting ligand conjugates |
| NO20035683D0 (en) * | 2003-12-18 | 2003-12-18 | Amersham Health As | Optical imaging of prostate cancer |
| NO20035681D0 (en) * | 2003-12-18 | 2003-12-18 | Amersham Health As | Optical imaging of lung cancer |
| NO20035682D0 (en) * | 2003-12-18 | 2003-12-18 | Amersham Health As | Optical imaging of oesophageal cancer and Barrett's oesophagus |
| NO20035748D0 (en) * | 2003-12-19 | 2003-12-19 | Amersham Health As | Optical imaging of vulnerable arteriosclerosis |
| US20070098631A2 (en) * | 2004-04-28 | 2007-05-03 | Guerbet | Diagnostic compounds comprising a scaffold coupled to a signal entity for medical imaging diagnostic |
| US7553810B2 (en) * | 2004-06-16 | 2009-06-30 | Pneumrx, Inc. | Lung volume reduction using glue composition |
| US7678767B2 (en) | 2004-06-16 | 2010-03-16 | Pneumrx, Inc. | Glue compositions for lung volume reduction |
| US20050281740A1 (en) * | 2004-06-16 | 2005-12-22 | Glen Gong | Imaging damaged lung tissue |
| US7608579B2 (en) * | 2004-06-16 | 2009-10-27 | Pneumrx, Inc. | Lung volume reduction using glue compositions |
| US20050281798A1 (en) * | 2004-06-16 | 2005-12-22 | Glen Gong | Targeting sites of damaged lung tissue using composition |
| US20050281739A1 (en) * | 2004-06-16 | 2005-12-22 | Glen Gong | Imaging damaged lung tissue using compositions |
| US7468350B2 (en) | 2004-06-16 | 2008-12-23 | Pneumrx, Inc. | Glue composition for lung volume reduction |
| CA2570261C (en) * | 2004-07-08 | 2014-06-10 | Pneumrx, Inc. | Pleural effusion treatment device, method and material |
| EP1619501B1 (en) * | 2004-07-22 | 2007-09-26 | Bayer Schering Pharma Aktiengesellschaft | Use of cyanine dyes for the diagnosis of disease associated with angiogenesis |
| GB0421308D0 (en) * | 2004-09-24 | 2004-10-27 | Amersham Plc | Enzyme inhibitor imaging agents |
| WO2006107794A2 (en) * | 2005-04-01 | 2006-10-12 | The Board Of Regents Of The University Of Texas System | Poly(peptide) as a chelator: methods of manufacture and uses |
| US8349991B2 (en) * | 2005-04-19 | 2013-01-08 | Massachusetts Institute Of Technology | Amphiphilic polymers and methods of use thereof |
| WO2007030012A2 (en) * | 2005-09-05 | 2007-03-15 | Stichting Voor De Technische Wetenscahappen | Extracellular matrix imaging |
| US20070140974A1 (en) * | 2005-12-15 | 2007-06-21 | General Electric Company | Targeted nanoparticles for magnetic resonance imaging |
| CA2638911C (en) | 2006-02-06 | 2018-01-23 | Burnham Institute For Medical Research | Methods and compositions related to targeting tumors and wounds |
| US8758723B2 (en) * | 2006-04-19 | 2014-06-24 | The Board Of Regents Of The University Of Texas System | Compositions and methods for cellular imaging and therapy |
| EP2064300A4 (en) * | 2006-09-20 | 2013-05-22 | Pneumrx Inc | Tissue adhesive compositions and methods thereof |
| US10925977B2 (en) | 2006-10-05 | 2021-02-23 | Ceil>Point, LLC | Efficient synthesis of chelators for nuclear imaging and radiotherapy: compositions and applications |
| WO2008136869A2 (en) | 2006-12-06 | 2008-11-13 | Burnham Institute For Medical Research | Methods and compositions related to targeting wounds, regenerating tissue, and tumors |
| CA2674378A1 (en) | 2007-01-03 | 2008-07-17 | Burnham Institute For Medical Research | Methods and compositions related to clot binding compounds |
| DE102007036570A1 (en) | 2007-08-03 | 2009-02-19 | Siemens Ag | Screening test for detection of prostate disease and device and diagnostic substance for performing the test |
| DE102007037008B4 (en) * | 2007-08-06 | 2015-09-10 | Siemens Aktiengesellschaft | Diagnostic substance for use in a method for determining the aggressiveness of a prostate tumor |
| DE102007041836A1 (en) * | 2007-09-03 | 2009-03-05 | Siemens Ag | Method of imaging a prostate tumor and contrast agent |
| US20090074672A1 (en) * | 2007-09-17 | 2009-03-19 | Sri International | Tumor Boundary Imaging |
| CA2699912A1 (en) | 2007-09-19 | 2009-03-26 | Oncofluor, Inc. | Method for imaging and treating organs and tissues |
| US20100143258A1 (en) * | 2008-12-05 | 2010-06-10 | General Electric Company | Tumor margin imaging agents |
| WO2010075540A1 (en) * | 2008-12-23 | 2010-07-01 | Burnham Institute For Medical Research | Methods and compositions for synaphically-targeted treatment for cancer |
| US20110256055A1 (en) | 2008-12-23 | 2011-10-20 | Ge Healthcare Limited | Application of 99mtc peptide-based compound as a bone marrow imaging agent |
| US11096901B2 (en) | 2009-03-06 | 2021-08-24 | Metaqor Llc | Dynamic bio-nanoparticle platforms |
| US11235062B2 (en) * | 2009-03-06 | 2022-02-01 | Metaqor Llc | Dynamic bio-nanoparticle elements |
| WO2011008996A2 (en) * | 2009-07-15 | 2011-01-20 | The Regents Of The University Of California | Peptides whose uptake in cells is controllable |
| US20110081293A1 (en) | 2009-10-07 | 2011-04-07 | Sanford-Burnham Medical Research Institute | Methods and compositions related to clot-binding lipid compounds |
| WO2011049964A1 (en) | 2009-10-19 | 2011-04-28 | Lab Scientific Group | Rna detection and quantitation |
| EP2512497A1 (en) | 2009-12-18 | 2012-10-24 | Sanford-Burnham Medical Research Institute | Methods and compositions related to clot-binding compounds |
| US9610359B2 (en) | 2009-12-23 | 2017-04-04 | Burnham Institute For Medical Research | Methods and compositions related to annexin 1-binding compounds |
| WO2011127405A1 (en) | 2010-04-08 | 2011-10-13 | Sanford-Burnham Medical Research Institute | Methods and compositions for enhanced delivery of compounds |
| WO2012136813A2 (en) | 2011-04-07 | 2012-10-11 | Universitetet I Oslo | Agents for medical radar diagnosis |
| CA2838188C (en) | 2011-06-04 | 2017-04-18 | Rochester General Hospital Research Institute | Compositions and methods related to p6 of haemophilus influenzae |
| US20140308342A1 (en) | 2011-11-11 | 2014-10-16 | Yale University | Reprogramming urokinase into an antibody-recruiting anticancer agent |
| WO2014120837A2 (en) | 2013-01-29 | 2014-08-07 | The Regents Of The University Of California | Pretargeted activatable cell penetrating peptide with intracellulary releaseable prodrug |
| WO2014120974A1 (en) | 2013-01-30 | 2014-08-07 | Avelas Biosciences, Inc. | Selective delivery molecules and methods of use |
| US20170151339A1 (en) * | 2014-06-30 | 2017-06-01 | Tarveda Therapeutics, Inc. | Targeted conjugates and particles and formulations thereof |
| US10111969B2 (en) | 2014-09-17 | 2018-10-30 | Rigshospitalet | uPAR targeting peptide for use in peroperative optical imaging of invasive cancer |
| US10385380B2 (en) | 2014-10-02 | 2019-08-20 | The Regents Of The University Of California | Personalized protease assay to measure protease activity in neoplasms |
| EP3037820A1 (en) * | 2014-12-27 | 2016-06-29 | Miltenyi Biotec GmbH | Cell detection methods and reagents having a releasable labelling moiety |
| US20180221513A1 (en) * | 2015-03-16 | 2018-08-09 | Northwestern University | Contrast-agent-labeled peptide amphiphile nanofibers |
| US10596259B2 (en) | 2015-05-20 | 2020-03-24 | The Regents Of The University Of California | Tumor radiosensitization with monomethyl auristatin E (MMAE) and derivatives thereof |
| KR20180112060A (en) | 2016-02-23 | 2018-10-11 | 타베다 세라퓨틱스, 인코포레이티드 | HSP90 targeted conjugates and their particles and formulations |
| EP3490615A4 (en) * | 2016-07-27 | 2020-04-01 | The Trustees of Columbia University in the City of New York | GELBUND COMPOSITIONS FOR RADIATION THERAPY AND USES THEREOF |
| JP2020506904A (en) | 2017-01-27 | 2020-03-05 | シグナルアールエックス ファーマシューティカルズ,インコーポレイテッド | Thienopyranones and furanopyranones as kinases, bromodomains and checkpoint inhibitors |
| EP3412303A1 (en) | 2017-06-08 | 2018-12-12 | Medizinische Universität Innsbruck | Improved pharmacokinetics and cholecystokinin-2 receptor (cck2r) targeting for diagnosis and therapy |
| KR20220044612A (en) | 2019-03-22 | 2022-04-08 | 리플렉시온 파마슈티컬스, 인크. | D-peptidic compounds for vegf |
Family Cites Families (24)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5672334A (en) * | 1991-01-16 | 1997-09-30 | Access Pharmaceuticals, Inc. | Invivo agents comprising cationic metal chelators with acidic saccharides and glycosaminoglycans |
| MY106120A (en) * | 1988-12-05 | 1995-03-31 | Novartis Ag | Peptide derivatives. |
| AU638043B2 (en) * | 1989-07-20 | 1993-06-17 | Novartis Ag | Labeled polypeptide derivatives |
| US5183900A (en) | 1990-11-21 | 1993-02-02 | Galardy Richard E | Matrix metalloprotease inhibitors |
| US6107459A (en) * | 1991-02-08 | 2000-08-22 | Diatide, Inc. | Technetium-99m labeled peptides for diagnostic imaging |
| ES2193143T3 (en) | 1992-03-05 | 2003-11-01 | Univ Texas | USE OF IMMUNOCONJUGADOS FOR THE DIAGNOSIS AND / OR THERAPY OF VASCULARIZA TUMORS. |
| US5508020A (en) * | 1992-06-05 | 1996-04-16 | Diatech, Inc. | Technetium-99M labeled peptides for imaging |
| GB9215665D0 (en) * | 1992-07-23 | 1992-09-09 | British Bio Technology | Compounds |
| CN1701814A (en) * | 1992-11-13 | 2005-11-30 | 马克斯普朗克科学促进协会 | F1K-1 is a receptor for vascular endothelial growth factor |
| US5512591A (en) * | 1993-02-18 | 1996-04-30 | President And Fellows Of Harvard College | Treatments for diseases characterized by neovascularization |
| JP3670309B2 (en) * | 1993-04-01 | 2005-07-13 | 第一製薬株式会社 | Bicyclic heterocyclic compounds |
| US5480970A (en) | 1993-12-22 | 1996-01-02 | Resolution Pharmaceuticals | Metal chelators |
| US5753230A (en) * | 1994-03-18 | 1998-05-19 | The Scripps Research Institute | Methods and compositions useful for inhibition of angiogenesis |
| US6645933B1 (en) * | 1995-08-01 | 2003-11-11 | Helsinki University Licensing Ltd. Oy | Receptor ligand VEGF-C |
| GB9502065D0 (en) * | 1995-02-02 | 1995-03-22 | Nycomed Imaging As | Contrast media |
| US6027711A (en) * | 1995-06-07 | 2000-02-22 | Rhomed Incorporated | Structurally determined metallo-constructs and applications |
| DE19522774A1 (en) * | 1995-06-27 | 1997-01-02 | Ifu Gmbh | Appliance for spectroscopic examination of specimens taken from human body |
| AU719434B2 (en) * | 1996-02-13 | 2000-05-11 | Astrazeneca Ab | Quinazoline derivatives as VEGF inhibitors |
| CN1304058C (en) * | 1996-03-12 | 2007-03-14 | Pg-Txl有限公司 | Water Soluble Paclitaxel Products |
| DE69716900T2 (en) * | 1996-04-10 | 2003-07-03 | Merck & Co., Inc. | Alpha v Beta 3 ANTAGONISTS |
| GB9708265D0 (en) * | 1997-04-24 | 1997-06-18 | Nycomed Imaging As | Contrast agents |
| EP0946202B1 (en) * | 1996-10-28 | 2003-09-10 | Amersham Health AS | Contrast agents |
| WO1998039469A1 (en) * | 1997-03-04 | 1998-09-11 | Bio-Technology General Corp. | Isolation of tissue specific peptide ligands and their use for targeting pharmaceuticals to organs |
| WO1999040947A2 (en) | 1998-02-11 | 1999-08-19 | Resolution Pharmaceuticals Inc. | Angiogenesis targeting molecules |
-
1997
- 1997-04-24 GB GBGB9708265.5A patent/GB9708265D0/en active Pending
-
1998
- 1998-04-24 DK DK04007226T patent/DK1442751T3/en active
- 1998-04-24 DE DE69837975T patent/DE69837975T2/en not_active Expired - Lifetime
- 1998-04-24 AU AU70687/98A patent/AU7068798A/en not_active Abandoned
- 1998-04-24 EP EP98917461A patent/EP0977600B1/en not_active Expired - Lifetime
- 1998-04-24 JP JP54530798A patent/JP4993419B2/en not_active Expired - Fee Related
- 1998-04-24 AT AT98917461T patent/ATE270116T1/en not_active IP Right Cessation
- 1998-04-24 EP EP04007226A patent/EP1442751B1/en not_active Expired - Lifetime
- 1998-04-24 ES ES04007226T patent/ES2287599T3/en not_active Expired - Lifetime
- 1998-04-24 WO PCT/GB1998/001197 patent/WO1998047541A1/en not_active Ceased
- 1998-04-24 ES ES98917461T patent/ES2224379T3/en not_active Expired - Lifetime
- 1998-04-24 AT AT04007226T patent/ATE365054T1/en not_active IP Right Cessation
- 1998-04-24 DE DE69824842T patent/DE69824842T2/en not_active Expired - Lifetime
-
1999
- 1999-10-22 US US09/422,977 patent/US6610269B1/en not_active Expired - Fee Related
-
2003
- 2003-06-17 US US10/462,836 patent/US7413727B2/en not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| US6610269B1 (en) | 2003-08-26 |
| EP0977600A2 (en) | 2000-02-09 |
| WO1998047541A1 (en) | 1998-10-29 |
| US20040009122A1 (en) | 2004-01-15 |
| EP0977600B1 (en) | 2004-06-30 |
| ATE365054T1 (en) | 2007-07-15 |
| US7413727B2 (en) | 2008-08-19 |
| GB9708265D0 (en) | 1997-06-18 |
| ES2224379T3 (en) | 2005-03-01 |
| AU7068798A (en) | 1998-11-13 |
| EP1442751B1 (en) | 2007-06-20 |
| JP2002511845A (en) | 2002-04-16 |
| EP1442751A1 (en) | 2004-08-04 |
| DE69824842D1 (en) | 2004-08-05 |
| ES2287599T3 (en) | 2007-12-16 |
| ATE270116T1 (en) | 2004-07-15 |
| DE69824842T2 (en) | 2005-11-17 |
| JP4993419B2 (en) | 2012-08-08 |
| DK1442751T3 (en) | 2007-09-24 |
| DE69837975D1 (en) | 2007-08-02 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE69837975T2 (en) | Diagnostic imaging method | |
| US6051207A (en) | Contrast agents | |
| US6264914B1 (en) | Contrast agents | |
| Lux et al. | Advances in gadolinium-based MRI contrast agent designs for monitoring biological processes in vivo | |
| DE69820867T2 (en) | LIGHT IMAGING CONTRAST AGENTS | |
| DE69826263T2 (en) | SONODYNAMIC THERAPY WITH ULTRASOFT SENSITIZER | |
| DE69735901T2 (en) | ENHANCING OR IN CONNECTION WITH DIAGNOSTIC / THERAPEUTIC AGENTS | |
| Barrett et al. | Dendrimers in medical nanotechnology | |
| WO2007127958A2 (en) | Detection and imaging of target tissue | |
| RU2289579C2 (en) | Perfluoroalkyl-containing complexes with polar residues, method for their preparing, pharmaceutical agent | |
| US11052163B2 (en) | Homing agents | |
| JP4878119B2 (en) | Enantiomerically pure (4S, 8S)-and (4R, 8R) -4-p-nitrobenzyl-8-methyl-3,6,9-triaza-3N, 6N, 9N-tricarboxymethyl-1,11-undecane Diacids and their derivatives, processes for their production and their use for the production of pharmaceuticals | |
| DE69724817T2 (en) | CONTRAST AGENTS | |
| US20140363378A1 (en) | Self-assembling molecules that accumulate in acidic tumor microenvironments | |
| DE69735006T2 (en) | CONTRAST AGENTS | |
| US20170224833A1 (en) | Self-assembling molecules that accumulate in acidic tumor microenvironments | |
| Amreddy et al. | Multifunctional dendrimers for theranostic applications |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 8364 | No opposition during term of opposition | ||
| 8328 | Change in the person/name/address of the agent |
Representative=s name: HAMMONDS LLP, LONDON, GB |
|
| R082 | Change of representative |
Ref document number: 1442751 Country of ref document: EP Representative=s name: J D REYNOLDS & CO., GB |