DE102008050957A1 - New ecdysone compounds useful for treating age-related diseases such as osteoporosis, osteoarthritis, incontinence, obesity, arteriosclerosis, hypertonus, metabolic syndrome, anemias, hyperandrogenemia, cellulite and menopausal hot flushes - Google Patents
New ecdysone compounds useful for treating age-related diseases such as osteoporosis, osteoarthritis, incontinence, obesity, arteriosclerosis, hypertonus, metabolic syndrome, anemias, hyperandrogenemia, cellulite and menopausal hot flushes Download PDFInfo
- Publication number
- DE102008050957A1 DE102008050957A1 DE200810050957 DE102008050957A DE102008050957A1 DE 102008050957 A1 DE102008050957 A1 DE 102008050957A1 DE 200810050957 DE200810050957 DE 200810050957 DE 102008050957 A DE102008050957 A DE 102008050957A DE 102008050957 A1 DE102008050957 A1 DE 102008050957A1
- Authority
- DE
- Germany
- Prior art keywords
- alkyl
- substituted
- treatment
- complaints
- incontinence
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 title claims description 19
- 206010021639 Incontinence Diseases 0.000 title claims description 16
- 208000001132 Osteoporosis Diseases 0.000 title claims description 15
- 201000008482 osteoarthritis Diseases 0.000 title claims description 15
- 208000008589 Obesity Diseases 0.000 title claims description 14
- 235000020824 obesity Nutrition 0.000 title claims description 14
- 208000001145 Metabolic Syndrome Diseases 0.000 title claims description 13
- 201000000690 abdominal obesity-metabolic syndrome Diseases 0.000 title claims description 13
- 208000007502 anemia Diseases 0.000 title claims description 13
- 208000035484 Cellulite Diseases 0.000 title claims description 12
- 230000036232 cellulite Effects 0.000 title claims description 12
- 206010003210 Arteriosclerosis Diseases 0.000 title claims description 11
- 208000011775 arteriosclerosis disease Diseases 0.000 title claims description 11
- 201000010066 hyperandrogenism Diseases 0.000 title claims description 10
- 206010049752 Peau d'orange Diseases 0.000 title claims description 9
- 201000010099 disease Diseases 0.000 title claims description 8
- 206010027304 Menopausal symptoms Diseases 0.000 title claims description 4
- 150000002058 ecdysones Chemical class 0.000 title abstract description 4
- 206010020852 Hypertonia Diseases 0.000 title description 2
- 150000001875 compounds Chemical class 0.000 claims abstract description 28
- 239000003814 drug Substances 0.000 claims abstract description 22
- 125000000217 alkyl group Chemical group 0.000 claims abstract description 19
- 125000000753 cycloalkyl group Chemical group 0.000 claims abstract description 19
- 239000000419 plant extract Substances 0.000 claims abstract description 15
- 241000196324 Embryophyta Species 0.000 claims abstract description 9
- 125000002252 acyl group Chemical group 0.000 claims abstract description 9
- 125000000304 alkynyl group Chemical group 0.000 claims abstract description 9
- 125000003118 aryl group Chemical group 0.000 claims abstract description 9
- 125000003342 alkenyl group Chemical group 0.000 claims abstract description 7
- 150000003839 salts Chemical class 0.000 claims abstract description 7
- 235000015872 dietary supplement Nutrition 0.000 claims abstract description 5
- 241001535125 Heliosperma pusillum Species 0.000 claims abstract description 4
- 241000592274 Polypodium vulgare Species 0.000 claims abstract description 4
- 101100516563 Caenorhabditis elegans nhr-6 gene Proteins 0.000 claims abstract description 3
- 101100516572 Caenorhabditis elegans nhr-8 gene Proteins 0.000 claims abstract description 3
- 235000013376 functional food Nutrition 0.000 claims abstract description 3
- 229910052717 sulfur Inorganic materials 0.000 claims abstract description 3
- 239000000654 additive Substances 0.000 claims abstract 2
- 239000012050 conventional carrier Substances 0.000 claims abstract 2
- -1 cyclodextrin Chemical class 0.000 claims description 25
- 230000009245 menopause Effects 0.000 claims description 19
- 238000011282 treatment Methods 0.000 claims description 19
- 101000857870 Squalus acanthias Gonadoliberin Proteins 0.000 claims description 13
- 229910052739 hydrogen Inorganic materials 0.000 claims description 13
- 239000001257 hydrogen Substances 0.000 claims description 13
- 208000035475 disorder Diseases 0.000 claims description 11
- 239000000579 Gonadotropin-Releasing Hormone Substances 0.000 claims description 10
- 206010060800 Hot flush Diseases 0.000 claims description 10
- 206010020772 Hypertension Diseases 0.000 claims description 10
- XLXSAKCOAKORKW-AQJXLSMYSA-N gonadorelin Chemical compound C([C@@H](C(=O)NCC(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N1[C@@H](CCC1)C(=O)NCC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H]1NC(=O)CC1)C1=CC=C(O)C=C1 XLXSAKCOAKORKW-AQJXLSMYSA-N 0.000 claims description 10
- 229940035638 gonadotropin-releasing hormone Drugs 0.000 claims description 10
- 230000002267 hypothalamic effect Effects 0.000 claims description 10
- 238000011321 prophylaxis Methods 0.000 claims description 9
- 125000001424 substituent group Chemical group 0.000 claims description 9
- 125000004399 C1-C4 alkenyl group Chemical group 0.000 claims description 8
- 208000033830 Hot Flashes Diseases 0.000 claims description 7
- 208000024891 symptom Diseases 0.000 claims description 7
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 claims description 6
- 208000031709 Skin Manifestations Diseases 0.000 claims description 4
- 241000133430 Tinospora Species 0.000 claims description 4
- 241000206389 Helleborus Species 0.000 claims description 3
- 239000000546 pharmaceutical excipient Substances 0.000 claims description 3
- 229920001450 Alpha-Cyclodextrin Polymers 0.000 claims description 2
- 201000001320 Atherosclerosis Diseases 0.000 claims description 2
- 229920000858 Cyclodextrin Polymers 0.000 claims description 2
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 2
- HFHDHCJBZVLPGP-RWMJIURBSA-N alpha-cyclodextrin Chemical compound OC[C@H]([C@H]([C@@H]([C@H]1O)O)O[C@H]2O[C@@H]([C@@H](O[C@H]3O[C@H](CO)[C@H]([C@@H]([C@H]3O)O)O[C@H]3O[C@H](CO)[C@H]([C@@H]([C@H]3O)O)O[C@H]3O[C@H](CO)[C@H]([C@@H]([C@H]3O)O)O3)[C@H](O)[C@H]2O)CO)O[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@@H]3O[C@@H]1CO HFHDHCJBZVLPGP-RWMJIURBSA-N 0.000 claims description 2
- 229940043377 alpha-cyclodextrin Drugs 0.000 claims description 2
- HFHDHCJBZVLPGP-UHFFFAOYSA-N schardinger α-dextrin Chemical compound O1C(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(O)C2O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC2C(O)C(O)C1OC2CO HFHDHCJBZVLPGP-UHFFFAOYSA-N 0.000 claims description 2
- 150000002431 hydrogen Chemical group 0.000 claims 5
- 230000000694 effects Effects 0.000 abstract description 11
- 229910052760 oxygen Inorganic materials 0.000 abstract description 2
- 239000000463 material Substances 0.000 abstract 2
- 241000206417 Helleborus foetidus Species 0.000 abstract 1
- 240000003428 Tinospora crispa Species 0.000 abstract 1
- 230000000202 analgesic effect Effects 0.000 abstract 1
- 230000001539 anorectic effect Effects 0.000 abstract 1
- 230000000567 anti-anemic effect Effects 0.000 abstract 1
- 230000003257 anti-anginal effect Effects 0.000 abstract 1
- 230000002456 anti-arthritic effect Effects 0.000 abstract 1
- 230000003178 anti-diabetic effect Effects 0.000 abstract 1
- 230000003110 anti-inflammatory effect Effects 0.000 abstract 1
- 230000003356 anti-rheumatic effect Effects 0.000 abstract 1
- 230000003208 anti-thyroid effect Effects 0.000 abstract 1
- 239000003472 antidiabetic agent Substances 0.000 abstract 1
- 239000003435 antirheumatic agent Substances 0.000 abstract 1
- 229940043671 antithyroid preparations Drugs 0.000 abstract 1
- 206010061428 decreased appetite Diseases 0.000 abstract 1
- 230000010534 mechanism of action Effects 0.000 abstract 1
- 230000000324 neuroprotective effect Effects 0.000 abstract 1
- 210000003932 urinary bladder Anatomy 0.000 description 12
- 229940079593 drug Drugs 0.000 description 10
- NKDFYOWSKOHCCO-YPVLXUMRSA-N 20-hydroxyecdysone Chemical compound C1[C@@H](O)[C@@H](O)C[C@]2(C)[C@@H](CC[C@@]3([C@@H]([C@@](C)(O)[C@H](O)CCC(C)(O)C)CC[C@]33O)C)C3=CC(=O)[C@@H]21 NKDFYOWSKOHCCO-YPVLXUMRSA-N 0.000 description 9
- 210000003205 muscle Anatomy 0.000 description 9
- HVYWMOMLDIMFJA-DPAQBDIFSA-N cholesterol Chemical compound C1C=C2C[C@@H](O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CCCC(C)C)[C@@]1(C)CC2 HVYWMOMLDIMFJA-DPAQBDIFSA-N 0.000 description 8
- 241001465754 Metazoa Species 0.000 description 7
- UPEZCKBFRMILAV-UHFFFAOYSA-N alpha-Ecdysone Natural products C1C(O)C(O)CC2(C)C(CCC3(C(C(C(O)CCC(C)(C)O)C)CCC33O)C)C3=CC(=O)C21 UPEZCKBFRMILAV-UHFFFAOYSA-N 0.000 description 7
- UPEZCKBFRMILAV-JNEQICEOSA-N Ecdysone Natural products O=C1[C@H]2[C@@](C)([C@@H]3C([C@@]4(O)[C@@](C)([C@H]([C@H]([C@@H](O)CCC(O)(C)C)C)CC4)CC3)=C1)C[C@H](O)[C@H](O)C2 UPEZCKBFRMILAV-JNEQICEOSA-N 0.000 description 6
- 241000700159 Rattus Species 0.000 description 6
- UPEZCKBFRMILAV-JMZLNJERSA-N ecdysone Chemical compound C1[C@@H](O)[C@@H](O)C[C@]2(C)[C@@H](CC[C@@]3([C@@H]([C@@H]([C@H](O)CCC(C)(C)O)C)CC[C@]33O)C)C3=CC(=O)[C@@H]21 UPEZCKBFRMILAV-JMZLNJERSA-N 0.000 description 6
- 210000003903 pelvic floor Anatomy 0.000 description 6
- 208000020084 Bone disease Diseases 0.000 description 5
- 206010066218 Stress Urinary Incontinence Diseases 0.000 description 5
- NKDFYOWSKOHCCO-UHFFFAOYSA-N beta-ecdysone Natural products C1C(O)C(O)CC2(C)C(CCC3(C(C(C)(O)C(O)CCC(C)(O)C)CCC33O)C)C3=CC(=O)C21 NKDFYOWSKOHCCO-UHFFFAOYSA-N 0.000 description 5
- 150000002057 ecdysone derivatives Chemical class 0.000 description 5
- 150000002061 ecdysteroids Chemical class 0.000 description 5
- 125000004435 hydrogen atom Chemical class [H]* 0.000 description 5
- 230000001575 pathological effect Effects 0.000 description 5
- 230000003389 potentiating effect Effects 0.000 description 5
- 208000022170 stress incontinence Diseases 0.000 description 5
- 150000003626 triacylglycerols Chemical class 0.000 description 5
- VOXZDWNPVJITMN-ZBRFXRBCSA-N 17β-estradiol Chemical compound OC1=CC=C2[C@H]3CC[C@](C)([C@H](CC4)O)[C@@H]4[C@@H]3CCC2=C1 VOXZDWNPVJITMN-ZBRFXRBCSA-N 0.000 description 4
- 210000000988 bone and bone Anatomy 0.000 description 4
- 235000012000 cholesterol Nutrition 0.000 description 4
- 238000012360 testing method Methods 0.000 description 4
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- NMJREATYWWNIKX-UHFFFAOYSA-N GnRH Chemical compound C1CCC(C(=O)NCC(N)=O)N1C(=O)C(CC(C)C)NC(=O)C(CC=1C2=CC=CC=C2NC=1)NC(=O)CNC(=O)C(NC(=O)C(CO)NC(=O)C(CC=1C2=CC=CC=C2NC=1)NC(=O)C(CC=1NC=NC=1)NC(=O)C1NC(=O)CC1)CC1=CC=C(O)C=C1 NMJREATYWWNIKX-UHFFFAOYSA-N 0.000 description 3
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 3
- 208000000921 Urge Urinary Incontinence Diseases 0.000 description 3
- 206010046543 Urinary incontinence Diseases 0.000 description 3
- 239000000556 agonist Substances 0.000 description 3
- 239000003098 androgen Substances 0.000 description 3
- 239000005557 antagonist Substances 0.000 description 3
- 230000009286 beneficial effect Effects 0.000 description 3
- 210000004369 blood Anatomy 0.000 description 3
- 239000008280 blood Substances 0.000 description 3
- 210000001185 bone marrow Anatomy 0.000 description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 3
- 102000015694 estrogen receptors Human genes 0.000 description 3
- 108010038795 estrogen receptors Proteins 0.000 description 3
- 238000001727 in vivo Methods 0.000 description 3
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 3
- 210000000963 osteoblast Anatomy 0.000 description 3
- 210000002997 osteoclast Anatomy 0.000 description 3
- 239000013641 positive control Substances 0.000 description 3
- 238000002360 preparation method Methods 0.000 description 3
- 239000002904 solvent Substances 0.000 description 3
- 210000003708 urethra Anatomy 0.000 description 3
- 206010046494 urge incontinence Diseases 0.000 description 3
- 230000001836 utereotrophic effect Effects 0.000 description 3
- 206010000599 Acromegaly Diseases 0.000 description 2
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 2
- 208000011231 Crohn disease Diseases 0.000 description 2
- 241000238424 Crustacea Species 0.000 description 2
- 208000014311 Cushing syndrome Diseases 0.000 description 2
- 208000002197 Ehlers-Danlos syndrome Diseases 0.000 description 2
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 2
- JMBQKKAJIKAWKF-UHFFFAOYSA-N Glutethimide Chemical compound C=1C=CC=CC=1C1(CC)CCC(=O)NC1=O JMBQKKAJIKAWKF-UHFFFAOYSA-N 0.000 description 2
- 206010019468 Hemiplegia Diseases 0.000 description 2
- 206010020365 Homocystinuria Diseases 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 2
- 206010058359 Hypogonadism Diseases 0.000 description 2
- 208000001826 Marfan syndrome Diseases 0.000 description 2
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 2
- 206010031243 Osteogenesis imperfecta Diseases 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- 208000007452 Plasmacytoma Diseases 0.000 description 2
- 206010037211 Psychomotor hyperactivity Diseases 0.000 description 2
- LCTONWCANYUPML-UHFFFAOYSA-N Pyruvic acid Chemical compound CC(=O)C(O)=O LCTONWCANYUPML-UHFFFAOYSA-N 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 2
- 239000002253 acid Substances 0.000 description 2
- 150000007513 acids Chemical class 0.000 description 2
- 239000004480 active ingredient Substances 0.000 description 2
- 230000002280 anti-androgenic effect Effects 0.000 description 2
- 239000000051 antiandrogen Substances 0.000 description 2
- 239000002585 base Substances 0.000 description 2
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 2
- 238000004166 bioassay Methods 0.000 description 2
- 229910052791 calcium Inorganic materials 0.000 description 2
- 239000011575 calcium Substances 0.000 description 2
- 210000003321 cartilage cell Anatomy 0.000 description 2
- POZRVZJJTULAOH-LHZXLZLDSA-N danazol Chemical compound C1[C@]2(C)[C@H]3CC[C@](C)([C@](CC4)(O)C#C)[C@@H]4[C@@H]3CCC2=CC2=C1C=NO2 POZRVZJJTULAOH-LHZXLZLDSA-N 0.000 description 2
- 229960000766 danazol Drugs 0.000 description 2
- 206010012601 diabetes mellitus Diseases 0.000 description 2
- 229960005309 estradiol Drugs 0.000 description 2
- 229930182833 estradiol Natural products 0.000 description 2
- 230000001076 estrogenic effect Effects 0.000 description 2
- 239000000284 extract Substances 0.000 description 2
- 210000004907 gland Anatomy 0.000 description 2
- 229960002972 glutethimide Drugs 0.000 description 2
- 230000036541 health Effects 0.000 description 2
- 229920000669 heparin Polymers 0.000 description 2
- 210000003016 hypothalamus Anatomy 0.000 description 2
- 230000002163 immunogen Effects 0.000 description 2
- 230000006872 improvement Effects 0.000 description 2
- 229910052500 inorganic mineral Inorganic materials 0.000 description 2
- 239000002428 insect molting hormone Substances 0.000 description 2
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 2
- 150000002632 lipids Chemical class 0.000 description 2
- 208000008585 mastocytosis Diseases 0.000 description 2
- 230000004060 metabolic process Effects 0.000 description 2
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 2
- 239000011707 mineral Substances 0.000 description 2
- 239000013642 negative control Substances 0.000 description 2
- 210000000056 organ Anatomy 0.000 description 2
- 230000001350 orogenic effect Effects 0.000 description 2
- 239000000843 powder Substances 0.000 description 2
- 230000035755 proliferation Effects 0.000 description 2
- 210000002307 prostate Anatomy 0.000 description 2
- 230000009467 reduction Effects 0.000 description 2
- 230000004044 response Effects 0.000 description 2
- 206010039073 rheumatoid arthritis Diseases 0.000 description 2
- 210000001625 seminal vesicle Anatomy 0.000 description 2
- 210000005070 sphincter Anatomy 0.000 description 2
- 239000007921 spray Substances 0.000 description 2
- 239000003270 steroid hormone Substances 0.000 description 2
- 238000007920 subcutaneous administration Methods 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- 239000003826 tablet Substances 0.000 description 2
- 238000002560 therapeutic procedure Methods 0.000 description 2
- 210000002303 tibia Anatomy 0.000 description 2
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 2
- 230000002485 urinary effect Effects 0.000 description 2
- 210000002700 urine Anatomy 0.000 description 2
- 201000010653 vesiculitis Diseases 0.000 description 2
- BUHVIAUBTBOHAG-FOYDDCNASA-N (2r,3r,4s,5r)-2-[6-[[2-(3,5-dimethoxyphenyl)-2-(2-methylphenyl)ethyl]amino]purin-9-yl]-5-(hydroxymethyl)oxolane-3,4-diol Chemical compound COC1=CC(OC)=CC(C(CNC=2C=3N=CN(C=3N=CN=2)[C@H]2[C@@H]([C@H](O)[C@@H](CO)O2)O)C=2C(=CC=CC=2)C)=C1 BUHVIAUBTBOHAG-FOYDDCNASA-N 0.000 description 1
- BJEPYKJPYRNKOW-REOHCLBHSA-N (S)-malic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O BJEPYKJPYRNKOW-REOHCLBHSA-N 0.000 description 1
- 125000000196 1,4-pentadienyl group Chemical group [H]C([*])=C([H])C([H])([H])C([H])=C([H])[H] 0.000 description 1
- 125000004973 1-butenyl group Chemical group C(=CCC)* 0.000 description 1
- 125000004972 1-butynyl group Chemical group [H]C([H])([H])C([H])([H])C#C* 0.000 description 1
- 125000006039 1-hexenyl group Chemical group 0.000 description 1
- RTBFRGCFXZNCOE-UHFFFAOYSA-N 1-methylsulfonylpiperidin-4-one Chemical compound CS(=O)(=O)N1CCC(=O)CC1 RTBFRGCFXZNCOE-UHFFFAOYSA-N 0.000 description 1
- 125000006023 1-pentenyl group Chemical group 0.000 description 1
- 125000006017 1-propenyl group Chemical group 0.000 description 1
- 125000000530 1-propynyl group Chemical group [H]C([H])([H])C#C* 0.000 description 1
- 125000004974 2-butenyl group Chemical group C(C=CC)* 0.000 description 1
- 125000000069 2-butynyl group Chemical group [H]C([H])([H])C#CC([H])([H])* 0.000 description 1
- 125000006040 2-hexenyl group Chemical group 0.000 description 1
- 125000006020 2-methyl-1-propenyl group Chemical group 0.000 description 1
- 125000006022 2-methyl-2-propenyl group Chemical group 0.000 description 1
- 125000006024 2-pentenyl group Chemical group 0.000 description 1
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 1
- 125000001494 2-propynyl group Chemical group [H]C#CC([H])([H])* 0.000 description 1
- HXWZQRICWSADMH-SEHXZECUSA-N 20-hydroxyecdysone Natural products CC(C)(C)CC[C@@H](O)[C@@](C)(O)[C@H]1CC[C@@]2(O)C3=CC(=O)[C@@H]4C[C@@H](O)[C@@H](O)C[C@]4(C)[C@H]3CC[C@]12C HXWZQRICWSADMH-SEHXZECUSA-N 0.000 description 1
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 1
- 125000006047 4-methyl-1-pentenyl group Chemical group 0.000 description 1
- 201000004384 Alopecia Diseases 0.000 description 1
- 241000238421 Arthropoda Species 0.000 description 1
- 239000005711 Benzoic acid Substances 0.000 description 1
- 125000000882 C2-C6 alkenyl group Chemical group 0.000 description 1
- 125000003601 C2-C6 alkynyl group Chemical group 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- 229920001268 Cholestyramine Polymers 0.000 description 1
- 102000008186 Collagen Human genes 0.000 description 1
- 108010035532 Collagen Proteins 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- DCEFCUHVANGEOE-UHFFFAOYSA-N Ecdysterone Natural products CC(CC(C)(C)O)C(O)C(C)(O)C1CCC2(O)C3=CC(=O)C4CC(O)C(O)CC4(C)C3CCC12C DCEFCUHVANGEOE-UHFFFAOYSA-N 0.000 description 1
- IAJILQKETJEXLJ-UHFFFAOYSA-N Galacturonsaeure Natural products O=CC(O)C(O)C(O)C(O)C(O)=O IAJILQKETJEXLJ-UHFFFAOYSA-N 0.000 description 1
- HTTJABKRGRZYRN-UHFFFAOYSA-N Heparin Chemical compound OC1C(NC(=O)C)C(O)OC(COS(O)(=O)=O)C1OC1C(OS(O)(=O)=O)C(O)C(OC2C(C(OS(O)(=O)=O)C(OC3C(C(O)C(O)C(O3)C(O)=O)OS(O)(=O)=O)C(CO)O2)NS(O)(=O)=O)C(C(O)=O)O1 HTTJABKRGRZYRN-UHFFFAOYSA-N 0.000 description 1
- 241000238631 Hexapoda Species 0.000 description 1
- 201000002980 Hyperparathyroidism Diseases 0.000 description 1
- 206010020850 Hyperthyroidism Diseases 0.000 description 1
- 206010061216 Infarction Diseases 0.000 description 1
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 1
- 206010072742 Late onset hypogonadism syndrome Diseases 0.000 description 1
- 208000030289 Lymphoproliferative disease Diseases 0.000 description 1
- OKJIRPAQVSHGFK-UHFFFAOYSA-N N-acetylglycine Chemical compound CC(=O)NCC(O)=O OKJIRPAQVSHGFK-UHFFFAOYSA-N 0.000 description 1
- 231100000214 OECD 441 Hershberger Bioassay in Rats Toxicity 0.000 description 1
- 206010033892 Paraplegia Diseases 0.000 description 1
- OFOBLEOULBTSOW-UHFFFAOYSA-N Propanedioic acid Natural products OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 1
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 1
- KNDHRUPPBXRELB-UHFFFAOYSA-M [4-[3-(4-ethylphenyl)butyl]phenyl]-trimethylazanium;chloride Chemical compound [Cl-].C1=CC(CC)=CC=C1C(C)CCC1=CC=C([N+](C)(C)C)C=C1 KNDHRUPPBXRELB-UHFFFAOYSA-M 0.000 description 1
- 210000001015 abdomen Anatomy 0.000 description 1
- 210000000579 abdominal fat Anatomy 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 210000000577 adipose tissue Anatomy 0.000 description 1
- IAJILQKETJEXLJ-QTBDOELSSA-N aldehydo-D-glucuronic acid Chemical compound O=C[C@H](O)[C@@H](O)[C@H](O)[C@H](O)C(O)=O IAJILQKETJEXLJ-QTBDOELSSA-N 0.000 description 1
- 229910001413 alkali metal ion Inorganic materials 0.000 description 1
- 231100000360 alopecia Toxicity 0.000 description 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 1
- BJEPYKJPYRNKOW-UHFFFAOYSA-N alpha-hydroxysuccinic acid Natural products OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- MDFFNEOEWAXZRQ-UHFFFAOYSA-N aminyl Chemical compound [NH2] MDFFNEOEWAXZRQ-UHFFFAOYSA-N 0.000 description 1
- 229940030486 androgens Drugs 0.000 description 1
- JFCQEDHGNNZCLN-UHFFFAOYSA-N anhydrous glutaric acid Natural products OC(=O)CCCC(O)=O JFCQEDHGNNZCLN-UHFFFAOYSA-N 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 235000006708 antioxidants Nutrition 0.000 description 1
- 206010003246 arthritis Diseases 0.000 description 1
- 235000010323 ascorbic acid Nutrition 0.000 description 1
- 229960005070 ascorbic acid Drugs 0.000 description 1
- 239000011668 ascorbic acid Substances 0.000 description 1
- 235000003704 aspartic acid Nutrition 0.000 description 1
- 229960005261 aspartic acid Drugs 0.000 description 1
- 230000000923 atherogenic effect Effects 0.000 description 1
- 235000010233 benzoic acid Nutrition 0.000 description 1
- 229960004365 benzoic acid Drugs 0.000 description 1
- OQFSQFPPLPISGP-UHFFFAOYSA-N beta-carboxyaspartic acid Natural products OC(=O)C(N)C(C(O)=O)C(O)=O OQFSQFPPLPISGP-UHFFFAOYSA-N 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 230000008033 biological extinction Effects 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 238000009534 blood test Methods 0.000 description 1
- 230000037182 bone density Effects 0.000 description 1
- 235000008429 bread Nutrition 0.000 description 1
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 1
- 210000001217 buttock Anatomy 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- 125000004432 carbon atom Chemical group C* 0.000 description 1
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 210000000845 cartilage Anatomy 0.000 description 1
- 230000015556 catabolic process Effects 0.000 description 1
- 210000004027 cell Anatomy 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 229960001678 colestyramine Drugs 0.000 description 1
- 229920001436 collagen Polymers 0.000 description 1
- 238000002591 computed tomography Methods 0.000 description 1
- 230000001143 conditioned effect Effects 0.000 description 1
- 210000002808 connective tissue Anatomy 0.000 description 1
- 208000018631 connective tissue disease Diseases 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 230000001054 cortical effect Effects 0.000 description 1
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000000640 cyclooctyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 1
- 230000007850 degeneration Effects 0.000 description 1
- 238000006731 degradation reaction Methods 0.000 description 1
- 235000005911 diet Nutrition 0.000 description 1
- 230000037213 diet Effects 0.000 description 1
- 230000010339 dilation Effects 0.000 description 1
- 239000002270 dispersing agent Substances 0.000 description 1
- 239000008298 dragée Substances 0.000 description 1
- 210000004177 elastic tissue Anatomy 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 230000002124 endocrine Effects 0.000 description 1
- 229940011871 estrogen Drugs 0.000 description 1
- 239000000262 estrogen Substances 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 1
- 230000007717 exclusion Effects 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 230000002349 favourable effect Effects 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 239000007941 film coated tablet Substances 0.000 description 1
- 235000013305 food Nutrition 0.000 description 1
- 235000019253 formic acid Nutrition 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- 239000003862 glucocorticoid Substances 0.000 description 1
- 229940097043 glucuronic acid Drugs 0.000 description 1
- 230000001456 gonadotroph Effects 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 229960002897 heparin Drugs 0.000 description 1
- 125000000592 heterocycloalkyl group Chemical group 0.000 description 1
- 238000002657 hormone replacement therapy Methods 0.000 description 1
- 230000000642 iatrogenic effect Effects 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 230000007574 infarction Effects 0.000 description 1
- 230000002757 inflammatory effect Effects 0.000 description 1
- 230000000968 intestinal effect Effects 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 239000002949 juvenile hormone Substances 0.000 description 1
- 229930014550 juvenile hormone Natural products 0.000 description 1
- 150000003633 juvenile hormone derivatives Chemical class 0.000 description 1
- 210000000629 knee joint Anatomy 0.000 description 1
- 239000004310 lactic acid Substances 0.000 description 1
- 235000014655 lactic acid Nutrition 0.000 description 1
- 230000001418 larval effect Effects 0.000 description 1
- 239000008141 laxative Substances 0.000 description 1
- 229940125722 laxative agent Drugs 0.000 description 1
- 238000000670 ligand binding assay Methods 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 210000001699 lower leg Anatomy 0.000 description 1
- 230000001589 lymphoproliferative effect Effects 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- 239000011976 maleic acid Substances 0.000 description 1
- 239000001630 malic acid Substances 0.000 description 1
- 235000011090 malic acid Nutrition 0.000 description 1
- 230000001404 mediated effect Effects 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 230000002503 metabolic effect Effects 0.000 description 1
- 230000029052 metamorphosis Effects 0.000 description 1
- 229940098779 methanesulfonic acid Drugs 0.000 description 1
- 238000000034 method Methods 0.000 description 1
- 230000027939 micturition Effects 0.000 description 1
- 235000013336 milk Nutrition 0.000 description 1
- 239000008267 milk Substances 0.000 description 1
- 210000004080 milk Anatomy 0.000 description 1
- 230000003562 morphometric effect Effects 0.000 description 1
- 238000013425 morphometry Methods 0.000 description 1
- 230000003387 muscular Effects 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000001280 n-hexyl group Chemical group C(CCCCC)* 0.000 description 1
- 125000000740 n-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 210000001989 nasopharynx Anatomy 0.000 description 1
- 230000000422 nocturnal effect Effects 0.000 description 1
- 230000000771 oncological effect Effects 0.000 description 1
- 238000009806 oophorectomy Methods 0.000 description 1
- 230000002611 ovarian Effects 0.000 description 1
- 208000024449 overflow incontinence Diseases 0.000 description 1
- 235000006408 oxalic acid Nutrition 0.000 description 1
- 229940116315 oxalic acid Drugs 0.000 description 1
- 125000003538 pentan-3-yl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 1
- 239000008194 pharmaceutical composition Substances 0.000 description 1
- 235000011007 phosphoric acid Nutrition 0.000 description 1
- 230000007505 plaque formation Effects 0.000 description 1
- 239000004014 plasticizer Substances 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 201000009395 primary hyperaldosteronism Diseases 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 230000002062 proliferating effect Effects 0.000 description 1
- 239000003380 propellant Substances 0.000 description 1
- 125000006239 protecting group Chemical group 0.000 description 1
- 230000000541 pulsatile effect Effects 0.000 description 1
- 229940107700 pyruvic acid Drugs 0.000 description 1
- 239000002994 raw material Substances 0.000 description 1
- 230000011514 reflex Effects 0.000 description 1
- 230000027272 reproductive process Effects 0.000 description 1
- 239000003340 retarding agent Substances 0.000 description 1
- 229920006395 saturated elastomer Polymers 0.000 description 1
- 235000015067 sauces Nutrition 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 230000035938 sexual maturation Effects 0.000 description 1
- 206010040882 skin lesion Diseases 0.000 description 1
- 231100000444 skin lesion Toxicity 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 239000000243 solution Substances 0.000 description 1
- 238000013223 sprague-dawley female rat Methods 0.000 description 1
- 238000010025 steaming Methods 0.000 description 1
- 150000003431 steroids Chemical class 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 238000005728 strengthening Methods 0.000 description 1
- 239000013589 supplement Substances 0.000 description 1
- 230000035900 sweating Effects 0.000 description 1
- 229940037128 systemic glucocorticoids Drugs 0.000 description 1
- 239000007885 tablet disintegrant Substances 0.000 description 1
- 239000011975 tartaric acid Substances 0.000 description 1
- 235000002906 tartaric acid Nutrition 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 239000005495 thyroid hormone Substances 0.000 description 1
- 229940036555 thyroid hormone Drugs 0.000 description 1
- 238000003325 tomography Methods 0.000 description 1
- 210000000689 upper leg Anatomy 0.000 description 1
- 230000003202 urodynamic effect Effects 0.000 description 1
- 210000004291 uterus Anatomy 0.000 description 1
- 230000002792 vascular Effects 0.000 description 1
- 235000013311 vegetables Nutrition 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
- 230000003313 weakening effect Effects 0.000 description 1
- 239000000080 wetting agent Substances 0.000 description 1
- 230000037303 wrinkles Effects 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/56—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids
- A61K31/575—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids substituted in position 17 beta by a chain of three or more carbon atoms, e.g. cholane, cholestane, ergosterol, sitosterol
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
Description
Die Erfindung betrifft Ecdyson-Derivate, Arzneimittel die diese oder deren Salze enthalten, auch in Form eines Pflanzenextraktes oder eines Nahrungsergänzungsmittels, und die Verwendung der Ecdyson-Derivate, Ecdysteroiden zur Behandlung und Prophylaxe von Alterserkrankungen, insbesondere Osteoporose, Osteoarthritis, Inkontinenz sowie Fettleibigkeit, Arteriosklerose, Hypertonus, insbesondere des metabolischen Syndroms, Anämien, Hyperandrogenämie, Menopausale Kontinenzstörungen, menopause Hitzewallungen, die mit einer Hyperstimulation des hypothalamischen Gonadotropin Releasing Hormon-Pulsgenerators assoziiert sind oder zur Behandlung von menopause und klimakterischen Beschwerden (Frau) oder andropause Beschwerden (Mann) sowie alterstypische Hauterscheinungen, insbesondere Zellulite.The The invention relates to ecdysone derivatives, medicines containing these or their salts, also in the form of a plant extract or of a dietary supplement, and the use of the Ecdysone derivatives, ecdysteroids for the treatment and prophylaxis of Age disorders, especially osteoporosis, osteoarthritis, incontinence as well as obesity, arteriosclerosis, hypertension, in particular metabolic syndrome, anemia, hyperandrogenemia, Menopausal continence disorders, menopause hot flashes, the with hyperstimulation of hypothalamic gonadotropin releasing Hormone pulse generator are associated or used to treat menopause and climacteric complaints (woman) or andropause complaints (Man) as well as age-typical skin symptoms, in particular cellulite.
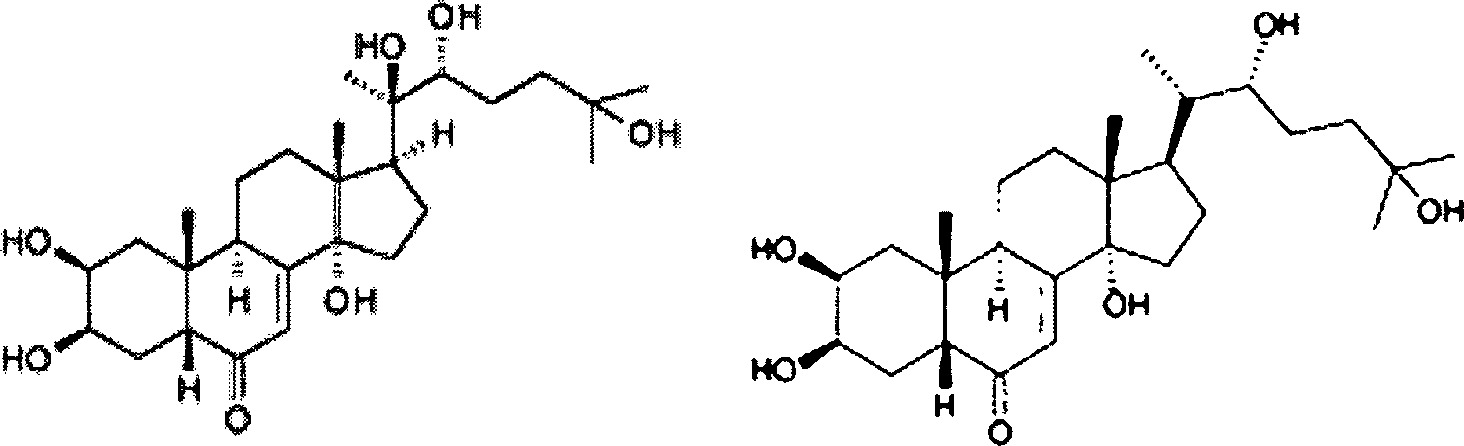
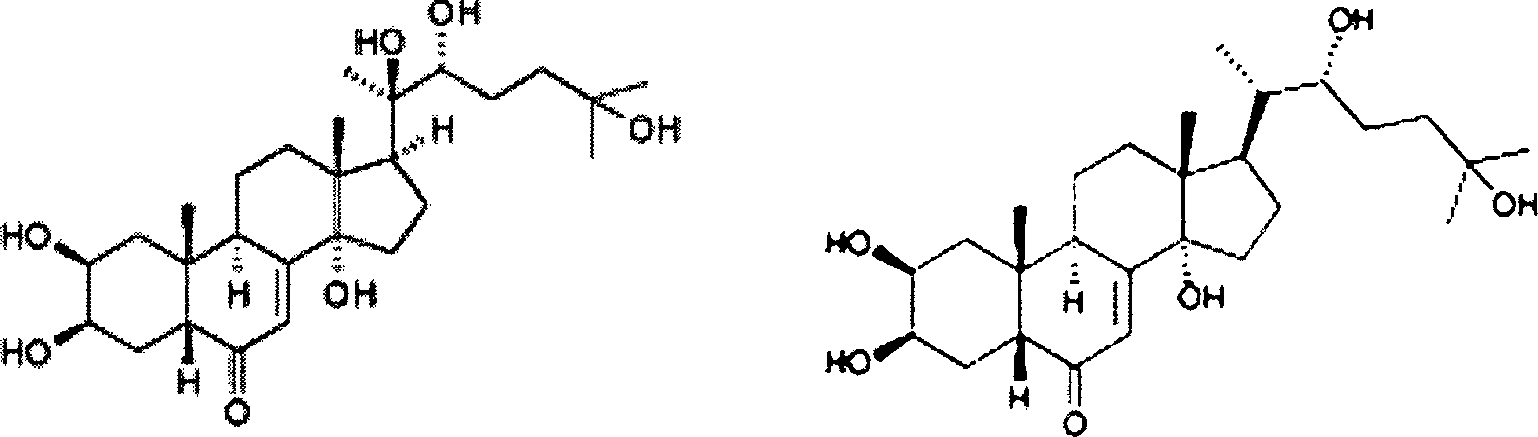
Ecdyson (”Häutungshormon”, (22R)-2β,3β, 14,22,25-Pentahydroxy-5β-cholest-7-en-6-on) ist das Steroidhormon der Arthropoden. Es wird von der Prothoraxdrüse gebildet, wirkt als Gegenspieler zum Juvenilhormon und reguliert die Larvenhäutung und die Metamorphose. Ecdysteroide sind im erwachsenen Tier ebenfalls an der sexuellen Reifung und an Fortpflanzungsvorgängen beteiligt (gonadotrope Wirkung). Die Erfindung betrifft ebenfalls Ecdysteroide im Sammelbegriff für Steroidhormone wie eben Ecdyson oder 20-OH-Ecdyson („Ecdysteron”), die bei vielen Invertebratengruppen vorkommen. Produziert werden Ecdysteroide ebenfalls in den Prothoraxdrüsen der Insekten. Das bekannte Ecdyson ist identisch mit dem Crustecdyson, dem Häutungshormon der Crustaceen (Krebstiere). Ecdyson kommt in 1000-mal höherer Konzentration auch in Pflanzen vor (Phytoectosteroide im Gegensatz zu Zooectosteroiden). Für Ecdyson-Derivate ist vor allem die En-on-Struktur im Ring B und 14 OH im Ring C charakteristisch.ecdysone ("Molting hormone", (22R) -2β, 3β, 14,22,25-pentahydroxy-5β-cholest-7-en-6-one) is the steroid hormone the arthropods. It is formed by the prothorax gland, acts as an antagonist to juvenile hormone and regulates the larval membrane and the metamorphosis. Ecdysteroids are also on in the adult animal sexual maturation and reproductive processes (gonadotropic effect). The invention also relates to ecdysteroids in the collective term for steroid hormones like just Ecdyson or 20-OH ecdysone ("ecdysterone") found in many invertebrate groups occurrence. Ecdysteroids are also produced in the prothorax glands the insects. The well-known ecdysone is identical to the crustecdysone, the molting hormone of crustaceans (crustaceans). ecdysone comes in 1000 times higher concentration in plants (phytoectosteroids as opposed to zooectosteroids). For Ecdysone derivatives is mainly the eneone structure in ring B and 14 OH in the ring C characteristic.
Abb. 1: Links: „20-OH-Ecdyson” = beta-Ecdyson ((2β,3β,5β,22R)-2,3,14,20,22,25-hexahydroxycholest-7-en-6-on) Rechts: Ecdyson ((2β,3β,5β,22R)-2,3,14,22,25-hexahydroxycholest-7-en-6-on) Fig. 1: Left: "20-OH-ecdysone" = beta-ecdysone ((2β, 3β, 5β, 22R) -2,3,14,20,22,25-hexahydroxy-cholest-7-en-6-one) Right: Ecdysone ((2β, 3β, 5β, 22R) -2,3,14,22,25-hexahydroxycholest-7-en-6-one)
Überraschenderweise wurde nunmehr gefunden, dass Ecdyson-Derivate potente Arzneimittel zur Behandlung und Prophylaxe von Osteoporose, Arthritis, Inkontinenz sowie Fettleibigkeit, Arteriosklerose, Hypertonus, insbesondere des metabolischen Syndroms darstellen.Surprisingly it has now been found that ecdysone derivatives are potent drugs for the treatment and prophylaxis of osteoporosis, arthritis, incontinence as well as obesity, arteriosclerosis, hypertension, in particular of the metabolic syndrome.
Die
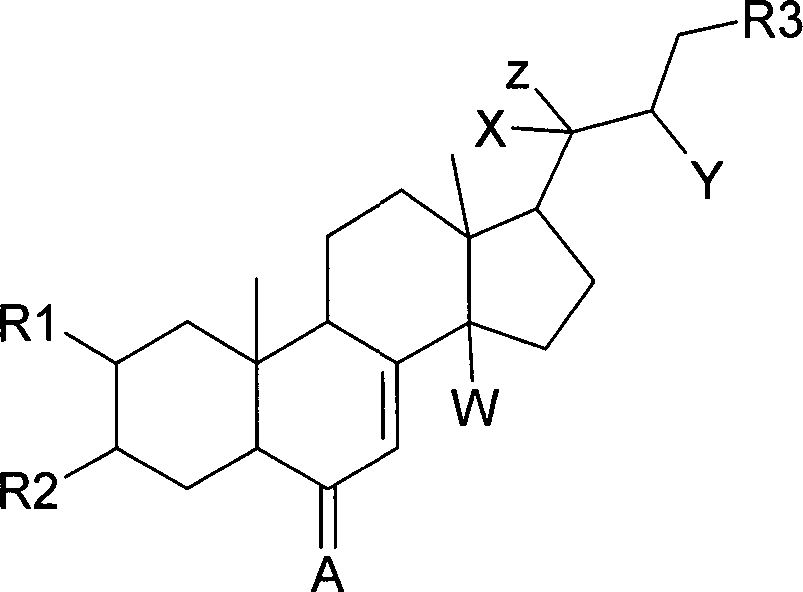
Erfindung betrifft Ecdyson-Derivate der allgemeinen Formel I: wobei jeweils
R1 und
R2 unabhängig voneinander
Hydrogen, substituiertes
oder unsubstituiertes Alkyl, substituiertes oder unsubstituiertes
Cycloalkyl, substituiertes oder unsubstituiertes Cycloalkyl(C0-9)alkyl,
substituiertes oder unsubstituiertes Alkenyl, substituiertes oder
unsubstituiertes Alkinyl, substituiertes oder unsubstituiertes Acyl,
substituiertes oder unsubstituiertes Aryl sind,
und/oder OR11
und OR21 ist, wobei R11 die Bedeutung von R1 hat und R21 die Bedeutung
von R2 hat,
R3 C(R4)(R5)K ist, mit R4 und R5 unabhängig
voneinander Hydrogen, C1-C4 Alkyl, C1-C4 Alkenyl, C1-C4-Alkinyl,
substituiertes oder unsubstituiertes Cycloalkyl, substituiertes
oder unsubstituiertes Cycloalkyl(C0-9)alkyl, substituiertes oder
unsubstituiertes Acyl, substituiertes oder unsubstituiertes Aryl,
und
K
ist OH, SH, NH2, NHR6, wobei R6 C1-C4 Alkyl, C1-C4 Alkenyl annehmen
kann,
A O, S, NH, N-R7, wobei R7 unabhängig von R6
die gleiche Bedeutung wie R6 annehmen kann.The invention relates to ecdysone derivatives of the general formula I: each one
R1 and R2 are independent of each other
Hydrogen, substituted or unsubstituted alkyl, substituted or unsubstituted cycloalkyl, substituted or unsubstituted cycloalkyl (C0-9) alkyl, substituted or unsubstituted alkenyl, substituted or unsubstituted alkynyl, substituted or unsubstituted acyl, substituted or unsubstituted aryl,
and / or OR11 and OR21, where R11 has the meaning of R1 and R21 has the meaning of R2,
R3 is C (R4) (R5) K, with R4 and R5 independently hydrogen, C1-C4 alkyl, C1-C4 alkenyl, C1-C4 alkynyl, substituted or unsubstituted cycloalkyl, substituted or unsubstituted cycloalkyl (C0-9) alkyl , substituted or unsubstituted acyl, substituted or unsubstituted aryl,
and
K is OH, SH, NH 2, NHR 6, where R 6 can be C 1 -C 4 alkyl, C 1 -C 4 alkenyl,
AO, S, NH, N-R7, where R7 can assume the same meaning as R6 independently of R6.
W,
X, Y unabhängig voneinander
Hydrogen, OH, SH, NH2,
NHR8, wobei R8 C1-C4 Alkyl, C1-C4 Alkenyl annehmen kann,
Z
Hydrogen, OH, SH, NH2, C1-C4 Alkyl, C1-C4 Alkenyl, C1-C4-Alkinyl,
substituiertes oder unsubstituiertes Cycloalkyl, substituiertes
oder unsubstituiertes Cycloalkyl(C0-9)alkyl, substituiertes oder
unsubstituiertes Acyl, substituiertes oder unsubstituiertes Aryl
sein kann,
bedeutet, deren Stereoisomere, Tautomere und deren
physiologisch verträglichen Salze oder Einschlussverbindungen.W, X, Y independently
Hydrogen, OH, SH, NH2, NHR8, where R8 can assume C1-C4 alkyl, C1-C4 alkenyl,
Z is hydrogen, OH, SH, NH2, C1-C4 alkyl, C1-C4 alkenyl, C1-C4 alkynyl, substituted or unsubstituted cycloalkyl, substituted or unsubstituted cycloalkyl (C0-9) alkyl, substituted or unsubstituted acyl, substituted or unsubstituted aryl can be,
means their stereoisomers, tautomers and their physiologically acceptable salts or inclusion compounds.
Sofern
diese Formel I nicht genuine oder native Ecdysteroiden abdeckt,
können diese Derivate mittels üblichen Methoden
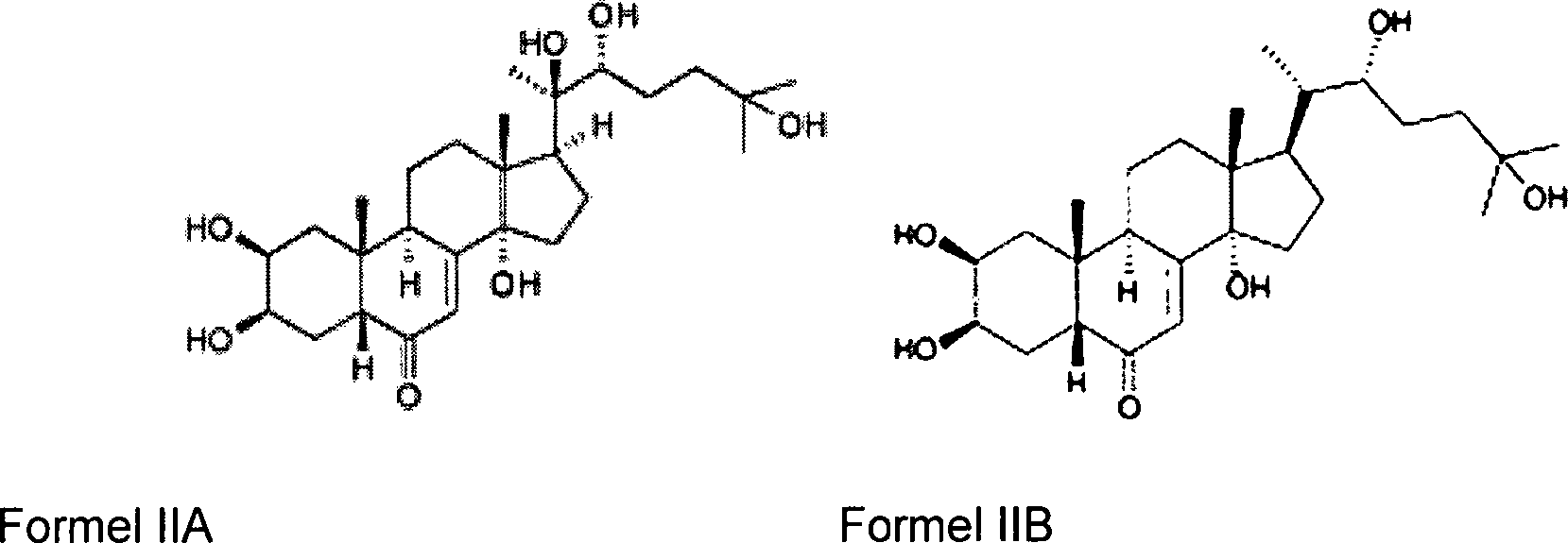
der organischen Chemie aus den Formel IIA und Formel IIB (unten)
gewonnen werden, ggfs. unter Verwendung von Schutzgruppen (siehe
z. B.
Ganz besonders bevorzugt ist jedoch die Verbindung der Formel IIA oder Formel IIB (supra) oder dessen Stereoisomere, Tautomere und deren physiologisch verträglichen Salze oder Einschlussverbindungen, insbesondere deren natives Vorkommen in Pflanzenextrakten.However, very particular preference is given to the compound of the formula IIA or formula IIB (supra) or its stereoisomers, tautomers and their physiologically tolerated salts or inclusion compounds, in particular their native occurrence in plant extracts.
Die Erfindung betrifft bevorzugt außerdem Verbindungen der Formel I mit A = O und W = OH.The Invention also preferably relates to compounds of Formula I with A = O and W = OH.
Weiterhin bevorzugt ist R1 und R2 mit OH, O-C1-C4-Alkyl, O-C1-C4-Alkenyl.Farther R1 and R2 are preferably OH, O-C1-C4-alkyl, O-C1-C4-alkenyl.
Weiterhin bevorzugt ist mindestens ein W, X, Y gleich OH, oder mindestens zwei Substituenten aus W, X, Y gleich OH.Farther preferably at least one W, X, Y is OH, or at least two substituents of W, X, Y is OH.
Weiterhin bevorzugt ist mindestens ein Substituent aus X, Y oder beide gleich Hydrogen, OH, C1-C4 Alkyl, vorzugsweise CH3.Farther preferably at least one substituent of X, Y or both is the same Hydrogen, OH, C1-C4 alkyl, preferably CH3.
Z ist vorzugsweise O, CH3, Hydrogen.Z is preferably O, CH3, hydrogen.
Insbesondere ist es vorteilhaft möglich über R1 und R2 am Ring A eine Erhöhung der Wasserlöslichkeit zu bewirken, dies erfolgt erfindungsgemäß z. B. über die Einführung von Gruppen, die vermehrt Wasserstoffbrückenbindungen ausbilden können und/oder polar und/oder ionisch sind.Especially it is advantageously possible via R1 and R2 on the ring A to increase the water solubility, This is done according to the invention z. B. over the introduction of groups that increase hydrogen bonds can form and / or are polar and / or ionic.
Diese erfindungsgemäßen Verbindungen werden zur Herstellung von Arzneimitteln zur Behandlung und Prophylaxe von Alterserkrankungen, insbesondere oder ausgewählt aus der Gruppe Osteoporose, Osteoarthritis, Inkontinenz sowie Fettleibigkeit, Arteriosklerose, Hypertonus, insbesondere des metabolischen Syndroms, Anämien, Hyperandrogenämie, Menopausale Kontinenzstörungen, menopause Hitzewallungen, die mit einer Hyperstimulation des hypothalamischen Gonadotropin Releasing Hormon-Pulsgenerators assoziiert sind oder zur Behandlung von menopause und klimakterischen Beschwerden (Frau) oder andropause Beschwerden (Mann) sowie alterstypische Hauterscheinungen, insbesondere Zellulite, verwendet.These compounds according to the invention are used for the preparation of medicaments for the treatment and prophylaxis of geriatric diseases, in particular or selected from the group osteoporosis, osteoarthritis, incontinence and obesity, arteriosclerosis, hypertension, in particular of the metabolic syndrome, anemias, hyperandrogenemia, menopausal continence disorders, menopause hot flushes are associated with hyperstimulation of the hypothalamic gonadotropin releasing hormone pulse generator or used for the treatment of menopause and menopausal symptoms (woman) or andropause complaints (man) and age-typical skin manifestations, in particular cellulite.
Weiterhin betrifft die Erfindung ein Arzneimittel enthaltend obige Verbindungen der Formel I oder Formel IIA bzw. IIB samt den üblichen Trägern und Hilfsstoffen. In einer weiteren bevorzugten Ausführungsform können diese Verbindungen Bestandteil eines Pflanzenextraktes sein oder in einem Pflanzenextrakt angereichert sein.Farther The invention relates to a medicament containing the above compounds of formula I or formula IIA or IIB together with the usual Carriers and excipients. In a further preferred Embodiment, these compounds may be part a plant extract or enriched in a plant extract be.
Im Rahmen dieser Erfindung wird mithilfe der erfindungsgemäßen Arzneimittel in einer bevorzugten Ausführungsform pathologische Osteoarthritis, insbesondere Arthrose (Osteoarthritis, syn. Arthrosis deformans) behandelt.in the This invention is achieved by means of the invention Medicaments in a preferred embodiment pathological Osteoarthritis, especially osteoarthritis (osteoarthritis, syn. Arthrosis deformans).
In einer weiteren bevorzugten Ausführungsform wird mithilfe der erfindungsgemäßen Arzneimittel pathologische Inkontinenz, vorzugsweise Harninkontinenz behandelt. Dies ist eine gestörte Reservoirfunktion der Harnblase mit unwillkürlichem Harnabgang, erfindungsgemäß ist die Form der Stressinkontinenz bevorzugt, andere Formen wie Dranginkontinenz, Reflexinkontinenz, Überlaufinkontinenz, extraurethrale Harninkontinenz sind jedoch umfasst. Eine Erhöhung des Blasendrucks über den des urethralen Verschlussdrucks führt zu ungewolltem Harnabgang (Harninkontinenz). Ursache der Inkontinenz ist häufig die Erschlaffung der Beckenbodenmuskulatur. Das führt bei Erhöhung des Innendrucks im Bauchraum zu unwillkürlichem Harnabgang (= Stressinkontinenz), die erfindungsgemäß umfasst ist.In Another preferred embodiment is using the drugs according to the invention pathological Incontinence, preferably treated for urinary incontinence. this is a disturbed reservoir function of the bladder with involuntary Urinary output, according to the invention is the form of stress incontinence other forms such as urge incontinence, reflex incontinence, overflow incontinence, however, extraurethral urinary incontinence is included. An increase the bladder pressure above that of the urethral occlusive pressure leads to unwanted urine output (urinary incontinence). reason Incontinence is often the relaxation of the pelvic floor muscles. This leads to an increase in the internal pressure in the abdomen to involuntary urination (= stress incontinence), the is included according to the invention.
Zusätzlich entwickelt sich häufig eine übererregbare Blase (nervous bladder). Hierbei kontrahiert sich die Blasenmuskulatur unwillkürlich, ohne daß der Verschlussdruck der Urethra ebenfalls ansteigt. Das führt ebenfalls zu ungewolltem Harnabgang (= Drang (Urge) Inkontinenz), die erfindungsgemäß umfasst ist. Ferner umfasst sind synonyme Begriffe wie Blasendrang oder Blasenschwäche.additionally often develops an overexcitable bladder (nervous bladder). Here, the bladder muscles contract involuntarily, without the closing pressure of the Urethra also rises. This also leads to unwanted Urinary outflow (= urge urge incontinence), which comprises according to the invention is. Also included are synonymous terms such as bubble urine or Bladder weakness.
Durch günstige Wirkungen auf die Beckenbodenmuskulatur und gleichzeitig auf die „nervöse” Überaktivität der Blasenmuskulatur können die erfindungsgemäßen Arzneimittel die häufig vorkommende Mischform beider Inkontinenzarten günstig beeinflussen bzw. deren Entstehung verhindern.By beneficial effects on the pelvic floor muscles and at the same time on the "nervous" overactivity The bladder muscles can the inventive Medicines the common form of both types of incontinence influence favorably or prevent their formation.
In einer weiteren bevorzugten Ausführungsform wird mithilfe der erfindungsgemäßen Arzneimittel pathologische Fettleibigkeit (Obesity), Arteriosklerose, Hypertonus, insbesondere des metabolischen Syndroms behandelt.In Another preferred embodiment is using the drugs according to the invention pathological Obesity, arteriosclerosis, hypertension, in particular of the metabolic syndrome.
In einer weiteren bevorzugten Ausführungsform wird mithilfe der erfindungsgemäßen Arzneimittel pathologische Osteoporose behandelt.In Another preferred embodiment is using the drugs according to the invention pathological Treated osteoporosis.
Im Rahmen dieser Erfindung werden ebenfalls mithilfe der erfindungsgemäßen Arzneimittel pathologisch primäre und sekundäre Osteoporose behandelt.in the The scope of this invention will also be understood by means of the invention Pharmaceutical pathological primary and secondary Treated osteoporosis.
Primäre Osteoporose, wie idiopathisch, postmenopausal (Typ I), senil (Typ II). Sekundäre Osteoporose, wie:
- – endokrin, metabolisch (Cushing-Syndrom, Hyperthyreose, Hypogonadismus, Hyperparathyroidismus, Akromegalie, Diabetes mellitus, Homocystinurie),
- – iatrogen, medikamentös (Glukokortikoide, Heparine, Schilddrüsenhormone, GnRH-Agonisten, Danazol, Glutethimid, Laxanzien, Colestyramin),
- – myelogen, onkologisch (Plasmozytom, Mastozytose, lymphoproliferative Erkrankungen, diffuse Knochenmarkkarzinose),
- – parainfektiös, immunogen (rheumatoide Arthritis, Enteritis regionalis Crohn),
- – Inaktivität, Immobilisation (Bettruhe, Paraplegie, Hemiplegie),
- – hereditäre Bindegewebeerkrankungen (Osteogenesis imperfecta, Marfan-Syndrom, Ehlers-Danlos-Syndrom),
- – komplexe Osteopathien (renale Osteopathie, intestinale Osteopathie).
- - endocrine, metabolic (Cushing's syndrome, hyperthyroidism, hypogonadism, hyperparathyroidism, acromegaly, diabetes mellitus, homocystinuria),
- - iatrogenic, medicinal (glucocorticoids, heparins, thyroid hormones, GnRH agonists, danazol, glutethimide, laxatives, colestyramine),
- - myelogen, oncological (plasmocytoma, mastocytosis, lymphoproliferative diseases, diffuse bone marrow carcinosis),
- - parainfectious, immunogenic (rheumatoid arthritis, regional enteritis Crohn),
- - inactivity, immobilization (bed rest, paraplegia, hemiplegia),
- - hereditary connective tissue diseases (osteogenesis imperfecta, Marfan syndrome, Ehlers-Danlos syndrome),
- - complex osteopathies (renal osteopathy, intestinal osteopathy).
In einer weiteren Ausführungsform werden mithilfe der erfindungsgemäßen Arzneimittel Anämien behandelt, hierbei sind sämtliche Formen der Anämie (auch so genannte Blutarmut) umfasst.In Another embodiment will be using the inventive Treated drug anemias, here are all Forms of anemia (also called anemia).
In
einer weiteren Ausführungsform werden die erfindungsgemäßen
Arzneimittel alternativ zur so genannten Hormonersatztherapie eingesetzt.
Besonders vorteilhaft binden die erfindungsgemäßen
Verbindungen nicht an Estrogenrezeptoren und zeigen keine uterotrope,
estrogene oder andogene Wirkung (siehe
Dieser
Ausschluss der uterotropen, estrogenen oder andogenen Wirkung der
erfindungsgemäßen Arzneimittel erfolgt mittels
Liganden-Bindungsassays (Uterotropie- bzw. Hershberger-Assays (
In einer weiteren Ausführungsform werden mithilfe der erfindungsgemäßen Arzneimittel Hyperandrogenämie, Menopausale Kontinenzstörungen, menopause Hitzewallungen, die mit einer Hyperstimulation des hypothalamischen Gonadotropin Releasing Hormon-Pulsgenerators assoziiert sind oder zur Behandlung von menopause und klimakterischen Beschwerden (Frau) oder andropause Beschwerden (Mann) behandelt.In Another embodiment will be using the inventive Drug hyperandrogenemia, menopausal continence disorders, Menopause hot flashes with hyperstimulation of the hypothalamic Gonadotropin Releasing Hormone Pulse Generator are associated or for the treatment of menopause and climacteric complaints (woman) or andropause complaints (man).
In der Menopause kommt es zu einem Absinken der Estradiolspiegel in Folge des Erlöschen der Ovarialfunktion. Dies resultiert in einer Abschwächung proliferativer Prozesse und führt im Hypothalamus zu einer Verstärkung der Aktivität des GnRH-Pulsgenerators. (Der Gonadotropin-Releasing-Hormon-Pulsgenerator ist eine Art Taktgeber im Hypothalamus und taktet die pulsatile Ausschüttung von LH, wobei Steroide die Amplitude und die Frequenz beeinflussen.) Durch Überaktivität des hypothalamischen GnRH Pulsgenerators kommt es bei klimakterischen/postmenopausalen Frauen und bei andropausalen Männern zu zahlreichen psychovegetativen Beschwerden (Weitstellung der Hautgefäße, so genannte „hot flushes” mit nächtlichem Schwitzen).In Menopause causes a decrease in estradiol levels Consequence of the extinction of the ovarian function. This results in a weakening of proliferative processes and leads in the hypothalamus to increase the activity of the GnRH pulse generator. (The gonadotropin releasing hormone pulse generator is a kind of clock in the hypothalamus, clocking the pulsatile Distribution of LH, where steroids the amplitude and the Frequency.) Due to overactivity of the hypothalamic GnRH pulse generator occurs in climacteric / postmenopausal Women and in andropausal men to numerous psycho-vegetative Discomfort (dilation of the skin vessels, so-called "hot flushes "with nocturnal sweating).
In Abwesenheit genügend hohem Estradiolspiegel im Blut überwiegen im Knochengewebe die Aktivität der Osteoklasten und der Abbau der Knochenmasse, der mit erhöhter Bruchgefahr des Skelettes einhergeht. Gleichzeitig besteht langfristig die Gefahr der Plaquebildung im Gefäßsystem und damit das erhöhte Risiko von Infarkten.In Absence of sufficiently high estradiol levels in the blood outweigh in bone tissue the activity of osteoclasts and the Degradation of the bone mass, with increased risk of breakage of the Skeletons go along. At the same time there is danger in the long run the plaque formation in the vascular system and thus the increased risk of infarcts.
Die
Erfinder konnten in Tierversuchen günstige Wirkungen auf
klimakterische/postmenopausale/andropausale Symptome bzw Erkrankungen
mittels der erfindungsgemäßen Arzneimittel nachweisen.
Nachteilig ist, das Estrogene in ovarektomierten (ovx) Ratten das
Gewicht des Uterus stimulieren und Androgene in orchiektomierten
(orx) Ratten die Gewichte der Prostata und der Samenblase stimulieren
(
In einer weiteren Ausführungsform werden mithilfe der erfindungsgemäßen Arzneimittel alterstypische Hauterscheinungen behandelt.In Another embodiment will be using the inventive Medicines treated age-typical skin symptoms.
Im Rahmen dieser Erfindung werden unter „alterstypische Hauterscheinungen” solche Hauterscheinungen verstanden, wie z. B. Falten, Zellulite, Orangenhaut, Hautrötungen, pergamentähnliche Veränderungen, Alopezie, jedoch ist Zellulite bevorzugt. Zellulite ist eine nichtentzündliche, konstitutionell bedingte umschriebene Degeneration der kollagenen und elastischen Fasern des subkutanen Bindegewebes in der Oberschenkel- und Glutäalregion und geht einher zumeist mit Obesity.in the For the purposes of this invention, "age-typical skin manifestations" are those Skin symptoms understood, such as. As wrinkles, cellulite, orange peel, Skin redness, parchment-like changes, Alopecia, however, cellulite is preferred. Cellulite is a non-inflammatory, constitutionally conditioned circumscribed degeneration of collagen and elastic fibers of the subcutaneous connective tissue in the thigh and gluteal region and goes along mostly with obesity.
Alle
vorbenannten Indikationen sind z. B. im
In
der Beschreibung und den Ansprüchen gelten für
die einzelnen Substituenten folgende Definitionen:
Der Term „Alkyl” für
sich oder als Teil eines anderen Substituenten bedeutet ein lineares
oder verzweigtes Alkylketten-Radikal der jeweils angegebenen Länge
und optional eine CH2-Gruppe durch eine
Carbonylfunktion ersetzt sein kann. So bedeutet C1-4-Alkyl
z. B. Methyl, Ethyl, 1-Propyl, 2-Propyl, 2-Methyl-2-propyl, 2-Methyl-1-propyl,
1-Butyl, 2-Butyl, C1-6-Alkyl z. B. C1-4-Alkyl, Pentyl, 1-Pentyl, 2-Pentyl, 3-Pentyl,
1-Hexyl, 2-Hexyl, 3-Hexyl, 4-Methyl-1-Pentyl oder 3,3-Dimethyl-butyl.In the description and the claims, the following definitions apply to the individual substituents:
The term "alkyl" by itself or as part of another substituent means a linear or branched alkyl chain radical of the particular length given and optionally a CH 2 group may be replaced by a carbonyl. Thus, C 1-4 -alkyl z. Methyl, ethyl, 1-propyl, 2-propyl, 2-methyl-2-propyl, 2-methyl-1-propyl, 1-butyl, 2-butyl, C 1-6 alkyl e.g. C 1-4 alkyl, pentyl, 1-pentyl, 2-pentyl, 3-pentyl, 1-hexyl, 2-hexyl, 3-hexyl, 4-methyl-1-pentyl or 3,3-dimethyl-butyl ,
Der Term „Alkenyl” für sich oder als Teil eines anderen Substituenten bedeutet ein lineares oder verzweigtes Alkylketten-Radikal mit einer oder mehreren C=C-Doppelbindungen der jeweils angegebenen Länge, wobei mehrere Doppelbindungen bevorzugt konjugiert sind. So bedeutet C2-6-Alkenyl z. B. Ethenyl, 1-Propenyl, 2-Propenyl, 2-Methyl-2-propenyl, 2-Methyl-1-propenyl, 1-Butenyl, 2-Butenyl, 1,3-Butdienyl, 2,4-Butdienyl, 1-Pentenyl, 2-Pentenyl, 3-Pentenyl, 1,3-Pentdienyl, 2,4-Pentdienyl, 1,4-Pentdienyl, 1-Hexenyl, 2-Hexenyl, 1,3-Hediexyl, 4-Methyl-1-Pentenyl oder 3,3-Dimethyl-butenyl.The term "alkenyl" by itself or as part of another substituent means a linear or branched alkyl chain radical having one or more C = C double bonds of the respective length specified, wherein a plurality of double bonds are preferably conjugated. Thus, C 2-6 alkenyl z. Ethenyl, 1-propenyl, 2-propenyl, 2-methyl-2-propenyl, 2-methyl-1-propenyl, 1-butenyl, 2-butenyl, 1,3-butadienyl, 2,4-butadienyl, 1- Pentenyl, 2-pentenyl, 3-pentenyl, 1,3-pentadienyl, 2,4-pentadienyl, 1,4-pentadienyl, 1-hexenyl, 2-hexenyl, 1,3-hexyl, 4-methyl-1-pentenyl or 3,3-dimethyl-butenyl.
Der Term „Alkinyl” für sich oder als Teil eines anderen Substituenten bedeutet ein lineares oder verzweigtes Alkylketten-Radikal mit einer oder mehreren C-C-Dreifachbindungen der jeweils angegebenen Länge, wobei auch zusätzliche Doppelbindungen vorliegen können. So bedeutet C2-6-Alkinyl z. B. Ethinyl, 1-Propinyl, 2-Propinyl, 2-Methyl-2-propinyl, 2-Methyl-1-propinyl, 1-Butinyl, 2-Butinyl, 1-Pentinyl, 2-Pentinyl, 3-Pentinyl, 1,4-Pentdiinyl, 1-Pentin-4-enyl, 1-Hexinyl, 2-Hexinyl, 1,3-Hexdiinyl, 4-Methyl-1-pentinyl oder 3,3-Dimethyl-butinyl.The term "alkynyl", alone or as part of another substituent, means a linear or branched alkyl chain radical having one or more C-C triple bonds of the particular length indicated, it also being possible for additional double bonds to be present. Thus, C 2-6 -alkynyl z. Ethynyl, 1-propynyl, 2-propynyl, 2-methyl-2-propynyl, 2-methyl-1-propynyl, 1-butynyl, 2-butynyl, 1-pentynyl, 2-pentynyl, 3-pentynyl, 1, 4-pentdiinyl, 1-pentyne-4-enyl, 1-hexynyl, 2-hexynyl, 1,3-hexdiynyl, 4-methyl-1-pentynyl or 3,3-dimethylbutynyl.
Der Term „Cycloalkyl” für sich oder als Teil eines anderen Substituenten beinhaltet gesättigte, cyclische Kohlenwasserstoffgruppen, mit 3 bis 8 C-Atomen wie z. B. Cyclopropyl, Cyclobutyl, Cyclopentyl, Cyclohexyl, 4-Methyl-cyclohexyl, Cyclohexylmethylen, Cycloheptyl oder Cyclooctyl, als auch Heterocycloalkyl wie folgt definiert.Of the Term "cycloalkyl" alone or as part another substituent includes saturated, cyclic Hydrocarbon groups, having 3 to 8 carbon atoms such as. Cyclopropyl, Cyclobutyl, cyclopentyl, cyclohexyl, 4-methylcyclohexyl, cyclohexylmethylene, Cycloheptyl or cyclooctyl, as well as heterocycloalkyl as follows Are defined.
Die Verbindungen der Formel I oder Formel IIA bzw. IIB können als solche oder falls sie acidische oder basische Gruppen aufweisen in Form ihrer Salze mit physiologisch verträglichen Basen oder Säuren vorliegen. Beispiele für solche Säuren sind: Salzsäure, Zitronensäure, Trifluoressigsäure, Weinsäure, Milchsäure, Phosphorsäure, Methansulfonsäure, Essigsäure, Ameisensäure, Maleinsäure, Fumarsäure, Bernsteinsäure, Hydroxybernsteinsäure, Schwefelsäure, Glutarsäure, Asparaginsäure, Brenztraubensäure, Benzoesäure, Glucuronsäure, Oxalsäure, Ascorbinsäure und Acetylglycin. Beispiele für Basen sind Alkaliionen, bevorzugt Na, K, Erdalkaliionen, bevorzugt Ca, Mg, Ammoniumionen.The Compounds of the formula I or formula IIA or IIB can as such or if they have acidic or basic groups in the form of their salts with physiologically acceptable bases or acids. Examples of such acids are: hydrochloric acid, citric acid, trifluoroacetic acid, Tartaric acid, lactic acid, phosphoric acid, Methanesulfonic acid, acetic acid, formic acid, Maleic acid, fumaric acid, succinic acid, Malic acid, sulfuric acid, glutaric acid, Aspartic acid, pyruvic acid, benzoic acid, Glucuronic acid, oxalic acid, ascorbic acid and acetylglycine. Examples of bases are alkali metal ions, preferably Na, K, alkaline earth ions, preferably Ca, Mg, ammonium ions.
Ebenfalls können die erfindungsgemäßen Verbindungen in Form von Einschlussverbindungen vorliegen, wie Cyclodextrin, insbesondere alpha-Cyclodextrin.Also can the compounds of the invention in the form of inclusion compounds, such as cyclodextrin, especially alpha-cyclodextrin.
Die erfindungsgemäßen Verbindungen können in üblicher Weise oral verabfolgt werden. Die Applikation kann auch i. v., i. m., mit Dämpfen oder Sprays durch den Nasen-Rachenraum erfolgen.The Compounds according to the invention can be administered orally in the usual way. The application can i. v., i. m., with steaming or sprays through the Nasopharynx done.
Die Dosierung hängt vom Alter, Zustand und Gewicht des Patienten sowie von der Applikationsart ab. In der Regel beträgt die tägliche Wirkstoffdosis pro Person zwischen etwa 0,1 μg/kg und 1 g/kg bei oraler Gabe. Diese Dosis kann in 2 bis 4 Einzeldosen oder einmalig am Tag als Slow-release-Form gegeben werden.The Dosage depends on the age, condition and weight of the patient as well as the type of application. Usually amounts to the daily dose of active ingredient per person between about 0.1 μg / kg and 1 g / kg when given orally. This dose can be taken in 2 to 4 single doses or once a day as a slow-release form.
Die
neuen Verbindungen können in den gebräuchlichen
galenischen Applikationsformen fest oder flüssig angewendet
werden, z. B. als Tabletten, Filmtabletten, Kapseln, Pulver, Granulate,
Dragees, Lösungen, oder Sprays. Diese werden in üblicher
Weise hergestellt. Die Wirkstoffe können dabei mit den üblichen
galenischen Hilfsmitteln wie Tablettenbindern, Füllstoffen,
Konservierungsmitteln, Tablettensprengmitteln, Fließreguliermitteln,
Weichmachern, Netzmitteln, Dispergiermitteln, Emulgatoren, Lösungsmitteln,
Retardierungsmitteln, Antioxidantien und/oder Treibgasen verarbeitet
werden (vgl:
In einer weiteren Ausführungsform der Erfindung betrifft die Erfindung ebenfalls Pflanzen oder Pflanzenextrakte, die eine Verbindung nach Formel I oder Formel IIA und/oder IIB enthalten.In Another embodiment of the invention relates to Invention also plants or plant extracts containing a compound according to formula I or formula IIA and / or IIB.
Insbesondere betrifft die Erfindung solche Fraktionen von Pflanzenextrakten, die eine Verbindung nach Formel I oder Formel IIA bzw. Formel IIB enthalten.Especially the invention relates to such fractions of plant extracts, the one compound of formula I or formula IIA or formula IIB contain.
Die Pflanzenextrakte können in üblicher Weise mit wässrigen, ethanolischen, Lösungsmitteln verschiedener Polarität aus dem pflanzlichen Rohmaterial oder der Pflanzendroge erhalten werden und ggfs. weiter mit Lösungsmitteln aufgearbeitet oder angereichert werden.The Plant extracts can in the usual way with aqueous, ethanolic, solvents of various Polarity from the vegetable raw material or the plant drug be obtained and, if necessary, further worked up with solvents or enriched.
Daher betrifft die Erfindung ebenfalls ein Arzneimittel enthaltend mindestens eine Verbindung nach Formel I insbesondere eine Verbindung nach Formel IIA oder Formel IIB oder dessen Stereoisomere, Tautomere und deren physiologisch verträglichen Salze in einem Pflanzenextrakt oder Pflanzen. Bevorzugte Pflanzen, die zumindest einen Anteil, Gehalt an Formel IIA oder Formel IIB sind Tinospora cordiofolia, Helleborus foetdissima, Silene pusilla, Spinatia oleacia, Polypodium vulgare. Erfindungsgemäß umfasst sind alle Pflanzen und Extrakte, die mindestens einen Gehalt von 1 bis 500 μg/kg oder mehr an Formel IIA oder Formel IIB aufweisen.Therefore The invention also relates to a medicament containing at least a compound according to formula I, in particular a compound according to Formula IIA or Formula IIB or its stereoisomers, tautomers and their physiologically acceptable salts in a plant extract or plants. Preferred plants containing at least a proportion, Content of formula IIA or formula IIB are Tinospora cordiofolia, Helleborus foetdissima, Silene pusilla, Spinatia oleacia, Polypodium vulgare. According to the invention includes all plants and Extracts containing at least 1 to 500 μg / kg or more of Formula IIA or Formula IIB.
In einer weiteren Ausführungsform betrifft die Erfindung ein Nahrungsergänzungsmittel, insbesondere ein Functional Food, enthaltend einen erfindungsgemäßen Pflanzenextrakt oder eine Pflanze, vorzugsweise ausgewählt aus der Gruppe Tinospora cordiofolia, Helleborus foetdissima, Silene pusilla, Spinatia oleacia, Polypodium vulgare.In a further embodiment, the invention relates to a dietary supplement, in particular a functional food containing a plant extract according to the invention or a plant, preferably selected from the group Tinospora cordiofolia, Helleborus foetdissima, Silene pusilla, Spinatia oleacia, Polypodium vulgare.
Ein solches Nahrungsergänzungsmittel kann ein weiteres Nahrungsmittel ergänzen, wie z. B. Milch, Calziumhaltige Mittel, Brot und andere.One Such supplements can be another food supplement, such. Milk, calcium-containing agents, bread and other.
Weiterhin kann es in Form einer Zubereitung (Soßen, Getränk, Fertigpulver) verabreicht werden. Ebenfalls können pharmazeutische Formulierungen, wie oben dargelegt, entsprechend adaptiert werden.Farther may it be in the form of a preparation (sauces, drink, Finished powder). Also can be pharmaceutical Formulations, as stated above, adapted accordingly.
Nachfolgende Beispiele und Figuren dienen zur Erläuterung der Erfindung, ohne die Erfindung auf diese Beispiele einzuschränken.subsequent Examples and figures serve to illustrate the invention, without limiting the invention to these examples.
Beispiele:Examples:
- Ecd = Ecdyson (Formel IIA) und E2 = beta Ecdyson (Formel IIB)Ecd = ecdysone (formula IIA) and E2 = beta ecdysone (formula IIB)
Zum Studium div. alterstypischer Leiden wurden weibliche oder männliche Ratten kastriert. Vor Kastration und nach 3-monatiger oraler Gabe von Ecd wurden zahlreiche Organ- und Blutuntersuchungen durchgeführt.To the Studies of various age-related conditions were female or male Castrated rats. Before castration and after 3 months of oral administration Ecd has performed numerous organ and blood tests.
Zu Kontrollzwecken wurden scheinbehandelte, kastrierte Tiere als Negativkontrollen mitgeführt. Positive Kontrollen waren intakte männliche und E2-behandelte ovariektomierte (ovx) Tiere.To For control purposes, sham-treated, castrated animals were negative controls carried. Positive controls were intact male and E2-treated ovariectomized (ovx) animals.
Vor
Kastration und nach 3-monatiger Gabe der Testsubstanzen wurden mittels
quantitativer Computertomographie (
- – Corticale und spongiöse Knochendichten in der Metaphyse der Tibia,
- – die Größe diverser Fettdepots.
- Cortical and cancellous bone densities in the metaphysis of the tibia,
- - the size of various fat deposits.
Weibliche Sprague-Dawley Ratten (3 Monate alt, ca. 250g schwer) wurden ovariektomiert (ovx) und mit einem Tinospora cordiofolia-haltigen Extrakt, mit 20 OH-Ecdyson (β-Ecdyson = Ecd)) oder mit Estradiol 17β („E2”) (Positivkontrollen) getestet. Die Testsubstanzen waren dem Soja-freien Futter beigemengt. Negativkontrollen erhielten Soja-freies Haltungsfutter.Female Sprague-Dawley rats (3 months old, about 250g in weight) were ovariectomized (ovx) and with a Tinospora cordiofolia-containing extract, with 20 OH-ecdysone (β-ecdysone = ecd)) or with estradiol 17β ("E2") (Positive controls) tested. The test substances were soy-free Added food. Negative controls were obtained from soy-free diet.
Nach 3-monatiger Applikation wurden die Tiere getötet, diverse Organe sowie Blut asserviert.To The animals were killed for 3 months, various Organs and blood asserved.
Beispiel 1: Indikation Metabolisches SyndromExample 1: Indication metabolic syndrome
Das metabolische Syndrom ist gekennzeichnet durch Fettleibigkeit (Obesitas). Auch Ratten werden nach Ovariektomie (ovx) fett und dadurch erheblich schwerer als gleichaltrige E2 behandelte positive Kontrolltiere. Das reflektiert sich in der Größe div. Fettdepots. E2 reduziert die Größe der Fettdepots. Die Behandlung mit den erfindungsgemäßen Verbindungen oder entsprechenden Pflanzenextrakten reduziert die Größe der Fettdepots signifikant.The Metabolic syndrome is characterized by obesity (obesity). Even rats become fat after ovariectomy (ovx) and thus considerably heavier than age-matched E2 treated positive control animals. This is reflected in the size of various fat deposits. E2 reduces the size of the fat deposits. Treatment with the compounds of the invention or corresponding Plant extracts reduces the size of fat deposits significant.
Im
Ergebnis reduziert Ecd die abdominellen Fettdepots (
Ecd hat keinen signifikanten Effekt auf die LDL, erhöht die HDL und senkt Cholesterin und die Triglyceride signifikant.ecd has no significant effect on the LDL, which increases HDL and significantly lowers cholesterol and triglycerides.
Beispiel 2: Indikation Arteriosklerose, HypertonusExample 2 Indication Arteriosclerosis, hypertension
Eine Arteriosklerose und als Folge dieser ein Hypertonus entwickelt sich bei ungünstigem Verhältnis von HDL (die „guten” Lipide) zu LDL und zu den Triglyceriden (beides sind „schlechte” = atherogene Lipide).A Atherosclerosis and as a result of this a hypertonicity develops at unfavorable ratio of HDL (the "good" lipids) to LDL and triglycerides (both are "bad" = atherogenic lipids).
Nach 3-monatiger Therapie mit E2 ist das Gesamtcholesterin und die LDL gesenkt, jedoch die „ganz schlechten” Triglyceride erhöht.To 3 months of E2 therapy is total cholesterol and LDL lowered, but the "very bad" triglycerides elevated.
Ecd
hat keinen signifikanten Effekt auf die LDL, erhöht vorteilhaft
die HDL und senkt Cholesterin und die Triglyceride signifikant (
Beispiel 3: Indikation OsteoporoseExample 3: Indication Osteoporosis
Ovariektomierte
(ovx) Tiere verlieren innerhalb von 3 Monaten über 50%
ihrer Knochenmasse (gemessen mit quantitativer Computertomographie,
An
einer Osteoblasten-Zellinie, den sogenannten SAOS-Zellen, konnte
ebenfalls eine Wirkung gezeigt werden, die der von Östradiol-17-beta
entspricht. Es sei nochmals betont, dass diese Ecdyson-Wirkung keinesfalls über Östrogenrezeptoren
mediiert wird. Ecd hemmt die Aktivität von Osteoclasten
und fördert die Aktivität von Osteoblasten (
Beispiel 4: Indikation OsteoarthritisExample 4: Indication Osteoarthritis
Die Osteoarthritis ist bedingt durch Abnahme von Knorpelmasse in Gelenkspalten. Die Proliferation von Knorpelzellen wird in vitro und in vivo durch E2 stimuliert. Auch Ecd stimuliert Proliferation von Knorpelzellen im Kniegelenk.The Osteoarthritis is caused by decrease of cartilage mass in joint space. The proliferation of cartilage cells is performed in vitro and in vivo E2 stimulates. Ecd also stimulates proliferation of cartilage cells in the knee joint.
Ecd
hemmt die Aktivität von Osteoclasten und fördert
die Aktivität von Osteoblasten. Dies ist in den
Beispiel 5: Indikation klimakterische/menopause BeschwerdenExample 5: Indication climacteric / menopause complaints
Eine
Reduktion der LH-Spiegel im Blut ist ein Hinweis auf eine günstige
Wirkung von Ecd auf Hot Flushes (
Beispiel 6: Indikation AnämieExample 6: Indication Anemia
Bei
der morphometrischen Aufarbeitung histologischer Knochenpräparate
wurde ebenfalls das rote Knochenmark gemessen. Sowohl E2 als auch
Ecd in allen Dosierungen erhöht die Fläche des
roten Knochenmarks signifikant (
Beispiel 7: Indikation InkontinenzExample 7: Indication incontinence
Ursache der Stress-Inkontinenz ist die Erschlaffung der Beckenbodenmuskulatur. E2 und Ecd bewirkt eine Zunahme der Muskulatur im Schließmuskel (Rhabdosphinkter) Harnblaseder.reason Stress incontinence is the relaxation of the pelvic floor muscles. E2 and ecd causes an increase in the muscles in the sphincter (Rhabdosphincter) urinary bladder.
Die Stressinkontinenz ist Folge der Senkung des Beckenbodens unter anderem auf der Basis erschlaffender Beckenbodenmuskulatur.The Stress incontinence is the result of lowering the pelvic floor among others on the basis of relaxed pelvic floor muscles.
Muskelstärkende
Maßnahmen haben hier zu signifikanten Verbesserungen geführt.
Da E2 den gesamten Muskelapparat stärkt, ist auch die Beckenbodenmuskulatur
günstig beeinflusst, mit der Folge der Verbesserung der
Stressinkontinenz. Die Erfinder haben die ovx Ratte als Modell zum
Studium der Urge-Inkontinenz entwickelt. Über konzentrisch
verlaufende biluminale Katheter mit Auslässen in Blase
und Sphincter urethrae können die Erfinder die Blase füllen
und Blasen- und Urethra Drucke zur Urodynamik aufzeichnen (
Beispiel 8: Indikation alterstypische HauterscheinungenExample 8: Indication age-typical skin lesions
Wie
bereits in Beispiel 1 führt Ecd zum Fettabbau bei. Weitere
Untersuchungen zeigen ebenfalls, dass Ecd die Abnahme der Epidermisdicke
verhindert (
ZITATE ENTHALTEN IN DER BESCHREIBUNGQUOTES INCLUDE IN THE DESCRIPTION
Diese Liste der vom Anmelder aufgeführten Dokumente wurde automatisiert erzeugt und ist ausschließlich zur besseren Information des Lesers aufgenommen. Die Liste ist nicht Bestandteil der deutschen Patent- bzw. Gebrauchsmusteranmeldung. Das DPMA übernimmt keinerlei Haftung für etwaige Fehler oder Auslassungen.This list The documents listed by the applicant have been automated generated and is solely for better information recorded by the reader. The list is not part of the German Patent or utility model application. The DPMA takes over no liability for any errors or omissions.
Zitierte Nicht-PatentliteraturCited non-patent literature
- - Organikum, 22. Auflage, Wiley-VCH, Weinheim, 2004 [0006] Organikum, 22nd Edition, Wiley-VCH, Weinheim, 2004 [0006]
- - W. Owens, E. Zeiger et al.: The OECD program to validate the rat Hershberger bioassay to screen compounds for in vivo androgen and antiandrogen responses. Phase 1: use of a potent agonist and a potent antagonist to test the standardized protocol. Environ. Health Perspect. (2006) 114, 8: S. 1259–1265 [0026] - W. Owens, E. Zeiger et al .: The OECD Hershberger bioassay to screen compounds for in vivo androgen and antiandrogen responses. Phase 1: use of a potent agonist and a potent antagonist to test the standardized protocol. Environ. Health Perspect. (2006) 114, 8: pp. 1259-1265 [0026]
- - Pschyrembel, Klinisches Wörterbuch, de Gruyter, Berlin (2007) [0033] - Pschyrembel, Clinical Dictionary, de Gruyter, Berlin (2007) [0033]
- - H. Sucker et al.: Pharmazeutische Technologie, Thieme-Verlag, Stuttgart, 1978 [0042] H. Sucker et al .: Pharmaceutical Technology, Thieme-Verlag, Stuttgart, 1978 [0042]
- - Journal für Mineralstoffwechsel 2002, 9 (4): 22–31 [0053] - Journal of Mineral Metabolism 2002, 9 (4): 22-31 [0053]
Claims (7)
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE200810050957 DE102008050957A1 (en) | 2008-10-10 | 2008-10-10 | New ecdysone compounds useful for treating age-related diseases such as osteoporosis, osteoarthritis, incontinence, obesity, arteriosclerosis, hypertonus, metabolic syndrome, anemias, hyperandrogenemia, cellulite and menopausal hot flushes |
| PCT/DE2009/001401 WO2010040345A2 (en) | 2008-10-10 | 2009-10-12 | Ecdysone derivatives and the use thereof |
| DE212009000115U DE212009000115U1 (en) | 2008-10-10 | 2009-10-12 | Ecdysone derivatives and their use |
| DE112009004836T DE112009004836A5 (en) | 2008-10-10 | 2009-10-12 | ECDYSONE DERIVATIVES AND THEIR USE |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE200810050957 DE102008050957A1 (en) | 2008-10-10 | 2008-10-10 | New ecdysone compounds useful for treating age-related diseases such as osteoporosis, osteoarthritis, incontinence, obesity, arteriosclerosis, hypertonus, metabolic syndrome, anemias, hyperandrogenemia, cellulite and menopausal hot flushes |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| DE102008050957A1 true DE102008050957A1 (en) | 2010-04-15 |
Family
ID=41821193
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE200810050957 Withdrawn DE102008050957A1 (en) | 2008-10-10 | 2008-10-10 | New ecdysone compounds useful for treating age-related diseases such as osteoporosis, osteoarthritis, incontinence, obesity, arteriosclerosis, hypertonus, metabolic syndrome, anemias, hyperandrogenemia, cellulite and menopausal hot flushes |
Country Status (1)
| Country | Link |
|---|---|
| DE (1) | DE102008050957A1 (en) |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1990003778A1 (en) * | 1988-10-03 | 1990-04-19 | Lvmh Recherche | Hydrated lipidic lamellar phases or liposomes based on ecdysteroids |
| US20050191385A1 (en) * | 2004-10-25 | 2005-09-01 | Amato Daniel K. | Natural product derivatives as food supplements and pharmaceuticals |
| US20080004496A1 (en) * | 2003-03-31 | 2008-01-03 | Naoki Hasegawa | Magnifying image pickup unit for an endoscope, an endoscope for in vivo cellular observation that uses it, and an endoscopic, in vivo cellular observation method |
-
2008
- 2008-10-10 DE DE200810050957 patent/DE102008050957A1/en not_active Withdrawn
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1990003778A1 (en) * | 1988-10-03 | 1990-04-19 | Lvmh Recherche | Hydrated lipidic lamellar phases or liposomes based on ecdysteroids |
| US20080004496A1 (en) * | 2003-03-31 | 2008-01-03 | Naoki Hasegawa | Magnifying image pickup unit for an endoscope, an endoscope for in vivo cellular observation that uses it, and an endoscopic, in vivo cellular observation method |
| US20050191385A1 (en) * | 2004-10-25 | 2005-09-01 | Amato Daniel K. | Natural product derivatives as food supplements and pharmaceuticals |
Non-Patent Citations (5)
| Title |
|---|
| H. Sucker et al.: Pharmazeutische Technologie, Thieme-Verlag, Stuttgart, 1978 |
| Journal für Mineralstoffwechsel 2002, 9 (4): 22-31 |
| Organikum, 22. Auflage, Wiley-VCH, Weinheim, 2004 |
| Pschyrembel, Klinisches Wörterbuch, de Gruyter, Berlin (2007) |
| W. Owens, E. Zeiger et al.: The OECD program to validate the rat Hershberger bioassay to screen compounds for in vivo androgen and antiandrogen responses. Phase 1: use of a potent agonist and a potent antagonist to test the standardized protocol. Environ. Health Perspect. (2006) 114, 8: S. 1259-1265 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE69008476T2 (en) | Pharmaceutical composition for the treatment of osteoporosis. | |
| DE68917219T2 (en) | Therapeutic product for the treatment of symptoms during or after the menopause. | |
| DE60001271T2 (en) | HYDROXYMATAIRESINOL IN CANCER PREVENTION | |
| DE69712642T2 (en) | TRANSDERMAL APPLICATION OF NATURAL STEROID HORMONES | |
| DE60318092T2 (en) | PHARMACEUTICAL COMPOSITION CONTAINING ESTETROL DERIVATIVES AND APPLICATION IN CANCER TREATMENT | |
| EP1011682A2 (en) | Hormonal contraceptive | |
| DE602005005165T2 (en) | PROCESS FOR IMPROVING THE BIOVERABILITY OF OSPEMIFES | |
| Yadav et al. | A review on herbal medicinal plant for treatment of polycystic ovarian syndrome (PCOS) | |
| US20070269538A1 (en) | Method for accelerating secretion of estrogen and regenerating tissue cells of female sexual organs | |
| DE10206390A1 (en) | Use of phytoestrogen-containing extracts that selectively modulate the estrogen receptor beta | |
| WO2011120925A1 (en) | Parenteral pharmaceutical form which releases aromatse inhibitor and gestagens, for the treatment of endometriosis | |
| DE3121152A1 (en) | "USE OF THE COMBINATION OF AN AROMATASE INHIBITOR WITH AN ANTIANDROGEN FOR PROPHYLAXIS AND THERAPY OF PROSTATE HYPERPLASIA" | |
| EP0799042A1 (en) | Compounds with progesterone-antagonistic and anti-oestrogen properties intended for combined use in female contraception | |
| DE60318447T2 (en) | PHARMACEUTICAL COMPOSITION CONTAINING ESTETROL DERIVATIVES AND APPLICATION IN CANCER TREATMENT | |
| EP1100509A1 (en) | Use of biogenic estrogen sulfamates for hormone replacement therapy | |
| DE212009000115U1 (en) | Ecdysone derivatives and their use | |
| EP1843745A1 (en) | Dosage forms of active ingredients containing hydroxystilbene for treating menopausal complaints | |
| WO1997032588A2 (en) | Combination of dehydroepiandrosterone and aromatase inhibitors and use of this combination to produce a medicament for treating relative and absolute androgen deficiency in men | |
| DE102009011264A1 (en) | New ecdysone compounds useful for treating age-related diseases such as osteoporosis, osteoarthritis, incontinence, obesity, arteriosclerosis, hypertonus, metabolic syndrome, anemias, hyperandrogenemia, cellulite and menopausal hot flushes | |
| DE69427815T2 (en) | OSTEOGENESIS PROMOTER AND AGENT AGAINST OSTEOPOROSE | |
| DE102008050957A1 (en) | New ecdysone compounds useful for treating age-related diseases such as osteoporosis, osteoarthritis, incontinence, obesity, arteriosclerosis, hypertonus, metabolic syndrome, anemias, hyperandrogenemia, cellulite and menopausal hot flushes | |
| Nandini et al. | Effect of extracts of Murraya koenigii spreng. and Morus alba linn. on the age of attainment of puberty and ovarian folliculogenesis in rats | |
| EP0442350B1 (en) | Medical preparation containing stigmasta-4-en-3-one and the use thereof | |
| EP1427430B1 (en) | Use of extracts of the genus cimicifuga as organoselective medicines for treating diseases of the genitourinary system caused by sex hormones | |
| WO1995005828A1 (en) | Progesterone-antagonistic and anti-oestrogen compounds for the therapy of leiomyomata uteri |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| OP8 | Request for examination as to paragraph 44 patent law | ||
| R118 | Application deemed withdrawn due to claim for domestic priority |
Effective date: 20110411 |