DE102005036542A1 - CTL prodrug - Google Patents
CTL prodrug Download PDFInfo
- Publication number
- DE102005036542A1 DE102005036542A1 DE102005036542A DE102005036542A DE102005036542A1 DE 102005036542 A1 DE102005036542 A1 DE 102005036542A1 DE 102005036542 A DE102005036542 A DE 102005036542A DE 102005036542 A DE102005036542 A DE 102005036542A DE 102005036542 A1 DE102005036542 A1 DE 102005036542A1
- Authority
- DE
- Germany
- Prior art keywords
- region
- polypeptide
- fasl
- receptor
- polypeptide according
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
- 239000000651 prodrug Substances 0.000 title description 42
- 229940002612 prodrug Drugs 0.000 title description 42
- 108090000765 processed proteins & peptides Proteins 0.000 claims abstract description 64
- 102000004196 processed proteins & peptides Human genes 0.000 claims abstract description 54
- 229920001184 polypeptide Polymers 0.000 claims abstract description 52
- 210000004027 cell Anatomy 0.000 claims abstract description 41
- 238000012545 processing Methods 0.000 claims abstract description 28
- 102000004127 Cytokines Human genes 0.000 claims abstract description 14
- 108090000695 Cytokines Proteins 0.000 claims abstract description 14
- 230000004071 biological effect Effects 0.000 claims abstract description 11
- 210000004899 c-terminal region Anatomy 0.000 claims abstract description 8
- 238000001727 in vivo Methods 0.000 claims abstract description 8
- 102000010834 Extracellular Matrix Proteins Human genes 0.000 claims abstract description 6
- 108010037362 Extracellular Matrix Proteins Proteins 0.000 claims abstract description 6
- 210000002744 extracellular matrix Anatomy 0.000 claims abstract description 6
- 229920002521 macromolecule Polymers 0.000 claims abstract description 4
- 206010028980 Neoplasm Diseases 0.000 claims description 35
- 239000003446 ligand Substances 0.000 claims description 26
- 102100040247 Tumor necrosis factor Human genes 0.000 claims description 25
- 230000027455 binding Effects 0.000 claims description 23
- 102000005962 receptors Human genes 0.000 claims description 22
- 108020003175 receptors Proteins 0.000 claims description 22
- 108091005804 Peptidases Proteins 0.000 claims description 21
- 239000004365 Protease Substances 0.000 claims description 21
- 108020004707 nucleic acids Proteins 0.000 claims description 14
- 102000039446 nucleic acids Human genes 0.000 claims description 14
- 150000007523 nucleic acids Chemical class 0.000 claims description 14
- 239000013598 vector Substances 0.000 claims description 14
- 108090000623 proteins and genes Proteins 0.000 claims description 13
- 239000012634 fragment Substances 0.000 claims description 12
- 102000004169 proteins and genes Human genes 0.000 claims description 12
- 239000008194 pharmaceutical composition Substances 0.000 claims description 11
- 125000003275 alpha amino acid group Chemical group 0.000 claims description 10
- 238000005829 trimerization reaction Methods 0.000 claims description 10
- 238000000034 method Methods 0.000 claims description 8
- 230000033115 angiogenesis Effects 0.000 claims description 7
- 238000003776 cleavage reaction Methods 0.000 claims description 7
- 230000014509 gene expression Effects 0.000 claims description 7
- 230000007017 scission Effects 0.000 claims description 7
- 239000011159 matrix material Substances 0.000 claims description 6
- 125000003729 nucleotide group Chemical group 0.000 claims description 6
- 102000003978 Tissue Plasminogen Activator Human genes 0.000 claims description 5
- 108090000373 Tissue Plasminogen Activator Proteins 0.000 claims description 5
- 102000003990 Urokinase-type plasminogen activator Human genes 0.000 claims description 5
- 108090000435 Urokinase-type plasminogen activator Proteins 0.000 claims description 5
- 108010052621 fas Receptor Proteins 0.000 claims description 5
- 102000018823 fas Receptor Human genes 0.000 claims description 5
- 239000002773 nucleotide Substances 0.000 claims description 5
- 230000008569 process Effects 0.000 claims description 5
- 229960000187 tissue plasminogen activator Drugs 0.000 claims description 5
- 108010006035 Metalloproteases Proteins 0.000 claims description 4
- 102000005741 Metalloproteases Human genes 0.000 claims description 4
- 241001529936 Murinae Species 0.000 claims description 4
- 150000001875 compounds Chemical class 0.000 claims description 4
- 239000001963 growth medium Substances 0.000 claims description 4
- 230000003902 lesion Effects 0.000 claims description 4
- 230000008807 pathological lesion Effects 0.000 claims description 4
- 238000002360 preparation method Methods 0.000 claims description 4
- 230000001225 therapeutic effect Effects 0.000 claims description 4
- 108010054265 Factor VIIa Proteins 0.000 claims description 3
- 102000008394 Immunoglobulin Fragments Human genes 0.000 claims description 3
- 108010021625 Immunoglobulin Fragments Proteins 0.000 claims description 3
- 241000700605 Viruses Species 0.000 claims description 3
- 230000003993 interaction Effects 0.000 claims description 3
- 102000015212 Fas Ligand Protein Human genes 0.000 claims description 2
- 108010039471 Fas Ligand Protein Proteins 0.000 claims description 2
- 102000001706 Immunoglobulin Fab Fragments Human genes 0.000 claims description 2
- 108010054477 Immunoglobulin Fab Fragments Proteins 0.000 claims description 2
- 108060008683 Tumor Necrosis Factor Receptor Proteins 0.000 claims description 2
- 239000000443 aerosol Substances 0.000 claims description 2
- 230000003321 amplification Effects 0.000 claims description 2
- 201000011510 cancer Diseases 0.000 claims description 2
- 239000000969 carrier Substances 0.000 claims description 2
- 108010057085 cytokine receptors Proteins 0.000 claims description 2
- 102000003675 cytokine receptors Human genes 0.000 claims description 2
- 239000003085 diluting agent Substances 0.000 claims description 2
- 210000002889 endothelial cell Anatomy 0.000 claims description 2
- 210000003527 eukaryotic cell Anatomy 0.000 claims description 2
- 239000007788 liquid Substances 0.000 claims description 2
- 238000003199 nucleic acid amplification method Methods 0.000 claims description 2
- 239000000546 pharmaceutical excipient Substances 0.000 claims description 2
- 210000001236 prokaryotic cell Anatomy 0.000 claims description 2
- 230000002062 proliferating effect Effects 0.000 claims description 2
- 239000007787 solid Substances 0.000 claims description 2
- 210000004881 tumor cell Anatomy 0.000 claims description 2
- 102000003298 tumor necrosis factor receptor Human genes 0.000 claims description 2
- 102100037486 Reverse transcriptase/ribonuclease H Human genes 0.000 claims 3
- 102100031988 Tumor necrosis factor ligand superfamily member 6 Human genes 0.000 claims 2
- 108050002568 Tumor necrosis factor ligand superfamily member 6 Proteins 0.000 claims 2
- 230000000890 antigenic effect Effects 0.000 claims 1
- 210000000170 cell membrane Anatomy 0.000 claims 1
- 238000012258 culturing Methods 0.000 claims 1
- 230000000259 anti-tumor effect Effects 0.000 abstract description 5
- 230000002401 inhibitory effect Effects 0.000 abstract description 3
- 230000002519 immonomodulatory effect Effects 0.000 abstract description 2
- 101710088083 Glomulin Proteins 0.000 description 19
- 102100023832 Prolyl endopeptidase FAP Human genes 0.000 description 19
- 102000035195 Peptidases Human genes 0.000 description 18
- 230000000694 effects Effects 0.000 description 18
- 102000037865 fusion proteins Human genes 0.000 description 16
- 108020001507 fusion proteins Proteins 0.000 description 16
- 230000008685 targeting Effects 0.000 description 14
- 239000003112 inhibitor Substances 0.000 description 13
- 230000004913 activation Effects 0.000 description 9
- 150000001413 amino acids Chemical class 0.000 description 7
- 230000001419 dependent effect Effects 0.000 description 7
- 238000006467 substitution reaction Methods 0.000 description 6
- 210000001519 tissue Anatomy 0.000 description 6
- 239000013543 active substance Substances 0.000 description 5
- 230000001404 mediated effect Effects 0.000 description 5
- 102100038126 Tenascin Human genes 0.000 description 4
- 239000012528 membrane Substances 0.000 description 4
- 239000000126 substance Substances 0.000 description 4
- 230000009885 systemic effect Effects 0.000 description 4
- 108090001007 Interleukin-8 Proteins 0.000 description 3
- 108010076504 Protein Sorting Signals Proteins 0.000 description 3
- 238000007792 addition Methods 0.000 description 3
- 230000002776 aggregation Effects 0.000 description 3
- 238000004220 aggregation Methods 0.000 description 3
- 230000001413 cellular effect Effects 0.000 description 3
- 238000010276 construction Methods 0.000 description 3
- 238000012217 deletion Methods 0.000 description 3
- 230000037430 deletion Effects 0.000 description 3
- 230000003211 malignant effect Effects 0.000 description 3
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 2
- 102100026802 72 kDa type IV collagenase Human genes 0.000 description 2
- 102000014914 Carrier Proteins Human genes 0.000 description 2
- 102000004190 Enzymes Human genes 0.000 description 2
- 108090000790 Enzymes Proteins 0.000 description 2
- 241000238631 Hexapoda Species 0.000 description 2
- 241000235058 Komagataella pastoris Species 0.000 description 2
- 102100030412 Matrix metalloproteinase-9 Human genes 0.000 description 2
- 108010015302 Matrix metalloproteinase-9 Proteins 0.000 description 2
- 206010027476 Metastases Diseases 0.000 description 2
- 102000046283 TNF-Related Apoptosis-Inducing Ligand Human genes 0.000 description 2
- 102000007000 Tenascin Human genes 0.000 description 2
- 108010008125 Tenascin Proteins 0.000 description 2
- 108091008605 VEGF receptors Proteins 0.000 description 2
- 102100033177 Vascular endothelial growth factor receptor 2 Human genes 0.000 description 2
- 230000009471 action Effects 0.000 description 2
- 239000000427 antigen Substances 0.000 description 2
- 102000036639 antigens Human genes 0.000 description 2
- 108091007433 antigens Proteins 0.000 description 2
- 230000006907 apoptotic process Effects 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- 108091008324 binding proteins Proteins 0.000 description 2
- 238000006243 chemical reaction Methods 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 238000004140 cleaning Methods 0.000 description 2
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 2
- 208000035475 disorder Diseases 0.000 description 2
- 210000003038 endothelium Anatomy 0.000 description 2
- 238000005516 engineering process Methods 0.000 description 2
- 229940088598 enzyme Drugs 0.000 description 2
- 230000004927 fusion Effects 0.000 description 2
- NITYDPDXAAFEIT-DYVFJYSZSA-N ilomastat Chemical compound C1=CC=C2C(C[C@@H](C(=O)NC)NC(=O)[C@H](CC(C)C)CC(=O)NO)=CNC2=C1 NITYDPDXAAFEIT-DYVFJYSZSA-N 0.000 description 2
- 229960003696 ilomastat Drugs 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- 230000021995 interleukin-8 production Effects 0.000 description 2
- 230000009878 intermolecular interaction Effects 0.000 description 2
- 238000001990 intravenous administration Methods 0.000 description 2
- 210000004962 mammalian cell Anatomy 0.000 description 2
- 230000004987 nonapoptotic effect Effects 0.000 description 2
- 239000002243 precursor Substances 0.000 description 2
- 239000000047 product Substances 0.000 description 2
- 230000006337 proteolytic cleavage Effects 0.000 description 2
- 230000028327 secretion Effects 0.000 description 2
- 239000006228 supernatant Substances 0.000 description 2
- 238000001262 western blot Methods 0.000 description 2
- BUHVIAUBTBOHAG-FOYDDCNASA-N (2r,3r,4s,5r)-2-[6-[[2-(3,5-dimethoxyphenyl)-2-(2-methylphenyl)ethyl]amino]purin-9-yl]-5-(hydroxymethyl)oxolane-3,4-diol Chemical compound COC1=CC(OC)=CC(C(CNC=2C=3N=CN(C=3N=CN=2)[C@H]2[C@@H]([C@H](O)[C@@H](CO)O2)O)C=2C(=CC=CC=2)C)=C1 BUHVIAUBTBOHAG-FOYDDCNASA-N 0.000 description 1
- 101710151806 72 kDa type IV collagenase Proteins 0.000 description 1
- 125000001433 C-terminal amino-acid group Chemical group 0.000 description 1
- 108010029697 CD40 Ligand Proteins 0.000 description 1
- 101150013553 CD40 gene Proteins 0.000 description 1
- 102100032937 CD40 ligand Human genes 0.000 description 1
- 201000009030 Carcinoma Diseases 0.000 description 1
- 108091026890 Coding region Proteins 0.000 description 1
- 208000035473 Communicable disease Diseases 0.000 description 1
- 206010013710 Drug interaction Diseases 0.000 description 1
- 238000002965 ELISA Methods 0.000 description 1
- 102100038083 Endosialin Human genes 0.000 description 1
- 101710144543 Endosialin Proteins 0.000 description 1
- 108010067306 Fibronectins Proteins 0.000 description 1
- 102000016359 Fibronectins Human genes 0.000 description 1
- 241000287828 Gallus gallus Species 0.000 description 1
- 102100041003 Glutamate carboxypeptidase 2 Human genes 0.000 description 1
- 102100024025 Heparanase Human genes 0.000 description 1
- 206010019663 Hepatic failure Diseases 0.000 description 1
- 101000627872 Homo sapiens 72 kDa type IV collagenase Proteins 0.000 description 1
- 101000892862 Homo sapiens Glutamate carboxypeptidase 2 Proteins 0.000 description 1
- 108010047852 Integrin alphaVbeta3 Proteins 0.000 description 1
- 229940124761 MMP inhibitor Drugs 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- 108091028043 Nucleic acid sequence Proteins 0.000 description 1
- 206010060862 Prostate cancer Diseases 0.000 description 1
- 208000000236 Prostatic Neoplasms Diseases 0.000 description 1
- 102000001708 Protein Isoforms Human genes 0.000 description 1
- 108010029485 Protein Isoforms Proteins 0.000 description 1
- 102000007056 Recombinant Fusion Proteins Human genes 0.000 description 1
- 108010008281 Recombinant Fusion Proteins Proteins 0.000 description 1
- 108091028664 Ribonucleotide Proteins 0.000 description 1
- 240000004808 Saccharomyces cerevisiae Species 0.000 description 1
- 101100221606 Saccharomyces cerevisiae (strain ATCC 204508 / S288c) COS7 gene Proteins 0.000 description 1
- 206010039491 Sarcoma Diseases 0.000 description 1
- 102100040245 Tumor necrosis factor receptor superfamily member 5 Human genes 0.000 description 1
- 102000005789 Vascular Endothelial Growth Factors Human genes 0.000 description 1
- 108010019530 Vascular Endothelial Growth Factors Proteins 0.000 description 1
- 239000004480 active ingredient Substances 0.000 description 1
- 230000001154 acute effect Effects 0.000 description 1
- 230000004931 aggregating effect Effects 0.000 description 1
- 230000006229 amino acid addition Effects 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- 239000012867 bioactive agent Substances 0.000 description 1
- 230000000975 bioactive effect Effects 0.000 description 1
- 230000008436 biogenesis Effects 0.000 description 1
- 230000000903 blocking effect Effects 0.000 description 1
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 1
- 230000030833 cell death Effects 0.000 description 1
- 210000004978 chinese hamster ovary cell Anatomy 0.000 description 1
- 230000006552 constitutive activation Effects 0.000 description 1
- 238000004132 cross linking Methods 0.000 description 1
- 210000004748 cultured cell Anatomy 0.000 description 1
- 239000005547 deoxyribonucleotide Substances 0.000 description 1
- 125000002637 deoxyribonucleotide group Chemical group 0.000 description 1
- 239000003814 drug Substances 0.000 description 1
- 239000003623 enhancer Substances 0.000 description 1
- 239000013604 expression vector Substances 0.000 description 1
- 229940012414 factor viia Drugs 0.000 description 1
- 210000002950 fibroblast Anatomy 0.000 description 1
- MHMNJMPURVTYEJ-UHFFFAOYSA-N fluorescein-5-isothiocyanate Chemical compound O1C(=O)C2=CC(N=C=S)=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 MHMNJMPURVTYEJ-UHFFFAOYSA-N 0.000 description 1
- 238000001943 fluorescence-activated cell sorting Methods 0.000 description 1
- 238000001502 gel electrophoresis Methods 0.000 description 1
- 230000013595 glycosylation Effects 0.000 description 1
- 238000006206 glycosylation reaction Methods 0.000 description 1
- 108010037536 heparanase Proteins 0.000 description 1
- 210000003494 hepatocyte Anatomy 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 230000000415 inactivating effect Effects 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 230000006698 induction Effects 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- 230000010354 integration Effects 0.000 description 1
- 238000001361 intraarterial administration Methods 0.000 description 1
- 230000008863 intramolecular interaction Effects 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000002372 labelling Methods 0.000 description 1
- 108020001756 ligand binding domains Proteins 0.000 description 1
- 208000007903 liver failure Diseases 0.000 description 1
- 231100000835 liver failure Toxicity 0.000 description 1
- 230000014759 maintenance of location Effects 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 239000002609 medium Substances 0.000 description 1
- 201000001441 melanoma Diseases 0.000 description 1
- 208000030159 metabolic disease Diseases 0.000 description 1
- 230000009401 metastasis Effects 0.000 description 1
- 239000000203 mixture Substances 0.000 description 1
- 239000000178 monomer Substances 0.000 description 1
- 208000013435 necrotic lesion Diseases 0.000 description 1
- 239000013642 negative control Substances 0.000 description 1
- 230000001575 pathological effect Effects 0.000 description 1
- 230000010412 perfusion Effects 0.000 description 1
- 229920001481 poly(stearyl methacrylate) Polymers 0.000 description 1
- 239000013641 positive control Substances 0.000 description 1
- 230000004481 post-translational protein modification Effects 0.000 description 1
- 238000004321 preservation Methods 0.000 description 1
- 108020001580 protein domains Proteins 0.000 description 1
- 230000017854 proteolysis Effects 0.000 description 1
- 230000002797 proteolythic effect Effects 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 239000002336 ribonucleotide Substances 0.000 description 1
- 125000002652 ribonucleotide group Chemical group 0.000 description 1
- 210000002966 serum Anatomy 0.000 description 1
- 230000019491 signal transduction Effects 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 230000002269 spontaneous effect Effects 0.000 description 1
- 230000006641 stabilisation Effects 0.000 description 1
- 238000011105 stabilization Methods 0.000 description 1
- 210000002536 stromal cell Anatomy 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- 230000000699 topical effect Effects 0.000 description 1
- 238000013518 transcription Methods 0.000 description 1
- 230000035897 transcription Effects 0.000 description 1
- 230000002103 transcriptional effect Effects 0.000 description 1
- 230000010474 transient expression Effects 0.000 description 1
- 239000013638 trimer Substances 0.000 description 1
- 210000005166 vasculature Anatomy 0.000 description 1
- 230000003612 virological effect Effects 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
- C07K14/70575—NGF/TNF-superfamily, e.g. CD70, CD95L, CD153, CD154
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6835—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site
- A61K47/6849—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a receptor, a cell surface antigen or a cell surface determinant
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/01—Fusion polypeptide containing a localisation/targetting motif
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/30—Non-immunoglobulin-derived peptide or protein having an immunoglobulin constant or Fc region, or a fragment thereof, attached thereto
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Immunology (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Cell Biology (AREA)
- Public Health (AREA)
- Gastroenterology & Hepatology (AREA)
- Biophysics (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Toxicology (AREA)
- Zoology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Biochemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Genetics & Genomics (AREA)
- Molecular Biology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Epidemiology (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Peptides Or Proteins (AREA)
Abstract
Die vorliegende Erfindung betrifft ein Polypeptid mit vorzugsweise antitumoralen und/oder immunmodulierenden Zytokineigenschaften, welches durch Prozessierung in vivo aktivierbar ist, umfassend eine C-terminale Region mit spezifischer biologischer Aktivität, an dessen N-terminalen Ende eine inhibitorische Region, eine Region mit einer Prozessierungsstelle und eine Region, die ein Makromolekül auf einer Zelloberfläche oder eine Komponente der extrazellulären Matrix selektiv erkennt, angeordnet ist.The The present invention relates to a polypeptide having preferably antitumoral and / or immunomodulatory cytokine properties by Processing in vivo is activatable comprising a C-terminal Region of specific biological activity at the N-terminal end an inhibitory region, a region with a processing site and a region containing a macromolecule on a cell surface or a component of the extracellular Matrix selectively recognizes, is arranged.
Description
Die vorliegende Erfindung betrifft ein Polypeptid mit vorzugsweise antitumoralen und/oder immunmodulierenden Zytokineigenschaften, welches durch Prozessierung in vivo aktivierbar ist, umfassend eine C-terminale Region mit spezifischer biologischer Aktivität, an dessen N-terminalen Ende eine inhibitorische Region, eine Region mit einer Prozessierungsstelle und eine Region, die ein Makromolekül auf einer Zelloberfläche oder eine Komponente der extrazellulären Matrix selektiv erkennt, angeordnet ist.The The present invention relates to a polypeptide having preferably antitumoral and / or immunomodulatory cytokine properties by Processing in vivo is activatable comprising a C-terminal Region of specific biological activity at the N-terminal end an inhibitory region, a region with a processing site and a region containing a macromolecule on a cell surface or a component of the extracellular Matrix selectively recognizes, is arranged.
Der Einsatz von rekombinanten Liganden der TNF-Familie, z.B. TNF oder FasL (CD95L), zur Behandlung von beispielsweise Tumorerkrankungen ist bisher aufgrund von starken systemischen Nebenwirkungen, die als therapiebegrenzend anzusehen sind, stark eingeschränkt. So ist z.B. eine Behandlung mit TNF nur unter speziellen, aufwendigen Behandlungsprotokollen (z.B. mittels sog. "Isolated Limb Perfusion") bei sehr begrenzten Indikationen (Melanom/Sarkom-Metastasen der Extremitäten) mit Erfolg durchführbar. Aus diesen klinischen Daten kann man abschätzen, daß etwa eine 10- bis 100-fach höhere TNF-Dosis als die MTD (engl. "Maximum Tolerated Dose") zur anti-tumoralen Wirksamkeit erforderlich wäre, als es die massiven systemischen Nebenwirkungen zulassen würden. Behandlungskonzepte, die auf der Aktivierung von Fas, dem Rezeptor des FasL, beruhen, sind bisher keine versucht worden, da eine systemische Aktivierung dieses Rezeptors sehr schnell Apoptose in Hepatozyten induziert und so zu akutem, im Experimentaltier tödlich verlaufendem Leberversagen führt.Of the Use of recombinant ligands of the TNF family, e.g. TNF or FasL (CD95L), for the treatment of, for example, tumors So far, due to strong systemic side effects that as Therapy limiting are to be regarded, strongly limited. So is e.g. a treatment with TNF only under special, elaborate Treatment protocols (e.g., by so-called "Isolated Limb Perfusion") in very limited Indications (melanoma / sarcoma metastases of the extremities) with success feasible. From these clinical data one can estimate that about a 10 to 100-fold higher TNF dose as the MTD (Engl Tolerated can ") would be required for anti-tumoral efficacy, as it is the massive systemic Side effects would allow. Treatment concepts based on the activation of Fas, the receptor FasL, are so far no attempts have been made since a systemic Activation of this receptor very rapidly induces apoptosis in hepatocytes and thus to acute, in the experimental animal fatal liver failure leads.
Der vorliegenden Erfindung liegt daher die Aufgabe zugrunde, die unerwünschten Folgen einer Behandlung mit therapeutisch wirksamen Polypeptidwirkstoffen, wie z.B. FasL- oder TNF-haltigen Substanzen, zu vermeiden oder zu vermindern, während gleichzeitig die therapeutisch wirksamen, beispielsweise antitumoralen Eigenschaften der aktiven Substanz, wie FasL oder TNF, beibehalten oder sogar verstärkt werden.Of the The present invention is therefore based on the object, the undesirable Consequences of treatment with therapeutically active polypeptide active ingredients, such as. FasL or TNF-containing substances to avoid or to diminish while at the same time the therapeutically effective, for example antitumoral properties the active substance, such as FasL or TNF, or even enhanced.
Diese Aufgabe wird durch die in den Ansprüchen gekennzeichneten Ausführungsformen der vorliegenden Erfindung gelöst.These The object is achieved by the embodiments characterized in the claims solved the present invention.
Insbesondere wird erfindungsgemäß ein Polypeptid mit einer Aminosäuresequenz bereitgestellt, umfassend von N- nach C-terminal
- (1) eine Region („Inhibitor"), welche die biologische Aktivität der Region (4) durch intramolekulare oder intermolekulare Bindung und/oder Wechselwirkung hemmt,
- (2) eine Region, die mindestens eine Prozessierungsstelle aufweist,
- (3) eine Region(„Targeting-Modul"), die ein spezifisches Makromolekül auf einer Zelloberfläche und/oder eine Komponente der extrazellulären Matrix selektiv erkennt, und
- (4) eine Region („therapeutisch wirksame Region oder Substanz") mit einer biologischen Aktivität für ein spezifisches Zielmolekül,
- (1) a region ("inhibitor") which inhibits the biological activity of the region (4) by intramolecular or intermolecular bonding and / or interaction,
- (2) a region having at least one processing station,
- (3) a region ("targeting module") that selectively recognizes a specific macromolecule on a cell surface and / or a component of the extracellular matrix, and
- (4) a region ("therapeutically effective region or substance") having a biological activity for a specific target molecule,
Die Begriffe „Region" und „Modul" werden im folgenden synonym verwendet. Der Begriff „Fragment" bezeichnet eine verkürzte Form eines Moleküls. Die Begriffe „Derivat" und „Mutante" bezeichnen jedes Derivat bzw, jede Mutante eines Moleküls, die im wesentlichen die gleiche funktionalen und/oder biologischen Eigenschaften des Moleküls aufweisen. In Bezug auf Nukleinsäuren können Derivate bzw. Mutanten Deletionen, Additionen und/oder Substitutionen von Basen enthalten, deren Abwesenheit, Anwesenheit oder Substitution keinen wesentlichen Einfluß auf die Akti vität des Genprodukts hat, beispielsweise Basen, die in einem transkriptionell inaktiven Teil einer Nukleotidsequenz liegen. Dies schließt auch Derivate und Mutanten ein, welche bei unterschiedlicher Nukleotidsequenz die gleiche Aminosäuresequenz kodieren. Deletionen, Additionen und/oder Substitutionen, die zu einer geringfügigen Steigerung oder Verringerung der Transkriptionsrate führen, sind ebenfalls mit eingeschlossen. In Bezug auf Aminosäuresequenzen können Derivate bzw. Mutanten Deletionen, Additionen und/oder Substitutionen von Aminosäuren enthalten, deren Abwesenheit, Anwesenheit oder Substitution keinen wesentlichen Einfluß auf die Aktivität des Polypeptids hat, beispielsweise konservative Substitutionen von Aminosäuren, d.h. Ersetzen von Aminosäuren durch Aminosäuren mit ähnlichen chemischen Eigenschaften. Der Begriff „Derivat" schließt auch post-translationale Modifikationen, wie beispielsweise zum Wildtyp unterschiedliche Glykosylierungsmuster, ein.The Terms "region" and "module" are hereafter used synonymously. The term "fragment" refers to a truncated form of a molecule. The terms "derivative" and "mutant" refer to each Derivative, or each mutant of a molecule, which is essentially the have the same functional and / or biological properties of the molecule. In Terms of nucleic acids can Derivatives or mutants deletions, additions and / or substitutions of bases, their absence, presence or substitution no significant influence the activity of the gene product has, for example, bases that are transcriptional inactive part of a nucleotide sequence. This also includes Derivatives and mutants, which at different nucleotide sequence the same amino acid sequence encode. Deletions, additions and / or substitutions that belong to a slight increase or reduction in transcription rate are also included. In terms of amino acid sequences can Derivatives or mutants deletions, additions and / or substitutions of amino acids whose absence, presence or substitution does not exist significant influence the activity of the polypeptide, for example conservative substitutions of amino acids, i.e. Replacing amino acids by amino acids with similar ones chemical properties. The term "derivative" also includes post-translational Modifications, such as different from the wild type Glycosylation pattern, a.
Erfindungsgemäße Polypeptide werden nachstehend auch allgemein als "C-terminal TNF family Ligand (CTL)-Prodrug" bezeichnet. Sind im nachfolgenden erfindungsgemäße Polypeptide gemeint, in denen die Region (4) aus einem bestimmtem Liganden der TNF-Familie, z.B. dem FasL oder TNF abgeleitet ist, so werden diese entsprechend dieser Region benannt. Besteht die Region (4) z.B. aus einem FasL-Derivat so wird das erfindungsgemäße Polypeptid als FasL-Prodrug bezeichnet. Die erfindungsgemäßen CTL-Prodrugs sind modular aufgebaute Wirkstoffe und gemäß einer besonders bevorzugten Ausführungsform ein vorzugsweise homotrimeres oder homohexameres Fusionsprotein mit beispielsweise einem Zytokin als antitumoral wirksamer Substanz in Region (4), welches seine biologische Wirkung durch Verknüpfung mit drei weiteren Funktionsmodulen gezielt im erkrankten Gewebe, z.B. einem Tumorareal, freisetzt. Dies wird erreicht durch gentechnisches Anknüpfen der therapeutisch wirksamen Substanz, z.B. des FasL-Moleküls, an den C-Terminus eines für das Zielgewebe spezifischen Targeting-Moduls (3), z.B. tumorspezifische Antikörper oder Derivate davon, wie scFv-Antikörper, dem N-terminal durch eine prozessierbare Region (2) ein Inhibitor (1) gegen die therapeutisch wirksame Substanz (4) vorangeht, welcher selektiv im Zielgewebe, wie z.B. dem Tumorareal, durch Prozessierung der Region (2) inaktiviert wird, vorzugsweise durch gezielte proteolyti sche Abspaltung aus dem Fusionsprotein entfernt wird, und so ein am selektiven Targeting-Modul gebundener, bioaktiver Wirkstoff, z.B. FasL, entsteht.Polypeptides of the invention will also be referred to hereinafter generally as the "C-terminal TNF family ligand (CTL) prodrug". If in the following polypeptides according to the invention are meant in which the region (4) is derived from a particular ligand of the TNF family, for example the FasL or TNF, these are named corresponding to this region. Is the region (4) eg from a FasL derivative so the polypeptide of the invention is referred to as FasL prodrug. The CTL prodrugs according to the invention are modular active compounds and, according to a particularly preferred embodiment, a preferably homotrimeric or homohexameric fusion protein with, for example, a cytokine as antitumoral active substance in region (4), which specifically targets its biological activity in the diseased tissue by linking with three further functional modules, eg a tumor area, releases. This is achieved by genetically linking the therapeutically active substance, for example the FasL molecule, to the C terminus of a targeting tissue-specific targeting module (3), eg tumor-specific antibodies or derivatives thereof, such as scFv antibodies, N-terminally preceded by a processable region (2) an inhibitor (1) against the therapeutically active substance (4) which is selectively inactivated in the target tissue, such as the tumor area, by processing the region (2), preferably by targeted proteolytic cleavage from the Fusion protein is removed, and so bound to the selective targeting module, bioactive agent, such as FasL arises.
Das beispielsweise als therapeutisch wirksame Substanz einsetzbare Zytokin ist vorzugsweise ein Ligand der TNF-Familie, besonders bevorzugt FasL, TNF, TRAIL, CD40L, LIGHT oder APRIL oder ein biologisch wirksames Derivat oder eine biologisch wirksame Mutante dieser Moleküle. In einer bevorzugten Ausführungsform der vorliegenden Erfindung ist der Inhibitor (1) ein Peptid-Inhibitor, vorzugsweise eine extrazelluläre Domäne des zur Region (4) korrespondierenden Rezeptors. Der C-Terminus von Liganden der TNF-Familie kann für die optimale Aktivität des Moleküls sehr wichtig sein. Nach der Fusion von Peptiden an den C-Terminus ist die Aktivität dieser Zytokine daher oft sehr stark eingeschränkt. Dies gilt insbesondere für den FasL. Das CTL-Prodrug-Prinzip hat daher u.a. den Vorteil, daß bei der Konstruktion der Prodrug der C-Terminus der eigentlichen biologischen Wirkkomponente des Fusionsproteins frei bleibt und so nach der Prozessierung ein Zytokin-Derivat mit maximaler Aktivität entstehen kann.The For example, as a therapeutically effective substance usable cytokine is preferably a ligand of the TNF family, more preferably FasL, TNF, TRAIL, CD40L, LIGHT or APRIL or a biologically active Derivative or a biologically active mutant of these molecules. In a preferred embodiment In the present invention, the inhibitor (1) is a peptide inhibitor, preferably an extracellular domain of the receptor corresponding to the region (4). The C-terminus of ligands the TNF family can be used for the optimal activity of the molecule be very important. After the fusion of peptides to the C-terminus is the activity Therefore, these cytokines are often very severely restricted. This is especially true for the FasL. The CTL prodrug principle has therefore u.a. the advantage that in the construction the prodrug the C-terminus of the actual biological active component remains free of the fusion protein and so after processing a cytokine derivative with maximum activity can arise.
Viele Antikörperdomänen aggregieren spontan. Die Herstellung von Antikörper-Zytokin Fusionsproteinen nach dem Stand der Technik führt deshalb typischerweise häufig auch zur Aggregation des Fusionsproteins. Bei Verwendung von FasL im Zytokinmodul bewirkt diese Aggregation eine konstitutive Aktivierung des FasL, was eine ungerichtete, d.h. potentiell systemische Aktivität des betreffenden Fusionsproteins und damit gravierende Nebenwirkungen nach sich zieht. Das CTL-Prodrug-Prinzip hat daher u.a. den Vorteil, daß zur Konstruktion von Prodrugs mit freiem Liganden C-Terminus auch aggregierende Antikörperdomänen verwendet werden können.Lots Aggregate antibody domains spontaneous. The preparation of antibody-cytokine fusion proteins according to the state the technology leads therefore typically common also for the aggregation of the fusion protein. When using FasL In the cytokine module, this aggregation causes constitutive activation FasL, which is an undirected, i. potentially systemic activity of the subject Fusion protein and thus serious side effects. The CTL prodrug principle therefore has u.a. the advantage that to Construction of prodrugs with free ligand C-terminus also used aggregating antibody domains can be.
Mit dem erfindungsgemäßen Prodrug-Aufbau wird es ermöglicht, lokal hohe Wirkkonzentrationen der therapeutisch wirksamen Substanz, z.B. des FasL, zu erreichen, ohne daß es zu systemisch erhöhten Therapeutikum-Spiegeln (z.B. FasL im Serum) und damit therapielimitierenden Nebenwirkungen kommt. Insbesondere wird beispielsweise im Fall von FasL als therapeutisch wirksamer Region nach der Prozes sierung durch die Targeting-Modul- (z.B. Antikörper-) vermittelte zellständige Präsentation des FasL eine Wirkung erzielt, die der des natürlichen Membran-FasL entspricht, d.h. es kommt zur optimalen Aktivierung von Fas. Die differentielle biologische Wirkung löslicher und membranständiger Liganden einiger Mitglieder der TNF Familie, v.a. FasL, TNF, TRAIL, CD40, ist bekannt und hängt mit der Affinität der verschiedenen Formen der Liganden zu ihren Rezeptoren, der unterschiedlichen Bindung an Rezeptorsubtypen und/oder der unterschiedlichen Fähigkeit zur Rezeptor-Clusterbildung in der Membran und damit Aktivierung der Signalprozesse zusammen.With the prodrug structure according to the invention is it possible locally high active concentrations of the therapeutically active substance, e.g. FasL, without causing systemically elevated therapeutic levels (for example FasL in serum) and thus therapy-limiting side effects comes. In particular, in the case of FasL, for example, it is considered therapeutic effective region after being processed by the targeting module (e.g., antibody) mediated cellular presentation the FasL achieves an effect similar to that of the natural membrane FasL, i.e. Optimal activation of Fas occurs. The differential biological effect more soluble and membrane-bound Ligands of some members of the TNF family, v.a. FasL, TNF, TRAIL, CD40, is known and hangs with the affinity of different forms of ligands to their receptors, the different ones Binding to receptor subtypes and / or different ability for receptor clustering in the membrane and thus activation the signal processes together.
Durch Auswahl der Spezifität des Targeting-Moduls (3) und der Prozessierungsregion (2) kann ein auf die jeweilige Tumorentität spezifisch abgestimmtes/optimiertes Therapeutikum hergestellt werden. Durch die Herstellung einer CTL-Prodrug mit freiem C-Terminus, die sich im gewünschten Zielort durch einen Antikörperanteil anreichern lässt und dort durch Proteolyse aktiviert wird, wird eine lokale Aktivierung des entsprechenden Liganden und damit des zu diesem korrespondierenden Rezeptors in vivo ermöglicht. Die Aktivierung erfolgt dabei durch zellassoziierte Proteasen, die insbesondere am gewünschten Zielort vorkommen. Die lokale Aktivität wird dann zum einen durch die Spezifität des verwendeten Antiköpers bedingt, zum anderen aber auch durch die bevorzugte Expression entsprechender Proteasen am Zielort.By Selection of specificity of the targeting module (3) and the processing region (2) can be to the respective tumor entity specifically tailored / optimized therapeutic agent are produced. By preparing a CTL prodrug with free C-terminus, the in the desired Destination by an antibody portion enriched and there is activated by proteolysis, becomes a local activation the corresponding ligand and thus the corresponding to this Receptor in vivo allows. The activation takes place by cell-associated proteases, the especially at the desired Destination occur. The local activity is then on the one hand the specificity of the antibody used conditionally, but also by the preferred expression corresponding Proteases at the destination.
Die (Aminosäuresequenz-)Regionen bzw. Module des erfindungsgemäßen Polypeptids werden nachstehend in Bezug auf bevorzugte Ausführungsformen im Einzelnen beschrieben.The (Amino acid sequence) regions or modules of the polypeptide according to the invention are described in detail below with respect to preferred embodiments.
Das erfindungsgemäße Polypeptid basiert auf einer neuartigen Prodrug-Technologie und ist ein Konstrukt, das gemäß einer bevorzugten Ausführungsform ein rekombinantes Fusionsprotein ist, welches prinzipiell eine definierte Abfolge der folgenden Strukturelemente (im Monomer) umfaßt (N-terminal nach C-terminal): (1) ein spezifisch an die Region (4) bindendes und diese inaktivierendes Protein bzw. Peptid, (2) ein variables Linkerpeptid mit spezifischen Protease-Spaltstellen, (3) ein murines, humanisiertes oder humanes Einzelkettenantikörperfragment (scFv) definierter Anti genspezifität, bestehend aus VH-Linker-VL oder ein Peptid mit vergleichbarer Eigenschaft, und (4) einen Ligand der TNF-Familie, welcher beispielsweise dem Wildtyp-Ligand oder dessen extrazellulärer Domäne oder davon abgeleiteten biologisch aktiven Varianten entspricht.The polypeptide of the invention is based on a novel prodrug technology and is a construct which, according to a preferred embodiment, is a recombinant fusion protein which comprises in principle a defined sequence of the following structural elements (in the monomer) (N-terminal to C-terminal): (1 (2) a variable linker peptide having specific protease cleavage sites, (3) a murine, humanized or human single chain antibody fragment (scFv) of defined anti-gageneity, consisting of: (3) a protein or peptide specifically binding to and inactivating the region (4) V H -linker V L or a peptide with comparable property, and (4) a ligand of the TNF family which corresponds, for example, to the wild-type ligand or its extracellular domain or biologically active variants derived therefrom.
Das Inhibitor-Modul (1) ist gemäß einer bevorzugten Ausführungsform des erfindungsgemäßen Polypeptids ein Rezeptor bzw. dessen Ligandenbindungsdomäne für den Zytokinteil im Modul (4). Das Inhibitor-Modul weist bevorzugt mindestens eine Bindungsstelle für die therapeutisch wirksame Region (4) auf. In einer bevorzugten Ausführungsform der vorliegenden Erfindung umfaßt das Inhibitor-Modul im Falle der Verwendung von FasL in Region (1) die vollständige oder partielle extrazelluläre Domäne eines humanen Fas-Rezeptors. Andere, spezifisch FasL bindende Proteine, beispielsweise Fas-Fragmente oder Fas anderer Spezies-Herkunft oder Proteine viralen Ursprungs sowie jeweils davon abgeleitete synthetische Peptide, die FasL-Bindungseigenschaft besitzen und mit der FasL-Bindung an Fas-Rezeptoren interferieren, sind ebenfalls geeignet. In einer weiteren bevorzugten Ausführungsform der vorliegenden Erfindung ist der Zytokin-Rezeptor die vollständige oder partielle extrazelluläre Domäne eines Rezeptors der TNF-Rezeptorfamilie und/oder ein TNF-Ligand-bindendes Virus-Protein oder eine biologisch aktive Mutante dieser Domäne oder eine synthetische TNF-Ligand-bindende Verbindung. Aufgrund der Bindung bzw. Wechselwirkung des Inhibitors mit dem therapeutisch wirksamen Modul ist das erfindungsgemäße Fusionsprotein in diesem Zustand biologisch inaktiv, d.h. es befindet sich in der Proform (Prodrug).The Inhibitor module (1) is in accordance with a preferred embodiment of the polypeptide of the invention a receptor or its ligand binding domain for the cytokine part in the module (4). The inhibitor module preferably has at least one binding site for the therapeutically effective region (4). In a preferred embodiment of the present invention the inhibitor module in case of using FasL in region (1) the complete or partial extracellular domain a human Fas receptor. Other, specifically FasL binding proteins, for example Fas fragments or Fas of other species origin or Proteins of viral origin and synthetic derived therefrom Peptides, the FasL binding property and interfere with FasL binding to Fas receptors, are also suitable. In a further preferred embodiment In the present invention, the cytokine receptor is the full or partial extracellular domain a receptor of the TNF receptor family and / or a TNF ligand-binding Virus protein or a biologically active mutant of this domain or a synthetic TNF ligand-binding compound. Because of the bond or interaction of the inhibitor with the therapeutically effective Module is the fusion protein according to the invention biologically inactive in this state, i. it is in the proform (Prodrug).
Das Prozessierungsmodul (2) ist beispielsweise Protease-sensitiv (d.h. die Prozessierungsstelle entspricht der Erkennungssequenz einer Protease) und vorzugsweise in Aminosäurezusammensetzung und Gesamtlänge derart beschaffen, daß es eine hochaffine, stabile Bindung des im Molekül N-terminal befindlichen Moduls (1), z.B. eines FasL-Inhibitors (z.B. die extrazelluläre Fas-Rezeptordomäne) an die Region (4), z.B. FasL erlaubt, so daß hierdurch die Bindung des Liganden-Anteils des Moduls (4) an die zu diesem Liganden korrespondierenden, zellexprimierten Rezeptoren in vivo verhindert wird. Das Prozessierungsmodul („Linker") ist weiterhin vor zugsweise derart beschaffen, daß er mindestens eine, vorzugsweise mehrere selektive Spaltstellen für solche extrazellulären oder zellassozierten Proteasen enthält, die vorzugsweise selektiv im Tumorgewebe nachgewiesen werden. Beispiele für geeignete Spaltstellen sind diejenige für Urokinase-Typ Plasminogenaktivator (uPA), Gewebsplasminogenaktivator (tPA), den aktivierten Gerinnungsfaktor VIIa, Matrix-Metalloproteasen, wie MMP-2 und MMP-9, und für die hochselektiv im Stroma von Tumoren membranständig exprimierte FAP-Protease. Besonders bevorzugte Protease-sensitive Spaltstellen sind diejenige von mit dem Vorgang der Metastasierung und der Angiogenese in Verbindung stehenden Matrix-Metalloproteasen (z.B. MMP-9-Erkennungssequenz Gly-Pro-Leu-Gly-Val-Arg-Gly-Lys), von Heparanase, von Enzymen, die bevorzugt in nekrotischen Läsionen auftreten, sowie von Enzymen, die mit Prostatakrebs assoziiert sind (z.B. PSMA, PSA, spaltbares Prozessierungsmodul Glutaryl-(4-hydroxypropyl)-Ala-Ser-cyclohexaglycyl-Gln-Ser-Leu-COOH). Die Struktur des Linkers wird derart gewählt, daß die Protease-Erkennungssequenz frei zugänglich ist, d.h. eine effektive Prozessierung durch spezifische Proteasen möglich ist, und nach Spaltung des Fusionsproteins ggf. an dem abgespaltenen Teil, der das therapeutisch wirksamen Modul enthält, verbleibende Aminosäuren des Linkers die Bioaktivität der therapeutisch wirksamen Region nicht negativ beeinflussen.The Processing module (2) is, for example, protease-sensitive (i.e. the processing station corresponds to the recognition sequence of a Protease) and preferably in amino acid composition and total length so get that one high-affinity, stable binding of the N-terminal module in the molecule (1), e.g. a FasL inhibitor (e.g., the extracellular Fas receptor domain) to the Region (4), e.g. FasL allows, so that thereby the binding of the Ligand portion of the module (4) to the corresponding to this ligand, cell-expressed receptors in vivo is prevented. The processing module ("Linker") is still preferably before in such a way that he at least one, preferably a plurality of selective cleavage sites for such extracellular or cell-associated proteases, which are preferably selective be detected in tumor tissue. Examples of suitable cleavage sites are the one for Urokinase-type plasminogen activator (uPA), tissue plasminogen activator (tPA), the activated coagulation factor VIIa, matrix metalloproteases, like MMP-2 and MMP-9, and for the highly selectively in the stroma of tumors membrane-bound expressed FAP protease. Particularly preferred protease-sensitive cleavage sites are those of the process of metastasis and angiogenesis standing matrix metalloproteases (e.g., MMP-9 recognition sequence Gly-Pro-Leu-Gly-Val-Arg-Gly-Lys), of heparanase, of enzymes that preferentially occur in necrotic lesions, and enzymes associated with prostate cancer (e.g., PSMA, PSA, fissionable processing module glutaryl- (4-hydroxypropyl) -Ala-Ser-cyclohexaglycyl-Gln-Ser-Leu-COOH). The structure of the linker is chosen such that the protease recognition sequence freely accessible is, i. effective processing by specific proteases possible and after cleavage of the fusion protein, optionally at the cleaved Part containing the therapeutically effective module, remaining amino acids of the Linker's bioactivity therapeutically effective region.
In einer bevorzugten Ausführungsform weist das erfindungsgemäße Polypeptid zusätzlich ein Trimerisierungsmodul zwischen dem Inhibitor-Modul (1) und dem Prozessierungsmodul (2) oder zwischen dem Prozessierungsmodul (2) und dem Targeting-Modul (3) auf. Gemäß einer besonders bevorzugten Ausführungsform umfaßt das Trimerisierungsmodul ein natürlich vorkommendes oder synthetisches Peptid mit intrinsischen Trimerisierungseigenschaften. Ein besonders geeignetes Beispiel eines derartigen Peptids ist eine Domäne des Tenascin-Moleküls (AA 110-139, Swissprot #P10039, (Huhn) oder Swissprot #P24821 (Mensch)). Es gewährleistet die kovalente, homotrimere Verknüpfung des Fusionsproteins während der Biogenese und kann die Bindung des Inhibitor Moduls (1) an das therapeutisch wirksame Modul (4) verbessern. Die Liganden der TNF-Familie, insbesondere auch der FasL, haben intrinsische Trimerisierungseigenschaften. Eine optionale Trimerisierungsregion dient da her hauptsächlich dazu, Ligandentrimere zu stabilisieren. Wie wichtig eine Stabilisierung für den Erhalt der trimeren, potentiell aktiven Form ist, hängt vom Einzelfall ab.In a preferred embodiment has the polypeptide of the invention additionally a trimerization module between the inhibitor module (1) and the Processing module (2) or between the processing module (2) and the targeting module (3). According to a particularly preferred embodiment comprises the trimerization module is natural occurring or synthetic peptide having intrinsic trimerization properties. A particularly suitable example of such a peptide is one domain of the tenascin molecule (AA 110-139, Swissprot # P10039, (chicken) or Swissprot # P24821 (human)). It guarantees the covalent, homotrimeric linkage of the Fusion protein during biogenesis and can bind the inhibitor module (1) to the therapeutically effective module (4) improve. The ligands of the TNF family, especially the FasL, have intrinsic trimerization properties. An optional trimerization region is therefore mainly used to Stabilize ligand trimer. How important stabilization for the Preservation of the trimeric, potentially active form depends on Isolated case.
Das Targeting-Modul (3) bindet vorzugsweise an ein Zelloberflächenmolekül, das in Tumorläsionen und/oder proliferierenden Endothelzellen, die mit dem Prozeß der Angiogenese assoziiert sind, exprimiert wird. Gemäß einer anderen bevorzugten Ausführungsform ist das Targeting-Modul (3) für eine Komponente der extrazellulären Matrix spezifisch, die in Tumorläsionen und/oder Angiogenesebereichen pathologischer Läsionen vorhanden ist. Gemäß einer weiteren bevorzugten Ausführungsform ist das Targeting-Modul (3) für eine Komponente der malignen Tumorzelle selbst spezifisch. Vorzugsweise umfaßt die Region bzw. das Modul (3) einen Antikörper (z.B. murin, humanisiert oder human) oder ein Fragment davon, z.B. ein Fab-Fragment oder ein typisches, nach dem Stand der Technik hergestelltes Einzelkettenantikörperfragment (scFv) murinen, durch CDR-Grafting humanisierten oder vollständig humanen Ursprungs mit einer Spezifität für ein z.B. im Tumorgewebe vorzugsweise selektiv bzw. dominant exprimiertes Antigen, wobei dies prinzipiell auf den malignen Zellen selbst exprimiert sein kann, vorzugsweise aber im nicht-malignen Anteil des Tumors, den Stromazellen oder dem Tumorendothel, exprimiert wird. Derartige Antigene nicht-maligner Gewebeanteile eines soliden Tumors (Karzinoms) sind einerseits genetisch invariant, andererseits bei unterschiedlichsten Tumorentitäten vorkommend und damit universelle Tumormarker. Beispielsweise seien hier der VEGFR- bzw. der VEGFR/VEGF-Komplex (als Beispiel für Rezeptor-Liganden-Komplexe) sowie das Integrin αvβ3, das Endosialin und die Fibronektin-Isoform bFn als selektive Zielstrukturen des Tumorendothels und das sog. Fibroblast Activation Protein (FAP) als selektiver Marker für eine als Target dienende Komponente der extrazellulären Matrix, welche im Tumorstroma vorhanden ist, genannt, die beispielsweise mit spezifischen, hochaffinen scFv wirksam erfaßt werden können. Weitere Beispiele für geeignete Targeting-Module sind Peptide bzw. Proteindomänen, die z.B. natürlicherweise an eine Tumor- bzw. Tumorstroma- bzw. Tumorendothel-typische Struktur binden, aber auch artifizielle Antikörper und Spiegelmere.The targeting module (3) preferably binds to a cell surface molecule that is expressed in tumor lesions and / or proliferating endothelial cells associated with the process of angiogenesis. In another preferred embodiment, the targeting module (3) is specific for a component of the extracellular matrix present in tumor lesions and / or angiogenesis regions of pathological lesions. According to another preferred embodiment, the targeting module (3) is specific for a component of the malignant tumor cell itself. Preferably, the region or module (3) comprises an antibody (eg murine, humanized or human) or a fragment thereof, eg a Fab fragment or a typi In other words, a single-chain antibody fragment (scFv) produced by the prior art may be murine, CDR-grafted or completely human with specificity for, for example, an antigen which is preferentially or predominantly expressed in tumor tissue, and this may in principle be expressed on the malignant cells themselves , but preferably in the non-malignant portion of the tumor, the stromal cells or the tumor endothelium. Such antigens of non-malignant tissue portions of a solid tumor (carcinoma) are on the one hand genetically invariant, on the other hand occurring in a wide variety of tumor entities and thus universal tumor markers. Examples include the VEGFR or VEGFR / VEGF complex (as an example of receptor-ligand complexes) and the integrin αvβ3, the endosialin and the fibronectin isoform bFn as selective target structures of the tumor endothelium and the so-called fibroblast Activation Protein ( FAP) as a selective marker for a targeting component of the extracellular matrix present in the tumor stroma, which can be efficiently detected, for example, with specific, high affinity scFv. Further examples of suitable targeting modules are peptides or protein domains which, for example, naturally bind to a tumor or tumor stroma or tumor endothelium-typical structure, but also to artificial antibodies and spiegelmers.
Wie vorstehend ausgeführt, enthält das therapeutisch wirksame Modul (4) vorzugsweise eine Aminosäuresequenz eines Zytokins oder eines therapeutisch wirksamen Fragments davon. Vorzugsweise enthält die Region (4) die Aminosäuresequenz eines Liganden der TNF-Familie, vorzugsweise von FasL, mehr bevorzugt eines TNF-Liganden-Vorläuferproteins, vorzugsweise eines FasL-Vorläuferproteins, besonders bevorzugt von einem dem prozessierten, reifen Wildtyp-TNF-Liganden-Molekül identischen Protein oder davon abgeleiteten Derivaten oder Mutanten mit selektiven Rezeptorbindungseigenschaften oder Mutanten bzw. Derivaten, die hinsichtlich ihrer spezifischen Bioaktivität oder anderer Eigenschaften (Stabilität, Proteaseresistenz) optimiert wurden, und am meisten bevorzugt von einem dem prozessierten, reifen Wildtyp-FasL-Molekül identischen Protein, oder davon abgeleiteten Derivaten oder Mutanten mit selektiven Rezeptorbindungseigenschaften oder Mutanten bzw. Derivaten, die hinsichtlich ihrer spezifischen Bioaktivität oder anderer Eigenschaften (Stabilität, Proteaseresistenz) optimiert wurden.As stated above, contains the therapeutically active module (4) preferably an amino acid sequence a cytokine or a therapeutically effective fragment thereof. Preferably contains the region (4) the amino acid sequence of a Ligands of the TNF family, preferably FasL, more preferred a TNF ligand precursor protein, preferably a FasL precursor protein, particularly preferably identical to the processed, mature wild-type TNF ligand molecule Protein or derived derivatives or mutants with selective Receptor binding properties or mutants or derivatives that in terms of their specific bioactivity or other properties (Stability, Protease resistance), and most preferably from identical to the processed, mature wild-type FasL molecule Protein, or derived derivatives or mutants with selective Receptor binding properties or mutants or derivatives that in terms of their specific bioactivity or other properties (Stability, Protease resistance).
Das erfindungsgemäße Polypeptid kann weitere Regionen umfassen. Beispielsweise können zur vereinfachten Reinigung des rekombinant hergestellten Proteins und der in vitro Analytik geeignete Markierungssequenzen angefügt werden. So kann das erfindungsgemäße Polypeptid z.B. am N-Terminus und/oder zwischen zwei benachbarten Regionen mindestens eine detektierbare Markierung aufweisen. Eine solche detektierbare Markierung kann ein „tag", z.B. zur Reinigung, sein, z.B. ein Flag tag.The polypeptide of the invention may include other regions. For example, for simplified cleaning recombinantly produced protein and in vitro analysis appropriate labeling sequences are added. Thus, the polypeptide of the invention e.g. at the N-terminus and / or between two adjacent regions at least have a detectable label. Such a detectable Marking may be a "day", for example for cleaning, be, e.g. a flag day.
Die erfindungsgemäß bevorzugte FasL-Prodrug ist ein nicht kovalent verknüpftes, homotrimeres Molekül oder, wenn eine entsprechende Trimersierungsregion eingefügt wurde, ein kovalent verknüpftes, homotrimeres Molekül, oder bei intermolekularer Wechselwirkung ein homohexameres Molekül bestehend aus der oben im Detail erläuterten Fusion von vier Funktionsregionen, dem tumorspezifischem Antikörpermodul (3), dem FasL-Modul (4) und dem blockierendem FasL-Bindeprotein (extrazelluläre Rezeptordomäne oder davon abgeleitetes Peptid)-Modul (1) sowie dem zwischen Modul (1) und Modul (3) liegenden spezifischen Protease-Spaltstellen Modul (2), welches in diesem kompletten Zustand in Bezug auf die FasL-Wirkung inaktiv ist.The according to the invention preferred FasL prodrug is a non-covalently linked, homotrimeric molecule or, if a corresponding trimerization region has been inserted, a covalently linked, homotrimeric molecule, or in the case of an intermolecular interaction, a homohexameric molecule from the above explained in detail Fusion of four functional regions, the tumor-specific antibody module (3), the FasL module (4) and the blocking FasL binding protein (Extracellular receptor domain or derived peptide) module (1) and the between module (1) and module (3) specific protease cleavage module (2), which in this complete state in terms of FasL effect is inactive.
Die FasL-Prodrug wird nach in vivo Verabreichung durch den Antikörper-Anteil zunächst spezifisch im Tumorareal angereichert und dort durch die vom Tumor selbst oder vom reaktiven Tumorstroma/Tumorgefäßsystem gebildete Proteasen (z.B. FAP, uPA, tPA, MMP2, Faktor VIIa) prozessiert, d.h. das inhibierende Modul/Peptid (1) wird abgespalten. Nach selektiver proteolytischer Spaltung dissoziiert das FasL-Rezeptor-Fragment/Inhibitorpeptid vom FasL-Modul (4), letzteres wird somit bioaktiv (d.h. die biologische Aktivität der Region wird durch Prozessierung der Prozessierungsstelle in Region (2) freigesetzt). Der derart prozessierte FasL bindet nun bevorzugt an zellständige Fas-Rezeptoren, da diese sich nicht durch Diffusion vom Bindungsort entfernen. Die Selektivität der FasL-Wirkung wird mit der erfindungsgemäßen FasL-Prodrug also durch zwei Maßnahmen erreicht: Einerseits über die Region (3)-vermittelte selektive Anreicherung der inaktiven Prodrug im Tumor und der Retention des biologisch aktiven Fragments, bestehend aus Region (3) und Region (4), auch nach proteolytischer Aktivierung und andererseits über die ortsspezifische Umwandlung des Prodrugs durch Proteasen, welche ausschließlich oder bevorzugt im Tumorareal in signifikanter Aktivität nachweisbar sind.The FasL prodrug becomes in vivo administration by the antibody portion first specifically enriched in the tumor area and there by the tumor or proteases formed by the reactive tumor stroma / tumor vasculature (e.g., FAP, uPA, tPA, MMP2, Factor VIIa), i. the inhibiting Module / peptide (1) is cleaved off. After selective proteolytic Cleavage dissociates the FasL receptor fragment / inhibitor peptide from the FasL module (4), the latter thus becomes bioactive (i.e. activity The region is being processed by processing the processing center in Region (2) released). The thus processed FasL now binds preferred to cellular Fas receptors, as these are not diffused from the binding site remove. The selectivity the FasL effect is thus carried out with the FasL prodrug according to the invention two measures achieved: on the one hand over the region (3) -mediated selective enrichment of the inactive Prodrug in the tumor and the retention of the biologically active fragment, consisting of region (3) and region (4), also proteolytic Activation and on the other hand over the site-specific conversion of the prodrug by proteases, which exclusively or are preferably detectable in the tumor area in significant activity.
In einer bevorzugten Ausführungsform der vorliegenden Erfindung weist das CTL-Prodrug die Aminosäuresequenz SEQ ID Nr. 1 auf.In a preferred embodiment In the present invention, the CTL prodrug has the amino acid sequence of SEQ ID NO: 1.
Ein weiterer Gegenstand der vorliegenden Erfindung betrifft eine Nukleinsäure, umfassend eine Nukleotidsequenz, welche das erfindungsgemäße Polypeptid kodiert. Der Begriff „Nukleinsäure" bedeutet ein natives, halbsynthetisches, synthetisches oder modifiziertes Nukleinsäuremolekül aus Desoxyribonukleotiden und/oder Ribonukleotiden und/oder modifizierten Nukleotiden. In einer bevorzugten Ausführungsform der vorliegenden Erfindung weist die Nukleinsäure die Nukleotidsequenz mit der SEQ ID Nr. 2 auf.Another object of the present invention relates to a nucleic acid comprising a nucleotide sequence encoding the polypeptide of the invention. The term "nucleic acid" means a native, semisynthetic, synthetic or modified nucleic acid molecule of deoxyribonucleotides and / or ribonucleotides and / or modified nucleotides In a preferred embodiment In accordance with the present invention, the nucleic acid has the nucleotide sequence of SEQ ID NO: 2.
Desweiteren wird erfindungsgemäß ein Vektor, enthaltend die vorstehend definierte Nukleinsäure, bereitgestellt. Der erfindungsgemäße Vektor unterliegt keiner besonderen Einschränkung, wobei geeignete Vektoren im Stand der Technik bekannt sind.Furthermore becomes a vector according to the invention, containing the above-defined nucleic acid. The vector according to the invention is not subject to any particular restriction, with suitable vectors are known in the art.
Der Vektor ist vorzugsweise zur Expression und/oder Amplifikation in einer prokaryontischen und/oder eukaryontischen Zelle befähigt. Dazu enthält der Vektor vorzugsweise geeignete regulatorische Elemente, wie Promotoren, Enhancer, Terminationssequenzen usw. Der Vektor kann auch zur stabilen Integration der erfindungsgemäßen Nukleinsäure in das genetische Material einer Wirtszelle verwendet werden.Of the Vector is preferably for expression and / or amplification in a prokaryotic and / or eukaryotic cell. To contains the vector preferably contains suitable regulatory elements, such as promoters, Enhancers, termination sequences, etc. The vector may also be stable Integration of the nucleic acid according to the invention in the genetic material of a host cell.
Ein weiterer Gegenstand betrifft erfindungsgemäß eine Wirtszelle, enthaltend die vorstehend genannte Nukleinsäure und/oder den vorstehend genannten Vektor. Geeignete Wirtszellen sind beispielsweise alle Säugerzellen, insbesondere kultivierte Zellinien wie z.B. COS- oder CHO-Zellen.One Another subject of the invention relates to a host cell containing the aforementioned nucleic acid and / or the aforementioned vector. Suitable host cells For example, all mammalian cells, in particular cultured cell lines, e.g. COS or CHO cells.
Die vorliegende Erfindung stellt ebenfalls ein Verfahren zur Herstellung des erfindungsgemäßen Polypeptids bereit, umfassend die Schritte
- (a) des Züchtens der vorstehenden Wirtszelle in einem Kulturmedium unter geeigneten Bedingungen und
- (b) des Isolierens des erfindungsgemäßen Polypeptids aus den Wirtszellen und/oder dem Kulturmedium.
- (A) growing the above host cell in a culture medium under suitable conditions and
- (b) isolating the polypeptide of the invention from the host cells and / or the culture medium.
Das erfindungsgemäße Polypeptid wird vorzugsweise durch Expression mit Hilfe von geeigneten Expressionssystemen, vorzugsweise als sezerniertes Produkt selektionierbarer, stabiler Transfektanden der Zellinie CHO DG44 oder nach transienter Expression in COS7-Zellen, hergestellt. Andere, dem Stand der Technik entsprechende eukaryontische Expressionssysteme, z.B. Pichia pastoris, Insekten- oder Säugerzellen, mit den für das jeweilige Zellsystem für Sekretion geeigneten Expressionsvektoren, werden z.B. in Brocks et al. (Immunotechnology 3:173-184,1997) für Säuger- und Insektenzellen beschrieben. pPICZalpha-Vektoren (INVITROGEN) zur Expression und Sekretion in der Hefe Pichia pastoris, sind ebenfalls geeignet.The polypeptide of the invention is preferably expressed by expression with the aid of suitable expression systems, preferably selectable as a secreted product, more stable Transfectants of the cell line CHO DG44 or after transient expression in COS7 cells. Other, according to the prior art eukaryotic expression systems, e.g. Pichia pastoris, insect or mammalian cells, with the for the respective cell system for Secretion of suitable expression vectors, e.g. in Brocks et al. (Immunotechnology 3: 173-184, 1997) for mammalian and insect cells. pPICZalpha vectors (INVITROGEN) for expression and secretion in the yeast Pichia pastoris, are also suitable.
Das erfindungsgemäße Polypeptid, die Nukleinsäure und/oder der Vektor kann (können) vorteilhafter Weise zur Herstellung von pharmazeutischen Zusammenset zungen zur Behandlung krankhafter Störungen beispielsweise von Tumorerkrankungen in einem Individuum/Patient verwendet werden.The polypeptide of the invention, the nucleic acid and / or the vector can (can) Advantageously for the preparation of pharmaceutical compositions for the treatment of pathological disorders for example, of tumor diseases in an individual / patient be used.
Eine weitere Ausführungsform der vorliegenden Erfindung betrifft daher eine pharmazeutische Zusammensetzung, enthaltend in pharmazeutisch wirksamer Menge das erfindungsgemäße Polypeptid und/oder die erfindungsgemäße Nukleinsäure und/oder den erfindungsgemäßen Vektor, gegebenenfalls in Verbindung mit einem oder mehreren pharmazeutisch verträglichen Hilfsstoffen, Verdünnungsmitteln und/oder Trägern. Die pharmazeutische Zusammensetzung dient vorzugsweise zur therapeutischen Behandlung von Krebserkrankungen und/oder Infektionskrankheiten und/oder metabolischen Erkrankungen. Besonders bevorzugte Einsatzgebiete der pharmazeutischen Zusammensetzung sind die Behandlung solider Tumoren sowie die Angiogenese in pathologischen Läsionen. Die erfindungsgemäße pharmazeutische Zusammensetzung kann jegliche im vorliegenden Fachgebiet als geeignet bekannte Form annehmen. Vorzugsweise ist sie fest, flüssig oder aerosolartig.A another embodiment The present invention therefore relates to a pharmaceutical composition, containing in a pharmaceutically effective amount the polypeptide of the invention and / or the nucleic acid according to the invention and / or the vector of the invention, optionally in conjunction with one or more pharmaceutically acceptable Excipients, diluents and / or carriers. The pharmaceutical composition is preferably for therapeutic use Treatment of cancers and / or infectious diseases and / or metabolic diseases. Particularly preferred applications the pharmaceutical composition are the treatment solid Tumors and angiogenesis in pathological lesions. The inventive pharmaceutical Composition may be any suitable in the art take known form. Preferably, it is solid, liquid or of an aerosol.
Die vorliegende Erfindung umfaßt somit ebenfalls ein Behandlungsverfahren, welches die Verabreichung einer therapeutisch ausreichenden Menge der erfindungsgemäßen pharmazeutischen Zusammensetzung an einen die Behandlung benötigenden Patienten einschließt. Geeignete Verabreichungswege der pharmazeutischen Zusammensetzung sind einem Fachmann bekannt und umfassen beispielsweise die orale, intravenöse, intraarterielle, intramuskuläre, nasale, rektale und topische Applikation. Eine intravenöse Verabreichung kann z.B. in Form einer Bolusinjektion mit nachfolgenden Injektionsintervallen und/oder in Form einer Infusion durchgeführt werden. Mit der pharmeutischen Zusammensetzung der vorliegenden Erfindung können sowohl menschliche als auch tierische Patienten behandelt werden. Das Behandlungsverfahren wird bevorzugt bei Patienten mit den vorstehend genannten Erkrankungen angewendet.The present invention thus also a treatment method, which administration a therapeutically sufficient amount of the pharmaceutical composition of the invention to a treatment requiring Including patients. Suitable routes of administration of the pharmaceutical composition are known to a person skilled in the art and include, for example, the oral, intravenous, intra-arterial, intramuscular, nasal, rectal and topical application. Intravenous administration can e.g. in the form of a bolus injection with subsequent injection intervals and / or in the form of an infusion. With the pharmaceutical Composition of the present invention may be both human and also animal patients are treated. The treatment procedure is preferred in patients with the aforementioned disorders applied.
Die Figuren zeigen:The Figures show:
Die vorliegende Erfindung wird anhand der folgenden, nicht-einschränkenden Beispiele näher erläutert.The The present invention is illustrated by the following, non-limiting Examples explained in more detail.
Beispiel 1 Herstellung eines erfindungsgemäßen PolypeptidsExample 1 Preparation a polypeptide of the invention
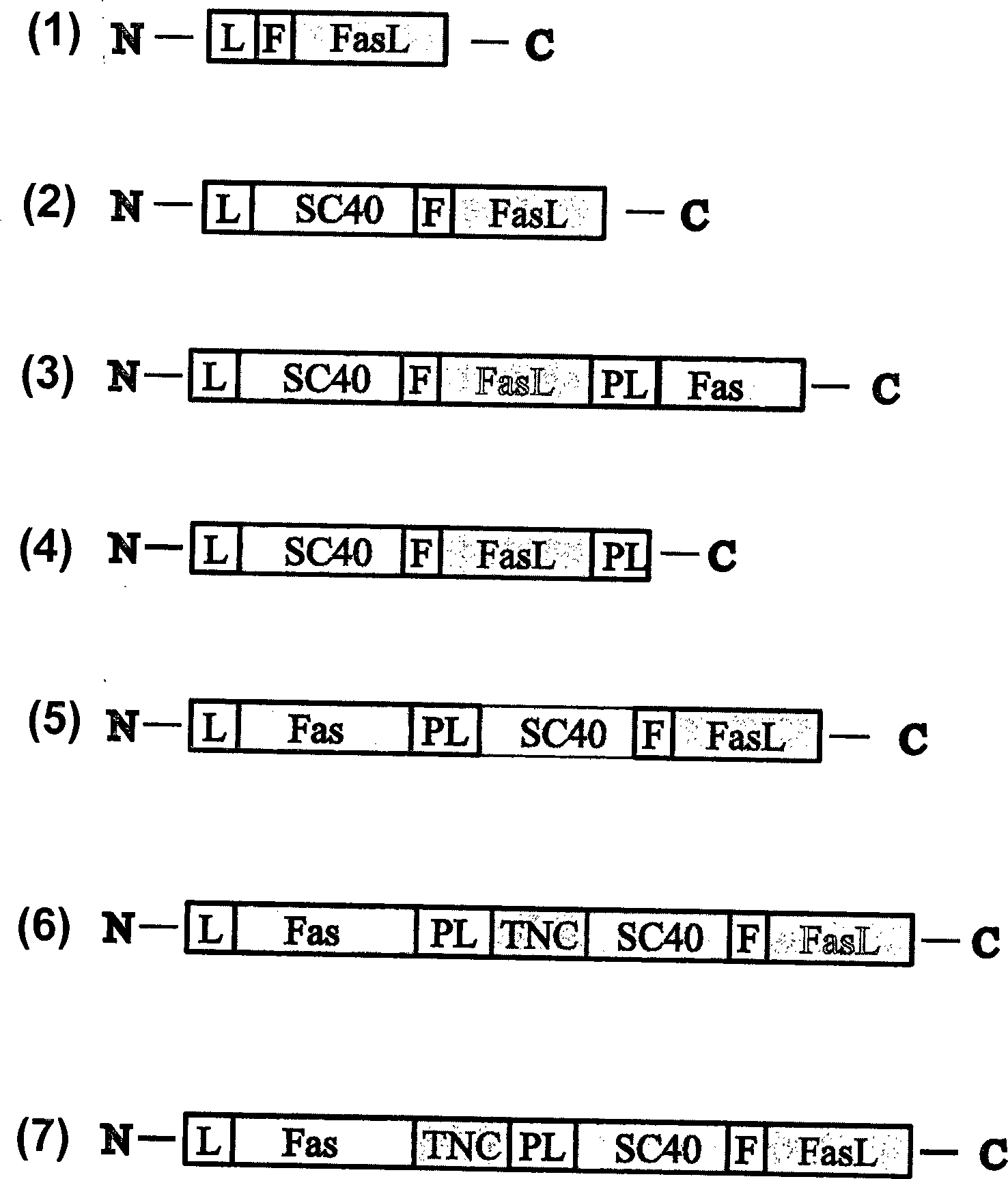
Das
mit einem N-terminalen Targeting-Modul versehene FasL-Modul wurde
durch gentechnisches N-terminales Anhängen des ligandenbindenden
Moduls des korrespondierenden Rezeptors Fas inhibiert, welches jedoch
durch Tumor-assoziierte Proteasen abgespalten werden kann. Hierzu
wurde das Rezeptorfragment mittels eines Linkers angehängt, der
entsprechenden Schnittstellen enthält (
Beispiel 2: Eine nach dem Schema des TNF-Selektokins (WO 02/22833) aufgebaute FasL-Prodrug ist zwar prozessierbar aber nicht oder nur sehr wenig aktiv.Example 2: One after FasL prodrug constructed according to the scheme of TNF-Selektokins (WO 02/22833) is indeed processable but not or only very little active.
Das
FasL-Modul wurde durch gentechnisches C-terminales Anhängen des
ligandenbindenden Moduls des korrespondierenden Rezeptors Fas inhibiert,
welches jedoch durch Tumor-assoziierte Proteasen abgespalten werden
kann. Hierzu wurde das Rezeptorfragment mittels eines Linkers angehängt, der
entsprechende Schnittstellen enthält. Durch ein N-terminates
Antikörper-Targeting-Modul kann
dieses als L-SC40-F-FasL-PL-Fas
bezeichnete FasL-Fusionsprotein im Zielgebiet angereichert werden.
Dieses FasL-Fusionsprotein wird nicht FAP-abhängig aktiviert (
Es folgt ein Sequenzprotokoll nach WIPO St. 25.It follows a sequence listing according to WIPO St. 25. Dieses kann von der amtlichen Veröffentlichungsplattform des DPMA heruntergeladen werden.This can from the official publication platform downloaded from the DPMA.
Claims (28)
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE102005036542A DE102005036542A1 (en) | 2005-08-03 | 2005-08-03 | CTL prodrug |
| PCT/EP2006/007581 WO2007014744A2 (en) | 2005-08-03 | 2006-07-31 | C-terminal tnf-family ligand (ctl) -prodrug |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE102005036542A DE102005036542A1 (en) | 2005-08-03 | 2005-08-03 | CTL prodrug |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| DE102005036542A1 true DE102005036542A1 (en) | 2007-02-08 |
Family
ID=37560705
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE102005036542A Ceased DE102005036542A1 (en) | 2005-08-03 | 2005-08-03 | CTL prodrug |
Country Status (2)
| Country | Link |
|---|---|
| DE (1) | DE102005036542A1 (en) |
| WO (1) | WO2007014744A2 (en) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2009022A1 (en) * | 2007-06-26 | 2008-12-31 | Apogenix GmbH | Trimeric death ligands with enhanced activity (tenascin) |
| CN115175926A (en) * | 2019-11-14 | 2022-10-11 | 狼人治疗公司 | Activatable cytokine polypeptides and methods of use thereof |
Families Citing this family (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1972350A1 (en) * | 2007-03-20 | 2008-09-24 | Rijksuniversiteit Groningen | Dual targeting system |
| EP2020249A1 (en) | 2007-08-01 | 2009-02-04 | Boehringer Ingelheim Pharma GmbH & Co. KG | Inhalator |
| CA3128656A1 (en) | 2007-08-22 | 2009-02-26 | The Regents Of The University Of California | Activatable binding polypeptides and methods of identification and use thereof |
| US8895702B2 (en) | 2008-12-08 | 2014-11-25 | City Of Hope | Development of masked therapeutic antibodies to limit off-target effects; application to anti-EGFR antibodies |
| CN106995495A (en) | 2009-01-12 | 2017-08-01 | 希托马克斯医疗有限责任公司 | Modified antibodies composition and its preparation and application |
| CN102481341B (en) | 2009-02-23 | 2017-05-17 | 希托马克斯医疗有限公司 | Proproteins and methods of use thereof |
| WO2010118477A1 (en) | 2009-04-17 | 2010-10-21 | Molecular Plant Breeding Nominees Ltd | Plant promoter operable in endosperm and uses thereof |
| WO2012042480A1 (en) | 2010-09-28 | 2012-04-05 | Kahr Medical Ltd. | Compositions and methods for treatment of hematological malignancies |
| JP6047142B2 (en) * | 2011-04-01 | 2016-12-21 | ウニヴェルズィテート シュトゥットガルト | Recombinant TNF ligand family member polypeptides having antibody binding domains and uses thereof |
| GB201402006D0 (en) | 2014-02-06 | 2014-03-26 | Oncomatryx Biopharma S L | Antibody-drug conjugates and immunotoxins |
| DK3489256T3 (en) | 2014-11-14 | 2021-05-25 | Hoffmann La Roche | Antigen-binding molecules comprising a TNF family ligand trimer |
| WO2016156291A1 (en) | 2015-03-31 | 2016-10-06 | F. Hoffmann-La Roche Ag | Antigen binding molecules comprising a trimeric tnf family ligand |
| AR106188A1 (en) | 2015-10-01 | 2017-12-20 | Hoffmann La Roche | ANTI-CD19 HUMANIZED HUMAN ANTIBODIES AND METHODS OF USE |
| EP3231813A1 (en) * | 2016-03-29 | 2017-10-18 | F. Hoffmann-La Roche AG | Trimeric costimulatory tnf family ligand-containing antigen binding molecules |
| WO2018178074A1 (en) | 2017-03-29 | 2018-10-04 | F. Hoffmann-La Roche Ag | Trimeric antigen binding molecules specific for a costimulatory tnf receptor |
| EP3986920B1 (en) | 2019-06-24 | 2025-04-16 | Universität Stuttgart | Tnfr2 agonists with improved stability |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2002022833A1 (en) * | 2000-09-15 | 2002-03-21 | Universität Stuttgart | Fusion protein from antibody cytokine-cytokine inhibitor (selectokine) for use as target-specific prodrug |
-
2005
- 2005-08-03 DE DE102005036542A patent/DE102005036542A1/en not_active Ceased
-
2006
- 2006-07-31 WO PCT/EP2006/007581 patent/WO2007014744A2/en not_active Ceased
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2002022833A1 (en) * | 2000-09-15 | 2002-03-21 | Universität Stuttgart | Fusion protein from antibody cytokine-cytokine inhibitor (selectokine) for use as target-specific prodrug |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2009022A1 (en) * | 2007-06-26 | 2008-12-31 | Apogenix GmbH | Trimeric death ligands with enhanced activity (tenascin) |
| WO2009000538A1 (en) * | 2007-06-26 | 2008-12-31 | Apogenix Gmbh | Trimeric death ligands with enhanced activity (tenascin) |
| CN115175926A (en) * | 2019-11-14 | 2022-10-11 | 狼人治疗公司 | Activatable cytokine polypeptides and methods of use thereof |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2007014744A3 (en) | 2007-04-12 |
| WO2007014744A2 (en) | 2007-02-08 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE102005036542A1 (en) | CTL prodrug | |
| US20250043008A1 (en) | Fusion protein of interferon (ifn) and anti-pd-l1 antibody and use thereof | |
| EP1317556A1 (en) | Fusion protein from antibody cytokine-cytokine inhibitor (selectokine) for use as target-specific prodrug | |
| DE69332221T2 (en) | Hepatocyte growth factor variant | |
| EP1317488B1 (en) | Site-specific, antibody-mediated activation of proapoptotic cytokine: amaice (antibody-mediated apoptosis inducing cytokine) | |
| DE69936382T2 (en) | THERAPEUTIC USES OF IL-17 HOMOLOGOUS POLYPEPTIDE | |
| DE60125381T2 (en) | COMPOSITIONS AND METHODS FOR ANALOGUE OF G-CSF | |
| Paterson et al. | Exploiting transferrin receptor for delivering drugs across the blood-brain barrier | |
| US20210095047A1 (en) | PSMA Targeting Trispecific Proteins and Methods of Use | |
| DE69132925T2 (en) | PROTEIN POLYLIGANDS TIED TO STABLE PROTEIN CORE STRUCTURE | |
| DE69027121T3 (en) | BINDING LANDING FOR TUMORNROCROSIS FACTOR | |
| DE69133036T2 (en) | CYTOKINE IMMUNOCONJUGATE | |
| DE69931908T2 (en) | INCREASING THE ANTIBODY CYTOKIN FUSION PROTEIN-MEDIATED IMMUNE RESPONSE BY CO-ADMINISTRATION WITH AN ANGIOGENIC INHIBITOR | |
| DE60034579T3 (en) | BAFF RECEPTOR (BCMA), AN IMMUNO-REGULATORY MEDIUM | |
| JP2023041829A (en) | Serine protease molecules and therapies | |
| DE60034586T2 (en) | APRIL RECEPTOR (BCMA) AND USES THEREOF | |
| DE10235248B4 (en) | Fusion protein with enhanced in vivo activity of erythropoietin | |
| EP3505536B1 (en) | Antibodies directed against the prostate-specific stem cell antigen and its use | |
| DE1003781T1 (en) | INTERLEUKIN-18 BINDING PROTEINS, THEIR PRODUCTION AND USE | |
| DE69532436T2 (en) | SINGLE CHAIN FORMS OF THE CLYCOPROTEIN HORMONE QUARTET | |
| KR20190124247A (en) | CSF1R-based chimeric protein | |
| EP1551977B1 (en) | Selective, local activation of members of the tnf ligand family of systemically inactive non-antibody tnf ligand fusion proteins | |
| DE69912743T2 (en) | TREATMENT OF FOLLICULAR LYMPHOMAS USING INHIBITORS OF THE LYMPHOTOXIN (LT) ACTIVATION WAY | |
| WO2007144046A2 (en) | Agent for the treatment of malignant diseases | |
| DE69904010T2 (en) | USE OF VIP TO CREATE A MEDICINE TO TREAT ENDOTOXIC SHOCKS IN MAMMALS |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| OP8 | Request for examination as to paragraph 44 patent law | ||
| 8131 | Rejection |