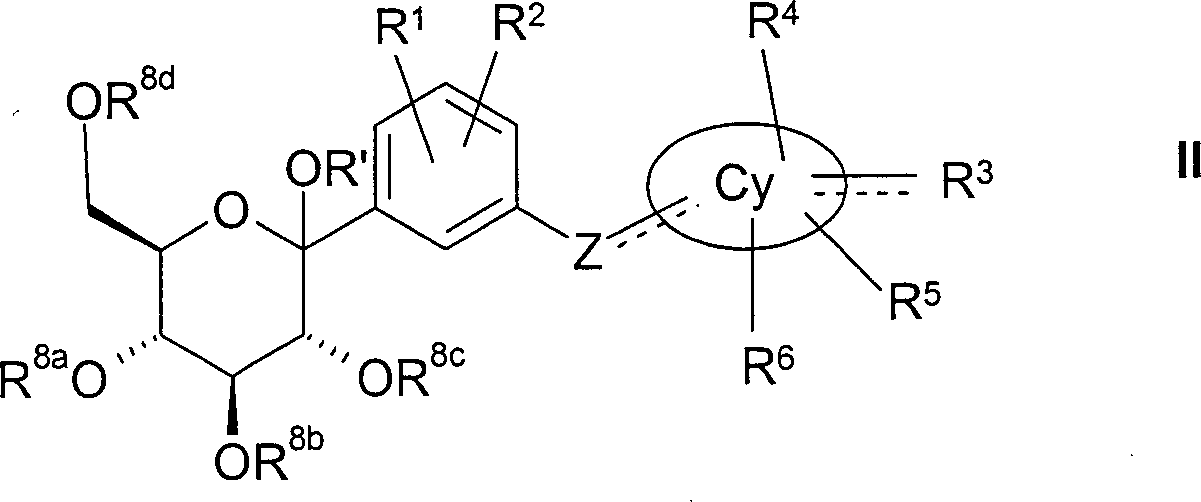
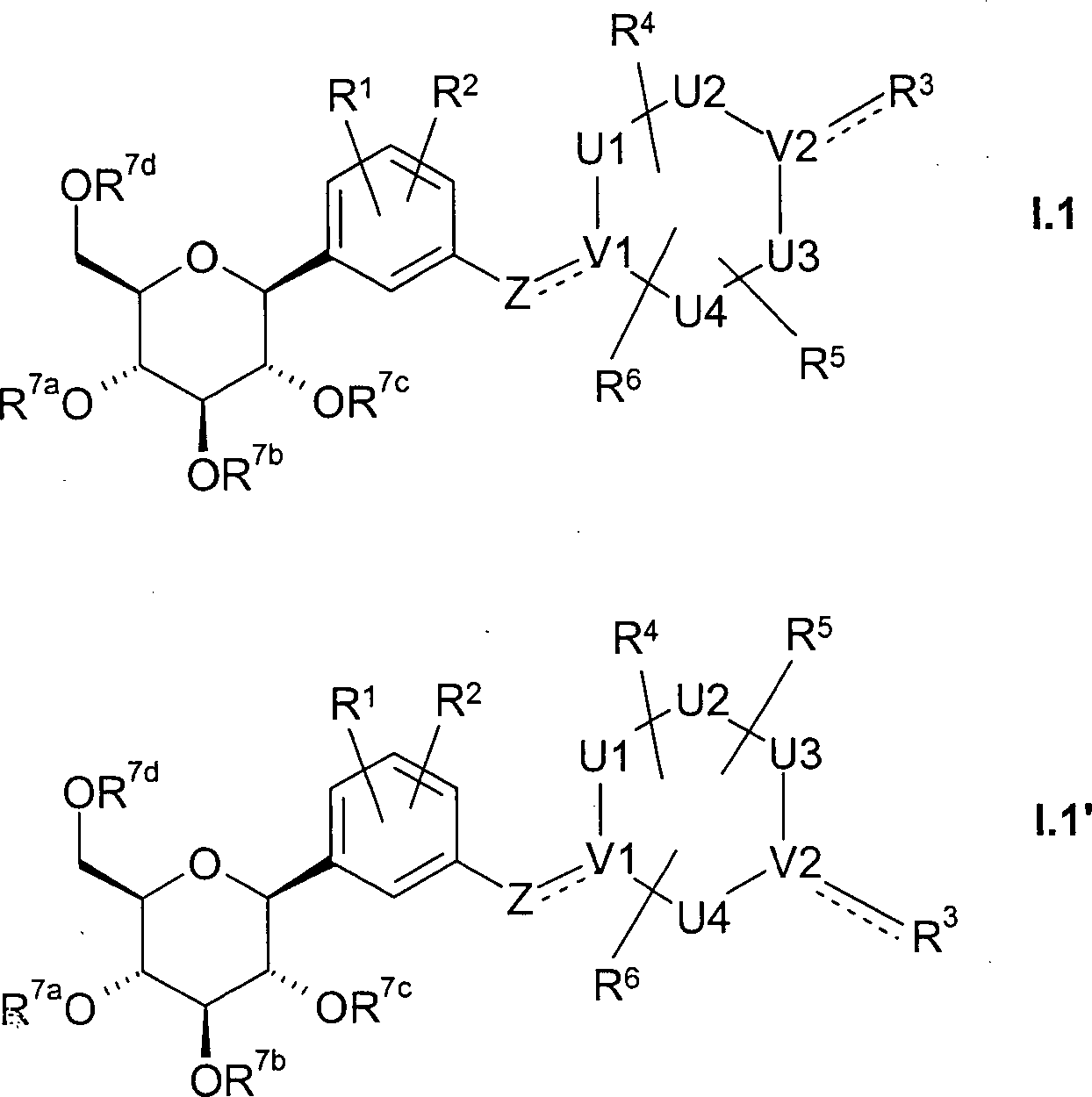
DE102004046012A1 - New D-glucopyranosylphenyl-substituted cyclic compounds useful as sodium-dependent glucose cotransporter inhibitors for treating metabolic diseases, e.g. diabetes - Google Patents
New D-glucopyranosylphenyl-substituted cyclic compounds useful as sodium-dependent glucose cotransporter inhibitors for treating metabolic diseases, e.g. diabetes Download PDFInfo
- Publication number
- DE102004046012A1 DE102004046012A1 DE102004046012A DE102004046012A DE102004046012A1 DE 102004046012 A1 DE102004046012 A1 DE 102004046012A1 DE 102004046012 A DE102004046012 A DE 102004046012A DE 102004046012 A DE102004046012 A DE 102004046012A DE 102004046012 A1 DE102004046012 A1 DE 102004046012A1
- Authority
- DE
- Germany
- Prior art keywords
- alkyl
- substituted
- cycloalkyl
- alkoxy
- group
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
- 102100037202 Sodium/myo-inositol cotransporter 2 Human genes 0.000 title claims abstract description 13
- 101710090560 Sodium/myo-inositol cotransporter 2 Proteins 0.000 title claims abstract description 13
- 208000030159 metabolic disease Diseases 0.000 title claims description 8
- 206010012601 diabetes mellitus Diseases 0.000 title claims description 7
- 239000003112 inhibitor Substances 0.000 title abstract description 13
- 150000001923 cyclic compounds Chemical class 0.000 title abstract 3
- 125000000217 alkyl group Chemical group 0.000 claims abstract description 134
- 229910052801 chlorine Inorganic materials 0.000 claims abstract description 90
- 229910052739 hydrogen Inorganic materials 0.000 claims abstract description 90
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims abstract description 68
- 229910052731 fluorine Inorganic materials 0.000 claims abstract description 66
- 229910002091 carbon monoxide Inorganic materials 0.000 claims abstract description 62
- 229910052760 oxygen Inorganic materials 0.000 claims abstract description 60
- 150000003839 salts Chemical class 0.000 claims abstract description 54
- 229910005965 SO 2 Inorganic materials 0.000 claims abstract description 51
- 125000003545 alkoxy group Chemical group 0.000 claims abstract description 48
- 125000000753 cycloalkyl group Chemical group 0.000 claims abstract description 40
- RWRDLPDLKQPQOW-UHFFFAOYSA-N Pyrrolidine Chemical compound C1CCNC1 RWRDLPDLKQPQOW-UHFFFAOYSA-N 0.000 claims abstract description 39
- 229910052717 sulfur Inorganic materials 0.000 claims abstract description 36
- 125000003118 aryl group Chemical group 0.000 claims abstract description 35
- GLUUGHFHXGJENI-UHFFFAOYSA-N Piperazine Chemical compound C1CNCCN1 GLUUGHFHXGJENI-UHFFFAOYSA-N 0.000 claims abstract description 34
- 229910052794 bromium Inorganic materials 0.000 claims abstract description 32
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 claims abstract description 26
- 125000000392 cycloalkenyl group Chemical group 0.000 claims abstract description 26
- 125000001072 heteroaryl group Chemical group 0.000 claims abstract description 23
- 229910052757 nitrogen Inorganic materials 0.000 claims abstract description 23
- YNAVUWVOSKDBBP-UHFFFAOYSA-N Morpholine Chemical compound C1COCCN1 YNAVUWVOSKDBBP-UHFFFAOYSA-N 0.000 claims abstract description 20
- 125000003342 alkenyl group Chemical group 0.000 claims abstract description 20
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims abstract description 18
- 125000001153 fluoro group Chemical group F* 0.000 claims abstract description 17
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 claims abstract description 16
- 125000000304 alkynyl group Chemical group 0.000 claims abstract description 15
- 125000005842 heteroatom Chemical group 0.000 claims abstract description 15
- 229920006395 saturated elastomer Polymers 0.000 claims abstract description 15
- 125000005129 aryl carbonyl group Chemical group 0.000 claims abstract description 11
- 125000002947 alkylene group Chemical group 0.000 claims abstract description 10
- 125000004453 alkoxycarbonyl group Chemical group 0.000 claims abstract description 8
- 125000004448 alkyl carbonyl group Chemical group 0.000 claims abstract description 8
- 125000002883 imidazolyl group Chemical group 0.000 claims abstract description 6
- 125000004076 pyridyl group Chemical group 0.000 claims abstract description 6
- 125000000168 pyrrolyl group Chemical group 0.000 claims abstract description 6
- 125000004450 alkenylene group Chemical group 0.000 claims abstract description 5
- 125000002541 furyl group Chemical group 0.000 claims abstract description 5
- 125000001544 thienyl group Chemical group 0.000 claims abstract description 5
- 125000001624 naphthyl group Chemical group 0.000 claims abstract description 4
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 claims abstract description 4
- -1 D-Glucopyranosyl-phenyl Chemical group 0.000 claims description 146
- 150000001875 compounds Chemical class 0.000 claims description 113
- 239000000460 chlorine Substances 0.000 claims description 85
- 239000001257 hydrogen Substances 0.000 claims description 83
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 claims description 82
- 125000001424 substituent group Chemical group 0.000 claims description 59
- 239000011737 fluorine Substances 0.000 claims description 58
- 125000001570 methylene group Chemical group [H]C([H])([*:1])[*:2] 0.000 claims description 53
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 claims description 52
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 claims description 51
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 41
- 125000004093 cyano group Chemical group *C#N 0.000 claims description 36
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 34
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 32
- 125000000325 methylidene group Chemical group [H]C([H])=* 0.000 claims description 31
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 claims description 30
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 claims description 29
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 claims description 29
- 125000004433 nitrogen atom Chemical group N* 0.000 claims description 25
- 239000000203 mixture Substances 0.000 claims description 24
- 229910052799 carbon Inorganic materials 0.000 claims description 23
- 238000011282 treatment Methods 0.000 claims description 22
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 claims description 21
- 239000003814 drug Substances 0.000 claims description 20
- 125000004432 carbon atom Chemical group C* 0.000 claims description 19
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 claims description 19
- 239000000126 substance Substances 0.000 claims description 17
- 238000004519 manufacturing process Methods 0.000 claims description 15
- 238000000034 method Methods 0.000 claims description 15
- 125000003601 C2-C6 alkynyl group Chemical group 0.000 claims description 14
- RGSFGYAAUTVSQA-UHFFFAOYSA-N Cyclopentane Chemical compound C1CCCC1 RGSFGYAAUTVSQA-UHFFFAOYSA-N 0.000 claims description 14
- 102000000070 Sodium-Glucose Transport Proteins Human genes 0.000 claims description 14
- 108010080361 Sodium-Glucose Transport Proteins Proteins 0.000 claims description 14
- 238000002360 preparation method Methods 0.000 claims description 14
- 125000006272 (C3-C7) cycloalkyl group Chemical group 0.000 claims description 13
- 125000001841 imino group Chemical group [H]N=* 0.000 claims description 13
- 238000011321 prophylaxis Methods 0.000 claims description 13
- 125000000882 C2-C6 alkenyl group Chemical group 0.000 claims description 12
- 125000004769 (C1-C4) alkylsulfonyl group Chemical group 0.000 claims description 11
- 201000010099 disease Diseases 0.000 claims description 11
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 11
- 125000001434 methanylylidene group Chemical group [H]C#[*] 0.000 claims description 11
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 claims description 11
- 125000006698 (C1-C3) dialkylamino group Chemical group 0.000 claims description 10
- 125000004429 atom Chemical group 0.000 claims description 10
- 125000000623 heterocyclic group Chemical group 0.000 claims description 10
- 230000002401 inhibitory effect Effects 0.000 claims description 10
- 125000000000 cycloalkoxy group Chemical group 0.000 claims description 9
- QBPPRVHXOZRESW-UHFFFAOYSA-N 1,4,7,10-tetraazacyclododecane Chemical class C1CNCCNCCNCCN1 QBPPRVHXOZRESW-UHFFFAOYSA-N 0.000 claims description 8
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical group [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 claims description 8
- 125000005740 oxycarbonyl group Chemical group [*:1]OC([*:2])=O 0.000 claims description 8
- 239000001301 oxygen Substances 0.000 claims description 8
- 125000004194 piperazin-1-yl group Chemical group [H]N1C([H])([H])C([H])([H])N(*)C([H])([H])C1([H])[H] 0.000 claims description 8
- 125000000876 trifluoromethoxy group Chemical group FC(F)(F)O* 0.000 claims description 8
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 claims description 7
- 125000003830 C1- C4 alkylcarbonylamino group Chemical group 0.000 claims description 7
- 208000002249 Diabetes Complications Diseases 0.000 claims description 7
- 125000004414 alkyl thio group Chemical group 0.000 claims description 7
- 125000003917 carbamoyl group Chemical group [H]N([H])C(*)=O 0.000 claims description 7
- 239000000969 carrier Substances 0.000 claims description 7
- 125000006576 di-(C1-C3-alkyl)-aminocarbonyl group Chemical group 0.000 claims description 7
- 239000003085 diluting agent Substances 0.000 claims description 7
- PNDPGZBMCMUPRI-UHFFFAOYSA-N iodine Chemical compound II PNDPGZBMCMUPRI-UHFFFAOYSA-N 0.000 claims description 7
- 125000004573 morpholin-4-yl group Chemical group N1(CCOCC1)* 0.000 claims description 7
- 125000000587 piperidin-1-yl group Chemical group [H]C1([H])N(*)C([H])([H])C([H])([H])C([H])([H])C1([H])[H] 0.000 claims description 7
- 230000008569 process Effects 0.000 claims description 7
- 206010012655 Diabetic complications Diseases 0.000 claims description 6
- ORILYTVJVMAKLC-UHFFFAOYSA-N adamantane Chemical compound C1C(C2)CC3CC1CC2C3 ORILYTVJVMAKLC-UHFFFAOYSA-N 0.000 claims description 6
- 125000004391 aryl sulfonyl group Chemical group 0.000 claims description 6
- 125000004104 aryloxy group Chemical group 0.000 claims description 6
- 125000004465 cycloalkenyloxy group Chemical group 0.000 claims description 6
- 125000004786 difluoromethoxy group Chemical group [H]C(F)(F)O* 0.000 claims description 6
- 125000001028 difluoromethyl group Chemical group [H]C(F)(F)* 0.000 claims description 6
- DMEGYFMYUHOHGS-UHFFFAOYSA-N heptamethylene Natural products C1CCCCCC1 DMEGYFMYUHOHGS-UHFFFAOYSA-N 0.000 claims description 6
- 125000005223 heteroarylcarbonyl group Chemical group 0.000 claims description 6
- VDFVNEFVBPFDSB-UHFFFAOYSA-N 1,3-dioxane Chemical compound C1COCOC1 VDFVNEFVBPFDSB-UHFFFAOYSA-N 0.000 claims description 5
- WQADWIOXOXRPLN-UHFFFAOYSA-N 1,3-dithiane Chemical compound C1CSCSC1 WQADWIOXOXRPLN-UHFFFAOYSA-N 0.000 claims description 5
- 125000003282 alkyl amino group Chemical group 0.000 claims description 5
- 125000005163 aryl sulfanyl group Chemical group 0.000 claims description 5
- 229910052796 boron Inorganic materials 0.000 claims description 5
- 125000005171 cycloalkylsulfanyl group Chemical group 0.000 claims description 5
- 125000005144 cycloalkylsulfonyl group Chemical group 0.000 claims description 5
- 125000000816 ethylene group Chemical group [H]C([H])([*:1])C([H])([H])[*:2] 0.000 claims description 5
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 claims description 5
- 125000004768 (C1-C4) alkylsulfinyl group Chemical group 0.000 claims description 4
- 125000005913 (C3-C6) cycloalkyl group Chemical group 0.000 claims description 4
- IMLSAISZLJGWPP-UHFFFAOYSA-N 1,3-dithiolane Chemical compound C1CSCS1 IMLSAISZLJGWPP-UHFFFAOYSA-N 0.000 claims description 4
- DHXVGJBLRPWPCS-UHFFFAOYSA-N Tetrahydropyran Chemical compound C1CCOCC1 DHXVGJBLRPWPCS-UHFFFAOYSA-N 0.000 claims description 4
- 125000000499 benzofuranyl group Chemical group O1C(=CC2=C1C=CC=C2)* 0.000 claims description 4
- 125000004196 benzothienyl group Chemical group S1C(=CC2=C1C=CC=C2)* 0.000 claims description 4
- 125000003236 benzoyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C(*)=O 0.000 claims description 4
- 125000002619 bicyclic group Chemical group 0.000 claims description 4
- 125000005149 cycloalkylsulfinyl group Chemical group 0.000 claims description 4
- 239000002934 diuretic Substances 0.000 claims description 4
- 229940079593 drug Drugs 0.000 claims description 4
- 125000005553 heteroaryloxy group Chemical group 0.000 claims description 4
- ORTFAQDWJHRMNX-UHFFFAOYSA-N hydroxidooxidocarbon(.) Chemical group O[C]=O ORTFAQDWJHRMNX-UHFFFAOYSA-N 0.000 claims description 4
- 125000001041 indolyl group Chemical group 0.000 claims description 4
- 125000002183 isoquinolinyl group Chemical group C1(=NC=CC2=CC=CC=C12)* 0.000 claims description 4
- 230000036961 partial effect Effects 0.000 claims description 4
- 125000002943 quinolinyl group Chemical group N1=C(C=CC2=CC=CC=C12)* 0.000 claims description 4
- 125000000472 sulfonyl group Chemical group *S(*)(=O)=O 0.000 claims description 4
- 125000003396 thiol group Chemical group [H]S* 0.000 claims description 4
- 201000001320 Atherosclerosis Diseases 0.000 claims description 3
- 210000002237 B-cell of pancreatic islet Anatomy 0.000 claims description 3
- 206010007558 Cardiac failure chronic Diseases 0.000 claims description 3
- 206010020772 Hypertension Diseases 0.000 claims description 3
- 208000008589 Obesity Diseases 0.000 claims description 3
- 125000004457 alkyl amino carbonyl group Chemical group 0.000 claims description 3
- 239000002220 antihypertensive agent Substances 0.000 claims description 3
- 229940030600 antihypertensive agent Drugs 0.000 claims description 3
- 125000005135 aryl sulfinyl group Chemical group 0.000 claims description 3
- 125000002837 carbocyclic group Chemical group 0.000 claims description 3
- 229940030606 diuretics Drugs 0.000 claims description 3
- 230000005764 inhibitory process Effects 0.000 claims description 3
- 150000007522 mineralic acids Chemical class 0.000 claims description 3
- 235000020824 obesity Nutrition 0.000 claims description 3
- 150000007524 organic acids Chemical class 0.000 claims description 3
- 235000005985 organic acids Nutrition 0.000 claims description 3
- 125000004430 oxygen atom Chemical group O* 0.000 claims description 3
- 125000004434 sulfur atom Chemical group 0.000 claims description 3
- RAOIDOHSFRTOEL-UHFFFAOYSA-N tetrahydrothiophene Chemical compound C1CCSC1 RAOIDOHSFRTOEL-UHFFFAOYSA-N 0.000 claims description 3
- 125000006559 (C1-C3) alkylamino group Chemical group 0.000 claims description 2
- 125000006597 (C1-C3) alkylcarbonylamino group Chemical group 0.000 claims description 2
- 125000004455 (C1-C3) alkylthio group Chemical group 0.000 claims description 2
- 125000004760 (C1-C4) alkylsulfonylamino group Chemical group 0.000 claims description 2
- 125000004214 1-pyrrolidinyl group Chemical group [H]C1([H])N(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 claims description 2
- 125000001054 5 membered carbocyclic group Chemical group 0.000 claims description 2
- 125000004008 6 membered carbocyclic group Chemical group 0.000 claims description 2
- 208000010444 Acidosis Diseases 0.000 claims description 2
- 208000032928 Dyslipidaemia Diseases 0.000 claims description 2
- 206010060378 Hyperinsulinaemia Diseases 0.000 claims description 2
- 201000001431 Hyperuricemia Diseases 0.000 claims description 2
- 208000013016 Hypoglycemia Diseases 0.000 claims description 2
- 206010022489 Insulin Resistance Diseases 0.000 claims description 2
- 208000007976 Ketosis Diseases 0.000 claims description 2
- 208000001145 Metabolic Syndrome Diseases 0.000 claims description 2
- 206010027417 Metabolic acidosis Diseases 0.000 claims description 2
- 206010030113 Oedema Diseases 0.000 claims description 2
- 201000000690 abdominal obesity-metabolic syndrome Diseases 0.000 claims description 2
- 125000004658 aryl carbonyl amino group Chemical group 0.000 claims description 2
- 125000004657 aryl sulfonyl amino group Chemical group 0.000 claims description 2
- 125000001246 bromo group Chemical group Br* 0.000 claims description 2
- 125000001309 chloro group Chemical group Cl* 0.000 claims description 2
- 230000007850 degeneration Effects 0.000 claims description 2
- 208000018914 glucose metabolism disease Diseases 0.000 claims description 2
- 125000005224 heteroarylcarbonylamino group Chemical group 0.000 claims description 2
- 125000005143 heteroarylsulfonyl group Chemical group 0.000 claims description 2
- 230000003451 hyperinsulinaemic effect Effects 0.000 claims description 2
- 201000008980 hyperinsulinism Diseases 0.000 claims description 2
- 230000004140 ketosis Effects 0.000 claims description 2
- 208000001072 type 2 diabetes mellitus Diseases 0.000 claims description 2
- RAHZWNYVWXNFOC-UHFFFAOYSA-N Sulphur dioxide Chemical group O=S=O RAHZWNYVWXNFOC-UHFFFAOYSA-N 0.000 claims 1
- 125000004981 cycloalkylmethyl group Chemical group 0.000 claims 1
- 208000016097 disease of metabolism Diseases 0.000 claims 1
- 230000000694 effects Effects 0.000 abstract description 7
- 238000012360 testing method Methods 0.000 abstract description 4
- 230000003178 anti-diabetic effect Effects 0.000 abstract description 2
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 abstract description 2
- 125000002346 iodo group Chemical group I* 0.000 abstract description 2
- 125000004785 fluoromethoxy group Chemical group [H]C([H])(F)O* 0.000 abstract 2
- 125000004216 fluoromethyl group Chemical group [H]C([H])(F)* 0.000 abstract 2
- 125000005843 halogen group Chemical group 0.000 abstract 2
- KQKLLBVOWSTIFZ-RBWPFNQVSA-N 4-[(3,4-dimethoxyphenyl)methyl]-3-[[3,4-dimethoxy-5-[(2s,3r,4r,5s,6r)-3,4,5-trihydroxy-6-(hydroxymethyl)oxan-2-yl]phenyl]methyl]oxolan-2-one Chemical compound C1=C(OC)C(OC)=CC=C1CC1C(CC=2C=C(C(OC)=C(OC)C=2)[C@H]2[C@@H]([C@@H](O)[C@H](O)[C@@H](CO)O2)O)C(=O)OC1 KQKLLBVOWSTIFZ-RBWPFNQVSA-N 0.000 abstract 1
- 208000001953 Hypotension Diseases 0.000 abstract 1
- 125000003806 alkyl carbonyl amino group Chemical group 0.000 abstract 1
- 230000001539 anorectic effect Effects 0.000 abstract 1
- 230000003110 anti-inflammatory effect Effects 0.000 abstract 1
- 230000002402 anti-lipaemic effect Effects 0.000 abstract 1
- 239000003472 antidiabetic agent Substances 0.000 abstract 1
- 229960002708 antigout preparations Drugs 0.000 abstract 1
- 125000003435 aroyl group Chemical group 0.000 abstract 1
- 206010061428 decreased appetite Diseases 0.000 abstract 1
- 208000021822 hypotensive Diseases 0.000 abstract 1
- 230000001077 hypotensive effect Effects 0.000 abstract 1
- 230000010534 mechanism of action Effects 0.000 abstract 1
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 69
- 239000000243 solution Substances 0.000 description 62
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 51
- 150000003254 radicals Chemical class 0.000 description 41
- 238000001819 mass spectrum Methods 0.000 description 35
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 30
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 28
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 27
- 239000002904 solvent Substances 0.000 description 25
- 239000013543 active substance Substances 0.000 description 23
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 22
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 20
- 210000004027 cell Anatomy 0.000 description 18
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 17
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 17
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 14
- 238000006243 chemical reaction Methods 0.000 description 14
- 229910052938 sodium sulfate Inorganic materials 0.000 description 14
- 235000011152 sodium sulphate Nutrition 0.000 description 14
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 13
- 239000002253 acid Substances 0.000 description 13
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 12
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 12
- 125000004122 cyclic group Chemical group 0.000 description 12
- 239000012074 organic phase Substances 0.000 description 11
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 10
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 10
- 239000000741 silica gel Substances 0.000 description 10
- 229910002027 silica gel Inorganic materials 0.000 description 10
- 125000006376 (C3-C10) cycloalkyl group Chemical group 0.000 description 9
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 9
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 9
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 9
- KZMGYPLQYOPHEL-UHFFFAOYSA-N Boron trifluoride etherate Chemical compound FB(F)F.CCOCC KZMGYPLQYOPHEL-UHFFFAOYSA-N 0.000 description 8
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 8
- 239000004480 active ingredient Substances 0.000 description 8
- 239000005557 antagonist Substances 0.000 description 8
- 229910052736 halogen Inorganic materials 0.000 description 8
- 239000011734 sodium Substances 0.000 description 8
- 108091006269 SLC5A2 Proteins 0.000 description 7
- 102100020888 Sodium/glucose cotransporter 2 Human genes 0.000 description 7
- 238000003776 cleavage reaction Methods 0.000 description 7
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 7
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 7
- 229910052751 metal Inorganic materials 0.000 description 7
- 239000002184 metal Substances 0.000 description 7
- 230000007017 scission Effects 0.000 description 7
- 239000011780 sodium chloride Substances 0.000 description 7
- 238000003786 synthesis reaction Methods 0.000 description 7
- WMFOQBRAJBCJND-UHFFFAOYSA-M Lithium hydroxide Chemical compound [Li+].[OH-] WMFOQBRAJBCJND-UHFFFAOYSA-M 0.000 description 6
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 6
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 6
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 6
- 229960000583 acetic acid Drugs 0.000 description 6
- 230000015572 biosynthetic process Effects 0.000 description 6
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 6
- HGCIXCUEYOPUTN-UHFFFAOYSA-N cyclohexene Chemical compound C1CCC=CC1 HGCIXCUEYOPUTN-UHFFFAOYSA-N 0.000 description 6
- 150000002367 halogens Chemical class 0.000 description 6
- 150000002902 organometallic compounds Chemical class 0.000 description 6
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 6
- FPGGTKZVZWFYPV-UHFFFAOYSA-M tetrabutylammonium fluoride Chemical compound [F-].CCCC[N+](CCCC)(CCCC)CCCC FPGGTKZVZWFYPV-UHFFFAOYSA-M 0.000 description 6
- AQRLNPVMDITEJU-UHFFFAOYSA-N triethylsilane Chemical compound CC[SiH](CC)CC AQRLNPVMDITEJU-UHFFFAOYSA-N 0.000 description 6
- RIOQSEWOXXDEQQ-UHFFFAOYSA-N triphenylphosphine Chemical compound C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-N 0.000 description 6
- 229920002261 Corn starch Polymers 0.000 description 5
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 5
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 5
- 239000000556 agonist Substances 0.000 description 5
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 5
- 239000002775 capsule Substances 0.000 description 5
- 239000008120 corn starch Substances 0.000 description 5
- 230000000875 corresponding effect Effects 0.000 description 5
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 5
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 5
- 235000019359 magnesium stearate Nutrition 0.000 description 5
- 125000004674 methylcarbonyl group Chemical group CC(=O)* 0.000 description 5
- XUWHAWMETYGRKB-UHFFFAOYSA-N piperidin-2-one Chemical compound O=C1CCCCN1 XUWHAWMETYGRKB-UHFFFAOYSA-N 0.000 description 5
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 5
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 5
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 5
- 125000006239 protecting group Chemical group 0.000 description 5
- PHOQVHQSTUBQQK-SQOUGZDYSA-N D-glucono-1,5-lactone Chemical compound OC[C@H]1OC(=O)[C@H](O)[C@@H](O)[C@@H]1O PHOQVHQSTUBQQK-SQOUGZDYSA-N 0.000 description 4
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 4
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 4
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 4
- YTPLMLYBLZKORZ-UHFFFAOYSA-N Thiophene Chemical compound C=1C=CSC=1 YTPLMLYBLZKORZ-UHFFFAOYSA-N 0.000 description 4
- 150000007513 acids Chemical class 0.000 description 4
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 4
- 239000003638 chemical reducing agent Substances 0.000 description 4
- LPIQUOYDBNQMRZ-UHFFFAOYSA-N cyclopentene Chemical compound C1CC=CC1 LPIQUOYDBNQMRZ-UHFFFAOYSA-N 0.000 description 4
- 238000001035 drying Methods 0.000 description 4
- VSEAAEQOQBMPQF-UHFFFAOYSA-N morpholin-3-one Chemical compound O=C1COCCN1 VSEAAEQOQBMPQF-UHFFFAOYSA-N 0.000 description 4
- IWELDVXSEVIIGI-UHFFFAOYSA-N piperazin-2-one Chemical compound O=C1CNCCN1 IWELDVXSEVIIGI-UHFFFAOYSA-N 0.000 description 4
- 230000001681 protective effect Effects 0.000 description 4
- 125000003226 pyrazolyl group Chemical group 0.000 description 4
- 235000011121 sodium hydroxide Nutrition 0.000 description 4
- 239000000829 suppository Substances 0.000 description 4
- 125000000026 trimethylsilyl group Chemical group [H]C([H])([H])[Si]([*])(C([H])([H])[H])C([H])([H])[H] 0.000 description 4
- CSRZQMIRAZTJOY-UHFFFAOYSA-N trimethylsilyl iodide Chemical compound C[Si](C)(C)I CSRZQMIRAZTJOY-UHFFFAOYSA-N 0.000 description 4
- YEJRWHAVMIAJKC-UHFFFAOYSA-N 4-Butyrolactone Chemical compound O=C1CCCO1 YEJRWHAVMIAJKC-UHFFFAOYSA-N 0.000 description 3
- UEVFFMZHGNYDKM-UHFFFAOYSA-N 5-bromo-2-chlorophenol Chemical compound OC1=CC(Br)=CC=C1Cl UEVFFMZHGNYDKM-UHFFFAOYSA-N 0.000 description 3
- OZJPLYNZGCXSJM-UHFFFAOYSA-N 5-valerolactone Chemical compound O=C1CCCCO1 OZJPLYNZGCXSJM-UHFFFAOYSA-N 0.000 description 3
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 3
- WFDIJRYMOXRFFG-UHFFFAOYSA-N Acetic anhydride Chemical compound CC(=O)OC(C)=O WFDIJRYMOXRFFG-UHFFFAOYSA-N 0.000 description 3
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 3
- BVOZUYJLXINXTG-DHJDKVCWSA-N C1C[C@@H](OC)CC[C@H]1OC1=CC([C@]2(O)[C@@H]([C@@H](O)[C@H](O)[C@@H](CO)O2)O)=CC=C1Cl Chemical compound C1C[C@@H](OC)CC[C@H]1OC1=CC([C@]2(O)[C@@H]([C@@H](O)[C@H](O)[C@@H](CO)O2)O)=CC=C1Cl BVOZUYJLXINXTG-DHJDKVCWSA-N 0.000 description 3
- LXGBGZOYKCDRQU-WGSAOQKQSA-N C=1C=CC=CC=1[Si](C=1C=CC=CC=1)(C(C)(C)C)O[C@H]1CC[C@H](O)CC1 Chemical compound C=1C=CC=CC=1[Si](C=1C=CC=CC=1)(C(C)(C)C)O[C@H]1CC[C@H](O)CC1 LXGBGZOYKCDRQU-WGSAOQKQSA-N 0.000 description 3
- BVOZUYJLXINXTG-NNFODTCUSA-N COC1CCC(CC1)Oc1cc(ccc1Cl)[C@@]1(O)O[C@H](CO)[C@@H](O)[C@H](O)[C@H]1O Chemical compound COC1CCC(CC1)Oc1cc(ccc1Cl)[C@@]1(O)O[C@H](CO)[C@@H](O)[C@H](O)[C@H]1O BVOZUYJLXINXTG-NNFODTCUSA-N 0.000 description 3
- FOTWJKHCRNLWCZ-AEGUCURASA-N COC1CCC(Cc2cccc(c2)[C@@]2(O)O[C@H](CO)[C@@H](O)[C@H](O)[C@H]2O)CC1 Chemical compound COC1CCC(Cc2cccc(c2)[C@@]2(O)O[C@H](CO)[C@@H](O)[C@H](O)[C@H]2O)CC1 FOTWJKHCRNLWCZ-AEGUCURASA-N 0.000 description 3
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical group [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 3
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 3
- SJRJJKPEHAURKC-UHFFFAOYSA-N N-Methylmorpholine Chemical compound CN1CCOCC1 SJRJJKPEHAURKC-UHFFFAOYSA-N 0.000 description 3
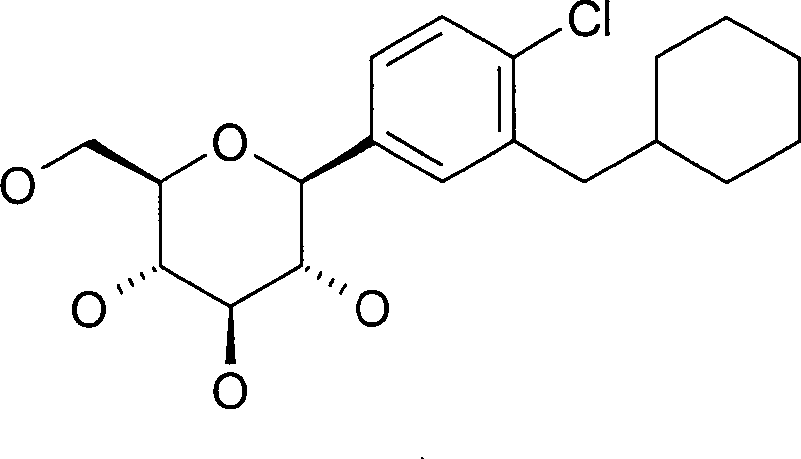
- XVCDHHNWKIEYQH-UJWQCDCRSA-N OC[C@H]1O[C@@](O)([C@H](O)[C@@H](O)[C@@H]1O)c1ccc(Cl)c(CC2CCCCC2)c1 Chemical compound OC[C@H]1O[C@@](O)([C@H](O)[C@@H](O)[C@@H]1O)c1ccc(Cl)c(CC2CCCCC2)c1 XVCDHHNWKIEYQH-UJWQCDCRSA-N 0.000 description 3
- QPJKQPJQEYAXRK-URBAORLTSA-N O[C@]1([C@H](O)[C@@H](O)[C@H](O)[C@H](O1)CO)C1=CC(=CC=C1)C=C1CCC(CC1)O Chemical compound O[C@]1([C@H](O)[C@@H](O)[C@H](O)[C@H](O1)CO)C1=CC(=CC=C1)C=C1CCC(CC1)O QPJKQPJQEYAXRK-URBAORLTSA-N 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- 125000002777 acetyl group Chemical group [H]C([H])([H])C(*)=O 0.000 description 3
- 239000002333 angiotensin II receptor antagonist Substances 0.000 description 3
- 239000003054 catalyst Substances 0.000 description 3
- 238000004587 chromatography analysis Methods 0.000 description 3
- 239000002299 complementary DNA Substances 0.000 description 3
- 230000001419 dependent effect Effects 0.000 description 3
- 239000002552 dosage form Substances 0.000 description 3
- 125000003754 ethoxycarbonyl group Chemical group C(=O)(OCC)* 0.000 description 3
- 125000004672 ethylcarbonyl group Chemical group [H]C([H])([H])C([H])([H])C(*)=O 0.000 description 3
- 239000007903 gelatin capsule Substances 0.000 description 3
- 235000012209 glucono delta-lactone Nutrition 0.000 description 3
- 229960003681 gluconolactone Drugs 0.000 description 3
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 3
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 description 3
- 229910052740 iodine Inorganic materials 0.000 description 3
- 239000008101 lactose Substances 0.000 description 3
- 230000000144 pharmacologic effect Effects 0.000 description 3
- TYJJADVDDVDEDZ-UHFFFAOYSA-M potassium hydrogencarbonate Chemical class [K+].OC([O-])=O TYJJADVDDVDEDZ-UHFFFAOYSA-M 0.000 description 3
- 239000000843 powder Substances 0.000 description 3
- HNJBEVLQSNELDL-UHFFFAOYSA-N pyrrolidin-2-one Chemical compound O=C1CCCN1 HNJBEVLQSNELDL-UHFFFAOYSA-N 0.000 description 3
- 235000017557 sodium bicarbonate Nutrition 0.000 description 3
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 3
- 125000001412 tetrahydropyranyl group Chemical group 0.000 description 3
- 125000003831 tetrazolyl group Chemical group 0.000 description 3
- NOOLISFMXDJSKH-KXUCPTDWSA-N (-)-Menthol Chemical compound CC(C)[C@@H]1CC[C@@H](C)C[C@H]1O NOOLISFMXDJSKH-KXUCPTDWSA-N 0.000 description 2
- HSINOMROUCMIEA-FGVHQWLLSA-N (2s,4r)-4-[(3r,5s,6r,7r,8s,9s,10s,13r,14s,17r)-6-ethyl-3,7-dihydroxy-10,13-dimethyl-2,3,4,5,6,7,8,9,11,12,14,15,16,17-tetradecahydro-1h-cyclopenta[a]phenanthren-17-yl]-2-methylpentanoic acid Chemical compound C([C@@]12C)C[C@@H](O)C[C@H]1[C@@H](CC)[C@@H](O)[C@@H]1[C@@H]2CC[C@]2(C)[C@@H]([C@H](C)C[C@H](C)C(O)=O)CC[C@H]21 HSINOMROUCMIEA-FGVHQWLLSA-N 0.000 description 2
- SXZHCAYLXOHCCO-UHFFFAOYSA-N (5-bromo-2-chlorophenoxy)-tri(propan-2-yl)silane Chemical compound CC(C)[Si](C(C)C)(C(C)C)OC1=CC(Br)=CC=C1Cl SXZHCAYLXOHCCO-UHFFFAOYSA-N 0.000 description 2
- 125000006702 (C1-C18) alkyl group Chemical group 0.000 description 2
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 description 2
- UWYZHKAOTLEWKK-UHFFFAOYSA-N 1,2,3,4-tetrahydroisoquinoline Chemical compound C1=CC=C2CNCCC2=C1 UWYZHKAOTLEWKK-UHFFFAOYSA-N 0.000 description 2
- LBUJPTNKIBCYBY-UHFFFAOYSA-N 1,2,3,4-tetrahydroquinoline Chemical compound C1=CC=C2CCCNC2=C1 LBUJPTNKIBCYBY-UHFFFAOYSA-N 0.000 description 2
- WNXJIVFYUVYPPR-UHFFFAOYSA-N 1,3-dioxolane Chemical compound C1COCO1 WNXJIVFYUVYPPR-UHFFFAOYSA-N 0.000 description 2
- HBEDSQVIWPRPAY-UHFFFAOYSA-N 2,3-dihydrobenzofuran Chemical compound C1=CC=C2OCCC2=C1 HBEDSQVIWPRPAY-UHFFFAOYSA-N 0.000 description 2
- VHYFNPMBLIVWCW-UHFFFAOYSA-N 4-Dimethylaminopyridine Chemical compound CN(C)C1=CC=NC=C1 VHYFNPMBLIVWCW-UHFFFAOYSA-N 0.000 description 2
- DPKKRQAEYWOISP-UHFFFAOYSA-N 5-bromo-2-chlorobenzaldehyde Chemical compound ClC1=CC=C(Br)C=C1C=O DPKKRQAEYWOISP-UHFFFAOYSA-N 0.000 description 2
- 150000007578 6-membered cyclic compounds Chemical class 0.000 description 2
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 2
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 2
- VHCOUPJDHUIDPY-AOOOYVTPSA-N C1C[C@@H](O)CC[C@H]1OC1=CC(Br)=CC=C1Cl Chemical compound C1C[C@@H](O)CC[C@H]1OC1=CC(Br)=CC=C1Cl VHCOUPJDHUIDPY-AOOOYVTPSA-N 0.000 description 2
- BVOZUYJLXINXTG-ABUWFKSUSA-N C1C[C@@H](OC)CC[C@@H]1OC1=CC([C@]2(O)[C@@H]([C@@H](O)[C@H](O)[C@@H](CO)O2)O)=CC=C1Cl Chemical compound C1C[C@@H](OC)CC[C@@H]1OC1=CC([C@]2(O)[C@@H]([C@@H](O)[C@H](O)[C@@H](CO)O2)O)=CC=C1Cl BVOZUYJLXINXTG-ABUWFKSUSA-N 0.000 description 2
- PXNBIVAMUBHHFF-SOJCKMGWSA-N COC1CCC(Cc2cc(ccc2Cl)[C@@]2(O)O[C@H](CO)[C@@H](O)[C@H](O)[C@H]2O)CC1 Chemical compound COC1CCC(Cc2cc(ccc2Cl)[C@@]2(O)O[C@H](CO)[C@@H](O)[C@H](O)[C@H]2O)CC1 PXNBIVAMUBHHFF-SOJCKMGWSA-N 0.000 description 2
- KNEUGQRYMVHNCC-WVTYJSCVSA-N COC1CCC(Cc2cccc(c2)[C@@]2(O)O[C@H](COC(C)=O)[C@@H](OC(C)=O)[C@H](OC(C)=O)[C@H]2OC(C)=O)CC1 Chemical compound COC1CCC(Cc2cccc(c2)[C@@]2(O)O[C@H](COC(C)=O)[C@@H](OC(C)=O)[C@H](OC(C)=O)[C@H]2OC(C)=O)CC1 KNEUGQRYMVHNCC-WVTYJSCVSA-N 0.000 description 2
- 241000819038 Chichester Species 0.000 description 2
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 2
- KDXKERNSBIXSRK-RXMQYKEDSA-N D-lysine Chemical compound NCCCC[C@@H](N)C(O)=O KDXKERNSBIXSRK-RXMQYKEDSA-N 0.000 description 2
- NOOLISFMXDJSKH-UHFFFAOYSA-N DL-menthol Natural products CC(C)C1CCC(C)CC1O NOOLISFMXDJSKH-UHFFFAOYSA-N 0.000 description 2
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 2
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 2
- DTHNMHAUYICORS-KTKZVXAJSA-N Glucagon-like peptide 1 Chemical compound C([C@@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCCCN)C(=O)NCC(=O)N[C@@H](CCCNC(N)=N)C(N)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCCCN)NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CCC(N)=O)NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C)NC(=O)[C@@H](N)CC=1N=CNC=1)[C@@H](C)O)[C@@H](C)O)C(C)C)C1=CC=CC=C1 DTHNMHAUYICORS-KTKZVXAJSA-N 0.000 description 2
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 2
- 239000012981 Hank's balanced salt solution Substances 0.000 description 2
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 2
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 2
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 2
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 2
- UFWIBTONFRDIAS-UHFFFAOYSA-N Naphthalene Chemical compound C1=CC=CC2=CC=CC=C21 UFWIBTONFRDIAS-UHFFFAOYSA-N 0.000 description 2
- POXYJVAQRGQTEB-UJWQCDCRSA-N OC[C@H]1O[C@@](O)([C@H](O)[C@@H](O)[C@@H]1O)c1ccc(Cl)c(C=C2CCCCC2)c1 Chemical compound OC[C@H]1O[C@@](O)([C@H](O)[C@@H](O)[C@@H]1O)c1ccc(Cl)c(C=C2CCCCC2)c1 POXYJVAQRGQTEB-UJWQCDCRSA-N 0.000 description 2
- ZSUPMFQDMPEXPJ-RZTOPHRASA-N O[C@]1([C@H](O)[C@@H](O)[C@H](O)[C@H](O1)CO)C1=CC(=CC=C1)CC1CCC(CC1)O Chemical compound O[C@]1([C@H](O)[C@@H](O)[C@H](O)[C@H](O1)CO)C1=CC(=CC=C1)CC1CCC(CC1)O ZSUPMFQDMPEXPJ-RZTOPHRASA-N 0.000 description 2
- 108010016731 PPAR gamma Proteins 0.000 description 2
- OFBQJSOFQDEBGM-UHFFFAOYSA-N Pentane Chemical compound CCCCC OFBQJSOFQDEBGM-UHFFFAOYSA-N 0.000 description 2
- 102100038831 Peroxisome proliferator-activated receptor alpha Human genes 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- KAESVJOAVNADME-UHFFFAOYSA-N Pyrrole Chemical compound C=1C=CNC=1 KAESVJOAVNADME-UHFFFAOYSA-N 0.000 description 2
- SMWDFEZZVXVKRB-UHFFFAOYSA-N Quinoline Chemical compound N1=CC=CC2=CC=CC=C21 SMWDFEZZVXVKRB-UHFFFAOYSA-N 0.000 description 2
- YASAKCUCGLMORW-UHFFFAOYSA-N Rosiglitazone Chemical compound C=1C=CC=NC=1N(C)CCOC(C=C1)=CC=C1CC1SC(=O)NC1=O YASAKCUCGLMORW-UHFFFAOYSA-N 0.000 description 2
- 108091006277 SLC5A1 Proteins 0.000 description 2
- KEAYESYHFKHZAL-UHFFFAOYSA-N Sodium Chemical compound [Na] KEAYESYHFKHZAL-UHFFFAOYSA-N 0.000 description 2
- WQDUMFSSJAZKTM-UHFFFAOYSA-N Sodium methoxide Chemical compound [Na+].[O-]C WQDUMFSSJAZKTM-UHFFFAOYSA-N 0.000 description 2
- 102000058090 Sodium-Glucose Transporter 1 Human genes 0.000 description 2
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 2
- 108010084455 Zeocin Proteins 0.000 description 2
- RGQKALCUPVQXEP-OUUBHVDSSA-N [(2r,3r,4s,5r,6r)-3,4,5-triacetyloxy-6-(4-chloro-3-hydroxyphenyl)-6-hydroxyoxan-2-yl]methyl acetate Chemical compound CC(=O)O[C@@H]1[C@@H](OC(C)=O)[C@H](OC(C)=O)[C@@H](COC(=O)C)O[C@]1(O)C1=CC=C(Cl)C(O)=C1 RGQKALCUPVQXEP-OUUBHVDSSA-N 0.000 description 2
- NXQXDXQLWNHTSC-XYPQWYOHSA-N [(2r,3r,4s,5r,6r)-3,4,5-triacetyloxy-6-[4-chloro-3-tri(propan-2-yl)silyloxyphenyl]-6-hydroxyoxan-2-yl]methyl acetate Chemical compound C1=C(Cl)C(O[Si](C(C)C)(C(C)C)C(C)C)=CC([C@]2(O)[C@@H]([C@@H](OC(C)=O)[C@H](OC(C)=O)[C@@H](COC(C)=O)O2)OC(C)=O)=C1 NXQXDXQLWNHTSC-XYPQWYOHSA-N 0.000 description 2
- DHKHKXVYLBGOIT-UHFFFAOYSA-N acetaldehyde Diethyl Acetal Natural products CCOC(C)OCC DHKHKXVYLBGOIT-UHFFFAOYSA-N 0.000 description 2
- 150000001241 acetals Chemical class 0.000 description 2
- 125000002252 acyl group Chemical group 0.000 description 2
- RDOXTESZEPMUJZ-UHFFFAOYSA-N anisole Chemical compound COC1=CC=CC=C1 RDOXTESZEPMUJZ-UHFFFAOYSA-N 0.000 description 2
- 239000007864 aqueous solution Substances 0.000 description 2
- 239000003125 aqueous solvent Substances 0.000 description 2
- 238000003556 assay Methods 0.000 description 2
- 239000012131 assay buffer Substances 0.000 description 2
- 239000002585 base Substances 0.000 description 2
- 210000000227 basophil cell of anterior lobe of hypophysis Anatomy 0.000 description 2
- 125000001584 benzyloxycarbonyl group Chemical group C(=O)(OCC1=CC=CC=C1)* 0.000 description 2
- LPCWKMYWISGVSK-UHFFFAOYSA-N bicyclo[3.2.1]octane Chemical compound C1C2CCC1CCC2 LPCWKMYWISGVSK-UHFFFAOYSA-N 0.000 description 2
- 239000003613 bile acid Substances 0.000 description 2
- UORVGPXVDQYIDP-UHFFFAOYSA-N borane Chemical compound B UORVGPXVDQYIDP-UHFFFAOYSA-N 0.000 description 2
- ILAHWRKJUDSMFH-UHFFFAOYSA-N boron tribromide Chemical compound BrB(Br)Br ILAHWRKJUDSMFH-UHFFFAOYSA-N 0.000 description 2
- 239000000872 buffer Substances 0.000 description 2
- 150000001721 carbon Chemical group 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 239000003795 chemical substances by application Substances 0.000 description 2
- KQIADDMXRMTWHZ-UHFFFAOYSA-N chloro-tri(propan-2-yl)silane Chemical compound CC(C)[Si](Cl)(C(C)C)C(C)C KQIADDMXRMTWHZ-UHFFFAOYSA-N 0.000 description 2
- HVYWMOMLDIMFJA-DPAQBDIFSA-N cholesterol Chemical compound C1C=C2C[C@@H](O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CCCC(C)C)[C@@]1(C)CC2 HVYWMOMLDIMFJA-DPAQBDIFSA-N 0.000 description 2
- 235000015165 citric acid Nutrition 0.000 description 2
- NNBZCPXTIHJBJL-UHFFFAOYSA-N decalin Chemical compound C1CCCC2CCCCC21 NNBZCPXTIHJBJL-UHFFFAOYSA-N 0.000 description 2
- 125000000532 dioxanyl group Chemical group 0.000 description 2
- 239000012894 fetal calf serum Substances 0.000 description 2
- 239000008103 glucose Substances 0.000 description 2
- 239000001963 growth medium Substances 0.000 description 2
- 229940093915 gynecological organic acid Drugs 0.000 description 2
- 150000002430 hydrocarbons Chemical group 0.000 description 2
- 238000011534 incubation Methods 0.000 description 2
- PQNFLJBBNBOBRQ-UHFFFAOYSA-N indane Chemical compound C1=CC=C2CCCC2=C1 PQNFLJBBNBOBRQ-UHFFFAOYSA-N 0.000 description 2
- 238000003780 insertion Methods 0.000 description 2
- 230000037431 insertion Effects 0.000 description 2
- AWJUIBRHMBBTKR-UHFFFAOYSA-N isoquinoline Chemical compound C1=NC=CC2=CC=CC=C21 AWJUIBRHMBBTKR-UHFFFAOYSA-N 0.000 description 2
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 2
- UBJFKNSINUCEAL-UHFFFAOYSA-N lithium;2-methylpropane Chemical compound [Li+].C[C-](C)C UBJFKNSINUCEAL-UHFFFAOYSA-N 0.000 description 2
- 239000011777 magnesium Substances 0.000 description 2
- 229910052749 magnesium Inorganic materials 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- 239000002609 medium Substances 0.000 description 2
- 229940098779 methanesulfonic acid Drugs 0.000 description 2
- 125000001160 methoxycarbonyl group Chemical group [H]C([H])([H])OC(*)=O 0.000 description 2
- 239000002480 mineral oil Substances 0.000 description 2
- 235000010446 mineral oil Nutrition 0.000 description 2
- 230000003287 optical effect Effects 0.000 description 2
- CTSLXHKWHWQRSH-UHFFFAOYSA-N oxalyl chloride Chemical compound ClC(=O)C(Cl)=O CTSLXHKWHWQRSH-UHFFFAOYSA-N 0.000 description 2
- 108091008725 peroxisome proliferator-activated receptors alpha Proteins 0.000 description 2
- 239000008194 pharmaceutical composition Substances 0.000 description 2
- UYWQUFXKFGHYNT-UHFFFAOYSA-N phenylmethyl ester of formic acid Natural products O=COCC1=CC=CC=C1 UYWQUFXKFGHYNT-UHFFFAOYSA-N 0.000 description 2
- CWCMIVBLVUHDHK-ZSNHEYEWSA-N phleomycin D1 Chemical compound N([C@H](C(=O)N[C@H](C)[C@@H](O)[C@H](C)C(=O)N[C@@H]([C@H](O)C)C(=O)NCCC=1SC[C@@H](N=1)C=1SC=C(N=1)C(=O)NCCCCNC(N)=N)[C@@H](O[C@H]1[C@H]([C@@H](O)[C@H](O)[C@H](CO)O1)O[C@@H]1[C@H]([C@@H](OC(N)=O)[C@H](O)[C@@H](CO)O1)O)C=1N=CNC=1)C(=O)C1=NC([C@H](CC(N)=O)NC[C@H](N)C(N)=O)=NC(N)=C1C CWCMIVBLVUHDHK-ZSNHEYEWSA-N 0.000 description 2
- HYAFETHFCAUJAY-UHFFFAOYSA-N pioglitazone Chemical compound N1=CC(CC)=CC=C1CCOC(C=C1)=CC=C1CC1C(=O)NC(=O)S1 HYAFETHFCAUJAY-UHFFFAOYSA-N 0.000 description 2
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 2
- VVWRJUBEIPHGQF-UHFFFAOYSA-N propan-2-yl n-propan-2-yloxycarbonyliminocarbamate Chemical compound CC(C)OC(=O)N=NC(=O)OC(C)C VVWRJUBEIPHGQF-UHFFFAOYSA-N 0.000 description 2
- 230000009467 reduction Effects 0.000 description 2
- 238000000926 separation method Methods 0.000 description 2
- 125000003808 silyl group Chemical group [H][Si]([H])([H])[*] 0.000 description 2
- 229910052708 sodium Inorganic materials 0.000 description 2
- 239000012312 sodium hydride Substances 0.000 description 2
- 229910000104 sodium hydride Inorganic materials 0.000 description 2
- 239000007858 starting material Substances 0.000 description 2
- 238000003756 stirring Methods 0.000 description 2
- 239000000725 suspension Substances 0.000 description 2
- 239000011975 tartaric acid Substances 0.000 description 2
- 235000002906 tartaric acid Nutrition 0.000 description 2
- RMMXLENWKUUMAY-UHFFFAOYSA-N telmisartan Chemical compound CCCC1=NC2=C(C)C=C(C=3N(C4=CC=CC=C4N=3)C)C=C2N1CC(C=C1)=CC=C1C1=CC=CC=C1C(O)=O RMMXLENWKUUMAY-UHFFFAOYSA-N 0.000 description 2
- 125000005931 tert-butyloxycarbonyl group Chemical group [H]C([H])([H])C(OC(*)=O)(C([H])([H])[H])C([H])([H])[H] 0.000 description 2
- 125000002873 tetrahydrofuranonyl group Chemical group 0.000 description 2
- 125000003718 tetrahydrofuranyl group Chemical group 0.000 description 2
- 125000002673 tetrahydropyranonyl group Chemical group O1C(C(CCC1)*)=O 0.000 description 2
- 125000005958 tetrahydrothienyl group Chemical group 0.000 description 2
- 229930192474 thiophene Natural products 0.000 description 2
- 230000009466 transformation Effects 0.000 description 2
- UAYWVJHJZHQCIE-UHFFFAOYSA-L zinc iodide Chemical compound I[Zn]I UAYWVJHJZHQCIE-UHFFFAOYSA-L 0.000 description 2
- 229940075966 (+)- menthol Drugs 0.000 description 1
- DBGIVFWFUFKIQN-VIFPVBQESA-N (+)-Fenfluramine Chemical compound CCN[C@@H](C)CC1=CC=CC(C(F)(F)F)=C1 DBGIVFWFUFKIQN-VIFPVBQESA-N 0.000 description 1
- NOOLISFMXDJSKH-AEJSXWLSSA-N (+)-menthol Chemical compound CC(C)[C@H]1CC[C@H](C)C[C@@H]1O NOOLISFMXDJSKH-AEJSXWLSSA-N 0.000 description 1
- XUFXOAAUWZOOIT-SXARVLRPSA-N (2R,3R,4R,5S,6R)-5-[[(2R,3R,4R,5S,6R)-5-[[(2R,3R,4S,5S,6R)-3,4-dihydroxy-6-methyl-5-[[(1S,4R,5S,6S)-4,5,6-trihydroxy-3-(hydroxymethyl)-1-cyclohex-2-enyl]amino]-2-oxanyl]oxy]-3,4-dihydroxy-6-(hydroxymethyl)-2-oxanyl]oxy]-6-(hydroxymethyl)oxane-2,3,4-triol Chemical compound O([C@H]1O[C@H](CO)[C@H]([C@@H]([C@H]1O)O)O[C@H]1O[C@@H]([C@H]([C@H](O)[C@H]1O)N[C@@H]1[C@@H]([C@@H](O)[C@H](O)C(CO)=C1)O)C)[C@@H]1[C@@H](CO)O[C@@H](O)[C@H](O)[C@H]1O XUFXOAAUWZOOIT-SXARVLRPSA-N 0.000 description 1
- IFDLIPHHFXSDRC-UHFFFAOYSA-M (3-bromophenyl)methyl-triphenylphosphanium;bromide Chemical compound [Br-].BrC1=CC=CC(C[P+](C=2C=CC=CC=2)(C=2C=CC=CC=2)C=2C=CC=CC=2)=C1 IFDLIPHHFXSDRC-UHFFFAOYSA-M 0.000 description 1
- SCHBQPIVMBDOQF-UHFFFAOYSA-N (5-bromo-2-chlorophenyl)methanol Chemical compound OCC1=CC(Br)=CC=C1Cl SCHBQPIVMBDOQF-UHFFFAOYSA-N 0.000 description 1
- 125000006273 (C1-C3) alkyl group Chemical group 0.000 description 1
- 125000006717 (C3-C10) cycloalkenyl group Chemical group 0.000 description 1
- NENLYAQPNATJSU-UHFFFAOYSA-N 1,2,3,4,4a,5,6,7,8,8a-decahydroisoquinoline Chemical compound C1NCCC2CCCCC21 NENLYAQPNATJSU-UHFFFAOYSA-N 0.000 description 1
- POTIYWUALSJREP-UHFFFAOYSA-N 1,2,3,4,4a,5,6,7,8,8a-decahydroquinoline Chemical compound N1CCCC2CCCCC21 POTIYWUALSJREP-UHFFFAOYSA-N 0.000 description 1
- CXWGKAYMVASWDQ-UHFFFAOYSA-N 1,2-dithiane Chemical compound C1CCSSC1 CXWGKAYMVASWDQ-UHFFFAOYSA-N 0.000 description 1
- ZPCJPJQUVRIILS-UHFFFAOYSA-N 1-bromo-3-(bromomethyl)benzene Chemical compound BrCC1=CC=CC(Br)=C1 ZPCJPJQUVRIILS-UHFFFAOYSA-N 0.000 description 1
- 125000004972 1-butynyl group Chemical group [H]C([H])([H])C([H])([H])C#C* 0.000 description 1
- 125000000530 1-propynyl group Chemical group [H]C([H])([H])C#C* 0.000 description 1
- WSNDAYQNZRJGMJ-UHFFFAOYSA-N 2,2,2-trifluoroethanone Chemical compound FC(F)(F)[C]=O WSNDAYQNZRJGMJ-UHFFFAOYSA-N 0.000 description 1
- YQTCQNIPQMJNTI-UHFFFAOYSA-N 2,2-dimethylpropan-1-one Chemical group CC(C)(C)[C]=O YQTCQNIPQMJNTI-UHFFFAOYSA-N 0.000 description 1
- LBLYYCQCTBFVLH-UHFFFAOYSA-N 2-Methylbenzenesulfonic acid Chemical compound CC1=CC=CC=C1S(O)(=O)=O LBLYYCQCTBFVLH-UHFFFAOYSA-N 0.000 description 1
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 1
- FHEYFIGWYQJVDR-ACJLOTCBSA-N 2-[[3-[(2r)-2-[[(2r)-2-(3-chlorophenyl)-2-hydroxyethyl]amino]propyl]-1h-indol-7-yl]oxy]acetic acid Chemical compound C1([C@@H](O)CN[C@@H](CC=2C3=CC=CC(OCC(O)=O)=C3NC=2)C)=CC=CC(Cl)=C1 FHEYFIGWYQJVDR-ACJLOTCBSA-N 0.000 description 1
- 125000000069 2-butynyl group Chemical group [H]C([H])([H])C#CC([H])([H])* 0.000 description 1
- 125000001494 2-propynyl group Chemical group [H]C#CC([H])([H])* 0.000 description 1
- TZOYXRMEFDYWDQ-UHFFFAOYSA-N 3,4-dihydro-1h-quinolin-2-one Chemical compound C1=CC=C2NC(=O)CCC2=C1 TZOYXRMEFDYWDQ-UHFFFAOYSA-N 0.000 description 1
- BMYNFMYTOJXKLE-UHFFFAOYSA-N 3-azaniumyl-2-hydroxypropanoate Chemical compound NCC(O)C(O)=O BMYNFMYTOJXKLE-UHFFFAOYSA-N 0.000 description 1
- 125000000474 3-butynyl group Chemical group [H]C#CC([H])([H])C([H])([H])* 0.000 description 1
- 239000003148 4 aminobutyric acid receptor blocking agent Substances 0.000 description 1
- DIUNXCAPYBCIBO-UHFFFAOYSA-N 4-bromo-1-chloro-2-(4-methoxycyclohexyl)oxybenzene Chemical compound C1CC(OC)CCC1OC1=CC(Br)=CC=C1Cl DIUNXCAPYBCIBO-UHFFFAOYSA-N 0.000 description 1
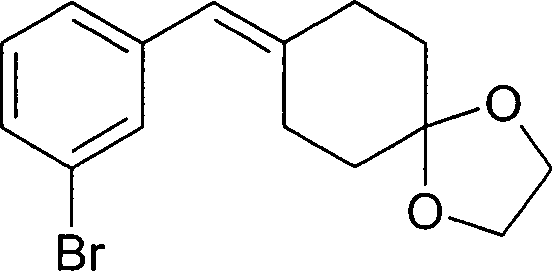
- RZEFZXHBYRCTNV-UHFFFAOYSA-N 4-bromo-1-chloro-2-(cyclohexylidenemethyl)benzene Chemical compound ClC1=CC=C(Br)C=C1C=C1CCCCC1 RZEFZXHBYRCTNV-UHFFFAOYSA-N 0.000 description 1
- UAMVKOTWSHJOSY-UHFFFAOYSA-N 4-bromo-1-chloro-2-methoxybenzene Chemical compound COC1=CC(Br)=CC=C1Cl UAMVKOTWSHJOSY-UHFFFAOYSA-N 0.000 description 1
- KEWSCDNULKOKTG-UHFFFAOYSA-N 4-cyano-4-ethylsulfanylcarbothioylsulfanylpentanoic acid Chemical compound CCSC(=S)SC(C)(C#N)CCC(O)=O KEWSCDNULKOKTG-UHFFFAOYSA-N 0.000 description 1
- PFTGXSGDFZZZFY-UHFFFAOYSA-N 4-methoxycyclohexan-1-ol Chemical compound COC1CCC(O)CC1 PFTGXSGDFZZZFY-UHFFFAOYSA-N 0.000 description 1
- 102000006902 5-HT2C Serotonin Receptor Human genes 0.000 description 1
- 108010072553 5-HT2C Serotonin Receptor Proteins 0.000 description 1
- NFFXEUUOMTXWCX-UHFFFAOYSA-N 5-[(2,4-dioxo-1,3-thiazolidin-5-yl)methyl]-2-methoxy-n-[[4-(trifluoromethyl)phenyl]methyl]benzamide Chemical compound C1=C(C(=O)NCC=2C=CC(=CC=2)C(F)(F)F)C(OC)=CC=C1CC1SC(=O)NC1=O NFFXEUUOMTXWCX-UHFFFAOYSA-N 0.000 description 1
- IMVDZFOSXJSXFP-UHFFFAOYSA-N 5-chloro-2-propyl-3-[[4-[2-(2h-tetrazol-5-yl)phenyl]phenyl]methyl]imidazole-4-carbaldehyde Chemical compound CCCC1=NC(Cl)=C(C=O)N1CC1=CC=C(C=2C(=CC=CC=2)C2=NNN=N2)C=C1 IMVDZFOSXJSXFP-UHFFFAOYSA-N 0.000 description 1
- 239000005541 ACE inhibitor Substances 0.000 description 1
- 208000009304 Acute Kidney Injury Diseases 0.000 description 1
- 229940077274 Alpha glucosidase inhibitor Drugs 0.000 description 1
- 101100460776 Arabidopsis thaliana NPY2 gene Proteins 0.000 description 1
- 101100460788 Arabidopsis thaliana NPY5 gene Proteins 0.000 description 1
- XUKUURHRXDUEBC-KAYWLYCHSA-N Atorvastatin Chemical compound C=1C=CC=CC=1C1=C(C=2C=CC(F)=CC=2)N(CC[C@@H](O)C[C@@H](O)CC(O)=O)C(C(C)C)=C1C(=O)NC1=CC=CC=C1 XUKUURHRXDUEBC-KAYWLYCHSA-N 0.000 description 1
- XUKUURHRXDUEBC-UHFFFAOYSA-N Atorvastatin Natural products C=1C=CC=CC=1C1=C(C=2C=CC(F)=CC=2)N(CCC(O)CC(O)CC(O)=O)C(C(C)C)=C1C(=O)NC1=CC=CC=C1 XUKUURHRXDUEBC-UHFFFAOYSA-N 0.000 description 1
- PTQXTEKSNBVPQJ-UHFFFAOYSA-N Avasimibe Chemical compound CC(C)C1=CC(C(C)C)=CC(C(C)C)=C1CC(=O)NS(=O)(=O)OC1=C(C(C)C)C=CC=C1C(C)C PTQXTEKSNBVPQJ-UHFFFAOYSA-N 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-M Bromide Chemical compound [Br-] CPELXLSAUQHCOX-UHFFFAOYSA-M 0.000 description 1
- 0 C*(C)C1=CC([C@@]([C@@]2O*)O[C@@](C*)[C@](*)[C@@]2O*)=CCC1 Chemical compound C*(C)C1=CC([C@@]([C@@]2O*)O[C@@](C*)[C@](*)[C@@]2O*)=CCC1 0.000 description 1
- 239000004072 C09CA03 - Valsartan Substances 0.000 description 1
- 239000002947 C09CA04 - Irbesartan Substances 0.000 description 1
- 239000002081 C09CA05 - Tasosartan Substances 0.000 description 1
- 239000005537 C09CA07 - Telmisartan Substances 0.000 description 1
- VHCOUPJDHUIDPY-MGCOHNPYSA-N C1C[C@@H](O)CC[C@@H]1OC1=CC(Br)=CC=C1Cl Chemical compound C1C[C@@H](O)CC[C@@H]1OC1=CC(Br)=CC=C1Cl VHCOUPJDHUIDPY-MGCOHNPYSA-N 0.000 description 1
- DIUNXCAPYBCIBO-XYPYZODXSA-N C1C[C@@H](OC)CC[C@@H]1OC1=CC(Br)=CC=C1Cl Chemical compound C1C[C@@H](OC)CC[C@@H]1OC1=CC(Br)=CC=C1Cl DIUNXCAPYBCIBO-XYPYZODXSA-N 0.000 description 1
- GHIQLFVRONNVQM-RQLQUUKGSA-N C1C[C@@H](OC)CC[C@@H]1OC1=CC([C@]2(O)[C@@H]([C@@H](OC(C)=O)[C@H](OC(C)=O)[C@@H](COC(C)=O)O2)OC(C)=O)=CC=C1Cl Chemical compound C1C[C@@H](OC)CC[C@@H]1OC1=CC([C@]2(O)[C@@H]([C@@H](OC(C)=O)[C@H](OC(C)=O)[C@@H](COC(C)=O)O2)OC(C)=O)=CC=C1Cl GHIQLFVRONNVQM-RQLQUUKGSA-N 0.000 description 1
- GHIQLFVRONNVQM-GBQVRQMJSA-N C1C[C@@H](OC)CC[C@H]1OC1=CC([C@]2(O)[C@@H]([C@@H](OC(C)=O)[C@H](OC(C)=O)[C@@H](COC(C)=O)O2)OC(C)=O)=CC=C1Cl Chemical compound C1C[C@@H](OC)CC[C@H]1OC1=CC([C@]2(O)[C@@H]([C@@H](OC(C)=O)[C@H](OC(C)=O)[C@@H](COC(C)=O)O2)OC(C)=O)=CC=C1Cl GHIQLFVRONNVQM-GBQVRQMJSA-N 0.000 description 1
- PINLEUAXLIRXEY-NCNPMDCVSA-N CC(=O)OC[C@H]1O[C@@](O)([C@H](OC(C)=O)[C@@H](OC(C)=O)[C@@H]1OC(C)=O)c1ccccc1C=C1CCC(O)CC1 Chemical compound CC(=O)OC[C@H]1O[C@@](O)([C@H](OC(C)=O)[C@@H](OC(C)=O)[C@@H]1OC(C)=O)c1ccccc1C=C1CCC(O)CC1 PINLEUAXLIRXEY-NCNPMDCVSA-N 0.000 description 1
- KZILDZRVQBBKPO-BHGSEUJGSA-N CC(O[C@H]([C@H]([C@H](c1cccc(C=C(CC2)CCC2O)c1)O/C1=C\OC(C)=O)OC(C)=O)[C@@H]1OC(C)=O)=O Chemical compound CC(O[C@H]([C@H]([C@H](c1cccc(C=C(CC2)CCC2O)c1)O/C1=C\OC(C)=O)OC(C)=O)[C@@H]1OC(C)=O)=O KZILDZRVQBBKPO-BHGSEUJGSA-N 0.000 description 1
- SUAAUFJDCMYHIO-HQKAVCLOSA-N COC1CCC(CC1)=Cc1ccccc1[C@@]1(O)O[C@H](COC(C)=O)[C@@H](OC(C)=O)[C@H](OC(C)=O)[C@H]1OC(C)=O Chemical compound COC1CCC(CC1)=Cc1ccccc1[C@@]1(O)O[C@H](COC(C)=O)[C@@H](OC(C)=O)[C@H](OC(C)=O)[C@H]1OC(C)=O SUAAUFJDCMYHIO-HQKAVCLOSA-N 0.000 description 1
- MQKXDRDAVXLGSH-RKFAPSRVSA-N COc1ccc(Cc2cc(ccc2Cl)[C@@]2(O)O[C@H](COC(C)=O)[C@@H](OC(C)=O)[C@H](OC(C)=O)[C@H]2OC(C)=O)cc1 Chemical compound COc1ccc(Cc2cc(ccc2Cl)[C@@]2(O)O[C@H](COC(C)=O)[C@@H](OC(C)=O)[C@H](OC(C)=O)[C@H]2OC(C)=O)cc1 MQKXDRDAVXLGSH-RKFAPSRVSA-N 0.000 description 1
- GHOSNRCGJFBJIB-UHFFFAOYSA-N Candesartan cilexetil Chemical compound C=12N(CC=3C=CC(=CC=3)C=3C(=CC=CC=3)C3=NNN=N3)C(OCC)=NC2=CC=CC=1C(=O)OC(C)OC(=O)OC1CCCCC1 GHOSNRCGJFBJIB-UHFFFAOYSA-N 0.000 description 1
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 1
- 229910004664 Cerium(III) chloride Inorganic materials 0.000 description 1
- JZUFKLXOESDKRF-UHFFFAOYSA-N Chlorothiazide Chemical compound C1=C(Cl)C(S(=O)(=O)N)=CC2=C1NCNS2(=O)=O JZUFKLXOESDKRF-UHFFFAOYSA-N 0.000 description 1
- 102100037637 Cholesteryl ester transfer protein Human genes 0.000 description 1
- 229920001268 Cholestyramine Polymers 0.000 description 1
- ZDRKOHALCBUAHG-IURCNINISA-N ClC1=C(C=C(C=C1)[C@]1(O)[C@H](OC(C)=O)[C@@H](OC(C)=O)[C@H](OC(C)=O)[C@H](O1)COC(C)=O)C=C1CCCCC1 Chemical compound ClC1=C(C=C(C=C1)[C@]1(O)[C@H](OC(C)=O)[C@@H](OC(C)=O)[C@H](OC(C)=O)[C@H](O1)COC(C)=O)C=C1CCCCC1 ZDRKOHALCBUAHG-IURCNINISA-N 0.000 description 1
- 108091026890 Coding region Proteins 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- 208000008960 Diabetic foot Diseases 0.000 description 1
- 102100025012 Dipeptidyl peptidase 4 Human genes 0.000 description 1
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 1
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 1
- 108010011459 Exenatide Proteins 0.000 description 1
- KRHYYFGTRYWZRS-UHFFFAOYSA-M Fluoride anion Chemical compound [F-] KRHYYFGTRYWZRS-UHFFFAOYSA-M 0.000 description 1
- 102000027487 Fructose-Bisphosphatase Human genes 0.000 description 1
- 108010017464 Fructose-Bisphosphatase Proteins 0.000 description 1
- 229940098788 GABA receptor antagonist Drugs 0.000 description 1
- 101710198884 GATA-type zinc finger protein 1 Proteins 0.000 description 1
- 108091007911 GSKs Proteins 0.000 description 1
- CEAZRRDELHUEMR-URQXQFDESA-N Gentamicin Chemical compound O1[C@H](C(C)NC)CC[C@@H](N)[C@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](NC)[C@@](C)(O)CO2)O)[C@H](N)C[C@@H]1N CEAZRRDELHUEMR-URQXQFDESA-N 0.000 description 1
- 229930182566 Gentamicin Natural products 0.000 description 1
- 229940122904 Glucagon receptor antagonist Drugs 0.000 description 1
- FAEKWTJYAYMJKF-QHCPKHFHSA-N GlucoNorm Chemical compound C1=C(C(O)=O)C(OCC)=CC(CC(=O)N[C@@H](CC(C)C)C=2C(=CC=CC=2)N2CCCCC2)=C1 FAEKWTJYAYMJKF-QHCPKHFHSA-N 0.000 description 1
- 102000003638 Glucose-6-Phosphatase Human genes 0.000 description 1
- 108010086800 Glucose-6-Phosphatase Proteins 0.000 description 1
- 102000007390 Glycogen Phosphorylase Human genes 0.000 description 1
- 108010046163 Glycogen Phosphorylase Proteins 0.000 description 1
- 102000004103 Glycogen Synthase Kinases Human genes 0.000 description 1
- 201000005569 Gout Diseases 0.000 description 1
- 102100030488 HEAT repeat-containing protein 6 Human genes 0.000 description 1
- 239000007995 HEPES buffer Substances 0.000 description 1
- 229940121710 HMGCoA reductase inhibitor Drugs 0.000 description 1
- 101000880514 Homo sapiens Cholesteryl ester transfer protein Proteins 0.000 description 1
- 101000990566 Homo sapiens HEAT repeat-containing protein 6 Proteins 0.000 description 1
- 101000801684 Homo sapiens Phospholipid-transporting ATPase ABCA1 Proteins 0.000 description 1
- 101000684208 Homo sapiens Prolyl endopeptidase FAP Proteins 0.000 description 1
- 101000716688 Homo sapiens Sodium/glucose cotransporter 1 Proteins 0.000 description 1
- 101000716682 Homo sapiens Sodium/glucose cotransporter 2 Proteins 0.000 description 1
- 206010010164 Hypertension complications Diseases 0.000 description 1
- 102000004877 Insulin Human genes 0.000 description 1
- 108090001061 Insulin Proteins 0.000 description 1
- 102000036770 Islet Amyloid Polypeptide Human genes 0.000 description 1
- 108010041872 Islet Amyloid Polypeptide Proteins 0.000 description 1
- ONIBWKKTOPOVIA-BYPYZUCNSA-N L-Proline Chemical compound OC(=O)[C@@H]1CCCN1 ONIBWKKTOPOVIA-BYPYZUCNSA-N 0.000 description 1
- COLNVLDHVKWLRT-QMMMGPOBSA-N L-phenylalanine Chemical compound OC(=O)[C@@H](N)CC1=CC=CC=C1 COLNVLDHVKWLRT-QMMMGPOBSA-N 0.000 description 1
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 1
- 206010054805 Macroangiopathy Diseases 0.000 description 1
- 229920000168 Microcrystalline cellulose Polymers 0.000 description 1
- MZRVEZGGRBJDDB-UHFFFAOYSA-N N-Butyllithium Chemical compound [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 description 1
- AHLBNYSZXLDEJQ-UHFFFAOYSA-N N-formyl-L-leucylester Natural products CCCCCCCCCCCC(OC(=O)C(CC(C)C)NC=O)CC1OC(=O)C1CCCCCC AHLBNYSZXLDEJQ-UHFFFAOYSA-N 0.000 description 1
- 101150111774 NPY5R gene Proteins 0.000 description 1
- 102000003729 Neprilysin Human genes 0.000 description 1
- 108090000028 Neprilysin Proteins 0.000 description 1
- PVNIIMVLHYAWGP-UHFFFAOYSA-N Niacin Chemical compound OC(=O)C1=CC=CN=C1 PVNIIMVLHYAWGP-UHFFFAOYSA-N 0.000 description 1
- PXHVJJICTQNCMI-UHFFFAOYSA-N Nickel Chemical compound [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 1
- OXHJVOWIWQDJCK-YHBQERECSA-N O([C@H]1CC[C@@H](CC1)O[Si](C(C)(C)C)(C=1C=CC=CC=1)C=1C=CC=CC=1)C1=CC(Br)=CC=C1Cl Chemical compound O([C@H]1CC[C@@H](CC1)O[Si](C(C)(C)C)(C=1C=CC=CC=1)C=1C=CC=CC=1)C1=CC(Br)=CC=C1Cl OXHJVOWIWQDJCK-YHBQERECSA-N 0.000 description 1
- OXHJVOWIWQDJCK-ZRZAMGCNSA-N O([C@H]1CC[C@H](CC1)O[Si](C(C)(C)C)(C=1C=CC=CC=1)C=1C=CC=CC=1)C1=CC(Br)=CC=C1Cl Chemical compound O([C@H]1CC[C@H](CC1)O[Si](C(C)(C)C)(C=1C=CC=CC=1)C=1C=CC=CC=1)C1=CC(Br)=CC=C1Cl OXHJVOWIWQDJCK-ZRZAMGCNSA-N 0.000 description 1
- AXDXBNWVMRCRDT-BLUBZBIGSA-N OCC([C@H]([C@@H]([C@H]1O)O)O)O[C@H]1c1cccc(C=C(CC2)CCC2O)c1 Chemical compound OCC([C@H]([C@@H]([C@H]1O)O)O)O[C@H]1c1cccc(C=C(CC2)CCC2O)c1 AXDXBNWVMRCRDT-BLUBZBIGSA-N 0.000 description 1
- 239000005480 Olmesartan Substances 0.000 description 1
- 102000000536 PPAR gamma Human genes 0.000 description 1
- 102100038824 Peroxisome proliferator-activated receptor delta Human genes 0.000 description 1
- 102100038825 Peroxisome proliferator-activated receptor gamma Human genes 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 102100040918 Pro-glucagon Human genes 0.000 description 1
- ONIBWKKTOPOVIA-UHFFFAOYSA-N Proline Natural products OC(=O)C1CCCN1 ONIBWKKTOPOVIA-UHFFFAOYSA-N 0.000 description 1
- 229940123924 Protein kinase C inhibitor Drugs 0.000 description 1
- LCTONWCANYUPML-UHFFFAOYSA-M Pyruvate Chemical compound CC(=O)C([O-])=O LCTONWCANYUPML-UHFFFAOYSA-M 0.000 description 1
- 239000007868 Raney catalyst Substances 0.000 description 1
- 229910000564 Raney nickel Inorganic materials 0.000 description 1
- 208000033626 Renal failure acute Diseases 0.000 description 1
- 208000017442 Retinal disease Diseases 0.000 description 1
- 206010038923 Retinopathy Diseases 0.000 description 1
- RYMZZMVNJRMUDD-UHFFFAOYSA-N SJ000286063 Natural products C12C(OC(=O)C(C)(C)CC)CC(C)C=C2C=CC(C)C1CCC1CC(O)CC(=O)O1 RYMZZMVNJRMUDD-UHFFFAOYSA-N 0.000 description 1
- 229940123518 Sodium/glucose cotransporter 2 inhibitor Drugs 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- 229940100389 Sulfonylurea Drugs 0.000 description 1
- 229940123464 Thiazolidinedione Drugs 0.000 description 1
- 229910021627 Tin(IV) chloride Inorganic materials 0.000 description 1
- JLRGJRBPOGGCBT-UHFFFAOYSA-N Tolbutamide Chemical compound CCCCNC(=O)NS(=O)(=O)C1=CC=C(C)C=C1 JLRGJRBPOGGCBT-UHFFFAOYSA-N 0.000 description 1
- KJADKKWYZYXHBB-XBWDGYHZSA-N Topiramic acid Chemical compound C1O[C@@]2(COS(N)(=O)=O)OC(C)(C)O[C@H]2[C@@H]2OC(C)(C)O[C@@H]21 KJADKKWYZYXHBB-XBWDGYHZSA-N 0.000 description 1
- 241000471214 Trachelospermum asiaticum Species 0.000 description 1
- 108090000631 Trypsin Proteins 0.000 description 1
- 102000004142 Trypsin Human genes 0.000 description 1
- 102000008316 Type 4 Melanocortin Receptor Human genes 0.000 description 1
- 108010021436 Type 4 Melanocortin Receptor Proteins 0.000 description 1
- 101710204865 Tyrosine-protein phosphatase 1 Proteins 0.000 description 1
- 208000025865 Ulcer Diseases 0.000 description 1
- LEHOTFFKMJEONL-UHFFFAOYSA-N Uric Acid Chemical compound N1C(=O)NC(=O)C2=C1NC(=O)N2 LEHOTFFKMJEONL-UHFFFAOYSA-N 0.000 description 1
- TVWHNULVHGKJHS-UHFFFAOYSA-N Uric acid Natural products N1C(=O)NC(=O)C2NC(=O)NC21 TVWHNULVHGKJHS-UHFFFAOYSA-N 0.000 description 1
- 229940116731 Uricosuric agent Drugs 0.000 description 1
- FZNCGRZWXLXZSZ-CIQUZCHMSA-N Voglibose Chemical compound OCC(CO)N[C@H]1C[C@](O)(CO)[C@@H](O)[C@H](O)[C@H]1O FZNCGRZWXLXZSZ-CIQUZCHMSA-N 0.000 description 1
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 1
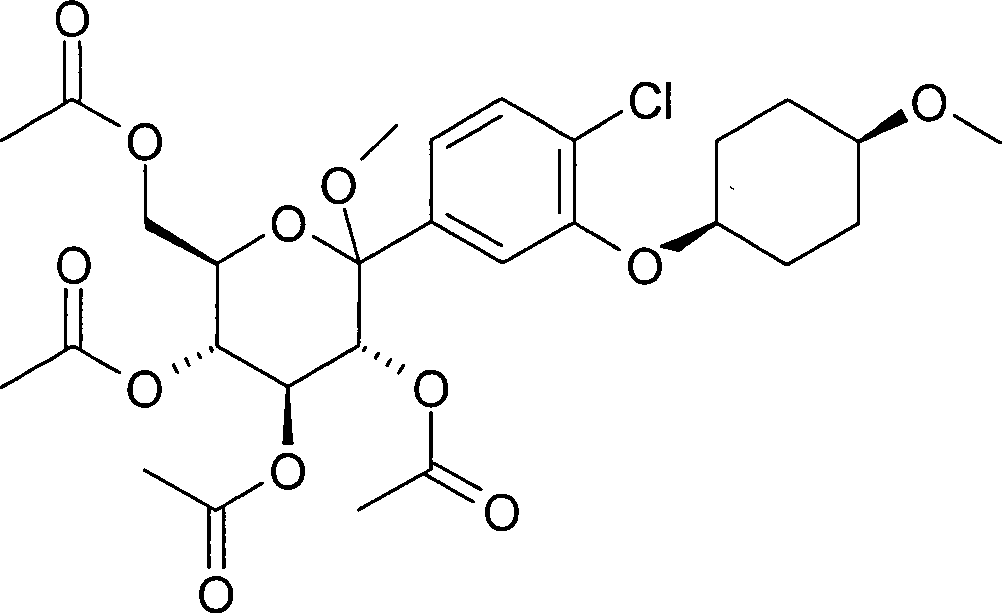
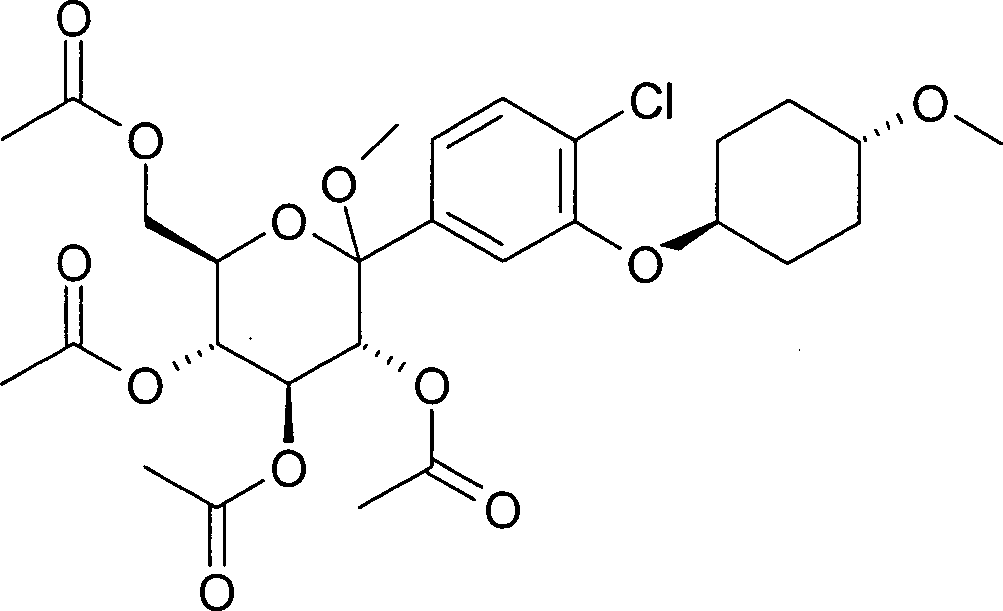
- GHIQLFVRONNVQM-UAKLGFHKSA-N [(2r,3r,4s,5r,6r)-3,4,5-triacetyloxy-6-[4-chloro-3-(4-methoxycyclohexyl)oxyphenyl]-6-hydroxyoxan-2-yl]methyl acetate Chemical compound C1CC(OC)CCC1OC1=CC([C@]2(O)[C@@H]([C@@H](OC(C)=O)[C@H](OC(C)=O)[C@@H](COC(C)=O)O2)OC(C)=O)=CC=C1Cl GHIQLFVRONNVQM-UAKLGFHKSA-N 0.000 description 1
- FDKIDFYIEWFERB-UHFFFAOYSA-N [2-butyl-5-chloro-3-[[4-[2-(2h-tetrazol-5-yl)phenyl]phenyl]methyl]imidazol-4-yl]methanol;potassium Chemical compound [K].CCCCC1=NC(Cl)=C(CO)N1CC1=CC=C(C=2C(=CC=CC=2)C=2NN=NN=2)C=C1 FDKIDFYIEWFERB-UHFFFAOYSA-N 0.000 description 1
- KNDHRUPPBXRELB-UHFFFAOYSA-M [4-[3-(4-ethylphenyl)butyl]phenyl]-trimethylazanium;chloride Chemical compound [Cl-].C1=CC(CC)=CC=C1C(C)CCC1=CC=C([N+](C)(C)C)C=C1 KNDHRUPPBXRELB-UHFFFAOYSA-M 0.000 description 1
- CIUQDSCDWFSTQR-UHFFFAOYSA-N [C]1=CC=CC=C1 Chemical compound [C]1=CC=CC=C1 CIUQDSCDWFSTQR-UHFFFAOYSA-N 0.000 description 1
- 229960002632 acarbose Drugs 0.000 description 1
- XUFXOAAUWZOOIT-UHFFFAOYSA-N acarviostatin I01 Natural products OC1C(O)C(NC2C(C(O)C(O)C(CO)=C2)O)C(C)OC1OC(C(C1O)O)C(CO)OC1OC1C(CO)OC(O)C(O)C1O XUFXOAAUWZOOIT-UHFFFAOYSA-N 0.000 description 1
- 125000004036 acetal group Chemical group 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 201000011040 acute kidney failure Diseases 0.000 description 1
- 208000012998 acute renal failure Diseases 0.000 description 1
- 125000005073 adamantyl group Chemical group C12(CC3CC(CC(C1)C3)C2)* 0.000 description 1
- 239000000670 adrenergic alpha-2 receptor antagonist Substances 0.000 description 1
- 229940127252 advanced glycation end product inhibitor Drugs 0.000 description 1
- 230000001476 alcoholic effect Effects 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 239000003288 aldose reductase inhibitor Substances 0.000 description 1
- 229940090865 aldose reductase inhibitors used in diabetes Drugs 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 150000001340 alkali metals Chemical class 0.000 description 1
- 239000003888 alpha glucosidase inhibitor Substances 0.000 description 1
- 102000030484 alpha-2 Adrenergic Receptor Human genes 0.000 description 1
- 108020004101 alpha-2 Adrenergic Receptor Proteins 0.000 description 1
- 150000001371 alpha-amino acids Chemical class 0.000 description 1
- 235000008206 alpha-amino acids Nutrition 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 150000001408 amides Chemical class 0.000 description 1
- 235000001014 amino acid Nutrition 0.000 description 1
- 150000001413 amino acids Chemical class 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 229940126317 angiotensin II receptor antagonist Drugs 0.000 description 1
- 229940044094 angiotensin-converting-enzyme inhibitor Drugs 0.000 description 1
- 239000003524 antilipemic agent Substances 0.000 description 1
- 229940127218 antiplatelet drug Drugs 0.000 description 1
- 230000006907 apoptotic process Effects 0.000 description 1
- 239000008346 aqueous phase Substances 0.000 description 1
- 229910052786 argon Inorganic materials 0.000 description 1
- 239000012300 argon atmosphere Substances 0.000 description 1
- 150000001500 aryl chlorides Chemical class 0.000 description 1
- 125000005002 aryl methyl group Chemical group 0.000 description 1
- 239000012298 atmosphere Substances 0.000 description 1
- 229960005370 atorvastatin Drugs 0.000 description 1
- 229950010046 avasimibe Drugs 0.000 description 1
- 239000002876 beta blocker Substances 0.000 description 1
- 229940097320 beta blocking agent Drugs 0.000 description 1
- IIBYAHWJQTYFKB-UHFFFAOYSA-N bezafibrate Chemical compound C1=CC(OC(C)(C)C(O)=O)=CC=C1CCNC(=O)C1=CC=C(Cl)C=C1 IIBYAHWJQTYFKB-UHFFFAOYSA-N 0.000 description 1
- 229960000516 bezafibrate Drugs 0.000 description 1
- GPRLTFBKWDERLU-UHFFFAOYSA-N bicyclo[2.2.2]octane Chemical compound C1CC2CCC1CC2 GPRLTFBKWDERLU-UHFFFAOYSA-N 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- SIPUZPBQZHNSDW-UHFFFAOYSA-N bis(2-methylpropyl)aluminum Chemical compound CC(C)C[Al]CC(C)C SIPUZPBQZHNSDW-UHFFFAOYSA-N 0.000 description 1
- 229910000085 borane Inorganic materials 0.000 description 1
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 239000006227 byproduct Substances 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 229960004349 candesartan cilexetil Drugs 0.000 description 1
- 229930003827 cannabinoid Natural products 0.000 description 1
- 239000003557 cannabinoid Substances 0.000 description 1
- 239000001768 carboxy methyl cellulose Substances 0.000 description 1
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 1
- 239000008112 carboxymethyl-cellulose Substances 0.000 description 1
- 239000006143 cell culture medium Substances 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- VYLVYHXQOHJDJL-UHFFFAOYSA-K cerium trichloride Chemical compound Cl[Ce](Cl)Cl VYLVYHXQOHJDJL-UHFFFAOYSA-K 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- JUFFVKRROAPVBI-PVOYSMBESA-N chembl1210015 Chemical compound C([C@@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(=O)N[C@H]1[C@@H]([C@@H](O)[C@H](O[C@H]2[C@@H]([C@@H](O)[C@@H](O)[C@@H](CO[C@]3(O[C@@H](C[C@H](O)[C@H](O)CO)[C@H](NC(C)=O)[C@@H](O)C3)C(O)=O)O2)O)[C@@H](CO)O1)NC(C)=O)C(=O)NCC(=O)NCC(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CO)C(=O)N[C@@H](CO)C(=O)NCC(=O)N[C@@H](C)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CO)C(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCSC)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CO)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)CNC(=O)[C@@H](N)CC=1NC=NC=1)[C@@H](C)O)[C@@H](C)O)C(C)C)C1=CC=CC=C1 JUFFVKRROAPVBI-PVOYSMBESA-N 0.000 description 1
- IJOOHPMOJXWVHK-UHFFFAOYSA-N chlorotrimethylsilane Chemical compound C[Si](C)(C)Cl IJOOHPMOJXWVHK-UHFFFAOYSA-N 0.000 description 1
- 235000012000 cholesterol Nutrition 0.000 description 1
- PMMYEEVYMWASQN-IMJSIDKUSA-N cis-4-Hydroxy-L-proline Chemical compound O[C@@H]1CN[C@H](C(O)=O)C1 PMMYEEVYMWASQN-IMJSIDKUSA-N 0.000 description 1
- 229960001678 colestyramine Drugs 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 229940099112 cornstarch Drugs 0.000 description 1
- WZHCOOQXZCIUNC-UHFFFAOYSA-N cyclandelate Chemical compound C1C(C)(C)CC(C)CC1OC(=O)C(O)C1=CC=CC=C1 WZHCOOQXZCIUNC-UHFFFAOYSA-N 0.000 description 1
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- QRAKRDZMIONMRZ-UHFFFAOYSA-M cyclohexyl(triphenyl)phosphanium;bromide Chemical compound [Br-].C1CCCCC1[P+](C=1C=CC=CC=1)(C=1C=CC=CC=1)C1=CC=CC=C1 QRAKRDZMIONMRZ-UHFFFAOYSA-M 0.000 description 1
- 125000006547 cyclononyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 125000000640 cyclooctyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- ZSWFCLXCOIISFI-UHFFFAOYSA-N cyclopentadiene Chemical group C1C=CC=C1 ZSWFCLXCOIISFI-UHFFFAOYSA-N 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- PWAPCRSSMCLZHG-UHFFFAOYSA-N cyclopentylidene Chemical group [C]1CCCC1 PWAPCRSSMCLZHG-UHFFFAOYSA-N 0.000 description 1
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 1
- 230000002074 deregulated effect Effects 0.000 description 1
- 229960004597 dexfenfluramine Drugs 0.000 description 1
- VDCSGNNYCFPWFK-UHFFFAOYSA-N diphenylsilane Chemical compound C=1C=CC=CC=1[SiH2]C1=CC=CC=C1 VDCSGNNYCFPWFK-UHFFFAOYSA-N 0.000 description 1
- LOZWAPSEEHRYPG-UHFFFAOYSA-N dithiane Natural products C1CSCCS1 LOZWAPSEEHRYPG-UHFFFAOYSA-N 0.000 description 1
- 230000001882 diuretic effect Effects 0.000 description 1
- 239000008298 dragée Substances 0.000 description 1
- 229960000573 eprosartan mesylate Drugs 0.000 description 1
- DJSLTDBPKHORNY-XMMWENQYSA-N eprosartan methanesulfonate Chemical compound CS(O)(=O)=O.C=1C=C(C(O)=O)C=CC=1CN1C(CCCC)=NC=C1\C=C(C(O)=O)/CC1=CC=CS1 DJSLTDBPKHORNY-XMMWENQYSA-N 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- 150000002170 ethers Chemical class 0.000 description 1
- IIEWJVIFRVWJOD-UHFFFAOYSA-N ethyl cyclohexane Natural products CCC1CCCCC1 IIEWJVIFRVWJOD-UHFFFAOYSA-N 0.000 description 1
- 230000005284 excitation Effects 0.000 description 1
- 229960001519 exenatide Drugs 0.000 description 1
- 239000013604 expression vector Substances 0.000 description 1
- 239000000284 extract Substances 0.000 description 1
- OLNTVTPDXPETLC-XPWALMASSA-N ezetimibe Chemical compound N1([C@@H]([C@H](C1=O)CC[C@H](O)C=1C=CC(F)=CC=1)C=1C=CC(O)=CC=1)C1=CC=C(F)C=C1 OLNTVTPDXPETLC-XPWALMASSA-N 0.000 description 1
- 229960000815 ezetimibe Drugs 0.000 description 1
- 230000002349 favourable effect Effects 0.000 description 1
- 229960002297 fenofibrate Drugs 0.000 description 1
- YMTINGFKWWXKFG-UHFFFAOYSA-N fenofibrate Chemical compound C1=CC(OC(C)(C)C(=O)OC(C)C)=CC=C1C(=O)C1=CC=C(Cl)C=C1 YMTINGFKWWXKFG-UHFFFAOYSA-N 0.000 description 1
- 229940125753 fibrate Drugs 0.000 description 1
- 238000011049 filling Methods 0.000 description 1
- 239000000706 filtrate Substances 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 239000000796 flavoring agent Substances 0.000 description 1
- 235000019634 flavors Nutrition 0.000 description 1
- 238000012632 fluorescent imaging Methods 0.000 description 1
- 238000003682 fluorination reaction Methods 0.000 description 1
- 125000002485 formyl group Chemical group [H]C(*)=O 0.000 description 1
- 238000001640 fractional crystallisation Methods 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- 239000012362 glacial acetic acid Substances 0.000 description 1
- 229960004580 glibenclamide Drugs 0.000 description 1
- WIGIZIANZCJQQY-RUCARUNLSA-N glimepiride Chemical compound O=C1C(CC)=C(C)CN1C(=O)NCCC1=CC=C(S(=O)(=O)NC(=O)N[C@@H]2CC[C@@H](C)CC2)C=C1 WIGIZIANZCJQQY-RUCARUNLSA-N 0.000 description 1
- 229960004346 glimepiride Drugs 0.000 description 1
- 150000002303 glucose derivatives Chemical class 0.000 description 1
- 230000009229 glucose formation Effects 0.000 description 1
- ZNNLBTZKUZBEKO-UHFFFAOYSA-N glyburide Chemical compound COC1=CC=C(Cl)C=C1C(=O)NCCC1=CC=C(S(=O)(=O)NC(=O)NC2CCCCC2)C=C1 ZNNLBTZKUZBEKO-UHFFFAOYSA-N 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 229940116364 hard fat Drugs 0.000 description 1
- 102000052194 human SLC5A1 Human genes 0.000 description 1
- 102000052543 human SLC5A2 Human genes 0.000 description 1
- BNRNAKTVFSZAFA-UHFFFAOYSA-N hydrindane Chemical compound C1CCCC2CCCC21 BNRNAKTVFSZAFA-UHFFFAOYSA-N 0.000 description 1
- 229960002003 hydrochlorothiazide Drugs 0.000 description 1
- XMBWDFGMSWQBCA-UHFFFAOYSA-N hydrogen iodide Chemical compound I XMBWDFGMSWQBCA-UHFFFAOYSA-N 0.000 description 1
- 239000002471 hydroxymethylglutaryl coenzyme A reductase inhibitor Substances 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 238000001727 in vivo Methods 0.000 description 1
- LPAGFVYQRIESJQ-UHFFFAOYSA-N indoline Chemical compound C1=CC=C2NCCC2=C1 LPAGFVYQRIESJQ-UHFFFAOYSA-N 0.000 description 1
- 230000004941 influx Effects 0.000 description 1
- 229940125396 insulin Drugs 0.000 description 1
- 239000000543 intermediate Substances 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- INQOMBQAUSQDDS-UHFFFAOYSA-N iodomethane Chemical compound IC INQOMBQAUSQDDS-UHFFFAOYSA-N 0.000 description 1
- 229960002198 irbesartan Drugs 0.000 description 1
- YCPOHTHPUREGFM-UHFFFAOYSA-N irbesartan Chemical compound O=C1N(CC=2C=CC(=CC=2)C=2C(=CC=CC=2)C=2[N]N=NN=2)C(CCCC)=NC21CCCC2 YCPOHTHPUREGFM-UHFFFAOYSA-N 0.000 description 1
- 125000006328 iso-butylcarbonyl group Chemical group [H]C([H])([H])C([H])(C(*)=O)C([H])([H])[H] 0.000 description 1
- 125000004491 isohexyl group Chemical group C(CCC(C)C)* 0.000 description 1
- 125000001972 isopentyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])C([H])([H])* 0.000 description 1
- 208000017169 kidney disease Diseases 0.000 description 1
- 239000004310 lactic acid Substances 0.000 description 1
- 235000014655 lactic acid Nutrition 0.000 description 1
- 229960001375 lactose Drugs 0.000 description 1
- 229960004873 levomenthol Drugs 0.000 description 1
- 229930013686 lignan Natural products 0.000 description 1
- 235000009408 lignans Nutrition 0.000 description 1
- 150000005692 lignans Chemical class 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 229910052744 lithium Inorganic materials 0.000 description 1
- 239000012280 lithium aluminium hydride Substances 0.000 description 1
- 150000002642 lithium compounds Chemical class 0.000 description 1
- WGOPGODQLGJZGL-UHFFFAOYSA-N lithium;butane Chemical compound [Li+].CC[CH-]C WGOPGODQLGJZGL-UHFFFAOYSA-N 0.000 description 1
- 210000004185 liver Anatomy 0.000 description 1
- 239000012160 loading buffer Substances 0.000 description 1
- ZEUXAIYYDDCIRX-UHFFFAOYSA-N losartan carboxylic acid Chemical compound CCCCC1=NC(Cl)=C(C(O)=O)N1CC1=CC=C(C=2C(=CC=CC=2)C2=NNN=N2)C=C1 ZEUXAIYYDDCIRX-UHFFFAOYSA-N 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 150000002681 magnesium compounds Chemical class 0.000 description 1
- 229940057948 magnesium stearate Drugs 0.000 description 1
- DQZLQYHGCKLKGU-UHFFFAOYSA-N magnesium;propane Chemical compound [Mg+2].C[CH-]C.C[CH-]C DQZLQYHGCKLKGU-UHFFFAOYSA-N 0.000 description 1
- LVKCSZQWLOVUGB-UHFFFAOYSA-M magnesium;propane;bromide Chemical compound [Mg+2].[Br-].C[CH-]C LVKCSZQWLOVUGB-UHFFFAOYSA-M 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 239000000155 melt Substances 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 230000028161 membrane depolarization Effects 0.000 description 1
- 238000002779 membrane potential assay Methods 0.000 description 1
- 150000002739 metals Chemical class 0.000 description 1
- XZWYZXLIPXDOLR-UHFFFAOYSA-N metformin Chemical compound CN(C)C(=N)NC(N)=N XZWYZXLIPXDOLR-UHFFFAOYSA-N 0.000 description 1
- 229960003105 metformin Drugs 0.000 description 1
- UZKWTJUDCOPSNM-UHFFFAOYSA-N methoxybenzene Substances CCCCOC=C UZKWTJUDCOPSNM-UHFFFAOYSA-N 0.000 description 1
- 239000008108 microcrystalline cellulose Substances 0.000 description 1
- 235000019813 microcrystalline cellulose Nutrition 0.000 description 1
- 229940016286 microcrystalline cellulose Drugs 0.000 description 1
- 125000002950 monocyclic group Chemical group 0.000 description 1
- 229910000403 monosodium phosphate Inorganic materials 0.000 description 1
- 235000019799 monosodium phosphate Nutrition 0.000 description 1
- PSHKMPUSSFXUIA-UHFFFAOYSA-N n,n-dimethylpyridin-2-amine Chemical compound CN(C)C1=CC=CC=N1 PSHKMPUSSFXUIA-UHFFFAOYSA-N 0.000 description 1
- WGLUNLJVYNJMBU-UHFFFAOYSA-N n-[2-(dimethylamino)ethyl]-n-[(3-methyl-1-oxo-2,4-dihydroisoquinolin-3-yl)methyl]decanamide Chemical compound C1=CC=C2C(=O)NC(CN(CCN(C)C)C(=O)CCCCCCCCC)(C)CC2=C1 WGLUNLJVYNJMBU-UHFFFAOYSA-N 0.000 description 1
- 125000001280 n-hexyl group Chemical group C(CCCCC)* 0.000 description 1
- 125000000740 n-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000006252 n-propylcarbonyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C(*)=O 0.000 description 1
- 230000017074 necrotic cell death Effects 0.000 description 1
- 239000013642 negative control Substances 0.000 description 1
- 125000001971 neopentyl group Chemical group [H]C([*])([H])C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 201000001119 neuropathy Diseases 0.000 description 1
- 230000007823 neuropathy Effects 0.000 description 1
- 229960003512 nicotinic acid Drugs 0.000 description 1
- 235000001968 nicotinic acid Nutrition 0.000 description 1
- 239000011664 nicotinic acid Substances 0.000 description 1
- UMRZSTCPUPJPOJ-KNVOCYPGSA-N norbornane Chemical compound C1C[C@H]2CC[C@@H]1C2 UMRZSTCPUPJPOJ-KNVOCYPGSA-N 0.000 description 1
- 125000002868 norbornyl group Chemical group C12(CCC(CC1)C2)* 0.000 description 1
- 125000005482 norpinyl group Chemical group 0.000 description 1
- 125000002347 octyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- VTRAEEWXHOVJFV-UHFFFAOYSA-N olmesartan Chemical compound CCCC1=NC(C(C)(C)O)=C(C(O)=O)N1CC1=CC=C(C=2C(=CC=CC=2)C=2NN=NN=2)C=C1 VTRAEEWXHOVJFV-UHFFFAOYSA-N 0.000 description 1
- 229960005117 olmesartan Drugs 0.000 description 1
- 238000006053 organic reaction Methods 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 150000002900 organolithium compounds Chemical class 0.000 description 1
- 125000002524 organometallic group Chemical group 0.000 description 1
- 125000001181 organosilyl group Chemical group [SiH3]* 0.000 description 1
- AHLBNYSZXLDEJQ-FWEHEUNISA-N orlistat Chemical compound CCCCCCCCCCC[C@H](OC(=O)[C@H](CC(C)C)NC=O)C[C@@H]1OC(=O)[C@H]1CCCCCC AHLBNYSZXLDEJQ-FWEHEUNISA-N 0.000 description 1
- 229960001243 orlistat Drugs 0.000 description 1
- 125000001715 oxadiazolyl group Chemical group 0.000 description 1
- 125000002971 oxazolyl group Chemical group 0.000 description 1
- 108091008765 peroxisome proliferator-activated receptors β/δ Proteins 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- 239000012071 phase Substances 0.000 description 1
- JTJMJGYZQZDUJJ-UHFFFAOYSA-N phencyclidine Chemical class C1CCCCN1C1(C=2C=CC=CC=2)CCCCC1 JTJMJGYZQZDUJJ-UHFFFAOYSA-N 0.000 description 1
- COLNVLDHVKWLRT-UHFFFAOYSA-N phenylalanine Natural products OC(=O)C(N)CC1=CC=CC=C1 COLNVLDHVKWLRT-UHFFFAOYSA-N 0.000 description 1
- 125000000843 phenylene group Chemical class C1(=C(C=CC=C1)*)* 0.000 description 1
- NHKJPPKXDNZFBJ-UHFFFAOYSA-N phenyllithium Chemical compound [Li]C1=CC=CC=C1 NHKJPPKXDNZFBJ-UHFFFAOYSA-N 0.000 description 1
- 229930029653 phosphoenolpyruvate Natural products 0.000 description 1
- DTBNBXWJWCWCIK-UHFFFAOYSA-N phosphoenolpyruvic acid Chemical compound OC(=O)C(=C)OP(O)(O)=O DTBNBXWJWCWCIK-UHFFFAOYSA-N 0.000 description 1
- 229960005095 pioglitazone Drugs 0.000 description 1
- 229940096701 plain lipid modifying drug hmg coa reductase inhibitors Drugs 0.000 description 1
- 239000000106 platelet aggregation inhibitor Substances 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 229940093430 polyethylene glycol 1500 Drugs 0.000 description 1
- 229940093429 polyethylene glycol 6000 Drugs 0.000 description 1
- 229910000027 potassium carbonate Inorganic materials 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 239000000047 product Substances 0.000 description 1
- 239000003881 protein kinase C inhibitor Substances 0.000 description 1
- 125000003373 pyrazinyl group Chemical group 0.000 description 1
- 125000002098 pyridazinyl group Chemical group 0.000 description 1
- 125000000714 pyrimidinyl group Chemical group 0.000 description 1
- 239000011541 reaction mixture Substances 0.000 description 1
- 239000000018 receptor agonist Substances 0.000 description 1
- 229940044601 receptor agonist Drugs 0.000 description 1
- 239000002464 receptor antagonist Substances 0.000 description 1
- 229940044551 receptor antagonist Drugs 0.000 description 1
- 102000005962 receptors Human genes 0.000 description 1
- 108020003175 receptors Proteins 0.000 description 1
- 238000001953 recrystallisation Methods 0.000 description 1
- 238000010992 reflux Methods 0.000 description 1
- 229960002354 repaglinide Drugs 0.000 description 1
- 125000006413 ring segment Chemical group 0.000 description 1
- 229960004586 rosiglitazone Drugs 0.000 description 1
- 239000011833 salt mixture Substances 0.000 description 1
- HZXJVDYQRYYYOR-UHFFFAOYSA-K scandium(iii) trifluoromethanesulfonate Chemical compound [Sc+3].[O-]S(=O)(=O)C(F)(F)F.[O-]S(=O)(=O)C(F)(F)F.[O-]S(=O)(=O)C(F)(F)F HZXJVDYQRYYYOR-UHFFFAOYSA-K 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- UNAANXDKBXWMLN-UHFFFAOYSA-N sibutramine Chemical compound C=1C=C(Cl)C=CC=1C1(C(N(C)C)CC(C)C)CCC1 UNAANXDKBXWMLN-UHFFFAOYSA-N 0.000 description 1
- 229960004425 sibutramine Drugs 0.000 description 1
- 238000007873 sieving Methods 0.000 description 1
- 150000004756 silanes Chemical class 0.000 description 1
- RMAQACBXLXPBSY-UHFFFAOYSA-N silicic acid Chemical compound O[Si](O)(O)O RMAQACBXLXPBSY-UHFFFAOYSA-N 0.000 description 1
- 239000000377 silicon dioxide Substances 0.000 description 1
- 235000012239 silicon dioxide Nutrition 0.000 description 1
- 229960002855 simvastatin Drugs 0.000 description 1
- RYMZZMVNJRMUDD-HGQWONQESA-N simvastatin Chemical compound C([C@H]1[C@@H](C)C=CC2=C[C@H](C)C[C@@H]([C@H]12)OC(=O)C(C)(C)CC)C[C@@H]1C[C@@H](O)CC(=O)O1 RYMZZMVNJRMUDD-HGQWONQESA-N 0.000 description 1
- 239000012279 sodium borohydride Substances 0.000 description 1
- 229910000033 sodium borohydride Inorganic materials 0.000 description 1
- BEOOHQFXGBMRKU-UHFFFAOYSA-N sodium cyanoborohydride Chemical compound [Na+].[B-]C#N BEOOHQFXGBMRKU-UHFFFAOYSA-N 0.000 description 1
- AJPJDKMHJJGVTQ-UHFFFAOYSA-M sodium dihydrogen phosphate Chemical compound [Na+].OP(O)([O-])=O AJPJDKMHJJGVTQ-UHFFFAOYSA-M 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- HPRAYQNGLXYUQM-UHFFFAOYSA-N spiro[4.5]decane-1,4,8-trione Chemical compound O=C1CCC(=O)C11CCC(=O)CC1 HPRAYQNGLXYUQM-UHFFFAOYSA-N 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 229960004793 sucrose Drugs 0.000 description 1
- 238000001308 synthesis method Methods 0.000 description 1
- 125000006253 t-butylcarbonyl group Chemical group [H]C([H])([H])C(C(*)=O)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 239000003826 tablet Substances 0.000 description 1
- 229960000651 tasosartan Drugs 0.000 description 1
- ADXGNEYLLLSOAR-UHFFFAOYSA-N tasosartan Chemical compound C12=NC(C)=NC(C)=C2CCC(=O)N1CC(C=C1)=CC=C1C1=CC=CC=C1C=1N=NNN=1 ADXGNEYLLLSOAR-UHFFFAOYSA-N 0.000 description 1
- 229960005187 telmisartan Drugs 0.000 description 1
- MHYGQXWCZAYSLJ-UHFFFAOYSA-N tert-butyl-chloro-diphenylsilane Chemical compound C=1C=CC=CC=1[Si](Cl)(C(C)(C)C)C1=CC=CC=C1 MHYGQXWCZAYSLJ-UHFFFAOYSA-N 0.000 description 1
- 125000001973 tert-pentyl group Chemical group [H]C([H])([H])C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- CXWXQJXEFPUFDZ-UHFFFAOYSA-N tetralin Chemical compound C1=CC=C2CCCCC2=C1 CXWXQJXEFPUFDZ-UHFFFAOYSA-N 0.000 description 1
- OULAJFUGPPVRBK-UHFFFAOYSA-N tetratriacontan-1-ol Chemical compound CCCCCCCCCCCCCCCCCCCCCCCCCCCCCCCCCCO OULAJFUGPPVRBK-UHFFFAOYSA-N 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 125000001113 thiadiazolyl group Chemical group 0.000 description 1
- 150000001467 thiazolidinediones Chemical class 0.000 description 1
- 125000000335 thiazolyl group Chemical group 0.000 description 1
- HPGGPRDJHPYFRM-UHFFFAOYSA-J tin(iv) chloride Chemical compound Cl[Sn](Cl)(Cl)Cl HPGGPRDJHPYFRM-UHFFFAOYSA-J 0.000 description 1
- XJDNKRIXUMDJCW-UHFFFAOYSA-J titanium tetrachloride Chemical compound Cl[Ti](Cl)(Cl)Cl XJDNKRIXUMDJCW-UHFFFAOYSA-J 0.000 description 1
- 229960005371 tolbutamide Drugs 0.000 description 1
- 229960004394 topiramate Drugs 0.000 description 1
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 238000000844 transformation Methods 0.000 description 1
- 229910052723 transition metal Inorganic materials 0.000 description 1
- 150000003624 transition metals Chemical class 0.000 description 1
- ZGYICYBLPGRURT-UHFFFAOYSA-N tri(propan-2-yl)silicon Chemical group CC(C)[Si](C(C)C)C(C)C ZGYICYBLPGRURT-UHFFFAOYSA-N 0.000 description 1
- 125000004665 trialkylsilyl group Chemical group 0.000 description 1
- 125000004306 triazinyl group Chemical group 0.000 description 1
- 125000001425 triazolyl group Chemical group 0.000 description 1
- CEAWWDXUKYZTJL-UHFFFAOYSA-N triethyl(phenyl)silane Chemical group CC[Si](CC)(CC)C1=CC=CC=C1 CEAWWDXUKYZTJL-UHFFFAOYSA-N 0.000 description 1
- 125000004044 trifluoroacetyl group Chemical group FC(C(=O)*)(F)F 0.000 description 1
- XQKBFQXWZCFNFF-UHFFFAOYSA-K triiodosamarium Chemical compound I[Sm](I)I XQKBFQXWZCFNFF-UHFFFAOYSA-K 0.000 description 1
- FTVLMFQEYACZNP-UHFFFAOYSA-N trimethylsilyl trifluoromethanesulfonate Chemical compound C[Si](C)(C)OS(=O)(=O)C(F)(F)F FTVLMFQEYACZNP-UHFFFAOYSA-N 0.000 description 1
- MMYRBBZVCDXGHG-UHFFFAOYSA-N tripropylsilicon Chemical group CCC[Si](CCC)CCC MMYRBBZVCDXGHG-UHFFFAOYSA-N 0.000 description 1
- 125000002221 trityl group Chemical group [H]C1=C([H])C([H])=C([H])C([H])=C1C([*])(C1=C(C(=C(C(=C1[H])[H])[H])[H])[H])C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- 239000012588 trypsin Substances 0.000 description 1
- 231100000397 ulcer Toxicity 0.000 description 1
- 229940116269 uric acid Drugs 0.000 description 1
- 230000003424 uricosuric effect Effects 0.000 description 1
- 229960004699 valsartan Drugs 0.000 description 1
- SJSNUMAYCRRIOM-QFIPXVFZSA-N valsartan Chemical compound C1=CC(CN(C(=O)CCCC)[C@@H](C(C)C)C(O)=O)=CC=C1C1=CC=CC=C1C1=NN=N[N]1 SJSNUMAYCRRIOM-QFIPXVFZSA-N 0.000 description 1
- PXXNTAGJWPJAGM-UHFFFAOYSA-N vertaline Natural products C1C2C=3C=C(OC)C(OC)=CC=3OC(C=C3)=CC=C3CCC(=O)OC1CC1N2CCCC1 PXXNTAGJWPJAGM-UHFFFAOYSA-N 0.000 description 1
- SYOKIDBDQMKNDQ-XWTIBIIYSA-N vildagliptin Chemical compound C1C(O)(C2)CC(C3)CC1CC32NCC(=O)N1CCC[C@H]1C#N SYOKIDBDQMKNDQ-XWTIBIIYSA-N 0.000 description 1
- 229960001729 voglibose Drugs 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- 229910052725 zinc Inorganic materials 0.000 description 1
- 239000011701 zinc Substances 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H7/00—Compounds containing non-saccharide radicals linked to saccharide radicals by a carbon-to-carbon bond
- C07H7/04—Carbocyclic radicals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Diabetes (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Endocrinology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Genetics & Genomics (AREA)
- Biotechnology (AREA)
- Emergency Medicine (AREA)
- Biochemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Hematology (AREA)
- Obesity (AREA)
- Molecular Biology (AREA)
- General Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
Description
Gegenstand der vorliegenden Erfindung sind D-Glucopyranosyl-phenyl-substituierte Cyclen der allgemeinen Formel I wobei die Reste R1 bis R6, Z, Cy sowie R7a, R7b, R7c und R7d nachfolgend definiert sind, einschließlich deren Tautomere, deren Stereoisomere, deren Gemische und deren Salze. Ein weiterer Gegenstand dieser Erfindung betrifft Arzneimittel enthaltend eine erfindungsgemäße Verbindung der Formel I sowie die Verwendung einer erfindungsgemäßen Verbindung zur Herstellung eines Arzneimittels zur Behandlung von Stoffwechselerkrankungen. Darüber hinaus sind Verfahren zur Herstellung eines Arzneimittels sowie einer erfindungsgemäßen Verbindung Gegenstand dieser Erfindung.The present invention relates to D-glucopyranosyl-phenyl-substituted cyclen of the general formula I. wherein the radicals R 1 to R 6 , Z, Cy and R 7a , R 7b , R 7c and R 7d are defined below, including their tautomers, their stereoisomers, their mixtures and their salts. A further subject of this invention relates to medicaments containing a compound of the formula I according to the invention and to the use of a compound according to the invention for the preparation of a medicament for the treatment of metabolic diseases. In addition, processes for the preparation of a medicament and of a compound according to the invention are the subject of this invention.
In der Literatur werden Verbindungen, die eine Hemmwirkung auf den natriumabhängigen Glucose-Cotransporter SGLT besitzen, zur Behandlung von Krankheiten, insbesondere von Diabetes vorgeschlagen.In In the literature, compounds which have an inhibitory effect on the sodium-dependent Glucose cotransporter SGLT possess, for the treatment of diseases, especially suggested by diabetes.
Aus den internationalen Offenlegungsschriften WO 98/31697, WO 01/27128, WO 02/083066 und WO 03/099836 sind Glucopyranosyl-substituierte Aromaten sowie deren Herstellung und deren mögliche Aktivität als SGLT2-Inhibitoren bekannt.Out International Publication WO 98/31697, WO 01/27128, WO 02/083066 and WO 03/099836 are glucopyranosyl-substituted Aromatics and their production and their possible activity as SGLT2 inhibitors known.
Aufgabe der ErfindungObject of the invention
Der vorliegenden Erfindung liegt die Aufgabe zugrunde, neue Pyranosyl-substituierte Phenyle aufzuzeigen, insbesondere solche, die eine Aktivität bezüglich des natriumabhängigen Glucose-Cotransporters SGLT, insbesondere SGLT2 besitzen. Eine weitere Aufgabe der vorliegenden Erfindung besteht im Aufzeigen von Pyranosyl-substituierten Phenylen, die in vitro und/oder in vivo im Vergleich mit bekannten, strukturähnlichen Verbindungen eine erhöhte Hemmwirkung bezüglich des natriumabhängigen Glucose-Cotransporters SGLT2 besitzen und/oder verbesserte pharmakologische oder pharmakokinetische Eigenschaften aufweisen.Of the present invention is based on the object, new pyranosyl-substituted Phenyle show, especially those that have activity in the sodium-dependent Glucose cotransporters SGLT, in particular SGLT2 possess. Another The object of the present invention is to show pyranosyl-substituted Phenylene in vitro and / or in vivo in comparison with known, structurally similar Compounds an increased Inhibitory effect with respect of the sodium dependent Possess glucose-cotransporters SGLT2 and / or improved pharmacological or pharmacokinetic properties.
Ferner ist es eine Aufgabe der vorliegenden Erfindung, neue Arzneimittel bereit zu stellen, welche zur Prophylaxe und/oder Behandlung von Stoffwechselerkrankungen, insbesondere von Diabetes geeignet sind.Further It is an object of the present invention to provide new medicines to provide, which for the prophylaxis and / or treatment of Metabolic disorders, especially of diabetes are suitable.
Ebenfalls eine Aufgabe dieser Erfindung ist es, ein Verfahren zur Herstellung der erfindungsgemäßen Verbindungen bereit zu stellen.Also An object of this invention is to provide a method of preparation the compounds of the invention to provide.
Weitere Aufgaben der vorliegenden Erfindung ergeben sich für den Fachmann unmittelbar aus den vorhergehenden und nachfolgenden Ausführungen.Further Objects of the present invention will be apparent to those skilled in the art directly from the preceding and following remarks.
Gegenstand der ErfindungSubject of the invention
Ein
erster Gegenstand der vorliegenden Erfindung sind D-Glucopyranosyl-phenyl-substituierte Cyclen der
allgemeinen Formel I Cy einen
5- oder 6-gliedrigen gesättigten
oder einfach ungesättigten
Carbocyclus bedeutet, der im Ring ein, zwei oder drei Heteroatome
unabhängig
voneinander ausgewählt
aus N, O und S aufweisen kann, und
der mit R4,
R5 und R6 über eine
Einfachbindung und mit R3 über eine
Einfach- oder eine
Doppelbindung substituiert ist, und
in dem eine oder zwei Methylengruppen
durch CO oder eine Sulfanylgruppe durch SO oder SO2 ersetzt
sein kann, und
in dem zusätzlich
ein oder mehrere an Kohlenstoff gebundene H-Atome durch Fluor ersetzt
sein können,
Z
-O-, -CH2-, -CH=, -NRN-,
-CO-, -S-, -SO- oder -SO2- bedeutet, wobei
H-Atome der Methylen-
oder Methanylyliden-Brücke
unabhängig
voneinander durch CH3 oder F substituiert
sein können;
R1 Wasserstoff, Fluor, Chlor, Brom, Iod, C1-6-Alkyl, C2-6-Alkinyl,
C2-6-Alkenyl, C3-10-Cycloalkyl, C3-10-Cycloalkyl-C1-3-alkyl,
C5-10-Cycloalkenyl, C5-10-Cycloalkenyl-C1-3-alkyl, C1-4-Alkylcarbonyl,
Arylcarbonyl, Heteroarylcarbonyl, Aminocarbonyl, C1-4-Alkylaminocarbonyl,
Di-(C1-3-Alkyl)aminocarbonyl, Pyrrolidin-1-ylcarbonyl,
Piperidin-1-ylcarbonyl, Morpholin-4-ylcarbonyl, Piperazin-1-ylcarbonyl,
4-(C1-4-Alkyl)piperazin-1-ylcarbonyl, C1-4-Alkoxycarbonyl, Amino, C1-4-Alkylamino,
Di-(C1-3-alkyl)amino, Pyrrolidin-1-yl, Piperidin-1-yl,
Morpholin-4-yl, Piperazin-1-yl, 4-(C1-4-Alkyl)piperazin-1-yl,
C1-4-Alkylcarbonylamino,
C1-6-Alkyloxy, C3-10-Cycloalkyloxy,
C5-10-Cycloalkenyloxy, Aryloxy, C1-4-Alkylsulfanyl, C1-4-Alkylsulfinyl,
C1-4-Alkylsulfonyl, C3-10-Cycloalkylsulfanyl,
C3-10-Cycloalkylsulfinyl, C3-10-Cycloalkylsulfonyl,
C5-10-Cycloalkenylsulfanyl, C5-10-Cycloalkenylsulfinyl,
C5-10-Cycloalkenylsulfonyl, Arylsulfanyl,
Arylsulfinyl, Arylsulfonyl, Hydroxy, Cyan und Nitro,
wobei
Alkyl-, Alkenyl-, Alkinyl-, Cycloalkyl- und Cycloalkenyl-Reste teilweise
oder vollständig
fluoriert oder ein- oder zweifach mit gleichen oder verschiedenen
Substituenten ausgewählt
aus Chlor, Hydroxy, C1-3-Alkoxy und C1-3-Alkyl substituiert sein können, und
wobei
in Cycloalkyl- und Cycloalkenyl-Resten ein oder zwei Methylengruppen
unabhängig
voneinander durch O, S, CO, SO oder SO2 substituiert
sein können,
und
wobei in N-Heterocycloalkyl-Resten eine Methylengruppe
durch CO oder SO2 substituiert sein kann,
und
R2 Wasserstoff, Fluor, Chlor, Brom,
Hydroxy, C1-4-Alkyl, C1-4-Alkoxy,
Cyan oder Nitro, wobei Alkyl-Reste ein- oder mehrfach mit Fluor
substituiert sein können,
oder
für
den Fall, dass R1 und R2 an
zwei miteinander benachbarte C-Atome des Phenylrings gebunden sind,
können
R1 und R2 derart
miteinander verbunden sein, dass R1 und
R2 zusammen eine C3-5-Alkylen-,
C3-5-Alkenylen- oder Butadienylen-Brücke bilden,
die teilweise oder vollständig
fluoriert oder ein- oder
zweifach mit gleichen oder verschiedenen Substituenten ausgewählt aus
Chlor, Hydroxy, C1-3-Alkoxy und C1-3-Alkyl substituiert sein kann, und in
der eine oder zwei Methylengruppen unabhängig voneinander durch O, S,
CO, SO, SO2 oder NRN ersetzt
sein können,
und in der im Falle einer Butadienylen-Brücke eine oder zwei Methingruppen
durch ein N-Atom ersetzt sein können,
R3 Wasserstoff, Fluor, Chlor, Brom, C1-6-Alkyl, C2-6-Alkinyl,
C2-6-Alkenyl, C3-10-Cycloalkyl, C3-10-Cycloalkyl-C1-3-alkyl,
C5-10-Cycloalkenyl, C5-10-Cycloalkenyl-C1-3-alkyl, Aryl, Heteroaryl, Aryl-C1-3-alkyl, Heteroaryl-C1-3-alkyl, C1-4-Alkylcarbonyl,
Arylcarbonyl, Heteroarylcarbonyl, Aminocarbonyl, C1-4-Alkylaminocarbonyl,
Di-(C1-3-Alkyl)aminocarbonyl, Pyrrolidin-1-ylcarbonyl,
Piperidin-1-ylcarbonyl, Morpholin-4-ylcarbonyl, Piperazin-1-ylcarbonyl,
4-(C1-4-Alkyl)piperazin-1-ylcarbonyl,
Hydroxycarbonyl, C1-4-Alkoxycarbonyl, C1-4-Alkylamino,
Di-(C1-3-alkyl)amino, Pyrrolidin-1-yl, Piperidin-1-yl,
Morpholin-4-yl, Piperazin-1-yl, 4-(C1-4-Alkyl)piperazin-1-yl,
C1-4-Alkylcarbonylamino, Arylcarbonylamino,
Heteroarylcarbonylamino, C1-4-Alkylsulfonylamino,
Arylsulfonylamino, C1-6-Alkoxy, C3-10-Cycloalkyloxy, C5-10-Cycloalkenyloxy,
Aryloxy, Heteroaryloxy, C1-4-Alkylsulfanyl,
C1-4-Alkylsulfinyl, C1-4-Alkylsulfonyl,
C3-10-Cycloalkylsulfanyl, C3-10-Cycloalkylsulfinyl,
C3-10-Cycloalkylsulfonyl, C5-10-Cycloalkenylsulfanyl,
C5-10-Cycloalkenylsulfinyl, C5-10-Cycloalkenylsulfonyl,
Arylsulfanyl, Arylsulfinyl, Arylsulfonyl, Amino, Hydroxy, Cyan oder
Nitro bedeutet, und
wobei Alkyl-, Alkenyl-, Alkinyl-, Cycloalkyl-
und Cycloalkenyl-Reste teilweise oder vollständig fluoriert oder ein- oder
zweifach mit gleichen oder verschiedenen Substituenten ausgewählt aus
Chlor, Hydroxy, C1-3-Alkoxy und C1-3-Alkyl substituiert sein können, und
wobei
in Cycloalkyl- und Cycloalkenyl-Resten ein oder zwei Methylengruppen
unabhängig
voneinander durch O, S, CO, SO oder SO2 substituiert
sein können,
und
wobei in N-Heterocycloalkyl-Resten eine Methylengruppe
durch CO oder SO2 substituiert sein kann,
oder
R3 bedeutet eine über eine
Doppelbindung mit Cy verbundene Gruppe Y,
R4 Wasserstoff,
Fluor, Chlor, Cyan, Nitro, Amino, C1-3-Alkyl-amino,
Di-(C1-3-Alkyl)amino,
C1-3-Alkylcarbonylamino, C1-3-Alkyl,
C1-3-Alkoxy, Hydroxycarbonyl, C1-3-Alkoxycarbonyl
oder durch 1 bis 3 Fluoratome substituiertes Methyl- oder Methoxy
bedeutet, und
für
den Fall, dass R3 und R4 an
dem selben C-Atom des Cyclus Cy gebunden sind, können R3 und
R4 derart miteinander verbunden sein, dass
R3 und R4 zusammen
eine C2-6-Alkylen- oder C4-6-Alkenylen-Brücke bilden, die
teilweise oder vollständig
fluoriert oder ein- oder zweifach mit gleichen oder verschiedenen
Substituenten ausgewählt
aus Chlor, Hydroxy, C1-3-Alkoxy und C1-3-Alkyl substituiert sein kann und in der
eine oder zwei Methylengruppen unabhängig voneinander durch O, S,
CO, SO, SO2 oder NRN substituiert
sein können,
oder
für
den Fall, dass R3 und R4 an
zwei benachbarte Atome des Cyclus Cy bebunden sind, können R3 und R4 derart miteinander
verbunden sein, dass R3 und R4 zusammen
mit den beiden benachbarten Atomen des Cyclus Cy einen anellierten
gesättigten
oder ein- oder mehrfach ungesättigten
5- oder 6-gliedrigen
Carbocyclus bilden, in dem eine oder zwei Methylengruppen unabhängig voneinander
durch O, S, CO, SO, SO2 oder NRN und/oder
eine oder zwei Methingruppen durch N ersetzt sein können, und
der ein- oder mehrfach fluoriert oder ein- oder zweifach mit gleichen
oder verschiedenen Substituenten ausgewählt aus Chlor, Hydroxy, C1-3-Alkoxy und C1-3-Alkyl
oder im Falle eines aromatischen anellierten Cyclus ein- oder zweifach
mit gleichen oder verschiedenen Substituenten L substituiert sein
kann,
R5 Wasserstoff, Fluor, Chlor,
Cyan, C1-3-Alkyl, C1-3-Alkoxy
oder durch 1 bis 3 Fluoratome substituiertes Methyl- oder Methoxy
bedeutet, und
R4 und R5 sind
derart miteinander verbunden, dass R4 und
R5 zusammen eine C1-4-Alkylen-
oder C2-4-Alkenylen-Brücke bilden, die mit 2, 3 oder
4 Atomen des Cyclus Cy einen anellierten oder verbrückten Cyclus
bildet und die teilweise oder vollständig fluoriert oder ein- oder
zweifach mit gleichen oder verschiedenen Substituenten ausgewählt aus
Chlor, Hydroxy, C1-3-Alkoxy und C1-3-Alkyl
substituiert sein kann, und in der ein oder zwei Methylengruppen
unabhängig
voneinander durch O, S, CO, SO, SO2 oder
NRN substituiert sein können, und
R6 Wasserstoff,
C1-3-Alkyl oder Fluor bedeutet, oder
R4, R5 und R6 sind derart miteinander verbunden, dass
R4, R5 und R6 zusammen eine C3-6-Alkantriyl-Brücke bilden,
die zuammen mit dem Cyclus Cy ein verbrücktes bicyclisches oder ein
tricyclisches System bildet, wobei die Alkantriyl-Brücke ein-
oder mehrfach fluoriert oder ein- oder zweifach mit gleichen oder
verschiedenen Substituenten ausgewählt aus Chlor, Hydroxy, C1-3-Alkoxy und C1-3-Alkyl
substituiert sein kann, und in der ein oder zwei Methylengruppen
unabhängig
voneinander durch O, CO, SO2 oder NRN substituiert sein können, und
Y Sauerstoff,
oder
Methyliden, Fluormethyliden, Chlormethyliden, C1-6-Alkyl-methyliden, C2-6-Alkenyl-methyliden,
C2-6-Alkinyl-methyliden, C3-10-Cycloalkyl-methyliden,
C5-10-Cycloalkenyl-methyliden,
C3-10-Cycloalkyliden, C5-10-Cycloalkenyliden,
C3-10-Cycloalkyl-C1-3-alkyl-methyliden, C5-10-Cycloalkenyl-C1-3-alkyl-methyliden, Arylmethyliden, Heteroarylmethyliden,
Aryl-C1-3-alkyl-methyliden oder Heteroaryl-C1-3-alkyl-methyliden bedeutet,
wobei
Alkyl-, Alkenyl-, Alkinyl-, Cycloalkyl-, Cycloalkenyl-, Cycloalkyliden-
und Cycloalkenyliden-Reste teilweise oder vollständig fluoriert oder ein- oder
zweifach mit gleichen oder verschiedenen Substituenten ausgewählt aus
Chlor, Cyan, Hydroxy, C1-3-Alkoxy, C1-3-Alkylsulfanyl und C1-3-Alkyl
substituiert sein können,
und
wobei die zuvor angeführte
unsubstituierte Methylidengruppe oder die zuvor angeführten einfach
substituierten Methylidengruppen zusätzlich einfach mit Fluor, Chlor,
C1-3-Alkyl, Trifluormethyl, C1-4-Alkoxy,
Cyan oder Nitro substituiert sein können, und
wobei in Cycloalkyl-,
Cycloalkenyl-, Cycloalkyliden- und Cycloalkenyliden-Resten ein oder zwei
Methylengruppen unabhängig
voneinander durch O, S, CO, SO, SO2 oder
NRN substituiert sein können, oder
Y bedeutet
eine Gruppe gemäß der Teilformel
in der
D Carbonyl
oder Sulfonyl,
RY Wasserstoff, Fluor,
Chlor, Cyan, Trifluormethyl oder C1-3-Alkyl
bedeutet,
B eine Einfachbindung, -O- oder -NRN-
bedeutet,
RB Wasserstoff, C1-6-Alkyl-, C3-6-Alkenyl-,
C3-6-Alkinyl-, C3-10-Cycloalkyl-,
C5-10-Cycloalkenyl-,
C3-10-Cycloalkyl-C1-3-alkyl-,
C5-10-Cycloalkenyl-C1-3-alkyl-,
Aryl, Heteroaryl, Aryl-C1-3-alkyl- oder
Heteroaryl-C1-3-alkyl- bedeutet,
wobei
Alkyl-, Cycloalkyl- und Cycloalkenyl-Reste teilweise oder vollständig fluoriert
oder ein- oder zweifach mit gleichen oder verschiedenen Substituenten
ausgewählt
aus Chlor, Cyan, Hydroxy, C1-3-Alkoxy und
C1-3-Alkyl substituiert
sein können,
oder
RB und B miteinander unter Ausbildung
eines heterocyclischen Rings ausgewählt aus Pyrrolidin, Morpholin, Piperidin,
Piperazin und 4-(C1-4-Alkyl)piperazin verbunden
sind, wobei der heterocyclische Ring über die Iminogruppe an die
Gruppe D gebunden ist,
RN unabhängig voneinander
H oder C1-4-Alkyl,
L unabhängig voneinander
ausgewählt
aus der Gruppe bestehend aus Fluor, Chlor, Brom, Iod, C1-3-Alkyl,
Difluormethyl, Trifluormethyl, C1-3-Alkoxy,
Difluormethoxy, Trifluormethoxy und Cyan,
R7a,
R7b, R7c, R7d unabhängig
voneinander eine Bedeutung ausgewählt aus der Gruppe Wasserstoff,
(C1-18-Alkyl)carbonyl, (C1-18-Alkyl)oxycarbonyl,
Arylcarbonyl und Aryl-(C1-3-alkyl)-carbonyl
besitzen,
wobei unter den bei der Definition der vorstehend
genannten Reste erwähnten
Arylgruppen Phenyl- oder Naphthylgruppen zu verstehen sind, welche
unabhängig
voneinander ein- oder zweifach mit gleichen oder verschiedenen Resten
L substituiert sein können;
und
unter den bei der Definition der vorstehend erwähnten Reste
erwähnten
Heteroarylgruppen eine Pyrrolyl-, Furanyl-, Thienyl-, Imidazolyl-,
Pyridyl-, Indolyl-, Benzofuranyl-Benzothiophenyl-,
Chinolinyl- oder Isochinolinylgruppe zu verstehen ist,
oder
eine Pyrrolyl-, Furanyl-, Thienyl-, Imidazolyl- oder Pyridylgruppe
zu verstehen ist, in der eine oder zwei Methingruppen durch Stickstoffatome
ersetzt sind,
oder eine Indolyl-, Benzofuranyl-, Benzothiophenyl-,
Chinolinyl- oder Isochinolinylgruppe zu verstehen ist, in der eine
bis drei Methingruppen durch Stickstoffatome ersetzt sind,
wobei
die vorstehend erwähnten
Heteroarylgruppen unabhängig
voneinander ein oder zweifach mit gleichen oder verschiedenen Resten
L substituiert sein können;
wobei
unter dem bei der Definition der vorstehend erwähnten Reste erwähnten N-Heterocycloalkyl-Rest
ein gesättigter
carbocyclischer Ring, der eine Imino-Gruppe im Ring aufweist, zu
verstehen ist, der eine weitere Imino-Gruppe oder ein O- oder S-Atom im Ring aufweisen
kann, und
wobei, soweit nichts anderes erwähnt wurde, die vorstehend erwähnten Alkylgruppen
geradkettig oder verzweigt sein können,
deren Tautomere,
deren Stereoisomere, deren Gemische und deren Salze, insbesondere
deren physiologisch verträglichen
Salze,
wobei, folgende Verbindung (D1) nicht mit umfasst ist:
(D1)
3-[(3-β-D-glucopyranosyl-4,5-dimethoxyphenyl)methyl]-4-[(3,4-dimethoxyphenyl)methyl]-dihydro-2(3H)-furanon.A first subject of the present invention are D-glucopyranosyl-phenyl-substituted cyclen of the general formula I. Cy is a 5- or 6-membered saturated or monounsaturated carbocycle which in the ring may have one, two or three heteroatoms independently selected from N, O and S, and
which is substituted with R 4 , R 5 and R 6 via a single bond and with R 3 via a single or a double bond, and
in which one or two methylene groups may be replaced by CO or a sulfanyl group by SO or SO 2 , and
in which additionally one or more carbon-bonded hydrogen atoms may be replaced by fluorine,
Z is -O-, -CH 2 -, -CH =, -NR N -, -CO-, -S-, -SO- or -SO 2 -, where H atoms of the methylene or methanylylidene bridge independently of one another may be substituted by CH 3 or F;
R 1 is hydrogen, fluorine, chlorine, bromine, iodine, C 1-6 -alkyl, C 2-6 -alkynyl, C 2-6 -alkenyl, C 3-10 -cycloalkyl, C 3-10 -cycloalkyl-C 1- 3 -alkyl, C 5-10 -cycloalkenyl, C 5-10 -cycloalkenyl-C 1-3 -alkyl, C 1-4 -alkylcarbonyl, arylcarbonyl, heteroarylcarbonyl, aminocarbonyl, C 1-4 -alkylaminocarbonyl, di- (C 1 3- alkyl) aminocarbonyl, pyrrolidin-1-ylcarbonyl, piperidin-1-ylcarbonyl, morpholin-4-ylcarbonyl, piperazin-1-ylcarbonyl, 4- (C 1-4 alkyl) piperazin-1-ylcarbonyl, C 1 4 alkoxycarbonyl, amino, C 1-4 alkylamino, di (C 1-3 alkyl) amino, pyrrolidin-1-yl, piperidin-1-yl, morpholin-4-yl, piperazin-1-yl, 4 (C 1-4 alkyl) piperazin-1-yl, C 1-4 alkylcarbonylamino, C 1-6 alkyloxy, C 3-10 cycloalkyloxy, C 5-10 cycloalkenyloxy, aryloxy, C 1-4 Alkylsulfanyl, C 1-4 alkylsulfinyl, C 1-4 alkylsulfonyl, C 3-10 cycloalkylsulfanyl, C 3-10 cycloalkylsulfinyl, C 3-10 cycloalkylsulfonyl, C 5-10 cycloalkenylsulfanyl, C 5-10 cycloalkenylsulfinyl , C 5-10 cycloalkenylsulfonyl, arylsulfanyl, arylsulfine yl, arylsulfonyl, hydroxy, cyano and nitro,
wherein alkyl, alkenyl, alkynyl, cycloalkyl and cycloalkenyl radicals are partially or completely fluorinated or mono- or disubstituted by identical or different substituents selected from chlorine, hydroxy, C 1-3 alkoxy and C 1-3 alkyl substituted can be, and
wherein in cycloalkyl and cycloalkenyl radicals one or two methylene groups can be substituted independently of one another by O, S, CO, SO or SO 2 , and
wherein in N-heterocycloalkyl radicals a methylene group may be substituted by CO or SO 2 , and
R 2 is hydrogen, fluorine, chlorine, bromine, hydroxyl, C 1-4 -alkyl, C 1-4 -alkoxy, cyano or nitro, where alkyl radicals may be mono- or polysubstituted by fluorine, or
in the event that R 1 and R 2 are bonded to two adjacent C atoms of the phenyl ring, R 1 and R 2 may be linked together such that R 1 and R 2 together form a C 3-5 alkylene, C 3-5 alkenylene or butadienylene bridge which may be partially or completely fluorinated or mono- or disubstituted by identical or different substituents selected from chlorine, hydroxy, C 1-3 alkoxy and C 1-3 alkyl, and in which one or two methylene groups can be replaced independently of one another by O, S, CO, SO, SO 2 or NR N , and in which in the case of a butadienylene bridge one or two methine groups can be replaced by an N atom,
R 3 is hydrogen, fluorine, chlorine, bromine, C 1-6 -alkyl, C 2-6 -alkynyl, C 2-6 -alkenyl, C 3-10 -cycloalkyl, C 3-10 -cycloalkyl-C 1-3 alkyl, C 5-10 -cycloalkenyl, C 5-10 -cycloalkenyl-C 1-3 -alkyl, aryl, heteroaryl, arylC 1-3 -alkyl, heteroarylC 1-3 -alkyl, C 1-4 - Alkylcarbonyl, arylcarbonyl, heteroarylcarbonyl, aminocarbonyl, C 1-4 alkylaminocarbonyl, di (C 1-3 alkyl) aminocarbonyl, pyrrolidin-1-ylcarbonyl, piperidin-1-ylcarbonyl, morpholin-4-ylcarbonyl, piperazin-1-ylcarbonyl , 4- (C 1-4 -alkyl) -piperazin-1-ylcarbonyl, hydroxycarbonyl, C 1-4 -alkoxycarbonyl, C 1-4 -alkylamino, di- (C 1-3 -alkyl) -amino, pyrrolidin-1-yl , Piperidin-1-yl, morpholin-4-yl, piperazin-1-yl, 4- (C 1-4 alkyl) piperazin-1-yl, C 1-4 alkylcarbonylamino, arylcarbonylamino, heteroarylcarbonylamino, C 1-4 Alkylsulfonylamino, arylsulfonylamino, C 1-6 alkoxy, C 3-10 cycloalkyloxy, C 5-10 cycloalkenyloxy, aryloxy, heteroaryloxy, C 1-4 alkylsulfanyl, C 1-4 alkylsulfinyl, C 1-4 alkylsulfonyl , C 3-10 -cycloalkylsulfanyl, C 3-10 cycloalkylsulfinyl, C 3-10 cycloalkylsulfonyl, C 5-10 cycloalkenylsulfanyl, C 5-10 cycloalkenylsulfinyl, C 5-10 cycloalkenylsulfonyl, arylsulfanyl, arylsulfinyl, arylsulfonyl, amino, hydroxy, cyano or nitro, and
wherein alkyl, alkenyl, alkynyl, cycloalkyl and cycloalkenyl radicals are partially or completely fluorinated or mono- or disubstituted by identical or different substituents selected from chlorine, hydroxy, C 1-3 alkoxy and C 1-3 alkyl substituted can be, and
wherein in cycloalkyl and cycloalkenyl radicals one or two methylene groups can be substituted independently of one another by O, S, CO, SO or SO 2 , and
wherein in N-heterocycloalkyl radicals a methylene group may be substituted by CO or SO 2 , or
R 3 represents a group Y connected via a double bond with Cy,
R 4 is hydrogen, fluorine, chlorine, cyano, nitro, amino, C 1-3 alkylamino, di (C 1-3 alkyl) amino, C 1-3 alkylcarbonylamino, C 1-3 alkyl, C 1-3 denotes alkoxy, hydroxycarbonyl, C 1-3 -alkoxycarbonyl or methyl or methoxy substituted by 1 to 3 fluorine atoms, and
in the event that R 3 and R 4 are bonded to the same C-atom of the Cy cycle, R 3 and R 4 may be linked together such that R 3 and R 4 together form a C 2-6 alkylene or C Form 4-6 alkenylene bridge which may be partially or fully fluorinated or mono- or disubstituted by identical or different substituents selected from chloro, hydroxy, C 1-3 alkoxy and C 1-3 alkyl and in which one or two methylene groups may be independently substituted by O, S, CO, SO, SO 2 or NR N , or
in the event that R 3 and R 4 are attached to two adjacent atoms of the Cy cycle, R 3 and R 4 may be linked together such that R 3 and R 4 together with the two adjacent atoms of the Cy cycle form a fused saturated or unsaturated group form a mono- or polyunsaturated 5- or 6-membered carbocycle in which one or two methylene groups can be replaced independently by O, S, CO, SO, SO 2 or NR N and / or one or two methine groups by N, and which is mono- or polyfluorinated or mono- or disubstituted by identical or different substituents selected from chlorine, hydroxyl, C 1-3 -alkoxy and C 1-3 -alkyl or in the case of an aromatic fused cycle, once or twice with identical or different substituents Substituents L may be substituted,
R 5 is hydrogen, fluorine, chlorine, cyano, C 1-3 -alkyl, C 1-3 -alkoxy or methyl or methoxy substituted by 1 to 3 fluorine atoms, and
R 4 and R 5 are bonded together such that R 4 and R 5 together form a C 1-4 alkylene or C 2-4 alkenylene bridge fused with 2, 3 or 4 atoms of the Cy cycle forms bridged Cyclus and which may be partially or completely fluorinated or mono- or disubstituted by identical or different substituents selected from chlorine, hydroxy, C 1-3 alkoxy and C 1-3 alkyl, and in the one or two methylene groups independently may be substituted by O, S, CO, SO, SO 2 or NR N , and
R 6 is hydrogen, C 1-3 -alkyl or fluorine, or
R 4 , R 5 and R 6 are joined together such that R 4 , R 5 and R 6 together form a C 3-6 alkanetriyl bridge which together with the Cy cycle forms a bridged bicyclic or tricyclic system, wherein the alkanetriyl bridge may be mono- or polyfluorinated or mono- or disubstituted by identical or different substituents selected from chlorine, hydroxy, C 1-3 -alkoxy and C 1-3 -alkyl, and in which one or two methylene groups are independent may be substituted by O, CO, SO 2 or NR N , and
Y oxygen, or
Methylidene, fluoromethylidene, chloromethylidene, C 1-6 alkylmethylidene, C 2-6 alkenylmethylidene, C 2-6 alkynylmethylidene, C 3-10 cycloalkylmethylidene, C 5-10 cycloalkenylmethylidene , C 3-10 cycloalkylidene, C 5-10 cycloalkenylidene, C 3-10 cycloalkyl C 1-3 alkylmethylidene, C 5-10 cycloalkenyl C 1-3 alkylmethylidene, arylmethylidene, heteroarylmethylidene , Aryl-C 1-3 -alkyl-methylidene or heteroaryl-C 1-3 -alkyl-methylidene,
wherein alkyl, alkenyl, alkynyl, cycloalkyl, cycloalkenyl, cycloalkylidene and cycloalkenylidene radicals are partially or completely fluorinated or mono- or disubstituted by identical or different substituents selected from chlorine, cyano, hydroxy, C 1-3 -alkoxy , C 1-3 -alkylsulfanyl and C 1-3 -alkyl, and
in addition, the above-mentioned unsubstituted methylidene group or the above-mentioned monosubstituted methylidene groups may be easily substituted with fluorine, chlorine, C 1-3 alkyl, trifluoromethyl, C 1-4 alkoxy, cyano or nitro, and
wherein in cycloalkyl, cycloalkenyl, cycloalkylidene and cycloalkenylidene radicals one or two methylene groups may be independently substituted by O, S, CO, SO, SO 2 or NR N , or
Y represents a group according to the sub-formula
in the
D is carbonyl or sulfonyl,
R Y is hydrogen, fluorine, chlorine, cyano, trifluoromethyl or C 1-3 -alkyl,
B is a single bond, -O- or -NR N -,
R B is hydrogen, C 1-6 alkyl, C 3-6 alkenyl, C 3-6 alkynyl, C 3-10 cycloalkyl, C 5-10 cycloalkenyl, C 3-10 cycloalkyl C 1-3 alkyl, C 5-10 cycloalkenyl C 1-3 alkyl, aryl, heteroaryl, arylC 1-3 alkyl or heteroarylC 1-3 alkyl,
wherein alkyl, cycloalkyl and cycloalkenyl radicals may be partially or completely fluorinated or mono- or disubstituted by identical or different substituents selected from chlorine, cyano, hydroxy, C 1-3 alkoxy and C 1-3 alkyl, or
R B and B are joined together to form a heterocyclic ring selected from pyrrolidine, morpholine, piperidine, piperazine and 4- (C 1-4 alkyl) piperazine, wherein the heterocyclic ring is bonded to the group D via the imino group,
R N independently of one another are H or C 1-4 -alkyl,
L is independently selected from the group consisting of fluorine, chlorine, bromine, iodine, C 1-3 -alkyl, difluoromethyl, trifluoromethyl, C 1-3 -alkoxy, difluoromethoxy, trifluoromethoxy and cyano,
R 7a , R 7b , R 7c , R 7d independently of one another are selected from the group consisting of hydrogen, (C 1-18 -alkyl) carbonyl, (C 1-18 -alkyl) oxycarbonyl, arylcarbonyl and aryl- (C 1-3 alkyl) carbonyl,
wherein the aryl groups mentioned in the definition of the abovementioned radicals are to be understood as meaning phenyl or naphthyl groups which may be independently of one another monosubstituted or disubstituted by identical or different radicals L; and
the heteroaryl groups mentioned in the definition of the abovementioned radicals are pyrrolyl, furanyl, thienyl, imidazolyl, pyridyl, indolyl, benzofuranyl, benzothiophenyl, quinolinyl or isoquinolinyl groups,
or a pyrrolyl, furanyl, thienyl, imidazolyl or pyridyl group in which one or two methine groups are replaced by nitrogen atoms,
or an indolyl, benzofuranyl, benzothiophenyl, quinolinyl or isoquinolinyl group in which one to three methine groups are replaced by nitrogen atoms,
wherein the above-mentioned heteroaryl groups may be independently substituted one or two times with the same or different L groups;
wherein the N-heterocycloalkyl radical mentioned in the definition of the abovementioned radicals is to be understood as meaning a saturated carbocyclic ring which has an imino group in the ring which contains a further imino group or an O or S atom in the ring can have, and
Unless otherwise stated, the abovementioned alkyl groups may be straight-chain or branched,
their tautomers, their stereoisomers, their mixtures and their salts, in particular their physiologically tolerated salts,
wherein, the following compound (D1) is not included:
(D1) 3 - [(3-.beta.-D-glucopyranosyl-4,5-dimethoxyphenyl) methyl] -4 - [(3,4-dimethoxyphenyl) methyl] -dihydro-2 (3H) -furanone.
Die erfindungsgemäßen Verbindungen der allgemeinen Formel I und ihre physiologisch verträglichen Salze weisen wertvolle pharmakologische Eigenschaften auf, insbesondere eine Hemmwirkung auf den natriumabhängigen Glucose-Cotransporter SGLT, insbesondere SGLT2. Ferner können erfindunsgemäße Verbindungen eine Hemmwirkung auf den natriumabhängigen Glucose-Cotransporter SGLT1 aufweisen. Verglichen mit einer möglichen Hemmwirkung auf SGLT1 hemmen die erfindungsgemäßen Verbindungen vorzugsweise selektiv SGLT2.The Compounds of the invention the general formula I and their physiologically acceptable salts have valuable pharmacological properties, in particular an inhibitory effect on the sodium-dependent glucose cotransporter SGLT, especially SGLT2. Furthermore, can erfindunsgemäße connections an inhibitory effect on the sodium-dependent glucose cotransporter SGLT1 have. Compared with a possible inhibitory effect on SGLT1 inhibit the compounds of the invention preferably selective SGLT2.
Gegenstand der vorliegenden Erfindung sind auch die physiologisch verträglichen Salze der erfindungsgemäßen Verbindungen mit anorganischen oder organischen Säuren.object The present invention also includes the physiologically acceptable Salts of the compounds of the invention with inorganic or organic acids.
Die Verbindung (D1) 3-[(3,β-D-glucopyranosyl-4,5-dimethoxyphenyl)methyl]-4-[(3,4-dimethoxyphenyl)methyl]-dihydro-2(3H)-furanon (Chemical Abstracts Registry No. 106678-86-8) wird in Abe, Fumiko; Yamauchi, Tatsuo; Lignans from Trachelospermum asiaticum, Chemical & Pharmaceutical Bulletin (1986), 34 (19), 4340-5 genannt, jedoch ohne einen Zusammenhang mit einer inhibierenden Wirkung auf SGLT aufzuzeigen.The Compound (D1) 3 - [(3, β-D-glucopyranosyl-4,5-dimethoxyphenyl) methyl] -4 - [(3,4-dimethoxyphenyl) methyl] dihydro-2 (3H) -furanone (Chemical Abstracts Registry No. 106678-86-8) is in Abe, Fumiko; Yamauchi, Tatsuo; Lignans from Trachelospermum asiaticum, Chemical & Pharmaceutical Bulletin (1986), 34 (19), 4340-5, but without a link with an inhibitory effect on SGLT.
Daher ist die Verwendung der erfindungsgemäßen Verbindungen, einschließlich der physiologisch verträglichen Salze, einschließlich der vorstehend explizit ausgeschlossenen Verbindung (D1) oder eines seiner physiologisch verträglichen Salze, als Arzneimittel ebenfalls ein Gegenstand dieser Erfindung.Therefore is the use of the compounds of the invention, including physiologically compatible Salts, including the above explicitly excluded compound (D1) or a its physiologically tolerable Salts, as a medicament also an object of this invention.
Ein weiterer Gegenstand dieser Erfindung sind Arzneimittel, enthaltend mindestens eine erfindungsgemäße Verbindung oder ein erfindungsgemäßes physiologisch verträgliches Salz, einschließlich der vorstehend explizit ausgeschlossenen Verbindung (D1) oder eines seiner physiologisch verträglichen Salze, neben gegebenenfalls einem oder mehreren inerten Trägerstoffen und/oder Verdünnungsmitteln.Another object of this invention are pharmaceutical compositions containing at least one compound of the invention or a physiologically acceptable salt according to the invention, including the vorste explicitly excluded compound (D1) or one of its physiologically acceptable salts, in addition to optionally one or more inert carriers and / or diluents.
Ebenfalls ein Gegenstand dieser Erfindung ist die Verwendung mindestens einer erfindungsgemäßen Verbindung oder eines physiologisch verträglichen Salzes solch einer Verbindung, einschließlich der vorstehend explizit ausgeschlossenen Verbindung (D1) oder eines seiner physiologisch verträglichen Salze, zur Herstellung eines Arzneimittels, das zur Behandlung oder Prophylaxe von Erkrankungen oder Zuständen geeignet ist, die durch Inhibierung des natriumabhängigen Glucose-Cotransporters SGLT, insbesondere SGLT2 beeinflussbar sind.Also An object of this invention is the use of at least one compound of the invention or a physiologically acceptable one Salt of such a compound, including the above explicitly excluded compound (D1) or one of its physiological acceptable Salts for the manufacture of a medicament for the treatment or Prophylaxis of diseases or conditions suitable by Inhibition of the sodium-dependent Glucose cotransporter SGLT, in particular SGLT2 can be influenced.
Ein weiterer Gegenstand dieser Erfindung ist die Verwendung mindestens einer erfindungsgemäßen Verbindung oder eines seiner physiologisch verträglichen Salze, einschließlich der vorstehend explizit ausgeschlossenen Verbindung (D1) oder eines seiner physiologisch verträglichen Salze, zur Herstellung eines Arzneimittels, das zur Behandlung von Stoffwechselerkrankungen geeignet ist.One Another object of this invention is the use of at least a compound of the invention or one of its physiologically acceptable salts, including the explicitly excluded compound (D1) or a its physiologically tolerable Salts for the manufacture of a medicament for the treatment of Metabolic disorders is suitable.
Ein weiterer Gegenstand dieser Erfindung ist die Verwendung mindestens einer erfindungsgemäßen Verbindung oder eines seiner physiologisch verträglichen Salze, einschließlich der vorstehend explizit ausgeschlossenen Verbindung (D1) oder eines seiner physiologisch verträglichen Salze, zur Herstellung eines Arzneimittels zur Inhibition des natriumabhängigen Glucose-Cotransporters SGLT, insbesondere SGLT2.One Another object of this invention is the use of at least a compound of the invention or one of its physiologically acceptable salts, including the explicitly excluded compound (D1) or a its physiologically tolerable Salts, for the manufacture of a medicament for inhibiting the sodium-dependent glucose cotransporter SGLT, especially SGLT2.
Ferner ist ein Verfahren zur Herstellung eines erfindungsgemäßen Arzneimittels Gegenstand dieser Erfindung, dadurch gekennzeichnet, dass auf nicht-chemischem Wege eine erfindungsgemäße Verbindung oder eines seiner physiologisch verträglichen Salze, einschließlich der vorstehend explizit ausgeschlossenen Verbindung (D1) oder eines seiner physiologisch verträglichen Salze, in einen oder mehrere inerte Trägerstoffe und/oder Verdünnungsmittel eingearbeitet wird.Further is a process for the preparation of a medicament according to the invention Subject of this invention, characterized in that on non-chemical Ways a compound of the invention or one of its physiologically compatible Salts, including the above explicitly excluded compound (D1) or a its physiologically tolerable Salts, in one or more inert carriers and / or diluents is incorporated.
Gegenstand der vorliegenden Erfindung ist auch ein Verfahren zur Herstellung der erfindungsgemäßen Verbindungen der allgemeinen Formel I, dadurch gekennzeichnet, dass
- a) zur Herstellung von Verbindungen der allgemeinen Formel I, die wie vor- und nachstehend definiert ist, eine Verbindung der allgemeinen Formel II in der R' H, C1-4-Alkyl, (C1-18-Alkyl)carbonyl, (C1-18-Alkyl)oxycarbonyl, Arylcarbonyl oder Aryl-(C1-3-alkyl)-carbonyl bedeutet, worin die Alkyl- oder Arylgruppen ein- oder mehrfach mit Halogen substituiert sein können; R8a, R8b, R8c, R8d unabhängig voneinander eine zuvor und nachstehend für die Reste R7a, R7b, R7c, R7d angegebenen Bedeutungen aufweisen oder eine RaRbRcSi-Gruppe oder eine Ketal- oder Acetalgruppe bedeuten, wobei jeweils zwei benachbarte Reste R8a, R8b, R8c, R8d eine cyclische Ketal- oder Acetalgruppe bilden können, und wobei Alkyl- und/oder Arylgruppen ein- oder mehrfach halogeniert sein können; und Ra, Rb, Rc unabhängig voneinander C1-4-Alkyl, Aryl oder Aryl-C1-3-alkyl bedeuten, worin die Aryl- oder Alkylgruppen ein- oder mehrfach mit Halogen substituiert sein können; wobei unter den bei der Definition der vorstehend genannten Reste erwähnten Arylgruppen Phenyl- oder Naphthylgruppen, vorzugsweise Phenylgruppen zu verstehen sind; und in der die Reste R1 bis R6 und die Brücke Z sowie der Cyclus Cy wie vor- und nachstehend definiert sind; mit einem Reduktionsmittel in Gegenwart einer Säure umgesetzt wird, wobei die eventuell vorhandenen Schutzgruppen gleichzeitig oder nachträglich abgespalten werden; oder
- b) zur Herstellung von Verbindungen der allgemeinen Formel I, in der R7a, R7b, R7c und R7d Wasserstoff bedeuten, in einer Verbindung der allgemeinen Formel III in der Z, Cy, R8a, R8b, R8c, R8d sowie R1 bis R6 wie zuvor und nachstehend definiert sind, wobei mindestens einer der Reste R8a, R8b, R8c und R8d nicht Wasserstoff bedeutet, die nicht Wasserstoff bedeutenden Reste R8a, R8b, R8c bzw. R8d entfernt werden, insbesondere hydrolysiert werden; und erforderlichenfalls ein bei den vorstehend beschriebenen Umsetzungen gemäß Verfahren a) oder b) verwendeter Schutzrest wieder abgespalten wird und/oder gewünschtenfalls eine so erhaltene Verbindung der allgemeinen Formel I selektiv an einer Hydroxygruppe derivatisiert oder diese substituiert wird und/oder gewünschtenfalls eine so erhaltene Verbindung der allgemeinen Formel I in ihre Stereoisomere aufgetrennt wird und/oder gewünschtenfalls eine so erhaltene Verbindung der allgemeinen Formel I in ihre Salze, insbesondere für die pharmazeutische Anwendung in ihre physiologisch verträglichen Salze, überführt wird.
- a) for the preparation of compounds of general formula I, which is as defined above and below, a compound of general formula II wherein R 'is H, C 1-4 alkyl, (C 1-18 alkyl) carbonyl, (C 1-18 alkyl) oxycarbonyl, arylcarbonyl or aryl- (C 1-3 alkyl) carbonyl, wherein the alkyl or aryl groups may be mono- or polysubstituted by halogen; R 8a , R 8b , R 8c , R 8d independently of one another have meanings given previously and below for the radicals R 7a , R 7b , R 7c , R 7d or a R a R b R c Si group or a ketal or Each of two adjacent radicals R 8a , R 8b , R 8c , R 8d can form a cyclic ketal or acetal group, and wherein alkyl and / or aryl groups may be mono- or polyhalogenated; and R a , R b , R c independently of one another are C 1-4 -alkyl, aryl or arylC 1-3 -alkyl, in which the aryl or alkyl groups may be mono- or polysubstituted by halogen; wherein the aryl groups mentioned in the definition of the abovementioned radicals are phenyl or naphthyl groups, preferably phenyl groups; and in which the radicals R 1 to R 6 and the bridge Z and the cycle Cy are as defined above and below; is reacted with a reducing agent in the presence of an acid, wherein the protective groups are optionally cleaved simultaneously or subsequently; or
- b) for the preparation of compounds of general formula I in which R 7a , R 7b , R 7c and R 7d are hydrogen, in a compound of general formula III in which Z, Cy, R 8a , R 8b , R 8c , R 8d and R 1 to R 6 are as defined above and below, where at least one of the radicals R 8a , R 8b , R 8c and R 8d is not hydrogen, the radicals R 8a , R 8b , R 8c or R 8d which are not hydrogen-significant are removed, in particular hydrolyzed; and, if necessary, a protective moiety used in the reactions described above according to process a) or b) is cleaved off again and / or, if desired, a compound of general formula I thus obtained is selectively derivatized or substituted on a hydroxy group and / or, if desired, a compound of this type general formula I is separated into its stereoisomers and / or, if desired, a compound of the general formula I thus obtained in its salts, in particular for the pharmaceutical application into their physiologically acceptable salts, is transferred.
Detailierte Beschreibung der ErfindungDetailed description the invention
Sofern nicht anders angegeben besitzen die Gruppen, Reste und Substituenten, insbesondere R1 bis R6, Y, Z, Cy, L, RN, R7a, R7b, R7c, R7d, RY, D, B, RB, die zuvor und nachfolgend angegebenen Bedeutungen.Unless otherwise stated, the groups, radicals and substituents, in particular R 1 to R 6 , Y, Z, Cy, L, R N , R 7a , R 7b , R 7c , R 7d , R Y , D, B, R have B , the meanings given above and below.
Kommen Reste, Substituenten oder Gruppen in einer Verbindung mehrfach vor, so können diese eine gleiche oder verschiedene Bedeutungen aufweisen.Come Residues, substituents or groups in a compound several times, so can these have the same or different meanings.
Die vorstehend und nachfolgend verwendete, beispielsweise in den Gruppen Y, R1 und R3 vorkommende Bezeichnung Aryl bedeutet vorzugsweise Phenyl. Gemäß der allgemeinen Definition und sofern nichts anderes angegeben ist, kann die Aryl-Gruppe, insbesondere die Phenylgruppe, ein- oder zweifach mit gleichen oder verschiedenen Resten L substituiert sein.The term aryl used above and below, for example in the groups Y, R 1 and R 3 , preferably denotes phenyl. In accordance with the general definition and unless stated otherwise, the aryl group, in particular the phenyl group, may be monosubstituted or disubstituted by identical or different radicals L.
Die vorstehend und nachfolgend verwendete, beispielsweise in den Gruppen Y, R1 und R3 vorkommende Bezeichnung Heteroaryl bedeutet vorzugsweise Pyridinyl, Pyrimidinyl, Pyridazinyl, Pyrazinyl, Triazinyl, Imidazolyl, Pyrazolyl, Triazolyl, Tetrazolyl, Oxazolyl, Oxadiazolyl, Thiazolyl oder Thiadiazolyl. Gemäß der allgemeinen Definition und sofern nichts anderes angegeben ist, kann die Heteroaryl-Gruppe ein- oder zweifach mit gleichen oder verschiedenen Resten L substituiert sein.The term heteroaryl used above and below, for example in the groups Y, R 1 and R 3 , preferably denotes pyridinyl, pyrimidinyl, pyridazinyl, pyrazinyl, triazinyl, imidazolyl, pyrazolyl, triazolyl, tetrazolyl, oxazolyl, oxadiazolyl, thiazolyl or thiadiazolyl. In accordance with the general definition and unless stated otherwise, the heteroaryl group may be monosubstituted or disubstituted by identical or different radicals L.
Bevorzugte Bedeutungen des Cyclus Cy sind Cyclopentan, Cyclohexan, Pyrrolidin, Piperidin, Piperazin, Morpholin, Tetrahydrofuran, Tetrahydropyran, 1,3-Dioxan, 1,4-Dioxan, Tetrahydrothiophen, Dithiolan und 1,3-Dithian, in denen eine Methylengruppe durch CO ersetzt sein kann, und die wie zuvor angegeben mit R3, R4, R5 und R6 substituiert sind, und in denen ein oder mehrere an Kohlenstoff gebundene H-Atome durch Fluor ersetzt sein können.Preferred meanings of the Cy cycle are cyclopentane, cyclohexane, pyrrolidine, piperidine, piperazine, morpholine, tetrahydrofuran, tetrahydropyran, 1,3-dioxane, 1,4-dioxane, tetrahydrothiophene, dithiolane and 1,3-dithiane in which a methylene group is replaced by CO may be substituted, and which are substituted as previously indicated with R 3 , R 4 , R 5 and R 6 , and in which one or more carbon-bonded H atoms may be replaced by fluorine.
Ist in den zuvor angegebenen cyclischen Gruppen eine Methylengruppe durch CO ersetzt, so sind hiervon bevorzugte Bedeutungen der Gruppe Cy ausgewählt aus Tetrahydrofuranon, Tetrahydropyranon, Piperidinon, Piperazinon und Morpholinon.is in the previously given cyclic groups, a methylene group replaced by CO, so are preferred meanings of the group Cy selected from tetrahydrofuranone, tetrahydropyranone, piperidinone, piperazinone and morpholinone.
Des weiteren kann in den zuvor für Cy als bevorzugt angegebenen Gruppen jeweils eine Doppelbindung vorliegen. Bevorzugte Bedeutungen solcher einfach ungesättigter Cyclen Cy sind Cyclopenten und Cyclohexen. Für den Fall, dass Substituenten R3, R4, R5 und/oder R6 miteinander verbunden sind, kann diese Doppelbindung auch Bestandteil eines anellierten cyclischen Systems sein.Furthermore, in each case one double bond may be present in the groups previously indicated as being preferred for Cy. Preferred meanings of such monounsaturated Cy are cyclopentene and cyclohexene. In the event that substituents R 3 , R 4 , R 5 and / or R 6 are bonded together, this double bond may also be part of a fused cyclic system.
Besonders bevorzugte Bedeutungen des Cyclus Cy sind Cyclopentan, Cyclohexan, Pyrrolidin, Piperidin, Piperazin, Tertrahydrofuran und 1,3-Dioxan, die wie zuvor angegeben mit R3, R4, R5 und R6 substituiert sind, und in denen ein oder mehrere an Kohlenstoff gebundene H-Atome durch Fluor ersetzt sein können.Particularly preferred meanings of the Cy cycle are cyclopentane, cyclohexane, pyrrolidine, piperidine, piperazine, tetrahydrofuran and 1,3-dioxane, which are substituted as previously indicated by R 3 , R 4 , R 5 and R 6 , and in which one or more carbon atoms bound to carbon may be replaced by fluorine.
Entsprechend der Anzahl der Ringatome des Cyclus Cy können die erfindungsgemäßen Verbindungen der Formel I in zwei Ausführungsformen gegliedert werden.Corresponding the number of ring atoms of the Cy cycle can be the compounds of the invention of the formula I in two embodiments be articulated.
Gemäß einer
ersten Ausführungsform
sind diejenigen erfindungsgemäßen Verbindungen
der Formel I bevorzugt, in denen die Gruppe Cy einen 6-gliedrigen
gesättigten
oder einfach ungesättigten
Carbocyclus bedeutet, der im Ring ein, zwei oder drei, vorzugsweise
ein oder zwei Heteroatome unabhängig
voneinander ausgewählt
aus N, O und S aufweisen kann, und
der mit R4,
R5 und R6 über eine
Einfachbindung und mit R3 über eine
Einfach- oder eine Doppelbindung substituiert ist, und
in dem
eine Methylengruppe durch CO oder eine Sulfanylgruppe durch SO oder
SO2 ersetzt sein kann, und
in dem ein
oder mehrere an Kohlenstoff gebundene H-Atome durch Fluor ersetzt
sein können,
und
in denen die übrigen
Substituenten und Gruppen die zuvor und nachfolgend angegebenen
Bedeutungen aufweisen.According to a first embodiment, those compounds of the formula I according to the invention are preferred in which the group Cy is a 6-membered saturated or monounsaturated carbocycle having in the ring one, two or three, preferably one or two heteroatoms independently selected from N, O. and S, and
which is substituted with R 4 , R 5 and R 6 via a single bond and with R 3 via a single or a double bond, and
in which a methylene group may be replaced by CO or a sulfanyl group by SO or SO 2 , and
in which one or more carbon-bonded hydrogen atoms may be replaced by fluorine, and
in which the other substituents and groups have the meanings given above and below.
Gemäß dieser Ausführungsform bevorzugte Cyclen Cy sind Cyclohexan, Piperidin, Piperazin, Morpholin, Tetrahydropyran, 1,3-Dioxan, 1,4-Dioxan und 1,3-Dithian, in denen eine Methylengruppe durch CO ersetzt sein kann, und die wie zuvor angegeben mit R3, R4, R5 und R6 substituiert sind, und in denen ein oder mehrere an Kohlenstoff gebundene H-Atome durch Fluor ersetzt sein können.Cyclones Cy preferred according to this embodiment are cyclohexane, piperidine, piperazine, morpholine, tetrahydropyran, 1,3-dioxane, 1,4-dioxane and 1,3-dithiane, in which a methylene group may be replaced by CO, and which are as indicated above with R 3 , R 4 , R 5 and R 6 are substituted, and in which one or more carbon-bonded H atoms may be replaced by fluorine.
Ist in den zuvor angegebenen cyclischen Gruppen eine Methylengruppe durch CO ersetzt, so sind hiervon bevorzugte Bedeutungen der Gruppe Cy ausgewählt aus Tetrahydropyranon, Piperidinon, Piperazinon und Morpholinon.is in the previously given cyclic groups, a methylene group replaced by CO, so are preferred meanings of the group Cy selected from tetrahydropyranone, piperidinone, piperazinone and morpholinone.
Des weiteren kann in den zuvor für Cy als bevorzugt angegebenen Gruppen jeweils eine Doppelbindung vorliegen. Eine bevorzugte Bedeutung solcher einfach ungesättigter Cyclen Cy ist Cyclohexen. Für den Fall, dass Substituenten R3, R4, R5 und/oder R6 miteinander verbunden sind, kann diese Doppelbindung auch Bestandteil eines anellierten cyclischen Systems sein.Furthermore, in each case one double bond may be present in the groups previously indicated as being preferred for Cy. A preferred meaning of such monounsaturated Cy cycles is cyclohexene. In the event that substituents R 3 , R 4 , R 5 and / or R 6 are bonded together, this double bond may also be part of a fused cyclic system.
Besonders bevorzugte Cy sind hierbei Cyclohexan, Cyclohexen, Piperidin, Piperazin und 1,3-Dioxan, die wie zuvor angegeben mit R3, R4, R5 und R6 substituiert sind, und in denen ein oder mehrere an Kohlenstoff gebundene H-Atome durch Fluor ersetzt sein können.Particularly preferred Cy are here cyclohexane, cyclohexene, piperidine, piperazine and 1,3-dioxane, which are substituted as previously indicated with R 3 , R 4 , R 5 and R 6 , and in which one or more carbon atoms bonded to carbon atoms may be replaced by fluorine.
Gemäß einer
zweiten Ausführungsform
sind diejenigen erfindungsgemäßen Verbindungen
der Formel I bevorzugt, in denen die Gruppe Cy einen 5-gliedrigen
gesättigten
oder einfach ungesättigten
Carbocyclus bedeutet, der im Ring ein, zwei oder drei, vorzugsweise
ein oder zwei Heteroatome unabhängig
voneinander ausgewählt
aus N, O und S aufweisen kann, und
der mit R4,
R5 und R6 über eine
Einfachbindung und mit R3 über eine
Einfach- oder eine Doppelbindung substituiert ist, und
in dem
eine Methylengruppe durch CO oder eine Sulfanylgruppe durch SO oder
SO2 ersetzt sein kann, und
in dem ein
oder mehrere an Kohlenstoff gebundene H-Atome durch Fluor ersetzt
sein können,
und
in denen die übrigen
Substituenten und Gruppen die zuvor und nachfolgend angegebenen
Bedeutungen aufweisen.According to a second embodiment, those compounds of the formula I according to the invention are preferred in which the group Cy is a 5-membered saturated or monounsaturated carbocycle having in the ring one, two or three, preferably one or two heteroatoms independently selected from N, O and S, and
which is substituted with R 4 , R 5 and R 6 via a single bond and with R 3 via a single or a double bond, and
in which a methylene group may be replaced by CO or a sulfanyl group by SO or SO 2 , and
in which one or more carbon-bonded hydrogen atoms may be replaced by fluorine, and
in which the other substituents and groups have the meanings given above and below.
Gemäß dieser Ausführungsform bevorzugte Cyclen Cy sind Cyclopentan, Pyrrolidin, Tetrahydrofuran, Dithiolan und Tetrahydrothiophen, in denen eine Methylengruppe durch CO ersetzt sein kann, und die wie zuvor angegeben mit R3, R4, R5 und R6 substituiert sind, und in denen ein oder mehrere an Kohlenstoff gebundene H-Atome durch Fluor ersetzt sein können.According to this embodiment, preferred Cy's are cyclopentane, pyrrolidine, tetrahydrofuran, dithiolane and tetrahydrothiophene, in which a methylene group may be replaced by CO and which are substituted with R 3 , R 4 , R 5 and R 6 as indicated above, and in which one or more carbon atoms bound to carbon may be replaced by fluorine.
Ist in den zuvor angegebenen cyclischen Gruppen eine Methylengruppe durch CO ersetzt, so ist eine bevorzugte Bedeutung der Gruppe Cy Tetrahydrofuranon.is in the previously given cyclic groups, a methylene group replaced by CO, a preferred meaning of the group Cy Tetrahydrofuranone.
Des weiteren kann in den zuvor für Cy als bevorzugt angegebenen Gruppen jeweils eine Doppelbindung vorliegen. Eine bevorzugte Bedeutung solcher einfach ungesättigter Cyclen Cy ist Cyclopenten. Für den Fall, dass Substituenten R3, R4, R5 und/oder R6 miteinander verbunden sind, kann diese Doppelbindung auch Bestandteil eines anellierten cyclischen Systems sein.Furthermore, in each case one double bond may be present in the groups previously indicated as being preferred for Cy. A preferred meaning of such monounsaturated Cy cycles is cyclopentene. In the event that substituents R 3 , R 4 , R 5 and / or R 6 are bonded together, this double bond may also be part of a fused cyclic system.
Besonders bevorzugte Cy sind hierbei Cyclopentan, Pyrrolidin und Tetrahydrofuran, die wie zuvor angegeben mit R3, R4, R5 und R6 substituiert sind, und in denen ein oder mehrere an Kohlenstoff gebundene H-Atome durch Fluor ersetzt sein können.Particularly preferred Cy here are cyclopentane, pyrrolidine and tetrahydrofuran, which are substituted as previously indicated with R 3 , R 4 , R 5 and R 6 , and in which one or more carbon-bonded hydrogen atoms may be replaced by fluorine.
Für den Fall, dass Cy einen 6-gliedrigen Cyclus bedeutet, steht der Rest R3 vorzugsweise in 3- oder 4-Position zur Brücke Z, besonders bevorzugt in 4-Position zur Brücke Z.In the event that Cy is a 6-membered cycle, the radical R 3 is preferably in the 3- or 4-position to the bridge Z, more preferably in the 4-position to the bridge Z.
Für den Fall, dass Cy einen 5-gliedrigen Cyclus bedeutet, steht der Rest R3 vorzugsweise in 3-Position zur Brücke Z.In the event that Cy represents a 5-membered cycle, the radical R 3 is preferably in the 3-position to the bridge Z.
Daher
lassen sich bevorzugte Verbindungen gemäß der ersten Ausführungsform,
in der Cy einen 6-gliedrigen Cyclus bedeutet, durch die Formeln
I.1 und I.1' beschreiben: in denen
V1,
V2 unabhängig
voneinander C oder N bedeuten,
U1, U2, U3, U4 unabhängig voneinander
C, N, O, CO oder SO2 bedeuten,
mit
der Maßgabe,
dass in dem durch U und V gebildeten Ring maximal 2 Heteroatome
ausgewählt
aus N und O vorhanden sind, wobei diese Heteroatome nicht unmittelbar
miteinander verbunden sind, und maximal eine Gruppe ausgewählt aus
CO und SO2 vorhanden ist, und verbleibende
freie chemische Bindungen an C- und N-Atomen
mit Wasserstoff abgesättigt
sind; und
in denen die übrigen
Gruppen und Substituenten eine der zuvor oder nachfolgend angegebenen
Bedeutungen aufweisen.Therefore, preferred compounds according to the first embodiment, in which Cy is a 6-membered cycle, are described by the formulas I.1 and I.1 ': in which
V1, V2 independently of one another denote C or N,
U1, U2, U3, U4 independently of one another denote C, N, O, CO or SO 2 ,
with the proviso that in the ring formed by U and V at most 2 heteroatoms selected from N and O are present, these heteroatoms are not directly connected to each other, and at most one group selected from CO and SO 2 is present, and remaining free chemical Bonds to C and N atoms are saturated with hydrogen; and
in which the remaining groups and substituents have one of the meanings given above or below.
Ferner
lassen sich bevorzugte Verbindungen gemäß der zweiten Ausführungsform,
in der Cy einen 5-gliedrigen Cyclus bedeutet, durch die Formel I.2
beschreiben: in denen
V1,
V2 unabhängig
voneinander C oder N bedeuten,
U1, U2, U3 unabhängig voneinander
C, N, O, CO oder SO2 bedeuten,
mit
der Maßgabe,
dass in dem durch U und V gebildeten Ring maximal 2 Heteroatome
ausgewählt
aus N und O vorhanden sind, wobei diese Heteroatome nicht unmittelbar
miteinander verbunden sind, und maximal eine Gruppe ausgewählt aus
CO und SO2 vorhanden ist, und verbleibende
freie chemische Bindungen an C- und N-Atomen
mit Wasserstoff abgesättigt
sind; und
in denen die übrigen
Gruppen und Substituenten eine der zuvor oder nachfolgend angegebenen
Bedeutungen aufweisen.Furthermore, preferred compounds according to the second embodiment, in which Cy is a 5-membered cycle, can be described by the formula I.2: in which
V1, V2 independently of one another denote C or N,
U1, U2, U3 independently of one another denote C, N, O, CO or SO 2 ,
with the proviso that in the ring formed by U and V at most 2 heteroatoms selected from N and O are present, these heteroatoms are not directly connected to each other, and at most one group selected from CO and SO 2 is present, and remaining free chemical Bonds to C and N atoms are saturated with hydrogen; and
in which the remaining groups and substituents have one of the meanings given above or below.
Nachfolgend
werden bevorzugte Bedeutungen der übrigen Gruppen und Substituenten
in den erfindungsgemäßen Verbindungen
der allgemeinen Formel I, insbesondere der Formeln I.1, I.1' und I.2, angegeben:
Bevorzugt
bedeutet R1 Wasserstoff, Fluor, Chlor, Brom,
Iod, C1-6-Alkyl, C2-6-Alkinyl,
C2-6-Alkenyl, C3-10-Cycloalkyl,
C3-10-Cycloalkenyl, C1-4-Alkylcarbonyl,
Aminocarbonyl, C1-4-Alkylaminocarbonyl,
Di-(C1-3-Alkyl)aminocarbonyl, C1-4-Alkoxycarbonyl,
C1-4-Alkylamino,
Di-(C1-3-alkyl)amino, Pyrrolidin-1-yl, Piperidin-1-yl,
Morpholin-4-yl, C1-4-Alkylcarbonylamino, C1-6-Alkyloxy,
C3-10-Cycloalkyloxy, C5-10-Cycloalkenyloxy,
C1-4-Alkylsulfanyl,
C1-4-Alkylsulfonyl, C3-10-Cycloalkylsulfanyl,
C3-10-Cycloalkylsulfonyl, C3-10-Cycloalkenylsulfanyl,
C5-10-Cycloalkenylsulfonyl, Hydroxy und
Cyan,
wobei Alkyl-, Alkenyl-, Alkinyl-, Cycloalkyl- und Cycloalkenyl-Reste
teilweise oder vollständig
fluoriert oder ein- oder zweifach mit gleichen oder verschiedenen
Substituenten ausgewählt
aus Chlor, Hydroxy, C1-3-Alkoxy und C1-3-Alkyl substituiert sein können, und
wobei
in Cycloalkyl- und Cycloalkenyl-Resten ein oder zwei Methylengruppen
unabhängig
voneinander durch O, S, CO, SO oder SO2 substituiert
sein können,
und
wobei in N-Heterocycloalkyl-Resten eine Methylengruppe
durch CO oder SO2 substituiert sein kann.The following are preferred meanings of the other groups and substituents in the compounds of the general formula I, in particular the formulas I.1, I.1 'and I.2, given:
R 1 is preferably hydrogen, fluorine, chlorine, bromine, iodine, C 1-6 -alkyl, C 2-6 -alkynyl, C 2-6 -alkenyl, C 3-10 -cycloalkyl, C 3-10 -cycloalkenyl, C 1-4 alkylcarbonyl, aminocarbonyl, C 1-4 -alkylaminocarbonyl, di- (C 1-3 alkyl) aminocarbonyl, C 1-4 alkoxycarbonyl, C 1-4 alkylamino, di- (C 1-3 alkyl ) amino, pyrrolidin-1-yl, piperidin-1-yl, morpholin-4-yl, C 1-4 -alkylcarbonylamino, C 1-6 -alkyloxy, C 3-10 -cycloalkyloxy, C 5-10 -cycloalkenyloxy, C 1-4 alkylsulfanyl, C 1-4 alkylsulfonyl, C 3-10 cycloalkylsulfanyl, C 3-10 cycloalkylsulfonyl, C 3-10 cycloalkenylsulfanyl, C 5-10 cycloalkenylsulfonyl, hydroxy and cyano,
wherein alkyl, alkenyl, alkynyl, cycloalkyl and cycloalkenyl radicals are partially or completely fluorinated or mono- or disubstituted by identical or different substituents selected from chlorine, hydroxy, C 1-3 alkoxy and C 1-3 alkyl substituted can be, and
wherein in cycloalkyl and cycloalkenyl radicals one or two methylene groups can be substituted independently of one another by O, S, CO, SO or SO 2 , and
where in N-heterocycloalkyl radicals a methylene group may be substituted by CO or SO 2 .
Bedeutet die Gruppe R1 einen Cycloalkyl- oder Cycloalkenyl-Rest, in dem ein oder zwei Methylengruppen unabhängig voneinander durch O, S, CO, SO oder SO2 substituiert sind, so sind bevorzugte Bedeutungen des Rests R1 ausgewählt aus der Gruppe bestehend aus Tetrahydrofuranyl, Tetrahydrofuranonyl, Tetrahydrothienyl, Tetrahydropyranyl, Tetrahydropyranonyl, Dioxanyl und Trioxanyl.If the group R 1 is a cycloalkyl or cycloalkenyl radical in which one or two methylene groups are independently of each other substituted by O, S, CO, SO or SO 2 , preferred meanings of the radical R 1 are selected from the group consisting of tetrahydrofuranyl , Tetrahydrofuranonyl, tetrahydrothienyl, tetrahydropyranyl, tetrahydropyranonyl, dioxanyl and trioxanyl.
Bedeutet die Gruppe R1 einen N-Heterocycloalkyl-Rest, in dem eine Methylengruppe durch CO oder SO2 substituiert ist, so sind bevorzugte Bedeutungen des Rests R1 ausgewählt aus der Gruppe bestehend aus Pyrrolidinon, Piperidinon, Piperazinon und Morpholinon.If the group R 1 is an N-heterocycloalkyl radical in which a methylene group is substituted by CO or SO 2 , preferred meanings of the radical R 1 are selected from the group consisting of pyrrolidinone, piperidinone, piperazinone and morpholinone.
Besonders bevorzugt bedeutet R1 Wasserstoff, Fluor, Chlor, Brom, Iod, C1-6-Alkyl, C2-6-Alkinyl, C2-6-Alkenyl, C3-10-Cycloalkyl, C5-10-Cycloalkenyl, C1-6-Alkyloxy, C3-10-Cycloalkyloxy oder Cyan, wobei in Cycloalkyl- und Cycloalkenylgruppen ein oder zwei Methyleneinheiten unabhängig voneinander durch O oder CO ersetzt und Alkyl-, Alkenyl- und Alkinyl-Reste teilweise oder vollständig fluoriert sein können.R 1 particularly preferably denotes hydrogen, fluorine, chlorine, bromine, iodine, C 1-6 -alkyl, C 2-6 -alkynyl, C 2-6 -alkenyl, C 3-10 -cycloalkyl, C 5-10 -cycloalkenyl, C 1-6 alkyloxy, C 3-10 cycloalkyloxy or cyano, wherein in cycloalkyl and cycloalkenyl groups one or two methylene units independently of one another can be replaced by O or CO and alkyl, alkenyl and alkynyl radicals can be partially or completely fluorinated.
Beispiele der ganz besonders bevorzugten R1 sind Wasserstoff, Fluor, Chlor, Brom, Methyl, Ethyl, Isopropyl, Trifluormethyl, Ethinyl, Methoxy, Cyclopentyloxy und Cyan.Examples of the most preferred R 1 are hydrogen, fluorine, chlorine, bromine, methyl, ethyl, isopropyl, trifluoromethyl, ethynyl, methoxy, cyclopentyloxy and cyano.
Bevorzugte Bedeutungen des Rests R2 sind Wasserstoff, Fluor, Chlor, Brom, Methyl, Hydroxy, Methoxy, Ethoxy, Trifluormethoxy, Cyan, Nitro und durch 1 bis 3 Fluoratome substituiertes Methyl.Preferred meanings of the radical R 2 are hydrogen, fluorine, chlorine, bromine, methyl, hydroxyl, methoxy, ethoxy, trifluoromethoxy, cyano, nitro and methyl substituted by 1 to 3 fluorine atoms.
Besonders bevorzugte Bedeutungen des Rests R2 sind Wasserstoff, Fluor, Hydroxy, Methoxy, Ethoxy und Methyl, insbesondere Wasserstoff und Methyl.Particularly preferred meanings of the radical R 2 are hydrogen, fluorine, hydroxyl, methoxy, ethoxy and methyl, in particular hydrogen and methyl.
Für den Fall, dass R1 und R2 an zwei miteinander benachbarte C-Atome des Phenylrings gebunden sind, können R1 und R2 derart miteinander verbunden sein, dass R1 und R2 zusammen vorzugsweise eine C3-4-Alkylen- oder Butadienylen-Brücke bilden, in der ein oder zwei Methyleneinheiten unabhängig voneinander durch O, NRN oder CO ersetzt sein können, und in der im Falle einer Butadienylen-Brücke eine Methingruppe durch ein N-Atom ersetzt sein kann. Bevorzugt bilden hierbei die miteinander verbundenen Reste R1 und R2 zusammen mit dem Phenylring, mit dem diese verbunden sind, ein bicyclisches Ringsystem ausgewählt aus Indan, Dihydroindol, Dihydrobenzofuran, Tetrahydrochinolin, Dihydrochinolinon, Tetrahydroisochinolin, Dihydroisochinolinon, Tetrahydronaphthalin, Naphthalin, Chinolin oder Isochinolin.In the event that R 1 and R 2 are bonded to two adjacent C atoms of the phenyl ring, R 1 and R 2 may be linked together such that R 1 and R 2 together preferably a C 3-4 alkylene or Butadienylene bridge in which one or two methylene units may be replaced independently of one another by O, NR N or CO, and in which in the case of a butadienylene bridge a methine group may be replaced by an N atom. Preferably, the interconnected radicals R 1 and R 2 together with the phenyl ring to which they are attached form a bicyclic ring system selected from indane, dihydroindole, dihydrobenzofuran, tetrahydroquinoline, dihydroquinolinone, tetrahydroisoquinoline, dihydroisoquinolinone, tetrahydronaphthalene, naphthalene, quinoline or isoquinoline.
Der Substituent R3 weist die eingangs aufgeführten Bedeutungen auf. Für den Fall, dass R3 an ein N-Atom gebunden ist, bedeutet R3 vorzugsweise nicht Halogen oder Alkyl-, Cycloalkyl-, Cycloalkenyl- oder Arylsulfanyl.The substituent R 3 has the meanings listed above. In the event that R 3 is bonded to an N atom, R 3 is preferably not halogen or alkyl, cycloalkyl, cycloalkenyl or arylsulfanyl.
Ist
der Rest R3 über eine Einfachbindung an
Cy gebunden, so bedeutet R3 vorzugsweise
Wasserstoff, Fluor, Chlor, C1-6-Alkyl, C2-6-Alkinyl, C2-6-Alkenyl,
C3-10-Cycloalkyl,
C3-10-Cycloalkyl-methyl, C5-10-Cycloalkenyl, C3-10-Cycloalkenyl-methyl, Aryl, Heteroaryl,
C1-4-Alkylcarbonyl, Aminocarbonyl, C1-4-Alkylaminocarbonyl, Di-(C1-3-Alkyl)aminocarbonyl,
C1-4-Alkoxycarbonyl, Di-(C1-3-alkyl)amino,
Pyrrolidin-1-yl, Piperidin-1-yl, Morpholin-4-yl, C1-4-Alkylcarbonylamino,
C1_6-Alkoxy, C3-10-Cycloalkyloxy, C5-10-Cycloalkenyloxy,
Aryloxy, Heteroaryloxy, C1-4-Alkylsulfanyl,
C1-4-Alkylsulfonyl,
C3-10-Cycloalkylsulfanyl, C3-10-Cycloalkylsulfonyl,
C5-10-Cycloalkenylsulfanyl, C5-10-Cycloalkenylsulfonyl,
Hydroxy und Cyan, und
für
den Fall, dass R3 an ein N-Atom gebunden
ist, bedeutet R3 vorzugsweise Wasserstoff,
Cyan, C1-4-Alkyl, C2-6-Alkinyl,
C2-6-Alkenyl, C3-6-Cycloalkyl,
C3-6-Cycloalkyl-C1-3-alkyl,
C5-6-Cycloalkenyl, C5-6-Cycloalkenyl-C1-3-alkyl, Aryl, Heteroaryl, Aryl-C1-3-alkyl,
Heteroaryl-C1-3-alkyl, C1-4-Alkylcarbonyl,
Arylcarbonyl, Heteroarylcarbonyl, C1-4-Alkylsulfonyl,
Arylsulfonyl oder Heteroarylsulfonyl,
wobei Alkyl-, Alkenyl-,
Alkinyl-, Cycloalkyl- und Cycloalkenyl-Reste teilweise oder vollständig fluoriert
oder ein- oder zweifach mit gleichen oder verschiedenen Substituenten
ausgewählt
aus Chlor, Hydroxy, C1-3-Alkoxy und C1-3-Alkyl substituiert sein können, und
wobei
in Cycloalkyl- und Cycloalkenyl-Resten ein oder zwei Methylengruppen
unabhängig
voneinander durch O, S, CO, SO oder SO2 substituiert
sein können,
und
wobei in N-Heterocycloalkyl-Resten eine Methylengruppe
durch CO oder SO2 substituiert sein kann,
wobei
die Begriffe Aryl und Heteroaryl wie zuvor definiert sind und Aryl-
und Heteroaryl-Gruppen unabhängig voneinander
ein- oder zweifach mit gleichen oder verschiedenen Resten L substituiert
sein können.If the radical R 3 is bonded to Cy via a single bond, R 3 is preferably hydrogen, fluorine, chlorine, C 1-6 -alkyl, C 2-6 -alkynyl, C 2-6 -alkenyl, C 3-10 -cycloalkyl , C 3-10 -cycloalkyl-methyl, C 5-10 -cycloalkenyl, C 3-10 -cycloalkenyl-methyl, aryl, heteroaryl, C 1-4 -alkylcarbonyl, aminocarbonyl, C 1-4 -alkylaminocarbonyl, di- (C 1-3 alkyl) aminocarbonyl, C 1-4 alkoxycarbonyl, di (C 1-3 alkyl) amino, pyrrolidin-1-yl, piperidin-1-yl, morpholin-4-yl, C 1-4 alkylcarbonylamino, C 1 _ 6 alkoxy, C 3-10 cycloalkyloxy, C 5-10 cycloalkenyloxy, aryloxy, heteroaryloxy, C 1-4 alkylsulfanyl, C 1-4 alkylsulfonyl, C 3-10 -Cycloalkylsulfanyl, C 3 -10- cycloalkylsulfonyl, C 5-10 -cycloalkenylsulfanyl, C 5-10 -cycloalkenylsulfonyl, hydroxy and cyano, and
in the case where R 3 is bonded to an N atom, R 3 is preferably hydrogen, cyano, C 1-4 -alkyl, C 2-6 -alkynyl, C 2-6 -alkenyl, C 3-6 -cycloalkyl , C 3-6 cycloalkylC 1-3 alkyl, C 5-6 cycloalkenyl, C 5-6 cycloalkenylC 1-3 alkyl, aryl, heteroaryl, arylC 1-3 alkyl, heteroaryl C 1-3 alkyl, C 1-4 alkylcarbonyl, arylcarbonyl, heteroarylcarbonyl, C 1-4 alkylsulfonyl, arylsulfonyl or heteroarylsulfonyl,
wherein alkyl, alkenyl, alkynyl, cycloalkyl and cycloalkenyl radicals are partially or completely fluorinated or mono- or disubstituted by identical or different substituents selected from chlorine, hydroxy, C 1-3 alkoxy and C 1-3 alkyl substituted can be, and
wherein in cycloalkyl and cycloalkenyl radicals one or two methylene groups can be substituted independently of one another by O, S, CO, SO or SO 2 , and
where in N-heterocycloalkyl radicals a methylene group may be substituted by CO or SO 2 ,
wherein the terms aryl and heteroaryl are as defined above and aryl and heteroaryl groups may be independently of one another mono- or disubstituted by identical or different radicals L substituted.
Bedeutet die Gruppe R3 einen Cycloalkyl- oder Cycloalkenyl-Rest, in dem ein oder zwei Methylengruppen unabhängig voneinander durch O, S, CO, SO oder SO2 substituiert sind, so sind bevorzugte Bedeutungen der Gruppe R3 ausgewählt aus der Gruppe bestehend aus Tetrahydrofuranyl, Tetrahydrofuranonyl, Tetrahydrothienyl, Tetrahydropyranyl, Tetrahydropyranonyl und Dioxanyl.If the group R 3 is a cycloalkyl or cycloalkenyl radical in which one or two methylene groups are independently of each other substituted by O, S, CO, SO or SO 2 , preferred meanings of the group R 3 are selected from the group consisting of tetrahydrofuranyl , Tetrahydrofuranonyl, tetrahydrothienyl, tetrahydropyranyl, tetrahydropyranonyl and dioxanyl.
Bedeutet die Gruppe R3 einen N-Heterocycloalkyl-Rest, in dem eine Methylengruppe durch CO oder SO2 substituiert ist, so sind bevorzugte Bedeutungen des Rests R3 ausgewählt aus der Gruppe bestehend aus Pyrrolidinon, Piperidinon, Piperazinon und Morpholinon.If the group R 3 is an N-heterocycloalkyl radical in which a methylene group is substituted by CO or SO 2 , preferred meanings of the radical R 3 are selected from the group consisting of pyrrolidinone, piperidinone, piperazinone and morpholinone.
Besonders
bevorzugte Bedeutungen von R3 sind Wasserstoff,
Cyan, Hydroxy, C1-6-Alkyl, C2-6-Alkinyl, C1-4-Alkyloxy, C3-10-Cycloalkyl,
C3-10-Cycloalkyloxy, Phenyl, C1-4-Alkylcarbonyl, C1-4-Alkyloxycarbonyl, Pyrrolidinon-N-yl,
Pyrazolyl, Tetrazolyl und Hydroxy, und
für den Fall, dass R3 an
ein N-Atom gebunden ist, bedeutet R3 besonders
bevorzugt Wasserstoff, Cyan, C1-4-Alkyl,
C3-6-Cycloalkyl, Aryl, C1-4-Alkylcarbonyl
oder C1-4-Alkylsulfonyl,
wobei in den Cycloalkylgruppen
ein oder zwei Methyleneinheiten unabhängig voneinander durch O oder
CO ersetzt und Alkylreste ein- oder mehrfach fluoriert sein können, und
wobei ein Phenyl-, Pyrazolyl- oder Tetrazolyl-Rest ein- oder zweifach
mit gleichen oder verschiedenen Substituenten L substituiert sein
kann.Particularly preferred meanings of R 3 are hydrogen, cyano, hydroxy, C 1-6 -alkyl, C 2-6 -alkynyl, C 1-4 -alkyloxy, C 3-10 -cycloalkyl, C 3-10 -cycloalkyloxy, phenyl, C 1-4 alkylcarbonyl, C 1-4 alkyloxycarbonyl, pyrrolidinone-N-yl, pyrazolyl, tetrazolyl and hydroxy, and
in the case where R 3 is bonded to an N atom, R 3 particularly preferably denotes hydrogen, cyano, C 1-4 -alkyl, C 3-6 -cycloalkyl, aryl, C 1-4 -alkylcarbonyl or C 1 4- alkylsulfonyl,
wherein in the cycloalkyl groups one or two methylene units are independently replaced by O or CO and alkyl radicals may be mono- or polyfluorinated, and wherein a phenyl, pyrazolyl or tetrazolyl radical may be mono- or disubstituted by identical or different substituents L. ,
Ganz
besonders bevorzugte Reste R3 sind Wasserstoff,
Cyan, Hydroxy, Methyl, Ethyl, Isopropyl, tertButyl, 2-Methylpropyl,
Phenyl, Methoxy, Ethoxy, Isopropyloxy, Cyclopentyloxy, Methoxycarbonyl;
N-Pyrrolidinonyl, 1H-Pyrazol-1-yl, 2H-Tetrazol-5-yl und 2-Methyl-2H-tetrazol-5-yl,
und
für
den Fall, dass R3 an ein N-Atom gebunden
ist, bedeutet R3 ganz besonders bevorzugt
Wasserstoff, Methyl, Ethyl, Isopropyl, tert.Butyl, 2-Methylpropyl
oder Methylcarbonyl.Very particularly preferred radicals R 3 are hydrogen, cyano, hydroxyl, methyl, ethyl, isopropyl, tert-butyl, 2-methylpropyl, phenyl, methoxy, ethoxy, isopropyloxy, cyclopentyloxy, methoxycarbonyl; N-pyrrolidinonyl, 1H-pyrazol-1-yl, 2H-tetrazol-5-yl and 2-methyl-2H-tetrazol-5-yl, and
in the event that R 3 is bonded to an N atom, R 3 is very particularly preferably hydrogen, methyl, ethyl, isopropyl, tert-butyl, 2-methylpropyl or methylcarbonyl.
Ist der Rest R3 über eine Doppelbindung an Cy gebunden, so besitzt R3 eine Bedeutung ausgewählt aus der Gruppe Y.If the radical R 3 is bonded to Cy via a double bond, then R 3 has a meaning selected from the group Y.
Die
Gruppe Y bedeutet vorzugsweise Sauerstoff, C1-6-Alkyl-methyliden,
C2-6-Alkinylmethyliden, C2-6-Alkenyl-methyliden,
C3-7-Cycloalkyl-methyliden oder C3-7-Cycloalkyliden,
wobei
die vorstehend genannten Alkyl-, Alkenyl- und Alkinyl-Reste teilweise
oder vollständig
fluoriert und unabhängig
voneinander ein- oder zweifach mit Substituenten ausgewählt aus
Chlor, Hydroxy, C1-3-Alkoxy und C1-3-Alkyl substituiert sein können, und
wobei
die zuvor angeführte
unsubstituierte Methylidengruppe oder die zuvor angeführten einfach
substituierten Methylidengruppen zusätzlich einfach mit Fluor, C1-3-Alkyl, Trifluormethyl oder Cyan substituiert
sein können, und
wobei
in einer Cycloalkyliden-Gruppe eine Methylengruppe durch O, S oder
NRN oder eine Ethylengruppe durch -NRN-CO-, -CO-NRN-,
-O-CO- oder -CO-O- ersetzt sein kann.The group Y is preferably oxygen, C 1-6 -alkyl-methylidene, C 2-6 -alkynylmethylidene, C 2-6 -alkenyl-methylidene, C 3-7 -cycloalkyl-methylidene or C 3-7 -cycloalkylidene,
wherein the abovementioned alkyl, alkenyl and alkynyl radicals can be partially or fully fluorinated and independently of one another mono- or disubstituted by substituents selected from chlorine, hydroxyl, C 1-3 -alkoxy and C 1-3 -alkyl, and
in addition, the above-mentioned unsubstituted methylidene group or the above-mentioned monosubstituted methylidene groups may be easily substituted with fluorine, C 1-3 alkyl, trifluoromethyl or cyano, and
wherein in a cycloalkylidene group a methylene group may be replaced by O, S or NR N or an ethylene group may be replaced by -NR N -CO-, -CO-NR N -, -O-CO- or -CO-O-.
Für den Fall, dass in einer Cycloalkyliden-Gruppe eine Methylengruppe durch O, S oder NRN oder eine Ethylengruppe durch -NRN-CO-, -CO-NRN-, -O-CO- oder -CO-O- ersetzt ist, ist die Bedeutung solch einer substituierten Cycloalkyliden-Gruppe vorzugsweise ausgewählt aus der Gruppe bestehend aus Dihydrofuranyliden, Dihydropyranyliden, Dihydrothiophenyliden, Pyrrolidinyliden, Piperidinyliden, Dihydrofuranonyliden, Dihydropyranonyliden, Pyrrolidinonyliden, N-Methylpyrrolidinonyliden, Piperidinonyliden und N-Methylpiperidinonyliden.In the case where in a cycloalkylidene group, a methylene group is replaced by O, S or NR N or an ethylene group by -NR N -CO-, -CO-NR N -, -O-CO- or -CO-O- , is the meaning of such a sub substituted cycloalkylidene group preferably selected from the group consisting of dihydrofuranylidene, dihydropyranylidene, dihydrothiophenylidene, pyrrolidinylidene, piperidinylidene, dihydrofuranonylidene, dihydropyranonylidene, pyrrolidinonylidene, N-methylpyrrolidinonylidene, piperidinonylidene and N-methylpiperidinonylidene.
Ganz besonders bevorzugte Bedeutungen der Gruppe Y sind Sauerstoff, C1-6-Alkyl-methyliden, C3-7-Cycloalkyl-methyliden und C3-7-Cycloalkyliden.Very particularly preferred meanings of the group Y are oxygen, C 1-6 -alkyl-methylidene, C 3-7 -cycloalkyl-methylidene and C 3-7 -cycloalkylidene.
Beispiele der ganz besonders bevorzugten Bedeutungen der Gruppe Y sind Sauerstoff, Ethyliden, Isobutyliden, Cyclopentyl-methyliden und Cyclopentyliden.Examples the most preferred meanings of the group Y are oxygen, Ethylidene, isobutylidene, cyclopentylmethylidene and cyclopentylidene.
Gemäß einer
weiteren bevorzugten Variante bedeutet Y vorzugsweise eine Gruppe
gemäß der Teilformel
T in der
RY Wasserstoff,
Fluor, Cyan, Trifluormethyl oder C1-3-Alkyl
bedeutet,
D Carbonyl oder Sulfonyl bedeutet,
B eine Einfachbindung,
-O- oder -NRN- bedeutet,
RB C1-6-Alkyl-, C3-7-Cycloalkyl-,
C5-7-Cycloalkenyl-, C3-7-Cycloalkyl-C1-3-alkyl-, C5-7-Cycloalkenyl-C1-3-alkyl-, Aryl, Heteroaryl, Aryl-C1-3-alkyl- oder Heteroaryl-C1-3-alkyl- bedeutet,
wobei
Alkyl-, Cycloalkyl- und Cycloalkenyl-Reste teilweise oder vollständig fluoriert
oder ein- oder zweifach mit gleichen oder verschiedenen Substituenten
ausgewählt
aus Cyan, Hydroxy, C1-3-Alkoxy und C1-3-Alkyl substituiert sein können, oder
RB und B miteinander unter Ausbildung eines
heterocyclischen Rings ausgewählt
aus Pyrrolidin, Morpholin, Piperidin, Piperazin und 4-(C1-4-Alkyl)piperazin verbunden sind, wobei
der heterocyclische Ring über
die Iminogruppe an die Gruppe D gebunden ist.According to a further preferred variant, Y preferably denotes a group according to the partial formula T. in the
R Y is hydrogen, fluorine, cyano, trifluoromethyl or C 1-3 -alkyl,
D is carbonyl or sulfonyl,
B is a single bond, -O- or -NR N -,
R B is C 1-6 alkyl, C 3-7 cycloalkyl, C 5-7 cycloalkenyl, C 3-7 cycloalkyl C 1-3 alkyl, C 5-7 cycloalkenyl C 1 3- alkyl, aryl, heteroaryl, arylC 1-3 -alkyl or heteroarylC 1-3 -alkyl-,
wherein alkyl, cycloalkyl and cycloalkenyl radicals may be partially or completely fluorinated or mono- or disubstituted by identical or different substituents selected from cyano, hydroxy, C 1-3 alkoxy and C 1-3 alkyl, or
R B and B are joined together to form a heterocyclic ring selected from pyrrolidine, morpholine, piperidine, piperazine and 4- (C 1-4 alkyl) piperazine, wherein the heterocyclic ring is bonded to the group D via the imino group.
Sind in den Resten oder Gruppen Y, R1 oder R3 Cycloalkyl- oder Cycloalkenyl-Ringe vorhanden, in denen zwei Methylengruppen durch O oder S ersetzt sind oder durch CO, SO oder SO2 ersetzt sind, so sind diese Methylengruppen vorzugsweise nicht unmittelbar miteinander verbunden. Sind jedoch zwei Methylengruppen durch O und CO ersetzt, so können diese unmittelbar miteinander verbunden sein, so dass eine Carboxy-Gruppe gebildet wird. Für den Fall, dass Y, R1 oder R3 eine Cycloalkyl- oder Cycloalkenyl-Gruppe mit ein oder zwei erfindungsgemäß ersetzten Methylengruppen ist, so bedeutet die betreffende Gruppe Y, R1 bzw. R3 vorzugsweise eine Cycloalkyl- oder Cycloalkenyl-Gruppe, in der eine Methylengruppe durch O, S, CO, SO oder SO2 substituiert oder eine Ethylengruppe durch -O-CO- oder -CO-O- substituiert ist.If cycloalkyl or cycloalkenyl rings in the radicals or groups Y, R 1 or R 3 are present in which two methylene groups have been replaced by O or S or have been replaced by CO, SO or SO 2 , these methylene groups are preferably not directly adjacent to one another connected. However, when two methylene groups are replaced by O and CO, they may be directly linked together to form a carboxy group. In the event that Y, R 1 or R 3 is a cycloalkyl or cycloalkenyl group having one or two methylene groups replaced according to the invention, the relevant group Y, R 1 or R 3 is preferably a cycloalkyl or cycloalkenyl group, in which a methylene group is substituted by O, S, CO, SO or SO 2 or an ethylene group is substituted by -O-CO- or -CO-O-.
Nachfolgend
werden Bedeutungen weiterer Reste und Substituenten angegeben, die
gemäß der allgemeinen
Formel I, der Formeln I.1 und I.2 als auch gemäß der zuvor beschriebenen Ausführungsformen
als bevorzugt anzusehen sind:
Bevorzugte Bedeutungen des Rests
R4 sind Wasserstoff, Methyl und Fluor, insbesondere
Wasserstoff. Für
den Fall, dass R4 an ein N-Atom gebunden
ist, bedeutet R4 bevorzugt Wasserstoff oder
Methyl.The following are meanings of further radicals and substituents which are to be regarded as preferred according to the general formula I, the formulas I.1 and I.2 as well as according to the embodiments described above:
Preferred meanings of the radical R 4 are hydrogen, methyl and fluorine, in particular hydrogen. In the event that R 4 is bonded to an N atom, R 4 is preferably hydrogen or methyl.
Für den Fall, dass R3 und R4 an dem selben C-Atom von Cy gebunden sind, können R3 und R4 derart miteinander verbunden sein, dass R3 und R4 zusammen vorzugsweise eine C4-5-Alkylen-Brücke bilden, in der ein oder zwei Methyleneinheiten unabhängig voneinander durch O, NRN oder CO substituiert sein können. Bevorzugt bilden hierbei die miteinander verbundenen Reste R3 und R4 zusammen mit dem Kohlenstoffatom von Cy, mit dem diese verbunden sind, einen Ring ausgewählt aus Cyclopentan, Tetrahydrofuran, Tetrahydrofuranon, Pyrrolidin, Pyrrolidinon, Dioxolan, Dithiolan, Cyclohexan, Piperidin, Piperidinon, Tetrahydropyran, Tetrahydropyranon, Dithian und Dioxan, insbesondere Dioxolan.In the event that R 3 and R 4 are bonded to the same C atom of Cy, R 3 and R 4 may be linked together such that R 3 and R 4 together preferably form a C 4-5 alkylene bridge in which one or two methylene units can be substituted independently of one another by O, NR N or CO. Preferably, the interconnected radicals R 3 and R 4 together with the carbon atom of Cy to which they are attached form a ring selected from cyclopentane, tetrahydrofuran, tetrahydrofuranone, pyrrolidine, pyrrolidinone, dioxolane, dithiolane, cyclohexane, piperidine, piperidinone, tetrahydropyran , Tetrahydropyranone, dithiane and dioxane, especially dioxolane.
Für den Fall, dass R3 und R4 an zwei benachbarte C-Atome des Cyclus Cy bebunden sind, können R3 und R4 derart miteinander verbunden sein, dass R3 und R4 zusammen mit den beiden genannten benachbarten Atomen des Cyclus Cy vorzugsweise einen anellierten Cyclohexan-, Benzol- oder Cyclopentadien-Ring bilden, in dem eine oder zwei Methylengruppen unabhängig voneinander durch O, S oder NRN und/oder eine oder zwei Methingruppen durch N ersetzt sein können, und der ein- oder mehrfach fluoriert oder ein- oder zweifach mit gleichen oder verschiedenen Substituenten ausgewählt aus Chlor, Hydroxy, C1-3-Alkoxy und C1-3-Alkyl oder im Falle eines aromatischen anellierten Rings ein- oder zweifach mit gleichen oder verschiedenen Substituenten L substituiert sein kann.In the event that R 3 and R 4 are attached to two adjacent C atoms of the Cy cycle, R 3 and R 4 may be linked together in such a way that R 3 and R 4 together with the two mentioned adjacent atoms of the Cy cycle are preferably form a fused cyclohexane, benzene or cyclopentadiene ring in which one or two methylene groups independently of one another may be replaced by N , S or NR N and / or one or two methine groups by N, and the one or more fluorinated or a - or doubly with identical or different substituents selected from chlorine, hydroxy, C 1-3 alkoxy and C 1-3 alkyl or in the case of an aromatic fused ring, it may be monosubstituted or disubstituted by identical or different substituents L.
Bevorzugt bilden hierbei die miteinander verbundenen Reste R3 und R4 zusammen mit den beiden genannten benachbarten Atomen des Cyclus Cy einen anellierten Cyclohexan-, Benzol-, Furan-, Thiophen- oder Pyrrol-Ring, insbesondere Cyclohexan- oder Benzol-Ring, der ein- oder mehrfach fluoriert oder ein- oder zweifach mit gleichen oder verschiedenen Substituenten ausgewählt aus Chlor, Hydroxy, C1-3-Alkoxy und C1-3-Alkyl oder im Falle eines aromatischen anellierten Rings ausgewählt aus Benzol, Furan, Thiophen oder Pyrrol ein- oder zweifach mit gleichen oder verschiedenen Substituenten L substituiert sein kann.Preferably, the interconnected radicals R 3 and R 4 together with the two said adjacent atoms of the Cy cycle form a fused cyclohexane, benzene, furan, thiophene or pyrrole ring, in particular cyclohexane or benzene ring, the one - or polyfluorinated or mono- or disubstituted by identical or different substituents selected from chlorine, hydroxy, C 1-3 alkoxy and C 1-3 alkyl or in the case of an aromatic fused ring selected from benzene, furan, thiophene or pyrrole - or may be substituted twice with identical or different substituents L.
Bevorzugte Bedeutungen des Rests R5 sind Wasserstoff, Methyl und Fluor, insbesondere Wasserstoff. Für den Fall, dass R5 an ein N-Atom gebunden ist, bedeutet R5 bevorzugt Wasserstoff oder Methyl.Preferred meanings of the radical R 5 are hydrogen, methyl and fluorine, in particular hydrogen. In the case where R 5 is bonded to an N atom, R 5 is preferably hydrogen or methyl.
Für den Fall, dass R4 und R5 miteinander verbunden sind und mit 2, 3 oder 4 Atomen des Cyclus Cy einen anellierten oder verbrückten Cyclus bilden, bedeuten R4 und R5 zusammen vorzugsweise eine C2-4-Alkylen-Brücke, in der ein oder zwei Methyleneinheiten unabhängig voneinander durch O, NRN oder CO substituiert sein können. Bevorzugt bilden hierbei die miteinander verbundenen Reste R4 und R5 zusammen mit Cy einen bicyclischen Ring ausgewählt aus Bicyclo[2.2.1]heptan, Bicyclo[2.2.2]octan, Bicyclo[3.2.1]octan, Octahydroinden und Decalin, in denen ein oder zwei Methyleneinheiten unabhängig voneinander durch O, NRN oder CO substituiert sein können. Besonders bevorzugt bilden hierbei die miteinander verbundenen Reste R4 und R5 zusammen mit Cy ein Bicyclo[3.2.1]octan-System.In the case where R 4 and R 5 are bonded together and form a fused or bridged cycle with 2, 3 or 4 atoms of the Cy cycle, R 4 and R 5 together are preferably a C 2-4 -alkylene bridge, in the one or two methylene units may be independently substituted by O, NR N or CO. Preferably, the interconnected radicals R 4 and R 5 together with Cy form a bicyclic ring selected from bicyclo [2.2.1] heptane, bicyclo [2.2.2] octane, bicyclo [3.2.1] octane, octahydroindene and decalin, in which one or two methylene units may be independently substituted by O, NR N or CO. Particularly preferably, the interconnected radicals R 4 and R 5 together with Cy form a bicyclo [3.2.1] octane system.
Sind in den zuvor angeführten bicyclischen Ringen ein oder zwei Methyleneinheiten unabhängig voneinander durch O, NRN oder CO ersetzt, so sind hierbei bevorzugte Bedeutungen Decahydrochinolin, Decahydroisochinolin, Octahydrochinolinon, Octahydroisochinolinon, Decahydrochinoxalin, Octahydrochinoxalinon, Octahydrobenzoxazin.Are replaced in the above-mentioned bicyclic rings one or two methylene units are independently replaced by O, NR N or CO, as are in this case preferred meanings decahydroquinoline, decahydroisoquinoline, Octahydrochinolinon, Octahydroisochinolinon, Decahydrochinoxalin, Octahydrochinoxalinon, Octahydrobenzoxazin.
Bevorzugte Bedeutungen des Rests R6 sind Wasserstoff, Methyl und Fluor, insbesondere Wasserstoff. Für den Fall, dass R6 an ein N-Atom gebunden ist, bedeutet R6 bevorzugt Wasserstoff oder Methyl.Preferred meanings of the radical R 6 are hydrogen, methyl and fluorine, in particular hydrogen. In the event that R 6 is bonded to an N atom, R 6 is preferably hydrogen or methyl.
Für den Fall, dass die Reste R4, R5 und R6 miteinander verbunden sind, bilden diese zusammen vorzugsweise eine C4-5-Alkantriyl-Brücke, die zuammen mit dem Cyclus Cy ein tricyclisches System bildet, wobei die Alkantriyl-Brücke ein- oder mehrfach fluoriert oder ein- oder zweifach mit gleichen oder verschiedenen Substituenten ausgewählt aus Chlor, Hydroxy, C1-3-Alkoxy und C1-3-Alkyl substituiert sein kann, und in der ein oder zwei Methylengruppen unabhängig voneinander durch O, CO, SO2 oder NRN substituiert sein können. Vorzugsweise bildet hierbei die C4-5-Alkantriyl-Brücke zuammen mit dem Cyclus Cy ein tricyclisches System ausgewählt aus Tricyclononan, Tricyclodekan und Tricycloundekan, besonders bevorzugt Adamantan, bildet, das unsubstituiert ist oder ein- oder mehrfach fluoriert oder ein- oder zweifach mit gleichen oder verschiedenen Substituenten ausgewählt aus Chlor, Hydroxy, C1-3-Alkoxy und C1-3-Alkyl substituiert sein kann.In the event that the radicals R 4 , R 5 and R 6 are joined together, these together preferably form a C 4-5 alkanetriyl bridge, which forms a tricyclic system together with the Cy cycle, the alkanetriyl bridge - or polyfluorinated or mono- or disubstituted by identical or different substituents selected from chlorine, hydroxy, C 1-3 alkoxy and C 1-3 alkyl may be substituted, and in the one or two methylene groups independently of each other by O, CO , SO 2 or NR N may be substituted. Preferably, in this case, the C 4-5 alkanetriyl bridge together with the Cy cycle forms a tricyclic system selected from tricyclononane, tricyclodecane and tricycloundekane, particularly preferably adamantane, which is unsubstituted or monofluorinated or polysubstituted or mono- or di-identical or various substituents selected from chlorine, hydroxy, C 1-3 alkoxy, and C 1-3 alkyl.
Bevorzugte Bedeutungen des Rests Z sind -O-, -CH2-, -CF2-, -C(CH3)2-, -CH=, -NRN-, und -CO-, insbesondere -O-, -CH2- und -CH=, ganz besonders bevorzugt -CH2- und -O-.Preferred meanings of the radical Z are -O-, -CH 2 -, -CF 2 -, -C (CH 3 ) 2 -, -CH =, -NR N -, and -CO-, in particular -O-, -CH 2 - and -CH =, most preferably -CH 2 - and -O-.
Die Substituenten R7a, R7b, R7c, R7d bedeuten unabhängig voneinander vorzugsweise Wasserstoff, (C1-8-Alkyl)oxycarbonyl-, (C1-18-Alkyl)carbonyl, Benzoyl, insbesondere Wasserstoff oder (C1-6-Alkyl)oxycarbonyl-, (C1-8-Alkyl)carbonyl, besonders bevorzugt Wasserstoff, Methoxycarbonyl, Ethoxycarbonyl, Methylcarbonyl oder Ethylcarbonyl. Ganz besonders bevorzugt bedeuten R7a, R7b, R7c und R7d Wasserstoff.The substituents R 7a , R 7b , R 7c , R 7d independently of one another preferably denote hydrogen, (C 1-8 -alkyl) oxycarbonyl, (C 1-18 -alkyl) carbonyl, benzoyl, in particular hydrogen or (C 1-6 Alkyl) oxycarbonyl, (C 1-8 alkyl) carbonyl, particularly preferably hydrogen, methoxycarbonyl, ethoxycarbonyl, methylcarbonyl or ethylcarbonyl. Most preferably, R 7a , R 7b , R 7c and R 7d are hydrogen.
Die Verbindungen der Formel I, in denen R7a, R7b, R7c und R7d eine erfindungsgemäße, von Wasserstoff verschiedene Bedeutung aufweisen, beispielsweise C1-8-Alkylcarbonyl, eignen sich bevorzugt als Zwischenprodukte bei der Synthese von Verbindungen der Formel I in denen R7a, R7b, R7c und R7d Wasserstoff bedeuten.The compounds of the formula I in which R 7a , R 7b , R 7c and R 7d have a meaning other than hydrogen according to the invention, for example C 1-8 -alkylcarbonyl, are preferably suitable as intermediates in the synthesis of compounds of the formula I in R 7a , R 7b , R 7c and R 7d are hydrogen.
Die Substituenten L sind unabhängig voneinander vorzugsweise ausgewählt aus der Gruppe bestehend aus Fluor, Chlor, Brom, C1-3-Alkyl, Difluormethyl, Trifluormethyl, C1-3-Alkoxy, Difluormethoxy, Trifluormethoxy und Cyan, besonders bevorzugt aus der Gruppe bestehend aus Fluor, Chlor, Methyl, Trifluormethyl, Methoxy und Difluormethoxy. Falls der Substituent L mit einem N-Atom verbunden ist, sind bevorzugte Bedeutungen L ausgewählt aus C1-3-Alkyl, Difluormethyl und Trifluormethyl.The substituents L are, independently of one another, preferably selected from the group consisting of fluorine, chlorine, bromine, C 1-3 -alkyl, difluoromethyl, trifluoromethyl, C 1-3 -alkoxy, difluoromethoxy, trifluoromethoxy and cyano, particularly preferably from the group consisting of Fluorine, chlorine, methyl, trifluoromethyl, methoxy and difluoromethoxy. If the substituent L is connected to an N atom, preferred meanings L are selected from C 1-3 -alkyl, difluoromethyl and trifluoromethyl.
Besonders
bevorzugte Verbindungen der allgemeinen Formel I sind ausgewählt aus
der Gruppe der Formeln I.1a bis I.1d und 1.2a bis 1.2d, insbesondere
der Formel I.1c und I.2c: in denen
V1,
V2 unabhängig
voneinander C oder N bedeuten,
U1, U2, U3, U4 unabhängig voneinander
C, N, O, CO oder SO2 bedeuten,
mit
der Maßgabe,
dass in dem durch U und V gebildeten Ring maximal 2 Heteroatome
ausgewählt
aus N und O vorhanden sind, wobei diese Heteroatome nicht unmittelbar
miteinander verbunden sind, und maximal eine Gruppe ausgewählt aus
CO und SO2 vorhanden ist, und verbleibende
freie chemische Bindungen an C- und N-Atomen
mit Wasserstoff abgesättigt
sind; und
in denen R1 bis R6, Z, R7a, R7b, R7c, R7d wie zuvor definiert sind.Particularly preferred compounds of the general formula I are selected from the group of the formulas I.1a to I.1d and 1.2a to 1.2d, in particular of the formulas I.1c and I.2c: in which
V1, V2 independently of one another denote C or N,
U1, U2, U3, U4 independently of one another denote C, N, O, CO or SO 2 ,
with the proviso that in the ring formed by U and V at most 2 heteroatoms selected from N and O are present, these heteroatoms are not directly connected to each other, and at most one group selected from CO and SO 2 is present, and remaining free chemical Bonds to C and N atoms are saturated with hydrogen; and
in which R 1 to R 6 , Z, R 7a , R 7b , R 7c , R 7d are as defined above .
Ganz besonders bevorzugt sind diejenigen Verbindungen der Formeln I.1a, I.1b, I.1c und I.1d, insbesondere der Formel I.1c, in denen die Gruppen U1, U2, U3, U4, V1 und V2 Kohlenstoff bedeuten, d.h. der durch die Gruppen U und V gebildete Cyclus Cyclohexan bedeutet.All Particular preference is given to those compounds of the formulas I.1a, I.1b, I.1c and I.1d, in particular of the formula I.1c, in which the Groups U1, U2, U3, U4, V1 and V2 represent carbon, i. of the By the groups U and V formed cycle cyclohexane means.
Ganz
besonders bevorzugt sind diejenigen Verbindungen der Formeln I.1a
bis I.1d bzw. 1.2a bis 1.2d, insbesondere der Formel I.1 c und 1.2c,
in denen die Reste R1 bis R6,
Z, R7a, R7b, R7c, R7d die zuvor
als bevorzugt angegebenen Bedeutungen aufweisen, insbesondere in
denen
R1 Wasserstoff, Fluor, Chlor,
Brom, C1-6-Alkyl, C2-6-Alkinyl,
C2-6-Alkenyl, C3-7-Cycloalkyl, C5-7-Cycloalkenyl, C1-6-Alkyloxy,
C3-7-Cycloalkyloxy oder Cyan bedeutet, wobei
in Cycloalkyl- und Cycloalkenylgruppen ein oder zwei Methyleneinheiten
unabhängig
voneinander durch O oder CO ersetzt und Alkyl-, Alkenyl- und Alkinyl-Reste
teilweise oder vollständig
fluoriert sein können;
besonders bevorzugt Wasserstoff, Fluor, Chlor, Brom, Methyl, Ethyl,
Isopropyl, Trifluormethyl, Ethinyl, Methoxy, Cyclopentyloxy oder
Cyan bedeutet; und
R3 (1) Wasserstoff,
Cyan, Hydroxy, C1-6-Alkyl, C2-6-Alkinyl,
C1-4-Alkyloxy, C3-7-Cycloalkyl, C3-7-Cycloalkyloxy, Phenyl, C1-4-Alkylcarbonyl,
C1-4-Alkyloxycarbonyl,
Pyrrolidinon-N-yl, Pyrazolyl, Tetrazolyl und Hydroxy, und für den Fall,
dass R3 an ein N-Atom gebunden ist, bedeutet
R3 bevorzugt Wasserstoff, Cyan, C1-4-Alkyl, C3-6-Cycloalkyl,
Aryl, C1-4-Alkylcarbonyl oder C1-4-Alkylsulfonyl,
wobei in den Cycloalkylgruppen ein oder zwei Methyleneinheiten unabhängig voneinander
durch O oder CO ersetzt und Alkylreste teilweise oder vollständig fluoriert sein
können,
und wobei der Phenyl-Rest ein- oder zweifach mit gleichen oder verschiedenen
Substituenten L substituiert sein kann; besonders beovorzugt bedeutet
R3 Wasserstoff, Cyan, Hydroxy, Methyl, Ethyl,
Isopropyl, tertButyl, 2-Methylpropyl,
Phenyl, Methoxy, Ethoxy, Isopropyloxy, Cyclopentyloxy, Methoxycarbonyl, N-Pyrrolidinonyl,
1H-Pyrazol-1-yl, 2H-Tetrazol-5-yl und 2-Methyl-2H-tetrazol-5-yl, und für den Fall,
dass R3 an ein N-Atom gebunden ist, bedeutet
R3 besonders bevorzugt Wasserstoff, Methyl,
Ethyl, Isopropyl, tert.Butyl, 2-Methylpropyl oder Methylcarbonyl;
oder bedeutet, und
Y (1)
Sauerstoff bedeutet; oder
(2) C1-6-Alkyl-methyliden,
C2-6-Alkinyl-methyliden, C2-6-Alkenyl-methyliden,
C3-7-Cycloalkyl-methyliden oder C3-7-Cycloalkyliden bedeutet, wobei die vorstehend
genannten Alkyl-, Alkenyl- und Alkinyl-Reste teilweise oder vollständig fluoriert
und unabhängig
voneinander ein- oder
zweifach mit Substituenten ausgewählt aus Chlor, Hydroxy, C1-3-Alkoxy
und C1-3-Alkyl substituiert sein können,
wobei
die zuvor angeführte
unsubstituierte Methylidengruppe oder die zuvor angeführten einfach
substituierten Methylidengruppen zusätzlich einfach mit Fluor, C1-3-Alkyl, Trifluormethyl oder Cyan substituiert
sein können, und
wobei
in einer Cycloalkyliden-Gruppe eine Methylengruppe durch O, S oder
NRN oder eine Ethylengruppe durch -NRN-CO-, -CO-NRN-,
-O-CO- oder -CO-O-
ersetzt sein kann;
besonders bevorzugt bedeutet X hierbei C1-6-Alkyl-methyliden, C3-6-Cycloalkyl-methyliden
oder C3-7-Cycloalkyliden; oder
(3)
eine Gruppe gemäß der Teilformel
T bedeutet, in der
RY Wasserstoff, Fluor, Cyan, Trifluormethyl
oder C1-3-Alkyl bedeutet,
D Carbonyl
oder Sulfonyl bedeutet,
B eine Einfachbindung, -O- oder -NRN- bedeutet,
RB C1-6-Alkyl-, C3-7-Cycloalkyl-,
C5-7-Cycloalkenyl-, C3-7-Cycloalkyl-C1-3-alkyl-,
C5-7-Cycloalkenyl-C1-3-alkyl-,
Aryl, Heteroaryl, Aryl-C1-3-alkyl- oder Heteroaryl-C1-3-alkyl- bedeutet,
wobei Alkyl-, Cycloalkyl-
und Cycloalkenyl-Reste teilweise oder vollständig fluoriert oder ein- oder
zweifach mit gleichen oder verschiedenen Substituenten ausgewählt aus
Cyan, Hydroxy, C1-3-Alkoxy und C1-3-Alkyl
substituiert sein können,
oder
RB und B miteinander unter Ausbildung
eines heterocyclischen Rings ausgewählt aus Pyrrolidin, Morpholin, Piperidin,
Piperazin und 4-(C1-4-Alkyl)-piperazin verbunden sind, wobei
der heterocyclische Ring über
die Iminogruppe an die C=O-Gruppe gebunden ist;
R2 Wasserstoff,
Fluor, Chlor, Brom, Methyl, Hydroxy, Methoxy, Ethoxy, Trifluormethoxy,
Cyan, Nitro oder durch 1 bis 3 Fluoratome substituiertes Methyl
bedeutet, besonders bevorzugt Wasserstoff, Fluor, Hydroxy, Methoxy, Ethoxy
oder Methyl, insbesondere Wasserstoff oder Methyl bedeutet, und
R4, R5, R6 jeweils
unabhängig
voneinander Wasserstoff, Methyl oder Fluor, insbesondere Wasserstoff
bedeutet, und für
den Fall, dass der Substituent an ein N-Atom gebunden ist, jeweils
unabhängig
Wasserstoff oder Methyl bedeutet; oder
die Reste R4,
R5 und R6 sind miteinander
unter Bildung einer C4-5-Alkantriyl-Brücke verbunden
und bilden zuammen mit dem Cyclus Cy ein tricyclisches System ausgewählt aus
Tricyclononan, Tricyclodekan und Tricycloundekan, besonders bevorzugt
Adamantan, das unsubstituiert ist oder ein- oder mehrfach fluoriert
oder ein- oder zweifach mit gleichen oder verschiedenen Substituenten
ausgewählt
aus Chlor, Hydroxy, C1-3-Alkoxy und C1-3-Alkyl substituiert sein kann;
Z
Sauerstoff, Methyliden oder Methylen, besonders bevorzugt Methylen,
und
R7a, R7b,
R7c, R7d unabhängig voneinander
Wasserstoff, (C1-8-Alkyl)oxycarbonyl-, (C1-18-Alkyl)carbonyl
oder Benzoyl, insbesondere Wasserstoff oder (C1-6-Alkyl)oxycarbonyl-,
(C1-8-Alkyl)carbonyl bedeuten, besonders bevorzugt
Wasserstoff, Methoxycarbonyl, Ethoxycarbonyl, Methylcarbonyl oder
Ethylcarbonyl, ganz besonders bevorzugt Wasserstoff bedeuten, und
L
unabhängig
voneinander Fluor, Chlor, Brom, C1-3-Alkyl,
Difluormethyl, Trifluormethyl, C1-3-Alkoxy,
Difluormethoxy, Trifluormethoxy und Cyan bedeuten; und falls L an
ein N-Atom gebunden ist, unabhängig
voneinander C1-3-Alkyl, Difluormethyl oder
Trifluormethyl;
einschließlich
deren Tautomere, deren Stereoisomere, deren Gemische und deren Salze,
insbesondere deren physiologisch verträglichen Salze.Very particular preference is given to those compounds of the formulas I.1a to I.1d or 1.2a to 1.2d, in particular of the formulas I.1c and 1.2c, in which the radicals R 1 to R 6 , Z, R 7a , R 7b , R 7c , R 7d have the meanings given above as preferred, in particular in which
R 1 is hydrogen, fluorine, chlorine, bromine, C 1-6 -alkyl, C 2-6 -alkynyl, C 2-6 -alkenyl, C 3-7 -cycloalkyl, C 5-7 -cycloalkenyl, C 1-6 - Alkyloxy, C 3-7 cycloalkyloxy or cyano, wherein in cycloalkyl and cycloalkenyl groups one or two methylene units independently replaced by O or CO and alkyl, alkenyl and alkynyl radicals may be partially or completely fluorinated; particularly preferably hydrogen, fluorine, chlorine, bromine, methyl, ethyl, isopropyl, trifluoromethyl, ethynyl, methoxy, cyclopentyloxy or cyano means; and
R 3 is (1) hydrogen, cyano, hydroxy, C 1-6 alkyl, C 2-6 alkynyl, C 1-4 alkyloxy, C 3-7 cycloalkyl, C 3-7 cycloalkyloxy, phenyl, C 1 -4- alkylcarbonyl, C 1-4 -alkyloxycarbonyl, pyrrolidinon-N-yl, pyrazolyl, tetrazolyl and hydroxy, and in the case where R 3 is attached to an N-atom, R 3 is preferably hydrogen, cyano, C 1 -4 alkyl, C 3-6 cycloalkyl, aryl, C 1-4 alkylcarbonyl or C 1-4 alkylsulfonyl, wherein in the cycloalkyl groups one or two methylene units are independently replaced by O or CO and alkyl radicals are partially or completely fluorinated and wherein the phenyl radical may be mono- or disubstituted by identical or different substituents L; most preferably, R 3 is hydrogen, cyano, hydroxy, methyl, ethyl, isopropyl, tert -butyl, 2-methylpropyl, phenyl, methoxy, ethoxy, isopropyloxy, cyclopentyloxy, methoxycarbonyl, N-pyrrolidinonyl, 1H-pyrazol-1-yl, 2H-tetrazole -5-yl and 2-methyl-2H-tetrazol-5-yl, and in the case where R 3 is bonded to an N atom, R 3 particularly preferably denotes hydrogen, methyl, ethyl, isopropyl, tert-butyl, 2-methylpropyl or methylcarbonyl; or means, and
Y (1) is oxygen; or
(2) C 1-6 alkyl-methylidene, C 2-6 -alkynyl-methylidene, C 2-6 -alkenyl-methylidene, C 3-7 -cycloalkyl-methylidene or C 3-7 -cycloalkylidene, wherein the above mentioned alkyl, alkenyl and alkynyl radicals may be partially or completely fluorinated and independently of one another mono- or disubstituted by substituents selected from chlorine, hydroxyl, C 1-3 -alkoxy and C 1-3 -alkyl,
in addition, the above-mentioned unsubstituted methylidene group or the above-mentioned monosubstituted methylidene groups may be easily substituted with fluorine, C 1-3 alkyl, trifluoromethyl or cyano, and
wherein in a cycloalkylidene group a methylene group may be replaced by O, S or NR N or an ethylene group may be replaced by -NR N -CO-, -CO-NR N -, -O-CO- or -CO-O-;
X is particularly preferably C 1-6 -alkyl-methylidene, C 3-6 -cycloalkyl-methylidene or C 3-7 -cycloalkylidene; or
(3) a group according to sub-formula T means in the
R Y is hydrogen, fluorine, cyano, trifluoromethyl or C 1-3 -alkyl,
D is carbonyl or sulfonyl,
B is a single bond, -O- or -NR N -,
R B is C 1-6 alkyl, C 3-7 cycloalkyl, C 5-7 cycloalkenyl, C 3-7 cycloalkyl C 1-3 alkyl, C 5-7 cycloalkenyl C 1 3- alkyl, aryl, heteroaryl, arylC 1-3 -alkyl or heteroarylC 1-3 -alkyl-,
wherein alkyl, cycloalkyl and cycloalkenyl radicals may be partially or completely fluorinated or mono- or disubstituted by identical or different substituents selected from cyano, hydroxy, C 1-3 alkoxy and C 1-3 alkyl, or
R B and B are joined together to form a heterocyclic ring selected from pyrrolidine, morpholine, piperidine, piperazine, and 4- (C 1-4 alkyl) piperazine, wherein the heterocyclic ring is bonded to the C = O group via the imino group is;
R 2 is hydrogen, fluorine, chlorine, bromine, methyl, hydroxyl, methoxy, ethoxy, trifluoromethoxy, cyano, nitro or methyl substituted by 1 to 3 fluorine atoms, particularly preferably hydrogen, fluorine, hydroxyl, methoxy, ethoxy or methyl, in particular hydrogen or Methyl means, and
R 4 , R 5 , R 6 are each independently of one another hydrogen, methyl or fluoro, in particular hydrogen, and in the event that the substituent is bonded to an N atom, each independently is hydrogen or methyl; or
R 4 , R 5 and R 6 are joined together to form a C 4-5 alkanetriyl bridge and together with the Cy cycle form a tricyclic system selected from tricyclononane, tricyclodecane and tricycloundekane, more preferably adamantane which is unsubstituted or mono- or polyfluorinated or mono- or disubstituted by identical or different substituents selected from chlorine, hydroxy, C 1-3 alkoxy and C 1-3 alkyl may be substituted;
Z is oxygen, methylidene or methylene, more preferably methylene, and
R 7a , R 7b , R 7c , R 7d are independently hydrogen, (C 1-8 alkyl) oxycarbonyl, (C 1-18 alkyl) carbonyl or benzoyl, in particular hydrogen or (C 1-6 alkyl) oxycarbonyl -, (C 1-8 alkyl) carbonyl, particularly preferably hydrogen, methoxycarbonyl, ethoxycarbonyl, methylcarbonyl or ethylcarbonyl, very particularly preferably hydrogen, and
L independently of one another are fluorine, chlorine, bromine, C 1-3 -alkyl, difluoromethyl, trifluoromethyl, C 1-3 -alkoxy, difluoromethoxy, trifluoromethoxy and cyano; and when L is attached to an N atom, independently of one another, C 1-3 alkyl, difluoromethyl or trifluoromethyl;
including their tautomers, their stereoisomers, their mixtures and their salts, in particular their physiologically acceptable salts.
Gemäß einer Variante der zuvor angeführten Ausführungsformen sind diejenigen Verbindungen auch bevorzugt, in denen die cyclische Gruppe Cy, die den Substituenten R3 trägt, mindestens einen weiteren, von Wasserstoff verschiedenen Substituenten R4, R5 und/oder R6 aufweist. Nach dieser Variante sind diejenigen Verbindungen auch bevorzugt, die einen Substituenten R4 in der Bedeutung Methyl oder Fluor aufweisen.According to a variant of the abovementioned embodiments, those compounds are also preferred in which the cyclic group Cy carrying the substituent R 3 has at least one further substituent R 4 , R 5 and / or R 6 which is different from hydrogen. According to this variant, those compounds are also preferred which have a substituent R 4 meaning methyl or fluorine.
Besonders bevorzugte Verbindungen der allgemeinen Formel I sind ausgewählt aus der Gruppe
- (a) 1-Chlor-2-(4-methoxy-cyclohexyloxy)-4-β-D-glucopyranos-1-yl-benzol,
- (b) 1-Chlor-2-(cyclohexylmethyl)-4-β-D-glucopyranos-1-yl-benzol,
- (c) 1-Chlor-2-(4-methoxy-cyclohexylmethyl)-4-β-D-glucopyranos-1-yl-benzol,
- (d) 1-Chlor-4-β-D-glucopyranos-1-yl-2-(cis-4-methoxy-cyclohexyloxy)-benzol
- (e) 1-Chlor-4-β-D-glucopyranos-1-yl-2-(trans-4-methoxy-cyclohexyloxy)-benzol
- (f) 1-β-D-glucopyranos-1-yl-3-(4-methoxy-cyclohexylmethyl)-benzol
- (g) 1-β-D-glucopyranos-1-yl-3-(4-hydroxy-cyclohexylidenmethyl)-benzol
- (h) 1-β-D-glucopyranos-1-yl-3-(4-hydroxy-cyclohexylmethyl)-bnzol
- (a) 1-chloro-2- (4-methoxycyclohexyloxy) -4-β-D-glucopyranos-1-yl-benzene,
- (b) 1-chloro-2- (cyclohexylmethyl) -4-β-D-glucopyranos-1-yl-benzene,
- (c) 1-chloro-2- (4-methoxycyclohexylmethyl) -4-β-D-glucopyranos-1-yl-benzene,
- (d) 1-Chloro-4-β-D-glucopyranos-1-yl-2- (cis-4-methoxycyclohexyloxy) benzene
- (e) 1-Chloro-4-β-D-glucopyranos-1-yl-2- (trans-4-methoxycyclohexyloxy) benzene
- (f) 1-β-D-glucopyranos-1-yl-3- (4-methoxycyclohexylmethyl) benzene
- (g) 1-β-D-glucopyranos-1-yl-3- (4-hydroxycyclohexylidenemethyl) benzene
- (h) 1-β-D-glucopyranos-1-yl-3- (4-hydroxycyclohexylmethyl) benzene
Im folgenden werden Begriffe, die zuvor und nachfolgend zur Beschreibung der erfindungsgemäßen Verbindungen verwendet werden, näher definiert.in the Following are terms used previously and below for description the compounds of the invention be used, closer Are defined.
Die Bezeichnung Halogen bezeichnet ein Atom ausgewählt aus der Gruppe bestehend aus F, Cl, Br und I, insbesondere F, Cl und Br.The Designation Halogen denotes an atom selected from the group consisting from F, Cl, Br and I, especially F, Cl and Br.
Die austauschbar verwendeten Bezeichnungen "teilweise oder vollständig fluoriert sein kann" und "ein oder mehrfach fluoriert sein kann" bedeuten, dass die so bezeichnete Gruppe nicht fluoriert ist oder einen oder mehrere Fluor-Substituenten aufweist, wobei dies auch die vollständige Fluorierung der bezeichneten Gruppe mit einschließt.The interchangeably used terms "partially or completely fluorinated can be "and" one or more times fluorinated "can mean that the group so designated is not fluorinated or one or more Having fluorine substituents, which also includes the complete fluorination the designated group includes.
Die Bezeichnung C1-n-Alkyl, wobei n einen Wert von 1 bis 18 besitzen kann, bedeutet eine gesättigte, verzweigte oder unverzweigte Kohlenwasserstoffgruppe mit 1 bis n C-Atomen. Beispiele solcher Gruppen umfassen Methyl, Ethyl, n-Propyl, iso-Propyl, Butyl, iso-Butyl, sec-Butyl, tert-Butyl, n-Pentyl, iso-Pentyl, neo-Pentyl, tert-Pentyl, n-Hexyl, iso-Hexyl, etc.The term C 1-n- alkyl, where n can have a value of 1 to 18, denotes a saturated, branched or unbranched hydrocarbon group having 1 to n C atoms. Examples of such groups include methyl, ethyl, n-propyl, iso-propyl, butyl, iso-butyl, sec-butyl, tert-butyl, n-pentyl, iso-pentyl, neo-pentyl, tert-pentyl, n-hexyl, iso-hexyl, etc.
Die Bezeichnung Methylen bedeutet eine -CH2-Gruppe und die Bezeichnung Methin bedeutet eine CH-Gruppe.The term methylene means a -CH 2 group and the term methine means a CH group.
Die Bezeichnung Methyliden bedeutet einen über eine Doppelbindung verbundenen Rest der Teilformel The term methylidene means a radical of the partial formula linked via a double bond
Die Bezeichnung C1-n-Alkyl-methyliden bedeutet eine Methyliden-Gruppe, in der ein Wasserstoff-Atom durch eine C1-n-Alkyl-Gruppe substituiert ist.The term C 1-n -alkylmethylidene means a methylidene group in which one hydrogen atom is substituted by a C 1-n -alkyl group.
Die Bezeichnung Methanylyliden bedeutet eine über eine Einfachbindung und eine Doppelbindung verbundene CH-Brücke der Teilformel The term methanylyliden means a CH-bridge of the partial formula connected via a single bond and a double bond
Die Bezeichnung "Butadienylen" bedeutet die Gruppe The term "butadienylene" means the group
Der Begriff C2-n-Alkinyl, wobei n einen Wert von 3 bis 6 besitzt, bezeichnet eine verzweigte oder unverzweigte Kohlenwasserstoffgruppe mit 2 bis n C-Atomen und einer C≡C-Dreifachbindung. Beispiele solcher Gruppen umfassen Ethinyl, 1-Propinyl, 2-Propinyl, iso-Propinyl, 1-Butinyl, 2-Butinyl, 3-Butinyl, 2-Methyl-1-propinyl, 1-Pentinyl, 2-Pentinyl, 3-Pentinyl, 4-Pentinyl, 3-Methyl-2-butinyl, 1-Hexinyl, 2-Hexinyl, 3-Hexinyl, 4-Hexinyl-, 5-Hexinyl etc.The term C 2-n alkynyl, wherein n has a value of 3 to 6, denotes a branched or unbranched hydrocarbon group having 2 to n C atoms and a C≡C triple bond. Examples of such groups include ethynyl, 1-propynyl, 2-propynyl, isopropynyl, 1-butynyl, 2-butynyl, 3-butynyl, 2-methyl-1-propynyl, 1-pentynyl, 2-pentynyl, 3-pentynyl, 4-pentynyl, 3-methyl-2-butynyl, 1-hexynyl, 2-hexynyl, 3-hexynyl, 4-hexynyl, 5-hexynyl, etc.
Der Begriff C1-n-Alkoxy oder C1-n-Alkyloxy bezeichnet eine C1-n-Alkyl-O-Gruppe, worin C1-n-Alkyl wie oben definiert ist. Beispiele solcher Gruppen umfassen Methoxy, Ethoxy, n-Propoxy, iso-Propoxy, n-Butoxy, iso-Butoxy, sec-Butoxy, tert-Butoxy, n-Pentoxy, iso-Pentoxy, neo-Pentoxy, tert-Pentoxy, n-Hexoxy, iso-Hexoxy etc.The term C 1-n -alkoxy or C 1-n -alkyloxy refers to a C 1-n -alkyl-O-group wherein C 1-n -alkyl is as defined above. Examples of such groups include methoxy, ethoxy, n-propoxy, iso -propoxy, n-butoxy, iso-butoxy, sec-butoxy, tert-butoxy, n-pentoxy, iso-pentoxy, neo-pentoxy, tert-pentoxy, n- Hexoxy, iso-hexoxy etc.
Der Begriff C1-n-Alkylcarbonyl bezeichnet eine C1-n-Alkyl-C(=O)-Gruppe, worin C1-n-Alkyl wie oben definiert ist. Beispiele solcher Gruppen umfassen Methylcarbonyl, Ethylcarbonyl, n-Propylcarbonyl, iso-Propylcarbonyl, n-Butylcarbonyl, iso-Butylcarbonyl, sec-Butylcarbonyl, tert-Butylcarbonyl, n-Pentylcarbonyl, iso-Pentylcarbonyl, neo-Pentylcarbonyl, tert-Pentylcarbonyl, n-Hexylcarbonyl, iso-Hexylcarbonyl, etc.The term C 1-n -alkylcarbonyl refers to a C 1-n -alkyl-C (= O) group, wherein C 1-n -alkyl is as defined above. Examples of such groups include methylcarbonyl, ethylcarbonyl, n-propylcarbonyl, iso -propylcarbonyl, n-butylcarbonyl, iso-butylcarbonyl, sec-butylcarbonyl, tert -butylcarbonyl, n-pentylcarbonyl, iso-pentylcarbonyl, neo-pentylcarbonyl, tert-pentylcarbonyl, n- Hexylcarbonyl, iso-hexylcarbonyl, etc.
Der Begriff C3-n-Cycloalkyl bezeichnet eine gesättigte mono-, bi-, tri- oder spirocarbocyclische Gruppe mit 3 bis n C-Atomen. Beispiele solcher Gruppen umfassen Cyclopropyl, Cyclobutyl, Cyclopentyl, Cyclohexyl, Cycloheptyl, Cyclooctyl, Cyclononyl, Cyclododecyl, Bicyclo[3.2.1.]octyl, Spiro[4.5]decyl, Norpinyl, Norbonyl, Norcaryl, Adamantyl, etc. Vorzugsweise umfasst der Begriff C3-7-Cycloalkyl gesättigte monocyclische Gruppen.The term C 3-n -cycloalkyl denotes a saturated mono-, bi-, tri- or spirocarbocyclic group having 3 to n C atoms. Examples of such groups include cyclopropyl, cyclobutyl, cyclopentyl, cyclohexyl, cycloheptyl, cyclooctyl, cyclononyl, cyclododecyl, bicyclo [3.2.1.] Octyl, spiro [4.5] decyl, norpinyl, norbornyl, norcaryl, adamantyl, etc. Preferably, the term C includes 3-7 cycloalkyl saturated monocyclic groups.
Der Begriff C3-n-Cycloalkyloxy bezeichnet eine C3-n-Cycloalkyl-O-Gruppe, worin C3-n-Cycloalkyl wie oben definiert ist. Beispiele solcher Gruppen umfassen Cyclopropyloxy, Cyclobutyloxy, Cyclopentyloxy, Cyclohexyloxy, Cycloheptyloxy, etc.The term C 3-n -cycloalkyloxy refers to a C 3-n -cycloalkyl-O-group wherein C 3-n -cycloalkyl is as defined above. Examples of such groups include cyclopropyloxy, cyclobutyloxy, cyclopentyloxy, cyclohexyloxy, cycloheptyloxy, etc.
Der Begriff C5-n-Cycloalkenyl bezeichnet eine C5-n-Cycloalkyl-Gruppe, die wie oben definiert ist und zusätzlich mindestens eine ungesättigte C=C-Doppelbindung hat.The term C 5-n -cycloalkenyl denotes a C 5-n -cycloalkyl group which is as defined above and additionally has at least one unsaturated C =C double bond.
Der Begriff C3-n-Cycloalkylcarbonyl bezeichnet eine C3-n-Cycloalkyl-C(=O)-Gruppe, worin C3-n-Cycloalkyl wie oben definiert ist.The term C 3-n -cycloalkylcarbonyl refers to a C 3-n -cycloalkyl-C (= O) group, wherein C 3-n -cycloalkyl is as defined above.
Der Begriff Tri-(C1-4-alkyl)silyl umfasst Silyl-Gruppen, die gleiche oder zwei oder drei verschiedene Alkylgruppen aufweisen.The term tri (C 1-4 alkyl) silyl includes silyl groups having the same or two or three different alkyl groups.
Der Begriff Di-(C1-3-alkyl)amino umfasst Amino-Gruppen, die gleiche oder zwei verschiedene Alkylgruppen aufweisen.The term di (C 1-3 alkyl) amino includes amino groups having the same or different alkyl groups.
Der Begriff N-Heterocycloalkyl bezeichnet einen gesättigten carbocyclischen Ring, der eine Imino-Gruppe im Ring aufweist, und der zusätzlich eine weitere Imino-Gruppe oder ein O- oder S-Atom im Ring aufweisen kann. Beispiele solcher N-Heterocycloalkyl-Gruppen sind Pyrrolidin, Piperidin, Piperazin und Morpholin.Of the Term N-heterocycloalkyl refers to a saturated carbocyclic ring, which has an imino group in the ring, and in addition a another imino group or may have an O or S atom in the ring. Examples of such N-heterocycloalkyl groups are pyrrolidine, piperidine, piperazine and morpholine.
Falls in Gruppen, beispielsweise in X, R1 oder R3, vorkommende Alkyl-Reste substituiert, beispielsweise fluoriert, sein können, so umfasst dies nicht nur Alkyl-Reste in den Gruppen die unmittelbar Alkyl bedeuten, sondern auch in anderen, Alkyl-Reste aufweisenden Bedeutungen, wie beispielsweise Alkoxy, Alkylcarbonyl, Alkoxyalkyl, etc. So umfasst beispielsweise X, R1 und R3 in der Bedeutung Alkoxy, wobei Alkylreste teilweise oder vollständig fluoriert sein können, auch Difluormethoxy und Trifluormethoxy.If in groups, for example in X, R 1 or R 3 , occurring alkyl radicals substituted, for example fluorinated, may be, this includes not only alkyl radicals in the groups which are directly alkyl, but also in other, alkyl radicals For example, X, R 1 and R 3 in the meaning alkoxy, wherein alkyl radicals may be partially or fully fluorinated, also difluoromethoxy and trifluoromethoxy.
Die vorstehend und nachfolgend verwendete Schreibweise, bei der in einer cyclischen Gruppe, beispielsweise einer Phenylgruppe oder in der Gruppe Cy, eine Bindung eines Substituenten zur Mitte der cyclischen Gruppe hin dargestellt ist, bedeutet, sofern nicht anders angegeben, dass dieser Substituent an jede freie, ein H-Atom tragende Position der cyclischen Gruppe gebunden sein kann. So können an eine Methylengruppe der cyclischen Gruppe auch zwei Substituenten gebunden sein.The spelling used above and below, in which in one cyclic group, for example, a phenyl group or in the Group Cy, a bond of a substituent to the center of the cyclic Group is indicated, unless otherwise stated, that this substituent at any free, carrying a H atom position the cyclic group may be bonded. So can to a methylene group the cyclic group may also be bonded to two substituents.
Die erfindungsgemäßen Verbindungen sind unter Anwendung im Prinzip bekannter Syntheseverfahren erhältlich. Bevorzugt werden die Verbindungen nach den nachfolgend näher erläuterten erfindungsgemäßen Herstellungsverfahren erhalten.The Compounds of the invention are obtainable using in principle known synthesis methods. Preferably, the compounds are explained in more detail below inventive production process receive.
Die nachfolgend beschriebenen Glucose-Derivate können aus D-Gluconolacton oder eines Derivats davon durch Addition der gewünschten Arylgruppe in Form einer Organometallverbindung (Schema 1) aufgebaut werden.The Glucose derivatives described below may be prepared from D-gluconolactone or a derivative thereof by addition of the desired aryl group in the form an organometallic compound (Scheme 1).
Schema 1: Addition einer Organometallverbindung an ein Gluconolacton Scheme 1: Addition of an organometallic compound to a gluconolactone
Die Reaktion gemäß Schema 1 wird am besten ausgehend von mit Chlor-, Brom- oder Iod-substituierten Aromaten durchgeführt. Daraus kann die entsprechende Organometallverbindung entweder über einen so genannten Halogen-Metall-Austausch oder über eine Insertion des Metalls in die Kohlenstoff-Halogen-Bindung hergestellt werden. Der Halogen-Metallaustausch kann beispielweise mit einer Organolithiumverbindung wie z.B. n-, sec- oder tert-Butyllithium durchgeführt werden und liefert dabei den entsprechenden lithiierten Aromaten. Die analoge Magnesiumverbindung kann ebenfalls über einen Halogen-Metallaustausch mit einer geeigneten Grginard-Verbindung wie z.B. Isopropylmagnesiumbromid oder Diisopropylmagnesium generiert werden. Die Reaktionen werden vorzugsweise zwischen 0 und –100°C, besonders bevorzugt zwischen –30 und –80°C in Lösungsmitteln wie beispielsweise Ether, Tetrahydrofuran, Toluol, Hexan oder Methylenchlorid durchgeführt. Die so erhaltenen Magnesium- bzw. Lithium-Verbindungen können mit Metallsalzen, wie z.B. Certrichlorid, zu weiteren zur Addition geeigneten Organometallverbindungen ummetalliert werden. Alternativ können die Organometallverbindungen auch durch Insertion eines Metalls in die Kohlenstoff-Halogen-Bindung eines Arylchlorids, -bromids oder -iodids dargestellt werden. Hierzu eignen sich Metalle wie z.B. Lithium oder Magnesium. Die Addition der Organometallverbindungen an das Gluconolacton bzw. Derivaten davon erfolgt vorzugsweise bei Temperaturen zwischen 0 und –100°C, besonders bevorzugt bei –30 bis –80°C. Als Lösungsmittel eignen sich z.B. Ether, Toluol, Methylenchlorid, Hexan, Tetrahydrofuran oder Gemische daraus (siehe M. Schlosser, Organometallics in Synthesis, John Wiley & Sons, Chichester/New York/Brisbane/Toronto/Singapore, 1994).The reaction according to Scheme 1 is best carried out starting from chloro, bromo or iodo substituted aromatics. From this, the corresponding organometallic compound can be prepared either via a so-called halogen-metal exchange or via an insertion of the metal into the carbon-halogen bond. The halogen-metal exchange can be carried out for example with an organolithium compound such as n-, sec- or tert-butyllithium and thereby provides the corresponding lithiated flavor The analogous magnesium compound can also be generated via a halogen-metal exchange with a suitable Grginard compound such as isopropylmagnesium bromide or diisopropylmagnesium. The reactions are preferably carried out between 0 and -100 ° C, more preferably between -30 and -80 ° C in solvents such as ether, tetrahydrofuran, toluene, hexane or methylene chloride. The magnesium or lithium compounds thus obtained can be metalated with metal salts, such as cerium trichloride, to form further organometallic compounds suitable for addition. Alternatively, the organometallic compounds may also be prepared by insertion of a metal into the carbon-halogen bond of an aryl chloride, bromide or iodide. For this purpose, metals such as lithium or magnesium are suitable. The addition of the organometallic compounds to the gluconolactone or derivatives thereof is preferably carried out at temperatures between 0 and -100 ° C, more preferably at -30 to -80 ° C. Suitable solvents are, for example, ethers, toluene, methylene chloride, hexane, tetrahydrofuran or mixtures thereof (see M. Schlosser, Organometallics in Synthesis, John Wiley & Sons, Chichester / New York / Brisbane / Toronto / Singapore, 1994).
Die Synthese der aromatischen Reste sind Standardtransformationen in der Organischen Chemie und gehören zum allgemeinen Fachwissen oder sind zumindest aus der Fachliteratur als Methoden in der organischen Synthese bekannt und für den Fachmann im Hinblick auf die erfindungsgemäßen Verbindungen ohne Weiteres anwendbar (siehe u.a. J. March, Advanced Organic Reactions, Reactions, Mechanisms, and Structure, 4. Edition, John Wiley & Sons, Chichester/New York/Brisbane/Toronto/Singapore, 1992 und darin zitierte Literatur und Synthesebeispiele I-IX, XI-XIV und 2).The Synthesis of aromatic residues are standard transformations in of organic chemistry and belong to general expertise or are at least from the specialist literature as methods in organic synthesis and known to those skilled in the art in view of the compounds of the invention readily applicable (see, inter alia, J. March, Advanced Organic Reactions, Reactions, Mechanisms, and Structure, 4th Edition, John Wiley & Sons, Chichester / New York / Brisbane / Toronto / Singapore, 1992 and literature cited therein and Synthesis Examples I-IX, XI-XIV and 2).
Zur
Herstellung von Verbindungen der allgemeinen Formel I wird gemäß dem erfindungsgemäßen Verfahren
a) eine Verbindung der allgemeinen Formel II in der
Z, Cy und R', R1 bis R6 wie zuvor
definiert sind und
R8a, R8b,
R8c und R8d wie
zuvor definiert sind und beispielsweise unabhängig voneinander Acetyl, Pivaloyl,
Benzoyl, tert-Butoxycarbonyl, Benzyloxycarbonyl, Trialkylsilyl,
Benzyl oder substituiertes Benzyl bedeuten,
mit einem Reduktionsmittel
in Gegenwart einer Säure
umgesetzt.For the preparation of compounds of the general formula I, according to the process a) of the invention, a compound of the general formula II in which Z, Cy and R ', R 1 to R 6 are as previously defined and
R 8a , R 8b , R 8c and R 8d are as defined above and represent, for example, independently of one another acetyl, pivaloyl, benzoyl, tert-butoxycarbonyl, benzyloxycarbonyl, trialkylsilyl, benzyl or substituted benzyl,
reacted with a reducing agent in the presence of an acid.
Für die Umsetzung eignen sich als Reduktionsmittel beispielsweise Silane, wie Triethyl-, Tripropyl-, Triisopropyl- oder Diphenylsilan, Natriumborhydrid, Natriumcyanoborhydrid, Zinkborhydrid, Boran, Lithiumaluminiumhydrid, Diisobutylaluminiumhydrid oder Samariumiodid. Die Reduktionen finden vorzugsweise in Gegenwart einer geeigneten Säure, wie z.B. Salzsäure, Toluolsulfonsäure, Trifluoressigsäure, Essigsäure, Bortrifluoridetherat, Trimethylsilyltriflat, Titantetrachlorid, Zinntetrachlorid, Scandiumtriflat oder Zinkiodid statt. In Abhängigkeit vom Reduktionsmittel und der Säure kann die Reaktion in einem Lösungsmittel, wie beispielsweise Methylenchlorid, Chloroform, Acetonitril, Toluol, Hexan, Diethylether, Tetrahydrofuran, Dioxan, Ethanol, Wasser oder Gemischen daraus bei Temperaturen zwischen –60°C und 120°C durchgeführt werden. Ein besonders geeignete Reagenzienkombination besteht beispielsweise aus Triethylsilan und Bortrifluorid-Etherat, die zweckmäßigerweise in Acetonitril oder Dichlormethan bei Temperaturen von –60°C und 60°C zum Einsatz kommt. Des Weiteren kann Wasserstoff in Gegenwart eines Übergangsmetallkatalysators, wie z.B. Palldium auf Kohle oder Raney-Nickel, in Lösungsmitteln wie Tetrahydrofuran, Ethylacetat, Methanol, Ethanol, Wasser oder Essigsäure, für die dargestellte Transformation angewendet werden.For the implementation Suitable reducing agents are, for example, silanes, such as triethyl-, Tripropyl, triisopropyl or diphenylsilane, sodium borohydride, Sodium cyanoborohydride, zinc borohydride, borane, lithium aluminum hydride, Diisobutylaluminum hydride or samarium iodide. Find the reductions preferably in the presence of a suitable acid, e.g. Hydrochloric acid, toluenesulfonic acid, trifluoroacetic acid, acetic acid, boron trifluoride etherate, Trimethylsilyl triflate, titanium tetrachloride, tin tetrachloride, scandium triflate or zinc iodide instead. Dependent on of the reducing agent and the acid can the reaction be in a solvent, such as methylene chloride, chloroform, acetonitrile, toluene, Hexane, diethyl ether, tetrahydrofuran, dioxane, ethanol, water or Mixtures thereof are carried out at temperatures between -60 ° C and 120 ° C. A particularly suitable Reagent combination consists for example of triethylsilane and Boron trifluoride etherate, conveniently in acetonitrile or Dichloromethane at temperatures of -60 ° C and 60 ° C is used. Furthermore may be hydrogen in the presence of a transition metal catalyst, such as. Palladium on carbon or Raney nickel, in solvents such as tetrahydrofuran, ethyl acetate, methanol, ethanol, water or Acetic acid, for the represented transformation can be applied.
Alternativ
werden zur Herstellung von Verbindungen der allgemeinen Formel I
gemäß dem erfindungsgemäßen Verfahren
b) in einer Verbindung der allgemeinen Formel III in der
Cy, Z und R1 bis R6 wie
zuvor definiert sind und
R8a bis R8d eine der zuvor definierten Schutzgruppen,
wie z.B. eine Acyl-, Arylmethyl-, Acetal-, Ketal- oder Silylgruppe
bedeuten, die Schutzgruppen abgespalten.Alternatively, for the preparation of compounds of general formula I according to the inventive method b) in a compound of general formula III in which Cy, Z and R 1 to R 6 are as previously defined and
R 8a to R 8d represent one of the protective groups defined above, such as, for example, an acyl, arylmethyl, acetal, ketal or silyl group, the protective groups are split off.
Die Abspaltung eines verwendeten Acyl-, Acetal- oder Ketal-Schutzrestes erfolgt beispielsweise hydrolytisch in einem wässrigen Lösungsmittel, z.B. in Wasser, Isopropanol/Wasser, Essigsäure/Wasser, Tetrahydrofuran/Wasser oder Dioxan/Wasser, in Gegenwart einer Säure wie Trifluoressigsäure, Salzsäure oder Schwefelsäure oder in Gegenwart einer Alkalibase wie Lithiumhydroxid, Natriumhydroxid oder Kaliumhydroxid oder aprotisch, z.B. in Gegenwart von Jodtrimethylsilan, bei Temperaturen zwischen 0 und 120°C, vorzugsweise bei Temperaturen zwischen 10 und 100°C. Die Abspaltung eines Trifluoracetylrestes erfolgt vorzugswsise durch Behandlung mit einer Säure wie Salzsäure gegebenenfalls in Gegenwart eines Lösungsmittels wie Essigsäure bei Temperaturen zwischen 50 und 120°C oder durch Behandlung mit Natronlauge gegebenenfalls in Gegenwart eines Lösungsmittels wie Tetrahydrofuran oder Methanol bei Temperaturen zwischen 0 und 50°C.The Cleavage of a used acyl, acetal or ketal protecting group For example, it is carried out hydrolytically in an aqueous solvent, e.g. in water, Isopropanol / water, acetic acid / water, Tetrahydrofuran / water or dioxane / water, in the presence of an acid such as trifluoroacetic, hydrochloric acid or sulfuric acid or in the presence of an alkali metal base such as lithium hydroxide, sodium hydroxide or potassium hydroxide or aprotic, e.g. in the presence of iodotrimethylsilane, at temperatures between 0 and 120 ° C, preferably at temperatures between 10 and 100 ° C. The cleavage of a trifluoroacetyl radical is preferably carried out by Treatment with an acid like hydrochloric acid optionally in the presence of a solvent such as acetic acid Temperatures between 50 and 120 ° C or by treatment with caustic soda optionally in the presence of a solvent such as tetrahydrofuran or methanol at temperatures between 0 and 50 ° C.
Die Abspaltung eines Trimethylsilylrestes erfolgt beispielsweise in Wasser, einem wässrigen Lösemittelgemisch oder einem niederen Alkohol wie Methanol oder Ethanol in Gegenwart einer Base wie Lithiumhydroxid, Natriumhydroxid, Kaliumcarbonat oder Natriummethylat. In wässrigen oder alkoholischen Lösungsmitteln eignen sich ebenfalls Säuren, wie z.B. Salzsäure, Trifluoressigsäure oder Essigsäure. Zur Abspaltung in organischen Lösungsmitteln, wie beispielsweise Diethylether, Tetrahydrofuran oder Dichlormethan, eignen sich auch Fluoridreagenzien, wie z.B. Tetrabutylammoniumfluorid.The Cleavage of a Trimethylsilylrestes takes place for example in Water, an aqueous Solvent mixture or a lower alcohol such as methanol or ethanol in the presence a base such as lithium hydroxide, sodium hydroxide, potassium carbonate or sodium methylate. In aqueous or alcoholic solvents are also acids, such as. Hydrochloric acid, trifluoroacetic or acetic acid. For cleavage in organic solvents, such as diethyl ether, tetrahydrofuran or dichloromethane, Also suitable are fluoride reagents, e.g. Tetrabutylammonium fluoride.
Die Abspaltung eines Benzyl-, Methoxybenzyl- oder Benzyloxycarbonylrestes erfolgt vorteilhaft hydrogenolytisch, z.B. mit Wasserstoff in Gegenwart eines Katalysators wie Palladium/Kohle in einem geeigneten Lösungsmittel wie Methanol, Ethanol, Essigsäureethylester oder Eisessig, gegebenenfalls unter Zusatz einer Säure wie Salzsäure bei Temperaturen zwischen 0 und 100°C, vorzugsweise jedoch bei Raumtemperaturen zwischen 20 und 60°C, und bei einem Wasserstoffdruck von 1 bis 7 bar, vorzugsweise jedoch von 3 bis 5 bar. Die Abspaltung eines 2,4-Dimethoxy-benzylrestes erfolgt jedoch vorzugsweise in Trifluoressigsäure in Gegenwart von Anisol.The Cleavage of a benzyl, methoxybenzyl or Benzyloxycarbonylrestes advantageously takes place hydrogenolytically, e.g. with hydrogen in the presence a catalyst such as palladium / carbon in a suitable solvent such as methanol, ethanol, ethyl acetate or glacial acetic acid, optionally with the addition of an acid such as hydrochloric acid at temperatures between 0 and 100 ° C, but preferably at room temperatures between 20 and 60 ° C, and at a hydrogen pressure of 1 to 7 bar, but preferably from 3 to 5 bar. The cleavage of a 2,4-dimethoxy-benzyl radical takes place however, preferably in trifluoroacetic acid in the presence of anisole.
Die Abspaltung eines tert.-Butyl- oder tert.-Butyloxycarbonylrestes erfolgt vorzugsweise durch Behandlung mit einer Säure wie Trifluoressigsäure oder Salzsäure oder durch Behandlung mit Jodtrimethylsilan gegebenenfalls unter Verwendung eines Lösungsmittels wie Methylenchlorid, Dioxan, Methanol oder Diethylether.The Cleavage of a tert-butyl or tert-Butyloxycarbonylrestes is preferably carried out by treatment with an acid such as trifluoroacetic or hydrochloric acid or optionally by treatment with iodotrimethylsilane Use of a solvent such as methylene chloride, dioxane, methanol or diethyl ether.
Bei den vorstehend beschriebenen Umsetzungen können gegebenenfalls vorhandene reaktive Gruppen wie Ethinyl-, Hydroxy-, Amino-, Alkylamino- oder Iminogruppen während der Umsetzung durch übliche Schutzgruppen geschützt werden, welche nach der Umsetzung wieder wie u.a. oben beschrieben abgespalten werden.at The reactions described above may optionally be present reactive groups such as ethynyl, hydroxy, amino, alkylamino or Imino groups during the implementation by conventional protecting groups protected which, after the implementation again like u.a. described above be split off.
Beispielsweise kommt als Schutzrest für eine Ethinylgruppe die Trimethylsilyl-gruppe in Betracht.For example comes as a protective rest for an ethynyl group is the trimethylsilyl group.
Beispielsweise kommen als Schutzrest für eine Hydroxygruppe die Trimethylsilyl-, Acetyl-, Trityl-, Benzyl- oder Tetrahydropyranylgruppe in Betracht.For example come as a protective rest for a hydroxy group the trimethylsilyl, acetyl, trityl, benzyl or tetrahydropyranyl group.
Als Schutzreste für eine Amino-, Alkylamino- oder Iminogruppe kommen beispielsweise die Formyl-, Acetyl-, Trifluoracetyl-, Ethoxycarbonyl-, tert.-Butoxycarbonyl-, Benzyloxycarbonyl-, Benzyl-, Methoxybenzyl- oder 2,4-Dimethoxybenzylgruppe in Betracht.When Protection residues for an amino, alkylamino or imino group, for example the formyl, acetyl, trifluoroacetyl, ethoxycarbonyl, tert-butoxycarbonyl, Benzyloxycarbonyl, benzyl, methoxybenzyl or 2,4-dimethoxybenzyl group into consideration.
Des Weiteren können die so erhaltenen Verbindungen der allgemeinen Formel I selektiv an einer Hydroxygruppe derivatisiert oder die Hydroxygruppe selbst substituiert werden.Furthermore, the compounds of the general formula I thus obtained can be obtained selectively on a Hy droxygruppe derivatized or the hydroxy group itself be substituted.
Ferner können die erhaltenen Verbindungen der allgemeinen Formel I, wie bereits eingangs erwähnt wurde, in ihre Enantiomeren und/oder Diastereomeren aufgetrennt werden. So können beispielsweise cis-/trans-Gemische in ihre cis- und trans-Isomere, und Verbindungen mit mindestens einem optisch aktiven Kohlenstoffatom in ihre Enantiomeren aufgetrennt werden.Further can the obtained compounds of general formula I, as already was mentioned in the beginning, be separated into their enantiomers and / or diastereomers. So can for example cis / trans mixtures into their cis and trans isomers, and compounds having at least one optically active carbon atom be separated into their enantiomers.
So lassen sich beispielsweise die erhaltenen cis-/trans-Gemische durch Chromatographie in ihre cis- und trans-Isomeren, die erhaltenen Verbindungen der allgemeinen Formel I, welche in Racematen auftreten, nach an sich bekannten Methoden (siehe Allinger N. L. und Eliel E. L. in "Topics in Stereochemistry", Vol. 6, Wiley Interscience, 1971) in ihre optischen Antipoden und Verbindungen der allgemeinen Formel I mit mindestens 2 asymmetrischen Kohlenstoffatomen auf Grund ihrer physikalischchemischen Unterschiede nach an sich bekannten Methoden, z.B. durch Chromatographie und/oder fraktionierte Kristallisation, in ihre Diastereomeren auftrennen, die, falls sie in racemischer Form anfallen, anschließend wie oben erwähnt in die Enantiomeren getrennt werden können.So For example, the resulting cis / trans mixtures can be allowed to pass through Chromatography into their cis and trans isomers, the obtained Compounds of general formula I, which occur in racemates after methods known per se (see Allinger N.L. and Eliel E.L. in "Topics in Stereochemistry", Vol. 6, Wiley Interscience, 1971) into their optical antipodes and compounds of the general Formula I with at least 2 asymmetric carbon atoms due their physicochemical differences according to known Methods, e.g. by chromatography and / or fractional crystallisation, into their diastereomers, which, if they are in racemic Form incurred, then as mentioned above can be separated into the enantiomers.
Die Enantiomerentrennung erfolgt vorzugsweise durch Säulentrennung an chiralen Phasen oder durch Umkristallisieren aus einem optisch aktiven Lösungsmittel oder durch Umsetzen mit einer, mit der racemischen Verbindung Salze oder Derivate wie z.B. Ester oder Amide bildenden optisch aktiven Substanz, insbesondere Säuren und ihre aktivierten Derivate oder Alkohole, und Trennen des auf diese Weise erhaltenen diastereomeren Salzgemisches oder Derivates, z.B. auf Grund von verschiedenen Löslichkeiten, wobei aus den reinen diastereomeren Salzen oder Derivaten die freien Antipoden durch Einwirkung geeigneter Mittel freigesetzt werden können. Besonders gebräuchliche, optisch aktive Säuren sind z.B. die D- und L-Formen von Weinsäure oder Dibenzoylweinsäure, Di-O-Tolylweinsäure, Äpfelsäure, Mandelsäure, Camphersulfonsäure, Glutaminsäure, Asparaginsäure oder Chinasäure. Als optisch aktiver Alkohol kommt beispielsweise (+)- oder (–)-Menthol und als optisch aktiver Acylrest in Amiden beispielsweise (+)- oder (–)-Menthyloxycarbonyl in Betracht.The Enantiomer separation is preferably carried out by column separation on chiral phases or by recrystallization from an optical active solvents or by reacting with one, with the racemic compound salts or derivatives such as e.g. Ester or amide-forming optically active Substance, especially acids and their activated derivatives or alcohols, and separating the this diastereomeric salt mixture or derivative obtained, e.g. due to different solubilities, where from the pure diastereomeric salts or derivatives of the free antipodes can be released by the action of appropriate means. Especially common, optically active acids are e.g. the D and L forms of tartaric or dibenzoyltartaric, di-O-toluenoic, malic, mandelic, camphorsulfonic, glutamic, aspartic or China acid. As an optically active alcohol, for example, (+) - or (-) - menthol and as an optically active acyl radical in amides, for example (+) - or (-) - menthyloxycarbonyl into consideration.
Des Weiteren können die erhaltenen Verbindungen der Formel I in ihre Salze, insbesondere für die pharmazeutische Anwendung in ihre physiologisch verträglichen Salze mit anorganischen oder organischen Säuren, übergeführt werden. Als Säuren kommen hierfür beispielsweise Salzsäure, Bromwasserstoffsäure, Schwefelsäure, Methansulfonsäure, Phosphorsäure, Fumarsäure, Bernsteinsäure, Milchsäure, Zitronensäure, Weinsäure oder Maleinsäure in Betracht.Of Further can the compounds of the formula I obtained in their salts, in particular for the pharmaceutical Use in their physiologically acceptable salts with inorganic or organic acids. As acids come for this for example, hydrochloric acid, Hydrobromic acid, sulfuric acid, methanesulfonic acid, phosphoric acid, fumaric acid, succinic acid, lactic acid, citric acid, tartaric acid or maleic into consideration.
Weiterhin können die erhaltenen Verbindungen in Gemische, beispielsweise in 1:1 oder 1:2 Gemische mit Aminosäuren, insbesondere mit alpha-Aminosäuren wie Prolin oder Phenylalanin, übergeführt werden, die besonders günstige Eigenschaften wie hohe Kristallinität aufweisen können.Farther can the compounds obtained in mixtures, for example in 1: 1 or 1: 2 mixtures with amino acids, especially with alpha-amino acids like proline or phenylalanine, the most favorable Properties such as high crystallinity may have.
Die als Ausgangsstoffe verwendeten Verbindungen der allgemeinen Formeln II und III sind teilweise literaturbekannt oder können nach an sich literaturbekannten Verfahren sowie in Analogie zu den in den Beispielen beschriebenen Verfahren, gegebenenfalls unter zusätzlicher Einführung von Schutzresten, erhalten werden.The used as starting materials compounds of the general formulas II and III are partly known from the literature or can after in literature known methods and in analogy to the in Examples described in the examples, optionally with additional introduction of protective residues.
Die erfindungsgemäßen Verbindungen sind vorteilhaft auch nach den in den nachfolgenden Beispielen beschriebenen Verfahren zugänglich, wobei diese hierzu auch mit dem Fachmann beispielsweise aus der Literatur bekannten Verfahren, insbesondere den in den WO 98/31697, WO 01/27128, WO 02/083066 und WO 03/099836 beschriebenen Verfahren, kombiniert werden können.The Compounds of the invention are also advantageous according to those described in the following examples Method accessible, this also with the expert, for example, from the literature known methods, in particular those described in WO 98/31697, WO 01/27128, WO 02/083066 and WO 03/099836, combined can be.
Wie bereits eingangs erwähnt, weisen die erfindungsgemäßen Verbindungen der allgemeinen Formel I und ihre physiologisch verträglichen Salze wertvolle pharmakologische Eigenschaften auf, insbesondere eine Hemmwirkung auf den natriumabhängigen Glucose-Cotransporter SGLT, vorzugsweise SGLT2.As already mentioned at the beginning, have the compounds of the invention the general formula I and their physiologically acceptable Salts have valuable pharmacological properties, in particular an inhibitory effect on the sodium-dependent glucose cotransporter SGLT, preferably SGLT2.
Die
biologischen Eigenschaften der neuen Verbindungen können wie
folgt geprüft
werden:
Die Fähigkeit
der Substanzen die SGLT-2 Aktivität zu hemmen, kann in einem
Versuchsaufbau gezeigt werden, in dem eine CHO-K1 Zelllinie (ATCC
No. CCL 61) oder alternativ eine HEK293 Zelllinie (ATCC No. CRL-1573),
die stabil mit einem Expressionsvektor pZeoSV (Invitrogen, EMBL
accession number L36849) transfiziert ist, der die cDNA für die kodierende
Sequenz des humanen Natrium Glucose Cotransporters 2 (Genbank Acc.
No. NM_003041) enthält
(CHO-hSGLT2 bzw. HEK-hSGLT2).
Diese Zelllinien transportieren Natrium-abhängig 14C-markiertes
alpha-Methyl-Glucopyranosid
(14C-AMG, Amersham) in das Zellinnere.The biological properties of the new compounds can be tested as follows:
The ability of the substances to inhibit SGLT-2 activity can be demonstrated in an experimental setup in which a CHO-K1 cell line (ATCC No. CCL 61) or alternatively a HEK293 cell line (ATCC No. CRL-1573), stable with an expression vector pZeoSV (Invitrogen, EMBL accession number L36849) which contains the cDNA for the coding sequence of the human sodium glucose cotransporter 2 (Genbank Acc No. NM_003041) (CHO-hSGLT2 or HEK-hSGLT2). These cell lines transport sodium-dependent 14 C-labeled alpha-methyl-glucopyranoside ( 14 C-AMG, Amersham) into the cell interior.
Der
SGLT-2 Assay wird wie folgt durchgeführt:
CHO-hSGLT2 Zellen
werden in Ham's
F12 Medium (BioWhittaker) mit 10% fötalem Kälberserum und 250 μg/ml Zeocin
(Invitrogen), HEK293-hSGLT2 Zellen in DMEM Medium mit 10% fötalem Kälberserum
und 250 μg/ml
Zeocin (Invitrogen) kultiviert. Die Zellen werden von den Kulturflaschen
durch zweimaliges Waschen mit PBS und anschließende Behandlung mit Trypsin/EDTA
abgelöst.
Nachzugabe von Zellkulturmedium werden die Zellen abzentrifugiert,
in Kulturmedium resuspendiert und in einem Casy-cell-counter gezählt. Anschließend werden
40.000 Zellen pro Loch in eine weiße, Poly-D-Lysin beschichtete
96-Loch Platte ausgesät
und über
Nacht bei 37°C,
5% CO2 inkubiert. Die Zellen werden zweimal
mit 250μl
Assaypuffer (Hanks Balanced Salt Solutioni, 137 mM NaCl, 5,4 mM
KCl, 2,8 mM CaCl2, 1,2 mM MgSO4 und
10 mM HEPES (pH7,4), 50 μg/ml Gentamycin)
gewaschen. In jedes Loch werden dann 250 μl Assaypuffer und 5 μl Testverbindung
hinzugegeben und für
weitere 15 Minuten im Brutschrank inkubiert. Als Negativkontrolle
werden 5 μl
10% DMSO eingesetzt. Durch Zugabe von 5 μl 14C-AMG
(0.05 μCi)
in jedes Loch wird die Reaktion gestartet. Nach einer 2 stündigen Inkubation
bei 37°C,
5% CO2 werden die Zellen wiederum mit 250 μl PBS (20°C) gewaschen
und anschließend
durch Zugabe von 25 μl
0.1 N NaOH lysiert (5 min. bei 37°C).
Pro Loch werden 200 μl
MicroScint20 (Packard) hinzugefügt
und für
weitere 20 min bei 37°C
inkubiert. Nach dieser Inkubation wird die Radioaktivität des aufgenommenen 14C-AMG in einem Topcount (Packard) mittels
eines 14C-Szintillationsprogramms gemessen.The SGLT-2 assay is performed as follows:
CHO-hSGLT2 cells are cultured in Ham's F12 medium (BioWhittaker) with 10% fetal calf serum and 250 μg / ml Zeocin (Invitrogen), HEK293-hSGLT2 cells in DMEM medium with 10% fetal calf serum and 250 μg / ml Zeocin (Invitrogen). The cells are detached from the culture flasks by washing twice with PBS and subsequent treatment with trypsin / EDTA. After addition of cell culture medium, the cells are centrifuged off, resuspended in culture medium and counted in a Casy cell counter. Subsequently, 40,000 cells per well are seeded in a white, poly-D-lysine coated 96-well plate and incubated overnight at 37 ° C, 5% CO 2 . Cells are washed twice with 250μl assay buffer (Hanks Balanced Salt Solutioni, 137mM NaCl, 5.4mM KCl, 2.8mM CaCl 2 , 1.2mM MgSO 4 and 10mM HEPES (pH 7.4), 50μg / ml Gentamycin). 250 μl of assay buffer and 5 μl of test compound are then added to each well and incubated for an additional 15 minutes in the incubator. The negative control used is 5 μl of 10% DMSO. By adding 5 μl of 14 C-AMG (0.05 μCi) to each well, the reaction is started. After a 2 hour incubation at 37 ° C., 5% CO 2 , the cells are again washed with 250 μl PBS (20 ° C.) and subsequently lysed by addition of 25 μl 0.1 N NaOH (5 min at 37 ° C.). 200 μl MicroScint20 (Packard) are added per well and incubated for a further 20 min at 37 ° C. After this incubation, the radioactivity of the ingested 14 C-AMG is measured in a Topcount (Packard) using a 14 C scintillation program.
Zur Bestimmung der Selektivität gegenüber dem humanen SGLT1 wird ein analoger Test aufgebaut, in dem die cDNA für hSGLT1 (Genbank Acc. No. NM000343) statt der hSGLT2 cDNA in CHO-K1 bzw. HEK293 Zellen exprimiert wird.to Determination of selectivity across from the human SGLT1 an analogous test is constructed in which the cDNA for hSGLT1 (Genbank Acc No. NM000343) instead of the hSGLT2 cDNA in CHO-K1 or HEK293 cells is expressed.
Alternativ kann für hSGLT1 und hSGLT2 auch die Messung des zellulären Membranpotentials zur biologischen Testung von Substanzen herangezogen werden. Hierzu können die weiter oben beschriebenen Zellmodelle angewendet werden. Für den Test werden 10.000 Zellen pro Loch einer poly-D-Lysin beschichteten schwarzen 384-Loch-Platte mit durchsichtigem Boden in Kulturmedium ausgesät und 16 Stunden bei 37°C, 5% CO2 inkubiert. Anschließend werden die Zellen zweimal mit glucosefreiem HBSS Puffer (12,67 mol/l CaCl2, 4,93 mmol/l MgCl2, 4,07 mmol/l MgSO4, 4,41 mmol/l KH2PO4; pH 7,4) gewaschen und mit 20μl HBSS überschichtet. Nach Zugabe von 20 μl Ladepuffer (Membrane Potential Assay Kit Explorer R8126, Molecular Devices GmbH, Ismaning) und 20 μl der zu testenden Substanz in geeigneter Konzentration wird für weitere 30 min. bei 37°C, 5% CO2 inkubiert. Die Messung erfolgt im Fluorescent Imaging Plate Reader (Molecular Devices GmbH, Ismaning) bei 485 nm Anregungswellenlänge und wird durch Zugabe von 20μl Stimulationspuffer (140 mM NaCl und 120 mM Glucose) gestartet. Die durch den Glucose-induzierten Na+-Einstrom verursachte Depolarisation der Zelle kann als Fluoreszenzänderung gemessen und quantifiziert werden.Alternatively, for hSGLT1 and hSGLT2, the measurement of cellular membrane potential can also be used for the biological testing of substances. For this purpose, the cell models described above can be used. For the assay, 10,000 cells per well of a poly-D-lysine coated 384-well black plate with clear bottom are seeded in culture medium and incubated for 16 hours at 37 ° C, 5% CO 2 . The cells are then washed twice with glucose-free HBSS buffer (12.67 mol / l CaCl 2 , 4.93 mmol / l MgCl 2 , 4.07 mmol / l MgSO 4 , 4.41 mmol / l KH 2 PO 4 , pH 7 , 4) and overlaid with 20 μl of HBSS. After addition of 20 .mu.l loading buffer (Membrane Potential Assay Kit Explorer R8126, Molecular Devices GmbH, Ismaning) and 20 .mu.l of the substance to be tested in a suitable concentration is for a further 30 min. incubated at 37 ° C, 5% CO 2 . The measurement takes place in the Fluorescent Imaging Plate Reader (Molecular Devices GmbH, Ismaning) at 485 nm excitation wavelength and is started by adding 20 μl stimulation buffer (140 mM NaCl and 120 mM glucose). The depolarization of the cell caused by the glucose-induced Na + influx can be measured and quantified as a change in fluorescence.
Die erfindungsgemäßen Verbindungen der allgemeinen Formel I können beispielsweise EC50-Werte unter 1000 nM, insbesondere unter 200 nM, besonders bevorzugt unter 50 nM aufweisen.The Compounds of the invention of general formula I can for example, EC50 values below 1000 nM, in particular below 200 nM, more preferably below 50 nM.
Im Hinblick auf die Fähigkeit, die SGLT Aktivität zu hemmen, sind die erfindungsgemäßen Verbindungen der allgemeinen Formel I und ihre entsprechenden pharmazeutisch akzeptablen Salze prinzipiell geeignet, alle diejenigen Zustände oder Krankheiten zu behandeln und/oder vorbeugend zu behandeln, die durch eine Hemmung der SGLT Aktivität, insbesondere der SGLT-2 Aktivität beeinflusst werden können. Daher sind erfindungsgemäße Verbindungen insbesondere zur Prophylaxe oder Behandlung von Krankheiten, insbesondere Stoffwechselerkrankungen, oder Zuständen wie Diabetes mellitus Typ 1 und Typ 2, diabetische Komplikationen (wie z.B. Retinopathie, Nephropathie oder Neuropathien, diabetischer Fuß, Ulcus, Makroangiopathien), metabolische Azidose oder Ketose, reaktiver Hypoglykämie, Hyperinsulinämie, Glukosestoffwechselstörung, Insulinresistenz, Metabolischem Syndrom, Dyslipidämien unterschiedlichster Genese, Atherosklerose und verwandte Erkrankungen, Adipositas, Bluthochdruck, chronisches Herzversagen, Ödeme, Hyperurikämie geeignet. Darüber hinaus sind diese Substanzen geeignet, die beta-Zelldegeneration wie z.B. Apoptose oder Nekrose von pankreatischen beta-Zellen zu verhindern. Die Substanzen sind weiter geeignet, die Funktionalität von pankreatischen Zellen zu verbessern oder wiederherzustellen, daneben die Anzahl und Größe von pankreatischen beta-Zellen zu erhöhen. Die erfindungsgemäßen Verbindungen sind ebenfalls als Diuretika oder Antihypertensiva einsetzbar und zur Prophylaxe und Behandlung des akuten Nierenversagens geeignet.in the Regard to the ability the SGLT activity to inhibit, the compounds of the invention are the general Formula I and its corresponding pharmaceutically acceptable salts in principle suitable to treat all those conditions or diseases and / or preventively treat by inhibiting the SGLT Activity, especially the SGLT-2 activity can be influenced. Therefore, compounds of the invention in particular for the prophylaxis or treatment of diseases, in particular Metabolic diseases, or conditions such as diabetes mellitus Type 1 and Type 2, diabetic complications (such as retinopathy, Nephropathy or neuropathies, diabetic foot, ulcer, macroangiopathies), metabolic Acidosis or ketosis, reactive hypoglycemia, hyperinsulinemia, glucose metabolism disorder, insulin resistance, Metabolic syndrome, dyslipidemias different genesis, atherosclerosis and related diseases, Obesity, hypertension, chronic heart failure, edema, hyperuricemia suitable. About that In addition, these substances are suitable, the beta cell degeneration such. Apoptosis or To prevent necrosis of pancreatic beta cells. The substances are more suitable for the functionality of pancreatic cells To improve or restore, in addition, the number and size of pancreatic increase beta cells. The compounds of the invention are also useful as diuretics or antihypertensives and suitable for the prophylaxis and treatment of acute renal failure.
Ganz besonders sind die erfindungsgemäßen Verbindungen, einschließlich deren physiologisch verträglichen Salze, zur Prophylaxe oder Behandlung von Diabetes, insbesondere Diabetes mellitus Typ 1 und Typ 2, und/oder diabetischen Komplikationen geeignet.All especially the compounds according to the invention, including their physiologically acceptable Salts, for the prophylaxis or treatment of diabetes, in particular Diabetes mellitus type 1 and type 2, and / or diabetic complications suitable.
Die zur Erzielung einer entsprechenden Wirkung bei der Behandlung oder Prophylaxe erforderliche Dosierung hängt üblicherweise von der zu verabreichenden Verbindung, vom Patienten, von der Art und Schwere der Krankheit oder des Zustandes und der Art und Häufigkeit der Verabreichung ab und liegt im Ermessen des zu behandelnden Arztes. Zweckmäßigerweise kann die Dosierung bei intravenöser Gabe im Bereich von 1 bis 100 mg, vorzugsweise 1 bis 30 mg, und bei oraler Gabe im Bereich von 1 bis 1000 mg, vorzugsweise 1 bis 100 mg, jeweils 1 bis 4 × täglich, liegen. Hierzu lassen sich die erfindungsgemäß hergestellten Verbindungen der Formel I, gegebenenfalls in Kombination mit anderen Wirksubstanzen, zusammen mit einem oder mehreren inerten üblichen Trägerstoffen und/oder Verdünnungsmitteln, z.B. mit Maisstärke, Milchzucker, Rohrzucker, mikrokristalliner Zellulose, Magnesiumstearat, Polyvinylpyrrolidon, Zitronensäure, Weinsäure, Wasser, Wasser/Ethanol, Wasser/Glycerin, Wasser/Sorbit, Wasser/Polyethylenglykol, Propylenglykol, Cetylstearylalkohol, Carboxymethylcellulose oder fetthaltigen Substanzen wie Hartfett oder deren geeigneten Gemischen, in übliche galenische Zubereitungen wie Tabletten, Dragees, Kapseln, Pulver, Lösungen, Suspensionen oder Zäpfchen einarbeiten.The dosage required to achieve a corresponding effect in the treatment or prophylaxis usually depends on the compound to be administered, on the patient, on the type and Severity of the disease or condition, and the nature and frequency of administration, and is at the discretion of the physician to be treated. Conveniently, the dosage with intravenous administration in the range of 1 to 100 mg, preferably 1 to 30 mg, and in oral administration in the range of 1 to 1000 mg, preferably 1 to 100 mg, each 1 to 4 times a day. For this purpose, the compounds of the formula I according to the invention, optionally in combination with other active substances, together with one or more inert customary carriers and / or diluents, for example with corn starch, lactose, cane sugar, microcrystalline cellulose, magnesium stearate, polyvinylpyrrolidone, citric acid, tartaric acid, Water, water / ethanol, water / glycerol, water / sorbitol, water / polyethylene glycol, propylene glycol, cetylstearyl alcohol, carboxymethylcellulose or fatty substances such as hard fat or their suitable mixtures in common pharmaceutical preparations such as tablets, dragees, capsules, powders, solutions, suspensions or Incorporate suppositories.
Die erfindungsgemäßen Verbindungen können auch in Kombination mit anderen Wirkstoffen, insbesondere zur Behandlung und/oder Prophylaxe der zuvor angegebenen Krankheiten und Zustände verwendet werden. Für solche Kombinationen kommen als weitere Wirksubstanzen insbesondere solche in Betracht, die beispielsweise die therapeutische Wirksamkeit eines erfindungsgemäßen SGLT-Antagonisten im Hinblick auf eine der genannten Indikationen verstärken und/oder die eine Reduzierung der Dosierung eines erfindungsgemäßen SGLT-Antagonisten erlauben. Zu den zu einer solchen Kombination geeigneten Therapeutika gehören z.B. Antidiabetika, wie etwa Metformin, Sulfonylharnstoffe (z.B. Glibenclamid, Tolbutamid, Glimepiride), Nateglinide, Repaglinide, Thiazolidindione (z.B. Rosiglitazone, Pioglitazone), PPAR-gamma-Agonisten (z.B. GI 262570) und -Antagonisten, PPAR-gamma/alpha Modulatoren (z.B. KRP 297), alpha-Glucosidasehemmer (z.B. Acarbose, Voglibose), DPPIV Inhibitoren (z.B. LAF237, MK-431), alpha2-Antagonisten, Insulin und Insulinanaloga, GLP-1 und GLP-1 Analoga (z.B. Exendin-4) oder Amylin. Daneben sind weitere als Kombinationspartner geeignete Wirkstoffe Inhibitoren der Proteintyrosinphosphatase 1, Substanzen, die eine deregulierte Glucoseproduktion in der Leber beeinflussen, wie z.B. Inhibitoren der Glucose-6-phosphatase, oder der Fructose-1,6-bisphosphatase, der Glycogenphosphorylase, Glucagonrezeptor Antagonisten und Inhibitoren der Phosphoenolpyruvatcarboxykinase, der Glykogensynthasekinase oder der Pyruvatdehydrokinase, Lipidsenker, wie etwa HMG-CoA-Reduktasehemmer (z.B. Simvastatin, Atorvastatin), Fibrate (z.B. Bezafibrat, Fenofibrat), Nikotinsäure und deren Derivate, PPAR-alpha Agonisten, PPAR-delta Agonisten, ACAT Inhibitoren (z.B. Avasimibe) oder Cholesterolresorptionsinhibitoren wie zum Beispiel Ezetimibe, gallensäurebindende Substanzen wie zum Beispiel Colestyramin, Hemmstoffe des ilealen Gallensäuretransportes, HDL-erhöhende Verbindungen wie zum Beispiel Inhibitoren von CETP oder Regulatoren von ABC1 oder Wirkstoffe zur Behandlung von Obesitas, wie etwa Sibutramin oder Tetrahydrolipstatin, Dexfenfluramin, Axokine, Antagonisten des Cannabinoid1 Rezeptors, MCH-1 Rezeptorantagonisten, MC4 Rezeptor Agonisten, NPY5 oder NPY2 Antagonisten oder β3-Agonisten wie SB-418790 oder AD-9677 ebenso wie Agonisten des 5HT2c Rezeptors.The Compounds of the invention can also in combination with other active substances, in particular for treatment and / or prophylaxis of the aforementioned diseases and conditions. For such combinations come as further active substances in particular those into consideration, for example, the therapeutic efficacy of a SGLT antagonist according to the invention in terms of to reinforce one of the indicated indications and / or a reduction allow the dosage of a SGLT antagonist of the invention. Therapeutics suitable for such combination include e.g. Antidiabetics, such as metformin, sulfonylureas (e.g., glibenclamide, Tolbutamide, glimepiride), nateglinides, repaglinide, thiazolidinediones (e.g., rosiglitazone, pioglitazone), PPAR gamma agonists (e.g., GI 262570) and antagonists, PPAR-gamma / alpha modulators (e.g., KRP 297), alpha-glucosidase inhibitors (e.g., acarbose, voglibose), DPPIV Inhibitors (e.g., LAF237, MK-431), alpha2 antagonists, insulin and insulin analogs, GLP-1 and GLP-1 analogs (e.g., exendin-4) or Amylin. In addition, other suitable as combination partners active ingredients Inhibitors of protein tyrosine phosphatase 1, substances that have a deregulated glucose production in the liver, e.g. Inhibitors of glucose-6-phosphatase, or fructose-1,6-bisphosphatase, glycogen phosphorylase, glucagon receptor antagonists and inhibitors the phosphoenolpyruvate carboxykinase, the glycogen synthase kinase or pyruvate dehydrokinase, lipid lowering agents such as HMG CoA reductase inhibitors (e.g., simvastatin, atorvastatin), fibrates (e.g., bezafibrate, fenofibrate), niacin and their derivatives, PPAR-alpha agonists, PPAR-delta agonists, ACAT inhibitors (e.g., Avasimibe) or cholesterol resorption inhibitors such as ezetimibe, bile acid-binding substances such as for example colestyramine, inhibitors of ileal bile acid transport, HDL-raising Compounds such as inhibitors of CETP or regulators of ABC1 or agents for the treatment of obesity, such as sibutramine or tetrahydrolipstatin, dexfenfluramine, axokines, antagonists of the cannabinoid 1 receptor, MCH-1 receptor antagonist, MC4 receptor Agonists, NPY5 or NPY2 antagonists or β3 agonists such as SB-418790 or AD-9677 as well as agonists of the 5HT2c receptor.
Daneben ist eine Kombination mit Medikamenten zur Beeinflussung des Bluthochdrucks, des chronischen Herzversagens oder der Atherosklerose wie z.B. A-II Antagonisten oder ACE Inhibitoren, ECE-Inhibitoren, Diuretika, β-Blocker, Ca-Antagonisten, zentral wirksamen Antihypertensiva, Antagonisten des alpha-2-adrenergen Rezeptors, Inhibitoren der neutralen Endopeptidase, Thrombozytenaggregationshemmer und anderen oder Kombinationen daraus geeignet. Beispiele von Angiotensin II Rezeptor Antagonisten sind Candesartan Cilexetil, Kalium Losartan, Eprosartan Mesylat, Valsartan, Telmisartan, Irbesartan, EXP-3174, L-158809, EXP-3312, Olmesartan, Medoxomil, Tasosartan, KT-3-671, GA-0113, RU-64276, EMD-90423, BR-9701, etc. Angiotensin II Rezeptor Antagonisten werden vorzugsweise zur Behandlung oder Prophylaxe von Bluthochdruck und diabetischen Komplikationen verwendet, oft in Kombination mit einem Diuretikum wie Hydrochlorothiazide.Besides is a combination with drugs to influence high blood pressure, chronic heart failure or atherosclerosis, e.g. A-II Antagonists or ACE inhibitors, ECE inhibitors, diuretics, β-blockers, Ca antagonists, centrally acting antihypertensives, antagonists of the alpha-2-adrenergic receptor, Inhibitors of neutral endopeptidase, platelet aggregation inhibitors and others or combinations thereof. Examples of angiotensin II receptor antagonists are candesartan cilexetil, potassium losartan, Eprosartan Mesylate, Valsartan, Telmisartan, Irbesartan, EXP-3174, L-158809, EXP-3312, olmesartan, medoxomil, tasosartan, KT-3-671, GA-0113, RU-64276, EMD-90423, BR-9701, etc. Angiotensin II receptor antagonists are preferably used for the treatment or prophylaxis of hypertension and diabetic complications, often in combination with a diuretic such as hydrochlorothiazide.
Zur Behandlung oder Prophylaxe der Gicht ist eine Kombination mit Harnsäuresynthese Inhibitoren oder Urikosurika geeignet.to Treatment or prophylaxis of gout is a combination with uric acid synthesis Inhibitors or uricosurics suitable.
Zur Behandlung oder Prophylaxe diabetischer Komplikationen kann eine Kombination mit GABA-Rezeptor-Antagonisten, Na-Kanal-Blockern, Topiramat, Protein-Kinase C Inhibitoren, advanced glycation endproduct Inhibitoren oder Aldose Reduktase Inhibitoren erfolgen.to Treatment or prophylaxis of diabetic complications may be one Combination with GABA receptor antagonists, Na channel blockers, topiramate, Protein kinase C inhibitors, advanced glycation endproduct inhibitors or aldose reductase inhibitors.
Die Dosis für die zuvor angeführten Kombinationspartner beträgt hierbei zweckmäßigerweise 1/5 der üblicherweise empfohlenen niedrigsten Dosierung bis zu 1/1 der normalerweise empfohlenen Dosierung.The Dose for the previously mentioned Combination partner is this expediently 1/5 of the usual recommended lowest dosage up to 1/1 of the normally recommended Dosage.
Daher betrifft ein weiterer Gegenstand dieser Erfindung die Verwendung einer erfindungsgemäßen Verbindung oder eines physiologisch verträglichen Salzes solch einer Verbindung in Kombination mit mindestens einem der zuvor als Kombinationspartner beschriebenen Wirkstoffe zur Herstellung eines Arzneimittels, das zur Behandlung oder Prophylaxe von Erkrankungen oder Zuständen geeignet ist, die durch Inhibierung des natriumabhängigen Glucose-Cotransporters SGLT beeinflussbar sind. Hierbei handelt es sich vorzugsweise um eine Stoffwechselerkrankung, insbesondere eine der zuvor angeführten Erkrankungen oder Zustände, ganz besonders Diabetes oder diabetischer Komplikationen.Therefore, another object of this invention relates to the use of a compound of the invention or a physiologically acceptable salt of such a compound in combination with at least one of the active ingredients previously described as combination partners for the preparation of a medicament, which is suitable for the treatment or prophylaxis of diseases or conditions which can be influenced by inhibition of the sodium-dependent glucose cotransporter SGLT. This is preferably a metabolic disorder, in particular one of the previously mentioned diseases or conditions, especially diabetes or diabetic complications.
Die Verwendung der erfindungsgemäßen Verbindung, oder eines physiologisch verträglichen Salzes hiervon, in Kombination mit einem weiteren Wirkstoff kann zeitgleich oder zeitlich versetzt, insbesondere aber zeitnah erfolgen. Bei einer zeitgleichen Verwendung werden beide Wirkstoffe dem Patienten zusammen verabreicht; bei einer zeitlich versetzten Verwendung werden beide Wirkstoffe dem Patienten in einem Zeitraum von kleiner gleich 12, insbesondere kleiner gleich 6 Stunden nacheinander verabreicht.The Use of the compound according to the invention, or a physiologically acceptable one Salt thereof, in combination with another active ingredient at the same time or offset in time, but in particular carried out promptly. When used concurrently, both agents are given to the patient administered together; with a staggered use both drugs to the patient in a period of less than or equal 12, in particular less than or equal to 6 hours administered sequentially.
Folglich betrifft ein weiterer Gegenstand dieser Erfindung ein Arzneimittel, das eine erfindungsgemäße Verbindung oder ein physiologisch verträgliches Salz solch einer Verbindung sowie mindestens einen der zuvor als Kombinationspartner beschriebenen Wirkstoffe neben gegebenenfalls einem oder mehreren inerten Trägerstoffen und/oder Verdünnungsmitteln aufweist.consequently another subject of this invention relates to a pharmaceutical the one compound of the invention or a physiologically acceptable Salt of such a compound and at least one of the previously as Combination partners described active ingredients in addition to, where appropriate one or more inert carriers and / or diluents having.
So weist beispielsweise ein erfindungsgemäßes Arzneimittel eine Kombination aus einer erfindungsgemäßen Verbindung der Formel I oder eines physiologisch verträglichen Salzes solch einer Verbindung sowie mindestens einem Angiotensin II Rezeptor Antagonisten neben gegebenenfalls einem oder mehreren inerten Trägerstoffen und/oder Verdünnungsmitteln auf.So For example, a pharmaceutical composition according to the invention has a combination from a compound according to the invention of the formula I or a physiologically acceptable salt of such a Compound and at least one angiotensin II receptor antagonist optionally together with one or more inert carriers and / or diluents on.
Die erfindungsgemäße Verbindung, oder eines physiologisch verträglichen Salzes, und der damit zu kombinierende weitere Wirkstoff können zusammen in einer Darreichungsform, beispielsweise einer Tablette oder Kapsel, oder getrennt in zwei gleichen oder verschiedenen Darreichungsformen, beispielsweise als sogenanntes kit-of-parts, vorliegen.The compound of the invention, or a physiologically acceptable one Salt, and the other active ingredient to be combined together in a dosage form, for example a tablet or capsule, or separately in two identical or different dosage forms, for example, as a so-called kit-of-parts, present.
Vorstehend und nachfolgend werden in Strukturformeln H-Atome von Hydroxylgruppen nicht in jedem Fall explizit dargestellt. Die nachfolgenden Beispiele sollen die vorliegende Erfindung näher erläutern ohne diese zu beschränken: above and subsequently, in structural formulas, H atoms of hydroxyl groups not explicitly shown in each case. The following examples are intended to illustrate the present invention without limiting it:
Herstellung der Ausgangsverbindungen:Preparation of the starting compounds:
Beispiel IExample I
5-Brom-2-chlor-phenol 5-bromo-2-chloro-phenol
Zu
einer eisgekühlten
Lösung
von 20 g 5-Brom-2-chlor-anisol in 300 ml Dichlormethan werden 96
ml einer 1 M Lösung
von Bortribromid in Dichlormethan gegeben. Die Reaktionslösung wird
14 h bei Raumtemperatur gerührt
und dann im Eisbad abgekühlt.
Die gekühlte
Lösung
wird mit wässriger
gesättigter
Kaliumcarbonatlösung
versetzt, die wässrige
Phase mit 1 M Salzsäure
sauer gestellt und mit Dichlormethan extrahiert. Die vereinigten
organischen Phasen werden über
Natriumsulfat getrocknet und das Lösungsmittel vollständig entfernt.
Ausbeute:
17,9 g (96% der Theorie)
Massenspektrum (ESI+):
m/z = 205/207/209 (Brom+Chlor) [M+H]+ To an ice-cooled solution of 20 g of 5-bromo-2-chloroanisole in 300 ml of dichloromethane are added 96 ml of a 1 M solution of boron tribromide in dichloromethane. The reaction solution is stirred for 14 h at room temperature and then cooled in an ice bath. The cooled solution is treated with aqueous saturated potassium carbonate solution, the aqueous phase acidified with 1 M hydrochloric acid and extracted with dichloromethane. The combined organic phases are dried over sodium sulfate and the solvent is completely removed.
Yield: 17.9 g (96% of theory)
Mass spectrum (ESI + ): m / z = 205/207/209 (bromine + chlorine) [M + H] +
Beispiel IIExample II
1-Brom-4-chlor-3-(tri-isopropyl-silyloxy)-benzol 1-bromo-4-chloro-3- (tri-isopropyl-silyloxy) benzene
Zu
einer eisgekühlten
Lösung
von 9,2 g 5-Brom-2-chlor-phenol und 9,4 ml Triethylamin in 120 ml
Dichlormethan werden 9,2 g Triisopropylsilylchlorid in 20 ml Dichlormethan
und zuletzt 0,5 g 4-Dimethylaminopyridin gegeben. Die Reaktion wird
18 h bei Raumtemperatur gerührt
und dann mit 100 ml Dichlormethan verdünnt. Die verdünnte Lösung wird
mit 1 M Salzsäure
und mit wässriger Natriumhydrogencarbonatlösung gewaschen, über Natriumsulfat
getrocknet und das Lösungsmittel
entfernt. Der Rückstand
wird über
Kieselgel gereinigt (Cyclohexan/Ethylacetat 9:1→1:1).
Ausbeute: 9,4 g
(59% der Theorie)
Massenspektrum (ESI+):
m/z = 363/365/367 (Brom+Chlor) [M+H]+ To an ice-cooled solution of 9.2 g of 5-bromo-2-chloro-phenol and 9.4 ml of triethylamine in 120 ml of dichloromethane are added 9.2 g of triisopropylsilyl chloride in 20 ml of dichloromethane and finally 0.5 g of 4-dimethylaminopyridine. The reaction is stirred for 18 h at room temperature and then diluted with 100 ml of dichloromethane. The diluted solution is washed with 1 M hydrochloric acid and with aqueous sodium bicarbonate solution, dried over sodium sulfate and the solvent removed. The residue is purified over silica gel (cyclohexane / ethyl acetate 9: 1 → 1: 1).
Yield: 9.4 g (59% of theory)
Mass spectrum (ESI + ): m / z = 363/365/367 (bromine + chlorine) [M + H] +
Beispiel IIIExample III
cis-4-(tert-Butyl-diphenylsilyloxy)-cyclohexanol und trans-4-(tert-Butyl-diphenylsilyloxy)-cyclohexanol cis-4- (tert-butyl-diphenylsilyloxy) -cyclohexanol and trans-4- (tert-butyl-diphenylsilyloxy) -cyclohexanol
Zu einer eisgekühlten Lösung von 10,0 g 1,4-Cyclohexandiol (cis/trans-Gemisch ca. 1:1) und 14,6 g Imidazol in 15 ml trockenem Dimethylformamid und 20 ml trockenem Tetrahydrofuran wird eine Lösung von 29,4 g tert-Butyldiphenylsilylchlorid in 20 ml Dimethylformamid getropft. Die Reaktionslösung wird 1 h im Eisbad gerührt und dann mit 100 ml wässriger Natriumchloridlösung versetzt. Die organische Phase wird abgetrennt und die wässrige mit Ethylacetat extrahiert. Die vereinigten organischen Phasen werden über Natriumsulfat getrocknet, und das Lösungsmittel wird vollständig entfernt. Der Rückstand wird chromatografisch gereinigt und in die beiden isomeren Produkte aufgetrennt (Ethylacetat/Cyclohexan 1:1).To an ice-cold one solution of 10.0 g of 1,4-cyclohexanediol (cis / trans mixture about 1: 1) and 14.6 g Imidazole in 15 ml dry dimethylformamide and 20 ml dry Tetrahydrofuran becomes a solution of 29.4 g of tert-butyldiphenylsilyl chloride in 20 ml of dimethylformamide dripped. The reaction solution is stirred for 1 h in an ice bath and then with 100 ml of aq Sodium chloride solution added. The organic phase is separated and the aqueous with Extracted ethyl acetate. The combined organic phases are over sodium sulfate dried, and the solvent will be complete away. The residue is purified by chromatography and in the two isomeric products separated (ethyl acetate / cyclohexane 1: 1).
cis-4-(tert-Butyl-diphenylsilyloxy)-cyclohexanol:cis-4- (tert-Butyl-diphenylsilyloxy) cyclohexanol:
- Ausbeute: 4,9 g (16% der Theorie)Yield: 4.9 g (16% of theory)
- Massenspektrum (ESI+): m/z = 355 [M+H]+ Mass spectrum (ESI + ): m / z = 355 [M + H] +
trans-4-(tert-Butyl-diphenylsilyloxy)-cyclohexanol:trans-4- (tert-Butyl-diphenylsilyloxy) cyclohexanol:
- Ausbeute: 4,8 g (16% der Theorie)Yield: 4.8 g (16% of theory)
- Massenspektrum (ESI+): m/z = 355 [M+H]+ Mass spectrum (ESI + ): m / z = 355 [M + H] +
Beispiel IVExample IV
1-Brom-3-[cis-4-(tert-butyl-diphenylsilyloxyl-cyclohexyloxyl-4-chlor-benzol 1-Bromo-3- [cis-4- (tert-butyl-diphenylsilyloxyl-cyclohexyloxyl-4-chloro-benzene
Zu
einer Lösung
von 1,85 g trans-4-(tert-Butyl-diphenylsilyloxy)-cyclohexanol in
20 ml trockenem Tetrahydrofuran werden in der genannten Reihenfolge
4,8 g 5-Brom-2-chlor-phenol,
4,5 g Triphenylphoshin und 3,3 ml Diisopropylazodicarboxylat gegeben.
Die Lösung
wird 48 h bei 55°C
gerührt
und dann mit wässriger Kaliumcarbonatlösung versetzt.
Dann wird mit Ethylacetat extrahiert, über Natriumsulfat getrocknet
und das Lösungsmittel
entfernt. Der Rückstand
wird über
Kieselgel gereinigt (Cyclohexan/Ethylacetat 4:1).
Ausbeute:
3,5 g (72% der Theorie)
Massenspektrum (ESI+):
m/z = 543/545/547 (Brom und Chlor) [M+H]+ To a solution of 1.85 g of trans-4- (tert-butyl-diphenylsilyloxy) -cyclohexanol in 20 ml of dry tetrahydrofuran are added in the order mentioned 4.8 g of 5-bromo-2-chloro-phenol, 4.5 g of triphenylphosphine and 3.3 ml of diisopropyl azodicarboxylate. The solution is stirred for 48 h at 55 ° C and then treated with aqueous potassium carbonate solution. It is then extracted with ethyl acetate, dried over sodium sulfate and the solvent removed. The residue is purified over silica gel (cyclohexane / ethyl acetate 4: 1).
Yield: 3.5 g (72% of theory)
Mass spectrum (ESI + ): m / z = 543/545/547 (bromine and chlorine) [M + H] +
Analog Beispiel IV wird folgende Verbindung erhalten: (1) 1-Brom-3-[trans-4-(tert-butyl-diphenylsilyloxy)-cyclohexyloxy]-4-chlor-benzol Massenspektrum (ESI+): m/z = 543/545/547 (Brom und Chlor) [M+H]+ The following compound is obtained analogously to Example IV: (1) 1-bromo-3- [trans-4- (tert-butyl-diphenylsilyloxy) -cyclohexyloxy] -4-chlorobenzene Mass spectrum (ESI + ): m / z = 543/545/547 (bromine and chlorine) [M + H] +
Beispiel VExample V
1-Brom-4-chlor-3-(cis-4-hydroxy-cyclohexyloxy)-benzol 1-bromo-4-chloro-3- (cis-4-hydroxy-cyclohexyloxy) benzene
Zu
einer eisgekühlten
Lösung
von 4,8 g 1-Brom-3-[cis-4-(tert-butyl-diphenylsilyloxy)cyclohexyloxy]-4-chlor-benzol
in 25 ml trockenem Tetrahydrofuran werden 8,8 ml einer 1 M Lösung von
Tetrabutylammoniumfluorid in Tetrahydrofuran gegeben. Die Lösung wird
14 h bei Raumtemperatur gerührt
und dann mit Wasser versetzt. Danach wird mit Ethylacetat extrahiert, über Natriumsulfat
getrocknet und das Lösungsmittel
entfernt. Der Rückstand
wird über
Kieselgel gereinigt (Cyclohexan/Ethylacetat 1:0→ 3:2).
Ausbeute: 2,1 g
(79% der Theorie)
Massenspektrum (ESI+):
m/z = 327/329/331 (Brom und Chlor) [M+Na]+ To an ice-cooled solution of 4.8 g of 1-bromo-3- [cis-4- (tert-butyl-diphenylsilyloxy) cyclohexyloxy] -4-chlorobenzene in 25 ml of dry tetrahydrofuran is added 8.8 ml of a 1 M solution of Added tetrabutylammonium fluoride in tetrahydrofuran. The solution is stirred for 14 h at room temperature and then treated with water. It is then extracted with ethyl acetate, dried over sodium sulfate and the solvent removed. The residue is purified on silica gel (cyclohexane / ethyl acetate 1: 0 → 3: 2).
Yield: 2.1 g (79% of theory)
Mass spectrum (ESI + ): m / z = 327/329/331 (bromine and chlorine) [M + Na] +
Analog Beispiel V wird folgende Verbindung erhalten: (1) 1-Brom-4-chlor-3-(trans-4-hydroxy-cyclohexyloxy)-benzol Massenspektrum (ESI+): m/z = 327/329/331 (Brom und Chlor) [M+Na]+ Analogously to Example V, the following compound is obtained: (1) 1-Bromo-4-chloro-3- (trans-4-hydroxycyclohexyloxy) benzene Mass spectrum (ESI + ): m / z = 327/329/331 (bromine and chlorine) [M + Na] +
Beispiel VIExample VI
1-Brom-4-chlor-3-(cis-4-methoxy-cyclohexyloxy)-benzol 1-bromo-4-chloro-3- (cis-4-methoxy-cyclohexyloxy) benzene
Unter
Argonatmosphäre
werden zu einer eisgekühlten
Lösung
von 2,1 g 1-Brom-4-chlor-3-(cis-4-hydroxy-cyclohexyloxy)-benzol
in 10 ml trockenem Tetrahydrofuran 0,28 g Natriumhydrid (60% in
Mineralöl)
gegeben. Die Lösung
wird 30 min im Eisbad gerührt
und dann werden 0,44 ml Methyliodid zugegeben. Die Reaktionslösung wird
6 h bei Raumtemperatur gerührt
und dann mit Wasser versetzt. Danach wird mit Ethylacetat extrahiert, über Natriumsulfat
getrocknet und das Lösungsmittel
entfernt. Der Rückstand
wird über
Kieselgel gereinigt (Cyclohexan/Ethylacetat 1:0→1:1).
Ausbeute: 1,8 g
(80% der Theorie)
Massenspektrum (ESI+):
m/z = 319/321/323 (Brom und Chlor) [M+H]+ Under an argon atmosphere, 0.28 g of sodium hydride (60% in mineral oil) is added to an ice-cooled solution of 2.1 g of 1-bromo-4-chloro-3- (cis-4-hydroxycyclohexyloxy) benzene in 10 ml of dry tetrahydrofuran , The solution is stirred for 30 minutes in an ice bath and then 0.44 ml of methyl iodide are added. The reaction solution is stirred for 6 h at room temperature and then treated with water. It is then extracted with ethyl acetate, dried over sodium sulfate and the solvent removed. The residue is purified over silica gel (cyclohexane / ethyl acetate 1: 0 → 1: 1).
Yield: 1.8 g (80% of theory)
Mass spectrum (ESI + ): m / z = 319/321/323 (bromine and chlorine) [M + H] +
Analog Beispiel VI wird folgende Verbindung erhalten: (1) 1-Brom-4-chlor-3-(trans-4-methoxy-cyclohexyloxy)-benzol Massenspektrum (ESI+): m/z = 319/321/323 (Brom und Chlor) [M+H]+ The following compound is obtained analogously to Example VI: (1) 1-bromo-4-chloro-3- (trans-4-methoxy-cyclohexyloxy) -benzene Mass spectrum (ESI + ): m / z = 319/321/323 (bromine and chlorine) [M + H] +
Beispiel VIIExample VII
5-Brom-2-chlor-benzaldehyd 5-bromo-2-chloro-benzaldehyde
Zu
einer –60°C kalten
Lösung
von 4,4 ml Oxalylchlorid in 125 ml Dichlormethan werden 7 ml Dimethylsulfoxid
in 25 ml Dichlormethan getropft. Nach 5 min Rühren wird eine Lösung von
10,0 g 5-Brom-2-chlor-benzylalkohol in 50 ml Tetrahydrofuran zugegeben
und weitere 15 min bei –60°C gerührt. Dann
werden 31,5 ml Triethylamin zugesetzt und die Reaktionslösung im
Kühlbad
auf Raumtemperatur erwärmen gelassen.
Bei Raumtemperatur wird Wasser zugegeben, die organische Phase,
abgetrennt und mit 1 M Salzsäure
gewaschen. Nach Trocknen über
Natriumsulfat wird das Lösungsmittel
vollständig
entfernt.
Ausbeute: 9,7 g (98% der Theorie)
Massenspektrum
(ESI+): m/z = 218/220/222 (Brom+Chlor) [M+H]+ To a -60 ° C cold solution of 4.4 ml of oxalyl chloride in 125 ml of dichloromethane 7 ml of dimethyl sulfoxide are added dropwise in 25 ml of dichloromethane. After stirring for 5 minutes, a solution of 10.0 g of 5-bromo-2-chloro-benzyl alcohol in 50 ml of tetrahydrofuran is added and the mixture is stirred at -60 ° C. for a further 15 min. Then 31.5 ml Triethylamine added and the reaction solution allowed to warm to room temperature in a cooling bath. At room temperature, water is added, the organic phase, separated and washed with 1 M hydrochloric acid. After drying over sodium sulfate, the solvent is completely removed.
Yield: 9.7 g (98% of theory)
Mass spectrum (ESI + ): m / z = 218/220/222 (bromine + chlorine) [M + H] +
Beispiel VIIIExample VIII
1-Brom-4-chlor-3-cyclohexylidenmethyl-benzol 1-bromo-4-chloro-3-cyclohexylidenemethyl-benzene
Zu
einer eisgekühlten
Lösung
von 2,9 g Cyclohexyl-triphenylphosphoniumbromid in 5 ml Tetrahydrofuran
werden 3,55 ml einer 1,9 M Lösung
Phenyllithium in Diethylether/Cyclohexan (70/30) getropft. Die Lösung wird
1 h im Eisbad gerührt.
Dann wird eine Lösung
von 1,5 g 5-Brom-2-chlor-benzaldehyd in 5 ml Tetrahydrofuran zugegeben
und die Reaktionslösung
4 h bei Raumtemperatur gerührt.
Danach wird Wasser zugegeben, mit Ethylacetat extrahiert und die
organische Phase über
Natriumsulfat getrocknet. Nach Entfernen des Lösungsmittels wird der Rückstand über Kieselgel
gereinigt (Gyclohexan/Ethylacetat 1:1).
Ausbeute: 0,66 g (34%
der Theorie)
Massenspektrum (ESI+):
m/z = 284/286/288 (Brom+Chlor) [M]+ 3.55 ml of a 1.9 M solution of phenyl lithium in diethyl ether / cyclohexane (70/30) are added dropwise to an ice-cooled solution of 2.9 g of cyclohexyltriphenylphosphonium bromide in 5 ml of tetrahydrofuran. The solution is stirred for 1 h in an ice bath. Then, a solution of 1.5 g of 5-bromo-2-chloro-benzaldehyde in 5 ml of tetrahydrofuran is added and the reaction solution is stirred for 4 h at room temperature. Thereafter, water is added, extracted with ethyl acetate and the organic phase dried over sodium sulfate. After removal of the solvent, the residue is purified on silica gel (cyclohexane / ethyl acetate 1: 1).
Yield: 0.66 g (34% of theory)
Mass spectrum (ESI + ): m / z = 284/286/288 (bromine + chlorine) [M] +
Beispiel IXExample IX
8-(3-Brom-benzyliden)-1,4-dioxo-spiro[4.5]dekan 8- (3-bromo-benzylidene) -1,4-dioxo-spiro [4.5] dean
Eine
Lösung
von 8,0 g 3-Brombenzylbromid und 8,4 g Triphenylphosphin in 100
ml Toluol wird 12 h unter Rückfluss
gerührt.
Danach wird der entstandene Niederschlag abfiltriert, mit Toluol
gewaschen und bei 50°C
getrocknet. Das getrocknete 3-Brombenzyl-triphenylphosphoniumbromid
wird zu einer eisgekühlten
Suspension von 1,64 g Natriumhydrid (60% in Mineralöl) in 50
ml trockenem Tetrahydrofuran gegeben und die resultierende Reaktionsmischung
1 h bei 45°C
gerührt.
Dann werden bei Raumtemperatur 5,4 g 1,4-Dioxo-spiro[4.5]dekan-8-on
zugegeben und die Reaktionslösung
12 h bei Raumtemperatur gerührt.
Danach wird Wasser zugegeben, die organische Phase abgetrennt, die
wässrige
mit Dichlormethan extrahiert, und die vereinigten organischen Phasen
werden über
Natriumsulfat getrocknet. Nach Entfernen des Lösungsmittels wird der Rückstand über Kieselgel
gereinigt (Cyclohexan/Ethylacetat 1:0→7:3).
Ausbeute: 3,35 g
(31 % der Theorie)
Massenspektrum (ESI+):
m/z = 308/310 (Brom) [M]+ A solution of 8.0 g of 3-bromobenzyl bromide and 8.4 g of triphenylphosphine in 100 ml of toluene is stirred for 12 hours under reflux. Thereafter, the resulting precipitate is filtered off, washed with toluene and dried at 50 ° C. The dried 3-bromobenzyl-triphenylphosphonium bromide is added to an ice-cooled suspension of 1.64 g of sodium hydride (60% in mineral oil) in 50 ml of dry tetrahydrofuran and the resulting reaction mixture is stirred for 1 h at 45 ° C. 5.4 g of 1,4-dioxo-spiro [4.5] decane-8-one are then added at room temperature and the reaction solution is stirred at room temperature for 12 h. Thereafter, water is added, the organic phase is separated, the aqueous extracted with dichloromethane, and the combined organic phases are dried over sodium sulfate. After removal of the solvent, the residue is purified on silica gel (cyclohexane / ethyl acetate 1: 0 → 7: 3).
Yield: 3.35 g (31% of theory)
Mass spectrum (ESI + ): m / z = 308/310 (bromine) [M] +
Beispiel XExample X
2,3,4,6-Tetrakis-O-(trimethylsilyl)-D-glucopyranon 2,3,4,6-tetrakis-O- (trimethylsilyl) -D-glucopyranone
Eine
Lösung
von 20 g D-Glucono-1,5-lacton und 98,5 ml N-Methylmorpholin in 200
ml Tetrahydrofuran wird auf –5°C abgekühlt. Dann
werden 85 ml Trimethylsilylchlorid so zugetropft, dass die Temperatur
nicht über 5°C steigt.
Die Lösung
wird danach 1 h bei Raumtemperatur, 5 h bei 35°C und noch einmal 14 h bei Raumtemperatur
gerührt.
Nach Zugabe von 300 ml Toluol wird die Lösung im Eisbad abgekühlt, und
es werden 500 ml Wasser so zugegeben, dass die Temperatur nicht über 10°C steigt.
Die organische Phase wird anschließend abgetrennt und jeweils
einmal mit wässriger
Natriumdihydrogenphosphatlösung,
Wasser und gesättigter wässriger
Natriumchloridlösung
gewaschen. Das Lösungsmittel
wird entfernt, der Rückstand
in 250 ml Toluol aufgenommen und das Lösungsmittel erneut vollständig entfernt.
Ausbeute:
52,5 g (ca. 90% rein)
Massenspektrum (ESI+):
m/z = 467 [M+H]+ A solution of 20 g of D-glucono-1,5-lactone and 98.5 ml of N-methylmorpholine in 200 ml of tetrahydrofuran is cooled to -5 ° C. Then, 85 ml of trimethylsilyl chloride are added dropwise so that the temperature does not rise above 5 ° C. The solution is then stirred for 1 h at room temperature, 5 h at 35 ° C and another 14 h at room temperature. After adding 300 ml of toluene, the solution is cooled in an ice bath and 500 ml of water are added so that the temperature does not rise above 10 ° C. The organic phase is then separated off and washed once each with aqueous sodium dihydrogenphosphate solution, water and saturated aqueous sodium chloride solution. The solvent is removed, the residue is taken up in 250 ml of toluene and the solvent is completely removed again.
Yield: 52.5 g (about 90% pure)
Mass Spectrum (ESI + ): m / z = 467 [M + H] +
Beispiel XIExample XI
1-Chlor-4-(2,3,4,6-tetra-O-acetyl-1-methoxy-D-glucopyranos-1-yl)-2-(tri-isopropylsilyloxy)-benzol 1-chloro-4- (2,3,4,6-tetra-O-acetyl-1-methoxy-D-glucopyranos-1-yl) -2- (tri-isopropylsilyloxy) benzene
Eine
Lösung
von 5,0 g 4-Brom-1-chlor-2-(tri-isopropyl-silyloxy)-benzol in 60
ml trockenem Diethylether wird unter Argon auf –80°C abgekühlt. Zu der gekühlten Lösung werden
17,7 ml einer 1,7 M Lösung
von tert-Butyllithium in Pentan getropft. Die Lösung wird 30 min bei –80°C gerührt und
dann über
eine Umdrücknadel
zu einer –80°C-kalten
Lösung
von 7,3 g 2,3,4,6-Tetrakis-O-(trimethylsilyl)-D-glucopyranon in
40 ml Diethylether getropft. Die resultierende Lösung wird 4 h bei –78°C gerührt. Danach
wird eine Lösung
von 3 ml Methansulfonsäure
in 80 ml Methanol zugegeben und die Lösung 16 h bei Raumtemperatur
gerührt.
Die Lösung wird
anschließend
mit Ethyldiisopropylamin neutralisiert und eingeengt. Der Rückstand
wird in Toluol aufgenommen und erneut eingeengt. Dann wird der Rückstand
in 36 ml Toluol gelöst
und 3,4 ml Ethyldiisopropylamin zur Lösung gegeben. Die Lösung wird
im Eisbad abgekühlt
und danach werden 6,3 ml Acetanhydrid und 0,17 g Dimethylaminopyridin
zugegeben. Die Lösung
wird 6 h bei Raumtemperatur gerührt
und dann mit wässriger
Natriumhydrogencarbonatlösung
versetzt. Die organische Phase wird abgetrennt und die wässrige mit Ethylacetat
extrahiert. Nach Trocknen der vereinten organischen Extrakte über Natriumsulfat
und Entfernen des Lösungsmittels
wird der Rückstand über Kieselgel
chromatografiert (Cyclohexan/Ethylacetat 6:1→1:1).
Ausbeute: 5,8 g
(65% der Theorie)
Massenspektrum (ESI+):
m/z = 662/664 (Chlor) [M+NH4]+ A solution of 5.0 g of 4-bromo-1-chloro-2- (triisopropylsilyloxy) benzene in 60 ml of dry diethyl ether is cooled to -80 ° C under argon. To the cooled solution, 17.7 ml of a 1.7 M solution of tert-butyllithium in pentane are added dropwise. The solution is stirred for 30 min at -80 ° C and then via a transfer needle to a -80 ° C-cold solution of 7.3 g of 2,3,4,6-tetrakis-O- (trimethylsilyl) -D-glucopyranon in 40 ml of diethyl ether added dropwise. The resulting solution is stirred for 4 h at -78 ° C. Thereafter, a solution of 3 ml of methanesulfonic acid in 80 ml of methanol is added and the solution is stirred for 16 h at room temperature. The solution is then neutralized with ethyldiisopropylamine and concentrated. The residue is taken up in toluene and concentrated again. Then the residue is dissolved in 36 ml of toluene and 3.4 ml of ethyldiisopropylamine are added to the solution. The solution is cooled in an ice bath and then 6.3 ml of acetic anhydride and 0.17 g of dimethylaminopyridine are added. The solution is stirred for 6 h at room temperature and then treated with aqueous sodium bicarbonate solution. The organic phase is separated and the aqueous extracted with ethyl acetate. After drying the combined organic extracts over sodium sulfate and removing the solvent, the residue is chromatographed on silica gel (cyclohexane / ethyl acetate 6: 1 → 1: 1).
Yield: 5.8 g (65% of theory)
Mass spectrum (ESI + ): m / z = 662/664 (chlorine) [M + NH 4 ] +
Analog Beispiel XI werden folgende Verbindungen erhalten: (1) 1-Chlor-4-(2,3,4,6-tetra-O-acetyl-1-methoxy-D-glucopyranos-1-yl)-2-(cis-4-methoxy-cyclohexyloxy)-benzol Massenspektrum (ESI+): m/z = 618/620 (Chlor) [M+NH4]+ (2) 1-Chlor-4-(2,3,4,6-tetra-O-acetyl-1-methoxy-D-glucopyranos-1-yl)-2-(trans-4-methoxy-cyclohexyloxy)-benzol Massenspektrum (ESI+): m/z = 618/620 (Chlor) [M+NH4]+ (3) 1-Chlor-4-(2,3,4,6-tetra-O-acetyl-1-methoxy-D-glucopyranos-1-yl)-2-cyclohexylidenmethyl-benzol Massenspektrum (ESI+): m/z = 584/586 (Chlor) [M+NH4]+ (4) 1-(2,3,4,6-tetra-O-acetyl-1-methoxy-D-glucopyranos-1-yl)-3-(4,4-dimethoxycyclohexylidenmethyl)-benzol ausgehend von 8-(3-Brom-benzyliden)-1,4-dioxospiro[4.5]dekan Massenspektrum (ESI+): m/z = 610 [M+NH4]+ The following compounds are obtained analogously to Example XI: (1) 1-Chloro-4- (2,3,4,6-tetra-O-acetyl-1-methoxy-D-glucopyranos-1-yl) -2- (cis-4-methoxycyclohexyloxy) benzene Mass spectrum (ESI + ): m / z = 618/620 (chlorine) [M + NH 4 ] + (2) 1-chloro-4- (2,3,4,6-tetra-O-acetyl-1-methoxy -D-glucopyranos-1-yl) -2- (trans-4-methoxy-cyclohexyloxy) benzene Mass spectrum (ESI + ): m / z = 618/620 (chlorine) [M + NH 4 ] + (3) 1-chloro-4- (2,3,4,6-tetra-O-acetyl-1-methoxy -D-glucopyranos-1-yl) -2-cyclohexylidenemethyl-benzene Mass spectrum (ESI + ): m / z = 584/586 (chlorine) [M + NH 4 ] + (4) 1- (2,3,4,6-tetra-O-acetyl-1-methoxy-D-glucopyranos-1-yl) -3- (4,4-dimethoxycyclohexylidenemethyl) benzene starting from 8- (3 bromo-benzylidene) -1,4-dioxospiro [4.5] dean Mass spectrum (ESI + ): m / z = 610 [M + NH 4 ] +
Beispiel XIIExample XII
1-Chlor-4-(2,3,4,6-tetra-O-acetyl-β-D-glucopyranos-1-yl)-2-(tri-isopropyl-silyloxy)-benzol 1-chloro-4- (2,3,4,6-tetra-O-acetyl-β-D-glucopyranos-1-yl) -2- (tri-isopropyl-silyloxy) benzene
Eine
Lösung
von 5,83 g 1-Chlor-4-(2,3,4,6-tetra-O-acetyl-1-methoxy-D-glucopyranos-1-yl)-2-(tri-isopropyl-silyloxy)-benzol
in 100 ml Acetonitril und 0,22 ml Wasser wird im Eisbad abgekühlt. Dann
werden 7 ml Triethylsilan und 1,5 ml Bortrifluoridetherat zugegeben.
Die Lösung
wird 1 h im Eisbad und danach bei Raumtemperatur gerührt. Nach
5 h werden noch einmal 6 ml Triethylsilan und 1,2 ml Bortrifluoridetherat
zugegeben. Nach weiteren 5 h Rühren
bei Raumtemperatur wird wässrige
Natriumhydrogencarbonatlösung
zugesetzt, 0,5 h gerührt
und dann mit Ethylacetat extrahiert. Die organische Phase wird über Natriumsulfat
getrocknet und bis zur Trockene eingeengt.
Ausbeute: 4,80 g
(86% der Theorie)
Massenspektrum (ESI+):
m/z = 637/639 (Chlor) [M+Na]+ A solution of 5.83 g of 1-chloro-4- (2,3,4,6-tetra-O-acetyl-1-methoxy-D-glucopyranos-1-yl) -2- (tri-isopropyl-silyloxy) benzene in 100 ml of acetonitrile and 0.22 ml of water is cooled in an ice bath. Then, 7 ml of triethylsilane and 1.5 ml of boron trifluoride etherate are added. The solution is stirred for 1 h in an ice bath and then at room temperature. After 5 h, a further 6 ml of triethylsilane and 1.2 ml of boron trifluoride etherate are added. After stirring at room temperature for a further 5 h, aqueous sodium bicarbonate solution is added, stirred for 0.5 h and then extracted with ethyl acetate. The organic phase is dried over sodium sulfate and concentrated to dryness.
Yield: 4.80 g (86% of theory)
Mass spectrum (ESI + ): m / z = 637/639 (chlorine) [M + Na] +
Analog Beispiel XII werden folgende Verbindungen erhalten: (1) 1-Chlor-4-(2,3,4,6-tetra-O-acetyl-β-D-glucopyranos-1-yl)-2-(cis-4-methoxycyclohexyloxy)-benzol Massenspektrum (ESI+): m/z = 589/591 (Chlor) [M+NH4]+ (2) 1-Chlor-4-(2,3,4,6-tetra-O-acetyl-β-D-glucopyranos-1-yl)-2-(trans-4-methoxycyclohexyloxy)-benzol Massenspektrum (ESI+): m/z = 589/591 (Chlor) [M+NH4]+ (3) 1-Chlor-4-(2,3,4,6-tetra-O-acetyl-β-D-glucopyranos-1-yl)-2-cyclohexylidenmethylbenzol Massenspektrum (ESI+): m/z = 559/561 (Chlor) [M+Na]+ (4) 1-(2,3,4,6-tetra-O-acetyl-β-D-glucopyranos-1-yl)-2-(4-methoxycyclohexylidenmethyl)-benzol ausgehend von 1-(2,3,4,6-tetra-O-acetyl-1-methoxy-D-glucopyranos-1-yl)-3-(4,4-dimethoxy-cyclohexylidenmethyl)-benzol Massenspektrum (ESI+): m/z = 550 [M+NH4]+ (5) 1-(2,3,4,6-tetra-O-acetyl-β-D-glucopyranos-1-yl)-2-(4-hydroxycyclohexylidenmethyl)-benzol als Nebenprodukt bei der Synthese von Beispiel XII (4) ausgehend von 1-(2,3,4,6-tetra-O-acetyl-1-methoxy-D-glucopyranos-1-yl)-3-(4,4-dimethoxy-cyclohexylidenmethyl)-benzol Massenspektrum (ESI+): m/z = 566 (Chlor) [M+NH4]+ The following compounds are obtained analogously to Example XII: (1) 1-Chloro-4- (2,3,4,6-tetra-O-acetyl-β-D-glucopyranos-1-yl) -2- (cis-4-methoxycyclohexyloxy) benzene Mass spectrum (ESI + ): m / z = 589/591 (chlorine) [M + NH 4 ] + (2) 1-chloro-4- (2,3,4,6-tetra-O-acetyl-β-D -glucopyranos-1-yl) -2- (trans-4-methoxycyclohexyloxy) benzene Mass spectrum (ESI + ): m / z = 589/591 (chlorine) [M + NH 4 ] + (3) 1-chloro-4- (2,3,4,6-tetra-O-acetyl-β-D -glucopyranos-1-yl) -2-cyclohexylidenmethylbenzol Mass spectrum (ESI + ): m / z = 559/561 (chlorine) [M + Na] + (4) 1- (2,3,4,6-tetra-O-acetyl-β-D-glucopyranos-1-yl) -2- (4-methoxycyclohexylidenemethyl) benzene starting from 1- (2,3,4 , 6-tetra-O-acetyl-1-methoxy-D-glucopyranos-1-yl) -3- (4,4-dimethoxy-cyclohexylidenemethyl) benzene Mass Spectrum (ESI + ): m / z = 550 [M + NH 4 ] + (5) 1- (2,3,4,6-tetra-O-acetyl-β-D-glucopyranos-1-yl) -2 - (4-hydroxycyclohexylidenemethyl) -benzene as a by-product in the synthesis of Example XII (4) starting from 1- (2,3,4,6-tetra-O-acetyl-1-methoxy-D-glucopyranos-1-yl) -3- (4,4-dimethoxy-cyclohexylidenemethyl) benzene Mass spectrum (ESI + ): m / z = 566 (chlorine) [M + NH 4 ] +
Beispiel XIIIExample XIII
1-Chlor-4-(2,3,4,6-tetra-O-acetyl-β-D-glucopyranos-1-yl)-2-hydroxy-benzol 1-chloro-4- (2,3,4,6-tetra-O-acetyl-β-D-glucopyranos-1-yl) -2-hydroxy-benzene
Zu
einer eisgekühlten
Lösung
von 4,80 g 1-Chlor-4-(2,3,4,6-tetra-O-acetyl-β-D-glucopyranos-1-yl)-2-(tri-isopropyl-silyloxy)-benzol
in 25 ml trockenem Tetrahydrofuran werden 5 ml einer 1 M Lösung von
Tetrabutylammoniumfluorid in Tetrahydrofuran gegeben. Die Lösung wird
14 h bei Raumtemperatur gerührt
und dann mit Wasser versetzt. Es wird mit Ethylacetat extrahiert, über Natriumsulfat
getrocknet und das Lösungsmittel
entfernt. Der Rückstand
wird in Cyclohexan/Ethylacetat (5:1) verrührt und dann getrocknet.
Ausbeute:
1,70 g (86% der Theorie)
Massenspektrum (ESI+):
m/z = 476/478 (Chlor) [M+NH4]+ To an ice-cooled solution of 4.80 g of 1-chloro-4- (2,3,4,6-tetra-O-acetyl-β-D-glucopyranos-1-yl) -2- (tri-isopropyl-silyloxy) -benzene in 25 ml of dry tetrahydrofuran are added 5 ml of a 1 M solution of tetrabutylammonium fluoride in tetrahydrofuran. The solution is stirred for 14 h at room temperature and then treated with water. It is extracted with ethyl acetate, dried over sodium sulfate and the Solvent removed. The residue is stirred in cyclohexane / ethyl acetate (5: 1) and then dried.
Yield: 1.70 g (86% of theory)
Mass spectrum (ESI + ): m / z = 476/478 (chlorine) [M + NH 4 ] +
Beispiel XIVExample XIV
1-Chlor-4-(2,3,4,6-tetra-O-acetyl-β-D-glucopyranos-1-yl)-2-(4-methoxy-cyclohexyloxy)-benzol 1-chloro-4- (2,3,4,6-tetra-O-acetyl-β-D-glucopyranos-1-yl) -2- (4-methoxy-cyclohexyloxy) benzene
Zu
einer Lösung
von 0,25 g 1-Chlor-4-(2,3,4,6-tetra-O-acetyl-β-D-glucopyranos-1-yl)-2-hydroxy-benzol
in 3 ml Tetrahydrofuran werden in der genannten Reihenfolge 0,08
g 4-Methoxycyclohexanol, 0,16 g Triphenylphoshin und 0,12 ml Diisopropylazodicarboxylat
gegeben. Die Lösung
wird 14 h bei Raumtemperatur gerührt
und dann mit wässriger
Kaliumcarbonatlösung
versetzt. Dann wird mit Ethylacetat extrahiert, über Natriumsulfat getrocknet
und das Lösungsmittel
entfernt. Der Rückstand
wird über
Kieselgel gereinigt (Cyclohexan/Ethylacetat 7:3→1:1).
Ausbeute: 0,05 g
(16% der Theorie) To a solution of 0.25 g of 1-chloro-4- (2,3,4,6-tetra-O-acetyl-β-D-glucopyranos-1-yl) -2-hydroxybenzene in 3 ml of tetrahydrofuran 0.08 g of 4-methoxycyclohexanol, 0.16 g of triphenylphosphine and 0.12 ml of diisopropyl azodicarboxylate are added in the order named. The solution is stirred for 14 h at room temperature and then treated with aqueous potassium carbonate solution. It is then extracted with ethyl acetate, dried over sodium sulfate and the solvent removed. The residue is purified over silica gel (cyclohexane / ethyl acetate 7: 3 → 1: 1).
Yield: 0.05 g (16% of theory)
Herstellung der Endverbindungen:Preparation of the end compounds:
Beispiel 1example 1
1-Chlor-4-β-D-glucopyranos-1-yl-2-(4-methoxy-cyclohexyloxy)-benzol 1-chloro-4-β-D-glucopyranos-1-yl-2- (4-methoxy-cyclohexyloxy) benzene
Zu
einer Lösung
von 0,05 g 1-Chlor-4-(2,3,4,6-tetra-O-acetyl-β-D-glucopyranos-1-yl)-2-(4-methoxy-benzyl)-benzol
in 3 ml Methanol werden 0,13 ml 4 M Kaliumhydroxidlösung gegeben.
Die Lösung
wird 3 h bei Raumtemperatur gerührt
und dann mit 1 M Salzsäure
neutralisiert. Die Lösung
wird vom Methanol befreit, mit wässriger
Natriumchloridlösung
versetzt und mit Ethylacetat extrahiert. Die organische Phase wird über Natriumsulfat
getrocknet und das Lösungsmittel
entfernt. Der Rückstand
wird über
Kieselgel gereinigt (Dichlormethan/Methanol 1:0→3:1).
Ausbeute: 0,01 g
(28% der Theorie)
Massenspektrum (ESI+):
m/z = 420/422 (Chlor) [M+NH4]+ To a solution of 0.05 g of 1-chloro-4- (2,3,4,6-tetra-O-acetyl-β-D-glucopyranos-1-yl) -2- (4-methoxybenzyl) - benzene in 3 ml of methanol is added 0.13 ml of 4M potassium hydroxide solution. The solution is stirred for 3 h at room temperature and then neutralized with 1 M hydrochloric acid. The solution is freed from methanol, treated with aqueous sodium chloride solution and extracted with ethyl acetate. The organic phase is dried over sodium sulfate and the solvent removed. The residue is purified over silica gel (dichloromethane / methanol 1: 0 → 3: 1).
Yield: 0.01 g (28% of theory)
Mass spectrum (ESI + ): m / z = 420/422 (chlorine) [M + NH 4 ] +
Analog Beispiel 1 werden folgende Verbindungen erhalten: (1) 1-Chlor-4-β-D-glucopyranos-1-yl-2-(cis-4-methoxy-cyclohexyloxy)-benzol Massenspektrum (ESI+): m/z = 403/405 (Chlor) [M+H]+ (2) 1-Chlor-4-β-D-glucopyranos-1-yl-2-(trans-4-methoxy-cyclohexyloxy)-benzol Massenspektrum (ESI+): m/z = 420/422 (Chlor) [M+NH4]+ (3) 1-Chlor-4-β-D-glucopyranos-1-yl-2-cyclohexylidenmethyl-benzol Massenspektrum (ESI+): m/z = 386/388 (Chlor) [M+NH4]+ (4) 1-β-D-glucopyranos-1-yl-3-(4-methoxy-cyclohexylmethyl)-benzol ausgehend von 1-(2,3,4,6-tetra-O-acetyl-β-D-glucopyranos-1-yl)-3-(4-methoxy-cyclohexylmethyl)benzol [siehe Beispiel 2(1)] Massenspektrum (ESI+): m/z = 367 [M+H]+ (5) 1-β-D-glucopyranos-1-yl-3-(4-hydroxy-cyclohexylidenmethyl)-benzol Massenspektrum (ESI+): m/z = 368 [M+NH4]+ Analogously to Example 1, the following compounds are obtained: (1) 1-Chloro-4-β-D-glucopyranos-1-yl-2- (cis-4-methoxycyclohexyloxy) benzene Mass spectrum (ESI + ): m / z = 403/405 (chlorine) [M + H] + (2) 1-chloro-4-β-D-glucopyranos-1-yl-2- (trans-4-methoxy) cyclohexyloxy) -benzene Mass spectrum (ESI + ): m / z = 420/422 (chlorine) [M + NH 4 ] + (3) 1-chloro-4-β-D-glucopyranos-1-yl-2-cyclohexylidenemethylbenzene Mass spectrum (ESI + ): m / z = 386/388 (chlorine) [M + NH 4 ] + (4) 1-β-D-glucopyranos-1-yl-3- (4-methoxycyclohexylmethyl) benzene *** 1- (2,3,4,6-tetra-O-acetyl-β-D-glucopyranos-1-yl) -3- (4-methoxycyclohexylmethyl) benzene [see Example 2 (1)] Mass spectrum (ESI + ): m / z = 367 [M + H] + (5) 1-β-D-glucopyranos-1-yl-3- (4-hydroxycyclohexylidenemethyl) benzene Mass spectrum (ESI + ): m / z = 368 [M + NH 4 ] +
Beispiel 2Example 2
1-Chlor-4-β-D-glucopyranos-1-yl-2-cyclohexylmethyl-benzol 1-chloro-4-β-D-glucopyranos-1-yl-2-cyclohexylmethyl-benzene
Zu
einer Lösung
von 0,10 g 1-Chlor-4-β-D-glucopyranos-1-yl-2-cyclohexylidenmethylbenzol
in 5 ml Ethylacetat werden 40 mg 10% Palladium auf Kohle gegeben.
Die Lösung
wird 1 h unter Wasserstoffatmosphäre (1 atm) bei Raumtemperatur
gerührt.
Danach wird der Katalysator abfiltriert, das Filtrat eingeengt und der
Rückstand über Kieselgel
chromatografiert (Dichlormethan/Methanol 4:1).
Ausbeute: 0,07
g (70% der Theorie)
Massenspektrum (ESI+):
m/z = 388/390 (Chlor) [M+NH4]+ To a solution of 0.10 g of 1-chloro-4-β-D-glucopyranos-1-yl-2-cyclohexylidenemethylbenzene in 5 mL of ethyl acetate is added 40 mg of 10% palladium on carbon. The solution is stirred for 1 h under a hydrogen atmosphere (1 atm) at room temperature. Thereafter, the catalyst is filtered off, the filtrate was concentrated and the residue chromatographed on silica gel (dichloromethane / methanol 4: 1).
Yield: 0.07 g (70% of theory)
Mass spectrum (ESI + ): m / z = 388/390 (chlorine) [M + NH 4 ] +
Analog Beispiel 2 werden folgende Verbindungen erhalten: (1) 1-(2,3,4,6-tetra-O-acetyl-β-D-glucopyranos-1-yl)-3-(4-methoxy-cyclohexylmethyl)benzol Massenspektrum (ESI+): m/z = 535 [M+H]+ (2) 1-β-D-glucopyranos-1-yl-3-(4-hydroxy-cyclohexylmethyl)-benzol Massenspektrum (ESI+): m/z = 370 [M+NH4]+ The following compounds are obtained analogously to Example 2: (1) 1- (2,3,4,6-tetra-O-acetyl-β-D-glucopyranos-1-yl) -3- (4-methoxycyclohexylmethyl) benzene Mass spectrum (ESI + ): m / z = 535 [M + H] + (2) 1-β-D-glucopyranos-1-yl-3- (4-hydroxycyclohexylmethyl) benzene Mass spectrum (ESI + ): m / z = 370 [M + NH 4 ] +
Analog den vorstehend genannten Beispielen und anderen literaturbekannten Verfahren werden auch folgende Verbindungen hergestellt: Analogously to the abovementioned examples and other processes known from the literature, the following compounds are also prepared:
Nachfolgend werden Beispiele zu Darreichungsformen beschrieben, worin die Angabe "Wirkstoff" eine oder mehrere erfindungsgemäße Verbindungen, einschließlich deren Salze bedeutet. Im Falle einer der beschriebenen Kombinationen mit einem oder mehreren weiteren Wirksubstanzen umfasst der Begriff "Wirkstoff" auch die weiteren Wirksubstanzen.following Examples of dosage forms are described in which the term "active ingredient" is one or more compounds of the invention, including their salts means. In the case of one of the combinations described with one or more further active substances, the term "active substance" also includes the other Active substances.
Beispiel AExample A
Tabletten mit 100 mg WirksubstanzTablets with 100 mg active substance
Zusammensetzung:
Herstellungverfahren:Production process:
Wirkstoff,
Milchzucker und Stärke
werden gemischt und mit einer wäßrigen Lösung des
Polyvinylpyrrolidons gleichmäßig befeuchtet.
Nach Siebung der feuchten Masse (2.0 mm-Maschenweite) und Trocknen
im Hordentrockenschrank bei 50°C
wird erneut gesiebt (1.5 mm-Maschenweite) und das Schmiermittel
zugemischt. Die pressfertige Mischung wird zu Tabletten verarbeitet.
Beispiel BExample B
Tabletten mit 150 mg WirksubstanzTablets with 150 mg active substance
Zusammensetzung:
Herstellung:production:
Die mit Milchzucker, Maisstärke und Kieselsäure gemischte Wirksubstanz wird mit einer 20%igen wäßrigen Polyvinylpyrrolidonlösung befeuchtet und durch ein Sieb mit 1.5 mm-Maschenweite geschlagen.The with milk sugar, corn starch and silica mixed active substance is moistened with a 20% aqueous solution of polyvinylpyrrolidone and beaten through a sieve of 1.5 mm mesh size.
Das
bei 45°C
getrocknete Granulat wird nochmals durch dasselbe Sieb gerieben
und mit der angegebenen Menge Magnesiumstearat gemischt. Aus der
Mischung werden Tabletten gepreßt.
Beispiel CExample C
Hartgelatine-Kapseln mit 150 mg WirksubstanzHard gelatin capsules with 150 mg active substance
Zusammensetzung:
Herstellung:production:
Der Wirkstoff wird mit den Hilfsstoffen vermengt, durch ein Sieb von 0.75 mm-Maschenweite gegeben und in einem geeigneten Gerät homogen gemischt.Of the Active substance is mixed with the excipients, through a sieve of 0.75 mm mesh size and homogeneous in a suitable device mixed.
Die
Endmischung wird in Hartgelatine-Kapseln der Größe 1 abgefüllt.
Beispiel DExample D
Suppositorien mit 150 mg WirksubstanzSuppositories with 150 mg active substance
Zusammensetzung:
Herstellung:production:
Nach dem Aufschmelzen der Suppositorienmasse wird der Wirkstoff darin homogen verteilt und die Schmelze in vorgekühlte Formen gegossen.To the melting of the suppository mass becomes the active ingredient therein distributed homogeneously and the melt poured into pre-cooled molds.
Beispiel EExample E
Ampullen mit 10 mg WirksubstanzAmpoules with 10 mg active substance
Zusammensetzung:
Herstellung:production:
Die Wirksubstanz wird in der erforderlichen Menge 0.01 n HCl gelöst, mit Kochsalz isotonisch gestellt, sterilfiltriert und in 2 ml Ampullen abgefüllt.The Active substance is dissolved in the required amount of 0.01 N HCl, with Saline is isotonic, sterilized by filtration and in 2 ml ampoules bottled.
Beispiel FExample F
Ampullen mit 50 mg WirksubstanzAmpoules with 50 mg active substance
Zusammensetzung:
Herstellung:production:
Die Wirksubstanz wird in der erforderlichen Menge 0.01 n HCl gelöst, mit Kochsalz isotonisch gestellt, sterilfiltriert und in 10 ml Ampullen abgefüllt.The Active substance is dissolved in the required amount of 0.01 N HCl, with Saline is isotonic, sterile filtered and in 10 ml ampoules bottled.
Claims (22)
Priority Applications (6)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE102004046012A DE102004046012A1 (en) | 2004-09-21 | 2004-09-21 | New D-glucopyranosylphenyl-substituted cyclic compounds useful as sodium-dependent glucose cotransporter inhibitors for treating metabolic diseases, e.g. diabetes |
| PCT/EP2005/007956 WO2006010557A1 (en) | 2004-07-27 | 2005-07-21 | D-glucopyranosyl phenyl-substituted cyclene, medicaments containing these compounds, their use, and method for the production thereof |
| CA002574451A CA2574451A1 (en) | 2004-07-27 | 2005-07-21 | D-glucopyranosyl phenyl-substituted cyclene, medicaments containing these compounds, their use, and method for the production thereof |
| JP2007522988A JP2008508213A (en) | 2004-07-27 | 2005-07-21 | D-glucopyranosyl-phenyl-substituted cyclics, pharmaceuticals containing such compounds, their use and methods for their production |
| EP05775126A EP1773800A1 (en) | 2004-07-27 | 2005-07-21 | D-glucopyranosyl phenyl-substituted cyclene, medicaments containing these compounds, their use, and method for the production thereof |
| US11/190,315 US7417032B2 (en) | 2004-07-27 | 2005-07-27 | D-xylopyranosyl-phenyl-substituted cycles, medicaments containing such compounds, their use and process for their manufacture |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE102004046012A DE102004046012A1 (en) | 2004-09-21 | 2004-09-21 | New D-glucopyranosylphenyl-substituted cyclic compounds useful as sodium-dependent glucose cotransporter inhibitors for treating metabolic diseases, e.g. diabetes |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| DE102004046012A1 true DE102004046012A1 (en) | 2006-03-23 |
Family
ID=36001685
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE102004046012A Withdrawn DE102004046012A1 (en) | 2004-07-27 | 2004-09-21 | New D-glucopyranosylphenyl-substituted cyclic compounds useful as sodium-dependent glucose cotransporter inhibitors for treating metabolic diseases, e.g. diabetes |
Country Status (1)
| Country | Link |
|---|---|
| DE (1) | DE102004046012A1 (en) |
-
2004
- 2004-09-21 DE DE102004046012A patent/DE102004046012A1/en not_active Withdrawn
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP1797107B1 (en) | D-pyranosyl-substituted phenyls, medicaments containing said compounds, use thereof, and method for the production thereof | |
| EP1765842B1 (en) | D-xylopyranosyl-substituted phenyls, medicaments containing said compounds, the use thereof, and methods for producing the same | |
| EP1773800A1 (en) | D-glucopyranosyl phenyl-substituted cyclene, medicaments containing these compounds, their use, and method for the production thereof | |
| EP1660509B1 (en) | Glucopyranosyloxy- pyrazoles, pharmaceutical compositions containing these compounds, the use thereof and processes for the preparation thereof | |
| WO2006018150A1 (en) | D-xylopyranosyl-phenyl-substituited cyclene, medicaments containing said compounds, use thereof and method for the production thereof | |
| EP1730131B1 (en) | Glucopyranosyl-substituted benzol derivatives, drugs containing said compounds, the use thereof and method for the production thereof | |
| EP1771460A1 (en) | Methylidene-d-xylopyranosyl-substituted and oxo-d-xylopyranosyl-substituted phenyls, medicaments containing these compounds, their use and method for the production thereof | |
| DE102004012676A1 (en) | New glucopyranosyl-substituted benzene derivatives are sodium-dependent glucose cotransporter inhibitors, useful for treating e.g. metabolic disorders (type 1 and type 2 diabetes mellitus or metabolic acidosis) | |
| EP1699807A2 (en) | Glucopyranosyloxy-substituted aromates, medicaments containing said compounds, the use thereof, and methods for producing the same | |
| DE102004039096A1 (en) | New D-xylopyranosyl-phenyl-substituted cycle compounds useful for treating e.g. diabetes mellitus, complications of diabetes, metabolic acidosis or ketosis | |
| DE102004046583A1 (en) | New D-xylopyranosyl-phenyl-substituted cycle compounds useful for treating e.g. diabetes mellitus, complications of diabetes, metabolic acidosis or ketosis | |
| DE102004046012A1 (en) | New D-glucopyranosylphenyl-substituted cyclic compounds useful as sodium-dependent glucose cotransporter inhibitors for treating metabolic diseases, e.g. diabetes | |
| DE102004036314A1 (en) | New D-glucopyranosylphenyl-substituted cyclic compounds useful as sodium-dependent glucose cotransporter inhibitors for treating metabolic diseases, e.g. diabetes | |
| DE102004032823A1 (en) | New D-xylopyranosyl-substituted phenyl compounds are sodium-dependent glucose cotransporter inhibitors useful to prevent or treat e.g. diabetes mellitus, complications of diabetes, metabolic acidosis or ketosis | |
| DE102004040168A1 (en) | New glucopyranosyl-substituted benzene derivatives are sodium-dependent glucose cotransporter inhibitors, useful for treating e.g. metabolic disorders (type 1 and type 2 diabetes mellitus or metabolic acidosis) | |
| DE102004054603A1 (en) | New D-xylopyranosyl-substituted phenyl compounds are sodium-dependent glucose cotransporter inhibitors useful to prevent or treat e.g. diabetes mellitus, complications of diabetes, metabolic acidosis or ketosis | |
| DE102004061145A1 (en) | New glucopyranosyl-substituted benzene derivatives are sodium-dependent glucose cotransporter inhibitors, useful for treating e.g. metabolic disorders (type 1 and type 2 diabetes mellitus or metabolic acidosis) | |
| DE10359960A1 (en) | New glucopyranosyloxy-pyrazole derivatives are sodium dependent glucose cotransporter inhibitors used for treating and preventing metabolic disorders, particularly diabetes | |
| DE10339549A1 (en) | New glucopyranosyloxy-pyrazole derivatives are sodium dependent glucose cotransporter inhibitors used for treating and preventing metabolic disorders, particularly diabetes |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| R005 | Application deemed withdrawn due to failure to request examination |
Effective date: 20110922 |