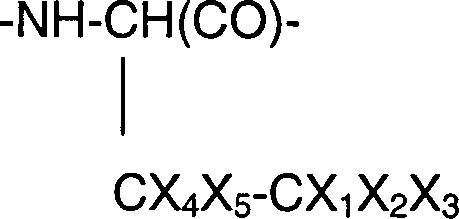DE102004011988A1 - Cyclosporin derivatives and pharmaceutical compositions containing them - Google Patents
Cyclosporin derivatives and pharmaceutical compositions containing them Download PDFInfo
- Publication number
- DE102004011988A1 DE102004011988A1 DE102004011988A DE102004011988A DE102004011988A1 DE 102004011988 A1 DE102004011988 A1 DE 102004011988A1 DE 102004011988 A DE102004011988 A DE 102004011988A DE 102004011988 A DE102004011988 A DE 102004011988A DE 102004011988 A1 DE102004011988 A1 DE 102004011988A1
- Authority
- DE
- Germany
- Prior art keywords
- cyclosporin
- cyclosporin analog
- group
- analog according
- methyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K7/00—Peptides having 5 to 20 amino acids in a fully defined sequence; Derivatives thereof
- C07K7/64—Cyclic peptides containing only normal peptide links
- C07K7/645—Cyclosporins; Related peptides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Immunology (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Pharmacology & Pharmacy (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Animal Behavior & Ethology (AREA)
- General Chemical & Material Sciences (AREA)
- Public Health (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Engineering & Computer Science (AREA)
- Communicable Diseases (AREA)
- Oncology (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Genetics & Genomics (AREA)
- Molecular Biology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Transplantation (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
Die vorliegende Erfindung betrifft neue cyclische Peptide aus der Cyclosporin-Reihe, deren Fähigkeit, die Proteinphosphatase Calzineurin inhibieren zu können und dadurch immunsuppressiv zu wirken, geschaltet werden kann. Unerwarteterweise wurde gefunden, dass sich durch Modifikation der Hydroxylgruppe eines [D-Ser]·8·-Cyclosporins mittels geeigneter aktivierbarer Substitutienten die immunsuppressive Wirkung solcher Cyclosporinderivate ausschalten lässt. Da therapeutisch verwendete Dosen von Cyclosporin A zahlreiche unerwünschte Nebenwirkungen besitzen, besteht der Wert vorliegender Erfindung darin, dass die immunsuppressive Aktivität der bereitgestellten Cyclosporinderivate abgeschaltet werden kann. Es besteht auch die Möglichkeit, das nicht-immunsuppressive Cyclosporinderivat im Gemisch mit der Muttersubstanz oder aber ausschließlich therapeutisch einzusetzen. Bei therapeutischer Anwendung erfindungsgemäßer schaltbarer Cyclosporinderivate kann deren Wirkung während der Therapie beeinflusst werden.The present invention relates to novel cyclic peptides of the cyclosporin series, whose ability to inhibit the protein phosphatase calcineurin can be switched and thereby act immunosuppressive. Unexpectedly, it has been found that by modifying the hydroxyl group of a [D-Ser] .8.-cyclosporin by means of suitable activatable substituents, it is possible to eliminate the immunosuppressive effect of such cyclosporin derivatives. Since therapeutically used doses of cyclosporin A have many undesirable side effects, the value of the present invention is that the immunosuppressive activity of the provided cyclosporin derivatives can be switched off. It is also possible to use the non-immunosuppressive cyclosporin derivative in a mixture with the parent substance or exclusively therapeutically. In the case of therapeutic use of switchable cyclosporin derivatives according to the invention, their effect during the therapy can be influenced.
Description
Hintergrund der Erfindungbackground the invention
Pathobiochemische Veränderungen des Immunsystems liegen einer großen Gruppe von Autoimmunerkrankungen und chronischen Entzündungen zu Grunde, wie z.B folgende Erkrankungen.: Systemischer lupus Erythematosus (SLE), Chronische rheumatoide Arthritis, Typ 1 Diabetes, chronisch entzündliche Darmerkrankungen, Gallenzirrhose, Uveitis, multiple Sklerose und andere Erkrankungen wie Morbus Crohn, Colitis ulzerosa, bullöses Pemphigoid, Sarkosidose, Psoriasis, atopische Dermatitis, Ichthyosis oder Graves Opthalmopathie. Obwohl die zugrunde liegende Pathogenese jeweils unterschiedlich sein kann, ist das gemeinsame biochemische Merkmal dieser Erkrankungen das Auftreten von Autoantikörpern bzw. autoaggressiven Lymphozyten, welche zur Entzündung und letztendlich Zerstörung der betroffenen Zellen führen. In gleicher Weise kann es nach Knochenmark- oder Organtransplantation zur Bildung von Antikörpern, bzw. gegen das Transplantat gerichteten Immunzellen kommen, was letztendlich zur Transplantatabstoßung führt. Wie zahlreiche Publikationen (z.B.: Altschuh D. Journal of Molecular Recognition. 15(5): 277–285, 2002; Griffiths B. und Emery P. Lupus. 10(3): 165–170, 2001; Nasonov EL. Et al. Terapevticheskii Arkhiv. 72(5): 67–71, 2000; Winkler M. Biodrugs. 14(3): 185–193, 2000) und Patentschriften (z.B.: US 491488; US5948755) zeigen, lassen sich Transplantatabstoßungen therapeutisch durch Gabe von Cyclosporinen verhindern. Ein weiterer relativ gut untersuchter Indikationsbereich bestimmter Cyclosporine, wie z.B. Cyclosporin A (CsA) liegt in der beobachteten Hemmwirkung gegen das Humane Immunodefizienzvirus (HIV) (wie z. B.: Zavyalov V.P. et al. APMIS. 103(6): 401–415, 1995). Untersuchungen an kortikosteorid-abhängigen Asthmapatienten zeigen, daß hier die Lungenfunktion durch CsA als Therapeutikum verbessert werden kann (z.B.: Powell N. et al. Journal of Allergy & Clinical Immunology. 108(6): 915–917, 2001; Eckstein J.W. und Fung J. Expert Opinion on Investigational Drugs. 12(4): 647–653, 2003). Die bekannteste Nebenwirkung von CsA ist seine Nephrotoxizität und darüber hinaus auch Nebenwirkungen wie abnormale Leberfunktion, Hirsutismus, Zahnfleischhypertrophie, Tremor, Hyperästhesie und gastrointestinale Störungen und Zunahme der Inzidenz für unterschiedliche Tumore (z.B.: Herman M. Journal of Laboratory & Clinical Medicine 137(1): 14–20, 2001; Landewe R.B.M. et al. Nature Medicine 5(7): 714, 1999).pathobiochemical changes of the immune system are a large group of autoimmune diseases and chronic inflammation underlying, such as the following diseases .: Systemic lupus erythematosus (SLE), Chronic Rheumatoid Arthritis, Type 1 Diabetes, Chronic inflammatory Intestinal diseases, biliary cirrhosis, uveitis, multiple sclerosis and other diseases such as Crohn's disease, ulcerative colitis, bullous pemphigoid, Sarcosidosis, Psoriasis, Atopic Dermatitis, Ichthyosis or Graves Opthalmopathy. Although the underlying pathogenesis respectively may be different, is the common biochemical feature these diseases the occurrence of autoantibodies or autoaggressive Lymphocytes, which cause inflammation and finally destruction lead the affected cells. In the same way it can after bone marrow or organ transplantation for the formation of antibodies, or against the graft-targeted immune cells come what ultimately leads to graft rejection. Like many publications (e.g., Altschuh D. Journal of Molecular Recognition 15 (5): 277-285, 2002; Griffiths B. and Emery P. Lupus. 10 (3): 165-170, 2001; Nasonov EL. et al. Terapevticheskii Arkhiv. 72 (5): 67-71, 2000; Winkler M. Biodrugs. 14 (3): 185-193, 2000) and patents (e.g., US 491488; US 5948755) graft rejections therapeutically by administering cyclosporins. Another relatively well-researched indication of certain cyclosporins, such as. Cyclosporin A (CsA) has the observed inhibitory effect against Human Immunodeficiency Virus (HIV) (such as: Zavyalov V. P. et al. APMIS. 103 (6): 401-415, 1995). Investigations on corticosteroid-dependent asthma patients show that here the lung function can be improved by CsA as a therapeutic agent (e.g., Powell N. et al., Journal of Allergy & Clinical Immunology, 108 (6): 915-917, 2001; Eckstein J.W. and Fung J. Expert Opinion on Investigational Drugs. 12 (4): 647-653, 2003). The best known side effect of CsA is its nephrotoxicity and beyond Side effects such as abnormal liver function, hirsutism, gum hypertrophy, Tremor, hyperesthesia and gastrointestinal disorders and Increase in incidence for different tumors (e.g., Herman M. Journal of Laboratory & Clinical Medicine 137 (1): 14-20, 2001; Landewe R.B.M. et al. Nature Medicine 5 (7): 714, 1999).
Cyclosporine sind eine Familie von immunsuppressiven Verbindungen, welche sich durch Fermentation verschiedener Pilze, wie z.B. Tolypocladium inflatum gewinnen lassen (Lexikon der Biochemie, Spektrumverlag, Deutschland). Generell kann die Klasse der Cyclosporine als cyclische Peptide mit 11 Aminosäuren (Formel I) beschrieben werden.cyclosporine are a family of immunosuppressant compounds which are by fermentation of various fungi, e.g. Tolypocladium inflatum to win (Lexikon der Biochemie, Spektrumverlag, Germany). Generally speaking, the class of cyclosporins can be called cyclic peptides with 11 amino acids (formula I).
Dabei steht bei der Verbindung Cyclosporin A (CsA) R1 für Methyl(4R)-4-[(E)-2-butenyl]-4-methyl-L-threonin, R2 für α-Aminobuttersäure, R3 für N-Methyl-glycin, R4, R6, R9 und R10 für N-Methyl-L-leucin, R5 für L-Valin, R1 für L-Alanin, R8 für D-Alanin und R11 für N-Methyl-L-valin.The compound cyclosporin A (CsA) R 1 is methyl (4R) -4 - [(E) -2-butenyl] -4-methyl-L-threonine, R 2 is α-aminobutyric acid, R 3 is N- Methyl glycine, R 4 , R 6 , R 9 and R 10 for N-methyl-L-leucine, R 5 for L-valine, R 1 for L-alanine, R 8 for D-alanine and R 11 for N- methyl-L-valine.
Die biologische Aktivität von CsA ist vielfältig. So hemmt CsA die Aktivität des Enzyms Peptidyl-Prolyl cis/trans – Isomerase (PPlase) vom Cyclophilin-Typ, wie dies auch in Beispiel 1a dargestellt ist. Diese auch als Faltungshelferenzyme oder als Peptidyl-Prolyl cis/trans Isomerasen bezeichneten Proteine, im weiteren als PPlasen bezeichnet, werden entsprechend den Empfehlungen des „Nomenclature Committee of the International Union of Biochemistry and Molecular Biology" („Enzyme Nomenclature", Academic Press, 1992) unter der EC Nummer 5.2.1.8 zusammengefaßt. Diese Enzyme können die cis/trans-Isomerisierung von Peptidbindungen in Peptiden und Proteinen katalysieren (Schiene-Fischer C. et al. Biological Chemistry. 383(12): 1865–1873, 2002; Tradler T. et al. FEBS Letters. 407(2): 184–190, 1997; Ivery M.T.G. Medicinal Research Reviews. 20(6): 452–484, 2000. Es konnte in zahlreichen Publikationen gezeigt werden, daß diese Katalyse sowohl bei der Proteinfaltung als auch bei der zellulären Signalweiterleitung eine Schalterfunktion ausüben kann. Von den verschiedenen Mitgliedern dieser PPlasen, im humanen Genom sind mindestens 12 genetisch unterschiedliche Cyclophiline kodiert, wird insbesondere der Interaktion zu Cyclophilin 18 (Cyp18) eine besondere Bedeutung für die Immunsuppression zugeschrieben. So hemmt der binäre CsA/Cyp18 – Komplex die Proteinphosphatase Calzineurin (Liu et al.: Cell 66 (1991) 807), wie dies auch in Beispiel 1b zusammenfassend dargestellt ist. Die Hemmung dieser Phosphatase in Lymphozyten führt letztendlich, wie zahlreiche Publikationen zeigen (z.B.: Ho et al.: Clin. Immun. and Immunopathology 80 (1996) 40), zur Immunsuppression. Die Bestimmung dieser Wirkung ist in Beispiel 2 dargestellt. Die Interaktion von CsA zu Cyp18 erfolgt über die Reste 9, 10, 11, 1, 2 des CsA, die auch als „binding domain" bezeichnet werden. Demgegenüber bindet Calzineurin an CsA über die als „effector domain" bezeichneten Reste 4, 5, 6, 7, 8 des CsA. Eine weitere pharmakologisch wichtige Wirkung von CsA ist die Sensitivierung von Krebszellen gegenüber Chemotherapeutika, wie Vincistin (VCR) oder Daunorubicin (DNR). So wird seit längerem ein als „multi drug resistance" (MDR) in der Literatur bezeichnetes Phänomen beobachtet (z.B.: Duraj J. et al. Anticancer Research. 22(6A): 3425–8, 2002; Chorvath B. et al. International Journal of Cancer. 72(5): 916–7, 1997; Li G. et al. Chinese Journal of Oncology. 24(4): 370–4, 2002; Suarez L. et al. Haematologica. 86(12): 1287–95, 2001), daß Tumorzellen gegenüber anfänglich wirksamen Therapeutika resistent werden. Daß diese unerwünschte Resistenz durch therapeutische Verabreichung von CsA vorteilhaft beeinflußt werden kann, konnte in mehreren Untersuchungen dargestellt werden, so z.B.: Yamamoto M et al. Anti-Cancer Drugs. 6(4): 570–7, 1995; Slater L. et al. Proc. Am Assoc. Cancer Res. 27 (1982) 392; Pallis M. et al. Leukemia & Lymphoma. 43(6): 1221–8, 2002; Jachez B. und Loor F. Anti-Cancer Drugs. 4(6): 605–15, 1993; Malingre M.M. et al. British Journal of Cancer. 84(1): 42–7, 2001.The biological activity of CsA is manifold. CsA, for example, inhibits the activity of the cyclophilin-type enzyme peptidyl-prolyl cis / trans isomerase (PPlase), as shown in Example 1a. These proteins, also referred to as folding helper enzymes or peptidyl-prolyl cis / trans isomerases, hereinafter referred to as PPlases, are prepared according to the recommendations of the Nomenclature Committee of the International Union of Biochemistry and Molecular Biology ("Enzyme Nomenclature", Academic Press, 1992 ) under EC number 5.2.1.8. These enzymes can catalyze the cis / trans isomerization of peptide bonds in peptides and proteins (Rail-Fischer C. et al., Biological Chemistry, 383 (12): 1865-1873, 2002; Tradler T. et al., FEBS Letters. 2): 184-190, 1997; Ivery MTG Medicinal Research Reviews 20 (6): 452-484, 2000. It has been demonstrated in numerous publications that this catalysis performs a switch function in both protein folding and cellular signal transduction Of the various members of these PPlases, at least 12 genetically distinct cyclophilins are encoded in the human genome, the interaction with cyclophilin 18 (Cyp18) is believed to be of particular importance for immunosuppression, with the binary CsA / Cyp18 complex inhibiting the protein phosphatase calcineurin (Liu et al .: Cell 66 (1991) 807), as also summarized in Example 1b The inhibition of this phosphatase in lymphocytes ultimately leads, as a result of the e show numerous publications (eg: Ho et al .: Clin. Immune. and Immunopathology 80 (1996) 40), for immunosuppression. The determination of this effect is shown in Example 2. The interaction of CsA to Cyp18 occurs via residues 9, 10, 11, 1, 2 of CsA, which are also referred to as "binding domain." In contrast, calcineurin binds to CsA via residues 4, 5, 6, 7, 8 of CsA designated as "effector domain". Another pharmacologically important effect of CsA is the sensitization of cancer cells to chemotherapeutics, such as vincistin (VCR) or daunorubicin (DNR). For example, a phenomenon known as "multi drug resistance" (MDR) has long been reported in the literature (eg, Duraj J. et al, Anticancer Research, 22 (6A): 3425-8, 2002, Chorvath B. et al., International Journal of Cancer 72 (5): 916-7, 1997, Li G. et al., Chinese Journal of Oncology, 24 (4): 370-4, 2002, Suarez L. et al., Haematologica, 86 (12): 1287-95, 2001) that tumor cells can become resistant to initially effective therapeutics.This undesirable resistance can be favorably influenced by therapeutic administration of CsA has been demonstrated in several studies, including: Yamamoto M et al., Anti-Cancer Drugs. 6 (4): 570-7, 1995, Slater L. et al., Proc., Assoc. Cancer Res 27 (1982) 392, Pallis M. et al., Leukemia & Lymphoma, 43 (6): 1221-8, 2002; Jachez B. and Loor F. Anti-Cancer Drugs 4 (6): 605-15, 1993; Malingre MM et al., British Journal of Cancer. 84 (1): 42-7, 2001.
Möglicherweise über eine Inhibierung der Allergen induzierten Proliferation und IL-5 Produktion spezieller weißer Blutzellen (periphere mononucleäre Blutzellen (PBMC)) bewirkt CsA eine Verbesserung der Lungenfunktion bei Asthmatikern (Powell N. et al. Journal of Allergy & Clinical Immunology. 108(6): 915–917, 2001). Auch der Schutz der Lunge durch CsA-Gaben gegenüber hypoxischen Schäden wird therapeutisch genutzt, z.B.: Matthew et al. American Journal of Physiology – Lung Cellular & Molecular Physiology. 20(5): L786–L795, 1999). Solche Effekte konnten in verschiedenen Studien an größeren Patientenkollektiven abgesichert werden (so z.B.: Lock S.H. et al American Journal of Respiratory & Critical Care Medicine. 153(2): 509–514, 1996).Maybe over one Inhibition of allergen-induced proliferation and IL-5 production special white Blood cells (peripheral mononuclear Blood Cells (PBMC)) causes CsA to improve lung function in asthmatics (Powell N. et al., Journal of Allergy & Clinical Immunology. 108 (6): 915-917, 2001). Also, the protection of the lungs by CsA-gifts against hypoxic damage is used therapeutically, for example: Matthew et al. American Journal of Physiology - lung Cellular & Molecular Physiology. 20 (5): L786-L795, 1999). Such effects could be found in different studies on larger patient populations be secured (so for example: Lock S.H. et al American Journal of Respiratory & Critical Care Medicine. 153 (2): 509-514, 1996).
Eine weitere wichtige pharmakologische Wirkung von CsA ist seine starke Hemmwirkung gegen Retroviren, insbesondere gegenüber dem humanen Immundefizienzvirus (HIV). Diese Wirkung konnte von unterschiedlichsten Autoren nachgewiesen werden, so z.B.: Franke EK. und Luban J. Virology. 222(1): 279–82, 1996; Drewe J. et al. Biochemical Pharmacology. 57(10): 1147–52, 1999; Tourne L. et al. Journal of the American Academy of Dermatology. 37 (3 Pt 1): 501–2, 199; Saphire AC et al. Immunologic Research. 21(2-3): 211–7, 2000 oder wurde in Patentschriften niedergelegt, z.B.: WO97/04005; US6270957; US5948755. Während CsA als Immunsuppressivum in den unterschiedlichsten Rezepturen derzeit weltweit angewendet wird, ist sein Einsatz zur Behandlung der MDR oder von HIV-Infektionen auf Grund der benötigten hohen Dosen und den damit verbundenen Nebenwirkungen nicht möglich. Allerdings legen einige Arbeiten nahe, daß nicht-immunsuppressiv wirkende Cyclosporine, obwohl noch Inhibitoren der PPlase-aktivität, sowohl zur Behandlung von HIV-Infektionen (Bartz et al. (1995), Proc. Natl. Acad. Sci USA 92: 5381, Rosenwirth et al. (1994) Antimicrobial Agents and Chemotherapy 38: 1763; US6270957) als auch der MDR (Lopez et al. Leukemia Research 27(5): 413–423, 2003; Atadja P. et al. Cancer & Metastasis Reviews 17(2): 163–168, 1998; Naito M. Tsuruo T. Cancer Chemotherapy & Pharmacology. 40 (Suppl S): S 20–S 24, 1997) geeignet sind, ohne die für CsA beobachteten Nebenwirkungen zu zeigen.A Another important pharmacological effect of CsA is its strong Inhibitory activity against retroviruses, especially against the human immunodeficiency virus (HIV). This effect was proven by different authors become, so for example: Franke EK. and Luban J. Virology. 222 (1): 279-82, 1996; Drewe J. et al. Biochemical Pharmacology. 57 (10): 1147-52, 1999; Tour L. et al. Journal of the American Academy of Dermatology. 37 (3 Pt 1): 501-2, 199; Sapphire AC et al. Immunologic Research. 21 (2-3): 211-7, 2000 or has been deposited in patents, e.g., WO97 / 04005; US6270957; US5948755. While CsA as an immunosuppressant in a wide variety of formulations currently being used worldwide, its use is for treatment the MDR or HIV infections due to the high levels needed Doses and associated side effects not possible. Indeed Some work suggests that non-immunosuppressive Cyclosporins, although still inhibitors of PPlase activity, both used to treat HIV infections (Bartz et al., 1995), Proc. Natl. Acad Sci USA 92: 5381, Rosenwirth et al. (1994) Antimicrobial Agents and Chemotherapy 38: 1763; US6270957) as well as the MDR (Lopez et al., Leukemia Research 27 (5): 413-423, 2003; Atadja P. et al. Cancer & Metastasis Reviews 17 (2): 163-168, 1998; Naito M. Tsuruo T. Cancer Chemotherapy & Pharmacology. 40 (Suppl S): S 20-S 24, 1997) are suitable, without for CsA observed to show side effects.
Wie zahlreiche Untersuchungsbefunde belegen (Pong K. und Zaleska MM. Current Drug Targets – Cns & Neurological Disorders. 2(6): 349–56, 2003; Gold BG. und Villafranca JE. Current Topics in Medicinal Chemistry. 3(12): 1368–75, 2003; Udina E. und Navarro X. Neurologia. 17(4): 200–13, 2002 ) besitzt CsA auch neuroprotective bzw. regenerative Eigenschaften bei verschiedenen neurologischen Indikationen wie z.B. bei Alzheimer, Amyotropher Lateralsclerose, oder Parkinson.As Numerous examination findings prove (Pong K. and Zaleska MM. Current Drug Targets - Cns & Neurological Disorders. 2 (6): 349-56, 2003; Gold BG. and Villafranca JE. Current Topics in Medicinal Chemistry. 3 (12): 1368-75, 2003; Udina E. and Navarro X. Neurologia. 17 (4): 200-13, 2002 ) CsA also has neuroprotective or regenerative properties in various neurological indications, e.g. in Alzheimer's, Amyotrophic lateral sclerosis, or Parkinson's.
Weiterhin sind insbesondere die antimikrobiellen (High KP. Transplantation. 57(12): 1689–700, 1994) und antiparasitären (z.B.: Bell A. et al. General Pharmacology. 27(6): 963–71, 1996; Chappell LH et al. Parasitology. 105 Suppl: S25–40, 1992) Eigenschaften in der Tier- und Humanmedizin beschrieben.Farther In particular, the antimicrobial (High KP. Transplantation. 57 (12): 1689-700, 1994) and anti-parasitic (e.g., Bell A. et al., General Pharmacology 27 (6): 963-71, 1996; Chappell LH et al. Parasitology. 105 Suppl: S25-40, 1992) Properties in of animal and human medicine.
Nicht-immunsuppressive CyclosporineNon-immunosuppressive cyclosporine
Um selektiv die unterschiedlichen Wirkungen von CsA entweder als Inhibitor der PPlase-Aktivität von Cyclophilinen oder die über Hemmung der Calzineurinaktivität führende immunsuppressive Eigenschaft nutzen zu können, wurden zahlreiche Veränderungen an cyclischen Peptiden der Cyclosporin-Reihe durchgeführt. So gelang es insbesondere durch Änderungen an der „effector domain" Cyclosporinderivate zu schaffen, die nicht-immunsuppressiv wirken und Calzineurin nicht mehr inhibieren. Allgemein sind nicht immunsuppressive cyclische Peptide der Cyclosporin-Reihe unter anderem in US4914188, EP484281 oder WO9704005 beansprucht. Die dort konkret aufgeführten Substanzen, wie z.B. (gamma-Hydroxy-N-methylleucin)-Cyclosporin, Melle-4-Cyclosporin oder McVal-4-Cyclosporin und McAla-6- oder McAbu-6-Cyclosporin haben praktisch keine immunsuppressive Aktivität. Obwohl diese Substanzen die PPlase-Aktivität von Cyp18 noch inhibieren, wirken sie nicht mehr nephrotoxisch (US4914188). Überraschenderweise können diese nicht-immunsuppressiven Substanzen bei gleichzeitiger Gabe von immunsuppressivem CsA dessen nephrotoxische Eigenschaft lindern, ohne dessen immunsuppressive Eigenschaften zu verschlechtern, wie dies in der Patentschrift US4914188 und auch in der Literatur, wie z.B. Lazarova T et al.: J. Med. Chem. 46 (3003) 674 aufgeführt ist. Ein möglicher Kompensationsmechanismus dieser nicht-immunsuppresiven Verbindungen ergibt sich aus Beispiel 2.In order to selectively utilize the differential effects of CsA either as an inhibitor of PPlase activity of cyclophilins or the immunosuppressive property leading to inhibition of calcineurin activity, numerous changes have been made to cyclic peptides of the cyclosporin series. In particular, changes to the "effector domain" have made it possible to create cyclosporin derivatives which are non-immunosuppressive and no longer inhibit calcineurin. [Allgemein Allgemein] Generally, non-immunosuppressive cyclic peptides of the cyclosporin series are claimed in, inter alia, US4914188, EP484281 or WO9704005 Substances such as (gamma-hydroxy-N-methylleucine) -cyclosporin, melle-4-cyclosporin or McVal-4-cyclosporin and McAla-6 or McAbu-6-cyclosporin have virtually no immunosuppressive activity, although these substances are the PPlase Inhibit activity of Cyp18, they no longer have a nephrotoxic effect (US4914188) .Non-surprisingly, these non-immunosuppressants with simultaneous administration of immunosuppressive CsA to relieve its nephrotoxic property without impairing its immunosuppressive properties, as described in the patent US4914188 and in the literature, such as Lazarova T et al .: J.Med.Chem. 46 (3003). 674 is listed. A possible compensation mechanism of these non-immunosuppressant compounds is shown in Example 2.
Die der vorliegenden Anmeldung zugrundeliegende Aufgabe ist die Bereitstellung neuer Cyclosporinderivate, die immunsuppressiv durch Hemmung der Proteinphosphatase Calzineurin wirken, aber gezielt manipulierbar diese Eigenschaft verlieren können, unter Beibehaltung der PPlase-Inhibition.The The object underlying the present application is the provision new cyclosporin derivatives immunosuppressive by inhibition of Protein phosphatase calcineurin act, but specifically manipulated can lose this property while retaining PPlase inhibition.
Eine weitere Aufgabe der Erfindung ist die Bereitstellung von pharmazeutischen Zusammensetzungen, die für die therapeutische Anwendung der bereitgestellten Cyclosporinderivate in der Medizin geeignet sind, sowie von Hilfsmitteln, mit deren Hilfe die Eigenschaften der bereitgestellten Cyclosporinderivate gezielt in gewünschter Weise verändert werden können.A Another object of the invention is the provision of pharmaceutical Compositions for the therapeutic use of the provided cyclosporin derivatives are suitable in medicine, as well as aids, with their Help the properties of the provided cyclosporin derivatives targeted in desired Way changed can be.
Eine weitere Aufgabe der Erfindung, ist die Bereitstellung von Verfahren, mit denen die erfindungsgemäßen Cyclosporinderivate hergestellt werden können.A Another object of the invention is the provision of methods with which the cyclosporin derivatives of the invention can be produced.
Die Lösung dieser Aufgaben sind die in den Ansprüchen beschriebenen erfindungsgemäßen Gegenstände.The solution These objects are the objects of the invention described in the claims.
Entsprechend dem oben aufgeführten Konzept einer „Effector Domain" sollten chemische Modifizierungen der R8-Position (N-Methyl-glycin), die noch zu dieser Domäne gehören, die Inhibierungskonstanten der Proteinphosphatase Calzineurin und damit die immunsuppressiven Eigenschaften von CsA signifikant beeinflussen. Wie in der nachstehenden Tabelle 1 gezeigt, beeinflussen erstaunlicherweise selbst großvolumige Änderungen, wie die Einführung eines (Nitroveratryl) oxycarbonylrestes die Inhibierung von Calzineurin nur unwesentlich (Verbindung 11, Tabelle 1). Table 1. Cyp 18- und CaN-Inhibition verschiedener CsA-Derivate According to the above-mentioned concept of an "effector domain", chemical modifications of the R 8 -position (N-methyl-glycine) still belonging to this domain should significantly influence the inhibition constants of the protein phosphatase calcineurin and thus the immunosuppressive properties of CsA surprisingly, even large volume changes, such as the introduction of a (nitroveratryl) oxycarbonyl radical, only marginally affect the inhibition of calcineurin (Compound 11, Table 1). Table 1. Cyp 18 and CaN inhibition of various CsA derivatives
Auch die Einführung stark geladener Gruppen, wie die Einführung unterschiedlicher Phosphoryl-D-Serine (Verbindung 3, 4, und 5), oder die Einführung eines O-Methyl- bzw. O-Carboxymethyl-D-Serins (Verbindung 2 bzw. 6) haben kaum Einfluß auf die Calzineurin-Inhibierung. Das gleiche gilt für die umfangreichen Änderungen, die in den Strukturen der Verbindungen 7 bis 11 der Tabelle 1 aufgeführt sind. Um so überraschender war, daß unter den gewählten Testbedingungen für die Verbindung Cs12 und ihre nicht in der Tabelle aufgeführten Analoga, die durch Zuführung von geeigneter Energie, wie z.B.: UV-Licht von 330 nm (Beispiel 3,4) oder durch Einwirkung eines Enzyms (Beispiel 5) oder durch Änderung des pH-Wertes (Beispiel 6) aus einer Verbindung Cs10 oder ihren Analoga hergestellt werden kann, keine Inhibition der Proteinphosphatase Calzineurin mehr feststellbar war. Damit werden mit dieser überraschenden Entdeckung zwei unterschiedliche Cyclosporinderivate (Cs10 und Cs12) bereitgestellt:Also the introduction strongly charged groups, such as the introduction of different phosphoryl-D-serines (Compound 3, 4, and 5), or the introduction of an O-methyl or O-carboxymethyl-D-serine (Compound 2 or 6) have little influence on the calcineurin inhibition. The same applies the extensive changes, which are listed in the structures of compounds 7 to 11 of Table 1. All the more surprising was that under the chosen one Test conditions for the compound Cs12 and its analogues not shown in the table, by feeder of suitable energy, such as: UV light of 330 nm (example 3,4) or by the action of an enzyme (Example 5) or by modification of the pH (Example 6) from a compound Cs10 or their Analogs can be produced, no inhibition of protein phosphatase Calzineurin was more detectable. This will be surprising with this Discovery of two different cyclosporin derivatives (Cs10 and Cs12) provided:
Cs10:Cs10:
Verbindungen, welche der Struktur von Cs10 entsprechen und die PPlase-aktivität von Cyp18 signifikant inaktivieren können, wobei hier unter signifikant ein IC50-Wert von kleiner 10 µM verstanden wird, die weiterhin die Eigenschaft besitzen Calzineurin signifikant zu inhibieren, wobei hier unter signifikant ein IC50-Wert von kleiner 10 µM verstanden wird, und welche die Eigenschaft besitzen, sich mittels geeigneter Aktivierung in eine Verbindung, welche der Struktur von Cs12 oder ihren Analoga in Tabelle 1 entspricht, umwandeln lassen, wobei die Aktivierung bei photolabilen Gruppen mittels geeigneten Lichtquellen erfolgt, bei pH-sensitiven Gruppen durch eine ausreichende pH-Änderung und bei katalyseempfindlichen Gruppen durch die Wirkung des entsprechenden Enzyms.Compounds which correspond to the structure of Cs10 and which can significantly inactivate the PPlase activity of Cyp18, which is understood here to mean significantly an IC 50 value of less than 10 μM, which furthermore possess the property of significantly inhibiting calcineurin IC 50 value of less than 10 μM, and which have the property to be converted by suitable activation into a compound which corresponds to the structure of Cs12 or its analogues in Table 1, wherein the activation in photolabile groups by means of suitable light sources occurs in pH-sensitive groups by a sufficient pH change and catalytically sensitive groups by the effect the corresponding enzyme.
Cs12:Cs12:
Verbindungen, welche aus der Struktur Cs10 (Tabelle 1) oder ihren Analoga mittels geeigneter Aktivierung erhalten wurden und der Struktur Cs12 oder ihren Analoga entsprechen, oder gezielt mittels chemischer Synthese hergestellt wurden und der Struktur Cs12 oder ihren Analoga entsprechen, wobei all diese Verbindungen die Eigenschaft besitzen, die PPlase-aktivität von Cyp18 signifikant inaktivieren zu können, wobei hier unter signifikant ein IC50-Wert von kleiner 10 µM verstanden wird, und wobei für diese Substanzen weiterhin gilt, daß sie die Eigenschaft besitzen, Calzineurin nicht signifikant zu inhibieren, wobei hier unter nicht signifikant ein IC50-Wert von größer 10 µM verstanden wird.Compounds obtained from the structure Cs10 (Table 1) or its analogues by appropriate activation and corresponding to the structure Cs12 or its analogues, or produced by chemical synthesis and corresponding to the structure Cs12 or its analogues, all of which have the property have to significantly inactivate the PPlase activity of Cyp18, which is understood to mean significantly an IC 50 value of less than 10 μM, and these substances furthermore have the property that they do not significantly inhibit calcineurin here by not significantly an IC 50 value of greater than 10 μM is understood.
Wie
in den Beispielen (7, 8, 9) aufgeführt wurde, lassen sich die
Substanzen des Typs Cs10 und Cs12 sowie ihre Analoga auf unterschiedlichste
Weise in größeren Mengen
herstellen. Die im weiteren aufgeführten Analoga A10 und A12 entsprechen in
ihren Eigenschaften bezüglich
der Inhibition bezogen auf Cyp18 bzw. Calzineurin den Substanzen
Cs10 und Cs12 und können
wie folgt beschaffen sein: worin
R1 für Methyl(4R)-4-[(E)-2-butenyl)-4-methyl-L-threonin
(MeBMT) oder Dihydro-McBMT
steht;
R2 für α-Aminobuttersäure (Abu)
oder ein an einer oder mehreren Positionen der Seitenkette fluoriertes
Derivat dieser Aminosäure
steht; wie z.B. worin X1 bis
X5 unabhängig
voneinander für
H oder F stehen, mit der Maßgabe,
daß mindestens
eins der X1, X2,
X3, X4 and X5 für
F steht;
R3 für N-Methyl-glycin (Sar), N-Methyl-D-alanin
oder ein fluoriertes Derivat davon steht;
R4,
R6, R9 and R10 unabhängig
voneinander für
N-Methyl-L-leucin (MeLeu) oder ein fluoriertes Derivat davon stehen;
R5 für
L-Valin (Val) oder ein fluoriertes Derivat davon steht; R7 für
L-Ala oder ein fluoriertes Derivat davon steht, und
R11 für
L-MeVal oder ein fluoriertes Derivat davon steht.As shown in the examples (7, 8, 9), the substances of the type Cs10 and Cs12 and their analogs can be prepared in a variety of ways in larger quantities. The analogs A10 and A12 listed below correspond in their properties with respect to the inhibition with respect to Cyp18 or calcineurin to the substances Cs10 and Cs12 and may be as follows: wherein
R 1 is methyl (4R) -4 - [(E) -2-butenyl) -4-methyl-L-threonine (MeBMT) or dihydro-McBMT;
R 2 is α-aminobutyric acid (Abu) or a derivative of this amino acid fluorinated at one or more positions on the side chain; such as wherein X 1 to X 5 independently represent H or F, with the proviso that at least one of X 1 , X 2 , X 3 , X 4 and X 5 is F;
R 3 is N-methyl-glycine (Sar), N-methyl-D-alanine or a fluorinated derivative thereof;
R 4 , R 6 , R 9 and R 10 independently represent N-methyl-L-leucine (MeLeu) or a fluorinated derivative thereof;
R 5 is L-valine (Val) or a fluorinated derivative thereof; R 7 is L-Ala or a fluorinated derivative thereof, and
R 11 is L-MeVal or a fluorinated derivative thereof.
Eine
weitere Ausführungsform
sind Cyclosporin-Analoga der Formel (I), worin R1 für McBmt
oder Dihydro-MeBmt steht;
R2 für Abu steht;
R3 für
Sar oder D-MeAla steht;
R4, R6, R9 und R10 unabhängig
voneinander für
McLeu oder ein fluoriertes Analog stehen können;
R5 für Val oder
ein fluoriertes Analog steht;
R7 für Ala steht;
und
R11 für McVal oder ein fluoriertes
Analog steht.Another embodiment is cyclosporin analogs of formula (I) wherein R 1 is McBmt or dihydro-MeBmt;
R 2 is Abu;
R 3 is Sar or D-MeAla;
R 4 , R 6 , R 9 and R 10 may independently represent McLeu or a fluorinated analog;
R 5 is Val or a fluorinated analog;
R 7 is Ala; and
R 11 represents McVal or a fluorinated analog.
Eine
weitere Ausführungsform
sind Cyclosporin-Analoga der Formel (I), wobei R1 für McBmt
steht;
R2 für Abu steht;
R3 für
Sar steht;
R4, R6,
R9 and R10 für McLeu
stehen;
R5 für Val steht;
R1 für
Ala steht; und
R11 für McVal
steht.Another embodiment is cyclosporin analogs of formula (I) wherein R 1 is McBmt;
R 2 is Abu;
R 3 is sar;
R 4 , R 6 , R 9 and R 10 represent McLeu;
R 5 is Val;
R 1 is Ala; and
R 11 stands for McVal.
In allen oben ausgeführten Verbindungen steht R8 für
- (a)wobei X für O oder S steht, Y für H oder Methyl steht, m einen Wert zwischen 0 und 5 hat, n eine ganze Zahl zwischen 3 und 10 ist, Z für N-R12R13 oder NHC(O)OR14 steht, wobei R12 für H, Methyl, Ethyl, n-Propyl, iso-Propyl oder eine photolysierbare Gruppe steht und R13 für H oder einen C1-C8-Alkylrest steht, und R14 für eine säure-/basenlabile oder eine enzymatisch spaltbare Gruppe steht; oder
- (b)wobei X für O, S oder CH2 steht, Y für H oder Methyl steht, m einen Wert zwischen 0 und 5 hat, n eine ganze Zahl zwischen 3 und 10 ist, Z für N-R12R13 oder NHC(O)OR14 steht, wobei R12 für H, Methyl, Ethyl, n-Propyl, iso-Propyl oder eine photolysierbare Gruppe steht, und R13 für H oder einen C1-C8-Alkylrest steht, und R14 für eine säure-/basenlabile oder eine enzymatisch spaltbare Gruppe steht.
- (A) wherein X is O or S, Y is H or methyl, m has a value between 0 and 5, n is an integer between 3 and 10, Z is NR 12 R 13 or NHC (O) OR 14 , where R 12 is H, methyl, ethyl, n-propyl, iso-propyl or a photolysable group and R 13 is H or a C 1 -C 8 -alkyl radical, and R 14 is an acid / base labile or an enzymatically cleavable group ; or
- (B) where X is O, S or CH 2 , Y is H or methyl, m has a value between 0 and 5, n is an integer between 3 and 10, Z is NR 12 R 13 or NHC (O) OR 14 wherein R 12 is H, methyl, ethyl, n-propyl, iso-propyl or a photolysable group, and R 13 is H or a C 1 -C 8 alkyl radical, and R 14 is an acid / base labile or a enzymatically cleavable group.
Die photolysierbare Gruppe kann eine gegebenenfalls substituierte Nitroarylgruppe sein. Beispiele für die gegebenenfalls substituierte Nitroarylgruppe sind 2-Nitroveratryloxycarbonyl (NVOC), α-Carboxy-2-Nitrobenzyl (CNB), 1-(2-Nitrophenyl)ethyl (NPE), 1-(4,5-Dimethoxy-2-Nitrophenyl)ethyl (DMNPE) oder 5-Carboxymethoxy-2-Nitrobenzyl (CMNB). Die säure-/basenlabile oder enzymatisch spaltbare Gruppe kann z.B. Methyl, Ethyl, Methoxymethyl (MOM), -CH2CH2F, Methylthiomethyl (MTM), β-Glucuronid, D-Glucopyranosyl, β-D-Galactopyranosyl, tetra-O-Acetyl-D-Glucopyranosyl, oder tetra-O-Acetyl-β-D-Galactopyranosyl sein.The photolysable group may be an optionally substituted nitroaryl group. Examples of the optionally substituted nitroaryl group are 2-nitroveratryloxycarbonyl (NVOC), α-carboxy-2-nitrobenzyl (CNB), 1- (2-nitrophenyl) ethyl (NPE), 1- (4,5-dimethoxy-2-nitrophenyl) ethyl (DMNPE) or 5-carboxymethoxy-2-nitrobenzyl (CMNB). The acid / base labile or enzymatically cleavable group can be, for example, methyl, ethyl, methoxymethyl (MOM), -CH 2 CH 2 F, methylthiomethyl (MTM), β-glucuronide, D-glucopyranosyl, β-D-galactopyranosyl, tetra-O- Acetyl-D-glucopyranosyl, or tetra-O-acetyl-β-D-galactopyranosyl.
Bevorzugte Beispiele erfindungsgemäßer Verbindungen sind das [O-(NVOCNH(CH2)5NHC(O) CH2-)D-Ser]8 CsA oder das [O-(NH2(CH2)5NHC(O)CH2-) D-Ser]8 CsA.Preferred examples of compounds according to the invention are the [O- (NVOCNH (CH 2 ) 5 NHC (O) CH 2 -) D-Ser] 8 CsA or the [O- (NH 2 (CH 2 ) 5 NHC (O) CH 2 - ) D-Ser] 8 CsA.
Die erfindungsgemäße Verbindungen vom Typ A12 können nach üblichen Verfahren unter Verwendung von [D-Ser]8- oder [D-Cys]8-CsA (wobei D-Ser oder D-Cys auch durch andere geeignete Aminosäuren ersetzt werden können), CPG-Bromacetat und einer Verbindung der Formel NH2(CH2)nNH-APG hergestellt werden, wobei n eine ganze Zahl zwischen 3 und 10 ist, APG eine Aminoschutzgruppe und CPG eine Carboxylschutzgruppe bedeutet.The A12 compounds of the invention may be prepared by conventional methods using [D-Ser] 8 or [D-Cys] 8 -CsA (where D-Ser or D-Cys may also be replaced by other suitable amino acids), CPG- Bromoacetate and a compound of the formula NH 2 (CH 2 ) n NH-APG, where n is an integer between 3 and 10, APG is an amino-protecting group and CPG is a carboxyl-protecting group.
Die erfindungsgemäßen Verbindungen vom Typ A10 können gleichermaßen nach üblichen Verfahren unter Verwendung von [D-Ser]8- oder [D-Cys]8-CsA (wobei D-Ser oder D-Cys auch durch andere geeignete Aminosäuren ersetzt werden können), CPG-Bromacetat und einer Verbindung ausgewählt aus der Gruppe umfassend NVOC, CNB, NPE, DMNPE und CMNB hergestellt werden, wobei n eine ganze Zahl zwischen 3 und 10 ist, APG eine Aminoschutzgruppe und CPG eine Carboxylschutzgruppe bedeutet.Likewise, the A10 type compounds of the present invention can be replaced by conventional methods using [D-Ser] 8 or [D-Cys] 8 CsA (where D-Ser or D-Cys may also be replaced by other suitable amino acids) CPG Bromoacetate and a compound selected from the group comprising NVOC, CNB, NPE, DMNPE and CMNB, where n is an integer between 3 and 10, APG is an amino-protecting group and CPG is a carboxyl-protecting group.
Als Amino- bzw. Carboxylschutzgruppen können übliche Schutzgruppen verwendet werden, wie sie dem Fachmann z.B. aus N. Sewald, H.-D. Jakubke, Peptides: Chemistry and Biology, Verlag Wiley-VCH bekannt sind. Beispiele für Aminoschutzgruppen sind Carbobenzoxy, Boc, Fmoc, Bpoc, NPS, Triphenylmethyl oder Tosyl. Beispiele für Carboxyschutzgruppen sind Methyl, Ethyl, tert. Butyl, Benzyl, Nitrobenzyl oder Methoxybenzyl. Bevorzugt sind tert. Butyl als Carboxyschutzgruppe und Boc als Aminoschutzgruppe.When Amino or carboxyl protecting groups can be used as customary protecting groups as they are known to those skilled in the art, e.g. from N. Sewald, H.-D. Jakubke, Peptides: Chemistry and Biology, published by Wiley-VCH. Examples of amino protecting groups are carbobenzoxy, Boc, Fmoc, Bpoc, NPS, triphenylmethyl or tosyl. examples for Carboxy protecting groups are methyl, ethyl, tert. Butyl, benzyl, nitrobenzyl or methoxybenzyl. Preference is given to tert. Butyl as carboxy-protecting group and Boc as amino protecting group.
Beispiele für die Herstellung der erfindungsgemäßen Verbindungen sind in den Beispielen 7, 8 und 9 angegeben.Examples for the Preparation of the compounds of the invention are given in Examples 7, 8 and 9.
Spezifitätsänderungspecificity change
Die geeignete Methode zur Änderung der Spezifität einer Substanz des Typs A10 zu einer Substanz des Typs A12, wird durch die aktivierbare Gruppierung bestimmt. Solche aktivierbaren Gruppierungen und ihre geeigneten Aktivierungsmethoden sind dem Fachmann bekannt und wurden mehrfach ausführlich beschrieben. Je nach beabsichtigter Methode lassen sich durch Beeinflussung dieser chemischen Funktionalitäten aus einer Muttersubstanz gezielt eine oder mehrere Tochtersubstanzen herstellen, wobei die Tochtersubstanz erfindungsgemäß eine gegenüber der Proteinphosphatase Calzineurin geänderte Spezifität aufweist.
- a) Photoschaltung: Durch Licht schaltbare chemische Gruppierungen sind seit längerem bekannt und Gegenstand zahlreicher Patentschriften so z.B. in US6392089, US6242258, US6160024, US5952311, US5767288, US6057096, US5786198, US5780287, EP1208079 oder US5503721 bzw. sind in Übersichtsarbeiten, wie z.B.: Pirrung, M.C. et al. J.Org.Chem 60 (1995) 1116; Gurney A.M. et al. Physiological Reviews 67 (1987) 583; Pillai V.N.R. Reviewspp 1–27 (1980); Cameron J.F. et al. J.Chem.Soc. Chem. Commun 923 (1995); Pirrung M.C. et al. J.Org.Chem 59 (1994) 3890; McCray J.A. et al. Annu.Rev.Biophys.Chem. 18 (1989) 239; Cummings R.T. et al. Tetrahedron Letters 29 (1988) 65; Mendel D. et al. J.Am. Chem. Soc. 113 (1991) 2578 oder Sheehan J.C. et al. J. Am. Chem. Soc 93 (1971) 7222 beispielgebend dargestellt. Ebenso wurden zahlreiche Verfahren dokumentiert, mit deren Hilfe die gewünschte Aktivierung durchgeführt werden kann, so z.B. in US6461567, US6524447, US6397102, US6433343, US5459322, US6258319, US5854967, US5683661 oder US5503721. So wird zum Beispiel zur Umwandlung von Substanz Cs10 in Substanz Cs12 vorzugsweise UV-Licht mit einer Wellenlänge von etwa 330 nm benutzt. Wahl der Lichtquelle und Dauer der Bestrahlung der Substanz um die gewünschte Umwandlung von A10 nach A12 zu erreichen, hängen naturgemäß neben der verwendeten photolabilen Gruppe und Stärke der Lichtquelle von weiteren Faktoren ab. Befindet sich A10 z.B. in Körperflüssigkeiten, wie z.B. Blut, werden Teile der Lichtenergie auch von absorbierenden Blutbestandteilen absorbiert werden. Beim Bestrahlen von Hautbereichen, sind wiederum andere störende Effekte, wie z.B. durch unterschiedliche Pigmentierung zu erwarten. Eine optimale Aktivierung ist aber leicht an der Bildungsgeschwindigkeit von A12 zu erkennen wie dies in Beispiel 3 dargestellt ist.
- b) Enzymatische Schaltung: Die gezielte Einführung von Substratanaloga in eine als Elternsubstanz bezeichnete Verbindung, aus der dann durch Wirkung unterschiedlicher Enzyme eine gewünschte Tochtersubstanz entsteht, ist dem Fachmann bekannt und in der Literatur umfassend dokumentiert (z.B.: Gum A.W. et al. Chem.Eur.J. 6 (2000) 3714; deBont D.B.A. et al. BioorganicMedicinal Chemistry 5 (1997) 405; Lazarova T. et al J.Med.Chem. 46 (2003) 674). So kann z.B. durch Einführung einer Estergruppierung die Aktivität von Hydrolasen/Esterasen, durch Einführung einer geeigneten sensitiven Peptidbindung die Aktivität von Proteasen oder bei Verwendung von Glucose- oder Galactosederivaten die Aktivität von Glycosidasen genutzt werden, um A10 in A12 zu verwandeln. Beispiel 5 zeigt die gezielte Hydrolyse einer solchen Muttersubstanz A10 am Beispiel einer Estergruppierung.
- c) pH-Schaltung: Die gezielte Einführung von Substratanaloga in eine als Elternsubstanz bezeichnete Verbindung, aus der dann durch Säure- oder Basenkatalyse eine gewünschte Tochtersubstanz entsteht, ist dem Fachmann bekannt und in der Literatur umfassend dokumentiert, wie z.B. in „Catalysis in Chemistry and Enzymology" von William P. Jencks. (1987). Geeignet für diese nichtenzymatische Katalyse sind chemische Bindungen, welche gegenüber Säuren – oder Basen, im einfachsten Fall gegenüber Protonen oder Hydroxylionen, empfindlich sind. Charakteristisches Kennzeichen solcher chemischer Bindungen ist, daß die Hydrolysegeschwindigkeit in einem direkten Zusammenhang zur Konzentration der katalytisch wirksamen Ionen steht. Beispiel 6 zeigt die Umwandlung eines Substanzanalogen der Verbindung A10 in die Verbindung A12 mittels erhöhter Hydroxylionenkonzentration.
- a) Photo Switching: Light-switchable chemical groupings have been known for some time and are the subject of numerous patents such as in US6392089, US6242258, US6160024, US5952311, US5767288, US6057096, US5786198, US5780287, EP1208079 or US5503721 or are in reviews, such as: Pirrung, MC et al. J. Org. Chem 60 (1995) 1116; Gurney AM et al. Physiological Reviews 67 (1987) 583; Pillai VNR Review 1-27 (1980); Cameron JF et al. J. Chem. Chem. Commun 923 (1995); Pirrung MC et al. J. Org. Chem 59 (1994) 3890; McCray JA et al. Annu.Rev.Biophys.Chem. 18 (1989) 239; Cummings RT et al. Tetrahedron Letters 29 (1988) 65; Mendel D. et al. J. Am Chem. Soc. 113 (1991) 2578 or Sheehan JC et al. J. Am. Chem. Soc. 93 (1971) 7222 by way of example. Numerous methods have also been documented by means of which the desired activation can be carried out, for example in US6461567, US6524447, US6397102, US6433343, US5459322, US6258319, US5854967, US5683661 or US5503721. For example, for the conversion of Substance Cs10 in Substance Cs12, UV light having a wavelength of approximately 330 nm is preferably used. Choice of the light source and duration of irradiation of the substance in order to achieve the desired conversion of A10 to A12, of course, depending on the photolabile group used and strength of the light source depend on other factors. For example, if A10 is in body fluids such as blood, some of the light energy will also be absorbed by absorbing blood components. When irradiating skin areas, in turn, other disturbing effects, such as expected by different pigmentation. However, optimal activation is easily recognized by the rate of formation of A12 as shown in Example 3.
- b) Enzymatic Circuit: The targeted introduction of substrate analogues into a compound designated as the parent substance, from which a desired daughter substance is then produced by the action of different enzymes, is known to the person skilled in the art and comprehensively documented in the literature (for example: Gum AW et al., Chem J. 6 (2000) 3714; deBont DBA et al., Bioorganic Medicine Chemistry 5 (1997) 405; Lazarova T. et al J. Med. Chem. 46 (2003) 674). Thus, for example, by introducing an ester grouping, the activity of hydrolases / esterases, the introduction of a suitable sensitive peptide bond, the activity of proteases or, if glucose or galactose derivatives are used, the activity of glycosidases can be used to convert A10 into A12. Example 5 shows the specific hydrolysis of such a parent substance A10 using the example of an ester grouping.
- c) pH-switching: The targeted introduction of substrate analogues into a compound designated as the parent substance, from which a desired daughter substance is then formed by acid or base catalysis, is known to the person skilled in the art and comprehensively documented in the literature, as described, for example, in "Catalysis in Chemistry and Enzymology "by William P. Jencks (1987). Suitable for this nonenzymatic catalysis are chemical bonds which are sensitive to acids or bases, in the simplest case to protons or hydroxyl ions is a direct relationship to the concentration of the catalytically active ions Example 6 shows the conversion of a substance analog of the compound A10 into the compound A12 by means of increased hydroxyl ion concentration.
Ort der Aktivierung:Place of activation:
Neben der Anwendung für wissenschaftliche Zwecke, wo die Aktivierung und Wandlung der Substanz A10 zu A12 bei gleichzeitiger Änderung der Spezifität in einer Küvette erfolgt, ist ein Hauptgebiet der Anwendung für medizinische Zwecke zu sehen. Hier kann es von Vorteil sein, die Substanz A10 äußerlich, nasal, oral, intrakranial, parenteral, mittels Tropf, Katheter oder ähnlicher Hilfsmittel zu verabreichen, um anschließend mittels gezielter Aktivierung die immunsuppressive Eigenschaft durch Wandlung der Verbindung A10 in A12 lokal im gewünschten Gewebe/Blutzellen aufzuheben. Die Bestrahlung kann dabei großflächig über die Haut, wie z.B. zur Behandlung von erhöhtem Bilirubin üblich (US3877437, US6464715, US6045575) oder mittels Katheter, wie z.B. in US5503721 oder US6176842 beschrieben, lokal durchgeführt werden. Es kann aber auch von Vorteil sein, zeitweise extrakorporal befindliche Körperflüssigkeiten, Zellmaterial oder ganze Organe so einer Aktivierung zu unterziehen, daß nur die sich in diesen Körperflüssigkeiten, Zellen oder Organen befindlichen Substanzanteile der Substanz A10 in A12 überführt werden. Methoden um zeitweise extrakorporale Flüssigkeiten zu erhalten sind dem klinischen Mediziner bekannt. So kann z.B. mittels Plasmapherese (z.B.: US6099734) weitgehend zellfreie Körperflüssigkeit erhalten werden. Oder es kann mittels der weit angewendeten Dialysetechniken (z.B.: US5277820) Blut extrakorporal kontinuierlich zugänglich gemacht werden. Beiden Methoden ist gemeinsam, daß kontinuierlich Körperflüssigkeit extrakorporal verbracht wird, hier einer Aktivierung zugänglich ist und anschließend dem natürlichen Körperflüssigkeitslauf wieder zugeführt wird. Es kann aber auch ein diskontinuierliches Vorgehen von Vorteil sein. So können Körperflüssigkeiten, Organe, Gewebe oder Zellen wie z.B. Knochenmark, entnommen werden um diese oder nur Bestandteile dieser Körperflüssigkeiten, Organe, Gewebe oder Zellen einer Aktivierung zugänglich zu machen, um die immunsuppressiven Eigenschaften von Cs10 durch Überführen in Cs12 zu eliminieren. Anschließend können diese Körperflüssigkeiten, Organe, Gewebe oder Zellen bzw. Bestandteile dieser Körperflüssigkeiten, Organe, Gewebe oder Zellen wieder mittels dem Fachmann bekannter Techniken entweder der Person, aus dem das Material entnommen wurde oder, wenn dies von Vorteil ist, einer anderen Person so verabreicht werden, daß die durch Überführen von A10 in A12 erhaltenen Vorteile einen therapeutischen Nutzen für die Empfängerperson hat.In addition to the application for scientific purposes, where the activation and conversion of the substance A10 to A12 occurs while changing the specificity in a cuvette, a main area of application for medical purposes is to be seen. Here it may be advantageous to administer the substance A10 externally, nasally, orally, intracranially, parenterally, by means of a drip, catheter or similar aids, in order subsequently to locally activate the immunosuppressive property by converting the compound A10 into A12 in the desired tissue. To pick up blood cells. Irradiation can be carried out over the skin over a large area, as is customary, for example, for the treatment of elevated bilirubin (US Pat. No. 3,877,437, US Pat. No. 6,664,715, US Pat. No. 6,045,575) or by means of catheters, as described, for example, in US Pat. No. 5,503,721 or US Pat. However, it may also be advantageous to temporarily subject extracorporeal body fluids, cell material or entire organs to such an activation that only the substance constituents of the substance A10 present in these body fluids, cells or organs are converted into A12. Methods to temporarily extracorporeal liquid The clinical physician is well-known. Thus, for example, by means of plasmapheresis (eg US6099734) largely cell-free body fluid can be obtained. Or it can be made continuously available extracorporeally by means of the widely used dialysis techniques (eg: US5277820). Both methods have in common that body fluid is spent extracorporeally, here an activation is accessible and then fed back to the natural body fluid flow. But it can also be a discontinuous procedure of advantage. Thus, body fluids, organs, tissues or cells, such as bone marrow, can be harvested to make them or only components of these body fluids, organs, tissues or cells accessible for activation to eliminate the immunosuppressive properties of Cs10 by conversion into Cs12. Subsequently, these body fluids, organs, tissues or cells or components of these body fluids, organs, tissues or cells can be re-administered to another person using techniques known to those skilled in the art either from the person from whom the material was taken or, if beneficial that the benefits obtained by converting A10 to A12 will have a therapeutic benefit to the recipient.
Verabreichung der SubstanzenAdministration of the substances
Substanzen, die unter A10 bzw. A12 zusammengefaßt sind, können entweder jeweils als Einzelsubstanz oder als Gemisch in therapeutischen Anwendungen enthalten sein und sollen weiterhin als wirksames Agens bezeichnet werden. Dabei kann es von Vorteil sein, A12 aus A10 während der Therapie durch Substanzaktivierung herzustellen. In Fällen, wo der immunsuppressive Effekt von Verbindungen des Typs A10 gänzlich unerwünscht ist, kann es auch von Vorteil sein, auf die Substanzaktivierung zu verzichten und Verbindungen des Typs A12 therapeutisch zu verabreichen. Die Verabreichungen selbst können oral, topisch oder parenteral in Formulierungen erfolgen. Die Formulierungen können zusätzlich konventionelle nichttoxische pharmazeutisch akzeptable Trägerstoffe, Adjuvanten und Lösungsmittel enthalten. Unter dem Begriff parenteral werden subkutane, intravenöse, intramuskulare, intrakranale oder intrasternale Injektionen oder Infusionstechniken verstanden.substances which are summarized under A10 and A12, either each as a single substance or as a mixture in therapeutic applications and should continue to be called an effective agent. It can It may be beneficial to use A12 from A10 during drug activation therapy manufacture. In cases, where the immunosuppressive effect of A10 compounds is entirely undesirable, it may also be beneficial to forego the substance activation and to administer therapeutically A12 compounds. The Administerments can self be made orally, topically or parenterally in formulations. The formulations can additionally conventional non-toxic pharmaceutically acceptable carriers, Adjuvants and solvents contain. Under the term parenteral subcutaneous, intravenous, intramuscular, intracranial or intrasternal injections or infusion techniques Understood.
Die pharmazeutischen Zusammensetzungen können den oder die aktiven Wirkstoffe oder gegebenenfalls mit A10 deren Vorstufe in einer für die orale Anwendung geeigneten Form enthalten, z.B. als Aerosol, Tabletten, Pastillen, Bonbons, wäßrige oder ölige Suspensionen, Puder oder Körner, Emulsionen, harte oder weiche Kapseln, in Sirup oder Elixieren.The Pharmaceutical compositions may contain the active ingredient (s) or optionally with A10 their precursor in one for the oral Use suitable form, e.g. as aerosol, tablets, Pastilles, candies, aqueous or oily suspensions, Powder or grains, Emulsions, hard or soft capsules, in syrup or elixirs.
Aerosole, wobei unter Aerosol eine Dispersion fester oder flüssiger Teilchen in Gasen verstanden wird, lassen sich mittels vielfältiger, dem Fachmann bekannter Methoden herstellen, wobei insbesondere durch Bereitstellung von vom Patienten zu bedienender Gefäße, welche das Therapeutikum und gegebenenfalls weitere Stoffe enthalten können, das therapeutisch anwendbare Aerosol unmittelbar vor der Anwendung erst erzeugt wird. Technische Lösungen, insbesondere zur Herstellung von Aerosolen, die auf Grund ihrer physikalischen Beschaffenheit einer wirksamen Tröpfchengröße gut durch die Lunge aufgenommen werden können sind in großem Umfang beschrieben worden und anwendbar, so z.B.: US06136295, US05985309, US06447753, US06447752, US06436443, US06399102, US06338809, USRE037053, US05855913. Anwendbare Aerosole für die therapeutische Anwendung von Cyclosporinen sind ebenfalls mehrfach der Gegenstand von Patentschriften (wie z.B.: US06241969, US05958378, US06413547, US05693336, US05683714).aerosols, wherein aerosol is a dispersion of solid or liquid particles in gases, can be manufacture methods known in the art, in particular by Provision of patient-to-use vessels, which may contain the therapeutic and optionally other substances that Therapeutically applicable aerosol immediately before use is produced. Technical solutions, in particular for the production of aerosols, due to their physical condition of an effective droplet size well absorbed by the lungs can be are in big Scope has been described and applicable, such as: US06136295, US05985309, US06447753, US06447752, US06436443, US06399102, US06338809, USRE037053, US05855913. Applicable aerosols for the therapeutic use of cyclosporins are also multiple the subject matter of patents (such as: US06241969, US05958378, US Pat. US06413547, US05693336, US05683714).
Zusammensetzungen, die für den oralen Gebrauch bestimmt sind, lassen sich mittels dem Fachmann bekannter Methoden herstellen. Solche Zusammensetzungen können weitere Stoffe enthalten, welche eine pharmazeutisch elegante Herstellung ermöglichen und weiterhin für eine positive Akzeptanz beim Patienten bewirken, wie z.B. eine oder mehrere Substanzen, die aus der Gruppe der Süßmacher, der Aromastoffe oder der Farbstoffe ausgewählt werden können.compositions the for are intended for oral use, can be known by those skilled in the art Establish methods. Such compositions may contain other substances, which enable a pharmaceutically elegant production and continue for cause positive acceptance in the patient, e.g. one or several substances selected from the group of sweeteners, flavorings or the Dyes selected can be.
Tabletten, welche das aktive Agens als Beimischung mit nicht-toxischen pharmazeutisch akzeptablen Substanzen enthalten, lassen sich mittels dem Fachmann bekannter Methoden herstellen. Als Arzneiträger oder als für die Tablettenherstellung wichtige Mittel können verschiedene Stoffen genutzt werden. So kann als (a) inerter Stoff z.B. Kalziumkarbonat, Laktose, Kalziumphosphat oder Natriumphosphat; als (b) granulierender Stoff z.B. Stärke oder Alginsäure; als (c) Stützstoff z.B. Gelatine, Stärke oder Gummiarabicum, und als (d) Dispersionsmittel z.B. Magnesiumstearat, Stearinsäure oder Talkum verwendet werden. Die Tabletten selbst können ungeschützt oder mit einer äußeren Schutzhülle versehen sein, um die Verweilzeit im Verdauungstrakt zu verzögern und damit eine zeitlich längere Wirkung zu erreichen. Materialien, die Einfluß auf die Verweilzeit nehmen, sind z.B. Glycerolmonostearat oder Glyceroldistearat. Mittels bekannter Techniken (z.B.: US4256108, US4160452, US4265874) lassen sich auch Tabletten herstellen, welche das aktive Agens zeitlich kontrolliert oder bezogen auf den Verdauungstrakt in definierten Bereichen aus der Tablette freisetzen.tablets, which the active agent as an admixture with non-toxic pharmaceutical contain acceptable substances, can be determined by a person skilled in the art produce known methods. As excipients or as for the production of tablets important resources can different substances are used. Thus, as (a) inert substance e.g. Calcium carbonate, lactose, calcium phosphate or sodium phosphate; as (b) granulating agent e.g. Starch or alginic acid; when (c) proppant e.g. Gelatin, starch or gum arabic, and as (d) dispersing agent e.g. magnesium stearate, stearic acid or talc. The tablets themselves may be unprotected or provided with an outer protective cover be to delay the residence time in the digestive tract and thus a longer time To achieve effect. Materials that influence the residence time, are e.g. Glycerol monostearate or glyceryl distearate. By means of known Techniques (e.g. US4256108, US4160452, US4265874) can also be used Make tablets that temporally control the active agent or based on the digestive tract in defined areas release the tablet.
In einigen Fällen kann es von Vorteil sein, Formulierungen für den oralen Gebrauch in der Form von Gelatinekapseln, in denen das aktive Agens mit einer oder mehreren weiteren inerten Substanzen gemischt ist, bereitzustellen. Solche Substanzen können z.B. Kalziumkarbonat, Kalziumphosphat oder Kaolin sein. Die Gelatinekapseln können aber auch neben dem aktiven Agens Wasser oder Öle, wie z.B. Nußöl, Olivenöl oder auch Paraffinöl enthalten.In some cases It may be beneficial to use formulations for oral use in the Form of gelatin capsules in which the active agent with one or more several other inert substances mixed. Such substances can e.g. Calcium carbonate, calcium phosphate or kaolin. The gelatine capsules can but also, in addition to the active agent, water or oils, e.g. Nut oil, olive oil or too paraffin oil contain.
Wäßrige Suspensionen enthalten das aktive Agens üblicherweise in Mischungen mit Beimengungen, welche erforderlich für ihre Herstellung sind, wie z.B. (a) Suspensions vermittelnde Stoffe wie Natriumcarboxymethylcellulose, Methylcellulose, Hydroxypropylmethylcellulose, Natriumalgenat, Polyvinylpyrrolidon, Tragantgummi und Gummiarabikum; (b) Dispergierende oder die Benetzung vermittelnde Stoffe, wie natürlich vorkommende Phosphatide wie z.B. Lecithin; (c) Kondensationsprodukte eines Alkylenoxids mit einer Fettsäure, wie z.B. Polyoxyethylenstearat; (d) Kondensationsprodukte eines Ethylenoxids mit einem langkettigen aliphatischen Alkohol, wie z.B. Heptadekaethyleneoxycetanol; (e) Kondensationsprodukte eines Ethylenoxids mit einem Partialester, der von einer Fettsäure und einem Hexitol, wie z.B. Polyoxyethylensorbitolmonooleat, oder (f) Kondensationsprodukte eines Ethylenoxids mit einem Partialester, welcher von einer Fettsäure und einem Hexitolanhydrid, wie z.B. Polyoxyethylensorbitnamonooleat gebildet wird.Aqueous suspensions usually contain the active agent in mixtures with admixtures, which are necessary for their preparation are such as (a) suspending agents such as sodium carboxymethyl cellulose, Methylcellulose, hydroxypropylmethylcellulose, sodium algenate, polyvinylpyrrolidone, gum tragacanth and gum arabic; (b) dispersing or wetting agent Fabrics, like natural occurring phosphatides such as e.g. lecithin; (c) condensation products an alkylene oxide with a fatty acid, e.g. polyoxyethylene; (d) condensation products of an ethylene oxide with a long chain aliphatic alcohol, e.g. Heptadekaethyleneoxycetanol; (E) Condensation products of an ethylene oxide with a partial ester, that of a fatty acid and a hexitol, e.g. Polyoxyethylene sorbitol monooleate, or (f) Condensation products of an ethylene oxide with a partial ester, which of a fatty acid and a hexitol anhydride, e.g. Polyoxyethylensorbitnamonooleat is formed.
Die wäßrigen Suspensionen können auch einen oder mehrere Konservierungsstoffe, wie z.B. Ethyl- oder N-Propyl-p-hydroxybenzoat; einen oder mehrere Farbstoffe, einen oder mehrere Aromastoffe und einen oder mehrere Geschmacksstoffe wie z.B. Saccharose oder Saccharin enthalten.The aqueous suspensions can also one or more preservatives, e.g. Ethyl or N-propyl-p-hydroxybenzoate; one or more dyes, one or more flavorings and one or more flavorings such as. Contain sucrose or saccharin.
Ölige Suspensionen können durch Versetzen des aktiven Agens in ein pflanzliches Öl oder Mischungen dieser Öle, wie z.B. Arachisöl, Olivenöl, Sesamöl, Nußöl oder aber in ein mineralisches Öl, wie z.B. flüssiges Paraffin, erhalten werden. Die ölige Suspension kann ein Verdickungsmittel, wie z.B. Bienenwachs, Paraffin oder Cetylalkohol enthalten. Zusätzlich können Süßmittel, Aromastoffe oder Farbstoffe zugesetzt sein, um eine gute Akzeptanz beim Patienten zu erreichen. Zur Verlängerung der Haltbarkeit der Zusammensetzung können Antioxidantien wie z.B. Ascorbinsäure zugesetzt sein. Ebenso kann der Zusatz dispergierender Puder unterschiedlicher Korngröße zur Herstellung der wäßrigen Lösung vorteilhaft sein. Diese Zusätze ermöglichen eine relativ homogene und stabile Mischung zusammen mit allen anderen oben erwähnten vorteilhaften Zusätzen.Oily suspensions can by putting the active agent in a vegetable oil or mixtures these oils, such as. arachis, Olive oil, Sesame oil, Nut oil or else in a mineral oil, such as. liquid Paraffin, to be obtained. The oily Suspension may be a thickening agent, such as e.g. Beeswax, paraffin or cetyl alcohol. additionally can Sweetener, Flavorings or dyes may be added to a good acceptance reach the patient. To extend the shelf life of Composition can Antioxidants such as e.g. Ascorbic acid added. As well can the addition of dispersing powders of different particle size for the production the aqueous solution advantageous be. These accessories allow one relatively homogeneous and stable mixture together with all others mentioned above advantageous additives.
Die pharmazeutische Zusammensetzung kann auch in Form einer Öl-in-Wasser-Emulsion vorliegen. Dabei kann die ölige Phase ein pflanzliches Öl, wie z.B. Olivenöl oder Arachisöl, oder aber ein mineralisches Öl, wie z.B. flüssiges Paraffin oder eine Mixtur dieser Öle enthalten. Emulsionsvermittler- oder Stabilisierungszusätze können dabei sein: (1) natürlich vorkommende Gummi, wie z.B. Gummi Arabicum oder Tragantgummi, (2) natürlich vorkommende Phosphatide, wie z.B. aus der Sojabohne oder Lecithin, (3) Ester oder Partialester, die von Fettsäuren und Hexitolanhydriden abgeleitet wurden, wie z.B. Sorbitolmonooleat, (4) Kondensationsprodukte der oben erwähnten Partialester mit Ethylenoxid, z.B. Polyoxyethylensorbitol-monooleat. Die Emulsionen selbst können wiederum Zusätze, wie Süßmittel, Aromastoffe oder Farbstoffe enthalten.The Pharmaceutical composition may also be in the form of an oil-in-water emulsion. there can the oily Phase a vegetable oil, such as. olive oil or arachis oil, or a mineral oil, such as. liquid Paraffin or a mixture of these oils contain. Emulsionsvermittler- or stabilizing additives can to be there: (1) of course occurring gums, e.g. Gum arabic or gum tragacanth, (2) Naturally occurring phosphatides, e.g. from soybean or lecithin, (3) esters or partial esters derived from fatty acids and hexitol anhydrides have been derived, such as Sorbitol monooleate, (4) condensation products the above mentioned Partial ester with ethylene oxide, e.g. Polyoxyethylene monooleate. The emulsions themselves can again additives, like sweeteners, Flavorings or dyes included.
Sirupe und Elixiere können mit Süßmitteln, wie z.B. Glyzerin, Propylenglykol, Sorbitol oder Saccharose versetzt sein. Diese Formulierungen können zusätzlich weitere Stoffe, wie ein Demulgator, ein Emulgator, ein Konservierungsmittel, ein Aromastoff ein Farbstoff oder auch mehrere dieser Zusätze enthalten.syrups and elixirs can with sweeteners, such as. Glycerol, propylene glycol, sorbitol or sucrose be. These formulations can additionally other substances, such as a demulsifier, an emulsifier, a preservative, a flavoring agent containing a dye or more of these additives.
Die pharmazeutischen Zusammensetzung kann sich auch in der Form einer sterilen injizierbaren wäßrigen oder öligen Suspension befinden. Solche Suspensionen lassen sich mittels dem Fachmann bekannten Methoden durch Verwendung dispergierender, emulgierender oder benetzender Zusätze, wie sie oben aufgeführt wurden, herstellen. Die sterile injizierbare Zusammensetzung kann auch in Form einer sterilen injizierbaren Lösung oder Suspension mit einem nicht-toxischen parenteral-verträglichen Lösungsmittel oder Verdünnungsmittel, wie z.B. 1,3-Butandiol bestehen. Zu den akzeptablen Zusatzstoffen zählen auch insbesondere Wasser, Ringerlösung und isotonische Natriumchloridlösung. Auch sterile nichtflüchtige pharmazeutisch allgemein verwendete Öle können als Lösungsmittel oder Suspensionszusatz verwendet werden, einschließlich synthetischer Mono- oder Diglyzeride. Zusätzlich können Fettsäuren, wie z.B. Ölsäure in diesen injizierbaren Zubereitungen enthalten sein.The pharmaceutical composition can also take the form of a sterile injectable aqueous or oily suspension are located. Such suspensions can be prepared by methods known to those skilled in the art by using dispersing, emulsifying or wetting Additions, as listed above were, manufacture. The sterile injectable composition can also in the form of a sterile injectable solution or suspension with a non-toxic parenteral-compatible solvent or diluents, such as. 1,3-butanediol consist. The acceptable additives include, in particular, water, Ringer's solution and isotonic sodium chloride solution. Also sterile non-volatile Generally used oils may be used as a solvent or as an additive to the suspension be used, including synthetic Mono or diglycerides. additionally can fatty acids, such as. Oleic acid in these be included in injectable preparations.
Ein aktives Agens der Formel 1 kann auch in einem zur rektalen oder intravaginalen Anwendung üblichen Zäpfchen enthalten sein. Solche für die rektale Anwendung üblichen Suppositorien lassen sich mittels dem Fachmann bekannten Methoden und bei Verwendung bekannter Stoffe und Zusätze herstellen. Dabei wird das aktive Agens mit einem gebräuchlichen, nicht-reizenden Arzneistoffträger, der dadurch gekennzeichnet ist, daß er bei Raumtemperatur fest und bei Körpertemperatur flüssig ist und deshalb im Rektum schmilzt und so das aktive Agens freisetzen kann, gemischt. Gebräuchliche Arzneistoffträger zum Anfertigen von Rektalzäpfchen sind z. B. Kakaobutter und verschiedene Polyäthylenglycole.An active agent of the formula 1 can also be present in a suppository which is customary for rectal or intravaginal use. Such suppositories customary for rectal use can be prepared by methods known to the person skilled in the art and using known substances and additives. In this case, the active agent with a conventional, non-irritating excipient, which is characterized in that it is solid at room temperature and liquid at body temperature and therefore melts in the rectum and so the active agent can release, mixed. Common excipients for making rectal suppository are z. As cocoa butter and various polyethylene glycols.
Für äußerliche Anwendungen, können z.B. Cremes, Salben, Schäume, Lotions oder Suspensionen, die das wirksame Agens enthalten, verwendet werden.For external Applications, can e.g. Creams, ointments, foams, Lotions or suspensions containing the active agent used become.
Die Menge des aktiven Agens, welches mit einem oder mehreren der oben aufgeführten Trägermaterialien zusammengeführt wird, um eine der oben aufgeführten Anwendungsformen herzustellen, kann sehr unterschiedlich sein. Die Menge hängt sowohl von der Anwendungsart als auch vom Anwendungsziel ab. So kann z.B. eine Formulierung zur oralen Aufnahme von 5 mg bis zu 1 g des aktiven Agens enthalten, wobei die oben aufgeführten Zusatzstoffe zwischen 5 und 95% der totalen Menge ausmachen können. Es kann aber auch teilweise erforderlich sein, beträchtlich geringere Mengen des aktiven Agens zu verwenden oder aber Mengen, welche 1 g übersteigen. Vorzugsweise Dosisformen können zwischen 25 und 500 mg des aktiven Agens enthalten. Es liegt aber in der Natur medizinischer Anwendungen, daß spezifische Dosismengen des aktiven Agens sowohl von der Art des Agens selbst abhängen aber auch von den individuellen Eigenschaften des zu behandelnden Patienten, wie z.B. Alter, Körpergewicht, allgemeiner Gesundheitszustand, Geschlecht, Ernährung, Zeitpunkt und Art der Verabreichung, Geschwindigkeit der Ausscheidung, der eventuellen Kombination mit anderen Pharmaka, der Therapieart und der spezifischen Erkrankung.The Amount of active agent associated with one or more of the above listed support materials together is going to be one of the above Making application forms can be very different. The Quantity hangs depending on the type of application as well as the application target. So can e.g. a formulation for oral intake of 5 mg up to 1 g of the containing active agent, wherein the additives listed above between 5 and 95% of the total amount. It can also be partial be necessary, considerable use smaller amounts of the active agent or quantities, which exceed 1 g. Preferably, dosage forms may between 25 and 500 mg of the active agent. It lies however in the nature of medical applications, that specific dose levels of the active Agent depends both on the type of agent itself but also on the individual Properties of the patient to be treated, e.g. Age, body weight, general health, sex, diet, time and nature of Administration, rate of elimination, eventual Combination with other drugs, the type of therapy and the specific Illness.
Die Figuren zeigen:The Figures show:
Die nachfolgenden Beispiele erläutern die vorliegende Erfindung, ohne diese auf die beschriebenen Beispiele einzuschränken.The explain the following examples the present invention, without this to the examples described limit.
Beispiel 1: EnzymaktivitätsassaysExample 1: enzyme activity assays
Zur Klassifizierung der CsA-Derivate wurde die Inhibition der PPlase-Aktivität der kommerziell verfügbaren humanen PPlase Cyp18 (Sigma: C3805) und die Phosphataseaktivität des kommerziell verfügbaren Calzineurins (Sigma: C1907) verwendet.
- a) Der PPlase-aktivitätsassay wurde nach Fischer et al. Biomed. Biochim Acta 43 (1984) 1101 durchgeführt, mit Suc-AFPF-NHNp als Substrat und alpha-Chymotrypsin (Merck, Darmstdt) als Hilfsprotease in 30 mM HEPES-Puffer bei pH 7,8 und 7°C. Nach 10 min Vorinkubation einer gewünschten Konzentration des Inhibitors mit 2.5 nM Cyp18, wurde die Reaktion durch aufeinanderfolgende Zugabe von Substrat und Chymotrypsin gestartet und bei 390 nm mit einem Spektralphotometer (HP 8452) die Absorption gemessen. Die IC50-Werte konnten durch Auftragen der nach einer Geschwindigkeitsgleichung 1. Ordnung berechneten Geschwindigkeitskonstanten gegen die Inhibitorkonzentration berechnet werden.
- b) Die Aktivität
der Proteinphosphatase Calzineurin wurde nach Baumgraß et al.
J.Biol.Chem. 276 (2002) 47914 mittels biotinyliertem RII-Peptid
bestimmt. Dazu wurde das RII-Peptid mit PKA und gamma 33P-ATP phosphoryliert
und nachfolgend mittels einer 1 ml RP-C2 Extraktionssäule (Amchro,
Sulzbach) bis zur chromatografischen Einheitlichkeit (HPLC, 0 zu
100 Azetonitril-Gradient) gereinigt. Das so hergestellte Peptid (PRII)
wurde im „Scintillation
Proximity"-Assay
verwendet. Im einzelnen wurden zusammen mit geeigneten Konzentrationen
an Inhibitor eine Mischung aus Calmodulin (50 nM) und Calzineurin
(1.32 nM) in Assay-Puffer (40 mM Tris/HCl, pH 7.5, 100 mM NaCl,
6 mM MgCl2, 0.5 mM DTT, 1 mM CaCl2, 0.1 mg/ml BSA) für 30 min bei 30°C inkubiert.
Danach wurde PRII bei einer Endkonzentraion von 100 nM bei einem
Endvolumen von 100 μl
für weitere
30 min bei 30°C
inkubiert. Danach wurden 90 μl
abgenommen und in kommerziellen mit Streptavidin belegten Titerplatten
(ScintiStrip) inkubiert. Nach 20 min Inkubation bei 22°C wurden die
Platten gewaschen und das nichtumgesetzte PRII mittels MicroBeta-Counter
(Wallac, Turku, Finnland) bestimmt.
1 zeigt eine typische Abhängigkeit der CaN-Aktivität von der Inhibitorkonzentration.
- a) The PPlase activity assay was performed according to Fischer et al. Biomed. Biochim Acta 43 (1984) 1101, with Suc-AFPF-NHNp as substrate and alpha-chymotrypsin (Merck, Darmstdt) as auxiliary protease in 30 mM HEPES buffer at pH 7.8 and 7 ° C. After preincubation of a desired concentration of the inhibitor with 2.5 nM Cyp18 for 10 min, the reaction was started by successive addition of substrate and chymotrypsin and the absorption was measured at 390 nm using a spectrophotometer (HP 8452). The IC 50 values could be calculated by plotting the rate constants calculated from a first-order rate equation versus the inhibitor concentration.
- b) The activity of the protein phosphatase calcineurin was determined according to Baumgraß et al. J. Biol. 276 (2002) 47914 using biotinylated RII peptide. For this purpose, the RII peptide was phosphorylated with PKA and gamma 33 P-ATP and subsequently purified by means of a 1 ml RP-C2 extraction column (Amchro, Sulzbach) until chromatographic homogeneity (HPLC, 0 to 100 acetonitrile gradient). The peptide thus prepared (PRII) was used in the Scintillation Proximity Assay Specifically, together with appropriate concentrations of inhibitor, a mixture of calmodulin (50 nM) and calcineurin (1.32 nM) in assay buffer (40 mM Tris / HCl , pH 7.5, 100 mM NaCl, 6 mM MgCl 2 , 0.5 mM DTT, 1 mM CaCl 2 , 0.1 mg / ml BSA) for 30 min at 30 ° C. Thereafter, PRII was incubated at a final concentration of 100 nM at a final volume of 100 μl was incubated for a further 30 min at 30 ° C. Thereafter, 90 μl were removed and incubated in commercial streptavidin-coated titer plates (ScintiStrip) .After incubation for 20 min at 22 ° C., the plates were washed and the unreacted PRII was incubated by means of MicroBeta counter (Fig. Wallac, Turku, Finland).
1 shows a typical dependence of CaN activity on inhibitor concentration.
Beispiel 2: Kompetition der CaN-InhibitionExample 2: Competition CaN inhibition
Die
Phosphataseaktivität
von Calzineurin kann durch den Cyp18/CsA Komplex inhibiert werden.
So führt
die Gabe von 1 µM
dieses Kompexes zur fast vollständigen
Hemmung einer CaN-Konzentration von 1.32 nM, wie dies in
Beispiel 3: ImunsuppressionExample 3: Imunsuppression
T-Zellproliferation: Um den Einfluß der Inhibitoren auf die T-Zellproliferation zu bestimmen, wurden 2 × 106 Zellen (periphere mononucleäre Blutzellen, PBMC) je ml mit 5-(6-)Carboxyfluzoresceine-Diacetatsuccinimidylester markiert und mit anti-CD3 plus anti-CD28 Antikörpern in der Gegenwart geeigneter Inhibitorkonzentrationen (Inhibitorstammlösung: 1 mg/ml DMSO) bei einer DMSO-Endkonzentration von 0.5% für 5 Tage bei 37°C kultiviert und anschließend einer Durchflußzytometrie (BD FACScalibur) unterzogen.T cell proliferation: To determine the effect of the inhibitors on T cell proliferation, 2 x 10 6 cells (peripheral blood mononuclear cells, PBMC) per ml were labeled with 5- (6-) carboxyfluoresoresin diacetate succinimidyl ester and anti-CD3 plus anti -CD28 antibodies in the presence of suitable inhibitor concentrations (inhibitor stock solution: 1 mg / ml DMSO) at a final DMSO concentration of 0.5% for 5 days at 37 ° C and then subjected to flow cytometry (BD FACScalibur).
Cytokin-Produktion: Dazu wurden 2 × 106 Zellen (PBMC) mit der gewünschten Inhibitorkonzentration bei 37°C für 10 min vorinkubiert. Anschließend wurden die Zellen mit 10 ng/ml PMA und 1 μl Ionomycin (Sigma, Steinheim) für 2 Stunden und nach Zugabe von Brefeldin A (5 μg/ml) für weitere 3 Stunden inkubiert. Nach Fixierung der Zellen mit 2% Paraformaldehyd für 20 min, Permeabilisieren mit einer Lösung aus 0.5% Saponin, und 1 % FCS in PBS konnte die Cytokinkonzentration mittels Durchflußzytometrie und Anticytokin PE-conjugierten Antikörpern (BD Biosciences) bestimmt werden. Diese Arbeitweise zum Nachweis der Cytokinproduktion wurde umfassend von Wittmann, B. et al. 1999 in Blood (Vol. 94, Seite 1717–1726) publiziert.Cytokine production: To this end, 2x10 6 cells (PBMC) with the desired inhibitor concentration were preincubated at 37 ° C for 10 min. Subsequently, the cells were incubated with 10 ng / ml PMA and 1 μl of ionomycin (Sigma, Steinheim) for 2 hours and after addition of brefeldin A (5 μg / ml) for a further 3 hours. After fixing the cells with 2% paraformaldehyde for 20 min, permeabilizing with a solution of 0.5% saponin, and 1% FCS in PBS, the cytokine concentration could be determined by flow cytometry and anticytokine PE-conjugated antibodies (BD Biosciences). This procedure for detecting cytokine production was comprehensively described by Wittmann, B. et al. 1999 in Blood (Vol. 94, pages 1717-1726).
Luciferase
Reporter Genassay: Um den Einfluß gewünschter Inhibitorkonzentrationen
und der Photoschaltung sichtbar machen zu können, wurden mit NFAT-luc Reporterplasmid
(Strategene, Niederlande) durch Elektroporation (Amaxa, Köln) transfizierte
Jurkat-Zellen hergestellt. Nach Inkubation dieser Zellen für 20 min und
einer weiteren Inkubation mit oder ohne Bestrahlung bei 366 nm für 30 min,
wurden die Zellen durch Zugabe von 10 ng/ml PMA und 1 μg/ml Ionomycin
stimuliert und weitere 5 h inkubiert. Danach wurde die Konzentration
an Luziferase mittels kommerziellem Luziferaseassay (Promega, Mannheim)
bestimmt. Als interner Kontrollstandard wurde die Expression von
mit β-Galaktosidase
kotransfizierten Zellen genutzt. Die erhaltenen Ergebnisse sind
in den
Beispiel 4: Photoschaltung (I)Example 4: Photo switching (I)
Die
Photokonversion von Cs10 in Cs12 läßt sich leicht mittels RP-HPLC-Trennung
und nachfolgender Massenspektrometrie durchführen, wie dies beispielgebend
hier dargestellt ist. Dazu wird Licht mit einer Handlampe (Dr. Gröbel UV-Elektronik
GmbH, 2-5062, 254/366 nm) für
10, 20, 30 oder 60 min auf eine äthanolische Probe
von Cs10 (10 mg/ml) bei 23°C
in einer Küvette
gerichtet. Unmittelbar nach der Bestrahlung wird die Probe mittels
HPLC getrennt. Die
Beispiel 5: Photoschaltung (II)Example 5: Photo switching (II)
Der
im Beispiel 3 aufgeführte
NFAT-Reporter-Gen-Assay ist gut geeignet den Effekt einer Aktivierung der
Substanz Cs10 zu Cs12 anhand der NFAT-Translokation sichtbar zu
machen. Wie in
- a) Die Zugabe von PMA/Ionomycin führt zur NFAT Reportergenaktivierung
- b) Die zusätzliche Gabe zu (a) von Cs10 hemmt diese Aktivierung dosisabhängig
- c) Die zusätzliche Gabe zu (a) von mit Licht bestrahltem Cs10 hemmt diese Aktivierung nur in hohen Dosen
- d) Die Bestrahlung der Zellen nach Applikation von Cs10 führt zu ähnlichen Effekten wie die Applikation von Substanz Cs12
- a) The addition of PMA / ionomycin leads to NFAT reporter gene activation
- b) The additional administration to (a) of Cs10 inhibits this activation in a dose-dependent manner
- c) The addition of (a) light-irradiated Cs10 inhibits this activation only in high doses
- d) The irradiation of the cells after application of Cs10 leads to similar effects as the application of substance Cs12
Beispiel 6: Aktivierung durch enzymatische SpaltungExample 6: Activation by enzymatic cleavage
Durch
Herstellung eines Cyclosporinderivates bei dem in 8-Position (entsprechend
Formel 1) der Substituent -CH2-O-CH2C(O)NH(CH2)2NHC(O)OC2H5 entsprechend einem Analoga des Typs A10
eingeführt
wurde, wird diese Verbindung nun von Esterasen (EC 3.1.1) als Substrat
akzeptiert. Nach Hydrolyse des Ethylesters kommt es zur spontanen
CO2-Abspaltung und zur Bildung eines A12-Analoga,
welches hier einem Cyclosporinderivat mit einem Substituent -CH2-O-CH2C(O)NH(CH2)2NH2 entspricht.
Als Esterase wurde eine kommerzielle Carboxylesterase (Sigma, E3019)
aus Schweineleber bei folgenden Reaktionsbedingungen verwendet:
100 μg CsA8-CH2-O-CH2C(O)NH(CH2)2NHC(O)OC2H5 werden in 100 μl DMSO gelöst und anschließend zu
2 ml 25 mM Trispuffer (pH 8), welcher 30 Units Esterase enthält gegeben
und über
Nacht bei Raumtemperatur (ca. 23°C)
stehen gelassen. Die Trennung des Reaktionsansatzes mittels HPLC
zeigt ein
Beispiel 7: Aktivierung durch Änderung des pH-WertesExample 7: Activation by change of the pH
Durch
Herstellung eines Cyclosporinderivates bei dem in 8-Position (entsprechend
Formel 1) der Substituent -CH2-O-CH2C(O)NH(CH2)3NHC(O)OCH3 entsprechend
einem Analoga des Typs A10, eingeführt wurde, wird diese Verbindung
empfindlich gegenüber
einer Katalyse durch Säuren-
oder Basen. Nach Hydrolyse des Methylesters kommt es zur spontanen
CO2-Abspaltung und zur Bildung eines A12-Analoga, welches
hier einem Cyclosporinderivat mit einem Substituenten -CH2-O-CH2C(O)NH(CH2)3NH2 entspricht.
Folgende Reaktionsbedingung wurde angewendet: 200 μg CsA8-CH2-O-CH2C(O)NH(CH2)3NHC(O)OCH3 werden
in 150 μl DMSO
gelöst
und anschließend
zu 2 ml 50 mM Glycinpuffer (pH 13), gegeben und über Nacht bei Raumtemperatur
(ca. 23°C)
stehen gelassen. Die Trennung des Reaktionsansatzes mittels HPLC
zeigt ein der
Beispiel 8: Synthese von [O-carboxymethyl D-Ser]8 CsA (Cs6)Example 8: Synthesis of [O-carboxymethyl D-Ser] 8 CsA (Cs6)
Eine Lösung von 60 mg [D-Ser]8 CsA, tert-butyl Bromoacetat (20 mg) und 5 mg Benzyltriethylammoniumchlorid in 1 ml CH2Cl2 wurde für zwei Stunden bei 23°C mit 2 ml 30% NaOH wäßriger Lösung verrührt. Danach wurde die Lösung mit 10 ml Wasser verdünnt und zwei mal mit Äther extrahiert. Danach wurde die organische Phase mit Na2SO4 getrocknet. Anschließend wurden ohne weitere Trennschritte 30 ml methanolische KON-Lösung (60 mM) dazugegeben und für weitere drei Stunden gerührt. Nach Zugabe einer äquivalenten Menge Essigsäure, wurde mittels Rotationsverdampfer der größte Teil Essigsäure und Methanol entfernt. Danach wurden 200 ml Äthylazetat hinzugegeben und die Mischung mit Wasser gewaschen. Nach Separation der organischen Phase und Trocknung mit Na2SO4, wurde die gesuchte Verbindung mittels RP HPLC (94%) abgetrennt. Das MALDI-Massenspektrum (m/z) von 1276.8 [MH]+ stimmte sehr gut mit dem berechneten von cal. 1275.7 überein.A solution of 60 mg of [D-Ser] 8 CsA, tert-butyl bromoacetate (20 mg) and 5 mg of benzyltriethylammonium chloride in 1 ml of CH 2 Cl 2 was stirred for 2 hours at 23 ° C with 2 ml of 30% NaOH aqueous solution. Thereafter, the solution was diluted with 10 ml of water and extracted twice with ether. Thereafter, the organic phase was dried with Na 2 SO 4 . Then, without further separation steps, 30 ml of methanolic KON solution (60 mM) were added thereto and the mixture was stirred for a further three hours. After adding an equivalent amount of acetic acid, most of the acetic acid and methanol were removed by rotary evaporation. Thereafter, 200 ml of ethyl acetate were added and the mixture was washed with water. After separation of the organic phase and drying with Na 2 SO 4 , the desired compound was separated by RP HPLC (94%). The MALDI mass spectrum (m / z) of 1276.8 [MH] + agreed very well with the calculated cal. 1275.7.
Beispiel 9: Synthese von [O-(NH2(CH2)5NHC(O)-CH2-)D-Ser]8 CsA (Cs12)Example 9: Synthesis of [O- (NH 2 (CH 2 ) 5 NHC (O) -CH 2 -) D-Ser] 8 CsA (Cs12)
Ein Teil (100 mg) Cs6 (Beispiel 8), 3 Teile von NH2(CH2)5NNBoc, 4 Teile von PyBop und 8 Teile von DIPEA werden zu 5 ml CH2Cl2 gegeben und bei 23°C über Nacht gerührt. Danach werden 40 m1 Äthyl acetate hinzugegeben und die organische Phase nacheinander mit 5% NaHSO4, 5% NaHCO3 and gesättigter wäßriger NaCl-Lösung gewaschen, and anschließend mit Na2SO4 getrocknet. Nach Entfernen des Lösungsmittels mittels Vakuumverdampfer konnte das Produkt (Cs9) mittels C8 HPLC (96%) abgetrennt werden. Das MALDI-Massenspektrum (m/z) von 1461.3 [MH]+ stimmte sehr gut mit dem berechneten von 1460.2 überein. Zur Entfernung der Boc-Schutzgruppe wurde Cs9 mit 5 ml ZnCl2/Äther in Äther unter Schutzgas (N2) für 3 Stunden versetzt. Danach wurde durch Zugabe von 0.1 ml Wasser and 15 ml Acetonitril gefällt und anschließend filtriert. Nach Entfernen des organischen Lösungsmittels mittels Vakuumverdampfer konnte Cs12 mittels C8 HPLC (86%) erhalten werden. Das Produkt konnte mittels 1H NMR: δ: 9.50(m), 8.42(m), 8.08(m), 7.56(m), 6.84(m), 5.62(s), 5.52(s), 5.40(m), 5.28(m), 5.19(s), 4.60(m), 4.10(m), 3.58–3.40(m), 3.14(m), 3.03(m), 2.84(m), 2.75(m), 2.70(s), 1.81(m), 1.72(m), 1.59(m), 1.18–1.40(m), 0.70–1.15(m) und MALDI-Massenspektrometrie (m/z) mit 1361.3 [MH]+ bestimmt werden und entsprach damit gut der berechneten Masse von 1360.1 One part (100 mg) of Cs6 (Example 8), 3 parts of NH 2 (CH 2 ) 5 NNBoc, 4 parts of PyBop and 8 parts of DIPEA are added to 5 ml of CH 2 Cl 2 and stirred at 23 ° C overnight , Thereafter, 40 ml of ethyl acetate are added and the organic phase washed successively with 5% NaHSO 4 , 5% NaHCO 3 and saturated aqueous NaCl solution, and then dried with Na 2 SO 4 . After removal of the solvent by means of a vacuum evaporator, the product (Cs9) could be separated off by means of C8 HPLC (96%). The MALDI mass spectrum (m / z) of 1461.3 [MH] + agreed very well with the calculated one of 1460.2. To remove the Boc protecting group, Cs9 was added with 5 ml of ZnCl 2 / ether in ether under inert gas (N 2 ) for 3 hours. It was then precipitated by the addition of 0.1 ml of water and 15 ml of acetonitrile and then filtered. After removal of the organic solvent by means of a vacuum evaporator, Cs12 could be obtained by means of C8 HPLC (86%). The product was analyzed by 1 H NMR: δ: 9.50 (m), 8.42 (m), 8.08 (m), 7.56 (m), 6.84 (m), 5.62 (s), 5.52 (s), 5.40 (m), 5.28 (m), 5.19 (s), 4.60 (m), 4.10 (m), 3.58-3.40 (m), 3.14 (m), 3.03 (m), 2.84 (m), 2.75 (m), 2.70 (s ), 1.81 (m), 1.72 (m), 1.59 (m), 1.18-1.40 (m), 0.70-1.15 (m), and MALDI mass spectrometry (m / z) are determined to be 1361.3 [MH] + and corresponded thereto good of the calculated mass of 1360.1
Beispiel 10: Synthese von [O-(NVOCNH(CH2)5NHC(O)CH2-)D-Ser]8 CsA (Cs10)Example 10: Synthesis of [O- (NVOCNH (CH 2 ) 5 NHC (O) CH 2 -) D-Ser] 8 CsA (Cs10)
Ein Teil (30 mg) Cs12, 2 Teile von NVOC-Cl, 4 Teile von DIPEA werden zu 2 ml DMF gegeben und bei 23°C über Nacht gerührt. Anschließend wurden 40 ml Äthylazetat hinzugegeben und die organische Phase nacheinander mit 5% NaHSO4, 5% NaHCO3 und gesättigter wäßriger Kochsalzlösung gewaschen und nachfolgend mit Na2SO4 getrocknet. Nach einengen mittels Rotationsverdampfer konnte das Produkt mittels C8 HPLC (90%) abgetrennt werden. Das MALDI-Massenspektrum (m/z) von 1601.0 [MH]+ stimmte sehr gut mit dem berechneten von cal. 1599.6 überein.One part (30 mg) of Cs12, 2 parts of NVOC-Cl, 4 parts of DIPEA are added to 2 ml of DMF and stirred at 23 ° C overnight. Subsequently, 40 ml of ethyl acetate were added and the organic phase washed successively with 5% NaHSO 4 , 5% NaHCO 3 and saturated aqueous sodium chloride solution and subsequently dried with Na 2 SO 4 . After narrowing with a rotary evaporator, the product was separated by C8 HPLC (90%). The MALDI mass spectrum (m / z) of 1601.0 [MH] + agreed very well with the calculated cal. 1599.6.
Beispiel 11: Einfluß von Cs12 auf die ProliferationExample 11: Influence of Cs12 on proliferation
Cs12
wird entweder chemisch entsprechend Beispiel 8 synthetisiert oder
mittels Bestrahlung aus Cs10 (Beispiel 3) hergestellt. Blutzellen
(PBMCs) werden mit CFSE markiert und mit anti-CD3/anti-CD28 stimuliert,
wie dies in Beispiel 2 (T-Zellproliferation)
angegeben ist. Nach Inkubation mit DMSO (als Kontrolle), Cs12 (1 µM) oder
CsA (50 nM) über
5 Tage wird die Markierung in Abhängigkeit von der Zellzahl mittels
FACS gemessen. In
Beispiel 12: Einfluß von Cs12 auf die CytokinbildungExample 12: Influence of Cs12 on cytokine production
Cs12
wird entweder chemisch entsprechend Beispiel 8 synthetisiert oder
mittels Bestrahlung aus Cs10 (Beispiel 4) hergestellt. Eine FACS-Analyse
und Stimulationsprozedur mit PMA/Ionomycin, einschließlich der
notwendigen Gabe von Brefeldin während
der Stimulationsproezdur von PBMC wurde weitgehend analog der in
Beispiel 2 (T-Zellproliferation) angegeben Prozedur durchgeführt und
stützt
sich im wesentlichen auf die in der Literatur üblichen Prozedeuren (wie z.B.
Wittmann, B. et al. Blood 94 (1999) 1717). Die Effektoren werden
10 min vor der oben beschriebenen Stimulierung zu den PBM-Zellen
bei 37°C
zugegeben. In
Claims (32)
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE102004011988A DE102004011988A1 (en) | 2004-03-11 | 2004-03-11 | Cyclosporin derivatives and pharmaceutical compositions containing them |
| PCT/EP2005/000919 WO2005087798A1 (en) | 2004-03-11 | 2005-01-31 | D-ser!8-cyclosporine modified on the hydroxyl group having a switchable inhibiting effect on protein phosphatase calcineurine and specific manipulipulatability obtained therewith of the immunosuppressive effect while maintaining inhibition of peptidyl-prolyl-cis-trans-isomerase (ppi) e.g. for the treatment of autoimmune d |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE102004011988A DE102004011988A1 (en) | 2004-03-11 | 2004-03-11 | Cyclosporin derivatives and pharmaceutical compositions containing them |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| DE102004011988A1 true DE102004011988A1 (en) | 2005-09-22 |
Family
ID=34877587
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE102004011988A Withdrawn DE102004011988A1 (en) | 2004-03-11 | 2004-03-11 | Cyclosporin derivatives and pharmaceutical compositions containing them |
Country Status (2)
| Country | Link |
|---|---|
| DE (1) | DE102004011988A1 (en) |
| WO (1) | WO2005087798A1 (en) |
Cited By (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7361636B2 (en) | 2004-10-06 | 2008-04-22 | Amr Technology, Inc. | Cyclosporin alkynes and their utility as pharmaceutical agents |
| US7378391B2 (en) | 2004-09-29 | 2008-05-27 | Amr Technology, Inc. | Cyclosporin alkyne analogues and their pharmaceutical uses |
| US7511013B2 (en) | 2004-09-29 | 2009-03-31 | Amr Technology, Inc. | Cyclosporin analogues and their pharmaceutical uses |
| US7538084B2 (en) | 2003-03-17 | 2009-05-26 | Amr Technology, Inc. | Cyclosporins |
| EP2116263A1 (en) * | 2008-05-05 | 2009-11-11 | Max-Planck-Gesellschaft zur Förderung der Wissenschaften e.V. | Reversibly light-switchable drug-conjugates |
| US7696166B2 (en) | 2006-03-28 | 2010-04-13 | Albany Molecular Research, Inc. | Use of cyclosporin alkyne/alkene analogues for preventing or treating viral-induced disorders |
| US7696165B2 (en) | 2006-03-28 | 2010-04-13 | Albany Molecular Research, Inc. | Use of cyclosporin alkyne analogues for preventing or treating viral-induced disorders |
| EP2705856A1 (en) * | 2012-09-07 | 2014-03-12 | Deutsches Zentrum für Neurodegenerative Erkrankungen e.V. | Compounds for the treatment of neurodegenerative disorders |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1810675A1 (en) | 2006-01-18 | 2007-07-25 | Institut Curie | Method for treating Huntington's disease by inhibiting dephosphorylation of huntingtin at S421 |
| US7576057B2 (en) | 2006-11-20 | 2009-08-18 | Scynexis, Inc. | Cyclic peptides |
| PL2651965T3 (en) | 2010-12-15 | 2019-04-30 | Contravir Pharmaceuticals Inc | Cyclosporine analogue molecules modified at amino acid 1 and 3 |
-
2004
- 2004-03-11 DE DE102004011988A patent/DE102004011988A1/en not_active Withdrawn
-
2005
- 2005-01-31 WO PCT/EP2005/000919 patent/WO2005087798A1/en not_active Ceased
Cited By (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7538084B2 (en) | 2003-03-17 | 2009-05-26 | Amr Technology, Inc. | Cyclosporins |
| US7378391B2 (en) | 2004-09-29 | 2008-05-27 | Amr Technology, Inc. | Cyclosporin alkyne analogues and their pharmaceutical uses |
| US7511013B2 (en) | 2004-09-29 | 2009-03-31 | Amr Technology, Inc. | Cyclosporin analogues and their pharmaceutical uses |
| US7361636B2 (en) | 2004-10-06 | 2008-04-22 | Amr Technology, Inc. | Cyclosporin alkynes and their utility as pharmaceutical agents |
| US7632807B2 (en) | 2004-10-06 | 2009-12-15 | Albany Molecular Research, Inc. | Cyclosporin alkynes and their utility as pharmaceutical agents |
| US7696166B2 (en) | 2006-03-28 | 2010-04-13 | Albany Molecular Research, Inc. | Use of cyclosporin alkyne/alkene analogues for preventing or treating viral-induced disorders |
| US7696165B2 (en) | 2006-03-28 | 2010-04-13 | Albany Molecular Research, Inc. | Use of cyclosporin alkyne analogues for preventing or treating viral-induced disorders |
| EP2116263A1 (en) * | 2008-05-05 | 2009-11-11 | Max-Planck-Gesellschaft zur Förderung der Wissenschaften e.V. | Reversibly light-switchable drug-conjugates |
| EP2705856A1 (en) * | 2012-09-07 | 2014-03-12 | Deutsches Zentrum für Neurodegenerative Erkrankungen e.V. | Compounds for the treatment of neurodegenerative disorders |
| WO2014037260A1 (en) * | 2012-09-07 | 2014-03-13 | Deutsches Zentrum Für Neurodegenerative Erkrankungen E.V. | Compounds for the treatment of neurodegenerative disorders |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2005087798A1 (en) | 2005-09-22 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE69928938T2 (en) | NEW CYCLOSPORIN WITH IMPROVED EFFECT | |
| CA1338319C (en) | Cyclosporin derivative with modified "8-amino acid" | |
| DE3100974C2 (en) | ||
| US8129342B2 (en) | High purity lipopeptides | |
| DE60011678T2 (en) | DEPSIPEPTIDES AND ITS ANALOGS FOR USE AS IMMUNOSUP PRESSIVES | |
| DE3888357T2 (en) | Cyclosporin derivatives that carry a modified amino acid at position 8. | |
| DE69905368T2 (en) | OXYDED THYMOSINE BETA 4 | |
| DE60208180T2 (en) | MODIFIED CYCLOSPORIN APPLICABLE AS MEDICAMENT PREPARATION AND USE THEREOF | |
| DE3509809A1 (en) | CYCLOSPORINE, THEIR PRODUCTION AND USE | |
| LV12125B (en) | CYCLFILINE ROTAMASE ACTIVITIES INHIBITORS | |
| EP0629636A1 (en) | Lipopeptides from actinoplanes sp. endowed with pharmacological activity, process for their preparation and their use | |
| DE102004011988A1 (en) | Cyclosporin derivatives and pharmaceutical compositions containing them | |
| DE69011006T2 (en) | Antibiotic agents. | |
| DE60124532T2 (en) | NEW POLYPEPTIDES FROM BEEKE POISON AND METHOD FOR THEIR USE | |
| DE2822951A1 (en) | NEW POLYPEPTIDES WITH THYMAL ACTIVITY OR ANTAGONISTIC ACTIVITY AND METHODS FOR THEIR PRODUCTION | |
| EP2471806A2 (en) | Cyclosporine derivates | |
| DE60202356T2 (en) | TRIPEPTIDES AND THEIR DERIVATIVES FOR THE TREATMENT OF POST-LESIONAL DISEASES OF THE NERVOUS SYSTEM | |
| EP0307553B1 (en) | Modified splenopentines, their process of preparation and their use | |
| WO2010063483A2 (en) | Active ingredient-peptide construct for extracellular enrichment | |
| DE102005009784B4 (en) | Peptide mimetics, process for their preparation, pharmaceutical compositions containing them and their use as inhibitors of proteasomes and for the induction of apoptosis | |
| DE60038735T2 (en) | PSEUDOMYCIN ANALOG | |
| EP0622375A1 (en) | Chrysospermines, peptide drugs from Apiocrea chrysosperma having pharmacological activity, process for their production, and their use | |
| EP1572226B1 (en) | Peptides having a high cysteine content | |
| DE1805280A1 (en) | New cyclopeptides and their production | |
| JPH02184699A (en) | Novel cyclosporin derivative improved in "8-amino acid" |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 8139 | Disposal/non-payment of the annual fee |