CN116209459A - Il-10突变蛋白及其融合蛋白 - Google Patents
Il-10突变蛋白及其融合蛋白 Download PDFInfo
- Publication number
- CN116209459A CN116209459A CN202180051906.4A CN202180051906A CN116209459A CN 116209459 A CN116209459 A CN 116209459A CN 202180051906 A CN202180051906 A CN 202180051906A CN 116209459 A CN116209459 A CN 116209459A
- Authority
- CN
- China
- Prior art keywords
- seq
- amino acid
- acid sequence
- chain variable
- heavy chain
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- H—ELECTRICITY
- H02—GENERATION; CONVERSION OR DISTRIBUTION OF ELECTRIC POWER
- H02J—CIRCUIT ARRANGEMENTS OR SYSTEMS FOR SUPPLYING OR DISTRIBUTING ELECTRIC POWER; SYSTEMS FOR STORING ELECTRIC ENERGY
- H02J50/00—Circuit arrangements or systems for wireless supply or distribution of electric power
- H02J50/005—Mechanical details of housing or structure aiming to accommodate the power transfer means, e.g. mechanical integration of coils, antennas or transducers into emitting or receiving devices
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/52—Cytokines; Lymphokines; Interferons
- C07K14/54—Interleukins [IL]
- C07K14/5428—IL-10
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/21—Immunoglobulins specific features characterized by taxonomic origin from primates, e.g. man
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/33—Crossreactivity, e.g. for species or epitope, or lack of said crossreactivity
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/52—Constant or Fc region; Isotype
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/55—Fab or Fab'
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/60—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/94—Stability, e.g. half-life, pH, temperature or enzyme-resistance
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Immunology (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Genetics & Genomics (AREA)
- Biophysics (AREA)
- Biochemistry (AREA)
- Molecular Biology (AREA)
- Gastroenterology & Hepatology (AREA)
- Zoology (AREA)
- Toxicology (AREA)
- Engineering & Computer Science (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Pain & Pain Management (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Rheumatology (AREA)
- Computer Networks & Wireless Communication (AREA)
- Power Engineering (AREA)
- Peptides Or Proteins (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Epidemiology (AREA)
Abstract
本披露总体上涉及作为单体稳定的IL‑10的突变蛋白、与TREM‑1结合的抗原结合蛋白、和包含IL‑10突变蛋白和抗原结合部分的抗原结合蛋白、以及其组合物,所述抗原结合部分是例如抗TREM‑1抗体。本披露还提供了使用这些组合物治疗炎性疾病,如炎性肠病或溃疡性结肠炎的方法。
Description
相关申请的交叉引用
本申请要求于2020年6月26日提交的美国临时专利申请号63/045,041和于2020年12月14日提交的美国临时专利申请号63/199,218的优先权,这些申请的披露内容通过引用以其整体并入本文。
技术领域
本披露涉及白介素-10的突变蛋白和包含IL-10和抗原结合部分的抗原结合蛋白(如抗TREM-1或抗PD-1抗体),用于治疗炎性病症,如炎性肠病。
通过引用并入以电子方式提交的材料
作为本披露的一部分的序列表以文本文件的形式与本说明书同时提交。含有序列表的文本文件的名称为“55384_Seqlisting.txt”,创建于2021年6月22日,并且大小为5,726,194字节。序列表的主题通过引用以其整体并入本文。
背景技术
白介素-10(IL-10)是参与多种免疫调节过程的重要的细胞因子(参见Ouyang和O’Garra,Immunity[免疫力],50(4):871-891 2019)。特别地,根据免疫系统细胞的类型,其具有免疫抑制或免疫刺激作用。IL-10抑制单核细胞和组织巨噬细胞中炎性细胞因子、MHCII、CD86和ICAM的上调。据报道,IL-10也可以增强Treg细胞的抑制活性。然而,IL-10也刺激CD8+T细胞激活和B细胞激活。IL-10与炎性肠病(IBD)有较强的遗传相关性。患有IL-10、IL-10R1、或IL-10R2纯合子功能缺失性突变的患者出现严重的婴儿型IBD(Kotlarz,Gastroenterology[胃肠病学],2012;Glocker,NEM,2009)。据报道,在GWAS中,IL10rs3024505也与IBD相关,RAF为0.16,OR为1.46,p值为10-42(Jostins L,2012)。聚乙二醇化IL-10在克罗恩病(Crohn’sDisease)研究中显示出适度疗效,这可能是由于剂量限制毒性(Schreiber等人,Gastroenterology[胃肠病学]119:1461,2000)。先前的使用髓细胞中IL-10R1基因敲除的小鼠的研究表明,IL-10对髓细胞的抗炎活性对于控制结肠炎的发展很重要(Zigmond等人,Immunity[免疫力],40(5):720-33,2014)。
发明内容
本披露提供了作为单体稳定的IL-10的突变蛋白,并且可用于治疗炎性疾病。预期IL-10突变蛋白保留/恢复IL-10对单核细胞和巨噬细胞的抑制活性,并减小IL-10对CD8+T细胞和B细胞的刺激。本披露还提供了可用于治疗炎性疾病的针对TREM-1的抗体。在另一方面中,本披露提供了可用于治疗炎性疾病的包含IL-10突变蛋白和抗原结合部分的抗原结合蛋白,该抗原结合部分是例如抗TREM-1或抗PD-1抗体。
本文提供了人白介素-10(IL-10)突变蛋白,其包含与SEQ ID NO:2中列出的氨基酸序列具有至少90%同一性的氨基酸序列,其中所述IL-10突变蛋白具有选自以下的至少一个突变:螺旋环AB、螺旋环CD、螺旋环DE、螺旋A、螺旋B、螺旋C、螺旋D、螺旋E和/或螺旋F中的突变。在多个实施例中,本披露的IL-10突变蛋白包含螺旋A、螺旋F或螺旋环AB中的至少一个突变。在多个实施例中,IL-10突变蛋白与SEQ ID NO:2中列出的氨基酸序列具有至少95%同一性。在多个实施例中,IL-10突变蛋白氨基酸序列与SEQ ID NO:2中列出的氨基酸序列具有96%、97%、98%或99%同一性。
在多个实施例中,IL-10突变蛋白包含SEQ ID NO:2的残基N10、H14、F15、P20、M22、L23、R24、R27、D28、K34、T35、Q38、M39、K40、D41、Q42、L43、D44、N45、L46、L47、L48、K49、F56、K57、Y59、L60、Q63、E67、Q70、M77、Q79、N82、Q83、D84、P85、D86、I87、A89、H90、S93、T100、L103、H109、R110、L112、E115、N116、A127、K130、I136、Y137、K138、S141、E142、D144、I145、E151、M154、M156、K157、或N160中的一个或多个中的突变,和/或在螺旋D和螺旋E之间添加4到8个氨基酸。在多个实施例中,突变是SEQ ID NO:2的R27L、K34D、D41G、L46K、Q38E、Q38R、Q38D、K138L、K138D、或I87A,任选地包含在螺旋D和螺旋E之间添加6个氨基酸。在多个实施例中,突变是SEQ ID NO:2的N10Q、N10I、N10K、R27L、K34D、D41G、L46K、Q38E、Q38R、Q38D、K138L、K138D、I87A、H14Q、F15Y、M22V、K49T、K49S、F56Y、K57N、Y59T、L60Q、Q63E、Q63L、E67C、Q70E、Q70K、M77R、M77V、Q79R、Q79C、D84R、A89P、H90E、H90Q、S93E、S93Q、T100R、L103E、H109D、R110P、R110Q、L112V、E115K、N116D、N116Q、A127M、K130Q、I136C、Y137C、M154V、M156C、K157N、或N160D,任选地包含在螺旋D和螺旋E之间添加4到8个氨基酸。在多个实施例中,IL10突变蛋白涵盖如表16或表17或表21以及本文披露内容中列出的IL10突变的组合。在多个实施例中,螺旋D和螺旋E之间的氨基酸是GGGSGG(SEQ ID NO:2676)。在多个实施例中,某些IL-10突变蛋白的氨基酸序列在SEQ ID NO:3-10,以及SEQ ID NO:2138、2140、2142、2144、2146、2148、2150、2152、2154、2156、2158、2160、2162、2164、2166、2168、2170、2172、2174、2176、2178、2180、2182、2360、2362、2364、2366、2368、2370、2372、2374、2376、2378、2380、2382、2384、2386、2388、2390、2392、2394、2396、2398、2400、2402、2404、2406、2408、2410、2412、2414、2416、2418、2420、2422、2424、2426、2428、2430、2432、2434、2436、2438、2440、2442、2444、2446、2448、2450、2452、2454、2456、2458、2460、2462、2464、2466、2468、2470、2472、2474、2476、2478、2480、2482、2484、2486、2488、2490、2492、2494、2496、2500、2502、2504、2506、2508、2510、2512、2514、2516、2518、2520、2522、2524、2526、2528、2530、2532、2534、2536、2540、和2777-2791中列出。
在多个实施例中,本披露提供了人白介素-10(IL-10)突变蛋白,该IL-10突变蛋白包含与以下氨基酸中列出的氨基酸序列具有至少90%同一性的氨基酸序列:SEQ ID NO:3-10或SEQ ID NO:2138、2140、2142、2144、2146、2148、2150、2152、2154、2156、2158、2160、2162、2164、2166、2168、2170、2172、2174、2176、2178、2180、2182、2360、2362、2364、2366、2368、2370、2372、2374、2376、2378、2380、2382、2384、2386、2388、2390、2392、2394、2396、2398、2400、2402、2404、2406、2408、2410、2412、2414、2416、2418、2420、2422、2424、2426、2428、2430、2432、2434、2436、2438、2440、2442、2444、2446、2448、2450、2452、2454、2456、2458、2460、2462、2464、2466、2468、2470、2472、2474、2476、2478、2480、2482、2484、2486、2488、2490、2492、2494、2496、2500、2502、2504、2506、2508、2510、2512、2514、2516、2518、2520、2522、2524、2526、2528、2530、2532、2534、2536、2538、或2540和2777-2791。在多个实施例中,突变蛋白包含与本文所述的突变蛋白序列具有至少95%、96%、97%、98%、或99%同一性的氨基酸序列。
在多个实施例中,与野生型(wt)IL-10相比,IL-10突变蛋白减少了髓细胞中TNF-α产生方面的抑制,降低了CD8+T细胞刺激方面的水平,和/或降低了B细胞刺激方面的水平。在多个实施例中,抗TREM-1/IL-10突变蛋白抗原结合蛋白抑制髓细胞中TNF-α产生。在多个实施例中,抗TREM-1/IL-10突变蛋白抗原结合蛋白抑制髓细胞中TNF-α产生,同时减少CD8+T细胞和B细胞激活。
在多个实施例中,IL-10突变蛋白与将抗原结合蛋白靶向髓细胞、B细胞或T细胞的结合部分融合。在多个实施例中,结合蛋白与髓细胞、CD8+T细胞、CD4+T细胞、或B细胞上的细胞表面蛋白结合。
在多个实施例中,IL-10突变蛋白进一步包含半衰期延长部分。在多个实施例中,半衰期延长部分是Fc结构域。在多个实施例中,半衰期延长部分是聚乙二醇(PEG)等。
在多个实施例中,突变蛋白是二聚体。在多个实施例中,突变蛋白二聚体包含两种不同的突变蛋白单体。在多个实施例中,突变蛋白二聚体包含相同的突变蛋白单体。
进一步提供了分离的核酸分子,其包含编码如本文所述的IL-10突变蛋白的核苷酸序列。在多个实施例中,IL-10突变蛋白的多核苷酸序列在SEQ ID NO:11-18中列出。
本披露还考虑了表达载体,该表达载体包含含有编码可操作地连接到表达控制序列的IL-10突变蛋白的核苷酸序列的核酸分子。
本文提供了重组宿主细胞,该重组宿主细胞包含含有编码IL-10突变蛋白的核苷酸序列的核酸或载体。在多个实施例中,宿主细胞是哺乳动物细胞。在多个实施例中,宿主细胞是CHO细胞。还提供了使用宿主细胞产生IL-10突变蛋白的方法以及通过该方法产生的IL-10突变蛋白,该方法包括培养宿主细胞并回收IL-10突变蛋白。
本披露还提供了包含如本文所述的IL-10突变蛋白和药学上可接受的载剂的药物组合物。预期药物组合物可以为无菌药物组合物。
在另一个方面,本披露提供了分离的抗原结合蛋白,其中该抗原结合蛋白:
a.是抗体或抗体片段;
b.与髓细胞1上表达的具有SEQ ID NO:20中列出的氨基酸序列的人触发受体(TREM-1)结合;
c.包含轻链可变结构域,该轻链可变结构域包含:
i.轻链CDR1,其包含选自SEQ ID NO:30、50、70、90、110、130、150、170、190、210、230、250、270、290和2190的氨基酸序列;
ii.轻链CDR2,其包含选自SEQ ID NO:31、51、71、91、111、131、151、171、191、211、231、251、271、291和2191的氨基酸序列;
iii.轻链CDR3,其包含选自SEQ ID NO:32、52、72、92、112、132、152、172、192、212、232、252、272、292和2192的氨基酸序列;并且
d.包含重链可变结构域,该重链可变结构域包含:
i.重链CDR1,其包含选自SEQ ID NO:36、56、76、96、116、136、156、176、196、216、236、256、276、296和2196的氨基酸序列;
ii.重链CDR2,其包含选自SEQ ID NO:37、57、77、97、117、137、157、177、197、217、237、257、277、297和2197的氨基酸序列;和
iii.重链CDR3,其包含选自SEQ ID NO:38、58、78、98、118、138、158、178、198、218、238、258、278、298和2198的氨基酸序列。
在多个实施例中,
a.轻链CDR1序列在SEQ ID NO:30、50、70、110、150、170、或290中列出;
b.轻链CDR2序列在SEQ ID NO:31、51、71、111、151、171、或291中列出;
c.轻链CDR3序列在SEQ ID NO:32、52、72、112、152、172、或292中列出;
d.重链CDR1序列在SEQ ID NO:36、56、76、116、156、176、或296中列出;
e.重链CDR2序列在SEQ ID NO:37、57、77、117、157、177、或297中列出;和
f.重链CDR3序列在SEQ ID NO:38、58、78、118、158、178、或298中列出。
在多个实施例中,
a.轻链CDR1序列在SEQ ID NO:50或110中列出;
b.轻链CDR2序列在SEQ ID NO:51或111中列出;
c.轻链CDR3序列在SEQ ID NO:52或112中列出;
d.重链CDR1序列在SEQ ID NO:56或116中列出;
e.重链CDR2序列在SEQ ID NO:57或117中列出;和
f.重链CDR3序列在SEQ ID NO:58或118中列出。
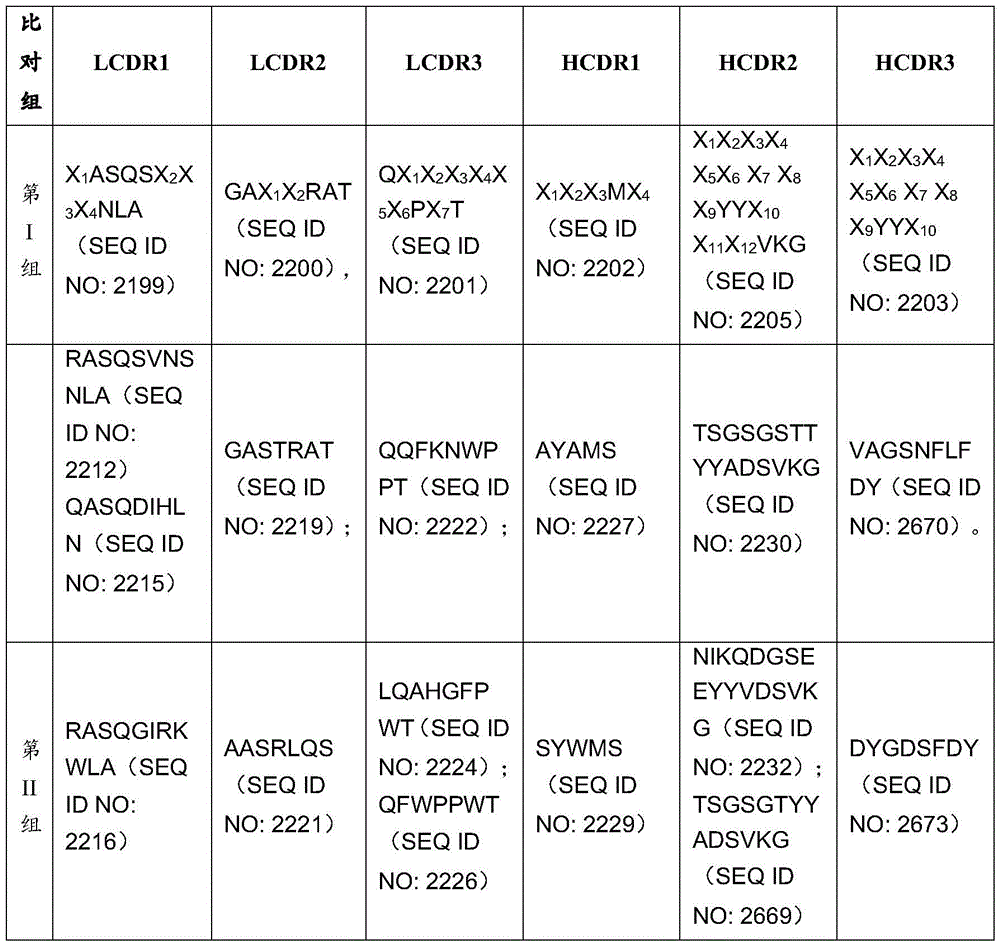
还考虑了本文披露的TREM-1抗体重链和轻链CDR和/或可变区序列的共有序列。例如,在多个实施例中,TREM-1抗体包含抗原结合结构域,该抗原结合结构域包含具有包含选自下组的LCDR1氨基酸序列的轻链可变区的序列,该组由以下组成:
X1ASQSX2X3X4NLA(SEQ ID NO:2199),其中X1是R或Q,其中X2是V或I,其中X3是N或S,并且其中X4是S、H、I、V或A;
QASX1DIX2X3X4LN(SEQ ID NO:2204),其中X1是R或Q,其中X2是R、S、N或F,其中X3是K或N,并且其中X4是H、Y或D;
RASQSVNSNLA(SEQ ID NO:2212);
QASQDIRKHLN(SEQ ID NO:2213);
RASQDISSNLN(SEQ ID NO:2214);
QASQDIHLN(SEQ ID NO:2215);
RASQGIRKWLA(SEQ ID NO:2216);
RASQSVNSNLA(SEQ ID NO:2217)和
SGDKLGERVS(SEQ ID NO:2218)。
在多个实施例中,TREM-1抗体包含抗原结合结构域,该抗原结合结构域包含具有包含选自下组的LCDR2氨基酸序列的轻链可变区的序列,该组由以下组成:
GAX1X2RAT(SEQ ID NO:2200),其中X1是S或Y,并且其中X2是T或I;
X1X2X3X4LET(SEQ ID NO:2206),其中X1是D、G或H,其中X2是A、V或T,其中X3是S、A或Y,并且其中X4是T或N;
GASTRAT(SEQ ID NO:2219);
DASNLET(SEQ ID NO:2220);和
AASRLQS(SEQ ID NO:2221)。
在多个实施例中,TREM-1抗体包含抗原结合结构域,该抗原结合结构域包含具有包含选自下组的LCDR3氨基酸序列的轻链可变区的序列,该组由以下组成:
QX1X2X3X4X5X6PX7T(SEQ ID NO:2201);其中X1是Q、H或E,其中X2是F或Y,其中X3是K、Y或I,其中X4是N、T、L、I、或M;其中X5是W、F、H或Y,其中X6不存在或是P;其中X7是W、N、Y、H或L;
QX1YX3X4X5PX6T(SEQ ID NO:2207),其中X1是Q或H,其中X2是D、A或G,其中X3是N或K;其中X4是L或I,并且其中X5是I或L;
QQFKNWPPT(SEQ ID NO:2222);
QHYDNLPIT(SEQ ID NO:2223);
LQAHGFPWT(SEQ ID NO:2224);
QQYDNLPLT(SEQ ID NO:2225)和
QFWPPWT(SEQ ID NO:2226)。
在多个实施例中,TREM-1抗体包含抗原结合结构域,该抗原结合结构域包含具有包含选自下组的HCDR1氨基酸序列的重链可变区的序列,该组由以下组成:
X1X2X3MX4(SEQ ID NO:2202),其中X1是A、R、T或S,其中X2是Y或N,其中X3是A或W,并且其中X4是S或N;
X1YDIN(SEQ ID NO:2208),其中X1是R或S;GYYX1H(SEQ ID NO:2723),其中X1是M或I;
AYAMS(SEQ ID NO:2227);
RYDIN(SEQ ID NO:2228);和
SYWMS(SEQ ID NO:2229)。
在多个实施例中,TREM-1抗体包含抗原结合结构域,该抗原结合结构域包含具有包含选自下组的HCDR2氨基酸序列的重链可变区的序列,该组由以下组成:
X1X2X3X4X5X6 X7 X8 X9YYX10 X11X12VKG(SEQ ID NO:2205),其中X1是T、E、或S,其中X2不存在或是M、V、或I,其中X3是S、R或K,其中X4是G或Q,其中X5是S、D或H,其中X6是G、S、L、或A,其中X7是S、G、或R,其中X8是T、S、P或E,其中X9是T或I,其中X10是A或V,其中X11是D或E,并且其中X12是S或A;
X1X2NPX3X4GX5X6GX7 X8 X9X10FX11X12(SEQ ID NO:2209),其中X1是W或R,其中X2是M或L,其中X3是N、Q、或K,其中X4是S、A、或R,其中X5是N、或Q,其中X6是S、A、或T,其中X7是S、Q、或Y,其中X8是V或T,其中X9是Q或K,其中X10是K或N,其中X11是R或Q,并且其中X12是G或D;
TSGSGSTTYYADSVKG(SEQ ID NO:2230);
WMNPNSGNSSVQKFRG(SEQ ID NO:2231);
NIKQDGSEEYYVDSVKG(SEQ ID NO:2232);和
TSGSGTYYADSVKG(SEQ ID NO:2669)。
在多个实施例中,TREM-1抗体包含抗原结合结构域,该抗原结合结构域包含具有包含选自下组的HCDR3氨基酸序列的重链可变区的序列,该组由以下组成:
X1X2X3X4X5X6 X7 F X8YYX9(SEQ ID NO:2203),其中X1是V、E、A或G,其中X2是A、F、Y或G,其中X3是G、S、Y或W,其中X4是S或R,其中X5不存在或是N,其中X6是F、S、Y、或不存在,其中X7是L或F或不存在,其中X8是D或E,并且其中X9是Y、H或S;
X1X2X3X4 X5X6 X7 X8 X9X10X11X12FX13X14(SEQ ID NO:2210);其中X1是G、L或R,其中X2是G、I、或R,其中X3是Y、R、I、G、或A,其中X4是T、S、Y、或V,其中X5是S或Y,其中X6是S、A、I、或R,其中X7是W、A、或S,其中X8不存在或是S,其中X9不存在或是F、W、或Y,其中X10是R、S、H、K、或E,其中X11是W、H、Y、或F,其中X12是Y、V、A、或S,其中X13是D或Q,并且其中X14是L、Y、I、或H;
VAGSNFLFDY(SEQ ID NO:2670);
GGYTSSWRWYFDL(SEQ ID NO:2671);
GGYTSSWSRWYFDL(SEQ ID NO:2672);和
DYGDSFDY(SEQ ID NO:2673)。
在多个实施例中,本文提供了分离的抗原结合蛋白,其中该抗原结合蛋白:
a.是抗体或抗体片段;
b.与具有SEQ ID NO:20中列出的氨基酸序列的人TREM-1结合;
c.包含轻链可变结构域,该轻链可变结构域包含:
i.包含氨基酸序列X1ASQSX2X3X4NLA(SEQ ID NO:2199)的轻链CDR1,其中X1是R或Q,其中X2是V或I,其中X3是N或S,并且其中X4是S、H、I、V或A;
ii.包含氨基酸序列GAX1X2RAT(SEQ ID NO:2200)的轻链CDR2,其中X1是S或Y,并且其中X2是T或I;和
iii.包含氨基酸序列QX1X2X3X4X5X6PX7T(SEQ ID NO:2201)的轻链CDR3;其中X1是Q、H或E,其中X2是F或Y,其中X3是K、Y或I,其中X4是N、T、L、I、或M;其中X5是W、F、H或Y,其中X6不存在或是P;其中X7是W、N、Y、H或L;并且
d.包含重链可变结构域,该重链可变结构域包含:
i.包含氨基酸序列X1X2X3MX4(SEQ ID NO:2202)的重链CDR1,其中X1是A、R、T或S,其中X2是Y或N,其中X3是A或W,并且其中X4是S或N;
ii.包含氨基酸序列X1X2X3X4X5X6 X7 X8 X9YYX10 X11X12VKG(SEQ ID NO:2205)的重链CDR2,其中X1是T、E、或S,其中X2不存在或是M、V、或I,其中X3是S、R或K,其中X4是G或Q,其中X5是S、D或H,其中X6是G、S、L、或A,其中X7是S、G、或R,其中X8是T、S、P或E,其中X9是T或I,其中X10是A或V,其中X11是D或E,并且其中X12是S或A;和
iii.包含氨基酸序列X1X2X3X4X5X6 X7 F X8YYX9(SEQ ID NO:2203)的重链CDR3,其中X1是V、E、A或G,其中X2是A、F、Y或G,其中X3是G、S、Y或W,其中X4是S或R,其中X5不存在或是N,其中X6是F、S、Y、或不存在,其中X7是L或F或不存在,其中X8是D或E,并且其中X9是Y、H或S。
在多个实施例中,抗原结合蛋白包含:
a.轻链可变结构域,该轻链可变结构域包含:
i.包含氨基酸序列RASQSVNSNLA(SEQ ID NO:2212)的轻链CDR1;
ii.包含氨基酸序列GASTRAT(SEQ ID NO:2219)的轻链CDR2;
iii.包含氨基酸序列QQFKNWPPT(SEQ ID NO:2222)的轻链CDR3;和
b.重链可变结构域,该重链可变结构域包含:
i.包含氨基酸序列AYAMS(SEQ ID NO:2227)的重链CDR1;
ii.包含氨基酸序列TSGSGSTTYYADSVKG(SEQ ID NO:2230)的重链CDR2;和
iii.包含氨基酸序列VAGSNFLFDY(SEQ ID NO:2670)的重链CDR3。
在多个实施例中,本披露提供了分离的抗原结合蛋白,其中该抗原结合蛋白:
a.是抗体或抗体片段;
b.与具有SEQ ID NO:20中列出的氨基酸序列的人TREM-1结合;
c.包含轻链可变结构域,该轻链可变结构域包含:
i.包含氨基酸序列QASX1DIX2X3X4LN(SEQ ID NO:2204)的轻链CDR1,其中X1是R或Q,其中X2是R、S、N或F,其中X3是K或N,并且其中X4是H、Y或D;
ii.包含氨基酸序列X1X2X3X4LET(SEQ ID NO:2206)的轻链CDR2,其中X1是D、G或H,其中X2是A、V或T,其中X3是S、A或Y,并且其中X4是T或N;
iii.包含氨基酸序列QX1YX3X4X5PX6T(SEQ ID NO:2207)的轻链CDR3,其中X1是Q或H,其中X2是D、A或G,其中X3是N或K;其中X4是L或I,并且其中X5是I或L;并且
d.包含重链可变结构域,该重链可变结构域包含:
i.包含氨基酸序列X1YDIN(SEQ ID NO:2208)的重链CDR1,其中X1是R或S;
ii.包含氨基酸序列X1X2NPX3X4GX5X6GX7 X8 X9X10FX11X12(SEQ ID NO:2209)的重链CDR2,其中X1是W或R,其中X2是M或L,其中X3是N、Q、或K,其中X4是S、A、或R,其中X5是N、或Q,其中X6是S、A、或T,其中X7是S、Q、或Y,其中X8是V或T,其中X9是Q或K,其中X10是K或N,其中X11是R或Q,并且其中X12是G或D;和
iii.包含氨基酸序列X1X2X3X4 X5X6 X7 X8 X9X10X11X12FX13X14(SEQ ID NO:2210)的重链CDR3;其中X1是G、L或R,其中X2是G、I、或R,其中X3是Y、R、I、G、或A,其中X4是T、S、Y、或V,其中X5是S或Y,其中X6是S、A、I、或R,其中X7是W、A、或S,其中X8不存在或是S,其中X9不存在或是F、W、或Y,并且其中X10是R、S、H、K、或E,其中X11是W、H、Y、或F,其中X12是Y、V、A、或S,其中X13是D或Q,并且其中X14是L、Y、I、或H。
在多个实施例中,抗原结合蛋白包含:
a.轻链可变结构域,该轻链可变结构域包含:
i.包含氨基酸序列QASQDIRKHLN(SEQ ID NO:2213)的轻链CDR1;
ii.包含氨基酸序列DASNLET(SEQ ID NO:2220)的轻链CDR2;和
iii.包含氨基酸序列QHYDNLPIT(SEQ ID NO:2223)的轻链CDR3;和
b.重链可变结构域,该重链可变结构域包含:
i.包含氨基酸序列RYDIN(SEQ ID NO:2228)的重链CDR1;
ii.包含氨基酸序列WMNPNSGNSSVQKFRG(SEQ ID NO:2231)的重链CDR2;和
iii.包含氨基酸序列GGYTSSWRWYFDL(SEQ ID NO:2671)或GGYTSSWSRWYFDL(SEQID NO:2672)的重链CDR3。
在多个实施例中,本披露提供了分离的抗原结合蛋白,其中该抗原结合蛋白:
a.是抗体或抗体片段;
b.与髓细胞1上表达的具有SEQ ID NO:20中列出的氨基酸序列的人触发受体(TREM-1)结合;
c.包含一组选自以下的CDR序列:
i)SEQ ID NO:30(LCDR1)、SEQ ID NO:31(LCDR2)、SEQ ID NO:32(LCDR3)、SEQ IDNO:36(HCDR1)、SEQ ID NO:37(HCDR2)和SEQ ID NO:38(HCDR3);
ii)SEQ ID NO:50(LCDR1)、SEQ ID NO:51(LCDR2)、SEQ ID NO:52(LCDR3)、SEQ IDNO:56(HCDR1)、SEQ ID NO:57(HCDR2)和SEQ ID NO:58(HCDR3);
iii)SEQ ID NO:70(LCDR1)、SEQ ID NO:71(LCDR2)、SEQ ID NO:72(LCDR3)、SEQID NO:76(HCDR1)、SEQ ID NO:77(HCDR2)和SEQ ID NO:78(HCDR3);
iv)SEQ ID NO:90(LCDR1)、SEQ ID NO:91(LCDR2)、SEQ ID NO:92(LCDR3)、SEQ IDNO:96(HCDR1)、SEQ ID NO:97(HCDR2)和SEQ ID NO:98(HCDR3);
v)SEQ ID NO:110(LCDR1)、SEQ ID NO:111(LCDR2)、SEQ ID NO:112(LCDR3)、SEQID NO:116(HCDR1)、SEQ ID NO:117(HCDR2)和SEQ ID NO:118(HCDR3);
vi)SEQ ID NO:130(LCDR1)、SEQ ID NO:131(LCDR2)、SEQ ID NO:132(LCDR3)、SEQID NO:136(HCDR1)、SEQ ID NO:137(HCDR2)和SEQ ID NO:138(HCDR3);
vii)SEQ ID NO:150(LCDR1)、SEQ ID NO:151(LCDR2)、SEQ ID NO:152(LCDR3)、SEQ ID NO:156(HCDR1)、SEQ ID NO:157(HCDR2)和SEQ ID NO:158(HCDR3);
viii)SEQ ID NO:170(LCDR1)、SEQ ID NO:171(LCDR2)、SEQ ID NO:172(LCDR3)、SEQ ID NO:176(HCDR1)、SEQ ID NO:177(HCDR2)和SEQ ID NO:178(HCDR3);
ix)SEQ ID NO:190(LCDR1)、SEQ ID NO:191(LCDR2)、SEQ ID NO:192(LCDR3)、SEQID NO:196(HCDR1)、SEQ ID NO:197(HCDR2)和SEQ ID NO:198(HCDR3);
x)SEQ ID NO:210(LCDR1)、SEQ ID NO:211(LCDR2)、SEQ ID NO:212(LCDR3)、SEQID NO:216(HCDR1)、SEQ ID NO:217(HCDR2)和SEQ ID NO:218(HCDR3);
xi)SEQ ID NO:230(LCDR1)、SEQ ID NO:231(LCDR2)、SEQ ID NO:232(LCDR3)、SEQID NO:236(HCDR1)、SEQ ID NO:237(HCDR2)和SEQ ID NO:238(HCDR3);
xii)SEQ ID NO:250(LCDR1)、SEQ ID NO:251(LCDR2)、SEQ ID NO:252(LCDR3)、SEQ ID NO:256(HCDR1)、SEQ ID NO:257(HCDR2)和SEQ ID NO:258(HCDR3);
xiii)SEQ ID NO:270(LCDR1)、SEQ ID NO:271(LCDR2)、SEQ ID NO:272(LCDR3)、SEQ ID NO:276(HCDR1)、SEQ ID NO:277(HCDR2)和SEQ ID NO:278(HCDR3);
xiv)SEQ ID NO:290(LCDR1)、SEQ ID NO:291(LCDR2)、SEQ ID NO:292(LCDR3)、SEQ ID NO:296(HCDR1)、SEQ ID NO:297(HCDR2)和SEQ ID NO:298(HCDR3);或
xv)SEQ ID NO:2190(LCDR1)、SEQ ID NO:2191(LCDR2)、SEQ ID NO:2192(LCDR3)、SEQ ID NO:2196(HCDR1)、SEQ ID NO:2197(HCDR2)和SEQ ID NO:2198(HCDR3)。
在多个实施例中,抗TREM-1抗原结合蛋白包含一组选自以下的CDR序列:
i)SEQ ID NO:30(LCDR1)、SEQ ID NO:31(LCDR2)、SEQ ID NO:32(LCDR3)、SEQ IDNO:36(HCDR1)、SEQ ID NO:37(HCDR2)和SEQ ID NO:38(HCDR3);
ii)SEQ ID NO:50(LCDR1)、SEQ ID NO:51(LCDR2)、SEQ ID NO:52(LCDR3)、SEQ IDNO:56(HCDR1)、SEQ ID NO:57(HCDR2)和SEQ ID NO:58(HCDR3);
iii)SEQ ID NO:70(LCDR1)、SEQ ID NO:71(LCDR2)、SEQ ID NO:72(LCDR3)、SEQID NO:76(HCDR1)、SEQ ID NO:77(HCDR2)和SEQ ID NO:78(HCDR3);
iv)SEQ ID NO:110(LCDR1)、SEQ ID NO:111(LCDR2)、SEQ ID NO:112(LCDR3)、SEQID NO:116(HCDR1)、SEQ ID NO:117(HCDR2)和SEQ ID NO:118(HCDR3);
v)SEQ ID NO:150(LCDR1)、SEQ ID NO:151(LCDR2)、SEQ ID NO:152(LCDR3)、SEQID NO:156(HCDR1)、SEQ ID NO:157(HCDR2)和SEQ ID NO:158(HCDR3);
vi)SEQ ID NO:170(LCDR1)、SEQ ID NO:171(LCDR2)、SEQ ID NO:172(LCDR3)、SEQID NO:176(HCDR1)、SEQ ID NO:177(HCDR2)和SEQ ID NO:178(HCDR3);或
vii)SEQ ID NO:290(LCDR1)、SEQ ID NO:291(LCDR2)、SEQ ID NO:292(LCDR3)、SEQ ID NO:296(HCDR1)、SEQ ID NO:297(HCDR2)和SEQ ID NO:298(HCDR3)。
在多个实施例中,抗TREM-1抗原结合蛋白包含一组选自以下的CDR序列:SEQ IDNO:50(LCDR1)、SEQ ID NO:51(LCDR2)、SEQ ID NO:52(LCDR3)、SEQ ID NO:56(HCDR1)、SEQID NO:57(HCDR2)和SEQ ID NO:58(HCDR3);或SEQ ID NO:110(LCDR1)、SEQ ID NO:111(LCDR2)、SEQ ID NO:112(LCDR3)、SEQ ID NO:116(HCDR1)、SEQ ID NO:117(HCDR2)和SEQID NO:118(HCDR3)。
在多个实施例中,抗TREM-1抗原结合蛋白或抗原结合蛋白的抗TREM1抗原结合部分包含:
a.轻链可变结构域,其包含选自下组的氨基酸序列,该组由以下组成:
i.与选自SEQ ID NO:41、61、81、101、121、141、161、181、201、221、241、261、281、301和2185的氨基酸序列具有至少80%同一性的序列;
ii.由与选自SEQ ID NO:39、59、79、99、119、139、159、179、199、219、239、259、279、299和2183的核酸序列具有至少80%同一性的多核苷酸序列编码的序列;
iii.由在中等严格条件下与由选自SEQ ID NO:39、59、79、99、119、139、159、179、199、219、239、259、279、299和2183的核酸序列组成的多核苷酸的互补序列杂交的多核苷酸编码的序列;和
b.重链可变结构域,其包含选自下组的氨基酸序列,该组由以下组成:
i.与选自SEQ ID NO:42、62、82、102、122、142、162、182、202、222、242、262、282、302和2186的氨基酸序列具有至少80%同一性的序列;
ii.由与选自SEQ ID NO:40、60、80、100、120、140、160、180、200、220、240、260、280、300和2184的氨基酸序列具有至少80%同一性的多核苷酸序列编码的序列;
iii.由在中等严格条件下与由选自SEQ ID NO:40、60、80、100、120、140、160、180、200、220、240、260、280、300和2184的核酸序列组成的多核苷酸互补序列杂交的多核苷酸编码的序列。
在多个实施例中,抗TREM-1抗原结合蛋白或抗原结合蛋白的抗TREM1抗原结合部分包含:
a.轻链可变结构域,其包含选自下组的氨基酸序列,该组由以下组成:
i.与选自SEQ ID NO:41、61、81、121、161、181、和301的氨基酸序列具有至少80%同一性的序列;
ii.由与选自SEQ ID NO:39、59、79、119、159、179、和299的核酸序列具有至少80%同一性的多核苷酸序列编码的序列;
iii.由在中等严格条件下与由选自SEQ ID NO:39、59、79、119、159、179、和299的核酸序列组成的多核苷酸的互补序列杂交的多核苷酸编码的序列;和
b.重链可变结构域,其包含选自下组的氨基酸序列,该组由以下组成:
i.与选自SEQ ID NO:42、62、82、122、162、182、和302的氨基酸序列具有至少80%同一性的序列;
ii.由与选自SEQ ID NO:40、60、80、120、160、180、和300的氨基酸序列具有至少80%同一性的多核苷酸序列编码的序列;
iii.由在中等严格条件下与由选自SEQ ID NO:40、60、80、120、160、180、和300的核酸序列组成的多核苷酸的互补序列杂交的多核苷酸编码的序列。
在多个实施例中,抗TREM-1抗原结合蛋白或抗原结合蛋白的抗TREM1抗原结合部分包含:
a.轻链可变结构域,其包含选自下组的氨基酸序列,该组由以下组成:
i.与选自SEQ ID NO:61和121的氨基酸序列具有至少80%同一性的序列;
ii.由与选自SEQ ID NO:59和119的核酸序列具有至少80%同一性的多核苷酸序列编码的序列;
iii.由在中等严格条件下与由选自SEQ ID NO:59和119的核酸序列组成的多核苷酸的互补序列杂交的多核苷酸编码的序列;和
b.重链可变结构域,其包含选自下组的氨基酸序列,该组由以下组成:
i.与选自SEQ ID NO:62和122的氨基酸序列具有至少80%同一性的序列;
ii.由与选自SEQ ID NO:60和120的氨基酸序列具有至少80%同一性的多核苷酸序列编码的序列;
iii.由在中等严格条件下与由选自SEQ ID NO:60和120的核酸序列组成的多核苷酸的互补序列杂交的多核苷酸编码的序列。
在多个实施例中,抗TREM-1抗原结合蛋白或抗原结合蛋白的抗TREM1抗原结合部分包含:
i)SEQ ID NO:41中列出的轻链可变结构域和SEQ ID NO:42中列出的重链可变结构域;
ii)SEQ ID NO:61中列出的轻链可变结构域和SEQ ID NO:62中列出的重链可变结构域;
iii)SEQ ID NO:81中列出的轻链可变结构域和SEQ ID NO:82中列出的重链可变结构域;
iv)SEQ ID NO:101中列出的轻链可变结构域和SEQ ID NO:102中列出的重链可变结构域;
v)SEQ ID NO:121中列出的轻链可变结构域和SEQ ID NO:122中列出的重链可变结构域;
vi)SEQ ID NO:161中列出的轻链可变结构域和SEQ ID NO:162中列出的重链可变结构域;
vii)SEQ ID NO:181中列出的轻链可变结构域和SEQ ID NO:182中列出的重链可变结构域;
viii)SEQ ID NO:201中列出的轻链可变结构域和SEQ ID NO:202中列出的重链可变结构域;
x)SEQ ID NO:221中列出的轻链可变结构域和SEQ ID NO:222中列出的重链可变结构域;
xi)SEQ ID NO:241中列出的轻链可变结构域和SEQ ID NO:242中列出的重链可变结构域;
xii)SEQ ID NO:261中列出的轻链可变结构域和SEQ ID NO:262中列出的重链可变结构域;
xiii)SEQ ID NO:281中列出的轻链可变结构域和SEQ ID NO:282中列出的重链可变结构域;
xiv)SEQ ID NO:301中列出的轻链可变结构域和SEQ ID NO:302中列出的重链可变结构域;或
xv)SEQ ID NO:2185中列出的轻链可变结构域和SEQ ID NO:2186中列出的重链可变结构域。
在多个实施例中,抗TREM-1抗原结合蛋白或抗原结合蛋白的抗TREM1抗原结合部分包含:
i)SEQ ID NO:41中列出的轻链可变结构域和SEQ ID NO:42中列出的重链可变结构域;
ii)SEQ ID NO:61中列出的轻链可变结构域和SEQ ID NO:62中列出的重链可变结构域;
iii)SEQ ID NO:81中列出的轻链可变结构域和SEQ ID NO:82中列出的重链可变结构域;
iv)SEQ ID NO:121中列出的轻链可变结构域和SEQ ID NO:122中列出的重链可变结构域;
v)SEQ ID NO:161中列出的轻链可变结构域和SEQ ID NO:162中列出的重链可变结构域;
vi)SEQ ID NO:181中列出的轻链可变结构域和SEQ ID NO:182中列出的重链可变结构域;或
vii)SEQ ID NO:301中列出的轻链可变结构域和SEQ ID NO:302中列出的重链可变结构域。
在多个实施例中,抗TREM-1抗原结合蛋白或抗原结合蛋白的抗TREM1抗原结合部分包含:SEQ ID NO:61中列出的轻链可变结构域和SEQ ID NO:62中列出的重链可变结构域;或SEQ ID NO:121中列出的轻链可变结构域和SEQ ID NO:122中列出的重链可变结构域。
在多个实施例中,氨基酸序列可与SEQ ID NO:42、62、82、102、122、142、162、182、202、222、242、262、282、302和2186,以及SEQ ID NO:41、61、81、101、121、141、161、181、201、221、241、261、281、301和2185具有80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%同一性。
在多个实施例中,抗原结合蛋白包含与选自SEQ ID NO:42、62、82、102、122、142、162、182、202、222、242、262、282、302和2186的重链可变区氨基酸序列具有至少90%同一性的氨基酸序列。在多个实施例中,抗原结合蛋白包含与SEQ ID NO:41、61、81、101、121、141、161、181、201、221、241、261、281、301和2185中列出的轻链可变区氨基酸序列具有至少90%同一性的氨基酸序列。
在多个实施例中,抗原结合蛋白包含与选自SEQ ID NO:42、62、82、122、162、182、和302的重链可变区氨基酸序列具有至少90%同一性的氨基酸序列。在多个实施例中,抗原结合蛋白包含与选自SEQ ID NO:41、61、81、121、161、181、和301的轻链可变区氨基酸序列具有至少90%同一性的氨基酸序列。
在多个实施例中,抗原结合蛋白包含与选自SEQ ID NO:62和122的重链可变区氨基酸序列具有至少90%同一性的氨基酸序列。在多个实施例中,抗原结合蛋白包含与选自SEQ ID NO:61和121的轻链可变区氨基酸序列具有至少90%同一性的氨基酸序列。
在多个实施例中,抗抗原结合蛋白的一个或多个重链框架氨基酸被来自另一人抗体氨基酸序列的相应的一个或多个氨基酸替代。在多个实施例中,抗原结合蛋白的一个或多个轻链框架氨基酸被来自另一人抗体氨基酸序列的相应的一个或多个氨基酸替代。
在一些情况下,本文披露的序列可以含有可用于重组体产生的N末端信号序列。本文考虑了缺乏信号序列的抗TREM-1抗体或抗原结合蛋白的序列。示例性信号序列包括MDMRVPAQLLGLLLLWLRGARC(SEQ ID NO:2674);MAWALLLLTLLTQGTGSWASYEL(SEQ ID NO:2675),以及编码此类信号序列的核酸。
在多个实施例中,抗TREM-1抗原结合蛋白进一步包含连接至所述轻链可变区的人轻链恒定区。
在多个实施例中,重链恒定区选自IgG、IgM、IgA、IgD、IgE的重链恒定区、其片段、其组合、以及其修饰,这些修饰中一个至十个重链框架氨基酸被来自另一人抗体氨基酸序列的相应的一个或多个氨基酸替代。
在多个实施例中,本文所述的抗TREM-1抗原结合蛋白抑制TREM-1配体与TREM-1的结合。
还考虑了抗原结合蛋白,其与如本文所述的抗TREM-1抗原结合蛋白竞争与具有SEQ ID NO:20的序列的人TREM-1蛋白结合。
在多个实施例中,抗原结合蛋白选自由以下组成的组:人抗体、人源化抗体、嵌合抗体、单克隆抗体、重组抗体、Fab、F(ab’)2、Fab2、单价IgG、scFv、scFv-Fc、IgG1抗体、IgG2抗体、IgG3抗体、和IgG4抗体。在多个实施例中,抗TREM-1抗原结合蛋白是IgG2抗体。在多个实施例中,抗TREM-1抗原结合蛋白是IgG1抗体。在多个实施例中,IgG1抗体是IGg1z或IgG1z-SEFL2抗体。在多个实施例中,抗原结合蛋白是单价IgG。
在多个实施例中,抗原结合蛋白是人抗体。
还提供了包含编码如本文所述的抗TREM-1抗原结合蛋白的重链的核苷酸序列的分离的核酸分子、包含编码如本文所述的抗TREM-1抗原结合蛋白的轻链的核苷酸序列的分离的核酸分子、以及包含编码如本文所述的抗TREM-1抗原结合蛋白的重链和轻链的核苷酸序列的分离的核酸分子。
在多个实施例中,抗原结合蛋白包含与选自SEQ ID NO:40、60、80、100、120、140、160、180、200、220、240、260、280、和300和2184的重链可变区多核苷酸序列具有至少90%同一性的氨基酸序列。在多个实施例中,抗原结合蛋白包含与SEQ ID NO:39、59、79、99、119、139、159、179、199、219、239、259、279、299和2183中列出的轻链可变区多核苷酸序列具有至少90%同一性的氨基酸序列。
在多个实施例中,抗原结合蛋白包含与选自SEQ ID NO:40、60、80、120、160、180、和300的重链可变区多核苷酸序列具有至少90%同一性的氨基酸序列。在多个实施例中,抗原结合蛋白包含与选自SEQ ID NO:39、59、79、119、159、179、和299的轻链可变区多核苷酸序列具有至少90%同一性的氨基酸序列。
在多个实施例中,抗原结合蛋白包含与选自SEQ ID NO:60和120的重链可变区多核苷酸序列具有至少90%同一性的氨基酸序列。在多个实施例中,抗原结合蛋白包含与选自SEQ ID NO:59和119的轻链可变区多核苷酸序列具有至少90%同一性的氨基酸序列。
进一步考虑了表达载体,其包含可操作地连接到表达控制序列的如本文所述的抗TREM-1抗原结合蛋白重链和/或轻链的核酸分子。
本披露提供了重组宿主细胞,该重组宿主细胞包含含有编码如本文所述的抗TREM-1抗原结合蛋白或抗体的重链的核苷酸序列的核酸分子;或编码如本文所述的轻链或抗TREM-1抗体的核酸分子;或编码如本文所述的抗TREM-1抗体的重链和轻链核酸分子的核酸分子;或包含编码如本文所述的抗TREM-1抗体的重链和/或轻链的核酸分子的载体。在多个实施例中,宿主细胞是哺乳动物细胞。在多个实施例中,宿主细胞是CHO细胞。
进一步提供了使用宿主细胞产生抗原结合蛋白的方法以及通过该方法产生的抗原结合蛋白,该方法包括培养宿主细胞并回收所述抗原结合蛋白。
还提供了包含如本文所述的抗TREM-1抗原结合蛋白和药学上可接受的载剂的无菌药物组合物。
进一步考虑了抗原结合蛋白,其包含抗原结合部分和一个或两个IL-10部分,其中:
a.该抗原结合部分是抗体或抗体片段,
b.每个IL-10部分独立地是单价或二价,
c.每个IL-10部分独立地选自具有与SEQ ID NO:2具有90%同一性的序列的一种或多种人IL-10突变蛋白,并且
d.至少一个IL-10部分与该抗原结合部分共价结合。
在多个实施例中,至少一个IL-10部分与抗原结合部分的C末端融合。在多个实施例中,至少一个IL-10部分与抗原结合部分的N末端融合。在多个实施例中,至少一个IL-10部分与抗原结合部分的N末端和C末端融合。在多个实施例中,IL-10部分在抗原结合部分的内部位点处融合。在多个实施例中,至少一个IL-10部分与抗原结合部分的重链和/或轻链融合。在多个实施例中,重链和/或轻链是修饰的或工程化的重链或轻链。
还提供了抗原结合蛋白,其包含:
(a)具有式A-L-M或M-L-A的多肽序列,其中
i)A是与SEQ ID NO:20中列出的TREM-1蛋白结合的IgG抗体的免疫球蛋白重链,
ii)L是包含4至20个氨基酸的接头肽,并且
iii)M是与SEQ ID NO:2中列出的wt IL-10具有至少90%序列同一性的IL-10突变蛋白;和
(b)结合SEQ ID NO:20中列出的TREM-1蛋白的IgG抗体的免疫球蛋白轻链,
其中(a)的免疫球蛋白重链和(b)的免疫球蛋白轻链形成结合TREM-1的IgG抗体部分,其中该蛋白质包含(a)的多肽的一个或两个分子以及(b)的轻链的一个或两个分子,任选地其中(a)的仅1个多肽包含M部分。
在多个实施例中,与wt IL-10相比,抗原结合蛋白减少了髓细胞中TNF-α产生方面的抑制,降低了CD8+T细胞刺激方面的水平,和/或降低了B细胞刺激方面的水平。
在抗原结合蛋白的多个实施例中:
a.抗原结合部分是抗体,并且
b.IL-10部分与该抗体的每条重链融合。
在抗原结合蛋白的多个实施例中,每个IL-10部分是单体。在多个实施例中,抗原结合蛋白包含两种不同的突变蛋白单体。在多个实施例中,抗原结合蛋白包含两种相同的突变蛋白单体。
在抗原结合蛋白的多个实施例中:每个IL-10部分包含与SEQ ID NO:2中列出的氨基酸序列具有至少90%同一性的氨基酸序列,并且每个IL-10部分独立地包含选自以下的至少一个突变:螺旋环AB、螺旋环CD、螺旋环DE、螺旋A、螺旋B、螺旋C、螺旋D、螺旋E和/或螺旋F中的突变。
在抗原结合蛋白的多个实施例中,至少一个IL-10部分包含螺旋A中的至少一个突变。在抗原结合蛋白的多个实施例中,至少一个IL-10部分包含螺旋F中的至少一个突变。在抗原结合蛋白的多个实施例中,至少一个IL-10部分包含螺旋环AB中的至少一个突变。
在多个实施例中,例如与wt IL-10相比,人类受试者中抗TREM-1/IL-10突变蛋白抗原结合蛋白缺乏CD8+T细胞刺激和/或B细胞刺激。
在多个实施例中,与wt IL-10相比,IL-10突变蛋白减少了髓细胞中TNF-α产生方面的抑制,降低了CD8+T细胞刺激方面的水平,和/或降低了B细胞刺激方面的水平。
在多个实施例中,IL-10突变蛋白抗原结合蛋白(例如抗TREM-1/IL-10突变蛋白抗原结合蛋白)抑制髓细胞中TNF-α产生。在多个实施例中,IL-10突变蛋白抗原结合蛋白(例如抗TREM-1/IL-10突变蛋白抗原结合蛋白)抑制髓细胞中TNF-α产生,但仍缺乏CD8+T细胞和B细胞激活。
在多个实施例中,具有与针对CD8+细胞和/或B细胞上细胞表面蛋白的抗原结合配偶体融合的IL-10突变蛋白的抗原结合蛋白增强了人类受试者中CD8+T细胞刺激方面的水平和/或B细胞刺激方面的水平。
在抗原结合蛋白的多个实施例中,每个IL-10突变蛋白独立地包含SEQ ID NO:2的残基N10、H14、F15、P20、M22、L23、R24、R27、D28、K34、T35、Q38、M39、K40、D41、Q42、L43、D44、N45、L46、L47、L48、K49、F56、K57、Y59、L60、Q63、E67、Q70、M77、Q79、N82、Q83、D84、P85、D86、I87、A89、H90、S93、T100、L103、H109、R110、L112、E115、N116、A127、K130、I136、Y137、K138、S141、E142、D144、I145、E151、M154、M156、K157、N160中的一个或多个中的突变,和/或在螺旋D和螺旋E之间添加4-8个氨基酸。
在多个实施例中,每个IL-10突变蛋白独立地包含选自下组的一个或多个突变,该组由以下组成:SEQ ID NO:2的R27L、K34D、D41G、L46K、Q38E、Q38R、Q38D、K138L、K138D、或I87A,任选地包含在螺旋D和螺旋E之间添加氨基酸。在多个实施例中,每个IL-10突变蛋白独立地包含选自下组的一个或多个突变,该组由以下组成:SEQ ID NO:2的N10Q、N10I、N10KR27L、K34D、D41G、L46K、Q38E、Q38R、Q38D、K138L、K138D、I87A、H14Q、F15Y、M22V、K49T、K49S、F56Y、K57N、Y59T、L60Q、Q63E、Q63L、E67C、Q70E、Q70K、M77R、M77V、Q79R、Q79C、D84R、A89P、H90E、H90Q、S93E、S93Q、T100R、L103E、H109D、R110P、R110Q、L112V、E115K、N116D、N116Q、A127M、K130Q、I136C、Y137C、M154V、M156C、K157N、或N160D,任选地包含在螺旋D和螺旋E之间添加氨基酸。
在多个实施例中,每个IL-10突变蛋白独立地包含选自下组的一个或多个突变,该组由以下组成:SEQ ID NO:2的R27L、K34D、D41G、L46K、Q38E、Q38R、Q38D、K138L、K138D、或I87A,任选地包含在螺旋D和螺旋E之间添加六个氨基酸。在多个实施例中,螺旋D和螺旋E之间的氨基酸是GGGSGG(SEQ ID NO:2676)。在多个实施例中,每个IL-10突变蛋白独立地包含选自下组的一个或多个突变,该组由以下组成:SEQ ID NO:2的N10Q、N10I、N10K、R27L、K34D、D41G、L46K、Q38E、Q38R、Q38D、K138L、K138D、I87A、H14Q、F15Y、M22V、K49T、K49S、F56Y、K57N、Y59T、L60Q、Q63E、Q63L、E67C、Q70E、Q70K、M77R、M77V、Q79R、Q79C、D84R、A89P、H90E、H90Q、S93E、S93Q、T100R、L103E、H109D、R110P、R110Q、L112V、E115K、N116D、N116Q、A127M、K130Q、I136C、Y137C、M154V、M156C、K157N、或N160D,任选地包含在螺旋D和螺旋E之间添加六个氨基酸。在多个实施例中,螺旋D和螺旋E之间的氨基酸是GGGSGG(SEQ ID NO:2676)。
在抗原结合蛋白的多个实施例中,每个IL-10突变蛋白与SEQ ID NO:2中列出的氨基酸序列具有至少95%同一性。在多个实施例中,IL-10突变蛋白的氨基酸序列在SEQ IDNO:3-10中列出。在多个实施例中,IL-10突变蛋白的氨基酸序列在SEQ ID NO:3-10以及SEQID NO:2138、2140、2142、2144、2146、2148、2150、2152、2154、2156、2158、2160、2162、2164、2166、2168、2170、2172、2174、2176、2178、2180、2182、2360、2362、2364、2366、2368、2370、2372、2374、2376、2378、2380、2382、2384、2386、2388、2390、2392、2394、2396、2398、2400、2402、2404、2406、2408、2410、2412、2414、2416、2418、2420、2422、2424、2426、2428、2430、2432、2434、2436、2438、2440、2442、2444、2446、2448、2450、2452、2454、2456、2458、2460、2462、2464、2466、2468、2470、2472、2474、2476、2478、2480、2482、2484、2486、2488、2490、2492、2494、2496、2500、2502、2504、2506、2508、2510、2512、2514、2516、2518、2520、2522、2524、2526、2528、2530、2532、2534、2536、2538、2540和2777-2791中列出。
在多个实施例中,抗原结合蛋白包含与抗原结合部分的至少一个C末端融合的至少一个接头,并且IL-10部分与每个接头的C末端共价结合。在多个实施例中,接头为4至18个氨基酸长。在多个实施例中,接头为六个氨基酸长。在多个实施例中,接头是3聚体、4聚体、5聚体、6聚体、7聚体或8聚体肽。在多个实施例中,接头包含GS残基。
在多个实施例中,抗原结合蛋白包含“掩埋的”IL-10突变蛋白。在多个实施例中,抗原结合蛋白包含:(a)抗TREM1结合部分的Fab部分,(b)与TREM1-结合部分的Fab部分的C末端融合的至少一个G4接头,(c)IL-10部分与每个接头的C末端共价结合;另一个G4接头与IL10部分的C末端融合;Fc区与该第二个G4接头的C末端共价连接。具体实施方式中进一步描述了所考虑的另外的接头。
在多个实施例中,抗原结合蛋白中的抗原结合部分进一步包含连接至所述抗原结合蛋白的抗体部分的重链可变区的人重链恒定区。在多个实施例中,抗原结合蛋白进一步包含连接至所述抗原结合蛋白的抗体部分的轻链可变区的人轻链恒定区。
在抗原结合蛋白的多个实施例中,抗原结合部分选自由以下组成的组:人抗体、人源化抗体、嵌合抗体、单克隆抗体、重组抗体、Fab、F(ab’)2、Fab2、单价IgG、scFv、scFv-Fc、IgG1抗体、IgG2抗体、IgG3抗体、和IgG4抗体。在多个实施例中,抗原结合部分是IgG。在多个实施例中,抗原结合部分是IgG2抗体。在多个实施例中,抗原结合部分是IgG1抗体。在抗原结合蛋白的多个实施例中,抗体是IgG1z或IgG1z-SEFL2抗体。在多个实施例中,抗原结合部分是单价IgG。在多个实施例中,抗原结合部分的重链恒定区选自IgG、IgM、IgA、IgD、IgE的重链恒定区、其片段、其组合、以及其修饰,这些修饰中一个至十个重链框架氨基酸被来自另一人抗体恒定区的相应的一个或多个氨基酸替代。
在抗原结合蛋白的多个实施例中,抗原结合部分与具有SEQ ID NO:22中列出的氨基酸序列的人PD-1结合。在多个实施例中,抗原结合部分与具有SEQ ID NO:20中列出的氨基酸序列的人TREM-1结合。在多个实施例中,抗原结合部分以至少10-8M的结合亲和力与人TREM-1结合。在多个实施例中,抗原结合部分以至少10-8M至10-15M或10-8M至10-12M,或10-8M、10-9M、10-10M、10-11M、10-12M、10-13M、10-14M、或10-15M的结合亲和力结合其抗原。
在抗原结合蛋白的多个实施例中,抗TREM-1抗原结合部分包含:
a.轻链可变结构域,其包含:
i.轻链CDR1,其包含选自SEQ ID NO:30、50、70、90、110、130、150、170、190、210、230、250、270、290和2190的氨基酸序列;
ii.轻链CDR2序列,其包含选自SEQ ID NO:31、51、71、91、111、131、151、171、191、211、231、251、271、291和2191的氨基酸序列;
iii.轻链CDR3序列,其包含选自SEQ ID NO:32、52、72、92、112、132、152、172、192、212、232、252、272、292和2192的氨基酸序列;和
b.包含重链可变结构域,该重链可变结构域包含:
i.重链CDR1,其包含选自SEQ ID NO:36、56、76、96、116、136、156、176、196、216、236、256、276、296和2196的氨基酸序列;
ii.重链CDR2序列,其包含选自SEQ ID NO:37、57、77、97、117、137、157、177、197、217、237、257、277、297和2197的氨基酸序列;和
iii.重链CDR3序列,其包含选自SEQ ID NO:38、58、78、98、118、138、158、178、198、218、238、258、278、298和2198的氨基酸序列。
在抗原结合蛋白的多个实施例中,抗TREM-1抗原结合部分包含:
a.轻链CDR1序列在SEQ ID NO:30、50、70、110、150、170、或290中列出;
b.轻链CDR2序列在SEQ ID NO:31、51、71、111、151、171、或291中列出;
c.轻链CDR3序列在SEQ ID NO:32、52、72、112、152、172、或292中列出;
d.重链CDR1序列在SEQ ID NO:36、56、76、116、156、176、或296中列出;
e.重链CDR2序列在SEQ ID NO:37、57、77、117、157、177、或297中列出;和
f.重链CDR3序列在SEQ ID NO:38、58、78、118、158、178、或298中列出。
在抗原结合蛋白的多个实施例中,抗TREM-1抗原结合部分包含:
a.轻链CDR1序列在SEQ ID NO:50或110中列出;
b.轻链CDR2序列在SEQ ID NO:51或111中列出;
c.轻链CDR3序列在SEQ ID NO:52或112中列出;
d.重链CDR1序列在SEQ ID NO:56或116中列出;
e.重链CDR2序列在SEQ ID NO:57或117中列出;和
f.重链CDR3序列在SEQ ID NO:58或118中列出。
在多个实施例中,抗TREM-1抗原结合蛋白或抗原结合蛋白的抗TREM1抗原结合部分包含选自以下的一组CDR序列:
i)SEQ ID NO:30(LCDR1)、SEQ ID NO:31(LCDR2)、SEQ ID NO:32(LCDR3)、SEQ IDNO:36(HCDR1)、SEQ ID NO:37(HCDR2)和SEQ ID NO:38(HCDR3);
ii)SEQ ID NO:50(LCDR1)、SEQ ID NO:51(LCDR2)、SEQ ID NO:52(LCDR3)、SEQ IDNO:56(HCDR1)、SEQ ID NO:57(HCDR2)和SEQ ID NO:58(HCDR3);
iii)SEQ ID NO:70(LCDR1)、SEQ ID NO:71(LCDR2)、SEQ ID NO:72(LCDR3)、SEQID NO:76(HCDR1)、SEQ ID NO:77(HCDR2)和SEQ ID NO:78(HCDR3);
iv)SEQ ID NO:90(LCDR1)、SEQ ID NO:91(LCDR2)、SEQ ID NO:92(LCDR3)、SEQ IDNO:96(HCDR1)、SEQ ID NO:97(HCDR2)和SEQ ID NO:98(HCDR3);
v)SEQ ID NO:110(LCDR1)、SEQ ID NO:111(LCDR2)、SEQ ID NO:112(LCDR3)、SEQID NO:116(HCDR1)、SEQ ID NO:117(HCDR2)和SEQ ID NO:118(HCDR3);
vi)SEQ ID NO:130(LCDR1)、SEQ ID NO:131(LCDR2)、SEQ ID NO:132(LCDR3)、SEQID NO:136(HCDR1)、SEQ ID NO:137(HCDR2)和SEQ ID NO:138(HCDR3);
vii)SEQ ID NO:150(LCDR1)、SEQ ID NO:151(LCDR2)、SEQ ID NO:152(LCDR3)、SEQ ID NO:156(HCDR1)、SEQ ID NO:157(HCDR2)和SEQ ID NO:158(HCDR3);
viii)SEQ ID NO:170(LCDR1)、SEQ ID NO:171(LCDR2)、SEQ ID NO:172(LCDR3)、SEQ ID NO:176(HCDR1)、SEQ ID NO:177(HCDR2)和SEQ ID NO:178(HCDR3);
ix)SEQ ID NO:190(LCDR1)、SEQ ID NO:191(LCDR2)、SEQ ID NO:192(LCDR3)、SEQID NO:196(HCDR1)、SEQ ID NO:197(HCDR2)和SEQ ID NO:198(HCDR3);
x)SEQ ID NO:210(LCDR1)、SEQ ID NO:211(LCDR2)、SEQ ID NO:212(LCDR3)、SEQID NO:216(HCDR1)、SEQ ID NO:217(HCDR2)和SEQ ID NO:218(HCDR3);
xi)SEQ ID NO:230(LCDR1)、SEQ ID NO:231(LCDR2)、SEQ ID NO:232(LCDR3)、SEQID NO:236(HCDR1)、SEQ ID NO:237(HCDR2)和SEQ ID NO:238(HCDR3);
xii)SEQ ID NO:250(LCDR1)、SEQ ID NO:251(LCDR2)、SEQ ID NO:252(LCDR3)、SEQ ID NO:256(HCDR1)、SEQ ID NO:257(HCDR2)和SEQ ID NO:258(HCDR3);
xiii)SEQ ID NO:270(LCDR1)、SEQ ID NO:271(LCDR2)、SEQ ID NO:272(LCDR3)、SEQ ID NO:276(HCDR1)、SEQ ID NO:277(HCDR2)和SEQ ID NO:278(HCDR3);
xiv)SEQ ID NO:290(LCDR1)、SEQ ID NO:291(LCDR2)、SEQ ID NO:292(LCDR3)、SEQ ID NO:296(HCDR1)、SEQ ID NO:297(HCDR2)和SEQ ID NO:298(HCDR3);和
xv)SEQ ID NO:2190(LCDR1)、SEQ ID NO:2191(LCDR2)、SEQ ID NO:2192(LCDR3)、SEQ ID NO:2196(HCDR1)、SEQ ID NO:2197(HCDR2)和SEQ ID NO:2198(HCDR3)。
在多个实施例中,抗TREM-1抗原结合蛋白或抗原结合蛋白的抗TREM1抗原结合部分包含选自以下的一组CDR序列:
i)SEQ ID NO:30(LCDR1)、SEQ ID NO:31(LCDR2)、SEQ ID NO:32(LCDR3)、SEQ IDNO:36(HCDR1)、SEQ ID NO:37(HCDR2)和SEQ ID NO:38(HCDR3);
ii)SEQ ID NO:50(LCDR1)、SEQ ID NO:51(LCDR2)、SEQ ID NO:52(LCDR3)、SEQ IDNO:56(HCDR1)、SEQ ID NO:57(HCDR2)和SEQ ID NO:58(HCDR3);
iii)SEQ ID NO:70(LCDR1)、SEQ ID NO:71(LCDR2)、SEQ ID NO:72(LCDR3)、SEQID NO:76(HCDR1)、SEQ ID NO:77(HCDR2)和SEQ ID NO:78(HCDR3);
iv)SEQ ID NO:110(LCDR1)、SEQ ID NO:111(LCDR2)、SEQ ID NO:112(LCDR3)、SEQID NO:116(HCDR1)、SEQ ID NO:117(HCDR2)和SEQ ID NO:118(HCDR3);
v)SEQ ID NO:150(LCDR1)、SEQ ID NO:151(LCDR2)、SEQ ID NO:152(LCDR3)、SEQID NO:156(HCDR1)、SEQ ID NO:157(HCDR2)和SEQ ID NO:158(HCDR3);
vi)SEQ ID NO:170(LCDR1)、SEQ ID NO:171(LCDR2)、SEQ ID NO:172(LCDR3)、SEQID NO:176(HCDR1)、SEQ ID NO:177(HCDR2)和SEQ ID NO:178(HCDR3);和
vii)SEQ ID NO:290(LCDR1)、SEQ ID NO:291(LCDR2)、SEQ ID NO:292(LCDR3)、SEQ ID NO:296(HCDR1)、SEQ ID NO:297(HCDR2)和SEQ ID NO:298(HCDR3)。
在多个实施例中,抗TREM-1抗原结合蛋白或抗原结合蛋白的抗TREM1抗原结合部分包含选自以下的一组CDR序列:SEQ ID NO:50(LCDR1)、SEQ ID NO:51(LCDR2)、SEQ IDNO:52(LCDR3)、SEQ ID NO:56(HCDR1)、SEQ ID NO:57(HCDR2)和SEQ ID NO:58(HCDR3);以及SEQ ID NO:150(LCDR1)、SEQ ID NO:151(LCDR2)、SEQ ID NO:152(LCDR3)、SEQ ID NO:156(HCDR1)、SEQ ID NO:157(HCDR2)和SEQ ID NO:158(HCDR3)。
在多个实施例中,抗TREM-1抗原结合蛋白或抗原结合蛋白的抗TREM1抗原结合部分包含:
a.轻链可变结构域,其包含选自下组的氨基酸序列,该组由以下组成:
i.与选自SEQ ID NO:41、61、81、101、121、141、161、181、201、221、241、261、281、301和2185的氨基酸序列具有至少80%同一性的序列;
ii.由与选自SEQ ID NO:39、59、79、99、119、139、159、179、199、219、239、259、279、299和2183的核酸序列具有至少80%同一性的多核苷酸序列编码的序列;
iii.由在中等严格条件下与由选自SEQ ID NO:39、59、79、99、119、139、159、179、199、219、239、259、279、299和2183的核酸序列组成的多核苷酸的互补序列杂交的多核苷酸编码的序列;和
b.重链可变结构域,其包含选自下组的氨基酸序列,该组由以下组成:
i.与选自SEQ ID NO:42、62、82、102、122、142、162、182、202、222、242、262、282、302和2186的氨基酸序列具有至少80%同一性的序列;
ii.由与选自SEQ ID NO:40、60、80、100、120、140、160、180、200、220、240、260、280、300和2184的氨基酸序列具有至少80%同一性的多核苷酸序列编码的序列;
iii.由在中等严格条件下与由选自SEQ ID NO:40、60、80、100、120、140、160、180、200、220、240、260、280、300和2184的核酸序列组成的多核苷酸的互补序列杂交的多核苷酸编码的序列。
在多个实施例中,抗TREM-1抗原结合蛋白或抗原结合蛋白的抗TREM1抗原结合部分包含:
a.轻链可变结构域,其包含选自下组的氨基酸序列,该组由以下组成:
i.与选自SEQ ID NO:41、61、81、121、161、181、和301的氨基酸序列具有至少80%同一性的序列;
ii.由与选自SEQ ID NO:39、59、79、119、159、179、和299的核酸序列具有至少80%同一性的多核苷酸序列编码的序列;
iii.由在中等严格条件下与由选自SEQ ID NO:39、59、79、119、159、179、和299的核酸序列组成的多核苷酸的互补序列杂交的多核苷酸编码的序列;和
b.重链可变结构域,其包含选自下组的氨基酸序列,该组由以下组成:
i.与选自SEQ ID NO:42、62、82、122、162、182、和302的氨基酸序列具有至少80%同一性的序列;
ii.由与选自SEQ ID NO:40、60、80、120、160、180、和300的氨基酸序列具有至少80%同一性的多核苷酸序列编码的序列;
iii.由在中等严格条件下与由选自SEQ ID NO:40、60、80、120、160、180、和300的核酸序列组成的多核苷酸的互补序列杂交的多核苷酸编码的序列。
在抗原结合蛋白的多个实施例中,抗TREM-1抗原结合部分包含:
a.轻链可变结构域,其包含选自下组的氨基酸序列,该组由以下组成:
i.与选自SEQ ID NO:61和121的氨基酸序列具有至少80%同一性的序列;
ii.由与选自SEQ ID NO:59和119的核酸序列具有至少80%同一性的多核苷酸序列编码的序列;
iii.由在中等严格条件下与由选自SEQ ID NO:59和119的核酸序列组成的多核苷酸的互补序列杂交的多核苷酸编码的序列;和
b.重链可变结构域,其包含选自下组的氨基酸序列,该组由以下组成:
i.与选自SEQ ID NO:62和122的氨基酸序列具有至少80%同一性的序列;
ii.由与选自SEQ ID NO:60和120的氨基酸序列具有至少80%同一性的多核苷酸序列编码的序列;
iii.由在中等严格条件下与由选自SEQ ID NO:60和120的核酸序列组成的多核苷酸的互补序列杂交的多核苷酸编码的序列。
在多个实施例中,氨基酸序列可与SEQ ID NO:41、61、81、101、121、141、161、181、201、221、241、261、281、301和2185,以及SEQ ID NO:42、62、82、102、122、142、162、182、202、222、242、262、282、302和2186具有80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%同一性。
在抗原结合蛋白的多个实施例中,抗原结合部分包含与选自SEQ ID NO:42、62、82、102、122、142、162、182、202、222、242、262、282、302和2186的重链可变区氨基酸序列具有至少90%同一性的氨基酸序列。
在抗原结合蛋白的多个实施例中,抗原结合部分包含与选自SEQ ID NO:41、61、81、101、121、141、161、181、201、221、241、261、281、301和2185的轻链可变区氨基酸序列具有至少90%同一性的氨基酸序列。
在多个实施例中,抗TREM-1抗原结合蛋白或抗原结合蛋白的抗TREM1抗原结合部分包含:
i)SEQ ID NO:41中列出的轻链可变结构域和SEQ ID NO:42中列出的重链可变结构域;
ii)SEQ ID NO:61中列出的轻链可变结构域和SEQ ID NO:62中列出的重链可变结构域;
iii)SEQ ID NO:81中列出的轻链可变结构域和SEQ ID NO:82中列出的重链可变结构域;
iv)SEQ ID NO:101中列出的轻链可变结构域和SEQ ID NO:102中列出的重链可变结构域;
v)SEQ ID NO:121中列出的轻链可变结构域和SEQ ID NO:122中列出的重链可变结构域;
vi)SEQ ID NO:141中列出的轻链可变结构域和SEQ ID NO:142中列出的重链可变结构域;
vii)SEQ ID NO:161中列出的轻链可变结构域和SEQ ID NO:162中列出的重链可变结构域;
viii)SEQ ID NO:181中列出的轻链可变结构域和SEQ ID NO:182中列出的重链可变结构域;
ix)SEQ ID NO:201中列出的轻链可变结构域和SEQ ID NO:202中列出的重链可变结构域;
x)SEQ ID NO:221中列出的轻链可变结构域和SEQ ID NO:222中列出的重链可变结构域;
xi)SEQ ID NO:241中列出的轻链可变结构域和SEQ ID NO:242中列出的重链可变结构域;
xii)SEQ ID NO:261中列出的轻链可变结构域和SEQ ID NO:262中列出的重链可变结构域;
xiii)SEQ ID NO:281中列出的轻链可变结构域和SEQ ID NO:282中列出的重链可变结构域;
xiv)SEQ ID NO:301中列出的轻链可变结构域和SEQ ID NO:302中列出的重链可变结构域;或
xv)SEQ ID NO:2185中列出的轻链可变结构域和SEQ ID NO:2186中列出的重链可变结构域。
在多个实施例中,抗TREM-1抗原结合蛋白或抗原结合蛋白的抗TREM1抗原结合部分包含:
i)SEQ ID NO:41中列出的轻链可变结构域和SEQ ID NO:42中列出的重链可变结构域;
ii)SEQ ID NO:61中列出的轻链可变结构域和SEQ ID NO:62中列出的重链可变结构域;
iii)SEQ ID NO:81中列出的轻链可变结构域和SEQ ID NO:82中列出的重链可变结构域;
iv)SEQ ID NO:121中列出的轻链可变结构域和SEQ ID NO:122中列出的重链可变结构域;
v)SEQ ID NO:161中列出的轻链可变结构域和SEQ ID NO:162中列出的重链可变结构域;
vi)SEQ ID NO:181中列出的轻链可变结构域和SEQ ID NO:182中列出的重链可变结构域;或
vii)SEQ ID NO:301中列出的轻链可变结构域和SEQ ID NO:302中列出的重链可变结构域。
在多个实施例中,抗TREM-1抗原结合蛋白或抗原结合蛋白的抗TREM1抗原结合部分包含:SEQ ID NO:61中列出的轻链可变结构域和SEQ ID NO:62中列出的重链可变结构域;或SEQ ID NO:121中列出的轻链可变结构域和SEQ ID NO:122中列出的重链可变结构域。
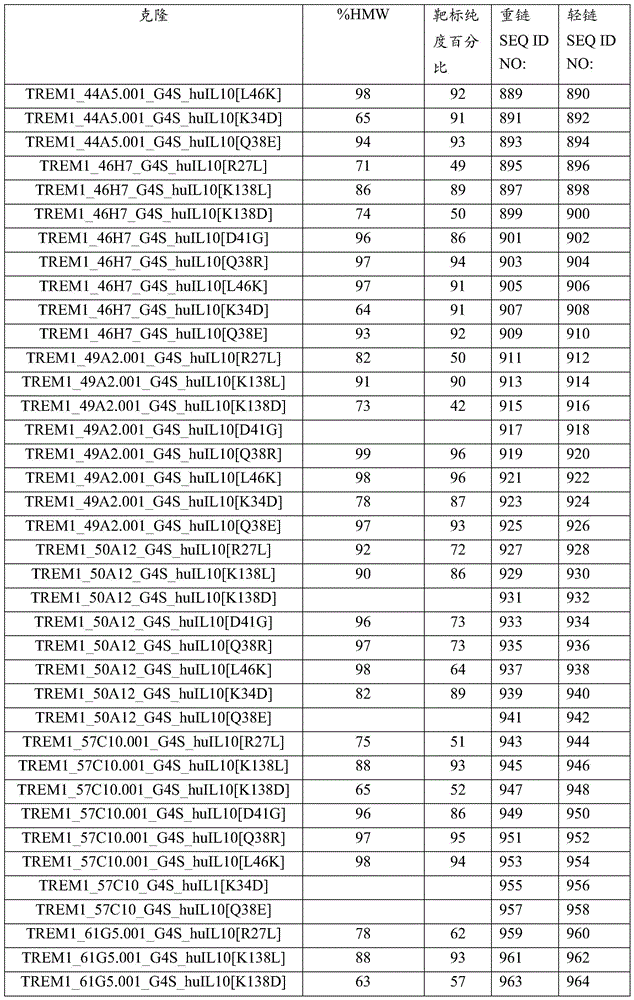
在多个实施例中,抗原结合蛋白具有以下氨基酸序列中任一个中列出的轻链氨基酸序列:SEQ ID NO:864、866、868、870、872、874、876、878、880、882、884、886、888、890、892、894、896、898、900、902、904、906、908、910、912、914、916、918、920、922、924、926、928、930、932、934、936、938、940、942、944、946、948、950、952、954、956、958、960、962、964、966、968、970、972、974、976、978、980、982、984、986、988、990、992、994、996、998、1000、1002、1004、1006、1008、1010、1012、1014、1016、1018、1020、1022、1024、1026、1028、1030、1032、1034、1036、1038、1040、1042、1044、1046、1048、1050、1052、1054、1056、1058、1060、1062、1064、1066、1068、1070、1072、1074、1076、1078、1080、1082、1084、和1086。
在多个实施例中,TREM-1抗体或抗原结合蛋白具有以下氨基酸序列中任一个中列出的轻链氨基酸序列:SEQ ID NO:2543、2544、2545、2546、2547、2548、2549、2550、2551、2552、2553、2554、2555、2556、2557、2558、2559、2560、2561、2562、2563、2564、2565、2566、2567、2568、2569、2570、2571、2572、2573、2574、2575、2576、2577、2578、2579、2580、2581、2582、2583、2584、2585、2586、2587、2588、2589、2590、2591、2592、2593、2594、2595、2596、2597、2598、2599、2600、2601、2602、2603、2604、2605。
在多个实施例中,TREM-1抗体或抗原结合蛋白具有以下氨基酸序列中任一个中列出的轻链氨基酸序列:SEQ ID NO:2233、2235、2237、2239、2241、2243、2245、2247、2249、2251、2253、2255、2257、2259、2261、2263、2265、2267、2269、2271、2273、2275、2277、2279、2281、2283、2285、2287、2289、2291、2293、2295、2297、2299、2301、2303、2305、2307、2309、2311、2313、2315、2317、2319、2321、2323、2325、2327、2329、2331、2333、2335、2337、2339、2341、2343、2345、2347、2349、2351、2353、2355、和2357。
在多个实施例中,抗原结合蛋白具有以下氨基酸序列中任一个中列出的重链氨基酸序列:SEQ ID NO:863、865、867、869、871、873、875、877、879、881、883、885、887、889、891、893、895、897、899、901、903、905、907、909、911、913、915、917、919、921、923、925、927、929、931、933、935、937、939、941、943、945、947、949、951、953、955、957、959、961、963、965、967、969、971、973、975、977、979、981、983、985、987、989、991、993、995、997、999、1001、1003、1005、1007、1009、1011、1013、1015、1017、1019、1021、1023、1025、1027、1029、1031、1033、1035、1037、1039、1041、1043、1045、1047、1049、1051、1053、1055、1057、1059、1061、1063、1065、1067、1069、1071、1073、1075、1077、1079、1081、1083、和1085。
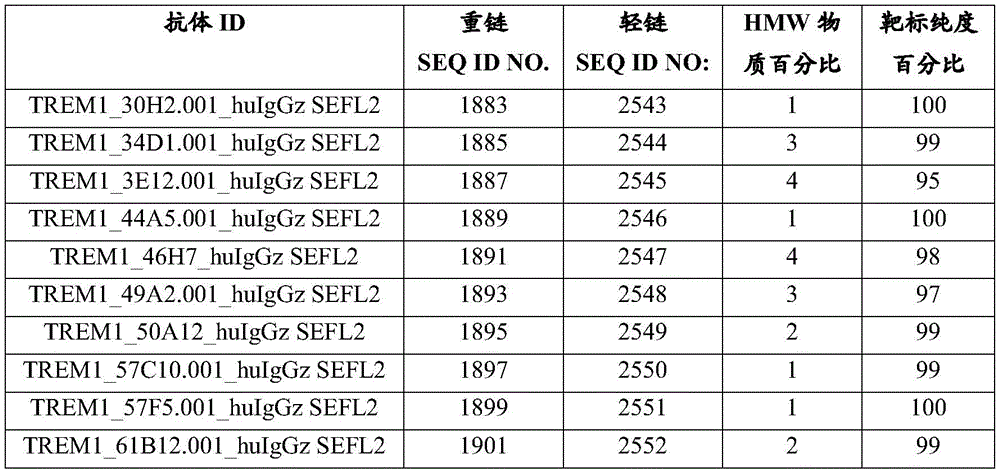
在多个实施例中,TREM-1抗体或抗原结合蛋白具有以下氨基酸序列中任一个中列出的重链氨基酸序列:SEQ ID NO:1883、1885、1887、1889、1891、1893、1895、1897、1899、1901、1903、1905、1907、1909、1911、1913、1915、1917、1919、1921、1923、1925、1927、1929、1931、1933、1935、1937、1939、1941、1943、1945、1947、1949、1951、1953、1955、1957、1959、1961、1963、1965、1967、1969、1971、1973、1975、1977、1979、1981、1983、1985、1987、1989、1991、1993、1995、1997、1999、2001、2003、2005、和2007。
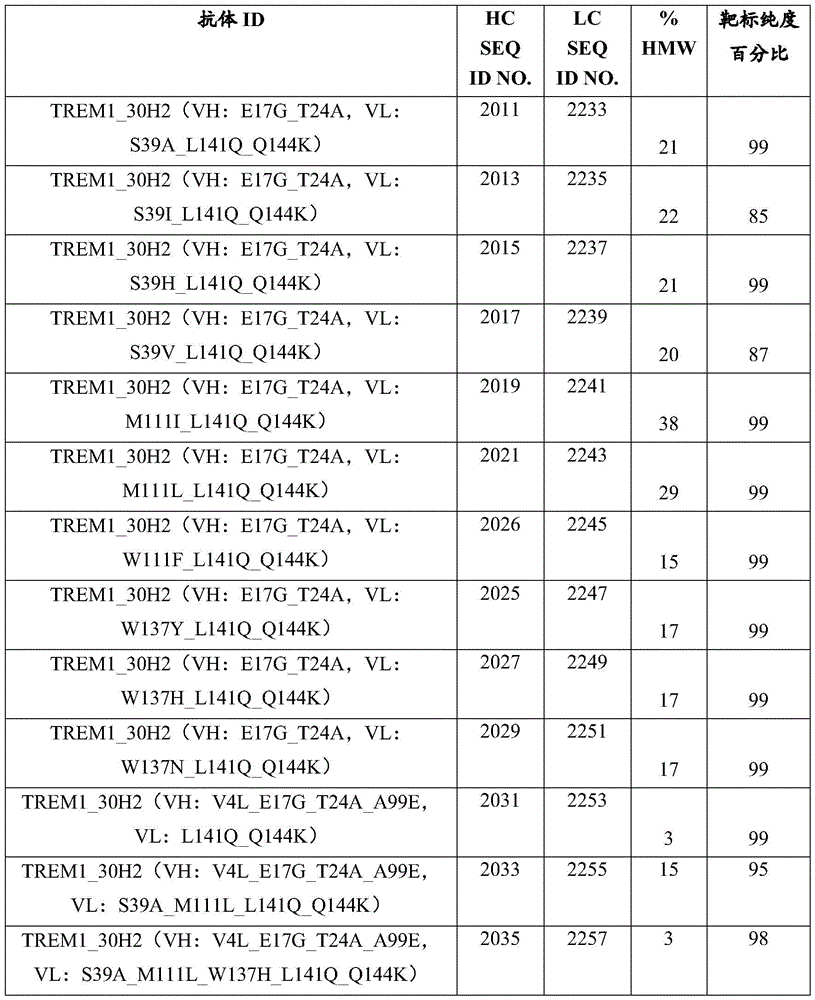
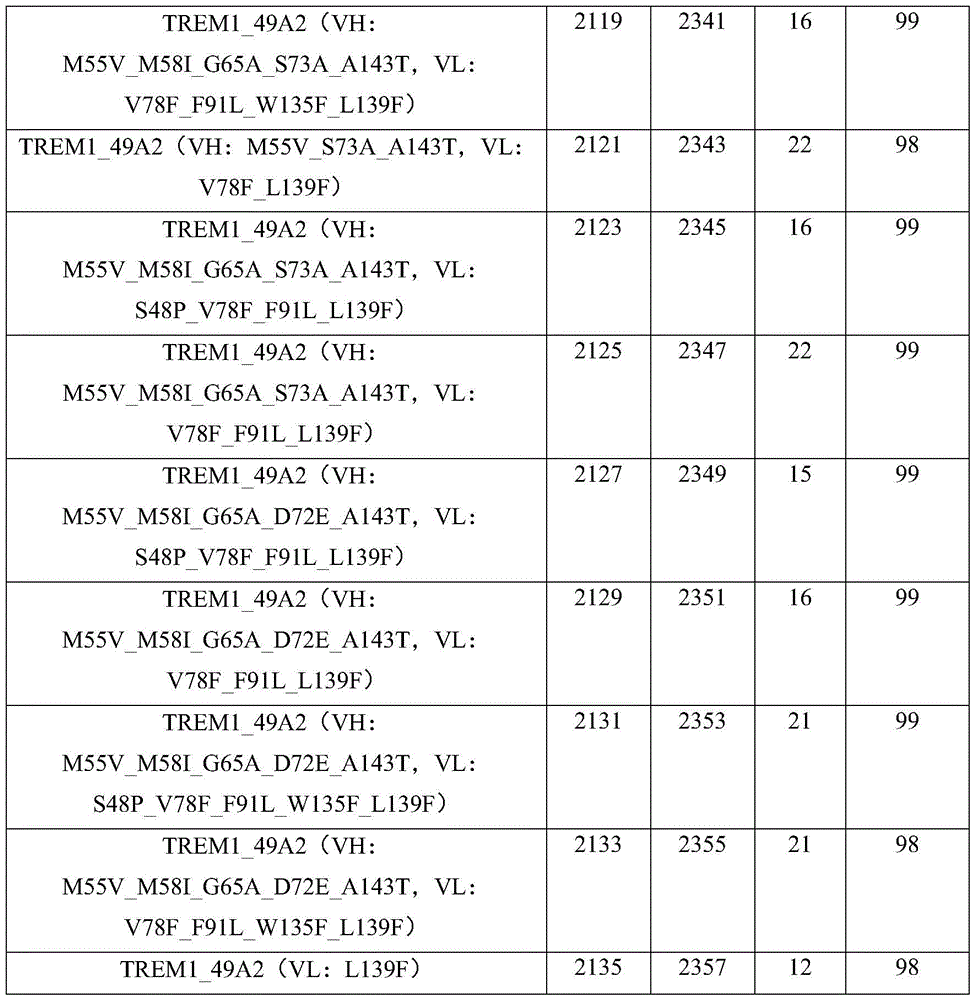
在多个实施例中,TREM-1抗体或抗原结合蛋白具有以下氨基酸序列中任一个中列出的重链氨基酸序列:SEQ ID NO:2011、2013、2015、2017、2019、2021、2026、2025、2027、2029、2031、2033、2035、2037、2039、2041、2043、2045、2047、2049、2051、2053、2055、2057、2059、2061、2063、2065、2067、2069、2071、2073、2075、2077、2079、2081、2083、2085、2087、2089、2091、2093、2095、2097、2099、2101、2103、2105、2107、2109、2111、2113、2115、2117、2119、2121、2123、2125、2127、2129、2131、2133、和2135。
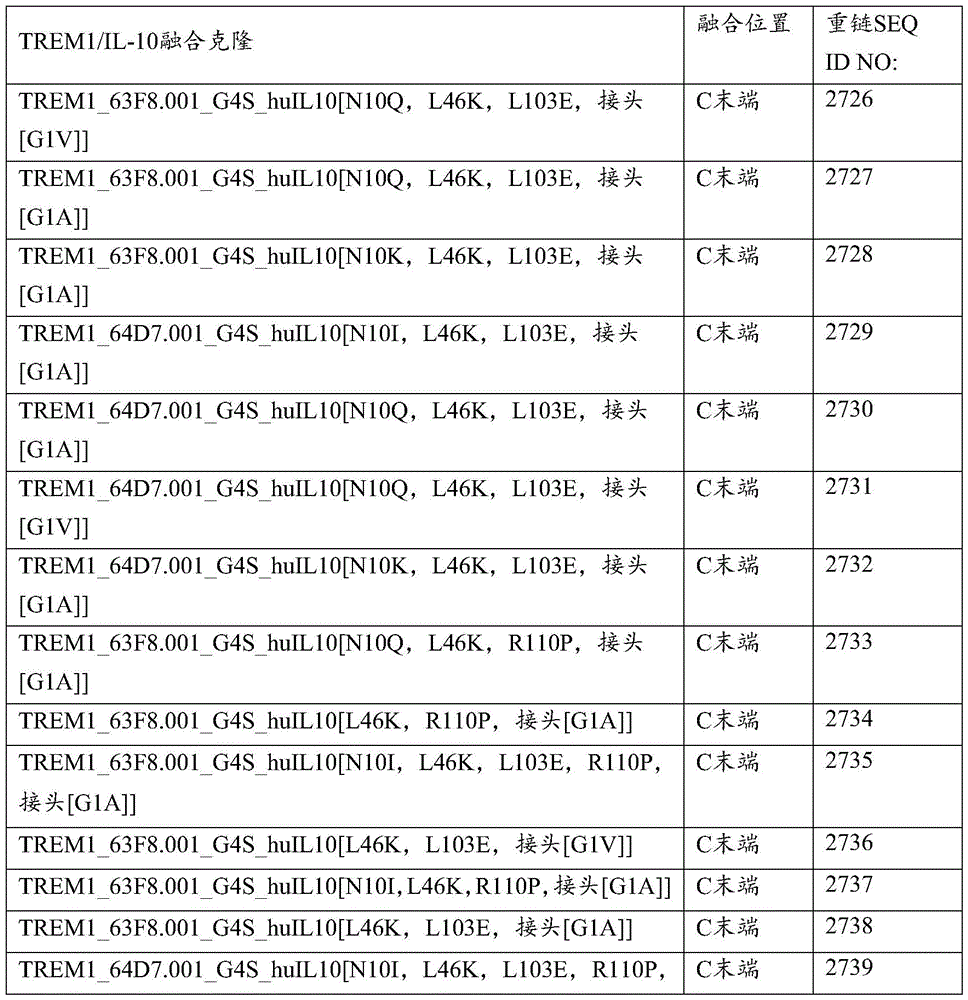
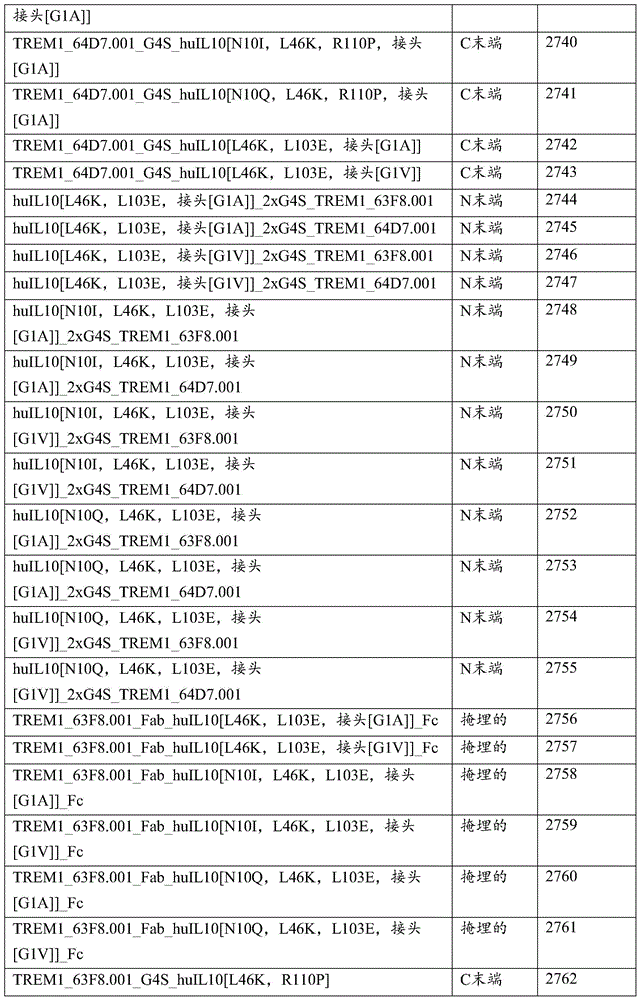
在多个实施例中,抗原结合蛋白具有SEQ ID NO:2726-2776中任一个中列出的重链氨基酸序列。
在多个实施例中,抗原结合蛋白具有以下氨基酸序列中任一个中列出的重链氨基酸序列:SEQ ID NO:863、865、867、869、871、873、875、877、879、881、883、885、887、889、891、893、895、897、899、901、903、905、907、909、911、913、915、917、919、921、923、925、927、929、931、933、935、937、939、941、943、945、947、949、951、953、955、957、959、961、963、965、967、969、971、973、975、977、979、981、983、985、987、989、991、993、995、997、999、1001、1003、1005、1007、1009、1011、1013、1015、1017、1019、1021、1023、1025、1027、1029、1031、1033、1035、1037、1039、1041、1043、1045、1047、1049、1051、1053、1055、1057、1059、1061、1063、1065、1067、1069、1071、1073、1075、1077、1079、1081、1083、和1085,以及以下氨基酸序列中列出的相应的轻链氨基酸序列:SEQ ID NO:864、866、868、870、872、874、876、878、880、882、884、886、888、890、892、894、896、898、900、902、904、906、908、910、912、914、916、918、920、922、924、926、928、930、932、934、936、938、940、942、944、946、948、950、952、954、956、958、960、962、964、966、968、970、972、974、976、978、980、982、984、986、988、990、992、994、996、998、1000、1002、1004、1006、1008、1010、1012、1014、1016、1018、1020、1022、1024、1026、1028、1030、1032、1034、1036、1038、1040、1042、1044、1046、1048、1050、1052、1054、1056、1058、1060、1062、1064、1066、1068、1070、1072、1074、1076、1078、1080、1082、1084、和1086。
在多个实施例中,TREM-1抗体或抗原结合蛋白具有以下氨基酸序列中任一个中列出的重链氨基酸序列:SEQ ID NO:1883、1885、1887、1889、1891、1893、1895、1897、1899、1901、1903、1905、1907、1909、1911、1913、1915、1917、1919、1921、1923、1925、1927、1929、1931、1933、1935、1937、1939、1941、1943、1945、1947、1949、1951、1953、1955、1957、1959、1961、1963、1965、1967、1969、1971、1973、1975、1977、1979、1981、1983、1985、1987、1989、1991、1993、1995、1997、1999、2001、2003、2005、和2007,以及以下氨基酸序列中列出的相应的轻链氨基酸序列:SEQ ID NO:2543、2544、2545、2546、2547、2548、2549、2550、2551、2552、2553、2554、2555、2556、2557、2558、2559、2560、2561、2562、2563、2564、2565、2566、2567、2568、2569、2570、2571、2572、2573、2574、2575、2576、2577、2578、2579、2580、2581、2582、2583、2584、2585、2586、2587、2588、2589、2590、2591、2592、2593、2594、2595、2596、2597、2598、2599、2600、2601、2602、2603、2604、和2605。
在多个实施例中,TREM-1抗体或抗原结合蛋白具有以下氨基酸序列中任一个中列出的重链氨基酸序列:SEQ ID NO:2011、2013、2015、2017、2019、2021、2026、2025、2027、2029、2031、2033、2035、2037、2039、2041、2043、2045、2047、2049、2051、2053、2055、2057、2059、2061、2063、2065、2067、2069、2071、2073、2075、2077、2079、2081、2083、2085、2087、2089、2091、2093、2095、2097、2099、2101、2103、2105、2107、2109、2111、2113、2115、2117、2119、2121、2123、2125、2127、2129、2131、2133、和2135,以及以下氨基酸序列中列出的相应的轻链氨基酸序列:SEQ ID NO:2233、2235、2237、2239、2241、2243、2245、2247、2249、2251、2253、2255、2257、2259、2261、2263、2265、2267、2269、2271、2273、2275、2277、2279、2281、2283、2285、2287、2289、2291、2293、2295、2297、2299、2301、2303、2305、2307、2309、2311、2313、2315、2317、2319、2321、2323、2325、2327、2329、2331、2333、2335、2337、2339、2341、2343、2345、2347、2349、2351、2353、2355、和2357。
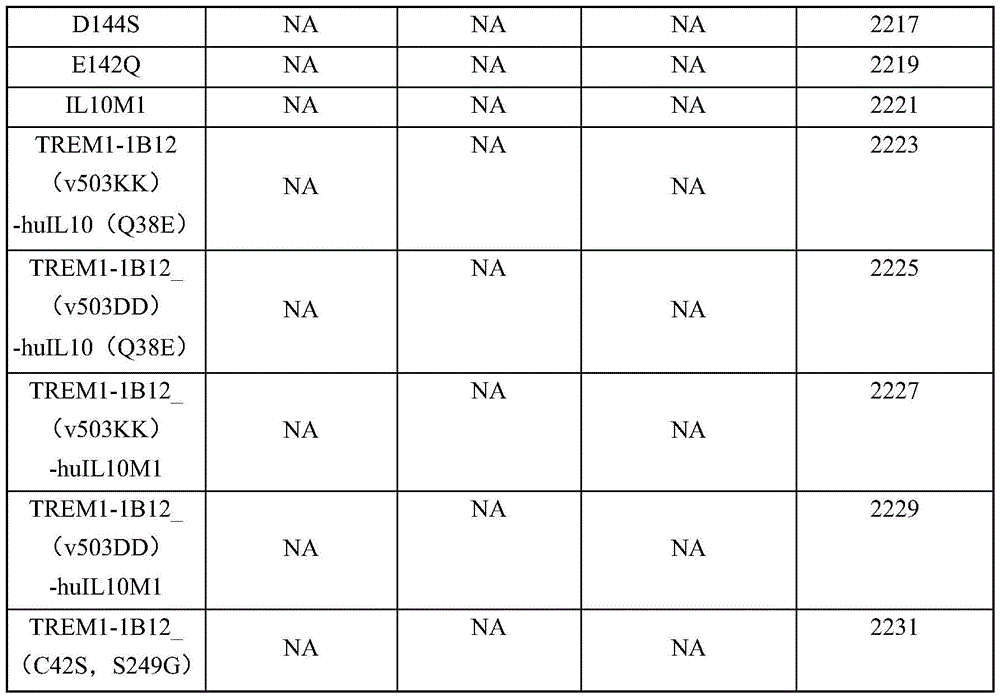
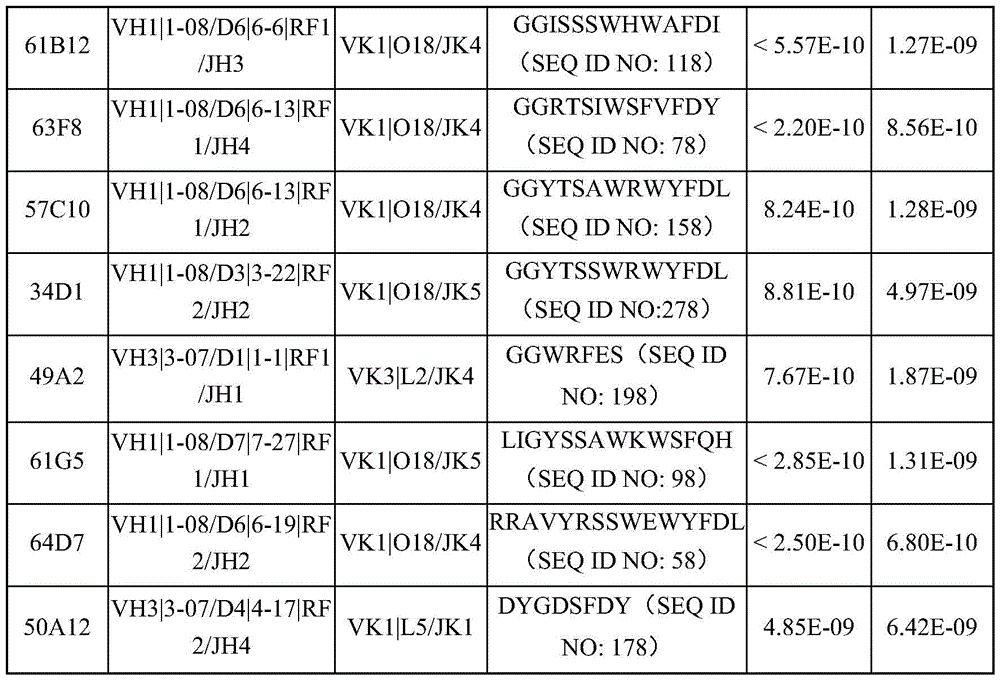
在多个实施例中,抗原结合蛋白具有如表10、表11、表13A、或表13B中列出的重链和轻链对,或利用表16、表17或表22中列出的重链抗原结合蛋白。
某些抗原结合蛋白重链和轻链的核酸序列在SEQ ID NO:303到526(二价)和SEQID NO:527到862(单价)中列出。TREM-1变体抗体重链可变区的核酸序列在SEQ ID NO:1884、1886、1888、1890、1892、1894、1896、1898、1900、1902、1904、1906、1908、1910、1912、1914、1916、1918、1920、1922、1924、1926、1928、1930、1932、1934、1936、1938、1940、1942、1944、1946、1948、1950、1952、1954、1956、1958、1960、1962、1964、1966、1968、1970、1972、1974、1976、1978、1980、1982、1984、1986、1988、1990、1992、1994、1996、1998、2000、2002、2004、2006、和2008中列出,以及也在SEQ ID NO:2012、2014、2016、2018、2020、2022、2024、2026、2028、2030、2032、2034、2036、2038、2040、2042、2044、2046、2048、2050、2052、2054、2056、2058、2060、2062、2064、2066、2068、2070、2072、2074、2076、2078、2080、2082、2084、2086、2088、2090、2092、2094、2096、2098、2100、2102、2104、2106、2108、2110、2112、2114、2116、2118、2120、2122、2124、2126、2128、2130、2132、2134、和2136中列出;并且TREM-1变体抗体轻链可变区核苷酸序列在SEQ ID NO:2606、2607、2608、2609、2610、2611、2612、2613、2614、2615、2616、2617、2618、2619、2620、2621、2622、2623、2624、2625、2626、2627、2628、2629、2630、2631、2632、2633、2634、2635、2636、2637、2638、2639、2640、2641、2642、2643、2644、2645、2646、2647、2648、2649、2650、2651、2652、2653、2654、2655、2656、2657、2658、2659、2660、2661、2662、2663、2664、2665、2666、2667、2668中列出,以及也在SEQ ID NO:2234、2236、2238、2240、2242、2244、2246、2248、2250、2252、2254、2256、2258、2260、2262、2264、2266、2268、2270、2272、2274、2276、2278、2280、2282、2284、2286、2288、2290、2292、2294、2296、2298、2300、2302、2304、2306、2308、2310、2312、2314、2316、2318、2320、2322、2324、2326、2328、2330、2332、2334、2336、2338、2340、2342、2344、2346、2348、2350、2352、2354、2356、和2358中列出。
在抗原结合蛋白的多个实施例中,抗抗原结合蛋白的一个或多个重链框架氨基酸被来自另一人抗体氨基酸序列的相应的一个或多个氨基酸替代。在多个实施例中,抗原结合蛋白的一个或多个轻链框架氨基酸被来自另一人抗体氨基酸序列的相应的一个或多个氨基酸替代。
在多个实施例中,抗TREM-1抗原结合蛋白进一步包含连接至所述轻链可变区的人轻链恒定区。
在抗原结合蛋白的多个实施例中:该抗原结合蛋白包含两条轻链和两条重链:每条重链包含在该重链的C末端处附接的IL-10部分;每个重链-IL-10部分抗原结合蛋白包含与选自以下的序列具有至少90%同一性的氨基酸序列:SEQ ID NO:863、865、867、869、871、873、875、877、879、881、883、885、887、889、891、893、895、897、899、901、903、905、907、909、911、913、915、917、919、921、923、925、927、929、931、933、935、937、939、941、943、945、947、949、951、953、955、957、959、961、963、965、967、969、971、973、975、977、979、981、983、985、987、989、991、993、995、997、999、1001、1003、1005、1007、1009、1011、1013、1015、1017、1019、1021、1023、1025、1027、1029、1031、1033、1035、1037、1039、1041、1043、1045、1047、1049、1051、1053、1055、1057、1059、1061、1063、1065、1067、1069、1071、1073、1075、1077、1079、1081、1083、和1085;并且每条轻链包含与选自以下的序列具有至少90%同一性的氨基酸序列:SEQ ID NO:864、866、868、870、872、874、876、878、880、882、884、886、888、890、892、894、896、898、900、902、904、906、908、910、912、914、916、918、920、922、924、926、928、930、932、934、936、938、940、942、944、946、948、950、952、954、956、958、960、962、964、966、968、970、972、974、976、978、980、982、984、986、988、990、992、994、996、998、1000、1002、1004、1006、1008、1010、1012、1014、1016、1018、1020、1022、1024、1026、1028、1030、1032、1034、1036、1038、1040、1042、1044、1046、1048、1050、1052、1054、1056、1058、1060、1062、1064、1066、1068、1070、1072、1074、1076、1078、1080、1082、1084、和1086。
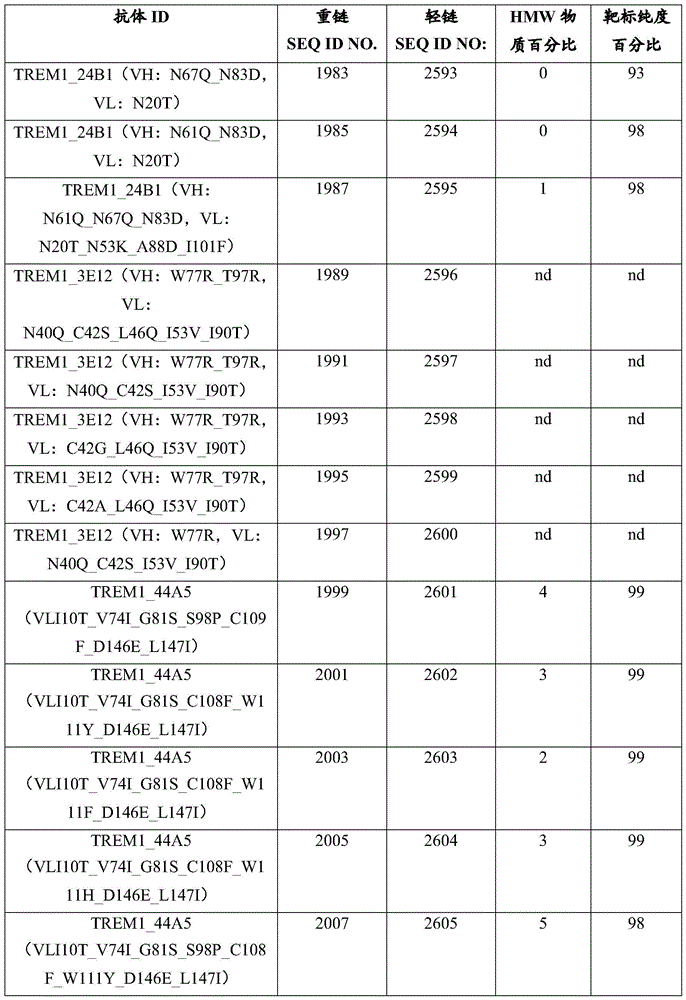
在多个实施例中,本文提供了TREM-1抗体重链和/或轻链可变区的变体。TREM-1抗体重链可变区变体序列在SEQ ID NO:1883、1885、1887、1889、1891、1893、1895、1897、1899、1901、1903、1905、1907、1909、1911、1913、1915、1917、1919、1921、1923、1925、1927、1929、1931、1933、1935、1937、1939、1941、1943、1945、1947、1949、1951、1953、1955、1957、1959、1961、1963、1965、1967、1969、1971、1973、1975、1977、1979、1981、1983、1985、1987、1989、1991、1993、1995、1997、1999、2001、2003、2005、2007、2011、2013、2015、2017、2019、2021、2026、2025、2027、2029、2031、2033、2035、2037、2039、2041、2043、2045、2047、2049、2051、2053、2055、2057、2059、2061、2063、2065、2067、2069、2071、2073、2075、2077、2079、2081、2083、2085、2087、2089、2091、2093、2095、2097、2099、2101、2103、2105、2107、2109、2111、2113、2115、2117、2119、2121、2123、2125、2127、2129、2131、2133、2135、2726-2776以及表10、表11、表13A、表13B和表22中列出。
TREM-1抗体轻链可变区变体序列在SEQ ID NO:2543、2544、2545、2546、2547、2548、2549、2550、2551、2552、2553、2554、2555、2556、2557、2558、2559、2560、2561、2562、2563、2564、2565、2566、2567、2568、2569、2570、2571、2572、2573、2574、2575、2576、2577、2578、2579、2580、2581、2582、2583、2584、2585、2586、2587、2588、2589、2590、2591、2592、2593、2594、2595、2596、2597、2598、2599、2600、2601、2602、2603、2604、2605、2233、2235、2237、2239、2241、2243、2245、2247、2249、2251、2253、2255、2257、2259、2261、2263、2265、2267、2269、2271、2273、2275、2277、2279、2281、2283、2285、2287、2289、2291、2293、2295、2297、2299、2301、2303、2305、2307、2309、2311、2313、2315、2317、2319、2321、2323、2325、2327、2329、2331、2333、2335、2337、2339、2341、2343、2345、2347、2349、2351、2353、2355、2357、表10和表11中列出。预期TREM-1-IL-10抗原结合蛋白包含如本文披露的TREM-1抗体变体重链和/或轻链序列。
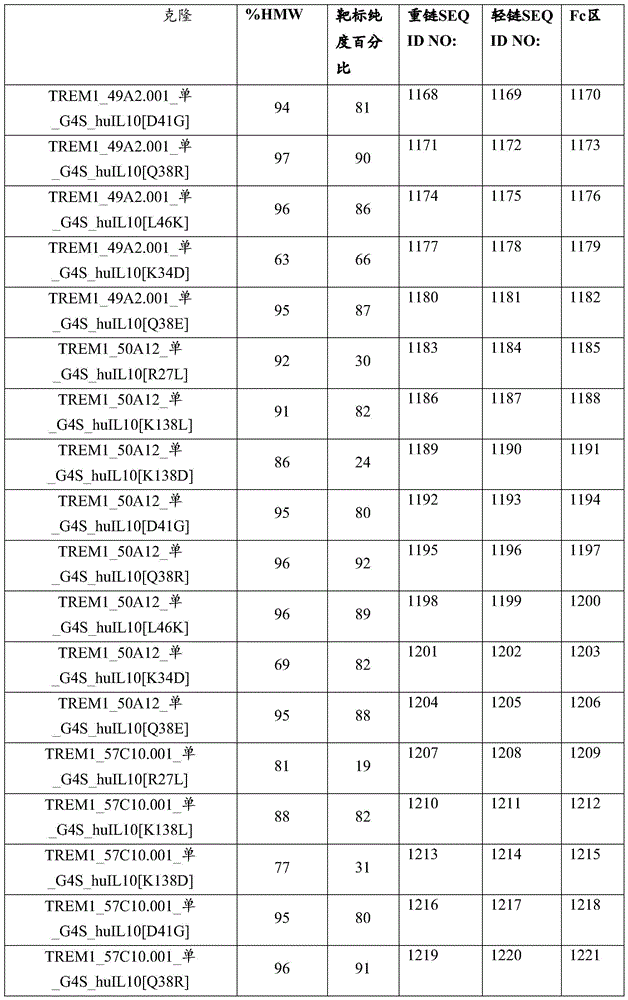
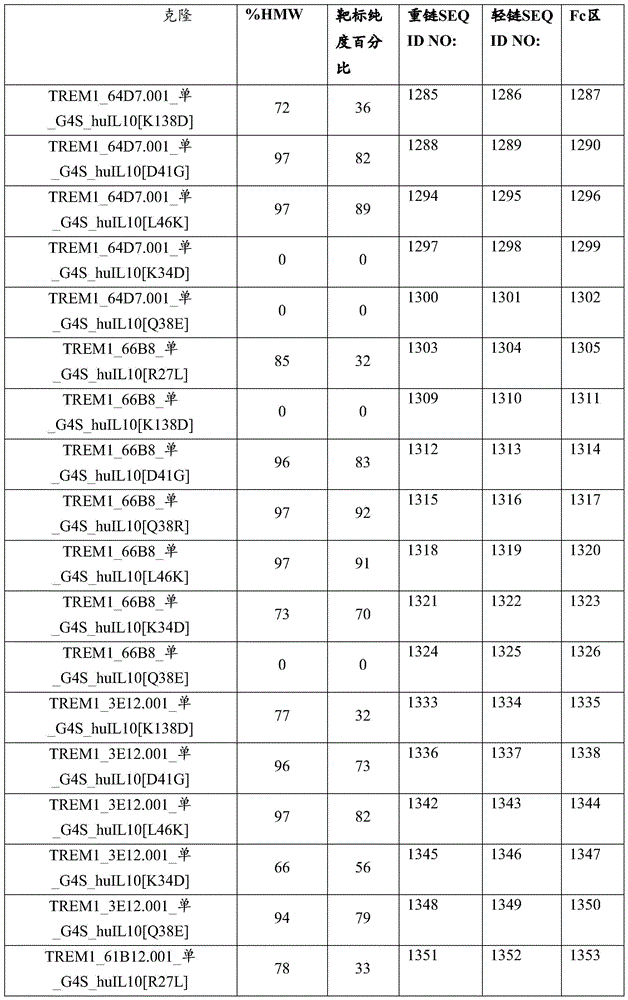
在多个实施例中,抗原结合蛋白可以是单价。在多个实施例中,重链-IL-10部分抗原结合蛋白包含与选自以下的序列具有至少90%同一性的氨基酸序列:SEQ ID NO:1087、1090、1093、1096、1105、1108、1111、1114、1117、1123、1126、1129、1132、1138、1141、1147、1150、1153、1156、1159、1162、1165、1168、1171、1174、1177、1180、1183、1186、1189、1192、1195、1198、1201、1204、1207、1210、1213、1216、1219、1222、1225、1228、1231、1237、1240、1243、1246、1252、1255、1258、1261、1264、1267、1270、1273、1276、1279、1285、1288、1294、1297、1300、1303、1309、1312、1315、1318、1321、1324、1333、1336、1342、1345、1348、1351、1354、1357、1360、1363、1366、1369、1372、1375、1378、1381、1384、1387、1390、1393、1396、1399、1402、1408、1411、1414、1417、和1420。在多个实施例中,轻链包含与选自以下的序列具有至少90%同一性的氨基酸序列:SEQ ID NO:1088、1091、1094、1097、1106、1109、1112、1115、1118、1124、1127、1130、1133、1139、1142、1148、1151、1154、1157、1160、1163、1166、1169、1172、1175、1178、1181、1184、1187、1190、1193、1196、1199、1202、1205、1208、1211、1214、1217、1220、1223、1226、1229、1232、1238、1241、1244、1247、1253、1256、1259、1262、1265、1268、1271、1274、1277、1280、1286、1289、1295、1298、1301、1304、1310、1313、1316、1319、1322、1325、1334、1337、1343、1346、1349、1352、1355、1358、1361、1364、1367、1370、1373、1376、1379、1382、1385、1388、1391、1394、1397、1400、1403、1409、1412、1415、1418和1421。在多个实施例中,单价抗原结合蛋白进一步包含Fc区,例如,如SEQ ID NO:1089、1092、1095、1098、1107、1110、1113、1116、1119、1125、1128、1131、1134、1140、1143、1149、1152、1155、1158、1161、1164、1167、1170、1173、1176、1179、1182、1185、1188、1191、1194、1197、1200、1203、1206、1209、1212、1215、1218、1221、1224、1227、1230、1233、1239、1242、1245、1248、1254、1257、1260、1263、1266、1269、1272、1275、1278、1281、1287、1290、1296、1299、1302、1305、1311、1314、1317、1320、1323、1326、1335、1338、1344、1347、1350、1353、1356、1359、1362、1365、1368、1371、1374、1377、1380、1383、1386、1389、1392、1395、1398、1401、1404、1410、1413、1416、1419和1422中列出的。单价抗原结合蛋白和Fc区可以如表13B中列出的组装或匹配。
在抗原结合蛋白的多个实施例中:该抗原结合蛋白包含一条或两条轻链和一条或两条重链:每条重链包含在该重链的C末端处附接的IL-10部分;每个重链-IL-10部分抗原结合蛋白包含与选自以下的序列具有至少90%同一性的氨基酸序列:SEQ ID NO:2137、2139、2141、2143、2145、2147、2149、2151、2153、2155、2157、2159、2161、2163、2165、2167、2169、2171、2173、2175、2177、2179、2181、2359、2361、2363、2365、2367、2369、2371、2373、2375、2377、2379、2381、2383、2385、2387、2389、2391、2393、2395、2397、2399、2401、2403、2405、2407、2409、2411、2143、2415、2417、2419、2421、2423、2425、2427、2429、2431、2433、2435、2437、2439、2441、2443、2445、2447、2449、2451、2453、2455、2457、2459、2461、2463、2465、2467、2469、2471、2473、2475、2477、2479、2481、2483、2485、2487、2489、2491、2493、2495、2497、2498、2499、2501、2503、2505、2507、2509、2511、2513、2515、2517、2519、2521、2523、2525、2527、2529、2531、2533、2535、2537、2539、和2726-2776,以及如表16、或表17、或表21或表22中列出的。
在多个实施例中,抗原结合蛋白包含选自以下的氨基酸序列:SEQ ID NO:2137、2139、2141、2143、2145、2147、2149、2151、2153、2155、2157、2159、2161、2163、2165、2167、2169、2171、2173、2175、2177、2179、2181、2359、2361、2363、2365、2367、2369、2371、2373、2375、2377、2379、2381、2383、2385、2387、2389、2391、2393、2395、2397、2399、2401、2403、2405、2407、2409、2411、2143、2415、2417、2419、2421、2423、2425、2427、2429、2431、2433、2435、2437、2439、2441、2443、2445、2447、2449、2451、2453、2455、2457、2459、2461、2463、2465、2467、2469、2471、2473、2475、2477、2479、2481、2483、2485、2487、2489、2491、2493、2495、2497、2498、2499、2501、2503、2505、2507、2509、2511、2513、2515、2517、2519、2521、2523、2525、2527、2529、2531、2533、2535、2537、和2539。在多个实施例中,抗原结合蛋白的重链部分与相应的轻链克隆(例如,抗体61B12(SEQ ID NO:105,但缺乏信号序列或SEQ IDNO:2552、TREM1_61B12.001_huIgGz SEFL2轻链、或SEQ ID NO:1042、1044、1046、1048、1052、1054),或如SEQ ID NO:2233至2358、表10或表11中列出的)配对。
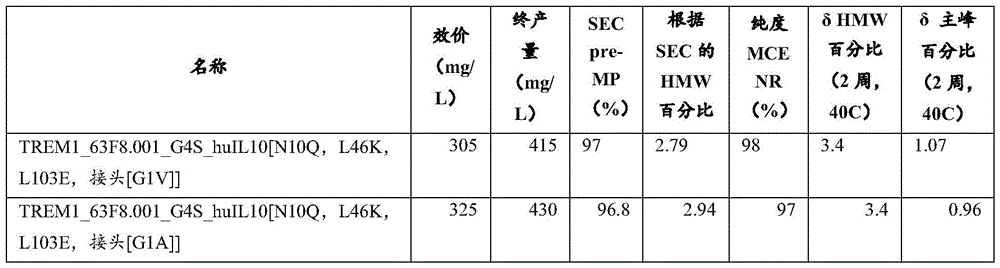
在多个实施例中,抗原结合蛋白具有与SEQ ID NO:2726-2776中任一个中列出的序列具有至少90%同一性的重链氨基酸序列。在多个实施例中,抗原结合蛋白具有SEQ IDNO:2726-2776中任一个中列出的重链氨基酸序列。在多个实施例中,抗原结合蛋白具有SEQID NO:2727-2732中任一个中列出的重链氨基酸序列。在多个实施例中,重链与相应的轻链克隆配对,例如,对于克隆63F8.001的SEQ ID NO:976或SEQ ID NO:2554(但缺乏信号序列),以及对于64D7.001的SEQ ID NO:992或SEQ ID NO:2555(但缺乏信号序列)。在多个实施例中,抗原结合蛋白包含SEQ ID NO:2727或2728的重链氨基酸序列,和SEQ ID NO:976或SEQ ID NO:2554中列出的轻链氨基酸序列,或如本文所述的对于克隆63F8或63F8.001的其他轻链序列。在多个实施例中,抗原结合蛋白包含SEQ ID NO:2729、2730、2731或2732的重链氨基酸序列,和SEQ ID NO:992或SEQ ID NO:2555中列出的轻链氨基酸序列,或如本文所述的对于64D7或64D7.001的其他轻链序列。
在抗原结合蛋白的多个实施例中,抗原结合部分抑制一个或多个TREM-1配体与TREM-1结合。
在多个实施例中,抗原结合蛋白包含抗原结合部分和一个或两个IL-10突变蛋白部分,其中:
a.该抗原结合部分是抗体或抗体片段,
b.每个IL-10部分独立地是单价或二价,
c.每个IL-10部分独立地选自具有与SEQ ID NO:2具有90%同一性的序列的一种或多种人IL-10突变蛋白,
d.至少一个IL-10部分与该抗原结合部分共价结合,并且
e.该抗原结合部分与本文所述的抗TREM-1抗原结合部分竞争与人TREM-1蛋白结合。
在抗原结合蛋白的多个实施例中,抗原结合部分是人抗体。
还提供了包含编码如本文所述的抗原结合蛋白的重链区的核苷酸序列的分离的核酸分子、包含编码如本文所述的抗原结合蛋白的轻链区的核苷酸序列的分离的核酸分子、以及包含编码抗原结合蛋白的重链区的核苷酸序列并且进一步包含编码如本文所述的抗原结合蛋白的轻链区的核苷酸序列的分离的核酸分子。
本披露提供了一个或多个表达载体,其包含可操作地连接到表达控制序列的编码如本文所述的抗原结合蛋白的一个或多个核酸分子。
还考虑了重组宿主细胞,其包含含有如本文所述的抗原结合蛋白的核酸分子、或含有所述核酸的载体。在多个实施例中,宿主细胞是哺乳动物细胞。在多个实施例中,宿主细胞是CHO细胞。本披露提供了使用本文所述的宿主细胞产生抗原结合蛋白的方法,该方法包括培养宿主细胞并回收所述抗体,以及提供了通过该方法产生的抗原结合蛋白。
本披露考虑了包含如本文所述的抗原结合蛋白和药学上可接受的载剂的药物组合物。还提供了包含本披露的IL-10突变蛋白的药物组合物。进一步提供了包含本披露的抗TREM-1抗体或抗体片段的药物组合物。预期药物组合物是无菌药物组合物。
在一方面,本披露提供了治疗有需要的受试者的炎性疾病的方法,该方法包括施用如本文所述的IL-10突变蛋白或包含IL-10突变蛋白的组合物。
在相关方面,本披露提供了治疗有需要的受试者的炎性疾病的方法,该方法包括施用如本文所述的抗TREM-1抗原结合蛋白或包含如本文所述的抗TREM-1抗原结合蛋白的组合物。在多个实施例中,该方法进一步包括与抗TREM-1抗原结合蛋白组合施用如本文所述的抗IL-10突变蛋白。在多个实施例中,抗TREM-1抗原结合蛋白和IL-10突变蛋白以同一组合物或以不同组合物施用。
还提供了治疗有需要的受试者的炎性疾病的方法,该方法包括施用如本文所述的抗原结合蛋白或包含如本文所述的抗原结合蛋白的组合物。在多个实施例中,提供了治疗有需要的受试者的炎性疾病的方法,该方法包括施用如本文所述的抗TREM-1/IL-10突变蛋白抗原结合蛋白或包含所述抗原结合蛋白的组合物。
在多个实施例中,炎性疾病选自由以下组成的组:炎性肠病、溃疡性结肠炎、克罗恩病、肠易激综合征、类风湿性关节炎、银屑病、银屑病关节炎、或细胞因子释放综合征(CRS)。在一个实施例中,炎性疾病是炎性肠病。在一个实施例中,炎性疾病是溃疡性结肠炎。在一个实施例中,炎性疾病是克罗恩病。在一个实施例中,炎性疾病是肠易激综合征。在一个实施例中,炎性疾病是类风湿性关节炎。在一个实施例中,炎性疾病是银屑病。在一个实施例中,炎性疾病是银屑病关节炎。在一个实施例中,炎性疾病是细胞因子释放综合征。
在多个实施例中,与wt IL-10相比,用IL-10突变蛋白治疗减少了髓细胞中TNF-α产生方面的抑制,降低了CD8+T细胞刺激方面的水平,和/或降低了B细胞刺激方面的水平。在多个实施例中,用IL-10突变蛋白抗原结合蛋白(例如抗TREM-1/IL-10突变蛋白抗原结合蛋白)治疗抑制髓细胞中TNF-α产生。在多个实施例中,用IL-10突变蛋白抗原结合蛋白(例如抗TREM-1/IL-10突变蛋白抗原结合蛋白)治疗抑制髓细胞中TNF-α产生,同时减少CD8+T细胞和B细胞激活。在多个实施例中,治疗在受试者中抑制髓细胞中TNF-α产生,无CD8+T细胞刺激和/或B细胞刺激。在多个实施例中,治疗降低了受试者中TNF-α的水平。
在多个实施例中,治疗通过静脉内或皮下施用进行。在多个实施例中,治疗通过每周一次、每两周一次、每三周一次、每4周一次、每月一次、每3个月一次、或每六个月一次施用进行。
在多个实施例中,方法包括施用一种或两种另外的治疗剂。在多个实施例中,另外的治疗剂选自皮质类固醇、NSAID、止痛剂、免疫抑制剂、抗炎剂、TNFα抑制剂、IL-12/IL-23抑制剂、IL-17和IFN-γ。
本披露还提供了包含如本文所述的IL-10突变蛋白的组合物,用于在治疗炎性疾病中使用。在某些实施例中,本披露提供了包含如本文所述的IL-10突变蛋白的组合物在制备用于治疗炎性疾病的药物中的用途。
进一步考虑了包含如本文所述的抗TREM-1抗体或抗原结合片段的组合物,用于在治疗炎性疾病中使用。在某些实施例中,本披露提供了包含如本文所述的抗TREM-1抗体或其抗原结合片段的组合物在制备用于治疗炎性疾病的药物中的用途。
还考虑了包含如本文所述的抗TREM-1抗体或抗原结合片段的组合物与如本文所述的抗IL-10突变蛋白组合,用于在治疗炎性疾病中使用。在多个实施例中,本披露提供了包含如本文所述的抗TREM-1抗体或抗原结合片段的组合物与如本文所述的抗IL-10突变蛋白组合在制备用于治疗炎性疾病的药物中的用途。
还考虑了包含如本文所述的抗原结合蛋白(例如抗TREM-1/IL-10突变蛋白抗原结合蛋白)的组合物,用于在治疗炎性疾病中使用。进一步考虑了包含如本文所述的抗原结合蛋白(例如抗TREM-1/IL-10突变蛋白抗原结合蛋白)的组合物在制备用于治疗炎性疾病的药物中的用途。
在多个实施例中,炎性疾病是炎性肠病、溃疡性结肠炎、克罗恩病、肠易激综合征、类风湿性关节炎、银屑病、银屑病关节炎、或细胞因子释放综合征(CRS)。在一个实施例中,炎性疾病是溃疡性结肠炎。在一个实施例中,炎性疾病是克罗恩病。在一个实施例中,炎性疾病是肠易激综合征。在一个实施例中,炎性疾病是类风湿性关节炎。在一个实施例中,炎性疾病是银屑病。在一个实施例中,炎性疾病是银屑病关节炎。在一个实施例中,炎性疾病是细胞因子释放综合征。
应当理解,本文所述的每个特征或实施例或组合是本发明任何方面的非限制性、说明性示例,并且因此,意在与本文所述的任何其他特征或实施例或组合相结合。例如,在使用如“一个实施例”、“一些实施例”、“某些实施例”、“另外的实施例”、“特定的示例性实施例”和/或“另一个实施例”的语言描述特征的情况下,这些实施例的类型中的每一种都是旨在与本文所述的任何其他特征或特征的组合相结合而不必列出每一种可能的组合的特征的非限制性示例。这些特征或特征的组合适用于本发明的任何方面。在披露了落入范围内的值的实例的情况下,这些实例中的任何一个都被考虑为范围的可能端点,这些端点之间的任何和所有数值都被考虑,并且考虑了上下端点的任何和所有组合。
本文的标题是为了方便读者,而不旨在进行限制。本发明的其他方面、实施例和变化将自具体实施方式和/或附图和/或权利要求书变得显而易见。
附图说明
图1A-1C示出了二价和单价抗TREM1 mAb/IL-10突变蛋白抗原结合蛋白的示例性示意图。图1D展示了IL-10突变蛋白与抗原结合蛋白附接的位置。
图2示出了二价和单价TREM-1结合均显著提高了IL-10突变蛋白对单核细胞激活的抑制。
图3A-3B说明了抗TREM-1mAb/IL-10突变蛋白抗原结合蛋白不刺激CD8+T细胞(图3A)和B细胞(图3B)激活。
图4A-4H说明了对不同融合蛋白构建体而言,TREM-1结合显著提高了IL-10突变蛋白对单核细胞激活的抑制。
图5A-5B示出了IL-10突变蛋白对人(图5A)或小鼠(图5B)单核细胞的效力,如TNF水平所示,与单独的抗体或IL-10突变蛋白相比,通过融合蛋白的TREM-1结合改善了该效力。
图6A-6D示出了通过TNFα释放测量,在人(图6C-6D)或食蟹猴(图6A-6B)PBMC中抗人TREM-1抗体对配体(PGLYRP1/PGN)介导的TREM-1信号传导的抑制。
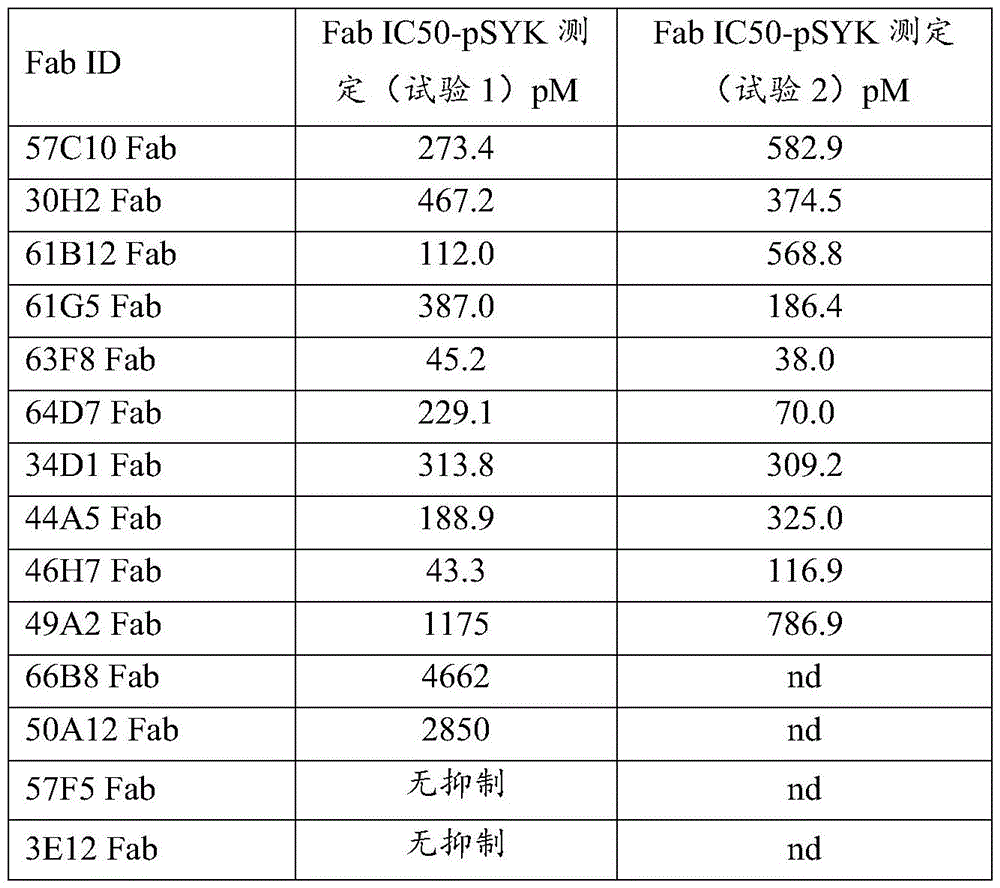
图7示出了通过脾酪氨酸激酶的磷酸化(pSYK)测量,在过表达人TREM-1/DAP12的细胞系中抗人TREM-1Fab对配体(PGLYRP1/PGN)介导的信号转导的抑制。
具体实施方式
本披露提供了IL-10突变蛋白和包含IL-10突变蛋白的抗原结合蛋白。根据本披露的抗原结合蛋白/融合蛋白显示出对免疫细胞的靶向性和对细胞活性和细胞因子应答的调节的改善,可用于治疗炎性疾病,如炎性肠病、克罗恩病、溃疡性结肠炎或类风湿性关节炎。因此,对髓细胞的靶向IL-10抑制活性可以为炎性肠病(IBD)提供有效的治疗而不引起副作用。本文考虑的IL-10突变蛋白抗原结合蛋白包含可以将IL-10突变蛋白靶向炎性细胞的抗原结合部分。合适的抗原结合部分包括抗TREM-1抗体和抗PD-1抗体。
定义
术语“多肽结合剂”或“抗原结合蛋白”是指能够特异性结合抗原(例如,靶标或其信号传导配偶体),或能够以可测量的结合亲和力结合抗原的多肽。多肽结合剂的实例包括抗体、肽体、多肽和肽,任选地与其他肽部分或非肽部分缀合。多肽结合剂可与之结合的抗原包括能够引起抗体应答的或以大于非特异性结合的可检测的结合亲和力与多肽结合剂结合的任何蛋白质或非蛋白质分子。调节性多肽结合剂与之结合的抗原可包括靶标、靶标的信号传导配偶体、和/或包含该靶标及其信号传导配偶体的复合物。如本文考虑的抗原结合蛋白可进一步包含另一个多肽的部分,例如,作为融合蛋白的一部分的异源部分。在这种情况下,抗原结合蛋白可以包含IL-10突变蛋白和抗原结合部分(如抗体或其抗原结合片段),其与抗原结合部分或其片段融合、连接或相继。
术语“抗体”以最广义使用并且包括完全组装的抗体、四聚体抗体、单克隆抗体、多克隆抗体、多特异性抗体(例如,双特异性抗体)、可以结合抗原(例如,Fab’、F’(ab)2、Fv、单链抗体、双抗体)的抗体片段、以及包含前述项的重组肽(只要其展现所需生物活性即可)。“免疫球蛋白”或“四聚体抗体”是由各自包含可变区和恒定区的两条重链和两条轻链组成的四聚体糖蛋白。抗原结合部分可通过重组DNA技术或通过完整抗体的酶促或化学裂解产生。抗体片段或抗原结合部分尤其包括Fab、Fab'、F(ab')2、Fv、结构域抗体(dAb)、互补决定区(CDR)片段、CDR移植抗体、单链抗体(scFv)、单链抗体片段、嵌合抗体、双抗体、三抗体、四抗体、微型抗体、线性抗体;螯合重组抗体、三抗体或双抗体、胞内抗体、纳米抗体、小模块免疫药物(SMIP)、抗原结合结构域免疫球蛋白融合蛋白、骆驼化抗体、含VHH抗体、或其变体或衍生物,以及含有足够赋予对多肽的抗原特异性结合的免疫球蛋白的至少一部分(如一个、两个、三个、四个、五个或六个CDR序列)的多肽(只要抗体保留所需生物活性即可)。
如本文所用的术语“单价IgG”是指其中单个抗原结合片段(Fab)与完整恒定结构域片段(Fc)融合的IgG,该完整恒定结构域片段通过Fc内CH3结构域中的突变经工程化以异源二聚化。单价IgG还称为“单臂”抗体。
术语“单克隆抗体”是指自基本上均质的抗体群体(即构成该群体的个体抗体除可少量存在的天然存在的可能突变外均一致)获得的抗体。
如本文所用的“抗体变体”是指在天然抗体可变区结构域的可变区中含有至少一个氨基酸取代、缺失、或插入的抗体多肽序列。变体可以与未修饰的抗体基本上同源或基本上相同。
“分离的”抗体是已经从其天然环境的组分鉴定并且分离和回收的抗体。其天然环境的污染组分是会干扰该抗体的诊断或治疗用途的物质,并且可包括酶、激素和其他蛋白质或非蛋白质溶质。在优选的实施例中,将抗体纯化(1)至如通过劳里法测量的大于95%重量、最优选地大于99%重量的抗体,(2)至足以获得通过使用转杯式测序仪发现的N端或内部氨基酸序列的至少15个残基的程度,或(3)至通过SDS-PAGE在还原或非还原条件下使用考马斯蓝或优选地银染法或HPLC方法发现的均质性。分离的抗体包括重组细胞内的原位抗体,因为抗体的天然环境的至少一种组分将不存在。然而,通常的是,通过至少一个纯化步骤制备分离的抗体。
如本文所用的“重链可变区”是指包含所述抗体重链可变结构域的至少一个互补决定区(CDR)的抗体分子区。重链可变区可以含有所述抗体重链的一个、两个、或三个CDR。
如本文所用的“轻链可变区”是指包含所述抗体轻链可变结构域的至少一个互补决定区(CDR)的抗体分子区。轻链可变区可以含有所述抗体轻链的一个、两个、或三个CDR,取决于抗体,该轻链可以是κ或λ轻链。
如本文所用,“特异性结合”的抗体为“抗原特异性的”、“对抗原靶标具有特异性”或与抗原“免疫反应”是指本发明的抗体或多肽结合剂以比相似序列的其他抗原更大的亲和力结合抗原。在一方面,本发明的抗原结合蛋白或其片段、变体、或衍生物,与其对其他(即非人类)物种的类似抗原的结合亲和力相比,将以更大的亲和力与人抗原结合,但识别和结合靶标的同源物的多肽结合剂也在本发明的范围内。
术语“表位”是指任何分子能够在抗原结合区的一个或多个中被选择性结合剂识别和结合的部分。表位通常由以下组成:分子例如氨基酸或碳水化合物侧链的化学活性表面分组,并且具有特定的三维结构特征、以及特定的电荷特征。如本文所用的表位可以是连续的或不连续的。
当与本发明的多肽结合剂和多肽结合使用时,术语“衍生物”是指通过如下技术进行化学修饰的多肽:泛素化、与治疗剂或诊断剂缀合、标记(例如用放射性核素或各种酶)、共价聚合物附着,如聚乙二醇化(用聚乙二醇衍生)以及通过化学合成插入或取代氨基酸(如鸟氨酸),这些氨基酸通常不在人类蛋白质中出现。衍生物保留了本发明的未衍生化的分子的结合特性。
如本文所用的“接头”是指连接两个多肽的肽。接头长度可以是1-80个氨基酸。在一些实施例中,接头可以是2-40、3-40、3-30、或3-20个氨基酸长。在一些实施例中,接头可以是18、17、16、15、14、13、12、11、10、9、8、7、6、5、4或3个氨基酸长的肽。在其他实施例中,接头可以是3-25、3-18、5-20、6-18、或10-20个氨基酸长。在其他实施例中,接头可以是约2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、或30个氨基酸长。在许多情况下,接头缺乏游离半胱氨酸残基(即,并且因此不涉及二硫键),并且也不含有N-糖基化位点(即Asn–Xxx–Ser/Thr,其中X可以是除脯氨酸以外的任何氨基酸)。在某些实施例中,具有序列G3SG2(SEQ ID NO:2676)或G4S(SEQ ID NO:2725)的肽是抗TREM-1抗原结合蛋白与IL-10突变蛋白之间的接头。其他合适的接头的实例包括G2、G3、G3S(SEQ ID NO:2705)、G3P(SEQ ID NO:2706)、G3q(SEQ ID NO:2707)、和G5(SEQ ID NO:2705)等。上述接头中的每个大写字母是指氨基酸的常规单字母代码,以及每个数字是指接头中氨基酸的串连重复序列数。例如,“G3SG2(SEQ ID NO:2676)”是指具有序列Gly-Gly-Gly-Ser-Gly-Gly(SEQ ID NO:2676)的接头。“G4S”是指具有序列Gly-Gly-Gly-Gly-Ser(SEQ IDNO:2725)的接头。
用于治疗疾病的药物的“治疗有效量”是指能够降低疾病的严重程度、减少与疾病或其治疗相关的一个或多个症状的严重程度、或推迟更严重的症状或更严重的疾病的发生的量,这些症状或疾病在治疗后可能以一定的频率出现。
本文提到的任何疾病的“治疗”涵盖减轻疾病的至少一种症状、降低疾病的严重程度、或推迟或防止疾病发展到更严重的症状,在一些情况下,这些症状可能伴随该疾病或导致至少一种其他疾病。治疗并不意味着疾病被完全治愈。有用的治疗剂只需降低疾病的严重程度、减少与疾病或其治疗相关的一个或多个症状的严重程度、或推迟更严重的症状或更严重的疾病的发生,这些症状或疾病在治疗后可能以一定的频率出现。例如,如果疾病是炎性肠病,则用作治疗的治疗剂可以减少肠道中不同炎症部位的数量或肠道受影响的总范围。它可以减轻疼痛和/或肿胀,减少腹泻、便秘或呕吐等症状,和/或防止肠道穿孔。
“受试者”涵盖哺乳动物和非哺乳动物。哺乳动物的实例包括但不限于哺乳动物类的任何成员:人、非人灵长类动物,如黑猩猩、以及其他猿类和猴类;农场动物,如牛、马、绵羊、山羊、猪;家畜,如兔、狗、和猫;实验室动物,包括啮齿动物,如大鼠、小鼠和豚鼠等。非哺乳动物的实例包括但不限于鸟、鱼等。术语不表示特定的年龄或性别。
如本文所用的“髓细胞”是指衍生自骨髓系的血液祖细胞的免疫细胞亚群,并且包括粒细胞、单核细胞、巨噬细胞、树突状细胞(DC)。髓细胞在保护性免疫中发挥重要功能,通常具有吞噬和抗原呈递细胞(APC)功能。参见例如,de Kleer等人,Front.Immunol.[免疫学 前沿],5:423,2014。
白介素-10
白介素-10(IL-10)是参与多种免疫调节过程的炎性细胞因子。IL-10通过由两个IL-10受体-1(IL10R1)和两个IL-10受体-2(IL-10R2)蛋白组成的受体复合物发出信号。IL-10的生物活性形式是与IL-10R1/IL-10R2结合并通过Jak1/Tyk2和stat3路径发出信号的同二聚体。与IL-10R2相比,IL-10对IL-10R1的亲和力更高。IL-10表达为包含18个氨基酸的信号肽的178个氨基酸的蛋白质。IL-10同二聚体二级结构表现为螺旋-转角-螺旋结构域交换,每个结构域由6个α-螺旋组成,即A、B、C、D、E和F螺旋。人IL-10的核苷酸和氨基酸序列分别在SEQ ID NO:1和SEQ ID NO:2中列出。SEQ ID NO:2是指缺乏信号序列的成熟人IL-10。
人IL-10(hIL-10)与爱泼斯坦巴尔(Epstein Barr)病毒IL-10(vIL-10)具有约83%序列同一性和相似的二级结构。vIL-10抑制炎性细胞因子产生并抑制巨噬细胞中MHCII表达,并且预防T细胞增殖。vIL-10不共刺激胸腺细胞和肥大细胞增殖,也不诱导B细胞MHC II类表达,并且对细胞表面IL-10R1的亲和力较低。Ala87(人的Ile)是参与降低vIL-10的免疫刺激活性的关键残基。
人IL-10与食蟹猴IL-10(食蟹猴IL-10)具有大约96%序列同一性,而人IL-10R1与食蟹猴IL-10R1具有大约93%序列同一性。人和食蟹猴IL-10R1之间结合界面处有4个氨基酸的差异。I45T和E46G是在与IL-10的AB环相互作用的环上,尽管相互作用主要是主链。A189T和S192T在与螺旋A相互作用的环上,但与IL-10没有直接的作用。在IL-10中,人和食蟹猴IL-10的IL-10R1结合界面附近有2个氨基酸的差异,人的N21和L46均与IL-10/IL-10R1相互作用表面相邻。
先前的研究已经表明,IL-10对髓细胞的抑制足以治疗炎性肠病(IBD)。然而,剂量限制毒性已经阻碍了IL-10的临床功效。为了避免这个问题,本文提供了IL-10的突变蛋白,其设计为具有降低的活性以最小化全身性不良副作用但仍保留用于治疗IBD的免疫抑制特性。用活性减弱的IL-10突变蛋白治疗可以减轻细胞因子的一些免疫刺激作用。为了解决优选的免疫抑制作用可能下降的问题,IL-10突变蛋白与靶向部分(例如,抗体)融合,以增加单核细胞、调节性T细胞和CD4+T细胞中的局部浓度。
IL-10的突变蛋白靶向IL-10蛋白的不同部分,包括在螺旋A、螺旋F和AB环中与IL-10R1相互作用的位点Ia和在螺旋A、螺旋F、AB环、螺旋B、螺旋C、CD环、和螺旋E中与IL-10R1相互作用的位点Ib。突变蛋白包括在以下残基中的一个或多个处的变化:位点Ia(螺旋A),K34、T35、Q38;位点Ia(螺旋F),I136、Y137、K138、S141、E142、D144、I145;位点Ib(螺旋A),H14、F15、M22、P20、L23、R24、R27、D28;位点Ib(F),E151、M154、M156、K157、N160;位点Ia(AB环),M39、K40、D41、Q42、L43、D44、N45、L46、L47、L48、K49;螺旋B,F56、K57、Y59;螺旋C,L60、E67、Q70、M77、M79;CD环,N82、Q83、D84、P85、D86、I87;螺旋D,A89、H90、S93、T100、L103、H109、R110、L112、E115、N116;或螺旋E,A127、K130。
某些IL-10突变蛋白的氨基酸序列在SEQ ID NO:3-10,以及SEQ ID NO:2138、2140、2142、2144、2146、2148、2150、2152、2154、2156、2158、2160、2162、2164、2166、2168、2170、2172、2174、2176、2178、2180、2182、2360、2362、2364、2366、2368、2370、2372、2374、2376、2378、2380、2382、2384、2386、2388、2390、2392、2394、2396、2398、2400、2402、2404、2406、2408、2410、2412、2414、2416、2418、2420、2422、2424、2426、2428、2430、2432、2434、2436、2438、2440、2442、2444、2446、2448、2450、2452、2454、2456、2458、2460、2462、2464、2466、2468、2470、2472、2474、2476、2478、2480、2482、2484、2486、2488、2490、2492、2494、2496、2500、2502、2504、2506、2508、2510、2512、2514、2516、2518、2520、2522、2524、2526、2528、2530、2532、2534、2536、2538、2540、和2777-2791、以及表1、表16、表17和表21中列出。
本文所述的IL-10突变蛋白和抗原结合蛋白可通过本领域已知的方法进行结合亲和力的筛选。例如,可以使用凝胶迁移率测定、免疫印迹、放射性标记竞争测定、色谱法共分馏、共沉淀、交联、ELISA、表面等离子体共振(SPR)、KinExA等,这些方法描述于例如,Current Protocols in Molecular Biology[分子生物学实验指南],(1999)John Wiley&Sons,纽约中,其通过引用以其整体并入本文。
与wt IL-10活性相比,本披露的IL-10突变蛋白优选地具有降低的效力。在多个实施例中,与wt IL-10相比,IL-10突变蛋白具有约10倍至约5000倍的降低的效力。在多个实施例中,IL-10突变蛋白具有低约10倍至1000倍的效力、低约50倍至500倍的效力、约100倍至500倍或更低的效力。在多个实施例中,在LPS刺激测定中测量效力。在一些实施例中,测定读数是单核细胞/髓细胞中LPS诱导的TNFα产生。
抗原结合蛋白和抗体
免疫球蛋白可变结构域表现出通过三个高变区或CDR连接的相对保守的框架区(FR)的相同的一般结构。从N-末端到C-末端,轻链和重链二者包含结构域FR1、CDR1、FR2、CDR2、FR3、CDR3和FR4。每个结构域的氨基酸的分配根据Kabat的定义,Sequences ofProteins of Immunological Interest[感兴趣的免疫蛋白的序列](NationalInstitutes of Health[国立卫生研究院]),贝塞斯达,马里兰州(1987和1991)),或Chothia&Lesk,J.Mol.Biol.[分子生物学],196:901-917,1987;Chothia等人,Nature[自 然],342:878-883,1989。
抗体的高变区是指负责抗原结合的抗体的CDR氨基酸残基。高变区包含来自CDR的氨基酸残基[例如,轻链可变结构域中的残基24-34(L1)、50-56(L2)和89-97(L3)以及重链可变结构域中的31-35(H1)、50-65(H2)和95-102(H3),这些如Kabat等人,Sequences of Proteins of Immunological Interest[感兴趣的免疫蛋白的序列],第5版.PublicHealth Service[公共卫生署],National Institutes of Health[国立卫生研究院],贝塞斯达,马里兰州(1991)中所描述]和/或来自高变环的那些残基(例如,轻链可变结构域中的残基26-32(L1)、50-52(L2)和91-96(L3)以及重链可变结构域中的26-32(H1)、53-55(H2)和96-101(H3),这些如[Chothia等人,J.Mol.Biol.[分子生物学]196:901-917(1987)]中所描述)。CDR也已被鉴定,并根据免疫基因学(ImMunoGenTics,IMGT)编号进行编号(Lefranc,M.-P.,The Immunologist[免疫学家],7,132-136(1999);Lefranc,M.-P.等人,Dev.Comp.Immunol.[发展与比较免疫学],27,55-77(2003)),其描述了轻链和重链可变结构域中的CDR位置,如下:CDR1,大约残基27至38;CDR2,大约残基56至65;以及CDR3,大约残基105至116(种系)或残基105至117(重排)。在一个实施例中,预期CDR位于与本文披露的抗体重链或轻链长度大致相似的重链或轻链的轻链可变结构域中的大约残基26-31(L1)、49-51(L2)和88-98(L3)处以及重链可变结构域中的大约残基26-33(H1)、51-58(H2)和97-110(H3)处。然而,本领域技术人员理解,当鉴定特定抗体的序列时,CDR残基的实际位置可能与上述预测的残基不同。如本文披露的CDR是按照Kabat方法(Kabat和Wu,1991)定义的,并使用安进公司(Amgen)参考编号进行编号。安进公司参考编号是基于结构的编号系统,建立在Honegger和Plückthun(J Mol Biol.[分子生物学杂志]309(3):657-70,2001)中描述的抗体可变区的Honegger和Plückthun编号系统的基础上。在多个实施例中,考虑了工程化IgG1抗体。在多个实施例中,抗体是如本文所述的IgG1z或IgG1z-SEFL2抗体。
框架区(或FR)残基是除高变区残基之外的那些可变结构域残基。
如下所述,本文考虑的抗体(包括单克隆、人、人源化、和本文所述的其他抗体),通常重组或通过体外或体内操纵遗传密码的其他方法产生,因此不一定反映自然界中发现的特定抗体。
在多个实施例中,抗原结合蛋白与细胞表面蛋白特异性结合,使得IL-10或IL-10突变蛋白针对特定的细胞类型。此类目标细胞类型包括髓细胞、CD8+T细胞、CD4+T细胞、和B细胞。抗原结合蛋白可以与TREM-1特异性结合,使IL-10部分针对髓细胞;对于CD8+T细胞,与PD1、CD8、LAG3、NKG2D、NKG7或其他CD8+T细胞表面蛋白特异性结合;对于CD4+T细胞,与CD4或其他CD4+T细胞表面蛋白(如CD30、OX40、41BB、ICOS)结合;以及对于B细胞,与CD20、CD19或其他B细胞表面蛋白(如BAFFR)结合。
在多个实施例中,抗原结合蛋白与在免疫检查点调节中发挥作用的细胞表面蛋白特异性结合。此类免疫检查点调节剂包括PD-1、CTLA4、CD28、CD80、CD86等。
在多个实施例中,抗原结合蛋白与在特定组织或器官(例如肠或肺)上比在其他器官或组织上更多地表达的细胞表面蛋白特异性结合。这种组织或器官特异性细胞表面蛋白包括肠道中的MAdCAM1、肺中的表面活性物质或RAGE。IL-10突变蛋白与这种抗原结合蛋白的融合蛋白了用于治疗炎性疾病,如IBD、哮喘、和慢性阻塞性肺病(COPD)。
在多个实施例中,抗原结合蛋白与在肿瘤/癌细胞上比在无癌的细胞中更多地表达的细胞表面蛋白特异性结合。这种肿瘤/癌特异性抗原包括BCMA、CD19、CD20、CD22、CD70、CD123、CEA、CDH3、CLDN6、CLL1、CS1、DCAF4L2、FLT3、GABRP、MageB2、MART-1、MSLN、MUC1(例如,MUC1-C)、MUC12、MUC13、MUC16、mutFGFR3、PRSS21、PSMA、RNF43、STEAP1、STEAP2、TM4SF5、PD-1、CTLA4、EGFR、VEGF、OX40、或FcRL5。
抗TREM-1抗原结合蛋白
先前表征TREM-1信号传导的研究利用TREM-1的激动抗体来模拟受体的配体激活(Tessarz等人,Immunol Lett[免疫学通讯]116(2):111-6,2008;Vandestienne等人,JClin Invest[临床研究杂志]131(2):e142468,2021)。诱饵肽也已被尝试调节TREM-1活性(参见例如,国际专利公开号WO 2014037565 A)。
本披露涵盖编码靶特异性抗体的氨基酸分子的用途。本文所述的抗TREM-1抗原结合蛋白差异地调节人TREM-1与其配体的相互作用。
在一些实施例中,提供了抗原结合蛋白,该抗原结合蛋白包含多肽,该多肽具有与SEQ ID NO:42、62、82、102、122、142、162、182、202、222、242、262、282、302和2186中列出的重链可变区具有至少约65%、70%、75%、80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高同一性的氨基酸序列,和/或与SEQ ID NO:41、61、81、101、121、141、161、181、201、221、241、261、281、301和2185中列出的轻链可变区具有至少约65%、70%、75%、80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高同一性的氨基酸序列,该抗体进一步包含HCDR1、HCDR2、HCDR3、LCDR1、LCDR2或LCDR3中的至少一个、两个、三个、四个、五个或全部。在一些实施例中,与轻链可变区具有百分比同一性的氨基酸序列可以包含轻链CDR的一个、两个或三个。在其他实施例中,与重链可变区具有百分比同一性的氨基酸序列可以包含重链CDR的一个、两个或三个。
在另一个实施例中,提供了抗原结合蛋白,该抗原结合蛋白包含多肽,该多肽具有与以上列出的抗体序列的重链可变区中的所有三个HCDR或以下CDR具有至少约65%、70%、75%、80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更多同一性的氨基酸序列:SEQ ID NO:36、56、76、96、116、136、156、176、196、216、236、256、276、296和2196中列出的重链CDR1序列;重链CDR2序列在SEQ ID NO:37、57、77、97、117、137、157、177、197、217、237、257、277、297和2197中列出;以及SEQ ID NO:38、58、78、98、118、138、158、178、198、218、238、258、278、298和2198中列出的重链CDR3序列。
在相关的实施例中,提供了抗原结合蛋白,该抗原结合蛋白包含多肽,该多肽具有与以上列出的抗体序列的轻链可变区中的所有三个LCDR或以下CDR具有至少约65%、70%、75%、80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更多同一性的氨基酸序列:轻链CDR1序列在SEQ IDNO:30、50、70、90、110、130、150、170、190、210、230、250、270、290和2190中列出;轻链CDR2序列在SEQ ID NOS:31、51、71、91、111、131、151、171、191、211、231、251、271、291和2191中列出;轻链CDR3序列在SEQ ID NO:32、52、72、92、112、132、152、172、192、212、232、252、272、292和2192中列出。
预期本披露的抗体可在抗体的CDR区具有一个、两个或更多个氨基酸取代,例如非保守或保守取代。还考虑了本文披露的TREM-1抗体重链和轻链CDR和/或可变区序列的共有序列。例如,TREM-1抗体或抗原结合蛋白/融合蛋白可以包含以下序列。在多个实施例中,TREM-1抗体包含抗原结合结构域,该抗原结合结构域包含具有包含选自下组的LCDR1氨基酸序列的轻链可变区的序列,该组由以下组成:X1ASQSX2X3X4NLA(SEQ ID NO:2199),其中X1是R或Q,其中X2是V或I,其中X3是N或S,并且其中X4是S、H、I、V或A;QASX1DIX2X3X4LN(SEQ IDNO:2204),其中X1是R或Q,其中X2是R、S、N或F,其中X3是K或N,并且其中X4是H、Y或D;RASQSVNSNLA(SEQ ID NO:2212);QASQDIRKHLN(SEQ ID NO:2213);RASQDISSNLN(SEQ IDNO:2214);QASQDIHLN(SEQ ID NO:2215);RASQGIRKWLA(SEQ ID NO:2216)或RASQSVNSNLA(SEQ ID NO:2217)以及SGDKLGERVS(SEQ ID NO:2218)。
在多个实施例中,TREM-1抗体包含抗原结合结构域,该抗原结合结构域包含具有包含选自下组的LCDR2氨基酸序列的轻链可变区的序列,该组由以下组成:GAX1X2RAT(SEQID NO:2200),其中X1是S或Y,并且其中X2是T或I;氨基酸序列X1X2X3X4LET(SEQ ID NO:2206),其中X1是D、G或H,其中X2是A、V或T,其中X3是S、A或Y,并且其中X4是T或N;GASTRAT(SEQ ID NO:2219);DASNLET(SEQ ID NO:2220);以及AASRLQS(SEQ ID NO:2221)。
在多个实施例中,TREM-1抗体包含抗原结合结构域,该抗原结合结构域包含具有包含选自下组的LCDR3氨基酸序列的轻链可变区的序列,该组由以下组成:QX1X2X3X4X5X6PX7T(SEQ ID NO:2201);其中X1是Q、H或E,其中X2是F或Y,其中X3是K、Y或I,其中X4是N、T、L、I、或M;其中X5是W、F、H或Y,其中X6不存在或是P;其中X7是W、N、Y、H或L;QX1YX3X4X5PX6T(SEQ ID NO:2207),其中X1是Q或H,其中X2是D、A或G,其中X3是N或K;其中X4是L或I,并且其中X5是I或L;QQFKNWPPT(SEQ ID NO:2222);QHYDNLPIT(SEQ ID NO:2223);LQAHGFPWT(SEQ ID NO:2224);QQYDNLPLT(SEQ ID NO:2225)以及QFWPPWT(SEQ ID NO:2226)。
在多个实施例中,TREM-1抗体包含抗原结合结构域,该抗原结合结构域包含具有包含选自下组的HCDR1氨基酸序列的重链可变区的序列,该组由以下组成:X1X2X3MX4(SEQID NO:2202),其中X1是A、R、T或S,其中X2是Y或N,其中X3是A或W,并且其中X4是S或N;序列X1YDIN(SEQ ID NO:2208),其中X1是R或S;GYYX1H(SEQ ID NO:2723),其中X1是M或I;AYAMS(SEQ ID NO:2227);RYDIN(SEQ ID NO:2228);以及SYWMS(SEQ ID NO:2229)。
在多个实施例中,TREM-1抗体包含抗原结合结构域,该抗原结合结构域包含具有包含选自下组的HCDR2氨基酸序列的重链可变区的序列,该组由以下组成:X1X2X3X4X5X6 X7X8 X9YYX10 X11X12VKG(SEQ ID NO:2205),其中X1是T、E、或S,其中X2不存在或是M、V、或I,其中X3是S、R或K,其中X4是G或Q,其中X5是S、D或H,其中X6是G、S、L、或A,其中X7是S、G、或R,其中X8是T、S、P或E,其中X9是T或I,其中X10是A或V,其中X11是D或E,并且其中X12是S或A;X1X2NPX3X4GX5X6GX7 X8X9X10FX11X12(SEQ ID NO:2209),其中X1是W或R,其中X2是M或L,其中X3是N、Q、或K,其中X4是S、A、或R,其中X5是N、或Q,其中X6是S、A、或T,其中X7是S、Q、或Y,其中X8是V或T,其中X9是Q或K,其中X10是K或N,其中X11是R或Q,并且其中X12是G或D;TSGSGSTTYYADSVKG(SEQ ID NO:2230);WMNPNSGNSSVQKFRG(SEQ ID NO:2231);NIKQDGSEEYYVDSVKG(SEQ ID NO:2232);以及TSGSGTYYADSVKG(SEQ ID NO:2669)。
在多个实施例中,TREM-1抗体包含抗原结合结构域,该抗原结合结构域包含具有包含选自下组的HCDR3氨基酸序列的重链可变区的序列,该组由以下组成:X1X2X3X4X5X6 X7F X8YYX9(SEQ ID NO:2203),其中X1是V、E、A或G,其中X2是A、F、Y或G,其中X3是G、S、Y或W,其中X4是S或R,其中X5不存在或是N,其中X6是F、S、Y、或不存在,其中X7是L或F或不存在,其中X8是D或E,并且其中X9是Y、H或S;X1X2X3X4 X5X6 X7 X8X9X10X11X12FX13X14(SEQ ID NO:2210);其中X1是G、L或R,其中X2是G、I、或R,其中X3是Y、R、I、G、或A,其中X4是T、S、Y、或V,其中X5是S或Y,其中X6是S、A、I、或R,其中X7是W、A、或S,其中X8不存在或是S,其中X9不存在或是F、W、或Y,其中X10是R、S、H、K、或E,其中X11是W、H、Y、或F,其中X12是Y、V、A、或S,其中X13是D或Q,并且其中X14是L、Y、I、或H;VAGSNFLFDY(SEQ ID NO:2670);GGYTSSWRWYFDL(SEQ ID NO:2671);GGYTSSWSRWYFDL(SEQ ID NO:2672);以及DYGDSFDY(SEQ ID NO:2673)。
在多个实施例中,抗TREM-1抗原结合蛋白或抗原结合蛋白的抗TREM1抗原结合部分包含选自以下的一组CDR序列:
i)SEQ ID NO:30(LCDR1)、SEQ ID NO:31(LCDR2)、SEQ ID NO:32(LCDR3)、SEQ IDNO:36(HCDR1)、SEQ ID NO:37(HCDR2)和SEQ ID NO:38(HCDR3);
ii)SEQ ID NO:50(LCDR1)、SEQ ID NO:51(LCDR2)、SEQ ID NO:52(LCDR3)、SEQ IDNO:56(HCDR1)、SEQ ID NO:57(HCDR2)和SEQ ID NO:58(HCDR3);
iii)SEQ ID NO:70(LCDR1)、SEQ ID NO:71(LCDR2)、SEQ ID NO:72(LCDR3)、SEQID NO:76(HCDR1)、SEQ ID NO:77(HCDR2)和SEQ ID NO:78(HCDR3);
iv)SEQ ID NO:90(LCDR1)、SEQ ID NO:91(LCDR2)、SEQ ID NO:92(LCDR3)、SEQ IDNO:96(HCDR1)、SEQ ID NO:97(HCDR2)和SEQ ID NO:98(HCDR3);
v)SEQ ID NO:110(LCDR1)、SEQ ID NO:111(LCDR2)、SEQ ID NO:112(LCDR3)、SEQID NO:116(HCDR1)、SEQ ID NO:117(HCDR2)和SEQ ID NO:118(HCDR3);
vi)SEQ ID NO:130(LCDR1)、SEQ ID NO:131(LCDR2)、SEQ ID NO:132(LCDR3)、SEQID NO:136(HCDR1)、SEQ ID NO:137(HCDR2)和SEQ ID NO:138(HCDR3);
vii)SEQ ID NO:150(LCDR1)、SEQ ID NO:151(LCDR2)、SEQ ID NO:152(LCDR3)、SEQ ID NO:156(HCDR1)、SEQ ID NO:157(HCDR2)和SEQ ID NO:158(HCDR3);
viii)SEQ ID NO:170(LCDR1)、SEQ ID NO:171(LCDR2)、SEQ ID NO:172(LCDR3)、SEQ ID NO:176(HCDR1)、SEQ ID NO:177(HCDR2)和SEQ ID NO:178(HCDR3);
ix)SEQ ID NO:190(LCDR1)、SEQ ID NO:191(LCDR2)、SEQ ID NO:192(LCDR3)、SEQID NO:196(HCDR1)、SEQ ID NO:197(HCDR2)和SEQ ID NO:198(HCDR3);
x)SEQ ID NO:210(LCDR1)、SEQ ID NO:211(LCDR2)、SEQ ID NO:212(LCDR3)、SEQID NO:216(HCDR1)、SEQ ID NO:217(HCDR2)和SEQ ID NO:218(HCDR3);
xi)SEQ ID NO:230(LCDR1)、SEQ ID NO:231(LCDR2)、SEQ ID NO:232(LCDR3)、SEQID NO:236(HCDR1)、SEQ ID NO:237(HCDR2)和SEQ ID NO:238(HCDR3);
xii)SEQ ID NO:250(LCDR1)、SEQ ID NO:251(LCDR2)、SEQ ID NO:252(LCDR3)、SEQ ID NO:256(HCDR1)、SEQ ID NO:257(HCDR2)和SEQ ID NO:258(HCDR3);
xiii)SEQ ID NO:270(LCDR1)、SEQ ID NO:271(LCDR2)、SEQ ID NO:272(LCDR3)、SEQ ID NO:276(HCDR1)、SEQ ID NO:277(HCDR2)和SEQ ID NO:278(HCDR3);
xiv)SEQ ID NO:290(LCDR1)、SEQ ID NO:291(LCDR2)、SEQ ID NO:292(LCDR3)、SEQ ID NO:296(HCDR1)、SEQ ID NO:297(HCDR2)和SEQ ID NO:298(HCDR3);和
xv)SEQ ID NO:2190(LCDR1)、SEQ ID NO:2191(LCDR2)、SEQ ID NO:2192(LCDR3)、SEQ ID NO:2196(HCDR1)、SEQ ID NO:2197(HCDR2)和SEQ ID NO:2198(HCDR3)。
在多个实施例中,抗TREM-1抗原结合蛋白或抗原结合蛋白的抗TREM1抗原结合部分包含选自以下的一组CDR序列:
i)SEQ ID NO:30(LCDR1)、SEQ ID NO:31(LCDR2)、SEQ ID NO:32(LCDR3)、SEQ IDNO:36(HCDR1)、SEQ ID NO:37(HCDR2)和SEQ ID NO:38(HCDR3);
ii)SEQ ID NO:50(LCDR1)、SEQ ID NO:51(LCDR2)、SEQ ID NO:52(LCDR3)、SEQ IDNO:56(HCDR1)、SEQ ID NO:57(HCDR2)和SEQ ID NO:58(HCDR3);
iii)SEQ ID NO:70(LCDR1)、SEQ ID NO:71(LCDR2)、SEQ ID NO:72(LCDR3)、SEQID NO:76(HCDR1)、SEQ ID NO:77(HCDR2)和SEQ ID NO:78(HCDR3);
iv)SEQ ID NO:110(LCDR1)、SEQ ID NO:111(LCDR2)、SEQ ID NO:112(LCDR3)、SEQID NO:116(HCDR1)、SEQ ID NO:117(HCDR2)和SEQ ID NO:118(HCDR3);
v)SEQ ID NO:150(LCDR1)、SEQ ID NO:151(LCDR2)、SEQ ID NO:152(LCDR3)、SEQID NO:156(HCDR1)、SEQ ID NO:157(HCDR2)和SEQ ID NO:158(HCDR3);
vi)SEQ ID NO:170(LCDR1)、SEQ ID NO:171(LCDR2)、SEQ ID NO:172(LCDR3)、SEQID NO:176(HCDR1)、SEQ ID NO:177(HCDR2)和SEQ ID NO:178(HCDR3);和
vii)SEQ ID NO:290(LCDR1)、SEQ ID NO:291(LCDR2)、SEQ ID NO:292(LCDR3)、SEQ ID NO:296(HCDR1)、SEQ ID NO:297(HCDR2)和SEQ ID NO:298(HCDR3)。
在多个实施例中,抗TREM-1抗原结合蛋白或抗原结合蛋白的抗TREM1抗原结合部分包含选自以下的一组CDR序列:轻链SEQ ID NO:50(LCDR1)、SEQ ID NO:51(LCDR2)、SEQID NO:52(LCDR3)、SEQ ID NO:56(HCDR1)、SEQ ID NO:57(HCDR2)和SEQ ID NO:58(HCDR3);和重链SEQ ID NO:110(LCDR1)、SEQ ID NO:111(LCDR2)、SEQ ID NO:112(LCDR3)、SEQ IDNO:116(HCDR1)、SEQ ID NO:117(HCDR2)和SEQ ID NO:118(HCDR3)。
在相关的实施例中,框架的残基发生改变。可以改变的重链框架区位于指定的H-FR1、H-FR2、H-FR3和H-FR4区内,这些区围绕着重链CDR残基,并且可以改变的轻链框架区的残基位于指定的L-FR1、L-FR2、L-FR3和L-FR4区内,这些区围绕着轻链CDR残基。框架区内的氨基酸可以被替代,例如,用人框架或人共有框架中鉴定的任何合适的氨基酸替代。进一步考虑了框架区可以发生改变,但本文所述的抗原结合蛋白或抗体保留了亲本抗体的CDR、LCDR1-3和/或HCDR-3。
抗体片段包含完整全长抗体的一部分,优选完整抗体的抗原结合区或可变区。抗体片段的实例包括Fab、Fab’、F(ab’)2、Fcab、和Fv片段;双抗体;线性抗体;单链抗体分子(例如,scFv);多特异性抗体片段,如双特异性、三特异性等抗体(例如,双抗体、三抗体、四抗体);微型抗体;螯合重组抗体;三抗体或双抗体;内抗体;纳米抗体;结合结构域免疫球蛋白融合蛋白;骆驼化抗体;含有VHH的抗体;以及从抗体片段形成的其他多肽。参见例如,Holliger&Hudson,2005 Nat.Biotech.[自然生物技术]23:1126-36;Eyer&Hruska,Veterinarni Medicina[兽医学]57:439-513,2012。
本披露的抗原结合化合物优选地保留10-8、10-9、10-10、10-11、10-12、10-13、10-14、10-15M或更小的对TREM-1的结合亲和力,如通过表面等离子体共振或KinexA测量的。本披露的抗原结合化合物对TREM-1具有从10-9至10-12、或从10-10至10-13、或从10-10至10-15M的结合亲和力。使用标准方法,例如,在25℃(例如,室温)下进行SPR测定。
在多个实施例中,抗体是IgG1抗体。在某些实施例中,抗体是IgG1z抗体。
本文提供了结合TREM-1的全长抗体的实例,这些全长抗体具有SEQ ID NO:26、46、66、86、106、126、146、166、186、206、226、246、266、286和2186中列出的重链氨基酸序列;以及SEQ ID NO:25、45、65、85、105、125、145、165、185、205、225、245、265、285和2185中列出的相应的轻链氨基酸序列。
包含IL-10的抗原结合蛋白
本文进一步考虑了IL-10突变蛋白与抗体或靶向免疫细胞亚群的其他结合蛋白之间的抗原结合蛋白。示例性抗体或抗原结合蛋白包括靶向TREM-1或靶向检查点抑制剂的抗体或结合蛋白,如PD-1、PD-L1、PD-L2、CTLA4、靶向TNFα的抗体或结合蛋白、或靶向IL-12/IL-23的抗体或结合蛋白。
针对检查点抑制剂的抗体包括但不限于PD-1抗体,如派姆单抗(默沙东公司(Merck Sharp&Dohme Corp.))、纳武单抗(时美施贵宝公司(Bristol-Myers Squibb)),以及描述于以下中的针对PD-1的抗体:美国专利号8,735,553;8,617,546;8,008,449、8,741,295、8,552,154、8,354,509、8,779,105、7,563,869、8,287,856、8,927,697、8,088,905、7,595,048、8,168,179、6,808,710、7,943,743、8,246,955、和8,217,149以及国际专利公开WO 2019/140196;抗CTLA-4抗体,如伊匹单抗和曲美木单抗,以及抗PD-L1抗体,如度伐鲁单抗。
IL-10突变蛋白/抗TREM-1抗体抗原结合蛋白的示例性序列在SEQ ID NO:863、865、867、869、871、873、875、877、879、881、883、885、887、889、891、893、895、897、899、901、903、905、907、909、911、913、915、917、919、921、923、925、927、929、931、933、935、937、939、941、943、945、947、949、951、953、955、957、959、961、963、965、967、969、971、973、975、977、979、981、983、985、987、989、991、993、995、997、999、1001、1003、1005、1007、1009、1011、1013、1015、1017、1019、1021、1023、1025、1027、1029、1031、1033、1035、1037、1039、1041、1043、1045、1047、1049、1051、1053、1055、1057、1059、1061、1063、1065、1067、1069、1071、1073、1075、1077、1079、1081、1083、和1085,以及SEQ ID NO:864、866、868、870、872、874、876、878、880、882、884、886、888、890、892、894、896、898、900、902、904、906、908、910、912、914、916、918、920、922、924、926、928、930、932、934、936、938、940、942、944、946、948、950、952、954、956、958、960、962、964、966、968、970、972、974、976、978、980、982、984、986、988、990、992、994、996、998、1000、1002、1004、1006、1008、1010、1012、1014、1016、1018、1020、1022、1024、1026、1028、1030、1032、1034、1036、1038、1040、1042、1044、1046、1048、1050、1052、1054、1056、1058、1060、1062、1064、1066、1068、1070、1072、1074、1076、1078、1080、1082、1084、和1086中列出。另外的TREM-1重链IL10抗原结合蛋白在SEQ ID NO:2137、2139、2141、2143、2145、2147、2149、2151、2153、2155、2157、2159、2161、2163、2165、2167、2169、2171、2173、2175、2177、2179、2181、2359、2361、2363、2365、2367、2369、2371、2373、2375、2377、2379、2381、2383、2385、2387、2389、2391、2393、2395、2397、2399、2401、2403、2405、2407、2409、2411、2143、2415、2417、2419、2421、2423、2425、2427、2429、2431、2433、2435、2437、2439、2441、2443、2445、2447、2449、2451、2453、2455、2457、2459、2461、2463、2465、2467、2469、2471、2473、2475、2477、2479、2481、2483、2485、2487、2489、2491、2493、2495、2497、2498、2499、2501、2503、2505、2507、2509、2511、2513、2515、2517、2519、2521、2523、2525、2527、2529、2531、2533、2535、2537、2539和2726-2776中列出。
单价抗TREM-1抗体抗原结合蛋白的实例在氨基酸SEQ ID NO:1087至1422和表13B中列出。
编码包含IL-10突变蛋白的抗原结合蛋白和抗TREM-1抗体的核酸在SEQ ID NO:303至862中列出,TREM-1变体抗体重链可变区在SEQ ID NO:2012、2014、2016、2018、2020、2022、2024、2026、2028、2030、2032、2034、2036、2038、2040、2042、2044、2046、2048、2050、2052、2054、2056、2058、2060、2062、2064、2066、2068、2070、2072、2074、2076、2078、2080、2082、2084、2086、2088、2090、2092、2094、2096、2098、2100、2102、2104、2106、2108、2110、2112、2114、2116、2118、2120、2122、2124、2126、2128、2130、2132、2134、和2136中列出,以及TREM-1变体抗体轻链可变区在SEQ ID NO:2234、2236、2238、2240、2242、2244、2246、2248、2250、2252、2254、2256、2258、2260、2262、2264、2266、2268、2270、2272、2274、2276、2278、2280、2282、2284、2286、2288、2290、2292、2294、2296、2298、2300、2302、2304、2306、2308、2310、2312、2314、2316、2318、2320、2322、2324、2326、2328、2330、2332、2334、2336、2338、2340、2342、2344、2346、2348、2350、2352、2354、2356、和2358中列出。
本文提供了抗原结合蛋白,其包含抗原结合部分和一个或两个IL-10部分,其中:a.该抗原结合部分是抗体或抗体片段,b.每个IL-10部分独立地是单价或二价,c.每个IL-10部分独立地选自具有与SEQ ID NO:2具有90%同一性的序列的一种或多种人IL-10突变蛋白,并且d.至少一个IL-10部分与该抗原结合部分共价结合。在多个实施例中,至少一个IL-10部分与抗原结合部分的C末端融合。
在抗原结合蛋白的多个实施例中:a.抗原结合部分是抗体,并且b.IL-10部分与该抗体的每条重链融合。
在抗原结合蛋白的多个实施例中,每个IL-10部分是单体。在多个实施例中,抗原结合蛋白包含两种不同的突变蛋白单体。在多个实施例中,抗原结合蛋白包含两种相同的突变蛋白单体。
在多个实施例中,对于抗原结合蛋白:每个IL-10部分包含与SEQ ID NO:2中列出的氨基酸序列具有至少90%同一性的氨基酸序列,并且每个IL-10部分独立地包含选自以下的至少一个突变:螺旋环AB、螺旋环CD、螺旋环DE、螺旋A、螺旋B、螺旋C、螺旋D、螺旋E和/或螺旋F中的突变。
在多个实施例中,至少一个IL-10部分包含螺旋A中的至少一个突变。在多个实施例中,至少一个IL-10部分包含螺旋F中的至少一个突变。在多个实施例中,至少一个IL-10部分包含螺旋环AB中的至少一个突变。
在多个实施例中,与wt IL-10相比,IL-10突变蛋白减少了髓细胞中TNF-α产生方面的抑制,降低了CD8+T细胞刺激方面的水平,和/或降低了B细胞刺激方面的水平。
在多个实施例中,IL-10突变蛋白抗原结合蛋白抑制髓细胞中TNF-α产生。在多个实施例中,IL-10突变蛋白抗原结合蛋白抑制髓细胞中TNF-α产生,同时减少CD8+T细胞和B细胞激活。
在多个实施例中,治疗抑制单核细胞中TNF-α产生,而受试者中无CD8+T细胞刺激和/或B细胞刺激。
在多个实施例中,每个IL-10突变蛋白独立地包含SEQ ID NO:2的残基N10、H14、F15、P20、M22、L23、R24、R27、D28、K34、T35、Q38、M39、K40、D41、Q42、L43、D44、N45、L46、L47、L48、K49、F56、K57、Y59、L60、Q3、E67、Q70、M77、Q79、N82、Q83、D84、P85、D86、I87、A89、H90、S93、T100、L103、H109、R110、L112、E115、N116、A127、K130、I136、Y137、K138、S141、E142、D144、I145、E151、M154、M156、K157、N160中的一个或多个中的突变,和/或在螺旋D和螺旋E之间添加4-8个氨基酸。
在多个实施例中,每个IL-10突变蛋白与SEQ ID NO:2中列出的氨基酸序列具有至少95%同一性。在多个实施例中,每个IL-10突变蛋白独立地包含选自下组的一个或多个突变,该组由以下组成:SEQ ID NO:2的R27L、K34D、D41G、L46K、Q38E、Q38R、Q38D、K138L、K138D、或I87A,任选地包含在螺旋D和螺旋E之间添加氨基酸。在多个实施例中,每个IL-10突变蛋白独立地包含选自下组的一个或多个突变,该组由以下组成:N10Q、N10I、N10K、R27L、K34D、D41G、L46K、Q38E、Q38R、Q38D、K138L、K138D、I87A、H14Q、F15Y、M22V、K49T、K49S、F56Y、K57N、Y59T、L60Q、Q63E、Q63L、E67C、Q70E、Q70K、M77R、M77V、Q79R、Q79C、D84R、A89P、H90E、H90Q、S93E、S93Q、T100R、L103E、H109D、R110P、R110Q、L112V、E115K、N116D、N116Q、A127M、K130Q、I136C、Y137C、M154V、M156C、K157N、或N160D,任选地包含在螺旋D和螺旋E之间添加氨基酸。在多个实施例中,螺旋D和螺旋E之间的氨基酸是GGGSGG(SEQ ID NO:2676)。任选地,IL-10突变蛋白具有如表1、表16、表17或表21中列出的突变的组合。
在多个实施例中,每个IL-10突变蛋白与SEQ ID NO:2中列出的氨基酸序列具有至少95%同一性。在多个实施例中,每个IL-10突变蛋白独立地包含选自下组的一个或多个突变,该组由以下组成:SEQ ID NO:2的N10、R27L、K34D、D41G、L46K、Q38E、Q38R、Q38D、K138L、K138D、或I87A,任选地包含在螺旋D和螺旋E之间添加六个氨基酸。在多个实施例中,每个IL-10突变蛋白独立地包含选自下组的一个或多个突变,该组由以下组成:SEQ ID NO:2的N10Q、N10I、N10K、R27L、K34D、D41G、L46K、Q38E、Q38R、Q38D、K138L、K138D、I87A、H14Q、F15Y、M22V、K49T、K49S、F56Y、K57N、Y59T、L60Q、Q63E、Q63L、E67C、Q70E、Q70K、M77R、M77V、Q79R、Q79C、D84R、A89P、H90E、H90Q、S93E、S93Q、T100R、L103E、H109D、R110P、R110Q、L112V、E115K、N116D、N116Q、A127M、K130Q、I136C、Y137C、M154V、M156C、K157N、或N160D,任选地包含在螺旋D和螺旋E之间添加六个氨基酸。在多个实施例中,螺旋D和螺旋E之间的氨基酸是GGGSGG(SEQ ID NO:2676)。在多个实施例中,IL-10突变蛋白的氨基酸序列在SEQ ID NO:3-10,以及SEQ ID NO:2138、2140、2142、2144、2146、2148、2150、2152、2154、2156、2158、2160、2162、2164、2166、2168、2170、2172、2174、2176、2178、2180、2182、2360、2362、2364、2366、2368、2370、2372、2374、2376、2378、2380、2382、2384、2386、2388、2390、2392、2394、2396、2398、2400、2402、2404、2406、2408、2410、2412、2414、2416、2418、2420、2422、2424、2426、2428、2430、2432、2434、2436、2438、2440、2442、2444、2446、2448、2450、2452、2454、2456、2458、2460、2462、2464、2466、2468、2470、2472、2474、2476、2478、2480、2482、2484、2486、2488、2490、2492、2494、2496、2500、2502、2504、2506、2508、2510、2512、2514、2516、2518、2520、2522、2524、2526、2528、2530、2532、2534、2536、2540和2777-2791中列出。
在多个实施例中,抗原结合蛋白包含与抗原结合部分的至少一个C末端融合的至少一个接头,并且IL-10突变蛋白部分与每个接头的C末端共价结合。在多个实施例中,接头为4至18个氨基酸长。在多个实施例中,接头为六个氨基酸长。在多个实施例中,接头是3聚体、4聚体、5聚体、6聚体、7聚体或8聚体肽。在多个实施例中,接头包含GS残基。下文描述了所考虑的另外的接头。
在多个实施例中,抗原结合蛋白进一步包含连接至抗原结合蛋白的抗体部分的所述重链可变区的人重链恒定区。在多个实施例中,抗原结合蛋白进一步包含连接至所述抗原结合蛋白的抗体部分的轻链可变区的人轻链恒定区。
在抗原结合蛋白的多个实施例中,抗原结合部分选自由以下组成的组:人抗体、人源化抗体、嵌合抗体、单克隆抗体、重组抗体、Fab、F(ab’)2、Fab2、单价IgG、scFv、scFv-Fc、IgG1抗体、IgG2抗体、IgG3抗体、和IgG4抗体。在多个实施例中,抗原结合部分是IgG。在多个实施例中,抗原结合部分是IgG2抗体。在多个实施例中,抗原结合部分是IgG1抗体。在多个实施例中,抗体是IgG1z抗体。在多个实施例中,抗原结合部分是单价IgG。在多个实施例中,抗原结合部分的重链恒定区选自IgG、IgM、IgA、IgD、IgE的重链恒定区、其片段、其组合、以及其修饰,这些修饰中一个至十个重链框架氨基酸被来自另一人抗体恒定区的相应的一个或多个氨基酸替代。
在抗原结合蛋白的多个实施例中,抗原结合部分与具有SEQ ID NO:22中列出的氨基酸序列的人PD-1结合。在多个实施例中,抗原结合部分与具有SEQ ID NO:20中列出的氨基酸序列的人TREM-1结合。在多个实施例中,抗原结合部分以至少10-8M的结合亲和力与人TREM-1结合。
在多个实施例中,抗原结合部分以10-8M至10-15M或10-8M至10-12M,或10-8M、10-9M、10-10M、10-11M、10-12M、10-13M、10-14M、或10-15M的结合亲和力结合其抗原。
在抗原结合蛋白的多个实施例中,抗TREM-1抗原结合部分包含:
a.轻链可变结构域,其包含:
i.轻链CDR1,其包含选自SEQ ID NO:30、50、70、90、110、130、150、170、190、210、230、250、270、290和2190的氨基酸序列;
ii.轻链CDR2,其包含选自SEQ ID NO:31、51、71、91、111、131、151、171、191、211、231、251、271、291和2191的氨基酸序列;
iii.轻链CDR3,其包含选自SEQ ID NO:32、52、72、92、112、132、152、172、192、212、232、252、272、292和2192的氨基酸序列;和
b.包含重链可变结构域,该重链可变结构域包含:
i.重链CDR1,其包含选自SEQ ID NO:36、56、76、96、116、136、156、176、196、216、236、256、276、296和2196的氨基酸序列;
ii.重链CDR2,其包含选自SEQ ID NO:37、57、77、97、117、137、157、177、197、217、237、257、277、297和2197的氨基酸序列;和
iii.重链CDR3,其包含选自SEQ ID NO:38、58、78、98、118、138、158、178、198、218、238、258、278、298和2198的氨基酸序列。
在抗原结合蛋白的多个实施例中,
a.轻链CDR1序列在SEQ ID NO:30、50、70、110、150、170、或290中列出;
b.轻链CDR2序列在SEQ ID NO:31、51、71、111、151、171、或291中列出;
c.轻链CDR3序列在SEQ ID NO:32、52、72、112、152、172、或292中列出;
d.重链CDR1序列在SEQ ID NO:36、56、76、116、156、176、或296中列出;
e.重链CDR2序列在SEQ ID NO:37、57、77、117、157、177、或297中列出;和
f.重链CDR3序列在SEQ ID NO:38、58、78、118、158、178、或298中列出。
在抗原结合蛋白的多个实施例中,
a.轻链CDR1序列在SEQ ID NO:50或110中列出;
b.轻链CDR2序列在SEQ ID NO:51或111中列出;
c.轻链CDR3序列在SEQ ID NO:52或112中列出;
d.重链CDR1序列在SEQ ID NO:56或116中列出;
e.重链CDR2序列在SEQ ID NO:57或117中列出;和
f.重链CDR3序列在SEQ ID NO:58或118中列出。
在抗原结合蛋白的多个实施例中,抗原结合蛋白包含一组选自以下的CDR序列:
i)SEQ ID NO:30(LCDR1)、SEQ ID NO:31(LCDR2)、SEQ ID NO:32(LCDR3)、SEQ IDNO:36(HCDR1)、SEQ ID NO:37(HCDR2)和SEQ ID NO:38(HCDR3);
ii)SEQ ID NO:50(LCDR1)、SEQ ID NO:51(LCDR2)、SEQ ID NO:52(LCDR3)、SEQ IDNO:56(HCDR1)、SEQ ID NO:57(HCDR2)和SEQ ID NO:58(HCDR3);
iii)SEQ ID NO:70(LCDR1)、SEQ ID NO:71(LCDR2)、SEQ ID NO:72(LCDR3)、SEQID NO:76(HCDR1)、SEQ ID NO:77(HCDR2)和SEQ ID NO:78(HCDR3);
iv)SEQ ID NO:90(LCDR1)、SEQ ID NO:91(LCDR2)、SEQ ID NO:92(LCDR3)、SEQ IDNO:96(HCDR1)、SEQ ID NO:97(HCDR2)和SEQ ID NO:98(HCDR3);
v)SEQ ID NO:110(LCDR1)、SEQ ID NO:111(LCDR2)、SEQ ID NO:112(LCDR3)、SEQID NO:116(HCDR1)、SEQ ID NO:117(HCDR2)和SEQ ID NO:118(HCDR3);
vi)SEQ ID NO:130(LCDR1)、SEQ ID NO:131(LCDR2)、SEQ ID NO:132(LCDR3)、SEQID NO:136(HCDR1)、SEQ ID NO:137(HCDR2)和SEQ ID NO:138(HCDR3);
vii)SEQ ID NO:150(LCDR1)、SEQ ID NO:151(LCDR2)、SEQ ID NO:152(LCDR3)、SEQ ID NO:156(HCDR1)、SEQ ID NO:157(HCDR2)和SEQ ID NO:158(HCDR3);
viii)SEQ ID NO:170(LCDR1)、SEQ ID NO:171(LCDR2)、SEQ ID NO:172(LCDR3)、SEQ ID NO:176(HCDR1)、SEQ ID NO:177(HCDR2)和SEQ ID NO:178(HCDR3);
ix)SEQ ID NO:190(LCDR1)、SEQ ID NO:191(LCDR2)、SEQ ID NO:192(LCDR3)、SEQID NO:196(HCDR1)、SEQ ID NO:197(HCDR2)和SEQ ID NO:198(HCDR3);
x)SEQ ID NO:210(LCDR1)、SEQ ID NO:211(LCDR2)、SEQ ID NO:212(LCDR3)、SEQID NO:216(HCDR1)、SEQ ID NO:217(HCDR2)和SEQ ID NO:218(HCDR3);
xi)SEQ ID NO:230(LCDR1)、SEQ ID NO:231(LCDR2)、SEQ ID NO:232(LCDR3)、SEQID NO:236(HCDR1)、SEQ ID NO:237(HCDR2)和SEQ ID NO:238(HCDR3);
xii)SEQ ID NO:250(LCDR1)、SEQ ID NO:251(LCDR2)、SEQ ID NO:252(LCDR3)、SEQ ID NO:256(HCDR1)、SEQ ID NO:257(HCDR2)和SEQ ID NO:258(HCDR3);
xiii)SEQ ID NO:270(LCDR1)、SEQ ID NO:271(LCDR2)、SEQ ID NO:272(LCDR3)、SEQ ID NO:276(HCDR1)、SEQ ID NO:277(HCDR2)和SEQ ID NO:278(HCDR3);
xiv)SEQ ID NO:290(LCDR1)、SEQ ID NO:291(LCDR2)、SEQ ID NO:292(LCDR3)、SEQ ID NO:296(HCDR1)、SEQ ID NO:297(HCDR2)和SEQ ID NO:298(HCDR3);和
xv)SEQ ID NO:2190(LCDR1)、SEQ ID NO:2191(LCDR2)、SEQ ID NO:2192(LCDR3)、SEQ ID NO:2196(HCDR1)、SEQ ID NO:2197(HCDR2)和SEQ ID NO:2198(HCDR3)。
在抗原结合蛋白的多个实施例中,抗TREM-1抗原结合部分包含:
a.轻链可变结构域,其包含选自下组的氨基酸序列,该组由以下组成:
i.与选自SEQ ID NO:41、61、81、101、121、141、161、181、201、221、241、261、281、301和2185的氨基酸序列具有至少80%同一性的序列;
ii.由与选自SEQ ID NO:39、59、79、99、119、139、159、179、199、219、239、259、279、299和2183的核酸序列具有至少80%同一性的多核苷酸序列编码的序列;
iii.由在中等严格条件下与由选自SEQ ID NO:39、59、79、99、119、139、159、179、199、219、239、259、279、299和2183的核酸序列组成的多核苷酸的互补序列杂交的多核苷酸编码的序列;和
b.重链可变结构域,其包含选自下组的氨基酸序列,该组由以下组成:
i.与选自SEQ ID NO:42、62、82、102、122、142、162、182、202、222、242、262、282、302和2186的氨基酸序列具有至少80%同一性的序列;
ii.由与选自SEQ ID NO:40、60、80、100、120、140、160、180、200、220、240、260、280、300和2184的氨基酸序列具有至少80%同一性的多核苷酸序列编码的序列;和
iii.由在中等严格条件下与由选自SEQ ID NO:40、60、80、100、120、140、160、180、200、220、240、260、280、300和2186的核酸序列组成的多核苷酸的互补序列杂交的多核苷酸编码的序列。
在抗原结合蛋白的多个实施例中,抗TREM-1抗原结合部分包含:
a.轻链可变结构域,其包含选自下组的氨基酸序列,该组由以下组成:
i.与选自SEQ ID NO:41、61、81、121、161、181、和301的氨基酸序列具有至少80%同一性的序列;
ii.由与选自SEQ ID NO:39、59、79、119、159、179、和299的核酸序列具有至少80%同一性的多核苷酸序列编码的序列;
iii.由在中等严格条件下与由选自SEQ ID NO:39、59、79、119、159、179、和299的核酸序列组成的多核苷酸的互补序列杂交的多核苷酸编码的序列;和
b.重链可变结构域,其包含选自下组的氨基酸序列,该组由以下组成:
i.与选自SEQ ID NO:42、62、82、122、162、182、和302的氨基酸序列具有至少80%同一性的序列;
ii.由与选自SEQ ID NO:40、60、80、120、160、180、和300的氨基酸序列具有至少80%同一性的多核苷酸序列编码的序列;
iii.由在中等严格条件下与由选自SEQ ID NO:40、60、80、120、160、180、和300的核酸序列组成的多核苷酸的互补序列杂交的多核苷酸编码的序列。
在抗原结合蛋白的多个实施例中,抗TREM-1抗原结合部分包含:
a.轻链可变结构域,其包含选自下组的氨基酸序列,该组由以下组成:
i.与选自SEQ ID NO:61和121的氨基酸序列具有至少80%同一性的序列;
ii.由与选自SEQ ID NO:59和119的核酸序列具有至少80%同一性的多核苷酸序列编码的序列;
iii.由在中等严格条件下与由选自SEQ ID NO:59和119的核酸序列组成的多核苷酸的互补序列杂交的多核苷酸编码的序列;和
b.重链可变结构域,其包含选自下组的氨基酸序列,该组由以下组成:
i.与选自SEQ ID NO:62和122的氨基酸序列具有至少80%同一性的序列;
ii.由与选自SEQ ID NO:60和120的氨基酸序列具有至少80%同一性的多核苷酸序列编码的序列;
iii.由在中等严格条件下与由选自SEQ ID NO:60和120的核酸序列组成的多核苷酸的互补序列杂交的多核苷酸编码的序列。
在多个实施例中,抗TREM-1抗原结合蛋白或抗原结合蛋白的抗TREM1抗原结合部分包含:
i)SEQ ID NO:41中列出的轻链可变结构域和SEQ ID NO:42中列出的重链可变结构域;
ii)SEQ ID NO:61中列出的轻链可变结构域和SEQ ID NO:62中列出的重链可变结构域;
iii)SEQ ID NO:81中列出的轻链可变结构域和SEQ ID NO:82中列出的重链可变结构域;
iv)SEQ ID NO:101中列出的轻链可变结构域和SEQ ID NO:102中列出的重链可变结构域;
v)SEQ ID NO:121中列出的轻链可变结构域和SEQ ID NO:122中列出的重链可变结构域;
vi)SEQ ID NO:141中列出的轻链可变结构域和SEQ ID NO:142中列出的重链可变结构域;
vii)SEQ ID NO:161中列出的轻链可变结构域和SEQ ID NO:162中列出的重链可变结构域;
viii)SEQ ID NO:181中列出的轻链可变结构域和SEQ ID NO:182中列出的重链可变结构域;
ix)SEQ ID NO:201中列出的轻链可变结构域和SEQ ID NO:202中列出的重链可变结构域;
x)SEQ ID NO:221中列出的轻链可变结构域和SEQ ID NO:222中列出的重链可变结构域;
xi)SEQ ID NO:241中列出的轻链可变结构域和SEQ ID NO:242中列出的重链可变结构域;
xii)SEQ ID NO:261中列出的轻链可变结构域和SEQ ID NO:262中列出的重链可变结构域;
xiii)SEQ ID NO:281中列出的轻链可变结构域和SEQ ID NO:282中列出的重链可变结构域;
xiv)SEQ ID NO:301中列出的轻链可变结构域和SEQ ID NO:302中列出的重链可变结构域;或者
xv)SEQ ID NO:2185中列出的轻链可变结构域和SEQ ID NO:2186中列出的重链可变结构域。
在抗原结合蛋白的多个实施例中,氨基酸序列可与SEQ ID NO:41、61、81、101、121、141、161、181、201、221、241、261、281、301和2185,以及SEQ ID NO:42、62、82、102、122、142、162、182、202、222、242、262、282、302和2186具有80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%同一性。
在抗原结合蛋白的多个实施例中,抗原结合部分包含与选自SEQ ID NO:42、62、82、102、122、142、162、182、202、222、242、262、282、302和2186的重链可变区氨基酸序列具有至少90%同一性的氨基酸序列。
在抗原结合蛋白的多个实施例中,抗原结合部分包含与选自SEQ ID NO:41、61、81、101、121、141、161、181、201、221、241、261、281、301和2185的轻链可变区氨基酸序列具有至少90%同一性的氨基酸序列。
在抗原结合蛋白的多个实施例中,抗原结合部分包含与选自SEQ ID NO:42、62、82、122、142、162、182、和302的序列具有至少90%同一性的重链氨基酸序列,以及与选自SEQ ID NO:41、61、81、121、141、161、181、和301的序列具有至少90%同一性的轻链氨基酸序列。
在抗原结合蛋白的多个实施例中,抗原结合部分包含与选自SEQ ID NO:62和122的序列具有至少90%同一性的重链氨基酸序列,以及与选自SEQ ID NO:61和121的序列具有至少90%同一性的轻链氨基酸序列。
在多个实施例中,抗原结合蛋白包含选自以下的重链氨基酸序列:SEQ ID NO:863、865、867、869、871、873、875、877、879、881、883、885、887、889、891、893、895、897、899、901、903、905、907、909、911、913、915、917、919、921、923、925、927、929、931、933、935、937、939、941、943、945、947、949、951、953、955、957、959、961、963、965、967、969、971、973、975、977、979、981、983、985、987、989、991、993、995、997、999、1001、1003、1005、1007、1009、1011、1013、1015、1017、1019、1021、1023、1025、1027、1029、1031、1033、1035、1037、1039、1041、1043、1045、1047、1049、1051、1053、1055、1057、1059、1061、1063、1065、1067、1069、1071、1073、1075、1077、1079、1081、1083、和1085,以及选自以下的轻链氨基酸序列:SEQ IDNO:864、866、868、870、872、874、876、878、880、882、884、886、888、890、892、894、896、898、900、902、904、906、908、910、912、914、916、918、920、922、924、926、928、930、932、934、936、938、940、942、944、946、948、950、952、954、956、958、960、962、964、966、968、970、972、974、976、978、980、982、984、986、988、990、992、994、996、998、1000、1002、1004、1006、1008、1010、1012、1014、1016、1018、1020、1022、1024、1026、1028、1030、1032、1034、1036、1038、1040、1042、1044、1046、1048、1050、1052、1054、1056、1058、1060、1062、1064、1066、1068、1070、1072、1074、1076、1078、1080、1082、1084、和1086。
在多个实施例中,本文提供了TREM-1抗体重链和/或轻链可变区的变体。TREM-1抗体重链可变区变体序列在SEQ ID NO:1883、1885、1887、1889、1891、1893、1895、1897、1899、1901、1903、1905、1907、1909、1911、1913、1915、1917、1919、1921、1923、1925、1927、1929、1931、1933、1935、1937、1939、1941、1943、1945、1947、1949、1951、1953、1955、1957、1959、1961、1963、1965、1967、1969、1971、1973、1975、1977、1979、1981、1983、1985、1987、1989、1991、1993、1995、1997、1999、2001、2003、2005、2007、2011、2013、2015、2017、2019、2021、2026、2025、2027、2029、2031、2033、2035、2037、2039、2041、2043、2045、2047、2049、2051、2053、2055、2057、2059、2061、2063、2065、2067、2069、2071、2073、2075、2077、2079、2081、2083、2085、2087、2089、2091、2093、2095、2097、2099、2101、2103、2105、2107、2109、2111、2113、2115、2117、2119、2121、2123、2125、2127、2129、2131、2133、2135以及表10和表11中列出,并且TREM-1抗体轻链可变区变体序列在SEQ ID NO:2543、2544、2545、2546、2547、2548、2549、2550、2551、2552、2553、2554、2555、2556、2557、2558、2559、2560、2561、2562、2563、2564、2565、2566、2567、2568、2569、2570、2571、2572、2573、2574、2575、2576、2577、2578、2579、2580、2581、2582、2583、2584、2585、2586、2587、2588、2589、2590、2591、2592、2593、2594、2595、2596、2597、2598、2599、2600、2601、2602、2603、2604、2605、2233、2235、2237、2239、2241、2243、2245、2247、2249、2251、2253、2255、2257、2259、2261、2263、2265、2267、2269、2271、2273、2275、2277、2279、2281、2283、2285、2287、2289、2291、2293、2295、2297、2299、2301、2303、2305、2307、2309、2311、2313、2315、2317、2319、2321、2323、2325、2327、2329、2331、2333、2335、2337、2339、2341、2343、2345、2347、2349、2351、2353、2355、2357、表10和表11中列出。预期TREM-1-IL-10抗原结合蛋白包含如本文披露的TREM-1抗体变体重链和/或轻链序列。
在抗原结合蛋白的多个实施例中,抗抗原结合蛋白的一个或多个重链框架氨基酸被来自另一人抗体氨基酸序列的相应的一个或多个氨基酸替代。在多个实施例中,抗原结合蛋白的一个或多个轻链框架氨基酸被来自另一人抗体氨基酸序列的相应的一个或多个氨基酸替代。
在多个实施例中,抗TREM-1抗原结合蛋白进一步包含连接至所述轻链可变区的人轻链恒定区。
在抗原结合蛋白的多个实施例中:该抗原结合蛋白包含两条轻链和两条重链:每条重链包含在该重链的C末端处附接的IL-10部分;每个重链-IL-10部分抗原结合蛋白包含与选自以下的序列具有至少90%同一性的氨基酸序列:SEQ ID NO:863、865、867、869、871、873、875、877、879、881、883、885、887、889、891、893、895、897、899、901、903、905、907、909、911、913、915、917、919、921、923、925、927、929、931、933、935、937、939、941、943、945、947、949、951、953、955、957、959、961、963、965、967、969、971、973、975、977、979、981、983、985、987、989、991、993、995、997、999、1001、1003、1005、1007、1009、1011、1013、1015、1017、1019、1021、1023、1025、1027、1029、1031、1033、1035、1037、1039、1041、1043、1045、1047、1049、1051、1053、1055、1057、1059、1061、1063、1065、1067、1069、1071、1073、1075、1077、1079、1081、1083、和1085;并且每条轻链包含与选自以下的序列具有至少90%同一性的氨基酸序列:SEQ ID NO:864、866、868、870、872、874、876、878、880、882、884、886、888、890、892、894、896、898、900、902、904、906、908、910、912、914、916、918、920、922、924、926、928、930、932、934、936、938、940、942、944、946、948、950、952、954、956、958、960、962、964、966、968、970、972、974、976、978、980、982、984、986、988、990、992、994、996、998、1000、1002、1004、1006、1008、1010、1012、1014、1016、1018、1020、1022、1024、1026、1028、1030、1032、1034、1036、1038、1040、1042、1044、1046、1048、1050、1052、1054、1056、1058、1060、1062、1064、1066、1068、1070、1072、1074、1076、1078、1080、1082、1084、和1086。
在多个实施例中,抗原结合蛋白可以是单价。在多个实施例中,重链-IL-10部分抗原结合蛋白包含与选自以下的序列具有至少90%同一性的氨基酸序列:SEQ ID NO:1087、1090、1093、1096、1105、1108、1111、1114、1117、1123、1126、1129、1132、1138、1141、1147、1150、1153、1156、1159、1162、1165、1168、1171、1174、1177、1180、1183、1186、1189、1192、1195、1198、1201、1204,1207、1210、1213、1216、1219、1222、1225、1228、1231、1237、1240、1243、1246、1252、1255、1258、1261、1264、1267、1270、1273、1276、1279、1285、1288、1294、1297、1300、1303、1309、1312、1315、1318、1321、1324、1333、1336、1342、1345、1348、1351、1354、1357、1360、1363、1366、1369、1372、1375、1378、1381、1384、1387、1390、1393、1396、1399、1402、1408、1411、1414、1417、和1420。在多个实施例中,轻链包含与选自以下的序列具有至少90%同一性的氨基酸序列:SEQ ID NO:1088、1091、1094、1097、1106、1109、1112、1115、1118、1124、1127、1130、1133、1139、1142、1148、1151、1154、1157、1160、1163、1166、1169、1172、1175、1178、1181、1184、1187、1190、1193、1196、1199、1202、1205,1208、1211、1214、1217、1220、1223、1226、1229、1232、1238、1241、1244、1247、1253、1256、1259、1262、1265、1268、1271、1274、1277、1280、1286、1289、1295、1298、1301、1304、1310、1313、1316、1319、1322、1325、1334、1337、1343、1346、1349、1352、1355、1358、1361、1364、1367、1370、1373、1376、1379、1382、1385、1388、1391、1394、1397、1400、1403、1409、1412、1415、1418和1421。在多个实施例中,单价抗原结合蛋白进一步包含例如,如在以下中列出的Fc区:SEQID NO:1089、1092、1095、1098、1107、1110、1113、1116、1119、1125、1128、1131、1134、1140、1143、1149、1152、1155、1158、1161、1164、1167、1170、1173、1176、1179、1182、1185、1188、1191、1194、1197、1200、1203、1206、1209、1212、1215、1218、1221、1224、1227、1230、1233、1239、1242、1245、1248、1254、1257、1260、1263、1266、1269、1272、1275、1278、1281、1287、1290、1296、1299、1302、1305、1311、1314、1317、1320、1323、1326、1335、1338、1344、1347、1350、1353、1356、1359、1362、1365、1368、1371、1374、1377、1380、1383、1386、1389、1392、1395、1398、1401、1404、1410、1413、1416、1419和1422。
在抗原结合蛋白的多个实施例中:该抗原结合蛋白包含两条轻链和两条重链:每条重链包含在该重链的C末端处附接的IL-10部分;每个重链-IL-10部分抗原结合蛋白包含与选自以下的序列具有至少90%同一性的氨基酸序列:SEQ ID NO:1883、1885、1887、1889、1891、1893、1895、1897、1899、1901、1903、1905、1907、1909、1911、1913、1915、1917、1919、1921、1923、1925、1927、1929、1931、1933、1935、1937、1939、1941、1943、1945、1947、1949、1951、1953、1955、1957、1959、1961、1963、1965、1967、1969、1971、1973、1975、1977、1979、1981、1983、1985、1987、1989、1991、1993、1995、1997、1999、2001、2003、2005、2007、2011、2013、2015、2017、2019、2021、2026、2025、2027、2029、2031、2033、2035、2037、2039、2041、2043、2045、2047、2049、2051、2053、2055、2057、2059、2061、2063、2065、2067、2069、2071、2073、2075、2077、2079、2081、2083、2085、2087、2089、2091、2093、2095、2097、2099、2101、2103、2105、2107、2109、2111、2113、2115、2117、2119、2121、2123、2125、2127、2129、2131、2133、2135,以及表10、表11、表16、和表17中列出的序列;并且每个轻链包含与选自以下的序列具有至少90%同一性的氨基酸序列:SEQ ID NO:2543、2544、2545、2546、2547、2548、2549、2550、2551、2552、2553、2554、2555、2556、2557、2558、2559、2560、2561、2562、2563、2564、2565、2566、2567、2568、2569、2570、2571、2572、2573、2574、2575、2576、2577、2578、2579、2580、2581、2582、2583、2584、2585、2586、2587、2588、2589、2590、2591、2592、2593、2594、2595、2596、2597、2598、2599、2600、2601、2602、2603、2604、2605、2233、2235、2237、2239、2241、2243、2245、2247、2249、2251、2253、2255、2257、2259、2261、2263、2265、2267、2269、2271、2273、2275、2277、2279、2281、2283、2285、2287、2289、2291、2293、2295、2297、2299、2301、2303、2305、2307、2309、2311、2313、2315、2317、2319、2321、2323、2325、2327、2329、2331、2333、2335、2337、2339、2341、2343、2345、2347、2349、2351、2353、2355、2357,以及表10和表11中列出的序列。在抗原结合蛋白的多个实施例中:该抗原结合蛋白包含两条轻链和两条重链:每条重链包含在该重链的C末端处附接的IL-10部分;每个重链-IL-10部分抗原结合蛋白包含与选自以下的序列具有至少90%同一性的氨基酸序列:SEQ ID NO:1883、1885、1887、1889、1891、1893、1895、1897、1899、1901、1903、1905、1907、1909、1911、1913、1915、1917、1919、1921、1923、1925、1927、1929、1931、1933、1935、1937、1939、1941、1943、1945、1947、1949、1951、1953、1955、1957、1959、1961、1963、1965、1967、1969、1971、1973、1975、1977、1979、1981、1983、1985、1987、1989、1991、1993、1995、1997、1999、2001、2003、2005、和2007,并且每条轻链包含与选自以下的序列具有至少90%同一性的氨基酸序列:SEQ ID NO:2543、2544、2545、2546、2547、2548、2549、2550、2551、2552、2553、2554、2555、2556、2557、2558、2559、2560、2561、2562、2563、2564、2565、2566、2567、2568、2569、2570、2571、2572、2573、2574、2575、2576、2577、2578、2579、2580、2581、2582、2583、2584、2585、2586、2587、2588、2589、2590、2591、2592、2593、2594、2595、2596、2597、2598、2599、2600、2601、2602、2603、2604、2605。
在抗原结合蛋白的多个实施例中:该抗原结合蛋白包含两条轻链和两条重链:每条重链包含在该重链的C末端处附接的IL-10部分;每个重链-IL-10部分抗原结合蛋白包含与选自以下的序列具有至少90%同一性的氨基酸序列:SEQ ID NO:2011、2013、2015、2017、2019、2021、2026、2025、2027、2029、2031、2033、2035、2037、2039、2041、2043、2045、2047、2049、2051、2053、2055、2057、2059、2061、2063、2065、2067、2069、2071、2073、2075、2077、2079、2081、2083、2085、2087、2089、2091、2093、2095、2097、2099、2101、2103、2105、2107、2109、2111、2113、2115、2117、2119、2121、2123、2125、2127、2129、2131、2133、和2135,并且每条轻链包含与选自以下的序列具有至少90%同一性的氨基酸序列:SEQ ID NO:2233、2235、2237、2239、2241、2243、2245、2247、2249、2251、2253、2255、2257、2259、2261、2263、2265、2267、2269、2271、2273、2275、2277、2279、2281、2283、2285、2287、2289、2291、2293、2295、2297、2299、2301、2303、2305、2307、2309、2311、2313、2315、2317、2319、2321、2323、2325、2327、2329、2331、2333、2335、2337、2339、2341、2343、2345、2347、2349、2351、2353、2355、和2357。
在多个实施例中,抗原结合蛋白包含与SEQ ID NO:2726-2776中任一个中列出的序列具有至少90%同一性的重链氨基酸序列。在多个实施例中,抗原结合蛋白包含SEQ IDNO:2726-2776中任一个中列出的重链氨基酸序列。在多个实施例中,抗原结合蛋白具有选自由SEQ ID NO:2727-2732组成的组的重链-IL-10部分氨基酸序列。
在多个实施例中,抗原结合蛋白包含SEQ ID NO:2727或2728的重链氨基酸序列,和SEQ ID NO:976或SEQ ID NO:2554中列出的轻链氨基酸序列,或其他63F8或63F8.001轻链。在多个实施例中,抗原结合蛋白包含SEQ ID NO:2729、2730、2731或2732的重链氨基酸序列,和SEQ ID NO:992或SEQ ID NO:2555中列出的轻链氨基酸序列,或其他64D7或64D7.001轻链。
在抗原结合蛋白的多个实施例中,抗TREM-1抗原结合部分抑制TREM-1与TREM-1配体的结合。
在多个实施例中,至少一个IL-10部分与抗原结合部分的N末端融合。在多个实施例中,至少一个IL-10部分与抗原结合部分的N末端和C末端融合。在多个实施例中,IL-10部分在抗原结合部分的内部位点处融合,例如,IL-10分子在CH1结构域和重链的铰链区之间,或在美国专利号8,008,453(将其整体通过引用并入本文)中描述的位点处融合。在多个实施例中,至少一个IL-10部分与抗原结合部分的重链和/或轻链融合。在多个实施例中,重链和/或轻链是修饰的或工程化的重链或轻链。
核酸分子
本披露还提供了编码IL-10突变蛋白、抗原结合蛋白和包含本文所述的抗原结合部分和IL-10部分的抗原结合蛋白(包括例如IL-10突变蛋白序列、抗原结合蛋白轻链、轻链可变区、轻链恒定区、抗原结合蛋白重链、重链可变区、重链恒定区、接头、融合蛋白以及任何和所有组分及其组合)的分离核酸。本发明的核酸包括与本发明的核酸具有至少80%、更优选至少约90%、更优选至少约95%、且最优选至少约98%同源性的核酸。当涉及特定序列时,术语“相似性百分比”、“同一性百分比”和“同源性百分比”如威斯康星大学(Universityof Wisconsin)软件程序中所述使用。本披露的核酸还包括互补核酸。在一些情况下,序列在比对时将是完全互补的(没有错配)。在其他情况下,序列中可能存在最高约20%的错配。在本发明的一些实施例中,提供了同时编码本披露抗体的重链和轻链的核酸。
可以将本披露的核酸克隆到载体中,如质粒、粘粒、杆粒、噬菌体、人工染色体(BAC、YAC)或病毒中,可以向该载体中插入另一种遗传序列或元件(DNA或RNA),以便实现所附序列或元件的复制。在一些实施例中,表达载体含有组成型活性启动子区段(诸如但不限于CMV、SV40、延伸因子或LTR序列)或诱导型启动子序列,例如类固醇诱导型pIND载体(英杰公司(Invitrogen)),其中可以调控核酸的表达。本发明的表达载体可以进一步包含调控序列,例如内部核糖体进入位点。例如,可以通过转染将表达载体引入细胞中。
还提供了表达载体,其包含以下可操作地连接的元件;转录启动子;第一核酸分子,其编码本披露的IL-10突变蛋白,抗原结合蛋白、抗体或抗原结合片段的重链,或融合蛋白;第二核酸分子,其编码本披露的抗原结合蛋白、抗体或抗原结合片段的轻链;以及转录终止子。在另一个实施例中,本披露提供了表达载体,该表达载体包含以下可操作地连接的元件;第一转录启动子;第一核酸分子,其编码本披露的IL-10突变蛋白,抗原结合蛋白、抗体或抗原结合片段的重链,或其融合蛋白;第一转录终止子;第二转录启动子,任选地,编码本披露的抗原结合蛋白、抗体或抗原结合片段的轻链的第二核酸分子;以及第二转录终止子。
分泌信号肽序列还可以任选地由表达载体编码,与目的编码序列可操作地连接,使得表达的多肽可以由重组宿主细胞分泌,如果需要,以便更容易地从细胞中分离目的多肽。例如,在一些实施例中,信号肽序列可以附加/融合到本文所述的IL-10突变蛋白、抗原结合蛋白、抗体或其抗原结合片段或融合蛋白多肽序列中的任一个的氨基末端上。
还提供了包含这种载体并表达IL-10突变蛋白、抗原结合蛋白重链和轻链、或含有抗原结合部分和IL-10部分的抗原结合蛋白的重组宿主细胞。重组宿主细胞可以是原核细胞(例如大肠杆菌细胞)、或真核细胞(例如哺乳动物细胞或酵母细胞)。酵母细胞包括酿酒酵母(Saccharomyces cerevisiae)、粟酒裂殖酵母(Schizosaccharomyces pombe)、和毕赤 酵母(Pichia pastoris)细胞。哺乳动物细胞包括VERO、海拉(HeLa)、中国仓鼠卵巢(CHO)、W138、幼仓鼠肾(BHK)、COS-7、MDCK、人胚胎肾系293、正常狗肾细胞系、正常猫肾细胞系、猴肾细胞、非洲绿猴肾细胞、COS细胞、以及非致瘤性小鼠成肌细胞G8细胞、成纤维细胞细胞系、骨髓瘤细胞系、小鼠NIH/3T3细胞、LMTK31细胞、小鼠塞托利细胞(sertoli cell)、人宫颈癌细胞、布法罗(buffalo)大鼠肝细胞、人肺细胞、人肝脏细胞、小鼠乳腺肿瘤细胞、TRI细胞、MRC 5细胞、和FS4细胞。本披露的产生重组蛋白的细胞还包括任何已知的昆虫表达细胞系,例如,像草地贪夜蛾(Spodoptera frugiperda)细胞。在一个实施例中,细胞是哺乳动物细胞。在某些实施例中,哺乳动物细胞是CHO细胞。
蛋白质纯化方法是本领域已知的,并且在本文中用于从细胞培养基中回收重组蛋白质。例如,蛋白质和抗体纯化的方法是本领域已知的,并且可以与本披露的抗体的产生一起使用。在一些实施例中,用于蛋白质和抗体纯化的方法包括过滤、亲和柱色谱法、阳离子交换色谱法、阴离子交换色谱法和浓缩。过滤步骤可以包括超滤,优选地包括超滤和渗滤。过滤优选进行至少约5至50次,更优选10至30次,最优选14至27次。亲和柱色谱可以使用例如亲和色谱法(马萨诸塞州比尔里卡的密理博公司(Millipore,Billerica,Mass.))进行。在多个实施例中,亲和色谱步骤包括柱色谱。洗脱液可以在溶剂洗涤剂中洗涤。阳离子交换色谱可包括例如SP-Sepharose阳离子交换色谱。阴离子交换色谱可包括例如但不限于Q-Sepharose快速流阴离子交换(Q-Sepharose Fast FlowAnion Exchange)。阴离子交换步骤优选是非结合的,从而允许除去包括DNA和BSA的污染物。抗体产物优选经纳米过滤,例如,使用Pall DV 20纳米过滤器。可以例如使用超滤和渗滤来浓缩抗体产物。该方法可以进一步包括尺寸排阻色谱法以除去聚集体的步骤。
在多个实施例中,SEQ ID NO:11-18中列出的核苷酸序列可用于表达本文的IL-10突变蛋白、或其片段、或其变体。
在一些实施例中,不同的核酸分子编码靶特异性抗体的重链可变区和轻链可变区。在其他实施例中,相同的核酸分子编码靶特异性抗体的重链可变区和轻链可变区。在一个实施例中,核酸编码本披露的靶特异性抗体,以及由本文所述的核酸编码的多肽中的任何一种。
在一些实施例中,核酸分子编码与SEQ ID NO:42、62、82、102、122、142、162、182、202、222、242、262、282、302和2186中列出的VH氨基酸序列具有至少70%、75%、80%、85%、90%、95%、96%、97%、98%或99%同一性的VH氨基酸序列。本披露的核酸分子进一步包括在高严格条件下与编码SEQ ID NO:42、62、82、102、122、142、162、182、202、222、242、262、282、302、和2186的重链可变区氨基酸序列的核酸序列杂交的核酸(如本文所述的那些核酸分子)或具有SEQ ID NO:40、60、80、100、120、140、160、180、200、220、240、260、280、300和2184中任何一个的重链可变区核酸序列的核酸。
在一些实施例中,核酸分子编码与SEQ ID NO:41、61、81、101、121、141、161、181、201、221、241、261、281、301和2185中列出的VL氨基酸序列具有至少70%、75%、80%、85%、90%、95%、96%、97%、98%或99%同一性的VL氨基酸序列。本披露的核酸分子进一步包括在高严格条件下与编码SEQ ID NO:41、61、81、101、121、141、161、181、201、221、241、261、281、301、和2185的轻链可变区氨基酸序列的核酸序列杂交的核酸(如本文所述的那些核酸分子)或具有SEQ ID NO:39、59、79、99、119、139、159、179、199、219、239、259、279、299和2183中任何一个的轻链可变区核酸序列的核酸。
在一方面,本披露的核酸分子包含编码本文列出的抗TREM-1抗原结合蛋白或其部分的VL氨基酸序列的核苷酸序列。在相关方面,VL氨基酸序列是共有序列。在一些实施例中,核酸编码所述抗体的轻链CDR的氨基酸序列。在一些实施例中,所述部分是包含LCDR1-CDR3的连续的部分。在相关方面,LCDR1-3氨基酸序列是共有序列。在一个实施例中,所述部分包含轻链CDR1、CDR2、或CDR3区中的至少一个、两个或三个,任选地具有不同的人或人共有框架,并且任选地在3个CDR中总共具有1个、或多达2个、或多达3个突变。
在一方面,本披露的核酸分子包含编码本文列出的抗TREM-1抗原结合蛋白或其部分的VH氨基酸序列的核苷酸序列。在相关方面,VH氨基酸序列是共有序列。在一些实施例中,核酸编码所述抗体的重链CDR的氨基酸序列。在一些实施例中,所述部分是包含HCDR1-CDR3的连续的部分。在相关方面,HCDR1-3氨基酸序列是共有序列。在一个实施例中,所述部分包含重链CDR1、CDR2、或CDR3区中的至少一个、两个或三个,任选地具有不同的人或人共有框架,并且任选地在3个CDR中总共具有1个、或多达2个、或多达3个突变。
某些抗原结合蛋白重链和轻链的核酸序列在SEQ ID NO:303到526(二价)和SEQID NO:527到862(单价)中列出。TREM-1变体抗体重链可变区的核酸序列在SEQ ID NO:2012、2014、2016、2018、2020、2022、2024、2026、2028、2030、2032、2034、2036、2038、2040、2042、2044、2046、2048、2050、2052、2054、2056、2058、2060、2062、2064、2066、2068、2070、2072、2074、2076、2078、2080、2082、2084、2086、2088、2090、2092、2094、2096、2098、2100、2102、2104、2106、2108、2110、2112、2114、2116、2118、2120、2122、2124、2126、2128、2130、2132、2134、和2136中列出,并且TREM-1变体抗体轻链可变区核苷酸序列在SEQ ID NO:2234、2236、2238、2240、2242、2244、2246、2248、2250、2252、2254、2256、2258、2260、2262、2264、2266、2268、2270、2272、2274、2276、2278、2280、2282、2284、2286、2288、2290、2292、2294、2296、2298、2300、2302、2304、2306、2308、2310、2312、2314、2316、2318、2320、2322、2324、2326、2328、2330、2332、2334、2336、2338、2340、2342、2344、2346、2348、2350、2352、2354、2356、和2358中列出。
在示例性实施例中,本披露的抗体包含人kappa(κ)或人lambda(λ)轻链或由其衍生的氨基酸序列、或人重链或由其衍生的序列、或一起以单链、二聚体、四聚体或其他形式的重链和轻链两者。
接头
接头或间隔子包括用于通过共价键或非共价键连接两个分子的肽或其他部分。本文考虑肽部分在IL-10突变蛋白多肽内,以提供稳定性和增加的IL-10序列间距,以便以单体形式进行适当折叠。本文还考虑了肽部分用于在本披露的抗原结合蛋白中使用,在抗原结合蛋白中的抗原结合部分和与之融合的IL-10单体/突变蛋白之间提供连接或间隔子。
将Fc区连接至IL-10突变蛋白的肽接头可以是本文所述的肽接头中的任何一种。在一些实施例中,接头可以是2-40、3-40、3-30、或3-20个氨基酸长。在多个实施例中,接头可以是3-25、4-18、4-20、5-20、6-18、或10-20个氨基酸长。在多个实施例中,接头可以是约2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、或30个氨基酸长。在多个实施例中,接头为4至18个氨基酸长。在某些实施例中,将Fc区连接至IL-10突变蛋白的肽接头长度为至少4个氨基酸、至少5个氨基酸、或至少6个氨基酸。在其他实施例中,将Fc区连接至羧基末端Fab片段的肽接头长度为至少8个氨基酸。
在一些实施例中,接头可连接至抗原结合蛋白中抗原结合部分的重链的C末端。在多个实施例中,接头是3聚体、4聚体、5聚体、6聚体、7聚体、8聚体、或重复的3聚体、4聚体、5聚体或6聚体。示例性接头包括Gly-Gly-Gly-Gly(SEQ ID NO:2677)、Gly-Gly、Gly-Gly-Gly、Gly-Gly-Gly-Ser(SEQ ID NO:2705)、Gly-Gly-Gly-Pro(SEQ ID NO:2706)、Gly-Gly-Gly-Gln(SEQ ID NO:2707)、Gly-Gly-Gly-Gly-Gly(SEQ ID NO:2708)、Gly-Gly-Gly-Gly-Ser(SEQ ID NO:2725)、(Gly3Ser)2(SEQ ID NO:2709)、(Gly4Ser)2(SEQ ID NO:2710)、(Gly3Ser)3(SEQ ID NO:2711)、(Gly4Ser)3(SEQ ID NO:2712)、(Gly3Ser)4(SEQ ID NO:2713)、(Gly4Ser)4(SEQ ID NO:2714)、(Gly3Ser)5(SEQ ID NO:2715)、(Gly4Ser)5(SEQ IDNO:2716)、(Gly3Ser)6(SEQ ID NO:2717)、(Gly4Ser)6(SEQ ID NO:2718)、Gly-Ser-Gly-Ser-Ala-Thr-Gly-Gly-Ser-Gly-Ser-Ser-Ala-Ser-Ser-Gly-Ser-Gly-Ser-Ala-Thr-His-Leu(SEQ ID NO:2719)、Gly-Ser-Gly-Ser-Ala-Thr-Gly-Gly-Ser-Gly-Ser-Val-Ala-Ser-Ser-Gly-Ser-Gly-Ser-Ala-Thr-His-Leu(SEQ ID NO:2720)、Gly-Ser-Gly-Ser-Ala-Thr-Gly-Gly-Ser-Gly-Ser-Ser-Ala-Ser-Ser-Gly-Ser-Gly-Ser-Ala-Thr-His-Leu(SEQ IDNO:2721)、Gly-Ser-Gly-Ser-Ala-Thr-Gly-Gly-Ser-Gly-Ser-Gly-Ala-SeGGGr-Ser-Gl y-Ser-Gly-Ser-Ala-Thr-Gly-Ser(SEQ ID NO:2722),以及实例中列出的接头。
在IL-10突变蛋白中还插入了接头或间隔子肽部分以保持稳定性。例如,可以在野生型IL-10或IL-10突变蛋白的DE螺旋环内添加4-8个氨基酸的序列。在多个实施例中,接头的长度是3、4、5、6、7、或8个氨基酸。在多个实施例中,接头为6个氨基酸。在多个实施例中,接头具有序列GGGSGG(SEQ ID NO:2676)。
衍生物
合适的可检测分子可以直接或间接连接至本披露的IL-10突变蛋白、抗原结合蛋白或融合蛋白。合适的可检测分子包括放射性核素、酶、底物、辅因子、抑制剂、荧光标记、化学发光标记、磁颗粒等。对于可检测分子或细胞毒性分子的间接附着,该可检测分子或细胞毒性分子可与互补/抗互补对中的一个成员缀合,其中其他成员与结合多肽或抗体部分结合。出于这些目的,生物素/链霉亲和素是示例性互补/抗互补对。
本披露的IL-10突变蛋白、抗原结合蛋白和包含抗原结合部分和IL-10部分的抗原结合蛋白还包括经修饰的衍生物,例如,通过将任何类型的分子共价附接到抗体上,使得共价附接不妨碍抗体与其表位结合。合适的衍生物的实例包括但不限于岩藻糖基化、糖基化、乙酰化、聚乙二醇化、磷酸化、或酰胺化的衍生物。本披露的IL-10突变蛋白、抗原结合蛋白和包含抗原结合部分和IL-10部分抗原结合蛋白及其衍生物本身可以通过已知的保护性/阻断性基团、蛋白水解裂解、与细胞配体或其他蛋白质连接等进行衍生。在本披露的一些实施例中,IL-10突变蛋白或抗原结合蛋白或包含抗原结合部分和IL-10部分的抗原结合蛋白的至少一条重链被聚乙二醇化。在一些实施例中,聚乙二醇化是N-连接的或通过氨基酸(例如,赖氨酸)的侧链连接。
糖基化可以促进抗体,特别是IgG1抗体的效应子功能。因此,在一些实施例中,本披露的IL-10突变蛋白、抗原结合蛋白或包含抗原结合部分和IL-10部分的抗原结合蛋白可包含一个或多个影响结合蛋白糖基化的水平或类型的氨基酸取代。多肽的糖基化典型地是N-连接或O-连接的。N-连接是指碳水化合物部分连接至天冬酰胺残基的侧链。三肽序列天冬酰胺-X-丝氨酸和天冬酰胺-X-苏氨酸(其中X为除脯氨酸以外的任何氨基酸)是将碳水化合物部分酶促连接至天冬酰胺侧链的识别序列。因此,在多肽中这些三肽序列中的任一个的存在产生潜在的糖基化位点。O-连接糖基化是指将糖N-乙酰半乳糖胺、半乳糖或木糖中的一种连接至羟基氨基酸,最常见的是丝氨酸或苏氨酸,尽管也可使用5-羟基脯氨酸或5-羟基赖氨酸。
在某些实施例中,通过向例如结合蛋白的Fc区中添加一个或多个糖基化位点来增加本文所述的IL-10突变蛋白、抗原结合蛋白以及包含抗原结合部分和IL-10部分的抗原结合蛋白的糖基化。在抗原结合蛋白中添加糖基化位点通常可以通过改变氨基酸序列,以使其含有上述三肽序列(对于N-连接的糖基化位点)中的一个或多个来实现。还可以通过向起始序列(对于O-连接的糖基化位点)添加或取代为一个或多个丝氨酸或苏氨酸残基来作出改变。为便利起见,可以通过在DNA层面上的变化,特别是通过使编码靶多肽的DNA在预先选择的碱基处突变,由此产生会翻译成所需氨基酸的密码子,来改变抗原结合蛋白的氨基酸序列。
本披露还涵盖了产生具有改变的碳水化合物结构而引起效应子活性改变的IL-10突变蛋白、抗原结合蛋白以及包含抗原结合部分和IL-10部分的抗原结合蛋白,包括岩藻糖基化不存在或减少的展现改善的ADCC活性的抗原结合蛋白。本领域中已知各种减少或消除岩藻糖基化的方法。例如,通过使抗体分子与FcγRIII受体结合来介导ADCC效应子活性,经显示此取决于在CH2结构域N297残基处N-连接的糖基化的碳水化合物结构。相较于天然、岩藻糖基化抗体,非岩藻糖基化抗体以增加的亲和力结合此受体且更有效地触发FcγRIII介导的效应子功能。例如,在α-1,6-岩藻糖基转移酶已敲除的CHO细胞中重组产生非岩藻糖基化抗体使抗体具有100倍增加的ADCC活性(参见Yamane-Ohnuki等人,Biotechnol Bioeng.[生物技术及生物工程]87(5):614-22,2004)。通过降低α-1,6-岩藻糖基转移酶或岩藻糖基化路径中的其他酶的活性,例如通过siRNA或反义RNA处理,将细胞系工程改造以敲除一种或多种酶,或与选择性糖基化抑制剂一起培养可以实现类似作用(参见Rothman等人,MolImmunol.[分子免疫学]26(12):1113-23,1989)。一些宿主细胞系,例如Lec13或大鼠杂交瘤YB2/0细胞系天然地产生岩藻糖基化程度较低的抗体(参见Shields等人,J Biol Chem.[生物化学杂志]277(30):26733-40,2002;以及Shinkawa等人,J Biol Chem.[生物化 学杂志]278(5):3466-73,2003)。还已确定例如经由在过表达GnTIII酶的细胞中重组产生抗体以增加等分碳水化合物的含量,可增加ADCC活性(参见Umana等人,Nat Biotechnol.[自然生物技术]17(2):176-80,1999)。
在其他实施例中,通过例如自结合蛋白的Fc区移除一个或多个糖基化位点来减少或消除本文所述的IL-10突变蛋白、抗原结合蛋白以及包含抗原结合部分和IL-10部分的抗原结合蛋白的糖基化。消除或改变N-连接的糖基化位点的氨基酸取代可以减少或消除抗原结合蛋白的N-连接的糖基化。在某些实施例中,本文所描述的双特异性抗原结合蛋白包含在位置N297(EU编号)处的突变,例如N297Q、N297A或N297G。在一个特定实施例中,本发明的双特异性抗原结合蛋白包含来自人类IgG1抗体的具有N297G突变的Fc区。为了改善含N297突变的分子的稳定性,可以对所述分子的Fc区进行进一步工程改造。例如,在一些实施例中,Fc区中的一个或多个氨基酸经半胱氨酸取代以促进二聚体状态下二硫键的形成。对应于IgG1 Fc区的V259、A287、R292、V302、L306、V323或I332(EU编号)的残基因此可以经半胱氨酸取代。在一个实施例中,特定残基对经半胱氨酸取代以使其优先彼此形成二硫键,由此限制或防止二硫键混乱。在某些实施例中,对包括但不限于,A287C与L306C、V259C与L306C、R292C与V302C、以及V323C与I332C。在特定实施例中,本文所描述的双特异性抗原结合蛋白包含来自人类IgG1抗体的具有R292C和V302C突变的Fc区。在此类实施例中,Fc区还可包含N297G突变。
还可能希望对本披露的IL-10突变蛋白、抗原结合蛋白以及包含抗原结合部分和IL-10部分的抗原结合蛋白进行修饰以增加血清半衰期,例如通过并入或添加补救受体结合表位(例如通过使适当区突变或通过将该表位并入肽标签中,接着使其与IL-10突变蛋白、抗原结合蛋白以及包含抗原结合部分和IL-10部分的抗原结合蛋白在任一端或在中间融合,例如通过DNA或肽合成;参见,例如WO96/32478)或添加例如PEG或其他水溶性聚合物的分子,包括多糖聚合物。补救受体结合表位优选构成这样一种区域,其中来自Fc区中一个或两个环的任一个或多个氨基酸残基转移至抗原结合蛋白中的类似位置。在一个实施例中,来自Fc区中一个或两个环的三个或更多个氨基酸残基经转移。在一个实施例中,自Fc区(例如IgG Fc区)的CH2结构域取得表位并将其转移至IL-10突变蛋白、抗原结合蛋白以及包含抗原结合部分和IL-10部分的抗原结合蛋白的CH1、CH3或VH区,或超过一个此类区。可替代地,自Fc区的CH2结构域取得表位并将其转移至抗原结合蛋白的CL区或VL区,或这两个区域。有关Fc变体及其与补救受体相互作用的说明,参见国际公开WO 97/34631和WO 96/32478。
本披露的IL-10突变蛋白、抗原结合蛋白以及包含抗原结合部分和IL-10部分蛋白的抗原结合蛋白包括具有单个或多个氨基酸取代、缺失、添加或替换的变体,这些变体保留了它们的生物特性。本领域普通技术人员可以生产具有单个或多个氨基酸取代、缺失、添加或替换的变体。这些变体尤其可以包括:(a)其中一个或多个氨基酸残基被保守或非保守氨基酸取代的变体,(b)其中一个或多个氨基酸被添加多肽中至或从多肽中缺失的变体,(c)其中一个或多个氨基酸包括取代基团的变体,以及(d)其中多肽与另一种肽或多肽融合的变体,如融合配偶体、蛋白质标签或其他化学部分,这些变体可赋予多肽有用的特性,例如,抗体的表位、多组氨酸序列、生物素部分等。本发明的抗体和双特异性抗体可包括变体,其中来自一个物种的氨基酸残基在保守或非保守位置被另一物种中相应的残基取代。在另一个实施例中,非保守位置处的氨基酸残基被保守或非保守残基取代。获得这些变体的技术(包括遗传(抑制、缺失、突变等)、化学和酶学技术)是本领域普通技术人员已知的。
治疗方法
IL-10可有力地抑制炎性细胞因子,如从髓细胞中产生的TNFα和IL-23。TNFα和IL-23都是治疗炎性肠病的有效靶标。IL-10还抑制抗原呈现细胞,包括抑制MHCII、CD86、和ICAM1的诱导。IL-10也激活CD8+T细胞和B细胞,尽管EC50较高,但在临床研究中可能导致IL-10的剂量限制毒性。rhIL-10的PK很差(t1/2=2.5-4小时),并且在临床上无法实现细胞类型的选择性。高剂量的rhIL-10刺激CD8+T细胞和B细胞,而低剂量则表现出组织和髓细胞覆盖不足。髓细胞特异性IL-10R1 KO小鼠与IL-10KO小鼠发生类似的结肠炎,这表明IL-10对髓细胞的抑制足以治疗炎性肠病(IBD)(Zigmond等人,Immunity[免疫力]40(5):720-33,2014)。因此,本文假设通过抗TREM-1mAb/IL10突变蛋白双特异性方法或另一种靶向部分将IL-10靶向到髓细胞,可以在髓细胞上达到足够的抗炎活性,而对CD8+细胞和B细胞没有刺激作用。
患有IL-10、IL-10R1、或IL-10R2纯合子功能缺失性突变的人类患者出现严重的婴儿型IBD(Kotlarz等人,Gastroenterology[胃肠病学],143:347–355,2012;Glocker,NEJM [新英格兰医学杂志],61(21):2033-45,2009)。IL-10是与IBD相关的基因突变之一(GWAS基因座,rs3024505RAF 0.16,或1.46,p值10-42,Jostins等人,Nature[自然]491:119-124,2012,deCODE rs3024505IBD或1.13,p值0.024)。
在髓细胞上表达的触发受体1(TREM1,TREM-1)是在中性粒细胞、单核细胞和巨噬细胞中表达的Ig家族成员。TREM-1抑制可能是治疗IBD的理想方法,因为TREM-1KO小鼠可以存活,并针对DSS结肠炎和T细胞转移结肠炎进行保护(Weber,PLoS Pathog[公共科学图书 馆-病原体],10(1):1003900,2014)。用TREM-1-Fc融合治疗提高了小鼠LPS攻击后的存活并降低了TNFα诱导(Bouchon,Nature[自然],410:1103-7,2001)。TREM-1在发炎的IBD组织中表达增加(Schenk等人,JClinInvest[临床研究杂志].117:3097-3106,2007),在CX3CR1creIL10R1fl/fl小鼠的结肠巨噬细胞中表达增加(Zimond,Immunity[免疫力],40(5):720-33,2014)并与DAP12结合,并在激活后诱导Syk磷酸化。本文假设TREM-1在IL-10抗原结合蛋白中作为理想的靶配偶体,因为其在髓细胞表面高度表达。
最近报道PGLYRP1(肽聚糖识别蛋白1)是TREM-1的配体(Read,J.Immunol[免疫学 杂志].194:1417-1421,2015),并且潜在的其他配体仍有待确定。据报道,抗TREM-1抗体可以减少从IBD患者中分离出的固有层细胞在TREM-1激动剂PGLYRP-1/肽聚糖的刺激下的炎性细胞因子的分泌(Brynjolfsson等人,Inflamm Bowel Dis[炎性肠病]22(8):1803-11,2016)。
IBD的治疗功效的读数包括评估IL-10IBD风险变体rs3024505者IL-10表达方面的调控、评估IBD患者血清和组织中IL-10水平的异质性、以及评估IBD风险变体与疾病严重程度、对疗法的应答的潜在相关性。
确定功效的其他措施包括髓细胞和IBD组织中降低的经IL-10诱导的表达谱,分析IBD样品中经受IL-10抑制的髓细胞衍生细胞因子(例如TNFα、IL-23)的异质性,以及确定IBD发炎的组织中单核细胞和巨噬细胞数的异质性和数量。预期本文用IL-10突变蛋白或抗原结合蛋白治疗将保留对髓细胞活性的抑制,并消除IL-10对CD8+T细胞和B细胞的激活。预期该治疗可降低受试者中的炎性细胞因子如TNF-α和IL-23的水平。
预期用包含抗TREM-1结合蛋白的本披露抗TREM-1抗原结合蛋白或包含抗原结合部分和IL-10部分抗原结合蛋白治疗,可以减少炎性细胞中TREM-1的表达。
克罗恩病涉及从口腔到肛门的消化道任何部分的异常炎症,尽管大多数患者的异常炎症局限于回结肠、小肠和结肠-肛门直肠区。典型地,炎症是不连续的。常见症状包括腹痛、厌食、体重减轻、发烧、腹泻、右下腹饱胀(fullness)和/或压痛、便秘、呕吐、以及肛周不适和排出。其他可能的症状包括外周关节炎、生长迟缓、巩膜外层炎、口糜、结节性红斑、坏疽性脓皮病、肾结石、尿液稀释和碱化受损、吸收不良和胆结石等。参见例如Strober等人,Medical Immunology[医学免疫学],第10版,第III节,第35章(2001);Merck Manual of Diagnosis and Therapy[默克诊疗手册],第17版,第3节,第31章(1999)。从克罗恩病患者中分离出的巨噬细胞产生的IL-12、IFNγ、TNFα和其他炎性细胞因子的量增加。
溃疡性结肠炎在几个方面与克罗恩病不同。首先,它一般局限于结肠,而克罗恩病可能发生在整个消化道。其次,溃疡性结肠炎主要只涉及肠道表层的炎症,而不像克罗恩病那样,炎症可以穿透肠壁或消化道的其他位置。最后,溃疡性结肠炎通常涉及连续的炎症区域,而不是克罗恩病典型的不连续的炎症部位。与克罗恩病一样,溃疡性结肠炎主要发现于城市地区。另外,遗传因素可能在溃疡性结肠炎中起作用,因为存在家族聚集性病例。在溃疡性结肠炎患者中观察到的自身抗体比克罗恩病患者更多。这些自身抗体通常针对结肠上皮细胞成分。其中最常见的是对过氧化氢酶、α-烯醇化酶、和乳铁蛋白有特异性的抗中性粒细胞胞质抗体。在某些情况下,这种抗体与结肠微生物发生交叉反应。
在临床试验中,通常使用克罗恩病活动指数(CDAI)对克罗恩病活性进行评分。CDAI提供了一个基于八个因素的疾病活性得分,包括(1)每天的水样便或软便的数量,(2)患者每天腹痛量的等级,(3)患者全身健康状况的等级,(4)其他症状的患者报告,包括关节炎、虹膜炎、葡萄膜炎、结节性红斑、坏疽性脓皮病、口糜、肛裂、瘘管、或脓肿、其他瘘管、或发烧,(5)服用复方苯乙哌啶片或其他阿片类止泻药的患者报告,(6)腹部包块,(7)红细胞比容,以及(8)体重。参见例如,Best等人(1976),Gastroenterol.[世界胃肠病学杂志]70:439-444,其相关部分通过引用并入本文。
溃疡性结肠炎的症状是可变的。它们可能包括腹泻、里急后重、腹部绞痛、大便带血和粘液、发烧以及直肠出血。也可能发生中毒性巨结肠,这是潜在的危及生命的情况,即结肠扩张超过约6厘米,并可能失去其肌肉张力和/或穿孔。可能伴随溃疡性结肠炎的其他症状包括外周关节炎、强直性脊柱炎、骶髂关节炎、前葡萄膜炎、结节性红斑、坏疽性脓皮病、巩膜外层炎、自身免疫性肝炎、原发性硬化性胆管炎、肝硬化、以及儿童生长发育迟缓。
在一些实施例中,患有炎性肠病(IBD),如克罗恩病或溃疡性结肠炎的患者可以在使用现有的IBD治疗方法之前、之后或同时使用如本文披露的IL-10突变蛋白、抗TREM-1抗原结合蛋白或其他抗原结合蛋白、或包含IL-10的抗原结合蛋白进行治疗。IBD的现有疗法包括,例如,柳氮磺吡啶、5-氨基水杨酸及其衍生物(如奥沙拉秦、巴柳氮、和美沙拉嗪)、抗TNF抗体(包括英利昔单抗、阿达木单抗、戈利木单抗、和培戈-瑟托利珠单抗)、口服或肠胃外施用的皮质类固醇(包括泼尼松、甲基泼尼松、布地奈德、或氢化可的松)、促肾上腺皮质激素、抗生素(包括甲硝唑,、环丙沙星、或利福昔明)、硫唑嘌呤、6-巯嘌呤、甲氨蝶呤、环孢霉素、他克莫司、以及沙利度胺。
在一个实施例中,本披露提供了在需要这种治疗的哺乳动物中抑制一种或多种促炎性细胞因子(例如,TNFα)的方法,该方法包括向需要这种治疗的受试者施用治疗有效量的本披露IL-10突变蛋白、抗原结合蛋白或抗体、或本文所述的融合蛋白。在优选的实施例中,受试者是哺乳动物。在一个实施例中,受试者是人。该方法可用于治疗以TNFα表达或活性升高为特征的疾病。本披露的IL-10突变蛋白、抗原结合蛋白或抗体、或包含本文所述的抗原结合部分和IL-10部分的抗原结合蛋白可与另一种药剂以同一配制品施用或分别施用。
类风湿性关节炎(RA)是慢性疾病,有全身症状,也有与关节特异性相关的症状。常见症状包括滑膜炎(导致关节疼痛和肿胀),以及各种实验室异常,如类风湿因子、抗瓜氨酸修饰蛋白(抗CCP)抗体和C反应蛋白(CRP)的水平高于正常,以及红细胞沉降率(ESR)升高。不太常见的症状包括例如涉及腱、韧带、血管、心脏和肺的各种关节外症状。疾病活性通常可以用多种指数来测量。参见例如,Anderson等人(2012),Arthritis Care&Res.[关节炎护 理与研究]64(5):640-647,其中讨论这种指数的部分通过引用并入本文。这种评分指数中包含的要素包括压痛关节的数量、肿胀关节的数量、功能评估以及各种实验室检查结果,如CRP、ESR等。
在一些实施例中,患有RA的患者可以在使用目前用于治疗RA的药物治疗之前、之后或同时使用如本文披露的IL-10突变蛋白、抗TREM-1抗原结合或本文所述的其他抗原结合蛋白、或包含抗原结合部分和IL-10部分的抗原结合蛋白进行治疗。目前用于治疗类风湿性关节炎(RA)的治疗药物包括非甾体抗炎药(NSAID)(如阿司匹林和环氧酶-2(COX-2)抑制剂)、疾病修饰性(disease modifying)抗炎药(DMARD,如甲氨蝶呤、来氟米特、和柳氮磺吡啶)、抗疟疾药物(如羟化氯喹)、环磷酰胺、D-青霉胺、硫唑嘌呤、金盐(gold salt)、肿瘤坏死因子抑制剂(如依那西普、英利昔单抗、阿达木单抗、戈利木单抗、和培戈-瑟托利珠单抗)、CD20抑制剂(如利妥昔单抗)、IL-1拮抗剂(如阿那白滞素)、IL-6抑制剂(如托珠单抗)、Janus激酶的抑制剂(JAK,如托法替尼)、阿巴西普、以及皮质类固醇等。
进一步考虑了IL-10突变蛋白、IL-10突变蛋白加抗原结合蛋白的组合,无论是以单独组合物还是以融合蛋白,都能增加IL-10作为抗炎性药物的治疗指数(TI)。在多个实施例中,当单独或与本披露的抗原结合蛋白组合施用时,IL-10突变蛋白的TI至少增加2、3、4、5、6、7、8、9、10倍或更多。
在多个实施例中,与wt IL-10相比,IL-10突变蛋白减少了髓细胞中TNF-α产生方面的抑制,降低了CD8+T细胞刺激方面的水平,和/或降低了B细胞刺激方面的水平。在多个实施例中,IL-10突变蛋白抗原结合蛋白抑制髓细胞中TNF-α产生。在多个实施例中,IL-10突变蛋白抗原结合蛋白抑制髓细胞中TNF-α产生,同时减少CD8+T细胞和B细胞激活。
在某些实施例中,使用分离的PBMC进行TNF-α抑制的测量。从受试者(人、小鼠、大鼠、食蟹猴等)的血液中分离PBMC,在体外用LPS刺激,并且在不同测试分子存在的情况下,使用例如ELISA ALPHALISA或MSD Vplex TNFα检测试剂盒来测定刺激前后TNFα的水平。
在某些实施例中,使用全血测定进行CD8+T细胞和/或B细胞激活的测量。从受试者中分离全血,在不同测试分子存在的情况下进行体外刺激,并且确定CD8+T细胞刺激水平或B细胞激活水平,例如通过检测由FACS测定的样品中pSTAT3水平。
施用和给药
本披露的方法包括施用包含如本文所述的IL-10突变蛋白、抗原结合蛋白或含有抗原结合部分和IL-10部分的抗原结合蛋白的药物组合物的步骤。在某些实施例中,药物组合物为无菌组合物。
既定剂量的治疗剂组合物的量可根据疗法施用的个体的体型以及所治疗的病症的特征而变化。
本披露提供了一种组合物,其包含本披露的IL-10突变蛋白、抗原结合蛋白或抗体、或含有如本文所述的抗原结合部分和IL-10部分的抗原结合蛋白、和药学上可接受的载剂。一种药物组合物,其包含本披露的IL-10突变蛋白、抗原结合蛋白或抗体、或含有如本文所述的抗原结合部分和IL-10部分的抗原结合蛋白,该药物组合物可以根据已知的方法配制以制备药学上有用的组合物,由此将治疗抗体与药学上可接受的载剂组合成混合物。如果组合物的施用可以被接受的病人耐受,则称其包含“药学上可接受的载剂”。无菌磷酸盐缓冲盐水是药学上可接受的载剂的一个实例。其他合适的载剂是本领域人员所熟知的。参见例如,Getman编辑,Remington's Pharmaceutical Sciences [雷明顿制药科学],第19版,Mack Publishing Company[马克出版公司](1995)。
对于药物用途,根据常规方法将本披露的多肽配制成用于经肠胃外,特别是静脉内或皮下递送。静脉内施用可通过推注、控释(例如使用微型泵或其他适当的技术)、或通过经一至数小时的典型时间段的输注。通常,药物配制品将包括本披露的IL-10突变蛋白、抗原结合蛋白或抗体、或本文所述的包含抗TREM-1部分和IL-10部分的抗原结合蛋白与药学上可接受的载剂(如盐水、缓冲盐水、5%右旋糖水溶液等)的组合。配制品可进一步包括一种或多种赋形剂、防腐剂、增溶剂、缓冲剂、防止蛋白质在小瓶表面损失的白蛋白等。当利用这种组合疗法时,本披露的IL-10突变蛋白、抗原结合蛋白或抗体、或本文所述的包含抗TREM-1部分和IL-10部分的抗原结合蛋白,可以组合在单个配制品中,也可以单独的配制品施用。配制品的方法在本领域是熟知的,例如在Gennaro编辑,Remington's Pharmaceutical Sciences[雷明顿制药科学],Mack Publishing Co.[麦克出版公司],Easton Pa.[宾夕法尼亚州伊斯顿](1990)中所披露的,将其通过引用并入本文。治疗剂量一般在每天0.1至100mg/kg患者体重的范围内,优选地每天0.5-20mg/kg,具体剂量由临床医生根据公认的标准确定,同时考虑要治疗的病症的性质和严重程度、患者的特征等。剂量的确定属于本领域的普通技术水平。更常见的,抗体将经一周或更短的时间施用,通常经一天至三天的时间段。通常,施用的抗体的剂量将根据患者的年龄、体重、身高、性别、一般身体状况和先前的病史等因素而变化。典型地,希望向接受者提供在约1pg/kg至10mg/kg(药剂量/患者体重)范围内的抗体剂量,尽管也可根据情况施用较低或较高剂量。
向受试者施用本披露的IL-10突变蛋白、抗原结合蛋白或抗体、或含有本文所述的抗原结合部分和IL-10部分的抗原结合蛋白可以是静脉内、动脉内、腹膜内、肌肉内、皮下、胸膜内、鞘内、通过区域导管灌注、或通过直接病变内注射。在多个实施例中,施用为静脉内或皮下。当通过注射施用IL-10突变蛋白、抗原结合蛋白或包含抗原结合部分和IL-10部分的抗原结合蛋白时,可以通过连续输注或单次或多次推注施用。
其他施用途径包括口服、粘膜-膜、肺和经皮。口服递送适用于聚酯微球、玉米醇溶蛋白微球、类蛋白微球、聚氰基丙烯酸酯微球和基于脂质的系统(参见例如,DiBase等人,“Oral Delivery of Microencapsulated Proteins[微胶囊蛋白的口服递送]”在Sanders等人编辑,Protein Delivery:Physical Systems[蛋白质递送:物理系统],第255-288页,Plenum Press[普莱纽姆出版社](1997))。鼻内递送的可行性通过这种胰岛素的施用方式举例说明(参见例如,Hinchcliffe等人,Adv.Drug Deliv.Rev.[先进药物递送评论],35:199(1999))。可以借助干粉分散器、液体气溶胶发生器或雾化器来制备和吸入包含本发明的抗体的干燥或液体颗粒(例如,Pettit等人,TIBTECH,16:343(1998);Patton等人,Adv.Drug Deliv.Rev.[先进药物递送评论],35:235(1999))。糖尿病管理系统说明了这种方法,该系统是手持式电子吸入器,可将雾化的胰岛素递送到肺部。研究表明,在低频超声波的帮助下,大至48,000kDa的蛋白质已经以治疗浓度穿过皮肤,这表明了经皮施用的可行性(Mitragotri等人,Science[科学],269:850(1995))。
出于治疗目的,以治疗有效量向患者施用包含本披露的IL-10突变蛋白、抗原结合蛋白或抗体、或含有如本文所述的抗原结合部分和IL-10部分的抗原结合蛋白、和药学上可接受的载剂的组合物。如果施用量具有生理学意义,则称以“治疗有效量”施用本披露的IL-10突变蛋白、抗原结合蛋白或抗体、或包含本文所述的抗原结合部分和IL-10部分的抗原结合蛋白与药学上可接受的载剂的组合。如果一种药剂的存在导致接受治疗的患者的生理学发生可检测的变化,那么这种药剂就具有生理学意义。例如,如果用于治疗炎症的药剂的存在能减轻炎性应答,则其具有生理学意义。可以通过多种方式评估有效治疗。在一个实施例中,通过减少的炎症确定有效治疗。在其他实施例中,通过抑制炎症来标志有效治疗。在仍其他实施例中,有效疗法通过患者健康状况的增加来测量,包括如体重增加、力量恢复、疼痛减轻、身体好转和来自患者身体状况更好的主观指示等迹象。
既定剂量的IL-10突变蛋白的量可根据疗法施用的个体的体型以及所治疗的病症的特征而变化。施用的IL-10突变蛋白的剂量在约0.05mg/kg至1mg/kg、或约0.05至0.5mg/kg的范围内。在多个实施例中,当与如本文所述的TREM-1抗体融合时,IL-10突变蛋白的剂量为约0.05mg/kg、0.1mg/kg、0.15mg/kg、0.2mg/kg、0.25mg/kg、0.3mg/kg、0.4mg/kg、0.5mg/kg、0.6mg/kg、0.75mg/kg、或1.0mg/kg,或当作为重量施用时,剂量为约1.0μg-50μg、或约1.0μg、3.0μg、5.0μg、7.5μg、10μg。
预期以30mg、40mg、50mg、60mg、70mg、80mg、90mg、100mg、125mg、150mg、200mg、250mg、300mg或更多的剂量施用抗原结合蛋白或包含抗原结合部分和IL-10部分(例如,包含抗TREM-1抗体序列)的抗原结合蛋白。IL-10突变蛋白或抗原结合蛋白可以30mg/ml、40mg/ml、50mg/ml、60mg/ml、70mg/ml、80mg/ml、90mg/ml、100mg/ml、125mg/ml、150mg/ml、200mg/ml、或250mg/ml的浓度配制。在多个实施例中,以约0.05mg/kg、0.25mg/kg、0.5mg/kg、0.75mg/kg、1.0mg/kg、1.25mg/kg、1.5mg/kg、2.0mg/kg、2.5mg/kg、3.0mg/kg、3.5mg/kg、4.0mg/kg、4.5mg/kg或5mg/kg的剂量施用例如,包含抗TREM-1抗体序列的抗原结合蛋白或融合蛋白。
每周一次、每周两次、每两周一次、每三周一次、每4周一次、每月一次、每3个月一次、或每六个月一次施用本文所述的组合物。
药物组合物(其包含本披露的IL-10突变蛋白、抗原结合蛋白或抗体、或含有如本文所述的抗原结合部分和IL-10部分的抗原结合蛋白)可以液体形式、气溶胶形式或固体形式提供。以可注射溶液和口服悬浮液为例说明液体形式。示例性固体形式包括胶囊、片剂、和控释型。后一种形式以微型泵和植入物为例进行说明(Bremer等人,Pharm.Biotechnol.[药物生物技术],10:239(1997);Ranade,“Implants in Drug Delivery[药物递送中的植入物]”,在Ranade等人编辑的,Drug Delivery Systems[药物递送系统],第95-123页,CRCPress[CRC出版社](1995);Bremer等人,“Protein Delivery with Infusion Pumps[用输液泵递送蛋白质]”,在Sanders等人编辑的,Protein Delivery:Physical Systems[蛋白质递送:物理系统],第239-254页,Plenum Press[普莱纽姆出版社](1997);Yewey等人,“Delivery of Proteins from a Controlled Release Injectable Implant[从控释注射式植入物中递送蛋白质]”,在Sanders等人编辑的,Protein Delivery:Physical Systems [蛋白质递送:物理系统],第93-117页,Plenum Press[普莱纽姆出版社](1997)。
配制品还可含有所治疗的具体适应症所必需的一种以上的活性化合物,优选那些具有互补活性而不会相互产生不利影响的活性化合物。可替代地,或此外,组合物可以包括增强其功能的药剂,例如,细胞毒性剂、细胞因子、化学治疗剂或生长抑制剂。此类分子合适地以对预期目的有效的量组合存在。
在一个实施例中,以组合疗法施用本披露的IL-10突变蛋白、抗原结合蛋白或抗体、或包含如本文所述的抗原结合部分和IL-10部分的抗原结合蛋白,即,与其他药剂(例如,可用于治疗病理病状或障碍,如自身免疫性障碍和炎性疾病的治疗剂)组合。在此上下文中,术语“组合”意指基本上同期、或者同时或依次给予药剂。如果依次给予,在第二种化合物开始施用时,两种化合物中的第一种优选在治疗部位仍能以有效浓度检测到。
预期本披露的治疗剂可在相同的配制品中同时给予。进一步考虑将药剂以单独的配制品施用并且兼行施用,兼行是指在彼此相隔30分钟内给予的药剂。进一步考虑,可以同时给予第二种药剂。
在另一个方面,在施用抗原结合蛋白组合物之前施用IL-10突变蛋白。在之前施用是指施用药剂,该施用是在用另一种药剂治疗前一周达至施用另一种药剂前30分钟的范围内施用。进一步考虑在施用另一种组合物或药剂继后施用药剂。继后施用是指从抗体治疗后30分钟到抗体施用后一周的施用,例如,30分钟、1小时、2小时,4小时、1天、2天等。进一步考虑,第二
例如,组合疗法可以包括将本披露的一种或多种IL-10突变蛋白、抗原结合蛋白或抗体、或包含本文所述的抗原结合部分和IL-10部分的抗原结合蛋白与一种或多种另外的治疗剂,例如一种或多种细胞因子和生长因子抑制剂、免疫抑制剂、抗炎剂、代谢抑制剂、酶抑制剂、和/或细胞毒性或细胞生长抑制剂共配制和/或共施用。
与本披露的IL-10突变蛋白、抗原结合蛋白或抗体、或包含本文所述的抗原结合部分和IL-10部分的抗原结合蛋白组合使用的治疗剂包括在炎性应答的不同阶段进行干扰的药剂。在一个实施例中,将本披露的IL-10突变蛋白、抗原结合蛋白或抗体、或包含如本文所述的抗原结合部分和IL-10部分的抗原结合蛋白与一种或多种另外的药剂共配制和/或共施用,这些另外的药剂如其他细胞因子或生长因子拮抗剂(例如,可溶性受体、肽抑制剂、小分子、配体融合物);或与其他靶标结合的抗体或其抗原结合片段(例如,与其他细胞因子或生长因子、其受体、或其他细胞表面分子结合的抗体);以及抗炎性细胞因子或其激动剂。可与本文所述的抗体组合使用的药剂的非限制性实例包括但不限于,一种或多种白介素(IL)或其受体的拮抗剂,例如,IL-1、IL-2、IL-6、IL-7、IL-8、IL-12、IL-13、IL-15、IL-16、IL17A-F、IL-18、IL-20、IL-21、IL-22、IL-23IL-25、IL-31、IL-32、IL-33的拮抗剂;细胞因子或生长因子或其受体的拮抗剂,如LT、EMAP-II、GM-CSF、FGF和PDGF的拮抗剂。本发明的抗体还可与例如针对细胞表面分子(如CD2、CD3、CD4、CD8、CD20(例如,CD20抑制剂利妥昔单抗)、CD25、CD28、CD30、CD40、CD45、CD69、CD80(B7.1)、CD86(B7.2)、CD90、或其配体(包括CD154(gp39或CD40L))、或LFA-1/ICAM-1和VLA-4/VCAM-1)的抗体的抑制剂组合(Yusuf-Makagiansar等人,Med.Res.Rev.[药物研究述评],22:146-167(2002))。可组合使用的示例性拮抗剂包括IL-1、IL-6、IL-12、TNFα、IL-15、IL-18、IL-20、IL-22、IL-23和IL-31的拮抗剂。
在其他实施例中,一种或多种IL-10突变蛋白、抗原结合蛋白或包含本披露的抗原结合部分和IL-10部分的抗原结合蛋白可与一种或多种抗炎药、免疫抑制剂、或代谢或酶抑制剂共配制和/或共施用。可与本文所述的抗体组合使用的药物或抑制剂的非限制性实例包括但不限于以下中的一种或多种:一种或多种非类固醇抗炎药(NSAID),例如,布洛芬、替尼达普、萘普生、美洛昔康、吡罗昔康、双氯芬酸、和吲哚美辛;柳氮磺吡啶;皮质类固醇,如泼尼松龙;一种或多种细胞因子抑制性抗炎药(CSAID);核苷酸生物合成的抑制剂,例如,嘌呤生物合成的抑制剂、叶酸拮抗剂(例如,甲氨蝶呤(N-[4-[[(2,4-二氨基-6-喋啶基)甲基]甲基氨基]苯甲酰基]-谷氨酸);以及嘧啶生物合成的抑制剂,例如,二氢乳清酸脱氢酶(DHODH)抑制剂。与本发明的一种或多种抗体(例如,双特异性抗体)组合使用的优选的治疗剂包括NSAID、CSAID、(DHODH)抑制剂(例如,来氟米特)、和叶酸拮抗剂(例如,甲氨蝶呤)。
另外的抑制剂包括以下中的一种或多种:皮质类固醇(口服、吸入和局部注射);免疫抑制剂,例如,环孢菌素、他克莫司(FK-506);以及mTOR抑制剂,例如,西罗莫司(雷帕霉素--)或雷帕霉素衍生物,例如,可溶性雷帕霉素衍生物(例如,酯雷帕霉素衍生物,例如,CCI-779);通过促炎性细胞因子(如IL-1)干扰信号传导的药剂(例如,IRAK、NIK、IKK、p38或MAP激酶抑制剂);COX2抑制剂,例如,塞来昔布、罗非昔布、及其变体;磷酸二酯酶抑制剂,例如,R973401(IV型磷酸二酯酶抑制剂);磷脂酶抑制剂,例如,胞质磷脂酶2的抑制剂(cPLA2)(例如,三氟甲基酮类似物);血管内皮细胞生长因子或生长因子受体的抑制剂,例如,VEGF抑制剂和/或VEGF-R抑制剂;以及血管发生的抑制剂。与本披露的IL-10突变蛋白、抗原结合蛋白或抗体、或本文所述的包含抗TREM-1部分和IL-10部分的抗原结合蛋白组合使用的优选的治疗剂是免疫抑制剂,例如,环孢菌素、他克莫司(FK-506);mTOR抑制剂,例如,西罗莫司(雷帕霉素)或雷帕霉素衍生物,例如,可溶性雷帕霉素衍生物(例如,酯雷帕霉素衍生物,例如,CCI-779);COX2抑制剂,例如,塞来昔布及其变体;以及磷脂酶抑制剂,例如,胞质磷脂酶2的抑制剂(cPLA2)(例如,三氟甲基酮类似物)。
试剂盒
本披露还考虑了包含一个或多个容器的试剂盒,这些试剂盒包含本披露的IL-10突变蛋白、抗原结合蛋白或抗体、或含有如本文所述的抗原结合部分和IL-10部分的抗原结合蛋白,最佳地在药学上可接受的载剂或组合物中。本披露的IL-10突变蛋白、抗原结合蛋白或抗体、或包含本文所述的抗原结合部分和IL-10部分的抗原结合蛋白可以作为单位剂量或作为将在注射前重构的无菌粉末以单剂量或多剂量的可注射溶液形式提供。可替代地,这种试剂盒可以包括用于施用一种或多种治疗剂的干粉分散器、液体气溶胶发生器或雾化器。这种试剂盒可进一步包括关于药物组合物的适应症和用法的说明书和书面信息。
还考虑了注射器,例如一次性使用或预填充注射器、无菌密封容器(例如小瓶、瓶子、容器、和/或试剂盒或包装),其包含上述IL-10突变蛋白、抗原结合蛋白或包含抗TREM-1部分和IL-10部分的抗原结合蛋白或组合物中的任何一种,任选地带有合适的使用说明。
在另一个实施例中,本发明提供了制品或单位剂形,其包含:(a)含有本披露的IL-10突变蛋白、抗原结合蛋白或抗体、或本文所述的包含抗TREM-1部分和IL-10部分的抗原结合蛋白的物质的组合物;(b)含有所述组合物的容器;以及(c)贴附于所述容器上的标签,或包括在所述容器中的包装说明书,其涉及所述抗体用于治疗免疫相关疾病的用途。
在另一个方面,组合物或试剂盒包含另外的活性成分,其可以例如是另外的抗体或本文所述的抗炎剂、细胞毒剂或其他药剂。优选地,组合物是无菌的。
实例
实例1-IL-10突变蛋白的产生
本文假设,与野生型IL-10相比表现出与IL-10R1/R2差异结合并表现出差异的免疫刺激活性的IL-10突变蛋白将作为免疫疗法使用。
通过在IL-10的环D和E之间插入6个氨基酸的接头(GGGSGG)(SEQ ID NO:2676),制成稳定的IL-10单体(IL-10M1)(Josephson等人,J.Biol.Chem[生物化学杂志],275:13552-13557,2000)。IL-10M1以hIL-10/IL-10R1的结构为模型。hIL-10的24个残基参与了结合界面,有两个相互作用表面,即IL-10的位点Ia-螺旋F和AB环以及IL-10R1的L2-L4,以及IL-10的位点螺旋A的Ib-N末端和螺旋F的C末端、IL-10R1的L5-L6。
根据病毒IL-10(83%的同源性)和食蟹猴(cyno)IL-10之间的结构差异,开发了IL-10突变算法。为了促进IL-10在融合蛋白中融合(例如与抗体融合)时的正确折叠,IL-10M1被用作突变蛋白设计的支架,以使最后两个α-螺旋折叠到N末端球状结构域上并形成功能性单体。以下描述的结构和序列分析的组合被用来帮助集中潜在的残基进行突变。为了缩小突变蛋白组的大小,使用ΔΔG结合能计算来确定对受体界面有最大不稳定影响的突变。
算法利用了IL-10和IL-10/IL-10R1的序列、突变和已知结构,重点关注侧链面向界面的残基,并最大化位点Ib的突变多样性。对单点突变进行了筛选,但Trp、Phe、Pro(排除)或Cys残基没有发生突变。通过在结合表面上的每个残基中选择至少一个突变来最大化序列多样性。
其他策略包括:将AB环中的每个残基突变为Gly或Pro以利于无序构象,在CD环中选择保守突变,包括截短N末端和C末端柔性环,并利用能量计算(即ΔΔG结合)来缩小突变组。
共制造并筛选了235个突变。针对IL-10R1的结合研究了以下残基的突变:P20、L23、R24、R27、D28、K34、T35、Q38、M39、K40、D41、Q42、L43,、D44、N45、L46、L47、L48、K49、N82、Q83、D84、P85、D86、I87、K138、S141、E142、D144、I145、或E151。N末端和C末端截短也包括在组中,以防它们改变IL-10活性。突变体的编号基于SEQ ID NO:2,该突变体是缺乏18个氨基酸信号肽的野生型人IL-10。
为进一步分析制造和选择的突变包括:AB环,D41G、L46K;位点Ia,Q38E(螺旋A)、Q38R(螺旋A)、K34D(螺旋A)、K138L(螺旋F)、K138D(螺旋F);位点Ib,R27L(螺旋A)。这些突变蛋白中的每一个还包括IL-10的螺旋D和E之间的GGGSGG(SEQ ID NO:2676)接头。示例性序列示于表1中。
表1:IL-10突变蛋白序列
除了突变分析外,还产生了插入D和E螺旋之间的不同大小的接头。罗塞塔重建模(Rosetta Remodel)(Huang等人,PLoS One.[公共科学图书馆期刊]2011;6(8):e24109)被用来建模IL-10的螺旋结构中插入不同的氨基酸后的蛋白质结构,包括3聚体、4聚体、5聚体和6聚体。GS接头在模型中得分很高。表2中列出了建模的接头序列。
表2:IL-10突变蛋白的接头
表3显示了选定的IL-10突变蛋白和IL-10突变蛋白与抗TREM-1抗体1B12的融合物在293细胞中对LPS诱导的TNF的抑制。融合分子的重链具有鉴定的序列;每个融合分子的轻链序列是抗体1B12(SEQ ID NO:2185)的轻链序列。
表3:IL-10突变蛋白和抗TREM-1抗体1B12对LPS的抑制
IL-10突变蛋白的目标是保留/恢复IL-10对单核细胞和巨噬细胞的抑制活性并减小IL-10对CD8+T细胞和B细胞的刺激。
实例2-抗TREM-1抗体
人们认为,为了延长IL-10的半衰期和活性,将其与细胞表面靶向部分融合将是有益的。产生了高亲和力的抗TREM-1单克隆抗体,并评估了其将IL-10靶向到免疫细胞并延长IL-10半衰期的能力。
用人和/或食蟹猴TREM1蛋白、TREM1表达载体和/或表达TREM1的CHO细胞免疫小鼠。对于基因免疫,根据制造商的说明书,使用基因枪系统(伯乐公司(BioRad),赫拉克勒斯,加利福尼亚州)经8周对小鼠进行了16次免疫。简而言之,将编码人TREM-1和DAP12、或食蟹猴TREM-1和DAP12的表达载体合并,将2μg总DNA包被到1.6um金珠(伯乐公司,赫拉克勒斯,加利福尼亚州)上,并递送至剃毛小鼠腹部的上皮中。对于可溶性蛋白免疫接种,将小鼠用代表N末端细胞外结构域的人或食蟹猴TREM-1重组蛋白进行免疫。用Alum和CpG-ODN或西格玛公司佐剂系统(Sigma Adjuvant System)辅佐的重组蛋白对动物进行免疫接种,经10-12周进行14-17次皮下注射,沿着位于尾根和肩胛下区域的小鼠背中线的两个位置递送。最初的可溶性蛋免疫接种递送了10μg,随后的强化免疫为5μg。对于细胞免疫接种,用200-400万个瞬时表达人TREM-1或食蟹猴TREM-1的以Alum和CpG-ODN为佐剂的CHO-S细胞对小鼠进行免疫接种。经10周,每周对动物进行1或2次免疫注射,共13次,交替进行腹膜内注射和尾根的皮下注射。在免疫接种研究期间的不同时间点(从4周到10周),对动物进行放血,并收集血浆,以评估TREM1特异性效价。使用瞬时转染的293T细胞,通过ACCURITM流式细胞仪(BD生命科学公司(BD Biosciences))上的活细胞FACS分析监测TREM1特异性血浆效价。将具有最高抗人和食蟹猴TREM1的抗原特异性血浆效价的动物处死并用于杂交瘤产生(Kohler和Milstein,1975)。
杂交瘤产生:对表现出合适抗原特异性血清效价的动物进行鉴定,并从每次收获的选定的小鼠中汇集脾脏和/或引流淋巴结。通过在合适的培养基中研磨或使用半自动组织离解仪GENTLEMACSTM离解器(美天旎生物技术公司(Miltenyi Biotec)),将脾细胞和淋巴细胞与淋巴组织解离。使用标准方法分离、扩增表达IgG的B细胞,并与合适的细胞融合配偶体融合。通过CELLINSIGHTTM,针对与在HEK293细胞上短暂表达的人类TREM-1的结合,测试杂交瘤上清液。简而言之,按照制造商的方案,使用293Fectin(英杰公司)将HEK293细胞用编码人TREM-1和DAP12的哺乳动物表达构建体以1:1比率或用模拟载体和仅DAP12瞬时共转染。第二天,将15,000个细胞/孔的转染HEK293细胞与等体积的耗尽型杂交瘤培养基试验样品和终浓度为15μg/mL的核染色剂Hoechst 33342(皮尔斯公司(Pierce))在384孔FMAT板(康宁公司(Corning))中组合,总体积为30μL/孔。在室温下孵育1小时后,用板洗涤器吸出上清液,并将孔在AquaMax上洗涤2个循环,每个循环用50μL/孔的FACS缓冲液(PBS(海克隆公司(Hyclone)),2%FBS(西格玛公司(Sigma)))。将细胞用5μg/mL AlexaFluor 488山羊抗人IgG Fc(杰克森免疫研究公司(Jackson ImmunoResearch))二级抗体染色,在Big Bear板式震荡器上摇动,并在室温下孵育20分钟。使用板洗涤器吸出上清液,使用50μL/孔的FACS缓冲液再次洗涤孔2个循环,并使用多点仪器将30μL的FACS缓冲液添加至各孔中。将板置于Big Bear板式震荡器上,以使细胞均匀分布在孔中,然后在CELLINSIGHTTMCX7平台上使用Cell Health Profiling Bio-App读取。
评估了初步筛选中鉴定的TREM-1特异性抗体对食蟹猴TREM-1的交叉反应性,以及对TREM-1而非DAP12的特异性。通过FACS(收获物1-6)或CELLINSIGHTTM(收获物8-9)测试TREM-1杂交瘤上清液与HEK293细胞上瞬时表达的人或食蟹猴TREM-1的结合。对于来自收获物1-6的TREM1抗体,使用293Fectin将HEK293细胞用编码人TREM-1和DAP12、食蟹猴TREM-1和DAP12的哺乳动物表达构建体以1:1比率或模拟载体和人DAP12瞬时共转染。第二天,将转染的HEK293细胞以50,000个细胞/孔转移到96孔FACS板中,并与终浓度为2.5μg/mL的归一化的杂交瘤上清液在4℃下孵育1小时。然后通过离心使细胞沉淀,通过翻动去除上清液,并将孔用200μL/孔的FACS缓冲液洗涤两次。将5μg/mL647山羊抗人IgGFc(杰克森免疫研究公司)二级检测抗体和2.5μg/mL 7-氨基放线菌素-D(西格玛公司)活力染色剂在4℃下与细胞孵育15分钟。通过离心使细胞沉淀,通过翻动去除上清液,并将孔用200μL/孔的FACS缓冲液再洗涤一次。在带有Intellicyt自动取样器的BD ACCURITMC6流式细胞仪上通过FACS检测显示人TREM-1或食蟹猴TREM-1特异性结合的TREM-1杂交瘤上清液。数据报导为相对于不相关对照抗体结合的几何平均值(GM)倍数。某些抗TREM-1抗体的结合结果示于表4。
表4:人/食蟹猴交叉反应性和特异性筛选中的TREM1抗体
评估了具有高质量TREM1特异性结合和人/食蟹猴交叉反应性的TREM1抗体阻断配体PGLYRP1与在HEK293细胞上瞬时表达的人TREM1/DAP12结合的能力。简而言之,使用293Fectin将HEK293细胞用编码人TREM1和DAP12的哺乳动物表达构建体以1:1比率或模拟载体和人DAP12瞬时共转染。第二天,将转染的HEK293细胞以50,000个细胞/孔转移到96孔FACS板中,并与终浓度为2.5μg/mL的归一化的杂交瘤上清液在4℃下孵育1小时。将人PGLYRP1-His(R&D系统公司(R&D Systems))与PGN-ECndss(肽聚糖,英杰公司(InvivoGen))组合,在室温下孵育15分钟,然后以7.5μg/mL PGLYRP1和30μg/mL PGN的最终浓度添加到孔中。然后摇动板并在4℃下孵育15分钟。然后通过离心使细胞沉淀,通过翻动去除上清液,并将孔用200μL的FACS缓冲液洗涤。将5μg/mL ALEXA647人抗His二级检测抗体和2.5μg/mL 7-氨基放线菌素-D(西格玛公司)活力染色剂添加到细胞,摇动,并且在4℃下孵育15分钟。将细胞用FACS缓冲液洗涤,通过离心沉淀,通过翻动去除上清液,并且再用FACS缓冲液洗涤一次。然后在带有Intellicyt自动取样器的BD ACCURITMC6流式细胞仪上运行细胞。共有518个TREM1抗体显示出所需的特定的PGLYRP1阻断活性。表5总结了选定的TREM-1单克隆抗体的受体-配体抑制。
表5:选定的TREM1抗体的受体-配体抑制
通过限制性抗原测定对TREM-1抗体进行相对亲和力排序:在使用珠(Luminex)在FACS上进行的限制性抗原测定中,TREM1杂交瘤上清液通过其与可溶性TREM-1的结合动力学在组中进行亲和力排序。简而言之,将内部生物素化的人TREM-1-His抗原(b-huTREM-1-His)在FACS缓冲液中连续稀释,并与等体积的珠(每个抗原浓度具有不同的唯一条形码编码的珠)组合,从30ng/mL的最终的b-huTREM-1-His抗原浓度开始,产生5点2倍的连续稀释系列。将抗原-珠混合物铺在96孔FACS板中的3个孔中,然后在室温避光下孵育30分钟。然后通过离心使珠沉淀,通过翻动去除上清液,并将孔用200μL/孔的FACS缓冲液洗涤两次。然后将不同的珠重悬、合并,并在免疫测定稳定剂(SurModics公司)中稀释以阻断非特异性结合。将归一化的TREM-1杂交瘤上清液与等体积的珠混合物在FACS板中组合,最终浓度为5μg/mL测试抗体,到0.5μL珠/孔。然后摇动板并在室温下孵育过夜,持续18小时。然后通过离心使珠沉淀,通过翻动去除上清液,并将孔用200μL/孔的FACS缓冲液洗涤两次。将488山羊抗人IgG F二级检测抗体(杰克森免疫研究公司)以5μg/mL添加到板中,摇动,并在室温下避光孵育15分钟。将珠用FACS缓冲液洗涤,通过离心沉淀,通过翻动去除上清液,并且再用FACS缓冲液洗涤一次。然后将珠重悬,并且在带有Intellicyt自动取样器的BDACCURITMC6流式细胞仪上运行。
与对照IgG抗体样品相比,显示至少两倍或更大信号的TREM-1杂交瘤样品被认为具有TREM-1特异性结合谱。抗体结合信号与抗体亲和力相关;抗体与靶抗原TREM-1的结合程度与测量的荧光强度相关,因此可以对整个组的亲和力进行相对比较。在限制性抗原筛选中,具有比基准抗体1B2更好的结合的TREM-1抗体被推进到轻链测序和人/食蟹猴亲和力差距分析。表6显示了使用在仪器信号检测线性范围内的代表性抗原涂层浓度的选定的TREM-1抗体的抗体结合数据。
表6:在有限抗原结合测定中选定的TREM1抗体的相对亲和力
TREM1的相对表位分组/分析:使用珠(Luminex)在FACS上对TREM1杂交瘤上清液进行表位分组测定(改良的抗体-抗体竞争测定)进行评估,以确定小组中相对独特的表位分组的种类。简而言之,一组15种不同的经独特条形码编码的珠分别与等体积的在FACS缓冲液中稀释的、最终浓度为100ng/mL的内部生物素化的人TREM-1-His抗原组合。将抗原-珠混合物铺在96孔FACS板中的3个孔中,然后在室温避光下孵育30分钟。然后通过离心使珠沉淀,通过翻动去除上清液,并将孔用200μL/孔的FACS缓冲液洗涤两次。选择具有不同的VDJ重排和良好的定量的15种不同TREM-1抗体,这些抗体在限制性抗原测定中显示出良好的结合,作为预涂珠的参考抗体。这15种抗体在FACS缓冲液中以5μg/mL的饱和浓度制备,并与15种不同的珠中的每种在室温下避光孵育1小时。通过离心使珠沉淀,通过翻动去除上清液,并将孔用200μL/孔的FACS缓冲液洗涤三次。然后将不同的珠重悬、合并,并在免疫测定稳定剂(SurModics公司)中稀释以阻断非特异性结合。将归一化的TREM-1杂交瘤上清液(测试抗体)与等体积的珠混合物在FACS板中组合,最终浓度为5μg/mL测试抗体,到0.5μL珠/孔。然后摇动板并在室温避光孵育持续1小时。然后通过离心使珠沉淀,通过翻动去除上清液,并将孔用200μL/孔的FACS缓冲液洗涤两次。将ALEXA488山羊抗人IgG F二级检测抗体(杰克森免疫研究公司)以5μg/mL添加到板中,摇动,并在室温下避光孵育15分钟。将珠用FACS缓冲液洗涤,通过离心沉淀,通过翻动去除上清液,并且再用FACS缓冲液洗涤一次。然后将珠重悬,并且在带有Intellicyt自动取样器的BD ACCURITMC6流式细胞仪上运行。
与参考抗体竞争TREM-1抗原上类似表位的测试抗体被阻止结合,而非竞争抗体能够与参考抗体结合以产生加性信号。然后用二级抗体检测总结合抗体。为了确定各个测试抗体的抗体竞争/结合谱,从每个竞争/结合反应(即整个参考抗体组)的参考抗体加测试抗体信号中减去仅参考抗体结合信号。下表7中显示了选择的TREM-1抗体的相对表位分组的概述。
表7:选择的靠前TREM1抗体的相对表位分组
| 抗体ID | 表位分组 |
| 3E12 | B |
| 34D1 | ND |
| 30H2 | ND |
| 44A5 | A |
| 46H7 | A |
| 49A2 | A |
| 50A12 | A.1 |
| 57C10 | A |
| 57F5 | A |
| 61B12 | A |
| 61G5 | A |
| 63F8 | A |
| 64D7 | A |
| 66B8 | A |
TREM1抗体人/食蟹猴亲和力差距确定:分析了具有独特CDR3序列的TREM-1抗体对人和食蟹猴TREM-1的亲和力,这些抗体在限制性抗原筛选中也显示出比基准抗体更好的结合。使用HTX仪器(福特生物公司)测定了114种TREM-1抗体的结合亲和力KD(M)、缔合速率常数ka(M-1s-1-)和解离速率常数kd(s-1)。简而言之,通过在测定缓冲液(10mM Tris,0.1%Triton X-100,150mM NaCl,1mM CaCl2,0.1mg/mL BSA,pH 7.6)中以1:10稀释至最终测试浓度为1μg/mL制备在DMEM空白培养基(null media)中相对于10μg/mL归一化的TREM-1杂交瘤上清液。在使用前将胺反应性第二代AR2G生物传感器(分子装置公司(Molecular Devices))在200μL纳米孔水中预孵育至少10分钟。然后将AR2G生物传感器在20mM EDC(1-乙基-3-[3-二甲氨基丙基]碳化二亚胺盐酸盐)(福特生物公司(ForteBio))与10mM NHS(N-羟基磺基琥珀酰亚胺)(福特生物公司)在纳米孔水中预混合的溶液中活化5分钟。将内部生成的小鼠抗人Fc单克隆抗体以10μg/mL在pH 5的10mM醋酸钠缓冲液中偶联至AR2G生物传感器,持续5分钟,用pH 8.5的1M乙醇胺淬灭5分钟,然后用于从溶液中捕获抗体。将TREM-1测试抗体加载至生物传感器上,持续5分钟,并取得基线测量值,持续1分钟。然后将重组可溶性人TREM-1-His蛋白与加载了抗体的生物传感器以3倍的稀释系列结合,涵盖从450nM到1.85nM或150nM到0.62nM的6个点。测量重组人TREM-1与装载了抗体的传感器的缔合5分钟,随后在缓冲液中解离10分钟。然后将生物传感器用pH 1.7的10mM甘氨酸再生,用相同的TREM-1抗体在相同的传感器上重新加载5分钟,并且用同样的方法测量食蟹猴TREM-1-His蛋白的缔合和解离。使用0nM的分析物参考传感器对数据进行了参考。在Genedata Screener软件中,使用1:1朗格缪尔(Langmuir)传质模型进行动力学分析。鉴定了符合设计目标的TREM-1抗体,并且在人和食蟹猴TREM-1之间显示出小于10倍的亲和力差异,其结合亲和力显示在表8中。
表8:具有<10倍的人和食蟹猴TREM-1亲和力差距的TREM1抗体
*A<符号表示在分配的10分钟解离时间内解离的TREM1少于10%,表明kd<1.76E-4s-1。根据kd<1.76E-4s-1计算<KD(M)。
抗体的选择基于与人或食蟹猴TREM-1的结合、与TREM2的结合的缺乏以及它们阻断PGLYRP1与TREM-1结合的能力。如表9中列出,选择了14种抗体进行进一步研究。
表9:抗TREM-1抗体克隆
实例3—抗TREM-1抗体的重新格式化
通过将κ轻链的VL结构域与CK结构域融合,将λ轻链的VL结构域与CL结构域融合,将VH结构域与CH1-CH2-CH3(221-447)序列融合,将活动中的先导抗TREM-1抗体转化为IgG1z亚型的抗体格式。该抗体同种型的CH2结构域通过引入N297G突变被工程化以降低效应子功能,并通过工程化的二硫键(R292C,V302C)以提高热稳定性;该抗体同种型被命名为IgG1z SEFL2。将先导抗TREM-1抗体进行额外的工程化以去除“热点”,即经计算预测或根据经验确定对分子的表达、纯化、热稳定性、胶体稳定性、长期储存稳定性、体内药代动力学和/或免疫原性有负面影响的残基。这些热点处的各种氨基酸突变是根据保守性、共变性、化学相似性、结构模型的预测以及其他抗体工程活动的先验知识设计的。设计了一小组合理设计的工程化的抗体,这些抗体包括单一突变和突变组合两者。
合理设计的热点工程化的变体的重组表达构建体是使用金门(Golden Gate)克隆方法生产的,以组装1)包含抗体可变结构域的合成DNA片段,2)先前克隆的含有必要的恒定结构域(即CK或CL、CH1-CH2-CH3(118-447)(R292C、N297G、V302C)的“部分载体”,和3)哺乳动物表达载体骨架。将重链(HC)组装到带有嘌呤霉素选择盒的载体骨架中,将轻链(LC)组装到带有潮霉素选择盒的载体骨架中。使用Lipofectamine LTX(吉布科公司(Gibco))在CHO-K1细胞中将HC和LC表达载体以1:1的比率共转染,在10ug/mL嘌呤霉素和500ug/mL潮霉素存在下通过每2–3天传代一次直到细胞活力>90%(Vi-CELL BLU,贝克曼库尔特公司(Beckman Coulter))来产生稳定的池。将稳定的池以2e6个活细胞/mL培养物接种在生产培养基中,并在36℃下在5%CO2中孵育6天。通过离心收获细胞上清液,并使用AmMagTM蛋白A磁珠(金斯瑞公司(GenScript))或MAG SEPHAROSETMPrismA(思拓凡公司(Cytiva))通过磁珠亲和色谱法纯化抗体。通过完整质谱法确认每个变体的身份。对于每个变体,使用蛋白A传感器通过ForteBio(颇尔生命科学公司(Pall Life Sciences))测量条件培养基中的表达效价。通过分析性尺寸排阻色谱法测量蛋白A亲和色谱法后存在的高分子量(%HMW)物质的百分比,并且通过使用LabChip GXII(珀金埃尔默公司(Perkin Elmer))的非还原性微毛细管电泳(MCE NR)测量靶蛋白纯度百分比。通过这一过程制备的变体的数据见表10。
表10:合理设计的热点工程化的TREM1抗体的组
活动中的三个抗TREM-1先导抗体(30H2(19330)、49A2(19333)和46H7(19332))的子集也通过酵母展示进行了工程化,以提高可制造性并保留对TREM-1的结合。对于每个抗体,都产生文库,其中将所有六个CDR中的每一个可能的相邻的残基对通过使用简并NNK密码子同时突变为所有可能的氨基酸。将文库展示在BJ5464的酵母衍生物的表面,其中Fd结构域与α-凝集素的N末端融合,并且LC没有与酵母表面融合。ALEXA647缀合的抗Fab抗体的结合测量展示的效率。使用抗生蛋白链菌素PE作为二级荧光,针对与生物素缀合的重组TREM-1ECD的高度结合,利用荧光激活细胞分选法(FACS)对文库进行分选。用针对HC和LC的框架1(FW1)和FW4结构域的特异性引物扩增存在于分类结合/显示双阳性池和显示阳性池中的可变结构域,并在Illumina MiSeq上进行2x300bp运行下的NGS分析。通过共同频率分析处理数据后选出突变,其中将阳性结合氨基酸频率的比率除以阳性展示氨基酸频率,然后将其相对于亲本序列比率归一化。富集值大于或等于亲本序列的序列被视为是有益的或可耐受的多样性,并被用于亲和力成熟后的额外合理抗体工程化。
靠前展示的工程化可变结构域被转换为IgG1z SEFL2的同型,并使用金门克隆方法进行克隆,以组装1)包含抗体可变结构域的合成DNA片段,2)先前克隆的含有必要的恒定结构域(即CK或CL、CH1-CH2-CH3(118-447)(R292C、N297G、V302C)的“部分载体”,和3)哺乳动物表达载体骨架。将重链(HC)组装到带有嘌呤霉素选择盒的载体骨架中,将轻链(LC)组装到带有潮霉素选择盒的载体骨架中。使用Lipofectamine LTX(吉布科公司)在CHO-K1细胞中将HC和LC表达载体以1:1的比率共转染,在10ug/mL嘌呤霉素和500ug/mL潮霉素存在下通过每2–3天传代一次直到细胞活力>90%(Vi-CELL BLU,贝克曼库尔特公司)来产生稳定的池。将稳定的池以2e6个活细胞/mL培养物接种在生产培养基中,并在36℃下在5%CO2中孵育6天。使用AMMAGTM蛋白A磁珠(金斯瑞公司)通过磁珠亲和色谱法纯化抗体。通过完整质谱法确认每个分子的身份。通过分析性尺寸排阻色谱法测量蛋白A亲和色谱法后存在的高分子量(%HMW)物质的百分比,并且通过使用LabChip GXII(珀金埃尔默公司)的非还原性微毛细管电泳(MCE NR)测量靶蛋白纯度百分比。通过酵母展示热点工程化制备的变体的数据见表11。
表11:酵母展示热点工程化的变体TREM1抗体
通过使用p-Syk(珀金埃尔默公司(Perkin-Elmer))分析细胞中Syk激酶的磷酸化水平,比较表达TREM-1/DAP12的HEK293细胞中的二价和单价抗TREM-1mAb。简而言之,在37℃/5%CO2下,将稳定表达人TREM1和DAP12的HEK293细胞在DMEM/F12Ham培养基(康宁公司)中培养,该培养基补充有10%透析FBS(吉布科公司)、2mMGlutaMAX(吉布科公司)、2mM L-谷氨酰胺(西格玛公司)、1%青霉素/链霉素(吉布科公司)和0.1mg/mL博来霉素(吉布科公司)。在实验前一天,将细胞使用胰蛋白酶-EDTA分离,并以400x g离心5分钟。将细胞沉淀重悬于完全培养基中,然后以400x g再次离心5分钟。离心后,将细胞以1x106个细胞/mL的浓度重悬于完全培养基中,并以100μL/孔或50,000个细胞/孔的终体积接种至96孔透明平底聚苯乙烯板(康宁公司)。将接种的板在37℃/5%CO2下过夜孵育,持续18至24小时。实验当天,从每个孔中取出70μL的培养基。将TREM1抗体在测定培养基(补充有10%热灭活FBS的DMEM/F12 HAM培养基)中以4倍系列稀释液稀释至最高终浓度的3倍。使用测定培养基以最终浓度的3倍制备交联试剂蛋白质G(西格玛公司)。将滴定的TREM1抗体与蛋白G或测定培养基以1比1混合,并将每种TREM1抗体+/-交联试剂的60μL添加到含有细胞的每个孔中。将这些板在室温下孵育1小时,然后从孔中取出所有培养基,再将细胞用25μL/孔的裂解缓冲液(M-Per哺乳动物蛋白提取试剂和1X Halt蛋白酶/磷酸酶抑制剂)裂解。将细胞与裂解缓冲液在冰上孵育1小时,然后将5μL的细胞裂解物转移到384孔白板(珀金埃尔默公司(PerkinElmer))的每个孔中,其中含有受体混合物(1nM抗pSyk、兔IgG(抗磷酸化Syk(Tyr525/526)(克隆C87C1))(细胞信号传导技术)、1nM生物素-抗Syk、小鼠IgG(克隆4D10)(BD生命科学公司)、10μg/mL抗兔IgG受体珠(珀金埃尔默公司)、和1X Halt抑制剂于1X免疫测定缓冲液(珀金埃尔默公司)中。将板在冰上进一步孵育2小时,然后以40μg/mL终浓度添加5μL的供体混合物(链霉亲和素-α-供体珠(珀金埃尔默公司)于1X免疫测定缓冲液中),并在室温下在黑暗中孵育1小时。孵育后,使用读板仪(珀金埃尔默公司)通过FRET(荧光共振能量转移)检测磷酸化-Syk(pSyk)信号。结果通过样品pSyk信号与基础pSyk信号的比例计算,其中比较各抗体的效力和最大信号变化。单独的二价抗TREM-1mAb处理在表达TREM-1/DAP12的细胞中诱导微弱信号。单价抗TREM-1mAb情况下没有观察到pSyk信号,并且二价和单价抗TREM-1mAb与蛋白G交联会导致pSyk诱导。
抗体序列的分枝和比对:提取输入抗体序列的VH和VL结构域,并将其与基于Honegger和Pluckthun的基于结构的IgG编号系统进行比对(J Mol Biol.[分子生物学杂志]309(3):657-70,2001)。使用未校正的模型从复合多序列比对中产生了距离矩阵,其中两个序列之间的距离是VH和VL结构域中错配的分数。最后,通过UPGMA(带算术平均值的非加权配对分组法)方法,使用距离矩阵来构建树(Sokal和Michener,University of KansasScience Bulletin.[堪萨斯大学科学通报]38:1409-1438,1958),并且相关序列基于0.2的分支遍历限制进行分组。基于氨基酸的化学相似性对比对进行了手动改进,以产生每个分枝组的共有CDR序列,产生的序列见表12。
表12:TREM-1抗原结合蛋白的共有序列
实例4-IL-10突变蛋白抗原结合蛋白的产生
评估了二价和单价抗TREM-1mAb/IL-10突变蛋白治疗性融合物的产生和选择、融合物的PK/PD、以及鼠二价和单价抗TREM-1mAb/IL-10突变蛋白情况下对结肠炎模型的影响。
将IL-10野生型、IL-10M1或IL-10突变蛋白与抗TREM-1抗体Fc结构域的C末端融合。对于几乎所有融合,最终的K残基从抗体的Fc区中去除(称为“desK”)。在一个实例中,抗TREM-1抗体与IL-10变体之间的接头是GGGGS(G4S)(SEQ ID NO:2725),并且内部IL-10接头是GGGSGG(SEQ ID NO:2676)(G3SG2)。
制备IL-10突变蛋白与抗TREM-1Ab片段的对称融合物:去除最终的Lys残基(K447-)并在抗体和细胞因子之间附加具有序列G4S(SEQ ID NO:2725)的5个氨基酸后,将IL-10M1或IL-10M1的工程化变体与抗TREM-1IgG1z SEFL2抗体的重链C末端融合,从而构建抗体-细胞因子融合物。抗体-细胞因子重组表达构建体是使用金门克隆生产的,以组装1)包含抗体可变结构域的合成DNA片段,2)包含接头加设计的细胞因子的合成DNA片段,3)先前克隆的含有必要的恒定结构域(即,CK或CL、和CH1-CH2-CH3(118-446)(R292C、N297G、V302C))的“部分载体”,和4)哺乳动物表达载体骨架。将融合的重链(HC)组装到带有嘌呤霉素选择盒的载体骨架中,将轻链(LC)组装到带有潮霉素选择盒的载体骨架中。使用LTX(吉布科公司)在CHO-K1细胞中将融合的HC和LC表达载体以1:1的比率共转染,在10μg/mL嘌呤霉素和500ug/mL潮霉素存在下通过每2–3天传代一次直到细胞活力>90%(Vi-CELL BLU,贝克曼库尔特公司)来产生稳定的池。将稳定的池以2e6个活细胞/mL培养物接种在生产培养基中,并在36℃下在5%CO2中孵育6天。通过离心收集细胞上清液,并使用自动化的3柱串联色谱法纯化抗体。
制备IL-10突变蛋白与抗TREM-1Ab片段的不对称融合物:不对称Fab-异源Fc-细胞因子融合物(又称“单价”抗体-细胞因子融合物)是通过将IL-10M1或IL-10M1的工程化变体与抗体重链的C末端和huFc(221-446)结构域的C末端融合而制成,两者都被进一步工程化为通过由安装在每条链的CH3结构域中的带相反电荷的突变(“电荷对突变”)驱动的静电转向来优先异二聚化。因此,Fab-异源Fc-细胞因子融合物是三链蛋白,这些蛋白包含1)抗体LC,2)IgG1zSEFL2同种型的抗体HC,该抗体HC已通过电荷对突变E356K和D399K进一步工程化,并且在去除最终Lys残基(K447-)并在抗体和细胞因子之间附加具有序列Gly-Gly-Gly-Gly-Ser(SEQ ID NO:2725)的5个氨基酸接头后,IL-10M1或IL-10M1的变体与C末端融合,以及3)IgG1z SEFL2同种型的huFc(221-446)结构域,其进一步用电荷对突变K392D、K409D、和K434D(在下面的序列中下划线)工程化,并且去除最终的Lys残基(K447-)并在Fc和细胞因子(例如IL-10突变蛋白,双下划线)之间添加具有序列Gly-Gly-Gly-Ser(SEQ ID NO:2725)(无下划线,黑体字)的5个氨基酸接头后,IL-10M1或IL-10M1的变体与C末端融合:
通过离心收集细胞上清液,并使用自动化的3柱串联色谱法纯化抗体融合物。抗体融合物被亲和捕获并立即通过凝胶过滤使用G25树脂(思拓凡公司)进行缓冲液交换,并使用200增加树脂(思拓凡公司)通过尺寸排阻进一步精制。通过完整质谱法确认每个变体的身份。对于每个变体,使用蛋白A传感器通过ForteBio(颇尔生命科学公司(Pall Life Sciences))测量条件培养基中的表达效价。通过分析性SEC测量尺寸排阻色谱法(SEC)后存在的高分子量(%HMW)物质的百分比,并且通过使用GXII(珀金埃尔默公司)的非还原性微毛细管电泳测量靶蛋白纯度百分比。通过在40℃下对样品施加应力1周和2周,评估了聚集倾向和单体稳定性。然后通过分析性SEC来分析应力样品和T0样品,以量化T0相比于受应力后的聚集(%HMW)和单体损失的增加。选定的分子的结果显示在表13A和13B中。通过抑制LPS刺激的PBMC中TNFα的产生来测量双特异性功能活性。
表13A:TREM-1-IL-10融合蛋白的特征
表13B:具有所示Fc序列的选定的融合蛋白的特征
如表14所示,用MicroCal(马尔文公司(Malvern))对具有代表性的分子子集进行差示扫描量热法(DSC)测量第一、第二和第三熔化转变(分别是Tm1、Tm2、Tm3)。
表14:IL-10突变蛋白-抗TREM-1抗体融合蛋白的熔化转变
| 抗TREM-1mAb | IL-10突变 | Tm1 | Tm2 | Tm3 |
| 61B12 | L46K | 77.8 | 80.8 | 87.6 |
| 61B12 | Q38R | 78.2 | 80.6 | 87.1 |
| 61B12 | Q38E | 77.9 | 80.7 | 87.9 |
概念验证(PoC)抗体-细胞因子分子产生为具有二价或单价细胞因子的融合物。将C末端IL-10M1或突变蛋白Q38E与代表性抗TREM1抗体1B12融合。对于这些PoC分子的所有版本,移除抗体的C末端处的末端Lys,并添加Gly-Gly-Gly-Gly-Ser(SEQ ID NO:2725)的序列来连接细胞因子和抗体(如前面所述)。此外,对于具有单价细胞因子的PoC分子版本,抗体的Fc部分被工程化为与前面提到的电荷对突变相同。单价细胞因子与抗体重链的正电荷(E356K和D399K)或负电荷(K392D、K409D和K434D)臂融合。
Fab抗体-细胞因子和PoC抗体-细胞因子重组表达构建体是使用金门克隆生产的,以组装1)包含抗体可变结构域的合成DNA片段,2)包含接头加设计的细胞因子的合成DNA片段,3)先前克隆的含有必要的恒定结构域(即,CK或CL、CH1-CH2-CH3(118-446)(R292C、N297G、V302C、E356K、D399K)、CH2-CH3(221-446)(R292C、N297G、V302C、K392D、K409D、K434D))的“部分载体”,和4)哺乳动物表达载体骨架。将融合的HC和融合的Fc结构域组装到带有嘌呤霉素选择盒的载体骨架中,将LC组装到带有潮霉素选择盒的载体骨架中。使用LTX(吉布科公司)在CHO-K1细胞中将融合的HC、融合的Fc和LC表达载体以1:1:1的比率共转染,在10ug/mL嘌呤霉素和500ug/mL潮霉素存在下通过每2–3天传代一次直到细胞活力>90%(Vi-CELL贝克曼库尔特公司)来产生稳定的池。将稳定的池以2e6个活细胞/mL培养物接种在生产培养基中,并在36℃下在5%CO2中孵育6天。
通过离心收集细胞上清液,并使用自动化的3柱串联色谱法纯化抗体融合物。使用CAPTURESELECTTMCH1 XL(赛默飞世尔公司(ThermoFisher))对Fab-异源Fc-细胞因子融合物进行亲和捕获,并立即通过凝胶过滤使用G25树脂(思拓凡公司)进行缓冲液交换,并使用200增加树脂(思拓凡公司)通过尺寸排阻进一步精制。通过完整质谱法确认每个变体的身份。对于每个变体,使用蛋白A传感器通过ForteBio(颇尔生命科学公司(Pall Life Sciences))测量条件培养基中的表达效价。通过分析性尺寸排阻色谱法(SEC)测量蛋白A亲和色谱法后存在的高分子量(%HMW)材料的百分比,并且通过使用GXII(珀金埃尔默公司)的非还原性微毛细管电泳测量靶蛋白纯度百分比。通过在40℃下对样品施加应力1周和2周,评估了聚集倾向和单体稳定性。然后通过分析性SEC来分析应力样品和T0样品,以量化受应力后相比于T0的聚集(%HMW)和单体损失的增加。通过抑制LPS刺激的PBMC中TNFα的产生来测量双特异性功能活性,并且选定的分子的结果显示在表15中。
表15:选定的双特异性细胞因子融合物的功能测定数据
N/A-不是正确的剂量曲线,1=>0.001至<0.01;2=>0.01至<0.1;3=>0.1至<1;4=>1至<10,5=>10
针对单核细胞激活来测试如上所述制备并与IL-10突变蛋白Q38E融合的单价和二价抗体。简而言之,使用Miltenyi单核细胞分离试剂盒II从冷冻的PBMC中分离出单核细胞。将纯化的单核细胞以105个细胞/孔接种在96圆孔TC处理板中的完全培养基中。将指定的测试蛋白质从11000pM以1:5连续稀释至0.005pM。将LPS以终浓度为10ng/mL添加到细胞中。将板在5.0%CO2,37℃下孵育过夜。使用MSD Vplex人TNFα检测试剂盒测量细胞上清液中的TNFα。图2示出了,二价抗TREM-1比单价抗TREM-1更有效,并且二价IL-10突变蛋白在C末端比单价IL-10突变蛋白更有效。
使用全血测定评估了IL-10、IL-10突变蛋白和IL-10/抗TREM-1抗原结合蛋白对免疫细胞活性的影响。将从健康的-未用药供体获得的新鲜肝素化人全血等分到96孔2.0mL深孔板中。在添加IL10试剂之前,将含有血液的板平衡至37℃,持续至少30分钟。将指定的测试试剂连续稀释并添加到全血中。将板在37℃下孵育30min。然后将板放在冰上,添加针对CD3(克隆UCHT-1)和CD4(克隆RPA-T4)的染色抗体,孵育10分钟。然后用1.4mL的BD固定/酶解缓冲液处理细胞,并在37℃下孵育20分钟。将细胞用2%FCS/PBS洗涤,直到裂解的RBC被清除。为了透化细胞,将200μL冰冷的BD Perm缓冲液III添加到每个孔中并充分混合。洗涤5次后,将CD20(克隆H1)、CD14(克隆RM052)和pSTAT3 pY705(克隆4/P-STAT3)添加到细胞中。在环境温度下以200-300RPM在板式震荡器上孵育一小时后(覆盖有铝箔以避光),通过用2%FCS/PBS洗涤2次迅速去除未结合的抗体。将细胞重悬于200μL 2%FCS/PBS洗涤缓冲液中,并使用BD LSRII流式细胞仪进行FACS分析。虽然IL-10单独诱导CD8++T细胞和B细胞增殖,但IL-10突变蛋白或抗TREM-1/IL-10突变蛋白诱导的CD8+T细胞和B细胞激活没有增加,抗TREM-1mAb/IL-10突变蛋白则证明了细胞类型特异性靶向作用的概念验证(图3)。
评估人单核细胞对LPS诱导的TNFα产生的抑制。使用Miltenyi单核细胞分离试剂盒II从冷冻的PBMC中分离出单核细胞。将纯化的单核细胞以105个细胞/孔接种在96圆孔TC处理板中的完全培养基中。将指定的具有多种IL-10突变蛋白的测试蛋白质从11000pM以1:5连续稀释至0.005pM。将LPS以终浓度为10ng/mL添加到细胞中。将板在5.0%CO2,37℃下孵育过夜。使用MSD Vplex人TNFα检测试剂盒测量细胞上清液中的TNFα。图4A-4H表明,与单独使用IL-10突变蛋白的培养物相比,具有不同IL-10突变蛋白的抗原结合蛋白在减少单核细胞中的TNFα方面更有效,表明TREM-1结合显著提高了IL-10突变蛋白对单核细胞激活的抑制。
为了评估对人单核细胞中LPS诱导的人TNFα产生方面的抑制,使用Miltenyi单核细胞分离试剂盒II从冷冻的PBMC中分离单核细胞。将纯化的单核细胞以105个细胞/孔接种在96圆孔TC处理板中的完全培养基中。将指定的测试蛋白质从11000pM以1:5连续稀释至0.005pM。将LPS以终浓度为10ng/mL添加到细胞中。将板在5.0%CO2,37℃下孵育过夜。使用MSD Vplex人TNFα检测试剂盒测量细胞上清液中的TNFα。为了评估对LPS诱导的小鼠TNFα产生方面的抑制,从C57Bl/6小鼠的股骨中分离出小鼠骨髓。将细胞以105个/孔接种在96圆孔TC处理板中的完全培养基中。将指定的测试试剂从11000pM以1:5连续稀释至0.005pM。将LPS以终浓度为10ng/mL添加到细胞中。将板在5.0%CO2,37℃下孵育过夜。使用MSD Vplex小鼠TNFα检测试剂盒测量细胞上清液中的小鼠TNFα。
图5显示,通过TREM-1结合,IL-10突变蛋白对人单核细胞中TNFα的抑制效力有明显改善(图5A)。对单核细胞的TNF抑制的改善取决于TREM-1结合,因为由于缺乏与小鼠TREM-1的交叉反应,对小鼠单核细胞的效力很小(图5B)。
这些结果表明,与野生型IL-10相比,包含IL-10突变蛋白和免疫细胞靶向部分(例如,抗TREM-1抗体)的抗原结合蛋白能够差异调节免疫细胞。抗原结合蛋白显著抑制骨髓细胞产生TNF-α。抗原结合蛋白不刺激CD8+T细胞和B细胞。IL-10突变蛋白抗原结合蛋白能够在不刺激免疫细胞的情况下抑制炎症,因此可以为治疗炎性肠病提供治疗益处。
实例5—IL-10M1的稳定性工程化
对于使用无偏方法的IL-10M1(SEQ ID NO:2211)的酵母展示稳定性工程化,使用II试剂盒在低诱变条件下产生了IL-10M1的基于易错PCR的文库,并在酵母上展示(IL10M1-EP文库)。该文库展示在BJ5464的酵母衍生物的表面,其中IL-10M1与α-凝集素的N末端融合。通过647缀合的抗HA抗体的结合测量展示的效率。使用抗生蛋白链菌素PE作为二级荧光,针对与生物素缀合的重组IL-10R-Fc的高度结合,利用荧光激活细胞分选法(FACS)对文库进行分选。
为了鉴定在应力条件下比野生型IL-10M1表现更好的突变体,对这个易错酵母文库施加了各种应力。作为蛋白质表达的应力,酵母细胞的IL-10M1-EP文库被诱导在20℃或30℃下展示IL-10M1突变变体。为了鉴定对这种应力表现出更高抗性的突变体,通过FACS对与IL-10R-Fc结合良好并在酵母表面良好展示(通过HA表位标签评估)的变体进行分选。将来自这些富集结合剂池以及初始IL-10M1 EP文库池的IL-10M1序列通过IL-10M1编码序列之外的引物进行扩增。然后使用Nextera文库制备试剂盒处理扩增子,并将其提交给Illumina MiSeq进行2x300bp运行的NGS分析。选择在30C诱导应力后在结合剂池中高度富集或耗尽的突变体序列进行重组,并对其稳定性进行评估,以评估该方法的预测能力(表15)。
为了鉴定可能更好地折叠和更少地暴露于蛋白分解的变体,进行了有限的蛋白分解实验。首先,将IL-10M1易错文库在20℃下诱导,并且将FACS分选以消除非IL10R结合剂。这产生了IL-10M1 EP结合剂文库。然后,将IL-10M1 EP结合剂文库在20℃下诱导,并加入有限量的胰蛋白酶、糜蛋白酶和嗜热菌蛋白酶。为了鉴定对这些蛋白酶表现出更高抗性的突变体,通过FACS对与IL-10R-Fc结合并在酵母表面展示的比母体IL-10M1分子更好的变体进行了分选,并按上述方法进行NGS分析。选择在抗蛋白酶池中高度富集或耗尽的突变体序列(例如,蛋白质应力富集、温度应力富集、温度和蛋白酶应力富集、蛋白酶应力耗尽、或温度应力耗尽)进行重组,并对稳定性进行评估,以评估该方法的预测能力(表16)。
表16:酵母展示选定的稳定性突变和原理
选择原理:a,蛋白质应力富集;b,温度应力富集;c,温度和蛋白酶应力富集;d,蛋白酶应力耗尽;e,温度应力耗尽
罗塞塔(Rosetta)稳定性工程化:通过计算设计,对稳定工程进行了探讨。使用RosettaScripts和Talaris2014评分函数对IL10M1突变蛋白进行结构建模。使用“fastrelax”协议,五个循环的骨架最小化和旋转体优化使衍生自PDB 1Y6K晶体结构的单体IL-10M1模型达到局部能量最小。弛豫后,对残基21-161进行单独筛选,并通过计算将其突变为20个标准氨基酸中的每个。随后,对肽骨架和周围的残基进行了50次基于蒙特卡洛(Monte Carlo)的模拟退火步骤。所有选定的设计也在L46K衰减突变的背景下进行了重建模和评分,以确认预测的行为不受影响。表17示出了IL10突变蛋白与抗体61B12的重链融合的SEQ ID NO;每种抗体中的轻链与抗体61B12中的轻链相同(SEQ ID NO:105,但缺乏信号序列)。
表17:罗塞塔稳定性克隆
为了选择具有更好的稳定性和表面特性的设计,使用Talaris2014评分和疏水溶剂可及表面积(hSASA)对最终模型进行了彼此相对排名。最终选择了15个具有低能量和降低的hSASA的评分良好的设计进行实验评估(表18)。
表18:前15个点突变的罗塞塔能量得分
| 突变 | 总分 | hsasa_列表 |
| Y59T | -0.93 | -52.55 |
| M77R | -3.10 | -51.16 |
| M77V | -2.39 | -53.92 |
| D84R | -1.03 | -44.39 |
| H90E | -1.47 | -38.28 |
| H90Q | -0.69 | -30.08 |
| K49T | -0.83 | -25.75 |
| K49S | -0.63 | -31.50 |
| A127M | -0.65 | -25.60 |
| F15Y | -0.42 | -23.10 |
| S93E | -1.84 | -19.97 |
| S93Q | -1.25 | -15.71 |
| L103E | -0.87 | -17.12 |
| T100R | -1.19 | -11.25 |
| Q79R | -1.42 | -10.33 |
可替代的合理的设计策略是探索引入二硫化物以稳定IL10M1的强制单体结构。对于这种方法,模板模型中的残基21-123被筛选为接近残基124-165。残基对被计算地突变为半胱氨酸,如果Cβ原子相互之间在以内,则强制形成二硫化物。使用Talaris2014评分和未加权的二硫化物潜力项对这些设计进行彼此相对排名。因此选择了5个具有低能量的交联设计进行实验评估(表19)。
表19.前5个二硫化物突变的罗塞塔能量得分
| 突变 | 总分 | dslf_fa13 |
| Q97C-I136C | 5.62 | -0.43 |
| K57C-M156C | 5.64 | 1.53 |
| K40C-Y137C | 5.69 | -0.56 |
| Q38C-S141C | 6.27 | -0.38 |
| E67C-V121C | 6.37 | -0.43 |
作为双特异性融合物的产生和测试:为增加稳定性而设计的突变蛋白变体被克隆为抗TREM1抗体61B2.001的二价C末端融合物,在CHO细胞中重组表达,并如实例3中所述进行纯化。通过完整质谱法确认每个变体的身份,并使用Slide-A-LyzerTMG2透析盒(20KMWCO,3mL(赛默飞世尔公司,目录号87735))将每个变体浓缩至10±1mg/mL。使用蛋白A传感器通过ForteBio(颇尔生命科学公司)测量条件培养基中的表达效价。通过分析性尺寸排阻色谱法(SEC)测量存在的高分子量(%HMW)物质的百分比,并且通过使用GXII(珀金埃尔默公司)的非还原性微毛细管电泳测量靶蛋白纯度百分比。通过在40℃下对样品施加应力2周,评估了聚集倾向和单体稳定性。然后通过分析性SEC来分析应力样品和T0样品,以量化受应力后相比于T0的聚集(%HMW)和单体损失的增加。通过抑制LPS刺激的PBMC中TNFα的产生来测量对分子的子集的双特异性功能活性;选定的分子的结果显示在表20中。
表20:工程化的IL-10M1突变蛋白与抗TREM1抗体61B2的融合物的产生和稳定性数据
这些结果表明,在纯化过程中和在40摄氏度下以中等高浓度(10mg/mL)应力下2周后,稳定性突变的一个子集成功地减少了抗TREM1抗体-IL10M1融合物/抗原结合蛋白变体的聚集程度。
最好的稳定性突变与旨在补救IL10M1的位置N10、N116、和/或第一和第二结构域之间GGSGG接头(以下称为接头体[G1])的第一位置的脱酰胺热点的突变相组合。新的IL10M1变体在三个不同位置与抗TREM1抗体63F8.001和64D7.001重链进行二价融合:N末端、C末端、或掩埋在Fab和Fc之间。
表21.IL-10突变蛋白中的脱酰胺热点
| IL-10突变蛋白 | SEQ ID NO: |
| huIL10[L46K,L103E,接头[G1A]] | 2777 |
| huIL10[L46K,L103E,接头[G1V]] | 2778 |
| huIL10[L46K,R110P,接头[G1A]] | 2779 |
| huIL10[L46K,R110P] | 2780 |
| huIL10[N10I,L46K,L103E,接头[G1A]] | 2781 |
| huIL10[N10I,L46K,L103E,接头[G1V]] | 2782 |
| huIL10[N10I,L46K,L103E,R110P,接头[G1A]] | 2783 |
| huIL10[N10I,L46K,L103E] | 2784 |
| huIL10[N10I,L46K,R110P,接头[G1A]] | 2785 |
| huIL10[N10K,L46K,L103E,接头[G1A]] | 2786 |
| huIL10[N10Q,L46K,L103E,接头[G1A]] | 2787 |
| huIL10[N10Q,L46K,L103E,接头[G1V]] | 2788 |
| huIL10[N10Q,L46K,L103E,N116Q] | 2789 |
| huIL10[N10Q,L46K,L103E] | 2790 |
| huIL10[N10Q,L46K,R110P,接头[G1A]] | 2791 |
C末端IgG-细胞因子融合物在CHO细胞中表达,纯化,浓缩至10mg/mL,并如实例4中所述进行测定。
通过将IL-10M1或IL-10M1的工程化的变体与序列为GGGSGGGS(SEQ ID NO:2676)的10个氨基酸接头融合到抗TREM-1IgG1z SEFL2重链的N-末端,构建N末端细胞因子-IgG融合物。抗体-细胞因子重组表达构建体是使用金门克隆生产的,以组装1)包含抗体可变结构域的合成DNA片段,2)包含设计的细胞因子加接头的合成DNA片段,3)先前克隆的含有必要的恒定结构域的“部分载体”,和4)哺乳动物表达载体骨架。将融合的重链(HC)组装到带有嘌呤霉素选择盒的载体骨架中,将轻链(LC)组装到带有潮霉素选择盒的载体骨架中。构建体在CHO细胞中表达,纯化,浓缩至10mg/mL,并如实例4中所述进行测定。
通过将IL-10M1或IL10M1的工程化的变体(具有序列GGGG(SEQ ID NO:2677)的前导接头和后尾接头)融合到抗TREM-1IgG1zSEFL2抗体的氨基酸C282和D283之间的铰链区(即EPSKC-GGGG-IL10M1-GGGG-DKTHC(SEQ ID NO:2724)),构建掩埋的Fab-细胞因子-Fc分子。Fab-细胞因子重组表达构建体是使用金门克隆生产的,以组装1)包含抗体可变结构域的合成DNA片段,2)包含设计的细胞因子加接头的合成DNA片段,3)先前克隆的含有必要的恒定结构域的“部分载体”,和4)哺乳动物表达载体骨架。将融合的重链(HC)组装到带有嘌呤霉素选择盒的载体骨架中,将轻链(LC)组装到带有潮霉素选择盒的载体骨架中。构建体在CHO细胞中表达,纯化,浓缩至10mg/mL,并如实例4中所述进行测定。
表22:IL-10突变蛋白-TREM-1抗体中的脱酰胺热点
表22中的重链分别与其轻链配偶体配对,例如,对于克隆63F8.001的SEQ ID NO:976或SEQ ID NO:2554(但缺乏信号序列MDMRVPAQLLGLLLLWLRGARC(SEQ ID NO:2674)),以及对于64D7.001的SEQ ID NO:992或SEQ ID NO:2555(但缺乏信号序列MDMRVPAQLLGLLLLWLRGARC(SEQ ID NO:2674))。鉴定了几种IL-10M1突变的组合,这些突变固定了脱酰胺位点,并以中等高浓度(10mg/mL)在40℃应力下10天后保持低聚集性。
表23:与抗TREM1抗体63F8和64D7连接的工程化的IL-10M1突变蛋白的抗原结合蛋白的产生和稳定性数据
通过BIACORETM分析(BIACORETMT200,传感器芯片:SCM5)测量选定的融合蛋白对人TREM1和食蟹猴TREM1的亲和力。BIACORETM条件包括:样品:0.244nM–500nM范围用于IL10/TREM1滴定;缔合:以50μl/min进行3分钟;解离:在50μl/min的条件下,IL10为15分钟,TREM1为30分钟;再生:10mM甘氨酸,pH 1.5,以30μl/min持续30s(2x)。
针对来自稳定转染Sf 21的细胞的huIL10Rα蛋白#274和在人HEK293细胞中表达的huIL10Rα蛋白#9100,测量亲和力。将结果显示在表24中。
表24:针对人TREM-1、食蟹猴TREM-1或IL-10R进行的所选融合蛋白的BIACORETM亲和力分析的结果
HuTREM1和食蟹猴TREM1与所选融合分子显示出紧密而稳定的结合。在测试的2个huIL10R中,huIL10R 274与9100版本相比显示出更强的结合力(10倍的差异)。IL10 R 274被选择用于未来的测试。
实例6-TREM-1抗体阻断人外周血单核细胞(PBMC)中配体介导的信号传导的功效
通过抑制配体与人类PBMC中的TREM-1受体结合,测试TREM-1抗体阻断信号传导的能力。将冷冻的人PBMC(IQ生物科学公司(IQ Biosciences))解冻,洗涤并重悬于完全细胞培养基(RPMI/10%FBS/2mM GlutaMax/1mM丙酮酸钠/44uMβ-巯基乙醇/1X DNA酶I)中。将PBMC以100K/孔接种于96孔细胞培养板中,并在37℃下使其平衡至少30分钟。将十三种抗TREM-1抗体在RPMI/10%FBS中稀释(3X连续稀释),产生的最终抗体浓度从0.000017nM到3nM。抗体57F5被排除在该分析之外,因为在该测定的先前迭代中,利用更高浓度的抗体,它未能显示出任何信号传导的抑制。在添加TREM-1配体之前,将抗体与PBMC预孵育30分钟。与肽聚糖(PGN)复合的肽聚糖识别蛋白1(PGLYRP1)是所描述的几个TREM-1配体之一,其与TREM-1受体的接合引发了炎性细胞因子(例如TNFα)的产生,并被用于这些测定中。为了将蛋白质进行复合,将人PGLYRP1(R&D系统公司)与衍生自大肠杆菌(英杰公司)的可溶性PGN以1.25:2的比率组合,并在37℃下孵育45分钟。将复合的PGLYRP1/PGN添加到PBMC/抗体中,并在37℃下孵育过夜。第二天,收集细胞培养基并通过人TNFαAlphalisa亲近测定(珀金埃尔默公司)检测TNFα。在Envision 2103多标签读板仪上测量615nm处的光发射。IC50值是使用GraphPad Prism(v8.4.3)计算,并在下表25中针对两个独立的测定列出。
表25.通过TNFα释放测量,TREM-1抗体对人PBMC中配体介导的信号传导的抑制
这些结果表明,TREM-1抗体结合人TREM-1,并重要的是证明抑制人原代细胞(PBMC)中配体诱导的TREM-1激活。
实例7-TREM-1抗体阻断食蟹猴外周血单核细胞(PBMC)中配体介导的信号传导的功效
通过抑制配体与食蟹猴PBMC中的TREM-1受体结合,测定TREM-1抗体阻断信号传导。将冷冻的食蟹猴PBMC(IQ生物科学公司(IQ Biosciences))解冻,洗涤并重悬于完全细胞培养基(RPMI/10%FBS/2mM GlutaMax/1mM丙酮酸钠/44uMβ-巯基乙醇/1X DNA酶I)中。将PBMC以100K/孔接种于96孔细胞培养板中,并在37℃下使其平衡至少30分钟。将十四种抗TREM-1抗体在RPMI/10%FBS中稀释(3X连续稀释),产生的最终抗体浓度从0.00017nM到30nM。在添加TREM-1配体之前,将抗体与PBMC预孵育30分钟。与肽聚糖(PGN)复合的肽聚糖识别蛋白1(PGLYRP1)是所描述的几个TREM-1配体之一,其与TREM-1受体的接合引发了炎性细胞因子(例如TNFα)的产生,并被用于该测定中。为了将蛋白质进行复合,将食蟹猴PGLYRP1(Creative BioMart公司)与衍生自大肠杆菌(英杰公司)的可溶性PGN以1.25:2的比率组合,并在37℃下孵育45分钟。将复合的PGLYRP1/PGN添加到PBMC/抗体中,并在37℃下孵育过夜。第二天,收集细胞培养基并通过食蟹猴TNFαAlphalisa亲近测定(珀金埃尔默公司)检测TNFα。在Envision 2103多标签读板仪上测量615nm处的光发射。IC50值是使用GraphPad Prism(v8.4.3)计算,并在表26中针对两个独立的测定列出。
表26.通过TNFα释放测量,TREM-1抗体对食蟹猴PBMC中配体介导的信号传导的抑制
这些结果表明,TREM-1抗体结合食蟹猴TREM-1,并且重要的是抑制食蟹猴原代细胞(PBMC)中配体诱导的TREM-1激活。此外,图6显示了TREM1抗体在食蟹猴和人PBMC中对PGLYRP1/PGN介导的TREM1信号传导的抑制。
实例8-TREM-1Fab阻断人TREM-1/Dap12-HEK293过表达细胞系中脾酪氨酸激酶(SYK)磷酸化的功效。
在过表达人TREM-1/Dap12的细胞系中,通过抑制配体与TREM-1受体的结合来测定TREM-1Fab阻断信号传导的能力,并确定IC50。脾酪氨酸激酶(SYK)的磷酸化是TREM-1信号传导级联的早期步骤,在本测定中被用于TREM-1信号传导的测量。将过表达人TREM-1及其专性衔接蛋白DNAX激活蛋白(Dap12)(12kDa)的HEK293细胞以50K/孔接种在CellBIND板(康宁公司)中的完全培养基(DMEM/10%FBS)中,并使其附着过夜。二价TREM-1抗体无法抑制该系统中的信号传导,可能是由于这些细胞中TREM-1受体的丰度很高并且二价抗体能够交联它们导致配体不依赖的受体激动的技术假象所致。因此,在该测定中,单价Fab被用作全抗体的替代物。将十四种抗TREM-1Fab在完全培养基中稀释(3X连续稀释),产生的最终抗体浓度从0.00017nM到30nM。在添加与TREM-1配体复合的人PGLYRP1(R&D系统公司)和来自大肠杆菌的可溶性PGN(英杰公司)之前,将Fab与TREM-1/Dap12-HEK293预孵育30分钟。为了使PGLYRP1和PGN复合,蛋白质以1:2比率组合并在37℃下孵育45分钟,然后添加到细胞/Fab。室温孵育一小时后,将细胞裂解,并且用pSYKUltraTMp-SYK(Tyr525/526)测定法(珀金埃尔默公司)测量细胞裂解物中磷酸化SYK的量。在Envision2103多标签读板仪上测量615nm处的光发射。IC50值是使用GraphPad Prism(v8.4.3)计算,并如表27所示针对两个独立的测定列出。
表27.通过SYK磷酸化测量,抗体对过表达人TREM-1/DAP12的细胞系中配体介导的信号转导的抑制
图7是显示抗TREM1 Fab抑制TREM1/DAP12-HEK293细胞中PGLYRP1/PGN介导的SYK磷酸化的图。
本文的任何单个实施例可以补充有来自本文的任何一个或多个其他实施例的一个或多个要素。
因此,应当理解的是,本发明不限于所披露的特定实施例,但是旨在涵盖如下中限定的处于本发明精神和范围之内的所有修改:所附权利要求书;以上说明书;以下编号的段落,和/或附图中所示。
实施例的实例:
段落1.一种人白介素-10(IL-10)突变蛋白,其包含与SEQ ID NO:2中列出的氨基酸序列具有至少90%同一性的氨基酸序列,其中所述IL-10突变蛋白具有选自以下的至少一个突变:螺旋环AB、螺旋环CD、螺旋环DE、螺旋A、螺旋B、螺旋C、螺旋D、螺旋E和/或螺旋F中的突变。
段落2.如段落1所述的IL-10突变蛋白,该IL-10突变蛋白包含螺旋A中的至少一个突变。
段落3.如段落1所述的IL-10突变蛋白,该IL-10突变蛋白包含螺旋F中的至少一个突变。
段落4.如段落1所述的IL-10突变蛋白,该IL-10突变蛋白包含螺旋环AB中的至少一个突变。
段落5.如段落1至4中任一项所述的IL-10突变蛋白,该IL-10突变蛋白包含SEQ IDNO:2的残基N10、H14、F15、P20、M22、L23、R24、R27、D28、K34、T35、Q38、M39、K40、D41、Q42、L43、D44、N45、L46、L47、L48、K49、F56、K57、Y59、L60、Q63、E67、Q70、M77、Q79、N82、Q83、D84、P85、D86、I87、A89、H90、S93、T100、L103、H109、R110、L112、E115、N116、A127、K130、I136、Y137、K138、S141、E142、D144、I145、E151、M154、M156、K157、或N160中的一个或多个中的突变,或在螺旋D和螺旋E之间添加4到8个氨基酸。
段落6.如段落1至5中任一项所述的IL-10突变蛋白,其中所述突变蛋白与SEQ IDNO:2中列出的氨基酸序列具有至少95%同一性。
段落7.如段落1至6中任一项所述的IL-10突变蛋白,其中该突变是以下中的一个或多个:SEQ ID NO:2的N10Q、N10I、N10K、R27L、K34D、D41G、L46K、Q38E、Q38R、Q38D、K138L、K138D、I87A、H14Q、F15Y、M22V、K49T、K49S、F56Y、K57N、Y59T、L60Q、Q63E、Q63L、E67C、Q70E、Q70K、M77R、M77V、Q79R、Q79C、D84R、A89P、H90E、H90Q、S93E、S93Q、T100R、L103E、H109D、R110P、R110Q、L112V、E115K、N116D、N116Q、A127M、K130Q、I136C、Y137C、M154V、M156C、K157N、或N160D,任选地包含在螺旋D和螺旋E之间添加6个氨基酸。
段落8.如段落1至7中任一项所述的IL-10突变蛋白,其中该IL-10突变蛋白减少了单核细胞中TNF-α产生方面的抑制,降低了人类受试者中CD8+T细胞刺激方面的水平,和/或降低了B细胞刺激方面的水平。
段落9.如段落5至7中任一项所述的IL-10突变蛋白,其中螺旋D和螺旋E之间的氨基酸是GGGSGG(SEQ ID NO:2676)。
段落10.如段落1至9中任一项所述的IL-10突变蛋白,其中该IL-10突变蛋白具有以下中任一个中列出的氨基酸序列:SEQ ID NO:3-10或SEQ ID NO:2138、2140、2142、2144、2146、2148、2150、2152、2154、2156、2158、2160、2162、2164、2166、2168、2170、2172、2174、2176、2178、2180、2182、2360、2362、2364、2366、2368、2370、2372、2374、2376、2378、2380、2382、2384、2386、2388、2390、2392、2394、2396、2398、2400、2402、2404、2406、2408、2410、2412、2414、2416、2418、2420、2422、2424、2426、2428、2430、2432、2434、2436、2438、2440、2442、2444、2446、2448、2450、2452、2454、2456、2458、2460、2462、2464、2466、2468、2470、2472、2474、2476、2478、2480、2482、2484、2486、2488、2490、2492、2494、2496、2500、2502、2504、2506、2508、2510、2512、2514、2516、2518、2520、2522、2524、2526、2528、2530、2532、2534、2536、2538、2540、和2777-2791。
段落11.一种人白介素-10(IL-10)突变蛋白,其包含与SEQ ID NO:2中列出的氨基酸序列具有至少90%同一性的氨基酸序列,其中所述IL-10突变蛋白具有SEQ ID NO:2的残基N10、H14、F15、P20、M22、L23、R24、R27、D28、K34、T35、Q38、M39、K40、D41、Q42、L43、D44、N45、L46、L47、L48、K49、F56、K57、Y59、L60、Q63、E67、Q70、M77、Q79、N82、Q83、D84、P85、D86、I87、A89、H90、S93、T100、L103、H109、R110、L112、E115、N116、A127、K130、I136、Y137、K138、S141、E142、D144、I145、E151、M154、M156、K157、或N160中的一个或多个中的至少一个突变。
段落12.如段落1至11中任一项所述的IL-10突变蛋白,该IL-10突变蛋白进一步包含半衰期延长部分。
段落13.如段落12所述的IL-10突变蛋白,其中该半衰期延长部分是Fc结构域。
段落14.如段落13所述的IL-10突变蛋白,其中该半衰期延长部分是聚乙二醇(PEG)。
段落15.如段落1-14中任一项所述的IL-10突变蛋白,其中该突变蛋白是二聚体。
段落16.一种分离的核酸分子,其包含编码如段落1至15中任一项所述的IL-10突变蛋白的核苷酸序列。
段落17.一种表达载体,其包含可操作地连接到表达控制序列的如段落16所述的核酸分子。
段落18.一种重组宿主细胞,其包含如段落16所述的核酸或如段落17所述的载体。
段落19.如段落18所述的宿主细胞,其中该宿主细胞是哺乳动物细胞。
段落20.如段落18或19所述的宿主细胞,其中该宿主细胞是CHO细胞。
段落21.一种使用如段落18至20中任一项所述的宿主细胞产生IL-10突变蛋白的方法,该方法包括培养该宿主细胞并回收该IL-10突变蛋白。
段落22.一种通过如段落21所述的方法产生的IL-10突变蛋白。
段落23.一种药物组合物,其包含如段落1-15中任一项所述的IL-10突变蛋白和药学上可接受的载剂。
段落24.一种分离的抗原结合蛋白,其中该抗原结合蛋白:
a.是抗体或抗体片段;
b.与具有SEQ ID NO:20中列出的氨基酸序列的人TREM-1结合;
c.包含轻链可变结构域,该轻链可变结构域包含:
i.轻链CDR1,其包含选自SEQ ID NO:30、50、70、90、110、130、150、170、190、210、230、250、270、290和2190的氨基酸序列;
ii.轻链CDR2,其包含选自SEQ ID NO:31、51、71、91、111、131、151、171、191、211、231、251、271、291和2191的氨基酸序列;
iii.轻链CDR3,其包含选自SEQ ID NO:32、52、72、92、112、132、152、172、192、212、232、252、272、292和2192的氨基酸序列;并且
d.包含重链可变结构域,该重链可变结构域包含:
i.重链CDR1,其包含选自SEQ ID NO:36、56、76、96、116、136、156、176、196、216、236、256、276、296和2196的氨基酸序列;
ii.重链CDR2,其包含选自SEQ ID NO:37、57、77、97、117、137、157、177、197、217、237、257、277、297和2197的氨基酸序列;和
iii.重链CDR3,其包含选自SEQ ID NO:38、58、78、98、118、138、158、178、198、218、238、258、278、298和2198的氨基酸序列。
段落25.如段落24所述的抗原结合蛋白,其中:
a.轻链CDR1序列在SEQ ID NO:30、50、70、110、150、170、或290中列出;
b.轻链CDR2序列在SEQ ID NO:31、51、71、111、151、171、或291中列出;
c.轻链CDR3序列在SEQ ID NO:32、52、72、112、152、172、或292中列出;
d.重链CDR1序列在SEQ ID NO:36、56、76、116、156、176、和296中列出;
e.重链CDR2序列在SEQ ID NO:37、57、77、117、157、177、和297中列出;和
f.重链CDR3序列在SEQ ID NO:38、58、78、118、158、和298中列出。
段落26.如段落24或25所述的抗原结合蛋白,其中:
a.轻链CDR1序列在SEQ ID NO:50或110中列出;
b.轻链CDR2序列在SEQ ID NO:51或111中列出;
c.轻链CDR3序列在SEQ ID NO:52或112中列出;
d.重链CDR1序列在SEQ ID NO:56或116中列出;
e.重链CDR2序列在SEQ ID NO:57或117中列出;和
f.重链CDR3序列在SEQ ID NO:58或118中列出。
段落27.如段落24至26所述的抗原结合蛋白,该抗原结合蛋白包含选自以下的一组CDR氨基酸序列:
i)SEQ ID NO:30(LCDR1)、SEQ ID NO:31(LCDR2)、SEQ ID NO:32(LCDR3)、SEQ IDNO:36(HCDR1)、SEQ ID NO:37(HCDR2)和SEQ ID NO:38(HCDR3);
ii)SEQ ID NO:50(LCDR1)、SEQ ID NO:51(LCDR2)、SEQ ID NO:52(LCDR3)、SEQ IDNO:56(HCDR1)、SEQ ID NO:57(HCDR2)和SEQ ID NO:58(HCDR3);
iii)SEQ ID NO:70(LCDR1)、SEQ ID NO:71(LCDR2)、SEQ ID NO:72(LCDR3)、SEQID NO:76(HCDR1)、SEQ ID NO:77(HCDR2)和SEQ ID NO:78(HCDR3);
iv)SEQ ID NO:90(LCDR1)、SEQ ID NO:91(LCDR2)、SEQ ID NO:92(LCDR3)、SEQ IDNO:96(HCDR1)、SEQ ID NO:97(HCDR2)和SEQ ID NO:98(HCDR3);
v)SEQ ID NO:110(LCDR1)、SEQ ID NO:111(LCDR2)、SEQ ID NO:112(LCDR3)、SEQID NO:116(HCDR1)、SEQ ID NO:117(HCDR2)和SEQ ID NO:118(HCDR3);
vi)SEQ ID NO:130(LCDR1)、SEQ ID NO:131(LCDR2)、SEQ ID NO:132(LCDR3)、SEQID NO:136(HCDR1)、SEQ ID NO:137(HCDR2)和SEQ ID NO:138(HCDR3);
vii)SEQ ID NO:150(LCDR1)、SEQ ID NO:151(LCDR2)、SEQ ID NO:152(LCDR3)、SEQ ID NO:156(HCDR1)、SEQ ID NO:157(HCDR2)和SEQ ID NO:158(HCDR3);
viii)SEQ ID NO:170(LCDR1)、SEQ ID NO:171(LCDR2)、SEQ ID NO:172(LCDR3)、SEQ ID NO:176(HCDR1)、SEQ ID NO:177(HCDR2)和SEQ ID NO:178(HCDR3);
ix)SEQ ID NO:190(LCDR1)、SEQ ID NO:191(LCDR2)、SEQ ID NO:192(LCDR3)、SEQID NO:196(HCDR1)、SEQ ID NO:197(HCDR2)和SEQ ID NO:198(HCDR3);
x)SEQ ID NO:210(LCDR1)、SEQ ID NO:211(LCDR2)、SEQ ID NO:212(LCDR3)、SEQID NO:216(HCDR1)、SEQ ID NO:217(HCDR2)和SEQ ID NO:218(HCDR3);
xi)SEQ ID NO:230(LCDR1)、SEQ ID NO:231(LCDR2)、SEQ ID NO:232(LCDR3)、SEQID NO:236(HCDR1)、SEQ ID NO:237(HCDR2)和SEQ ID NO:238(HCDR3);
xii)SEQ ID NO:250(LCDR1)、SEQ ID NO:251(LCDR2)、SEQ ID NO:252(LCDR3)、SEQ ID NO:256(HCDR1)、SEQ ID NO:257(HCDR2)和SEQ ID NO:258(HCDR3);
xiii)SEQ ID NO:270(LCDR1)、SEQ ID NO:271(LCDR2)、SEQ ID NO:272(LCDR3)、SEQ ID NO:276(HCDR1)、SEQ ID NO:277(HCDR2)和SEQ ID NO:278(HCDR3);
xiv)SEQ ID NO:290(LCDR1)、SEQ ID NO:291(LCDR2)、SEQ ID NO:292(LCDR3)、SEQ ID NO:296(HCDR1)、SEQ ID NO:297(HCDR2)和SEQ ID NO:298(HCDR3);或
xv)SEQ ID NO:2190(LCDR1)、SEQ ID NO:2191(LCDR2)、SEQ ID NO:2192(LCDR3)、SEQ ID NO:2196(HCDR1)、SEQ IDNO:2197(HCDR2)和SEQ ID NO:2198(HCDR3)。
段落28.如段落24至27中任一项所述的抗原结合蛋白,该抗原结合蛋白包含选自以下的一组CDR氨基酸序列:
i)SEQ ID NO:30(LCDR1)、SEQ ID NO:31(LCDR2)、SEQ ID NO:32(LCDR3)、SEQ IDNO:36(HCDR1)、SEQ ID NO:37(HCDR2)和SEQ ID NO:38(HCDR3);
ii)SEQ ID NO:50(LCDR1)、SEQ ID NO:51(LCDR2)、SEQ ID NO:52(LCDR3)、SEQ IDNO:56(HCDR1)、SEQ ID NO:57(HCDR2)和SEQ ID NO:58(HCDR3);
iii)SEQ ID NO:70(LCDR1)、SEQ ID NO:71(LCDR2)、SEQ ID NO:72(LCDR3)、SEQID NO:76(HCDR1)、SEQ ID NO:77(HCDR2)和SEQ ID NO:78(HCDR3);
iv)SEQ ID NO:110(LCDR1)、SEQ ID NO:111(LCDR2)、SEQ ID NO:112(LCDR3)、SEQID NO:116(HCDR1)、SEQ ID NO:117(HCDR2)和SEQ ID NO:118(HCDR3);
v)SEQ ID NO:150(LCDR1)、SEQ ID NO:151(LCDR2)、SEQ ID NO:152(LCDR3)、SEQID NO:156(HCDR1)、SEQ ID NO:157(HCDR2)和SEQ ID NO:158(HCDR3);
vi)SEQ ID NO:170(LCDR1)、SEQ ID NO:171(LCDR2)、SEQ ID NO:172(LCDR3)、SEQID NO:176(HCDR1)、SEQ ID NO:177(HCDR2)和SEQ ID NO:178(HCDR3);或
vii)SEQ ID NO:290(LCDR1)、SEQ ID NO:291(LCDR2)、SEQ ID NO:292(LCDR3)、SEQ ID NO:296(HCDR1)、SEQ ID NO:297(HCDR2)和SEQ ID NO:298(HCDR3)。
段落29.如段落24至28中任一项所述的抗原结合蛋白,该抗原结合蛋白包含选自以下的一组CDR氨基酸序列:SEQ ID NO:50(LCDR1)、SEQ ID NO:51(LCDR2)、SEQ ID NO:52(LCDR3)、SEQ ID NO:56(HCDR1)、SEQ ID NO:57(HCDR2)和SEQ ID NO:58(HCDR3);以及SEQID NO:110(LCDR1)、SEQ ID NO:111(LCDR2)、SEQ ID NO:112(LCDR3)、SEQ ID NO:116(HCDR1)、SEQ ID NO:117(HCDR2)和SEQ ID NO:118(HCDR3)。
段落30.如段落24至29中任一项所述的抗原结合蛋白,该抗原结合蛋白包含:
a.轻链可变结构域,其包含选自下组的氨基酸序列,该组由以下组成:
i.与选自SEQ ID NO:41、61、81、101、121、141、161、181、201、221、241、261、281、301和2185的氨基酸序列具有至少80%同一性的序列;
ii.由多核苷酸序列编码的与选自SEQ ID NO:41、61、81、101、121、141、161、181、201、221、241、261、281、301和2185的氨基酸序列具有至少80%同一性的序列;或
iii.由在中等严格条件下与由选自SEQ ID NO:39、59、79、99、119、139、159、179、199、219、239、259、279、299和2183的核酸序列组成的多核苷酸的互补序列杂交的多核苷酸编码的序列;和
b.重链可变结构域,其包含选自下组的氨基酸序列,该组由以下组成:
i.与选自SEQ ID NO:42、62、82、102、122、142、162、182、202、222、242、262、282、302和2186的氨基酸序列具有至少80%同一性的序列;
ii.由多核苷酸序列编码的与选自SEQ ID NO:42、62、82、102、122、142、162、182、202、222、242、262、282、302和2186的氨基酸序列具有至少80%同一性的序列;或者
iii.由在中等严格条件下与由选自SEQ ID NO:40、60、80、100、120、140、160、180、200、220、240、260、280、300和2184的核酸序列组成的多核苷酸的互补序列杂交的多核苷酸编码的序列。
段落31.如段落24至30中任一项所述的抗原结合蛋白,其中该抗原结合蛋白包含与选自下组的重链可变区氨基酸序列具有至少90%同一性的氨基酸序列,该组由以下组成:SEQ ID NO:42、62、82、102、122、142、162、182、202、222、242、262、282、302和2186。
段落32.如段落24至31中任一项所述的抗原结合蛋白,其中该抗原结合蛋白包含与选自下组的重链可变区氨基酸序列具有至少90%同一性的氨基酸序列,该组由以下组成:SEQ ID NO:42、62、82、122、162、182、和302。
段落33.如段落24至32中任一项所述的抗原结合蛋白,其中该抗原结合蛋白包含与选自由SEQ ID NO:62和122组成的组的重链可变区氨基酸序列具有至少90%同一性的氨基酸序列。
段落34.如段落24至33中任一项所述的抗原结合蛋白,其中该抗原结合蛋白包含与选自下组的轻链可变区氨基酸序列具有至少90%同一性的氨基酸序列,该组由以下组成:SEQ ID NO:41、61、81、101、121、141、161、181、201、221、241、261、281、301和2185。
段落35.如段落24至34中任一项所述的抗原结合蛋白,其中该抗原结合蛋白包含与选自下组的轻链可变区氨基酸序列具有至少90%同一性的氨基酸序列,该组由以下组成:SEQ ID NO:41、61、81、121、161、181、和301。
段落36.如段落24至35中任一项所述的抗原结合蛋白,其中该抗原结合蛋白包含与选自由SEQ ID NO:61和121组成的组的轻链可变区氨基酸序列具有至少90%同一性的氨基酸序列。
段落37.如段落24至36中任一项所述的抗原结合蛋白,该抗原结合蛋白包含:
i)SEQ ID NO:41中列出的轻链可变结构域和SEQ ID NO:42中列出的重链可变结构域;
ii)SEQ ID NO:61中列出的轻链可变结构域和SEQ ID NO:62中列出的重链可变结构域;
iii)SEQ ID NO:81中列出的轻链可变结构域和SEQ ID NO:82中列出的重链可变结构域;
iv)SEQ ID NO:101中列出的轻链可变结构域和SEQ ID NO:102中列出的重链可变结构域;
v)SEQ ID NO:121中列出的轻链可变结构域和SEQ ID NO:122中列出的重链可变结构域;
vi)SEQ ID NO:141中列出的轻链可变结构域和SEQ ID NO:142中列出的重链可变结构域;
vii)SEQ ID NO:161中列出的轻链可变结构域和SEQ ID NO:162中列出的重链可变结构域;
viii)SEQ ID NO:181中列出的轻链可变结构域和SEQ ID NO:182中列出的重链可变结构域;
ix)SEQ ID NO:201中列出的轻链可变结构域和SEQ ID NO:202中列出的重链可变结构域;
x)SEQ ID NO:221中列出的轻链可变结构域和SEQ ID NO:222中列出的重链可变结构域;
xi)SEQ ID NO:241中列出的轻链可变结构域和SEQ ID NO:242中列出的重链可变结构域;
xii)SEQ ID NO:261中列出的轻链可变结构域和SEQ ID NO:262中列出的重链可变结构域;
xiii)SEQ ID NO:281中列出的轻链可变结构域和SEQ ID NO:282中列出的重链可变结构域;
xiv)SEQ ID NO:301中列出的轻链可变结构域和SEQ ID NO:302中列出的重链可变结构域;或者
xv)SEQ ID NO:2185中列出的轻链可变结构域和SEQ ID NO:2186中列出的重链可变结构域。
段落38.如段落24至37中任一项所述的抗原结合蛋白,该抗原结合蛋白包含:
i)SEQ ID NO:41中列出的轻链可变结构域和SEQ ID NO:42中列出的重链可变结构域;
ii)SEQ ID NO:61中列出的轻链可变结构域和SEQ ID NO:62中列出的重链可变结构域;
iii)SEQ ID NO:81中列出的轻链可变结构域和SEQ ID NO:82中列出的重链可变结构域;
iv)SEQ ID NO:121中列出的轻链可变结构域和SEQ ID NO:122中列出的重链可变结构域;
v)SEQ ID NO:161中列出的轻链可变结构域和SEQ ID NO:162中列出的重链可变结构域;
vi)SEQ ID NO:181中列出的轻链可变结构域和SEQ ID NO:182中列出的重链可变结构域;或者
vii)SEQ ID NO:301中列出的轻链可变结构域和SEQ ID NO:302中列出的重链可变结构域。
段落39.如段落24至38中任一项所述的抗原结合蛋白,该抗原结合蛋白包含:SEQID NO:61中列出的轻链可变结构域和SEQ ID NO:62中列出的重链可变结构域;或SEQ IDNO:121中列出的轻链可变结构域和SEQ ID NO:122中列出的重链可变结构域。
段落40.如段落24至39中任一项所述的抗原结合蛋白,其中该抗抗原结合蛋白的一个或多个重链框架氨基酸被来自另一人抗体氨基酸序列的相应的一个或多个氨基酸替代。
段落41.如段落24至40中任一项所述的抗原结合蛋白,其中该抗原结合蛋白的一个或多个轻链框架氨基酸被来自另一人抗体氨基酸序列的相应的一个或多个氨基酸替代。
段落42.如段落24至41中任一项所述的抗原结合蛋白,其中该重链包含选自以下的恒定区:IgG、IgM、IgA、IgD、IgE的重链恒定区、其片段、其组合、以及其修饰,在这些修饰中一个至十个重链框架氨基酸被来自另一人抗体氨基酸序列的相应的一个或多个氨基酸替代。
段落43.一种抗原结合蛋白,其与如段落24至42中任一项所述的抗原结合蛋白竞争与具有SEQ ID NO:20的序列的人TREM-1结合。
段落44.如段落24至43中任一项所述的抗原结合蛋白,其中该抗原结合蛋白选自由以下组成的组:人抗体、人源化抗体、嵌合抗体、单克隆抗体、重组抗体、Fab、F(ab’)2、Fab2、单价IgG、scFv、scFv-Fc、IgG1抗体、IgG2抗体、IgG3抗体、和IgG4抗体。
段落45.如段落44所述的抗原结合蛋白,其中该抗原结合蛋白是IgG1抗体。
段落46.如段落44或45所述的抗原结合蛋白,其中该抗原结合蛋白是单价IgG。
段落47.如段落44至46中任一项所述的抗原结合蛋白,其中该抗原结合蛋白是人抗体。
段落48.如段落24至47中任一项所述的抗原结合蛋白,该抗原结合蛋白包含与选自SEQ ID NO:42、62、82、102、122、142、162、182、202、222、242、262、282、302和2186的序列具有至少90%同一性的重链氨基酸序列,以及与选自SEQ ID NO:41、61、81、101、121、141、161、181、201、221、241、261、281、301和2185的序列具有至少90%同一性的轻链氨基酸序列。
段落49.如段落24至48中任一项所述的抗原结合蛋白,该抗原结合蛋白具有选自SEQ ID NO:42、62、82、102、122、142、162、182、202、222、242、262、282、302和2186的重链氨基酸,以及具有SEQ ID NO:41、61、81、101、121、141、161、181、201、221、241、261、281、301和2185的轻链氨基酸序列。
段落50.如段落24至49中任一项所述的抗原结合蛋白,该抗原结合蛋白具有选自SEQ ID NO:42、62、82、122、162、182、和302的重链氨基酸。
段落51.如段落24至50中任一项所述的抗原结合蛋白,该抗原结合蛋白具有选自SEQ ID NO:62和122的重链氨基酸。
段落52.如段落24至51中任一项所述的抗原结合蛋白,该抗原结合蛋白具有选自SEQ ID NO:41、61、81、121、161、181、和301的轻链氨基酸。
段落53.如段落24至52中任一项所述的抗原结合蛋白,该抗原结合蛋白具有选自SEQ ID NO:61和121的轻链氨基酸。
段落54.一种分离的核酸分子,其包含编码如段落24至53中任一项所述的重链的核苷酸序列。
段落55.一种分离的核酸分子,其包含编码如段落24至53中任一项所述的轻链的核苷酸序列。
段落56.如段落54所述的核酸分子,该核酸分子进一步包含编码如段落24至53中任一项所述的轻链的核苷酸序列。
段落57.如段落54至56中任一项所述的核酸分子,其中编码该轻链可变区的核苷酸序列在SEQ ID NO:39、59、79、99、119、139、159、179、199、219、239、259、279、299和2183中列出,并且编码该重链可变区的核苷酸序列在SEQ ID NO:40、60、80、100、120、140、160、180、200、220、240、260、280、300和2184中列出。
段落58.一种表达载体,其包含可操作地连接到表达控制序列的如段落54至57中任一项所述的核酸分子。
段落59.一种重组宿主细胞,其包含如段落54所述的核酸分子;或如段落55所述的核酸分子;或如段落54所述的核酸分子和如段落55所述的核酸分子;或如段落56或57所述的核酸分子;或如段落58所述的载体。
段落60.如段落59所述的宿主细胞,其中该宿主细胞是哺乳动物细胞。
段落61.如段落59或60所述的宿主细胞,其中该宿主细胞是CHO细胞。
段落62.一种使用如段落59至61中任一项所述的宿主细胞产生抗原结合蛋白的方法,该方法包括培养该宿主细胞并回收所述抗原结合蛋白。
段落63.一种通过如段落62所述的方法产生的抗原结合蛋白。
段落64.一种药物组合物,其包含如段落24-53中任一项所述的抗体和药学上可接受的载剂。
段落65.一种抗原结合蛋白,其包含抗原结合部分和一个或两个IL-10部分,其中:
a.该抗原结合部分是抗体或抗体片段,
b.每个IL-10部分独立地是单价或二价,
c.每个IL-10部分独立地选自具有与SEQ ID NO:1具有90%同一性的序列的一种或多种人IL-10突变蛋白,并且
d.至少一个IL-10部分与该抗原结合部分共价结合。
段落66.如段落65所述的抗原结合蛋白,其中至少一个IL-10部分与该抗原结合部分的C末端融合。
段落67.一种抗原结合蛋白,其包含:
(a)具有式A-L-M或M-L-A的多肽序列,其中
i)A是与SEQ ID NO:20中列出的TREM-1蛋白结合的IgG抗体的免疫球蛋白重链,
ii)L是包含4至20个氨基酸的接头肽,并且
iii)M是与SEQ ID NO:2中列出的wt IL-10具有至少90%序列同一性的IL-10突变蛋白;和
(b)结合SEQ ID NO:20中列出的TREM-1蛋白的IgG抗体的免疫球蛋白轻链,
其中(a)的免疫球蛋白重链和(b)的免疫球蛋白轻链形成结合TREM-1的IgG抗体部分,其中该蛋白质包含(a)的多肽的一个或两个分子以及(b)的轻链的一个或两个分子,任选地其中(a)的仅1个多肽包含M部分。
段落68.如段落65至67中任一项所述的抗原结合蛋白,其中:
a.抗原结合部分是抗体,并且
b.IL-10部分与该抗体的每条重链融合。
段落69.如段落65至68中任一项所述的抗原结合蛋白,其中每个IL-10部分是单体。
段落70.如段落65至69中任一项所述的抗原结合蛋白,其中:
a.每个IL-10部分包含与SEQ ID NO:2中列出的氨基酸序列具有至少90%同一性的氨基酸序列,并且
b.每个IL-10部分独立地包含选自以下的至少一个突变:螺旋环AB、螺旋环CD、螺旋环DE、螺旋A、螺旋B、螺旋C、螺旋D、螺旋E和/或螺旋F中的突变。
段落71.如段落70所述的抗原结合蛋白,其中至少一个IL-10部分包含螺旋A中的至少一个突变。
段落72.如段落70所述的抗原结合蛋白,其中至少一个IL-10部分包含螺旋F中的至少一个突变。
段落73.如段落70所述的抗原结合蛋白,其中至少一个IL-10部分包含螺旋环AB中的至少一个突变。
段落74.如段落65至73中任一项所述的抗原结合蛋白,其中该抗原结合蛋白抑制髓细胞中TNF-α产生。
段落75.如段落65至74中任一项所述的抗原结合蛋白,其中该IL-10突变蛋白抗原结合蛋白抑制髓细胞中TNF-α产生,但仍缺乏CD8+T细胞和B细胞激活。
段落76.如段落65至75中任一项所述的抗原结合蛋白,其中每个IL-10部分独立地包含SEQ ID NO:2的残基N10、H14、F15、P20、M22、L23、R24、R27、D28、K34、T35、Q38、M39、K40、D41、Q42、L43、D44、N45、L46、L47、L48、K49、F56、K57、Y59、L60、Q63、E67、Q70、M77、Q79、N82、Q83、D84、P85、D86、I87、A89、H90、S93、T100、L103、H109、R110、L112、E115、N116、A127、K130、I136、Y137、K138、S141、E142、D144、I145、E151、M154、M156、K157、或N160中的一个或多个中的突变,或在螺旋D和螺旋E之间添加4-8个氨基酸。
段落77.如段落65至76中任一项所述的抗原结合蛋白,其中每个IL-10部分与SEQID NO:2中列出的氨基酸序列具有至少95%同一性。
段落78.如段落65至77中任一项所述的抗原结合蛋白,其中每个IL-10部分独立地包含选自下组的一个或多个突变,该组由以下组成:SEQ ID NO:2的N10Q、N10I、N10K、R27L、K34D、D41G、L46K、Q38E、Q38R、Q38D、K138L、K138D、I87A、H14Q、F15Y、M22V、K49T、K49S、F56Y、K57N、Y59T、L60Q、Q63E、Q63L、E67C、Q70E、Q70K、M77R、M77V、Q79R、Q79C、D84R、A89P、H90E、H90Q、S93E、S93Q、T100R、L103E、H109D、R110P、R110Q、L112V、E115K、N116D、N116Q、A127M、K130Q、I136C、Y137C、M154V、M156C、K157N、或N160D,任选地包含在螺旋D和螺旋E之间添加六个氨基酸。
段落79.如段落76至78中任一项所述的抗原结合蛋白,其中螺旋D和螺旋E之间的氨基酸是GGGSGG(SEQ ID NO:2676)。
段落80.如段落65至79中任一项所述的抗原结合蛋白,其中该IL-10部分具有以下中任一个中列出的氨基酸序列:SEQ ID NO:3-10或SEQ ID NO:2138、2140、2142、2144、2146、2148、2150、2152、2154、2156、2158、2160、2162、2164、2166、2168、2170、2172、2174、2176、2178、2180、2182、2360、2362、2364、2366、2368、2370、2372、2374、2376、2378、2380、2382、2384、2386、2388、2390、2392、2394、2396、2398、2400、2402、2404、2406、2408、2410、2412、2414、2416、2418、2420、2422、2424、2426、2428、2430、2432、2434、2436、2438、2440、2442、2444、2446、2448、2450、2452、2454、2456、2458、2460、2462、2464、2466、2468、2470、2472、2474、2476、2478、2480、2482、2484、2486、2488、2490、2492、2494、2496、2500、2502、2504、2506、2508、2510、2512、2514、2516、2518、2520、2522、2524、2526、2528、2530、2532、2534、2536、2538、2540、和2777-2791。
段落81.如段落65至80中任一项所述的抗原结合蛋白,其中:
a.该抗原结合蛋白包含与该抗原结合部分的至少一个C末端融合的至少一个接头,并且
b.IL-10部分与每个接头的C末端共价结合。
段落82.如段落81所述的抗原结合蛋白,其中该接头为4至18个氨基酸长。
段落83.如段落81或82所述的抗原结合蛋白,其中该接头为六个氨基酸长。
段落84.如段落65至83中任一项所述的抗原结合蛋白,该抗原结合蛋白进一步包含连接至所述重链可变区的人重链恒定区。
段落85.如段落65至84中任一项所述的抗原结合蛋白,该抗原结合蛋白进一步包含连接至所述轻链可变区的人轻链恒定区。
段落86.如段落65至85中任一项所述的抗原结合蛋白,该抗原结合蛋白具有以下中任一个中列出的重链氨基酸序列:SEQ ID NO:863、865、867、869、871、873、875、877、879、881、883、885、887、889、891、893、895、897、899、901、903、905、907、909、911、913、915、917、919、921、923、925、927、929、931、933、935、937、939、941、943、945、947、949、951、953、955、957、959、961、963、965、967、969、971、973、975、977、979、981、983、985、987、989、991、993、995、997、999、1001、1003、1005、1007、1009、1011、1013、1015、1017、1019、1021、1023、1025、1027、1029、1031、1033、1035、1037、1039、1041、1043、1045、1047、1049、1051、1053、1055、1057、1059、1061、1063、1065、1067、1069、1071、1073、1075、1077、1079、1081、1083、和1085。
段落87.如段落65至86中任一项所述的抗原结合蛋白,该抗原结合蛋白具有以下中任一个中列出的轻链氨基酸序列:SEQ ID NO:864、866、868、870、872、874、876、878、880、882、884、886、888、890、892、894、896、898、900、902、904、906、908、910、912、914、916、918、920、922、924、926、928、930、932、934、936、938、940、942、944、946、948、950、952、954、956、958、960、962、964、966、968、970、972、974、976、978、980、982、984、986、988、990、992、994、996、998、1000、1002、1004、1006、1008、1010、1012、1014、1016、1018、1020、1022、1024、1026、1028、1030、1032、1034、1036、1038、1040、1042、1044、1046、1048、1050、1052、1054、1056、1058、1060、1062、1064、1066、1068、1070、1072、1074、1076、1078、1080、1082、1084、和1086。
段落88.如段落65至87中任一项所述的抗原结合蛋白,该抗原结合蛋白具有以下中任一个中列出的重链氨基酸序列:SEQ ID NO:863、865、867、869、871、873、875、877、879、881、883、885、887、889、891、893、895、897、899、901、903、905、907、909、911、913、915、917、919、921、923、925、927、929、931、933、935、937、939、941、943、945、947、949、951、953、955、957、959、961、963、965、967、969、971、973、975、977、979、981、983、985、987、989、991、993、995、997、999、1001、1003、1005、1007、1009、1011、1013、1015、1017、1019、1021、1023、1025、1027、1029、1031、1033、1035、1037、1039、1041、1043、1045、1047、1049、1051、1053、1055、1057、1059、1061、1063、1065、1067、1069、1071、1073、1075、1077、1079、1081、1083、和1085,以及以下中列出的相应的轻链氨基酸序列:SEQ ID NO:864、866、868、870、872、874、876、878、880、882、884、886、888、890、892、894、896、898、900、902、904、906、908、910、912、914、916、918、920、922、924、926、928、930、932、934、936、938、940、942、944、946、948、950、952、954、956、958、960、962、964、966、968、970、972、974、976、978、980、982、984、986、988、990、992、994、996、998、1000、1002、1004、1006、1008、1010、1012、1014、1016、1018、1020、1022、1024、1026、1028、1030、1032、1034、1036、1038、1040、1042、1044、1046、1048、1050、1052、1054、1056、1058、1060、1062、1064、1066、1068、1070、1072、1074、1076、1078、1080、1082、1084、和1086。
段落89.如段落65至85中任一项所述的抗原结合蛋白,该抗原结合蛋白具有以下中任一个中列出的重链氨基酸序列:SEQ ID NO:1883、1885、1887、1889、1891、1893、1895、1897、1899、1901、1903、1905、1907、1909、1911、1913、1915、1917、1919、1921、1923、1925、1927、1929、1931、1933、1935、1937、1939、1941、1943、1945、1947、1949、1951、1953、1955、1957、1959、1961、1963、1965、1967、1969、1971、1973、1975、1977、1979、1981、1983、1985、1987、1989、1991、1993、1995、1997、1999、2001、2003、2005、和2007。
段落90.如段落65至85或89中任一项所述的抗原结合蛋白,该抗原结合蛋白具有以下中任一个中列出的轻链氨基酸序列:SEQ ID NO:2543、2544、2545、2546、2547、2548、2549、2550、2551、2552、2553、2554、2555、2556、2557、2558、2559、2560、2561、2562、2563、2564、2565、2566、2567、2568、2569、2570、2571、2572、2573、2574、2575、2576、2577、2578、2579、2580、2581、2582、2583、2584、2585、2586、2587、2588、2589、2590、2591、2592、2593、2594、2595、2596、2597、2598、2599、2600、2601、2602、2603、2604、和2605。
段落91.如段落65至85或88至90中任一项所述的抗原结合蛋白,该抗原结合蛋白具有以下中任一个中列出的重链氨基酸序列:SEQ ID NO:1883、1885、1887、1889、1891、1893、1895、1897、1899、1901、1903、1905、1907、1909、1911、1913、1915、1917、1919、1921、1923、1925、1927、1929、1931、1933、1935、1937、1939、1941、1943、1945、1947、1949、1951、1953、1955、1957、1959、1961、1963、1965、1967、1969、1971、1973、1975、1977、1979、1981、1983、1985、1987、1989、1991、1993、1995、1997、1999、2001、2003、2005、和2007,以及以下中列出的相应的轻链氨基酸序列:SEQ ID NO:2543、2544、2545、2546、2547、2548、2549、2550、2551、2552、2553、2554、2555、2556、2557、2558、2559、2560、2561、2562、2563、2564、2565、2566、2567、2568、2569、2570、2571、2572、2573、2574、2575、2576、2577、2578、2579、2580、2581、2582、2583、2584、2585、2586、2587、2588、2589、2590、2591、2592、2593、2594、2595、2596、2597、2598、2599、2600、2601、2602、2603、2604、和2605。
段落92.如段落65至85中任一项所述的抗原结合蛋白,该抗原结合蛋白具有以下中任一个中列出的重链氨基酸序列:SEQ ID NO:2011、2013、2015、2017、2019、2021、2026、2025、2027、2029、2031、2033、2035、2037、2039、2041、2043、2045、2047、2049、2051、2053、2055、2057、2059、2061、2063、2065、2067、2069、2071、2073、2075、2077、2079、2081、2083、2085、2087、2089、2091、2093、2095、2097、2099、2101、2103、2105、2107、2109、2111、2113、2115、2117、2119、2121、2123、2125、2127、2129、2131、2133、和2135。
段落93.如段落65至85或92中任一项所述的抗原结合蛋白,该抗原结合蛋白具有以下中任一个中列出的轻链氨基酸序列:SEQ ID NO:2233、2235、2237、2239、2241、2243、2245、2247、2249、2251、2253、2255、2257、2259、2261、2263、2265、2267、2269、2271、2273、2275、2277、2279、2281、2283、2285、2287、2289、2291、2293、2295、2297、2299、2301、2303、2305、2307、2309、2311、2313、2315、2317、2319、2321、2323、2325、2327、2329、2331、2333、2335、2337、2339、2341、2343、2345、2347、2349、2351、2353、2355、和2357。
段落94.如段落65至85或92至93中任一项所述的抗原结合蛋白,该抗原结合蛋白具有以下中任一个中列出的重链氨基酸序列:SEQ ID NO:2011、2013、2015、2017、2019、2021、2026、2025、2027、2029、2031、2033、2035、2037、2039、2041、2043、2045、2047、2049、2051、2053、2055、2057、2059、2061、2063、2065、2067、2069、2071、2073、2075、2077、2079、2081、2083、2085、2087、2089、2091、2093、2095、2097、2099、2101、2103、2105、2107、2109、2111、2113、2115、2117、2119、2121、2123、2125、2127、2129、2131、2133、和2135,以及以下中列出的相应的轻链氨基酸序列:SEQ ID NO:2233、2235、2237、2239、2241、2243、2245、2247、2249、2251、2253、2255、2257、2259、2261、2263、2265、2267、2269、2271、2273、2275、2277、2279、2281、2283、2285、2287、2289、2291、2293、2295、2297、2299、2301、2303、2305、2307、2309、2311、2313、2315、2317、2319、2321、2323、2325、2327、2329、2331、2333、2335、2337、2339、2341、2343、2345、2347、2349、2351、2353、2355、和2357。
段落95.如段落65至84中任一项所述的抗原结合蛋白,其中该抗原结合部分选自由以下组成的组:人抗体、人源化抗体、嵌合抗体、单克隆抗体、重组抗体、Fab、F(ab’)2、Fab2、单价IgG、scFv、scFv-Fc、IgG1抗体、IgG2抗体、IgG3抗体、和IgG4抗体。
段落96.如段落65至95中任一项所述的抗原结合蛋白,其中该抗原结合部分是IgG。
段落97.如段落65至96中任一项所述的抗原结合蛋白,其中该抗原结合部分是IgG1抗体。
段落98.如段落65至97中任一项所述的抗原结合蛋白,其中该抗原结合部分是单价IgG。
段落99.如段落65至98中任一项所述的抗原结合蛋白,其中该抗原结合部分的重链恒定区选自IgG、IgM、IgA、IgD、IgE的重链恒定区、其片段、其组合、以及其修饰,在这些修饰中一个至十个重链框架氨基酸被来自另一人抗体恒定区的相应的一个或多个氨基酸替代。
段落100.如段落65至99中任一项所述的抗原结合蛋白,其中该抗原结合部分与具有SEQ ID NO:22中列出的氨基酸序列的人PD-1结合。
段落101.如段落65至99中任一项所述的抗原结合蛋白,其中该抗原结合部分与具有SEQ ID NO:20中列出的氨基酸序列的人TREM-1结合。
段落102.如段落65至99或101中任一项所述的抗原结合蛋白,其中该抗原结合部分是抗TREM-1抗原结合部分,其包含:
a.轻链可变结构域,该轻链可变结构域包含:
i.轻链CDR1序列,其包含选自SEQ ID NO:30、50、70、90、110、130、150、170、190、210、230、250、270、290和2190的氨基酸序列;
ii.轻链CDR2序列,其包含选自SEQ ID NO:31、51、71、91、111、131、151、171、191、211、231、251、271、291和2190的氨基酸序列;
iii.轻链CDR3序列,其包含选自SEQ ID NO:32、52、72、92、112、132、152、172、192、212、232、252、272、292和2192的氨基酸序列;和
b.重链可变结构域,该重链可变结构域包含:
i.重链CDR1序列,其包含选自SEQ ID NO:36、56、76、96、116、136、156、176、196、216、236、256、276、296和2196的氨基酸序列;
ii.重链CDR2序列,其包含选自SEQ ID NO:37、57、77、97、117、137、157、177、197、217、237、257、277、297和2197的氨基酸序列;和
iii.重链CDR3序列,其包含选自SEQ ID NO:38、58、78、98、118、138、158、178、198、218、238、258、278、298和2198的氨基酸序列。
段落103.如段落101至102中任一项所述的抗原结合蛋白,其中:
a.轻链CDR1序列在SEQ ID NO:30、50、70、110、150、170、或290中列出;
b.轻链CDR2序列在SEQ ID NO:31、51、71、111、151、171、或291中列出;
c.轻链CDR3序列在SEQ ID NO:32、52、72、112、152、172、或292中列出;
d.重链CDR1序列在SEQ ID NO:36、56、76、116、156、176、和296中列出;
e.重链CDR2序列在SEQ ID NO:37、57、77、117、157、177、和297中列出;和
f.重链CDR3序列在SEQ ID NO:38、58、78、118、158、178、和298中列出。
段落104.如段落101至103中任一项所述的抗原结合蛋白,其中:
a.轻链CDR1序列在SEQ ID NO:50和110中列出;
b.轻链CDR2序列在SEQ ID NO:51和111中列出;
c.轻链CDR3序列在SEQ ID NOS:52和112中列出;
d.重链CDR1序列在SEQ ID NO:56和116中列出;
e.重链CDR2序列在SEQ ID NO:57和117中列出;和
f.重链CDR3序列在SEQ ID NO:58和118中列出。
段落105.如段落101至104中任一项所述的抗原结合蛋白,其中该抗原结合部分是包含选自以下的一组CDR氨基酸序列的抗TREM-1抗原结合部分:
i)SEQ ID NO:30(LCDR1)、SEQ ID NO:31(LCDR2)、SEQ ID NO:32(LCDR3)、SEQ IDNO:36(HCDR1)、SEQ ID NO:37(HCDR2)和SEQ ID NO:38(HCDR3);
ii)SEQ ID NO:50(LCDR1)、SEQ ID NO:51(LCDR2)、SEQ ID NO:52(LCDR3)、SEQ IDNO:56(HCDR1)、SEQ ID NO:57(HCDR2)和SEQ ID NO:58(HCDR3);
iii)SEQ ID NO:70(LCDR1)、SEQ ID NO:71(LCDR2)、SEQ ID NO:72(LCDR3)、SEQID NO:76(HCDR1)、SEQ ID NO:77(HCDR2)和SEQ ID NO:78(HCDR3);
iv)SEQ ID NO:90(LCDR1)、SEQ ID NO:91(LCDR2)、SEQ ID NO:92(LCDR3)、SEQ IDNO:96(HCDR1)、SEQ ID NO:97(HCDR2)和SEQ ID NO:98(HCDR3);
v)SEQ ID NO:110(LCDR1)、SEQ ID NO:111(LCDR2)、SEQ ID NO:112(LCDR3)、SEQID NO:116(HCDR1)、SEQ ID NO:117(HCDR2)和SEQ ID NO:118(HCDR3);
vi)SEQ ID NO:130(LCDR1)、SEQ ID NO:131(LCDR2)、SEQ ID NO:132(LCDR3)、SEQID NO:136(HCDR1)、SEQ ID NO:137(HCDR2)和SEQ ID NO:138(HCDR3);
vii)SEQ ID NO:150(LCDR1)、SEQ ID NO:151(LCDR2)、SEQ ID NO:152(LCDR3)、SEQ ID NO:156(HCDR1)、SEQ ID NO:157(HCDR2)和SEQ ID NO:158(HCDR3);
viii)SEQ ID NO:170(LCDR1)、SEQ ID NO:171(LCDR2)、SEQ ID NO:172(LCDR3)、SEQ ID NO:176(HCDR1)、SEQ ID NO:177(HCDR2)和SEQ ID NO:178(HCDR3);
ix)SEQ ID NO:190(LCDR1)、SEQ ID NO:191(LCDR2)、SEQ ID NO:192(LCDR3)、SEQID NO:196(HCDR1)、SEQ ID NO:197(HCDR2)和SEQ ID NO:198(HCDR3);
x)SEQ ID NO:210(LCDR1)、SEQ ID NO:211(LCDR2)、SEQ ID NO:212(LCDR3)、SEQID NO:216(HCDR1)、SEQ ID NO:217(HCDR2)和SEQ ID NO:218(HCDR3);
xi)SEQ ID NO:230(LCDR1)、SEQ ID NO:231(LCDR2)、SEQ ID NO:232(LCDR3)、SEQID NO:236(HCDR1)、SEQ ID NO:237(HCDR2)和SEQ ID NO:238(HCDR3);
xii)SEQ ID NO:250(LCDR1)、SEQ ID NO:251(LCDR2)、SEQ ID NO:252(LCDR3)、SEQ ID NO:256(HCDR1)、SEQ ID NO:257(HCDR2)和SEQ ID NO:258(HCDR3);
xiii)SEQ ID NO:270(LCDR1)、SEQ ID NO:271(LCDR2)、SEQ ID NO:272(LCDR3)、SEQ ID NO:276(HCDR1)、SEQ ID NO:277(HCDR2)和SEQ ID NO:278(HCDR3);
xiv)SEQ ID NO:290(LCDR1)、SEQ ID NO:291(LCDR2)、SEQ ID NO:292(LCDR3)、SEQ ID NO:296(HCDR1)、SEQ ID NO:297(HCDR2)和SEQ ID NO:298(HCDR3);或
xv)SEQ ID NO:2190(LCDR1)、SEQ ID NO:2191(LCDR2)、SEQ ID NO:2192(LCDR3)、SEQ ID NO:2196(HCDR1)、SEQ ID NO:2197(HCDR2)和SEQ ID NO:2198(HCDR3)。
段落106.如段落101至105中任一项所述的抗原结合蛋白,其中该抗TREM-1抗原结合部分包含:
a.轻链可变结构域,其包含选自下组的氨基酸序列,该组由以下组成:
i.与选自SEQ ID NO:41、61、81、101、121、141、161、181、201、221、241、261、281、301和2185的氨基酸序列具有至少80%同一性的序列;
ii.由多核苷酸序列编码的与选自SEQ ID NO:41、61、81、101、121、141、161、181、201、221、241、261、281、301和2185的氨基酸序列具有至少80%同一性的序列;
iii.由在中等严格条件下与由选自SEQ ID NO:39、59、79、99、119、139、159、179、199、219、239、259、279、299和2183的核酸序列组成的多核苷酸的互补序列杂交的多核苷酸编码的序列;和
b.重链可变结构域,其包含选自下组的氨基酸序列,该组由以下组成:
i.与选自SEQ ID NO:42、62、82、102、122、142、162、182、202、222、242、262、282、302和2186的氨基酸序列具有至少80%同一性的序列;
ii.由多核苷酸序列编码的与选自SEQ ID NO:42、62、82、102、122、142、162、182、202、222、242、262、282、302和2186的氨基酸序列具有至少80%同一性的序列;
iii.由在中等严格条件下与由选自SEQ ID NO:40、60、80、100、120、140、160、180、200、220、240、260、280、300和2184的核酸序列组成的多核苷酸的互补序列杂交的多核苷酸编码的序列。
段落107.如段落101至106中任一项所述的抗原结合蛋白,其中该抗TREM-1抗原结合部分包含与选自SEQ ID NO:42、62、82、102、122、142、162、182、202、222、242、262、282、302和2186的重链可变区氨基酸序列具有至少90%同一性的氨基酸序列。
段落108.如段落101至107中任一项所述的抗原结合蛋白,其中该抗TREM-1抗原结合部分包含与选自SEQ ID NO:41、61、81、101、121、141、161、181、201、221、241、261、281、301和2185的序列具有至少90%同一性的轻链可变区氨基酸序列。
段落109.选自如段落101至108中任一项所述的抗原结合蛋白,其中该抗TREM-1抗原结合部分的一个或多个重链框架氨基酸被来自另一人抗体氨基酸序列的相应的一个或多个氨基酸替代。
段落110.如段落101至109中任一项所述的抗原结合蛋白,该抗原结合蛋白包含与选自SEQ ID NO:42、62、82、122、162、182、和302的序列具有至少90%同一性的重链氨基酸序列,以及与选自SEQ ID NO:41、61、81、121、161、181、和301的序列具有至少90%同一性的轻链氨基酸序列。
段落111.如段落101至110中任一项所述的抗原结合蛋白,其中:
a.该抗原结合蛋白包含两条轻链和两条重链:
b.每条重链包含在该重链的C末端处附接的IL-10部分;
c.每个重链-IL-10部分抗原结合蛋白包含与选自以下的序列具有至少90%同一性的氨基酸序列:SEQ ID NO:863、865、867、869、871、873、875、877、879、881、883、885、887、889、891、893、895、897、899、901、903、905、907、909、911、913、915、917、919、921、923、925、927、929、931、933、935、937、939、941、943、945、947、949、951、953、955、957、959、961、963、965、967、969、971、973、975、977、979、981、983、985、987、989、991、993、995、997、999、1001、1003、1005、1007、1009、1011、1013、1015、1017、1019、1021、1023、1025、1027、1029、1031、1033、1035、1037、1039、1041、1043、1045、1047、1049、1051、1053、1055、1057、1059、1061、1063、1065、1067、1069、1071、1073、1075、1077、1079、1081、1083、和1085;并且
d.每个轻链-IL-10部分包含与选自以下的序列具有至少90%同一性的氨基酸序列:SEQ ID NO:864、866、868、870、872、874、876、878、880、882、884、886、888、890、892、894、896、898、900、902、904、906、908、910、912、914、916、918、920、922、924、926、928、930、932、934、936、938、940、942、944、946、948、950、952、954、956、958、960、962、964、966、968、970、972、974、976、978、980、982、984、986、988、990、992、994、996、998、1000、1002、1004、1006、1008、1010、1012、1014、1016、1018、1020、1022、1024、1026、1028、1030、1032、1034、1036、1038、1040、1042、1044、1046、1048、1050、1052、1054、1056、1058、1060、1062、1064、1066、1068、1070、1072、1074、1076、1078、1080、1082、1084、和1086。
段落112.如段落101至111中任一项所述的抗原结合蛋白,其中该抗原结合蛋白具有选自下组的重链-IL-10部分氨基酸序列,该组由以下组成:SEQ ID NO:2137、2139、2141、2143、2145、2147、2149、2151、2153、2155、2157、2159、2161、2163、2165、2167、2169、2171、2173、2175、2177、2179、2181、2359、2361、2363、2365、2367、2369、2371、2373、2375、2377、2379、2381、2383、2385、2387、2389、2391、2393、2395、2397、2399、2401、2403、2405、2407、2409、2411、2143、2415、2417、2419、2421、2423、2425、2427、2429、2431、2433、2435、2437、2439、2441、2443、2445、2447、2449、2451、2453、2455、2457、2459、2461、2463、2465、2467、2469、2471、2473、2475、2477、2479、2481、2483、2485、2487、2489、2491、2493、2495、2497、2498、2499、2501、2503、2505、2507、2509、2511、2513、2515、2517、2519、2521、2523、2525、2527、2529、2531、2533、2535、2537、2539和2726-2776。
段落113.如段落101至111中任一项所述的抗原结合蛋白,其中该抗原结合蛋白具有选自由SEQ ID NO:2727-2732组成的组的重链-IL-10部分氨基酸序列。
段落114.如段落113所述的抗原结合蛋白,该抗原结合蛋白包含SEQ ID NO:2727或2728的重链氨基酸序列,和SEQ ID NO:976或SEQ ID NO:2554中列出的轻链氨基酸序列。
段落115.如段落113所述的抗原结合蛋白,该抗原结合蛋白包含SEQ ID NO:2729、2730、2731或2732的重链氨基酸序列,和SEQ ID NO:992或SEQ ID NO:2555中列出的轻链氨基酸序列。
段落116.如段落101至115中任一项所述的抗原结合蛋白,其中该抗原结合部分抑制TREM-1配体与TREM-1的结合。
段落117.一种抗原结合蛋白,其包含抗原结合部分和一个或两个IL-10部分,其中:
a.该抗原结合部分是抗体或抗体片段;
b.每个IL-10部分独立地是单价或二价;
c.每个IL-10部分独立地选自具有与SEQ ID NO:2具有90%同一性的序列的一种或多种人IL-10突变蛋白;
d.至少一个IL-10部分与该抗原结合部分共价结合,和/或
e.该抗原结合部分与如段落81至116中任一项所述的抗原结合部分竞争与人TREM-1蛋白结合。
段落118.如段落117所述的抗原结合蛋白,其中该抗原结合部分是人抗体。
段落119.一种分离的核酸分子,其包含编码如段落65-118中任一项所述的抗原结合蛋白的重链区的核苷酸序列。
段落120.一种分离的核酸分子,其包含编码如段落65-118中任一项所述的抗原结合蛋白的轻链区的核苷酸序列。
段落121.如段落116所述的分离的核酸分子,该分离的核酸分子进一步包含编码如段落65-118中任一项所述的抗原结合蛋白的轻链区的核苷酸序列。
段落122.一种表达载体,其包含可操作地连接到表达控制序列的如段落119-121中任一项所述的核酸分子。
段落123.一组重组宿主细胞,其包含如段落119-121中任一项所述的核酸分子或如段落122所述的载体。
段落124.如段落123所述的宿主细胞,其中该宿主细胞是哺乳动物细胞。
段落125.如段落123或124所述的宿主细胞,其中该宿主细胞是CHO细胞。
段落126.一种使用如段落123至125中任一项所述的宿主细胞产生抗原结合蛋白的方法,该方法包括培养该宿主细胞并回收所述抗体。
段落127.一种通过如段落126所述的方法产生的抗原结合蛋白。
段落128.一种药物组合物,其包含如段落65-118中任一项所述的抗原结合蛋白和药学上可接受的载剂。
段落129.一种治疗有需要的受试者的炎性疾病的方法,该方法包括施用如段落1-15中任一项所述的IL-10突变蛋白或如段落23所述的组合物。
段落130.如段落129所述的方法,其中与wt IL-10相比,该IL-10突变蛋白减少了髓细胞中TNF-α产生方面的抑制,降低了CD8+T细胞刺激方面的水平,和/或降低了B细胞刺激方面的水平。
段落131.一种治疗有需要的受试者的炎性疾病的方法,该方法包括施用如段落24-53中任一项所述的抗TREM-1抗原结合蛋白或如段落64所述的组合物。
段落132.一种治疗有需要的受试者的炎性疾病的方法,该方法包括施用如段落65-118中任一项所述的抗原结合蛋白或如段落128所述的组合物。
段落133.如段落129-132中任一项所述的方法,其中该炎性疾病选自由以下组成的组:炎性肠病、溃疡性结肠炎、克罗恩病、肠易激综合征、类风湿性关节炎、银屑病、银屑病关节炎、和细胞因子释放综合征(CRS)。
段落134.如段落133所述的方法,其中该炎性疾病是炎性肠病。
段落135.如段落132-134中任一项所述的方法,其中该抗原结合蛋白抑制髓细胞中TNF-α产生。
段落136.如段落132-135中任一项所述的方法,其中该抗原结合蛋白抑制髓细胞中TNF-α产生,但仍缺乏CD8+T细胞和B细胞激活。
段落137.如段落129至136中任一项所述的方法,其中该治疗通过静脉内或皮下施用进行。
段落138.如段落129-137中任一项所述的方法,其中该治疗通过每周一次、每两周一次、每三周一次、每4周一次、每月一次、每3个月一次、或每六个月一次施用进行。
段落139.如段落129-137中任一项所述的方法,该方法进一步包括施用一种或两种另外的治疗剂。
段落140.如段落139所述的方法,其中该另外的治疗剂选自皮质类固醇、NSAID、止痛剂、免疫抑制剂、抗炎剂、TNFα抑制剂、IL-12/IL-23抑制剂、IL-17和IFN-γ。
段落141.一种包含如段落1-15中任一项所述的IL-10突变蛋白的组合物,用于在治疗炎性疾病中使用。
段落142.包含如段落1-15中任一项所述的IL-10突变蛋白的组合物在制备用于治疗炎性疾病的药物中的用途。
段落143.一种包含如段落24-53中任一项所述的抗TREM-1抗体或抗原结合片段的组合物,用于在治疗炎性疾病中使用。
段落144.包含如段落24-53中任一项所述的抗TREM-1抗体或其抗原结合片段的组合物在制备用于治疗炎性疾病的药物中的用途。
段落145.一种包含与如段落1-15中任一项所述的抗IL-10突变蛋白组合的如段落24-53中任一项所述的抗TREM-1抗体或抗原结合片段的组合物,用于在治疗炎性疾病中使用。
段落146.包含与如段落1-15中任一项所述的抗IL-10突变蛋白组合的如段落24-53中任一项所述的抗TREM-1抗体或抗原结合片段的组合物在制备用于治疗炎性疾病的药物中的用途。
段落147.一种包含如段落65-118中任一项所述的抗原结合蛋白的组合物,用于在治疗炎性疾病中使用。
段落148.包含如段落65-118中任一项所述的抗原结合蛋白的组合物在制备用于治疗炎性疾病的药物中的用途。
段落149.一种药物组合物,该药物组合物包含:
a.抗TREM-1抗原结合蛋白,以及
b.如段落1-15中任一项所述的IL-10突变蛋白。
段落150.如段落140所述的药物组合物,其进一步包含如段落24-53中任一项所述的抗TREM-1抗原结合蛋白。
段落151.如段落142、144、146、或148中任一项所述的用途,其中该炎性疾病选自由以下组成的组:炎性肠病、溃疡性结肠炎、克罗恩病、肠易激综合征、类风湿性关节炎、银屑病、银屑病关节炎、和细胞因子释放综合征(CRS)。
段落152.用于如段落141、143、145、或147中任一项所述使用的组合物,其中该炎性疾病选自由以下组成的组:炎性肠病、溃疡性结肠炎、克罗恩病、肠易激综合征、类风湿性关节炎、银屑病、银屑病关节炎、和细胞因子释放综合征(CRS)。
段落153.一种分离的抗原结合蛋白,其中该抗原结合蛋白:
a.是抗体或抗体片段;
b.与具有SEQ ID NO:20中列出的氨基酸序列的人TREM-1结合;
c.包含轻链可变结构域,该轻链可变结构域包含:
i.包含氨基酸序列X1ASQSX2X3X4NLA(SEQ ID NO:2199)的轻链CDR1,其中X1是R或Q,其中X2是V或I,其中X3是N或S,并且其中X4是S、H、I、V或A;
ii.包含氨基酸序列GAX1X2RAT(SEQ ID NO:2200)的轻链CDR2,其中X1是S或Y,并且其中X2是T或I;和
iii.包含氨基酸序列QX1X2X3X4X5X6PX7T(SEQ ID NO:2201)的轻链CDR3;其中X1是Q、H或E,其中X2是F或Y,其中X3是K、Y或I,其中X4是N、T、L、I、或M;其中X5是W、F、H或Y,其中X6不存在或是P;其中X7是W、N、Y、H或L;并且
d.包含重链可变结构域,该重链可变结构域包含:
i.包含氨基酸序列X1X2X3MX4(SEQ ID NO:2202)的重链CDR1,其中X1是A、R、T或S,其中X2是Y或N,其中X3是A或W,并且其中X4是S或N;
ii.包含氨基酸序列X1X2X3X4X5X6 X7 X8 X9YYX10 X11X12VKG(SEQ ID NO:2205)的重链CDR2,其中X1是T、E、或S,其中X2不存在或是M、V、或I,其中X3是S、R或K,其中X4是G或Q,其中X5是S、D或H,其中X6是G、S、L、或A,其中X7是S、G、或R,其中X8是T、S、P或E,其中X9是T或I,其中X10是A或V,其中X11是D或E,并且其中X12是S或A;和
iii.包含氨基酸序列X1X2X3X4X5X6 X7 F X8YYX9(SEQ ID NO:2203)的重链CDR3,其中X1是V、E、A或G,其中X2是A、F、Y或G,其中X3是G、S、Y或W,其中X4是S或R,其中X5不存在或是N,其中X6是F、S、Y、或不存在,其中X7是L或F或不存在,其中X8是D或E,并且其中X9是Y、H或S。
段落154.如段落153所述的分离的抗原结合蛋白,其中该抗原结合蛋白包含:
a.轻链可变结构域,该轻链可变结构域包含:
i.包含氨基酸序列RASQSVNSNLA(SEQ ID NO:2212)的轻链CDR1;
ii.包含氨基酸序列GASTRAT(SEQ ID NO:2219)的轻链CDR2;
iii.包含氨基酸序列QQFKNWPPT(SEQ ID NO:2222)的轻链CDR3;和
b.重链可变结构域,该重链可变结构域包含:
i.包含氨基酸序列AYAMS(SEQ ID NO:2227)的重链CDR1;
ii.包含氨基酸序列TSGSGSTTYYADSVKG(SEQ ID NO:2230)的重链CDR2;和
iii.包含氨基酸序列VAGSNFLFDY(SEQ ID NO:2670)的重链CDR3。
段落155.一种分离的抗原结合蛋白,其中该抗原结合蛋白:
a.是抗体或抗体片段;
b.与具有SEQ ID NO:20中列出的氨基酸序列的人TREM-1结合;
c.包含轻链可变结构域,该轻链可变结构域包含:
i.包含氨基酸序列QASX1DIX2X3X4LN(SEQ ID NO:2204)的轻链CDR1,其中X1是R或Q,其中X2是R、S、N或F,其中X3是K或N,并且其中X4是H、Y或D;
ii.包含氨基酸序列X1X2X3X4LET(SEQ ID NO:2206)的轻链CDR2,其中X1是D、G或H,其中X2是A、V或T,其中X3是S、A或Y,并且其中X4是T或N;
iii.包含氨基酸序列QX1YX3X4X5PX6T(SEQ ID NO:2207)的轻链CDR3,其中X1是Q或H,其中X2是D、A或G,其中X3是N或K;其中X4是L或I,并且其中X5是I或L;并且
d.包含重链可变结构域,该重链可变结构域包含:
i.包含氨基酸序列X1YDIN(SEQ ID NO:2208)的重链CDR1,其中X1是R或S;
ii.包含氨基酸序列X1X2NPX3X4GX5X6GX7 X8 X9X10FX11X12(SEQ ID NO:2209)的重链CDR2,其中X1是W或R,其中X2是M或L,其中X3是N、Q、或K,其中X4是S、A、或R,其中X5是N、或Q,其中X6是S、A、或T,其中X7是S、Q、或Y,其中X8是V或T,其中X9是Q或K,其中X10是K或N,其中X11是R或Q,并且其中X12是G或D;和
iii.包含氨基酸序列X1X2X3X4 X5X6 X7 X8 X9X10X11X12FX13X14(SEQ ID NO:2210)的重链CDR3;其中X1是G、L或R,其中X2是G、I、或R,其中X3是Y、R、I、G、或A,其中X4是T、S、Y、或V,其中X5是S或Y,其中X6是S、A、I、或R,其中X7是W、A、或S,其中X8不存在或是S,其中X9不存在或是F、W、或Y,并且其中X10是R、S、H、K、或E,其中X11是W、H、Y、或F,其中X12是Y、V、A、或S,其中X13是D或Q,并且其中X14是L、Y、I、或H。
段落156.如段落155所述的抗原结合蛋白,其中该抗原结合蛋白包含:
a.轻链可变结构域,该轻链可变结构域包含:
i.包含氨基酸序列QASQDIRKHLN(SEQ ID NO:2213)的轻链CDR1;
ii.包含氨基酸序列DASNLET(SEQ ID NO:2220)的轻链CDR2;和
iii.包含氨基酸序列QHYDNLPIT(SEQ ID NO:2223)的轻链CDR3;和
b.重链可变结构域,该重链可变结构域包含:
i.包含氨基酸序列RYDIN(SEQ ID NO:2228)的重链CDR1;
ii.包含氨基酸序列WMNPNSGNSSVQKFRG(SEQ ID NO:2231)的重链CDR2;和
iii.包含氨基酸序列GGYTSSWRWYFDL(SEQ ID NO:2671)或GGYTSSWSRWYFDL(SEQID NO:2672)的重链CDR3。
Claims (44)
1.一种人白介素-10(IL-10)突变蛋白,其包含与SEQ ID NO:2中列出的氨基酸序列具有至少90%同一性的氨基酸序列,其中所述IL-10突变蛋白具有选自以下的至少一个突变:螺旋环AB、螺旋环CD、螺旋环DE、螺旋A、螺旋B、螺旋C、螺旋D、螺旋E和/或螺旋F中的突变。
2.如权利要求2所述的IL-10突变蛋白,其中该突变是以下中的一个或多个:SEQ IDNO:2的R27L、K34D、D41G、L46K、Q38E、Q38R、Q38D、K138L、K138D、I87A、H14Q、F15Y、M22V、K49T、K49S、F56Y、K57N、Y59T、L60Q、Q63E、Q63L、E67C、Q70E、Q70K、M77R、M77V、Q79R、Q79C、D84R、A89P、H90E、H90Q、S93E、S93Q、T100R、L103E、H109D、R110P、R110Q、L112V、E115K、N116D、A127M、K130Q、I136C、Y137C、M154V、M156C、K157N、或N160D,任选地包含在螺旋D和螺旋E之间添加6个氨基酸。
3.如权利要求1或2所述的IL-10突变蛋白,其中该IL-10突变蛋白具有以下中任一个中列出的氨基酸序列:SEQ ID NO:3-10或SEQ ID NO:2138、2140、2142、2144、2146、2148、2150、2152、2154、2156、2158、2160、2162、2164、2166、2168、2170、2172、2174、2176、2178、2180、2182、2360、2362、2364、2366、2368、2370、2372、2374、2376、2378、2380、2382、2384、2386、2388、2390、2392、2394、2396、2398、2400、2402、2404、2406、2408、2410、2412、2414、2416、2418、2420、2422、2424、2426、2428、2430、2432、2434、2436、2438、2440、2442、2444、2446、2448、2450、2452、2454、2456、2458、2460、2462、2464、2466、2468、2470、2472、2474、2476、2478、2480、2482、2484、2486、2488、2490、2492、2494、2496、2500、2502、2504、2506、2508、2510、2512、2514、2516、2518、2520、2522、2524、2526、2528、2530、2532、2534、2536、2538、2540或2777-2791。
4.一种分离的核酸分子,其包含编码如权利要求1至3中任一项所述的IL-10突变蛋白的核苷酸序列。
5.一种分离的抗原结合蛋白,其中该抗原结合蛋白:
a.是抗体或抗体片段;
b.与具有SEQ ID NO:20中列出的氨基酸序列的人TREM-1结合;
c.包含轻链可变结构域,该轻链可变结构域包含:
i.轻链CDR1,其包含选自SEQ ID NO:30、50、70、90、110、130、150、170、190、210、230、250、270、290和2190的氨基酸序列;
ii.轻链CDR2,其包含选自SEQ ID NO:31、51、71、91、111、131、151、171、191、211、231、251、271、291和2191的氨基酸序列;
iii.轻链CDR3,其包含选自SEQ ID NO:32、52、72、92、112、132、152、172、192、212、232、252、272、292和2192的氨基酸序列;并且
d.包含重链可变结构域,该重链可变结构域包含:
i.重链CDR1,其包含选自SEQ ID NO:36、56、76、96、116、136、156、176、196、216、236、256、276、296和2196的氨基酸序列;
ii.重链CDR2,其包含选自SEQ ID NO:37、57、77、97、117、137、157、177、197、217、237、257、277、297和2197的氨基酸序列;和
iii.重链CDR3,其包含选自SEQ ID NO:38、58、78、98、118、138、158、178、198、218、238、258、278、298和2198的氨基酸序列。
6.如权利要求5所述的抗原结合蛋白,其中该抗原结合蛋白包含选自以下的一组CDR氨基酸序列:
i)SEQ ID NO:30(LCDR1)、SEQ ID NO:31(LCDR2)、SEQ ID NO:32(LCDR3)、SEQ ID NO:36(HCDR1)、SEQ ID NO:37(HCDR2)和SEQ ID NO:38(HCDR3);
ii)SEQ ID NO:50(LCDR1)、SEQ ID NO:51(LCDR2)、SEQ ID NO:52(LCDR3)、SEQ ID NO:56(HCDR1)、SEQ ID NO:57(HCDR2)和SEQ ID NO:58(HCDR3);
iii)SEQ ID NO:70(LCDR1)、SEQ ID NO:71(LCDR2)、SEQ ID NO:72(LCDR3)、SEQ IDNO:76(HCDR1)、SEQ ID NO:77(HCDR2)和SEQ ID NO:78(HCDR3);
iv)SEQ ID NO:90(LCDR1)、SEQ ID NO:91(LCDR2)、SEQ ID NO:92(LCDR3)、SEQ ID NO:96(HCDR1)、SEQ ID NO:97(HCDR2)和SEQ ID NO:98(HCDR3);
v)SEQ ID NO:110(LCDR1)、SEQ ID NO:111(LCDR2)、SEQ ID NO:112(LCDR3)、SEQ IDNO:116(HCDR1)、SEQ ID NO:117(HCDR2)和SEQ ID NO:118(HCDR3);
vi)SEQ ID NO:130(LCDR1)、SEQ ID NO:131(LCDR2)、SEQ ID NO:132(LCDR3)、SEQ IDNO:136(HCDR1)、SEQ ID NO:137(HCDR2)和SEQ ID NO:138(HCDR3);
vii)SEQ ID NO:150(LCDR1)、SEQ ID NO:151(LCDR2)、SEQ ID NO:152(LCDR3)、SEQ IDNO:156(HCDR1)、SEQ ID NO:157(HCDR2)和SEQ ID NO:158(HCDR3);
viii)SEQ ID NO:170(LCDR1)、SEQ ID NO:171(LCDR2)、SEQ ID NO:172(LCDR3)、SEQID NO:176(HCDR1)、SEQ ID NO:177(HCDR2)和SEQ ID NO:178(HCDR3);
ix)SEQ ID NO:190(LCDR1)、SEQ ID NO:191(LCDR2)、SEQ ID NO:192(LCDR3)、SEQ IDNO:196(HCDR1)、SEQ ID NO:197(HCDR2)和SEQ ID NO:198(HCDR3);
x)SEQ ID NO:210(LCDR1)、SEQ ID NO:211(LCDR2)、SEQ ID NO:212(LCDR3)、SEQ IDNO:216(HCDR1)、SEQ ID NO:217(HCDR2)和SEQ ID NO:218(HCDR3);
xi)SEQ ID NO:230(LCDR1)、SEQ ID NO:231(LCDR2)、SEQ ID NO:232(LCDR3)、SEQ IDNO:236(HCDR1)、SEQ ID NO:237(HCDR2)和SEQ ID NO:238(HCDR3);
xii)SEQ ID NO:250(LCDR1)、SEQ ID NO:251(LCDR2)、SEQ ID NO:252(LCDR3)、SEQ IDNO:256(HCDR1)、SEQ ID NO:257(HCDR2)和SEQ ID NO:258(HCDR3);
xiii)SEQ ID NO:270(LCDR1)、SEQ ID NO:271(LCDR2)、SEQ ID NO:272(LCDR3)、SEQID NO:276(HCDR1)、SEQ ID NO:277(HCDR2)和SEQ ID NO:278(HCDR3);
xiv)SEQ ID NO:290(LCDR1)、SEQ ID NO:291(LCDR2)、SEQ ID NO:292(LCDR3)、SEQ IDNO:296(HCDR1)、SEQ ID NO:297(HCDR2)和SEQ ID NO:298(HCDR3);或
xv)SEQ ID NO:2190(LCDR1)、SEQ ID NO:2191(LCDR2)、SEQ ID NO:2192(LCDR3)、SEQID NO:2196(HCDR1)、SEQ ID NO:2197(HCDR2)和SEQ ID NO:2198(HCDR3)。
7.如权利要求5或6所述的抗原结合蛋白,该抗原结合蛋白包含:
a.轻链可变结构域,其包含选自下组的氨基酸序列,该组由以下组成:
i.与选自SEQ ID NO:41、61、81、101、121、141、161、181、201、221、241、261、281、301和2185的氨基酸序列具有至少80%同一性的序列;
ii.由多核苷酸序列编码的与选自SEQ ID NO:41、61、81、101、121、141、161、181、201、221、241、261、281、301和2185的氨基酸序列具有至少80%同一性的序列;或
iii.由在中等严格条件下与由选自SEQ ID NO:39、59、79、99、119、139、159、179、199、219、239、259、279、299和2183的核酸序列组成的多核苷酸的互补序列杂交的多核苷酸编码的序列;和
b.重链可变结构域,其包含选自下组的氨基酸序列,该组由以下组成:
i.与选自SEQ ID NO:42、62、82、102、122、142、162、182、202、222、242、262、282、302和2186的氨基酸序列具有至少80%同一性的序列;
ii.由多核苷酸序列编码的与选自SEQ ID NO:42、62、82、102、122、142、162、182、202、222、242、262、282、302和2186的氨基酸序列具有至少80%同一性的序列;或者
iii.由在中等严格条件下与由选自SEQ ID NO:40、60、80、100、120、140、160、180、200、220、240、260、280、300和2184的核酸序列组成的多核苷酸的互补序列杂交的多核苷酸编码的序列。
8.如权利要求5至7中任一项所述的抗原结合蛋白,其中该抗原结合蛋白包含:
i)与SEQ ID NO:41中列出的轻链可变结构域具有至少90%同一性的氨基酸序列,和与SEQ ID NO:42中列出的重链可变结构域具有至少90%同一性的氨基酸序列;
ii)与SEQ ID NO:61中列出的轻链可变结构域具有至少90%同一性的氨基酸序列,和与SEQ ID NO:62中列出的重链可变结构域具有至少90%同一性的氨基酸序列;
iii)与SEQ ID NO:81中列出的轻链可变结构域具有至少90%同一性的氨基酸序列,和与SEQ ID NO:82中列出的重链可变结构域具有至少90%同一性的氨基酸序列;
iv)与SEQ ID NO:101中列出的轻链可变结构域具有至少90%同一性的氨基酸序列,和与SEQ ID NO:102中列出的重链可变结构域具有至少90%同一性的氨基酸序列;
v)与SEQ ID NO:121中列出的轻链可变结构域具有至少90%同一性的氨基酸序列,和与SEQ ID NO:122中列出的重链可变结构域具有至少90%同一性的氨基酸序列;
vi)与SEQ ID NO:141中列出的轻链可变结构域具有至少90%同一性的氨基酸序列,和与SEQ ID NO:142中列出的重链可变结构域具有至少90%同一性的氨基酸序列;
vii)与SEQ ID NO:161中列出的轻链可变结构域具有至少90%同一性的氨基酸序列,和与SEQ ID NO:162中列出的重链可变结构域具有至少90%同一性的氨基酸序列;
viii)与SEQ ID NO:181中列出的轻链可变结构域具有至少90%同一性的氨基酸序列,和与SEQ ID NO:182中列出的重链可变结构域具有至少90%同一性的氨基酸序列;
ix)与SEQ ID NO:201中列出的轻链可变结构域具有至少90%同一性的氨基酸序列,和与SEQ ID NO:202中列出的重链可变结构域具有至少90%同一性的氨基酸序列;
x)与SEQ ID NO:221中列出的轻链可变结构域具有至少90%同一性的氨基酸序列,和与SEQ ID NO:222中列出的重链可变结构域具有至少90%同一性的氨基酸序列;
xi)与SEQ ID NO:241中列出的轻链可变结构域具有至少90%同一性的氨基酸序列,和与SEQ ID NO:242中列出的重链可变结构域具有至少90%同一性的氨基酸序列;
xii)与SEQ ID NO:261中列出的轻链可变结构域具有至少90%同一性的氨基酸序列,和与SEQ ID NO:262中列出的重链可变结构域具有至少90%同一性的氨基酸序列;
xiii)与SEQ ID NO:281中列出的轻链可变结构域具有至少90%同一性的氨基酸序列,和与SEQ ID NO:282中列出的重链可变结构域具有至少90%同一性的氨基酸序列;
xiv)与SEQ ID NO:301中列出的轻链可变结构域具有至少90%同一性的氨基酸序列,和与SEQ ID NO:302中列出的重链可变结构域具有至少90%同一性的氨基酸序列;或者
xv)与SEQ ID NO:2185中列出的轻链可变结构域具有至少90%同一性的氨基酸序列,和与SEQ ID NO:2186中列出的重链可变结构域具有至少90%同一性的氨基酸序列。
9.一种分离的核酸分子,其包含编码如权利要求5至8中任一项所述的重链、如权利要求5至8中任一项所述的重链、或两者的核苷酸序列。
10.一种抗原结合蛋白,其包含抗原结合部分和一个或两个IL-10部分,其中:
a.该抗原结合部分是抗体或抗体片段,
b.每个IL-10部分独立地是单价或二价,
c.每个IL-10部分独立地选自具有与SEQ ID NO:2具有90%同一性的序列的一种或多种人IL-10突变蛋白,并且
d.至少一个IL-10部分与该抗原结合部分共价结合。
11.一种抗原结合蛋白,其包含:
(a)具有式A-L-M或M-L-A的多肽序列,其中
i)A是与SEQ ID NO:20中列出的TREM-1蛋白结合的IgG抗体的免疫球蛋白重链,
ii)L是包含4至20个氨基酸的接头肽,并且
iii)M是与SEQ ID NO:2中列出的wt IL-10具有至少90%序列同一性的IL-10突变蛋白;和
(b)结合SEQ ID NO:20中列出的TREM-1蛋白的IgG抗体的免疫球蛋白轻链,
其中(a)的免疫球蛋白重链和(b)的免疫球蛋白轻链形成结合TREM-1的IgG抗体部分,其中该蛋白质包含(a)的多肽的一个或两个分子以及(b)的轻链的一个或两个分子,任选地其中(a)的仅1个多肽包含M部分。
12.如权利要求10或11所述的抗原结合蛋白,其中:
a.每个IL-10部分包含与SEQ ID NO:2中列出的氨基酸序列具有至少90%同一性的氨基酸序列,并且
b.每个IL-10部分独立地包含选自以下的至少一个突变:螺旋环AB、螺旋环CD、螺旋环DE、螺旋A、螺旋B、螺旋C、螺旋D、螺旋E和/或螺旋F中的突变。
13.如权利要求10至12中任一项所述的抗原结合蛋白,其中每个IL-10部分独立地包含:
i)SEQ ID NO:2的残基N10、H14、F15、P20、M22、L23、R24、R27、D28、K34、T35、Q38、M39、K40、D41、Q42、L43、D44、N45、L46、L47、L48、K49、F56、K57、Y59、L60、Q63、E67、Q70、M77、Q79、N82、Q83、D84、P85、D86、I87、A89、H90、S93、T100、L103、H109、R110、L112、E115、N116、A127、K130、I136、Y137、K138、S141、E142、D144、I145、E151、M154、M156、K157、或N160中的一个或多个中的突变,或在螺旋D和螺旋E之间添加4-8个氨基酸;和/或
ii)选自下组的一个或多个突变,该组由以下组成:SEQ ID NO:2的N10Q、N10I、N10K、R27L、K34D、D41G、L46K、Q38E、Q38R、Q38D、K138L、K138D、I87A、H14Q、F15Y、M22V、K49T、K49S、F56Y、K57N、Y59T、L60Q、Q63E、Q63L、E67C、Q70E、Q70K、M77R、M77V、Q79R、Q79C、D84R、A89P、H90E、H90Q、S93E、S93Q、T100R、L103E、H109D、R110P、R110Q、L112V、E115K、N116D、N110Q、A127M、K130Q、I136C、Y137C、M154V、M156C、K157N、或N160D,任选地包含在螺旋D和螺旋E之间添加六个氨基酸。
14.如权利要求10至13中任一项所述的抗原结合蛋白,其中该IL-10部分具有以下中任一个中列出的氨基酸序列:SEQ ID NO:3-10或SEQ ID NO:2138、2140、2142、2144、2146、2148、2150、2152、2154、2156、2158、2160、2162、2164、2166、2168、2170、2172、2174、2176、2178、2180、2182、2360、2362、2364、2366、2368、2370、2372、2374、2376、2378、2380、2382、2384、2386、2388、2390、2392、2394、2396、2398、2400、2402、2404、2406、2408、2410、2412、2414、2416、2418、2420、2422、2424、2426、2428、2430、2432、2434、2436、2438、2440、2442、2444、2446、2448、2450、2452、2454、2456、2458、2460、2462、2464、2466、2468、2470、2472、2474、2476、2478、2480、2482、2484、2486、2488、2490、2492、2494、2496、2500、2502、2504、2506、2508、2510、2512、2514、2516、2518、2520、2522、2524、2526、2528、2530、2532、2534、2536、2538、2540或2777-2791。
15.如权利要求10至14中任一项所述的抗原结合蛋白,该抗原结合蛋白具有以下中任一个中列出的重链氨基酸序列:SEQ ID NO:863、865、867、869、871、873、875、877、879、881、883、885、887、889、891、893、895、897、899、901、903、905、907、909、911、913、915、917、919、921、923、925、927、929、931、933、935、937、939、941、943、945、947、949、951、953、955、957、959、961、963、965、967、969、971、973、975、977、979、981、983、985、987、989、991、993、995、997、999、1001、1003、1005、1007、1009、1011、1013、1015、1017、1019、1021、1023、1025、1027、1029、1031、1033、1035、1037、1039、1041、1043、1045、1047、1049、1051、1053、1055、1057、1059、1061、1063、1065、1067、1069、1071、1073、1075、1077、1079、1081、1083、和1085。
16.如权利要求10至15中任一项所述的抗原结合蛋白,该抗原结合蛋白具有以下中任一个中列出的轻链氨基酸序列:SEQ ID NO:864、866、868、870、872、874、876、878、880、882、884、886、888、890、892、894、896、898、900、902、904、906、908、910、912、914、916、918、920、922、924、926、928、930、932、934、936、938、940、942、944、946、948、950、952、954、956、958、960、962、964、966、968、970、972、974、976、978、980、982、984、986、988、990、992、994、996、998、1000、1002、1004、1006、1008、1010、1012、1014、1016、1018、1020、1022、1024、1026、1028、1030、1032、1034、1036、1038、1040、1042、1044、1046、1048、1050、1052、1054、1056、1058、1060、1062、1064、1066、1068、1070、1072、1074、1076、1078、1080、1082、1084、和1086。
17.如权利要求10至16中任一项所述的抗原结合蛋白,该抗原结合蛋白具有以下中任一个中列出的重链氨基酸序列:SEQ ID NO:863、865、867、869、871、873、875、877、879、881、883、885、887、889、891、893、895、897、899、901、903、905、907、909、911、913、915、917、919、921、923、925、927、929、931、933、935、937、939、941、943、945、947、949、951、953、955、957、959、961、963、965、967、969、971、973、975、977、979、981、983、985、987、989、991、993、995、997、999、1001、1003、1005、1007、1009、1011、1013、1015、1017、1019、1021、1023、1025、1027、1029、1031、1033、1035、1037、1039、1041、1043、1045、1047、1049、1051、1053、1055、1057、1059、1061、1063、1065、1067、1069、1071、1073、1075、1077、1079、1081、1083、和1085,以及以下中列出的相应的轻链氨基酸序列:SEQ ID NO:864、866、868、870、872、874、876、878、880、882、884、886、888、890、892、894、896、898、900、902、904、906、908、910、912、914、916、918、920、922、924、926、928、930、932、934、936、938、940、942、944、946、948、950、952、954、956、958、960、962、964、966、968、970、972、974、976、978、980、982、984、986、988、990、992、994、996、998、1000、1002、1004、1006、1008、1010、1012、1014、1016、1018、1020、1022、1024、1026、1028、1030、1032、1034、1036、1038、1040、1042、1044、1046、1048、1050、1052、1054、1056、1058、1060、1062、1064、1066、1068、1070、1072、1074、1076、1078、1080、1082、1084、和1086。
18.如权利要求10至14中任一项所述的抗原结合蛋白,该抗原结合蛋白具有以下中任一个中列出的重链氨基酸序列:SEQ ID NO:1883、1885、1887、1889、1891、1893、1895、1897、1899、1901、1903、1905、1907、1909、1911、1913、1915、1917、1919、1921、1923、1925、1927、1929、1931、1933、1935、1937、1939、1941、1943、1945、1947、1949、1951、1953、1955、1957、1959、1961、1963、1965、1967、1969、1971、1973、1975、1977、1979、1981、1983、1985、1987、1989、1991、1993、1995、1997、1999、2001、2003、2005、和2007。
19.如权利要求10至14或18中任一项所述的抗原结合蛋白,该抗原结合蛋白具有以下中任一个中列出的轻链氨基酸序列:SEQ IDNO:2543、2544、2545、2546、2547、2548、2549、2550、2551、2552、2553、2554、2555、2556、2557、2558、2559、2560、2561、2562、2563、2564、2565、2566、2567、2568、2569、2570、2571、2572、2573、2574、2575、2576、2577、2578、2579、2580、2581、2582、2583、2584、2585、2586、2587、2588、2589、2590、2591、2592、2593、2594、2595、2596、2597、2598、2599、2600、2601、2602、2603、2604、2605。
20.如权利要求10至14或18至19中任一项所述的抗原结合蛋白,该抗原结合蛋白具有以下中任一个中列出的重链氨基酸序列:SEQ ID NO:1883、1885、1887、1889、1891、1893、1895、1897、1899、1901、1903、1905、1907、1909、1911、1913、1915、1917、1919、1921、1923、1925、1927、1929、1931、1933、1935、1937、1939、1941、1943、1945、1947、1949、1951、1953、1955、1957、1959、1961、1963、1965、1967、1969、1971、1973、1975、1977、1979、1981、1983、1985、1987、1989、1991、1993、1995、1997、1999、2001、2003、2005、和2007,以及以下中列出的相应的轻链氨基酸序列:SEQ ID NO:2543、2544、2545、2546、2547、2548、2549、2550、2551、2552、2553、2554、2555、2556、2557、2558、2559、2560、2561、2562、2563、2564、2565、2566、2567、2568、2569、2570、2571、2572、2573、2574、2575、2576、2577、2578、2579、2580、2581、2582、2583、2584、2585、2586、2587、2588、2589、2590、2591、2592、2593、2594、2595、2596、2597、2598、2599、2600、2601、2602、2603、2604、2605。
21.如权利要求10至14中任一项所述的抗原结合蛋白,该抗原结合蛋白具有以下中任一个中列出的重链氨基酸序列:SEQ ID NO:2011、2013、2015、2017、2019、2021、2026、2025、2027、2029、2031、2033、2035、2037、2039、2041、2043、2045、2047、2049、2051、2053、2055、2057、2059、2061、2063、2065、2067、2069、2071、2073、2075、2077、2079、2081、2083、2085、2087、2089、2091、2093、2095、2097、2099、2101、2103、2105、2107、2109、2111、2113、2115、2117、2119、2121、2123、2125、2127、2129、2131、2133、和2135。
22.如权利要求10至14或21中任一项所述的抗原结合蛋白,该抗原结合蛋白具有以下中任一个中列出的轻链氨基酸序列:SEQ IDNO:2233、2235、2237、2239、2241、2243、2245、2247、2249、2251、2253、2255、2257、2259、2261、2263、2265、2267、2269、2271、2273、2275、2277、2279、2281、2283、2285、2287、2289、2291、2293、2295、2297、2299、2301、2303、2305、2307、2309、2311、2313、2315、2317、2319、2321、2323、2325、2327、2329、2331、2333、2335、2337、2339、2341、2343、2345、2347、2349、2351、2353、2355、和2357。
23.如权利要求10至14或21至22中任一项所述的抗原结合蛋白,该抗原结合蛋白具有以下中任一个中列出的重链氨基酸序列:SEQ ID NO:2011、2013、2015、2017、2019、2021、2026、2025、2027、2029、2031、2033、2035、2037、2039、2041、2043、2045、2047、2049、2051、2053、2055、2057、2059、2061、2063、2065、2067、2069、2071、2073、2075、2077、2079、2081、2083、2085、2087、2089、2091、2093、2095、2097、2099、2101、2103、2105、2107、2109、2111、2113、2115、2117、2119、2121、2123、2125、2127、2129、2131、2133、和2135,以及以下中列出的相应的轻链氨基酸序列:SEQ ID NO:2233、2235、2237、2239、2241、2243、2245、2247、2249、2251、2253、2255、2257、2259、2261、2263、2265、2267、2269、2271、2273、2275、2277、2279、2281、2283、2285、2287、2289、2291、2293、2295、2297、2299、2301、2303、2305、2307、2309、2311、2313、2315、2317、2319、2321、2323、2325、2327、2329、2331、2333、2335、2337、2339、2341、2343、2345、2347、2349、2351、2353、2355、和2357。
24.如权利要求10至23中任一项所述的抗原结合蛋白,其中该抗原结合部分是包含以下的抗TREM-1抗原结合部分:
a.轻链可变结构域,该轻链可变结构域包含:
i.轻链CDR1序列,其包含选自SEQ ID NO:30、50、70、90、110、130、150、170、190、210、230、250、270、290和2190的氨基酸序列;
ii.轻链CDR2序列,其包含选自SEQ ID NO:31、51、71、91、111、131、151、171、191、211、231、251、271、291和2190的氨基酸序列;
iii.轻链CDR3序列,其包含选自SEQ ID NO:32、52、72、92、112、132、152、172、192、212、232、252、272、292和2192的氨基酸序列;和
b.重链可变结构域,该重链可变结构域包含:
i.重链CDR1序列,其包含选自SEQ ID NO:36、56、76、96、116、136、156、176、196、216、236、256、276、296和2196的氨基酸序列;
ii.重链CDR2序列,其包含选自SEQ ID NO:37、57、77、97、117、137、157、177、197、217、237、257、277、297和2197的氨基酸序列;和
iii.重链CDR3序列,其包含选自SEQ ID NO:38、58、78、98、118、138、158、178、198、218、238、258、278、298和2198的氨基酸序列。
25.如权利要求10至24中任一项所述的抗原结合蛋白,其中该抗原结合部分是包含选自以下的一组CDR氨基酸序列的抗TREM-1抗原结合部分:
i)SEQ ID NO:30(LCDR1)、SEQ ID NO:31(LCDR2)、SEQ ID NO:32(LCDR3)、SEQ ID NO:36(HCDR1)、SEQ ID NO:37(HCDR2)和SEQ ID NO:38(HCDR3);
ii)SEQ ID NO:50(LCDR1)、SEQ ID NO:51(LCDR2)、SEQ ID NO:52(LCDR3)、SEQ ID NO:56(HCDR1)、SEQ ID NO:57(HCDR2)和SEQ ID NO:58(HCDR3);
iii)SEQ ID NO:70(LCDR1)、SEQ ID NO:71(LCDR2)、SEQ ID NO:72(LCDR3)、SEQ IDNO:76(HCDR1)、SEQ ID NO:77(HCDR2)和SEQ ID NO:78(HCDR3);
iv)SEQ ID NO:90(LCDR1)、SEQ ID NO:91(LCDR2)、SEQ ID NO:92(LCDR3)、SEQ ID NO:96(HCDR1)、SEQ ID NO:97(HCDR2)和SEQ ID NO:98(HCDR3);
v)SEQ ID NO:110(LCDR1)、SEQ ID NO:111(LCDR2)、SEQ ID NO:112(LCDR3)、SEQ IDNO:116(HCDR1)、SEQ ID NO:117(HCDR2)和SEQ ID NO:118(HCDR3);
vi)SEQ ID NO:130(LCDR1)、SEQ ID NO:131(LCDR2)、SEQ ID NO:132(LCDR3)、SEQ IDNO:136(HCDR1)、SEQ ID NO:137(HCDR2)和SEQ ID NO:138(HCDR3);
vii)SEQ ID NO:150(LCDR1)、SEQ ID NO:151(LCDR2)、SEQ ID NO:152(LCDR3)、SEQ IDNO:156(HCDR1)、SEQ ID NO:157(HCDR2)和SEQ ID NO:158(HCDR3);
viii)SEQ ID NO:170(LCDR1)、SEQ ID NO:171(LCDR2)、SEQ ID NO:172(LCDR3)、SEQID NO:176(HCDR1)、SEQ ID NO:177(HCDR2)和SEQ ID NO:178(HCDR3);
ix)SEQ ID NO:190(LCDR1)、SEQ ID NO:191(LCDR2)、SEQ ID NO:192(LCDR3)、SEQ IDNO:196(HCDR1)、SEQ ID NO:197(HCDR2)和SEQ ID NO:198(HCDR3);
x)SEQ ID NO:210(LCDR1)、SEQ ID NO:211(LCDR2)、SEQ ID NO:212(LCDR3)、SEQ IDNO:216(HCDR1)、SEQ ID NO:217(HCDR2)和SEQ ID NO:218(HCDR3);
xi)SEQ ID NO:230(LCDR1)、SEQ ID NO:231(LCDR2)、SEQ ID NO:232(LCDR3)、SEQ IDNO:236(HCDR1)、SEQ ID NO:237(HCDR2)和SEQ ID NO:238(HCDR3);
xii)SEQ ID NO:250(LCDR1)、SEQ ID NO:251(LCDR2)、SEQ ID NO:252(LCDR3)、SEQ IDNO:256(HCDR1)、SEQ ID NO:257(HCDR2)和SEQ ID NO:258(HCDR3);
xiii)SEQ ID NO:270(LCDR1)、SEQ ID NO:271(LCDR2)、SEQ ID NO:272(LCDR3)、SEQID NO:276(HCDR1)、SEQ ID NO:277(HCDR2)和SEQ ID NO:278(HCDR3);
xiv)SEQ ID NO:290(LCDR1)、SEQ ID NO:291(LCDR2)、SEQ ID NO:292(LCDR3)、SEQ IDNO:296(HCDR1)、SEQ ID NO:297(HCDR2)和SEQ ID NO:298(HCDR3);或
xv)SEQ ID NO:2190(LCDR1)、SEQ ID NO:2191(LCDR2)、SEQ ID NO:2192(LCDR3)、SEQID NO:2196(HCDR1)、SEQ IDNO:2197(HCDR2)和SEQ ID NO:2198(HCDR3)。
26.如权利要求10至25中任一项所述的抗原结合蛋白,其中该抗TREM-1抗原结合部分包含:
a.轻链可变结构域,其包含选自下组的氨基酸序列,该组由以下组成:
i.与选自SEQ ID NO:41、61、81、101、121、141、161、181、201、221、241、261、281、301和2185的氨基酸序列具有至少80%同一性的序列;
ii.由多核苷酸序列编码的与选自SEQ ID NO:41、61、81、101、121、141、161、181、201、221、241、261、281、301和2185的氨基酸序列具有至少80%同一性的序列;
iii.由在中等严格条件下与由选自SEQ ID NO:39、59、79、99、119、139、159、179、199、219、239、259、279、299和2183的核酸序列组成的多核苷酸的互补序列杂交的多核苷酸编码的序列;和
b.重链可变结构域,其包含选自下组的氨基酸序列,该组由以下组成:
i.与选自SEQ ID NO:42、62、82、102、122、142、162、182、202、222、242、262、282、302和2186的氨基酸序列具有至少80%同一性的序列;
ii.由多核苷酸序列编码的与选自SEQ ID NO:42、62、82、102、122、142、162、182、202、222、242、262、282、302和2186的氨基酸序列具有至少80%同一性的序列;
iii.由在中等严格条件下与由选自SEQ ID NO:40、60、80、100、120、140、160、180、200、220、240、260、280、300和2184的核酸序列组成的多核苷酸的互补序列杂交的多核苷酸编码的序列。
27.如权利要求10至26中任一项所述的抗原结合蛋白,其中该抗原结合部分是包含以下的抗TREM-1抗原结合部分:
i)与SEQ ID NO:41中列出的轻链可变结构域具有至少90%同一性的氨基酸序列,和与SEQ ID NO:42中列出的重链可变结构域具有至少90%同一性的氨基酸序列;
ii)与SEQ ID NO:61中列出的轻链可变结构域具有至少90%同一性的氨基酸序列,和与SEQ ID NO:62中列出的重链可变结构域具有至少90%同一性的氨基酸序列;
iii)与SEQ ID NO:81中列出的轻链可变结构域具有至少90%同一性的氨基酸序列,和与SEQ ID NO:82中列出的重链可变结构域具有至少90%同一性的氨基酸序列;
iv)与SEQ ID NO:101中列出的轻链可变结构域具有至少90%同一性的氨基酸序列,和与SEQ ID NO:102中列出的重链可变结构域具有至少90%同一性的氨基酸序列;
v)与SEQ ID NO:121中列出的轻链可变结构域具有至少90%同一性的氨基酸序列,和与SEQ ID NO:122中列出的重链可变结构域具有至少90%同一性的氨基酸序列;
vi)与SEQ ID NO:141中列出的轻链可变结构域具有至少90%同一性的氨基酸序列,和与SEQ ID NO:142中列出的重链可变结构域具有至少90%同一性的氨基酸序列;
vii)与SEQ ID NO:161中列出的轻链可变结构域具有至少90%同一性的氨基酸序列,和与SEQ ID NO:162中列出的重链可变结构域具有至少90%同一性的氨基酸序列;
viii)与SEQ ID NO:181中列出的轻链可变结构域具有至少90%同一性的氨基酸序列,和与SEQ ID NO:182中列出的重链可变结构域具有至少90%同一性的氨基酸序列;
ix)与SEQ ID NO:201中列出的轻链可变结构域具有至少90%同一性的氨基酸序列,和与SEQ ID NO:202中列出的重链可变结构域具有至少90%同一性的氨基酸序列;
x)与SEQ ID NO:221中列出的轻链可变结构域具有至少90%同一性的氨基酸序列,和与SEQ ID NO:222中列出的重链可变结构域具有至少90%同一性的氨基酸序列;
xi)与SEQ ID NO:241中列出的轻链可变结构域具有至少90%同一性的氨基酸序列,和与SEQ ID NO:242中列出的重链可变结构域具有至少90%同一性的氨基酸序列;
xii)与SEQ ID NO:261中列出的轻链可变结构域具有至少90%同一性的氨基酸序列,和与SEQ ID NO:262中列出的重链可变结构域具有至少90%同一性的氨基酸序列;
xiii)与SEQ ID NO:281中列出的轻链可变结构域具有至少90%同一性的氨基酸序列,和与SEQ ID NO:282中列出的重链可变结构域具有至少90%同一性的氨基酸序列;
xiv)与SEQ ID NO:301中列出的轻链可变结构域具有至少90%同一性的氨基酸序列,和与SEQ ID NO:302中列出的重链可变结构域具有至少90%同一性的氨基酸序列;或者
xv)与SEQ ID NO:2185中列出的轻链可变结构域具有至少90%同一性的氨基酸序列,和与SEQ ID NO:2186中列出的重链可变结构域具有至少90%同一性的氨基酸序列。
28.如权利要求24至27中任一项所述的抗原结合蛋白,其中:
a.该抗原结合蛋白包含两条轻链和两条重链:
b.每条重链包含在该重链的C末端处附接的IL-10部分;
c.每个重链-IL-10部分抗原结合蛋白包含与选自以下的序列具有至少90%同一性的氨基酸序列:SEQ ID NO:863、865、867、869、871、873、875、877、879、881、883、885、887、889、891、893、895、897、899、901、903、905、907、909、911、913、915、917、919、921、923、925、927、929、931、933、935、937、939、941、943、945、947、949、951、953、955、957、959、961、963、965、967、969、971、973、975、977、979、981、983、985、987、989、991、993、995、997、999、1001、1003、1005、1007、1009、1011、1013、1015、1017、1019、1021、1023、1025、1027、1029、1031、1033、1035、1037、1039、1041、1043、1045、1047、1049、1051、1053、1055、1057、1059、1061、1063、1065、1067、1069、1071、1073、1075、1077、1079、1081、1083、和1085;并且
d.每个轻链-IL-10部分包含与选自以下的序列具有至少90%同一性的氨基酸序列:SEQ ID NO:864、866、868、870、872、874、876、878、880、882、884、886、888、890、892、894、896、898、900、902、904、906、908、910、912、914、916、918、920、922、924、926、928、930、932、934、936、938、940、942、944、946、948、950、952、954、956、958、960、962、964、966、968、970、972、974、976、978、980、982、984、986、988、990、992、994、996、998、1000、1002、1004、1006、1008、1010、1012、1014、1016、1018、1020、1022、1024、1026、1028、1030、1032、1034、1036、1038、1040、1042、1044、1046、1048、1050、1052、1054、1056、1058、1060、1062、1064、1066、1068、1070、1072、1074、1076、1078、1080、1082、1084、和1086。
29.如权利要求10至14或24至27中任一项所述的抗原结合蛋白,其中该抗原结合蛋白具有选自下组的重链-IL-10部分氨基酸序列,该组由以下组成:SEQ ID NO:2137、2139、2141、2143、2145、2147、2149、2151、2153、2155、2157、2159、2161、2163、2165、2167、2169、2171、2173、2175、2177、2179、2181、2359、2361、2363、2365、2367、2369、2371、2373、2375、2377、2379、2381、2383、2385、2387、2389、2391、2393、2395、2397、2399、2401、2403、2405、2407、2409、2411、2143、2415、2417、2419、2421、2423、2425、2427、2429、2431、2433、2435、2437、2439、2441、2443、2445、2447、2449、2451、2453、2455、2457、2459、2461、2463、2465、2467、2469、2471、2473、2475、2477、2479、2481、2483、2485、2487、2489、2491、2493、2495、2497、2498、2499、2501、2503、2505、2507、2509、2511、2513、2515、2517、2519、2521、2523、2525、2527、2529、2531、2533、2535、2537、2539和2726-2776。
30.如权利要求10至14或24至28中任一项所述的抗原结合蛋白,其中该抗原结合蛋白具有选自由SEQ ID NO:2727-2732组成的组的重链-IL-10部分氨基酸序列。
31.如权利要求30所述的抗原结合蛋白,其包含SEQ ID NO:2727或2728的重链氨基酸序列,和SEQ ID NO:976或SEQ ID NO:2554中列出的轻链氨基酸序列。
32.如权利要求30所述的抗原结合蛋白,其包含SEQ ID NO:2729、2730、2731或2732的重链氨基酸序列,和SEQ ID NO:992或SEQ ID NO:2555中列出的轻链氨基酸序列。
33.一种抗原结合蛋白,其包含抗原结合部分和一个或两个IL-10部分,其中:
a.该抗原结合部分是抗体或抗体片段;
b.每个IL-10部分独立地是单价或二价;
c.每个IL-10部分独立地选自具有与SEQ ID NO:2具有90%同一性的序列的一种或多种人IL-10突变蛋白;
d.至少一个IL-10部分与该抗原结合部分共价结合,和/或
e.该抗原结合部分与如权利要求24至27中任一项所述的抗原结合部分竞争与人TREM-1蛋白结合。
34.一种分离的核酸分子,其包含编码如权利要求10-33中任一项所述的抗原结合蛋白的重链区、如权利要求10-33中任一项所述的抗原结合蛋白的轻链区、或两者的核苷酸序列。
35.一种治疗有需要的受试者的炎性疾病的方法,该方法包括施用
i)如权利要求1-3中任一项所述的IL-10突变蛋白;
ii)如权利要求5-8中任一项所述的抗TREM-1抗原结合蛋白;或
iii)如权利要求10-33中任一项所述的抗原结合蛋白。
36.如权利要求35所述的方法,其中该炎性疾病选自由以下组成的组:炎性肠病、溃疡性结肠炎、克罗恩病、肠易激综合征、类风湿性关节炎、银屑病、银屑病关节炎、和细胞因子释放综合征(CRS)。
37.一种用于在治疗炎性疾病中使用的组合物,该组合物包含
i)如权利要求1-3中任一项所述的IL-10突变蛋白;
ii)如权利要求5-8中任一项所述的抗TREM-1抗原结合蛋白;或
iii)如权利要求10-33中任一项所述的抗原结合蛋白。
38.包含如权利要求1-3中任一项所述的IL-10突变蛋白的组合物在制备用于治疗炎性疾病的药物中的用途。
39.组合物在制备用于治疗炎性疾病的药物中的用途,该组合物包含:
i)如权利要求1-3中任一项所述的IL-10突变蛋白;
ii)如权利要求5-8中任一项所述的抗TREM-1抗原结合蛋白;或
iii)如权利要求10-33中任一项所述的抗原结合蛋白。
40.包含与如权利要求1-3中任一项所述的抗IL-10突变蛋白组合的如权利要求5-8和10-33中任一项所述的抗TREM-1抗体或抗原结合片段的组合物在制备用于治疗炎性疾病的药物中的用途。
41.一种分离的抗原结合蛋白,其中该抗原结合蛋白:
a.是抗体或抗体片段;
b.与具有SEQ ID NO:20中列出的氨基酸序列的人TREM-1结合;
c.包含轻链可变结构域,该轻链可变结构域包含:
i.包含氨基酸序列X1ASQSX2X3X4NLA(SEQ ID NO:2199)的轻链CDR1,其中X1是R或Q,其中X2是V或I,其中X3是N或S,并且其中X4是S、H、I、V或A;
ii.包含氨基酸序列GAX1X2RAT(SEQ ID NO:2200)的轻链CDR2,其中X1是S或Y,并且其中X2是T或I;和
iii.包含氨基酸序列QX1X2X3X4X5X6PX7T(SEQ ID NO:2201)的轻链CDR3;其中X1是Q、H或E,其中X2是F或Y,其中X3是K、Y或I,其中X4是N、T、L、I、或M;其中X5是W、F、H或Y,其中X6不存在或是P;其中X7是W、N、Y、H或L;并且
d.包含重链可变结构域,该重链可变结构域包含:
i.包含氨基酸序列X1X2X3MX4(SEQ ID NO:2202)的重链CDR1,其中X1是A、R、T或S,其中X2是Y或N,其中X3是A或W,并且其中X4是S或N;
ii.包含氨基酸序列X1X2X3X4X5X6 X7 X8 X9YYX10X11X12VKG(SEQ ID NO:2205)的重链CDR2,其中X1是T、E、或S,其中X2不存在或是M、V、或I,其中X3是S、R或K,其中X4是G或Q,其中X5是S、D或H,其中X6是G、S、L、或A,其中X7是S、G、或R,其中X8是T、S、P或E,其中X9是T或I,其中X10是A或V,其中X11是D或E,并且其中X12是S或A;和
iii.包含氨基酸序列X1X2X3X4X5X6 X7 F X8YYX9(SEQ IDNO:2203)的重链CDR3,其中X1是V、E、A或G,其中X2是A、F、Y或G,其中X3是G、S、Y或W,其中X4是S或R,其中X5不存在或是N,其中X6是F、S、Y、或不存在,其中X7是L或F或不存在,其中X8是D或E,并且其中X9是Y、H或S。
42.如权利要求41所述的分离的抗原结合蛋白,其中该抗原结合蛋白包含:
a.轻链可变结构域,该轻链可变结构域包含:
i.包含氨基酸序列RASQSVNSNLA(SEQ ID NO:2212)的轻链CDR1;
ii.包含氨基酸序列GASTRAT(SEQ ID NO:2219)的轻链CDR2;
iii.包含氨基酸序列QQFKNWPPT(SEQ ID NO:2222)的轻链CDR3;和
b.重链可变结构域,该重链可变结构域包含:
i.包含氨基酸序列AYAMS(SEQ ID NO:2227)的重链CDR1;
ii.包含氨基酸序列TSGSGSTTYYADSVKG(SEQ ID NO:2230)的重链CDR2;和
iii.包含氨基酸序列VAGSNFLFDY(SEQ ID NO:2670)的重链CDR3。
43.一种分离的抗原结合蛋白,其中该抗原结合蛋白:
a.是抗体或抗体片段;
b.与具有SEQ ID NO:20中列出的氨基酸序列的人TREM-1结合;
c.包含轻链可变结构域,该轻链可变结构域包含:
i.包含氨基酸序列QASX1DIX2X3X4LN(SEQ ID NO:2204)的轻链CDR1,其中X1是R或Q,其中X2是R、S、N或F,其中X3是K或N,并且其中X4是H、Y或D;
ii.包含氨基酸序列X1X2X3X4LET(SEQ ID NO:2206)的轻链CDR2,其中X1是D、G或H,其中X2是A、V或T,其中X3是S、A或Y,并且其中X4是T或N;
iii.包含氨基酸序列QX1YX3X4X5PX6T(SEQ ID NO:2207)的轻链CDR3,其中X1是Q或H,其中X2是D、A或G,其中X3是N或K;其中X4是L或I,并且其中X5是I或L;并且
d.包含重链可变结构域,该重链可变结构域包含:
i.包含氨基酸序列X1YDIN(SEQ ID NO:2208)的重链CDR1,其中X1是R或S;
ii.包含氨基酸序列X1X2NPX3X4GX5X6GX7 X8X9X10FX11X12(SEQ ID NO:2209)的重链CDR2,其中X1是W或R,其中X2是M或L,其中X3是N、Q、或K,其中X4是S、A、或R,其中X5是N、或Q,其中X6是S、A、或T,其中X7是S、Q、或Y,其中X8是V或T,其中X9是Q或K,其中X10是K或N,其中X11是R或Q,并且其中X12是G或D;和
iii.包含氨基酸序列X1X2X3X4 X5X6 X7 X8X9X10X11X12FX13X14(SEQ ID NO:2210)的重链CDR3;其中X1是G、L或R,其中X2是G、I、或R,其中X3是Y、R、I、G、或A,其中X4是T、S、Y、或V,其中X5是S或Y,其中X6是S、A、I、或R,其中X7是W、A、或S,其中X8不存在或是S,其中X9不存在或是F、W、或Y,并且其中X10是R、S、H、K、或E,其中X11是W、H、Y、或F,其中X12是Y、V、A、或S,其中X13是D或Q,并且其中X14是L、Y、I、或H。
44.如权利要求43所述的抗原结合蛋白,其中该抗原结合蛋白包含:
a.轻链可变结构域,该轻链可变结构域包含:
i.包含氨基酸序列QASQDIRKHLN(SEQ ID NO:2213)的轻链CDR1;
ii.包含氨基酸序列DASNLET(SEQ ID NO:2220)的轻链CDR2;和
iii.包含氨基酸序列QHYDNLPIT(SEQ ID NO:2223)的轻链CDR3;和
b.重链可变结构域,该重链可变结构域包含:
i.包含氨基酸序列RYDIN(SEQ ID NO:2228)的重链CDR1;
ii.包含氨基酸序列WMNPNSGNSSVQKFRG(SEQ ID NO:2231)的重链CDR2;和
iii.包含氨基酸序列GGYTSSWRWYFDL(SEQ ID NO:2671)或GGYTSSWSRWYFDL(SEQ IDNO:2672)的重链CDR3。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US202063045041P | 2020-06-26 | 2020-06-26 | |
| US63/045041 | 2020-06-26 | ||
| US202063199218P | 2020-12-14 | 2020-12-14 | |
| US63/199218 | 2020-12-14 | ||
| PCT/US2021/039191 WO2021263167A2 (en) | 2020-06-26 | 2021-06-25 | Il-10 muteins and fusion proteins thereof |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN116209459A true CN116209459A (zh) | 2023-06-02 |
Family
ID=77071744
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202180051906.4A Pending CN116209459A (zh) | 2020-06-26 | 2021-06-25 | Il-10突变蛋白及其融合蛋白 |
Country Status (16)
| Country | Link |
|---|---|
| US (1) | US20230265145A1 (zh) |
| EP (1) | EP4172184A2 (zh) |
| JP (1) | JP2023531493A (zh) |
| KR (1) | KR20230027300A (zh) |
| CN (1) | CN116209459A (zh) |
| AU (1) | AU2021296917A1 (zh) |
| CA (1) | CA3187576A1 (zh) |
| CL (3) | CL2022003755A1 (zh) |
| CO (1) | CO2023000431A2 (zh) |
| CR (1) | CR20230025A (zh) |
| IL (1) | IL299149A (zh) |
| MX (1) | MX2022016548A (zh) |
| PE (1) | PE20231082A1 (zh) |
| TW (1) | TW202216743A (zh) |
| UY (1) | UY39298A (zh) |
| WO (1) | WO2021263167A2 (zh) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN116425857A (zh) * | 2023-06-09 | 2023-07-14 | 苏州依科赛生物科技股份有限公司 | 一种无糖基化修饰的il-15及制备方法 |
| CN117143235A (zh) * | 2023-10-26 | 2023-12-01 | 中国科学院苏州纳米技术与纳米仿生研究所 | 一种单克隆抗体及应用 |
| WO2025256479A1 (zh) * | 2024-06-12 | 2025-12-18 | 广东菲鹏制药股份有限公司 | 一种融合蛋白及其用途 |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| TW202426471A (zh) * | 2022-12-24 | 2024-07-01 | 大陸商廣東菲鵬製藥股份有限公司 | Il10突變體、融合蛋白和藥物 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2004044006A1 (en) * | 2002-11-14 | 2004-05-27 | Maxygen, Inc. | Conjugates of interleukin-10 and polymers |
| CN108503713A (zh) * | 2011-04-29 | 2018-09-07 | 罗切格利卡特公司 | 新的免疫缀合物 |
Family Cites Families (29)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DK0463151T3 (da) | 1990-01-12 | 1996-07-01 | Cell Genesys Inc | Frembringelse af xenogene antistoffer |
| US6673986B1 (en) | 1990-01-12 | 2004-01-06 | Abgenix, Inc. | Generation of xenogeneic antibodies |
| US6096871A (en) | 1995-04-14 | 2000-08-01 | Genentech, Inc. | Polypeptides altered to contain an epitope from the Fc region of an IgG molecule for increased half-life |
| CA2249195A1 (en) | 1996-03-18 | 1997-09-25 | Board Of Regents, The University Of Texas System | Immunoglobin-like domains with increased half lives |
| CA2273194C (en) | 1996-12-03 | 2011-02-01 | Abgenix, Inc. | Transgenic mammals having human ig loci including plural vh and vk regions and antibodies produced therefrom |
| DE19851675A1 (de) * | 1998-11-10 | 2000-05-11 | Bayer Ag | Menschliche Interleukin-10 Mutantenproteine |
| US6833268B1 (en) | 1999-06-10 | 2004-12-21 | Abgenix, Inc. | Transgenic animals for producing specific isotypes of human antibodies via non-cognate switch regions |
| US6808710B1 (en) | 1999-08-23 | 2004-10-26 | Genetics Institute, Inc. | Downmodulating an immune response with multivalent antibodies to PD-1 |
| EP2206517B1 (en) | 2002-07-03 | 2023-08-02 | Ono Pharmaceutical Co., Ltd. | Immunopotentiating compositions comprising anti-PD-L1 antibodies |
| JP4511943B2 (ja) | 2002-12-23 | 2010-07-28 | ワイス エルエルシー | Pd−1に対する抗体およびその使用 |
| EP2270051B1 (en) | 2003-01-23 | 2019-05-15 | Ono Pharmaceutical Co., Ltd. | Antibody specific for human PD-1 and CD3 |
| PL2161336T5 (pl) | 2005-05-09 | 2017-10-31 | Ono Pharmaceutical Co | Ludzkie przeciwciała monoklonalne przeciwko białku Programmed Death 1 (PD-1) oraz sposoby leczenia raka z zastosowaniem samych przeciwciał anty-PD-1 lub w połączeniu z innymi środkami immunoterapeutycznymi |
| CN104356236B (zh) | 2005-07-01 | 2020-07-03 | E.R.施贵宝&圣斯有限责任公司 | 抗程序性死亡配体1(pd-l1)的人单克隆抗体 |
| US8008453B2 (en) | 2005-08-12 | 2011-08-30 | Amgen Inc. | Modified Fc molecules |
| US20080260820A1 (en) * | 2007-04-19 | 2008-10-23 | Gilles Borrelly | Oral dosage formulations of protease-resistant polypeptides |
| CA2691357C (en) | 2007-06-18 | 2014-09-23 | N.V. Organon | Antibodies to human programmed death receptor pd-1 |
| US20090028857A1 (en) | 2007-07-23 | 2009-01-29 | Cell Genesys, Inc. | Pd-1 antibodies in combination with a cytokine-secreting cell and methods of use thereof |
| CA2736829C (en) | 2008-09-12 | 2018-02-27 | Isis Innovation Limited | Pd-1 specific antibodies and uses thereof |
| CA2998281C (en) | 2008-09-26 | 2022-08-16 | Dana-Farber Cancer Institute, Inc. | Human anti-pd-1 antobodies and uses therefor |
| KR101050829B1 (ko) | 2008-10-02 | 2011-07-20 | 서울대학교산학협력단 | 항 pd-1 항체 또는 항 pd-l1 항체를 포함하는 항암제 |
| EP4331604B9 (en) | 2008-12-09 | 2025-07-23 | F. Hoffmann-La Roche AG | Anti-pd-l1 antibodies and their use to enhance t-cell function |
| ES2629337T3 (es) | 2009-02-09 | 2017-08-08 | Inserm - Institut National De La Santé Et De La Recherche Médicale | Anticuerpos contra PD-1 y anticuerpos contra PD-L1 y usos de los mismos |
| NZ705899A (en) | 2012-09-07 | 2018-08-31 | Inst Nat Sante Rech Med | Inhibiting peptides derived from triggering receptor expressed on myeloid cells-1 (trem-1) trem-like transcript 1 (tlt-1) and uses thereof |
| CA2908208A1 (en) * | 2013-04-24 | 2014-10-30 | Armo Biosciences, Inc. | Interleukin-10 compositions and uses thereof |
| WO2015009955A1 (en) * | 2013-07-18 | 2015-01-22 | Xalud Therapeutics, Inc. | Methods for the treatment of inflammatory joint disease |
| PT3702373T (pt) | 2013-09-13 | 2022-09-27 | Beigene Switzerland Gmbh | Anticorpos anti-pd1 e a sua utilização como agentes terapêuticos e de diagnóstico |
| JP2017506075A (ja) * | 2014-02-06 | 2017-03-02 | エフ・ホフマン−ラ・ロシュ・アクチェンゲゼルシャフト | インターロイキン−10イムノコンジュゲート |
| JP7023853B2 (ja) * | 2016-03-04 | 2022-02-22 | アレクトル エルエルシー | 抗trem1抗体及びその使用方法 |
| UY38049A (es) | 2018-01-12 | 2019-07-31 | Amgen Inc | Anti-pd-1 anticuerpos y métodos de tratamiento |
-
2021
- 2021-06-25 KR KR1020237003104A patent/KR20230027300A/ko active Pending
- 2021-06-25 TW TW110123422A patent/TW202216743A/zh unknown
- 2021-06-25 US US18/001,913 patent/US20230265145A1/en active Pending
- 2021-06-25 CR CR20230025A patent/CR20230025A/es unknown
- 2021-06-25 CN CN202180051906.4A patent/CN116209459A/zh active Pending
- 2021-06-25 UY UY0001039298A patent/UY39298A/es unknown
- 2021-06-25 PE PE2022003048A patent/PE20231082A1/es unknown
- 2021-06-25 IL IL299149A patent/IL299149A/en unknown
- 2021-06-25 WO PCT/US2021/039191 patent/WO2021263167A2/en not_active Ceased
- 2021-06-25 JP JP2022578995A patent/JP2023531493A/ja active Pending
- 2021-06-25 MX MX2022016548A patent/MX2022016548A/es unknown
- 2021-06-25 AU AU2021296917A patent/AU2021296917A1/en active Pending
- 2021-06-25 EP EP21746606.9A patent/EP4172184A2/en active Pending
- 2021-06-25 CA CA3187576A patent/CA3187576A1/en active Pending
-
2022
- 2022-12-26 CL CL2022003755A patent/CL2022003755A1/es unknown
-
2023
- 2023-01-16 CO CONC2023/0000431A patent/CO2023000431A2/es unknown
-
2024
- 2024-11-26 CL CL2024003619A patent/CL2024003619A1/es unknown
- 2024-11-26 CL CL2024003618A patent/CL2024003618A1/es unknown
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2004044006A1 (en) * | 2002-11-14 | 2004-05-27 | Maxygen, Inc. | Conjugates of interleukin-10 and polymers |
| CN108503713A (zh) * | 2011-04-29 | 2018-09-07 | 罗切格利卡特公司 | 新的免疫缀合物 |
Non-Patent Citations (1)
| Title |
|---|
| K JOSEPHSON等: "Design and Analysis of an Engineered Human Interleukin-10 Monomer", J BIOL CHEM, vol. 275, no. 18, 5 May 2020 (2020-05-05), pages 13552 - 13557 * |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN116425857A (zh) * | 2023-06-09 | 2023-07-14 | 苏州依科赛生物科技股份有限公司 | 一种无糖基化修饰的il-15及制备方法 |
| CN116425857B (zh) * | 2023-06-09 | 2023-08-18 | 苏州依科赛生物科技股份有限公司 | 一种无糖基化修饰的il-15及制备方法 |
| CN117143235A (zh) * | 2023-10-26 | 2023-12-01 | 中国科学院苏州纳米技术与纳米仿生研究所 | 一种单克隆抗体及应用 |
| CN117143235B (zh) * | 2023-10-26 | 2024-02-09 | 中国科学院苏州纳米技术与纳米仿生研究所 | 一种单克隆抗体及应用 |
| WO2025256479A1 (zh) * | 2024-06-12 | 2025-12-18 | 广东菲鹏制药股份有限公司 | 一种融合蛋白及其用途 |
Also Published As
| Publication number | Publication date |
|---|---|
| CA3187576A1 (en) | 2021-12-30 |
| PE20231082A1 (es) | 2023-07-17 |
| US20230265145A1 (en) | 2023-08-24 |
| WO2021263167A2 (en) | 2021-12-30 |
| IL299149A (en) | 2023-02-01 |
| JP2023531493A (ja) | 2023-07-24 |
| CL2024003619A1 (es) | 2025-03-14 |
| AU2021296917A1 (en) | 2023-02-02 |
| EP4172184A2 (en) | 2023-05-03 |
| CO2023000431A2 (es) | 2023-03-27 |
| TW202216743A (zh) | 2022-05-01 |
| MX2022016548A (es) | 2023-03-14 |
| CR20230025A (es) | 2023-10-05 |
| CL2024003618A1 (es) | 2025-03-14 |
| UY39298A (es) | 2022-01-31 |
| CL2022003755A1 (es) | 2023-07-21 |
| KR20230027300A (ko) | 2023-02-27 |
| WO2021263167A3 (en) | 2022-04-21 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2923143T3 (es) | Anticuerpos monoclonales antagonistas contra CD40 y sus usos | |
| JP6163158B2 (ja) | Cd40lに拮抗する抗体ポリペプチド | |
| CN105026428B (zh) | PD‑l抗体、其抗原结合片段及其医药用途 | |
| JP6976322B2 (ja) | 新規抗ctla4抗体 | |
| JP6006404B2 (ja) | 抗BLyS抗体 | |
| US20170304437A1 (en) | Bispecific molecules capable of specifically binding to both ctla-4 and cd40 | |
| TW202132347A (zh) | 針對cd3和bcma的抗體和自其製備的雙特異性結合蛋白 | |
| CN116209459A (zh) | Il-10突变蛋白及其融合蛋白 | |
| HK1247214B (zh) | 一种pdl-1抗体、其药物组合物及其用途 | |
| CN106459217A (zh) | 多特异性抗体构建体 | |
| AU2016369307A1 (en) | Multi-specific antibody molecules having specificity for TNF-alpha, IL-17A and IL-17F | |
| JP7597784B2 (ja) | 胸腺間質性リンパ球新生因子(tslp)受容体シグナル伝達に干渉する薬剤 | |
| KR20230010691A (ko) | St2 항원 결합 단백질 | |
| KR20150128849A (ko) | 인터페론 알파 및 오메가 항체 길항제 | |
| JP7278623B2 (ja) | 抗cd27抗体およびその使用 | |
| CN113544152B (zh) | Flt3激动剂抗体及其用途 | |
| CN117751142A (zh) | 用trem-1抗原结合蛋白治疗心血管疾病 | |
| WO2022247826A1 (zh) | 靶向pd-l1和cd73的特异性结合蛋白 | |
| WO2022272018A1 (en) | Treatment of cardiovascular disease with trem-1 antigen binding proteins | |
| TW202500589A (zh) | 抗bdca2抗體 | |
| AU2024247517A1 (en) | Anti-il-25 antibodies and methods of use thereof | |
| HK40067877A (zh) | 针对cd3和bcma的抗体和自其制备的双特异性结合蛋白 | |
| BR122025021892A2 (pt) | Células hospedeiras |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination |