CN115397848A - Tat肽结合蛋白及其用途 - Google Patents
Tat肽结合蛋白及其用途 Download PDFInfo
- Publication number
- CN115397848A CN115397848A CN202180025971.XA CN202180025971A CN115397848A CN 115397848 A CN115397848 A CN 115397848A CN 202180025971 A CN202180025971 A CN 202180025971A CN 115397848 A CN115397848 A CN 115397848A
- Authority
- CN
- China
- Prior art keywords
- tat
- amino acid
- domain
- seq
- acid sequence
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C07K16/1147—
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
- A61P31/18—Antivirals for RNA viruses for HIV
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/569—Immunoassay; Biospecific binding assay; Materials therefor for microorganisms, e.g. protozoa, bacteria, viruses
- G01N33/56983—Viruses
- G01N33/56988—HIV or HTLV
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/31—Immunoglobulins specific features characterized by aspects of specificity or valency multispecific
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/565—Complementarity determining region [CDR]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/60—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments
- C07K2317/62—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments comprising only variable region components
- C07K2317/622—Single chain antibody (scFv)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/01—Fusion polypeptide containing a localisation/targetting motif
- C07K2319/10—Fusion polypeptide containing a localisation/targetting motif containing a tag for extracellular membrane crossing, e.g. TAT or VP22
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2333/00—Assays involving biological materials from specific organisms or of a specific nature
- G01N2333/005—Assays involving biological materials from specific organisms or of a specific nature from viruses
- G01N2333/08—RNA viruses
- G01N2333/15—Retroviridae, e.g. bovine leukaemia virus, feline leukaemia virus, feline leukaemia virus, human T-cell leukaemia-lymphoma virus
- G01N2333/155—Lentiviridae, e.g. visna-maedi virus, equine infectious virus, FIV, SIV
- G01N2333/16—HIV-1, HIV-2
- G01N2333/163—Regulatory proteins, e.g. tat, nef, rev, vif, vpu, vpr, vpt, vpx
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2500/00—Screening for compounds of potential therapeutic value
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Virology (AREA)
- Engineering & Computer Science (AREA)
- Chemical & Material Sciences (AREA)
- Molecular Biology (AREA)
- Immunology (AREA)
- Biomedical Technology (AREA)
- General Health & Medical Sciences (AREA)
- Hematology (AREA)
- AIDS & HIV (AREA)
- Medicinal Chemistry (AREA)
- Urology & Nephrology (AREA)
- Tropical Medicine & Parasitology (AREA)
- Organic Chemistry (AREA)
- Biotechnology (AREA)
- Genetics & Genomics (AREA)
- Biochemistry (AREA)
- Physics & Mathematics (AREA)
- Microbiology (AREA)
- Oncology (AREA)
- Cell Biology (AREA)
- Pathology (AREA)
- Animal Behavior & Ethology (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Communicable Diseases (AREA)
- Food Science & Technology (AREA)
- Pharmacology & Pharmacy (AREA)
- Analytical Chemistry (AREA)
- Veterinary Medicine (AREA)
- General Physics & Mathematics (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Public Health (AREA)
- General Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Biophysics (AREA)
- Plant Pathology (AREA)
Abstract
本发明包括TAT肽结合蛋白。具体而言,本发明涉及特异性结合TAT蛋白转导结构域的抗体。本发明的抗体可以是全长抗体或其抗原结合部分。本文还提供了本发明的抗体的制备方法和使用本发明的抗体检测、定量、纯化和分离TAT蛋白转导结构域(例如,包含TAT蛋白转导结构域的TAT融合分子)的方法,以及诊断和监测HIV和AIDS的方法。
Description
相关申请
本申请要求于2020年2月5日提交的美国临时专利申请第62/970,662号的优先权,其全部内容通过引用并入本文。
序列表
本申请包含以ASCII格式电子提交的序列表,在此通过引用将其整体并入本文。所述ASCII副本创建于2021年2月5日,命名为130197-00220_SL.txt,且大小为27400字节。
背景技术
人免疫缺陷病毒1型(HIV-1)TAT蛋白是HIV-1复制周期中的关键调节蛋白。HIV-1的野生型TAT基因是病毒RNA产生和病毒复制所必需的。TAT与细胞转录因子和细胞因子(例如,肿瘤坏死因子-α(TNF-α)相互作用,并改变多种基因在HIV-1感染的和未感染的细胞中的表达。
TAT也已被证明其可被细胞吸收和内化。因此,异源蛋白与TAT的融合已被用作细胞培养和活体动物中细胞递送异源蛋白的手段。
TAT特异性细胞毒性T淋巴细胞的存在与对HIV感染的强抗性相关(Allen等,Nature 2000 407(6802):386 390)。TAT介导的病因效应也可被抗TAT抗体中和。针对TAT保守区的抗体,例如富含半胱氨酸和富含赖氨酸的结构域,已表现出在抑制HIV复制中特别有效。在HIV-1感染患者中,针对HIV-1TAT蛋白的强体液免疫反应与外周血病毒载量呈现负相关(Re等,J.Clin.Virol.2001 21(1):819)。
本领域仍需要可用于检测和定量TAT肽的抗TAT抗体,例如用作融合分子的一部分用于细胞递送异源货物(cargo)部分的TAT肽。还需要在治疗HIV感染中用于治疗目的的抗TAT抗体。
发明内容
在某些方面,本发明提供了结合至TAT蛋白转导结构域的抗TAT结合蛋白,例如抗体及其抗原结合部分。
在一个方面,本发明提供了包含抗原结合结构域的结合蛋白,所述抗原结合结构域包含含有SEQ ID NO:4的氨基酸序列的重链CDR3结构域,其中所述结合蛋白能够结合TAT蛋白转导结构域。
在一些实施方案中,抗原结合结构域进一步包含含有SEQ ID NO:3的氨基酸序列的重链CDR2结构域。
在一些实施方案中,抗原结合结构域进一步包含含有SEQ ID NO:2的氨基酸序列的重链CDR1结构域。
在一些实施方案中,抗原结合结构域进一步包含含有选自由SEQ ID NO:8和SEQID NO:12组成的组的氨基酸序列的轻链CDR3结构域。
在一些实施方案中,抗原结合结构域进一步包含含有选自由SEQ ID NO:7和SEQID NO:11组成的组的氨基酸序列的轻链CDR2结构域。
在一些实施方案中,抗原结合结构域进一步包含含有选自由SEQ ID NO:6和SEQID NO:10组成的组的氨基酸序列的轻链CDR1结构域。
在另一个方面,本发明提供了包含抗原结合结构域的结合蛋白,所述抗原结合结构域包含:重链可变区,其包含含有SEQ ID NO:4所示氨基酸序列的CDR3结构域,含有SEQID NO:3所示氨基酸序列的CDR2结构域和含有SEQ ID NO:2所示氨基酸序列的CDR1结构域;和轻链可变区,其包含含有SEQ ID NO:8所示氨基酸序列的CDR3结构域,含有SEQ ID NO:7所示氨基酸序列的CDR2结构域和含有SEQ ID NO:6所示氨基酸序列的CDR1结构域;或轻链可变区,其包含含有SEQ ID NO:12所示氨基酸序列的CDR3结构域,含有SEQ ID NO:11所示氨基酸序列的CDR2结构域和含有SEQ ID NO:10所示氨基酸序列的CDR1结构域,其中所述结合蛋白能够结合TAT蛋白转导结构域。
在一些实施方案中,抗原结合结构域包含含有SEQ ID NO:1或SEQ ID NO:14所示氨基酸序列的重链可变区。
在一些实施方案中,抗原结合结构域包含含有SEQ ID NO:5所示氨基酸序列的轻链可变区,含有SEQ ID NO:9所示氨基酸序列的轻链可变区,或含有SEQ ID NO:13所示氨基酸序列的轻链可变区。
在一些实施方案中,抗原结合结构域包含含有SEQ ID NO:1所示氨基酸序列的重链可变区和含有SEQ ID NO:5所示氨基酸序列的轻链可变区。
在一些实施方案中,抗原结合结构域包含含有SEQ ID NO:1所示氨基酸序列的重链可变区和含有SEQ ID NO:9所示氨基酸序列的轻链可变区。
在一些实施方案中,抗原结合结构域包含含有SEQ ID NO:1所示氨基酸序列的重链可变区和含有SEQ ID NO:13所示氨基酸序列的轻链可变区。
在一些实施方案中,抗原结合结构域包含含有SEQ ID NO:14所示氨基酸序列的重链可变区和含有SEQ ID NO:5所示氨基酸序列的轻链可变区。
在另一个方面,本发明提供了包含抗原结合结构域的结合蛋白,所述抗原结合结构域包含含有SEQ ID NO:18的氨基酸序列的重链CDR3结构域,其中所述结合蛋白能够结合TAT蛋白转导结构域。
在一些实施方案中,抗原结合结构域进一步包含含有SEQ ID NO:17的氨基酸序列的重链CDR2结构域。
在一些实施方案中,抗原结合结构域进一步包含含有SEQ ID NO:16的氨基酸序列的重链CDR1结构域。
在一些实施方案中,抗原结合结构域进一步包含含有SEQ ID NO:22的氨基酸序列的轻链CDR3结构域。
在一些实施方案中,抗原结合结构域进一步包含含有SEQ ID NO:21的氨基酸序列的轻链CDR2结构域。
在一些实施方案中,抗原结合结构域进一步包含含有SEQ ID NO:20的氨基酸序列的轻链CDR1结构域。
在另一个方面,本发明提供了包含抗原结合结构域的结合蛋白,所述抗原结合结构域包含:重链可变区,其包含含有SEQ ID NO:18所示氨基酸序列的CDR3结构域,含有SEQID NO:17所示氨基酸序列的CDR2结构域和含有SEQ ID NO:16所示氨基酸序列的CDR1结构域;和轻链可变区,其包含含有SEQ ID NO:22所示氨基酸序列的CDR3结构域,含有SEQ IDNO:21所示氨基酸序列的CDR2结构域和含有SEQ ID NO:20所示氨基酸序列的CDR1结构域,其中所述结合蛋白能够结合TAT蛋白转导结构域。
在一些实施方案中,抗原结合结构域包含含有SEQ ID NO:15所示氨基酸序列的重链可变区。
在一些实施方案中,抗原结合结构域包含含有SEQ ID NO:19所示氨基酸序列的轻链可变区。
在一些实施方案中,抗原结合结构域包含含有SEQ ID NO:15所示氨基酸序列的重链可变区和含有SEQ ID NO:19所示氨基酸序列的轻链可变区。
在一些实施方案中,TAT蛋白转导结构域包含SEQ ID NO:23的氨基酸序列。
在一些实施方案中,TAT蛋白转导结构域基本上由SEQ ID NO:23的氨基酸序列组成。
在一些实施方案中,TAT蛋白转导结构域与货物部分共价连接。
在一些实施方案中,货物部分是多肽。
在一些实施方案中,货物部分是共济蛋白(frataxin)多肽。
在一些实施方案中,货物部分是抗体。
在一些实施方案中,货物部分是核酸。在一些实施方案中,核酸是siRNA、shRNA、miRNA、硫代磷酸酯修饰的RNA、适配体、磷酰二胺吗啉代寡核苷酸(PMO)或其任何组合。
在一些实施方案中,货物部分是小分子、脂质体包封蛋白、放射性核素或放射性核素标记的化合物或其任何组合。
在一些实施方案中,结合蛋白能够结合至与货物部分共价连接的TAT蛋白转导结构域。
在一些实施方案中,抗原结合结构域结合至包含SEQ ID NO:23的氨基酸残基的表位。
在一些实施方案中,本文公开的结合蛋白是抗体。
在另一个方面,本发明提供了包含本发明的结合蛋白的抗体构建体,其进一步包含接头多肽或免疫球蛋白恒定区。
在一些实施方案中,结合蛋白选自由以下组成的组:免疫球蛋白分子、单克隆抗体、鼠抗体、嵌合抗体、CDR移植抗体、人源化抗体、单域抗体、Fv、二硫键连接的Fv、scFv、双抗(diabody)、Fab、Fab’、F(ab’)2、多特异性抗体、双重特异性抗体(dual specificantibody)和双特异性抗体。
在一些实施方案中,抗体构建体包含结合蛋白,所述结合蛋白包含选自由以下组成的组的重链免疫球蛋白恒定区:IgM恒定区、IgG4恒定区、IgG1恒定区、IgE恒定区、IgG2恒定区、IgG3恒定区和IgA恒定区。
在一些实施方案中,重链免疫球蛋白恒定区不是IgM。
在另一个方面,本发明提供了编码本发明的结合蛋白氨基酸序列的分离的核酸。
在另一个方面,本发明提供了编码本发明的抗体构建体氨基酸序列的分离的核酸。
在另一个方面,本发明提供了包含本发明的分离核酸的载体。
在一些实施方案中,载体选自由以下组成的组:pcDNA、pTT、pTT3、pEFBOS、pBV、pJV、pBJ、pGEX、VSV、pBR322、pCMV-HA、pEN、YAC、BAC、λ噬菌体(Bacteriophage Lamda)、噬菌粒(Phagemid)、pCAS9、pCEN6、pYES1L、p3HPRT1、pFN2A、pBC、pTZ、pGEM、pGEMK、pEX、pSAR、pCEP、黏性质粒(Cosmid)、pBluescript、pKJK、pFloxin、pCP、pHR、pUC和pMAL。
在另一个方面,本发明提供了包含本发明的载体的宿主细胞。
在一些实施方案中,宿主细胞是原核细胞或真核细胞。在一些实施方案中,原核宿主细胞是大肠杆菌细胞。在一些实施方案中,真核细胞选自由以下组成的组:原生生物细胞、昆虫细胞、动物细胞、植物细胞和真菌细胞。在一些实施方案中,动物细胞是哺乳动物细胞或禽类细胞。在一些实施方案中,宿主细胞选自由以下组成的组:CHO细胞、COS细胞、酵母细胞、昆虫Sf9细胞、HEK-293细胞、ExpiCHO细胞、Expi-293f细胞和大肠杆菌细胞。在一些实施方案中,酵母细胞是酿酒酵母细胞。
在另一个方面,本发明提供了产生抗体或其抗原结合部分的方法,其包括在培养基中培养宿主细胞,从而表达分离的核酸并产生抗体。
在另一个方面,本发明提供了根据本发明的方法产生的抗体。
在另一个方面,本发明提供了包含本文所述的宿主细胞的转基因小鼠,其中所述小鼠表达由所述核酸编码的多肽或其抗原结合部分,所述多肽或其抗原结合部分与TAT蛋白转导结构域结合。
在另一个方面,本发明提供了产生本文所述的抗体构建体的杂交瘤。
在一些实施方案中,本发明的结合蛋白固定在固体支持物上。在一些实施方案中,固体支持物是板、珠或层析树脂。在一些实施方案中,珠或层析树脂包含蛋白A琼脂糖或蛋白G琼脂糖。
在一些实施方案中,本发明的结合蛋白与检测分子偶联。
在一些实施方案中,检测分子是辣根过氧化物酶、三联吡啶钌(sulfotag)、碱性磷酸酶、甲酚紫、量子点、FITC、红外分子、放射性同位素标记或EPR自旋示踪剂标签。
在另一个方面,本发明提供了检测和/或定量样品中TAT融合分子水平的方法,其包括在使本发明的结合蛋白与所述样品中TAT蛋白转导结构域结合的条件下,使样品与所述结合蛋白接触,从而检测和/或定量样品中TAT融合分子的水平。
在一些实施方案中,样品是生物样品。
在一些实施方案中,生物样品是液体样品或组织样品。
在一些实施方案中,TAT融合分子包含与货物部分共价连接的TAT蛋白转导结构域。
在一些实施方案中,货物部分是多肽。
在一些实施方案中,货物部分是共济蛋白多肽。
在一些实施方案中,货物部分是抗体。
在一些实施方案中,货物部分是核酸。在一些实施方案中,核酸是siRNA、shRNA、miRNA、硫代磷酸酯修饰的RNA、适配体、磷酰二胺吗啉代寡核苷酸(PMO)或其任何组合。
在一些实施方案中,货物部分是小分子、脂质体包封蛋白、放射性核素或放射性核素标记的化合物或其任何组合。
在一些实施方案中,评估TAT融合分子的稳定性。
在另一个方面,本发明提供了分离和/或纯化混合物中存在的TAT融合分子的方法,其中所述TAT融合分子包含与货物部分共价连接的TAT蛋白转导结构域,所述方法包括(a)在使得TAT融合分子与本发明的固定化结合蛋白结合的条件下,使包含TAT融合分子的混合物与固定化结合蛋白接触;(b)从固定化结合蛋白洗脱TAT融合分子。
在另一个方面,本发明提供了一种试剂盒,其包含至少一种用于特异性检测TAT蛋白转导结构域水平的试剂,其中所述检测试剂是本发明的结合蛋白。在一些实施方案中,TAT蛋白转导结构域与货物部分共价连接。在一些实施方案中,试剂盒进一步包含用于检测、定量或表征TAT蛋白转导结构域的说明书。
在另一个方面,本发明提供了抑制TAT融合分子跨细胞膜易位(translocation)的方法,其包括使TAT融合分子与本发明的抗原结合蛋白接触,从而抑制TAT融合分子跨细胞膜易位。
在另一个方面,本发明提供了抑制受试者中HIV-TAT蛋白活性的方法,其包括向受试者施用本发明的抗原结合蛋白,从而抑制受试者中HIV-TAT蛋白的活性。
附图说明
图1阐述了针对整个TAT-FXN融合分子产生的多克隆抗体识别药物,但不以TAT特异性方式识别药物。
图2阐述了针对KLH-TAT产生的多克隆抗体不识别成熟的共济蛋白,但识别BSA-TAT,这显示了对TAT表位的特异性。
图3是显示使用抗TAT兔多克隆抗体(AC1058)和可商购的抗共济蛋白抗体(ab124680、ab113691和ab110328)以及可商购的抗TAT抗体(ab63957)的示例性TAT共济蛋白融合分子免疫纯化后,由共济蛋白衍生的胰蛋白酶肽产生的相对峰面积的柱状图。
图4A和图4B显示了本发明的10种抗TAT抗体中的9种在人血浆中的药代动力学(PK)试验中捕获示例性TAT共济蛋白融合分子的能力。
图5A显示了本发明的10种抗TAT抗体中的9种结合至人血浆中的示例性TAT共济蛋白融合分子。图5B描绘了人血浆中抗药物抗体(ADA)测定的结果,其表明多克隆抗TAT抗体在ADA测定中可用作阳性对照。
具体实施方式
本发明涉及与TAT蛋白转导结构域结合的TAT肽结合蛋白,特别是抗TAT肽抗体或其抗原结合部分,包括包含TAT蛋白转导结构域的TAT融合分子及其用途。本发明的各个方面涉及抗体和抗体片段、其偶联物和其药物组合物,以及用于制备此类抗体和片段的核酸、重组表达载体和宿主细胞。在一个方面,本发明涉及包含抗原结合结构域的结合蛋白,其中所述结合蛋白能够结合至与货物部分共价连接的TAT蛋白转导结构域。在一些实施方案中,货物部分是多肽。在一些实施方案中,货物部分是共济蛋白多肽。在一些实施方案中,货物部分是抗体。
在一些实施方案中,货物部分是药理学活性化合物、小分子、脂质体包封蛋白、放射性核素或放射性核素标记的化合物、核酸(例如,siRNA、shRNA、miRNA、硫代磷酸酯修饰的RNA、适配体、磷酰二胺吗啉代寡核苷酸(PMO)或其任何组合)。本发明还包括使用本发明的结合蛋白(例如,抗体)以检测和/或定量样品中TAT肽(例如,TAT蛋白转导结构域或TAT融合分子)的水平,和以分离和/或纯化混合物中存在的TAT肽或TAT融合分子的方法。在一些实施方案中,TAT融合分子包含与货物部分共价连接的TAT蛋白转导结构域。在一些实施方案中,货物部分是多肽,例如,共济蛋白多肽。
在一些实施方案中,货物部分是药理学活性化合物、小分子、脂质体包封蛋白、放射性核素或放射性核素标记的化合物、核酸(例如,siRNA、shRNA、miRNA、硫代磷酸酯修饰的RNA、适配体、磷酰二胺吗啉代寡核苷酸(PMO)或其任何组合)。在一些实施方案中,本发明的方法还包括评估TAT融合分子的稳定性。
本发明还包括使用本发明的结合蛋白(例如,抗体)通过测定生物样品中TAT蛋白或TAT蛋白的一部分的存在来抑制TAT融合分子跨细胞膜的易位和抑制受试者中HIV-TAT蛋白的活性的方法。本发明还包括使用本发明的结合蛋白(例如,抗体)来诊断受试者中HIV感染的方法。
I.定义
除非本文另有定义,与本发明结合使用的科学和技术术语应具有本领域普通技术人员通常理解的含义。然而,术语的含义和范围应该是清楚的,如果有任何潜在的歧义,本文提供的定义优先于任何字典或外部定义。此外,除非上下文另有要求,否则单数术语应包括复数,并且复数术语应包括单数。在本申请中,除非另有说明,“或”的使用是指“和/或”。此外,术语“包括”以及例如“包含”和“含有”等其他形式的使用不是限制性的。此外,除非另有说明,术语如“元件”或“组分”既包括包含一个单元的元件和组分,也包括包含多于一个亚单元的元件和组分。术语“例如”在本文中用于表示短语“例如但不限于”,并且可与短语“例如但不限于”互换使用。
冠词“一个”和“一种”在本文中用于指该冠词的语法对象中的一个或多于一个(即,至少一个)。举例来说,“一个元件”是指一个元件或多于一个元件。
除非具体说明或从上下文明显看出,如本文所用,术语“约”应被理解为在本领域的正常公差范围内,例如在平均值的2个标准偏差内。约可以理解为在所述值的10%、9%、8%、7%、6%、5%、4%、3%、2%、1%、0.5%、0.1%、0.05%或0.01%内。除非从上下文另有明确说明,本文提供的所有数值都可以用术语“约”来修饰。
本文的任何变量的定义中化学基团列表的记载包括将该变量定义为任何单个基团或所列基团的组合。本文中变量或方面的实施方案的记载包括作为任何单个实施方案或与任何其他实施方案或其部分组合的实施方案。
本文提供的任何组合物或方法可以与本文提供的任何其他组合物和方法中的一种或多种组合。
本文提供的范围应理解为该范围内的所有值的简写。例如,1至50的范围应理解为包括由1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49或50组成的组中的任何数值、数值的组合或子范围。如本文所用,“一个或多个”应理解为1、2、3、4、5、6、7、8、9、10中的每个值和大于10的任何值。
通常,与本文所述的细胞和组织培养、分子生物学、免疫学、微生物学、遗传学以及蛋白质和核酸化学和杂交相关的命名法和技术是本领域熟知且常用的那些。除非另有说明,本发明的方法和技术通常根据本领域公知的常规方法进行,并且如在本说明书中引用和讨论的各种综合和更具体的参考文献中所述。根据制造商的说明书进行酶促反应和纯化技术,如本领域通常完成的或如本文所述。本文所述的与分析化学、合成有机化学以及医药和药物化学相关的命名法以及实验室程序和技术是本领域熟知且常用的那些。标准技术用于化学合成、化学分析、药物制备、制剂以及递送和患者的治疗。
为了可以更容易地理解本发明,选择的术语定义如下。
如本文所用,术语“多肽”或“肽”是指氨基酸的任何聚合链。术语“蛋白质”可与术语肽和多肽互换使用,也是指氨基酸的聚合链。术语“肽”或“多肽”包括天然或人工蛋白质、蛋白质片段和蛋白质序列的多肽类似物。多肽可以是单体的或聚合体的。
术语“分离蛋白质”或“分离多肽”或“分离肽”是由于其来源或衍生来源而不与以其天然状态伴随它的天然相关组分相关的蛋白质或多肽;基本上不含来自相同物种的其他蛋白质;由来自不同物种的细胞表达;或不是天然存在的。因此,化学合成的或在不同于其天然来源的细胞的细胞系统中合成的多肽将与其天然相关组分“分离”。通过使用本领域熟知的蛋白纯化技术分离,蛋白质还可以基本上不含其天然相关组分。分离的多肽的示例是分离抗体或其抗原结合部分。
本文可互换使用的术语“TAT肽”或“转录肽的反式激活因子”或“TAT”是指反式激活调节蛋白或其部分。TAT肽是由慢病毒HIV-1编码。TAT肽是病毒基因组的有效转录所必需的(Green及Lowenstein,1988Cell 55(6):1179-88)。全长蛋白包括86-101个氨基酸,这取决于亚型。在一些实施方案中,全长TAT蛋白具有如SEQ ID NO:24所示氨基酸序列,如下所示。
在体内,TAT提高HIV dsDNA的转录水平。在TAT存在之前,产生少量RNA转录物,从而允许产生TAT蛋白。然后TAT与细胞因子结合并介导它们的磷酸化,导致所有HIV基因的转录提高,提供正反馈循环。TAT还似乎在HIV疾病过程中发挥更直接的作用。TAT蛋白由培养物中感染的细胞释放,并被发现于HIV-1感染患者的血液中。
TAT蛋白能够通过细胞质膜易位并到达细胞核以反式激活病毒基因组。“TAT蛋白转导结构域”已被认为与细胞穿透相关(Vives等,J Biol Chem.1997Jun 20;272(25):16010-7,其内容通过引用并入本文)。
如本文所用,术语“TAT蛋白转导结构域”,“TAT-PTD”或“TAT易位肽”本文可互换使用的,其是指包含86个氨基酸的TAT蛋白质的氨基酸47-57(氨基酸YGRKKRRQRRR,SEQ IDNO:23)的TAT蛋白质结构域(Frankel等,Cell,vol.55,issue 6,1988;M.Green等,Cell,vol.55,issue 6,1988;Fawell等,PNAS,91(2),664-668,1994;USPN 6,348,185;其内容通过引用并入本文)。在一个实施方案中,本发明的TAT肽抗体与TAT蛋白转导结构域特异性结合。在一个实施方案中,TAT蛋白转导结构域包含SEQ ID NO:23(YGRKKRRQRRR)的氨基酸序列。在一些实施方案中,本发明的TAT肽结合蛋白与包含SEQ ID NO:23的氨基酸序列的TAT蛋白转导结构域特异性结合。在另一个实施方案中,本发明的TAT肽结合蛋白特异性与基本上由SEQ ID NO:23的氨基酸序列组成的TAT蛋白转导结构域结合。在另一个实施方案中,本发明的TAT肽结合蛋白与包含在TAT融合分子中的TAT蛋白转导结构域(例如SEQ ID NO:23)特异性结合。例如,在一个实施方案中,TAT融合分子包括TAT-共济蛋白融合分子。
如本文所用,“TAT活性”或“TAT肽活性”包括但不限于调节(例如,提高)病毒基因组的转录、提高HIV dsDNA的转录水平、调节细胞因子的磷酸化和TAT通过质膜的易位。
如本文所用,术语“TAT融合分子”或“TAT融合蛋白”是指与货物部分融合的TAT肽,例如TAT蛋白转导结构域。如本文所用,术语“货物部分”是指当与TAT肽(例如,TAT蛋白转导结构域)融合(例如,共价连接)时,可被转运至细胞中的任何分子。因此,货物部分不同于TAT肽或其任何片段。在一个实施方案中,货物部分以非成孔方式运输。在一个实施方案中,货物部分是多肽。在一个实施方案中,TAT融合分子是TAT-共济蛋白融合分子,且货物部分是共济蛋白多肽。示例性TAT-共济蛋白融合分子被描述于例如PCT/US2020/044069中,其全部内容通过引用并入本文。在另一个实施方案中,货物部分是选自由以下组成的组的治疗蛋白:阿巴瑞克、阿巴西普、阿昔单抗、阿达木单抗、阿柏西普、阿加糖酶β、阿比鲁肽、阿地白介素、阿法西普、阿仑单抗、阿仑单抗、阿糖苷酶、阿糖苷酶α、阿利罗单抗、阿利吉仑、α-1-蛋白酶抑制剂、阿替普酶、阿那白滞素、安塞司亭(Ancestim)、阿尼替普酶、炭疽人免疫球蛋白、抗血友病因子、抗抑制剂凝血复合物、抗凝血酶α、人抗凝血酶III、抗胸腺细胞球蛋白、抗胸腺细胞球蛋白(马)、抗胸腺细胞球蛋白(兔)、抑肽酶、阿西莫单抗、阿司福酶α(Asfotase Alfa)、天冬酰胺酶、菊欧文氏菌天冬酰胺酶(Asparaginase ErwiniaChrysanthemi)、阿特珠单抗、自体培养的软骨细胞、巴利昔单抗、贝卡普勒明、贝拉西普、贝利单抗、贝拉克坦(Beractant)、贝伐单抗、比伐卢定、博纳吐单抗、A型肉毒杆菌毒素、B型肉毒杆菌毒素、布伦妥昔单抗、布罗达鲁单抗、布舍瑞林、C1酯酶抑制剂(人)、Cl酯酶抑制剂(重组)、卡那奴单抗、卡那奴单抗、卡普马布、赛妥珠单抗、西妥昔单抗、绒毛膜促性腺激素α、绒毛膜促性腺激素(人)、绒毛膜促性腺激素(重组)、凝血因子IX、凝血因子VIIa、人凝血因子X、凝血因子XIII A-亚基(重组)、胶原酶、阿法可奈司他(Conestat alfa)、促肾上腺皮质激素、促皮质素(Cosyntropin)、达珠单抗、达托霉素、达雷木单抗、达贝泊汀阿尔法、去纤维肽(Defibrotide)、地尼白介素、地诺单抗、地西卢定、地高辛免疫Fab(绵羊)、地妥昔单抗、阿法链道酶(Dornase alfa)、替加色罗α(Drotrecogin alfa)、度拉鲁肽、依库珠单抗、依法珠单抗、艾芙莫罗凝血素α(Efmoroctocog alfa)、依洛硫酸酯酶α(Elosulfase alfa)、埃洛珠单抗、恩夫韦肽、依泊汀α、依泊汀δ、依替巴肽、依那西普、依洛尤单抗、艾塞那肽、因子IX复合物(人)、纤维蛋白原浓缩物(人)、纤维蛋白溶解素(纤溶酶)、非格司亭、非格司亭-sndz、促卵泡素α、促卵泡素β、加硫酶、胃内因子、吉妥珠单抗奥佐米星、醋酸格拉替雷、重组胰高血糖素、葡糖苷酶(Glucarpidase)、戈利木单抗、短杆菌肽D、甲型肝炎疫苗、乙型肝炎免疫球蛋白、人降钙素、人破伤风梭菌类毒素免疫球蛋白、人狂犬病病毒免疫球蛋白、人Rho(D)免疫球蛋白、人血清白蛋白、人水痘-带状疱疹免疫球蛋白、透明质酸酶、透明质酸酶(人重组)、伊布单抗、替伊莫单抗、依达珠单抗、艾度硫酸酯酶、伊米苷酶、人免疫球蛋白、英夫利昔单抗、门冬胰岛素、胰岛素、吉妥珠单抗奥佐米星、醋酸格拉替雷、重组胰高血糖素、葡糖苷酶、戈利木单抗、短杆菌肽D、甲型肝炎疫苗、乙型肝炎免疫球蛋白、人降钙素、人破伤风梭菌类毒素免疫球蛋白、人狂犬病病毒免疫球蛋白、人Rho(D)免疫球蛋白、人血清白蛋白、人水痘-带状疱疹免疫球蛋白、透明质酸酶、透明质酸酶(人重组)、伊布单抗、替伊莫单抗、依达珠单抗、艾度硫酸酯、伊米苷酶、人免疫球蛋白、英夫利昔单抗、门冬胰岛素、牛胰岛素、德谷胰岛素、地特胰岛素、甘精胰岛素、谷赖胰岛素、赖脯胰岛素、猪胰岛素、普通胰岛素、胰岛素(猪)、胰岛素-异佛烷(Insulin-isophane)、干扰素α-2a重组型、干扰素α-2b、干扰素alfacon-1、干扰素α-nl、干扰素α-n3、干扰素β-la、干扰素β-lb、干扰素γ-lb、静脉注射免疫球蛋白、易普利姆玛、伊克珠单抗、拉瑞诺酶、来格司亭、来匹卢定、亮丙瑞林、利拉鲁肽、芦西纳坦(Lucinactant)、重组人类黄体刺激素(Lutropin alfa)、美卡舍明、促性腺激素、美泊利单抗、甲氧基聚乙二醇-依泊汀β、美曲普汀、莫罗莫纳布、那他珠单抗、天然α干扰素或多铁素、耐妥尤单抗、奈西立肽、纳武单抗、奥比妥昔单抗、奥比妥珠单抗、奥克纤溶酶(Ocriplasmin)、奥法木单抗、奥马珠单抗、奥普瑞白介素、OspA脂蛋白、催产素、帕利弗明、帕利珠单抗、胰脂肪酶、帕尼单抗、牛培加酶、哌加他尼、培门冬酶、培非格司亭、聚乙二醇干扰素α-2a、聚乙二醇干扰素α-2b、聚乙二醇干扰素β-1a、培戈洛酶、培维索孟、派姆单抗、帕妥珠单抗、猪肺磷脂(Poractant alfa)、普兰林肽、Preotact、硫酸鱼精蛋白、人蛋白S、凝血酶原复合物浓缩物、豚草花粉提取物、雷莫芦单抗、雷珠单抗、拉布立酶、雷昔单抗、瑞替普酶、利罗那西普、利妥昔单抗、罗米波司亭、糖苷酶、鲑鱼降钙素、沙格司亭、沙妥莫单抗喷地肽(Satumomab Pendetide)、Sebelipase alfa、分泌素、苏金单抗、舍莫瑞林(Sermorelin)、血清白蛋白、碘化血清白蛋白、司妥昔单抗、塞莫凝血素α(Simoctocog Alfa)、Sipuleucel-T、生长激素重组体、生长激素重组体、链激酶、舒洛地特、重组蛋白舒索凝血素α(Susoctocog alfa)、他利苷酶α、替度鲁肽、替考拉宁、替奈普酶、特立帕肽、特沙莫林、血栓调节素阿尔法、胸腺素、甲状腺球蛋白、促甲状腺素α、托珠单抗、托西莫单抗、曲妥珠单抗、结核菌素纯化蛋白衍生物、妥罗凝血素α(Turoctocog alfa)、尿促卵泡素、尿激酶、优特克单抗、加压素、维多珠单抗、维拉苷酶α、血栓调节素α、胸腺嘧啶、甲状腺球蛋白、甲状腺激素、托西珠单抗、托西单抗、曲妥珠单抗、结核菌素纯化蛋白衍生物、妥罗凝血素α(Turoctocog alfa)、尿促卵泡素、尿激酶、优特克单抗、加压素、维多珠单抗、维拉苷酶α。在另一个实施方案中,蛋白质选自包括在Raghava,Gajendra P.S.;Usmani,SalmanSadullah;Bedi,Gursimran;Samuel,Jesse S.;Singh,Sandeep;Kalra,Sourav;等(2017):THPdb:Database of FDA Approved Peptide and Protein Therapeutics(其内容通过引用并入本文)中的那些。
在一个实施方案中,多肽货物部分的大小可以在约100kD和200nM之间。在另一个实施方案中,货物部分是药理学活性化合物、小分子、脂质体包封蛋白、放射性核素或放射性核素标记的的化合物、核酸(例如,siRNA、shRNA、miRNA、硫代磷酸酯修饰的RNA、适配体、磷酰二胺吗啉代寡核苷酸(PMO)或其任何组合)。在另一个实施方案中,TAT融合分子是组织渗透TAT融合分子。
本文所用的术语“TAT-共济蛋白融合分子”包括包含TAT蛋白转导结构域或其片段和共济蛋白肽或其片段的任何融合分子。在一个实施方案中,共济蛋白多肽与TAT肽(例如,TAT蛋白转导结构域)的融合允许整个融合蛋白通过细胞膜易位。示例性的TAT-共济蛋白融合分子被描述于美国专利系列第8,283,444号,其内容通过引入并入本文。
如本文所用,“进行检测”、“检测”、“测定”等应理解为识别样品中特定抗原(例如,TAT蛋白转导结构域或TAT融合分子)(例如,TAT-共济蛋白融合分子)而进行的测定。检测可以通过本领域已知的任何方法进行。例如,TAT蛋白转导结构域或TAT融合分子(例如,TAT-共济蛋白融合分子)可通过在使得本发明的结合蛋白与样品中的TAT蛋白转导结构域结合的条件下使包含TAT蛋白转导结构域或TAT融合分子的样品与结合蛋白接触来检测。在一个实施方案中,结合蛋白是固定化的。在另一个实施方案中,TAT转导结构域或TAT融合分子从固定化结合蛋白上被洗脱。
如本文所用,关于结合蛋白(例如,抗体、蛋白质或肽)与第二化学物质的相互作用的术语“特异性结合”或“特异性地结合”意思是该相互作用取决于化学物质上特定结构(例如,抗原决定簇或表位)的存在;例如,抗体识别并结合特异性的蛋白质结构而不是通常的蛋白质。如果抗体对表位“A”具有特异性,则在含有被标记的“A”和抗体的反应中,含有表位A(或游离未被标记的A)的分子的存在将减少与抗体结合的被标记的A的量。
在一个实施方案中,如本文所用,短语“特异性地结合至TAT蛋白转导结构域”或“与TAT蛋白转导结构域特异性结合”是指抗TAT结合蛋白与TAT蛋白转导结构域相互作用的能力,解离常数(KD)为约2,000nM或更低、约1,000nM或更低、约500nM或更低、约200nM或更低、约100nM或更低、约75nM或更低、约50nM或更低、约43nM或更低、约25nM或更低、约20nM或更低、约19nM或更低、约18nM或更低、约17nM或更低、约16nM或更低、约15nM或更低、约14nM或更低、约13nM或更低、约12nM或更低、约11nM或更低、约10nM或更低、约9nM或更低、约8nM或更低、约7nM或更低、约6nM或更低、约5nM或更低、约4nM或更低、约3nM或更低、约2nM或更低、约1nM或更低、约0.5nM或更低、约0.3nM或更低、约0.1nM或更低、或约0.01nM或更低、或约0.001nM或更低。
在另一个实施方案中,如本文所用,短语“特异性地结合至TAT蛋白转导结构域”或“与TAT蛋白转导结构域特异性结合”是指抗TAT结合蛋白与TAT蛋白转导结构域相互作用的能力,解离常数(KD)在约1pM(0.001nM)至2,000nM之间、在约500pM(0.5nM)至1,000nM之间、在约500pM(0.5nM)至500nM之间、在约1nM至200nM之间、在约1nM至100nM之间、在约1nM至50nM之间、在约1nM至20nM之间、或在约1nM至5nM之间。在一个实施方案中,通过表面等离子体共振测定KD。
如本文所用,术语“抗体”广泛地指包含四条多肽链(两条重(H)链和两条轻(L)链)的任何免疫球蛋白(Ig)分子或其任何功能性片段、突变体、变体或衍生物,其保留Ig分子的必要表位结合特征。这种突变体、变体或衍生抗体形式是本领域已知的。下面讨论其非限制性实施方案。
在全长抗体中,每条重链包含重链可变区(本文缩写为HCVR或VH)和重链恒定区。重链恒定区包含三个结构域CH1、CH2和CH3。每条轻链包含轻链可变区(本文缩写为LCVR或VL)和轻链恒定区。轻链恒定区包含一个结构域CL。VH和VL区可被进一步细分为称为互补决定区(CDR)的高变区,其穿插在被称为框架区(FR)的更保守的区域中。每个VH和VL含有三个CDR和四个FR,从氨基末端到羧基末端按以下顺序排列:FR1、CDR1、FR2、CDR2、FR3、CDR3、FR4。免疫球蛋白分子可以是任何类型(例如,IgG、IgE、IgM、IgD、IgA和IgY)、类别(例如,IgG1、IgG2、IgG3、IgG4、IgA1和IgA2)或亚类。在一个优选的实施方案中,免疫球蛋白分子是IgG1。
如本文所用,术语抗体的“抗原结合部分”(或简称为“抗体部分”)是指抗体的保留特异性结合抗原(例如,TAT蛋白转导结构域)的能力的一个或多个片段。已经表明,抗体的抗原结合功能可以通过全长抗体的片段来实现。此类抗体实施方案也可以是双特异性、双重特异性或多特异性形式;与两种或更多种不同抗原特异性结合。包含在术语抗体的“抗原结合部分”内的结合片段的示例包括(i)Fab片段,由VL、VH、CL和CH1结构域组成的单价片段;(ii)F(ab’)2片段,包含在铰链区通过二硫键连接的两个Fab片段的二价片段;(iii)由VH和CH1结构域组成的Fd片段;(iv)由抗体的单臂的VL和VH结构域组成的Fv片段,(v)dAb片段(Ward等,(1989)Nature341:544-546,Winter等,PCT公开号WO 90/05144Al,其通过引用并入本文),其包含单可变结构域;和(vi)分离的互补决定区(CDR)。此外,尽管Fv片段的两个结构域VL和VH由分开的基因编码,但它们可以使用重组方法通过合成接头连接,所述合成接头使它们能够被制成单个蛋白质链,其中VL和VH区配对以形成单价分子(称为单链Fv(scFv);参见例如,Bird等,(1988)Science 242:423-426;和Huston等,(1988)Proc.Natl.Acad.Sci.USA 85:5879-5883)。这种单链抗体也旨在被包括在术语抗体的“抗原结合部分”内。在某些实施方案中,scFv分子可以掺入融合蛋白中。其他形式的单链抗体(例如,双抗)也被包括在内。双抗是二价双特异性抗体,其中VH和VL结构域在单个多肽链上表达,但使用的接头太短而不允许相同链上的两个结构域之间配对,从而迫使结构域与另一条链的互补结构域配对并产生两个抗原结合位点(参见例如,Holliger,P.等,(1993)Proc.Natl.Acad.Sci.USA 90:6444-6448;Poljak,R.J.等,(1994)Structure2:1121-1123)。这种抗体结合部分是本领域已知的(Kontermann和Dubel编.,AntibodyEngineering(2001)Springer-Verlag.New York.790pp.(ISBN 3-540-41354-5))。
如本文所用,术语“抗体构建体”是指包含与接头多肽或免疫球蛋白恒定区连接的本文公开的一个或多个抗原结合部分的多肽。接头多肽包含通过肽键连接的两个或更多个氨基酸残基,并被用于连接一个或多个抗原结合部分。这种接头多肽是本领域熟知的(参见例如,Holliger,P.等,(1993)Proc.Natl.Acad.Sci.USA 90:6444-6448;Poljak,R.J.,等,(1994)Structure 2:1121-1123)。免疫球蛋白恒定区指重链或轻链恒定区。抗体部分(例如,Fab和F(ab’)2片段)可以使用常规技术由全抗体制备,例如,分别由全抗体的木瓜蛋白酶或胃蛋白酶消化制备。此外,抗体、抗体部分和免疫粘附分子可使用如本文所述的标准重组DNA技术获得。
如本文所用,“分离的结合蛋白”或“分离的抗体”是指基本上不含具有不同抗原特异性的其他结合蛋白的结合蛋白,例如抗体(例如,特异性结合TAT蛋白转导结构域的分离的抗体基本上不含特异性结合除TAT蛋白转导结构域以外的抗原的抗体)。此外,分离的结合蛋白可以基本上不含其他细胞物质和/或化学物质。
术语“人源化抗体”是指抗体,其包含来自非人物种(例如,小鼠)的重链和轻链可变区序列,但其中VH和/或VL序列的至少一部分已被改变为更“人样”,即更类似于人类种系可变区序列。特别地,术语“人源化抗体”是免疫特异性结合目的抗原的抗体或其变体、衍生物、类似物或片段,其包含基本上具有人抗体的氨基酸序列的框架(FR)区和基本上具有非人抗体的氨基酸序列的互补决定区(CDR)。如本文所用,在CDR背景下的术语“基本上”是指与非人抗体CDR的氨基酸序列具有至少80%,优选至少85%、至少90%、至少95%、至少98%或至少99%同一性的氨基酸序列的CDR。人源化抗体包含基本上所有的、至少一个、通常两个可变结构域(Fab、Fab’、F(ab’)2、FabC、Fv),其中所有或基本上所有的CDR区对应于非人免疫球蛋白(即,供体抗体)的CDR区,并且所有或基本上所有的框架区是人免疫球蛋白共有序列的框架区。优选地,人源化抗体还包含免疫球蛋白恒定区(Fc)的至少一部分,通常是人免疫球蛋白的恒定区的至少一部分。在一些实施方案中,人源化抗体包含轻链以及至少重链的可变结构域。抗体还可包含重链的CH1、铰链、CH2、CH3和CH4区。在一些实施方案中,人源化抗体仅包含人源化轻链。在其他实施方案中,人源化抗体仅包含人源化重链。在特定的实施方案中,人源化抗体仅包含轻链的人源化可变结构域和/或人源化重链。
人源化抗体可选自任何类型的免疫球蛋白,包括IgM、IgG、IgD、IgA和IgE以及任何同种型,所述同种型包括但不限于IgG1、IgG2、IgG3和IgG4。人源化抗体可以包含来自多于一个类型或同种型的序列,并且可以使用本领域熟知的技术选择特定的恒定区以优化期望的效应子功能。
术语“Kabat编号”、“Kabat定义”和“Kabat标记”在本文中可互换使用。本领域中公认的这些术语是指在抗体或其抗原结合部分的重链和轻链可变区中比其他氨基酸残基更易变(即,高变)的氨基酸残基的编号系统(Kabat等,(1971)Ann.NY Acad,Sci.190:382-391和Kabat,E.A.,等,(1991)Sequences of Proteins of Immunological Interest,第五版,U.S.Department of Health and Human Services,NIH Publication No.91-3242)。对于重链可变区,高变区的范围是CDR1的氨基酸位置31至35、CDR2的氨基酸位置50至65以及CDR3的氨基酸位置95至102。对于轻链可变区,高变区的范围是CDR1的氨基酸位置24至34、CDR2的氨基酸位置50至56以及CDR3的氨基酸位置89至97。
如本文所用,术语“CDR”是指抗体可变序列内的互补决定区。在重链(HC)和轻链(LC)的每个可变区中有三个CDR,对于每个可变区而言,它们被命名为CDR1、CDR2和CDR3(或具体为HC CDR1、HC CDR2、HC CDR3、LC CDR1、LC CDR2和LC CDR3)。如本文所用,术语“CDR组”是指出现于能够结合抗原的单个可变区的三个CDR的组。这些CDR的确切边界已根据不同的系统进行不同定义。Kabat描述的系统(Kabat等,Sequences of Proteins ofImmunological Interest(National Institutes of Health,Bethesda,Md.(1987)and(1991))不仅提供了适用于抗体的任何可变区的明确的残基编号系统,而且提供了限定三个CDR的精确的残基边界。这些CDR可被称为Kabat CDR。Chothia及其同事(Chothia&Lesk,J.Mol.Biol.196:901-917(1987)和Chothia等,Nature 342:877-883(1989))发现尽管在氨基酸序列水平上具有很大的多样性,但Kabat CDR内的某些亚部分采用几乎相同的肽骨架构象。这些亚部分被命名为L1、L2和L3或H1、H2和H3,其中“L”和“H”分别指轻链区和重链区。这些区域可称为Chothia CDR,其边界与Kabat CDR重叠。Padlan(FASEB J.9:133-139(1995))和MacCallum(J Mol Biol 262(5):732-45(1996))已经描述了定义与Kabat CDR重叠的CDR的其他边界。其他CDR边界定义可能不严格遵循上述系统之一,尽管鉴于特定残基或残基组或甚至整个CDR不显著影响抗原结合的预测或实验结果,它们可能缩短或延长,但仍然与Kabat CDR重叠。本文使用的方法可以利用根据这些系统中的任一者定义的CDR,尽管优选的实施方案使用Kabat或Chothia定义的CDR。
如本文所用,术语“框架”或“框架序列”是指去除CDR的可变区的剩余序列。因为CDR序列的确切定义可以由不同的系统确定,所以框架序列的含义也具有相应的不同解释。6个CDR(轻链的CDR-L1、CDR-L2和CDR-L3以及重链的CDR-H1、CDR-H2和CDR-H3)还将轻链和重链上的框架区分为每条链上的4个子区域(FR1、FR2、FR3和FR4),其中CDR1位于FR1和FR2之间、CDR2位于FR2和FR3之间、并且CDR3位于FR3和FR4之间。在没有将特定的子区域限定为FR1、FR2、FR3或FR4的情况下,如以其他方式所提及的,框架区表示单个天然存在的免疫球蛋白链的可变区内的FR组合。如本文所用,FR表示四个子区域中的一个,并且FRs表示构成框架区的四个子区域中的两个或更多个。
人源化抗体的框架区和CDR区不需要精确地对应于亲本序列,例如,供体抗体CDR或共有框架可以通过至少一个氨基酸残基的取代、插入和/或缺失来诱变,使得该位点的CDR或框架残基不对应于供体抗体或共有框架。然而,在优选的实施方案中,这种突变不是大范围的。通常,至少80%,优选地至少85%,更优选地至少90%,并且最优选至少95%的人源化抗体残基将对应于亲本FR和CDR序列的那些。如本文所用,术语“共有框架”是指共有免疫球蛋白序列中的框架区。如本文所用,术语“共有免疫球蛋白序列”是指由相关免疫球蛋白序列家族中最频繁出现的氨基酸(或核苷酸)形成的序列(参见例如,Winnaker,FromGenes to Clones(Verlagsgesellschaft,Weinheim,Germany 1987)。在免疫球蛋白家族中,共有序列中的每个位置被该家族中该位置最频繁出现的氨基酸占据。如果两个氨基酸出现的频率相同,则共有序列中可以包括任何一个。
关于肽或多肽序列的“百分比(%)氨基酸序列同一性”被定义为在序列比对并引入缺口(如果需要)以获得最大百分比序列同一性后,候选序列中的与特定肽或多肽序列中的氨基酸残基相同的氨基酸残基的百分比,不考虑视为序列相同的部分的任何保守取代。以测定百分比氨基酸同一性为目的的比对可通过本领域内技术人员已知的多种方式实现,例如,使用公开可用的计算机软件,例如BLAST、BLAST-2、ALIGN或Megalign(DNASTAR)软件。本领域内技术人员可以确定用于测量比对的适当参数,其中包括在进行比较的序列的全长上实现最大比对所需的任何算法。
术语“多价抗体”在本文中用于表示包含两个或更多个抗原结合位点的抗体。在某些实施方案中,多价抗体可以被工程化以具有三个或更多个抗原结合位点,并且通常不是天然存在的抗体。
术语“多特异性抗体”指能够结合两种或更多种不相关抗原的抗体。
术语“双重可变结构域”或“DVD”在本文中可互换使用,其是包含两个或更多个抗原结合位点的抗原结合蛋白,并且是四价或多价结合蛋白。这种DVD可以是单特异性的(即能够结合一种抗原),或者是多特异性的(即能够结合两种或更多种抗原)。包含两条重链DVD多肽和两条轻链DVD多肽的DVD结合蛋白被称为DVD Ig。DVD Ig的每一半包含重链DVD多肽、轻链DVD多肽和两个抗原结合位点。每个结合位点包含重链可变区和轻链可变区,具有参与每个抗原结合位点的抗原结合的总共6个CDR。在一个实施方案中,本文所述的CDR被用于抗TAT DVD。
术语“活性”包括结合蛋白(例如,抗体)对于抗原的活性,例如结合特异性/亲和力,例如,抗TAT-抗体结合TAT蛋白转导结构域抗原的活性。在一个实施方案中,抗TAT抗体活性包括但不限于体外结合至TAT蛋白转导结构域;体内结合至TAT蛋白转导结构域;以及减少或抑制HIV感染。
术语“表位”是指由结合蛋白(例如,抗体或抗体部分)结合的抗原区域。在某些实施方案中,表位决定簇包括分子的化学活性表面基团,例如氨基酸、糖侧链、磷酰基或磺酰基,并且在某些实施方案中,可以具有特定的三维结构特征和/或特定的电荷特征。在某些实施方案中,当抗体在蛋白质和/或大分子的复杂混合物中优先识别其靶抗原时,称为抗体特异性结合抗原。
如本文所用,术语“表面等离子体共振”是指一种光学现象,其允许通过检测生物传感器基质内蛋白质浓度的变化来分析实时生物特异性相互作用,例如使用BIAcore系统(Pharmacia Biosensor AB,Uppsala,Sweden and Piscataway,NJ)。有关进一步的描述,参见U.等,(1993)Ann.Biol.Clin.51:19-26;U.等,(1991)Biotechniques 11:620-627;Johnsson,B.等,(1995)J.Mol.Recognit.8:125-131;和Johnnson,B.等,(1991)Anal.Biochem.198:268-277。
如本文所用,术语“kon”或“ka”是指抗体与抗原结合形成抗体/抗原复合物的结合速率常数。
如本文所用,术语“koff”或“kd”是指抗体从抗体/抗原复合物解离的解离速率常数。
如本文所用,术语“KD”是指特定抗体-抗原相互作用的平衡解离常数。KD由ka/kd计算。
如本文所用,术语“竞争性结合”是指第一抗体与第二抗体竞争第三分子(例如抗原)上的结合位点的情况。在一个实施方案中,使用FACS分析测定两种抗体之间的竞争性结合。
术语“竞争性结合测定”是用于测定两种或更多种抗体是否结合同一表位的测定。在一个实施方案中,竞争性结合测定是竞争性萦光激活细胞分选(FACS)测定,其被用于通过测定标记抗体的萦光信号是否由于引入非标记抗体而减少来测定两种或更多种抗体是否结合同一表位,其中对同一表位的竞争性将降低萦光水平。
如本文所用,术语“标记的结合蛋白”是指被掺入标记的结合蛋白,例如抗体,所述标记提供了结合蛋白或靶部分的识别。优选地,标记是可检测的标记物,例如掺入放射性标记的氨基酸或附着至可通过标记的亲和素(例如,包含可通过光学或比色方法检测的萦光标记物或酶活性的链霉亲和素)检测的生物素部分的多肽。多肽的标记的示例包括但不限于以下:放射性同位素或放射性核素(例如,3H、14C、35S、90Y、99Tc、111In、125I、131I、177Lu、166Ho或153Sm);萦光标记(例如FITC、罗丹明、镧系元素磷光体),酶标记(例如,辣根过氧化物酶、萦光素酶、碱性磷酸酶);化学发光标记物;生物素基团;生物素、地高辛、由第二报道子识别的预定多肽表位(例如,亮氨酸拉链对序列、第二抗体的结合位点、金属结合结构域、表位标签);和磁性剂,例如钆螯合物。
如本文所用,术语“多核苷酸”是指两种或更多种核苷酸(核糖核苷酸或脱氧核苷酸,或任何一种核苷酸的修饰形式)的聚合形式。该术语包括DNA的单链和双链形式,但优选双链DNA。
如本文所用,术语“分离的多核苷酸”应意指多核苷酸(例如,基因组、cDNA或合成来源或其某一组合的多核苷酸),由于其来源,所述“分离的多核苷酸”:与自然界中发现的“分离的多核苷酸”的多核苷酸的全部或部分不相关;与其自然界中不连接的多核苷酸可操作地连接;或不作为较大序列的一部分出现在自然界中。
如本文所用,术语“载体”是指能够转运与其连接的另一个核酸的核酸分子。载体的一种类型是“质粒”,它是指环状的双链DNA环,其中可以连接另外的DNA片段。载体的另一种类型是病毒载体,其中另外的DNA片段可以连接至病毒基因组中。某些载体能够在引入它们的宿主细胞中自主复制(例如,具有细菌复制起点的细菌载体和游离型哺乳动物载体)。其他载体(例如,非游离型哺乳动物载体)可在被引入宿主细胞后整合到宿主细胞的基因组中,从而与宿主基因组一起复制。此外,某些载体能够指导与其可操作地连接的基因的表达。这种载体在本文中被称为“重组表达载体”(或简称为“表达载体”)。通常,重组DNA技术中使用的表达载体通常是质粒的形式。在本说明书中,“质粒”和“载体”可以互换使用,因为质粒是最常用的载体形式。然而,本发明旨在包括此类其他形式的表达载体,例如病毒载体(例如,复制缺陷型逆转录病毒、腺病毒和腺相关病毒),它们具有等同的功能。示例性载体包括例如,pcDNA、pTT、pTT3、pEFBOS、pBV、pJV、pBJ、pGEX、VSV、pBR322、pCMV-HA、pEN、YAC、BAC、噬菌体λ、噬菌粒、pCAS9、pCEN6、pYESIL、p3HPRTl、pFN2A、pBC、pTZ、pGEM、pGEMK、pEX、pSAR、pCEP、黏性质粒、pBluescript、pKJK、pFloxin、pCP、pHR、pUC和pMAL。其他质粒包括在国际公开第WO2005108568号中,其内容通过引用并入本文。
术语“可操作地连接”是指并置,其中所描述的组分处于允许它们以其预期方式起作用的关系。与编码序列“可操作地连接”的控制序列以在与控制序列相容的条件下实现编码序列表达的方式连接。“可操作地连接的”序列包括与目的基因相邻的表达控制序列和以反式或以一定距离作用以控制目的基因的表达控制序列。如本文所用,术语“表达控制序列”是指影响它们所连接的编码序列的表达和加工所必需的多核苷酸序列。表达控制序列包括适当的转录起始、终止、启动子和增强子序列;有效的RNA加工信号例如剪接和聚腺苷酸化信号;稳定细胞质mRNA的序列;提高翻译效率的序列(即,Kozak共有序列);增强蛋白质稳定性的序列;以及当需要时,增强蛋白质分泌的序列。这种控制序列的性质因宿主有机体而不同;在原核生物中,这种控制序列通常包括启动子、核糖体结合位点和转录终止序列;在真核生物中,这种控制序列通常包括启动子和转录终止序列。术语“控制序列”旨在包括其存在是表达和加工所必需的组分,并且还可以包括其存在是有利的其他组分,例如前导序列和融合配偶体序列。本发明的蛋白构建体可以使用本领域内已知的表达载体和宿主细胞表达和纯化,包括表达盒、载体、重组宿主细胞以及用于重组表达和蛋白酶解加工来自单个开放阅读框的重组多蛋白和前蛋白的方法(例如,WO2007/014162,其通过引用并入本文)。
如本文定义,“转化”是指外源DNA进入宿主细胞的任何程序。转化可以在天然或人工条件下使用本领域众所周知的各种方法进行。转化可依赖于任何已知的将外源核酸序列插入原核或真核宿主细胞的方法。根据被转化的宿主细胞来选择方法,并且所述方法可包括但不限于病毒感染、电穿孔、脂质转染和基因枪法。这种“转化的”细胞包括稳定转化的细胞,其中插入的DNA能够作为自主复制质粒或作为宿主染色体的一部分复制。它们还包括在有限时间内瞬时表达插入的DNA或RNA的细胞。
如本文所用,术语“重组宿主细胞”(或简称为“宿主细胞”)是指已引入外源DNA的细胞。应当理解,这种术语不仅意指特定的受试细胞,而且意指这种细胞的后代。因为可能由于突变或环境影响而在随后的世代中发生某些修饰,这样的后代可能实际上与亲本细胞不同,但仍然包含在本文所用的术语“宿主细胞”的范围内。优选地,宿主细胞包括选自任何生命界的原核和真核细胞。优选的真核细胞包括原生生物、真菌、植物和动物细胞。最优选地,宿主细胞包括但不限于原核细胞系大肠杆菌;哺乳动物细胞系CHO、HEK 293和COS;昆虫细胞系Sf9;以及真菌细胞,酿酒酵母。
标准技术可用于重组DNA、寡核苷酸合成以及组织培养和转化(例如,电穿孔、脂质转染)。酶促反应和纯化技术可以根据制造商的说明书或本领域通常实现的或如本文所述进行。前述技术和程序通常可以按照本领域内众所周知的以及如本说明书中引用和讨论的各种综合和更具体的参考文献中所描述的常规方法进行。参见例如,Sambrook等,Molecular Cloning:A Laboratory Manual(2d ed.,Cold Spring Harbor LaboratoryPress,Cold Spring Harbor,N.Y.(1989)),其出于任何目的通过引用并入本文。
如本文所用,术语“样品”以其最广泛的含义使用。如本文所用,“生物样品”包括但不限于来自存活的生物或先前存活的生物的任何量的物质。这些存活的生物包括但不限于人、小鼠、大鼠、猴、狗、兔和其他动物。这些物质包括但不限于血液、血清、尿液、滑液、细胞、器官、组织、骨髓、淋巴结和脾脏。
通过本发明方法治疗的“患者”或“受试者”可以指人或非人动物,优选哺乳动物。“受试者”是指任何动物,包括马、狗、猫、猪、山羊、兔、仓鼠、猴、豚鼠、大鼠、小鼠、蜥蜴、蛇、绵羊、牛、鱼和鸟。人类受试者可称为患者。应当注意,本文所述的临床观察是对人类受试者进行的,并且在至少一些实施方案中,受试者是人类。
术语“病症”和“疾病”是包容性地使用并且是指身体的任何部分、器官或系统(或其任何组合)自正常结构或功能出现的任何偏差。具体的疾病表现为特征性的症状和体征,包括生物、化学和物理变化,并且通常与多种其他因素有关,所述其他因素包括但不限于人口统计学、环境、就业、遗传和病史因素。某些特征性的体征、症状和相关因素可通过多种方法量化以产生重要的诊断信息。如本文所用,“TAT相关疾病”包括人免疫缺陷病毒(HIV)感染或获得性免疫缺陷综合征(AIDS)以及由HIV感染或AIDS引起或与之相关的症状。
如本文所用,术语“人免疫缺陷病毒”或“HIV”通常是指逆转录病毒,其是获得性免疫缺陷综合征(AIDS)、其变体(例如,猴获得性免疫缺陷综合征,SAIDS)以及与AIDS或其变体相关的疾病、病状或机会性感染的致病因素,并且包括其中任何进化枝或毒株的HIV-1型(HIV-1)和HIV-2型(HIV-2)、相关逆转录病毒(例如,猴免疫缺陷病毒(SIV))及其变体(例如工程化逆转录病毒,例如嵌合HIV病毒,例如猴人免疫缺陷病毒(SHIV))。HIV以前的名称包括人嗜T淋巴细胞病毒Ill(HTLV-III)、淋巴结病相关病毒(LAV)和AIDS相关逆转录病毒(ARV)。
如本文所用,并且如本领域所熟知的,“治疗”是用于获得有益或期望的结果(例如,临床结果)的方法。有益或期望的结果可包括但不限于疾病、病症或病状(例如,HIV感染)的治愈或根除;一种或多种症状或病状(例如,HIV感染)的减轻或改善;疾病、病症或病状(例如,HIV感染)的程度的减轻;疾病、病症或病状(例如,HIV感染)的状态的稳定(即不恶化);疾病、病症或病状(例如,HIV感染)的传播或散播的预防;疾病、病症或病状(例如,HIV感染)的进展的延迟或减缓;疾病、病症或病状(例如,HIV感染)的改善或减轻;以及缓解(部分或全部),不论是否可检测到。
如本文所用,“治愈”感染逆转录病毒(例如,人免疫缺陷病毒(HIV)(例如,HIV1型或HIV2型))的受试者(例如,人)是指在不存在抗逆转录病毒治疗(ART)的情况下获得并维持病毒学控制至少两个月(例如,2个月、2.5个月、3个月、4个月、5个月、6个月、1年、1.5年、2年、3年、4年或5年或更多年)。
本文所用的术语“表达”是指从DNA产生多肽的过程。该过程涉及基因转录为mRNA和该mRNA翻译成多肽。根据使用背景,“表达”可指RNA或蛋白质或两者的产生。
如本文所用,术语“获得”在本文中被理解为制造、购买或以其他方式拥有。
现在将详细参考本发明的示例性实施方案。虽然将结合示例性实施方案描述本发明,但是应当理解,本发明并不旨在被限定为这些实施方案。相反,本发明旨在覆盖可能包括在所附权利要求限定的本发明的精神和范围内的备选方案、修改和等同物。
II.结合TAT肽的结合蛋白
本发明的一个方面提供了分离的结合蛋白,例如,抗体或其抗原结合部分,其结合TAT肽,并且特异性地结合TAT蛋白转导结构域。下文也详细描述了抗-TAT肽抗体以及制备结合蛋白的方法、产生结合蛋白的方法。
A.抗TAT肽结合蛋白
本发明的特征在于包含抗原结合结构域的结合蛋白,例如抗体,所述结合蛋白能够结合TAT肽。特别是,所述结合蛋白能够结合TAT蛋白转导结构域。新颖的抗体在本文中被统称为“TAT肽抗体”或“抗TAT抗体”。
尽管本文全文使用术语“抗体”,但应当注意,抗体部分(即,抗TAT抗体的抗原结合部分)也包括在本公开内并且可包括在全文所描述的实施方案(方法和组合物)中。例如,如本文所述,抗TAT抗体部分可与药物偶联。在某些实施方案中,抗TAT抗体结合部分是Fab、Fab’、F(ab’)2、Fv、二硫键连接的Fv、scFv、单域抗体或双抗。
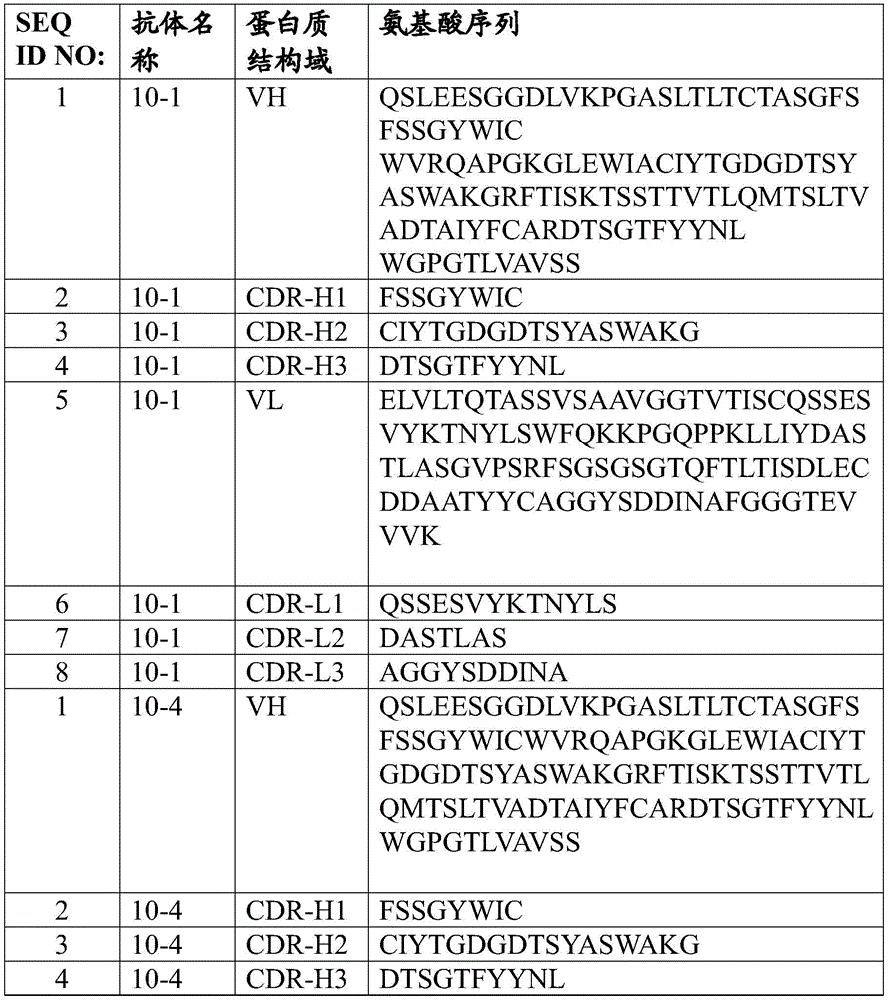
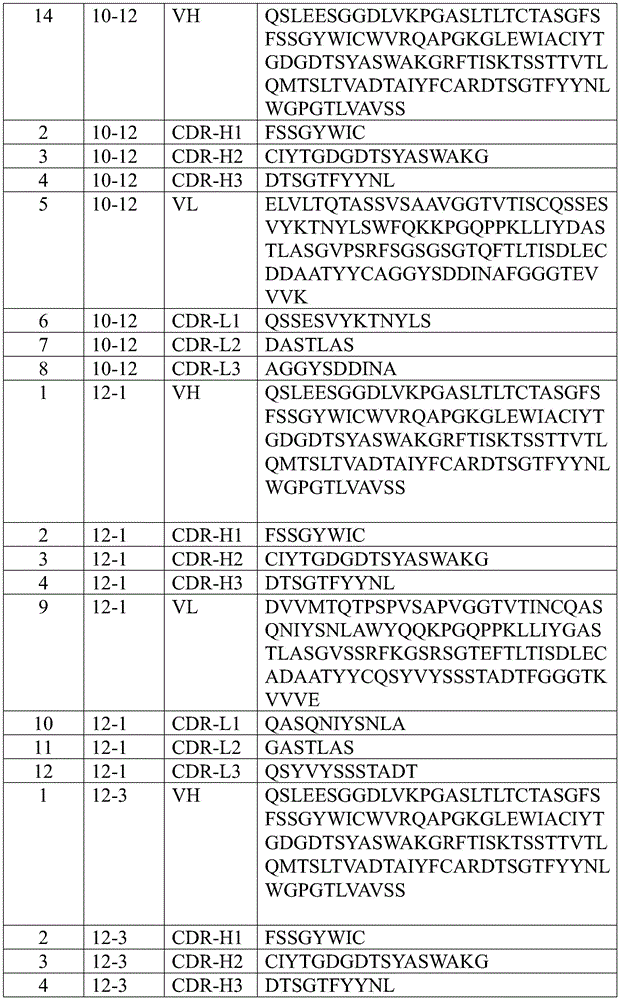
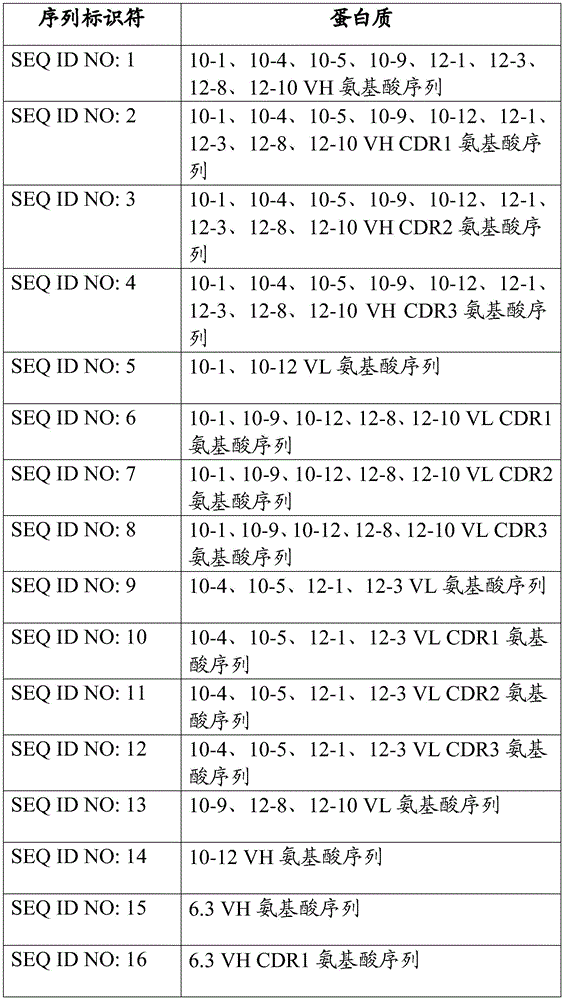
本发明优选的单克隆抗体的VH和VL区以及CDR的氨基酸序列的列表见实施例1的表1。
在一个方面,本发明的特征在于包含抗原结合结构域的结合蛋白,所述结合蛋白能够结合TAT蛋白转导结构域,所述抗原结合结构域包含含有选自由SEQ ID NO:1、14和15组成的组的氨基酸序列的重链可变区;和含有选自由5、9、13和19组成的组的氨基酸序列的轻链可变区。
在一个方面,本发明的特征在于包含抗原结合结构域的结合蛋白,所述结合蛋白能够结合TAT蛋白转导结构域,所述抗原结合结构域包含选自表1中列出的那些的重链CDR组(CDR1、CDR2和CDR3);以及选自表1中列出的那些的LC CDR组(CDR1、CDR2和CDR3)。
在一个方面,本发明的特征在于包含抗原结合结构域的结合蛋白,所述结合蛋白能够结合TAT蛋白转导结构域,所述抗原结合结构域包含含有选自由SEQ ID NO:4或SEQ IDNO:18组成的组的氨基酸序列的重链CDR3结构域。在一个实施方案中,结合蛋白还包含含有选自由SEQ ID NO:3或SEQ ID NO:17组成的组的氨基酸序列的重链CDR2结构域。在另一个实施方案中,结合蛋白还包含含有选自由SEQ ID NO:2或SEQ ID NO:16组成的组的氨基酸序列的重链CDR1结构域。在另一个实施方案中,结合蛋白还包含含有选自由SEQ ID NO:8、SEQ ID NO:12或SEQ ID NO:22组成的组的氨基酸序列的轻链CDR3结构域。在另一个实施方案中,结合蛋白还包含含有选自由SEQ ID NO:7、SEQ ID NO:11或SEQ ID NO:21组成的组的氨基酸序列的轻链CDR2结构域。在另一个实施方案中,结合蛋白还包含含有选自由SEQ IDNO:6、SEQ ID NO:10或SEQ ID NO:20组成的组的氨基酸序列的轻链CDR1结构域。
在另一个方面,本发明的特征在于包含抗原结合结构域的结合蛋白,所述结合蛋白能够结合TAT蛋白转导结构域,所述抗原结合结构域包含:重链可变区,其包含含有SEQID NO:4所示氨基酸序列的CDR3结构域,含有SEQ ID NO:3所示氨基酸序列的CDR2结构域和含有SEQ ID NO:2所示氨基酸序列的CDR1结构域,或重链可变区,其包含含有SEQ ID NO:18所示氨基酸序列的CDR3结构域,含有SEQ ID NO:17所示氨基酸序列的CDR2结构域和含有SEQ ID NO:16所示氨基酸序列的CDR1结构域;和轻链可变区,其包含含有SEQ ID NO:8所示氨基酸序列的CDR3结构域,含有SEQ ID NO:7所示氨基酸序列的CDR2结构域和含有SEQ IDNO:6所示氨基酸序列的CDR1结构域,或轻链可变区,其包含含有SEQ ID NO:12所示氨基酸序列的CDR3结构域,含有SEQ ID NO:11所示氨基酸序列的CDR2结构域和含有SEQ ID NO:10所示氨基酸序列的CDR1结构域,或轻链可变区,其包含含有SEQ ID NO:22所示氨基酸序列的CDR3结构域,含有SEQ ID NO:21所示氨基酸序列的CDR2结构域和含有SEQ ID NO:20所示氨基酸序列的CDR1结构域。
在其他方面,本发明的特征还在于包含抗原结合结构域的结合蛋白,所述结合蛋白能够结合TAT蛋白转导结构域,所述抗原结合结构域包含:重链可变区,其包含含有SEQID NO:4的氨基酸序列的CDR3结构域,含有SEQ ID NO:3的氨基酸序列的CDR2结构域和含有SEQ ID NO:2的氨基酸序列的CDR1结构域;和轻链可变区,其包含含有SEQ ID NO:8的氨基酸序列的CDR3结构域,含有SEQ ID NO:7的氨基酸序列的CDR2结构域和含有SEQ ID NO:6的氨基酸序列的CDR1结构域。
在其他方面,本发明的特征还在于包含抗原结合结构域的结合蛋白,所述结合蛋白能够结合TAT蛋白转导结构域,所述抗原结合结构域包含:重链可变区,其包含含有SEQID NO:4的氨基酸序列的CDR3结构域,含有SEQ ID NO:3的氨基酸序列的CDR2结构域和含有SEQ ID NO:2的氨基酸序列的CDR1结构域;和轻链可变区,其包含含有SEQ ID NO:12的氨基酸序列的CDR3结构域,含有SEQ ID NO:11的氨基酸序列的CDR2结构域和含有SEQ ID NO:10的氨基酸序列的CDR1结构域。
在其他方面,本发明的特征还在于包含抗原结合结构域的结合蛋白,所述结合蛋白能够结合TAT蛋白转导结构域,所述抗原结合结构域包含:重链可变区,其包含含有SEQID NO:18的氨基酸序列的CDR3结构域,含有SEQ ID NO:17的氨基酸序列的CDR2结构域和含有SEQ ID NO:16的氨基酸序列的CDR1结构域;和轻链可变区,其包含含有SEQ ID NO:22的氨基酸序列的CDR3结构域,含有SEQ ID NO:21的氨基酸序列的CDR2结构域和含有SEQ IDNO:20的氨基酸序列的CDR1结构域。
在进一步的实施方案中,抗原结合结构域包含含有SEQ ID NO:1所示氨基酸序列的重链可变区和含有SEQ ID NO:5所示氨基酸序列的轻链可变区。
在另一个进一步的实施方案中,抗原结合结构域包含含有SEQ ID NO:1所示氨基酸序列的重链可变区和含有SEQ ID NO:9所示氨基酸序列的轻链可变区。
在另一个进一步的实施方案中,抗原结合结构域包含含有SEQ ID NO:1所示氨基酸序列的重链可变区和含有SEQ ID NO:13所示氨基酸序列的轻链可变区。
在另一个进一步的实施方案中,抗原结合结构域包含含有SEQ ID NO:14所示氨基酸序列的重链可变区和含有SEQ ID NO:5所示氨基酸序列的轻链可变区。
在另一个进一步的实施方案中,抗原结合结构域包含含有SEQ ID NO:15所示氨基酸序列的重链可变区和含有SEQ ID NO:19所示氨基酸序列的轻链可变区。
在某些实施方案中,术语“10-1”是指产生抗体的杂交瘤,所述抗体包含(i)具有包含SEQ ID NO:1的氨基酸序列的一个可变重链;和(ii)具有包含SEQ ID NO:5的氨基酸序列的一个可变轻链。在某些实施方案中,10-1重链可变区包含含有SEQ ID NO:4的氨基酸序列的CDR3结构域、含有SEQ ID NO:3的氨基酸序列的CDR2结构域和含有SEQ ID NO:2的氨基酸序列的CDR1结构域,且轻链可变区包含含有SEQ ID NO:8的氨基酸序列的CDR3结构域、含有SEQ ID NO:7的氨基酸序列的CDR2结构域和含有SEQ ID NO:6的氨基酸序列的CDR1结构域。在某些实施方案中,如通过表面等离子体共振所测量,抗体10-1可具有至少约1×104M-1s-1至约6×106M-1s-1的对TAT蛋白转导结构域的结合速率常数(KON)。在其他实施方案中,如通过表面等离子体共振所测量,根据本发明的结合蛋白可具有至少约2.7×105M-1s-1的对TAT蛋白转导结构域的结合速率常数(KON)。在其他实施方案中,根据本发明的结合蛋白可具有1.0×10-12s-1或更低的对TAT蛋白转导结构域的解离常数(KD)。在某些优选的实施方案中,本发明的结合蛋白具有约1.0×10-7s-1或更低;1.0×10-8s-1或更低;1.0×10-9s-1或更低;1.0×10-10s-1或更低;1.0×10-11s-1或更低;和1.0×10-12s-1或更低的对TAT蛋白转导结构域的解离常数(KD)。根据本发明的优选实施方案,由10-1杂交瘤克隆产生的抗体构建体的同种型是IgG1K。
在一些实施方案中,抗TAT抗体或其抗原结合部分包含:含有SEQ ID NO:1所示氨基酸序列或与SEQ ID NO:1具有至少90%、95%、96%、97%、98%或99%同一性的序列的重链,和/或含有SEQ ID NO:5所示氨基酸序列或与SEQ ID NO:5具有至少90%、95%、96%、97%、98%或99%同一性的序列的轻链。
在某些实施方案中,术语“10-12”是指产生抗体的杂交瘤,所述抗体包含(i)具有包含SEQ ID NO:14的氨基酸序列的一个可变重链;和(ii)具有包含SEQ ID NO:5的氨基酸序列的一个可变轻链。在某些实施方案中,10-12重链可变区包含含有SEQ ID NO:4的氨基酸序列的CDR3结构域、含有SEQ ID NO:3的氨基酸序列的CDR2结构域和含有SEQ ID NO:2的氨基酸序列的CDR1结构域,且轻链可变区包含含有SEQ ID NO:8的氨基酸序列的CDR3结构域、含有SEQ ID NO:7的氨基酸序列的CDR2结构域和含有SEQ ID NO:6的氨基酸序列的CDR1结构域。在某些实施方案中,如通过表面等离子体共振所测量,抗体10-12可以具有至少约1×104M-1s-1至约6×106M-1s-1的对TAT蛋白转导结构域的结合速率常数(KON)。在其他实施方案中,如通过表面等离子体共振所测量,根据本发明的结合蛋白可具有至少约2.7×105M- 1s-1的对TAT蛋白转导结构域的结合速率常数(KON)。在其他实施方案中,根据本发明的结合蛋白可具有1.0×10-12s-1或更低的对TAT蛋白转导结构域的解离常数(KD)。在某些优选的实施方案中,根据本发明的结合蛋白具有约1.0×10-7s-1或更低;1.0×10-8s-1或更低;1.0×10-9s-1或更低;1.0×10-10s-1或更低;1.0×10-11s-1或更低;和1.0×10-12s-1或更低的对TAT蛋白转导结构域的解离常数(KD)。根据本发明的优选实施方案,由10-12杂交瘤克隆产生的抗体构建体的同种型是IgG1K。
在一些实施方案中,抗TAT抗体或其抗原结合部分包含:含有SEQ ID NO:14所示氨基酸序列或与SEQ ID NO:14具有至少90%、95%、96%、97%、98%或99%同一性的序列的重链,和/或含有SEQ ID NO:5所示氨基酸序列或与SEQ ID NO:5具有至少90%、95%、96%、97%、98%或99%同一性的序列的轻链。
在某些实施方案中,术语“10-4”、“10-5”、“12-1”和“12-3”是指产生抗体的杂交瘤,所述抗体包含(i)具有包含SEQ ID NO:1的氨基酸序列的一个可变重链;和(ii)具有包含SEQ ID NO:9的氨基酸序列的一个可变轻链。在某些实施方案中,10-4、10-5、12-1和12-3重链可变区包含含有SEQ ID NO:4的氨基酸序列的CDR3结构域、含有SEQ ID NO:3的氨基酸序列的CDR2结构域和含有SEQ ID NO:2的氨基酸序列的CDR1结构域,且轻链可变区包含含有SEQ ID NO:12的氨基酸序列的CDR3结构域、含有SEQ ID NO:11的氨基酸序列的CDR2结构域和含有SEQ ID NO:10的氨基酸序列的CDR1结构域。在某些实施方案中,如通过表面等离子体共振所测量,抗体10-4、10-5、12-1和12-3可以具有至少约1×104M-1s-1至约6×106M-1s-1的对TAT蛋白转导结构域的结合速率常数(KON)。在其他实施方案中,如通过表面等离子体共振所测量,根据本发明的结合蛋白可具有至少约2.7×105M-1s-1的对TAT蛋白转导结构域的结合速率常数(KON)。在其他实施方案中,根据本发明的结合蛋白可具有1.0×10-12s-1或更低的对TAT蛋白转导结构域的解离常数(KD)。在某些优选的实施方案中,根据本发明的结合蛋白具有约1.0×10-7s-1或更低;1.0×10-8s-1或更低;1.0×10-9s-1或更低;1.0×10-10s-1或更低;1.0×10-11s-1或更低;和1.0×10-12s-1或更低的对TAT蛋白转导结构域的解离常数(KD)。根据本发明的优选实施方案,由10-4、10-5、12-1和12-3杂交瘤克隆产生的抗体构建体的同种型是IgG1/K。
在一些实施方案中,抗TAT抗体或其抗原结合部分包含:含有SEQ ID NO:1所示氨基酸序列或与SEQ ID NO:1具有至少90%、95%、96%、97%、98%或99%同一性的序列的的重链,和/或含有SEQ ID NO:9所示氨基酸序列或与SEQ ID NO:9具有至少90%、95%、96%、97%、98%或99%同一性的序列的轻链。
在某些实施方案中,术语“10-9”、“12-8”和“12-10”是指产生抗体的杂交瘤,所述抗体包含(i)具有包含SEQ ID NO:1的氨基酸序列的一个可变重链;和(ii)具有包含SEQ IDNO:13的氨基酸序列的一个可变轻链。在某些实施方案中,10-9、12-8和12-10重链可变区包含含有SEQ ID NO:4的氨基酸序列的CDR3结构域、含有SEQ ID NO:3的氨基酸序列的CDR2结构域和含有SEQ ID NO:2的氨基酸序列的CDR1结构域,且轻链可变区包含含有SEQ ID NO:8的氨基酸序列的CDR3结构域、含有SEQ ID NO:7的氨基酸序列的CDR2结构域和含有SEQ IDNO:6的氨基酸序列的CDR1结构域。在某些实施方案中,如通过表面等离子体共振所测量,抗体10-9、12-8和12-10可以具有至少约1×104M-1s-1至约6×106M-1s-1的对TAT蛋白转导结构域的结合速率常数(KON)。在其他实施方案中,如通过表面等离子体共振所测量,根据本发明的结合蛋白可具有至少约2.7×105M-1s-1的对TAT蛋白转导结构域的结合速率常数(KON)。在其他实施方案中,根据本发明的结合蛋白可具有1.0×10-12s-1或更低的对TAT蛋白转导结构域的解离常数(KD)。在某些优选的实施方案中,根据本发明的结合蛋白具有约1.0×10-7s-1或更低;1.0×10-8s-1或更低;1.0×10-9s-1或更低;1.0×10-10s-1或更低;1.0×10-11s-1或更低;和1.0×10-12s-1或更低的对TAT蛋白转导结构域的解离常数(KD)。根据本发明的优选实施方案,由10-9、12-8和12-10杂交瘤克隆产生的抗体构建体的同种型是IgG1/K。
在一些实施方案中,抗TAT抗体或其抗原结合部分包含:含有SEQ ID NO:1所示氨基酸序列或与SEQ ID NO:1具有至少90%、95%、96%、97%、98%或99%同一性的序列的重链,和/或含有SEQ ID NO:13所示氨基酸序列或与SEQ ID NO:13具有至少90%、95%、96%、97%、98%或99%同一性的序列的轻链。
在某些实施方案中,术语“6.3”是指产生抗体的杂交瘤,所述抗体包含(i)具有包含SEQ ID NO:14的氨基酸序列的一个可变重链;和(ii)具有包含SEQ ID NO:5的氨基酸序列的一个可变轻链。在某些实施方案中,6.3重链可变区包含含有SEQ ID NO:4的氨基酸序列的CDR3结构域、含有SEQ ID NO:3的氨基酸序列的CDR2结构域和含有SEQ ID NO:2的氨基酸序列的CDR1结构域,且轻链可变区包含含有SEQ ID NO:8的氨基酸序列的CDR3结构域、含有SEQ ID NO:7的氨基酸序列的CDR2结构域和含有SEQ ID NO:6的氨基酸序列的CDR1结构域。在某些实施方案中,如通过表面等离子体共振所测量,抗体6.3可具有至少约1×104M- 1s-1至约6×106M-1s-1的对TAT蛋白转导结构域的结合速率常数(KON)。在其他实施方案中,如通过表面等离子体共振所测量,根据本发明的结合蛋白可具有至少约2.7×105M-1s-1的对TAT蛋白转导结构域的结合速率常数(KON)。在其他实施方案中,根据本发明的结合蛋白可具有1.0×10-12s-1或更低的对TAT蛋白转导结构域的解离常数(KD)。在某些优选的实施方案中,根据本发明的结合蛋白具有约1.0×10-7s-1或更低;1.0×10-8s-1或更低;1.0×10-9s-1或更低;1.0×10-10s-1或更低;1.0×10-11s-1或更低;和1.0×10-12s-1或更低的对TAT蛋白转导结构域的解离常数(KD)。根据本发明的优选实施方案,由6.3杂交瘤克隆产生的抗体构建体的同种型是IgG21K。
在一些实施方案中,抗TAT抗体或其抗原结合部分包含:含有SEQ ID NO:15所示氨基酸序列或与SEQ ID NO:15具有至少90%、95%、96%、97%、98%或99%同一性的序列的重链,和/或含有SEQ ID NO:19所示氨基酸序列或与SEQ ID NO:19具有至少90%、95%、96%、97%、98%或99%同一性的序列的轻链。
根据本发明的优选实施方案,本文所述的结合蛋白是抗体。
因此,本发明的特征在于包含本文所述结合蛋白的抗体构建体,其中所述抗体构建体还包含接头多肽或免疫球蛋白恒定区。
根据本发明的抗体构建体可包含选自由以下组成的组的重链免疫球蛋白恒定区:IgM恒定区、IgG4恒定区、IgG1恒定区、IgE恒定区、IgG2恒定区、IgG3恒定区和IgA恒定区。
此外,抗体可以包含轻链恒定区(κ轻链恒定区或λ轻链恒定区)。
在某些实施方案中,如通过表面等离子体共振所测量,根据本发明的结合蛋白可以具有选自由约1×104M-1s-1至约6×106M-1s-1组成的组的对TAT蛋白转导结构域的结合速率常数(KON)。在其他实施方案中,如通过表面等离子体共振所测量,根据本发明的结合蛋白可以具有至少约2.5×105M-1s-1和至少约2.7×105M-1s-1的对TAT肽的结合速率常数(KON)。
在其他实施方案中,根据本发明的结合蛋白可以具有的对TAT蛋白转导结构域的解离常数(KD)选自由以下组成的组:约1.0×10-7s-1或更低;1.0×10-8s-1或更低;1.0×10- 9s-1或更低;1.0×10-10s-1或更低;1.0×10-11s-1或更低;和1.0×10-12s-1或更低。在某些优选的实施方案中,根据本发明的结合蛋白具有1.0×10-7s-1或更低的对TAT肽的解离常数(KD)。
结合蛋白可选自免疫球蛋白分子、单克隆抗体、鼠抗体、嵌合抗体、CDR移植抗体、人源化抗体、单域抗体、Fv、二硫键连接的Fv、scFv、双抗、Fab、Fab’、F(ab’)2、多特异性抗体、双重特异性抗体和双特异性抗体。
或者,抗体部分可以是例如Fab片段或单链Fv片段。
Fc部分中替换氨基酸残基以改变抗体效应子功能是本领域已知的(Winter等,美国专利第5,648,260号;第5624821号)。抗体的Fc部分介导几种重要的效应子功能,例如,细胞因子诱导、ADCC、吞噬作用、补体依赖性细胞毒性(CDC)以及抗体和抗原-抗体复合物的半衰期/清除率。在一些情况下,这些效应子功能是治疗性抗体所需的,但在其他情况下可能是不必要的或甚至是有害的,这取决于治疗目的。某些人IgG同种型,特别是IgG1和IgG3,它们分别通过结合FcγR和补体C1q介导ADCC和CDC。新生儿Fc受体(FcRn)是决定抗体循环半衰期的关键组分。在另一个实施方案中,抗体的恒定区(例如抗体的Fc区)中至少一个氨基酸残基被替换,使得抗体的效应子功能被改变。
一个实施方案提供了标记的结合蛋白,其中本发明的抗体或抗体部分是衍生的一个或多个功能分子或货物分子或与一个或多个功能分子或货物分子连接。在一个实施方案中,货物部分是另一种肽或蛋白质,例如,共济蛋白多肽。在一个实施方案中,货物部分是选自下组的多肽:阿巴瑞克、阿巴西普、阿昔单抗、阿达木单抗、阿柏西普、阿加糖酶β、阿比鲁肽、阿地白介素、阿法西普、阿仑单抗、阿仑单抗、阿糖苷酶、阿糖苷酶α、阿利罗单抗、阿利吉仑α-1-蛋白酶抑制剂、阿替普酶、阿那白滞素、安塞司亭、阿尼替普酶、炭疽人免疫球蛋白、抗血友病因子、抗抑制剂凝血复合物、抗凝血酶α、人抗凝血酶III、抗胸腺细胞球蛋白、抗胸腺细胞球蛋白(马)、抗胸腺细胞球蛋白(兔)、抑肽酶、阿西莫单抗、阿司福酶α、天冬酰胺酶、菊欧文氏菌天冬酰胺酶(Asparaginase Erwinia Chrysanthemi)、阿特珠单抗、自体培养的软骨细胞、巴利昔单抗、贝卡普勒明、贝拉西普、贝利单抗、贝拉克坦、贝伐单抗、比伐卢定、博纳吐单抗、A型肉毒杆菌毒素、B型肉毒杆菌毒素、布伦妥昔单抗、布罗达鲁单抗、布舍瑞林、C1酯酶抑制剂(人)、Cl酯酶抑制剂(重组)、卡那奴单抗、卡那奴单抗、卡普马布、赛妥珠单抗、西妥昔单抗、绒毛膜促性腺激素α、绒毛膜促性腺激素(人)、绒毛膜促性腺激素(重组)、凝血因子IX、凝血因子VIIa、人凝血因子X、凝血因子XIII A-亚基(重组)、胶原酶、阿法可奈司他、促肾上腺皮质激素、促皮质素、达珠单抗、达托霉素、达雷木单抗、达贝泊汀阿尔法、去纤维肽、地尼白介素、地诺单抗、地西卢定、地高辛免疫Fab(绵羊)、地妥昔单抗、阿法链道酶、替加色罗α、度拉鲁肽、依库珠单抗、依法珠单抗、艾芙莫罗凝血素α、依洛硫酸酯酶α、埃洛珠单抗、恩夫韦肽、依泊汀α、依泊汀δ、依替巴肽、依那西普、依洛尤单抗、艾塞那肽、因子IX复合物(人)、纤维蛋白原浓缩物(人)、纤维蛋白溶解素(纤溶酶)、非格司亭、非格司亭-sndz、促卵泡素α、促卵泡素β、加硫酶、胃内因子、吉妥珠单抗奥佐米星、醋酸格拉替雷、重组胰高血糖素、葡糖苷酶、戈利木单抗、短杆菌肽D、甲型肝炎疫苗、乙型肝炎免疫球蛋白、人降钙素、人破伤风梭菌类毒素免疫球蛋白、人狂犬病病毒免疫球蛋白、人Rho(D)免疫球蛋白、人血清白蛋白、人水痘-带状疱疹免疫球蛋白、透明质酸酶,透明质酸酶(人重组),伊布单抗、替伊莫单抗、依达珠单抗、艾度硫酸酯酶、伊米苷酶、人免疫球蛋白、英夫利昔单抗、门冬胰岛素、胰岛素、吉妥珠单抗奥佐米星、醋酸格拉替雷、重组胰高血糖素、葡糖苷酶(Glucarpidase)、戈利木单抗、短杆菌肽D、甲型肝炎疫苗、乙型肝炎免疫球蛋白、人降钙素、人破伤风梭菌类毒素免疫球蛋白、人狂犬病病毒免疫球蛋白、人Rho(D)免疫球蛋白、人血清白蛋白、人水痘-带状疱疹免疫球蛋白、透明质酸酶、透明质酸酶(人重组)、伊布单抗、替伊莫单抗、依达珠单抗、艾度硫酸酯酶、伊米苷酶、人免疫球蛋白、英夫利昔单抗、门冬胰岛素、牛胰岛素、德谷胰岛素、地特胰岛素、甘精胰岛素、谷赖胰岛素、赖脯胰岛素、猪胰岛素、普通胰岛素、胰岛素(猪)、胰岛素-异佛烷(Insulin-isophane)、干扰素α-2a重组型、干扰素α-2b、干扰素alfacon-1、干扰素α-nl、干扰素α-n3、干扰素β-la、干扰素β-lb、干扰素γ-lb、静脉注射免疫球蛋白、易普利姆玛、伊克珠单抗、拉瑞诺酶、来格司亭、来匹卢定、亮丙瑞林、利拉鲁肽、芦西纳坦、重组人黄体刺激素、美卡舍明、促性腺激素、美泊利单抗、甲氧基聚乙二醇-依泊汀β、美曲普汀、莫罗莫纳布、那他珠单抗、天然α干扰素或多铁素、耐妥尤单抗、奈西立肽、纳武单抗、奥比妥昔单抗、奥比妥珠单抗、奥克纤溶酶、奥法木单抗、奥马珠单抗、奥普瑞白介素、OspA脂蛋白、催产素、帕利弗明、帕利珠单抗、胰脂肪酶、帕尼单抗、牛培加酶、哌加他尼、培门冬酶、培非格司亭、聚乙二醇干扰素α-2a、聚乙二醇干扰素α-2b、聚乙二醇干扰素β-1a、培戈洛酶、培维索孟、派姆单抗、帕妥珠单抗、猪肺磷脂(Poractant alfa)、普兰林肽、Preotact、硫酸鱼精蛋白、人蛋白S、凝血酶原复合物浓缩物、豚草花粉提取物、雷莫芦单抗、雷珠单抗、拉布立酶、雷昔单抗、瑞替普酶、利罗那西普、利妥昔单抗、罗米波司亭、糖苷酶、鲑鱼降钙素、沙格司亭、沙妥莫单抗喷地肽、Sebelipase alfa、分泌素、苏金单抗、舍莫瑞林、血清白蛋白、碘化血清白蛋白、司妥昔单抗、塞莫凝血素α、Sipuleucel-T、生长激素重组体、生长激素重组体、链激酶、舒洛地特、重组蛋白舒索凝血素α、他利苷酶α、替度鲁肽、替考拉宁、替奈普酶、特立帕肽、特沙莫林、血栓调节素阿尔法、胸腺素、甲状腺球蛋白、促甲状腺素α、托珠单抗、托西莫单抗、曲妥珠单抗、结核菌素纯化蛋白衍生物、妥罗凝血素α、尿促卵泡素、尿激酶、优特克单抗、加压素、维多珠单抗、维拉苷酶α、血栓调节素α、胸腺嘧啶、甲状腺球蛋白、甲状腺激素、托西珠单抗、托西单抗、曲妥珠单抗、结核菌素纯化蛋白衍生物、妥罗凝血素α、尿促卵泡素、尿激酶、优特克单抗、加压素、维多珠单抗、维拉苷酶α。
在另一个实施方案中,蛋白质选自包括在Raghava,Gajendra P.S.;Usmani,Salman Sadullah;Bedi,Gursimran;Samuel,Jesse S.;Singh,Sandeep;Kalra,Sourav等(2017):THPdb:Database of FDA Approved Peptide and Protein Therapeutics中的那些,它们的内容通过引用并入本文。
在另一个实施方案中,货物部分是药理学活性化合物、小分子、脂质体包封蛋白、放射性核素或放射性核素标记的化合物、核酸(例如,siRNA、shRNA、miRNA、硫代磷酸酯修饰的RNA、适配体、磷酰二胺吗啉代寡核苷酸(PMO)或其任何组合)。例如,本发明的标记的结合蛋白可以通过将本发明的抗体或抗体部分(通过化学偶联、遗传融合、非共价结合或其他方式)与一个或多个其他分子实体(例如,另一抗体(例如,双特异性抗体或双抗)、可检测的试剂、药剂、可以介导抗体或抗体部分与另一分子(例如,链霉亲和素核心区域或多组氨酸标签)结合的蛋白质或肽、和/或选自由以下组成的组的细胞毒性剂或治疗剂:有丝分裂抑制剂、抗肿瘤抗生素、免疫调节剂、基因治疗的载体、烷化剂、抗血管生成剂、抗代谢药、含硼剂、化学保护剂、激素、抗激素剂、皮质类固醇、光敏治疗剂、寡核苷酸、放射性核素剂、拓扑异构酶抑制剂、酪氨酸激酶抑制剂、放射增敏剂及其组合)功能性地连接而衍生。
本发明的结合蛋白可以被固定在固体支持物上。固体支持物是本领域已知的,并且包括例如板、珠或层析树脂,例如,trisacryl、琼脂糖凝胶(sepharose)、琼脂糖(agarose)、聚丙烯酰胺、poros、poroshell、captol、toyopearl、hypercel、纤维素类型、交联葡聚糖(葡聚糖)、安伯来特、amberchrome、amberjet、dowex、optipore、supelpak、combigel、monosphere、duolite、diaion、aminolink、sulfolink、carboxylink、glycolink、marathon或glycocatch。在一个实施方案中,珠或层析树脂包含蛋白A琼脂糖或蛋白G琼脂糖。
在一个实施方案中,抗体与成像剂或检测分子或标记(在本文中可互换使用)偶联。可用于本文所述的组合物和方法中的成像剂的示例包括但不限于放射性同位素标记(例如铟)、酶(例如辣根过氧化物酶)、萦光标记、发光标记、生物发光标记、磁性标记、生物素、SULFO-TAG标记的链霉亲和素、碱性磷酸酶、甲酚紫、量子点、异硫氰酸萦光素(FITC)、红外分子或电子顺磁共振(EPR)自旋示踪剂标记。
可用于衍生本发明的抗体或抗体部分的可检测试剂包括萦光化合物。示例性萦光可检测试剂包括萦光素、异硫氰酸萦光素、罗丹明、5-二甲胺-1-萘磺酰氯、藻红蛋白等。
抗体也可使用可检测的酶衍生,例如碱性磷酸酶、辣根过氧化物酶、葡萄糖氧化酶等。当用可检测的酶衍生抗体时,通过添加另外的试剂进行检测,酶使用所述另外的试剂产生可检测的反应产物。例如,当存在可检测的试剂辣根过氧化物酶时,过氧化氢和二氨基联苯胺的添加产生可检测的有色反应产物。抗体也可以用生物素衍生,并通过抗生物素蛋白或链霉亲和素结合的间接测量来检测。
在另一个实施方案中,本发明的抗体或抗原结合部分的糖基化是经修饰的。例如,可以制备无糖基化抗体(即,抗体缺乏糖基化)。糖基化可被改变以例如增加抗体对抗原的亲和力。这种糖修饰可通过例如改变抗体序列内的一个或多个糖基化位点来实现。例如,可以进行一个或多个氨基酸取代,导致一个或多个可变区糖基化位点的消除,从而消除该位点的糖基化。这种无糖基化可以增加抗体对抗原的亲和力。这种方法被更详细地描述于PCT公布WO2003016466A2和美国专利第5,714,350号和第6,350,861号中,其各自通过引用整体并入本文。
此外或可选地,可以制备具有改变的糖基化类型的本发明的修饰的抗体,例如具有减少的岩藻糖残基量的低岩藻糖基化抗体或具有增加的二等分GlcNAc结构的抗体。这种改变的糖基化模式已被证实增加了抗体的ADCC能力。这种糖修饰可通过例如在具有改变的糖基化机制的宿主细胞中表达抗体来完成。本领域内已经描述了具有改变的糖基化机制的细胞,并且该细胞可被用作宿主细胞以表达本发明的重组抗体从而产生具有改变的糖基化的抗体。参见,例如,Shields,R.L.等(2002)J.Biol.Chem.277:26733-26740;Umana等(1999)Nat.Biotech.17:176-1以及欧洲专利第EP 1,176,195号;PCT公布WO 03/035835;WO99/54342 80,其各自通过引用整体并入本文。
蛋白质糖基化取决于目标蛋白质的氨基酸序列以及表达该蛋白质的宿主细胞。不同的有机体可以产生不同的糖基化酶(例如,糖基转移酶和糖苷酶),并且具有不同的可利用的底物(核苷酸糖)。由于这些因素,蛋白质糖基化模式和糖基残基的组成可能不同(这取决于表达特定蛋白质的宿主系统)。本发明中有用的糖基残基可包括但不限于葡萄糖、半乳糖、甘露糖、岩藻糖、N-乙酰葡糖胺和唾液酸。优选地,糖基化结合蛋白包含糖基残基,使得糖基化模式是人类的。
本领域技术人员已知不同的蛋白质糖基化可导致不同的蛋白质特征。例如,与在哺乳动物细胞(例如CHO细胞系)中表达的相同蛋白相比,在微生物宿主(例如酵母)中产生的并利用酵母内源途径糖基化的治疗性蛋白的效力可能降低。这种糖蛋白在人类体内也可以是免疫原性的并在施用后显示出减少的体内半衰期。人类和其他动物中的特异性受体可识别特异性糖基残基并促进血流中蛋白质的快速清除。其他副作用可包括蛋白质折叠、溶解度、对蛋白酶的敏感性、运输、转运、区室化、分泌、被其他蛋白质或因子识别、抗原性或致敏性的变化。因此,专业人员可优选具有特定组成和糖基化模式的治疗性蛋白质,例如糖基化组成和模式与人类细胞或目标受试者动物的物种特异性细胞中产生的相同或至少相似。
表达与宿主细胞不同的糖基化蛋白可以通过遗传修饰宿主细胞以表达异源糖基化酶来实现。使用本领域已知的技术,专业人员可以产生显示人蛋白质糖基化的抗体或其抗原结合部分。例如,酵母菌株已被遗传修饰以表达非天然存在的糖基化酶,使得在这些酵母菌株中产生的糖基化蛋白(糖蛋白)表现出与动物细胞,尤其是人细胞相同的蛋白糖基化(美国专利公开号20040018590和20020137134以及PCT公开号WO2005100584A2)。
除了结合蛋白,本发明还涉及对本发明的这种结合蛋白具有特异性的抗独特型(抗-Id)抗体。抗-Id抗体是识别通常与另一抗体的抗原结合区相关的独特决定簇的抗体。抗-Id可通过用结合蛋白或其含CDR的区域免疫动物来制备。免疫动物将识别并应答免疫抗体的独特型决定簇并产生抗-Id抗体。抗-Id抗体也可用作“免疫原”以在另一动物中诱导免疫反应,从而产生所谓的抗抗-Id抗体。
此外,本领域技术人员将理解,可以使用经遗传工程化以表达各种糖基化酶的宿主细胞文库来表达目标蛋白质,使得文库的成员宿主细胞产生具有不同糖基化模式的目标蛋白质。然后,专业人员可以选择并分离具有特定新糖基化模式的目标蛋白质。优选地,具有特别选择的新糖基化模式的蛋白质表现出改善的或改变的生物学性质。
抗体可通过多种技术中的任何一种产生。例如,由宿主细胞表达,其中通过标准技术将编码重链和轻链的表达载体转染到宿主细胞中。术语“转染”的各种形式旨在包括通常用于将外源DNA引入原核或真核宿主细胞的各种技术,例如电穿孔、磷酸钙沉淀、DEAE-葡聚糖转染等。尽管在原核或真核宿主细胞中表达抗体是可能的,但是优选在真核细胞中表达抗体,最优选在哺乳动物宿主细胞中表达抗体,因为此类真核细胞(并且特别是哺乳动物细胞)比原核细胞更可能装配和分泌适当折叠和免疫活性的抗体。
用于表达本文公开的重组抗体的优选的哺乳动物宿主细胞包括中国仓鼠卵巢(CHO细胞)(包括dhfr-CHO细胞,其被描述于Urlaub和Chasin,(1980)Proc.Natl.Acad.Sci.USA 77:4216-4220中,与DHFR选择标记物一起使用,例如,如R.J.Kaufman和P.A.Sharp(1982)Mol.Biol.159:601-621中所描述的)、NS0骨髓瘤细胞、COS细胞和SP2细胞。当将编码抗体基因的重组表达载体引入哺乳动物宿主细胞时,通过培养宿主细胞足够长的时间以允许抗体在宿主细胞中表达,或更优选地,将抗体分泌到宿主细胞生长的培养基中来产生抗体。可以使用标准蛋白质纯化方法从培养基中回收抗体。
宿主细胞也可被用于产生功能性抗体片段,例如Fab片段或scFv分子。应当理解,上述程序的变化在本公开的范围内。例如,可能需要用编码本发明抗体轻链和/或重链的功能片段的DNA转染宿主细胞。重组DNA技术也可用于去除一些或全部编码对于结合目标抗原而言不是必需的轻链和重链之一或二者的DNA。由这种截短的DNA分子表达的分子也包括在本公开的抗体中。此外,通过标准化学交联方法使本公开的抗体与第二抗体交联可产生双功能抗体,其中一条重链和一条轻链是本公开的抗体,而另一条重链和轻链对除了目标抗原以外的抗原具有特异性。
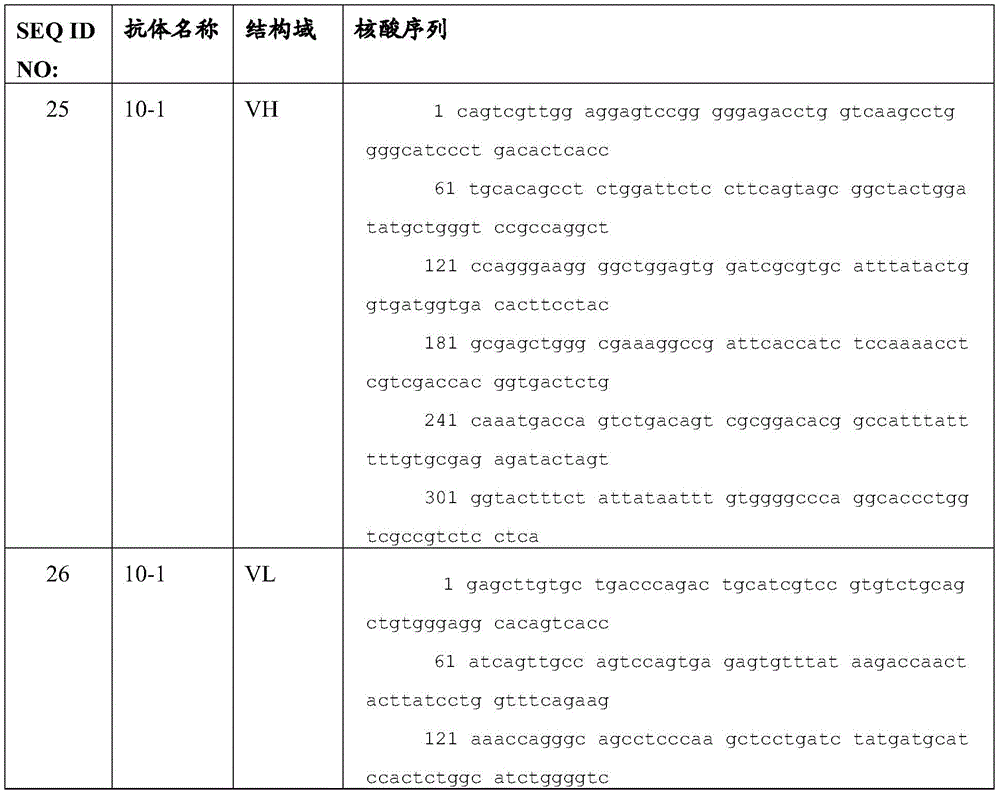
在用于抗体或其抗原结合部分的重组表达的优选系统中,通过磷酸钙介导转染将编码抗体重链和抗体轻链的重组表达载体引入dhfr-CHO细胞中。在重组表达载体内,抗体重链和轻链基因各自与CMV增强子/AdMLP启动子调控元件可操作地连接,以驱动基因的高水平转录。重组表达载体还携带DHFR基因,其允许使用氨甲蝶呤选择/扩增来选择已被载体转染的CHO细胞。培养所选择的转化株宿主细胞以允许抗体重链和轻链表达,并从培养基中回收完整的抗体。使用标准分子生物学技术制备重组表达载体、转染宿主细胞、选择转化株、培养宿主细胞以及从培养基中回收抗体。更进一步,本公开还提供了通过在合适的培养基中培养宿主细胞直到合成重组抗体来合成重组抗体的方法。可以使用对应于本文公开的氨基酸序列的核酸分子产生重组抗体。在一个实施方案中,SEQ ID NO:25-45(见下表2)所示的核酸分子被用于产生重组抗体。该方法可进一步包括从培养基中分离重组抗体。
B.制备抗TAT肽抗体的方法
本发明的抗体可通过本领域已知的多种技术的任何一种制备。
通过杂交瘤制备单克隆抗体的一般方法是公知的。永生的产生抗体的细胞系也可以通过融合以外的技术产生,例如用致癌DNA直接转化B淋巴细胞或用EB病毒转染。参见例如,M.Schreier等,“Hybridoma Techniques”(1980);Hammering等,“MonoclonalAntibodies And T cell Hybridomas”(1981);Kennett等,“Monoclonal Antibodies”(1980);还参见,美国专利号4,341,761;4,399,121;4,427,783;4,444,887;4,451,570;4,466,917;4,472,500;4,491,632和4,493,890。用于产生多克隆抗体的方法是本领域中众所周知的。参见,Nestor等人的美国专利第4,493,795号。
可以通过各种性质(即,亚型、表位、亲和力等)筛选针对TAT肽(例如,TAT转导结构域)产生的单克隆抗体组。
单克隆抗体,通常包含有用抗体分子的Fab和/或F(ab’)2部分,可以使用Antibodies-A Laboratory Manual,Harlow和Lane编辑,Cold Spring HarborLaboratory,New York(1988)(其通过引用并入本文)中描述的杂交瘤技术来制备。简言之,为了形成产生单克隆抗体组合物的杂交瘤,将骨髓瘤或其他自我延续细胞系与获取自用适当TAT肽(例如,TAT转导结构域)超免疫的哺乳动物脾脏的淋巴细胞融合。
通常使用聚乙二醇(PEG)6000融合脾细胞与骨髓瘤细胞。融合杂种通过它们对HAT的敏感性来选择。产生可用于实施本发明的单克隆抗体的杂交瘤通过它们与本发明抗体或结合成员的免疫反应能力和它们抑制靶细胞中特定肿瘤发生或过度增殖活性的能力来鉴定。
可用于实施本发明的单克隆抗体可通过启动包含营养培养基的单克隆杂交瘤培养来产生,所述营养培养基包含分泌具有适当抗原特异性的抗体分子的杂交瘤。在足以使杂交瘤分泌抗体分子到培养基中的条件下维持培养物一段时间。然后收集含抗体的培养基。然后可以通过众所周知的技术进一步分离抗体分子。
可用于制备这些组合物的培养基是本领域公知且可商购的,并且包括合成培养基、近交系小鼠等。示例性合成培养基是补充有4.5gm/l葡萄糖、20mm谷氨酰胺和20%胎牛血清的Dulbecco最低必需培养基(DMEM;Dulbecco等,Virol.8:396(1959))。示例性近交系小鼠品系是Balb/c。
1.使用杂交瘤技术制备抗TAT肽单克隆抗体
可以使用本领域已知的多种技术制备单克隆抗体,其中包括使用杂交瘤、重组和噬菌体展示技术或其组合。例如,可以使用杂交瘤技术产生单克隆抗体,其中包括本领域已知的和在例如Harlow等,Antibodies:A Laboratory Manual,(Cold Spring HarborLaboratory Press,2nd ed.1988);Hammerling等,在:Monoclonal Antibodies and T-Cell Hybridomas 563-681(Elsevier,N.Y.,1981)(所述参考文献通过引用整体并入本文)中教导的那些。本文所用的术语“单克隆抗体”不限于通过杂交瘤技术产生的抗体。术语“单克隆抗体”是指来源于单个克隆(包括任何真核、原核或噬菌体克隆)而不是产生它的方法的抗体。
使用杂交瘤技术产生和筛选特异性抗体的方法是本领域常规且熟知的。例如,单克隆抗体可通过培养分泌本发明的抗体的杂交瘤细胞的方法产生,其中,优选地,杂交瘤是通过融合分离自用本发明的抗原免疫的小鼠的脾细胞与骨髓瘤细胞产生的,然后筛选融合产生的杂交瘤以获得分泌能结合本发明的多肽的抗体的杂交瘤克隆。简言之,可以用TAT肽抗原(例如,TAT转导结构域抗原)免疫小鼠。在某些实施方案中,TAT肽抗原(例如,TAT转导结构域抗原)与佐剂一起施用以刺激免疫反应。这种佐剂包括完全或不完全弗氏佐剂、RIBI(胞壁酰二肽)或ISCOM(免疫刺激复合物)。这种佐剂可以通过将其隔离在局部沉积物中来保护多肽免于快速分散,或者它们可以包含刺激宿主分泌对巨噬细胞和免疫系统的其他组分具有趋化性的因子的物质。优选地,如果施用多肽,则免疫方案将包括在数周内分两次或多次施用多肽。
用TAT肽抗原免疫动物后,可从动物获得抗体和/或产生抗体的细胞。通过采血或处死动物,从动物获得含有抗TAT肽抗体的血清。可以直接使用从动物身上获得的血清,可从血清中获取免疫球蛋白部分,或可以从血清中纯化抗TAT肽抗体。以这种方式获得的血清或免疫球蛋白是多克隆的,因此具有异质性的一系列特性。
一旦检测到免疫反应,例如在小鼠血清中检测到抗原TAT肽(例如,TAT转导结构域抗原)的特异性抗体,即采集小鼠脾脏并分离脾细胞。然后通过众所周知的技术将脾细胞与任何合适的骨髓瘤细胞(例如可获取自ATCC的细胞系SP20的细胞)融合。通过有限稀释选择和克隆杂交瘤。然后通过本领域已知的方法测定杂交瘤克隆中分泌能够结合TAT肽(例如,TAT转导结构域)的抗体的细胞。可以通过用阳性杂交瘤克隆免疫小鼠来产生通常包含高水平抗体的腹水。
在另一个实施方案中,产生抗体的永生化杂交瘤可以通过免疫动物制备。免疫后,处死动物并将脾B细胞与永生化骨髓瘤细胞融合,这是本领域内众所周知的。参见例如,Harlow和Lane,同上。在优选的实施方案中,骨髓瘤细胞不分泌免疫球蛋白多肽(非分泌细胞系)。融合和抗生素筛选后,使用TAT肽或其部分或表达TAT肽或其部分的细胞筛选杂交瘤。使用酶联免疫吸附测定(ELISA)或放射免疫测定(RIA)进行初始筛选。ELISA筛选的示例提供于WO00/37504中,其通过引用并入本文。
选择产生抗TAT肽抗体的杂交瘤,克隆,并针对所需的特征进一步筛选,所述特征包括稳健的杂交瘤生长、高抗体产量和所需的抗体特征,如下文进一步讨论的。可以在同系的动物中、在缺乏免疫系统的动物(例如裸鼠)中在体内或在细胞培养物中在体外培养和扩增杂交瘤。选择、克隆和扩增杂交瘤的方法是本领域技术人员熟知的那些。
在优选的实施方案中,杂交瘤是小鼠杂交瘤,如本文所述。在另一个优选的实施方案中,杂交瘤在非人、非小鼠物种(例如,大鼠、绵阳、猪、山羊、牛或马)中产生。在另一个实施方案中,杂交瘤是人杂交瘤,其中人非分泌性骨髓瘤与表达抗TAT肽抗体的人细胞融合。
识别特异性表位的抗体片段可通过已知技术产生。例如,本发明的Fab和F(ab’)2片段可以通过使用酶(例如木瓜蛋白酶(以产生Fab片段)或胃蛋白酶(以产生F(ab’)2片段))对免疫球蛋白分子进行蛋白水解裂解来产生。F(ab’)2片段包含可变区、轻链恒定区和重链的CH1结构域。
2.使用选择淋巴细胞抗体法产生抗TAT肽单克隆抗体
在本发明的另一个方面,使用本领域内称为选择淋巴细胞抗体法(selectedlymphocyte antibody method,SLAM)的方法从单个分离的淋巴细胞产生重组抗体,如美国专利第5,627,052号、PCT公开号WO92/02551和Babcock,J.S.等,(1996)Proc.Natl.Acad.Sci.USA93:7843-7848中描述的。在该方法中,使用抗原特异性溶血空斑试验筛选分泌目标抗体的单个细胞,例如来源于上述任何一种免疫动物的淋巴细胞,其中使用接头(例如生物素)将抗原TAT肽、TAT肽的亚基(例如,TAT转导结构域抗原)或其片段偶联至绵羊红细胞,并用于鉴定分泌对TAT肽(例如,TAT转导结构域)具有特异性的抗体的单个细胞。在鉴定分泌抗体的目标细胞后,通过逆转录酶-PCR从细胞中拯救重链和轻链可变区cDNA,然后在哺乳动物宿主细胞(例如,COS或CHO细胞中)中,在适当的免疫球蛋白恒定区(例如,人恒定区)的背景下,表达这些可变区。用源自体内选择的淋巴细胞的扩增的免疫球蛋白序列转染宿主细胞,然后可以进行进一步的体外分析和选择,例如通过淘选转染的细胞以分离表达针对TAT肽(例如,TAT转导结构域)的抗体的细胞。扩增的免疫球蛋白序列可进一步例如通过体外亲和力成熟方法在体外操作,例如PCT公开号WO97/29131和PCT公开号WO00/56772中描述的那些。
3.使用重组抗体文库产生抗TAT肽单克隆抗体
体外方法也可用于制备本发明的抗体,其中筛选抗体文库以鉴定具有所需结合特异性的抗体。用于这种筛选重组抗体文库的方法是本领域熟知的,并且包括例如Ladner等,美国专利第5,223,409号;Kang等,PCT公开号WO 92/18619;Dower等,PCT公开号WO 91/17271;Winter等,PCT公开号WO 92/20791;Markland等,PCT公开号WO 92/15679;Breitling等,PCT公开号WO 93/01288;McCafferty等,PCT公开号WO 92/01047;Garrard等,PCT公开号WO 92/09690;Fuchs等,(1991)Bio/Technology 9:1370-1372;Hay等,(1992)Hum AntibodHybridomas 3:81-85;Huse等,(1989)Science 246:1275-1281;McCafferty等,Nature(1990)348:552-554;Griffiths等,(1993)EMBO J 12:725-734;Hawkins等,(1992)J MolBiol 226:889-896;Clackson等,(1991)Nature 352:624-628;Gram等,(1992)PNAS 89:3576-3580;Garrad等,(1991)Bio/Technology 9:1373-1377;Hoogenboom等,(1991)NucAcid Res 19:4133-4137;以及Barbas等,(1991)PNAS 88:7978-7982,US专利申请公开号20030186374和PCT公开号WO 97/29131中描述的方法,其各自的内容通过引用并入本文。
重组抗体文库可来自用TAT肽或TAT肽的一部分(例如TAT转导结构域)免疫的受试者。或者,重组抗体文库可以来自天然受试者,即未用TAT肽免疫的受试者,例如来自未用TAT肽免疫的人类受试者的人类抗体文库。通过用包含TAT肽的肽筛选重组抗体文库来选择本发明的抗体,从而选择识别TAT肽(例如,TAT转导结构域)的那些抗体。用于进行这种筛选和选择的方法是本领域熟知的,例如前面段落中的参考文献中所描述的。为了选择对TAT肽(例如,TAT转导结构域)具有特定结合亲和力的本发明的抗体,例如以特定koff速率常数从TAT转导结构域解离的那些,表面等离子体共振的本领域内已知的方法可被用于选择具有所需的koff速率常数的抗体。为了选择对TAT转导结构域具有特定中和活性的本发明的抗体,例如具有特定IC50的那些,可以使用本领域已知的用于评估TAT肽活性抑制的标准方法。
在一个方面,本发明涉及结合TAT肽,特别是人TAT肽的分离的抗体或其抗原结合部分。在不同实施方案中,抗体是重组抗体或单克隆抗体。
例如,本发明的抗体也可以使用本领域已知的各种噬菌体展示方法产生。在噬菌体展示方法中,功能性抗体结构域在携带编码它们的多核苷酸序列的噬菌体颗粒的表面上展示。特别地,这种噬菌体可用于展示由所有组成成分(repertoire)或组合抗体文库(例如,人或鼠)表达的抗原结合结构域。表达结合目标抗原的抗原结合结构域的噬菌体可以用抗原(例如,使用标记的抗原或固体表面或珠上结合或捕获的抗原)进行选择或鉴定。这些方法中使用的噬菌体通常是丝状噬菌体,包括由噬菌体表达的fd和M13结合结构域,其中Fab、Fv或二硫键稳定的Fv抗体结构域重组地融合到噬菌体基因III或基因VIII蛋白。可用于制备本发明的抗体的噬菌体展示方法的示例包括Brinkman等,J.Immunol.Methods 182:41-50(1995);Ames等,J.Immunol.Methods 184:177-186(1995);Kettleborough等,Eur.J.Immunol.24:952-958(1994);Persic等,Gene 187 9-18(1997);Burton等,Advancesin Immunology 57:191-280(1994);PCT申请号PCT/GB91/01134;PCT公开号WO 90/02809;WO 91/10737;WO92/01047;WO 92/18619;WO 93/11236;WO 95/15982;WO 95/20401;和美国专利号698,426;5,223,409;5,403,484;5,580,717;5,427,908;5,750,753;5,821,047;5,571,698;5,427,908;5,516,637;5,780,225;5,658,727;5,733,743和5,969,108中描述的那些,其各自通过引用整体并入本文。
如上文参考文献中所述,在噬菌体选择后,可以从噬菌体分离抗体编码区并将其用于产生包括人抗体或任何其他期望的抗原结合片段的完整抗体,并在任何期望的宿主中表达,所述宿主包括哺乳动物细胞、昆虫细胞、植物细胞、酵母和细菌,例如,如下文详细描述的。例如,也可使用本领域内已知的方法应用重组产生Fab、Fab’和F(ab’)2片段的技术,例如PCT公开WO92/22324;Mullinax等,BioTechniques12(6):864-869(1992);和Sawai等,AJRI 34:26-34(1995);和Better等,Science 240:1041-1043(1988)(所述参考文献通过引用整体并入本文)中公开的那些。可用于产生单链Fv和抗体的技术的示例包括美国专利4,946,778和5,258,498;Huston等,Methods in Enzymology203:46-88(1991);Shu等,PNAS90:7995-7999(1993);和Skerra等,Science 240:1038-1040(1988)中描述的那些。
作为通过噬菌体展示筛选重组抗体文库的替代方法,用于筛选大组合文库的本领域已知的其他方法可被用于鉴定本发明的双重特异性抗体。一种类型的备选表达系统是其中将重组抗体文库表达为RNA-蛋白融合体的系统,如Szostak和Roberts的PCT公开号WO98/31700以及Roberts,R.W.和Szostak,J.W.(1997)Proc.Natl.Acad.Sci.USA 94:12297-12302中所描述的。在该系统中,通过在其3’末端携带嘌呤霉素(一种肽基受体抗生素)的合成mRNA的体外翻译,mRNA和其编码的肽或蛋白质之间产生共价融合。因此,基于所编码的肽或蛋白质(例如,抗体或其部分)的特性,例如抗体或其部分与双重特异性抗原的结合,可以从mRNA的复杂混合物(例如,组合文库)中富集特定mRNA。从这些文库的筛选中回收的编码抗体或其部分的核酸序列可以通过如上所述的重组手段(例如,在哺乳动物宿主细胞中)表达,并且此外,可以通过对其中已将突变引入最初选择的序列中的mRNA-肽融合体进行另外的几轮筛选,或通过如上所述的用于重组抗体的体外亲和力成熟的其他方法进行进一步的亲和力成熟。
在另一种方法中,也可以使用本领域已知的酵母展示方法产生本发明的抗体。在酵母展示方法中,遗传方法可被用于将抗体结构域连接至酵母细胞壁上并将其展示在酵母表面上。特别地,这种酵母可被用于展示由所有组成成分或组合抗体文库(例如,人或鼠)表达的抗原结合结构域。可被用于制备本发明抗体的酵母展示方法的示例包括Wittrup等(美国专利第6,699,658号)公开的那些,其通过引用并入本文。
4.重组抗TAT肽抗体
本发明的抗体可通过本领域已知的多种技术中的任何一种产生。例如,由宿主细胞表达,其中通过标准技术将编码重链和轻链的表达载体转染到宿主细胞中。术语“转染”的各种形式旨在包括通常用于将外源DNA引入原核或真核宿主细胞的各种技术,例如电穿孔、磷酸钙沉淀、DEAE-葡聚糖转染等。尽管在原核或真核宿主细胞中表达本发明抗体是可能的,但是优选在真核细胞中表达抗体,最优选在哺乳动物宿主细胞中表达抗体,因为这种真核细胞(并且特别是哺乳动物细胞)比原核细胞更可能装配和分泌适当折叠和免疫活性的抗体。
在某些实施方案中,本发明的特征在于编码本文所述结合蛋白氨基酸序列的分离的核酸。在其他某些实施方案中,本发明的特征还在于编码本文所述的抗体构建体氨基酸序列的分离的核酸。在产生方法中,表达载体包含分离的核酸。这种表达载体的非限制性示例是pUC系列载体(Fermentas Life Sciences)、pBluescript系列载体(Stratagene,LaJolla,Calif.)、pET系列载体(Novagen,Madison,Wis.)、pGEX系列载体(PharmaciaBiotech,Uppsala,Sweden)和pEX系列载体(Clontech,Palo Alto,Calif.)。
宿主细胞包含本文所述的载体。根据本发明的实施方案,宿主细胞是原核细胞或真核细胞。例如,原核宿主细胞是大肠杆菌细胞。真核细胞可选自原生生物细胞、动物细胞、植物细胞或真菌细胞。动物细胞可选自哺乳动物细胞、鸟类细胞和昆虫细胞。优选地,宿主细胞选自CHO细胞、COS细胞、酵母细胞和昆虫Sf9细胞。在进一步相关的实施方案中,酵母细胞是酿酒酵母细胞。
用于表达本发明的重组抗体的优选的哺乳动物宿主细胞包括中国仓鼠卵巢(CHO细胞)(其中包括dhfr-CHO细胞,其被描述于Urlaub和Chasin,(1980)Proc.Natl.Acad.Sci.USA 77:4216-4220中,与DHFR选择标记物一起使用,例如,如R.J.Kaufman and P.A.Sharp(1982)Mol.Biol.159:601-621中所描述的)、NS0骨髓瘤细胞、COS细胞和SP2细胞。当将编码抗体基因的重组表达载体引入哺乳动物宿主细胞时,通过培养宿主细胞足够长的时间以允许抗体在宿主细胞中表达,或更优选地,将抗体分泌到宿主细胞生长的培养基中来产生抗体。可以使用标准蛋白质纯化方法从培养基中回收抗体。
宿主细胞也可被用于产生功能性抗体片段,例如Fab片段或scFv分子。应当理解,上述程序的变化在本发明的范围内。例如,可能需要用编码本发明抗体轻链和/或重链的功能片段的DNA转染宿主细胞。重组DNA技术也可用于去除一些或全部编码对于结合目标抗原而言不是必需的轻链和重链之一或二者的DNA。由这种截短的DNA分子表达的分子也包括在本发明的抗体中。此外,通过标准化学交联方法使本发明的抗体与第二抗体交联可产生双功能抗体,其中一条重链和一条轻链是本发明的抗体,而另一条重链和轻链对除了目标抗原以外的抗原具有特异性。
在用于本发明的抗体或其抗原结合部分的重组表达的优选系统中,通过磷酸钙介导转染将编码抗体重链和抗体轻链的重组表达载体引入dhfr-CHO细胞中。在重组表达载体内,抗体重链和轻链基因各自与CMV增强子/AdMLP启动子调控元件可操作地连接,以驱动基因的高水平转录。重组表达载体还携带DHFR基因,其允许使用氨甲蝶呤选择/扩增来选择已被载体转染的CHO细胞。培养所选择的转化株宿主细胞以允许抗体重链和轻链表达,并从培养基中回收完整的抗体。使用标准分子生物学技术制备重组表达载体、转染宿主细胞、选择转化株、培养宿主细胞以及从培养基中回收抗体。本发明还提供了通过在合适的培养基中培养本发明的宿主细胞直到合成本发明的重组抗体来合成本发明的重组抗体的方法。该方法可进一步包括从培养基中分离重组抗体。
本发明还涉及产生能够结合TAT肽的蛋白质、产生结合TAT肽的抗体或其抗原结合部分的多种方法,所述方法包括在培养基中培养如本文所述的宿主细胞,从而表达核酸并产生抗体。产生能够结合TAT肽的蛋白质的示例性方法包括在足以产生能够结合TAT肽的结合蛋白的条件下,在培养基中培养如本文所述的宿主细胞。
本发明的特征还在于根据所述方法产生的蛋白质。
5.人源化抗TAT肽抗体
人源化抗体是来自非人物种抗体的抗体分子,其结合期望的抗原,具有来自非人物种的一个或多个互补决定区(CDR)和来自人免疫球蛋白分子的框架区。已知的人Ig序列被公开于例如以下:ncbi.nlm.nih.gov/entrez-/query.fcgi;atcc.org/phage/hdb.html;sciquest.com/;abcam.com/;antibodyresource.com/onlinecomp.html;public.iastate.edu/.about.pedro/research_tools.html;mgen.uni-heidelberg.de/SD/IT/IT.html;whfreeman.com/immunology/CH-05/kuby05.htm;library.thinkquest.org/12429/Immune/Antibody.html;hhmi.org/grants/lectures/1996/vlab/;path.cam.ac.uk/.about.mrc7/m-ikeimages.html;antibodyresource.com/;mcb.harvard.edu/BioLinks/Immuno-logy,iimmunologylink.com/;pathbox.wustl.edu/.about.hcenter/index.-html;biotech.ufl.edu/.about.hcl/;pebio.com/pa/340913/340913.html-;nal.usda.gov/awic/pubs/antibody/;m.ehime-u.acjp/.about.yasuhito-/Elisa.html;biodesign.com/table.asp;icnet.uk/axp/facs/davies/lin-ks.html;biotech.ufl.edu/.about.fccl/protocol.html;isac-net.org/sites_geo.html;aximtl.imt.uni-marburg.de/.about.rek/AEP-Start.html;baserv.uci.kun.nl/.about.jraats/linksl.html;recab.uni-hd.de/immuno.bme.nwu.edu/;mrc-cpe.cam.ac.uk/imt-doc/pu-blic/INTRO.html;ibt.unam.mx/vir/V_mice.html;imgt.cnusc.fr:8104/;biochem.ucl.ac.uk/.about.martin/abs/index.html;antibody.bath.ac.uk/;abgen.cvm.tamu.edu/lab/wwwabgen.html;unizh.ch/.about.honegger/AHOsem-inar/Slide01.html;cryst.bbk.ac.uk/.about.ubcg07s/;nimr.mrc.ac.uk/CC/ccaewg/ccaewg.htm;path.cam.ac.uk/.about.mrc7/h-umanisation/TAHHP.html;ibt.unam.mx/vir/structure/stat_aim.html;biosci.missouri.edu/smithgp/index.html;cryst.bioc.cam.ac.uk/.abo-ut.fmolina/Web-pages/Pept/spottech.html;jerini.de/frroducts.htm;patents.ibm.com/ibm.html.,Kabat等,Sequences of Proteins of Immunological Interest,U.S.Dept.Health(1983),其各自通过引用整体并入本文。这种导入的序列可用于降低免疫原性或降低、增强或修饰结合、亲和力、结合速率、解离速率、亲合力、特异性、半衰期或本领域已知的任何其他合适的特征。
人框架区中的框架残基可用来自CDR供体抗体的相应残基取代以改变,优选改善抗原结合。这些框架取代通过本领域熟知的方法鉴定,例如,通过模拟CDR和框架残基的相互作用以鉴定对抗原结合重要的框架残基,以及通过序列比较以鉴定特定位置上独特的框架残基。(参见例如,Queen等,美国专利第5,585,089号;Riechmann等,Nature 332:323(1988),其通过引用整体并入本文)。三维免疫球蛋白模型通常是可获得的并且是本领域技术人员所熟悉的。阐明和展示所选的候选免疫球蛋白序列的可能三维构象结构的计算机程序是可获得的。这些展示的检查允许分析残基在候选免疫球蛋白序列功能中可能的作用,即分析影响候选免疫球蛋白结合其抗原的能力的残基。这样,可以从共有序列和输入序列中选择并组合FR残基,从而获得期望的抗体特征,例如增强的对靶抗原的亲和力。通常,CDR残基直接且最本质地参与影响对抗原结合。可以使用本领域已知的多种技术对抗体进行人源化,例如但不限于Jones等,Nature 321:522(1986);Verhoeyen等,Science 239:1534(1988));Sims等,J.Immunol.151:2296(1993);Chothia和Lesk,J.Mol.Biol.196:901(1987);Carter等,Proc.Natl.Acad.Sci.U.S.A.89:4285(1992);Presta等,J.Immunol.151:2623(1993),Padlan,Molecular Immunology 28(4/5):489-498(1991);Studnicka等,Protein Engineering 7(6):805-814(1994);Roguska.等,PNAS 91:969-973(1994);PCT公开号WO 91/09967,PCT/:US98/16280、US96/18978、US91/09630、US91/05939、US94/01234、GB89/01334、GB91/01134、GB92/01755;WO90/14443、WO90/14424、WO90/14430、EP 229246、EP 592,106;EP 519,596、EP 239,400、美国专利号5,565,332、5,723,323、5,976,862、5,824,514、5,817,483、5814476、5763192、5723323、5,766886、5,714,352、6,204,023、6,180,370、5,693,762、5,530,101、5,585,089、5,225,539;4,816,567中的那些,其各自通过引用并入本文,并且包括其中引用的参考文献。
本发明涵盖人源化抗TAT肽抗体。
III.抗TAT肽结合蛋白的用途
A.包含TAT肽的TAT融合分子的检测
考虑到它们结合TAT蛋白转导结构域的能力,使用常规免疫测定,例如酶联免疫吸附测定(ELISA)、放射免疫测定(RIA)、抗体标记的萤光成像或组织免疫组织化学,本发明的抗TAT结合蛋白(例如,抗体或其部分)可被用于检测TAT(例如,在生物样品中,例如血清、血浆、尿液、组织或细胞)。应当理解,本发明包括TAT肽多肽的任何片段的检测,只要该片段允许通过本发明的检测方法特异性鉴定TAT肽。在一个具体的实施方案中,本发明的TAT肽结合蛋白特异性结合TAT蛋白转导结构域。例如,ELISA抗体必须能够结合TAT肽片段(例如,TAT蛋白转导结构域)使得检测成为可能。
在另一个实施方案中,本发明的TAT结合蛋白(例如抗体)可被用于检测跨细胞递送系统,例如TAT-脂质体或TAT-纳米颗粒,例如用于递送小分子。
在一个实施方案中,本发明的TAT结合蛋白(例如抗体)可用于检测作为完整TAT融合分子一部分的TAT肽。例如,本发明的TAT结合蛋白可用于检测包含与货物部分连接的TAT蛋白转导结构域的完整TAT融合分子。在一个实施方案中,TAT结合蛋白(例如抗体)特异性结合完整TAT融合分子的TAT肽,例如TAT蛋白转导结构域,且不结合TAT融合分子的货物部分。
在一个实施方案中,货物部分是多肽。在一个实施方案中,多肽是共济蛋白,例如TAT融合分子是TAT-共济蛋白融合分子。在其他实施方案中,货物部分是核酸分子,例如DNA、mRNA、siRNA、shRNA。
在一些实施方案中,本发明的TAT结合蛋白(例如抗体)可用于在体外或体内检测、测量、验证TAT肽(例如,包含TAT蛋白转导结构域的TAT融合分子)的递送或定量其。因此,本发明的结合蛋白在体内或体外(例如在特定组织中)均能够检测、定量、验证递送和/或测量与TAT肽(例如,包含TAT蛋白转导结构域的TAT融合分子)偶联的货物部分(例如,前药或药物)。
在一些实施方案中,本发明的TAT结合蛋白(例如抗体)可用于例如通过用标记的抗TAT结合蛋白灌注组织来成像组织。在一些实施方案中,通过使用例如本文所述的红外偶联物、放射性同位素标记或电子顺磁共振(EPR)自旋示踪剂标记来标记抗体,本发明的TAT结合蛋白(例如抗体)可用于检测、定量和监测或追踪TAT肽(例如,包含TAT蛋白转导结构域的TAT融合分子)的药代动力学、递送和/或定位。
在一个方面,本发明的方法提供了用于检测和/或定量样品(例如,生物样品)中TAT融合分子水平的方法,其包括在使本发明的结合蛋白与样品中TAT蛋白转导结构域结合的条件下,使样品与结合蛋白接触,从而检测和/或定量样品中TAT融合分子的水平。在一个实施方案中,生物样品是液体(例如,血液)样品或组织样品。
在另一个方面,本发明的方法提供了检测和/或定量体内TAT融合分子水平的方法,其包括在使本发明的结合蛋白与TAT蛋白转导结构域结合的条件下,使样品与结合蛋白接触并成像结合蛋白,从而检测和/或定量体内TAT融合分子的水平。
在一些实施方案中,TAT融合分子包含与货物部分共价连接的TAT蛋白转导结构域。在一些实施方案中,货物部分是多肽。在一些实施方案中,货物部分是共济蛋白多肽。
在另一个实施方案中,货物部分是药理学活性化合物、小分子、脂质体包封蛋白、放射性核素或放射性核素标记的化合物、核酸(例如,siRNA、shRNA、miRNA、硫代磷酸酯修饰的RNA、适配体、磷酰二胺吗啉代寡核苷酸(PMO)或其任何组合)。
在一些实施方案中,本发明的方法还包括使用本发明的结合蛋白通过例如检测本文所述的TAT融合分子并测量TAT融合分子随时间的稳定性来评估TAT融合分子的稳定性。
在另一个方面,本发明的方法提供了用于分离和/或纯化混合物中存在的TAT融合分子的方法,其中TAT融合分子包含与货物部分共价连接的TAT蛋白转导结构域,所述方法包括(a)使包含TAT融合分子的混合物与本发明的固定化结合蛋白在使得TAT融合分子与固定化结合蛋白结合的条件下接触;(b)从固定化结合蛋白洗脱TAT融合分子。
在一些实施方案中,本发明的结合蛋白可用于富集混合物中完整的TAT融合分子。例如,混合物可包含完整和降解形式的TAT融合分子。
在一些实施方案中,本发明的结合蛋白是用辣根过氧化物酶、三联吡啶钌、碱性磷酸酶、甲酚紫、量子点、异硫氰酸萦光素(FITC)、红外分子、放射性同位素标记或EPR自旋示踪剂标记来标记。
在一个实施方案中,ELISA测定被用于检测和/或定量包含TAT蛋白转导结构域的TAT肽或包含TAT蛋白转导结构域的TAT融合分子。在示例性ELISA中,结合蛋白(例如,结合TAT蛋白转导结构域的抗体)被固定在显示蛋白亲和力的选定的表面上,例如聚苯乙烯微孔板中的孔上。然后,测试组合物或样品,例如含有TAT蛋白转导结构域(例如,与货物部分融合的TAT蛋白转导结构域)的血液或组织样品被添加至孔中。在结合和洗涤以去除非特异性结合的免疫复合物后,可以检测结合的抗原。检测通常通过添加与可检测标记连接的对靶蛋白具有特异性的第二抗体来实现。这种类型的ELISA是简单的“夹心ELISA”。还可以通过添加第二抗体,随后添加对第二抗体具有结合亲和力的第三抗体来实现检测,其中第三抗体与可检测标记连接。
在另一个示例性ELISA中,可能含有TAT蛋白转导结构域(例如,包含TAT蛋白转导结构域的TAT融合分子)的样品被固定在孔表面上,然后与本发明的抗TAT肽抗体接触。结合和洗涤以去除非特异性结合的免疫复合物后,检测结合的抗原。当初始抗体与可检测标记连接时,可直接检测免疫复合物。同样,可使用对第一抗体具有结合亲和力的第二抗体检测免疫复合物,其中第二抗体与可检测标记连接。
无论采用何种形式,ELISA具有某些共同的特征,例如包被、孵育或结合、洗涤以去除非特异性结合的物质、以及检测结合的免疫复合物。这些描述如下。
在用抗原或抗体包被板时,通常用抗原或抗体溶液孵育板的孔过夜或持续指定时间。然后洗涤板的孔以去除未完全吸附的物质。然后用对测试抗血清呈抗原性中性的非特异性蛋白质“包被”孔的任何剩余可用表面。这些包括牛血清白蛋白(BSA)、酪蛋白和奶粉溶液。包被允许封闭固定表面上的非特异性吸附位点,并由此减少由抗血清在表面上的非特异性结合引起的背景。
在ELISA中,使用二级或三级检测方式而不是直接检测程序可能更常见。因此,在蛋白质或抗体与孔结合后,用非反应性物质包被以减少背景,并洗涤以去除未结合的物质,在有效允许免疫复合物(抗原/抗体)形成的条件下,使固定表面与待测试的对照临床或生物样品接触。然后免疫复合物的检测需要标记的第二结合配体或抗体、或与标记的第三抗体或第三结合配体结合的第二结合配体或抗体。
短语“在有效允许免疫复合物(抗原/抗体)形成的条件下”是指所述条件优选地包括用溶液(例如BSA、牛丙种球蛋白(BGG)和磷酸盐缓冲盐水(PBS)/Tween)稀释抗原和抗体。这些添加的试剂也有助于减少非特异性背景。
“合适的”条件还指在足以允许有效结合的温度和时间段下进行孵育。孵育步骤通常在优选约25至27℃的温度下进行约1至2至4小时,或可在约4℃左右过夜。
在ELISA中的所有孵育步骤之后,洗涤接触的表面以去除未复合的物质。优选的洗涤程序包括用溶液(例如,PBS/Tween或硼酸盐缓冲液)洗涤。在测试样品和最初结合的物质之间形成特异性免疫复合物后,随后洗涤,即使微量免疫复合物的出现也可被测定。
为了提供检测手段,第二或第三抗体将连接相关的标记以允许检测。优选地,这将是在与适当的显色底物孵育后将产生显色的酶。因此,例如,人们希望在有利于进一步免疫复合物形成发展的条件下,将第一或第二免疫复合物与脲酶、葡萄糖氧化酶、碱性磷酸酶或过氧化氢酶偶联抗体接触并孵育一段时间(例如,在室温下在含PBS的溶液(如PBS-Tween)中孵育2小时)。
在与标记的抗体孵育后,随后洗涤以去除未结合的物质,例如通过与显色底物(例如,脲和溴甲酚紫)孵育定量标记的量。然后通过例如使用可见光谱分光光度计测量显色度来实现定量。
在某些实施方案中,使用本发明的抗TAT肽结合蛋白检测TAT肽的替代方法是采用蛋白质免疫沉淀与质谱分析法(例如,串联质谱,例如多反应监测质谱(IP-MRM))联用。IP-MRM在本领域中是已知的且被描述于例如Lin等(Journal of Proteome Research,2013,12,5996-6003)中。
B.标记
本发明提供了用于检测生物样品中的TAT肽(例如,TAT蛋白转导结构域或包含TAT蛋白转导结构域的TAT融合分子)的方法,该方法包括使生物样品与本发明的结合蛋白(例如抗体或抗体部分)接触并检测与TAT肽(例如,TAT蛋白转导结构域或包含TAT蛋白转导结构域的TAT融合分子)结合的结合蛋白(例如抗体(或抗体部分)),从而检测生物样品中的TAT肽(例如,TAT蛋白转导结构域或包含TAT蛋白转导结构域的TAT融合分子)。使用可检测物质直接或间接标记结合蛋白以促进结合或未结合抗体的检测。
合适的可检测物质包括各种酶、辅基、萦光材料、发光材料和放射性物质。合适的酶的示例包括辣根过氧化物酶、碱性磷酸酶、β-半乳糖苷酶或乙酰胆碱酯酶;合适的辅基复合物的示例包括链霉亲和素/生物素和亲和素/生物素;合适的萦光材料的示例包括伞形酮、萦光素、异硫氰酸萦光素、罗丹明、二氯三嗪胺萦光素、丹磺酰氯或藻红蛋白;发光材料的示例包括鲁米诺;合适的放射性物质的示例包括3H、14C、35S、90Y、99Tc、111In、125I、131I、177Lu、166Ho或153Sm。
在一些实施方案中,本发明的结合蛋白是用辣根过氧化物酶、SULFO-TAG标记的链霉亲和素、碱性磷酸酶、甲酚紫、量子点或异硫氰酸萦光素(FITC)、红外分子、放射性同位素标记或电子顺磁共振(EPR)自旋示踪剂标记来标记。
本领域技术人员将认识到,许多策略可被用于标记本发明的结合蛋白以能够在颗粒混合物中检测或区分它们。标记可以通过任何已知的方法附着,包括利用标记和靶标的非特异性或特异性相互作用的方法。标记可以提供可检测的信号或影响粒子在电场中的迁移。此外,标记可以直接或通过结合配偶体完成。
在一些实施方案中,标记包含结合TAT肽(例如,例如TAT蛋白转导结构域或包含TAT蛋白转导结构域的TAT融合分子)的结合配偶体,例如本文所述的TAT肽抗体,其中所述结合配偶体附着于萦光部分。本发明的组合物和方法可以利用高萦光部分(moiety),例如,当通过由激光器在部分的激发波长处发射光来模拟时,该部分能够发射至少约200个光子,其中所述激光器聚焦在含有所述部分的直径不小于约5微米的点上,并且其中由所述激光器导向所述点的总能量不超过约3微焦耳(microJoule)。下面更详细地描述适用于本发明的组合物和方法的部分。
萦光标记包括近红外(NIR)萦光团,其描述于例如Frangioni,2003,CurrentOpinions in Chemical Biology,7(5):626,其内容通过引用并入本文。
在一些实施方案中,本发明提供了用于检测生物分子的标记,生物分子包含与萦光部分连接的生物分子(例如本文所述的TAT肽抗体)的结合配偶体,其中当通过由激光器在部分的激发波长处发射光来模拟时,该萦光部分能够发射至少约200个光子,其中所述激光器聚焦在含有所述部分的直径不小于约5微米的点上,并且其中由所述激光器导向所述点的总能量不超过约3微焦耳。在一些实施方案中,部分包含多个萦光实体,例如约2至4个、2至5个、2至6个、2至7个、2至8个、2至9个、2至10个、或约3至5个、3至6个、3至7个、3至8个、3至9个、或3至10个萦光实体。在一些实施方案中,部分包含约2至4个萦光实体。萦光实体可以是萦光染料分子。在一些实施方案中,萦光染料分子包含至少一个取代吲哚环体系,其中吲哚环的3-碳上的取代基包含化学反应性基团或偶联物质。在一些实施方案中,染料分子是选自由以下组成的组Alexa Fluor分子:Alexa Fluor 488、Alexa Fluor 532、AlexaFluor 647、Alexa Fluor 680或Alexa Fluor 700。在一些实施方案中,染料分子是选自由以下组成的组Alexa Fluor分子:Alexa Fluor 488、Alexa Fluor 532、Alexa Fluor680或Alexa Fluor 700。在一些实施方案中,染料分子是Alexa Fluor647染料分子。在一些实施方案中,染料分子包含第一类型和第二类型的染料分子,例如两种不同的Alexa Fluor分子,例如其中第一类型和第二类型的染料分子具有不同的发射光谱。第一类型和第二类型染料分子的数量的比可以是例如4比1、3比1、2比1、1比1、1比2、1比3或1比4。结合配偶体可以是例如本文所述的TAT肽抗体。
在一些实施方案中,本发明提供了用于检测TAT肽(例如,TAT蛋白转导结构域或包含TAT蛋白转导结构域的TAT融合分子)的标记,其中所述标记包含TAT肽的结合配偶体和萦光部分,其中当通过由激光器在部分的激发波长处发射光来模拟时,该萦光部分能够发射至少约200个光子,其中所述激光器聚焦在含有所述部分的直径不小于约5微米的点上,并且其中由所述激光器导向所述点的总能量不超过约3微焦耳。在一些实施方案中,萦光部分包含萦光分子。在一些实施方案中,萦光部分包含多个萦光分子,例如约2至10个、2至8个、2至6个、2至4个、3至10个、3至8个或3至6个萦光分子。在一些实施方案中,标记部分包含约2至4个萦光分子。在一些实施方案中,萦光染料分子包含至少一个取代吲哚环体系,其中吲哚环的3-碳上的取代基包含化学反应性基团或偶联物质。在一些实施方案中,萦光分子选自由以下组成的组:Alexa Fluor 488、Alexa Fluor532、Alexa Fluor 647、Alexa Fluor680或Alexa Fluor 700。在一些实施方案中,萦光分子选自由以下组成的组:Alexa Fluor488、Alexa Fluor 532、Alexa Fluor 680或Alexa Fluor 700。在一些实施方案中,萦光分子是Alexa Fluor 647分子。在一些实施方案中,结合配偶体包含如本文所述的抗TAT肽抗体。
电子顺磁共振(EPR)自旋示踪剂标记也可用于检测TAT肽,例如,TAT蛋白转导结构域或包含TAT蛋白转导结构域的TAT融合分子,其中TAT抗体也被EPR示踪剂标记(参见,例如,Hubbell等,1998,Current Opinion in Structural Biology,8(5):649,其内容在此通过引用并入本文)。
作为标记抗体的替代方案,通过利用被可测定物质标记的TAT肽标准物和未被标记的TAT肽抗体的竞争免疫测定在生物流体样品中测定TAT肽(例如,TAT蛋白转导结构域或包含TAT蛋白转导结构域的TAT融合分子)。在该测定中,将生物样品、标记的TAT肽标准物和TAT肽抗体组合,并测定与未标记抗体结合的标记的标准物的量。生物样品中TAT肽(例如,TAT蛋白转导结构域或包含TAT蛋白转导结构域的TAT融合分子)的量与结合至抗TAT肽抗体的标记的标准物的量成反比。类似地,通过利用被可测定物质标记的TAT肽标准物和未被标记的TAT肽抗体的竞争免疫测定在生物流体样品中测定TAT肽(例如,TAT蛋白转导结构域或包含TAT蛋白转导结构域的TAT融合分子)。
C.本发明的治疗用途
结合蛋白(例如,抗体及其抗体部分)优选地能够在体内和体外中和TAT活性。
以前已经发现,TAT疫苗接种以及针对TAT蛋白的抗体的施用对于HIV-1感染是保护性的,并且可以产生长期抑制。此外,在急性暴露的情况下,抗TAT抗体的输注也可以阻断HIV-1复制的细胞外TAT自分泌/旁分泌反式激活(参见,例如,Moreau等,Journal ofGeneral Virology(2004),85,2893-2901;Bennasser,Y.等,(2002).Virology 303,174-180;Ensoli,B.等,(1990).Nature,345,84-86;Moreau,E.等,(2004).J Virol 78,3792-3796;Re,M.C.,Furlini,G.,Vignoli,M.(1995).J Acquir Immune Defic Syndr HumRetrovirol 10,408-416;Re,M.C.,Vignoli等,(2001).J Clin Virol 21,81-89;Richardson,M.W.,Mirchandani,J.等,(2003).Biomed Pharmacother57,4-14;Tikhonov,I.等,(2003)J Virol 77,3157-3166;Steinaa,L.等,(1994)Arch Virol 139,263–271;Silvera,P.等,(2002)J Virol 76,3800-3809,其内容通过引用并入本文)。
因此,本发明的结合蛋白可用于抑制TAT活性,例如在细胞培养物中、在人类受试者中或在其他哺乳动物受试者中,从而阻断或抑制HIV感染。在一个实施方案中,本公开提供了用于抑制TAT活性的方法,其包含使TAT与结合蛋白(例如,抗体或抗原结合部分)接触,使得TAT活性被抑制。
在另一个实施方案中,本文公开了用于在受试者中,有利地在患有TAT相关疾病(例如,HIV感染或AIDS)的受试者中降低TAT活性的方法。本公开提供了用于降低患有这种疾病的受试者中的TAT活性的方法,该方法包括向受试者施用结合蛋白,例如本公开的抗体或抗体部分,使得受试者中的TAT肽活性降低。优选地,受试者是人类受试者。
在另一个实施方案中,本文公开的是一种用于抑制受试者中HIV-TAT蛋白活性的方法,该方法包括向受试者施用本发明的抗原结合蛋白,从而抑制受试者中HIV-TAT蛋白的活性。
结合蛋白(例如,本公开的抗体)可出于治疗目的施用于人类受试者。此外,出于兽医目的或作为人类疾病的动物模型,可向包含TAT肽的非人哺乳动物施用结合蛋白,例如本公开的抗体,所述TAT肽能够与所述抗体结合。关于后者,这种动物模型可被用于评估本公开的抗体的治疗功效(例如,测试施用的剂量和时间过程)。
可用结合蛋白(例如,抗体及其抗原结合部分)治疗的疾病的非限制性示例包括HIV感染和AIDS及其相关症状。
在另一个方面,本申请的特征在于在受试者中治疗(例如治愈、压制、改善、抑制、延迟或预防TAT相关病症的发作、或预防其重现或复发)或预防TAT相关病症的方法。所述方法包括:以足以治疗或预防TAT相关病症的量向受试者施用结合蛋白,例如本文所述的抗TAT肽抗体或其部分。TAT拮抗剂(例如,抗TAT抗体或其部分)可以单独或与本文所述的其他治疗方式联合向受试者施用。
结合蛋白(例如,抗体及其抗原结合部分)可以单独或组合使用以治疗此类疾病。应当理解,抗体或其抗原结合部分可单独使用或与其他药剂(例如,治疗剂)组合使用,所述其他药剂由本领域技术人员出于其预期目的而选择。例如,另外的药剂可以是本领域公认的可用于治疗由抗体治疗的疾病或病症(例如,HIV或AIDS)或其相关症状的治疗剂。另外的药剂还可以是赋予治疗组合物有益属性的药剂,例如影响组合物粘度的药剂。
还应当理解,包括在本公开内的组合是可用于其预期目的的那些组合。下面列出的药剂是说明性的而不是限制性的。作为本公开的一部分的组合可以是本公开的抗体和至少一种另外的药剂。如果组合使得所形成的组合物可以表现其预期功能,那么组合还可以包括多于一种另外的药剂,例如两种或三种另外的药剂。
组合疗法可包括与一种或多种抗HIV剂一起配制和/或共同施用的一种或多种TAT拮抗剂(例如,抗TAT抗体或其部分)。术语“抗HIV剂”是指用于抑制或预防HIV感染和AIDS、或治疗或改善HIV感染或AIDS的症状的药物。在一个实施方案中,本发明的抗TAT抗体与一种或多种抗逆转录病毒疗法(ART)组合施用,所述抗逆转录病毒疗法包括但不限于非核苷逆转录酶抑制剂(NNRTI),例如依法韦仑(SustivaTM)、依曲韦林(IntelenceTM)和奈韦拉平(ViramuneTM);核苷或核苷酸逆转录酶抑制剂(NRTI),例如AbacavirTM(ZiagenTM),以及联合药物恩曲他滨/替诺福韦(TruvadaTM)、DescovyTM(替诺福韦艾拉酚胺/恩曲他滨)和拉米夫定-齐多夫定(CombivirTM);蛋白酶抑制剂(PI),例如阿扎那韦(ReyatazTM)、地瑞那韦(PrezistaTM)、福沙那韦(LexivaTM)和茚地那韦(CrixivanTM);进入或融合抑制剂,例如恩夫韦地(FuzeonTM)和马拉韦罗(SelzentryTM);和整合酶抑制剂,例如雷特格韦(IsentressTM)和度鲁特韦(TivicayTM)。
在特定的实施方案中,抗TAT抗体或ADC可单独施用或与另一种抗HIV剂一起施用,所述另一种抗HIV剂与抗体结合或协同作用以治疗与TAT活性相关的疾病。
本文提供的是用于治疗患者中的HIV或AIDS的方法,其包括向患者施用本发明的抗TAT结合蛋白(例如,抗体或其片段),其中组合疗法在所述受试者中表现出协同作用,例如,治疗协同作用。如本文所用,“协同作用”或“治疗协同作用”是指一种现象,其中用治疗剂的组合治疗患者表现出治疗上优于所述组合的单个组分各自以其最佳剂量使用的所实现的结果。例如,治疗上优异的结果是这样的结果,其中患者a)在接受治疗益处的同时表现出较低的不良事件发生率,所述治疗益处等于或大于所述组合的单个组分各自以与所述组合中相同的剂量作为单一疗法施用时的治疗益处,或b)在接受治疗益处的同时不表现出剂量限制性毒性,所述治疗益处大于当所述组合的单个组分各自以与所述组合中相同的剂量施用进行治疗取得的益处。
药物组合物可包括“治疗有效量”或“预防有效量”的抗体或抗体部分。“治疗有效量”是指在必要的剂量和时间段内有效实现所需治疗结果的量。抗体或抗体部分的治疗有效量可由本领域技术人员确定,并且可以依据多种因素而发生变化,例如个体的疾病状态、年龄、性别和体重,以及抗体或抗体部分在个体中引发期望的反应的能力。治疗有效量也是其中治疗有益效果超过抗体或抗体部分的任何毒性或有害作用果的量。“预防有效量”是指在必要的剂量和时间期间内有效实现预期的预防结果的量。通常,由于在疾病之前或疾病的早期阶段在受试者中使用预防剂量,所以预防有效量将小于治疗有效量。
可以调整剂量方案以提供最佳的期望反应(例如,治疗或预防反应)。例如,可以施用单次大剂量、可以随时间分多个剂量施用、或者可以根据治疗情况的紧急程度按比例减少或增加剂量。特别有利的是将肠胃外组合物配制成易于施用和剂量均匀的剂量单位形式。本文所用的剂量单位形式是指适合作为用于待治疗的哺乳动物受试者的单位剂量的物理离散单位;每个单位含有与所需药物载体相结合的经过计算可产生预期治疗效果的预定量的活性化合物。剂量单位形式的规格直接或间接取决于:(a)活性化合物的独特特征和待实现的特定治疗或预防效果,和(b)配伍成用于个体治疗敏感性的这种活性化合物的领域内到的固有限制。
抗体或抗体部分的治疗或预防有效量的示例性非限制性范围是0.1-20mg/kg,更优选1-10mg/kg。应注意,剂量值可随待缓解的病状的类型和严重程度而变化。还应当理解,对于任何特定的受试者,应当根据个体需要和施用或监督组合物施用的人的专业判断,随时间调整具体的给药方案,并且本文所示的剂量范围仅为示例性的而不旨在限制所要求保护的组合物的范围或实践。
D.本发明的诊断用途
在一些实施方案中,本文提供的任何抗TAT抗体可用于检测生物样品中TAT和HIV的存在。检测包括定量或定性检测。
本文公开的结合蛋白(例如,抗体)可用于多种目的,例如用于在受试者中检测HIV感染或诊断AIDS。这些方法可包括使来自被诊断为HIV或AIDS的受试者的样品与本文所述的结合蛋白(例如,抗体)接触,并检测结合蛋白(例如,抗体)与样品的结合。相对于结合蛋白(例如,抗体)与对照样品的结合,结合蛋白(例如,抗体)与样品的结合的增加证实了受试者患有HIV感染和/或AIDS。在一些实施方案中,方法进一步包括使结合TAT肽的第二抗体与样品接触,并检测第二抗体的结合。在一些非限制性示例中,相对于对照样品,抗体与样品结合的增加检测受试者中的TAT肽,从而诊断受试者中的HIV感染。
根据另一个实施方案,本发明提供了诊断方法。诊断方法通常包括使从患者获得的生物样品(例如,血液、血清、唾液、尿液、痰液、细胞拭子样品或组织活检样品)与TAT结合蛋白(例如,抗体)接触,并确定与对照样品或预定截止值相比,结合蛋白(例如,抗体)是否优先与样品结合,从而表明样品中TAT肽的存在。
在一些实施方案中,提供了用于诊断或检测方法的抗TAT结合蛋白,例如抗体。在另一个方面,提供了检测生物样品中TAT肽的存在的方法。在一些实施方案中,方法包括在允许抗TAT结合蛋白(例如,抗体)与TAT肽结合的条件下,使生物样品与如本文所述的抗TAT结合蛋白(例如,抗体)接触,并检测抗TAT结合蛋白(例如,抗体)与TAT肽之间是否形成复合物。这种方法可以是体外或体内方法。在一些实施方案中,抗TAT结合蛋白(例如,抗体)被用于选择适合用抗TAT结合蛋白(例如,抗体)治疗的受试者,例如其中使用HIV感染来选择患者。
可以使用本发明的结合蛋白(例如,抗体)诊断的示例性疾病包括TAT相关疾病,例如特征在于HIV感染的疾病,包括AIDS。
本发明的方法可以与本领域技术人员使用的任何其他方法结合实施,以提供TAT相关疾病的发生或复发的诊断。应当理解,本文提供的诊断和监测方法通常与本领域已知的其他方法结合使用。例如,本发明的方法可以与健康检查和其他已知的诊断方法结合实施。
还提供了用于评估治疗方案在受试者中的功效的方法。在这些方法中,评估一对样品(在较早时间点或在治疗方案之前获取自受试者的第一样品和在较晚时间点(例如,当受试者已经历治疗方案的至少一部分时的较晚时间点)获取自受试者的第二样品)中TAT肽的量。应当理解,本发明的方法包括以定期或不定期的间隔获得和分析多于两个样品(例如,3、4、5、6、7、8、9或更多个样品)以评估TAT肽水平。可以在连续或非连续受试者样品之间进行成对比较。
本发明提供了用于监测受试者中TAT相关疾病的治疗的方法,其通过(1)在向受试者施用治疗方案的至少一部分之前,使获取自受试者的第一生物样品与对TAT肽具有特异性的检测试剂接触;(2)在向受试者施用至少一部分治疗方案后,使获取自受试者的第二生物样品与对TAT肽特异的检测试剂接触;(3)通过各检测试剂测量在第一生物样品和第二生物样品中各自检测到的TAT肽的量;和(4)比较第一样品中TAT肽的表达水平与第二样品中TAT肽的表达水平,从而监测受试者中TAT相关疾病的治疗。
在某些实施方案中,本文提供的诊断和监测方法进一步包含获得受试者样品。
在某些实施方案中,本文提供的诊断和监测方法进一步包含基于检测到的TAT肽的水平为受试者选择治疗方案。
1.诊断方法
本发明的结合蛋白(例如,抗体或其抗原结合片段)可用于检测、定量、分离和/或纯化TAT肽(例如,TAT蛋白转导结构域)的方法。在本文提供的方法的一些实施方案中,TAT蛋白转导结构域包含在TAT融合分子中。因此,在一些实施方案中,本发明的结合蛋白(例如,抗体或其抗原结合片段)可用于检测、定量、分离和/或纯化TAT融合分子的方法中。应当理解,本文提供的任何方法可应用于TAT肽、TAT蛋白转导结构域和/或TAT融合分子。
用于检测生物样品中TAT肽(例如,TAT蛋白转导结构域或TAT融合分子)的存在或不存在或量或水平的示例性方法包括:从测试受试者处获得生物样品,并使所述生物样品与本发明的结合蛋白(例如,抗体或其抗原结合片段)接触以检测TAT肽(例如,TAT蛋白转导结构域或TAT融合分子)。
本文提供的用于检测生物样品中TAT肽(例如,TAT蛋白转导结构域或TAT融合分子)的存在或不存在或量或水平的方法包括:从受试者获得可能含有或可能不含有待检测的TAT肽(例如,TAT蛋白转导结构域或TAT融合分子)的生物样品,使所述样品与如本文所述的TAT肽结合蛋白(例如,抗体或其抗原结合片段)接触,并使样品与用于检测TAT肽(例如,TAT蛋白转导结构域-特异性结合剂复合物或TAT融合分子-特异性结合剂复合物(如果形成)的检测试剂接触。
方法包括在TAT肽(例如,TAT蛋白转导结构域或TAT融合分子)与本文所述的TAT肽抗体或其抗原结合片段之间形成瞬时或稳定复合物。方法需要复合物(如果形成)形成足够的时间以允许检测试剂与复合物结合并产生可检测的信号(例如萦光信号、来自酶反应(例如,过氧化物酶反应、磷酸酶反应、β-半乳糖苷酶反应或聚合酶反应)的产物的信号)。
完整抗体或其片段或衍生物(例如Fab或F(ab’)2)可用于本发明的方法中。这种TAT肽的检测策略用于例如ELISA、RIA、免疫沉淀反应、蛋白质印迹、抗体标记的萤光成像、组织免疫组织化学、免疫沉淀反应或免疫纯化,然后是质谱,例如免疫沉淀-多重反应监测(IPMRM)和免疫萦光测定法中。在某些实施方案中,例如,在ELISA、RIA、免疫沉淀反应、蛋白质印迹、免疫萦光测定中,TAT肽-特异性结合剂复合物被附着于用于检测TAT肽(例如,TAT蛋白转导结构域或TAT融合分子)的固体支持物上。复合物可以在基质上形成或在基质上捕获之前形成。对于凝胶内酶分析,TAT肽(例如,TAT蛋白转导结构域或TAT融合分子)在凝胶(通常为丙烯酰胺凝胶)中分解,所述凝胶中整合了酶的底物。
在另一个方面,本申请提供了用于体内(例如,在受试者体内成像)检测TAT肽(例如,TAT蛋白转导结构域或TAT融合分子)的存在的方法。所述方法可以被用于检测TAT肽(例如,TAT蛋白转导结构域)的存在,或用于检测或定量TAT融合分子,或用于在受试者中确定TAT融合分子的定位或验证TAT融合分子的递送。在例示性实施方案中,方法包括:(i)在允许抗体或片段与TAT肽结合的条件下,向受试者或对照受试者施用如本文所述的抗TAT肽抗体或其片段;和(ii)检测抗体或片段与TAT肽之间的复合物形成,其中所述受试者中的所述复合物形成相对于所述对照受试者的统计学上的显著变化表示TAT肽(例如,TAT蛋白转导结构域或TAT融合分子)的存在。
在一些实施方案中,本文提供的方法包括通过使获取自受试者的生物样品与本发明的TAT肽结合蛋白(例如,抗体或其抗原结合片段)接触以形成TAT肽(例如,TAG蛋白转导结构域或TAT融合分子)与TAT肽结合蛋白之间的复合物并纯化所述复合物,来检测生物样品中TAT肽(例如,TAT蛋白转导结构域或TAT融合分子)的存在或不存在或量或水平。在一些实施方案中,TAT肽结合蛋白可被固定在固体支持物(例如板、珠或层析树脂)上。在进一步的实施方案中,本文提供的方法可以包含基于质谱的分析,以在TAT肽(例如,TAT蛋白转导结构域或TAT融合分子)作为如上所述的复合物的一部分被纯化后,检测它的存在或不存在或量或水平。
在一些实施方案中,本文提供的方法包括通过使获取自受试者的生物样品与本发明的TAT肽结合蛋白(例如,抗体或其抗原结合片段)接触以形成TAT融合分子和TAT肽结合蛋白之间的复合物;纯化所述复合物;以及通过质谱分析所述TAT融合分子的至少一部分,来检测TAT融合分子的存在或不存在或量或水平。在一些实施方案中,TAT肽结合蛋白可被固定在固体支持物(例如板、珠或层析树脂)上。
在一些实施方案中,本文提供的方法包括通过使获取自受试者的生物样品与固定在固体支持物上的本发明的TAT-肽结合蛋白(例如,例如抗体或其抗原结合片段)接触以形成TAT融合分子和TAT-肽结合蛋白之间的复合物;纯化所述复合物;用蛋白酶(例如,胰蛋白酶)处理所述复合物以产生至少一种衍生自TAT融合分子的肽;以及通过质谱分析所述至少一种肽,来检测TAT融合分子的存在或不存在或量或水平。在一些实施方案中,TAT融合分子可以是TAT共济蛋白融合分子。
已经发现,本领域内已知的TAT肽结合蛋白,例如来自Abcam的市售的抗TAT小鼠单克隆IgM抗体(ab63957),当在用于检测生物样品中TAT共济失调蛋白融合分子的存在或不存在或量或水平的方法中使用时,其特征在于表现不佳。例如,已经发现,当将市售的抗TAT抗体用于从生物样品中免疫纯化TAT共济蛋白融合分子,然后用胰蛋白酶消化免疫纯化复合物并通过液相色谱和质谱(LC/MS)测定胰蛋白酶肽的水平时,所得质谱信号低于在将市售的抗共济蛋白抗体用于免疫纯化的类似实验中获得的质谱信号。这一结果表明市售的抗TAT抗体不能从生物样品中免疫纯化足够量的TAT共济蛋白融合分子,以允许对TAT共济蛋白融合分子的可靠检测和定量。本发明的TAT肽结合蛋白克服了上述表现不佳的问题,并允许对TAT融合分子(例如,TAT共济蛋白融合分子)的可靠的检测和定量。
因此,在一些方面,提供了用于检测样品中TAT融合分子的存在或定量TAT融合分子水平的方法,其包含使样品与本发明的TAT肽结合蛋白(例如,抗体或其抗原结合片段)接触,以形成TAT融合分子和TAT肽结合蛋白之间的复合物,从而检测样品中TAT融合分子的存在或定量TAT融合分子的水平,其中TAT肽结合蛋白表现出对TAT融合分子的特异性结合亲和力高于来自Abcam的抗TAT小鼠单克隆IgM抗体(ab63957)对TAT融合分子的特异性结合亲和力。在一些实施方案中,在包含一个或多个环境温度(例如20-25℃)、约7.4的pH、和磷酸缓冲盐水(PBS)缓冲液的条件下测量特异性结合亲和力。
在一些实施方案中,本发明的TAT肽结合蛋白的特征可在于KD比ab63957的KD低(即,更高亲和力)至少约2倍、至少约3倍、至少约4倍、至少约5倍、至少约6倍、至少约7倍、至少约8倍、至少约9倍、至少约10倍、至少约15倍、至少约20倍、至少约25倍、至少约100倍或至少约500倍。在一些实施方案中,KD在包含一个或多个环境温度(例如20-25℃)、约7.4的pH、和磷酸缓冲盐水(PBS)缓冲液的条件下测量。
在一些实施方案中,TAT融合分子是TAT共济蛋白融合分子。在一些实施方案中,样品可以是生物样品,例如,液体样品如血液样品、血浆样品或血清样品,或固体样品(例如,组织样品,如皮肤样品或口腔样品)。
在一些方面,提供了用于从样品分离或纯化TAT融合分子的方法,其包括使样品与本发明的TAT肽结合蛋白(例如,抗体或其抗原结合片段)接触,以形成TAT融合分子和TAT肽结合蛋白之间的复合物;以及从样品中分离或纯化所述复合物;其中TAT肽结合蛋白表现出对TAT融合分子的特异性结合亲和力高于来自Abcam的抗TAT小鼠单克隆IgM抗体(ab63957)对TAT融合分子的特异性结合亲和力。在一些实施方案中,在包含一个或多个环境温度(例如20-25℃)、约7.4的pH、和磷酸缓冲盐水(PBS)缓冲液条件下测量特异性结合。
在一些实施方案中,本发明的TAT肽结合蛋白的特征可在于KD比ab63957的KD低(即,更高亲和力)至少约2倍、至少约3倍、至少约4倍、至少约5倍、至少约6倍、至少约7倍、至少约8倍、至少约9倍、至少约10倍、至少约15倍、至少约20倍、至少约25倍、至少约100倍或至少约500倍。在一些实施方案中,KD在包含一个或多个环境温度(例如20-25℃)、约7.4的pH、和磷酸缓冲盐水(PBS)缓冲液的条件下测量。
在一些实施方案中,TAT融合分子是TAT共济蛋白融合分子。在一些实施方案中,样品可以是生物样品,例如液体样品如血液样品、血浆样品或血清样品,或固体样品(例如,组织样品,如皮肤样品或口腔样品)。
在一些方面,提供了用于检测样品中TAT融合分子的存在或定量样品中TAT融合分子水平的方法,其包括:
(a)使样品与本发明的TAT肽结合蛋白(例如,抗体或其抗原结合片段)接触,以形成TAT融合分子和TAT-肽结合蛋白之间的复合物,
(b)纯化所述复合物;
(c)用蛋白酶(例如,胰蛋白酶)处理所述复合物以产生至少一种衍生自TAT融合分子的肽;以及
(d)通过质谱分析所述至少一种肽,从而产生对应于所述肽的质谱信号;
其中步骤(d)中生成的所述质谱信号比使用来自Abcam的抗TAT小鼠单克隆IgM抗体(ab63957)进行步骤(a)时产生的质谱信号高至少约2至约10倍,例如,高至少约3倍、高至少约4倍、高至少约5倍、高至少约6倍、高至少约7倍、高至少约8倍、高至少约9倍或高至少约10倍。
在一些实施方案中,步骤(a)可以在包含一个或多个环境温度(例如20-25℃)、约7.4的pH、和磷酸缓冲盐水(PBS)缓冲液的条件下进行。
在一些实施方案中,TAT融合分子是TAT共济蛋白融合分子。在一些实施方案中,样品可以是生物样品,其可以是液体样品(例如,血液样品、血浆样品或血清样品)或固体样品(例如,组织样品,如皮肤样品或口腔样品)。
E.试剂盒
本发明提供了用于检测、定量、纯化和/或分离TAT肽,特别是包含TAT蛋白转导结构域的TAT融合分子的组合物和试剂盒。本发明还提供了用于诊断或监测TAT相关疾病或TAT相关疾病的复发的组合物和试剂盒。
这些试剂盒包含以下一项或多项:与TAT肽(例如,TAT蛋白转导结构域或包含TAT蛋白转导结构域的TAT融合分子)特异性结合的可检测的结合蛋白(例如,抗体),用于获取和/或制备用于染色的受试者组织样品的试剂,以及使用说明书。在一个实施方案中,结合蛋白(例如,抗体)是本文所述结合蛋白中的任何一种或多种。
本发明还包含用于检测生物样品中TAT肽(例如,TAT蛋白转导结构域或包含TAT蛋白转导结构域的TAT融合分子)的存在的试剂盒。这种试剂盒可用于检测、定量、纯化和/或分离TAT蛋白转导结构域或包含TAT蛋白转导结构域的TAT融合分子。这种试剂盒也可用于确定受试者是否患有TAT相关疾病。例如,试剂盒可以包含能够检测生物样品中的TAT肽(例如,TAT蛋白转导结构域或包含TAT蛋白转导结构域的TAT融合分子)的标记化合物或试剂,和用于检测和/或定量和/或分离和/或纯化样品中的TAT肽(例如,TAT蛋白转导结构域或包含TAT蛋白转导结构域的TAT融合分子)的装置。
试剂盒还可以包含试剂盒的使用说明书,其用于实践本文提供的任何方法或基于本文提供的教导解释使用试剂盒获得的结果。试剂盒还可以包含用于检测样品中与TAT相关疾病无关的对照蛋白的试剂,例如,组织样品的肌动蛋白、用于使样品中存在的靶抗原的量正常化的血液或血液来源样品中的白蛋白。该试剂盒还可以包含用于检测的纯化的TAT肽(例如,包含TAT蛋白转导结构域的TAT融合分子),以作为对照或用于对用该试剂盒进行的检测进行定量。
试剂盒包含用于诊断受试者中TAT相关疾病(例如,HIV感染或AIDS)的方法的试剂,所述试剂盒包含检测试剂,例如本发明的抗体,其中所述检测试剂对TAT肽(例如,TAT蛋白转导结构域或包含TAT蛋白转导结构域的TAT融合分子)具有特异性。在一个实施方案中,检测试剂是本文所述结合蛋白中的任何一种或多种。
对于基于抗体的试剂盒,试剂盒可以包含,例如:(1)与第一靶蛋白(例如,TAT肽)结合的第一抗体(例如,附着于固体支持物上);和任选地,(2)与第一靶蛋白或第一抗体结合并与可检测标记耦合的第二不同抗体。
特异性检测TAT肽(例如,包含TAT蛋白转导结构域的TAT融合分子)的试剂允许复杂混合物(例如,血清或组织样品)中的TAT肽(例如,包含TAT蛋白转导结构域的TAT融合分子)的检测和定量。在某些实施方案中,用于检测、定量、分离或纯化TAT肽(例如,包含TAT蛋白转导结构域的TAT融合分子)或用于诊断或监测TAT相关疾病的试剂盒包含至少一种特异性检测TAT肽(例如,包含TAT蛋白转导结构域的TAT融合分子)的试剂。
在某些实施方案中,试剂盒还包含用于检测、定量、分离或纯化TAT肽(例如,包含TAT蛋白转导结构域的TAT融合分子)或用于基于TAT肽(例如,包含TAT蛋白转导结构域的TAT融合分子)的表达水平诊断或监测TAT相关疾病的说明书。
在某些实施方案中,试剂盒还可包含但不限于缓冲剂、防腐剂、蛋白质稳定剂、反应缓冲液中的任何一种。试剂盒还可包含检测可检测标记(例如,酶或底物)所需的组分。试剂盒还可以包含对照样品或一系列对照样品,其可以被测定并与测试样品比较。对照可以是具有已知水平的靶TAT肽的对照血清样品或纯化蛋白质或核酸的对照样品(视情况而定)。试剂盒的每个组分可以被封装在单独的容器中,并且所有不同的容器可以和用于解释使用试剂盒进行的测定的结果的说明书一起位于单独的包装中。
本发明的试剂盒可任选地包含用于实施本发明的方法的其他组分。
IV.药物组合物
本发明还提供包含本发明的结合蛋白(例如,抗体或其抗原结合部分)和药学上可接受的载体的药物组合物。包含本发明抗体的药物组合物用于但不限于治疗TAT相关疾病和/或用于研究。在一个具体的实施方案中,药物组合物包含一种或多种结合蛋白(例如,本发明的抗体)。根据这些实施方案,组合物可进一步包含载体、稀释剂或赋形剂。
本发明的结合蛋白(例如,抗体或抗体部分)被掺入适合施用于受试者的药物组合物中。通常,药物组合物包含本发明的抗体或抗体部分和药学上可接受的载体。如本文所用,“药学上可接受的载体”包含生理学上相容的任何和所有溶剂、分散介质、包衣、抗细菌剂和抗真菌剂、等渗剂和吸收延迟剂等。药学上可接受的载体的示例包含水、盐水、磷酸盐缓冲盐水、右旋糖、甘油、乙醇等中的一种或多种及其组合。在许多情况下,优选的是组合物中包含等渗剂,例如糖、多元醇(例如,甘露醇、山梨醇或氯化钠)。药学上可接受的载体可以进一步包含少量的辅助物质,例如润湿剂或乳化剂、防腐剂或缓冲剂,其提高抗体或抗体部分的保存期限或有效性。
各种递送系统是已知的并且可用于施用一种或多种本发明的抗体,例如包封在脂质体中、微粒、微胶囊、能够表达抗体或抗体片段的重组细胞、受体介导的内吞作用(参见,例如,Wu和Wu,J.Biol.Chem.262:4429-4432(1987)),作为逆转录病毒或其他载体的部分的核酸构建体等。施用本发明的抗体的方法包括但不限于胃肠外施用(例如皮内、肌内、腹膜内、静脉内和皮下)、硬膜外施用、瘤内施用和粘膜施用(例如,鼻内和口服途径)。
本发明的药物组合物被配制成与其预期的施用途径相容。施用途径的示例包括但不限于肠胃外,例如静脉内、皮内、皮下、口服、鼻内(例如,吸入)、经皮(例如,局部)、经粘膜和直肠施用。在一个具体的实施方案中,根据常规方法将组合物配制成适于静脉内、皮下、肌内、口服、鼻内或局部施用于人的药物组合物。通常,用于静脉内施用的组合物是在无菌等渗水性缓冲液中的溶液。必要时,组合物还可以包含增溶剂和局部麻醉剂(例如,利多卡因)以减轻注射部位的疼痛。
如本领域技术人员将理解的,施用途径和/或模式将根据期望的结果而变化。
本领域技术人员容易想到的是,在不脱离本发明或本文公开的实施方案的范围的情况下,本文所述的本发明的方法的其他合适的修改和适应是显而易见的,并且可以使用合适的等同物进行。现在已经详细描述了本发明,通过参考以下实施例将更清楚地理解本发明,其中包含的这些实施例仅用于说明目的,而不旨在限制本发明。
实施例
实施例1:产生抗TAT肽抗体
进行实验以产生针对TAT蛋白转导结构域的兔单克隆抗体。产生兔多克隆和单克隆抗体,以及编码兔免疫球蛋白的表达质粒,其用于重组产生针对TAT部分(TAT蛋白转导结构域)的单克隆抗体。
研究发现,针对完整TAT-FXN融合分子的多克隆抗体识别药物,但不是以TAT特异性方式(见图1)。然而,针对KLH-TAT产生的多克隆抗体不识别成熟的共济蛋白,但识别BSA-TAT,这显示对TAT表位的特异性(见图2)。
简言之,用TAT免疫兔,然后收集血清、进行亲和纯化和脾杂交瘤融合以制备兔单克隆抗体(RabMab)。
先导优化包括融合后杂交瘤选择、通过EIA筛选的RabMab表达表征、有限稀释孔板接种、单细胞克隆分离和VH和VL测序,然后产生多毫克抗体。
方法
兔子中的免疫
通过用TAT肽抗原(MYGRKKRRQRRR-C,SEQ ID NO:46)与KLH或OVA耦合免疫兔E8332来获得多克隆抗体。所使用的TAT肽抗原包含TAT蛋白转导结构域的序列YGRKKRRQRRR(SEQID NO:23)。兔子在第一次取血(取血1)之前通过皮下注射接受4轮TAT肽,随后再注射一次并第二次取血(取血2)。取血2后,静脉内注射TAT肽,然后分离脾脏细胞。汇集取血1和2并通过用TAT肽抗原亲和纯化来纯化以产生多克隆抗TAT E8332多克隆抗体。血清效价数据和ELISA显示E8332对TAT共济蛋白融合分子和TAT肽抗原都有反应性,但对单独的共济蛋白没有反应性。
使用杂交瘤技术产生抗TAT单克隆抗体。脾脏细胞和骨髓瘤细胞融合后,选择抗TAT杂交瘤,并使克隆在半固态HAT选择培养基(次黄嘌呤-氨蝶呤-胸苷培养基)中生长。克隆在24孔多细胞培养物中生长至足够数量。在40个96孔培养板中进行单细胞接种,使得可从每孔的单个杂交瘤细胞中分离克隆。最后,针对培养板结合的BSA-TAT共济蛋白融合蛋白和BSA-共济蛋白进行ELISA。针对双抗原的多克隆筛选(扣除判读)允许针对TAT共济蛋白融合分子(BSA-TAT-共济蛋白)形式的TAT的克隆但不针对单独的共济蛋白(BSA-共济蛋白)的鉴定。
从杂交瘤中克隆VH和VL序列
为了测定CDR序列,从杂交瘤细胞中分离总RNA。进行第一和第二链cDNA合成。通过琼脂糖电泳分离PCR产物,切下片段并纯化。将片段直接克隆至表达载体中。将来自每个反应的克隆按比例放大用于小量制备规模的质粒纯化。
功能性重组VH和VL序列的鉴定
对于每个杂交瘤,测序每个质粒。对这些质粒进行DNA序列测定和分析。
结果
多克隆抗体
进行实验以比较如本文方法部分所描述产生的兔多克隆抗体与市售的抗共济蛋白(ab124680、ab113691、ab110328)和抗TAT(ab63957)抗体免疫纯化示例性TAT共济蛋白融合分子的能力。实验中使用的抗体描述于下表中。市售抗体来自Abcam。
首先将5种抗体生物素化,然后将其耦合至链霉亲和素包被的磁珠。将抗体耦合的珠加入含有示例性TAT共济蛋白融合分子的血浆样品中,并在室温下在PBS中孵育以发生结合。孵育后,用PBS洗涤珠并释放至消化缓冲液中。加入胰蛋白酶以产生示例性TAT共济蛋白融合分子的胰蛋白酶肽。消化后,加入甲酸以停止消化,去除珠并将消化的样品转移到干净的培养板中用于注射到液相色谱/质谱(LC/MS)系统。在LC/MS实验中,测定对应于共济蛋白衍生的胰蛋白酶肽GLNQIWNVK(SEQ ID NO:47)的峰强度。
实验结果示于图3中。具体而言,图3是显示用测试抗体免疫纯化示例性TAT共济蛋白融合分子后,由共济蛋白衍生的胰蛋白酶肽GLNQIWNVK(SEQ ID NO:47)产生的相对峰面积的条形图。图3中呈现的结果表明,当抗TAT抗体ab63957用于免疫纯化时产生的LC/MS信号比当使用抗共济蛋白抗体ab110328时产生的LC/MS信号低约5倍。结果还表明,使用抗TAT多克隆兔抗体进行免疫纯化产生的LC/MS信号比使用市售抗TAT抗体ab63957时高约5倍,而且与使用抗共济蛋白抗体ab110328时产生的LC/MS信号相似。这些结果证实了产生的多克隆兔抗体在免疫纯化示例性TAT共济蛋白融合分子方面比市售的抗TAT抗体ab63957有效得多。这些结果表明随后产生的抗TAT单克隆抗体将具有与多克隆抗体至少相同或更优异的免疫纯化TAT融合分子的能力。
单克隆抗体
通过本文所述的杂交瘤方法产生针对TAT蛋白转导结构域的单克隆抗体。
将10种抗体转化为针对TAT蛋白转导结构域的重组抗体。这些抗体被称为10-1、10-4、10-5、10-9、10-12、12-1、12-3、12-8、12-10和6.3。来自这10种抗体的重链和轻链的完整氨基酸序列如下表1中所示,示为SEQ ID NO:1-22。
抗体10-4、10-5、12-1、12-3具有相同的重链和轻链可变区序列;抗体10-9、12-8、12-10具有相同的重链和轻链可变区序列;抗体10-12和抗体10-1具有相同的重链和轻链可变区序列。抗体6.3具有独特的重链和轻链可变区序列。
除了一种抗体(抗体6.3)外,所有抗体具有相同的重链CDR序列。因此,高亲和力抗TAT单克隆抗体存在一个共有重链CDR组(SEQ ID NO:2、3和4)。
抗体10-1、10-9、10-12、12-8和12-10具有相同的轻链CDR序列,并且抗体10-4、10-5、12-1和12-3具有相同的轻链CDR序列。因此,高亲和力抗TAT单克隆抗体存在两个共有轻链CDR组(SEQ ID NO:6、7和8以及SEQ ID NO:10、11和12)。
表1:抗TAT人抗体重链和轻链可变区氨基酸序列
10种抗体的重链和轻链可变区的核酸序列如下表2所示。
表2:抗TAT人抗体重链和轻链可变区核酸序列
实施例2.筛选与TAT共济蛋白融合分子特异性结合的克隆
将实施例1中描述的10种高亲和力单克隆克隆的重和轻可变区的序列克隆至不同的兔IgG主链序列中以产生测试质粒。通过使用多克隆抗TAT捕获来改良夹心ELISA,以筛选对含有TAT的蛋白质具有适当捕获灵敏度的克隆,如下:用50μL 5μg/ml来自用测试质粒转染的克隆细胞的纯化表达抗体包被ELISA板,然后用高蛋白质缓冲液封闭。将用浓度范围为1000ng/ml至0.05ng/ml的加入TAT共济蛋白的50μL的缓冲液的校准液在室温下在包被的孔中孵育2小时,然后洗涤。然后将含有用HRP标记的已知的抗共济蛋白单克隆抗体的50μL缓冲液在孔中孵育1小时,随后洗涤,并与100μL TMB底物一起孵育20分钟。加入100μL 1N H2SO4终止检测反应,在450nm下读板。使用Softmax拟合曲线以测定灵敏度并比较表达该克隆的抗体。
在人血浆中的药代动力学(PK)测定中,10种鉴定的抗体中有9种(除抗体6.3外)能够有效地捕获包含TAT蛋白转导结构域和共济蛋白的示例性TAT融合分子(参见图4A和图4B)。
在人血浆中的结合测定中测试抗体与示例性TAT FXN融合分子的特异性结合。所用的结合测定是ADA或桥接测定,通常如以下实施例3中所描述。结合测定的结果示于图5A。结果表明,除了一种抗体(11563-1)以外,所有测试的重组抗体均表现出与TAT FXN融合分子的特异性结合。结果还表明,当置于不同的主链中时,抗TAT单克隆抗体的重链和轻链可变区的序列赋予特异性结合TAT-FXN融合分子的能力。这证实了高亲和力兔抗体的发现。除了克隆11563-1以外的所有克隆在高抗体浓度下显示钩状效应,如桥接/夹心试验所预期,其中捕获依赖于单一限定表位(TAT)。
实施例3.抗-TAT多克隆抗体在ADA测定中作为阳性对照是有效的
本实验的目的是比较通过本文所述方法产生的兔多克隆抗TAT抗体与市售的抗共济蛋白抗体,以确定兔多克隆抗TAT抗体是否可用于抗药物抗体(ADA)测定,以测试示例性TAT共济蛋白融合分子的免疫原性。
在测定中,示例性TAT共济蛋白融合分子的两种标记形式(生物素化和磺化标记形式)与具有限定浓度的抗体共孵育。在链霉亲和素板上孵育样品,洗去未结合的分子,随后读板以观察标记的(磺化标记的)抗体结合的量。这是一种桥接策略,其中能够结合两个TAT共济蛋白分子的高亲和力分子完成“桥接”,导致信号结合到板上。
结果示于图5B中。具体地,结果证实市售的抗共济蛋白单克隆抗体显示出桥接信号增强直至高达约10μg/ml抗体输入,并在更高浓度时信号减弱,这通常被描述为“钩状效应”。兔多克隆抗TAT抗体产生信号增强直至高达约50μg/ml,并保持最大信号至约200μg/ml的浓度。结果表明多克隆抗TAT抗体在ADA测定中作为阳性对照可以很好地发挥作用,以筛选临床样品例如用TAT共济蛋白融合分子治疗产生的潜在抗体。
序列表
等同物
本领域技术人员将认识到或仅使用常规实验能够确定本文所述的具体实施方案和方法的许多等同物。此类等同物旨在被包含在所附权利要求的范围内。
Claims (83)
1.一种包含抗原结合结构域的结合蛋白,所述抗原结合结构域包含含有SEQ ID NO:4的氨基酸序列的重链CDR3结构域,其中所述结合蛋白能够结合TAT蛋白转导结构域。
2.根据权利要求1所述的结合蛋白,其中所述抗原结合结构域进一步包含含有SEQ IDNO:3的氨基酸序列的重链CDR2结构域。
3.根据权利要求1或2所述的结合蛋白,其中所述抗原结合结构域进一步包含含有SEQID NO:2的氨基酸序列的重链CDR1结构域。
4.根据权利要求1-3中任一项所述的结合蛋白,其中所述抗原结合结构域进一步包含含有选自由SEQ ID NO:8和SEQ ID NO:12组成的组的氨基酸序列的轻链CDR3结构域。
5.根据权利要求1-4中任一项所述的结合蛋白,其中所述抗原结合结构域进一步包含含有选自由SEQ ID NO:7和SEQ ID NO:11组成的组的氨基酸序列的轻链CDR2结构域。
6.根据权利要求1-5中任一项所述的结合蛋白,其中所述抗原结合结构域进一步包含含有选自由SEQ ID NO:6和SEQ ID NO:10组成的组的氨基酸序列的轻链CDR1结构域。
7.一种包含抗原结合结构域的结合蛋白,所述抗原结合结构域包含:
重链可变区,其包含含有SEQ ID NO:4所示氨基酸序列的CDR3结构域,含有SEQ ID NO:3所示氨基酸序列的CDR2结构域和含有SEQ ID NO:2所示氨基酸序列的CDR1结构域;和
轻链可变区,其包含含有SEQ ID NO:8所示氨基酸序列的CDR3结构域,含有SEQ ID NO:7所示氨基酸序列的CDR2结构域和含有SEQ ID NO:6所示氨基酸序列的CDR1结构域;或轻链可变区,其包含含有SEQ ID NO:12所示氨基酸序列的CDR3结构域,含有SEQ ID NO:11所示氨基酸序列的CDR2结构域和含有SEQ ID NO:10所示氨基酸序列的CDR1结构域,
其中所述结合蛋白能够结合TAT蛋白转导结构域。
8.根据权利要求1-7中任一项所述的结合蛋白,其中所述抗原结合结构域包含含有SEQID NO:1或SEQ ID NO:14所示氨基酸序列的重链可变区。
9.根据权利要求1-8中任一项所述的结合蛋白,其中所述抗原结合结构域包含含有SEQID NO:5所示氨基酸序列的轻链可变区、含有SEQ ID NO:9所示氨基酸序列的轻链可变区、或含有SEQ ID NO:13所示氨基酸序列的轻链可变区。
10.根据权利要求1-9中任一项所述的结合蛋白,其中所述抗原结合结构域包含含有SEQ ID NO:1所示氨基酸序列的重链可变区和含有SEQ ID NO:5所示氨基酸序列的轻链可变区。
11.根据权利要求1-9中任一项所述的结合蛋白,其中所述抗原结合结构域包含含有SEQ ID NO:1所示氨基酸序列的重链可变区和含有SEQ ID NO:9所示氨基酸序列的轻链可变区。
12.根据权利要求1-9中任一项所述的结合蛋白,其中所述抗原结合结构域包含含有SEQ ID NO:1所示氨基酸序列的重链可变区和含有SEQ ID NO:13所示氨基酸序列的轻链可变区。
13.根据权利要求1-9中任一项所述的结合蛋白,其中所述抗原结合结构域包含含有SEQ ID NO:14所示氨基酸序列的重链可变区和含有SEQ ID NO:5所示氨基酸序列的轻链可变区。
14.一种包含抗原结合结构域的结合蛋白,所述抗原结合结构域包含含有SEQ ID NO:18的氨基酸序列的重链CDR3结构域,其中所述结合蛋白能够结合TAT蛋白转导结构域。
15.根据权利要求14所述的结合蛋白,其中所述抗原结合结构域进一步包含含有SEQID NO:17的氨基酸序列的重链CDR2结构域。
16.根据权利要求14或15所述的结合蛋白,其中所述抗原结合结构域进一步包含含有SEQ ID NO:16的氨基酸序列的重链CDR1结构域。
17.根据权利要求14-16中任一项所述的结合蛋白,其中所述抗原结合结构域进一步包含含有SEQ ID NO:22的氨基酸序列的轻链CDR3结构域。
18.根据权利要求14-17中任一项所述的结合蛋白,其中所述抗原结合结构域进一步包含含有SEQ ID NO:21的氨基酸序列的轻链CDR2结构域。
19.根据权利要求14-18中任一项所述的结合蛋白,其中所述抗原结合结构域进一步包含含有SEQ ID NO:20的氨基酸序列的轻链CDR1结构域。
20.一种包含抗原结合结构域的结合蛋白,所述抗原结合结构域包含:
重链可变区,其包含含有SEQ ID NO:18所示氨基酸序列的CDR3结构域,含有SEQ IDNO:17所示氨基酸序列的CDR2结构域和含有SEQ ID NO:16所示氨基酸序列的CDR1结构域;和
轻链可变区,其包含含有SEQ ID NO:22所示氨基酸序列的CDR3结构域,含有SEQ IDNO:21所示氨基酸序列的CDR2结构域和含有SEQ ID NO:20所示氨基酸序列的CDR1结构域,
其中所述结合蛋白能够结合TAT蛋白转导结构域。
21.根据权利要求14-20中任一项所述的结合蛋白,其中所述抗原结合结构域包含含有SEQ ID NO:15所示氨基酸序列的重链可变区。
22.根据权利要求14-21中任一项所述的结合蛋白,其中所述抗原结合结构域包含含有SEQ ID NO:19所示氨基酸序列的轻链可变区。
23.根据权利要求14-22中任一项所述的结合蛋白,其中所述抗原结合结构域包含含有SEQ ID NO:15所示氨基酸序列的重链可变区和含有SEQ ID NO:19所示氨基酸序列的轻链可变区。
24.根据权利要求1-23中任一项所述的结合蛋白,其中所述TAT蛋白转导结构域包含SEQ ID NO:23的氨基酸序列。
25.根据权利要求1-23中任一项所述的结合蛋白,其中所述TAT蛋白转导结构域基本上由SEQ ID NO:23的氨基酸序列组成。
26.根据权利要求1-25中任一项所述的结合蛋白,其中所述TAT蛋白转导结构域与货物部分共价连接。
27.根据权利要求26所述的结合蛋白,其中所述货物部分是多肽。
28.根据权利要求26所述的结合蛋白,其中所述货物部分是共济蛋白多肽。
29.根据权利要求26所述的结合蛋白,其中所述货物部分是抗体。
30.根据权利要求26所述的结合蛋白,其中所述货物部分是核酸。
31.根据权利要求30所述的结合蛋白,其中所述核酸是siRNA、shRNA、miRNA、硫代磷酸酯修饰的RNA、适配体、磷酰二胺吗啉代寡核苷酸(PMO)或其任何组合。
32.根据权利要求26所述的结合蛋白,其中所述货物部分是小分子、脂质体包封蛋白、放射性核素或放射性核素标记的化合物或其任何组合。
33.一种包含抗原结合结构域的结合蛋白,其中所述结合蛋白能够结合与货物部分共价连接的TAT蛋白转导结构域。
34.根据权利要求33所述的结合蛋白,其中所述抗原结合结构域结合包含SEQ ID NO:23的氨基酸残基的表位。
35.根据权利要求33所述的结合蛋白,其中所述货物部分是多肽。
36.根据权利要求33所述的结合蛋白,其中所述货物部分是共济蛋白多肽。
37.根据权利要求33所述的结合蛋白,其中所述货物部分是抗体。
38.根据权利要求33所述的结合蛋白,其中所述货物部分是核酸。
39.根据权利要求38所述的结合蛋白,其中所述核酸是siRNA、shRNA、miRNA、硫代磷酸酯修饰的RNA、适配体、磷酰二胺吗啉代寡核苷酸(PMO)或其任何组合。
40.根据权利要求33所述的结合蛋白,其中所述货物部分是小分子、脂质体包封蛋白、放射性核素或放射性核素标记的化合物或其任何组合。
41.根据权利要求1-40中任一项所述的结合蛋白,其中所述结合蛋白是抗体。
42.一种包含根据权利要求1-41中任一项所述的结合蛋白的抗体构建体,所述抗体构建体进一步包含接头多肽或免疫球蛋白恒定区。
43.根据权利要求42所述的抗体构建体,其中所述结合蛋白选自由以下组成的组:免疫球蛋白分子、单克隆抗体、鼠抗体、嵌合抗体、CDR移植抗体、人源化抗体、单域抗体、Fv、二硫键连接的Fv、scFv、双抗、Fab、Fab’、F(ab’)2、多特异性抗体、双重特异性抗体和双特异性抗体。
44.根据权利要求42和43中任一项所述的抗体构建体,其中所述结合蛋白包含选自由以下组成的组的重链免疫球蛋白恒定区:IgM恒定区、IgG4恒定区、IgG1恒定区、IgE恒定区、IgG2恒定区、IgG3恒定区和IgA恒定区。
45.根据权利要求44所述的抗体构建体,其中所述结合蛋白包含IgG1恒定区。
46.根据权利要求44所述的抗体构建体,其中所述重链免疫球蛋白恒定区不是IgM。
47.一种编码根据权利要求1-41中任一项所述的结合蛋白氨基酸序列的分离的核酸。
48.一种编码根据权利要求42-46中任一项所述的抗体构建体氨基酸序列的分离的核酸。
49.一种载体,其包含根据权利要求47或48所述的分离的核酸。
50.根据权利要求49所述的载体,其中所述载体选自由以下组成的组:pcDNA、pTT、pTT3、pEFBOS、pBV、pJV、pBJ、pGEX、VSV、pBR322、pCMV-HA、pEN、YAC、BAC、λ噬菌体、噬菌粒、pCAS9、pCEN6、pYES1L、p3HPRT1、pFN2A、pBC、pTZ、pGEM、pGEMK、pEX、pSAR、pCEP、黏性质粒、pBluescript、pKJK、pFloxin、pCP、pHR、pUC和pMAL。
51.一种宿主细胞,其包含根据权利要求49或50所述的载体。
52.根据权利要求51所述的宿主细胞,其中所述宿主细胞是原核细胞或真核细胞。
53.根据权利要求51所述的宿主细胞,其中所述原核宿主细胞是大肠杆菌细胞。
54.根据权利要求51所述的宿主细胞,其中所述真核细胞选自由以下组成的组:原生生物细胞、昆虫细胞、动物细胞、植物细胞和真菌细胞。
55.根据权利要求51所述的宿主细胞,其中所述动物细胞是哺乳动物细胞或禽类细胞。
56.根据权利要求51所述的宿主细胞,其中所述宿主细胞选自由以下组成的组:CHO细胞、COS细胞、酵母细胞、昆虫Sf9细胞、HEK-293细胞、ExpiCHO细胞、Expi-293f细胞和大肠杆菌细胞。
57.根据权利要求56所述的宿主细胞,其中所述酵母细胞是酿酒酵母细胞。
58.一种产生抗体或其抗原结合部分的方法,其包括在培养基中培养根据权利要求51-57中任一项所述的宿主细胞,从而表达所述分离的核酸并产生所述抗体。
59.一种抗体,其根据权利要求58所述的方法产生。
60.一种包含根据权利要求51-57中任一项所述的宿主细胞的转基因小鼠,其中所述小鼠表达由所述核酸编码的多肽或其抗原结合部分,所述多肽或其抗原结合部分与TAT蛋白转导结构域结合。
61.一种杂交瘤,其产生根据权利要求42-46中任一项所述的抗体构建体。
62.根据权利要求1-41中任一项所述的结合蛋白,其被固定在固体支持物上。
63.根据权利要求62所述的结合蛋白,其中所述固体支持物是板、珠或层析树脂。
64.根据权利要求63所述的结合蛋白,其中所述珠或层析树脂包含蛋白A琼脂糖或蛋白G琼脂糖。
65.根据权利要求1-41中任一项所述的结合蛋白,其与检测分子偶联。
66.根据权利要求65所述的结合蛋白,其中所述检测分子是辣根过氧化物酶、三联吡啶钌、碱性磷酸酶、甲酚紫、量子点、FITC、红外分子、放射性同位素标记或EPR自旋示踪剂标签。
67.一种检测和/或定量样品中TAT融合分子水平的方法,其包括在使根据权利要求1-41中任一项所述的结合蛋白与样品中TAT蛋白转导结构域结合的条件下,使所述样品与所述结合蛋白接触,从而检测和/或定量所述样品中TAT融合分子的水平。
68.根据权利要求67所述的方法,其中所述样品是生物样品。
69.根据权利要求68所述的方法,其中所述生物样品是液体样品或组织样品。
70.根据权利要求68所述的方法,其中所述TAT融合分子包含与货物部分共价连接的TAT蛋白转导结构域。
71.根据权利要求70所述的方法,其中所述货物部分是多肽。
72.根据权利要求70所述的方法,其中所述货物部分是共济蛋白多肽。
73.根据权利要求70所述的方法,其中所述货物部分是抗体。
74.根据权利要求70所述的方法,其中所述货物部分是核酸。
75.根据权利要求74所述的结合蛋白,其中所述核酸是siRNA、shRNA、miRNA、硫代磷酸酯修饰的RNA、适配体、磷酰二胺吗啉代寡核苷酸(PMO)或其任何组合。
76.根据权利要求70所述的结合蛋白,其中所述货物部分是小分子、脂质体包封蛋白、放射性核素或放射性核素标记的化合物或其任何组合。
77.根据权利要求67所述的方法,其进一步包括评估所述TAT融合分子的稳定性。
78.一种分离和/或纯化混合物中存在的TAT融合分子的方法,其中所述TAT融合分子包含与货物部分共价连接的TAT蛋白转导结构域,所述方法包括(a)在使得所述TAT融合分子与根据权利要求62-64中任一项所述的固定化结合蛋白结合的条件下,使包含所述TAT融合分子的所述混合物与所述固定化结合蛋白接触;(b)从所述固定化结合蛋白洗脱所述TAT融合分子。
79.一种试剂盒,其包含至少一种用于特异性检测TAT蛋白转导结构域水平的试剂,其中所述检测试剂是根据权利要求1-41中任一项所述的结合蛋白。
80.根据权利要求79所述的试剂盒,其中所述TAT蛋白转导结构域与货物部分共价连接。
81.根据权利要求79或80所述的试剂盒,其中所述试剂盒进一步包含用于检测、定量或表征所述TAT蛋白转导结构域的说明书。
82.一种抑制TAT融合分子跨细胞膜易位的方法,其包括使所述TAT融合分子与根据权利要求1-41中任一项所述的抗原结合蛋白接触,从而抑制所述TAT融合分子跨细胞膜易位。
83.一种抑制受试者中HIV-TAT蛋白的活性的方法,其包括向所述受试者施用根据权利要求1-41中任一项所述的抗原结合蛋白,从而抑制所述受试者中所述HIV-TAT蛋白的活性。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US202062970662P | 2020-02-05 | 2020-02-05 | |
| US62/970,662 | 2020-02-05 | ||
| PCT/US2021/016959 WO2021159024A1 (en) | 2020-02-05 | 2021-02-05 | Tat peptide binding proteins and uses thereof |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN115397848A true CN115397848A (zh) | 2022-11-25 |
Family
ID=74856923
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202180025971.XA Pending CN115397848A (zh) | 2020-02-05 | 2021-02-05 | Tat肽结合蛋白及其用途 |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US20230061973A1 (zh) |
| EP (1) | EP4100435A1 (zh) |
| KR (1) | KR20220137698A (zh) |
| CN (1) | CN115397848A (zh) |
| AU (1) | AU2021215936A1 (zh) |
| CA (1) | CA3167027A1 (zh) |
| IL (1) | IL295387A (zh) |
| WO (1) | WO2021159024A1 (zh) |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20100028359A1 (en) * | 2008-05-09 | 2010-02-04 | Abbott Gmbh & Co. Kg | Antibodies to receptor of advanced glycation end products (rage) and uses thereof |
| CN106661112A (zh) * | 2014-07-16 | 2017-05-10 | Ucb生物制药私人有限公司 | 具有针对cd45和cd79的特异性的分子 |
Family Cites Families (75)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5780A (en) | 1848-09-19 | Improvement in preparing shoe-pegs | ||
| US225A (en) | 1837-06-03 | Machine fob | ||
| US4491632A (en) | 1979-10-22 | 1985-01-01 | The Massachusetts General Hospital | Process for producing antibodies to hepatitis virus and cell lines therefor |
| US4444887A (en) | 1979-12-10 | 1984-04-24 | Sloan-Kettering Institute | Process for making human antibody producing B-lymphocytes |
| DE3167442D1 (en) | 1980-07-07 | 1985-01-10 | Nat Res Dev | Improvements in or relating to cell lines |
| US4341761A (en) | 1980-07-25 | 1982-07-27 | E. I. Du Pont De Nemours And Company | Antibodies to immunogenic peptides and their use to purify human fibroblast interferon |
| US4466917A (en) | 1981-02-12 | 1984-08-21 | New York University | Malaria vaccine |
| US4493890A (en) | 1981-03-23 | 1985-01-15 | Miles Laboratories, Inc. | Activated apoglucose oxidase and its use in specific binding assays |
| US4451570A (en) | 1981-03-26 | 1984-05-29 | The Regents Of The University Of California | Immunoglobulin-secreting human hybridomas from a cultured human lymphoblastoid cell line |
| US4399121A (en) | 1981-11-04 | 1983-08-16 | Miles Laboratories, Inc. | Iodothyronine immunogens and antibodies |
| US4427783A (en) | 1981-12-14 | 1984-01-24 | Hoffmann-La Roche Inc. | Immunoassay of thymosin α1 |
| US4816567A (en) | 1983-04-08 | 1989-03-28 | Genentech, Inc. | Recombinant immunoglobin preparations |
| US4493795A (en) | 1983-10-17 | 1985-01-15 | Syntex (U.S.A.) Inc. | Synthetic peptide sequences useful in biological and pharmaceutical applications and methods of manufacture |
| WO1986005803A1 (fr) | 1985-03-30 | 1986-10-09 | Marc Ballivet | Procede d'obtention d'adn, arn, peptides, polypeptides ou proteines, par une technique de recombinaison d'adn |
| US6492107B1 (en) | 1986-11-20 | 2002-12-10 | Stuart Kauffman | Process for obtaining DNA, RNA, peptides, polypeptides, or protein, by recombinant DNA technique |
| US5618920A (en) | 1985-11-01 | 1997-04-08 | Xoma Corporation | Modular assembly of antibody genes, antibodies prepared thereby and use |
| DE3600905A1 (de) | 1986-01-15 | 1987-07-16 | Ant Nachrichtentech | Verfahren zum dekodieren von binaersignalen sowie viterbi-dekoder und anwendungen |
| GB8607679D0 (en) | 1986-03-27 | 1986-04-30 | Winter G P | Recombinant dna product |
| US5225539A (en) | 1986-03-27 | 1993-07-06 | Medical Research Council | Recombinant altered antibodies and methods of making altered antibodies |
| US4946778A (en) | 1987-09-21 | 1990-08-07 | Genex Corporation | Single polypeptide chain binding molecules |
| WO1988007089A1 (en) | 1987-03-18 | 1988-09-22 | Medical Research Council | Altered antibodies |
| US5258498A (en) | 1987-05-21 | 1993-11-02 | Creative Biomolecules, Inc. | Polypeptide linkers for production of biosynthetic proteins |
| US5223409A (en) | 1988-09-02 | 1993-06-29 | Protein Engineering Corp. | Directed evolution of novel binding proteins |
| DE768377T1 (de) | 1988-09-02 | 1998-01-02 | Dyax Corp | Herstellung und Auswahl von Rekombinantproteinen mit verschiedenen Bindestellen |
| WO1990005144A1 (en) | 1988-11-11 | 1990-05-17 | Medical Research Council | Single domain ligands, receptors comprising said ligands, methods for their production, and use of said ligands and receptors |
| US5530101A (en) | 1988-12-28 | 1996-06-25 | Protein Design Labs, Inc. | Humanized immunoglobulins |
| EP0478627A4 (en) | 1989-05-16 | 1992-08-19 | William D. Huse | Co-expression of heteromeric receptors |
| CA2016841C (en) | 1989-05-16 | 1999-09-21 | William D. Huse | A method for producing polymers having a preselected activity |
| CA2016842A1 (en) | 1989-05-16 | 1990-11-16 | Richard A. Lerner | Method for tapping the immunological repertoire |
| GB8928874D0 (en) | 1989-12-21 | 1990-02-28 | Celltech Ltd | Humanised antibodies |
| AU7247191A (en) | 1990-01-11 | 1991-08-05 | Molecular Affinities Corporation | Production of antibodies using gene libraries |
| US5427908A (en) | 1990-05-01 | 1995-06-27 | Affymax Technologies N.V. | Recombinant library screening methods |
| GB9015198D0 (en) | 1990-07-10 | 1990-08-29 | Brien Caroline J O | Binding substance |
| ATE185601T1 (de) | 1990-07-10 | 1999-10-15 | Cambridge Antibody Tech | Verfahren zur herstellung von spezifischen bindungspaargliedern |
| CA2090126C (en) | 1990-08-02 | 2002-10-22 | John W. Schrader | Methods for the production of proteins with a desired function |
| US5698426A (en) | 1990-09-28 | 1997-12-16 | Ixsys, Incorporated | Surface expression libraries of heteromeric receptors |
| DE69129154T2 (de) | 1990-12-03 | 1998-08-20 | Genentech, Inc., South San Francisco, Calif. | Verfahren zur anreicherung von proteinvarianten mit geänderten bindungseigenschaften |
| DK1279731T3 (da) | 1991-03-01 | 2007-09-24 | Dyax Corp | Fremgangsmåde til udvikling af bindende miniproteiner |
| ATE269401T1 (de) | 1991-04-10 | 2004-07-15 | Scripps Research Inst | Bibliotheken heterodimerer rezeptoren mittels phagemiden |
| EP0519596B1 (en) | 1991-05-17 | 2005-02-23 | Merck & Co. Inc. | A method for reducing the immunogenicity of antibody variable domains |
| EP0590067A1 (en) | 1991-06-14 | 1994-04-06 | Xoma Corporation | Microbially-produced antibody fragments and their conjugates |
| DE4122599C2 (de) | 1991-07-08 | 1993-11-11 | Deutsches Krebsforsch | Phagemid zum Screenen von Antikörpern |
| ES2136092T3 (es) | 1991-09-23 | 1999-11-16 | Medical Res Council | Procedimientos para la produccion de anticuerpos humanizados. |
| DE69233782D1 (de) | 1991-12-02 | 2010-05-20 | Medical Res Council | Herstellung von Autoantikörpern auf Phagenoberflächen ausgehend von Antikörpersegmentbibliotheken |
| CA2507749C (en) | 1991-12-13 | 2010-08-24 | Xoma Corporation | Methods and materials for preparation of modified antibody variable domains and therapeutic uses thereof |
| US5714350A (en) | 1992-03-09 | 1998-02-03 | Protein Design Labs, Inc. | Increasing antibody affinity by altering glycosylation in the immunoglobulin variable region |
| US5733743A (en) | 1992-03-24 | 1998-03-31 | Cambridge Antibody Technology Limited | Methods for producing members of specific binding pairs |
| US5639641A (en) | 1992-09-09 | 1997-06-17 | Immunogen Inc. | Resurfacing of rodent antibodies |
| AU696293B2 (en) | 1993-12-08 | 1998-09-03 | Genzyme Corporation | Process for generating specific antibodies |
| PT1231268E (pt) | 1994-01-31 | 2005-11-30 | Univ Boston | Bancos de anticorpos policlonais |
| US5516637A (en) | 1994-06-10 | 1996-05-14 | Dade International Inc. | Method involving display of protein binding pairs on the surface of bacterial pili and bacteriophage |
| JP2978435B2 (ja) | 1996-01-24 | 1999-11-15 | チッソ株式会社 | アクリロキシプロピルシランの製造方法 |
| US6258562B1 (en) | 1996-02-09 | 2001-07-10 | Basf Aktiengesellschaft | Human antibodies that bind human TNFα |
| US5714352A (en) | 1996-03-20 | 1998-02-03 | Xenotech Incorporated | Directed switch-mediated DNA recombination |
| US6699658B1 (en) | 1996-05-31 | 2004-03-02 | Board Of Trustees Of The University Of Illinois | Yeast cell surface display of proteins and uses thereof |
| RU2233878C2 (ru) | 1997-01-21 | 2004-08-10 | Дзе Дженерал Хоспитал Корпорейшн | Способ отбора желательного белка и нуклеиновой кислоты, средства для его осуществления |
| PT1071700E (pt) | 1998-04-20 | 2010-04-23 | Glycart Biotechnology Ag | Modificação por glicosilação de anticorpos para melhorar a citotoxicidade celular dependente de anticorpos |
| CA2356215C (en) | 1998-12-23 | 2015-11-24 | Pfizer Inc. | Human monoclonal antibodies to ctla-4 |
| DK2168984T3 (da) | 1999-03-25 | 2012-12-10 | Abbott Gmbh & Co Kg | Humane antistoffer, som binder humant IL-12, og fremgangsmåder til pro-duktion heraf |
| ES2601882T5 (es) | 1999-04-09 | 2021-06-07 | Kyowa Kirin Co Ltd | Procedimiento para controlar la actividad de una molécula inmunofuncional |
| US7449308B2 (en) | 2000-06-28 | 2008-11-11 | Glycofi, Inc. | Combinatorial DNA library for producing modified N-glycans in lower eukaryotes |
| JP2004501642A (ja) | 2000-06-28 | 2004-01-22 | グライコフィ, インコーポレイテッド | 改変された糖タンパク質を生成するための方法 |
| US20040192898A1 (en) | 2001-08-17 | 2004-09-30 | Jia Audrey Yunhua | Anti-abeta antibodies |
| DE60232672D1 (de) | 2001-10-01 | 2009-07-30 | Dyax Corp | Mehrkettige eukaryontische display-vektoren und deren verwendungen |
| HUP0600342A3 (en) | 2001-10-25 | 2011-03-28 | Genentech Inc | Glycoprotein compositions |
| WO2005042560A2 (en) * | 2003-10-24 | 2005-05-12 | Wake Forest University Health Sciences | Non-viral delivery of compounds to mitochondria |
| AU2005233387B2 (en) | 2004-04-15 | 2011-05-26 | Glycofi, Inc. | Production of galactosylated glycoproteins in lower eukaryotes |
| WO2005108568A1 (en) | 2004-05-10 | 2005-11-17 | Basf Plant Science Gmbh | Methods for assembling multiple expression constructs |
| JP2009508470A (ja) | 2005-07-21 | 2009-03-05 | アボット・ラボラトリーズ | Sorf構築物並びにポリタンパク質、プロタンパク質及びタンパク質分解による方法を含む複数の遺伝子発現 |
| JP5470817B2 (ja) | 2008-03-10 | 2014-04-16 | 日産自動車株式会社 | 電池用電極およびこれを用いた電池、並びにその製造方法 |
| PT2581387E (pt) * | 2011-10-11 | 2015-12-30 | Univ Aix Marseille | Um anticorpo monoclonal tat anti hiv-1 |
| JP6136279B2 (ja) | 2013-01-15 | 2017-05-31 | 株式会社ジェイテクト | 転がり軸受装置 |
| TWI503850B (zh) | 2013-03-22 | 2015-10-11 | Polytronics Technology Corp | 過電流保護元件 |
| TWI510996B (zh) | 2013-10-03 | 2015-12-01 | Acer Inc | 控制觸控面板的方法以及使用該方法的可攜式電腦 |
| US9816280B1 (en) | 2016-11-02 | 2017-11-14 | Matthew Reitnauer | Portable floor |
-
2021
- 2021-02-05 CN CN202180025971.XA patent/CN115397848A/zh active Pending
- 2021-02-05 KR KR1020227030361A patent/KR20220137698A/ko active Pending
- 2021-02-05 IL IL295387A patent/IL295387A/en unknown
- 2021-02-05 WO PCT/US2021/016959 patent/WO2021159024A1/en not_active Ceased
- 2021-02-05 AU AU2021215936A patent/AU2021215936A1/en active Pending
- 2021-02-05 US US17/796,561 patent/US20230061973A1/en active Pending
- 2021-02-05 EP EP21709825.0A patent/EP4100435A1/en active Pending
- 2021-02-05 CA CA3167027A patent/CA3167027A1/en active Pending
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20100028359A1 (en) * | 2008-05-09 | 2010-02-04 | Abbott Gmbh & Co. Kg | Antibodies to receptor of advanced glycation end products (rage) and uses thereof |
| CN106661112A (zh) * | 2014-07-16 | 2017-05-10 | Ucb生物制药私人有限公司 | 具有针对cd45和cd79的特异性的分子 |
Non-Patent Citations (1)
| Title |
|---|
| 张华群等: "人类免疫缺陷病毒1型Tat蛋白N末端缺失突变体融合蛋白的表达及其免疫原性分析", 病毒学报, vol. 27, no. 06, 15 November 2011 (2011-11-15), pages 580 - 586 * |
Also Published As
| Publication number | Publication date |
|---|---|
| IL295387A (en) | 2022-10-01 |
| KR20220137698A (ko) | 2022-10-12 |
| WO2021159024A8 (en) | 2021-10-21 |
| WO2021159024A1 (en) | 2021-08-12 |
| US20230061973A1 (en) | 2023-03-02 |
| CA3167027A1 (en) | 2021-08-12 |
| EP4100435A1 (en) | 2022-12-14 |
| AU2021215936A1 (en) | 2022-08-25 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| TWI896628B (zh) | 針對嚴重急性呼吸症候群冠狀病毒2(SARS-CoV-2)之人單株抗體 | |
| CN102421795B (zh) | 针对肌钙蛋白i的抗体及其使用方法 | |
| US20210230269A1 (en) | Immune-stimulating monoclonal antibodies against human interleukin-2 | |
| CN113321731B (zh) | 结合人程序性死亡配体1(pd-l1)的抗体 | |
| CN104744591B (zh) | β淀粉样蛋白结合蛋白 | |
| CN104603149B (zh) | 与预防和治疗狂犬病感染相关的组合物和方法 | |
| JP2016020334A (ja) | デングウイルス中和抗体およびその使用 | |
| JP2025506172A (ja) | コロナウイルスを広く標的とするヒトモノクローナル抗体 | |
| US20240368257A1 (en) | Filamin a binding proteins and uses thereof | |
| KR20240008997A (ko) | 사스-코로나 바이러스 2 중화 항체 | |
| US12168699B2 (en) | Anti-polymeric IgA antibodies and methods of use | |
| WO2021238854A1 (zh) | 抗SARS-CoV-2刺突蛋白的单克隆抗体及其制备方法和用途 | |
| US20200024335A1 (en) | Filamin b binding proteins and uses thereof | |
| US20230061973A1 (en) | Tat peptide binding proteins and uses thereof | |
| US11780917B2 (en) | Anti-GM2AP antibody and applications thereof | |
| WO2024054822A1 (en) | Engineered sars-cov-2 antibodies with increased neutralization breadth | |
| WO2024231440A1 (en) | Bispecific anti-pseudomonas antibodies with modified fc regions and methods of use thereof | |
| EA049454B1 (ru) | ЧЕЛОВЕЧЕСКИЕ МОНОКЛОНАЛЬНЫЕ АНТИТЕЛА К КОРОНАВИРУСУ ТЯЖЕЛОГО ОСТРОГО РЕСПИРАТОРНОГО СИНДРОМА 2 (SARS-CoV-2) | |
| CN116670165A (zh) | SARS-CoV-2受体结合结构域的特异性抗体及治疗方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination |