CN102802620A - 使用某种α-7烟酸受体与乙酰胆碱酯酶抑制剂结合治疗认知障碍 - Google Patents
使用某种α-7烟酸受体与乙酰胆碱酯酶抑制剂结合治疗认知障碍 Download PDFInfo
- Publication number
- CN102802620A CN102802620A CN2010800312022A CN201080031202A CN102802620A CN 102802620 A CN102802620 A CN 102802620A CN 2010800312022 A CN2010800312022 A CN 2010800312022A CN 201080031202 A CN201080031202 A CN 201080031202A CN 102802620 A CN102802620 A CN 102802620A
- Authority
- CN
- China
- Prior art keywords
- donepezil
- thiophene
- chloro
- quinuclidin
- benzo
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/445—Non condensed piperidines, e.g. piperocaine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/21—Esters, e.g. nitroglycerine, selenocyanates
- A61K31/27—Esters, e.g. nitroglycerine, selenocyanates of carbamic or thiocarbamic acids, meprobamate, carbachol, neostigmine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/439—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom the ring forming part of a bridged ring system, e.g. quinuclidine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/473—Quinolines; Isoquinolines ortho- or peri-condensed with carbocyclic ring systems, e.g. acridines, phenanthridines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/55—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having seven-membered rings, e.g. azelastine, pentylenetetrazole
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
- A61P31/18—Antivirals for RNA viruses for HIV
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biomedical Technology (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Virology (AREA)
- Emergency Medicine (AREA)
- Oncology (AREA)
- Tropical Medicine & Parasitology (AREA)
- Molecular Biology (AREA)
- Hospice & Palliative Care (AREA)
- Psychiatry (AREA)
- AIDS & HIV (AREA)
- Communicable Diseases (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
本文描述了用于改善认知的方法以及相关的组合物,所述的方法包括向患者给药(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺或其药学上可接受的盐、以及乙酰胆碱酯酶抑制剂。
Description
背景技术
烟碱乙酰胆碱受体(nAChR)形成了受乙酰胆碱活化的离子通道家族。功能受体包含5个亚单元,并且具有众多的受体亚型。研究显示中枢烟碱乙酰胆碱受体与学习和记忆有关。α-7亚型的烟碱乙酰胆碱受体普遍存在于海马和脑皮层中。
WO 03/055878描述了多种据信可用于改善认知的α-7nAChR的激动剂。WO 03/055878表明,α-7nAChR的某些激动剂可用于改善感知能力、专注力、学习或记忆,特别是在认知损伤之后更是如此,其中所述的认知损伤类似于在(例如)诸如轻微的认知损伤、老年相关的学习和记忆损伤、老年相关的记忆丧失、阿尔茨海默氏疾病(AD)、精神分裂症以及某些其他的认知障碍之类的一些情况/疾病/综合征下发生的那些。(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺为所描述的化合物。
一些人将在阿尔茨海默氏患者中观察到的认知和功能的下降归因于中枢神经系统中胆碱的缺乏。已经用于治疗AD的至少4种药品(他克林、多奈哌齐(盐酸多奈哌齐;1-苯基-4-[(5,6-二甲氧基-1-茚酮)-2-基]甲基哌啶盐酸盐)、利凡斯的明((S)-N-乙基-N-甲基-3-[1-(二甲基氨基)乙基]-苯基氨基甲酸盐)以及加兰他敏(加兰他敏氢溴酸盐;(4aS,6R,8aS)-4a,5,9,10,11,12-六氢-3-甲氧基-11-甲基-6H-苯并氟代[3a,3,2-ef][2]苯骈吖庚因-6-醇氢溴酸盐))显示出会增加CNS中的乙酰胆碱的乙酰胆碱酯酶抑制剂的作用。
发明概述
令人惊奇的是,已经发现(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺能够改善正接受乙酰胆碱酯酶抑制剂(例如多奈哌齐或利凡斯的明)治疗的阿尔茨海默氏患者的认知。所述的方法能够改善已经受益于源于给药乙酰胆碱酯酶抑制剂而使得一个或多个认知方面得到增强的患者的认知。因此,在一个或多个认知方面已经受益于乙酰胆碱酯酶抑制剂的患者能够在一个或多个认知方面由于给药(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺及其药学上可接受的盐而进一步获益。
令人惊奇的是,此外还发现当给药亚临床剂量(subclinical dose)(即,不会改善记忆的剂量)的(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺、并结合同样给药亚临床剂量的乙酰胆碱酯酶抑制剂时,可以改善记忆。因此,患者可以受益(例如改善记忆或认知)于药品的组合,其中各种药品都以极低的、降低副作用或避免副作用的剂量给药。此外,药品的组合可以为大范围的患者和/或经过长期的治疗提供益处。例如,当某些乙酰胆碱酯酶抑制剂在几个月的治疗之后表现出效力降低时,所述的组合可以提供更长期的效力。
患者可以在以下一个或多个方面受益:处理的速度、注意力/警觉、工作记忆、视觉学习、语言学习、视觉学习、推理/解决问题、执行功能以及社会认知。重要的是,(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺及其药学上可接受的盐可以在此类经治疗的患者中以极低的剂量使用来改善认知,例如每日口服剂量为(或者不高于):3mg,2.70mg,2.50mg,2.25mg,2mg,1.75mg,1.50mg,1.25mg,1mg,0.7,0.5,0.3mg或者甚至0.1mg。因此,例如可以给药0.05-1.5mg的每日剂量、优选为1mg/日或者0.3mg/日给药。在缺乏给药用于改善认知的其他试剂时给药亚临床剂量的情况下,可以使用每日口服剂量低于0.5mg、0.3mg、0.1mg、0.05mg、0.03mg或0.01mg的(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺及其药学上可接受的盐。在缺乏给药用于改善认知的其他试剂时使用亚临床的水平时,可以使用低于0.5nM,0.4,0.3,0.2或0.1nM的(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺及其药学上可接受的盐。
对于多奈哌齐而言,使用(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺或其药学上可接受的盐的每日剂量可以为10mg,5mg,4.5mg,4mg,3.5mg,3mg,2.5mg,2mg,1mg或0.5mg。所述的每日剂量可以为5至0.5mg(例如4.5-1.0mg/日,4.5-2.0mg/日,4.0-2.0或者2.5mg/日)。对于利凡斯的明而言,结合使用的每日剂量可以为11,10,9,8,7,6或5mg。对于加兰他敏而言,结合使用的每日剂量可以为20,15,13,12,11,10,9,8,7,6或5mg。对于乙酰胆碱酯酶抑制剂而言,应该理解的是为了有效地改善记忆或认知,必须在取得血红细胞的乙酰胆碱酯酶抑制率为至少65%的条件下给药。在本文所述的方法中,可以以仅取得55%的较低剂量(50,45,40,35或30%抑制率)下给药乙酰胆碱酯酶抑制剂。
本文描述了改善认知的方法,包括向患者给药(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺或其药学上可接受的盐、以及乙酰胆碱酯酶抑制剂。在多种情况下:患者被诊断为阿尔茨海默氏疾病或前阿尔茨海默氏疾病(pre-Alzheimer’s disease);患者被诊断为轻微至中度的阿尔茨海默氏疾病;患者被诊断为中度至严重的阿尔茨海默氏疾病;乙酰胆碱酯酶抑制剂选自他克林,多奈哌齐,利凡斯的明和加兰他敏;乙酰胆碱酯酶抑制剂选自多奈哌齐,利凡斯的明和加兰他敏;乙酰胆碱酯酶抑制剂选自多奈哌齐和利凡斯的明;然后给药(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺或其药学上可接受的盐之前,对患者给药一段时期的乙酰胆碱酯酶抑制剂;之前的给药为至少1个月,之前的给药为至少3个月,之前的给药为至少6个月。在某些情况下:所述的方法的改善以下一个或多个方面:学习、延迟的记忆、注意力、工作记忆、视觉学习、处理的速度、警觉、语言学习、视觉动作功能、社会认知、长期记忆或者执行功能。
此外,本文还描述了改善认知的方法,包括向患者给药亚临床剂量(当在缺乏乙酰胆碱酯酶抑制剂的情况下进行给药时不会改善记忆的剂量)的(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺或其药学上可接受的盐、以及亚临床剂量(当在缺乏(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺或其药学上可接受的盐进行给药时不会改善记忆的剂量)的乙酰胆碱酯酶抑制剂。在多种情况下:口服给药1.0mg/日、0.5mg/日、0.3mg/日或0.1mg/日的(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺或其药学上可接受的盐。在多种情况下:乙酰胆碱酯酶抑制剂为多奈哌齐,并且以5mg/日、4.5mg/日、4.0mg/日、2.5mg/日、1.5mg/日或更少、1.0mg/日剂量口服给药;并且以取得10-65%稳定状态的血红细胞乙酰胆碱酯酶抑制率的剂量给药乙酰胆碱酯酶抑制剂。
此外,本文还描述了药物组合物,包含(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺或其药学上可接受的盐、以及乙酰胆碱酯酶抑制剂。在多种情况下:乙酰胆碱酯酶抑制剂选自他克林,多奈哌齐,利凡斯的明和加兰他敏;乙酰胆碱酯酶抑制剂选自多奈哌齐,利凡斯的明和加兰他敏;乙酰胆碱酯酶抑制剂选自多奈哌齐和利凡斯的明;以及乙酰胆碱酯酶抑制剂为多奈哌齐。
此外,本文还描述了每日单位剂量的药物组合物,包含不多于1.0mg的(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺或其药学上可接受的盐、乙酰胆碱酯酶抑制剂、以及药学上可接受的载体。在多种情况下,每日单位剂量的药物组合物包含不多于0.5(0.3或0.1)mg的(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺或其药学上可接受的盐。在多种情况下,每日单位剂量的药物组合物包含不多于5,4,3,2,1或0.5mg的多奈哌齐。
此外,本文还描述了经包装的药物,包含装有第一单位剂量的药物组合物、以及第二单位剂量的药物组合物的包装,所述的第一单位剂量的药物组合物包含(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺或其药学上可接受的盐,所述的第二单位剂量的药物组合物包含乙酰胆碱酯酶抑制剂。
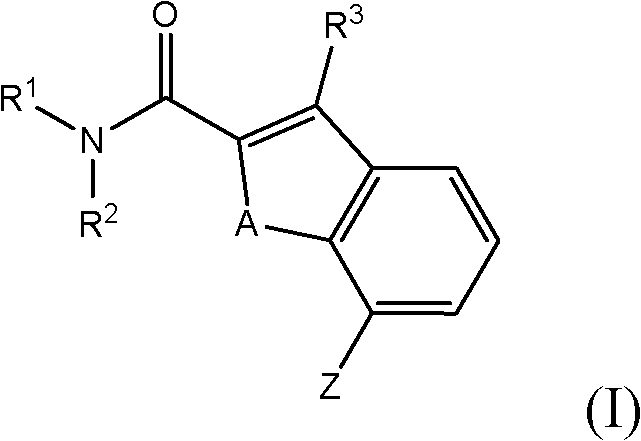
在另一个方面中,可以使用式I所示的乙酰胆碱酯酶抑制剂、或其盐或其溶剂化物或其盐的溶剂化物与乙酰胆碱酯酶抑制剂的组合来治疗患者:
其中
R1表示-1-氮杂双环[2.2.2]辛-3-基;
R2表示氢或C1-C6-烷基;
R3表示氢、卤素或C1-C6-烷基;
A表示氧或硫;以及
Z表示卤素,甲酰基,氨基甲酰基,氰基,三氟甲基,三氟甲氧基,硝基,氨基,甲酰胺基,乙酰胺基,C1-C6-烷基,C1-C6-烷氧基,C1-C6-烷基硫代,C1-C6-烷基氨基,杂芳基-羰基氨基,芳基羰基氨基,C1-C4-烷基磺酰基氨基,二(芳基磺酰基)氨基,C3-C6-环烷基羰基甲基或氨基(羟基亚氨基)甲基。
在另一个方面中,使用式I所示的化合物治疗患者,其中R2为氢;R3为卤素;A为硫;并且Z表示卤素,甲酰基,氨基甲酰基,氰基,三氟甲基,三氟甲氧基,硝基,氨基,甲酰胺基,乙酰胺基,C1-C6-烷基,C1-C6-烷氧基,C1-C6-烷基硫代,C1-C6-烷基氨基,杂芳基-羰基氨基,芳基羰基氨基,C1-C4-烷基磺酰基氨基,二(芳基磺酰基)氨基,C3-C6-环烷基羰基甲基或氨基(羟基亚氨基)甲基(具体为卤素,氰基,三氟甲基,三氟甲氧基,甲基,乙基,甲氧基以及乙氧基;更具体为卤素或氰基;甚至更具体为氯或氰基)。
本文描述了通过给药药物组合物来治疗患者的方法,其中所述的药物组合物包含(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺或其药学上可接受的盐(例如每日剂量为3mg,2.70mg,2.50mg,2.25mg,2mg,1.75mg,1.50mg,1.25mg,1mg,0.7mg,0.5mg,0.3mg,0.1mg,0.03mg或0.01mg)、以及联合一种或多种乙酰胆碱酯酶抑制剂。所述的治疗可以改善认知的一个或多个方面(例如视觉动作技巧、学习、延迟的记忆、注意力、工作记忆、视觉学习、处理的速度、警觉、语言学习、视觉动作功能、社会认知、长期记忆、实行功能等)。可以使用乙酰胆碱酯酶抑制剂在一段时期治疗患者,然后给药(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺。例如,可以使用乙酰胆碱酯酶抑制剂对患者治疗至少1周、至少1个月、至少2个月、至少3个月、至少4个月、至少6个月或者至少1年。所述的两种试剂可以在同一组合物中或者在两种不同的组合物中同时给药。此外,所述的试剂可以不同时给药。
此外,本文描述了包含(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺或其药学上可接受的盐、乙酰胆碱酯酶抑制剂(例如他克林,多奈哌齐,利凡斯的明或加兰他敏)以及药学上可接受的载体的药物组合物。
“剂量”为给予患者的活性药物组分(API)的量。例如,1mg是指每日口服给予各患者1mg的API。
“活性药物组分”包括盐酸(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺、(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺、盐酸(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺一水合物以及盐酸(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺溶剂化物、以及式I所示的化合物。
在此,溶剂化物表示溶剂与盐酸(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺或(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺的化学当量比为0.1至10个分子。溶剂分子包括但不限于水、甲醇、1,4-二噁烷、乙醇、异丙醇或丙酮。在一些情况下,水为优选的溶剂化合物。
附图简述
图1描述了(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺(口服)与多奈哌齐(口服)的组合在患者认知测试中的作用。
图2描述了在5月龄的雄性Wistar大鼠经东莨菪碱处理(静脉内注射)后,在目标物体识别任务中,(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺(口服)与多奈哌齐(口服)对分辨指数(d2)的影响(平均值+SEM)。当与媒介物/东莨菪碱条件下相比,EVP-6124与多奈哌齐的组合会逆转东莨菪碱诱导的记忆性能缺陷。与东莨菪碱条件下的差异以星号表示(Bonferroni t检验,*:P<0.05)。与0的差异以#表示(单样本t检验,###:P<0.001)。
发明详述
向AD患者给药(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺以及多奈哌齐
或利凡斯的明
在48位60-80岁轻微至中度AD患者的阶段1b研究中,在稳定的多奈哌齐(5或10mg/日)或利凡斯的明(给予6-12mg/日,其为两倍的日剂量,即,每剂量为3或6mg)上评估盐酸(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺的安全性和效力。
对患者给药安慰剂或者两种不同剂量的(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺(0.3或1.0mg/d)28天。通过不良事件、ECG以及临床实验室测量来评价安全性。通过CogState计算机化的认知测试以及NTB级别的亚组(语言流畅性,试验A和B)来测量认知效果。该分析的结果示于图1中。
(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺显示是安全的,并且耐受良好,而且不具有更通常在经处理及安慰剂患者中所报告的重大的不良事件;未报告有SAE。除了暴露于多奈哌齐或利凡斯的明以外还暴露于(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺的受试对象主要在非语言性的学习、记忆以及执行功能领域中显示出认知功能增强。
亚临床剂量的(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺以及多奈哌齐
会改善记忆
下文所述的研究检验了在5月龄雄性Wistar大鼠的目标物体认知任务中,亚阈值剂量的α7烟酸受体拮抗剂(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺以及AChE抑制剂多奈哌齐对由蕈毒碱拮抗剂东莨菪碱诱导的短期记忆缺陷的作用。目标物体认知任务允许评估(目标物体)信息在记忆中的强化(Ennaceur and Delacour,1988;Prickaerts et al.,1997)。在所述的任务重,对大鼠进行两种试验。在第一种试验中,将大鼠放入其中放置有两个相同的目标物体的场地中。通常,大鼠将视察两个目标物体达某一段时间。在延迟某一段时间后,对大鼠进行第二种试验。在该试验中,将大鼠再次放置在相同的场地中,但是其中的一个目标物体已经被新的目标物体所替代。与第一种试验相似,大鼠再次仔细查看两个目标物体。记录查看各目标物体的时间长短,以便确定大鼠是否花费了不同的查看两个目标物体的时间长短。可以基于这种评分,确定记忆性能。
多个研究显示,当在第一种试验和第二种之言之间间断1小时延迟时,Wistar大鼠显示出良好的目标物体记忆性能。但是,当使用24小时的延迟时,所述的大鼠在第二种试验中不能分辨新的与熟悉的目标物体,表明所述的大鼠不能记忆熟悉的目标物体(即,在第一种试验以及第二种试验中均呈现的目标物体)。使用6小时的延迟,分辨性能介于1小时延迟和24小时延迟的性能之间,表明在此类任务中遗忘是延迟时间依赖性的。
之前的研究发现,0.3mg/kg的(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺(口服)会完全减轻由蕈毒碱拮抗剂东莨菪碱(0.1mg/kg,静脉内注射)诱导的目标物体记忆缺陷,而0.03mg/kg的剂量则无效果。此外,还发现0.3mg/kg剂量的多奈哌齐(口服)会减轻东莨菪碱诱导的目标物体记忆缺陷,而0.1mg/kg的多奈哌齐则无效果。在初步的研究中,令人惊奇地发现结合给药亚阈值剂量的多奈哌齐和亚阈值剂量的(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺(当单独给予亚阈值剂量的这两种化合物时,它们对所述的性能都不具有效果),在患有由东莨菪碱诱导的目标物体记忆缺陷大鼠中会增强记忆性能。这表明所述的两种化合物对认知损伤具有额外的协同效果。
在本研究中,在学习试验之前的30分钟,大鼠接受注射蕈毒碱受体拮抗剂东莨菪碱(0.1mg/kg,静脉内注射给药)。在使用东莨菪碱处理之后,在学习试验之后的1小时,大鼠未显示出对目标物体的记忆。研究亚阈值剂量的(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺(0.03mg/kg,口服给药)与多奈哌齐(0.1mg/kg口服给药)的组合是否能够减轻东莨菪碱诱导的目标物体记忆缺陷。所有的药品都在第一种试验之前的30分钟给予。
对于动物试验,所有的试验程序都经Maastricht大学的地区伦理委员会批准,并且满足政府的指导方针。使用24只5月龄的雄性Wistar大鼠(Harlan,The Netherlands)(平均体重:465g)。所有这些24只动物中,仅有23只动物包含在最终的分析中,这是由于1只大鼠不停的逃出。将动物分别圈养在空调房间(大约20℃)中标准的3型Makrolon笼的锯末垫子上。将它们保持在12/12小时光/暗循环(从19.00至7.00h光照)下,并且自由获得食物和水。将大鼠圈养在相同的房间中,并在这种条件下对动物进行测试。播放轻柔的广播在房间中提供背景噪声。所有的测试都在9.00至最多18.00h之间实施。
根据东莨菪碱的早期剂量应答研究,确定0.1mg/kg的剂量为最有效的诱导记忆缺陷的剂量。每日制备东莨菪碱氢溴酸盐,并将其溶解于盐水中。静脉内给药东莨菪碱(注射体积为1mg/kg),30分钟之后进行试验1。将EVP-6124溶解于H2O中。每日制备所述的溶液,并在口服剂量为0.03mg/kg下进行测试(注射体积为2ml/kg)。给药总是在东莨菪碱即刻之后、在试验1之前的30分钟。将多奈哌齐溶解于盐水中。每日制备所述的溶液,并在口服剂量为0.1mg/kg下进行测试(注射体积为2ml/kg)。给药总是在(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺即刻之后、在试验1之前的30分钟。
首先测试媒介物和东莨菪碱条件。随后测试多奈哌齐、(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺以及这二者的组合(n=8/条件/测试天)。所有的大鼠都是用各剂量条件处理一次。但是1只大鼠由所述的研究中排除,这是因为连续地跳出所述的装置,因此n=23。试验者不清楚测试的条件/药品。
按照其他处所述进行目标物体认知测试(Ennaceur and Delacour,1988)。所述的装置由直径为83cm的环状场地构成。40cm高的墙壁的一半由灰色的聚氯乙烯制成,而另一半由透明的聚氯乙烯制成。在所述装置的不同部分中,光强度相等。将两个目标物体放置在距离灰色墙壁大约10cm远的对称位置处。各目标物体用于三个平行重复中。所述的目标物体为:1)由灰色聚氯乙烯基底构成的圆锥体(最大直径为18cm),并在顶部为由黄铜制成的一圈(总高度为16cm);2)标准的1L棕色透明玻璃瓶(直径为10cm,高度为22cm),其中添满水;3)具有2个孔(直径为1.9cm)的大块金属立方体(10.0x5.0x7.5cm);以及4)具有锥形顶(13.0x8.0x8.0cm)的大块铝质立方体。大鼠不能替代所述的目标物体。荧光红色灯管以及灯泡对所述装置的地板提供大约20lux的持续照射。
测试期间包含两种试验。各试验持续3分钟。在第一种试验(T1)过程中,所述的装置包含2个相同的目标物体(样品)。将大鼠总是在前方(透明)部分的中间处面对墙壁放置在所述的装置中。在第一查看时间之后,将大鼠放回它的饲养笼中。随后,在间隔预订的延迟时间之后,将大鼠放回至所述的装置中以用于第二种试验(T2),但是现在具有2个不同的目标物体,相同的一个目标物体(样品)以及新的目标物体。使用个人计算机人工记录在T1和T2过程中查看各目标物体所花费的时间。
仔细查看定义如下:鼻子直接指向目标物体,距离不到2cm和/或使用鼻子接触目标物体。坐在目标物体上不被认为是查看行为。为了避免嗅觉跟踪的存在,总是将目标物体彻底清洁。目标物体的所有组合以及位置都以平衡方式使用,以减少由于偏爱特定的位置或目标物体而产生的潜在的偏袒。
多个研究显示,当第一种试验和第二种试验之间间断1小时的延迟时间时,Wistar大鼠显示出良好的目标物体记忆性能。但是,当使用24小时的延迟时间时,所述的大鼠在第二种试验中不能分辨新的和熟悉的目标物体,表明大鼠不能记忆在第一种试验中呈现的目标物体。使用6小时的延迟时间,分辨性能介于1小时延迟时间与24小时延迟时间之间,表明在此类任务中遗忘是延迟时间依赖性的。在本研究中,使用1h的间隔时间。
在2周中,每天都对动物进行处理,并使它们在2天内适应所述的程序,即,每天2次使它们仔细查看所述的装置(不具有任何目标物体),每次3分钟。然后,使大鼠适于测试,并在第一种试验之前30分钟通过盐水注射进行静脉内及口服注射(分别为1.0ml/kg和2.0ml/kg),直到它们显示出稳定的分辨性能,即,在间隔1h时具有良好的分辨性能,而在间隔24h时不能分辨。接着,为对照期间(测试媒介物和东莨菪碱)。随后,开始测试药品(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺(0.03mg/kg)和多奈哌齐(0.1mg/kg)。总是在周一、周三和周五(或者周二和周四)测试化合物/媒介物,以便在化合物期间之间具有充分的冲洗时间。
基本的测量为大鼠在T1和T2过程中查看目标物体所花费的时间。在查看2个相同的样品中所花费的时间由‘a1’和‘a2’表示。在T2中在查看样品和新目标物体中所花费的时间分别由‘a’和‘b’表示。计算以下变量:e1=a1+a2,e2=a+b,和d2=(b-a)/e2(参见表1)。e1和e2分别为在T1和T2过程中2个目标物体的总查看时间的量度。D2为分辨的相对量度,其被校正为查看活动性(e2)。因此,在采用相似的处理、相似的间隔的试验之间,d2指数应该不具有差异。在该试验中具有5个条件,并且各大鼠都经历了各条件:
1)媒介物(东莨菪碱),媒介物(多奈哌齐)&媒介物((R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺)
2)东莨菪碱,媒介物(多奈哌齐)&媒介物((R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺)
3)东莨菪碱,多奈哌齐&媒介物((R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺)
4)东莨菪碱,媒介物(多奈哌齐)&(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺
5)东莨菪碱,多奈哌齐&(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺
进行单样本t统计以便根据每种处理条件评估d2是否不等于0。但是,d2值与0值的比较不具有差异可能并非是用于分析认知的最合适的方法(增加了制造I类错误的机会)。由此,还通过对象内(重复测量)ANOVA来评估效果。在各条件之间具有显著差异的情况下,进行Bonferroni校正的事后分析(post hoc analyse)。
表1.与目标物体识别测试有关的测量
e1为在第一种试验中查看2个相同目标物体(a1和a2)所花费的时间的量度,而e2为第二种试验中查看相似的(a)和新的目标物体(b)所花费的时间的量度;d2相当于在第二种试验过程中分辨原来的目标物体与新的目标物体的能力,并针对所述的试验过程中的查看时间进行校正。
在T1之前30分钟进行EVP-6124和多奈哌齐处理的结果总结于表2中。在T1的探究水平的处理条件之间未发现查看水平具有差异(e1:F(4,88)=1.138,n.s)。在T2中,在T2的探究水平的处理条件之间也未发现查看水平具有差异(e2:F(4,88)=0.888,n.s.)。
表2.在东莨菪碱处理后的目标物体识别测试的测量中使用药品EVP-6124和多奈哌齐的处理结果
在T1之前30分钟给药东莨菪碱(静脉内注射)、EVP-6124(口服)和多奈哌齐(口服)。在第一种试验和第二种试验之间的延迟时间间隔为1小时。不为0的d2测量值以星号表示(单样本t检验,***:P<0.001)。每个试验条件,n=23。
单样本t检验显示,结合给药的媒介物的条件的d2值不为0(参见表2B)。这与单独给药的东莨菪碱、(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺和多奈哌齐条件相反,它们未显示出差异。(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺和多奈哌齐处理对相对分辨指数d2的影响绘制于图1中。当对各组进行比较时,发现d2指数具有差异(F(4,88)=8.181,P<0.001)。结合的媒介物条件中的d2高于东莨菪碱、(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺和多奈哌齐条件下的d2(Bonferrone t检验;参见图2)。
为了评价在给药东莨菪碱(静脉内给药)之后结合给药的亚阈值剂量的药品(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺(口服给予)和多奈哌齐(口服给予)的认知增强效果,使用1h的延迟间隔时间。发现,在对着媒介物条件中,大鼠在所述的间隔时间后记忆了熟悉的目标物体。这与其中未发现对熟悉的目标物体具有更多的记忆的东莨菪碱(0.1mg/kg)条件相反。在本研究中,用于药品测试的东莨菪碱的剂量对动物的查看活动力不具有影响。
(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺和多奈哌齐都不能改变查看行为。相对分辨指数d2校正为查看活动性的改变(尽管在本研究中未观察到这种改变)。此外,由于对象内分析(即,与0相比)可以稳定地察觉目标物体识别的微小作用,所以为可靠的量度。多奈哌齐条件的d2以及(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺条件的d2均为0。同样,在各分析之间(即,比较单独使用的东莨菪碱处理的动物)显示,亚阈值剂量的EVP-6124(0.03mg/kg)和多奈哌齐(0.1mg/kg)在单独给予时都不会改善动物的记忆。这与结合条件相反,在所述的结合条件中一起给予压阈值剂量的(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺和多奈哌齐会完全逆转由东莨菪碱诱导的目标物体的记忆功能障碍。
参考文献
Boess,F.G.,Hendrix,M.,van der Staay,F.J.,Erb,C.,Schreiber,R.,vanStaveren,W.,de Vente,J.,Prickaerts,J.,Blokland,A.,Koenig,G.,2004.Inhibition of phosphodiesterase 2 increases neuronal cGMP,synaptic plasticityand memory performance.Neuropharmacology 47,1081-1092.
Blokland,A.,Prickaerts,J.,Honig,W.,De Vente,J.,1998.State-dependentimpairment in object recognition after hippocampal NOS inhibition.NeuroReport9,4205-4208.
Ennaceur,A.,Delacour,J.,1988.A new one-trial test for neurobiologicalstudies of memory in rats.1:Behavioral data.Behav.Brain Res.31,47-59.
Ennaceur,A.,Meliani,K.,1992.Effects of physostigmine and scopolamineon rats′performances in object-recognition and radial-maze tests.Psychopharmacology 109,321-330.
Ennaceur,A.,Cavoy,A.,Costa,J.C.,Delacour,J.1989.A new one-trial testfor neurobiological studies of memory in rats.II:Effects of piracetam andpramiracetam.Behav.Brain Res.33,197-207.
De Bruin,N.M.W.J.,Prickaerts,J.,Akkerman,S.,Lange,J.H.M.,Andriambeloson,E.,De Haan,M.,Wijnen,J.,Van Drimmelen,M.,Hissink,E.,Heijnk,L.Kruse,C.G.(In Press)SLV330,a cannabinoid CB1 receptor antagonist,ameliorates deficits in the T-maze,object recognition and social recognition tasksin rodents.Neurobiol.Learn.Mem.
Prickaerts,J.,Steinbusch,H.W.M.,Smits,J.F.M.,De Vente,J.,1997.Possible role of nitric oxide-cyclic GMP pathway in object recognition memory:Effects of 7-nitroindazole and zaprinast.Eur.J.Pharmacol.337,125-136.
Prickaerts,J.,Sik,A.,van Staveren,W.C.,Koopmans,G.,Steinbusch,H.W.,van der Staay,F.J.,de Vente,J.,Blokland,A.,2004.Phosphodiesterase type 5inhibition improves early memory consolidation of object information.Neurochem Int.45,915-928.
Prickaerts,J.,Sik,A.,van der Staay,F.J.,de Vente,J.,Blokland,A.,2005.Dissociable effects of acetylcholinesterase inhibitors and phosphodiesterase type5 inhibitors on object recognition memory:acquisition versus consolidation.Psychopharmacology 177,381-390.
Claims (38)
1.一种用于改善认知的方法,该方法包括向患者给药(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺或其药学上可接受的盐、以及乙酰胆碱酯酶抑制剂。
2.权利要求1所述的方法,其中所述的患者被诊断为患有阿尔茨海默氏疾病或前阿尔茨海默氏疾病。
3.权利要求1所述的方法,其中所述的患者被诊断为患有轻微至中度的阿尔茨海默氏疾病。
4.权利要求1所述的方法,其中所述的患者被诊断为患有中度至严重的阿尔茨海默氏疾病。
5.上述权利要求中的任意一项所述的方法,其中所述的乙酰胆碱酯酶抑制剂选自他克林、多奈哌齐、利凡斯的明和加兰他敏。
6.权利要求5所述的方法,其中所述的乙酰胆碱酯酶抑制剂选自多奈哌齐、利凡斯的明和加兰他敏。
7.权利要求5所述的方法,其中所述的乙酰胆碱酯酶抑制剂选自多奈哌齐和利凡斯的明。
8.上述权利要求中的任意一项所述的方法,其中在给药(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺或其药学上可接受的盐之前,在一段时间内向所述的患者给药乙酰胆碱酯酶抑制剂。
9.权利要求8所述的方法,其中所述的前期给药为至少1个月。
10.权利要求9所述的方法,其中所述的前期给药为至少3个月。
11.权利要求10所述的方法,其中所述的前期给药为至少6个月。
12.上述权利要求中的任意一项所述的方法,其中所述的方法改善以下一个或多个方面:学习、延迟的记忆、注意力、工作记忆、视觉学习、处理的速度、警觉、语言学习、视觉动作功能、社会认知、长期记忆或者执行功能。
13.权利要求1所述的方法,其中所述的(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺或其药学上可接受的盐、以及所述的乙酰胆碱酯酶抑制剂中的一者或二者以亚临床剂量给药。
14.权利要求13所述的方法,其中口服给予少于1.0mg/日的(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺或其药学上可接受的盐。
15.权利要求13所述的方法,其中口服给予少于0.5mg/日的(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺或其药学上可接受的盐。
16.权利要求13所述的方法,其中口服给予少于0.3mg/日的(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺或其药学上可接受的盐。
17.权利要求13所述的方法,其中口服给予少于0.1mg/日的(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺或其药学上可接受的盐。
18.权利要求13所述的方法,其中所述的乙酰胆碱酯酶抑制剂为多奈哌齐,并且口服给予少于5mg/日。
19.权利要求13所述的方法,其中所述的乙酰胆碱酯酶抑制剂为多奈哌齐,并且口服给予4.5mg/日或更少。
20.权利要求13所述的方法,其中所述的乙酰胆碱酯酶抑制剂为多奈哌齐,并且口服给予4.0mg/日或更少。
21.权利要求13所述的方法,其中所述的乙酰胆碱酯酶抑制剂为多奈哌齐,并且口服给予2.5mg/日或更少。
22.权利要求13所述的方法,其中所述的乙酰胆碱酯酶抑制剂为多奈哌齐,并且口服给予1.5mg/日或更少。
23.权利要求13所述的方法,其中所述的乙酰胆碱酯酶抑制剂为多奈哌齐,并且口服给予1.0mg/日或更少。
24.权利要求1所述的方法,其中所述的乙酰胆碱酯酶抑制剂以取得10-65%稳定状态的血红细胞乙酰胆碱酯酶抑制率的剂量给药。
25.一种药物组合物,包含:(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺或其药学上可接受的盐、以及乙酰胆碱酯酶抑制剂。
26.权利要求25所述的药物组合物,其中所述的乙酰胆碱酯酶抑制剂选自他克林、多奈哌齐、利凡斯的明和加兰他敏。
27.权利要求25所述的药物组合物,其中所述的乙酰胆碱酯酶抑制剂选自多奈哌齐、利凡斯的明和加兰他敏。
28.权利要求25所述的药物组合物,其中所述的乙酰胆碱酯酶抑制剂选自多奈哌齐和利凡斯的明。
29.权利要求25所述的药物组合物,其中所述的乙酰胆碱酯酶抑制剂为多奈哌齐。
30.一种每日单位剂量的药物组合物,包含:不多于1.0mg的(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺或其药学上可接受的盐、乙酰胆碱酯酶抑制剂、以及药学上可接受的载体。
31.权利要求30所述的每日单位剂量的药物组合物,包含:不多于0.5mg的(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺或其药学上可接受的盐。
32.权利要求31所述的每日单位剂量的药物组合物,包含:不多于0.3mg的(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺或其药学上可接受的盐。
33.权利要求31所述的每日单位剂量的药物组合物,包含:不多于0.1mg的(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺或其药学上可接受的盐。
34.权利要求31所述的每日单位剂量的药物组合物,包含不多于5mg的多奈哌齐。
35.权利要求31所述的每日单位剂量的药物组合物,包含不多于4mg的多奈哌齐。
36.权利要求31所述的每日单位剂量的药物组合物,包含不多于2.5mg的多奈哌齐。
37.权利要求31所述的每日单位剂量的药物组合物,包含不多于1mg的多奈哌齐。
38.一种经包装的药物,包含装有第一单位剂量的药物组合物、以及第二单位剂量的药物组合物的包装,所述的第一单位剂量的药物组合物包含(R)-7-氯-N-(奎宁环-3-基)苯并[b]噻吩-2-甲酰胺或其药学上可接受的盐,所述的第二单位剂量的药物组合物包含乙酰胆碱酯酶抑制剂。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US17726009P | 2009-05-11 | 2009-05-11 | |
| US61/177,260 | 2009-05-11 | ||
| PCT/US2010/034353 WO2010132423A1 (en) | 2009-05-11 | 2010-05-11 | Treatment of cognitive disorders with certain alpha-7 nicotinic acid receptors in combination with acetylcholinesterase inhibitors |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN102802620A true CN102802620A (zh) | 2012-11-28 |
Family
ID=42306679
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN2010800312022A Pending CN102802620A (zh) | 2009-05-11 | 2010-05-11 | 使用某种α-7烟酸受体与乙酰胆碱酯酶抑制剂结合治疗认知障碍 |
Country Status (15)
| Country | Link |
|---|---|
| US (2) | US20110124631A1 (zh) |
| EP (1) | EP2429518A1 (zh) |
| JP (1) | JP5808319B2 (zh) |
| CN (1) | CN102802620A (zh) |
| AU (1) | AU2010247835A1 (zh) |
| BR (1) | BRPI1014793A2 (zh) |
| CA (1) | CA2761716A1 (zh) |
| CL (1) | CL2011002847A1 (zh) |
| CO (1) | CO6460746A2 (zh) |
| EC (1) | ECSP11011453A (zh) |
| IL (1) | IL216281A0 (zh) |
| MX (1) | MX2011011972A (zh) |
| PE (1) | PE20120324A1 (zh) |
| RU (1) | RU2011150248A (zh) |
| WO (1) | WO2010132423A1 (zh) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN103333163A (zh) * | 2013-07-09 | 2013-10-02 | 广州中医药大学 | 一种苯并呋喃类衍生物及其制备方法和应用 |
Families Citing this family (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE10164139A1 (de) | 2001-12-27 | 2003-07-10 | Bayer Ag | 2-Heteroarylcarbonsäureamide |
| PE20130218A1 (es) | 2010-05-17 | 2013-03-20 | Envivo Pharmaceuticals Inc | Una forma cristalina de clorhidrato de (r)-7-cloro-n-(quinuclidin-3-il)benzo[b]tiofeno-2-carboxamida monohidratado |
| EP2640378A4 (en) * | 2010-11-18 | 2014-05-21 | Envivo Pharmaceuticals Inc | INFLAMMATION TREATMENT WITH CERTAIN NICOTINIC ACID ALPHA-7 RECEPTOR AGONISTS IN COMBINATION WITH ACETYLCHOLINESTERASE INHIBITORS |
| US20140155429A1 (en) * | 2011-05-09 | 2014-06-05 | Envivo Pharmaceuticals, Inc. | Treatment of Cognitive Disorders with Certain Alpha-7 Nicotinic Acid Receptor Agonists in Combination with Nicotine |
| WO2012177856A2 (en) * | 2011-06-21 | 2012-12-27 | Adispell, Inc. | Cognition modification |
| KR20140027939A (ko) | 2011-06-30 | 2014-03-07 | 도레이 카부시키가이샤 | 지양제 |
| RU2014103474A (ru) * | 2011-07-01 | 2015-08-10 | Энвиво Фармасьютикалз, Инк. | Способы лечения умеренных когнитивных нарушений |
| EP2846796A4 (en) * | 2012-05-08 | 2015-10-21 | Forum Pharmaceuticals Inc | METHODS OF MAINTAINING, PROCESSING OR ENHANCING COGNITIVE FUNCTION |
| JP6796056B2 (ja) | 2014-03-25 | 2020-12-02 | シナプテック・ディヴェロップメント・エルエルシーSynaptec Development Llc | 自閉症の治療 |
| FR3020819B1 (fr) | 2014-05-12 | 2020-02-14 | Arkema France | Procede d'impregnation de fibres naturelles par un polymere en dispersion aqueuse et utilisation desdites fibres dans les materiaux composites. |
| EP3297632A4 (en) * | 2015-05-18 | 2019-01-16 | Synaptec Development LLC | GALANTAMINE ELIMINATION OF AMYLOIDSS |
| EP3632431A4 (en) | 2017-06-02 | 2020-06-03 | FUJIFILM Toyama Chemical Co., Ltd. | AGENTS FOR PREVENTING OR TREATING BRAIN ATROPHY |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2003055878A1 (de) * | 2001-12-27 | 2003-07-10 | Bayer Healthcare Ag | 2-heteroarylcarbonsäureamide |
| CN1726033A (zh) * | 2002-12-11 | 2006-01-25 | 法马西亚和厄普乔恩公司 | 用α7烟碱乙酰胆碱受体激动剂和其它化合物的联合治疗疾病 |
Family Cites Families (80)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4605652A (en) * | 1985-02-04 | 1986-08-12 | A. H. Robins Company, Inc. | Method of enhancing memory or correcting memory deficiency with arylamido (and arylthioamido)-azabicycloalkanes |
| EP0385517B1 (en) * | 1985-03-14 | 1993-04-14 | BEECHAM GROUP plc | Medicaments for the treatment of emesis |
| HU202108B (en) * | 1986-07-30 | 1991-02-28 | Sandoz Ag | Process for producing pharmaceutical compositions containing serotonine antqgonistic derivatives of indol-carboxylic acid or imidazolyl-methyl-carbazol |
| US5198437A (en) * | 1987-12-10 | 1993-03-30 | Duphar International Research B.V. | 1,7-annelated indolecarboxylic acid esters and amides |
| NZ227229A (en) * | 1987-12-10 | 1991-03-26 | Duphar Int Res | Indole derivatives and pharmaceutical compositions |
| IE62662B1 (en) * | 1989-01-06 | 1995-02-22 | Elan Corp Plc | Use of nicotine in the treatment of conditions susceptible to said treatment |
| US5114947A (en) * | 1990-12-27 | 1992-05-19 | Erbamont Inc. | Method for alleviating anxiety using benzobicyclic carboxamides |
| SE9201478D0 (sv) * | 1992-05-11 | 1992-05-11 | Kabi Pharmacia Ab | Heteroaromatic quinuclidinenes, their use and preparation |
| US5977144A (en) * | 1992-08-31 | 1999-11-02 | University Of Florida | Methods of use and compositions for benzylidene- and cinnamylidene-anabaseines |
| SK282366B6 (sk) * | 1994-08-24 | 2002-01-07 | Astra Aktiebolag | Spiro-azabicyklická zlúčenina, farmaceutický prípravok s jej obsahom, spôsob prípravy, medziprodukty tohto spôsobu a jej použitie v medicíne |
| US5656638A (en) * | 1995-04-18 | 1997-08-12 | Geron Corporation | Telomerase inhibitors |
| US5703116A (en) * | 1995-04-18 | 1997-12-30 | Geron Corporation | Telomerase Inhibitors |
| US5863936A (en) * | 1995-04-18 | 1999-01-26 | Geron Corporation | Telomerase inhibitors |
| GB9606736D0 (en) * | 1996-02-19 | 1996-06-05 | Shire International Licensing | Therapeutic method |
| FR2756826B1 (fr) * | 1996-12-05 | 1999-01-08 | Adir | Nouveaux derives tetrahydropyridiniques substitues, leur procede de preparation et les compositions pharmaceutiques qui les contiennent |
| CN1157392C (zh) * | 1997-05-30 | 2004-07-14 | 神经研究公司 | 在尼古丁ach受体上作为胆碱能配体的8-氮杂双环(3,2,1)辛-2-烯以及辛烷衍生物 |
| US7214686B2 (en) * | 1997-06-30 | 2007-05-08 | Targacept, Inc. | Pharmaceutical compositions and methods for effecting dopamine release |
| US6875606B1 (en) * | 1997-10-23 | 2005-04-05 | The United States Of America As Represented By The Department Of Veterans Affairs | Human α-7 nicotinic receptor promoter |
| US6277870B1 (en) * | 1998-05-04 | 2001-08-21 | Astra Ab | Use |
| US6122528A (en) * | 1998-07-27 | 2000-09-19 | Motorola, Inc. | Combination radio carry case and programmer |
| AU6394399A (en) * | 1998-09-18 | 2000-04-10 | Rockefeller University, The | Lynx, a novel family of receptor ligands in the central nervous system, corresponding nucleic acids and proteins and uses thereof |
| US6953855B2 (en) * | 1998-12-11 | 2005-10-11 | Targacept, Inc. | 3-substituted-2(arylalkyl)-1-azabicycloalkanes and methods of use thereof |
| SE9900100D0 (sv) * | 1999-01-15 | 1999-01-15 | Astra Ab | New compounds |
| US5994177A (en) * | 1999-02-05 | 1999-11-30 | Taiwan Semiconductor Manufacturing Company, Ltd. | Dynamic threshold MOSFET using accumulated base BJT level shifter for low voltage sub-quarter micron transistor |
| FR2790474B1 (fr) * | 1999-03-05 | 2001-04-06 | Synthelabo | Derives de pyridopyranoazepines, leur preparation et leur application en therapeutique |
| FR2791678B1 (fr) * | 1999-03-30 | 2001-05-04 | Synthelabo | Derives de 1,4-diazabicyclo [3.2.2] nonane-4-carboxylates et -carboxamides, leur preparation et leur application en therapeutique |
| US6416735B1 (en) * | 1999-11-08 | 2002-07-09 | Research Triangle Institute | Ligands for α-7 nicotinic acetylcholine receptors based on methyllcaconitine |
| FR2804430B1 (fr) * | 2000-01-28 | 2002-03-22 | Sanofi Synthelabo | Derives de 4-heteroaryl-1,4-diazabicyclo[3.2.2] nonane, leur preparation et leur application en therapeutique |
| GB0010955D0 (en) * | 2000-05-05 | 2000-06-28 | Novartis Ag | Organic compounds |
| DE60106022T2 (de) * | 2000-06-06 | 2006-03-09 | Pfizer Products Inc., Groton | Thiophenverbindungen zur verwendung als antikrebsmittel |
| FR2810664B1 (fr) * | 2000-06-27 | 2004-12-24 | Adir | Nouveaux composes cyclopropaniques 1,1 et 1,2-dissubstitues, leur procede de preparation et les compositions pharmaceutiques qui les contiennent |
| US20030092613A1 (en) * | 2000-08-14 | 2003-05-15 | Lee Daniel H. S. | Alpha7 nicotinic receptor peptides as ligands for beta amyloid peptides |
| US6479510B2 (en) * | 2000-08-18 | 2002-11-12 | Pharmacia & Upjohn Company | Quinuclidine-substituted aryl compounds for treatment of disease |
| AU2001284645A1 (en) * | 2000-08-18 | 2002-03-04 | Pharmacia And Upjohn Company | Quinuclidine-substituted aryl compounds for treatment of disease |
| US6492385B2 (en) * | 2000-08-18 | 2002-12-10 | Pharmacia & Upjohn Company | Quinuclidine-substituted heteroaryl moieties for treatment of disease |
| AU2001282875A1 (en) * | 2000-08-21 | 2002-03-04 | Pharmacia And Upjohn Company | Quinuclidine-substituted heteroaryl moieties for treatment of disease |
| DE10044905A1 (de) * | 2000-09-12 | 2002-03-21 | Merck Patent Gmbh | (2-Azabicyclo[2.2.1]hept-7-yl)methanol-Derivate als nikontinische Acetylcholinrezeptor Agonisten |
| US6569865B2 (en) * | 2001-06-01 | 2003-05-27 | Astrazeneca Ab | Spiro 1-azabicyclo[2.2.2]octane-3,2′(3′h)-furo[2,3-b]pyridine |
| AR036040A1 (es) * | 2001-06-12 | 2004-08-04 | Upjohn Co | Compuestos de heteroarilo multiciclicos sustituidos con quinuclidinas y composiciones farmaceuticas que los contienen |
| ATE551340T1 (de) * | 2001-10-02 | 2012-04-15 | Pharmacia & Upjohn Co Llc | Azabicyclisch- substituierte annelierte heteroaryl-verbinungen für die behandlung von krankheiten |
| DE10156719A1 (de) * | 2001-11-19 | 2003-05-28 | Bayer Ag | Heteroarylcarbonsäureamide |
| FR2832712B1 (fr) * | 2001-11-23 | 2004-02-13 | Sanofi Synthelabo | Derives de 4-(oxadiazol-3-yl)-1,4-diazabicyclo[3.2.2]nonane, leur preparation et leur application en therapeutique |
| FR2832713B1 (fr) * | 2001-11-23 | 2004-02-13 | Sanofi Synthelabo | Derives de 4-(1,3,4-thiadiazol-2-yl)-1,4-diazabicyclo[3.2.2] nonane, leur preparation et leur application en therapeutique |
| FR2832714B1 (fr) * | 2001-11-23 | 2004-07-16 | Sanofi Synthelabo | Derives de 4-(oxazolopyridin-2-yl)-1,4-diazabicyclo[3.2.2] nonane, leur preparation et leur application en therapeutique |
| NZ554913A (en) * | 2001-12-14 | 2009-01-31 | Targacept Inc | Methods and compositions for the treatment of central nervous system disorders |
| DE10162375A1 (de) * | 2001-12-19 | 2003-07-10 | Bayer Ag | Bicyclische N-Aryl-amide |
| DE10211415A1 (de) * | 2002-03-15 | 2003-09-25 | Bayer Ag | Bicyclische N-Biarylamide |
| DE10211416A1 (de) * | 2002-03-15 | 2003-09-25 | Bayer Ag | Essig- und Propionsäureamide |
| US20030236287A1 (en) * | 2002-05-03 | 2003-12-25 | Piotrowski David W. | Positive allosteric modulators of the nicotinic acetylcholine receptor |
| AU2003267174A1 (en) * | 2002-05-09 | 2003-11-11 | Memory Pharmaceuticals Corporation | Qm-7 and qt-6 cells transfected with mutant cell surface expressed channel receptors and assays using the transfected cells |
| US6760062B2 (en) * | 2002-05-23 | 2004-07-06 | Northrop Grumman Corporation | Synchronizing subsystems of an electro-optical system |
| JP2006503811A (ja) * | 2002-07-17 | 2006-02-02 | ワーナー−ランバート・カンパニー、リミテッド、ライアビリティ、カンパニー | アロステリックカルボキシルマトリックスメタロプロテイナーゼ−13阻害薬とセレコキシブまたはバルデコキシブとの組み合わせ |
| DE10234424A1 (de) * | 2002-07-29 | 2004-02-12 | Bayer Ag | Benzothiophen-, Benzofuran- und Indolharnstoffe |
| WO2004014909A1 (en) * | 2002-08-13 | 2004-02-19 | Warner-Lambert Company Llc | Fused tetrahydropyridine derivatives as matrix metalloproteinase inhibitors |
| JP2006503008A (ja) * | 2002-08-13 | 2006-01-26 | ワーナー−ランバート カンパニー リミティド ライアビリティー カンパニー | マトリクスメタロプロテイナーゼ阻害物質としての4−ヒドロキシキノリン誘導体 |
| GB0220581D0 (en) * | 2002-09-04 | 2002-10-09 | Novartis Ag | Organic Compound |
| US20050031651A1 (en) * | 2002-12-24 | 2005-02-10 | Francine Gervais | Therapeutic formulations for the treatment of beta-amyloid related diseases |
| EP1611128A2 (en) * | 2003-03-28 | 2006-01-04 | Pharmacia & Upjohn Company LLC | Positive allosteric modulators of the nicotinic acetylcholine receptor |
| US20050119249A1 (en) * | 2003-12-02 | 2005-06-02 | Erik Buntinx | Method of treating neurodegenerative diseases using D4 and 5-HT2A antagonists, inverse agonists or partial agonists |
| US20050245531A1 (en) * | 2003-12-22 | 2005-11-03 | Abbott Laboratories | Fused bicycloheterocycle substituted quinuclidine derivatives |
| US7747172B2 (en) * | 2006-05-10 | 2010-06-29 | Hayee M Imran | Optical communication system having enhanced spectral efficiency using electronic signal processing |
| TWI432427B (zh) * | 2006-10-23 | 2014-04-01 | Cephalon Inc | 作為ALK及c-MET抑制劑之2,4-二胺基嘧啶之融合雙環衍生物 |
| GEP20125405B (en) * | 2007-05-11 | 2012-02-27 | Pfizer | Amino-heterocyclic compounds |
| MY150507A (en) * | 2007-08-31 | 2014-01-30 | Eisai R&D Man Co Ltd | Polycyclic compound |
| US7935815B2 (en) * | 2007-08-31 | 2011-05-03 | Eisai R&D Management Co., Ltd. | Imidazoyl pyridine compounds and salts thereof |
| ATE503754T1 (de) * | 2007-10-01 | 2011-04-15 | Comentis Inc | 1h-indol-3-carbonsäure-chinuclidin-4- ylmethylesterderivate als liganden für den nikotinischen alpha-7-acetylcholinrezeptor zur behandlung von alzheimer-krankheit |
| EP2280010B1 (en) * | 2007-11-21 | 2012-12-19 | Abbott Laboratories | Biaryl substituted azabicyclic alkane derivatives as nicotinic acetylcholine receptor activity modulators |
| WO2009091932A2 (en) * | 2008-01-18 | 2009-07-23 | Adamas Pharmaceuticals, Inc. | Treatment of mild dementia of the alzheimer's disease type |
| KR101611824B1 (ko) * | 2008-04-29 | 2016-04-12 | 파넥스트 | 세포 스트레스 반응 조절을 통한 알츠하이머 질환 및 관련 장애의 치료를 위한 신규 치료학적 접근법 |
| CN104127434B (zh) * | 2008-04-29 | 2017-10-13 | 法奈科斯公司 | 使用唑尼沙胺和阿坎酸治疗阿尔茨海默病和相关病症的组合组合物 |
| PT2282778T (pt) * | 2008-04-29 | 2017-04-27 | Pharnext | Novas abordagens terapêuticas no tratamento da doença de alzheimer e doenças relacionadas através de uma modulação da angiogénese |
| NZ593090A (en) * | 2008-11-13 | 2013-06-28 | Link Medicine Corp | Azaquinolinone derivatives and uses thereof |
| WO2010071846A2 (en) * | 2008-12-19 | 2010-06-24 | Afraxis, Inc. | Compounds for treating neuropsychiatric conditions |
| JP2012514011A (ja) * | 2008-12-30 | 2012-06-21 | ラモト アト テルーアビブ ユニバーシティー リミテッド | Napを用いる併用治療の方法 |
| TWI404721B (zh) * | 2009-01-26 | 2013-08-11 | Pfizer | 胺基-雜環化合物 |
| US8754100B2 (en) * | 2009-02-26 | 2014-06-17 | Eisai R&D Management Co., Ltd. | Nitrogen-containing fused heterocyclic compounds and their use as beta amyloid production inhibitors |
| CN102395371A (zh) * | 2009-04-13 | 2012-03-28 | 施万制药 | 用于治疗认知障碍的5-ht4受体促效剂化合物 |
| CN102548986A (zh) * | 2009-06-05 | 2012-07-04 | 链接医药公司 | 氨基吡咯烷酮衍生物及其用途 |
| WO2011057199A1 (en) * | 2009-11-06 | 2011-05-12 | Adenios, Inc. | Compositions for treating cns disorders |
| US20110274628A1 (en) * | 2010-05-07 | 2011-11-10 | Borschke August J | Nicotine-containing pharmaceutical compositions |
-
2010
- 2010-05-11 CN CN2010800312022A patent/CN102802620A/zh active Pending
- 2010-05-11 RU RU2011150248/02A patent/RU2011150248A/ru unknown
- 2010-05-11 PE PE2011001948A patent/PE20120324A1/es not_active Application Discontinuation
- 2010-05-11 EP EP20100718403 patent/EP2429518A1/en not_active Withdrawn
- 2010-05-11 CA CA 2761716 patent/CA2761716A1/en not_active Abandoned
- 2010-05-11 JP JP2012510926A patent/JP5808319B2/ja not_active Expired - Fee Related
- 2010-05-11 BR BRPI1014793A patent/BRPI1014793A2/pt not_active IP Right Cessation
- 2010-05-11 WO PCT/US2010/034353 patent/WO2010132423A1/en not_active Ceased
- 2010-05-11 MX MX2011011972A patent/MX2011011972A/es not_active Application Discontinuation
- 2010-05-11 AU AU2010247835A patent/AU2010247835A1/en not_active Abandoned
- 2010-12-27 US US12/979,139 patent/US20110124631A1/en not_active Abandoned
-
2011
- 2011-11-10 IL IL216281A patent/IL216281A0/en unknown
- 2011-11-11 EC ECSP11011453 patent/ECSP11011453A/es unknown
- 2011-11-11 CO CO11153648A patent/CO6460746A2/es not_active Application Discontinuation
- 2011-11-11 CL CL2011002847A patent/CL2011002847A1/es unknown
-
2014
- 2014-06-17 US US14/307,139 patent/US20150126546A1/en not_active Abandoned
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2003055878A1 (de) * | 2001-12-27 | 2003-07-10 | Bayer Healthcare Ag | 2-heteroarylcarbonsäureamide |
| CN1726033A (zh) * | 2002-12-11 | 2006-01-25 | 法马西亚和厄普乔恩公司 | 用α7烟碱乙酰胆碱受体激动剂和其它化合物的联合治疗疾病 |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN103333163A (zh) * | 2013-07-09 | 2013-10-02 | 广州中医药大学 | 一种苯并呋喃类衍生物及其制备方法和应用 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2012526821A (ja) | 2012-11-01 |
| ECSP11011453A (es) | 2011-12-30 |
| EP2429518A1 (en) | 2012-03-21 |
| CL2011002847A1 (es) | 2012-07-20 |
| MX2011011972A (es) | 2011-12-08 |
| PE20120324A1 (es) | 2012-04-17 |
| US20150126546A1 (en) | 2015-05-07 |
| CA2761716A1 (en) | 2010-11-18 |
| CO6460746A2 (es) | 2012-06-15 |
| AU2010247835A1 (en) | 2011-12-08 |
| BRPI1014793A2 (pt) | 2016-04-05 |
| IL216281A0 (en) | 2012-01-31 |
| RU2011150248A (ru) | 2013-06-20 |
| US20110124631A1 (en) | 2011-05-26 |
| JP5808319B2 (ja) | 2015-11-10 |
| WO2010132423A1 (en) | 2010-11-18 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN102802620A (zh) | 使用某种α-7烟酸受体与乙酰胆碱酯酶抑制剂结合治疗认知障碍 | |
| JP7288999B2 (ja) | ピラゾロキノリン誘導体とドネペジルの併用による認知症治療剤 | |
| US8404711B2 (en) | 5-HT4 receptor agonist compounds for treatment of cognitive disorders | |
| Vijayvargiya et al. | Systematic review with meta‐analysis: efficacy and safety of treatments for opioid‐induced constipation | |
| CN110603039B (zh) | 组合吡唑并喹啉衍生物和美金刚的痴呆治疗剂 | |
| KR20190045273A (ko) | 치매 치료 | |
| McLean et al. | Nicotinic α7 and α4β2 agonists enhance the formation and retrieval of recognition memory: potential mechanisms for cognitive performance enhancement in neurological and psychiatric disorders | |
| Zhu et al. | Methylphenidate and μ opioid receptor interactions: a pharmacological target for prevention of stimulant abuse | |
| Ghajar et al. | Citicoline (CDP‐choline) add‐on therapy to risperidone for treatment of negative symptoms in patients with stable schizophrenia: A double‐blind, randomized placebo‐controlled trial | |
| US20210393615A1 (en) | Methods for treating neurological conditions and exposure to nerve agents | |
| WO2022023813A1 (en) | Administration of modulators of 5-ht and/or ampa receptors for treating neurological conditions | |
| JP2024507492A (ja) | 精神療法を補助するためのメスカリン及びメスカリン類似体(スカリン)の効果 | |
| JP2020516625A (ja) | Nk1拮抗薬組み合わせおよびシヌクレイノパチーを治療する方法 | |
| JP2012500248A (ja) | 不安障害の治療 | |
| CA2566204A1 (en) | Method for improving cognitive function by co-administration of a gabab receptor antagonist and an acetylcholinesterase inhibitor | |
| Herbert et al. | One-trial cocaine-induced behavioral sensitization in preweanling rats: role of contextual stimuli. | |
| CA2808797A1 (en) | Treatment of cognitive disorders with certain alpha-7 nicotinic acid receptor agonists in combination with acetylcholinesterase inhibitors | |
| van Dijk et al. | Behavioural effects of trishomocubanes in rats with unilateral 6-hydroxydopamine lesions | |
| HUP9904578A2 (hu) | Xanomelin alkalmazása bipoláris depresszió kezelésére szolgáló gyógyszerkészítmények előállítására | |
| CN117529318A (zh) | 治疗阿尔茨海默病的方法 | |
| HK40103192A (zh) | 治疗阿尔茨海默病的方法 | |
| WO2025154076A1 (en) | Method of prolonging the survival of a subject with als | |
| HK40071665A (zh) | 在痴呆患者中治疗行为和精神症状 | |
| Barak et al. | P. 3. d. 021 Physostigmine reverses MK-801-induced but not amphetamine-induced effects on latent inhibition: focus on cholinergic treatments in schizophrenia | |
| Tiurina et al. | P. 6.012 Analysis of the impact of different forms of naltrexone on the syndrome of anhedonia and depression among heroin addicts |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C02 | Deemed withdrawal of patent application after publication (patent law 2001) | ||
| WD01 | Invention patent application deemed withdrawn after publication |
Application publication date: 20121128 |