CN102367240A - 含1,2,3-噻二唑母环的酰亚胺基噻唑酮化合物、中间体及其制备方法和应用 - Google Patents
含1,2,3-噻二唑母环的酰亚胺基噻唑酮化合物、中间体及其制备方法和应用 Download PDFInfo
- Publication number
- CN102367240A CN102367240A CN2011100275000A CN201110027500A CN102367240A CN 102367240 A CN102367240 A CN 102367240A CN 2011100275000 A CN2011100275000 A CN 2011100275000A CN 201110027500 A CN201110027500 A CN 201110027500A CN 102367240 A CN102367240 A CN 102367240A
- Authority
- CN
- China
- Prior art keywords
- group
- thiadiazole
- substituted
- branched
- phenyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- UGUHFDPGDQDVGX-UHFFFAOYSA-N 1,2,3-thiadiazole Chemical compound C1=CSN=N1 UGUHFDPGDQDVGX-UHFFFAOYSA-N 0.000 title 1
- YCJIOQMHUJJJGH-UHFFFAOYSA-N 1-imino-1,3-thiazole 1-oxide Chemical class N=S1(=O)C=CN=C1 YCJIOQMHUJJJGH-UHFFFAOYSA-N 0.000 title 1
- 150000001875 compounds Chemical class 0.000 title 1
- 238000002360 preparation method Methods 0.000 title 1
Landscapes
- Nitrogen- Or Sulfur-Containing Heterocyclic Ring Compounds With Rings Of Six Or More Members (AREA)
- Agricultural Chemicals And Associated Chemicals (AREA)
- Plural Heterocyclic Compounds (AREA)
Abstract
本发明涉及一种含1,2,3-噻二唑母环的酰亚胺基噻唑烷(硫)酮类化合物(A)及其酰基硫脲型中间体(B)以及可能的光学异构体、顺反异构体或农药学上可接受的盐的制备,及其作为植物病害防治剂的应用。该系列化合物对植物病害(如水稻纹枯病、水稻白叶枯病、水稻稻瘟病、番茄斑点病、瓜类炭疽病、瓜类白粉病等)有高的抗病诱导活性。
Description
技术领域
本发明涉及含1,2,3-噻二唑母环的酰亚胺基噻唑酮类化合物(烷酮或硫酮)、其酰基硫脲型中间体以及可能的光学异构体、顺反异构体或农药学上可接受的盐,它们的制备方法,以及它们作为植物病害防治剂的应用。
背景技术
传统农药大多是以直接杀死有害生物为目标,不可避免会带来农药公害的问题,因此绿色化学农药的研发、生产和应用成为事关工农业进步、环境生态可持续发展、食品安全与卫生乃至社会稳定的重大科学技术问题。在具有全新作用机制的新型绿色化学农药中,利用植物自身的防御系统以及有用次生代谢物来防病治虫是今后新农药开发的主要方向之一。
植物受病原物诱导可以产生系统的抗病性能,也称系统获得性抗性,化学物质(植物抗病激活剂)的诱导也能产生系统获得性抗性。与传统农药相比植物抗病激活剂有如下特点:(1)本身无明显杀菌或抑菌作用,在活体条件中才能激发植物的自身免疫;(2)诱导产生的抗病性具有持效和广谱特性;(3)诱导处理的植物经过一段时间后才能对病原菌表现抗性;(4)不易产生抗药性;(5)对不具有致病性的菌无影响,不污染环境,有利于维持生态系统复杂而又微妙的平衡和环境保护,是典型的生态型农药。因此,植物抗病激活剂成为当前新农药创制研究的新热点。
已报道的非生物源植物抗病激活剂有内源的乙烯(Et)、水杨酸(SA)、茉莉酸(JA),外源的有苯并噻二唑(BTH)、β-氨基丁酸(BABA)、2,6-二氯异烟酸(INA)及其甲脂、N-氰甲基-2-氯异烟酰胺(NCI)、烯丙异噻唑(Probenazole)、2,2-二氯-3,3-二甲基环丙羧酯(DDCC)、水杨酸甲酯(MeSA)衍生物、茉莉酸甲酯(MJ)等[J.Pesticide Sci,1992,6,107.Plant Pathology,1992,41,444.]。目前,已商品化的植物抗病激活剂有:Syngenta开发的植物激活剂活化酯BTH(苯并[1,2,3]-噻二唑-7-硫代羧酸甲酯)和日本农药株氏会社研发的植物激活剂噻酰菌胺TDL(3’-氯-4,4’-二甲基-1,2,3-噻二唑-5-甲酰苯胺)。研究证实,在先导化合物中引入1,2,3-噻二唑基团,通常会提高生物活性或者扩大其生物活性谱。
本发明目的在于,服务于保护生态环境,创建现代绿色农业的大方向,针对经济作物的病害防治,在合理设计的基础上,创制结构新颖、便于工业化生产、质量和成本可以得到很好控制的抗病激活剂。
发明内容
本发明目的在于,提供一类含1,2,3-噻二唑母环的酰亚胺基噻唑烷(硫)酮类化合物及其酰基硫脲型中间体的合成及其在植物保护方面的用途。
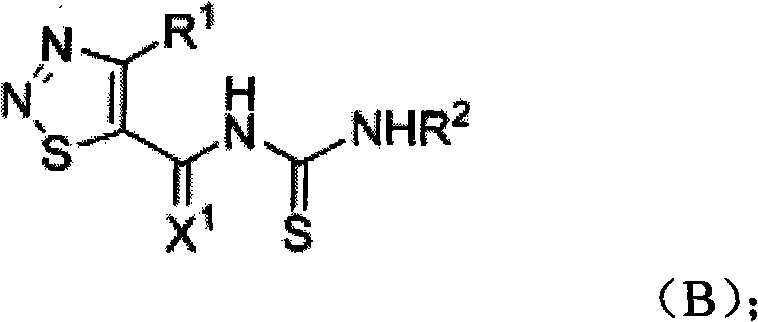
一种含1,2,3-噻二唑母环的酰基硫脲型中间体,其特征在于,含有如下的结构式:
其中,R1、R2各自独立地选自以下基团:H、C1~C9直链或支链或环状的饱和或不饱和烃基、带取代基的C1~C9直链或支链或环状的饱和或不饱和烃基、苯基、取代苯基、苄基、取代苄基以及五元或六元杂环;
所述取代基是卤代基、羟基、烷氧基、氨基、取代氨基、羧基、氰基、酯基,酰胺基或硝基;
所述五元或六元杂环含氮、氧、硫三种元素中的一种或多种;
X1为O或S。
所述R1还可以选自如下结构的基团: 其中A、B为H或C1~C9烷基。优选地,所述R1为甲基、乙基、丙基、氯甲基、溴甲基、苯基、取代苯基中的一种;更优选地,为甲基、乙基、氯甲基。
所述R2选自H、C1~C5饱和或不饱和烷基、氟或氯代的C1~C5饱和或不饱和烷基、苯基或取代苯基以及五元或六元杂环。
其中,R1、R2各自独立地选自以下基团:H、C1~C9直链或支链或环状的饱和或不饱和烃基、带取代基的C1~C9直链或支链或环状的饱和或不饱和烃基、苯基、取代苯基、苄基、取代苄基以及五元或六元杂环;
R3、R4各自独立选自以下基团:H、C1~C9直链或支链的饱和或不饱和烃基、带取代基的C1~C9直链或支链的饱和或不饱和烃基以及卤代基;或者R3和R4共同构成-CH2-Xm-(CH2)n-CH2-,其中X=O、NH、NR、S,m=0、1或2,n=0、1、2、3或4;或者R3和R4单键合并构成如下双键结构。
其中,R5、R6各自独立地选自以下基团:H、C1~C9直链或支链或环状的饱和或不饱和烃基、带取代基的C1~C9直链或支链或环状的饱和或不饱和烃基、苯基、取代苯基、苄基、取代苄基以及五元或六元杂环;
所述取代基是卤代基、羟基、烷氧基、氨基、取代氨基、羧基、氰基、酯基,酰胺基或硝基;
所述五元或六元杂环含氮、氧、硫三种元素中的一种或多种;
X1为O或S,X2为O或S;X1、X2为优选为O;
所述R1还可以是: 其中A、B为H或C1~C9烷基。
所述酰亚胺基噻唑酮化合物包含光学异构体、顺反异构体或农药学上可接受的盐。
上述酰亚胺基噻唑酮化合物的制备方法,包含如下步骤:
a)β-酮酯与乙酰肼形成的酰腙在一定反应温度和亚硫酰氯存在下进行环合反应;
b)上述环合反应的产物进行水解和酰氯化;
c)酰基异硫氰酸酯的原位合成与酰基硫脲衍生物的制备;
d)通过取代的卤代乙酸酯与上述产物的环合反应构建酰亚胺基噻唑酮杂环,得到所述酰亚胺基噻唑酮化合物;
e)在R3=R4=H的情况下,可通过Knoevenagel型反应制备具有下面结构特征的产物:
如上所述酰基硫脲型中间体和酰亚胺基噻唑酮化合物的应用,用于制备植物病害防治剂。植物病害的例子包括但不限于:水稻纹枯病、水稻白叶枯病、水稻稻瘟病、番茄斑点病、瓜类炭疽病、瓜类白粉病等。
所述R2优选C1~C3饱和烷基、苯基或取代苯基。
通式为(A)和(B)的化合物的合成方法如下:
其中,结构通式为5的化合物亦可通过化合物4(结构通式为5的化合物中R3=R4=H) 的Knoevenagel型反应制备。Knoevenagel型反应中,噻唑烷(硫)酮与醛的摩尔比为1∶1~1.5。
具体实施方式
下面通过实施例对本发明进行具体描述。有必要在此指出的是,以下实施例只用于对本发明作进一步说明,不能理解为对本发明保护范围的限制,该领域的专业技术人员根据本发明的内容作出的一些非本质的改进和调整,仍属于本发明的保护范围。
实施例1
在一个100mL圆底烧瓶中加入26.41g(0.3mol)乙酸乙酯,室温搅拌下缓慢滴入14.72g(0.25mol)水合肼,室温反应3h,反应结束后,减压蒸馏除去乙醇、水和剩余的乙酸乙酯,得粗品乙酰肼18.15g(产率98%)。
实施例2
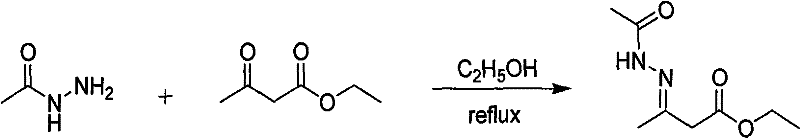
在一个50mL圆底烧瓶中加入14.82g(0.22mol)乙酰肼、10mL无水乙醇,搅拌下缓慢滴入26.03g(0.2mol)乙酰乙酸乙酯,滴加完毕后回流2h,反应结束后(TLC跟踪反应),减压蒸馏除去乙醇,将残留固体倒入50mL冰水中,过滤后干燥得粗产品35.75g(产率96%)。
实施例3
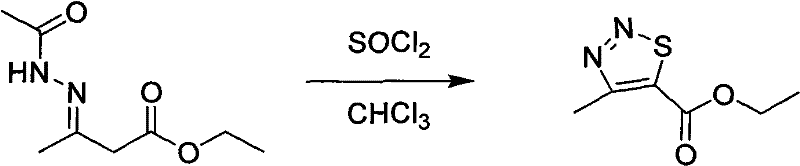
在一个100mL圆底烧瓶中加入17mL(0.24mol)氯化亚砜、20mL氯仿,冰浴冷却下分次 加入37.25g(0.2mol)3-乙酰腙-丁酸乙酯,保持温度加完。撤去冰浴,室温下继续搅拌6h,反应结束后(TLC跟踪),减压蒸馏除去氯仿和过量氯化亚砜,减压蒸馏,得到无色透明液体27.87g(产率81%)。
实施例4
在一个100mL圆底烧瓶中加入17.21g(0.1mol)4-甲基-1,2,3-噻二唑-5-甲酸乙酯、20mL无水乙醇,室温搅拌下滴入4.83g(0.12mol)氢氧化钠配成的饱和水溶液,室温下反应30min,反应结束后(TLC跟踪),减压蒸馏除去乙醇,向剩余水溶液中缓慢滴加浓盐酸,至体系为弱酸性,析出大量白色固体,过滤后重结晶(无水乙醇)得白色固体15.76g(产率92%)。
实施例5
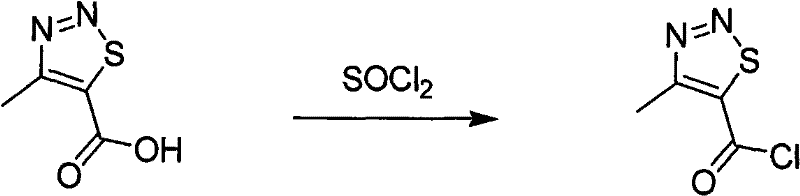
在一个50mL圆底烧瓶中加入7.24g(50mmol)4-甲基-1,2,3-噻二唑-5-甲酸、5mL(60mmol)氯化亚砜、两滴DMF,加热回流2h,反应结束后减压蒸馏除去过量氯化亚砜,减压蒸馏得无色液体7.77g(产率96%),密封保存。
实施例6
在一个50mL圆底烧瓶中加入0.84g(0.011mol)硫氰酸铵和5mL乙腈,冰浴搅拌下,缓慢滴加1.62g(0.01mol)4-甲基1,2,3-噻二唑-5-甲酰氯,滴加完毕后继续搅拌30min,反应结束后(TLC跟踪反应)。再滴加0.93g(0.01mol)苯胺与3mL乙腈配成的溶液,滴加完毕后继续搅拌30min。反应结束后(TLC跟踪反应),将混合物倒进30mL水中,滤出黄色沉淀、重结晶(95%乙醇)得到2.39g黄色固体(产率86%)。1H NMR(400MHz,DMSO-d6)δ(ppm):12.17(s,1H,O=C-NH),12.07(s,1H,Ph-NH),7.69(d,J=7.8Hz,2H,Ph-H),7.44(t,J=7.8Hz, 2H,Ph-H),7.29(t,J=7.3Hz,1H,Ph-H),2.82(s,3H,N-C-CH3)。
实施例7
在一个50mL圆底烧瓶中加入0.84g(0.011mol)硫氰酸铵和5mL乙腈,冰浴搅拌下,缓慢滴加1.62g(0.01mol)4-甲基1,2,3-噻二唑-5-甲酰氯,滴加完毕后继续搅拌30min,反应结束后(TLC跟踪反应)。再滴加1.07g(0.01mol)对甲苯胺与3mL乙腈配成的溶液,滴加完毕后继续搅拌30min,反应结束后(TLC跟踪反应),将混合物倒入30mL水中,滤出黄色沉淀、重结晶(95%乙醇)得到2.51g黄色固体(产率86%)。1H NMR(400MHz,DMSO-d6)δ(ppm):12.10(s,1H,O=C-NH),11.99(s,1H,Ph-NH),7.54(d,J=8.1Hz,2H,Ph-H),7.22(d,J=8.1Hz,2H,Ph-H),2.80(s,3H,N-C-CH3),2.31(s,3H,Ph-CH3)。
实施例8
在一个50mL圆底烧瓶中加入0.85g(0.011mol)硫氰酸铵和5mL乙腈,冰浴搅拌下,缓慢滴加1.62g(0.01mol)4-甲基1,2,3-噻二唑-5-甲酰氯。滴加完毕后继续搅拌30min,反应结束后(TLC跟踪反应),再滴加1.07g(0.01mol)邻甲苯胺与3mL乙腈配成的溶液。滴加完毕后继续搅拌30min,反应结束后(TLC跟踪反应),将混合物倒入30mL水中,滤出黄色沉淀、重结晶(95%乙醇)得到2.38g黄色固体(产率82%)。1H NMR(400MHz,DMSO-d6)δ(ppm):12.22(s,1H,O=C-NH),11.81(s,1H,Ph-NH),7.56(d,J=6.8Hz,1H,Ph-H),7.29(m,3H,Ph-H),2.83(s,3H,N-C-CH3),2.28(s,3H,Ph-CH3)。
实施例9
在一个50mL圆底烧瓶中加入1.46g(5mmol)N-(4-甲基1,2,3-噻二唑-5-甲酰)-N’-(4-甲基苯基)硫脲、1.01g(6mmol)溴乙酸乙酯、0.49g(6mmol)无水乙酸钠和5mL无水乙醇,加热回流,体系逐渐由黄色变成紫色,继续反应1h,反应结束后(TLC跟踪反应),减压蒸馏除去乙醇。所得固体重结晶(95%乙醇)得1.44g紫色固体(产率87%)。1H NMR(400MHz,DMSO-d6)δ(ppm):7.36(d,J=7.8Hz,2H,Ph-H),7.25(d,J=7.8Hz,2H,Ph-H),4.21(s,2H,CH2),2.70(s,3H,N-C-CH3),2.40(s,3H,Ph-CH3)。
实施例10
在一个50mL圆底烧瓶中加入1.48g(0.01mol)N-(4-甲基1,2,3-噻二唑-5-甲酰)-N’-(3-氟苯基)硫脲、1.00g(6mmol)溴乙酸乙酯、0.49g(6mmol)无水乙酸钠和5mL无水乙醇,加热回流,体系逐渐由黄色变成紫色,继续反应1h,反应结束后(TLC跟踪反应),减压蒸馏除去乙醇。所得固体重结晶(95%乙醇)得1.43g紫色固体(产率为88%)。1H NMR(400MHz,DMSO-d6)δ(ppm):7.64(m,1H,Ph-H),7.39(m,2H,Ph-H),7.30(d,J=8.0Hz,1H,Ph-H),4.25(s,2H,CH2),2.73(s,3H,N-C-CH3)。
实施例11
在一个25mL圆底烧瓶中加入0.15g(0.5mmol)3-(苯基)-2-(4-甲基1,2,3-噻二唑-5-甲酰)亚胺-4-噻唑烷酮、0.07g(0.6mmol)对甲基苯甲醛、两滴哌啶和5mL无水乙醇,回流反应30min,析出黄色固体,反应结束后(TLC跟踪反应)过滤、重结晶(氯仿:无水乙醇)得 0.20g黄色固体(产率95%)。1H NMR(400MHz,CDCl3)δ(ppm):8.03(s,1H,CH),7.60(d,J=7.45Hz,5H,Ph-H),7.36(t,J=8.63Hz,4H,Ph-H),2.89(s,3H,N-C-CH3),2.46(s,3H,Ph-CH3)。
实施例12
在一个25mL圆底烧瓶中加入0.16g(0.5mmol)3-(4-甲基苯基)-2-(4-甲基1,2,3-噻二唑-5-甲酰)亚胺-4-噻唑烷酮、0.06g(0.6mmol)苯甲醛、两滴哌啶和5mL无水乙醇,回流反应30min,析出黄色固体,反应结束后(TLC跟踪反应)过滤、重结晶(氯仿:无水乙醇)得0.20g黄色固体(产率99%)。1H NMR(400MHz,CDCl3)δ(ppm):8.03(s,1H,CH),7.67(s,2H,Ph-H),7.51(s,3H,Ph-H),7.37(s,2H,Ph-H),2.89(s,3H,N-C-CH3),2.48(s,3H,Ph-CH3)。
相关化合物的生物活性测试方法
按照供试药剂的有效含量计算出试验用制剂的稀释倍数,按试验浓度配好药剂,于黄瓜苗出土后立即进行第一次喷雾诱导(供试药剂及对照药剂均进行喷雾诱导),将供试药剂均匀喷施到叶片的正背面,以叶面雾滴均匀一致为宜,每隔3天诱导1次,连续诱导3次,第3次诱导后3天接种。各病原菌均采用喷雾方式接种。
按照下面分级标准调查病情计算防效。
病叶分级标准:
0级:无病斑;
1级:病斑面积占整个叶面积的5%以下;
3级:病斑面积占整个叶面积的6~10%;
5级:病斑面积占整个叶面积的11~25%;
7级:病斑面积占整个叶面积的26~50%;
9级:病斑面积占整个叶面积的50以上。
药效计算方法:根据病情指数按下列指数公式计算出防治效果,再按DMRT法测定处 理间防效的差异显著性。
本发明的部分化合物的诱导抗病活性示例
示例化合物的结构和编号如下所示:
表1是对番茄细菌性斑点病的诱导抗病活性示例[供试药剂均设50ppm(50mg/L)]
表1
表2是目标化合物对水稻纹枯病的诱导抗病结果[供试药剂均设50ppm(50mg/L)]
表2
| 化合物结构 | 平均病指 | 防效(%) |
| P-A-01 | 42.22 | 52.03 |
| P-A-02 | 27.78 | 68.44 |
[0102]
| P-A-03 | 41.48 | 52.88 |
| P-A-04 | 26.79 | 69.57 |
| P-A-05 | 44.44 | 49.51 |
| P-A-06 | 37.28 | 57.64 |
| P-B-01 | 33.09 | 62.41 |
| P-B-02 | 35.93 | 59.19 |
| P-B-03 | 49.88 | 43.34 |
| P-B-04 | 32.84 | 62.69 |
| P-B-05 | 37.90 | 56.94 |
| P-B-06 | 33.46 | 61.99 |
| P-C-01 | 25.80 | 70.69 |
| P-C-02 | 27.53 | 68.72 |
| P-C-03 | 13.33 | 84.85 |
| P-C-04 | 21.48 | 75.60 |
| P-C-05 | 20.00 | 77.28 |
| P-C-06 | 32.22 | 63.39 |
| P-C-07 | 31.98 | 63.67 |
| P-C-08 | 37.78 | 57.08 |
| P-C-09 | 29.14 | 66.90 |
| P-C-10 | 46.42 | 47.27 |
| P-C-11 | 45.93 | 47.83 |
| P-C-12 | 42.59 | 51.61 |
| P-C-13 | 56.54 | 35.76 |
| P-C-14 | 43.70 | 50.35 |
| P-C-15 | 64.20 | 27.07 |
| P-C-16 | 43.58 | 50.49 |
| P-C-17 | 9.88 | 88.78 |
| P-C-18 | 18.27 | 79.24 |
| P-C-19 | 40.12 | 54.42 |
| P-C-20 | 32.35 | 63.25 |
| P-C-21 | 21.36 | 75.74 |
| P-C-22 | 42.59 | 51.61 |
| P-C-23 | 34.69 | 60.59 |
| P-C-24 | 27.53 | 68.72 |
[0103]
| P-C-25 | 31.28 | 64.47 |
| P-C-26 | 29.38 | 66.62 |
| P-C-27 | 28.15 | 68.02 |
| P-C-28 | 46.79 | 46.84 |
| P-C-29 | 38.89 | 55.82 |
| P-C-30 | 27.16 | 69.14 |
| P-C-31 | 12.10 | 86.26 |
| P-C-32 | 35.68 | 59.47 |
| P-C-33 | 29.51 | 66.48 |
| P-C-34 | 27.04 | 69.28 |
| P-C-35 | 37.78 | 57.08 |
| P-C-36 | 29.51 | 66.48 |
| P-C-37 | 52.10 | 40.81 |
Claims (8)
2.根据权利要求1所述的一种含1,2,3-噻二唑母环的酰基硫脲型中间体,其特征在于,所述R1还可以选自如下结构的基团:
其中A、B为H或C1~C9烷基。
3.根据权利要求1所述的一种含1,2,3-噻二唑母环的酰基硫脲型中间体,其特征在于,所述R1为甲基、乙基、丙基、氯甲基、溴甲基、苯基、取代苯基中的一种。
4.根据权利要求1所述的一种含1,2,3-噻二唑母环的酰基硫脲型中间体,其特征在于,所述R2选自H、C1~C5饱和或不饱和烷基、氟或氯代的C1~C5饱和或不饱和烷基、苯基或取代苯基以及五元或六元杂环。
5.权利要求1至4任一所述的含1,2,3-噻二唑母环的酰基硫脲型中间体得到的酰亚胺基噻唑酮化合物,其特征在于,所述酰亚胺基噻唑酮化合物具有如下结构式:
其中,R1、R2各自独立地选自以下基团:H、C1~C9直链或支链或环状的饱和或不饱和烃基、带取代基的C1~C9直链或支链或环状的饱和或不饱和烃基、苯基、取代苯基、苄基、取代苄基以及五元或六元杂环;
R3、R4各自独立选自以下基团:H、C1~C9直链或支链的饱和或不饱和烃基、带取代基的C1~C9直链或支链的饱和或不饱和烃基以及卤代基;或者R3和R4共同构成-CH2-Xm-(CH2)n-CH2-,其中X=O、NH、NR、S,m=0、1或2,n=0、1、2、3或4;或者R3和R4单键合并构成如下双键结构。
其中,R5、R6各自独立地选自以下基团:H、C1~C9直链或支链或环状的饱和或不饱和烃基、带取代基的C1~C9直链或支链或环状的饱和或不饱和烃基、苯基、取代苯基、苄基、取代苄基以及五元或六元杂环;
所述取代基是卤代基、羟基、烷氧基、氨基、取代氨基、羧基、氰基、酯基,酰胺基或硝基;
所述五元或六元杂环含氮、氧、硫三种元素中的一种或多种;
X1为O或S,X2为O或S;
所述R1还可以是:其中A、B为H或C1~C9烷基。
6.根据权利要求6的含1,2,3-噻二唑母环的酰基硫脲型中间体得到的酰亚胺基噻唑酮化合物,其特征在于,所述酰亚胺基噻唑酮化合物包含光学异构体、顺反异构体或农药学上可接受的盐。
8.权利要求1、2、3、4、5或6所述的酰基硫脲型中间体或酰亚胺基噻唑酮化合物的应用,其特征在于,用于制备植物病害防治剂,所述植物病害包括水稻纹枯病、水稻白叶枯病、水稻稻瘟病、番茄斑点病、瓜类炭疽病或瓜类白粉病。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201110027500.0A CN102367240B (zh) | 2011-01-25 | 2011-01-25 | 含1,2,3-噻二唑母环的酰亚胺基噻唑酮化合物、中间体及其应用 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201110027500.0A CN102367240B (zh) | 2011-01-25 | 2011-01-25 | 含1,2,3-噻二唑母环的酰亚胺基噻唑酮化合物、中间体及其应用 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN102367240A true CN102367240A (zh) | 2012-03-07 |
| CN102367240B CN102367240B (zh) | 2014-06-18 |
Family
ID=45759836
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201110027500.0A Expired - Fee Related CN102367240B (zh) | 2011-01-25 | 2011-01-25 | 含1,2,3-噻二唑母环的酰亚胺基噻唑酮化合物、中间体及其应用 |
Country Status (1)
| Country | Link |
|---|---|
| CN (1) | CN102367240B (zh) |
Cited By (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN103012316A (zh) * | 2012-11-29 | 2013-04-03 | 浙江工业大学 | N-4-甲基-1,2,3-噻二唑-4-酰基-n-取代1,3,4-噻二唑基硫脲衍生物及其制备和应用 |
| CN103044413A (zh) * | 2012-11-29 | 2013-04-17 | 浙江工业大学 | 一种噻二唑基硫脲衍生物及其制备和作为植物生长调节剂的应用 |
| CN103058955A (zh) * | 2012-11-29 | 2013-04-24 | 浙江工业大学 | 一种噻二唑硫脲衍生物及其制备和作为植物生长调节剂的应用 |
| CN103102330A (zh) * | 2012-11-29 | 2013-05-15 | 浙江工业大学 | N-4-甲基-1,2,3-噻二唑-4-酰基-n-取代苯基硫脲衍生物及其制备和应用 |
| CN103613564A (zh) * | 2013-12-12 | 2014-03-05 | 浙江工业大学 | 一种含1,2,3-噻二唑的酰胺基脲衍生物的制备方法 |
| WO2015177063A1 (en) * | 2014-05-19 | 2015-11-26 | Syngenta Participations Ag | Insecticidally active amide derivatives with sulfur-substituted phenyl or pyridine groups |
| CN106665605A (zh) * | 2016-12-26 | 2017-05-17 | 蔡志浩 | 一种复方植物杀菌剂 |
| CN106665607A (zh) * | 2016-12-26 | 2017-05-17 | 蔡志浩 | 复方植物杀菌剂 |
| CN107935961A (zh) * | 2017-12-01 | 2018-04-20 | 赣南师范大学 | 一种2‑亚氨基噻唑烷‑4‑酮类化合物的制备方法 |
| US10494366B2 (en) | 2014-12-01 | 2019-12-03 | Syngenta Participations Ag | Pesticidally active amide heterocyclic derivatives with sulphur containing substituents |
| CN114040910A (zh) * | 2019-07-10 | 2022-02-11 | 拜耳公司 | 制备2-(苯基亚氨基)-1,3-噻唑烷-4-酮的方法 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1180297A (zh) * | 1995-03-31 | 1998-04-29 | 日本农药株式会社 | 农业和园艺病害防治剂和防治这些病害的方法 |
| CN1207739A (zh) * | 1995-12-07 | 1999-02-10 | 拜尔公司 | 1,2,3-噻二唑羧酸(硫)酯及其作为防治害虫剂和杀微生物剂的用途 |
| CN101020667A (zh) * | 2007-03-12 | 2007-08-22 | 南开大学 | 具有诱导金丝桃属植物次生代谢活性的新化合物 |
-
2011
- 2011-01-25 CN CN201110027500.0A patent/CN102367240B/zh not_active Expired - Fee Related
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1180297A (zh) * | 1995-03-31 | 1998-04-29 | 日本农药株式会社 | 农业和园艺病害防治剂和防治这些病害的方法 |
| CN1207739A (zh) * | 1995-12-07 | 1999-02-10 | 拜尔公司 | 1,2,3-噻二唑羧酸(硫)酯及其作为防治害虫剂和杀微生物剂的用途 |
| CN101020667A (zh) * | 2007-03-12 | 2007-08-22 | 南开大学 | 具有诱导金丝桃属植物次生代谢活性的新化合物 |
Cited By (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN103012316B (zh) * | 2012-11-29 | 2015-03-25 | 浙江工业大学 | N-4-甲基-1,2,3-噻二唑-4-酰基-n-取代1,3,4-噻二唑基硫脲衍生物及其制备和应用 |
| CN103044413A (zh) * | 2012-11-29 | 2013-04-17 | 浙江工业大学 | 一种噻二唑基硫脲衍生物及其制备和作为植物生长调节剂的应用 |
| CN103058955A (zh) * | 2012-11-29 | 2013-04-24 | 浙江工业大学 | 一种噻二唑硫脲衍生物及其制备和作为植物生长调节剂的应用 |
| CN103102330A (zh) * | 2012-11-29 | 2013-05-15 | 浙江工业大学 | N-4-甲基-1,2,3-噻二唑-4-酰基-n-取代苯基硫脲衍生物及其制备和应用 |
| CN103012316A (zh) * | 2012-11-29 | 2013-04-03 | 浙江工业大学 | N-4-甲基-1,2,3-噻二唑-4-酰基-n-取代1,3,4-噻二唑基硫脲衍生物及其制备和应用 |
| CN103102330B (zh) * | 2012-11-29 | 2015-02-25 | 浙江工业大学 | N-4-甲基-1,2,3-噻二唑-4-酰基-n-取代苯基硫脲衍生物及其制备和应用 |
| CN103058955B (zh) * | 2012-11-29 | 2015-02-25 | 浙江工业大学 | 一种噻二唑硫脲衍生物及其制备和作为植物生长调节剂的应用 |
| CN103613564B (zh) * | 2013-12-12 | 2015-05-06 | 浙江工业大学 | 一种含1,2,3-噻二唑的酰胺基脲衍生物的制备方法 |
| CN103613564A (zh) * | 2013-12-12 | 2014-03-05 | 浙江工业大学 | 一种含1,2,3-噻二唑的酰胺基脲衍生物的制备方法 |
| WO2015177063A1 (en) * | 2014-05-19 | 2015-11-26 | Syngenta Participations Ag | Insecticidally active amide derivatives with sulfur-substituted phenyl or pyridine groups |
| CN106458909A (zh) * | 2014-05-19 | 2017-02-22 | 先正达参股股份有限公司 | 具有硫取代的苯基或吡啶基团的具杀虫活性的酰胺衍生物 |
| US9701659B2 (en) | 2014-05-19 | 2017-07-11 | Syngenta Participations Ag | Insecticidally active amide derivatives with sulfur-substituted phenyl or pyridine groups |
| CN106458909B (zh) * | 2014-05-19 | 2020-03-17 | 先正达参股股份有限公司 | 具有硫取代的苯基或吡啶基团的具杀虫活性的酰胺衍生物 |
| US10494366B2 (en) | 2014-12-01 | 2019-12-03 | Syngenta Participations Ag | Pesticidally active amide heterocyclic derivatives with sulphur containing substituents |
| CN106665605A (zh) * | 2016-12-26 | 2017-05-17 | 蔡志浩 | 一种复方植物杀菌剂 |
| CN106665607A (zh) * | 2016-12-26 | 2017-05-17 | 蔡志浩 | 复方植物杀菌剂 |
| CN107935961A (zh) * | 2017-12-01 | 2018-04-20 | 赣南师范大学 | 一种2‑亚氨基噻唑烷‑4‑酮类化合物的制备方法 |
| CN107935961B (zh) * | 2017-12-01 | 2019-10-29 | 赣南师范大学 | 一种2-亚氨基噻唑烷-4-酮类化合物的制备方法 |
| CN114040910A (zh) * | 2019-07-10 | 2022-02-11 | 拜耳公司 | 制备2-(苯基亚氨基)-1,3-噻唑烷-4-酮的方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| CN102367240B (zh) | 2014-06-18 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN102367240A (zh) | 含1,2,3-噻二唑母环的酰亚胺基噻唑酮化合物、中间体及其制备方法和应用 | |
| US5475132A (en) | Antifungal agents based on amides containing a phenyl group | |
| EP0274642B1 (de) | Herbizide und fungizide Mittel auf Basis von substituierten Pyrazolin-5-on-Derivaten | |
| US4663327A (en) | 1-heteroaryl-4-aryl-pyrazolin-5-ones | |
| Ghattas et al. | Synthesis, in vitro antibacterial and in vivo anti-inflammatory activity of some new pyridines | |
| CN104059027B (zh) | 一类含1,2,4-三唑的(e)-甲氧基亚氨基苯乙酸甲酯类化合物及其制备方法和用途 | |
| CN105418505B (zh) | 吡唑酰胺类化合物及其制备法与用途 | |
| RU2475490C1 (ru) | N-АЦИЛИРОВАННЫЕ 3-АМИНО-4,6-ДИМЕТИЛТИЕНО[2,3-b]ПИРИДИН-2-КАРБОКСАМИДЫ В КАЧЕСТВЕ АНТИДОТОВ 2,4-Д НА ПОДСОЛНЕЧНИКЕ | |
| CN107200712A (zh) | 一类含取代基嘧啶芳基脒类化合物、其制备方法及应用 | |
| CN102977088B (zh) | 具有杀菌活性的4-叔丁基-5-(1,2,4-三唑-1-基)-2-酰氨基噻唑及制备方法 | |
| CN106543139B (zh) | 一种三唑酮类化合物及其用途 | |
| RU2557550C1 (ru) | Антидот гербицида 2,4-дихлорфеноксиуксусной кислоты на подсолнечнике | |
| CN115197131A (zh) | 偶氮类2-氨基烟酸苄酯衍生物及其制备方法和用途 | |
| CN103288771B (zh) | 异噻唑类化合物及其作为杀菌剂的用途 | |
| Akbari et al. | Synthesis, anti-bacterial, and antifungal activity of sydnone-based aromatic compounds | |
| CN108383790B (zh) | 一种含吡唑环的酰胺类化合物及其制备方法与应用 | |
| RU2383135C2 (ru) | Антидот 2,4-дихлорфеноксиуксусной кислоты на подсолнечнике | |
| EP0117482B1 (de) | Substituierte Maleinsäureimide und deren Verwendung als Schädlingsbekämpfungsmittel | |
| KR980009261A (ko) | 1,2,3-벤조티아디아졸 유도체 | |
| CN103570672B (zh) | 一种苯基取代噻吩甲酰肼类化合物及其制备方法和应用 | |
| CN104045634A (zh) | 含二氟甲基吡唑甲酰胺类化合物及其制备方法和用途 | |
| Panwar et al. | A green approach for the heterocyclization of 2-substituted benzimidazoles: Synthesis, characterisation and pharmacological evaluation | |
| CN102464618B (zh) | 吡唑酰胺类化合物及其应用 | |
| JPS6335554A (ja) | N−(2−シアノ−2−オキシミノアセチル)−アミノニトリル | |
| CN106234385B (zh) | 一种含苯并吡嗪结构的1,2,4-三唑衍生物作为杀菌剂的应用 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C14 | Grant of patent or utility model | ||
| GR01 | Patent grant | ||
| CF01 | Termination of patent right due to non-payment of annual fee |
Granted publication date: 20140618 Termination date: 20150125 |
|
| EXPY | Termination of patent right or utility model |