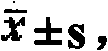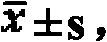CN102191209A - VEGF165和Ang-1双基因共表达载体及其应用 - Google Patents
VEGF165和Ang-1双基因共表达载体及其应用 Download PDFInfo
- Publication number
- CN102191209A CN102191209A CN 201010263189 CN201010263189A CN102191209A CN 102191209 A CN102191209 A CN 102191209A CN 201010263189 CN201010263189 CN 201010263189 CN 201010263189 A CN201010263189 A CN 201010263189A CN 102191209 A CN102191209 A CN 102191209A
- Authority
- CN
- China
- Prior art keywords
- ires
- ang
- vegf165
- epcs
- gene
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 101000808011 Homo sapiens Vascular endothelial growth factor A Proteins 0.000 title claims abstract description 108
- 102000058223 human VEGFA Human genes 0.000 title claims abstract description 103
- 230000004186 co-expression Effects 0.000 title abstract description 16
- 239000013604 expression vector Substances 0.000 title abstract description 9
- 108090000623 proteins and genes Proteins 0.000 claims abstract description 108
- 241000701161 unidentified adenovirus Species 0.000 claims abstract description 81
- 238000012546 transfer Methods 0.000 claims abstract description 39
- 230000000302 ischemic effect Effects 0.000 claims abstract description 31
- 239000013598 vector Substances 0.000 claims abstract description 31
- 230000033115 angiogenesis Effects 0.000 claims abstract description 24
- 210000004165 myocardium Anatomy 0.000 claims abstract description 20
- 238000002360 preparation method Methods 0.000 claims description 10
- 241000620209 Escherichia coli DH5[alpha] Species 0.000 claims description 9
- 239000003814 drug Substances 0.000 claims description 8
- 241000588724 Escherichia coli Species 0.000 claims description 6
- 238000004321 preservation Methods 0.000 claims description 4
- 241000894006 Bacteria Species 0.000 claims description 2
- 230000000968 intestinal effect Effects 0.000 claims 1
- 239000013612 plasmid Substances 0.000 abstract description 103
- 210000004027 cell Anatomy 0.000 abstract description 67
- 230000006801 homologous recombination Effects 0.000 abstract description 28
- 238000002744 homologous recombination Methods 0.000 abstract description 28
- 230000006798 recombination Effects 0.000 abstract description 27
- 238000005215 recombination Methods 0.000 abstract description 27
- 210000000130 stem cell Anatomy 0.000 abstract description 25
- 230000003511 endothelial effect Effects 0.000 abstract description 22
- 210000002216 heart Anatomy 0.000 abstract description 15
- 230000006870 function Effects 0.000 abstract description 7
- 230000003190 augmentative effect Effects 0.000 abstract 1
- 239000000047 product Substances 0.000 description 67
- 239000012634 fragment Substances 0.000 description 38
- 238000001415 gene therapy Methods 0.000 description 31
- 241000700605 Viruses Species 0.000 description 26
- 230000002792 vascular Effects 0.000 description 22
- 241000283973 Oryctolagus cuniculus Species 0.000 description 21
- 238000001976 enzyme digestion Methods 0.000 description 21
- 208000015181 infectious disease Diseases 0.000 description 21
- 238000010276 construction Methods 0.000 description 17
- 238000001514 detection method Methods 0.000 description 15
- XEEYBQQBJWHFJM-UHFFFAOYSA-N iron Substances [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 15
- 238000002054 transplantation Methods 0.000 description 15
- 210000004204 blood vessel Anatomy 0.000 description 14
- 238000002965 ELISA Methods 0.000 description 13
- 239000012228 culture supernatant Substances 0.000 description 13
- 230000001404 mediated effect Effects 0.000 description 13
- 230000002861 ventricular Effects 0.000 description 13
- 230000014509 gene expression Effects 0.000 description 12
- 239000000243 solution Substances 0.000 description 12
- 238000012360 testing method Methods 0.000 description 12
- 230000029087 digestion Effects 0.000 description 11
- 230000000694 effects Effects 0.000 description 11
- 108010073929 Vascular Endothelial Growth Factor A Proteins 0.000 description 10
- 102000005789 Vascular Endothelial Growth Factors Human genes 0.000 description 10
- 108010019530 Vascular Endothelial Growth Factors Proteins 0.000 description 10
- 238000000034 method Methods 0.000 description 10
- 230000001737 promoting effect Effects 0.000 description 10
- 101000702488 Rattus norvegicus High affinity cationic amino acid transporter 1 Proteins 0.000 description 9
- 238000010586 diagram Methods 0.000 description 9
- 230000004217 heart function Effects 0.000 description 9
- 208000031225 myocardial ischemia Diseases 0.000 description 9
- 238000004113 cell culture Methods 0.000 description 8
- 238000010367 cloning Methods 0.000 description 8
- 238000000338 in vitro Methods 0.000 description 8
- 238000001727 in vivo Methods 0.000 description 8
- 210000004185 liver Anatomy 0.000 description 8
- 239000003550 marker Substances 0.000 description 8
- 108091028043 Nucleic acid sequence Proteins 0.000 description 7
- QYOAUOAXCQAEMW-UTXKDXHTSA-N bleomycin A5 Chemical compound N([C@H](C(=O)N[C@H](C)[C@@H](O)[C@H](C)C(=O)N[C@@H]([C@H](O)C)C(=O)NCCC=1SC=C(N=1)C=1SC=C(N=1)C(=O)NCCCNCCCCN)[C@@H](O[C@H]1[C@H]([C@@H](O)[C@H](O)[C@H](CO)O1)O[C@@H]1[C@H]([C@@H](OC(N)=O)[C@H](O)[C@@H](CO)O1)O)C=1N=CNC=1)C(=O)C1=NC([C@H](CC(N)=O)NC[C@H](N)C(N)=O)=NC(N)=C1C QYOAUOAXCQAEMW-UTXKDXHTSA-N 0.000 description 7
- 238000002347 injection Methods 0.000 description 7
- 239000007924 injection Substances 0.000 description 7
- 210000003734 kidney Anatomy 0.000 description 7
- 210000001519 tissue Anatomy 0.000 description 7
- 238000013518 transcription Methods 0.000 description 7
- 230000035897 transcription Effects 0.000 description 7
- 239000012581 transferrin Substances 0.000 description 7
- 229920000936 Agarose Polymers 0.000 description 6
- 108020004414 DNA Proteins 0.000 description 6
- 102000004338 Transferrin Human genes 0.000 description 6
- 108090000901 Transferrin Proteins 0.000 description 6
- 108700004675 bleomycetin Proteins 0.000 description 6
- 210000002798 bone marrow cell Anatomy 0.000 description 6
- 238000010790 dilution Methods 0.000 description 6
- 239000012895 dilution Substances 0.000 description 6
- 238000009826 distribution Methods 0.000 description 6
- 229940079593 drug Drugs 0.000 description 6
- 238000001962 electrophoresis Methods 0.000 description 6
- 230000012010 growth Effects 0.000 description 6
- 238000003384 imaging method Methods 0.000 description 6
- 238000010166 immunofluorescence Methods 0.000 description 6
- 210000005259 peripheral blood Anatomy 0.000 description 6
- 239000011886 peripheral blood Substances 0.000 description 6
- 102000004169 proteins and genes Human genes 0.000 description 6
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 5
- 210000002565 arteriole Anatomy 0.000 description 5
- 239000002299 complementary DNA Substances 0.000 description 5
- 210000002889 endothelial cell Anatomy 0.000 description 5
- 238000010253 intravenous injection Methods 0.000 description 5
- 239000011630 iodine Substances 0.000 description 5
- 229910052740 iodine Inorganic materials 0.000 description 5
- 208000010125 myocardial infarction Diseases 0.000 description 5
- 210000002845 virion Anatomy 0.000 description 5
- 102000012410 DNA Ligases Human genes 0.000 description 4
- 108010061982 DNA Ligases Proteins 0.000 description 4
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 4
- 241000287828 Gallus gallus Species 0.000 description 4
- 240000000220 Panda oleosa Species 0.000 description 4
- 235000016496 Panda oleosa Nutrition 0.000 description 4
- 239000012980 RPMI-1640 medium Substances 0.000 description 4
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 4
- 230000015572 biosynthetic process Effects 0.000 description 4
- 230000035605 chemotaxis Effects 0.000 description 4
- 238000000605 extraction Methods 0.000 description 4
- 239000003102 growth factor Substances 0.000 description 4
- 238000003125 immunofluorescent labeling Methods 0.000 description 4
- 238000011532 immunohistochemical staining Methods 0.000 description 4
- 210000003205 muscle Anatomy 0.000 description 4
- 210000000056 organ Anatomy 0.000 description 4
- 230000010412 perfusion Effects 0.000 description 4
- 238000010839 reverse transcription Methods 0.000 description 4
- 229920006395 saturated elastomer Polymers 0.000 description 4
- 210000003932 urinary bladder Anatomy 0.000 description 4
- 210000003462 vein Anatomy 0.000 description 4
- 238000001712 DNA sequencing Methods 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- 238000010802 RNA extraction kit Methods 0.000 description 3
- 102000007238 Transferrin Receptors Human genes 0.000 description 3
- 108010033576 Transferrin Receptors Proteins 0.000 description 3
- 230000003321 amplification Effects 0.000 description 3
- 238000013461 design Methods 0.000 description 3
- 210000002257 embryonic structure Anatomy 0.000 description 3
- 238000002474 experimental method Methods 0.000 description 3
- 210000003414 extremity Anatomy 0.000 description 3
- 239000000499 gel Substances 0.000 description 3
- 239000001963 growth medium Substances 0.000 description 3
- 239000000463 material Substances 0.000 description 3
- 238000012544 monitoring process Methods 0.000 description 3
- 230000002107 myocardial effect Effects 0.000 description 3
- 238000003199 nucleic acid amplification method Methods 0.000 description 3
- 239000000700 radioactive tracer Substances 0.000 description 3
- 238000010079 rubber tapping Methods 0.000 description 3
- 238000002603 single-photon emission computed tomography Methods 0.000 description 3
- 238000002560 therapeutic procedure Methods 0.000 description 3
- 210000001685 thyroid gland Anatomy 0.000 description 3
- 108010047303 von Willebrand Factor Proteins 0.000 description 3
- 102100036537 von Willebrand factor Human genes 0.000 description 3
- FJQZXCPWAGYPSD-UHFFFAOYSA-N 1,3,4,6-tetrachloro-3a,6a-diphenylimidazo[4,5-d]imidazole-2,5-dione Chemical compound ClN1C(=O)N(Cl)C2(C=3C=CC=CC=3)N(Cl)C(=O)N(Cl)C12C1=CC=CC=C1 FJQZXCPWAGYPSD-UHFFFAOYSA-N 0.000 description 2
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 2
- 102000007469 Actins Human genes 0.000 description 2
- 108010085238 Actins Proteins 0.000 description 2
- 208000010370 Adenoviridae Infections Diseases 0.000 description 2
- 206010060931 Adenovirus infection Diseases 0.000 description 2
- 206010002091 Anaesthesia Diseases 0.000 description 2
- HTTJABKRGRZYRN-UHFFFAOYSA-N Heparin Chemical compound OC1C(NC(=O)C)C(O)OC(COS(O)(=O)=O)C1OC1C(OS(O)(=O)=O)C(O)C(OC2C(C(OS(O)(=O)=O)C(OC3C(C(O)C(O)C(O3)C(O)=O)OS(O)(=O)=O)C(CO)O2)NS(O)(=O)=O)C(C(O)=O)O1 HTTJABKRGRZYRN-UHFFFAOYSA-N 0.000 description 2
- 108090000723 Insulin-Like Growth Factor I Proteins 0.000 description 2
- LRHPLDYGYMQRHN-UHFFFAOYSA-N N-Butanol Chemical group CCCCO LRHPLDYGYMQRHN-UHFFFAOYSA-N 0.000 description 2
- 206010029113 Neovascularisation Diseases 0.000 description 2
- 108010038512 Platelet-Derived Growth Factor Proteins 0.000 description 2
- 102000010780 Platelet-Derived Growth Factor Human genes 0.000 description 2
- WCUXLLCKKVVCTQ-UHFFFAOYSA-M Potassium chloride Chemical compound [Cl-].[K+] WCUXLLCKKVVCTQ-UHFFFAOYSA-M 0.000 description 2
- 102000013275 Somatomedins Human genes 0.000 description 2
- 102000004142 Trypsin Human genes 0.000 description 2
- 108090000631 Trypsin Proteins 0.000 description 2
- 208000011589 adenoviridae infectious disease Diseases 0.000 description 2
- 230000037005 anaesthesia Effects 0.000 description 2
- 210000000709 aorta Anatomy 0.000 description 2
- 108010054176 apotransferrin Proteins 0.000 description 2
- 210000004369 blood Anatomy 0.000 description 2
- 239000008280 blood Substances 0.000 description 2
- 210000001185 bone marrow Anatomy 0.000 description 2
- AIYUHDOJVYHVIT-UHFFFAOYSA-M caesium chloride Chemical compound [Cl-].[Cs+] AIYUHDOJVYHVIT-UHFFFAOYSA-M 0.000 description 2
- 244000309466 calf Species 0.000 description 2
- 238000007675 cardiac surgery Methods 0.000 description 2
- 238000004587 chromatography analysis Methods 0.000 description 2
- 238000004140 cleaning Methods 0.000 description 2
- 108091036078 conserved sequence Proteins 0.000 description 2
- 230000006378 damage Effects 0.000 description 2
- 230000009977 dual effect Effects 0.000 description 2
- 238000002592 echocardiography Methods 0.000 description 2
- 229920001971 elastomer Polymers 0.000 description 2
- 238000005516 engineering process Methods 0.000 description 2
- 238000012637 gene transfection Methods 0.000 description 2
- 238000007490 hematoxylin and eosin (H&E) staining Methods 0.000 description 2
- 229960002897 heparin Drugs 0.000 description 2
- 229920000669 heparin Polymers 0.000 description 2
- 238000013115 immunohistochemical detection Methods 0.000 description 2
- 230000002055 immunohistochemical effect Effects 0.000 description 2
- 238000011534 incubation Methods 0.000 description 2
- 229910052742 iron Inorganic materials 0.000 description 2
- 210000005240 left ventricle Anatomy 0.000 description 2
- 238000012417 linear regression Methods 0.000 description 2
- 239000002502 liposome Substances 0.000 description 2
- 230000003387 muscular Effects 0.000 description 2
- 238000001543 one-way ANOVA Methods 0.000 description 2
- 238000004806 packaging method and process Methods 0.000 description 2
- 210000003516 pericardium Anatomy 0.000 description 2
- 229920000728 polyester Polymers 0.000 description 2
- 239000002243 precursor Substances 0.000 description 2
- 230000001023 pro-angiogenic effect Effects 0.000 description 2
- 230000008569 process Effects 0.000 description 2
- 238000000746 purification Methods 0.000 description 2
- 230000002285 radioactive effect Effects 0.000 description 2
- 230000002829 reductive effect Effects 0.000 description 2
- 238000011160 research Methods 0.000 description 2
- 210000002966 serum Anatomy 0.000 description 2
- 239000011734 sodium Substances 0.000 description 2
- 210000001562 sternum Anatomy 0.000 description 2
- 239000006228 supernatant Substances 0.000 description 2
- 230000002195 synergetic effect Effects 0.000 description 2
- 230000009466 transformation Effects 0.000 description 2
- 239000012588 trypsin Substances 0.000 description 2
- 238000002604 ultrasonography Methods 0.000 description 2
- 229940124549 vasodilator Drugs 0.000 description 2
- 239000003071 vasodilator agent Substances 0.000 description 2
- 238000005303 weighing Methods 0.000 description 2
- 238000001262 western blot Methods 0.000 description 2
- 206010067484 Adverse reaction Diseases 0.000 description 1
- 229920001817 Agar Polymers 0.000 description 1
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 description 1
- 102000009840 Angiopoietins Human genes 0.000 description 1
- 108010009906 Angiopoietins Proteins 0.000 description 1
- UXVMQQNJUSDDNG-UHFFFAOYSA-L Calcium chloride Chemical compound [Cl-].[Cl-].[Ca+2] UXVMQQNJUSDDNG-UHFFFAOYSA-L 0.000 description 1
- 208000003322 Coinfection Diseases 0.000 description 1
- 206010069729 Collateral circulation Diseases 0.000 description 1
- -1 DL2000marker Proteins 0.000 description 1
- 208000012661 Dyskinesia Diseases 0.000 description 1
- 102000002322 Egg Proteins Human genes 0.000 description 1
- 108010000912 Egg Proteins Proteins 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 240000001624 Espostoa lanata Species 0.000 description 1
- 235000009161 Espostoa lanata Nutrition 0.000 description 1
- 230000005526 G1 to G0 transition Effects 0.000 description 1
- 206010061216 Infarction Diseases 0.000 description 1
- 102100034343 Integrase Human genes 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- 241000713869 Moloney murine leukemia virus Species 0.000 description 1
- 206010028851 Necrosis Diseases 0.000 description 1
- 206010030113 Oedema Diseases 0.000 description 1
- 238000012408 PCR amplification Methods 0.000 description 1
- 229930182555 Penicillin Natural products 0.000 description 1
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 1
- 238000002123 RNA extraction Methods 0.000 description 1
- 108010092799 RNA-directed DNA polymerase Proteins 0.000 description 1
- 229920005654 Sephadex Polymers 0.000 description 1
- 239000012507 Sephadex™ Substances 0.000 description 1
- 108010006785 Taq Polymerase Proteins 0.000 description 1
- 208000032594 Vascular Remodeling Diseases 0.000 description 1
- 208000024248 Vascular System injury Diseases 0.000 description 1
- 208000012339 Vascular injury Diseases 0.000 description 1
- 208000027418 Wounds and injury Diseases 0.000 description 1
- 230000001464 adherent effect Effects 0.000 description 1
- 230000006838 adverse reaction Effects 0.000 description 1
- 239000008272 agar Substances 0.000 description 1
- FRHBOQMZUOWXQL-UHFFFAOYSA-L ammonium ferric citrate Chemical compound [NH4+].[Fe+3].[O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O FRHBOQMZUOWXQL-UHFFFAOYSA-L 0.000 description 1
- 235000011114 ammonium hydroxide Nutrition 0.000 description 1
- 230000003698 anagen phase Effects 0.000 description 1
- 238000000540 analysis of variance Methods 0.000 description 1
- 230000002491 angiogenic effect Effects 0.000 description 1
- 230000010100 anticoagulation Effects 0.000 description 1
- 210000001367 artery Anatomy 0.000 description 1
- BWKOZPVPARTQIV-UHFFFAOYSA-N azanium;hydron;2-hydroxypropane-1,2,3-tricarboxylate Chemical compound [NH4+].OC(=O)CC(O)(C(O)=O)CC([O-])=O BWKOZPVPARTQIV-UHFFFAOYSA-N 0.000 description 1
- 238000010009 beating Methods 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 230000008827 biological function Effects 0.000 description 1
- 210000004556 brain Anatomy 0.000 description 1
- 239000001110 calcium chloride Substances 0.000 description 1
- 229910001628 calcium chloride Inorganic materials 0.000 description 1
- 229940041514 candida albicans extract Drugs 0.000 description 1
- 230000000747 cardiac effect Effects 0.000 description 1
- 210000001715 carotid artery Anatomy 0.000 description 1
- 230000010261 cell growth Effects 0.000 description 1
- 239000006285 cell suspension Substances 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 210000000038 chest Anatomy 0.000 description 1
- 238000002648 combination therapy Methods 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 230000001447 compensatory effect Effects 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 210000004351 coronary vessel Anatomy 0.000 description 1
- 239000006059 cover glass Substances 0.000 description 1
- 238000012258 culturing Methods 0.000 description 1
- 238000005520 cutting process Methods 0.000 description 1
- 230000006866 deterioration Effects 0.000 description 1
- 230000003205 diastolic effect Effects 0.000 description 1
- 210000003278 egg shell Anatomy 0.000 description 1
- 238000010828 elution Methods 0.000 description 1
- 210000003989 endothelium vascular Anatomy 0.000 description 1
- 210000003743 erythrocyte Anatomy 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 239000000284 extract Substances 0.000 description 1
- 238000000556 factor analysis Methods 0.000 description 1
- 229960000301 factor viii Drugs 0.000 description 1
- 239000000834 fixative Substances 0.000 description 1
- 239000008098 formaldehyde solution Substances 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 238000003306 harvesting Methods 0.000 description 1
- 201000011066 hemangioma Diseases 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 230000001939 inductive effect Effects 0.000 description 1
- 230000007574 infarction Effects 0.000 description 1
- 230000000977 initiatory effect Effects 0.000 description 1
- 208000014674 injury Diseases 0.000 description 1
- 210000000994 inner shell membrane Anatomy 0.000 description 1
- 238000003780 insertion Methods 0.000 description 1
- 230000037431 insertion Effects 0.000 description 1
- 230000003601 intercostal effect Effects 0.000 description 1
- 210000000936 intestine Anatomy 0.000 description 1
- 238000010255 intramuscular injection Methods 0.000 description 1
- 239000007927 intramuscular injection Substances 0.000 description 1
- 238000006192 iodination reaction Methods 0.000 description 1
- 239000004313 iron ammonium citrate Substances 0.000 description 1
- 208000028867 ischemia Diseases 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 229930027917 kanamycin Natural products 0.000 description 1
- SBUJHOSQTJFQJX-NOAMYHISSA-N kanamycin Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CN)O[C@@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](N)[C@H](O)[C@@H](CO)O2)O)[C@H](N)C[C@@H]1N SBUJHOSQTJFQJX-NOAMYHISSA-N 0.000 description 1
- 229960000318 kanamycin Drugs 0.000 description 1
- 229930182823 kanamycin A Natural products 0.000 description 1
- 230000033001 locomotion Effects 0.000 description 1
- 210000003141 lower extremity Anatomy 0.000 description 1
- 210000004072 lung Anatomy 0.000 description 1
- 238000012423 maintenance Methods 0.000 description 1
- 210000001161 mammalian embryo Anatomy 0.000 description 1
- 230000035800 maturation Effects 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 239000002609 medium Substances 0.000 description 1
- 238000000386 microscopy Methods 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 230000017074 necrotic cell death Effects 0.000 description 1
- 239000013642 negative control Substances 0.000 description 1
- 238000011587 new zealand white rabbit Methods 0.000 description 1
- 238000011022 operating instruction Methods 0.000 description 1
- 210000003540 papillary muscle Anatomy 0.000 description 1
- 239000012188 paraffin wax Substances 0.000 description 1
- 230000036961 partial effect Effects 0.000 description 1
- 229940049954 penicillin Drugs 0.000 description 1
- 229960001412 pentobarbital Drugs 0.000 description 1
- WEXRUCMBJFQVBZ-UHFFFAOYSA-N pentobarbital Chemical compound CCCC(C)C1(CC)C(=O)NC(=O)NC1=O WEXRUCMBJFQVBZ-UHFFFAOYSA-N 0.000 description 1
- 210000004224 pleura Anatomy 0.000 description 1
- 201000003144 pneumothorax Diseases 0.000 description 1
- 239000001103 potassium chloride Substances 0.000 description 1
- 235000011164 potassium chloride Nutrition 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 230000002062 proliferating effect Effects 0.000 description 1
- 230000035755 proliferation Effects 0.000 description 1
- 239000012474 protein marker Substances 0.000 description 1
- 239000012264 purified product Substances 0.000 description 1
- 238000011555 rabbit model Methods 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 230000006884 regulation of angiogenesis Effects 0.000 description 1
- 108091008146 restriction endonucleases Proteins 0.000 description 1
- 239000000523 sample Substances 0.000 description 1
- 239000012488 sample solution Substances 0.000 description 1
- 238000012764 semi-quantitative analysis Methods 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 210000002460 smooth muscle Anatomy 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 210000000952 spleen Anatomy 0.000 description 1
- 238000010186 staining Methods 0.000 description 1
- 239000012128 staining reagent Substances 0.000 description 1
- 230000003068 static effect Effects 0.000 description 1
- 238000000528 statistical test Methods 0.000 description 1
- 238000011476 stem cell transplantation Methods 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 230000001360 synchronised effect Effects 0.000 description 1
- 238000011287 therapeutic dose Methods 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 238000001890 transfection Methods 0.000 description 1
- 230000009261 transgenic effect Effects 0.000 description 1
- 239000012137 tryptone Substances 0.000 description 1
- 238000011144 upstream manufacturing Methods 0.000 description 1
- 230000006444 vascular growth Effects 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
- 239000012138 yeast extract Substances 0.000 description 1
Images
Landscapes
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Abstract
本发明公开了一种VEGF165和Ang-1双基因共表达载体,所述双基因共表达载体含有人基因VEGF165和人Ang-1基因,所述双基因共表达载体为pAdTrack-CMV-Ang-1-IRES-VEGF165;将上述双基因重组转移载体与腺病毒骨架质粒pAdEasy-1同源重组后,在QBI-293A细胞中包装和扩增获得Ad-Ang-1-IRES-VEGF165双基因共表达重组腺病毒,然后用携带VEGF和Ang-1的双基因重组腺病毒感染血管内皮祖细胞,可促进缺血心肌的血管新生和改善心功能。
Description
技术领域
本发明属于重组载体领域,具体涉及VEGF165和Ang-1双基因共表达载体制备促进血管新生药物中的应用。
背景技术
众所周知,在血管新生中,有诸多的细胞和化学因子参与调控。目前认为:VEGF(血管内皮生长因子)具有特异性促进内皮细胞增殖、诱发新生血管生长,继而形成侧支循环等生物学作用,在血管新生的起始与维持阶段均有作用;FGF(成纤维细胞生长因子)主要参与初期过程;而Ang-1(血管生成素)、IGF(胰岛素样生长因子)与PDGF(血小板衍生生长因子)主要影响血管的成熟与稳定。实验研究揭示:外源性VEGF基因治疗可能明显改善缺血心肌的灌注及功能,并取得了一定的疗效(参见:Losordo DW,Vale PR,Symes JF,et al.1998,98:2800-2804.)。但新近的一些实验陆续提示:单独应用VEGF时,即使使用的是治疗剂量,有可能导致局部组织的明显水肿(参见:Dor Y,DjionovV,Abramovitch R,et al.2002,21(8):1939-1947.)、缺血肢体的坏死(参见:Masaki L,Yonemitsu Y,Yamashita A,et al.2002,90(9):966-973.)、血管瘤形成和心功能恶化等(参见:Lee RJ,Springer ML,Blanco-Bose WE,et al.2000,102:898-901.)。因此,在有效发挥VEGF血管新生治疗作用的同时,探讨如何避免和减少其不良反应的方案,是迫切需要解决的临床问题,基因的联合治疗可能是解决办法之一。
近年来,基因联合治疗心肌缺血成为研究的热点之一,有研究用VEGF和Ang-1两种基因分别在缺血局部注射,心肌梗塞的面积缩小,提示这两种基因治疗协同作用,鉴于类似的研究均是两次或分别进行基因转染,多是应用在缺血组织的局部,如缺血下肢或心肌(参见:Jho D,Mehta D,Ahmmed G,etal.2006,96(12):1282-1290;Shyu KG,Chang H,Isner JM.Life Sciences,2003,73(20):563-579.)。既往的联合基因治疗均是两个载体分别携带两个基因,先后或同时给予,在转基因治疗时需要两次基因转染,而且两个基因分别给予时剂量难以协调计算和基因转移效率低等缺点。尚未见到:由同一个腺病毒载体携带两种促进血管生成的基因,并共同在血管内皮祖细胞(EPCs)中表达,联合基因结合干细胞移植治疗缺血心肌,促进缺血区血管新生和改善心功能的报道。
发明内容
本发明目的是提供一种VEGF165和Ang-1双基因共表达载体。
为达到上述目的,本发明采用的技术方案是:一种VEGF165和Ang-1双基因共表达载体,所述双基因共表达载体含有人基因VEGF165和人Ang-1基因,所述双基因共表达质粒为pAdTrack-CMV-Ang-1-IRES-VEGF165。
进一步的技术方案中,将上述pAdTrack-CMV-Ang-1-IRES-VEGF165双基因重组转移质粒与腺病毒骨架质粒pAdEasy-1同源重组后,在QBI-293A细胞中包装和扩增获得Ad-Ang-1-IRES-VEGF165双基因共表达重组腺病毒,以便用携带VEGF和Ang-1的双基因重组腺病毒感染血管内皮祖细胞(EPCs),促进缺血心肌的血管新生和改善心功能。
因此,本发明要求保护pAdTrack-CMV-Ang-1-IRES-VEGF165双基因重组转移载体在制备促进缺血心肌的血管新生药物中的应用。
同时,本发明要求保护Ad-Ang-1-IRES-VEGF165双基因共表达重组腺病毒在制备促进缺血心肌的血管新生药物中的应用。
采用常规技术将上述pAdTrack-CMV-Ang-1-IRES-VEGF165双基因重组转移质粒导入宿主菌大肠杆菌中,然后进行保藏,该大肠杆菌的保藏信息为:保藏单位:中国典型培养物保藏中心;地址:中国武汉大学;保藏日期:2010年5月16日;保藏编号CCTCC NO:M 2010117;分类命名:大肠杆菌DH5α/pAdTrack-CMV-hAng-1-IRES-hVEGF165;Escherichia coli DH5α/pAdTrack-CMV-hAng-1-IRES-hVEGF165。
上述pAdTrack-CMV-Ang-1-IRES-VEGF165双基因重组转移载体的制备方法包括以下步骤:
(1)根据GenBank报道的IRES(内部核糖体插入位点)保守序列,设计引物P1、P2,以含有IRES片段的pGEZ-Term质粒为模板PCR扩增IRES目的基因片段,亚克隆至pAdTrack-CMV转移质粒构建pAdTrack-CMV-IRES双基因共表达转移空质粒,并经PCR、双酶切和DNA测序鉴定;
(2)根据GenBank报道的人VEGF165基因序列,设计引物P3、P4,以含有人VEGF165基因片段的pSV-K3-VEGF165质粒为模板PCR扩增人VEGF165目的基因片段,亚克隆至pAdTrack-CMV-IRES 构建pAdTrack-CMV-IRES-VEGF165单基因重组转移质粒,并经PCR、双酶切和DNA测序鉴定;
(3)根据GenBank报道的人Ang-1基因序列,设计引物P5、P6,以人骨髓细胞总RNA逆转录合成的cDNA为模板PCR(RT-PCR)扩增人Ang-1目的基因片段,分别亚克隆至pAdTrack-CMV-IRES和pAdTrack-CMV-IRES-VEGF165构建pAdTrack-CMV-Ang-1-IRES单基因重组转移质粒和pAdTrack-CMV-Ang-1-IRES-VEGF165双基因重组转移质粒并经PCR、双酶切和DNA测序鉴定。
进一步的技术方案中,将上述构建正确的pAdTrack-CMV-IRES空质粒、pAdTrack-CMV-IRES-VEGF165和pAdTrack-CMV-Ang-1-IRES单基因重组转移质粒及pAdTrack-CMV-Ang-1-IRES-VEGF165双基因重组转移质粒经Pme I酶切后分别与pAdEasy-1腺病毒骨架质粒在BJ5183大肠杆菌中同源重组,得到的重组腺病毒质粒pAdEasy-1-pAdTrack-CMV-IRES(pAd-IRES)、pAdEasy-1-pAdTrack-CMV-IRES-VEGF165(pAd-IRES-VEGF165)、pAdEasy-1-pAdTrack-CMV-Ang-1-IRES(pAd-Ang-1-IRES)和pAdEasy-1-pAdTrack-CMV-Ang-1-IRES-VEGF165(pAd-Ang-1-IRES-VEGF165)经Pac I酶切后再用脂质体分别转染QBI-293A细胞,经多轮感染和扩增后获得Ad-IRES空载体腺病毒、Ad-IRES-VEGF165单基因重组腺病毒、Ad-Ang-1-IRES单基因重组腺病毒和Ad-Ang-1-IRES-VEGF165双基因重组腺病毒,并利用RT-PCR和Western blot检测腺病毒为载体介导的外源性VEGF165和Ang-1基因在QBI-293A细胞中的转录和表达。
结果发现:分别以pGEZ-Term质粒、pSV-K3-VEGF165质粒和人骨髓细胞总RNA逆转录合成的cDNA为模板PCR均能扩增出581bp的IRES、576bp的人VEGF165和1497bp的人Ang-1目的基因片段,亚克隆的IRES、VEGF165和Ang-1基因片段其序列测定结果与GenBank报道的完全一致,成功构建了pAdTrack-CMV-IRES空质粒、pAdTrack-CMV-IRES-VEGF165单基因重组质粒、pAdTrack-CMV-Ang-1-IRES单基因重组质粒和pAdTrack-CMV-Ang-1-IRES-VEGF165双基因重组质粒,并成功获得了Ad-IRES空载体腺病毒、Ad-IRES-VEGF165单基因重组腺病毒、Ad-Ang-1-IRES单基因重组腺病毒和Ad-Ang-1-IRES-VEGF165双基因重组腺病毒;RT-PCR和Western blot证实Ad-IRES-VEGF165、Ad-Ang-1-IRES和Ad-Ang-1-IRES-VEGF165重组腺病毒介导的外源性VEGF165和Ang-1基因在QBI-293A细胞中能成功转录和表达。
由于血管内皮祖细胞(endothelial proganitor cells,EPCs)是一种骨髓和外周血存在的内皮细胞前体细胞,有高度增殖潜能,能以血管生成-即胚胎期的血管形成方式、参与人体缺血部位的代偿性血管重建。在血管损伤和组织缺血时,动员骨髓中的EPCs向外周血中释放并向缺血区趋化,鉴于EPCs本身的促进血管新生和趋化的功能,因此选用EPCs作为基因治疗的载体细胞是十分合理和有效的。
因此,进一步的技术方案中,在血管内皮祖细胞(EPCs)分离培养和Ad-Ang-1-IRES-VEGF165双基因重组腺病毒构建的基础上,将Ad-Ang-1-IRES-VEGF165体外感染EPCs细胞,以制备腺病毒为载体介导的VEGF165和Ang-1促血管生长因子双基因修饰的EPCs;感染结果表明,VEGF165和Ang-1重组腺病毒能高效感染EPCs细胞,其感染效率可达90%以上;间接免疫荧光和ELISA检测结果进一步证实腺病毒介导的外源性VEGF165和Ang-1基因能在EPCs细胞中共表达。
进一步的研究发现,经过VEGF165和Ang-1双基因修饰的血管内皮祖细胞,经过导管递送后,能显著促进外源性基因在体内的表达和新生血管形成,改善左心室收缩功能,减轻心室扩大,效果优于单基因修饰的血管祖细胞。
由于上述技术方案运用,本发明与现有技术相比具有下列优点:
1、本发明所述用IRES构建的VEGF165和Ang-1双基因共表达的腺病毒载体和用Ad-Ang-1-IRES-VEGF165修饰的血管内皮祖细胞(EPCs)可以作为治疗心肌缺血的药物。
2、本发明用Ad-Ang-1-IRES-VEGF165双基因修饰血管内皮祖细胞治疗心肌缺血的治疗方案,利用了EPCs向心肌缺血区趋化的特性,进行基因治疗,有效地避免造成非缺血区的血管新生等副作用。
附图说明
大肠杆菌的保藏信息为:保藏单位:中国典型培养物保藏中心;地址:中国武汉大学;保藏日期:2010年5月16日;保藏编号CCTCC NO:M 2010117;分类命名:大肠杆菌DH5α/pAdTrack-CMV-hAng-1-IRES-hVEGF165;Escherichia coli DH5α/pAdTrack-CMV-hAng-1-IRES-hVEGF165。
图1是实施例一中IRES介导的VEGF165和Ang-1双基因腺病毒共表达模式图;
图2是实施例一中pAdTrack-CMV-IRES改造空转移质粒的构建和鉴定图,其中,(A)PCR获得IRES片段:1.pGEZ-Term质粒为模板的IRES PCR产物;M.DL2000marker;(B)pAdTrack-CMV-IRES质粒PCR鉴定:1.pAdTrack-CMV-IRES质粒为模板的IRES PCR产物;M.DL2000marker;(C)pAdTrack-CMV-IRES质粒双酶切鉴定:1.pAdTrack-CMV-IRES质粒SalI、Not I双酶切;M.DL2000marker;
图3是实施例一中pAdTrack-CMV-IRES-VEGF165单基因重组转移质粒的构建和鉴定图,其中,(A)PCR获得VEGF165片段:1.pSV-K3-VEGF165质粒为模板的VEGF165 PCR产物;M.DL2000 marker;(B)pAdTrack-CMV-IRES-VEGF165质粒PCR鉴定:1.pAdTrack-CMV-IRES-VEGF165质粒为模板的VEGF165PCR产物;M.DL2000marker;(C)pAdTrack-CMV-IRES-VEGF165质粒Xho I、EcoR V双酶切鉴定:1.pAdTrack-CMV-IRES-VEGF165质粒Xho I、EcoR V双酶切;M.DL2000marker;(D)pAdTrack-CMV-IRES-VEGF165质粒Sal I、EcoR V双酶切鉴定:1.pAdTrack-CMV-IRES-VEGF165质粒SalI、EcoR V双酶切;M.DL2000marker;
图4是实施例一中pAdTrack-CMV-Ang-1-IRES单基因重组转移质粒的构建和鉴定图,其中,(A)RT-PCR获得Ang-1片段:1.骨髓细胞总RNA为模板的Ang-1RT-PCR产物;M.DL2000marker;(B)pAdTrack-CMV-Ang-1-IRES质粒PCR鉴定:1.pAdTrack-CMV-Ang-1-IRES质粒为模板的Ang-1PCR产物;M.DL2000marker;(C)pAdTrack-CMV-Ang-1-IRES质粒双酶切鉴定:1.pAdTrack-CMV-Ang-1-IRES质粒Bgl II、Sal I双酶切;M.DL2000marker;(D)pAdTrack-CMV-Ang-1-IRES质粒双酶切鉴定:1.pAdTrack-CMV-Ang-1-IRES质粒Bgl II、Not I双酶切;M.DL2000 marker;
图5是实施例一中pAdTrack-CMV-Ang-1-IRES-VEGF165双基因重组转移质粒的构建和鉴定图,其中,(A)RT-PCR获得Ang-1片段:1.骨髓细胞总RNA为模板的Ang-1RT-PCR产物;M.DL2000 marker;(B)pAdTrack-CMV-Ang-1-IRES-VEGF165质粒PCR鉴定:1.pAdTrack-CMV-Ang-1-IRES质粒为模板的Ang-1PCR产物;M.DL2000marker;(C)pAdTrack-CMV-Ang-1-IRES-VEGF165质粒双酶切鉴定:1.pAdTrack-CMV-Ang-1-IRES-VEGF165质粒Bgl II、SalI双酶切;M.DL2000marker;(D)pAdTrack-CMV-Ang-1-IRES-VEGF165质粒双酶切鉴定:1.pAdTrack-CMV-Ang-1-IRES-VEGF165质粒Bgl II、EcoR V双酶切;M.DL2000marker;
图6是实施例一中同源重组克隆质粒(BJ5183)琼脂糖电泳分子量大小鉴定图,其中,(A)pAd-IRES同源重组克隆质粒(BJ5183)分子量大小鉴定:1.pAdEasy-1;2.pAdTrack-CMV-IRES;3~8.为所挑的6个克隆,其中3,7,8为同源重组克隆;4,5,6为非同源重组克隆;(B)pAd-IRES-VEGF165同源重组克隆质粒(BJ5183)分子量大小鉴定:1.pAdEasy-1;2.pAdTrack-CMV-IRES-VEGF165;3~8.为所挑的6个克隆,其中3,4,6,7为同源重组克隆;5,8为非同源重组克隆;(C)pAd-Ang-1-IRES同源重组克隆质粒(BJ5183)分子量大小鉴定:1.pAdEasy-1;2.pAdTrack-CMV-Ang-1-IRES;3~8.为所挑的6个克隆,其中3,4,5,6,7,8均为同源重组克隆;(D)pAd-Ang-1-IRES-VEGF165同源重组克隆质粒(BJ5183)分子量大小鉴定:1.pAdEasy-1;2.pAdTrack-CMV-Ang-1-IRES-VEGF165;3~8.为所挑的6个克隆,其中3,4,5,6,7为同源重组克隆;8为非同源重组克隆;
图7是实施例一中同源重组克隆质粒(DH5α)琼脂糖电泳分子量大小鉴定图,其中,(A)pAd-IRES同源重组克隆质粒(DH5α)分子量大小鉴定:1.pAdEasy-1;2.pAdTrack-CMV-IRES;3~5.分别为图7(A)中的3个同源重组克隆;(B)pAd-IRES-VEGF165同源重组克隆质粒(DH5α)分子量大小鉴定:1.pAdEasy-1;2.pAdTrack-CMV-IRES-VEGF165;3~6.分别为图7(B)中的4个同源重组克隆;(C)pAd-Ang-1-IRES同源重组克隆质粒(DH5α)分子量大小鉴定:1.pAdEasy-1;2.pAdTrack-CMV-Ang-1-IRES;3~8.分别为图7(C)中的6个同源重组克隆;(D)pAd-Ang-1-IRES-VEGF165同源重组克隆质粒(DH5α)分子量大小鉴定:1.pAdEasy-1;2.pAdTrack-CMV-Ang-1-IRES-VEGF165;3~7.分别为图7(D)中的5个同源重组克隆;
图8是实施例一中同源重组质粒PCR鉴定图,其中,1.pAd-IRES为模板,P1,P2为引物IRES PCR阳性产物;2.pAd-IRES为模板,P3,P4为引物VEGF165PCR产物为阴性;3.pAd-IRES为模板,P5,P6为引物Ang-1PCR产物为阴性;4.pAd-IRES-VEGF165为模板,P1,P2为引物IRES PCR阳性产物;5.pAd-IRES-VEGF165为模板,P3,P4为引物VEGF165PCR阳性产物;6.pAd-IRES-VEGF165为模板,P5,P6为引物Ang-1PCR产物为阴性;7.pAd-Ang-1-IRES为模板,P1,P2为引物IRES PCR阳性产物;8.pAd-Ang-1-IRES为模板,P3,P4为引物VEGF165PCR产物为阴性;9.pAd-Ang-1-IRES为模板,P5,P6为引物Ang-1PCR阳性产物;10.pAd-Ang-1-IRES-VEGF165为模板,P1,P2为引物IRES PCR阳性产物;11.pAd-Ang-1-IRES-VEGF165为模板,P3,P4为引物VEGF165PCR阳性产物;12.pAd-Ang-1-IRES-VEGF165为模板,P5,P6为引物Ang-1PCR阳性产物;M.DL2000marker;
图9是实施例一中同源重组质粒PacI酶切鉴定图,其中,(A)pAd-IRES质粒PacI酶切鉴定:1.pAd-IRES PacI酶切;M.λ-Hind III digest DNAmarker;(B)pAd-IRES-VEGF165质粒PacI酶切鉴定:1.pAd-IRES-VEGF165PacI 酶切;M.λ-Hind III digest DNA marker;(C)pAd-Ang-1-IRES质粒PacI酶切鉴定:1.pAd-Ang-1-IRES PacI酶切;M.λ-Hind III digest DNA marker;(D)pAd-Ang-1-IRES-VEGF165质粒PacI酶切鉴定:1.pAd-Ang-1-IRES-VEGF165PacI 酶切;M.λ-Hind III digest DNA marker;
图10是实施例一中各组重组腺病毒感染QBI-293A细胞光镜和荧光照片,其中,A.QBI-293A;B.QBI-293A+Ad-IRES;C.QBI-293A+Ad-IRES-VEGF165;D.QBI-293A+Ad-Ang-1-IRES;E.QBI-293A+Ad-Ang-1-IRES-VEGF165;
图11是实施例一中VEGF165和Ang-1基因在QBI-293A细胞中的转录鉴定(RT-PCR)图,其中,图A 1.QBI-293A,P3,P4为引物;2.QBI-293A,P1,P2为引物IRES RT-PCR产物为阴性;3.QBI-293A,P5,P6为引物;M.DL2000marker;图B 1.QBI-293A+Ad-IRES,P1,P2为引物;2.QBI-293A+Ad-IRES,P3,P4为引物;3.QBI-293A+Ad-IRES,P5,P6为引物;M.DL2000marker;图C 1.QBI-293A+Ad-IRES-VEGF165,P1,P2为引物;2.QBI-293A+Ad-IRES-VEGF165,P3,P4为引物;3.QBI-293A+Ad-IRES-VEGF165,P5,P6为引物;M.DL2000marker;图D.1.QBI-293A+Ad-Ang-1-IRES,P1,P2为引物;2.QBI-293A+Ad-Ang-1-IRES,P3,P4为引物;3.QBI-293A+Ad-Ang-1-IRES,P5,P6为引物;M.DL2000marker;图E.1.QBI-293A+Ad-Ang-1-IRES-VEGF165,P1,P2为引物IRESRT-PCR产物;2.QBI-293A+Ad-Ang-1-IRES-VEGF165,P3,P4为引物VEGF165RT-PCR产物;3.QBI-293A+Ad-Ang-1-IRES-VEGF165,P5,P6为引物Ang-1RT-PCR产物;M.DL2000marker;
图12是实施例一中ELISA法检测Ad-Ang-1/VEGF165在293A细胞培养上清中VEGF165和Ang-1蛋白的表达水平图;
图13是实施例二中VEGF165和Ang-1重组腺病毒促CAM血管形成活性检测图;
图14是实施例二中各组重组腺病毒感染EPCs细胞光镜和荧光照片,其中,A.EPCs;B.EPCs+Ad-IRES;C.EPCs+Ad-IRES-VEGF165;D.EPCs+Ad-Ang-1-IRES;E.EPCs+Ad-Ang-1-IRES-VEGF165;
图15是实施例二中VEGF165ELISA标准曲线;
图16是实施例二中Ang-1ELISA标准曲线;
图17是实施例三中125I-Tf(Fe)2标记的EPCs在心肌梗塞兔活体内分布的动态观察图;
图18是实施例三中EPCs注射24小时后在各脏器内的分布图,其中,1.血液;2.脑;3.肺;4.心;5.肝脏;6.脾脏;7.肾脏;8.肠;9.肌肉;10.甲状腺;
图19是实施例三中RT-PCR鉴定外源性VEGF165和Ang-1基因在兔缺血心肌中的转录,其中,1.未治疗组,P1,P2为引物IRES RT-PCR产物为阴性;2.未治疗组,P3,P4为引物VEGF165RT-PCR产物为阴性;3.未治疗组,P5,P6为引物Ang-1RT-PCR产物为阴性;4.EPCs治疗组,P1,P2为引物IRES RT-PCR产物为阴性;5.EPCs治疗组,P3,P4为引物VEGF165RT-PCR产物为阴性;6.EPCs治疗组,P5,P6为引物Ang-1RT-PCR产物为阴性;7.EPCs+Ad-IRES治疗组,P1,P2为引物IRES RT-PCR产物;8.EPCs+Ad-IRES治疗组,P3,P4为引物VEGF165RT-PCR产物为阴性;9.EPCs+Ad-IRES,P5,P6为引物Ang-1RT-PCR产物为阴性;10.EPCs+Ad-IRES-VEGF165治疗组,P1,P2为引物IRES RT-PCR产物;11.EPCs+Ad-IRES-VEGF165治疗组,P3,P4为引物VEGF165RT-PCR产物;12.EPCs+Ad-IRES-VEGF165治疗组,P5,P6为引物Ang-1RT-PCR产物为阴性;13.EPCs+Ad-Ang-1-IRES治疗组,P1,P2为引物IRES RT-PCR产物;14.EPCs+Ad-Ang-1-IRES治疗组,P3,P4为引物VEGF165RT-PCR产物为阴性;15.EPCs+Ad-Ang-1-IRES治疗组,P5,P6为引物Ang-1RT-PCR 产物;16.EPCs+Ad-Ang-1-IRES-VEGF165治疗组,P1,P2为引物IRES RT-PCR产物;17.EPCs+Ad-Ang-1-IRES-VEGF165治疗组,P3,P4为引物VEGF165RT-PCR产物;18.EPCs+Ad-Ang-1-IRES-VEGF165治疗组,P5,P6为引物Ang-1RT-PCR产物;M.DL2000marker;
图20是实施例三中vWF因子的免疫组织化学染色照片;
图21是实施例三中α-actin的免疫组织化学染色照片。
具体实施方式
下面结合附图及实施例对本发明作进一步描述:
实施例一:VEGF165和Ang-1双基因重组载体的构建和鉴定,采用IRES介导的VEGF165和Ang-1双基因腺病毒共表达模式,示意图如图1所示。
(1)材料
Bgl II、Sal I、Not I、Xho I和EcoR V限制性内切酶、T4DNA连接酶、DL2000marker、Taq DNA聚合酶、dNTPmix、Oligo d(T)18购自TaKaRa公司;逆转录酶MMLV、λ-Hind III digest DNA marker和低分子量蛋白marker购自MBI公司;日常型小量质粒抽提试剂盒、PCR产物清洁试剂盒、DNA胶回收试剂盒均购自杭州维特洁生化技术有限公司;pGEZ-Term质粒、pSV-K3-VEGF165质粒、大肠杆菌DH5α由苏州大学医学院细胞与分子生物学教研室杨吉成教授惠赠;GFP标记的pAdTrack-CMV转移质粒、腺病毒骨架质粒pAdEasy-1、大肠杆菌BJ5183、腺病毒包装细胞QBI-293A由复旦大学生命科学学院微生物学教研室钟江教授惠赠;RPMI1640购自GIBCO公司;小牛血清购自杭州四季青公司;24孔和6孔细胞培养购自CORNING公司;人VEGF165抗体[VEGF(A-20):sc-152-G]、人Ang-1抗体[Ang-1(C-19):sc-6320]和兔抗山羊IgG-AP二抗购自Santa Cruz公司;引物(如表1)、UNIQ-10柱式Trizol总RNA抽提试剂盒、酵母提取物、胰蛋白胨、琼脂粉等生化试剂购自上海生工生物技术有限公司。
表1 PCR扩增所用引物及其序列
(2)pAdTrack-CMV-IRES改造空转移质粒的构建
PCR获得IRES目的片段:比对IRES的保守序列,设计引物P1、P2(如表1),以含有IRES片段的pGEZ-Term质粒为模板PCR扩增IRES目的片段,两端分别引入Sal I、Not I酶切位点,获得的IRES PCR产物经琼脂糖电泳鉴定。结果表明:扩增出IRES目的基因片段大小与预期扩增的IRES理论值大小(581bp)相一致[图2(A)]。
IRES片段亚克隆于pAdTrack-CMV转移质粒:将DNA清洁试剂盒纯化的IRES PCR产物和日常型小量质粒抽提试剂盒提取的转移质粒pAdTrack-CMV分别用Sal I、Not I 37℃双酶切5h后,割胶回收目的片段,并用T4DNA连接酶将其4℃连接过夜,继而连接产物转化大肠杆菌DH5α和Kana(50μg/ml)筛选挑单克隆,并用PCR、双酶切鉴定和DNA序列测定,阳性克隆菌保种备用。结果表明:重组载体pAdTrack-CMV-IRES经PCR能扩增出约581bp大小的条带[图2(B)]和Sal I、Not I双酶切同样能释放出相同大小的片段[图2(C)],均表明IRES目的基因片段已成功亚克隆于pAdTrack-CMV转移质粒中。DNA序列测定进一步证实成功构建了pAdTrack-CMV-IRES改造空转移质粒。
(3)pAdTrack-CMV-IRES-VEGF165单基因重组转移质粒的构建
以含有VEGF165基因片段的pSV-K3-VEGF165质粒为模板PCR扩增VEGF165目的片段,两端分别引入Xho I、EcoR V酶切位点,获得的VEGF165PCR产物经琼脂糖电泳鉴定。结果表明:扩增出VEGF165目的基因片段,其大小与预期扩增的VEGF165理论值大小(576bp)相一致[图3(A)]。
将纯化的VEGF165PCR产物和日常型小量质粒抽提试剂盒抽提的改造转移质粒pAdTrack-CMV-IRES分别用Xho I、EcoRV 37℃双酶切5h后,割胶回收目的片段,并用T4DNA连接酶将其4℃连接过夜,继而连接产物转化大肠杆菌DH5α和Kana筛选挑单克隆,并用PCR、双酶切鉴定和DNA序列测定,阳性克隆菌保种备用。结果表明:重组载体pAdTrack-CMV-IRES-VEGF165经PCR能扩增出约576bp大小的条带[图3(B)];经Xho I、EcoR V双酶切同样能释放出576bp大小的片段[图3(C)];经Sal I、EcoR V双酶切能释放出1157bp大小的IRES+VEGF165片段[图3(D)],均表明VEGF165目的基因片段已成功亚克隆于pAdTrack-CMV-IRES改造空转移质粒中。DNA序列测定进一步证实成功构建了pAdTrack-CMV-IRES-VEGF165单基因重组转移质粒。
(4)pAdTrack-CMV-Ang-1-IRES单基因重组转移质粒的构建
Ang-1基因的克隆:根据GenBank(登陆号:NM-001146)报道的人Ang-1cDNA序列设计上下游引物P5、P6(如表1),以骨髓细胞总RNA逆转录合成的cDNA为模板PCR扩增Ang-1目的基因片段,两端分别引入Bgl II、Sal I酶切位点,获得的Ang-1RT-PCR产物经琼脂糖电泳鉴定。结果表明:扩增出Ang-1目的基因片段,其大小与预期扩增的Ang-1理论值大小相一致[图4(A)]。
将上述纯化的Ang-1RT-PCR产物和日常型小量质粒抽提试剂盒抽提的转移质粒pAdTrack-CMV-IRES分别用Bgl II、Sal I 37℃双酶切5h后,割胶回收目的片段,并用T4DNA连接酶将其4℃连接过夜,继而连接产物转化大肠杆菌DH5α和Kana筛选挑单克隆,并用PCR、双酶切鉴定和DNA序列测定,阳性克隆菌保种备用。结果表明:重组载体pAdTrack-CMV-Ang-1-IRES经PCR能扩增出约1497bp大小的条带[图4(B)];经Bgl II、Sal I双酶切同样能释放出1497bp大小的片段[图4(C)];经Bgl II、Not I双酶切能释放出2078bp大小的Ang-1+IRES片段[图4(D)],均表明Ang-1目的基因片段已成功亚克隆于pAdTrack-CMV-IRES改造空转移质粒中。DNA序列测定进一步证实成功构建了pAdTrack-CMV-Ang-1-IRES单基因重组转移质粒。
(5)pAdTrack-CMV-Ang-1-IRES-VEGF165双基因重组转移质粒的构建
在pAdTrack-CMV-IRES-VEGF165单基因重组转移质粒构建的基础上,将以反转录合成的骨髓细胞总RNA的cDNA为模板,P5、P6为引物RT-PCR扩增的Ang-1目的基因片段[图5(A)]进一步亚克隆于pAdTrack-CMV-IRES-VEGF165单基因重组转移质粒中构建pAdTrack-CMV-Ang-1-IRES-VEGF165双基因重组转移质粒。重组载体pAdTrack-CMV-Ang-1-IRES-VEGF165经PCR能扩增出约1497bp大小的条带[图5(B)];经Bgl II、SalI双酶切同样能释放出1497bp大小的片段[图5(C)];经B gl II、EcoR V双酶切能释放出2654bp 大小的Ang-1+IRES+VEGF165片段[图5(D)],均表明Ang-1目的基因片段已成功亚克隆于pAdTrack-CMV-IRES-VEGF165单基因重组转移质粒中。DNA序列测定进一步证实成功构建了pAdTrack-CMV-Ang-1-IRES-VEGF165双基因重组转移质粒。
(6)重组腺病毒质粒的构建
将上述构建的pAdTrack-CMV-IRES、pAdTrack-CMV-IRES-VEGF165、pAdTrack-CMV-Ang-1-IRES和pAdTrack-CMV-Ang-1-IRES-VEGF165重组转移质粒用Pme I 37℃单酶切2h线性化后,分别与pAdEasy-1腺病毒骨架质粒氯化钙法共转化BJ5183感受态细菌,Kana筛选挑单克隆抽提质粒,琼脂糖电泳根据分子量大小初步筛选pAdEasy-1-pAdTrack-CMV-IRES(简称为pAd-IRES)、pAdEasy-1-pAdTrack-CMV-IRES-VEGF165(简称为pAd-IRES-VEGF165)、pAdEasy-1-pAdTrack-CMV-Ang-1-IRES (简称为pAd-Ang-1-IRES)和pAdEasy-1-pAdTrack-CMV-Ang-1-IRES-VEGF165(简称为pAd-Ang-1-IRES-VEGF165)同源重组克隆,琼脂糖电泳(图6)结果表明,pAdTrack-CMV-IRES与pAdEasy-1共转化组所挑的6个克隆有3个为阳性克隆;pAdTrack-CMV-IRES-VEGF165与pAdEasy-1共转化组所挑的6个克隆有4个为阳性克隆;pAdTrack-CMV-Ang-1-IRES与pAdEasy-1共转化组所挑的6个克隆均为阳性克隆;pAdTrack-CMV-Ang-1-IRES-VEGF165与pAdEasy-1共转化组所挑的6个克隆有5个为阳性克隆。将上述各组同源重组阳性克隆分别转化DH5α后抽提质粒(图7),并选择某一初步确定的同源重组阳性克隆进行PCR鉴定(图8)均可见预期大小的PCR产物和PacI酶切鉴定(图9)均可获得30kb大小的腺病毒基因组片段和独特的4.5kb大小的ori及卡那霉素抗性编码基因片段。
(7)重组腺病毒的包装、扩增及其效价检测
将构建的pAd-IRES、pAd-IRES-VEGF165、pAd-Ang-1-IRES和pAd-Ang-1-IRES-VEGF165同源重组腺病毒质粒经Pac I线性化后胶回收大片段,按LipofectamineTM2000操作说明分别转染70%贴壁的QBI-293A细胞。Pac I线性化的pAd-IRES、pAd-IRES-VEGF165、pAd-Ang-1-IRES 和pAd-Ang-1-IRES-VEGF165同源重组质粒经Lipofectamin脂质体分别转染QBI-293A细胞后,荧光显微镜下可见GFP的表达,且荧光强度随培养时间延长逐渐增强。转染10d后分别收集Ad-IRES、Ad-IRES-VEGF165、Ad-Ang-1-IRES和Ad-Ang-1-IRES-VEGF165第一代病毒,再二次感染QBI-293A细胞,在倒置荧光显微镜下可观察到荧光,并出现CPE,结果表明Ad-IRES、Ad-IRES-VEGF165、Ad-Ang-1-IRES和Ad-Ang-1-IRES-VEGF165在QBI-293A细胞中包装成功。二次感染4-6d后,收集细胞,用PBS悬浮,反复冻融获得Ad-IRES、Ad-IRES-VEGF165、Ad-Ang-1-IRES 和Ad-Ang-1-IRES-VEGF165第三代重组病毒子粗提液,并经多轮感染、扩增和CsCl梯度离心纯化后,最终分别获得5×1010pfu/ml滴度的Ad-IRES病毒子、2×1010pfu/ml滴度的Ad-IRES-VEGF165病毒子、3×1010pfu/ml滴度的Ad-Ang-1-IRES病毒子和4×1010pfu/ml滴度的Ad-Ang-1-IRES-VEGF165病毒子于-80℃保存备用。Ad-IRES、Ad-IRES-VEGF165、Ad-Ang-1-IRES和Ad-Ang-1-IRES-VEGF165感染QBI-293A细胞光镜CPE和荧光照片如图10。
其中,重组腺病毒的效价检测的方法为:将对数生长期的QBI-293A细胞,胰酶消化后,调整细胞浓度为1×105个/ml,在96孔板上按每孔100μl接种细胞,培养24h后,将收获的Ad-Ang-1-IRES-VEGF165、Ad-Ang-1-IRES、Ad-IRES-VEGF165重组腺病毒和空载体Ad-IRES腺病毒作10-4、10-5、10-6、10-7稀释后,每个稀释度按每孔100μl接种3孔,37℃,5%CO2细胞培养箱里培养18h后,荧光显微镜下,进行荧光计数,按病毒效价(pfu/ml)=(每孔荧光平均数×10)/稀释度公式计算病毒效价。
(8)重组腺病毒的鉴定
RT-PCR鉴定:用10MOI的Ad-Ang-1-IRES-VEGF165、Ad-Ang-1-IRES、Ad-IRES-VEGF165重组腺病毒和空载体Ad-IRES腺病毒分别感染QBI-293A细胞48h后,1000r/min离心5min收集上述病毒感染细胞和未感染病毒的QBI-293A细胞对照,PBS洗涤2~3次,按UNIQ-10柱式Trizol总RNA抽提试剂盒说明书操作提取各组QBI-293A细胞总RNA,用上述引物P1、P2;P3、P4;P5、P6进行RT-PCR,分别鉴定IRES、VEGF165和Ang-1基因在QBI-293A细胞中的转录。总RNA提取和RT-PCR体系和条件同前。
结果见图11:Ad-Ang-1-IRES-VEGF165感染组可产生预期大小的581bpIRES、576bp VEGF165和1497Ang-1PCR产物;Ad-IRES-VEGF165感染组均可产生预期大小的581bp IRES和576bp VEGF165PCR产物,而相应位置未产生1497Ang-1PCR产物;Ad-Ang-1-IRES感染组可产生预期大小的581bpIRES和1497Ang-1PCR产物,而相应位置未产生576bp VEGF165PCR产物;Ad-IRES感染组可产生预期大小的581bp IRES PCR产物,而相应位置未产生576bp VEGF165和1497Ang-1PCR产物;QBI-293A未感染病毒的细胞对照组在相应位置均未产生上述条带。RT-PCR鉴定结果表明成功构建了Ad-Ang-1-IRES-VEGF165(双基因)、Ad-Ang-1-IRES(单基因)、Ad-IRES-VEGF165(单基因)、Ad-IRES(空载体)腺病毒。
ELISA法检测Ad-Ang-1/VEGF165在293A细胞中VEGF165和Ang-1蛋白的表达:用10MOI的Ad-Ang-1-IRES-VEGF165、Ad-Ang-1-IRES、Ad-IRES-VEGF165重组腺病毒和空载体Ad-IRES腺病毒分别感染QBI-293A细胞48h后,收集各组细胞培养上清,按照ELISA检测试剂盒分别测定上清中Ang-1和VEGF的含量。
结果见图12和表2,进一步表明IRES介导的VEGF165和Ang-1双基因腺病毒表达载体导入的外源VEGF165和Ang-1基因均能成功地表达。
表2 ELISA法检测Ad-Ang-1/VEGF165在293A细胞培养上清中VEGF165和Ang-1蛋白的表达水平(pg/ml)
| 实验组别 | Ang-1(pg/ml) | VEGF165(pg/ml) |
| 293A细胞对照 | 2490.86±550.95 | 6455.33±653.68 |
| Ad-IRES空白对照 | 2323.20±260.55 | 6074.51±629.58 |
| Ad-IRES-Ang1 | 47022.53±3685.57 | 6274.51±609.59 |
| Ad-IRES-VEGF165 | 38783.13±3449.95 | 10367.12±1401.22 |
| Ad-IRES-Ang1-VEGF | 72652.53±4286.02 | 9558.13±1221.21 |
实施例二:实施例一所得VEGF165和Ang-1双基因腺病毒载体体外感染外周血血管内皮祖细胞
(1)材料
8d鸡胚购自苏州市孵化场;平阳霉素(PYM)购自苏州大学附属第一医院;24孔和6孔细胞培养购自CORNING公司;RPMI1640购自GIBCO公司;小牛血清购自杭州四季青公司;人VEGF165抗体[VEGF(A-20):sc-152-G]、人Ang-1抗体[Ang-1(C-19):sc-6320]购自Santa Cruz公司;免疫荧光染色试剂盒-抗山羊Cy3购自碧云天生物技术研究所;人VEGF、Ang-1ELISA检测试剂盒购自晶美公司。
(2)VEGF165和Ang-1重组腺病毒的活性检测(CAM试验)
将孵育8d的生长状态良好的鸡胚随机分成6组:Ad-IRES空载体组、Ad-IRES-VEGF165单基因组、Ad-Ang-1-IRES单基因组、Ad-Ang-1-IRES-VEGF165双基因组、NS组和平阳霉素(PYM)组(作为阴性对照),每组6只鸡胚。将Ad-IRES空载体组、Ad-IRES-VEGF165单基因组、Ad-Ang-1-IRES单基因组和Ad-Ang-1-IRES-VEGF165双基因组4组腺病毒子用PBS稀释均调整为1×108个/ml的浓度;平阳霉素(PYM)用PBS配置,浓度为10mg/L。用碘酒棉球擦拭鸡胚的气室端蛋壳,并用无菌镊子扎一小孔和撕掉内壳膜,暴露CAM。将已灭菌的直径为5mm的滤纸小圆片浸泡上述各组50μl样品液后置于CAM表面的中央,加药完毕用透明胶带纸封贴。孵育3d后,撕开透明胶带纸,加入甲醛与丙酮(1∶1)的固定液固定10min,取下CAM,将其平铺于载玻片上,对血管进行分类,主干血管定为一级血管,主干血管的分支血管定为二级血管,二级血管以下的分支定为三级血管,计算滤纸周围5mm范围内的血管主干和各级分支,以检测腺病毒介导的VEGF165和Ang-1的促CAM血管形成活性。
结果参见图13和表3,可见:Ad-IRES-VEGF165组、Ad-Ang-1-IRES组和Ad-Ang-1-IRES-VEGF165组较NS组CAM血管生长更旺盛,毛细血管更丰富,呈弥漫状、放射状血管形成,而Ad-IRES空载体组与NS比较无差别;Ad-IRES-VEGF165和Ad-Ang-1-IRES两组单基因组比较,其促CAM血管形成活性Ad-Ang-1-IRES要优于Ad-IRES-VEGF165;Ad-Ang-1-IRES-VEGF165双基因组与Ad-IRES-VEGF165和Ad-Ang-1-IRES两组单基因组比较,其促CAM血管形成能力均强于Ad-Ang-1-IRES和Ad-IRES-VEGF165单基因组。结果表明所构建的VEGF165和Ang-1重组腺病毒具有明显的促CAM血管形成活性,且呈显著的协同效应。
表3 VEGF165和Ang-1的促CAM血管形成的比较(n=6)
| 组别 | 一级血管# | 二级血管$ | 三级血管& |
| NS | 3.50±0.60a | 15.80±2.86a | 62.00±9.65a |
| Ad-IRES 1) | 3.55±0.58a | 15.90±2.82a | 61.50±9.57a |
| Ad-IRES-VEGF 1652) | 3.70±0.61a | 22.30±3.12b | 78.30±11.53b |
| Ad-Ang-1-IRES3) | 3.85±0.57a | 27.80±4.10c | 86.20±12.36c |
| Ad-Ang-1-IRES-VEGF 1654) | 4.38±0.62b | 36.60±6.15d | 98.60±13.82d |
| PYM | 2.82±0.56c | 10.70±2.13e | 40.70±6.81e |
#F=9.132,P<0.001,q检验:表中组间a,b,c字母相同,两组间差异无统计学意义(P>0.05),表中字母不同,两组间差异有统计学意义(P<0.05)
$F=38.357,P<0.0001,q检验:表中组间a,b,c,d,e有字母相同,两组间差异无统计学意义(P>0.05)组间无字母相同,两组间差异有统计学意义(P<0.05)
&F=27.246,P<0.0001,q检验:表中组间a,b,c,d,e有字母相同,两组间差异无统计学意义(P>0.05),组间无字母相同,两组间差异有统计学意义(P<0.05)
(3)按照现有技术进行EPCs细胞的分离培养和鉴定,参见文献:吕海涛,杨向军,程铖,等.兔外周血源的血管内皮祖细胞体外扩增研究.苏州大学学报医学版,2007.(3):341-346)。
(4)实施例一所得VEGF165和Ang-1重组腺病毒体外感染EPCs细胞
0.25%胰酶消化原代分离培养的EPCs,1000r/min离心5min收获细胞,PBS清洗2次后用10%FBS的RPMI1640完全培养基悬浮,计数后调整细胞浓度为1×105/ml,每孔500μl接种于24孔培养板培养过夜。次日进行VEGF165和Ang-1重组腺病毒体外感染EPCs细胞,分为5组:分别为EPCs细胞对照组、EPCs+Ad-IRES空病毒对照组、EPCs+Ad-IRES-VEGF165单基因组、EPCs+Ad-Ang-1-IRES单基因组和EPCs+Ad-Ang-1-IRES-VEGF165双基因组,实验各设3个平行孔。VEGF165和Ang-1重组腺病毒体外感染EPCs细胞方法:弃去培养基,PBS轻柔洗涤每孔细胞2次,分别向上述5组细胞中加入PBS(100l)、Ad-IRES病毒液(100μl病毒稀释液,剂量相当50MOI)、Ad-IRES-VEGF165病毒液(100μl病毒稀释液,剂量相当50MOI),Ad-Ang-1-IRES病毒液(100μl病毒稀释液,剂量相当50MOI)和Ad-Ang-1-IRES-VEGF165病毒液(100μl病毒稀释液,剂量相当50MOI),轻轻摇匀,使病毒液与细胞充分接触。置5%CO2、37℃培养箱中培养,2h后补加900μl 10%FBS的RPMI1640完全培养基继续培养。48h后分别在普通光镜视野下观察EPCs细胞生长形态和荧光视野下观察GFP绿色荧光表达情况,以判断50MOI重组腺病毒剂量对EPCs细胞生长的影响和对EPCs细胞的感染效率。
结果表明:感染48h后,在荧光显微镜下普通光镜视野下观察各组重组腺病毒感染组EPCs细胞均形态正常,生长良好,与未感染腺病毒EPCs细胞对照组无差别;在荧光视野下,各组重组腺病毒感染组EPCs细胞几乎所有细胞可观察到绿色荧光(图14),结果表明50MOI剂量病毒感染EPCs细胞对细胞本身无毒性,而且呈很高的感染效率,其可达90%以上。
(5)外源性VEGF165和Ang-1基因在EPCs细胞中的表达鉴定
取普通洁净盖玻片于70%乙醇中浸泡5min或更长时间,用PBS或0.9%NaCl等溶液洗涤3遍后消毒烘干。将盖玻片在无菌条件下置于6孔板内,种入EPCs细胞培养过夜,使约为50%-80%满。次日进行VEGF165和Ang-1重组腺病毒体外感染EPCs细胞,实验分组和感染方法同步骤(4)。感染48h后收集各组重组腺病毒感染EPCs爬片细胞及其培养上清分别进行间接免疫荧光和ELISA检测腺病毒介导的外源性VEGF165和Ang-1基因在EPCS细胞中的表达。
(6)间接免疫荧光检测
腺病毒介导的外源性VEGF165和Ang-1基因在EPCs细胞中的表达利用免疫荧光染色试剂盒-抗山羊Cy3进行间接免疫荧光检测,方法按免疫荧光染色试剂盒-抗山羊Cy3说明书进行。
将Ad-IRES空载体腺病毒、Ad-IRES-VEGF165单基因重组腺病毒、Ad-Ang-1-IRES单基因重组腺病毒和Ad-Ang-1-IRES-VEGF165双基因重组腺病毒以50MOI剂量分别感染6孔板中爬片的EPCs细胞。感染48h后,收集EPCs爬片细胞,利用免疫荧光染色试剂盒-抗山羊Cy3进行间接免疫荧光检测分别检测腺病毒介导的外源性VEGF165和Ang-1基因在EPCs细胞中的表达。
结果显示,所有EPCs(未感染和感染组)分别检测VEGF165和Ang-1蛋白表达时都出现红色荧光,但检测VEGF165时,EPCs细胞对照组、EPCs+Ad-IRES空载体腺病毒组和EPCs+Ad-Ang-1-IRES单基因腺病毒组荧光强度都弱于EPCs-Ad-IRES-VEGF165单基因腺病毒组和EPCs-Ad-Ang-1-IRES-VEGF165双基因腺病毒组;而在检测Ang-1时,EPCs细胞对照组、EPCs+Ad-IRES空载体腺病毒组和EPCs-Ad-IRES-VEGF165单基因腺病毒组也都弱于EPCs+Ad-Ang-1-IRES单基因腺病毒组和EPCs-Ad-Ang-1-IRES-VEGF165双基因腺病毒组。间接免疫荧光检测结果表明,EPCs血管内皮祖细胞本身也表达一定的VEGF165和Ang-1促血管生长因子,并且腺病毒介导的外源性VEGF165和Ang-1基因能在EPCs细胞中成功表达。
(7)ELISA蛋白定量鉴定
ELISA检测各组重组腺病毒感染EPCs细胞培养上清中VEGF165和Ang-1的蛋白浓度。
根据VEGF165和Ang-1标准品浓度及其OD值(表4)分别绘制标准曲线并进行统计学检验得直线回归方程(图15和图16)。再根据各组EPCs细胞培养上清VEGF165和Ang-1所测量的OD及其直线回归方程分别计算EPCs细胞培养上清VEGF165和Ang-1浓度,结果(表5、表6)显示,ELISA检测:Ad-IRES-VEGF165单基因感染组和Ad-Ang-1-IRES-VEGF165双基因感染组EPCs培养上清VEGF165浓度分别为1998.4±21.7、1992.9±14.8pg/mL;Ad-Ang-1-IRES单基因感染组和Ad-Ang-1-IRES-VEGF165双基因感染组EPCs培养上清Ang-1浓度分别为1298.7±62.3、1309.2±32.9pg/mL。各组EPCs细胞培养上清VEGF165和Ang-1ELISA定量检测结果进一步表明,腺病毒介导的外源性VEGF165和Ang-1基因能在EPCs细胞中成功表达和分泌。
表4 VEGF165和Ang-1标准品浓度及其OD值
| VEGF165标准品OD值 | 0 | 0.09 | 0.15 | 0.21 | 0.36 | 0.59 | 1.06 | 1.43 |
| VEGF165标准品浓度(pg/ml) | 0 | 31.25 | 62.5 | 125 | 250 | 500 | 1000 | 2000 |
| Ang-1标准品OD值 | 0 | 0.12 | 0.18 | 0.25 | 0.39 | 0.62 | 1.15 | 1.68 |
| Ang-1标准品浓度(pg/ml) | 0 | 31.25 | 62.5 | 125 | 250 | 500 | 1000 | 2000 |
| 组别 | 培养上清VEGF165浓度(pg/ml) |
| EPCs | 2519.92±272.97 |
| EPCs+Ad-IRES | 2362.31±272.97 |
| EPCs+Ad-IRES-VEGF 165 | 25908.03±1477.38 |
| EPCs+Ad-Ang-1-IRES | 2510.85±152.75 |
| EPCs+Ad-Ang-1-IRES-VEGF165 | 25055.07±1477.38 |
*单因素方差分析F=49627.1,P=0.00;
q检验:除了EPCs、EPCs+Ad-IRES与EPCs+Ad-Ang-1-IRES组及EPCs+Ad-IRES-VEGF165与EPCs+Ad-Ang-1-IRES-VEGF165组VEGF165浓度差别无统计学意义之外,其它组之间差别有统计学意义(P<0.05)。
| 组别 | 培养上清Ang-1浓度(pg/ml) |
| EPCs | 2630.67±180.83 |
| EPCs+Ad-IRES | 2526.27±180.83 |
| EPCs+Ad-IRES-VEGF 165 | 3899.48±1039.68 |
| EPCs+Ad-Ang-1-IRES | 4499.75±1039.68 |
| EPCs+Ad-Ang-1-IRES-VEGF 165 | 5226.01±125.01 |
*单因素方差分析F=3026.84,P=0.00;
q检验:除了EPCs、EPCs+Ad-IRES和EPCs+Ad-IRES-VEGF165组及EPCs+Ad-Ang-1-IRES与EPCs+Ad-Ang-1-IRES-VEGF165组Ang-1浓度差别无统计学意义之外,其它组之间差别有统计学意义(P<0.05)。
实施例三:实施例二所得VEGF165和Ang-1双基因修饰的外周血血管内皮祖细胞促进兔缺血心肌血管形成。
为了观察实施例二所得VEGF165和Ang-1基因修饰的EPCs在体内促进缺血组织的新血管形成作用,本实施例中,在兔心肌缺血模型上,将体外增殖并经VEGF165和Ang-1基因修饰的EPCs从动脉途径移植到缺血心肌,观察促进缺血组织的新生血管的疗效,以评价VEGF165和Ang-1双基因共表达载体和单基因修饰的EPCs的生物学功能。
(1)材料
选用清洁级新西兰大白兔(雄性,体重2.5-3.1kg)由苏州大学动物实验中心提供【许可证号:SCXK(苏)2002-0008】,在温度为18-25℃的条件下饲养。食用普通饲料,饮普通水;心脏手术专用的5/0号涤纶编织线和3/8医用无创伤缝合针购自上海元洪医疗器械厂;脱辅基转铁蛋白(apo-transferrin)和Iodogen购自SIGMA公司;柠檬酸铁胺购自上海山浦化工有限公司;Na125I购自中核高通公司;PD-10层析柱(Sephadex G25)购自美国GE公司;兔vWF相关的多克隆抗体(Novus公司),抗兔平滑肌actin抗体(Lab visionNeoMarkers公司)。
(2)按照现有技术建立兔缺血心肌模型,参见:赵江民,李瑞祥,羊惠君等,兔心肌梗塞模型制备方法的改进及其在M RI中的应用,华西医大学报,2002;33(4):640~644。
1%戊巴比妥钠(30mg/L)经耳缘静脉麻醉,术前常规心电图和心电监护,取胸骨正中切口,从第2-5肋间至剑突下逐层切开皮肤、肌肉至胸骨,沿着并紧贴胸骨左缘缓慢切开第3-4肋骨,开胸器充分暴露搏动的心脏,注意避免损伤胸膜而造成气胸;接着用两把无齿镊子镊取心包,并剪开心包,钳夹固定心包膜,无齿镊快速固定心尖,暴露左前降支,用心脏手术专用的5/0号涤纶编织线和3/8医用无创伤缝合针在左前降支近心尖端0.5cm处结扎,可见灌注区逐渐苍白,出现反常运动,同步心电监护,结扎前后心电图比较,证实形成心肌梗死,观察2-3min,情况稳定后,用4号线逐层关胸。术后3天肌注青霉素40万/天。
手术中的心电图或心电监护可以观察到冠状动脉前降支部分结扎后的肢体导联II,III,aVF上ST段显著的损伤性“弓背样”抬高,提示急性心肌缺血发生,结扎有效,说明心肌缺血的模型制作成功。
(3)动、静脉途径输注血管内皮祖细胞体内分布的对比研究
本实施例用放射性碘标记的铁饱和转铁蛋白【125I-Tf(Fe)2】作为示踪剂(实施例中,转铁蛋白的碘标记【125I-Tf(Fe)2】的标记率为88.12±1.77%,放射化学纯度为97.01±0.21%,标记品的放射性浓度为0.91mCi/mL),以血管内皮祖细胞上的转铁蛋白受体作为靶点,用闪烁扫描成像监测移植的血管内皮祖细胞在体内的动态分布。
血管内皮祖细胞的标记:
①铁饱和转铁蛋白的制备:溶于PBS(0.01mol/L,pH=7.4)的脱辅基转铁蛋白(10mg/mL)与溶于0.01mol/L NaHCO3的柠檬酸铁胺(0.1mg/mL)室温孵育4h,过量铁通过PBS透析4℃过夜移除。铁饱和转铁蛋白的终浓度通过OD454nm测定,通常饱和度应在90%以上。
②125I-Tf(Fe)2的制备(碘化反应):将20μg Iodogen涂于管底,加100μL0.25mol/L PB,加10μL(1mg/mL)Fe-transferrin,加1.8mCi Na125I,室温反应5min,加0.01mol/L PBS至总体积500μL终止反应。
③125I-Tf(Fe)2的纯化:PD-10柱用20mL 0.01mol/L PBS淋洗,5mL1%BSA饱和,再用10mL 0.01mol/L PBS淋洗,加样,以0.01mol/L PBS洗脱。
④125I-Tf(Fe)2的放射化学纯度测定:纯化后产品进行放射化学纯度测定,固定相为新华1号层析纸,移动相为正丁醇∶无水乙醇∶50%氨水=5∶1∶2(v/v)。产品Rf=0.0,游离碘Rf=0.5~0.6。
⑤125I-Tf(Fe)2与血管内皮祖细胞的结合试验:血管内皮祖细胞数为1×106/100μL,每管加入700μL上述标记产品,活度为23.68MBq(640μCi),37℃孵育1h,选取心肌梗塞模型兔6只,随机分为两组:静脉注射和动脉注射途径组,每组3只。
SPECT显像和输注的血管内皮祖细胞在体内分布与测定
在注射后30min、2h、24h进行SPECT显像,采用静态采集,250k计数,能峰为37keV,窗宽60%,画感兴趣区进行半定量分析。24h显像后静脉注射空气处死兔子,取血及各脏器,称量后用γ计数器进行测量,计算每克组织百分注射剂量。
血管内皮祖细胞是内皮细胞的前体细胞,富含转铁蛋白受体,与外源性的高纯度的转铁蛋白【Tf(Fe)2】亲和力很大,所以,用放射性碘标记的铁饱和转铁蛋白【125I-Tf(Fe)2】作为示踪剂,以血管内皮祖细胞上的转铁蛋白受体作为靶点,125I-Tf(Fe)2用闪烁扫描成像监测血管内皮祖细胞移植后在体内0.5h、2h和24h的动态分布。结果(如图17)显示:动脉注射组示踪剂0.5h主要浓集在心、肝和肾脏,2h主要浓集在心、肝、肾和膀胱,24h主要浓集在心、肝、甲状腺、肾和膀胱;而静脉注射组0.5h主要浓集在肝、心和肾脏,2h主要浓集在肝、心、肾和膀胱,24h主要浓集在肝、心、甲状腺、肾和膀胱。
在体的半定量结果提示(如表7):经过三因素方差分析,组别(动脉组与静脉组)存在差异(p=0.039),动脉组可见在心脏积聚的示踪的干细胞多于静脉组;动、静脉组不同时间观察点之间也有差异(p=0.0081),提示各组内0.5h、2h、24h等3个时间点之间存在统计学差异,动脉和静脉两组似乎均有一个共同的趋势:即24h后标记的EPCs未有逐渐减退,与2h的显像相比,反有增强趋势。提示EPCs对缺血心脏具有趋化性。
表7 125I-Tf(Fe)2标记的EPCs的SPECT显像的半定量结果
(各脏器感兴趣区的平均计数与肝脏比)
注:三因素方差分析:F组别=6.432,p=0.039;F时间=7.210,p=0.0081;F脏器=7.238,p=0.009
如图18,动脉、静脉注射组集聚在心脏的每克组织百分注射剂量分别为1.207%、1.067%。提示标记的EPCs可能向缺血心肌归巢,动脉注射途径优于静脉注射途径。
(4)双基因修饰的EPCs治疗兔心肌缺血移植实验
兔模型成功后第14天时,再次麻醉,无菌条件下,肝素生理盐水浸泡血管扩张鞘和导管。穿刺右侧颈动脉,置4F血管扩张鞘,肝素250U/Kg常规抗凝后,递送4F软质指路导管,根据压力曲线判断导管进入左心室。回撤导管头置于主动脉辧上,经向升主动脉灌注按照下述实验分组各自用50MOI腺病毒感染后的1×106个EPCs细胞悬液1mL,未治疗组输注等量培养基,接着推送生理盐水5mL,冲洗导管内可能滞留的EPCs。将造模成功并存活的兔30只,随机分为6组,每组5只,实验分组如下:①EPCs+Ad-Ang-1-IRES-VEGF165双基因治疗组:灌注携带VEGF165和Ang-1双基因腺病毒载体感染的EPCs;②EPCs+Ad-Ang-1-IRES单基因治疗组:灌注含Ang-1单基因腺病毒载体感染的EPCs;③EPCs+Ad-IRES-VEGF165单基因治疗组:灌注含VEGF165单基因腺病毒载体感染的EPCs;④EPCs+Ad-IRES空病毒治疗组:灌注空载体腺病毒感染的EPCs;⑤单纯EPCs治疗组:灌注EPCs(未感染空病毒、单基因和双基因病毒);⑥未治疗组:灌注等量培养基作为空白对照。
(5)心功能检测
分别于细胞移植前和移植后4周在麻醉状态下,用彩色多普勒超声心动仪检测心脏功能。左室收缩功能的测量指标包括:左室长轴切面或左室短轴乳头肌水平M超测量左室射血分数(LVEF)、左室舒张期内径(LVDD)。
兔心肌缺血后,M超声观察到:未治疗组兔左心室壁运动几乎平直,波动幅度明显减低,5个移植组的左室运动均较移植前有所恢复。各个实验组间的心功能改变如下的特点:单纯EPCs治疗组、EPCs+Ad-IRES空病毒治疗组治疗组与未治疗组相比:左室射血分数的变化幅度小,心室扩大的程度略好于未治疗组,但无统计学差异(P>0.05);EPCs+Ad-Ang-1-IRES单基因治疗组、EPCs+Ad-IRES-VEGF165单基因治疗组和EPCs+Ad-Ang-1-IRES-VEGF165双基因治疗组心脏收缩功能、左室舒张末期直径均好于未转染基因组(单纯EPCs治疗组、EPCs+Ad-IRES空病毒治疗组和未治疗组),差异有统计学意义(P<0.05);并且EPCs+Ad-Ang-1-IRES-VEGF165双基因治疗组的左心收缩功能和左室舒张末期直径指标明显优于单基因治疗组(EPCs+Ad-IRES-VEGF165单基因治疗组、EPCs+Ad-Ang-1-IRES单基因治疗组)(P<0.05)。各组移植前后的心功能比较如表8。
各组移植前后LVEF及LVDD比较:*P<0.05 **P<0.01
6组LVEF差值比较F=23.16,P<0.0001,q检验:表中组间a,b,c字母相同,两组间差异无统计学意义(P>0.05),表中字母不同,两组间差异有统计学意义(P<0.05);
6组LVDD差值比较F=8.59,P<0.0001,q检验:表中组间a,b,c有字母相同,两组间差异无统计学意义(P>0.05),组间无字母相同,两组间差异有统计学意义(P<0.05)。
(6)RT-PCR和免疫组化检测
标本的留取:细胞移植后4周,在心脏彩色超声结束后,从耳缘静脉快速推注10%氯化钾注射液(2mL.kg-1),使心脏停搏于舒张期。立即取下心脏,生理盐水冲洗后,保留左室,称量后取部分兔缺血心肌组织提取总RNA进行RT-PCR,检测外源性VEGF165和Ang-1基因在兔缺血心肌中的转录;其余即刻10%甲醛溶液固定24h,脱水、石蜡包埋,垂直于心室长轴方向每隔4um连续切片进行常规HE染色和免疫组化检测。
RT-PCR检测外源性VEGF165和Ang-1基因在兔缺血心肌中的转录:
按UNIQ-10柱式Trizol总RNA抽提试剂盒说明书操作提取未治疗组、单纯EPCs治疗组、EPCs+Ad-IRES空病毒治疗组、EPCs+Ad-IRES-VEGF165单基因治疗组、EPCs+Ad-Ang-1-IRES 单基因治疗组和EPCs+Ad-Ang-1-IRES-VEGF165双基因治疗组各组心肌总RNA,用上述引物P1、P2;P3、P4;P5、P6进行RT-PCR,分别鉴定IRES、VEGF165和Ang-1基因在兔缺血心肌中的转录。
结果参见图19:EPCs+Ad-Ang-1-IRES-VEGF165双基因治疗组可产生预期大小的581bp IRES、576bp VEGF165和1497Ang-1PCR产物;EPCs+Ad-IRES-VEGF165单基因治疗组均可产生预期大小的581bp IRES和576bp VEGF165 PCR产物,而相应位置未产生1497Ang-1 PCR产物;EPCs+Ad-Ang-1-IRES单基因治疗组可产生预期大小的581bp IRES和1497Ang-1PCR产物,而相应位置未产生576bp VEGF165 PCR产物;EPCs+Ad-IRES空病毒治疗组可产生预期大小的581bp IRES PCR产物,而相应位置未产生576bp VEGF165和1497Ang-1PCR产物;单纯EPCs治疗组和未治疗组在相应位置均未产生上述条带。RT-PCR鉴定结果表明VEGF165和Ang-1双基因重组腺病毒修饰的EPCs在兔缺血心肌中同样能介导VEGF165和Ang-1的转录。
常规HE染色和普通光学显微镜检查。
免疫组织化学染色检查缺血心肌的新生血管:
用VIII因子相关抗原的免疫组化法染色,以定量各个实验组新生毛细血管的数量。
用抗平滑肌α-action抗体免疫组化法染色小动脉,以定量新生小动脉的数量。
毛细血管密度观察:免疫组织化学染色的毛细血管呈棕黄色,计数方法为每张切片选择3个血管最高的区域,光镜下在单个视野进行计数,取平均的血管数。血管的判断标准:在抗VIII因子免疫组化切片上,不以红细胞的出现来确定是否为血管,也不以是否出现管腔来计数毛细血管。凡是染成棕黄色、数个内皮细胞或内皮细胞簇均作为1个毛细血管计数,凡管腔较大,带有较厚肌层的血管,均不计数为毛细血管。在抗平滑肌α-action免疫组化片上:凡染色阳性,管腔较大,或带有肌层的血管,均计数为小动脉。
新生血管密度评价(如表9、图20、图21):EPCs+Ad-IRES-VEGF165单基因治疗组EPCs+Ad-Ang-1-IRES单基因治疗组和EPCs+Ad-Ang-1-IRES-VEGF165双基因治疗组相对于未治疗组、单纯EPCs治疗组、EPCs+Ad-IRES空病毒治疗组都有明显的血管新生(P<0.05),血管梗死中央区和边缘区都有分布,但以边缘区更为明显。其中,EPCs+Ad-Ang-1-IRES-VEGF165双基因治疗组血管新生数量又明显多于单基因治疗组组(P<0.05)。单纯EPCs治疗组和EPCs+Ad-IRES空病毒治疗组虽然也有血管新生,但与空白对照组相比,无统计学意义(P>0.05);EPCs+Ad-Ang-1-IRES-VEGF165双基因治疗组新生血管数目与单基因治疗组(EPCs+Ad-IRES-VEGF165单基因治疗组和EPCs+Ad-Ang-1-IRES单基因治疗组)比较,有明显差异(P<0.05)。
| 组别 | 移植前后新生毛细血管数差值# | 移植前后小动脉数差值$ |
| 未治疗组 | 14.6±1.7a | 1.4±0.6a |
| 单纯EPC治疗组 | 18.4±2.1a | 1.6±0.6a |
| EPCs+Ad-IRES空病毒治疗组 | 17.6±2.4a | 2.2±1.3a |
| EPCs+Ad-IRES-VEGF165单基因治疗组 | 25.2±1.9b | 4.4±1.1b |
| EPCs+Ad-Ang-1-IRES单基因治疗组 | 24.8±2.9b | 4.0±1.0b |
| EPCs+Ad-Ang-1-IRES-VEGF165双基因治疗组 | 35.0±2.7c | 6.6±1.5c |
#6组移植前后新生毛细血管数差值比较:F=50.52,P<0.0001,q检验:表中组间a,b,c字母相同,两组间差异无统计学意义(P>0.05),表中字母不同,两组间差异有统计学意义(P<0.05)
$6组移植前后小动脉数差值比较:F=17.63,P<0.0001,q检验:表中组间a,b,c字母相同,两组间差异无统计学意义(P>0.05),组间字母不同,两组间差异有统计学意义(P<0.05)
因此,实施例三显示双基因或单基因修饰的自体外周血来源的血管内皮祖细胞移植治疗能诱导血管生长因子释放,促进缺血心肌血管新生和心功能改善。
Claims (5)
1.一种含有人VEGF165和人Ang-1双基因共表达载体的大肠杆菌,该大肠杆菌的保藏信息为:保藏单位:中国典型培养物保藏中心;地址:中国武汉大学;保藏日期:2010年5月16日;保藏编号CCTCC NO:M 2010117;分类命名:大肠杆菌DH5α/pAdTrack-CMV-hAng-1-IRES-hVEGF165;Escherichiacoli DH5α/pAdTrack-CMV-hAng-1-IRES-hVEGF165;所述双基因共表达载体为pAdTrack-CMV-Ang-1-IRES-VEGF165。
2.一种含有人VEGF165和人Ang-1双基因共表达载体,其特征在于,所述双基因共表达载体为pAdTrack-CMV-Ang-1-IRES-VEGF165。
3.VEGF165和Ang-1双基因共表达重组腺病毒,所述双基因共表达重组腺病毒为Ad-Ang-1-IRES-VEGF165。
4.pAdTrack-CMV-Ang-1-IRES-VEGF165双基因重组转移载体在制备促进缺血心肌的血管新生药物中的应用。
5.Ad-Ang-1-IRES-VEGF165双基因共表达重组腺病毒在制备促进缺血心肌的血管新生药物中的应用。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN 201010263189 CN102191209A (zh) | 2010-08-26 | 2010-08-26 | VEGF165和Ang-1双基因共表达载体及其应用 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN 201010263189 CN102191209A (zh) | 2010-08-26 | 2010-08-26 | VEGF165和Ang-1双基因共表达载体及其应用 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN102191209A true CN102191209A (zh) | 2011-09-21 |
Family
ID=44600084
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN 201010263189 Pending CN102191209A (zh) | 2010-08-26 | 2010-08-26 | VEGF165和Ang-1双基因共表达载体及其应用 |
Country Status (1)
| Country | Link |
|---|---|
| CN (1) | CN102191209A (zh) |
Cited By (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2012045286A1 (zh) * | 2010-10-09 | 2012-04-12 | 苏州大学 | 重组载体以及转基因骨髓基质细胞修饰的丝素膜及其应用 |
| CN102533831A (zh) * | 2012-02-16 | 2012-07-04 | 郑州大学 | 一种包含自剪切位点的组织特异性双基因沉默RNAi表达载体 |
| CN103602625A (zh) * | 2013-08-16 | 2014-02-26 | 苏州大学 | 含有重组腺病毒质粒的大肠杆菌及重组腺病毒的应用 |
| CN104428315A (zh) * | 2012-07-13 | 2015-03-18 | 罗氏格黎卡特股份公司 | 双特异性抗-vegf/抗-ang-2抗体及其在治疗眼血管疾病中的应用 |
| CN110760542A (zh) * | 2019-11-18 | 2020-02-07 | 天津大学 | 一种共表达znf580和vegf165双基因的质粒及应用 |
| US12503503B2 (en) | 2018-10-29 | 2025-12-23 | Hoffmann-La Roche Inc. | Bispecific anti-VEGF/ANG2 antibody formulation |
-
2010
- 2010-08-26 CN CN 201010263189 patent/CN102191209A/zh active Pending
Non-Patent Citations (5)
| Title |
|---|
| 《中国优秀硕士学位论文全文数据库医药卫生科技辑》 20041215 刘翔 《心肌内注射Ad-VEGF165和Ad-Ang1治疗大鼠急性心肌梗死的实验研究》 E062-100-7-28页 5 , 第4期 * |
| 《中国优秀硕士学位论文全文数据库医药卫生科技辑》 20090915 刘铁连 《Ang-1或/和VEGF165转基因细胞修饰的再生丝素膜诱导血管形成效应及分子机制研究》 E080-47-3-12页 1-3 , 第9期 * |
| 《中国优秀硕士学位论文全文数据库医药卫生科技辑》 20090915 刘铁连 《Ang-1或/和VEGF165转基因细胞修饰的再生丝素膜诱导血管形成效应及分子机制研究》 E080-47-3-12页 4-5 , 第9期 * |
| 《中国协和医科大学》 20010131 郑哲 《心肌注射VEGF121质粒治疗慢性缺血性心脏病的实验研究》 第27-30页 4 , * |
| 《国外医学情报》 20060331 诸葛素 《VEGF基因转染内皮前体细胞能促进血管新生》 第16页 5 第24卷, 第3期 * |
Cited By (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2012045286A1 (zh) * | 2010-10-09 | 2012-04-12 | 苏州大学 | 重组载体以及转基因骨髓基质细胞修饰的丝素膜及其应用 |
| CN102533831A (zh) * | 2012-02-16 | 2012-07-04 | 郑州大学 | 一种包含自剪切位点的组织特异性双基因沉默RNAi表达载体 |
| CN104428315A (zh) * | 2012-07-13 | 2015-03-18 | 罗氏格黎卡特股份公司 | 双特异性抗-vegf/抗-ang-2抗体及其在治疗眼血管疾病中的应用 |
| CN104428315B (zh) * | 2012-07-13 | 2017-09-29 | 罗氏格黎卡特股份公司 | 双特异性抗‑vegf/抗‑ang‑2抗体及其在治疗眼血管疾病中的应用 |
| CN103602625A (zh) * | 2013-08-16 | 2014-02-26 | 苏州大学 | 含有重组腺病毒质粒的大肠杆菌及重组腺病毒的应用 |
| CN103602625B (zh) * | 2013-08-16 | 2015-09-30 | 苏州大学 | 含有重组腺病毒质粒的大肠杆菌及重组腺病毒的应用 |
| US12503503B2 (en) | 2018-10-29 | 2025-12-23 | Hoffmann-La Roche Inc. | Bispecific anti-VEGF/ANG2 antibody formulation |
| CN110760542A (zh) * | 2019-11-18 | 2020-02-07 | 天津大学 | 一种共表达znf580和vegf165双基因的质粒及应用 |
| CN110760542B (zh) * | 2019-11-18 | 2022-07-26 | 天津大学 | 一种共表达znf580和vegf165双基因的质粒及应用 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN102191209A (zh) | VEGF165和Ang-1双基因共表达载体及其应用 | |
| JP2007527395A (ja) | 血管新生のための骨髄由来細胞および培地の注入方法 | |
| CA3124877A1 (en) | Oncolytic virus expressing interferon and application thereof | |
| WO2016197592A1 (zh) | 一种长链非编码rna hnf1a-as1在制备治疗人体恶性实体瘤药物中的应用 | |
| CN113234811A (zh) | CircRNA000338的应用及其药物 | |
| CN107385033B (zh) | piRNA-5938及其反义核酸在诊断、治疗缺血性心脏疾病中的应用 | |
| WO2025026111A1 (zh) | 一种装载减毒沙门氏菌的中性粒细胞及其制备方法和应用 | |
| CN113278591B (zh) | 一种心脏靶向性基因工程外泌体及其制备方法和应用 | |
| CN107119020B (zh) | 一种基于miR-9的肝损伤靶向间充质干细胞及其制备方法与应用 | |
| CN101186929B (zh) | 一种复制缺陷型重组腺病毒的构建方法 | |
| CN102453757B (zh) | 一种微小rna及其反义核酸在诊断、预防、治疗和/或预后评估心肌缺血性损伤中的用途 | |
| CN104524599A (zh) | 一种miRNA-532反义核苷酸药物组合物及其用途 | |
| Zhang et al. | An adenovirus-delivered peptide aptamer C1-1 targeting the core protein of hepatitis B virus inhibits viral DNA replication and production in vitro and in vivo | |
| Wang et al. | Recombinant human hepatocyte growth factor transfection alleviates hyperkinetic pulmonary artery hypertension in rabbit models | |
| CN101649328A (zh) | 表达多个外源基因的Ad5 D24条件复制型腺病毒载体及其构建方法和应用 | |
| CN107164331B (zh) | 一种基于miR-221的肝损伤靶向间充质干细胞及其制备方法与应用 | |
| CN114588264B (zh) | 敲低或抑制egr3的试剂在制备心肌缺血再灌注损伤药物中的应用 | |
| CN117965628B (zh) | 高表达lncRNA H19基因的腺病毒载体、重组腺病毒及其应用 | |
| JP2008512198A (ja) | 血管新生治療のための自己性または同種性前駆細胞の馴化培地 | |
| JP4736088B2 (ja) | Cd9遺伝子からなる心疾患を予防又は治療する医薬 | |
| CN109971786B (zh) | 核孔蛋白Nup54及其载体和重组腺病毒的用途 | |
| CN107828819B (zh) | 一种利用ANP或IgANP基因构建重组腺病毒的方法及重组腺病毒和应用 | |
| Zhang et al. | Sequential and timely transfection of hepatocyte growth factor and monocyte chemotactic protein-1 ameliorates hyperkinetic pulmonary artery hypertension in rabbits | |
| CN114432453B (zh) | 敲低或抑制clec4d的试剂在制备心肌缺血再灌注损伤药物中的应用 | |
| CN110714028B (zh) | 可控性上调Ang-(1-7)靶向性防治低氧性肺动脉高压的表达载体 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C02 | Deemed withdrawal of patent application after publication (patent law 2001) | ||
| WD01 | Invention patent application deemed withdrawn after publication |
Application publication date: 20110921 |