CN101675161A - 表层嵌合体(surface chimera)转基因植物的培育方法 - Google Patents
表层嵌合体(surface chimera)转基因植物的培育方法 Download PDFInfo
- Publication number
- CN101675161A CN101675161A CN200880010382A CN200880010382A CN101675161A CN 101675161 A CN101675161 A CN 101675161A CN 200880010382 A CN200880010382 A CN 200880010382A CN 200880010382 A CN200880010382 A CN 200880010382A CN 101675161 A CN101675161 A CN 101675161A
- Authority
- CN
- China
- Prior art keywords
- gene
- flower plant
- plant
- flower
- cell
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 230000009261 transgenic effect Effects 0.000 title description 6
- 238000009395 breeding Methods 0.000 title description 3
- 108090000623 proteins and genes Proteins 0.000 claims abstract description 228
- 240000008254 Rosa chinensis Species 0.000 claims abstract description 47
- 235000000664 Rosa chinensis Nutrition 0.000 claims abstract description 47
- 238000009396 hybridization Methods 0.000 claims abstract description 30
- 230000001568 sexual effect Effects 0.000 claims abstract description 12
- 241000196324 Embryophyta Species 0.000 claims description 120
- 238000000034 method Methods 0.000 claims description 55
- 108090000790 Enzymes Proteins 0.000 claims description 32
- 230000008676 import Effects 0.000 claims description 31
- 240000006497 Dianthus caryophyllus Species 0.000 claims description 26
- 235000009355 Dianthus caryophyllus Nutrition 0.000 claims description 26
- 229930003935 flavonoid Natural products 0.000 claims description 22
- 150000002215 flavonoids Chemical class 0.000 claims description 22
- 235000017173 flavonoids Nutrition 0.000 claims description 22
- 102000004190 Enzymes Human genes 0.000 claims description 19
- 244000225942 Viola tricolor Species 0.000 claims description 16
- 230000001413 cellular effect Effects 0.000 claims description 15
- 240000007377 Petunia x hybrida Species 0.000 claims description 14
- 239000002299 complementary DNA Substances 0.000 claims description 14
- VEVZSMAEJFVWIL-UHFFFAOYSA-O cyanidin cation Chemical compound [O+]=1C2=CC(O)=CC(O)=C2C=C(O)C=1C1=CC=C(O)C(O)=C1 VEVZSMAEJFVWIL-UHFFFAOYSA-O 0.000 claims description 14
- 238000005805 hydroxylation reaction Methods 0.000 claims description 12
- 108700016155 Acyl transferases Proteins 0.000 claims description 11
- 235000002637 Nicotiana tabacum Nutrition 0.000 claims description 10
- 241000450415 Nierembergia scoparia Species 0.000 claims description 9
- 240000001519 Verbena officinalis Species 0.000 claims description 9
- 235000018718 Verbena officinalis Nutrition 0.000 claims description 9
- 230000001404 mediated effect Effects 0.000 claims description 9
- 241000193830 Bacillus <bacterium> Species 0.000 claims description 8
- 108091023040 Transcription factor Proteins 0.000 claims description 8
- 239000003550 marker Substances 0.000 claims description 8
- 241000628997 Flos Species 0.000 claims description 7
- 235000007336 cyanidin Nutrition 0.000 claims description 7
- 210000001519 tissue Anatomy 0.000 claims description 7
- 235000004405 Ageratum conyzoides Nutrition 0.000 claims description 6
- 235000016535 Capraria biflora Nutrition 0.000 claims description 6
- 235000017309 Hypericum perforatum Nutrition 0.000 claims description 6
- 102000040945 Transcription factor Human genes 0.000 claims description 6
- 241001106476 Violaceae Species 0.000 claims description 6
- 125000003118 aryl group Chemical group 0.000 claims description 6
- 244000296912 Ageratum conyzoides Species 0.000 claims description 5
- 240000001436 Antirrhinum majus Species 0.000 claims description 5
- 108010044229 Dihydroflavanol 4-reductase Proteins 0.000 claims description 5
- 240000007164 Salvia officinalis Species 0.000 claims description 5
- 101150039994 dye gene Proteins 0.000 claims description 5
- 235000005412 red sage Nutrition 0.000 claims description 5
- 235000007516 Chrysanthemum Nutrition 0.000 claims description 4
- 244000189548 Chrysanthemum x morifolium Species 0.000 claims description 4
- 238000004519 manufacturing process Methods 0.000 claims description 4
- 235000004828 Rosa odorata Nutrition 0.000 claims description 3
- 240000002289 Rosa odorata Species 0.000 claims description 3
- 244000309464 bull Species 0.000 claims description 3
- 235000011299 Brassica oleracea var botrytis Nutrition 0.000 claims description 2
- 240000003259 Brassica oleracea var. botrytis Species 0.000 claims description 2
- 244000025254 Cannabis sativa Species 0.000 claims description 2
- 235000003392 Curcuma domestica Nutrition 0.000 claims description 2
- 244000008991 Curcuma longa Species 0.000 claims description 2
- 240000009034 Cyclamen persicum Species 0.000 claims description 2
- 235000004692 Eucalyptus globulus Nutrition 0.000 claims description 2
- 240000007002 Eucalyptus tereticornis Species 0.000 claims description 2
- 235000019134 Eucalyptus tereticornis Nutrition 0.000 claims description 2
- 241000597000 Freesia Species 0.000 claims description 2
- 241000245654 Gladiolus Species 0.000 claims description 2
- 244000068988 Glycine max Species 0.000 claims description 2
- 235000010469 Glycine max Nutrition 0.000 claims description 2
- 244000017020 Ipomoea batatas Species 0.000 claims description 2
- 235000002678 Ipomoea batatas Nutrition 0.000 claims description 2
- 240000001549 Ipomoea eriocarpa Species 0.000 claims description 2
- 235000005146 Ipomoea eriocarpa Nutrition 0.000 claims description 2
- 241000234435 Lilium Species 0.000 claims description 2
- 241001635593 Lisianthius Species 0.000 claims description 2
- 235000007688 Lycopersicon esculentum Nutrition 0.000 claims description 2
- 240000005561 Musa balbisiana Species 0.000 claims description 2
- 235000018290 Musa x paradisiaca Nutrition 0.000 claims description 2
- 244000223072 Narcissus jonquilla Species 0.000 claims description 2
- 235000013862 Narcissus jonquilla Nutrition 0.000 claims description 2
- 241000233855 Orchidaceae Species 0.000 claims description 2
- 241000013557 Plantaginaceae Species 0.000 claims description 2
- 235000002315 Rosa hybrid cultivar Nutrition 0.000 claims description 2
- 244000037691 Rosa hybrida Species 0.000 claims description 2
- 240000003768 Solanum lycopersicum Species 0.000 claims description 2
- 244000061456 Solanum tuberosum Species 0.000 claims description 2
- 235000002595 Solanum tuberosum Nutrition 0.000 claims description 2
- 241000219793 Trifolium Species 0.000 claims description 2
- 210000000081 body of the sternum Anatomy 0.000 claims description 2
- 235000003373 curcuma longa Nutrition 0.000 claims description 2
- 235000013976 turmeric Nutrition 0.000 claims description 2
- 235000013311 vegetables Nutrition 0.000 claims description 2
- 244000061176 Nicotiana tabacum Species 0.000 claims 1
- 238000009792 diffusion process Methods 0.000 abstract description 7
- 210000004027 cell Anatomy 0.000 description 57
- 239000010410 layer Substances 0.000 description 52
- 108020004414 DNA Proteins 0.000 description 36
- 238000006243 chemical reaction Methods 0.000 description 19
- 241000220317 Rosa Species 0.000 description 15
- 241000251477 Chimaera Species 0.000 description 14
- 235000002254 Viola papilionacea Nutrition 0.000 description 14
- 238000010413 gardening Methods 0.000 description 14
- 241000894007 species Species 0.000 description 14
- 241000589158 Agrobacterium Species 0.000 description 12
- 238000004458 analytical method Methods 0.000 description 12
- 230000014509 gene expression Effects 0.000 description 12
- 239000013612 plasmid Substances 0.000 description 11
- 241000282326 Felis catus Species 0.000 description 10
- 244000062175 Fittonia argyroneura Species 0.000 description 10
- 230000003321 amplification Effects 0.000 description 10
- 238000005516 engineering process Methods 0.000 description 10
- 238000003199 nucleic acid amplification method Methods 0.000 description 10
- 241000208125 Nicotiana Species 0.000 description 9
- GCPYCNBGGPHOBD-UHFFFAOYSA-N Delphinidin Natural products OC1=Cc2c(O)cc(O)cc2OC1=C3C=C(O)C(=O)C(=C3)O GCPYCNBGGPHOBD-UHFFFAOYSA-N 0.000 description 8
- JKHRCGUTYDNCLE-UHFFFAOYSA-O delphinidin Chemical compound [O+]=1C2=CC(O)=CC(O)=C2C=C(O)C=1C1=CC(O)=C(O)C(O)=C1 JKHRCGUTYDNCLE-UHFFFAOYSA-O 0.000 description 8
- 235000007242 delphinidin Nutrition 0.000 description 8
- 230000015572 biosynthetic process Effects 0.000 description 7
- 238000013467 fragmentation Methods 0.000 description 7
- 238000006062 fragmentation reaction Methods 0.000 description 7
- 210000000056 organ Anatomy 0.000 description 7
- 239000000049 pigment Substances 0.000 description 7
- 241000589155 Agrobacterium tumefaciens Species 0.000 description 6
- 102220369447 c.1352G>A Human genes 0.000 description 6
- 238000001514 detection method Methods 0.000 description 6
- 101150118163 h gene Proteins 0.000 description 6
- 239000000463 material Substances 0.000 description 6
- 239000000575 pesticide Substances 0.000 description 6
- 102220023256 rs387907547 Human genes 0.000 description 6
- 229940027257 timentin Drugs 0.000 description 6
- 229920001817 Agar Polymers 0.000 description 5
- 239000008272 agar Substances 0.000 description 5
- 102220369445 c.668T>C Human genes 0.000 description 5
- 239000000284 extract Substances 0.000 description 5
- 101150054900 gus gene Proteins 0.000 description 5
- 229930027917 kanamycin Natural products 0.000 description 5
- 229960000318 kanamycin Drugs 0.000 description 5
- SBUJHOSQTJFQJX-NOAMYHISSA-N kanamycin Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CN)O[C@@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](N)[C@H](O)[C@@H](CO)O2)O)[C@H](N)C[C@@H]1N SBUJHOSQTJFQJX-NOAMYHISSA-N 0.000 description 5
- 229930182823 kanamycin A Natural products 0.000 description 5
- 239000007788 liquid Substances 0.000 description 5
- 239000002609 medium Substances 0.000 description 5
- 101150010856 CRT gene Proteins 0.000 description 4
- 206010020649 Hyperkeratosis Diseases 0.000 description 4
- 206010021703 Indifference Diseases 0.000 description 4
- 101150109924 PHR1 gene Proteins 0.000 description 4
- 235000010627 Phaseolus vulgaris Nutrition 0.000 description 4
- 244000046052 Phaseolus vulgaris Species 0.000 description 4
- REFJWTPEDVJJIY-UHFFFAOYSA-N Quercetin Chemical compound C=1C(O)=CC(O)=C(C(C=2O)=O)C=1OC=2C1=CC=C(O)C(O)=C1 REFJWTPEDVJJIY-UHFFFAOYSA-N 0.000 description 4
- OJOBTAOGJIWAGB-UHFFFAOYSA-N acetosyringone Chemical compound COC1=CC(C(C)=O)=CC(OC)=C1O OJOBTAOGJIWAGB-UHFFFAOYSA-N 0.000 description 4
- 125000002252 acyl group Chemical group 0.000 description 4
- 239000002585 base Substances 0.000 description 4
- 230000005540 biological transmission Effects 0.000 description 4
- 230000000694 effects Effects 0.000 description 4
- 238000002474 experimental method Methods 0.000 description 4
- 230000035784 germination Effects 0.000 description 4
- 238000009499 grossing Methods 0.000 description 4
- 238000005259 measurement Methods 0.000 description 4
- 230000008521 reorganization Effects 0.000 description 4
- 102220023257 rs387907546 Human genes 0.000 description 4
- 239000000523 sample Substances 0.000 description 4
- 239000007787 solid Substances 0.000 description 4
- 238000012795 verification Methods 0.000 description 4
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 3
- 102000057234 Acyl transferases Human genes 0.000 description 3
- 241000894006 Bacteria Species 0.000 description 3
- 241000701489 Cauliflower mosaic virus Species 0.000 description 3
- 238000007400 DNA extraction Methods 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 3
- 101150066002 GFP gene Proteins 0.000 description 3
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 3
- 230000010933 acylation Effects 0.000 description 3
- 238000005917 acylation reaction Methods 0.000 description 3
- RTYJTGSCYUUYAL-YCAHSCEMSA-L carbenicillin disodium Chemical compound [Na+].[Na+].N([C@H]1[C@H]2SC([C@@H](N2C1=O)C([O-])=O)(C)C)C(=O)C(C([O-])=O)C1=CC=CC=C1 RTYJTGSCYUUYAL-YCAHSCEMSA-L 0.000 description 3
- 230000004087 circulation Effects 0.000 description 3
- 238000010276 construction Methods 0.000 description 3
- 238000011161 development Methods 0.000 description 3
- 230000018109 developmental process Effects 0.000 description 3
- 235000013399 edible fruits Nutrition 0.000 description 3
- 108010060641 flavanone synthetase Proteins 0.000 description 3
- 239000012634 fragment Substances 0.000 description 3
- 230000005089 fruit drop Effects 0.000 description 3
- 239000011521 glass Substances 0.000 description 3
- 238000011065 in-situ storage Methods 0.000 description 3
- XUWPJKDMEZSVTP-LTYMHZPRSA-N kalafungina Chemical compound O=C1C2=C(O)C=CC=C2C(=O)C2=C1[C@@H](C)O[C@H]1[C@@H]2OC(=O)C1 XUWPJKDMEZSVTP-LTYMHZPRSA-N 0.000 description 3
- 210000001161 mammalian embryo Anatomy 0.000 description 3
- 230000008774 maternal effect Effects 0.000 description 3
- 238000012216 screening Methods 0.000 description 3
- 239000000741 silica gel Substances 0.000 description 3
- 229910002027 silica gel Inorganic materials 0.000 description 3
- 238000009331 sowing Methods 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- UZKQTCBAMSWPJD-UQCOIBPSSA-N trans-Zeatin Natural products OCC(/C)=C\CNC1=NC=NC2=C1N=CN2 UZKQTCBAMSWPJD-UQCOIBPSSA-N 0.000 description 3
- UZKQTCBAMSWPJD-FARCUNLSSA-N trans-zeatin Chemical compound OCC(/C)=C/CNC1=NC=NC2=C1N=CN2 UZKQTCBAMSWPJD-FARCUNLSSA-N 0.000 description 3
- 229940023877 zeatin Drugs 0.000 description 3
- 101150017816 40 gene Proteins 0.000 description 2
- 108700028146 Genetic Enhancer Elements Proteins 0.000 description 2
- 108700007698 Genetic Terminator Regions Proteins 0.000 description 2
- IKMDFBPHZNJCSN-UHFFFAOYSA-N Myricetin Chemical compound C=1C(O)=CC(O)=C(C(C=2O)=O)C=1OC=2C1=CC(O)=C(O)C(O)=C1 IKMDFBPHZNJCSN-UHFFFAOYSA-N 0.000 description 2
- 101150101654 PSR1 gene Proteins 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- ZVOLCUVKHLEPEV-UHFFFAOYSA-N Quercetagetin Natural products C1=C(O)C(O)=CC=C1C1=C(O)C(=O)C2=C(O)C(O)=C(O)C=C2O1 ZVOLCUVKHLEPEV-UHFFFAOYSA-N 0.000 description 2
- HWTZYBCRDDUBJY-UHFFFAOYSA-N Rhynchosin Natural products C1=C(O)C(O)=CC=C1C1=C(O)C(=O)C2=CC(O)=C(O)C=C2O1 HWTZYBCRDDUBJY-UHFFFAOYSA-N 0.000 description 2
- 244000172533 Viola sororia Species 0.000 description 2
- 229930014669 anthocyanidin Natural products 0.000 description 2
- 150000001452 anthocyanidin derivatives Chemical class 0.000 description 2
- 235000008758 anthocyanidins Nutrition 0.000 description 2
- 229930015036 aurone Natural products 0.000 description 2
- OMUOMODZGKSORV-UVTDQMKNSA-N aurone Chemical compound O1C2=CC=CC=C2C(=O)\C1=C\C1=CC=CC=C1 OMUOMODZGKSORV-UVTDQMKNSA-N 0.000 description 2
- 230000001488 breeding effect Effects 0.000 description 2
- 239000013611 chromosomal DNA Substances 0.000 description 2
- 238000005520 cutting process Methods 0.000 description 2
- 230000008034 disappearance Effects 0.000 description 2
- 210000002615 epidermis Anatomy 0.000 description 2
- 230000035558 fertility Effects 0.000 description 2
- 108020004445 glyceraldehyde-3-phosphate dehydrogenase Proteins 0.000 description 2
- 239000001963 growth medium Substances 0.000 description 2
- 208000015181 infectious disease Diseases 0.000 description 2
- 238000003780 insertion Methods 0.000 description 2
- 230000037431 insertion Effects 0.000 description 2
- IYRMWMYZSQPJKC-UHFFFAOYSA-N kaempferol Chemical compound C1=CC(O)=CC=C1C1=C(O)C(=O)C2=C(O)C=C(O)C=C2O1 IYRMWMYZSQPJKC-UHFFFAOYSA-N 0.000 description 2
- MWDZOUNAPSSOEL-UHFFFAOYSA-N kaempferol Natural products OC1=C(C(=O)c2cc(O)cc(O)c2O1)c3ccc(O)cc3 MWDZOUNAPSSOEL-UHFFFAOYSA-N 0.000 description 2
- PCOBUQBNVYZTBU-UHFFFAOYSA-N myricetin Natural products OC1=C(O)C(O)=CC(C=2OC3=CC(O)=C(O)C(O)=C3C(=O)C=2)=C1 PCOBUQBNVYZTBU-UHFFFAOYSA-N 0.000 description 2
- 235000007743 myricetin Nutrition 0.000 description 2
- 229940116852 myricetin Drugs 0.000 description 2
- 238000006384 oligomerization reaction Methods 0.000 description 2
- HKUHOPQRJKPJCJ-UHFFFAOYSA-N pelargonidin Natural products OC1=Cc2c(O)cc(O)cc2OC1c1ccc(O)cc1 HKUHOPQRJKPJCJ-UHFFFAOYSA-N 0.000 description 2
- 235000006251 pelargonidin Nutrition 0.000 description 2
- XVFMGWDSJLBXDZ-UHFFFAOYSA-O pelargonidin Chemical compound C1=CC(O)=CC=C1C(C(=C1)O)=[O+]C2=C1C(O)=CC(O)=C2 XVFMGWDSJLBXDZ-UHFFFAOYSA-O 0.000 description 2
- 235000005875 quercetin Nutrition 0.000 description 2
- 229960001285 quercetin Drugs 0.000 description 2
- 230000006798 recombination Effects 0.000 description 2
- 238000005215 recombination Methods 0.000 description 2
- 230000001850 reproductive effect Effects 0.000 description 2
- 238000011160 research Methods 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- WTLNOANVTIKPEE-UHFFFAOYSA-N 2-acetyloxypropanoic acid Chemical compound OC(=O)C(C)OC(C)=O WTLNOANVTIKPEE-UHFFFAOYSA-N 0.000 description 1
- 101150081540 ANS gene Proteins 0.000 description 1
- 206010069754 Acquired gene mutation Diseases 0.000 description 1
- 241000724328 Alfalfa mosaic virus Species 0.000 description 1
- BSWHERGFUNMWGS-UHFFFAOYSA-N Asp-Ile Chemical compound CCC(C)C(C(O)=O)NC(=O)C(N)CC(O)=O BSWHERGFUNMWGS-UHFFFAOYSA-N 0.000 description 1
- 241001516553 Begonia cucullata Species 0.000 description 1
- 101000883516 Capra hircus Chitinase-3-like protein 1 Proteins 0.000 description 1
- 244000107780 Capraria biflora Species 0.000 description 1
- 102000002322 Egg Proteins Human genes 0.000 description 1
- 108010000912 Egg Proteins Proteins 0.000 description 1
- 108010067770 Endopeptidase K Proteins 0.000 description 1
- 101150112014 Gapdh gene Proteins 0.000 description 1
- 241000246500 Gentianella aspera Species 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 102100031181 Glyceraldehyde-3-phosphate dehydrogenase Human genes 0.000 description 1
- 101001022847 Homo sapiens E3 ubiquitin-protein ligase MYCBP2 Proteins 0.000 description 1
- 101001126102 Homo sapiens Pleckstrin homology domain-containing family B member 1 Proteins 0.000 description 1
- 240000003589 Impatiens walleriana Species 0.000 description 1
- 229930010555 Inosine Natural products 0.000 description 1
- UGQMRVRMYYASKQ-KQYNXXCUSA-N Inosine Chemical compound O[C@@H]1[C@H](O)[C@@H](CO)O[C@H]1N1C2=NC=NC(O)=C2N=C1 UGQMRVRMYYASKQ-KQYNXXCUSA-N 0.000 description 1
- 108010025815 Kanamycin Kinase Proteins 0.000 description 1
- 108090000364 Ligases Proteins 0.000 description 1
- 102000003960 Ligases Human genes 0.000 description 1
- VPRLICVDSGMIKO-UHFFFAOYSA-N Mannopine Natural products NC(=O)CCC(C(O)=O)NCC(O)C(O)C(O)C(O)CO VPRLICVDSGMIKO-UHFFFAOYSA-N 0.000 description 1
- 102100030462 Pleckstrin homology domain-containing family B member 1 Human genes 0.000 description 1
- 108091030071 RNAI Proteins 0.000 description 1
- 244000050053 Rosa multiflora Species 0.000 description 1
- 240000006066 Rosa rugosa Species 0.000 description 1
- 241000806737 Rosa wichuraiana Species 0.000 description 1
- 229920002684 Sepharose Polymers 0.000 description 1
- 108700025695 Suppressor Genes Proteins 0.000 description 1
- 108700005078 Synthetic Genes Proteins 0.000 description 1
- GAMYVSCDDLXAQW-AOIWZFSPSA-N Thermopsosid Natural products O(C)c1c(O)ccc(C=2Oc3c(c(O)cc(O[C@H]4[C@H](O)[C@@H](O)[C@H](O)[C@H](CO)O4)c3)C(=O)C=2)c1 GAMYVSCDDLXAQW-AOIWZFSPSA-N 0.000 description 1
- 108090000992 Transferases Proteins 0.000 description 1
- 240000008042 Zea mays Species 0.000 description 1
- 235000005824 Zea mays ssp. parviglumis Nutrition 0.000 description 1
- 235000002017 Zea mays subsp mays Nutrition 0.000 description 1
- 238000009825 accumulation Methods 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 238000000246 agarose gel electrophoresis Methods 0.000 description 1
- 230000001476 alcoholic effect Effects 0.000 description 1
- 239000003513 alkali Substances 0.000 description 1
- 125000003275 alpha amino acid group Chemical group 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 235000010208 anthocyanin Nutrition 0.000 description 1
- 229930002877 anthocyanin Natural products 0.000 description 1
- 239000004410 anthocyanin Substances 0.000 description 1
- 150000004636 anthocyanins Chemical class 0.000 description 1
- 230000000692 anti-sense effect Effects 0.000 description 1
- 101150024767 arnT gene Proteins 0.000 description 1
- 230000001580 bacterial effect Effects 0.000 description 1
- 238000010170 biological method Methods 0.000 description 1
- 102220369446 c.1274G>A Human genes 0.000 description 1
- FPPNZSSZRUTDAP-UWFZAAFLSA-N carbenicillin Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)C(C(O)=O)C1=CC=CC=C1 FPPNZSSZRUTDAP-UWFZAAFLSA-N 0.000 description 1
- 229960003669 carbenicillin Drugs 0.000 description 1
- GPRBEKHLDVQUJE-VINNURBNSA-N cefotaxime Chemical compound N([C@@H]1C(N2C(=C(COC(C)=O)CS[C@@H]21)C(O)=O)=O)C(=O)/C(=N/OC)C1=CSC(N)=N1 GPRBEKHLDVQUJE-VINNURBNSA-N 0.000 description 1
- 229960004261 cefotaxime Drugs 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 210000003763 chloroplast Anatomy 0.000 description 1
- 210000000349 chromosome Anatomy 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 239000000356 contaminant Substances 0.000 description 1
- 235000005822 corn Nutrition 0.000 description 1
- 230000002939 deleterious effect Effects 0.000 description 1
- 230000004069 differentiation Effects 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 238000001962 electrophoresis Methods 0.000 description 1
- 210000002919 epithelial cell Anatomy 0.000 description 1
- ZMMJGEGLRURXTF-UHFFFAOYSA-N ethidium bromide Chemical compound [Br-].C12=CC(N)=CC=C2C2=CC=C(N)C=C2[N+](CC)=C1C1=CC=CC=C1 ZMMJGEGLRURXTF-UHFFFAOYSA-N 0.000 description 1
- 229960005542 ethidium bromide Drugs 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 229930003944 flavone Natural products 0.000 description 1
- 150000002212 flavone derivatives Chemical class 0.000 description 1
- 235000011949 flavones Nutrition 0.000 description 1
- 230000009368 gene silencing by RNA Effects 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 102000006602 glyceraldehyde-3-phosphate dehydrogenase Human genes 0.000 description 1
- 229940088597 hormone Drugs 0.000 description 1
- 239000005556 hormone Substances 0.000 description 1
- 235000003642 hunger Nutrition 0.000 description 1
- 239000007943 implant Substances 0.000 description 1
- 230000001939 inductive effect Effects 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- 229960003786 inosine Drugs 0.000 description 1
- 230000000968 intestinal effect Effects 0.000 description 1
- JEIPFZHSYJVQDO-UHFFFAOYSA-N iron(III) oxide Inorganic materials O=[Fe]O[Fe]=O JEIPFZHSYJVQDO-UHFFFAOYSA-N 0.000 description 1
- VPRLICVDSGMIKO-SZWOQXJISA-N mannopine Chemical compound NC(=O)CC[C@@H](C(O)=O)NC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO VPRLICVDSGMIKO-SZWOQXJISA-N 0.000 description 1
- 108010083942 mannopine synthase Proteins 0.000 description 1
- 230000009456 molecular mechanism Effects 0.000 description 1
- 238000012544 monitoring process Methods 0.000 description 1
- 231100000350 mutagenesis Toxicity 0.000 description 1
- 235000015097 nutrients Nutrition 0.000 description 1
- 210000004681 ovum Anatomy 0.000 description 1
- 239000012188 paraffin wax Substances 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 238000002203 pretreatment Methods 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 235000018102 proteins Nutrition 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 239000000376 reactant Substances 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 238000005067 remediation Methods 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 102200076454 rs104894848 Human genes 0.000 description 1
- 102220023258 rs387907548 Human genes 0.000 description 1
- 230000007226 seed germination Effects 0.000 description 1
- 239000002356 single layer Substances 0.000 description 1
- 230000037439 somatic mutation Effects 0.000 description 1
- 238000010186 staining Methods 0.000 description 1
- 230000037351 starvation Effects 0.000 description 1
- 230000001954 sterilising effect Effects 0.000 description 1
- 238000004659 sterilization and disinfection Methods 0.000 description 1
- 239000012879 subculture medium Substances 0.000 description 1
- 230000002103 transcriptional effect Effects 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- 238000011144 upstream manufacturing Methods 0.000 description 1
- 210000003934 vacuole Anatomy 0.000 description 1
- VHBFFQKBGNRLFZ-UHFFFAOYSA-N vitamin p Natural products O1C2=CC=CC=C2C(=O)C=C1C1=CC=CC=C1 VHBFFQKBGNRLFZ-UHFFFAOYSA-N 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- 238000004383 yellowing Methods 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/79—Vectors or expression systems specially adapted for eukaryotic hosts
- C12N15/82—Vectors or expression systems specially adapted for eukaryotic hosts for plant cells, e.g. plant artificial chromosomes (PACs)
- C12N15/8241—Phenotypically and genetically modified plants via recombinant DNA technology
- C12N15/8261—Phenotypically and genetically modified plants via recombinant DNA technology with agronomic (input) traits, e.g. crop yield
- C12N15/8262—Phenotypically and genetically modified plants via recombinant DNA technology with agronomic (input) traits, e.g. crop yield involving plant development
- C12N15/8265—Transgene containment, e.g. gene dispersal
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/79—Vectors or expression systems specially adapted for eukaryotic hosts
- C12N15/82—Vectors or expression systems specially adapted for eukaryotic hosts for plant cells, e.g. plant artificial chromosomes (PACs)
- C12N15/8201—Methods for introducing genetic material into plant cells, e.g. DNA, RNA, stable or transient incorporation, tissue culture methods adapted for transformation
- C12N15/8202—Methods for introducing genetic material into plant cells, e.g. DNA, RNA, stable or transient incorporation, tissue culture methods adapted for transformation by biological means, e.g. cell mediated or natural vector
- C12N15/8205—Agrobacterium mediated transformation
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/79—Vectors or expression systems specially adapted for eukaryotic hosts
- C12N15/82—Vectors or expression systems specially adapted for eukaryotic hosts for plant cells, e.g. plant artificial chromosomes (PACs)
- C12N15/8241—Phenotypically and genetically modified plants via recombinant DNA technology
- C12N15/8242—Phenotypically and genetically modified plants via recombinant DNA technology with non-agronomic quality (output) traits, e.g. for industrial processing; Value added, non-agronomic traits
- C12N15/8243—Phenotypically and genetically modified plants via recombinant DNA technology with non-agronomic quality (output) traits, e.g. for industrial processing; Value added, non-agronomic traits involving biosynthetic or metabolic pathways, i.e. metabolic engineering, e.g. nicotine, caffeine
- C12N15/825—Phenotypically and genetically modified plants via recombinant DNA technology with non-agronomic quality (output) traits, e.g. for industrial processing; Value added, non-agronomic traits involving biosynthetic or metabolic pathways, i.e. metabolic engineering, e.g. nicotine, caffeine involving pigment biosynthesis
Landscapes
- Health & Medical Sciences (AREA)
- Genetics & Genomics (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Biotechnology (AREA)
- Molecular Biology (AREA)
- Biomedical Technology (AREA)
- Wood Science & Technology (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Zoology (AREA)
- General Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Plant Pathology (AREA)
- Microbiology (AREA)
- Biophysics (AREA)
- Physics & Mathematics (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- Cell Biology (AREA)
- Nutrition Science (AREA)
- Breeding Of Plants And Reproduction By Means Of Culturing (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
Abstract
本发明培育出导入基因仅在一部分细胞、例如花瓣的L1层的细胞等中存在,而在其他细胞、例如花粉细胞、胚珠细胞等的生殖细胞中不存在的月季。本发明的月季即使与其他月季杂交,导入基因也不会向其他月季转移,所以,可完全否定导入基因扩散的可能性。
Description
技术领域
本发明提供培育仅在一部分细胞中具有导入基因的嵌合基因重组植物的方法。
背景技术
由多个遗传上不同的细胞群组成的个体称作嵌合体。植物的嵌合体从其结构上可分为周缘嵌合体、部分嵌合体及扇形嵌合体,例如除嫁接外,可通过由突发的或放射线照射引起的体细胞突变、由药剂处理引起的染色体加倍来制备。
扇形嵌合体(sectorial chimera)是植物重叠结构引起的非结构性嵌合体,由生长点上非结构性混合存在的突变细胞的增殖所产生。即一个组织层自身即是嵌合体,多在花·叶·茎等的器官呈现不同颜色的条纹。扇形嵌合体通常不稳定、大多易消失,但也有极少发展成周缘嵌合体。
周缘嵌合体(periclinal chimera)是指由植物的组织层结构引起的结构性嵌合体,是扇形嵌合体发展、一个细胞层完全被突变细胞取代的状态。为周缘嵌合体时,一个组织层自身均匀,不是嵌合体。已知周缘嵌合体稳定,消失的几率小。植物的细胞组织基本上由3个细胞层构成,从外侧开始具有第1层(L1)、第2层(L2)、第3层(L3)的组织层结构。
由生长点的2层原套(tunica)产生的组织层为L1和L2,由原体(corpus)产生的组织层为L3。在几乎所有的植物种中,表皮均由L1层生成,L2层与生殖细胞系统有关。上述这些每个细胞层都具有不同性质的周缘嵌合体很多在园艺上都很重要、且产业价值高,但通过突发的方法、或通过放射线照射、药剂处理等人工诱变的方法得到周缘嵌合体的概率极低。
在将外源基因导入植物体时,人工培育出仅在一部分细胞中具有导入基因的嵌合体植物非常不容易。到目前为止,已有通过使用基因枪的方法向玉米的未成熟胚中导入基因,从而培育出仅在生殖细胞或L2细胞层中具有导入基因的嵌合体植物的例子(日本特表平10-503374号公报)。但是,通过农杆菌介导而导入基因时,培育嵌合体植物就更加困难。通过农杆菌介导而导入基因的方法中,以通过标记基因表达的抗药性等的性状为指标,筛选导入了基因的单一细胞,由该单一的基因导入细胞得到一个转化体植物个体。
因此,通常得到的基因重组植物由可遗传的单一细胞组成,是在所有的细胞中具有导入基因的植物。即使得到了仅在一部分细胞中具有外源基因的植物(嵌合体植物),那也是偶然的结果,利用现代技术进行仅在植物体的特定部分的细胞中导入基因的控制非常困难。而且认为,即使是偶然所得,形成如前所述的仅在一部分细胞层中具有基因的周缘嵌合体的概率也极低。
在筛选基因导入细胞的过程中,有时虽出现仅在其一部分细胞中导入了外源基因的嵌合细胞团或嵌合植物体,但此时通过全细胞层形成嵌合体、或一个组织层自身形成嵌合体,而不是完整的周缘嵌合体(仅在特定的细胞层中导入了外源基因,其细胞层自身均匀)。至今为止,培育出完整的周缘嵌合体转基因植物、并将其用分子生物学的方法证明的例子极少。到目前为止,虽已报道了以下实例,即发现了通过使用含有rol基因和脱离因子的载体,可培育出周缘嵌合体(日本特开2002-315460号),但此时为L3层的周缘嵌合体。
在基因重组植物中,被掺入染色体中的导入基因根据孟德尔定律可稳定传递给其后代。通过将这些基因重组植物作为杂交亲本使用,利用来自导入基因的性状进一步培育出新品种。
而且对于基因重组植物,担心的是其对生态系统(环境)的影响(导入基因向自然界的扩散等)。作为用于防止基因由基因重组植物向非转化体、野生植物扩散的技术,已知有(1)母系遗传的利用、(2)雄性不育的利用、(3)不育种子的利用等。母系遗传的利用是指通过在不传入花粉细胞的叶绿体的基因组中导入外源基因,从而防止通过花粉的基因扩散的方法。
雄性不育的利用是指或抑制花粉形成、或使花粉不具有生殖能力的方法,可由此进行遗传隔离。例如有使用雄性生殖器官特异性表达的启动子,组织特异性地制作有害的基因产物,从而抑制花粉形成的方法等。不育种子的利用是指通过直接抑制基因重组植物的种子形成,从而防止杂交或种子扩散这两者的方法,不能进行自留种的“终止子技术”等即为此方法。
假设只要可培育出生殖细胞中不携带导入基因的基因重组植物,即可在以其重组植物作为花粉亲本时、或作为种子亲本时的任一情况下,完全排出由杂交所导致的导入基因扩散的可能性。此结果对于将基因重组植物进行野外栽培、或进行产业利用的人来说,可减轻用于基因重组植物栽培的手续所造成的负担。此手续在日本国内是基于“通过规范基因重组生物等的使用等以确保生物多样性的相关法律(卡塔赫纳法)”的生物多样性影响评价等,在其他国家也有基于同样的法律的评价。
专利文献1日本特表平10-503374号公报
专利文献2日本特开2002-315460号
专利文献3USP 5480789
专利文献4WO 2005/017147
专利文献5PCT/JP96/00348
非专利文献1Firoozababy et al.Bio/Technology 12:883-888 1994
非专利文献2Lazo et al.Bio/Technology 9:963-967,1991
非专利文献3Fujiwara et al.Plant J.16 421-431,1998
非专利文献4Mitsuhara et al.Plant Vell Physiol.37,45-591996
发明内容
因此,本发明提供导入基因仅在植物体的一部分细胞中存在,例如在生殖细胞中不存在的基因导入的月季等的花卉植物。
本发明者为解决上述课题进行了种种研究,结果发现将外源基因通过根癌农杆菌介导而导入花卉植物时,有时再生的花卉植物会形成嵌合体植物。而且发现,通过从中选择周缘嵌合体的植物,可得到目的基因重组花卉植物,从而完成了本发明。因此,本发明提供外源基因在一部分细胞中存在,而在其他细胞中不存在的月季等的花卉植物。
优选所述一部分细胞构成一部分的细胞层。例如,上述其他细胞例如为花粉或胚珠。作为更加具体的例子,所述一部分细胞层为L1层、或L1层和L3层。作为外源基因,是与类黄酮的合成有关的基因,其中可例举与花色素苷的合成有关的基因等与花色有关的基因。
花卉植物为月季时,外源基因中,例如来自堇菜科植物的类黄酮3’,5’一羟基化酶基因、来自玄参科植物的芳香族酰基转移酶基因非常重要。所述堇菜科植物例如为堇菜科三色堇,所述玄参科植物例如为玄参科蓝猪耳。所述月季例如为月季品种WKS82等的杂交香水月季、丰花月季、微型月季。本发明的月季根据导入基因的效果,例如与基因导入前的月季相比,花色向蓝色方向改变。
花卉植物为康乃馨时,外源基因、例如所述外源基因是在来自金鱼草的查耳酮合成酶基因的启动子控制下的来自一串红的类黄酮3’、5’-羟基化酶基因cDNA、来自矮牵牛的二氢黄酮醇4-还原酶的染色基因、来自康乃馨的花色素合成酶基因中的一个~多个基因。所述康乃馨为大轮品系或中小轮品系。本发明的康乃馨根据导入基因的效果,例如,与基因导入前的康乃馨相比,花色向蓝色方向改变。
但是,外源基因不限于上述基因,也可以为在广泛的色素合成体系中发挥功能的基因、例如类黄酮合成体系中发挥功能的基因。此外,外源基因也可为如GFP基因、NPTII基因、GUS基因、SURB基因等的选择性标记基因。而且,外源基因可为编码转录因子的基因,例如编码myb类转录因子的基因,具体地说,也可为PHR1基因、Psr1基因。
本发明还提供与上述月季等的花卉植物具有相同性质的这些花卉植物的组织、及这些的营养增殖体。
本发明进一步提供包含在所述月季等花卉植物的制造方法中,通过农杆菌介导在月季中导入外源基因,选择该外源基因仅在一部分细胞中存在的月季的工序的方法。本发明更进一步提供通过权利要求3~27中任一项所述的生殖细胞中不携带外源基因的花卉植物,从而防止导入基因向自然界扩散的方法。
附图说明
图1为表示导入的基因在月季的各器官中有无存在的图。
图2表示导入的外源基因仅在L1层的细胞中表达,而在L2层及L3层中不表达。
图3是表示实施例2中使用的双元载体pSPB130的结构的图。
具体实施方式
本发明中使用的花卉植物只要是可通过农杆菌介导而导入外源基因的花卉植物,无特别限定。例如可例举月季、康乃馨、矮牵牛、蓝猪耳、烟草、马鞭草、赛亚麻、菊花、百合、牵牛花、金鱼草、仙客来、兰花、洋桔梗、小苍兰、非洲菊、唐菖蒲、霞草、长寿花、天竺葵、老鹳草、郁金香、菜籽、马铃薯、西红柿、毛白杨、香蕉、蓝桉、番薯、黄豆、苜蓿、鲁冰花、花椰菜等。其中,优选月季、康乃馨、矮牵牛、蓝猪耳、烟草、马鞭草、赛亚麻。其中,可特别优选使用月季和康乃馨。
作为本发明中使用的外源基因,希望为导入后在L1层的细胞中发挥功能的酶的基因。优选例如与花色有关的基因、选择性标记基因或编码转录因子的基因。作为与花色有关的基因,可例举与类黄酮的合成有关的酶的基因,例如与花色苷合成有关的基因、编码与噢哢合成有关的蛋白质的基因、编码控制液胞的pH的蛋白质的基因、编码脂肪族酰基转移酶的基因、编码黄酮合成酶的基因等。作为选择性标记基因,可例举GFP基因、NPTII基因、GUS基因、SURB基因等。作为编码转录因子的基因,可例举例如编码MYB类转录因子的基因、具体地说为PHR1基因、Psr1基因。但是,不限于这些具体列举的基因。
本发明中使用的月季可为园艺种或野性种中的任一个。其中,希望为商业上有用的杂交香水月季、丰花月季、壮花月季或微型月季等的园艺种(现代月季Rosa hybrida)。这些品种无特别限定。
在月季的愈伤组织中,在一定条件下,通过农杆菌介导,导入来自三色堇的类黄酮3’,5’-羟基化酶基因的表达盒以及来自蓝猪耳的芳香族酰基转移酶基因NPTII基因的表达盒所组成的T-DNA。因所得到的转化通过导入基因的作用而使花色发生变化,所以表明导入基因在花瓣细胞、特别是进行色素合成的花瓣的L1层细胞中存在。通过以从月季各器官分别提取的基因组DNA为模板的PCR,可证明花粉细胞中不存在导入基因。
此外,使用从该重组植物中得到的花粉与其他园艺种以及野生种的月季进行杂交试验时,从所得到的种子中完全未检测出导入基因。由此也可证明花粉细胞中不存在导入基因。进一步通过原位(in situ)杂交,证明导入基因仅在L1细胞层中存在。由此也证实由L2细胞层形成的花粉等的生殖细胞中不存在导入基因。因此,如上所述通过在上述月季愈伤组织中导入外源基因,可培育出仅在一部分细胞中具有导入基因的嵌合体植物。
其中,作为与类黄酮类的合成有关的酶的基因,可例举类黄酮3’,5’-羟基化酶基因、芳香族酰基转移酶基因。这些基因的来源无特别限定,优选可确认在月季中发挥功能的来自三色堇等堇菜科植物的类黄酮3’,5’-羟基化酶基因、或来自蓝猪耳等玄参科植物的芳香族酰基转移酶基因。
本发明中使用的康乃馨希望为商业上有用的大轮品系或中小轮品系。这些品种无特别限定。可为Feeling White、Brecross Doozy、Starzarl、Kortina Chanel等的任一品种。
对于康乃馨,在一定的条件下,通过农杆菌介导,导入了在来自金鱼草的查耳酮合成酶基因的启动子控制下的来自一串红的类黄酮3’、5’-羟基化酶基因cDNA、来自矮牵牛的二氢黄酮醇4-还原酶的染色基因、来自康乃馨的花色素合成酶基因SURB基因。因所得到的转化通过导入基因的作用而使花色发生变化,所以可证明导入基因在花瓣细胞、特别是进行色素合成的花瓣的L1层的细胞中存在。以从康乃馨的各器官中分别提取的基因组DNA为模板,通过PCR,可判断其是导入基因仅在L1层存在的嵌合体植物。
实施例
以下,通过实施例更具体地说明本发明。
实施例1.向月季中导入基因的方法
有关月季的转化,已报道了很多方法(例如,Firoozababy et al.Bio/Technology 12:883-888 1994,US 5480789、WO 2005/017147),根据这些方法,可将外源基因导入月季中。
具体地说,在根癌农杆菌(Agrobacterium tumefaciens)Ag10株(Lazo et al.Bio/Technology 9:963-967,1991)的菌液中,将由无菌苗的叶诱导的月季的愈伤组织浸泡5分钟,用灭菌滤纸拭去多余菌液后移入继代培养基中,进行2天暗处共培养。
而后,用加入了400mg/l羧苄青霉素的MS液体培养基洗涤,移入在继代用培养基中加入了50mg/l卡那霉素和200mg/l羧苄青霉素的筛选·除菌用培养基内。对筛选培养基中生长发育未受抑制、正常增殖的部分反复进行移植和培养、筛选卡那霉素抗性愈伤组织。
将显示卡那霉素抗性的转基因愈伤组织在添加了50mg/l卡那霉素、200mg/l羧苄青霉素的再分化用培养基中培养,得到卡那霉素抗性茎段。使所得到的茎段在1/2MS培养基(不添加卡那霉素)中生根后进行驯化。驯化个体上盆后,在封闭性温室中栽培使其开花。而后,用通常的营养增殖(扦插)进行维持·增殖。
实施例2.双元载体pSPB130的构建
通过将花色苷用芳香族酰基修饰而使花色苷稳定,且其颜色可向蓝色变化(例如,PCT/JP96/00348)。为进行酰基化后的花翠素型花色苷的生产,进行了以下实验。
从蓝猪耳(商品名:Summer Wave(商标))的花瓣中获得total RNA,进一步由此制备polyA+RNA。使用directional cDNA文库构建试剂盒(Stratagene公司),采用制造商推荐的方法,由该polyA+RNA构建以λZAPII(Stratagene公司)为载体的cDNA文库。
蓝猪耳的主要花色苷因其5位的葡萄糖被芳香族酰基修饰(Suzuki etal.Molecular Breeding 6,239-246,2000),所以,在蓝猪耳花瓣中花色苷酰基转移酶进行了表达。花色苷酰基转移酶中Asp-Phe-Gly-Trp-Gly-Lys.的氨基酸序列保守,通过将与此对应的合成DNA作为引物使用,可获得花色苷酰基转移酶基因(PCT/JP96/00348)。
具体地说,以蓝猪耳cDNA文库构建时合成的10ng单链cDNA为模板,以100ng的ATC引物(5’-GA(TC)TT(TC)GGITGGGGIAA-3’,I为肌苷,(TC)指任一方)(序列号:1)、100ng的寡聚dT引物(5’-TTTTTTTTTTTTTTTTTCTCGAG-3’)(序列号:2)为引物,使用Taq聚合酶(TAKARA、日本),在制造商推荐的条件下进行PCR。PCR进行了95℃1分钟、55℃1分钟、72℃1分钟为1循环的反应25循环。将所得到的约400bp的DNA片段通过Gene Clean II(BIO,101.Inc.)用制造商推荐的方法回收,亚克隆到pCR-TOPO上。
确定其碱基序列时发现了与龙胆的酰基转移酶基因(Fujiwara et al.Plant J.16 421-431,1998)同源的序列。且碱基序列使用引物标记法(Dye-primer法)(美国应用生物系统公司),使用测序仪310或377(均为美国应用生物系统公司制)确定。
将此DNA片段使用DIG标记检测试剂盒(日本Roche)通过DIG进行标记,用制造商推荐的方法将蓝猪耳的cDNA文库通过噬菌斑杂交法进行了筛选。随机选取12个带有所得到的阳性信号的克隆,从中回收质粒,确定碱基序列。这些序列显示出与花色苷酰基转移酶的良好的同源性。确定了这些克隆中作为pTAT7的克隆中所含有的cDNA的全碱基序列(序列号:3)。
将pBE2113-GUS(Mitsuhara et al.Plant Vell Physiol.37,45-591996)用SacI酶切后进行末端平滑化,插入8bp的XhoI接头(TaKaRa)。在此质粒的BamHI和XhoI位点插入将pTAT7用BamHI和XhoI酶切后得到的约1.7kb的DNA,得到pSPB120。通过将pSPB120用SnaBI和BamHI酶切后进行末端平滑化而连接,得到了pSPB120’。另外,将含有来自三色堇的F3’,5’H#40cDNA的质粒pCGP1961用BamHI完全酶切,回收进一步用XhoI部分酶切后得到的约1.8kb的DNA片段,将该片段与用BamHI和XhoI酶切后的pUE5H连接后所得到的质粒作为pUEBP40。
通过将pUEBP40用SnaBI和BamHI酶切后进行末端平滑化而连接,得到了pUEBP40’。回收将pUEBP40用HindIII部分酶切后得到的约2.7kb的DNA片段,与用HindIII部分酶切后的DNA片段连接。在所得到的质粒中,将从双元载体上的右边界开始,按新霉素磷酸转移酶基因、三色堇F3’5’H#40、蓝猪耳5AT基因的顺序分别同向连接的双元载体作为pSPB130(图3)。并致力于使本质粒在植物中三色堇F3’5’H#40基因和5AT基因结构性表达、并对基因进行花瓣特异性转录。将该质粒导入Agrobacterium tumefaciens Ag10株。
实施例3.向WKS82的三色堇F3’,5’H#40基因和蓝猪耳花色苷
5-酰基转移酶基因的导入
将pSPB130导入紫色系月季“WKS82”,得到89个体的转化体。确认出进行色素分析的44个体全部均有花翠素的积累。花翠素含有率最高达91%(平均49%)。花色由RHS色谱186d(GREYED-PURPLE GROUP)向80c(PURPLE-VIOLET GROUP)变化。代表性的转化体的分析值如下表所示。
表1
| Plant No. | acyl(%) | Del(%) | Del(mg/g) | Cya(mg/g) | Pel(mg/g) | M(mg/g) | Q(mg/g) | K(mg/g) |
| WKS82 control | 0.0 | 0.0% | 0.000 | 0.074 | 0.000 | 0.000 | 2.400 | 0.196 |
| 1 | 10.5 | 52.3% | 0.055 | 0.050 | 0.000 | 0.430 | 0.883 | 0.083 |
| 2 | 15.9 | 62.5% | 0.091 | 0.054 | 0.000 | 0.570 | 0.549 | 0.030 |
| 3 | 15.9 | 36.6% | 0.044 | 0.076 | 0.000 | 0.622 | 2.221 | 0.102 |
| 4 | 6.8 | 40.0% | 0.023 | 0.034 | 0.000 | 0.247 | 0.986 | 0.172 |
| 5 | 15.0 | 82.9% | 0.087 | 0.018 | 0.000 | 5.451 | 0.403 | 0.042 |
| 6 | 89.7% | 0.072 | 0.008 | 0.000 | 0.853 | 0.163 | 0.062 | |
| 7 | 9.5 | 89.5% | 0.101 | 0.012 | 0.000 | 0.719 | 0.144 | 0.019 |
| 8 | 14.7 | 11.4% | 0.012 | 0.090 | 0.000 | na | na | na |
| 9 | 11.6 | 29.3% | 0.024 | 0.059 | 0.000 | na | na | na |
| 10 | 8.7 | 15.2% | 0.010 | 0.053 | 0.000 | na | na | na |
| 11 | 7.9 | 59.0% | 0.046 | 0.032 | 0.000 | 0.580 | 0.619 | 0.022 |
| 12 | 8.5 | 55.6% | 0.060 | 0.048 | 0.000 | 1.318 | 1.615 | 0.165 |
| 13 | 13.9 | 42.3% | 0.026 | 0.035 | 0.000 | 0.603 | 1.094 | 0.052 |
| 14 | 10.1 | 10.3% | 0.008 | 0.073 | 0.000 | na | na | na |
| 15 | 10.6 | 18.8% | 0.018 | 0.079 | 0.000 | na | na | na |
| 16 | 9.3 | 11.7% | 0.009 | 0.066 | 0.000 | na | na | na |
| 17 | 14.3 | 76.2% | 0.112 | 0.035 | 0.000 | 3.741 | 1.587 | 0.377 |
| 18 | 12.7 | 76.7% | 0.101 | 0.031 | 0.000 | 1.608 | 0.656 | 0.075 |
| 19 | 9.8 | 71.7% | 0.057 | 0.022 | 0.000 | 1.403 | 0.455 | 0.041 |
| 20 | 5.3 | 14.1% | 0.011 | 0.068 | 0.000 | 0.132 | 2.999 | 0.720 |
| 21 | 3.5 | 18.5% | 0.008 | 0.035 | 0.000 | na | na | na |
| 21 | 7.7 | 23.1% | 0.017 | 0.055 | 0.000 | 0.141 | 0.929 | 0.034 |
| 22 | 5.4 | 19.0% | 0.015 | 0.065 | 0.000 | 0.297 | 4.128 | 1.350 |
Del:花翠素,Cya:花青素,Pel:花葵素,M:杨梅黄素,Q:槲皮素,K:山奈黄素,Del(%):总花色素中花翠素的比例,Acyl(%):总花色苷中酰基化的色素的比例,na:未进行分析
表2
| Plant No. | acyl(%) | Del(%) | Del(mg/g) | Cya(mg/g) | Pel(mg/g) | M(mg/g) | Q(mg/g) | K(mg/g) |
| 23 | 1.1 | 42.1% | 0.036 | 0.050 | 0.000 | 0.609 | 2.929 | 0.679 |
| 24 | 22.7 | 91.0% | 0.079 | 0.008 | 0.000 | 0.964 | 0.218 | 0.018 |
| 25 | 6.1 | 61.3% | 0.048 | 0.030 | 0.000 | 0.490 | 0.468 | 0.029 |
| 26 | 8.7 | 91.3% | 0.097 | 0.009 | 0.000 | 2.053 | 0.339 | 0.123 |
| 27 | 9.4 | 59.9% | 0.060 | 0.040 | 0.000 | 1.537 | 1.631 | 0.422 |
| 28 | 5.5 | 51.2% | 0.040 | 0.038 | 0.000 | 0.688 | 0.723 | 0.038 |
| 29 | 5.1 | 61.4% | 0.056 | 0.032 | 0.003 | 0.637 | 0.537 | 0.087 |
| 30 | 7.0 | 53.3% | 0.037 | 0.032 | 0.000 | 0.706 | 1.032 | 0.051 |
| 31 | 5.7 | 58.1% | 0.071 | 0.051 | 0.000 | 1.592 | 1.478 | 0.220 |
| 32 | 4.3 | 64.6% | 0.092 | 0.050 | 0.000 | 0.849 | 0.753 | 0.035 |
| 33 | 6.4 | 61.7% | 0.042 | 0.026 | 0.000 | 0.477 | 0.468 | 0.023 |
| 34 | 8.9 | 58.8% | 0.048 | 0.034 | 0.000 | 0.646 | 0.928 | 0.063 |
| 35 | 6.2 | 11.6% | 0.007 | 0.057 | 0.000 | 0.094 | 1.132 | 0.066 |
| 36 | 7.1 | 51.2% | 0.038 | 0.036 | 0.000 | 0.911 | 1.135 | 0.079 |
| 37 | 5.8 | 50.8% | 0.029 | 0.028 | 0.000 | 0.868 | 1.105 | 0.096 |
| 38 | 5.5 | 47.0% | 0.027 | 0.023 | 0.007 | 1.366 | 1.632 | 0.105 |
| 39 | 4.9 | 67.0% | 0.044 | 0.022 | 0.000 | 0.795 | 0.586 | 0.051 |
| 40 | 0.0 | 61.1% | 0.053 | 0.033 | 0.000 | 1.310 | 1.466 | 0.259 |
| 41 | 9.6 | 71.0% | 0.074 | 0.030 | 0.000 | 0.460 | 0.337 | 0.023 |
| 42 | 1.2 | 27.6% | 0.009 | 0.024 | 0.000 | na | na | na |
| 43 | 5.2 | 13.8% | 0.013 | 0.078 | 0.000 | na | na | na |
Del:花翠素,Cya:花青素,Pel:花葵素,M:杨梅黄素,Q:槲皮素,K:山奈黄素,Del(%):总花色素中花翠素的比例,Acyl(%):总花色苷中酰基化的色素的比例,na:未进行分析
实施例4.各器官中有无导入基因存在的确认
从“WKS82”(以下称宿主)及实施例3中培育出的重组体No.5及No.24(WKS82/130-4-1及WKS82/130-9-1;以下称重组体)的花瓣、叶、茎、根及花粉中,使用DNeasy Plant Mini Kit(QIAGEN)按照制造商推荐的方法提取基因组DNA。以提取的基因组DNA为模板,通过TaKaRa Ex Taq(TaKaRa)用PCR法进行导入基因(三色堇F3’5’H基因(序列号4)、蓝猪耳5AT基因(序列号3)、大肠杆菌NPTII基因)的扩增。
进而作为内源性对照进行了月季花色素合成酶(ANS)基因的扩增。PCR的反应条件为热变性94℃5分钟,而后重复进行94℃30秒、55℃30秒、72℃1分钟的25个循环,其后,进行72℃7分钟的延伸反应。将所得到的扩增产物用琼脂糖凝胶进行电泳,通过溴化乙锭染色进行扩增片段的检测。
且作为引物,三色堇F3’5’H基因的扩增使用BP40-F2和BP40-R3,蓝猪耳5AT基因的扩增使用TAT7-50F和TAT7-R1,NPTII基因的扩增使用NPTII-F和NPTII-R,ANS基因的扩增中使用RhANS69-r1和RhANS69-m1。
三色堇F3’5’H特异性引物
BP40-F2:5’-GAG CTA GGC CAC ATG CTT A-3’(序列号:5)
BP40-R3:5’-CTT TGC GCT CAT GAC TCG T-3’(序列号:6)
蓝猪耳5AT基因特异性引物
TAT7-50F:5’-AAC AAT ATG TGC AGT CCT CGA A-3’(序列号:7)
TAT7-R1:5’-AAC TCG CAT CGC CAA CTA C-3’(序列号:8)
NPTII基因特异性引物
NPTII-F:5’-GAT TGA ACA AGA TGG ATT GCA CGC-3’(序列号:9)
NPTII-R:5’-CGA AGA ACT CCA GCA TGA GAT CCC-3’(序列号:10)
ANS特异性引物
Rh ANS 69-r1:5’-TTT GAT CTT CCC ATT GAG C-3’(序列号:11)
Rh ANS 69-m1:5’-TCC GCG GTG GGA AGA TCC CC-3’(序列号:12)
通过PCR分析的结果,在本重组体的花瓣、叶、茎的基因组中虽检测出了导入基因,但在根、花粉的基因组中未检测出这些导入基因。结果如表3及图1所示。
此外,已知花瓣、叶、茎的表皮系统、萼片、雄蕊、雌蕊来自L1层及L2层,花粉和卵细胞来自L2层,叶、茎的内部组织、根来自L3层。由于在根及花粉的基因组中未检测出导入基因,所以可表明本重组体是导入基因仅在L1层存在的嵌合体植物。
表3:重组体各器官中导入基因存在的有无
实施例5.与园艺种的人工杂交(温室内)
根据通常方法,在园艺种即将开花之前进行去雄、套袋后,在雌蕊充分成熟时的晴天的上午,使温室内栽培的宿主或实施例3中培育出的重组体No.24(WKS82/130-9-1;以下称重组体)的花粉附着。而后,为不使其他花粉附着而再次套袋,观察种子有无形成。另外,花粉使用在回收开裂前的花药后,在放入了硅胶的干燥器内室温放置1天,第二天从开裂的花药中回收的新鲜花粉。作为杂交母本,使用壮花系四季开花的月季品种“伊丽莎白女王”、丰花系四季开花的月季品种“Gold Bunny”。
杂交后经过1个月以上,对于无生理落果、可看出结实的果实确认有无种子形成。进一步对通过与重组体杂交而得到的种子,为确认后代中导入基因的传递性,使用Nucleon PHYTOPURE for PLANT DNA EXTRACTION KIT(Amersham Biosciences)从所得到的种子中提取基因组DNA,再用REPLI-g Kit(QIAGEN)将其扩增后,用PCR法检测导入基因(三色堇F3’5’H基因)。
结果如表4所示。结实率在宿主及重组体间基本无差异。进一步对与重组体杂交所得到的种子进行分析,结果从这些种子中完全未检测出导入基因。由此表明,对于花粉的受精能力,虽然宿主和重组体间无差异,但由于重组体的花粉细胞中不含有导入基因等理由,导入基因未向后代传递。
表4:与园艺种的人工杂交
实施例6.与园艺种的人工杂交(野外)
根据通常方法,在园艺种即将开花之前进行去雄、套袋后,在雌蕊充分成熟时的晴天的上午,使在野外栽培的宿主或实施例3中培育出的重组体No.24(WKS82/130-9-1;以下称重组体)花粉附着。而后,为不使其他花粉附着而再次套袋,观察种子有无形成。另外,花粉使用在回收开裂前的花药后,在放入了硅胶的干燥器内室温放置1天,第二天从开裂的花药中回收的新鲜花粉。
作为杂交母本,使用壮花系四季开花的月季品种“伊丽莎白女王”、丰花系四季开花的月季品种“Gold Bunny”。
杂交后经过了3个月以上,对于无生理落果、可看出结实的果实确认有无种子形成。进一步回收与重组体杂交后所得到的种子,4℃下低温处理3个月后进行播种。为确认这些种子中有无导入基因的传递,从所得到的实生叶中使用DNeasy Plant Mini Kit(QIAGEN)提取基因组DNA,用PCR法进行导入基因(三色堇F3’5’H基因)的检测。另外,进行了作为内源性对照基因的月季中的3-磷酸甘油醛脱氢酶(GAPDH)基因的检测。
另外,低温处理种子的情况下,通常1个月左右即可看出发芽,但经过了3个月也只确认出其一部分种子发芽。因此,对未发芽的播种种子的一部分进行再回收,使用种子进行同样的分析。从再回收的种子中使用Nucleon PHYTOPURE for PLANT DNA EXTRACTION KIT(Amersham Biosciences)提取基因组DNA,再用REPLI-g Kit(QIAGEN)将其扩增后,用PCR法进行导入基因(三色堇F3’5’H基因)的检测。
结果如表5及表6所示。结实率在宿主及重组体间基本无差异。进而将与重组体杂交后所得到的实生苗用PCR法进行分析,未从这些实生苗中检测出来自重组体的导入基因。而且,在任一种子中均未检测出来自重组体的导入基因。由此表明,花粉的受精能力虽在宿主和重组体间无差异,但由于重组体的花粉细胞中不含有导入基因等理由,所以导入基因未向后代传递。
表5.与园艺种通过人工杂交的结实率及发芽个体中导入基因的检测率
表6.通过与园艺种人工杂交而得到的种子中导入基因的检测率
*1),2):回收种子数和分析种子数的不同,是因为从本分析的对象中去除了秕子(种子中空)、未能提取DNA、用PCR分析时未看出对照基因扩增的种子而产生。
实施例7.与野生种的人工杂交(野外)
根据通常方法,在园艺种即将开花之前进行去雄、套袋后,在雌蕊充分成熟时的晴天的上午,使野外栽培的宿主或实施例3中培育出的重组体No.24(WKS82/130-9-1;以下称重组体)的花粉附着。
而后,为不使其他花粉附着而再次套袋,观察种子有无形成。另外,花粉使用在回收开裂前的花药后,在放入了硅胶的干燥器内室温放置1天,第二天从开裂的花药中回收的新鲜花粉。
作为杂交母本,野生种使用野蔷薇(R.multiflora Thunb.ex Murray)、先叶蔷薇(R.wichuraiana Crep.)、玫瑰(R.rugosa Thunb.ex Murray)。
杂交后经过2个月以上,对于无生理落果、可看出结实的果实确认种子有无形成。进一步回收所得到的种子,4℃下低温处理3个月后进行播种。为确认这些植株中有无与宿主或重组体的杂交、导入基因有无传递,从所得到的实生的叶中使用DNeasy Plant Mini Kit(QIAGEN)提取基因组DNA,用PCR法进行分析。对于有无与宿主或重组体杂交,以与四季开花性有关的基因(KSN基因)为指标,对于导入基因有无传递,以来自重组体的导入基因三色堇F3’5’H基因作为指标。且作为内源性对照基因使用月季的GAPDH基因。
已有如下报道,KSN基因是在一季开花的月季的ksn基因(具有维持茎顶的功能)中插入了约9kb的转座子后产生的,且由此该基因的表达受到抑制,茎顶中的花芽形成抑制被解除,所以,促进了花芽形成,从而形成四季开花性1)。园艺种是纯合子中具有KSN基因。另一方面,一季开花的野生种在纯合子中具有ksn基因。因此,认为在野生种(一季开花)中,KSN基因只在与园艺种杂交时才被检测出。
此外,低温处理种子的情况下,通常1个月左右即可看出发芽,而经过3个月也只确认其一部分发芽。因此,对未发芽的播种种子的一部分进行再回收,使用种子进行同样的分析。从再回收的种子中使用Nucleon PHYTOPURE for PLANT DNA EXTRACTION KIT(Amersham Biosciences)提取基因组DNA,再用REPLI-g Kit(QIAGEN)将其扩增后,用PCR法进行与宿主或重组体有无杂交、导入基因有无传递的分析。
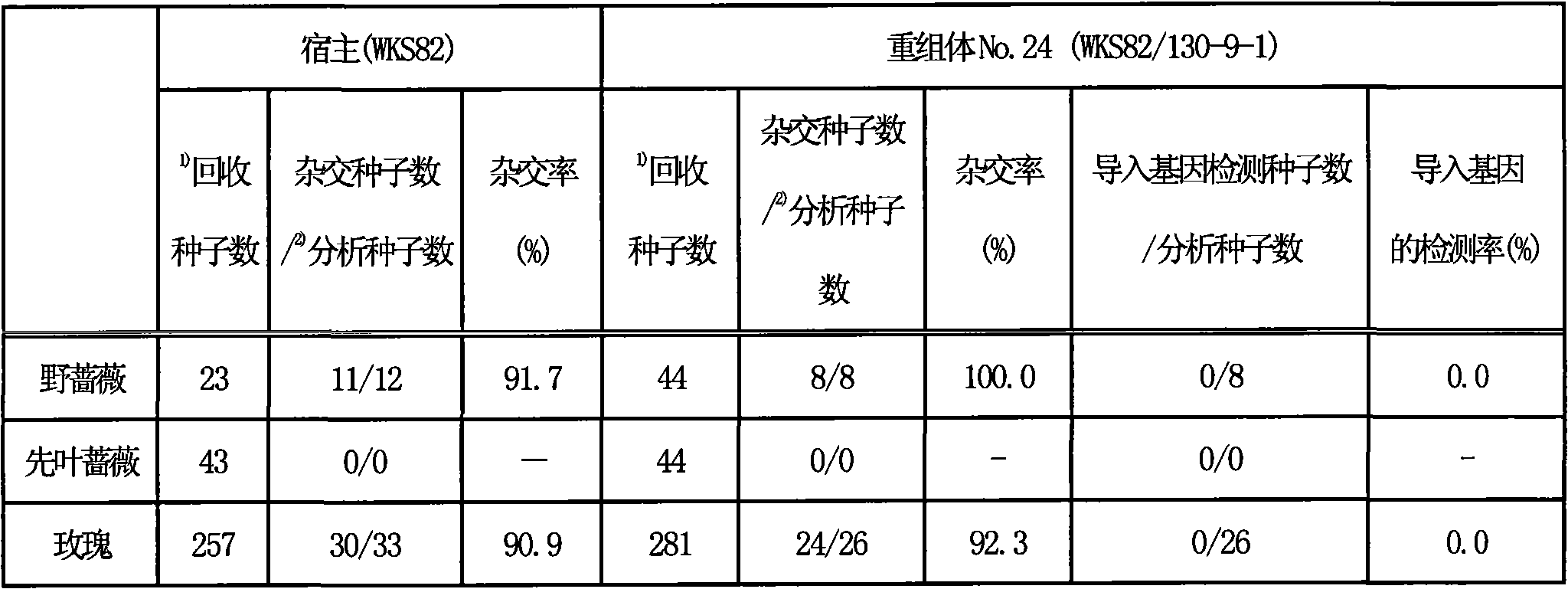
结果如表7及表8所示。以宿主、重组体的任一个作为花粉亲本时结实率均极低。将所得到的实生苗用PCR法分析,虽可确认出宿主或重组体与野生种进行了杂交,但未检测出来自重组体的导入基因。而且,再回收未发芽的播种种子,观察种子是否充实时,其几乎都是“秕子(种子中空)”,可确认形成正常的胚的个体极其少。对这些同样用PCR法分析,虽能确认宿主或重组体与野生种进行了杂交,但未检测出来自重组体的导入基因。由此,从重组体的花粉细胞中不含有导入基因等的理由来看,认为导入基因未向后代传递。
因此,即使本重组体与野生种(野蔷薇、先叶蔷薇、玫瑰)进行了杂交,但从重组体的花粉细胞中不含有导入基因是等的理由来看,可证明导入基因没有向后代传递的可能性。
而且对于先叶蔷薇,任一种子也均未能确认出正常的胚。
表7.通过与野生种(野蔷薇、先叶蔷薇、玫瑰)进行人工杂交的结实率及发芽个体中导入基因的检测率
表8.通过与野生种(野蔷薇、先叶蔷薇、玫瑰)进行人工杂交而得到的种子中导入基因的检测率
*1),2):回收种子数与分析种子数的不同是因为从本分析的对象中去除了秕子(种子中空)、未能提取DNA、用PCR分析时未看出对照基因扩增的种子而产生。
实施例8.原位(in situ)杂交
为进一步详细分析导入基因的定位,进行了原位(in situ)杂交。将5mm左右大小的花蕾沿垂直方向切成两半后,浸入甲醛固定液中固定。而后为进行脱水,将固定液按从50%乙醇~100%乙醇的顺序取代,进而取代(透明)成25%Lemosol。其后使石蜡逐渐浸润、包埋。将包埋样品用切片机切成薄片,与载玻片粘附。将载玻片进行水化,进行蛋白酶K处理、乙酰化等的预处理后,进行脱水、干燥。将DIG标记后的探针(BP40、TAT、NPTII、各基因的反义及正义探针)溶解于杂交溶液中,置于干燥的载玻片上使其反应。杂交后,洗涤载玻片,检测DIG。
如图2照片所示,导入基因仅在L1层的细胞中表达,而在L2层、L3层的细胞中不表达。由此可证明,导入基因仅存在于L1层而不存在于L2层、L3层中,因而由L2层产生的生殖细胞(花粉细胞、胚珠的细胞)中不存在导入基因。
实施例9:重组康乃馨的制备和分析
培育成导入基因仅存在于L1层的康乃馨。
重组康乃馨通过使用了农杆菌的基因导入如下制备。质粒pCGP2442(记载为Application No.US60/988,293申请日2007年11月15日)在其T-DNA区中,含有来自金鱼草的查耳酮合成酶基因的启动子控制下的来自一串红的类黄酮3’、5’-羟基化酶基因cDNA、来自矮牵牛的二氢黄酮醇4-还原酶的染色基因、来自康乃馨的花色素合成酶基因、还有作为转化用的选择标记在花椰菜花叶病毒35S启动子控制下的烟草的乙酰乳酸(Acetolactate)合成基因SURBcDNA。将其按照专利申请日本特表平11-505116中所述的方法导入农杆菌,进而导入到康乃馨品种KortinaChanel中。在所得到的重组康乃馨的花瓣中,可检测出天然康乃馨中不含有的花翠素。这表示导入基因至少在花瓣的上皮细胞中发挥作用。其中,对1系统(系统19907)进行了详细分析。此外,从系统19907中提取染色体DNA,将上述的pCGP2442的T-DNA上的基因作为探针使用,通过Southern杂交法进行分析时,可确认出导入基因被插入了染色体。
通过在含有5μg/L Glean的不含激素的MS固体培养基中植入系统19907和系统26898的茎段来制备组织培养物。4~5星期观察有无生根时,系统26898虽生根,但系统19907未生根。
而后,将从系统19907和系统26898及品种Kortina Chanel中得到的叶的切片在含有5μg/L Glean的half-strength MS固体medium with 0.5mg/L IAA和不含有Glean的half-strength MS固体medium with 0.5mg/L IAA中培养5星期。在含有5μg/L Glean的培养基中培养的系统19907和品种Kortina Chanel的叶片均发生了褐变。系统26898所得到的叶片为绿色、可见生根。
从系统19907的叶和根中,使用DNeasy Plant Mini Kit(QIAGEN公司)提取染色体DNA。以此DNA100ng为模板,使用用于扩增SuRB基因的合成引物(# 960 5’-ATT TCC GCC TCA TTA GAA GG-3’,# 1468 5’-GCC TCA TGT TTC CAT TTG TGC-3’)进行PCR。反应使用Hot Star Taq,在25μl的反应体积中进行15分钟95℃的反应后,进行96℃的反应1分钟、52℃的反应30秒,72℃的反应2分钟组成1循环的35循环,进而进行72℃的反应7分钟。将该反应物用琼脂糖凝胶电泳分析时,以来自叶的DNA为模板时,虽可观察到SURB的条带,但以来自根的DNA为模板时却未观察到SURB的条带。
已知叶由L1、L2、L3细胞组成,根由L2、L3细胞组成。由以上结果可判断,系统19907在L1细胞中有导入基因,但在L2,L3细胞中无导入基因,即系统19907是导入基因仅在L1层存在的嵌合体植物。
实施例10
对各种植物进行本发明技术的可应用性的探讨。
(1)感染矮牵牛的例子
花卉植物使用矮牵牛,导入作为外源基因的与类黄酮的合成有关的基因。
将在花椰菜花叶病毒(CaMV)35S启动子上游具有2个重复的增强子序列的El235S启动子序列(PlantCell Physiol.37,49-59(1996))、蝶豆的F3’5’H cDNA序列(如专利申请号WO 2004/020637中记载)、和胭脂碱合成酶(nos)的终止子序列导入双元载体pBinPlus(Trangenic Research,4,288-290(1995))中形成pSPB748(PlantCell Physiol.43,s227(2002)),从中将蝶豆F3’5’H cDNA与nos终止子连接的DNA片段(约2.0kb)用BamHI酶切和EcoRI的部分酶切来回收,通过导入pBluescriptII(sk-)(Stratagene公司)的BamHI/EcoRI位点,形成质粒pB-Bn。将具有6个重复的小鼠异物应答序列(XRE)的6xXRE启动子序列、GUS基因、和nos终止子导入pBluescriptII(ks+)(Stratagene)中形成pBlueSXXREGUS(Kodama(2003)Molecular mechanisms of chemical-inducible gene expression in higher plants for monitoring and remediation ofenvironmental contaminants,Diss.),从中将GUS基因和nos终止子的基因盒用XbaI和KpnI切出,在同一位点,插入从pB-Bn中用XbaI和KpnI酶切而切出的蝶豆F3’5’H和nos终止子连接的DNA片段(约2.0kb),得到pB-X6Bn。在双元载体pBin19上将在CaMV35S启动子和nos终止子组成的表达单元2组中分别附加了苜蓿花叶病毒的5’非翻译(UTR)序列的AhRV及Arnt正向插入,通过在插入后的载体pSKAVAt(Kodama(2003))的SalI位点上导入将pB-X6Bn用XhoI酶切而切出的6xXRE启动子序列、蝶豆F3’5’H cDNA、和nos终止子序列的基因盒(2.2kb),从而构建pSPB1459。
将pSPB1459导入根癌农杆菌Ag10株(BioTechnology 9,963-967(1991)),将矮牵牛(品种PL,Skr4 xSw63(与Nature,366,276-279相同))使用叶盘用农杆菌法进行转化。质粒向农杆菌中的导入、转化方法用公知的方法(Plant J.5,p81-92(1994))。品种PL因缺少类黄酮3’,5’-羟基化酶基因、类黄酮3’-羟基化酶基因而使花色为白色~浅粉色,但用于本实验目的的矮牵牛品种不限定PL。获得38系统独立的转化矮牵牛PAB。
(2):感染蓝猪耳的例子其1
花卉植物使用蓝猪耳,导入作为外源基因的选择性标记基因的GFP基因。
通过将CaMV35S-sGFP(S65T)-NOS3’(Curr.Biol.6,325-330(1996))用BamHI和EcoRI酶切,将sGFP基因和nos终止子基因的连接DNA(1.0kb)导入pBluescriptII(sk-)的BamHI/EcoRI位点,而构建质粒pB-Gn。从pBlueSXXREGUS-last中将GUS基因和nos终止子的基因盒用XbaI和KpnI切出,在相同位点插入从pB-Gn中用XbaI和KpnI酶切而切出的sGFP和nos终止子的基因盒(1.0kb),以构建pB-X6Gn。在pSKAVAt的SalI位点,导入将pB-X6Gn用XhoI酶切而切出的6xXRE启动子、sGFP和nos终止子的基因盒(1.2kb),构建pSPB1458。
将pSPB1458导入根癌农杆菌Ag10株中,使用叶盘用农杆菌法转化到蓝猪耳(品种Summer Wave Blue:SWB(三得利花卉株式会社))叶盘中。蓝猪耳的转化用公知的方法(Mol.Breeding 6,239-246(2000))。SWB的花色为蓝色,但用于本实验目的的蓝猪耳品种不限定于SWB。获得40系统独立的转化蓝猪耳系统TAG。
(3)感染蓝猪耳的例子其2
花卉植物使用蓝猪耳,导入作为外源基因的与类黄酮的合成有关的基因。
根据WO2005-059141中公开的方法,以蓝猪耳品种Summer Wave Blue为宿主植物,通过使用与上述同样的农杆菌的方法,导入具有与噢哢合成有关的基因的表达盒、和用于通过RNAi抑制花色苷合成体系基因表达的表达盒的构建物(pSFL307或pSFL308)。所得到的蓝猪耳中,花色由兰变成黄色。
(4)感染烟草、马鞭草、赛亚麻的例子
花卉植物使用烟草、马鞭草或赛亚麻,导入作为外源基因的转录因子基因。
将在磷酸饥饿条件下表达的拟南芥的PHR1基因(Genes & Development 15:2122-2133(2001))使用TOPO-TACloningKit(invitrogen株式会社)、根据解说书亚克隆到pCR2.1载体。将使用引物PHRf(5’-ATGGAGGCTCGTCCAGTTCAT-3’)和PHRr(5’-TCAATTATCGATTTTGGGACGC-3’)的PCR反应扩增的产物进行亚克隆,作为pSPB1892。具有将连接了35S启动子的增强子序列和甘露碱合成酶启动子的(Mac)启动子和甘露碱合成酶(mas)终止子的双元载体pSPB2311用SmaI切割,得到pSPB2311A。将pSPB1892用EcoRI切割后平滑化的片段插入pSPB2311A,得到pSPB2314。
而后,根据公知的方法(Plant J.5,81,1994)使用pSPB1898转化农杆菌(菌株:Ag10),使用具有此pSPB1898的转化体农杆菌,进行烟草、马鞭草、赛亚麻的转化。烟草、马鞭草、赛亚麻的转化分别根据公知的方法(Science 227,1229,1985;Plant Cell Rep.21,459,2003;PlantBiotech.23,19,2006)进行。对于所得到的植物体的基因导入,从各植物体的叶中提取DNA,以PHR1基因为模板,通过PCR来进行确认。得到烟草11个体、马鞭草16个体、赛亚麻1个体的PHR1转基因植物。
(5)感染非洲凤仙花、四季秋海棠的例子
花卉植物使用非洲凤仙花或四季秋海棠,导入作为外源基因的转录因子基因。
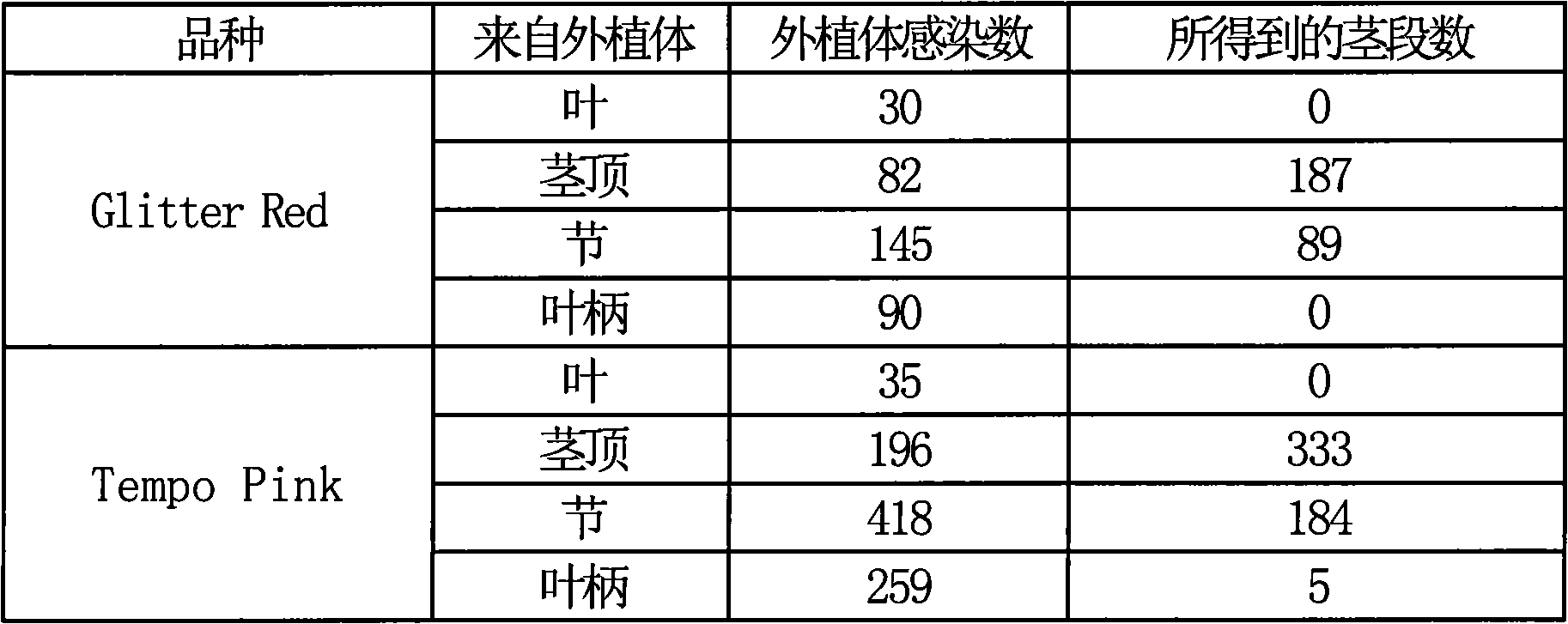
非洲凤仙花(Impatiens walleriana)的转化原则上根据US Patent6,121,511、使用品种Glitter Red(日本坂田种苗株式会社)和Tempo Pink(日本泷井种苗株式会社)进行。将从试管苗上切出的茎顶、节、叶柄、叶片用预培养液体培养基(添加1mg/L TDZ的MS培养基)预培养5天后,在预培养固体培养基(添加0.05mg/L NAA、6mg/L Zeatin、0.3%结冷胶的MS培养基)中静置48小时。其后,用导入了pSPB2314的农杆菌(菌株Ag10)感染,在选择培养基(添加0.05mg/L NAA、6mg/L Zeatin、100mg/LKanamycin、500mg/L Carbenicillin、100mg/L Cefotaxime、0.3%结冷胶的MS培养基)中培养4~8星期,得到茎段(表9)。叶片容易褐变,所以未得到茎段。茎顶及节上,由1个外植体可得到多个茎段,但也包含多个假阳性。从叶柄发出的茎段的出现时间较晚、数量少,但最确实。
四季秋海棠(Begonia Semperflorens)的转化使用品种AmbassadorWhite和Ambassador Scarlett(日本坂田种苗株式会社)进行。从试管苗切出叶片和叶柄,用导入了pSPB2314的农杆菌(菌株Ag10)感染,在共培养培养基(添加0.5mg/L IAA、0.1mg/L TDZ、0.5%PVP、2mg/L AgNO3、200μM Acetosyringone、0.3%结冷胶的MS培养基)上暗培养3天。其后,在预选择培养基(添加1mg/L BAP、1mg/L Zeatin、0.1mg/L IAA、500mg/L Timentin、50μM Acetosyringone、0.25%结冷胶的MS培养基)中培养3~5天,在选择培养基1(添加2mg/L TDZ、0.1mg/L NAA、100mg/L Kanamycin、500mg/L Timentin、0.4%琼脂的MS培养基)中连续培养2星期,在选择培养基2(添加0.2mg/L BAP、0.1mg/L NAA、100mg/L Kanamycin、500mg/L Timentin、0.4%琼脂的MS培养基)中连续培养2星期,在选择培养基3(添加100mg/L Kanamycin、500mg/L Timentin、0.4%琼脂的MS培养基)中连续培养3星期。其间形成的茎段生长到直径5mm以上时,削取周围的组织,移到选择培养基4(添加150mg/L Kanamycin、500mg/L Timentin、0.4%琼脂的MS培养基)中,进一步培养2~3星期后,移入生根培养基(添加100mg/L Kanamycin、500mg/L Timentin、0.4%琼脂的MS培养基)中得到生根茎段(表10)。
表9.非洲凤仙花的茎段数
表10.四季秋海棠的茎段数
| 品种 | 外植体感染数 | 所得到的茎段数 |
| Ambassador White | 940 | 13 |
| Ambassador Scarlett | 805 | 2 |
由以上可知,月季、康乃馨以外的花卉植物、例如矮牵牛、蓝猪耳、烟草、马鞭草、赛亚麻、非洲凤仙花、四季秋海棠等也可使用农杆菌导入外源基因。作为导入的外源基因,不限于此处列举的具体的基因,只要是导入后在L1细胞中发挥功能的基因,不论是何种基因,均可使用同样的方法导入这些花卉植物中。因本发明的技术可适应于可使用农杆菌导入外源基因的花卉植物,所以这些植物也可培育成本发明的花卉植物、即导入基因仅在转化体植物的一部分细胞中存在,而在其他细胞中不存在的花卉植物。
根据本发明公开的方法培育出的转化体植物是在包含生殖细胞等的L2细胞层中不具有导入基因,而仅在L1层的细胞中具有导入基因的嵌合体植物。因此种转化体的生殖细胞中不具有导入基因,所以,可阻止由没有权限的第三者自由地将该基因重组植物作为杂交亲本利用的可能性。
此外,对于基因重组植物,在担心导入基因向自然界扩散时,发现通过培育此种生殖细胞中不携带导入基因的基因重组植物,即可完全否认导入基因扩散的可能性。因此,对于欲将基因重组植物进行产业利用的人,可减轻基因重组植物用于商业利用时批准申请(在日本国内,根据“通过规范基因重组生物等的使用等以确保生物多样性的相关法律(卡塔赫纳法)”的生物多样性影响评价等)所造成的负担。
序列表
<110>International Flower Developments Proprietary Limited
<120>周缘嵌合体转基因月季的培育方法
(Method for producing periclinal chimera transgenic rose)
<130>V568-PCT
<160>12
<210>1
<211>17
<212>DNA
<213>人工序列(Artificial Sequence)
<220>
<221>
<222>
<223>ATC引物(ATC primer)
<400>1
gayttyggit ggggiaa 17
<210>2
<211>23
<212>DNA
<213>人工序列(Artificial Sequence)
<220>
<221>
<222>
<223>寡聚dT引物(Oligo dT primer)
<400>2
tttttttttt tttttttctc gag 23
<210>3
<211>1808
<212>DNA
<213>蓝猪耳
<220>
<221>
<222>
<223>
<400>3
cttcaaagcc aaaaagaaac aattaatca atg gct gtt gaa gcc ccc aaa aca 53
Met Ala Val Glu Ala Pro Lys Thr
1 5
ata tgt gca gtc ctc gaa aac tct ctt att aca cca caa agt acc gat 101
Ile Cys Ala Val Leu Glu Asn Ser Leu Ile Thr Pro Gln Ser Thr Asp
10 15 20
aca gaa caa act ctt tca ctc aca ttc ttt gac atc aaa tgg gtt cat 149
Thr Glu Gln Thr Leu Ser Leu Thr Phe Phe Asp Ile Lys Trp Val His
25 30 35 40
ttt cat cca atg caa tgc ctt gtg ttg tac aac ttc cca tgt tct aag 197
Phe His Pro Met Gln Cys Leu Val Leu Tyr Asn Phe Pro Cys Ser Lys
45 50 55
tca cat ttt ctc gaa gcc aca gtt ccg agc ttc aaa tca tca ctc tcc 245
Ser His Phe Leu Glu Ala Thr Val Pro Ser Phe Lys Ser Ser Leu Ser
60 65 70
aaa act ctc aga cac tat ctt cca tta tca gga aac tta tac tat cca 293
Lys Thr Leu Arg His Tyr Leu Pro Leu Ser Gly Asn Leu Tyr Tyr Pro
75 80 85
aac ccg acc cat gac atg gat gat gat gaa tcg aac atg ccc gag atc 341
Asn Pro Thr His Asp Met Asp Asp Asp Glu Ser Asn Met Pro Glu Ile
90 95 100
cgt tat aaa cct ggc gac tcg gtt tct cta acc gtt gca gag tac ttc 389
Arg Tyr Lys Pro Gly Asp Ser Val Ser Leu Thr Val Ala Glu Tyr Phe
105 110 115 120
tcc ggt cat gaa gac aat acg act act gaa gaa tac ttc aat tac ctc 437
Ser Gly His Glu Asp Asn Thr Thr Thr Glu Glu Tyr Phe Asn Tyr Leu
125 130 135
act gga aat ttc cag aga gat tgc gat caa ttc tat gat ctc tta ccc 485
Thr Gly Asn Phe Gln Arg Asp Cys Asp Gln Phe Tyr Asp Leu Leu Pro
140 145 150
gat ttt cga gac ccg gaa acc gaa tcc aat tgc aca gta atc cca ctt 533
Asp Phe Arg Asp Pro Glu Thr Glu Ser Asn Cys Thr Val Ile Pro Leu
155 160 165
ata gca gtt caa atc aca ctc ttt cca ggt gct ggg ata tgt ctg ggg 581
Ile Ala Val Gln Ile Thr Leu Phe Pro Gly Ala Gly Ile Cys Leu Gly
170 175 180
gtc atc aac agt cac gta gtt ggc gat gcg agt tcc ata gtg gga ttc 629
Val Ile Asn Ser His Val Val Gly Asp Ala Ser Ser Ile Val Gly Phe
185 190 195 200
atc aaa gct tgg agt aaa gtt gca atg tat gaa gac gat gaa gag att 677
Ile Lys Ala Trp Ser Lys Val Ala Met Tyr Glu Asp Asp Glu Glu Ile
205 210 215
cta gct aac aac aat ttg att cca tct tat gac aga tca gtc gtg aaa 725
Leu Ala Asn Asn Asn Leu Ile Pro Ser Tyr Asp Arg Ser Val Val Lys
220 225 230
gat cca aaa ggg atc aaa tct ttg ctc tgg aac aag atg aag aac gtg 773
Asp Pro Lys Gly Ile Lys Ser Leu Leu Trp Asn Lys Met Lys Asn Val
235 240 245
aaa tat caa ccc caa ccc gca aaa cat ctc cca aca aac aag gtc cga 821
Lys Tyr Gln Pro Gln Pro Ala Lys His Leu Pro Thr Asn Lys Val Arg
250 255 260
gcc aca tac acc ttg aga aag aac gat atc gag agg ctg aaa acc cga 869
Ala Thr Tyr Thr Leu Arg Lys Asn Asp Ile Glu Arg Leu Lys Thr Arg
265 270 275 280
atc cga tcc aag aaa cca ggc aca acc tgc tta tca tct ttc aca atc 917
Ile Arg Ser Lys Lys Pro Gly Thr Thr Cys Leu Ser Ser Phe Thr Ile
285 290 295
gca aca gcc tat gct tgg aca tgc ctt gca aaa tct gca gca gaa gct 965
Ala Thr Ala Tyr Ala Trp Thr Cys Leu Ala Lys Ser Ala Ala Glu Ala
300 305 310
gaa gaa caa gta gtc caa gac agt gac gac gag cac ttg ctc atg ccc 1013
Glu Glu Gln Val Val Gln Asp Ser Asp Asp Glu His Leu Leu Met Pro
315 320 325
gtt gat ttg aga cca aga ata gat cct cca tta cca cct tct tac ttt 1061
Val Asp Leu Arg Pro Arg Ile Asp Pro Pro Leu Pro Pro Ser Tyr Phe
330 335 340
gga aac tgc gtt ctt cca tct ttt gcg aaa acg acg cat ggg ctt ttg 1109
Gly Asn Cys Val Leu Pro Ser Phe Ala Lys Thr Thr His Gly Leu Leu
345 350 355 360
aaa gga gag tta ggg ctt ttt aat gca gtg gaa gtg att agt gat gtc 1157
Lys Gly Glu Leu Gly Leu Phe Asn Ala Val Glu Val Ile Ser Asp Val
365 370 375
att acc ggt atc gtt agc aag aaa tat gac ttg ttc aaa gac tta gac 1205
Ile Thr Gly Ile Val Ser Lys Lys Tyr Asp Leu Phe Lys Asp Leu Asp
380 385 390
aga caa ggt gag att ttt cgt gcc ttg ttc gga aaa cga gtg ttg gcg 1253
Arg Gln Gly Glu Ile Phe Arg Ala Leu Phe Gly Lys Arg Val Leu Ala
395 400 405
atc atg ggt tcg cct aag ttc gat ctc tac gaa gtt gat ttc ggg tgg 1301
Ile Met Gly Ser Pro Lys Phe Asp Leu Tyr Glu Val Asp Phe Gly Trp
410 415 420
ggt aag ccg aag aag att gaa cct gtg tcc att gat aga gag agg acg 1349
Gly Lys Pro Lys Lys Ile Glu Pro Val Ser Ile Asp Arg Glu Arg Thr
425 430 435 440
act atg tgg att agc aag tct ggc gag ttt gag ggt gga ttg gag att 1397
Thr Met Trp Ile Ser Lys Ser Gly Glu Phe Glu Gly Gly Leu Glu Ile
445 450 455
ggt ttt tct ttc aat aag aag aaa atg gat gct ttt ggc gag tgt ttt 1445
Gly Phe Ser Phe Asn Lys Lys Lys Met Asp Ala Phe Gly Glu Cys Phe
460 465 470
aac agc ggt ttg aag gat att taatttaaaa aattgtttag ctttgatgca 1496
Asn Ser Gly Leu Lys AspIle
475
tgcgttttat atatgttgtg aaataatgtg gtgtgcaata actagagtaa ctttaggtta 1556
ataaattcgg tttttctgtt aaatctggat gattcgtgca agcaaactgt cgatgcgttg 1616
gatggatgtc gggtggtgtg gagattgttg aagaaggaaa tggatgcttt ttttatggtg 1676
gtttgaagga tttgaatgtg tagattattg gtttattgag gttgtttata tttgtgtatg 1736
ttgtttatgc atgaaaaata tttagatccc aacattttat gtatgacgtg gtttaatatt 1796
tcgatttcga tc 1808
<210>4
<211>1781
<212>DNA
<213>三色堇
<220>
<221>
<222>
<223>
<400>4
gacaac atg gca att cta gtc acc gac ttc gtt gtc gcg gct ata att 48
Met Ala Ile Leu Val Thr Asp Phe Val Val Ala Ala Ile Ile
1 5 10
ttc ttg atc act cgg ttc tta gtt cgt tct ctt ttc aag aaa cca acc 96
Phe Leu Ile Thr Arg Phe Leu Val Arg Ser Leu Phe Lys Lys Pro Thr
15 20 25 30
cga ccg ctc ccc ccg ggt cct ctc ggt tgg ccc ttg gtg ggc gcc ctc 144
Arg Pro Leu Pro Pro Gly Pro Leu Gly Trp Pro Leu Val Gly Ala Leu
35 40 45
cct ctc cta ggc gcc atg cct cac gtc gca cta gcc aaa ctc gct aag 192
Pro Leu Leu Gly Ala Met Pro His Val Ala Leu Ala Lys Leu Ala Lys
50 55 60
aag tat ggt ccg atc atg cac cta aaa atg ggc acg tgc gac atg gtg 240
Lys Tyr Gly Pro Ile Met His Leu Lys Met Gly Thr Cys Asp Met Val
65 70 75
gtc gcg tcc acc ccc gag tcg gct cga gcc ttc ctc aaa acg cta gac 288
Val Ala Ser Thr Pro Glu Ser Ala Arg Ala Phe Leu Lys Thr Leu Asp
80 85 90
ctc aac ttc tcc aac cgc cca ccc aac gcg ggc gca tcc cac cta gcg 336
Leu Asn Phe Ser Asn Arg Pro Pro Asn Ala Gly Ala Ser His Leu Ala
95 100 105 110
tac ggc gcg cag gac tta gtc ttc gcc aag tac ggt ccg agg tgg aag 384
Tyr Gly Ala Gln Asp Leu Val Phe Ala Lys Tyr Gly Pro Arg Trp Lys
115 120 125
act tta aga aaa ttg agc aac ctc cac atg cta ggc ggg aag gcg ttg 432
Thr Leu Arg Lys Leu Ser Asn Leu His Met Leu Gly Gly Lys Ala Leu
130 135 140
gat gat tgg gca aat gtg agg gtc acc gag cta ggc cac atg ctt aaa 480
Asp Asp Trp Ala Asn Val Arg Val Thr Glu Leu Gly His Met Leu Lys
145 150 155
gcc atg tgc gag gcg agc cgg tgc ggg gag ccc gtg gtg ctg gcc gag 528
Ala Met Cys Glu Ala Ser Arg Cys Gly Glu Pro Val Val Leu Ala Glu
160 165 170
atg ctc acg tac gcc atg gcg aac atg atc ggt caa gtg ata ctc agc 576
Met Leu Thr Tyr Ala Met Ala Asn Met Ile Gly Gln Val Ile Leu Ser
175 180 185 190
cgg cgc gtg ttc gtg acc aaa ggg acc gag tct aac gag ttc aaa gac 624
Arg Arg Val Phe Val Thr Lys Gly Thr Glu Ser Asn Glu Phe Lys Asp
195 200 205
atg gtg gtc gag ttg atg acg tcc gcc ggg tac ttc aac atc ggt gac 672
Met Val Val Glu Leu Met Thr Ser Ala Gly Tyr Phe Asn Ile Gly Asp
210 215 220
ttc ata ccc tcg atc gct tgg atg gat ttg caa ggg atc gag cga ggg 720
Phe Ile Pro Ser Ile Ala Trp Met Asp Leu Gln Gly Ile Glu Arg Gly
225 230 235
atg aag aag ctg cac acg aag ttt gat gtg tta ttg acg aag atg gtg 768
Met Lys Lys Leu His Thr Lys Phe Asp Val Leu Leu Thr Lys Met Val
240 245 250
aag gag cat aga gcg acg agt cat gag cgc aaa ggg aag gca gat ttc 816
Lys Glu His Arg Ala Thr Ser His Glu Arg Lys Gly Lys Ala Asp Phe
255 260 265 270
ctc gac gtt ctc ttg gaa gaa tgc gac aat aca aat ggg gag aag ctt 864
Leu Asp Val Leu Leu Glu Glu Cys Asp Asn Thr Asn Gly Glu Lys Leu
275 280 285
agt att acc aat atc aaa gct gtc ctt ttg aat cta ttc acg gcg ggc 912
Ser Ile Thr Asn Ile Lys Ala Val Leu Leu Asn Leu Phe Thr Ala Gly
290 295 300
acg gac aca tct tcg agc ata atc gaa tgg gcg tta acg gag atg atc 960
Thr Asp Thr Ser Ser Ser Ile Ile Glu Trp Ala Leu Thr Glu Met Ile
305 310 315
aag aat ccg acg atc tta aaa aag gcg caa gag gag atg gat cga gtc 1008
Lys Asn Pro Thr Ile Leu Lys Lys Ala Gln Glu Glu Met Asp Arg Val
320 325 330
atc ggt cgt gat cgg agg ctg ctc gaa tcg gac ata tcg agc ctc ccg 1056
Ile Gly Arg Asp Arg Arg Leu Leu Glu Ser Asp Ile Ser Ser Leu Pro
335 340 345 350
tac cta caa gcc att gct aaa gaa acg tat cgc aaa cac ccg tcg acg 1104
Tyr Leu Gln Ala Ile Ala Lys Glu Thr Tyr Arg Lys His Pro Ser Thr
355 360 365
cct ctc aac ttg ccg agg att gcg atc caa gca tgt gaa gtt gat ggc 1152
Pro Leu Asn Leu Pro Arg Ile Ala Ile Gln Ala Cys Glu Val Asp Gly
370 375 380
tac tac atc cct aag gac gcg agg ctt agc gtg aac att tgg gcg atc 1200
Tyr Tyr Ile Pro Lys Asp Ala Arg Leu Ser Val Asn Ile Trp Ala Ile
385 390 395
ggt cgg gac ccg aat gtt tgg gag aat ccg ttg gag ttc ttg ccg gaa 1248
Gly Arg Asp Pro Asn Val Trp Glu Asn Pro Leu Glu Phe Leu Pro Glu
400 405 410
aga ttc ttg tct gaa gag aat ggg aag atc aat ccc ggt ggg aat gat 1296
Arg Phe Leu Ser Glu Glu Asn Gly Lys Ile Asn Pro Gly Gly Asn Asp
415 420 425 430
ttt gag ctg att ccg ttt gga gcc ggg agg aga att tgt gcg ggg aca 1344
Phe Glu Leu Ile Pro Phe Gly Ala Gly Arg Arg Ile Cys Ala Gly Thr
435 440 445
agg atg gga atg gtc ctt gta agt tat att ttg ggc act ttg gtc cat 1392
Arg Met Gly Met Val Leu Val Ser Tyr Ile Leu Gly Thr Leu Val His
450 455 460
tct ttt gat tgg aaa tta cca aat ggt gtc gct gag ctt aat atg gat 1440
Ser Phe Asp Trp Lys Leu Pro Asn Gly Val Ala Glu Leu Asn Met Asp
465 470 475
gaa agt ttt ggg ctt gca ttg caa aag gcc gtg ccg ctc tcg gcc ttg 1488
Glu Ser Phe Gly Leu Ala Leu Gln Lys Ala Val Pro Leu Ser Ala Leu
480 485 490
gtc agc cca cgg ttg gcc tca aac gcg tac gca acc tgagctaatg 1534
Val Ser Pro Arg Leu Ala Ser Asn Ala Tyr Ala Thr
495 500 505
ggctgggcct agttttgtgg gccttaattt agagactttt gtgttttaag gtgtgtactt 1594
tattaattgg gtgcttaaat gtgtgtttta atttgtattt atggttaatt atgactttat 1654
tgtataatta tttatttttc ccttctgggt attttatcca tttaattttt cttcagaatt 1714
atgatcatag ttatcagaat aaaattgaaa ataatgaatc ggaaaaaaaa aaaaaaaaaa 1774
aaaaaaa 1781
<210>5
<211>19
<212>DNA
<213>人工序列(Artificial Sequence)
<220>
<221>
<222>
<223>BP40-F2引物(BP40-F2 primer)
<400>5
gagctaggcc acatgctta 19
<210>6
<211>19
<212>DNA
<213>人工序列(Artificial Sequence)
<220>
<221>
<222>
<223>BP40-R3引物(BP40-R3primer)
<400>6
ctttgcgctc atgactcgt 19
<210>7
<211>22
<212>DNA
<213>人工序列(Artificial Sequence)
<220>
<221>
<222>
<223>TAT7-50F引物(TAT7-50F primer)
<400>7
aacaatatgt gcagtcctcg aa 22
<210>8
<211>19
<212>DNA
<213>人工序列(Artificial Sequence)
<220>
<221>
<222>
<223>ATC引物(ATC primer)
<400>8
aactcgcatc gccaactac 19
<210>9
<211>24
<212>DNA
<213>人工序列(Artificial Sequence)
<220>
<221>
<222>
<223>ATC引物(ATC primer)
<400>9
gattgaacaa gatggattgc acgc 24
<210>10
<211>24
<212>DNA
<213>人工序列(Artificial Sequence)
<220>
<221>
<222>
<223>ATC引物(ATC primer)
<400>10
cgaagaactc cagcatgaga tccc 24
<210>11
<211>19
<212>DNA
<213>人工序列(Artificial Sequence)
<220>
<221>
<222>
<223>Rh ANS 69-r1引物(Rh ANS 69-r1 primer)
<400>11
tttgatcttc ccattgagc 19
<210>12
<211>20
<212>DNA
<213>人工序列(Artificial Sequence)
<220>
<221>
<222>
<223>ATC引物(ATC primer)
<400>12
tccgcggtgg gaagatcccc 20
Claims (30)
1.一种花卉植物,其特征在于,一部分细胞中含有外源基因,而其他细胞中不含有外源基因。
2.根据权利要求1中所述的花卉植物,其中,所述一部分细胞构成一部分的细胞层。
3.根据权利要求1或2中所述的花卉植物,其中,所述其他细胞为花粉细胞或胚珠细胞。
4.根据权利要求1或2中所述的花卉植物,其中,所述其他细胞为构成L2层的细胞。
5.根据权利要求2或3中所述的花卉植物,其中,所述一部分细胞层为L1层、或L1层和L3层。
6.根据权利要求1~5中所述的花卉植物,其中,花卉植物为可通过农杆菌介导而导入外源基因的花卉植物。
7.根据权利要求6中所述的花卉植物,其中,花卉植物为月季、康乃馨、矮牵牛、蓝猪耳、烟草、马鞭草、赛亚麻、菊花、百合、牵牛花、金鱼草、仙客来、兰花、洋桔梗、小苍兰、非洲菊、唐菖蒲、霞草、长寿花、天竺葵、老鹳草、郁金香、菜籽、马铃薯、西红柿、毛白杨、香蕉、蓝桉、番薯、大豆、苜蓿、鲁冰花、花椰菜中的任一个。
8.根据权利要求1~7中任一项所述的花卉植物,其中,所述外源基因是导入后在L1层的细胞中发挥功能的基因。
9.根据权利要求8中所述的花卉植物,其中,所述外源基因是与花色有关的基因。
10.根据权利要求9中所述的花卉植物,其中,所述外源基因是与类黄酮的合成有关的基因。
11.根据权利要求10中所述的花卉植物,其中,所述外源基因是来自堇菜科植物的类黄酮3’,5’-羟基化酶基因、来自玄参科植物的芳香族酰基转移酶基因、来自一串红的类黄酮3’、5’-羟基化酶基因cDNA、来自矮牵牛的二氢黄酮醇4-还原酶的染色基因、来自康乃馨的花色素合成酶基因中的一个~多个基因。
12.根据权利要求8中所述的花卉植物,其中,所述外源基因是选择性标记的基因、或编码转录因子的基因。
13.根据权利要求7中所述的花卉植物,其中,花卉植物为月季。
14.根据权利要求13中所述的花卉植物,其中,所述月季为Rosa hybrida。
15.根据权利要求14中所述的花卉植物,其中,所述月季为杂交香水月季、丰花月季或微型月季。
16.根据权利要求13~15中任一项所述的花卉植物,其中,所述外源基因是与花色有关的基因。
17.根据权利要求16中任一项所述的花卉植物,其中,所述外源基因是与类黄酮的合成有关的基因。
18.根据权利要求17中所述的花卉植物,其中,所述外源基因是来自堇菜科植物的类黄酮3’,5’-羟基化酶基因、来自玄参科植物的芳香族酰基转移酶基因中的任一个或其两者。
19.根据权利要求18中所述的花卉植物,其中,所述堇菜科植物为堇菜科三色堇。
20.根据权利要求18中所述的花卉植物,其中,所述玄参科植物为玄参科蓝猪耳。
21.根据权利要求13~20中任一项所述的花卉植物,其中,与基因导入前的月季相比,花色向蓝色方向改变。
22.根据权利要求7中所述的花卉植物,其中,花卉植物为康乃馨。
23.根据权利要求22中所述的花卉植物,其中,所述康乃馨为中小轮品系或大轮品系。
24.根据权利要求22或23中所述的花卉植物,其中,所述外源基因是与花色有关的基因。
25.根据权利要求24中所述的花卉植物,其中,所述外源基因是与类黄酮的合成有关的酶的基因。
26.根据权利要求25中所述的花卉植物,其中,所述外源基因是来自一串红的类黄酮3’、5’-羟基化酶基因cDNA、来自矮牵牛的二氢黄酮醇4-还原酶的染色基因、来自康乃馨的花色素合成酶基因中的一个~多个基因。
27.根据权利要求22~26中任一项所述的花卉植物,其中,与基因导入前的康乃馨相比,花色向蓝色方向改变。
28.权利要求1~27中任一项所述的花卉植物的组织及其营养增殖体,其特征在于,其与所述花卉植物具有相同性质。
29.一种方法,其特征在于,其包含在权利要求1~27中任一项所述的花卉植物的制造方法中,将外源基因通过农杆菌介导而导入植物,选择该外源基因仅在一部分细胞中存在的植物的工序。
30.一种方法,其特征在于,通过培育出权利要求3~27中任一项所述的生殖细胞中不携带外源基因的花卉植物,从而防止导入基因向自然界扩散。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP089259/2007 | 2007-03-29 | ||
| JP2007089259 | 2007-03-29 | ||
| JP202291/2007 | 2007-08-02 | ||
| JP2007202291 | 2007-08-02 | ||
| PCT/JP2008/056746 WO2008120820A1 (ja) | 2007-03-29 | 2008-03-28 | 表層キメラ形質転換植物の作出方法 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN101675161A true CN101675161A (zh) | 2010-03-17 |
Family
ID=39808400
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN200880010382A Pending CN101675161A (zh) | 2007-03-29 | 2008-03-28 | 表层嵌合体(surface chimera)转基因植物的培育方法 |
Country Status (11)
| Country | Link |
|---|---|
| US (2) | US8183434B2 (zh) |
| EP (1) | EP2128255B1 (zh) |
| JP (2) | JPWO2008120820A1 (zh) |
| KR (1) | KR101458578B1 (zh) |
| CN (1) | CN101675161A (zh) |
| AU (1) | AU2008233555B2 (zh) |
| CA (1) | CA2682095C (zh) |
| CO (1) | CO6231053A2 (zh) |
| EC (1) | ECSP099661A (zh) |
| TW (1) | TW200845888A (zh) |
| WO (1) | WO2008120820A1 (zh) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN108330146A (zh) * | 2018-01-31 | 2018-07-27 | 天津大学 | 催化谷氨酰胺合成靛蓝获得蓝色花卉的转基因方法 |
| CN116584386A (zh) * | 2023-05-24 | 2023-08-15 | 北京林业大学 | 一种用于杨梅的组培培养基及杨梅种子萌发方法和杨梅组培快繁方法 |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2756087C (en) * | 2009-03-27 | 2017-04-18 | Suntory Holdings Limited | Compound contained in blue rose |
| CN104644715A (zh) * | 2013-11-22 | 2015-05-27 | 房世平 | 野菊花黄酮类化合物的复合酶法提取工艺 |
| MX2019007628A (es) | 2016-12-23 | 2019-09-06 | Keygene Nv | Rasgos complejos usando tecnologia de tejidos. |
| AU2017382035B2 (en) * | 2016-12-23 | 2024-05-23 | Keygene N.V. | Methods for the production of seed with improved seed germination properties |
| CN116042692A (zh) * | 2022-09-30 | 2023-05-02 | 山东和正生态农业开发有限公司 | 一种萱草的遗传转化方法及其应用 |
Family Cites Families (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US988293A (en) | 1905-11-15 | 1911-03-28 | John R Moffitt | Pulverizing-mill. |
| EP0536327A1 (en) * | 1990-06-25 | 1993-04-14 | Florigene Europe B.V. | Rose plants and methods for their production and genetic transformation |
| US5480789A (en) | 1991-04-01 | 1996-01-02 | Florigene Europe B.V. | Genetically transformed rose plants and methods for their production |
| KR100245488B1 (ko) | 1992-03-02 | 2000-02-15 | 히라타 다다시 | 신규 식물 유전자 |
| JPH10501139A (ja) * | 1994-06-10 | 1998-02-03 | ダニスコ エイ/エス | グアーの形質転換 |
| BR9508341A (pt) | 1994-07-29 | 1997-08-12 | Pioneer Hi Bred Int | Processo para produzir plantas de cereal transgênicas |
| JPH0970290A (ja) | 1995-02-17 | 1997-03-18 | Suntory Ltd | アシル基転移活性を有する蛋白質をコードする遺伝子 |
| AUPN298895A0 (en) * | 1995-05-16 | 1995-06-08 | International Flower Developments Pty Ltd | Transgenic plants exhibiting altered flower colour and methods for producing same |
| WO1998027546A1 (en) | 1996-12-16 | 1998-06-25 | Seagate Technology, Inc. | E-block head stack microactuator assembly |
| US6121511A (en) | 1997-09-12 | 2000-09-19 | Ball Horticultural Company | Production of transgenic impatiens |
| JP2003523724A (ja) * | 1999-03-12 | 2003-08-12 | エグゼリクシス プラント サイエンシーズ, インコーポレイテッド | 形質関連遺伝子の同定方法 |
| DE60123787T2 (de) * | 2000-06-02 | 2007-10-11 | International Flower Developments Pty. Ltd., Laverton North | Neuartige, aliphatische acyltransferase-gene |
| JP2002315460A (ja) | 2001-03-30 | 2002-10-29 | Nippon Paper Industries Co Ltd | 周縁キメラ体作成方法及びこの方法により作成された周縁キメラ体 |
| EP2292765B1 (en) | 2002-08-30 | 2013-06-19 | Suntory Holdings Limited | Flavonoid 3',5' Hydroxylase gene sequences and uses therefor |
| JP4690197B2 (ja) * | 2003-08-13 | 2011-06-01 | インターナショナル フラワー ディベロプメンツ プロプライアタリー リミティド | 花色が変更されたバラの製造方法 |
| JP4595631B2 (ja) * | 2005-03-31 | 2010-12-08 | 日本製紙株式会社 | 選抜マーカー遺伝子の影響が排除された遺伝子導入細胞、組織又は植物の作成方法 |
-
2008
- 2008-03-28 EP EP08739852.5A patent/EP2128255B1/en not_active Not-in-force
- 2008-03-28 KR KR1020097020300A patent/KR101458578B1/ko not_active Expired - Fee Related
- 2008-03-28 WO PCT/JP2008/056746 patent/WO2008120820A1/ja not_active Ceased
- 2008-03-28 US US12/532,522 patent/US8183434B2/en not_active Expired - Fee Related
- 2008-03-28 CA CA2682095A patent/CA2682095C/en not_active Expired - Fee Related
- 2008-03-28 CN CN200880010382A patent/CN101675161A/zh active Pending
- 2008-03-28 JP JP2009507564A patent/JPWO2008120820A1/ja active Pending
- 2008-03-28 AU AU2008233555A patent/AU2008233555B2/en not_active Ceased
- 2008-03-28 TW TW097111602A patent/TW200845888A/zh unknown
-
2009
- 2009-09-28 CO CO09106063A patent/CO6231053A2/es not_active Application Discontinuation
- 2009-09-29 EC EC2009009661A patent/ECSP099661A/es unknown
-
2010
- 2010-04-09 JP JP2010090721A patent/JP4624478B2/ja active Active
-
2012
- 2012-04-13 US US13/446,591 patent/US20120198589A1/en not_active Abandoned
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN108330146A (zh) * | 2018-01-31 | 2018-07-27 | 天津大学 | 催化谷氨酰胺合成靛蓝获得蓝色花卉的转基因方法 |
| CN116584386A (zh) * | 2023-05-24 | 2023-08-15 | 北京林业大学 | 一种用于杨梅的组培培养基及杨梅种子萌发方法和杨梅组培快繁方法 |
| CN116584386B (zh) * | 2023-05-24 | 2024-03-19 | 北京林业大学 | 一种用于杨梅的组培培养基及杨梅种子萌发方法和杨梅组培快繁方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20090127408A (ko) | 2009-12-11 |
| CO6231053A2 (es) | 2010-12-20 |
| EP2128255A1 (en) | 2009-12-02 |
| JP2010200754A (ja) | 2010-09-16 |
| ECSP099661A (es) | 2009-10-30 |
| AU2008233555A1 (en) | 2008-10-09 |
| WO2008120820A1 (ja) | 2008-10-09 |
| JP4624478B2 (ja) | 2011-02-02 |
| EP2128255A4 (en) | 2010-08-04 |
| TW200845888A (en) | 2008-12-01 |
| US8183434B2 (en) | 2012-05-22 |
| EP2128255B1 (en) | 2015-01-28 |
| AU2008233555B2 (en) | 2013-10-17 |
| CA2682095C (en) | 2014-06-03 |
| US20110088125A1 (en) | 2011-04-14 |
| KR101458578B1 (ko) | 2014-11-07 |
| CA2682095A1 (en) | 2008-10-09 |
| US20120198589A1 (en) | 2012-08-02 |
| JPWO2008120820A1 (ja) | 2010-07-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Gandikota et al. | Development of transgenic rice plants expressing maize anthocyanin genes and increased blast resistance | |
| Sharma et al. | An efficient method for the production of transgenic plants of peanut (Arachis hypogaea L.) through Agrobacterium tumefaciens-mediated genetic transformation | |
| CN118271412A (zh) | 与大豆中锈病抗性相关联的新颖的遗传基因座 | |
| Teixeira da Silva et al. | Methods for genetic transformation in Dendrobium | |
| HU219543B (hu) | Eljárás hímsteril növények és az eljárásban használható rekombináns DNS előállítására | |
| CN101675161A (zh) | 表层嵌合体(surface chimera)转基因植物的培育方法 | |
| Miljuš-Djukić et al. | Agrobacterium-mediated transformation and plant regeneration of buckwheat (Fagopyrum esculentum Moench.) | |
| Li et al. | Enhanced anthocyanin synthesis in foliage plant Caladium bicolor | |
| CN107858370B (zh) | 一种制备育性减低植物的方法 | |
| Yu et al. | Construction of an antisense CYP86MF gene plasmid vector and production of a male-sterile Chinese cabbage transformant by the pollen-tube method | |
| Wang et al. | Cosuppression of tobacco chalcone synthase using Petunia chalcone synthase construct results in white flowers | |
| Tóth et al. | Agrobacterium-mediated genetic transformation of the desiccation tolerant resurrection plant Ramonda myconi (L.) Rchb. | |
| Vleghels et al. | Expression of ENOD40 during tomato plant development | |
| RU2590722C2 (ru) | Способ получения лилий, содержащих в лепестках делфинидин | |
| Nakamura et al. | Environmental risk assessment and field performance of rose (Rosa× hybrida) genetically modified for delphinidin production | |
| CN108018286B (zh) | 玉米转化事件zm8-143的创制、检测与应用 | |
| US7129393B1 (en) | Transgenic plants and method for transforming carnations | |
| KR100970109B1 (ko) | 나리 유래의 약에 특이적인 프로모터, 재조합 벡터,형질전환체 및 그의 제조 방법 | |
| Mori et al. | Somaclonal variation and stability of GUS gene expression in transgenic agapanthus (Agapanthus praecox ssp. orientalis) plants at the flowering stage | |
| WO2000050613A2 (en) | Transgenic plants and method for transforming carnations | |
| Phillip et al. | Application of biotechnology to Lotus breeding | |
| US20100031393A1 (en) | Novel protein having acyltransferase activity and gene encoding the same | |
| JP4885736B2 (ja) | 花弁の有色体へ移行するペプチド及び該ペプチドを用いる黄色系の花弁を有する植物の作成方法 | |
| Otani et al. | Transgenic sweet potato with agronomically important genes | |
| CN118440955A (zh) | 过表达水稻p3a基因在提高植物抗非生物胁迫中的用途 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| ASS | Succession or assignment of patent right |
Owner name: SUNTORY LTD. Free format text: FORMER OWNER: FLORIGENE LIMITED Effective date: 20110908 |
|
| C41 | Transfer of patent application or patent right or utility model | ||
| TA01 | Transfer of patent application right |
Effective date of registration: 20110908 Address after: Osaka Japan Applicant after: Suntory Holdings Limited Address before: Vitoria Australia Applicant before: International Flower Developments PTY. Ltd. |
|
| C12 | Rejection of a patent application after its publication | ||
| RJ01 | Rejection of invention patent application after publication |
Application publication date: 20100317 |