BRPI0514723B1 - composições contendo componentes de agonista alfa-2-adrenérgico - Google Patents
composições contendo componentes de agonista alfa-2-adrenérgico Download PDFInfo
- Publication number
- BRPI0514723B1 BRPI0514723B1 BRPI0514723-9A BRPI0514723A BRPI0514723B1 BR PI0514723 B1 BRPI0514723 B1 BR PI0514723B1 BR PI0514723 A BRPI0514723 A BR PI0514723A BR PI0514723 B1 BRPI0514723 B1 BR PI0514723B1
- Authority
- BR
- Brazil
- Prior art keywords
- alpha
- components
- adrenergic agonist
- compositions
- adrenergic
- Prior art date
Links
- 239000000203 mixture Substances 0.000 title claims abstract description 188
- 239000000384 adrenergic alpha-2 receptor agonist Substances 0.000 title abstract description 110
- IWEGDQUCWQFKHS-UHFFFAOYSA-N 1-(1,3-dioxolan-2-ylmethyl)-4-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)pyrazole Chemical compound O1C(C)(C)C(C)(C)OB1C1=CN(CC2OCCO2)N=C1 IWEGDQUCWQFKHS-UHFFFAOYSA-N 0.000 claims description 51
- 229960001724 brimonidine tartrate Drugs 0.000 claims description 51
- 239000003755 preservative agent Substances 0.000 claims description 45
- 230000002335 preservative effect Effects 0.000 claims description 34
- 229920002134 Carboxymethyl cellulose Polymers 0.000 claims description 31
- -1 sodium perborate decahydrate Chemical class 0.000 claims description 30
- 239000001768 carboxy methyl cellulose Substances 0.000 claims description 29
- 235000010948 carboxy methyl cellulose Nutrition 0.000 claims description 28
- 239000008112 carboxymethyl-cellulose Substances 0.000 claims description 27
- 230000004410 intraocular pressure Effects 0.000 claims description 13
- OSVXSBDYLRYLIG-UHFFFAOYSA-N dioxidochlorine(.) Chemical compound O=Cl=O OSVXSBDYLRYLIG-UHFFFAOYSA-N 0.000 claims description 10
- 230000001590 oxidative effect Effects 0.000 claims description 7
- XNCOSPRUTUOJCJ-UHFFFAOYSA-N Biguanide Chemical compound NC(N)=NC(N)=N XNCOSPRUTUOJCJ-UHFFFAOYSA-N 0.000 claims description 5
- 229940123208 Biguanide Drugs 0.000 claims description 5
- 239000004155 Chlorine dioxide Substances 0.000 claims description 5
- 208000010412 Glaucoma Diseases 0.000 claims description 5
- 229920002413 Polyhexanide Polymers 0.000 claims description 5
- 229960000686 benzalkonium chloride Drugs 0.000 claims description 5
- CADWTSSKOVRVJC-UHFFFAOYSA-N benzyl(dimethyl)azanium;chloride Chemical compound [Cl-].C[NH+](C)CC1=CC=CC=C1 CADWTSSKOVRVJC-UHFFFAOYSA-N 0.000 claims description 5
- 235000019398 chlorine dioxide Nutrition 0.000 claims description 5
- LZZYPRNAOMGNLH-UHFFFAOYSA-M Cetrimonium bromide Chemical compound [Br-].CCCCCCCCCCCCCCCC[N+](C)(C)C LZZYPRNAOMGNLH-UHFFFAOYSA-M 0.000 claims description 2
- 229960002798 cetrimide Drugs 0.000 claims description 2
- 229960001922 sodium perborate Drugs 0.000 claims description 2
- 125000001453 quaternary ammonium group Chemical group 0.000 claims 3
- VAZJLPXFVQHDFB-UHFFFAOYSA-N 1-(diaminomethylidene)-2-hexylguanidine Polymers CCCCCCN=C(N)N=C(N)N VAZJLPXFVQHDFB-UHFFFAOYSA-N 0.000 claims 2
- KHSLHYAUZSPBIU-UHFFFAOYSA-M benzododecinium bromide Chemical compound [Br-].CCCCCCCCCCCC[N+](C)(C)CC1=CC=CC=C1 KHSLHYAUZSPBIU-UHFFFAOYSA-M 0.000 claims 2
- 229940073464 benzododecinium bromide Drugs 0.000 claims 2
- 239000004372 Polyvinyl alcohol Substances 0.000 abstract description 10
- 229920002451 polyvinyl alcohol Polymers 0.000 abstract description 10
- 239000000048 adrenergic agonist Substances 0.000 abstract description 8
- 238000005063 solubilization Methods 0.000 abstract description 7
- 230000007928 solubilization Effects 0.000 abstract description 7
- 229920000036 polyvinylpyrrolidone Polymers 0.000 abstract description 5
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 abstract description 5
- WHNWPMSKXPGLAX-UHFFFAOYSA-N N-Vinyl-2-pyrrolidone Chemical compound C=CN1CCCC1=O WHNWPMSKXPGLAX-UHFFFAOYSA-N 0.000 abstract description 3
- 230000002708 enhancing effect Effects 0.000 abstract description 3
- 229940069328 povidone Drugs 0.000 abstract description 3
- XSCHRSMBECNVNS-UHFFFAOYSA-N quinoxaline Chemical compound N1=CC=NC2=CC=CC=C21 XSCHRSMBECNVNS-UHFFFAOYSA-N 0.000 description 63
- XYLJNLCSTIOKRM-UHFFFAOYSA-N Alphagan Chemical compound C1=CC2=NC=CN=C2C(Br)=C1NC1=NCCN1 XYLJNLCSTIOKRM-UHFFFAOYSA-N 0.000 description 29
- 239000000243 solution Substances 0.000 description 29
- 238000009472 formulation Methods 0.000 description 27
- 239000007788 liquid Substances 0.000 description 24
- 229920000858 Cyclodextrin Polymers 0.000 description 21
- 235000002639 sodium chloride Nutrition 0.000 description 21
- 229960003679 brimonidine Drugs 0.000 description 18
- 150000001875 compounds Chemical class 0.000 description 17
- 229910052751 metal Inorganic materials 0.000 description 17
- 239000002184 metal Substances 0.000 description 17
- 239000000178 monomer Substances 0.000 description 17
- 235000010443 alginic acid Nutrition 0.000 description 16
- 229920000615 alginic acid Polymers 0.000 description 16
- 102000030484 alpha-2 Adrenergic Receptor Human genes 0.000 description 14
- 108020004101 alpha-2 Adrenergic Receptor Proteins 0.000 description 14
- 230000000694 effects Effects 0.000 description 14
- 150000002148 esters Chemical class 0.000 description 14
- 150000003839 salts Chemical class 0.000 description 14
- 239000007864 aqueous solution Substances 0.000 description 13
- 230000007935 neutral effect Effects 0.000 description 12
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 12
- 125000000129 anionic group Chemical group 0.000 description 11
- 239000000463 material Substances 0.000 description 11
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 10
- 229940003677 alphagan Drugs 0.000 description 10
- 230000001965 increasing effect Effects 0.000 description 10
- 229940054534 ophthalmic solution Drugs 0.000 description 10
- 239000002997 ophthalmic solution Substances 0.000 description 10
- 230000008901 benefit Effects 0.000 description 9
- 235000019422 polyvinyl alcohol Nutrition 0.000 description 9
- 239000000523 sample Substances 0.000 description 9
- 230000001225 therapeutic effect Effects 0.000 description 9
- MHAJPDPJQMAIIY-UHFFFAOYSA-N Hydrogen peroxide Chemical compound OO MHAJPDPJQMAIIY-UHFFFAOYSA-N 0.000 description 8
- 239000000539 dimer Substances 0.000 description 8
- 102000005962 receptors Human genes 0.000 description 8
- 108020003175 receptors Proteins 0.000 description 8
- 239000000872 buffer Substances 0.000 description 7
- QBWCMBCROVPCKQ-UHFFFAOYSA-N chlorous acid Chemical compound OCl=O QBWCMBCROVPCKQ-UHFFFAOYSA-N 0.000 description 7
- 230000007423 decrease Effects 0.000 description 7
- 239000012528 membrane Substances 0.000 description 7
- 229920000642 polymer Polymers 0.000 description 7
- 230000000699 topical effect Effects 0.000 description 7
- 239000001116 FEMA 4028 Substances 0.000 description 6
- 241001465754 Metazoa Species 0.000 description 6
- 239000000556 agonist Substances 0.000 description 6
- 229920006321 anionic cellulose Polymers 0.000 description 6
- 229920001586 anionic polysaccharide Polymers 0.000 description 6
- 150000004836 anionic polysaccharides Chemical class 0.000 description 6
- 229960004853 betadex Drugs 0.000 description 6
- 210000000170 cell membrane Anatomy 0.000 description 6
- 229940097362 cyclodextrins Drugs 0.000 description 6
- 230000006870 function Effects 0.000 description 6
- 150000002632 lipids Chemical class 0.000 description 6
- HFHDHCJBZVLPGP-UHFFFAOYSA-N schardinger α-dextrin Chemical compound O1C(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(O)C2O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC2C(O)C(O)C1OC2CO HFHDHCJBZVLPGP-UHFFFAOYSA-N 0.000 description 6
- 239000013543 active substance Substances 0.000 description 5
- 239000000783 alginic acid Substances 0.000 description 5
- 229960001126 alginic acid Drugs 0.000 description 5
- 229910052783 alkali metal Inorganic materials 0.000 description 5
- 235000011175 beta-cyclodextrine Nutrition 0.000 description 5
- 238000005119 centrifugation Methods 0.000 description 5
- 229910001919 chlorite Inorganic materials 0.000 description 5
- 229910052619 chlorite group Inorganic materials 0.000 description 5
- 238000001914 filtration Methods 0.000 description 5
- 239000000796 flavoring agent Substances 0.000 description 5
- 150000003252 quinoxalines Chemical class 0.000 description 5
- 238000003756 stirring Methods 0.000 description 5
- 238000012360 testing method Methods 0.000 description 5
- 210000001519 tissue Anatomy 0.000 description 5
- DKZMSQCWKJPFLT-UHFFFAOYSA-N 2,3-dihydroxybutanedioic acid;quinoxaline Chemical compound N1=CC=NC2=CC=CC=C21.OC(=O)C(O)C(O)C(O)=O DKZMSQCWKJPFLT-UHFFFAOYSA-N 0.000 description 4
- XTEGARKTQYYJKE-UHFFFAOYSA-M Chlorate Chemical compound [O-]Cl(=O)=O XTEGARKTQYYJKE-UHFFFAOYSA-M 0.000 description 4
- IAYPIBMASNFSPL-UHFFFAOYSA-N Ethylene oxide Chemical compound C1CO1 IAYPIBMASNFSPL-UHFFFAOYSA-N 0.000 description 4
- 229920002148 Gellan gum Polymers 0.000 description 4
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 4
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 4
- WCUXLLCKKVVCTQ-UHFFFAOYSA-M Potassium chloride Chemical compound [Cl-].[K+] WCUXLLCKKVVCTQ-UHFFFAOYSA-M 0.000 description 4
- 150000001340 alkali metals Chemical class 0.000 description 4
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 4
- 150000001768 cations Chemical class 0.000 description 4
- 239000003795 chemical substances by application Substances 0.000 description 4
- 239000000460 chlorine Substances 0.000 description 4
- 229910052801 chlorine Inorganic materials 0.000 description 4
- 239000007859 condensation product Substances 0.000 description 4
- 235000013355 food flavoring agent Nutrition 0.000 description 4
- 235000003599 food sweetener Nutrition 0.000 description 4
- 230000009931 harmful effect Effects 0.000 description 4
- 238000004128 high performance liquid chromatography Methods 0.000 description 4
- 239000004615 ingredient Substances 0.000 description 4
- 230000002401 inhibitory effect Effects 0.000 description 4
- 230000003993 interaction Effects 0.000 description 4
- 230000036961 partial effect Effects 0.000 description 4
- 229920001282 polysaccharide Polymers 0.000 description 4
- 239000005017 polysaccharide Substances 0.000 description 4
- 229910052700 potassium Inorganic materials 0.000 description 4
- 239000000047 product Substances 0.000 description 4
- 239000008213 purified water Substances 0.000 description 4
- 230000002829 reductive effect Effects 0.000 description 4
- 229910052708 sodium Inorganic materials 0.000 description 4
- 239000011734 sodium Substances 0.000 description 4
- 239000011780 sodium chloride Substances 0.000 description 4
- 239000000126 substance Substances 0.000 description 4
- 239000000725 suspension Substances 0.000 description 4
- 239000003765 sweetening agent Substances 0.000 description 4
- 229940095064 tartrate Drugs 0.000 description 4
- 239000003981 vehicle Substances 0.000 description 4
- NIXOWILDQLNWCW-UHFFFAOYSA-N 2-Propenoic acid Natural products OC(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 3
- CPELXLSAUQHCOX-UHFFFAOYSA-M Bromide Chemical compound [Br-] CPELXLSAUQHCOX-UHFFFAOYSA-M 0.000 description 3
- 229920001661 Chitosan Polymers 0.000 description 3
- GJSURZIOUXUGAL-UHFFFAOYSA-N Clonidine Chemical compound ClC1=CC=CC(Cl)=C1NC1=NCCN1 GJSURZIOUXUGAL-UHFFFAOYSA-N 0.000 description 3
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 3
- 241000282412 Homo Species 0.000 description 3
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 3
- 241000124008 Mammalia Species 0.000 description 3
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 239000002253 acid Substances 0.000 description 3
- 230000002378 acidificating effect Effects 0.000 description 3
- 239000004480 active ingredient Substances 0.000 description 3
- 150000004781 alginic acids Chemical class 0.000 description 3
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 3
- 150000001412 amines Chemical class 0.000 description 3
- 229920006318 anionic polymer Polymers 0.000 description 3
- 239000007900 aqueous suspension Substances 0.000 description 3
- 239000011575 calcium Substances 0.000 description 3
- 229910052791 calcium Inorganic materials 0.000 description 3
- 210000004027 cell Anatomy 0.000 description 3
- 229920002678 cellulose Polymers 0.000 description 3
- 239000001913 cellulose Substances 0.000 description 3
- 235000010980 cellulose Nutrition 0.000 description 3
- 150000005829 chemical entities Chemical class 0.000 description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 3
- 229960002896 clonidine Drugs 0.000 description 3
- 235000014113 dietary fatty acids Nutrition 0.000 description 3
- 239000000839 emulsion Substances 0.000 description 3
- 239000000194 fatty acid Substances 0.000 description 3
- 229930195729 fatty acid Natural products 0.000 description 3
- 235000010492 gellan gum Nutrition 0.000 description 3
- 239000000216 gellan gum Substances 0.000 description 3
- 230000002209 hydrophobic effect Effects 0.000 description 3
- WQYVRQLZKVEZGA-UHFFFAOYSA-N hypochlorite Chemical compound Cl[O-] WQYVRQLZKVEZGA-UHFFFAOYSA-N 0.000 description 3
- 230000001077 hypotensive effect Effects 0.000 description 3
- 150000002500 ions Chemical class 0.000 description 3
- 238000004519 manufacturing process Methods 0.000 description 3
- 230000007246 mechanism Effects 0.000 description 3
- 239000002609 medium Substances 0.000 description 3
- 150000002978 peroxides Chemical class 0.000 description 3
- 150000004804 polysaccharides Chemical class 0.000 description 3
- 239000011591 potassium Substances 0.000 description 3
- 230000003518 presynaptic effect Effects 0.000 description 3
- HNJBEVLQSNELDL-UHFFFAOYSA-N pyrrolidin-2-one Chemical compound O=C1CCCN1 HNJBEVLQSNELDL-UHFFFAOYSA-N 0.000 description 3
- 239000012488 sample solution Substances 0.000 description 3
- 230000003381 solubilizing effect Effects 0.000 description 3
- CNIIGCLFLJGOGP-UHFFFAOYSA-N 2-(1-naphthalenylmethyl)-4,5-dihydro-1H-imidazole Chemical compound C=1C=CC2=CC=CC=C2C=1CC1=NCCN1 CNIIGCLFLJGOGP-UHFFFAOYSA-N 0.000 description 2
- SMZOUWXMTYCWNB-UHFFFAOYSA-N 2-(2-methoxy-5-methylphenyl)ethanamine Chemical compound COC1=CC=C(C)C=C1CCN SMZOUWXMTYCWNB-UHFFFAOYSA-N 0.000 description 2
- FJKROLUGYXJWQN-UHFFFAOYSA-N 4-hydroxybenzoic acid Chemical compound OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 2
- OULQIRTYSJHFKP-UHFFFAOYSA-N 4h-imidazol-5-amine Chemical class N=C1CNC=N1 OULQIRTYSJHFKP-UHFFFAOYSA-N 0.000 description 2
- FHVDTGUDJYJELY-UHFFFAOYSA-N 6-{[2-carboxy-4,5-dihydroxy-6-(phosphanyloxy)oxan-3-yl]oxy}-4,5-dihydroxy-3-phosphanyloxane-2-carboxylic acid Chemical compound O1C(C(O)=O)C(P)C(O)C(O)C1OC1C(C(O)=O)OC(OP)C(O)C1O FHVDTGUDJYJELY-UHFFFAOYSA-N 0.000 description 2
- PAYRUJLWNCNPSJ-UHFFFAOYSA-N Aniline Chemical compound NC1=CC=CC=C1 PAYRUJLWNCNPSJ-UHFFFAOYSA-N 0.000 description 2
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 2
- 229920002101 Chitin Polymers 0.000 description 2
- WDZVGELJXXEGPV-YIXHJXPBSA-N Guanabenz Chemical compound NC(N)=N\N=C\C1=C(Cl)C=CC=C1Cl WDZVGELJXXEGPV-YIXHJXPBSA-N 0.000 description 2
- INJOMKTZOLKMBF-UHFFFAOYSA-N Guanfacine Chemical compound NC(=N)NC(=O)CC1=C(Cl)C=CC=C1Cl INJOMKTZOLKMBF-UHFFFAOYSA-N 0.000 description 2
- 229920000084 Gum arabic Polymers 0.000 description 2
- 208000001953 Hypotension Diseases 0.000 description 2
- 239000000232 Lipid Bilayer Substances 0.000 description 2
- CERQOIWHTDAKMF-UHFFFAOYSA-N Methacrylic acid Chemical compound CC(=C)C(O)=O CERQOIWHTDAKMF-UHFFFAOYSA-N 0.000 description 2
- 206010030043 Ocular hypertension Diseases 0.000 description 2
- KFSLWBXXFJQRDL-UHFFFAOYSA-N Peracetic acid Chemical compound CC(=O)OO KFSLWBXXFJQRDL-UHFFFAOYSA-N 0.000 description 2
- DLRVVLDZNNYCBX-UHFFFAOYSA-N Polydextrose Polymers OC1C(O)C(O)C(CO)OC1OCC1C(O)C(O)C(O)C(O)O1 DLRVVLDZNNYCBX-UHFFFAOYSA-N 0.000 description 2
- 229920002125 Sokalan® Polymers 0.000 description 2
- 229920002472 Starch Polymers 0.000 description 2
- 229920001615 Tragacanth Polymers 0.000 description 2
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Chemical compound NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 description 2
- 239000000205 acacia gum Substances 0.000 description 2
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 description 2
- 230000001800 adrenalinergic effect Effects 0.000 description 2
- 239000000695 adrenergic alpha-agonist Substances 0.000 description 2
- 230000002411 adverse Effects 0.000 description 2
- 229940072056 alginate Drugs 0.000 description 2
- 150000001342 alkaline earth metals Chemical class 0.000 description 2
- 102000030619 alpha-1 Adrenergic Receptor Human genes 0.000 description 2
- 108020004102 alpha-1 Adrenergic Receptor Proteins 0.000 description 2
- HFHDHCJBZVLPGP-RWMJIURBSA-N alpha-cyclodextrin Chemical compound OC[C@H]([C@H]([C@@H]([C@H]1O)O)O[C@H]2O[C@@H]([C@@H](O[C@H]3O[C@H](CO)[C@H]([C@@H]([C@H]3O)O)O[C@H]3O[C@H](CO)[C@H]([C@@H]([C@H]3O)O)O[C@H]3O[C@H](CO)[C@H]([C@@H]([C@H]3O)O)O3)[C@H](O)[C@H]2O)CO)O[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@@H]3O[C@@H]1CO HFHDHCJBZVLPGP-RWMJIURBSA-N 0.000 description 2
- 150000001413 amino acids Chemical class 0.000 description 2
- 239000008365 aqueous carrier Substances 0.000 description 2
- 239000012736 aqueous medium Substances 0.000 description 2
- 239000000305 astragalus gummifer gum Substances 0.000 description 2
- 150000001538 azepines Chemical class 0.000 description 2
- WHGYBXFWUBPSRW-FOUAGVGXSA-N beta-cyclodextrin Chemical compound OC[C@H]([C@H]([C@@H]([C@H]1O)O)O[C@H]2O[C@@H]([C@@H](O[C@H]3O[C@H](CO)[C@H]([C@@H]([C@H]3O)O)O[C@H]3O[C@H](CO)[C@H]([C@@H]([C@H]3O)O)O[C@H]3O[C@H](CO)[C@H]([C@@H]([C@H]3O)O)O[C@H]3O[C@H](CO)[C@H]([C@@H]([C@H]3O)O)O3)[C@H](O)[C@H]2O)CO)O[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@@H]3O[C@@H]1CO WHGYBXFWUBPSRW-FOUAGVGXSA-N 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 239000007975 buffered saline Substances 0.000 description 2
- 229960005069 calcium Drugs 0.000 description 2
- 125000002057 carboxymethyl group Chemical group [H]OC(=O)C([H])([H])[*] 0.000 description 2
- 235000010418 carrageenan Nutrition 0.000 description 2
- 229920001525 carrageenan Polymers 0.000 description 2
- 239000000679 carrageenan Substances 0.000 description 2
- 229940113118 carrageenan Drugs 0.000 description 2
- 210000000845 cartilage Anatomy 0.000 description 2
- 150000003943 catecholamines Chemical class 0.000 description 2
- 239000007979 citrate buffer Substances 0.000 description 2
- 239000003086 colorant Substances 0.000 description 2
- 230000021615 conjugation Effects 0.000 description 2
- 229960001894 detomidine Drugs 0.000 description 2
- JXMXDKHEZLKQPB-UHFFFAOYSA-N detomidine Chemical compound CC1=CC=CC(CC=2[N]C=NC=2)=C1C JXMXDKHEZLKQPB-UHFFFAOYSA-N 0.000 description 2
- HRLIOXLXPOHXTA-NSHDSACASA-N dexmedetomidine Chemical compound C1([C@@H](C)C=2C(=C(C)C=CC=2)C)=CN=C[N]1 HRLIOXLXPOHXTA-NSHDSACASA-N 0.000 description 2
- 229960004253 dexmedetomidine Drugs 0.000 description 2
- 239000008121 dextrose Substances 0.000 description 2
- 238000009792 diffusion process Methods 0.000 description 2
- 206010013781 dry mouth Diseases 0.000 description 2
- 150000004665 fatty acids Chemical class 0.000 description 2
- 239000000706 filtrate Substances 0.000 description 2
- 239000008103 glucose Substances 0.000 description 2
- 235000011187 glycerol Nutrition 0.000 description 2
- 229960002048 guanfacine Drugs 0.000 description 2
- 150000002357 guanidines Chemical class 0.000 description 2
- BXWNKGSJHAJOGX-UHFFFAOYSA-N hexadecan-1-ol Chemical compound CCCCCCCCCCCCCCCCO BXWNKGSJHAJOGX-UHFFFAOYSA-N 0.000 description 2
- 208000021822 hypotensive Diseases 0.000 description 2
- 150000002460 imidazoles Chemical class 0.000 description 2
- 150000002462 imidazolines Chemical class 0.000 description 2
- 230000005764 inhibitory process Effects 0.000 description 2
- 230000007794 irritation Effects 0.000 description 2
- 230000000670 limiting effect Effects 0.000 description 2
- 229940057995 liquid paraffin Drugs 0.000 description 2
- HRLIOXLXPOHXTA-UHFFFAOYSA-N medetomidine Chemical compound C=1C=CC(C)=C(C)C=1C(C)C1=CN=C[N]1 HRLIOXLXPOHXTA-UHFFFAOYSA-N 0.000 description 2
- 229960002140 medetomidine Drugs 0.000 description 2
- 150000002734 metacrylic acid derivatives Chemical class 0.000 description 2
- 150000002739 metals Chemical class 0.000 description 2
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 2
- 239000002480 mineral oil Substances 0.000 description 2
- 235000010446 mineral oil Nutrition 0.000 description 2
- 230000000324 neuroprotective effect Effects 0.000 description 2
- 239000002858 neurotransmitter agent Substances 0.000 description 2
- 231100000252 nontoxic Toxicity 0.000 description 2
- 230000003000 nontoxic effect Effects 0.000 description 2
- 239000004006 olive oil Substances 0.000 description 2
- 235000008390 olive oil Nutrition 0.000 description 2
- 150000002918 oxazolines Chemical class 0.000 description 2
- VLTRZXGMWDSKGL-UHFFFAOYSA-N perchloric acid Chemical compound OCl(=O)(=O)=O VLTRZXGMWDSKGL-UHFFFAOYSA-N 0.000 description 2
- 230000035699 permeability Effects 0.000 description 2
- 150000004965 peroxy acids Chemical class 0.000 description 2
- 125000000864 peroxy group Chemical group O(O*)* 0.000 description 2
- 239000000546 pharmaceutical excipient Substances 0.000 description 2
- 235000010482 polyoxyethylene sorbitan monooleate Nutrition 0.000 description 2
- 239000000244 polyoxyethylene sorbitan monooleate Substances 0.000 description 2
- 229920000053 polysorbate 80 Polymers 0.000 description 2
- 239000001103 potassium chloride Substances 0.000 description 2
- 235000011164 potassium chloride Nutrition 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 150000003856 quaternary ammonium compounds Chemical class 0.000 description 2
- 235000019812 sodium carboxymethyl cellulose Nutrition 0.000 description 2
- 229920001027 sodium carboxymethylcellulose Polymers 0.000 description 2
- 235000019698 starch Nutrition 0.000 description 2
- 230000009885 systemic effect Effects 0.000 description 2
- BYJAVTDNIXVSPW-UHFFFAOYSA-N tetryzoline Chemical compound N1CCN=C1C1C2=CC=CC=C2CCC1 BYJAVTDNIXVSPW-UHFFFAOYSA-N 0.000 description 2
- 150000004897 thiazines Chemical class 0.000 description 2
- 239000002562 thickening agent Substances 0.000 description 2
- XFYDIVBRZNQMJC-UHFFFAOYSA-N tizanidine Chemical compound ClC=1C=CC2=NSN=C2C=1NC1=NCCN1 XFYDIVBRZNQMJC-UHFFFAOYSA-N 0.000 description 2
- 229960000488 tizanidine Drugs 0.000 description 2
- 230000002588 toxic effect Effects 0.000 description 2
- 235000015112 vegetable and seed oil Nutrition 0.000 description 2
- 239000008158 vegetable oil Substances 0.000 description 2
- BPICBUSOMSTKRF-UHFFFAOYSA-N xylazine Chemical compound CC1=CC=CC(C)=C1NC1=NCCCS1 BPICBUSOMSTKRF-UHFFFAOYSA-N 0.000 description 2
- 229960001600 xylazine Drugs 0.000 description 2
- UHVMMEOXYDMDKI-JKYCWFKZSA-L zinc;1-(5-cyanopyridin-2-yl)-3-[(1s,2s)-2-(6-fluoro-2-hydroxy-3-propanoylphenyl)cyclopropyl]urea;diacetate Chemical compound [Zn+2].CC([O-])=O.CC([O-])=O.CCC(=O)C1=CC=C(F)C([C@H]2[C@H](C2)NC(=O)NC=2N=CC(=CC=2)C#N)=C1O UHVMMEOXYDMDKI-JKYCWFKZSA-L 0.000 description 2
- SFLSHLFXELFNJZ-QMMMGPOBSA-N (-)-norepinephrine Chemical compound NC[C@H](O)C1=CC=C(O)C(O)=C1 SFLSHLFXELFNJZ-QMMMGPOBSA-N 0.000 description 1
- YZOUYRAONFXZSI-SBHWVFSVSA-N (1S,3R,5R,6R,8R,10R,11R,13R,15R,16R,18R,20R,21R,23R,25R,26R,28R,30R,31S,33R,35R,36R,37S,38R,39S,40R,41S,42R,43S,44R,45S,46R,47S,48R,49S)-5,10,15,20,25,30,35-heptakis(hydroxymethyl)-37,39,40,41,42,43,44,45,46,47,48,49-dodecamethoxy-2,4,7,9,12,14,17,19,22,24,27,29,32,34-tetradecaoxaoctacyclo[31.2.2.23,6.28,11.213,16.218,21.223,26.228,31]nonatetracontane-36,38-diol Chemical compound O([C@@H]([C@H]([C@@H]1OC)OC)O[C@H]2[C@@H](O)[C@@H]([C@@H](O[C@@H]3[C@@H](CO)O[C@@H]([C@H]([C@@H]3O)OC)O[C@@H]3[C@@H](CO)O[C@@H]([C@H]([C@@H]3OC)OC)O[C@@H]3[C@@H](CO)O[C@@H]([C@H]([C@@H]3OC)OC)O[C@@H]3[C@@H](CO)O[C@@H]([C@H]([C@@H]3OC)OC)O3)O[C@@H]2CO)OC)[C@H](CO)[C@H]1O[C@@H]1[C@@H](OC)[C@H](OC)[C@H]3[C@@H](CO)O1 YZOUYRAONFXZSI-SBHWVFSVSA-N 0.000 description 1
- WZYRMLAWNVOIEX-MOJAZDJTSA-N (2s)-2-[(2r,3r,4s)-3,4-dihydroxyoxolan-2-yl]-2-hydroxyacetaldehyde Chemical group O=C[C@@H](O)[C@@H]1OC[C@H](O)[C@H]1O WZYRMLAWNVOIEX-MOJAZDJTSA-N 0.000 description 1
- ZORQXIQZAOLNGE-UHFFFAOYSA-N 1,1-difluorocyclohexane Chemical compound FC1(F)CCCCC1 ZORQXIQZAOLNGE-UHFFFAOYSA-N 0.000 description 1
- PZNPLUBHRSSFHT-RRHRGVEJSA-N 1-hexadecanoyl-2-octadecanoyl-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCCCCCC(=O)O[C@@H](COP([O-])(=O)OCC[N+](C)(C)C)COC(=O)CCCCCCCCCCCCCCC PZNPLUBHRSSFHT-RRHRGVEJSA-N 0.000 description 1
- IXPNQXFRVYWDDI-UHFFFAOYSA-N 1-methyl-2,4-dioxo-1,3-diazinane-5-carboximidamide Chemical compound CN1CC(C(N)=N)C(=O)NC1=O IXPNQXFRVYWDDI-UHFFFAOYSA-N 0.000 description 1
- IIZPXYDJLKNOIY-JXPKJXOSSA-N 1-palmitoyl-2-arachidonoyl-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCC\C=C/C\C=C/C\C=C/C\C=C/CCCCC IIZPXYDJLKNOIY-JXPKJXOSSA-N 0.000 description 1
- PLHMLIDUVYHXHF-ZQSHRCRISA-N 2,6-di-o-ethyl-β-cyclodextrin Chemical compound CCOC[C@H]([C@H]([C@@H]([C@H]1OCC)O)O[C@H]2O[C@@H]([C@@H](O[C@H]3O[C@H](COCC)[C@H]([C@@H]([C@H]3OCC)O)O[C@H]3O[C@H](COCC)[C@H]([C@@H]([C@H]3OCC)O)O[C@H]3O[C@H](COCC)[C@H]([C@@H]([C@H]3OCC)O)O[C@H]3O[C@H](COCC)[C@H]([C@@H]([C@H]3OCC)O)O3)[C@H](O)[C@H]2OCC)COCC)O[C@@H]1O[C@H]1[C@H](O)[C@@H](OCC)[C@@H]3O[C@@H]1COCC PLHMLIDUVYHXHF-ZQSHRCRISA-N 0.000 description 1
- XHZPRMZZQOIPDS-UHFFFAOYSA-N 2-Methyl-2-[(1-oxo-2-propenyl)amino]-1-propanesulfonic acid Chemical class OS(=O)(=O)CC(C)(C)NC(=O)C=C XHZPRMZZQOIPDS-UHFFFAOYSA-N 0.000 description 1
- CUJVBAPGYBSBHJ-YWBSARSQSA-N 2-[[(1R,3R,5R,6S,8R,10R,11S,13R,15R,16S,18R,20R,21R,23R,25R,26R,28R,30R,31R,33R,35R,36R,37R,38R,39R,40R,41R,42R,43R,44R,45R,46R,47R,48R,49R)-36,38,40,42-tetrakis(carboxymethoxy)-10,15-bis(carboxymethoxymethyl)-37,39,41,43,44,45,46,47,48,49-decahydroxy-20,25,30,35-tetrakis(hydroxymethyl)-2,4,7,9,12,14,17,19,22,24,27,29,32,34-tetradecaoxaoctacyclo[31.2.2.23,6.28,11.213,16.218,21.223,26.228,31]nonatetracontan-5-yl]methoxy]acetic acid Chemical compound OC[C@H]1O[C@@H]2O[C@H]3[C@H](O)[C@@H](O)[C@H](O[C@@H]3COCC(O)=O)O[C@H]3[C@H](O)[C@@H](O)[C@H](O[C@@H]3COCC(O)=O)O[C@H]3[C@H](O)[C@@H](O)[C@H](O[C@@H]3COCC(O)=O)O[C@@H]3[C@@H](CO)O[C@H](O[C@@H]4[C@@H](CO)O[C@H](O[C@@H]5[C@@H](CO)O[C@H](O[C@H]1[C@H](OCC(O)=O)[C@H]2O)[C@H](O)[C@H]5OCC(O)=O)[C@H](O)[C@H]4OCC(O)=O)[C@H](O)[C@H]3OCC(O)=O CUJVBAPGYBSBHJ-YWBSARSQSA-N 0.000 description 1
- UBLAMKHIFZBBSS-UHFFFAOYSA-N 3-Methylbutyl pentanoate Chemical compound CCCCC(=O)OCCC(C)C UBLAMKHIFZBBSS-UHFFFAOYSA-N 0.000 description 1
- NZAQRZWBQUIBSF-UHFFFAOYSA-N 4-(4-sulfobutoxy)butane-1-sulfonic acid Chemical compound OS(=O)(=O)CCCCOCCCCS(O)(=O)=O NZAQRZWBQUIBSF-UHFFFAOYSA-N 0.000 description 1
- 229940090248 4-hydroxybenzoic acid Drugs 0.000 description 1
- SQDAZGGFXASXDW-UHFFFAOYSA-N 5-bromo-2-(trifluoromethoxy)pyridine Chemical compound FC(F)(F)OC1=CC=C(Br)C=N1 SQDAZGGFXASXDW-UHFFFAOYSA-N 0.000 description 1
- QZHBYNSSDLTCRG-LREBCSMRSA-N 5-bromo-n-(4,5-dihydro-1h-imidazol-2-yl)quinoxalin-6-amine;(2r,3r)-2,3-dihydroxybutanedioic acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O.C1=CC2=NC=CN=C2C(Br)=C1NC1=NCCN1 QZHBYNSSDLTCRG-LREBCSMRSA-N 0.000 description 1
- HBLPYIOKPJVFQW-UHFFFAOYSA-N 6-ethyl-4,5,7,8-tetrahydro-[1,3]oxazolo[4,5-d]azepin-2-amine;hydron;dichloride Chemical compound Cl.Cl.C1CN(CC)CCC2=C1OC(N)=N2 HBLPYIOKPJVFQW-UHFFFAOYSA-N 0.000 description 1
- DHSSDEDRBUKTQY-UHFFFAOYSA-N 6-prop-2-enyl-4,5,7,8-tetrahydrothiazolo[4,5-d]azepin-2-amine Chemical compound C1CN(CC=C)CCC2=C1N=C(N)S2 DHSSDEDRBUKTQY-UHFFFAOYSA-N 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- 108060003345 Adrenergic Receptor Proteins 0.000 description 1
- 102000017910 Adrenergic receptor Human genes 0.000 description 1
- 229920001450 Alpha-Cyclodextrin Polymers 0.000 description 1
- 241000512259 Ascophyllum nodosum Species 0.000 description 1
- 241000894006 Bacteria Species 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 1
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 1
- 241000251730 Chondrichthyes Species 0.000 description 1
- 229920001287 Chondroitin sulfate Polymers 0.000 description 1
- 241000206575 Chondrus crispus Species 0.000 description 1
- KRKNYBCHXYNGOX-UHFFFAOYSA-K Citrate Chemical compound [O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O KRKNYBCHXYNGOX-UHFFFAOYSA-K 0.000 description 1
- 206010051625 Conjunctival hyperaemia Diseases 0.000 description 1
- 206010010741 Conjunctivitis Diseases 0.000 description 1
- 206010010744 Conjunctivitis allergic Diseases 0.000 description 1
- IVOMOUWHDPKRLL-KQYNXXCUSA-N Cyclic adenosine monophosphate Chemical compound C([C@H]1O2)OP(O)(=O)O[C@H]1[C@@H](O)[C@@H]2N1C(N=CN=C2N)=C2N=C1 IVOMOUWHDPKRLL-KQYNXXCUSA-N 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- 241001269524 Dura Species 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- DBVJJBKOTRCVKF-UHFFFAOYSA-N Etidronic acid Chemical compound OP(=O)(O)C(O)(C)P(O)(O)=O DBVJJBKOTRCVKF-UHFFFAOYSA-N 0.000 description 1
- 206010052140 Eye pruritus Diseases 0.000 description 1
- 241000192125 Firmicutes Species 0.000 description 1
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 1
- 241000233866 Fungi Species 0.000 description 1
- 108091006027 G proteins Proteins 0.000 description 1
- 102000030782 GTP binding Human genes 0.000 description 1
- 108091000058 GTP-Binding Proteins 0.000 description 1
- 229920002683 Glycosaminoglycan Polymers 0.000 description 1
- HTTJABKRGRZYRN-UHFFFAOYSA-N Heparin Chemical compound OC1C(NC(=O)C)C(O)OC(COS(O)(=O)=O)C1OC1C(OS(O)(=O)=O)C(O)C(OC2C(C(OS(O)(=O)=O)C(OC3C(C(O)C(O)C(O3)C(O)=O)OS(O)(=O)=O)C(CO)O2)NS(O)(=O)=O)C(C(O)=O)O1 HTTJABKRGRZYRN-UHFFFAOYSA-N 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 1
- 229920001612 Hydroxyethyl starch Polymers 0.000 description 1
- XQFRJNBWHJMXHO-RRKCRQDMSA-N IDUR Chemical compound C1[C@H](O)[C@@H](CO)O[C@H]1N1C(=O)NC(=O)C(I)=C1 XQFRJNBWHJMXHO-RRKCRQDMSA-N 0.000 description 1
- 235000010643 Leucaena leucocephala Nutrition 0.000 description 1
- 240000007472 Leucaena leucocephala Species 0.000 description 1
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- 229920002774 Maltodextrin Polymers 0.000 description 1
- 229930195725 Mannitol Natural products 0.000 description 1
- 235000019483 Peanut oil Nutrition 0.000 description 1
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 1
- 229920001100 Polydextrose Polymers 0.000 description 1
- 239000004743 Polypropylene Substances 0.000 description 1
- CQXADFVORZEARL-UHFFFAOYSA-N Rilmenidine Chemical compound C1CC1C(C1CC1)NC1=NCCO1 CQXADFVORZEARL-UHFFFAOYSA-N 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- 241000790234 Sphingomonas elodea Species 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- DPQAXNSOFFYKDS-UHFFFAOYSA-N Talipexole dihydrochloride Chemical compound Cl.Cl.C1CN(CC=C)CCC2=C1N=C(N)S2 DPQAXNSOFFYKDS-UHFFFAOYSA-N 0.000 description 1
- GSEJCLTVZPLZKY-UHFFFAOYSA-N Triethanolamine Chemical compound OCCN(CCO)CCO GSEJCLTVZPLZKY-UHFFFAOYSA-N 0.000 description 1
- IVOMOUWHDPKRLL-UHFFFAOYSA-N UNPD107823 Natural products O1C2COP(O)(=O)OC2C(O)C1N1C(N=CN=C2N)=C2N=C1 IVOMOUWHDPKRLL-UHFFFAOYSA-N 0.000 description 1
- WERKSKAQRVDLDW-ANOHMWSOSA-N [(2s,3r,4r,5r)-2,3,4,5,6-pentahydroxyhexyl] (z)-octadec-9-enoate Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO WERKSKAQRVDLDW-ANOHMWSOSA-N 0.000 description 1
- 235000010489 acacia gum Nutrition 0.000 description 1
- 150000001252 acrylic acid derivatives Chemical class 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 230000003213 activating effect Effects 0.000 description 1
- 125000006177 alkyl benzyl group Chemical group 0.000 description 1
- 208000002205 allergic conjunctivitis Diseases 0.000 description 1
- 229940043377 alpha-cyclodextrin Drugs 0.000 description 1
- 150000003868 ammonium compounds Chemical class 0.000 description 1
- 150000003863 ammonium salts Chemical class 0.000 description 1
- 230000036592 analgesia Effects 0.000 description 1
- 150000008064 anhydrides Chemical class 0.000 description 1
- 229940027983 antiseptic and disinfectant quaternary ammonium compound Drugs 0.000 description 1
- IEJXVRYNEISIKR-UHFFFAOYSA-N apraclonidine Chemical compound ClC1=CC(N)=CC(Cl)=C1NC1=NCCN1 IEJXVRYNEISIKR-UHFFFAOYSA-N 0.000 description 1
- 229960002610 apraclonidine Drugs 0.000 description 1
- 239000013011 aqueous formulation Substances 0.000 description 1
- 238000003556 assay Methods 0.000 description 1
- 206010003549 asthenia Diseases 0.000 description 1
- 208000024998 atopic conjunctivitis Diseases 0.000 description 1
- 235000013871 bee wax Nutrition 0.000 description 1
- 239000012166 beeswax Substances 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 229960001716 benzalkonium Drugs 0.000 description 1
- CYDRXTMLKJDRQH-UHFFFAOYSA-N benzododecinium Chemical compound CCCCCCCCCCCC[N+](C)(C)CC1=CC=CC=C1 CYDRXTMLKJDRQH-UHFFFAOYSA-N 0.000 description 1
- 102000012740 beta Adrenergic Receptors Human genes 0.000 description 1
- 108010079452 beta Adrenergic Receptors Proteins 0.000 description 1
- 230000037396 body weight Effects 0.000 description 1
- 210000000988 bone and bone Anatomy 0.000 description 1
- KGBXLFKZBHKPEV-UHFFFAOYSA-N boric acid Chemical compound OB(O)O KGBXLFKZBHKPEV-UHFFFAOYSA-N 0.000 description 1
- 239000004327 boric acid Substances 0.000 description 1
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 1
- 229910052794 bromium Inorganic materials 0.000 description 1
- 230000003139 buffering effect Effects 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- LLSDKQJKOVVTOJ-UHFFFAOYSA-L calcium chloride dihydrate Chemical compound O.O.[Cl-].[Cl-].[Ca+2] LLSDKQJKOVVTOJ-UHFFFAOYSA-L 0.000 description 1
- 229940052299 calcium chloride dihydrate Drugs 0.000 description 1
- 230000009460 calcium influx Effects 0.000 description 1
- 239000004202 carbamide Substances 0.000 description 1
- 229920003090 carboxymethyl hydroxyethyl cellulose Polymers 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 230000005754 cellular signaling Effects 0.000 description 1
- 229920002301 cellulose acetate Polymers 0.000 description 1
- 159000000006 cesium salts Chemical class 0.000 description 1
- 229960000541 cetyl alcohol Drugs 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- KXKPYJOVDUMHGS-OSRGNVMNSA-N chondroitin sulfate Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](OS(O)(=O)=O)[C@H](O)[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](C(O)=O)O1 KXKPYJOVDUMHGS-OSRGNVMNSA-N 0.000 description 1
- 229940059329 chondroitin sulfate Drugs 0.000 description 1
- 239000003240 coconut oil Substances 0.000 description 1
- 235000019864 coconut oil Nutrition 0.000 description 1
- 238000009833 condensation Methods 0.000 description 1
- 230000005494 condensation Effects 0.000 description 1
- 229920001577 copolymer Polymers 0.000 description 1
- 210000004087 cornea Anatomy 0.000 description 1
- 229940095074 cyclic amp Drugs 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 230000003001 depressive effect Effects 0.000 description 1
- 238000001514 detection method Methods 0.000 description 1
- 235000005911 diet Nutrition 0.000 description 1
- 230000037213 diet Effects 0.000 description 1
- 239000012470 diluted sample Substances 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- 125000000118 dimethyl group Chemical group [H]C([H])([H])* 0.000 description 1
- CDMADVZSLOHIFP-UHFFFAOYSA-N disodium;3,7-dioxido-2,4,6,8,9-pentaoxa-1,3,5,7-tetraborabicyclo[3.3.1]nonane;decahydrate Chemical compound O.O.O.O.O.O.O.O.O.O.[Na+].[Na+].O1B([O-])OB2OB([O-])OB1O2 CDMADVZSLOHIFP-UHFFFAOYSA-N 0.000 description 1
- 239000002270 dispersing agent Substances 0.000 description 1
- 239000003814 drug Substances 0.000 description 1
- 239000000890 drug combination Substances 0.000 description 1
- DUYCTCQXNHFCSJ-UHFFFAOYSA-N dtpmp Chemical compound OP(=O)(O)CN(CP(O)(O)=O)CCN(CP(O)(=O)O)CCN(CP(O)(O)=O)CP(O)(O)=O DUYCTCQXNHFCSJ-UHFFFAOYSA-N 0.000 description 1
- 230000002526 effect on cardiovascular system Effects 0.000 description 1
- 230000009881 electrostatic interaction Effects 0.000 description 1
- 239000003974 emollient agent Substances 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 239000003623 enhancer Substances 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 230000007717 exclusion Effects 0.000 description 1
- 230000029142 excretion Effects 0.000 description 1
- 238000000855 fermentation Methods 0.000 description 1
- 230000004151 fermentation Effects 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 229930182830 galactose Natural products 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 125000003147 glycosyl group Chemical group 0.000 description 1
- 229960004553 guanabenz Drugs 0.000 description 1
- 229960003050 guanabenz acetate Drugs 0.000 description 1
- 150000004820 halides Chemical class 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 229920000669 heparin Polymers 0.000 description 1
- 229960002897 heparin Drugs 0.000 description 1
- FBPFZTCFMRRESA-UHFFFAOYSA-N hexane-1,2,3,4,5,6-hexol Chemical compound OCC(O)C(O)C(O)C(O)CO FBPFZTCFMRRESA-UHFFFAOYSA-N 0.000 description 1
- 229920001519 homopolymer Polymers 0.000 description 1
- 239000000416 hydrocolloid Substances 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 229910052739 hydrogen Inorganic materials 0.000 description 1
- 229920003088 hydroxypropyl methyl cellulose Polymers 0.000 description 1
- 235000010979 hydroxypropyl methyl cellulose Nutrition 0.000 description 1
- 229960004716 idoxuridine Drugs 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 239000011630 iodine Substances 0.000 description 1
- 235000010445 lecithin Nutrition 0.000 description 1
- 239000000787 lecithin Substances 0.000 description 1
- 229940067606 lecithin Drugs 0.000 description 1
- 210000003041 ligament Anatomy 0.000 description 1
- 239000012669 liquid formulation Substances 0.000 description 1
- 229910052744 lithium Inorganic materials 0.000 description 1
- 229960005209 lofexidine Drugs 0.000 description 1
- KSMAGQUYOIHWFS-UHFFFAOYSA-N lofexidine Chemical compound N=1CCNC=1C(C)OC1=C(Cl)C=CC=C1Cl KSMAGQUYOIHWFS-UHFFFAOYSA-N 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- 229940050906 magnesium chloride hexahydrate Drugs 0.000 description 1
- DHRRIBDTHFBPNG-UHFFFAOYSA-L magnesium dichloride hexahydrate Chemical compound O.O.O.O.O.O.[Mg+2].[Cl-].[Cl-] DHRRIBDTHFBPNG-UHFFFAOYSA-L 0.000 description 1
- 229940091250 magnesium supplement Drugs 0.000 description 1
- 239000000594 mannitol Substances 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 230000010534 mechanism of action Effects 0.000 description 1
- 239000002207 metabolite Substances 0.000 description 1
- 125000005395 methacrylic acid group Chemical class 0.000 description 1
- 238000000034 method Methods 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 229960005016 naphazoline Drugs 0.000 description 1
- 229920001206 natural gum Polymers 0.000 description 1
- 229930014626 natural product Natural products 0.000 description 1
- 230000001537 neural effect Effects 0.000 description 1
- 210000002569 neuron Anatomy 0.000 description 1
- 230000004112 neuroprotection Effects 0.000 description 1
- 231100000956 nontoxicity Toxicity 0.000 description 1
- 229960002748 norepinephrine Drugs 0.000 description 1
- SFLSHLFXELFNJZ-UHFFFAOYSA-N norepinephrine Natural products NCC(O)C1=CC=C(O)C(O)=C1 SFLSHLFXELFNJZ-UHFFFAOYSA-N 0.000 description 1
- 239000003921 oil Substances 0.000 description 1
- 150000007530 organic bases Chemical class 0.000 description 1
- 239000007800 oxidant agent Substances 0.000 description 1
- 239000012188 paraffin wax Substances 0.000 description 1
- 239000000312 peanut oil Substances 0.000 description 1
- VLTRZXGMWDSKGL-UHFFFAOYSA-M perchlorate Inorganic materials [O-]Cl(=O)(=O)=O VLTRZXGMWDSKGL-UHFFFAOYSA-M 0.000 description 1
- 210000002856 peripheral neuron Anatomy 0.000 description 1
- 230000010399 physical interaction Effects 0.000 description 1
- 229940068196 placebo Drugs 0.000 description 1
- 239000000902 placebo Substances 0.000 description 1
- 229920002492 poly(sulfone) Polymers 0.000 description 1
- 229920002401 polyacrylamide Polymers 0.000 description 1
- 229920002239 polyacrylonitrile Polymers 0.000 description 1
- 235000013856 polydextrose Nutrition 0.000 description 1
- 239000001259 polydextrose Substances 0.000 description 1
- 229940035035 polydextrose Drugs 0.000 description 1
- 229920001155 polypropylene Polymers 0.000 description 1
- 239000004810 polytetrafluoroethylene Substances 0.000 description 1
- 229920001343 polytetrafluoroethylene Polymers 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 239000011148 porous material Substances 0.000 description 1
- 229960002816 potassium chloride Drugs 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 238000004321 preservation Methods 0.000 description 1
- 210000005215 presynaptic neuron Anatomy 0.000 description 1
- UIIIBRHUICCMAI-UHFFFAOYSA-N prop-2-ene-1-sulfonic acid Chemical compound OS(=O)(=O)CC=C UIIIBRHUICCMAI-UHFFFAOYSA-N 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- ROSDSFDQCJNGOL-UHFFFAOYSA-N protonated dimethyl amine Natural products CNC ROSDSFDQCJNGOL-UHFFFAOYSA-N 0.000 description 1
- 230000000241 respiratory effect Effects 0.000 description 1
- 230000026416 response to pain Effects 0.000 description 1
- 229960000764 rilmenidine Drugs 0.000 description 1
- 229910052701 rubidium Inorganic materials 0.000 description 1
- IGLNJRXAVVLDKE-UHFFFAOYSA-N rubidium atom Chemical compound [Rb] IGLNJRXAVVLDKE-UHFFFAOYSA-N 0.000 description 1
- CVHZOJJKTDOEJC-UHFFFAOYSA-N saccharin Chemical compound C1=CC=C2C(=O)NS(=O)(=O)C2=C1 CVHZOJJKTDOEJC-UHFFFAOYSA-N 0.000 description 1
- 229940081974 saccharin Drugs 0.000 description 1
- 235000019204 saccharin Nutrition 0.000 description 1
- 239000000901 saccharin and its Na,K and Ca salt Substances 0.000 description 1
- 239000000932 sedative agent Substances 0.000 description 1
- 230000001624 sedative effect Effects 0.000 description 1
- 239000008159 sesame oil Substances 0.000 description 1
- 235000011803 sesame oil Nutrition 0.000 description 1
- 235000010413 sodium alginate Nutrition 0.000 description 1
- 239000000661 sodium alginate Substances 0.000 description 1
- 229940005550 sodium alginate Drugs 0.000 description 1
- 229960002668 sodium chloride Drugs 0.000 description 1
- PFUVRDFDKPNGAV-UHFFFAOYSA-N sodium peroxide Chemical compound [Na+].[Na+].[O-][O-] PFUVRDFDKPNGAV-UHFFFAOYSA-N 0.000 description 1
- 159000000000 sodium salts Chemical class 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 235000011069 sorbitan monooleate Nutrition 0.000 description 1
- 239000001593 sorbitan monooleate Substances 0.000 description 1
- 229940035049 sorbitan monooleate Drugs 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 239000008347 soybean phospholipid Substances 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 230000004936 stimulating effect Effects 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- 230000001629 suppression Effects 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 239000000375 suspending agent Substances 0.000 description 1
- 235000020357 syrup Nutrition 0.000 description 1
- 239000006188 syrup Substances 0.000 description 1
- 210000002435 tendon Anatomy 0.000 description 1
- 229960000337 tetryzoline Drugs 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 231100000563 toxic property Toxicity 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- QQJLHRRUATVHED-UHFFFAOYSA-N tramazoline Chemical compound N1CCN=C1NC1=CC=CC2=C1CCCC2 QQJLHRRUATVHED-UHFFFAOYSA-N 0.000 description 1
- 229960001262 tramazoline Drugs 0.000 description 1
- AQLJVWUFPCUVLO-UHFFFAOYSA-N urea hydrogen peroxide Chemical compound OO.NC(N)=O AQLJVWUFPCUVLO-UHFFFAOYSA-N 0.000 description 1
- 230000002792 vascular Effects 0.000 description 1
- NLVXSWCKKBEXTG-UHFFFAOYSA-N vinylsulfonic acid Chemical compound OS(=O)(=O)C=C NLVXSWCKKBEXTG-UHFFFAOYSA-N 0.000 description 1
- 238000009736 wetting Methods 0.000 description 1
- 239000000080 wetting agent Substances 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/715—Polysaccharides, i.e. having more than five saccharide radicals attached to each other by glycosidic linkages; Derivatives thereof, e.g. ethers, esters
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/498—Pyrazines or piperazines ortho- and peri-condensed with carbocyclic ring systems, e.g. quinoxaline, phenazine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/715—Polysaccharides, i.e. having more than five saccharide radicals attached to each other by glycosidic linkages; Derivatives thereof, e.g. ethers, esters
- A61K31/716—Glucans
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/715—Polysaccharides, i.e. having more than five saccharide radicals attached to each other by glycosidic linkages; Derivatives thereof, e.g. ethers, esters
- A61K31/734—Alginic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/74—Synthetic polymeric materials
- A61K31/765—Polymers containing oxygen
- A61K31/78—Polymers containing oxygen of acrylic acid or derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/32—Macromolecular compounds obtained by reactions only involving carbon-to-carbon unsaturated bonds, e.g. carbomers, poly(meth)acrylates, or polyvinyl pyrrolidone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/36—Polysaccharides; Derivatives thereof, e.g. gums, starch, alginate, dextrin, hyaluronic acid, chitosan, inulin, agar or pectin
- A61K47/38—Cellulose; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0048—Eye, e.g. artificial tears
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Veterinary Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- Medicinal Chemistry (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Molecular Biology (AREA)
- Inorganic Chemistry (AREA)
- Ophthalmology & Optometry (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicinal Preparation (AREA)
Abstract
COMPOSIÇÕES CONTENDO COMPONENTES DE AGONISTA ALFA-2-ADRENÉRGICO. Composições úteis para melhorar eficácia de componentes de agonista alfa-2-adrenérgico incluem componentes de portador, componentes de agonista alfa-2-adrenérgico, componentes de realce de solubilidade que ajudam na solubilização dos componentes de agonista alfa-2-adrenérgico. Em uma modalidade, os componentes de agonista alfa-2-adrenérgico incluem agonistas alfa-2-adrenérgicos. Em outra modalidade, os componentes de realce de solubilidade incluem povidona ou álcool polivinílico.
Description
[00001] A presente invenção refere-se a composições contendo componentes alfa-2-adrenérgicos de agonista. Mais particularmente, a invenção refere-se a tais composições em que os componentes de agonista alfa-2-adrenérgico têm solubilidade realçada nas concentrações terapeuticamente eficazes, em que uma solução compreendendo os componentes alfa adrenérgico tem eficácia substancialmente similar a um determinado pH e concentração quando comparado a uma segunda solução compreendendo o componente alfa adrenérgico em um pH mais ácido e concentração mais alta.
[00002] Componentes de agonista alfa-2-adrenérgico incluem entidades químicas, tais como compostos, íons, complexos e similares, que são eficazes para agir em ou ligar- se aos receptores alfa-2-adrenérgicos e fornecem um efeito terapêutico. Quando empregado aqui, o termo "componente alfa- 2-adrenérgico" significa os agonistas e qualquer e todos os precursores, sais e ésteres destes, metabólitos destes e combinações destes.
[00003] Um dos desafios contínuos de formular composições tendo componentes de agonista alfa-2-adrenérgico é tornar tais componentes mais eficazes. Por exemplo, componentes de agonista alfa-2-adrenérgico em composições líquidas frequentemente beneficiam-se de ser solúveis nos veículos líquidos de tais composições. Tal solubilidade promove administração uniforme e precisa.
[00004] Adicionalmente, os componentes de agonista alfa-2-adrenérgico dispensados ou administrados deveriam ser vantajosamente solúveis em sistemas biológicos ou ambientes, por exemplo, para difusão in vivo eficaz ou realçada através de membranas celulares ou bicamadas lipídio. Alguns componentes de agonista alfa-2-adrenérgico, com pKa's mais altos, maior que cerca de 7, incluindo, por exemplo, brimonidina, tendem a difundir-se muito bem através de membranas de lipídio em valores de pH próximos ou
[00005] acima de seu pKa, porque quando em uma solução em tais circunstâncias eles são predominantemente não carregados em neutro em ambientes biológicos alcalinos. Sendo mais hidrofóbicos, neste pH elevado eles são mais capazes de penetrar as membranas celulares.
[00006] Porém, em valores de pH acima de cerca de 7 um fator de compensação entra em ação. Alguns destes mesmos componentes de agonista alfa-2-adrenérgico tendem a ficar menos solúveis em neutro em valores de pH biológico alcalino em soluções aquosas. Um tal decréscimo em solubilidade aquosa significa que menos do agente ativo está disponível na solução para penetrar membranas celulares a fim de liberar seu efeito terapêutico. Desse modo, mesmo que o composto solúvel seja mais capaz de penetrar membranas celulares por causa de seu estado não carregado, há menos do componente presente na solução para fornecer um tal efeito terapêutico. Desse modo, há um risco que a precipitação do componente de agonista alfa- 2-adrenérgico em valores de pH acima de cerca de 7,0 tornará os componentes de agonista alfa-2-adrenérgico menos eficazes e/ou seus efeitos terapêuticos mais variáveis em uma determinada dosagem.
[00007] Além disso, componentes de agonista alfa-2- adrenérgico solubilizados fornecem outros benefícios, por exemplo, irritação reduzida aos tecidos que interagem com componentes de agonista alfa-2-adrenérgico, do que os componentes de agonista alfa-2-adrenérgico insolúveis.
[00008] Um agonista alfa-2-adrenérgico específico, brimonidina, foi vendido como uma solução oftálmica aquosa a 0,2% sob o nome comercial ALPHAGAN®. Esta solução compreende tartarato de brimonidina a 0,2%, e é formulada em pH 6,5 em um tampão de citrato com cloreto de benzalcônio a 0,05% como um conservante.
[00009] Adicionalmente, brimonidina é da mesma forma comercializado como uma solução oftálmica a 0,15% sob o nome comercial ALPHAGAN P®. Esta solução é formulada em pH 7,2 e contém carboximetilcelulose e 0,005% de um conservante de óxi- cloro estabilizado (PURITE®).
[00010] Katz, e outros, J. Glaucoma 11:119 (Abril 2002), intitulado Twelve-Month Evaluation of Brimonidine Purite Versus Brimonidine in Patients with Glaucoma or Ocular Hypertension descreve que uma formulação contendo brimonidina a 0,15% e um conservante PURITE® tem uma eficácia similar quando administrado topicamente em pressão intraocular decrescente como uma segunda formulação contendo brimonidina a 0,2%. Este papel é por este meio incorporado por referência como parte desta descrição.
[00011] Continua a ser uma necessidade quanto a novas composições que contêm componentes de agonista alfa-2- adrenérgico que combinam um grau alto de eficácia com uma baixa incidência de efeitos colaterais, incluindo efeitos colaterais sistêmicos.
[00012] A presente invenção é baseada na descoberta de novas composições contendo componente de agonista alfa-2- adrenérgico que são capazes de liberar o agente ativo mais eficazmente para o tecido ou célula alvo. Este aumento na eficácia pode ser atribuído a dois fatores: solubilidade e um pH neutro ou alcalino. Será entendido que valores de pH determinados neste relatório descritivo devem ser medidos em temperatura ambiente.
[00013] Em uma modalidade, as composições presentes contêm certos materiais que são eficazes em pelo menos na ajuda ou auxílio na solubilização dos componentes de agonista alfa-2-adrenérgico nas composições, e preferivelmente em ambientes aos quais as composições são administradas ou introduzidas, por exemplo, ambientes biológicos, tal como o olho humano. Preferivelmente, solubilidade aquosa de componentes de agonista alfa-2-adrenérgico de acordo com a presente invenção facilitam a liberação consistente e predicável do efeito terapêutico ao tecido ou célula alvo.
[00014] Em outra modalidade, a presente invenção é esboçada em soluções aquosas contendo componentes de agonista alfa-2-adrenérgico que têm um pH acima de cerca de 7,0, preferivelmente entre cerca de pH 7,0 e cerca de pH 8,5, mais preferivelmente entre cerca de pH 7,2 e cerca de pH 8,2 ou cerca de pH 7,2, ainda mais preferivelmente entre cerca de pH 7,5 e cerca de pH 8,0 ou em cerca de pH 7,7. Nesta modalidade, a solução aquosa pode opcionalmente conter um material ou mistura de materiais que é eficaz pelo menos na ajuda ou auxílio na solubilização dos componentes de agonista alfa-2- adrenérgico.
[00015] Alternativamente, a solução pode necessitar de tais materiais de solubilização exógenos e compreender ou consistir essencialmente em um componente de agonista alfa-2- adrenérgico solúvel em solução aquosa em um valor de pH como indicado acima. Neste aspecto, o pH neutro ou alcalino permite a passagem do componente alfa-2-agonista através de membranas celulares mais facilmente.
[00016] Desse modo, quando o pH do componente de agonista alfa-2-adrenérgico solúvel está acima de cerca de 7,0, ele ajuda no transporte de tais componentes através de membranas de lipídio. Da mesma forma, uma vez que os componentes alfa adrenérgicos são solúveis, a dosagem do agonista alfa-2-adrenérgico é segura e reproduzível.
[00017] Certos componentes alfa-2-adrenérgicos foram conhecidos por ter efeitos colaterais indesejáveis. Por exemplo, clonidina e tizanidina foram mostradas ter efeitos sedativos e depressivos cardiovasculares e respiratórios quando administrados sistemicamente. Desse modo, qualquer formulação de agonista alfa-2-adrenérgico em que a eficácia pode ser mantida em uma dose eficaz mais baixa do que é geralmente empregada seria claramente vantajosa.
[00018] Em outro aspecto da invenção, composições contendo componente alfa-2-adrenérgico foram descritas as quais incluem conservante que fornecem vantagens significativas, por exemplo, interações adversas reduzidas com os componentes de agonista alfa-2-adrenérgico e/ou com os pacientes em que as composições são administradas, ao mesmo tempo que mantendo a eficácia do conservante. Preferivelmente, a composição alfa adrenérgica é brimonidina.
[00019] As composições presentes preferivelmente realçam ou mantêm a eficácia de componentes de agonista alfa- 2-adrenérgico anteriores, enquanto fornecendo benefícios adicionais não presentes em formulações anteriores. Isto é realizado mantendo-se o componente de agonista alfa-2- adrenérgico em solução aquosa enquanto simultaneamente mantendo um valor de pH acima de cerca de 7,0, preferivelmente entre cerca de pH 7,0 e cerca de pH 8,5, mais preferivelmente entre cerca de pH 7,2 e cerca de pH 8,2 ou cerca de pH 7,2, ainda mais preferivelmente entre cerca de pH 7,5 e cerca de pH 8,0 ou em cerca de pH 7,7. Aumentando-se a permeabilidade de membrana do componente de agonista alfa-2-adrenérgico é possível diminuir a concentração do agonista alfa 2 na formulação administrada, particularmente (mas não exclusivamente) brimonidina, desse modo reduzindo quaisquer efeitos colaterais sistêmicos, particularmente quando a formulação é determinada sistemicamente.
[00020] Dentro do âmbito de algumas modalidades da presente invenção, a concentração de brimonidina (incluindo e seus sais farmaceuticamente aceitáveis tal como o tartarato) em uma formulação oftálmica tópica pode ser reduzida abaixo de 0,2% (p/v) (preferivelmente entre cerca de 0,01% e cerca de 0,1% (p/v)), enquanto mantendo a mesma ou eficácia substancialmente similar como o produto ALPHAGAN®; uma formulação de tartarato de brimonidina a 0,2% que tem um pH de cerca de pH 6,6 a cerca de pH 6,8. Em outra modalidade, a concentração de brimonidina é preferivelmente cerca de 0,01% a cerca de 0,15% (p/v) em um pH acima de cerca de 7,0 (preferivelmente cerca de pH 7,2 - cerca de pH 7,7, com qualquer diferença na eficácia entre as duas formulações que necessitam de qualquer diferença significativa na eficácia.
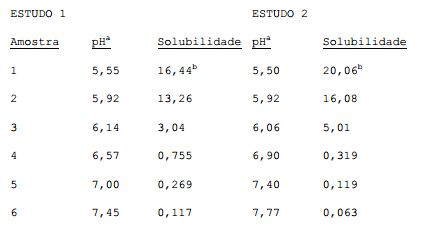
[00021] Como mostrado na Figura 1, a solubilidade de um agonista alfa-2-adrenérgico representativo, tartarato de 5- bromo-6-(2-imidozolin-2-ilamino) quinoxalina, diminui quando o pH da solução aquosa aumenta. O pKa de 5-bromo-6-(2- imidozolin-2-ilamino) quinoxalina é cerca de 7,4. Quando a solução fica mais alcalina, a maioria das moléculas na solução fica eletronicamente neutra, e portanto crescentemente hidrofóbica.
[00022] Figura 1 mostra que várias soluções contendo 5- bromo-6-(2-imidozolin-2-ilamino) quinoxalina compartilham completamente a mesma tendência geral; sua solubilidade diminui com o pH crescente. A curva identificada com uma cruz (*) é uma solução aquosa contendo o agente ativo sem carboximetilcelulose adicionado (CMC); tais soluções estão dentro do escopo de certas modalidades desta invenção.
[00023] Em um aspecto, a eficácia dos componentes de agonista alfa-2-adrenérgico é aumentada multiplicando-se a solubilidade dos componentes de agonista alfa-2-adrenérgico, preferivelmente em valores de pH mais altos do que neutros. Neste aspecto da invenção, a invenção inclui, além dos componentes de agonista alfa-2-adrenérgico, componentes de realce de solubilidade (SECs) em quantidades eficazes para realçar a solubilidade dos componentes de agonista alfa-2- adrenérgico em um determinado pH. Preferivelmente, estes SECs são aniônicos na natureza, e ainda mais preferivelmente, eles são poliméricos na natureza. Em uma modalidade, o SEC é um derivado de celulose, em outra modalidade o SEC não é um derivado de celulose ou uma ciclodextrina.
[00024] Neste aspecto da invenção, os componentes de agonista alfa-2-adrenérgico são mais solúveis nas composições presentes tendo, por exemplo, valores de pH de cerca de 7 ou maior, relativos a composições substancialmente idênticas que necessitam dos SECs. Em outra modalidade, os componentes de agonista alfa-2-adrenérgico das composições presentes são mais solúveis em ambientes biológicos neutros ou alcalinos em que as composições são administradas relativas aos componentes de agonista alfa-2-adrenérgico em composições similares sem os SECs. Este último aspecto é particularmente verdadeiro quando os compostos de agonista alfa-2-adrenérgico são liberados em seu sítio de ação topicamente.
[00025] Os componentes de agonista alfa-2-adrenérgico empregados na presente invenção incluem imino-imidazolinas, imidazolinas, imidazóis, azepinas, tiazinas, oxazolinas, guanidinas, catecolaminas, sais biologicamente compatíveis e ésteres e misturas destes. Preferivelmente, os componentes de agonista alfa-2-adrenérgico incluem componentes de quinoxalina. Componentes de quinoxalina incluem quinoxalina, sais biologicamente compatíveis destes, ésteres destes, outros derivados destes e similares, e misturas destes. Exemplos não limitantes de derivados de quinoxalina incluem (2-imidozolin- 2-ilamino) quinoxalina, 5-bromo-6-(2-imidozolin-2-ilamino) quinoxalina, e sais biologicamente compatíveis destes e ésteres destes, preferivelmente o tartarato de 5-bromo-6-(2- imidozolin-2-ilamino) quinoxalina, e similares e misturas destes. Em seguida, o tartarato de 5-bromo-6-(2-imidozolin-2- ilamino) quinoxalina é referido como "tartarato de brimonidina".
[00026] Em uma modalidade preferida, os componentes de agonista alfa-2-adrenérgico, tais como aqueles listados acima, são seletivos para os receptores alfa-2A-adrenérgicos, receptores de alfa-2B-adrenérgico e/ou receptores alfa-2D- adrenérgicos em relação à sua atividade em um ou mais outro receptor adrenérgico. Preferivelmente, os componentes de agonista alfa-2-adrenérgico são seletivos para os receptores alfa-2A-adrenérgico, receptores alfa-2B-adrenérgicos e/ou receptores alfa-2D-adrenérgicos em comparação à sua atividade nos receptores alfa-1-adrenérgicos.
[00027] Em uma modalidade, os componentes de agonista alfa-2-adrenérgico são pelo menos cerca de 30% não carregados nas composições agora descritas e reivindicadas, preferivelmente pelo menos cerca de 50% não carregados. Aqueles de experiência na técnica apreciarão que o pKa é o log negativo da constante de ionização (ou o pH em que o composto é 50% ionizado), e que uma referência neste pedido a um percentual específico do composto não carregado (tal como, por exemplo, pelo menos 30% ou 50% não carregado) é destinada a referir-se ao composto em uma base estequiométrica.
[00028] Ainda mais preferivelmente, os componentes de agonista alfa-2-adrenérgico solúveis são da mesma forma pelo menos cerca de 30% não carregados ou pelo menos cerca de 50% não carregados no ambiente biológico no qual as composições são administradas.
[00029] Quando os componentes de agonista alfa-2- adrenérgico são formulados com um SEC, o SEC pode incluir um componente polianiônico ou não iônico. Quando empregado aqui, o termo "componente polianiônico" se refere a uma entidade química, por exemplo, uma espécie ionicamente carregada, tal como um material polimérico ionicamente carregado, que inclui cargas aniônicas discretos múltiplas. SECs não iônicos podem incluir álcool polivinílico (PVA), po-livinil pirrolidona (povidona), e várias gomas e outros agentes não iônicos.
[00030] Em uma modalidade preferida, o SEC é um componente polianiônico, que pode ser selecionado de materiais poliméricos tendo cargas aniônicas múltiplas e misturas destes.
[00031] Componentes polianiônicos particularmente úteis são selecionados de polímeros aniônicos derivados de ácido acrílico (significando incluir polímeros de ácido acrílico, acrilatos e similares e misturas destes), polímeros aniônicos derivados de ácido metacrílico (significando incluir polímeros de ácido metacrílico, metacrilatos e similares e misturas destes), polímeros aniônicos derivados de ácido algínico (significando incluir ácido algínico, alginatos e similares e misturas destes), polímeros aniônicos de aminoácidos (significando incluir polímeros de aminoácidos, sais de aminoácido e similares e misturas destes), e similares, e misturas destes. Muitos componentes polianiônicos úteis são aqueles selecionados de derivados de celulose aniônicos e misturas destes, especialmente carboximetil celulose e seus derivados.
[00032] O componente polianiônico preferivelmente é suficientemente aniônico para interagir com ou de outra maneira afetar ou aumenta ou aumentar a solubilidade dos componentes alfa-2-adrenérgicos. Esta interação é preferivelmente suficiente para tornar os componentes alfa-2- adrenérgicos substancialmente completamente solúveis em concentrações terapeuticamente eficazes. A quantidade de SEC na composição preferivelmente está na faixa de cerca de 0,1% (p/v) a cerca de 30% (p/v), mais preferivelmente cerca de 0,2% (p/v) a cerca de 10% (p/v), e ainda mais preferivelmente cerca de 0,2% (p/v) a cerca de 0,6% (p/v).
[00033] As composições podem da mesma forma incluir componentes de portador, por exemplo, componentes de portador líquidos aquosos. Em uma modalidade, as composições têm valores de pH acima de cerca de 7,0, preferivelmente entre cerca de pH 7,0 e cerca de pH 8,5, mais preferivelmente entre cerca de 7,2 e cerca de 8,2, ainda mais preferivelmente entre cerca de 7,5 e cerca de 8,0. Além disso, preferivelmente estas composições são oftalmicamente aceitáveis.
[00034] Em outra modalidade preferida, uma composição é fornecida a qual inclui um componente de agonista alfa-2- adrenérgico em uma quantidade eficaz para fornecer pelo menos um benefício terapêutico em um paciente a quem a composição é administrada, um derivado de celulose aniônico em uma quantidade eficaz para aumentar a solubilidade do componente de agonista alfa-2-adrenérgico e um componente de portador líquido aquoso. O componente de agonista alfa-2-adrenérgico preferivelmente compreende um tartarato de 5-bromo-6-(2- imidozolin-2-ilamino) quinoxalina. O derivado de celulose aniônico preferivelmente compreende uma carboximetilcelulose. A concentração do derivado de celulose aniônico na composição deveria ser cerca de 0,2% (p/v) a cerca de 0,6% (p/v).
[00035] Nas modalidades preferidas da composição da invenção, a composição contém 5-bromo-6-(2-imidozolin-2- ilamino) quinoxalina ou um sal ou éster deste; a concentração deste agonista alfa-2-adrenérgico é menor do que 0,2%; preferivelmente entre 0,2% (p/v) e cerca de 0,001% (p/v), mais preferivelmente cerca de 0,15% (p/v) ou menos, ainda mais preferivelmente entre 0,15% (p/v) e cerca de 0,001% (p/v), preferivelmente cerca de 0,1% (p/v) ou menos.
[00036] Da mesma forma, as modalidades preferidas da composição desta invenção compreendem uma solução aquosa em pH neutro ou alcalino. Preferivelmente a composição é cerca de pH 7,0 ou maior em temperatura ambiente ou cerca de 7,2 ou maior em temperatura ambiente, ainda mais preferivelmente cerca de 7,5 ou maior em temperatura ambiente, mais preferivelmente em cerca de 7,7 ou maior em temperatura ambiente.
[00037] Em uma modalidade preferida, as presentes composições são oftalmicamente aceitáveis, por exemplo, as composições não têm propriedades tóxicas ou danosas que poderiam substancialmente prejudicar o olho humano ou do animal a quem as composições são administradas.
[00038] Em um aspecto da invenção, complexos podem ser formados nas composições. Em uma modalidade, os complexos incluem unidades de monômero derivadas a partir de pelo menos um componente de quinoxalina. Em uma modalidade preferida, os complexos da presente invenção são dímeros. Em uma modalidade particularmente preferida, os complexos são complexos, especialmente dímeros, de tartarato de bromonidina.
[00039] Em outro amplo aspecto da presente invenção, as composições são fornecidas a quais compreendem um componente de agonista alfa-2-adrenérgico e um componente conservante em uma quantidade eficaz para pelo menos ajudar conservando-se as composições. Preferivelmente, os componentes conservantes incluem componentes de óxi-cloro, tais como compostos, íons, complexos e similares que são biologicamente aceitáveis, quimicamente estáveis e não substancialmente ou significantemente e prejudicialmente afetam o componente de agonista alfa-2-adrenérgico nas composições ou os pacientes a quem as composições são administradas. Tais composições preferivelmente são substancialmente livres de ciclodextrinas nas composições ou nos pacientes a quem as composições são administradas.
[00040] Qualquer característica ou combinação de características descritas aqui está incluída dentro do escopo da presente invenção contanto que as características incluídas em qualquer tal combinação não sejam mutuamente inconsistentes visto que ficará evidente a partir do contexto, deste relatório descritivo, e do conhecimento de alguém de experiência ordinária na técnica. Quando as faixas numéricas são indicadas aqui, elas deveriam ser entendidas como descrevendo cada e todo valor individual que inclui dentro da faixa, isto é, que elas são uma simples abreviação da listagem de todos estes valores.
[00041] Vantagens adicionais e aspectos da presente invenção ficarão evidentes na seguinte descrição detalhada e reivindicações.
[00042] A figura 1 é um gráfico de tartarato de brimonidina solúvel em solução aquosa em temperatura ambiente plotado versus pH em várias concentrações de carboximetilcelulose.
[00043] Composições terapeuticamente eficazes compreendendo componentes de agonista alfa-2-adrenérgico são fornecidas. Estas composições fornecem a vantagem de ser formuladas em pH neutro ou alcalino, desse modo fornecendo uma dosagem do agente ativo em uma forma solúvel de lipídio mais substancialmente não carregada, mais solúvel em lipídeo. Desde que os componentes de agonista alfa-2-adrenérgico são mais capazes de cruzar membranas celulares as composições da presente invenção mantêm ou aumentam a eficácia relativa a uma composição formulada em pH ácido.
[00044] Cada aspecto das composições da invenção é necessariamente e terapeuticamente eficaz; uma composição que não é terapeuticamente eficaz não está destinada a incluir-se no âmbito de qualquer reivindicação a este respeito. Por "terapeuticamente eficaz" é significado que a composição é capaz de exercer um efeito medicamente benéfico estatisticamente significante quando empregada como prescrita ou direcionada, quando comparada a um placebo. Desse modo, uma composição prescrita para uso para diminuir a pressão intraocular é e deve ser destinada a se referir a uma composição tendo um efeito hipotensivo ocular estatisticamente significante quando empregada como direcionado.
[00045] Em uma modalidade, a presente invenção considera uma composição, tal como uma composição oftálmica tópica, compreendendo um componente de agonista alfa-2- adrenérgico formulado em solução aquosa em um pH tal que o componente alfa adrenérgico é pelo menos 30%, pelo menos 40%, pelo menos 50% ou pelo menos 60% não carregado.
[00046] Em uma modalidade particularmente preferida, a invenção é direcionada a uma composição compreendendo 5-bromo- 6-(2-imidozolin-2-ilamino) quinoxalina, ou sais deste, em que a solução é formulada em uma concentração menor do que 0,2% (p/v). Preferivelmente, o ingrediente ativo está presente na composição em uma concentração de preferivelmente entre 0,2% (p/v) e cerca de 0,001% (p/v), mais preferivelmente cerca de 0,15% (p/v) ou menos, ainda mais preferivelmente entre 0,15% (p/v) e cerca de 0,001% (p/v), mais preferivelmente cerca de 0,1% (p/v) ou menos.
[00047] Como um outro aspecto preferido desta modalidade da invenção, o 5-bromo-6-(2-imidozolin-2-ilamino) quinoxalina, ou sal deste, está em solução aquosa em um pH maior do que cerca de 7,0 em temperatura ambiente ou cerca de 7,2 ou maior em temperatura ambiente, ainda mais preferivelmente cerca de 7,5 ou maior em temperatura ambiente, mais preferivelmente em cerca de 7,7 ou maior em temperatura ambiente.
[00048] Em outra modalidade, os componentes de agonista alfa-2-adrenérgico nas presentes composições são tornados mais solúveis, particularmente em valores de pH neutros a alcalinos, e podem ser mais eficazmente utilizados como agentes terapêuticos. Os SECs empregados nas presentes composições podem ser eficazes na solubilização de componentes de agonista alfa-2-adrenérgico, componentes de agonista alfa-2-adrenérgico não carregados ou ambos. As presentes composições incluem componentes de portador líquidos e têm as características de líquido, por exemplo, soluções, líquido aquoso.
[00049] Componentes de agonista alfa-2-adrenérgico têm uma atividade estimuladora direcionada para pelo menos um dos subtipos de receptor de alfa 2, alfa 2A, alfa 2B ou alfa 2C. Preferivelmente, a atividade em tal(is) subtipo(s) é pelo menos 10 vezes maior do que em qualquer subtipo de receptor alfa 1 adrenérgico. Ainda mais preferivelmente, a atividade em um receptor alfa 2 é pelo menos 50 vezes maior, ou pelo menos 100 vezes maior ou pelo menos 1000 vezes maior do que em qualquer receptor de alfa 1. Alfa-2-agonistas exemplares incluem, sem limitação, xilazina, detomidina, medetomidina, clonidina, brimonidina, tizanidina, lofexidina, guanfacina, acetato de guanabenz, e dexmedetomidina.
[00050] Componentes de agonista alfa-2-adrenérgico são solúveis nas presentes composições em valores de pH maiores do que 7. Em uma modalidade, as presentes concentrações contêm os componentes de agonista alfa adrenérgicos em ou quase em seu limite de solubilidade aquoso em temperatura de ambiente e mantêm eficácia comparável a concentrações mais altas dos componentes de agonista alfa adrenérgico em uma composição similar em um pH de 7 ou abaixo.
[00051] Em uma modalidade preferida, os componentes de agonista alfa-2-adrenérgico são combinados com pelo menos um SEC nas composições presentemente reivindicadas, e portanto têm solubilidade aumentada nas presentes composições em valores de pH maiores do que 7, tal como, sem limitação, cerca de pH 7,2, cerca de pH 7,4, cerca de pH 7,7, e cerca de pH 8,0, quando comparados a componentes de agonista alfa-2-adrenérgico idênticos, em concentrações comparáveis, em composições necessitando de SECs.
[00052] Uma composição preferida compreende cerca de 0,1% (p/v) de brimonidina em um pH de cerca de 7,7. Ainda mais preferivelmente, uma tal composição da mesma forma compreende um SEC. O SEC pode ser selecionado a partir de qualquer SEC, porém SECs preferidos incluem carboximetil celulose, álcool polivinílico, ou polivinil pirrolidona.
[00053] Em outra modalidade, os componentes de agonista alfa-2-adrenérgico têm solubilidade aumentada nas presentes composições em valores de pH na faixa de cerca de 7 a cerca de 10 e, quando comparados a componentes de agonista alfa-2- adrenérgico idênticos em composições similares, em concentrações comparáveis, sem os SECs. Ainda mais preferivelmente os componentes de agonista alfa-2-adrenérgico nas composições da presente invenção têm tal solubilidade aumentada em valores de pH acima de cerca de 7,0, preferivelmente entre cerca de pH 7,0 e cerca de pH 8,5, mais preferivelmente entre cerca de 7,2 e cerca de 8,2, ainda mais preferivelmente entre cerca de 7,5 e cerca de 8,0, ou em cerca de pH 7,7.
[00054] Sem desejar estar limitado por qualquer teoria ou mecanismo de operação, acredita-se que os componentes de agonista alfa-2-adrenérgico solubilizados são mais capazes de cruzar membranas de lipídio relativas a componentes de agonista alfa-2-adrenérgico não solubilizados. Além disso, acredita-se da mesma forma que um componente de agonista alfa- 2-adrenérgicos não carregado seja mais capaz de cruzar uma membrana de lipídio do que aquele que é carregado.
[00055] Em uma modalidade, os SECs são capazes de solubilizar os componentes de agonista alfa-2-adrenérgico nos ambientes biológicos em que eles são introduzidos em concentrações terapeuticamente eficazes. Preferivelmente, os ambientes biológicos nos quais as presentes composições são introduzidas têm valores de pH variando de cerca de 7 a cerca de 9. Por exemplo, uma composição compreendendo um SEC e um componente de agonista alfa-2-adrenérgico pode ser topicamente administrada à superfície de um olho, que tem um pH de cerca de 7 em que o componente de agonista alfa-2-adrenérgico é substancialmente solúvel na área administrada. Além disso, os componentes de agonista alfa-2-adrenérgico solúveis na área administrada difundirão mais facilmente através das membranas de lipídio biológicas do que componentes de agonista alfa-2- adrenérgico que não são solúveis, seja na presença de SECs ou de outra maneira. Manter a solubilidade de componentes de agonista alfa-2-adrenérgico em solução aquosa preferivelmente reduz a irritação a tecidos sensíveis em contato ou interagindo com os componentes de agonista alfa-2-adrenérgico.
[00056] Claro, os componentes de agonista alfa-2- adrenérgico solúveis nas composições por meio desta descritos e reivindicados devem ser capazes de ser liberados em uma concentração terapeuticamente eficaz. Enquanto é claramente possível preparar uma solução contendo pequenas concentrações que tendem a desaparecer, de componentes de agonista alfa-2- adrenérgico solúveis, uma tal solução não é terapeuticamente útil a menos que seja eficaz para conferir um benefício ao mamífero que a recebe. Preferivelmente, as presentes composições são capazes de liberar um efeito terapêutico substancialmente igual a, ou maior do que, aquele fornecido por uma formulação do mesmo componente de agonista alfa-2- adrenérgico em um pH menor do que 7,0. Ainda mais preferivelmente, as presentes composições são capazes de liberar um efeito terapêutico substancialmente igual a, ou maior do que, aquele fornecido por uma formulação do mesmo componente de agonista alfa-2-adrenérgico em um pH menor do que 7,0, e em uma concentração mais baixa do agente ativo do que na formulação de pH inferior.
[00057] Em uma modalidade preferida os componentes de agonista alfa-2-adrenérgico presentemente úteis são escolhidos para beneficiarem-se de e ser estabilizados ou solubilizados pela presença dos SECs. Nesta modalidade, os componentes de agonista alfa-2-adrenérgico são fornecidos com solubilidade aparente aumentada preferivelmente solubilidade de água aparente aumentada, pela presença dos SECs.
[00058] Exemplos de componentes de agonista alfa-2- adrenérgico incluem moléculas contendo aminas. Preferivelmente, os componentes de agonista alfa-2-adrenérgico são moléculas contendo amina com pKa's maiores do que cerca de 7, mais preferivelmente cerca de 7 a cerca de 9.
[00059] Componentes de agonista alfa-2-adrenérgico incluem agonistas alfa-2-adrenérgicos. Quando aqui empregado, o termo agonista alfa-2 adrenérgico inclui entidades químicas, tais como compostos, sais, ésteres, íons, complexos e similares, que ligam-se a, e ativam, um ou mais dentre o receptor adrenérgico alfa 2 A, o receptor adrenérgico alfa 2 B e receptor adrenérgico alfa 2 C. Quando estimulada, esta proteína G acoplada a receptores realiza várias funções de sinalização de célula; uma ou mais podem estar envolvidas, por exemplo, na inibição da liberação pré-sináptica da norepineferina de neurotransmissor. Enquanto não desejando estar ligado por teoria, pensa-se que a estimulação de um ou mais dos subtipos de receptor alfa 2 resulte na supressão de influxo de cálcio no neurônio alvo, desse modo inibindo a liberação de neurotransmissores. Esta inibição de norepinferina em neurônios pré-sinápticos parece estar envolvida em analgesia inibindo-se a geração ou propagação da resposta à dor.
[00060] Enquanto os receptores alfa 2 são predominantemente encontrados em um sítio pré-sináptico, receptores alfa 2 podem da mesma forma ser encontrados em locais pós- e extra sinápticos e em neurônios do CNS e periféricos.
[00061] O agonista alfa-2 adrenérgico da invenção liga- se aos receptores alfa-2 adrenérgicos, e são capazes de causar uma diminuição ou inibição da liberação de norepinefrina neuronal nos sítios pré-sinápticos em células afetadas. Adicionalmente, eles podem trabalhar em receptores alfa-2 adrenérgicos pós-sinapticamente, por exemplo, inibindo-se a formação estimulada por receptor beta adrenérgico de AMP cíclica.
[00062] Agonistas alfa-2 adrenérgicos da mesma forma incluem compostos que têm atividade neuroprotetora. Por exemplo, 5-bromo-6-(2-imidozolin-2-ilamino) quinoxalina é um agonista alfa-2-adrenérgico que tem uma atividade neuroprotetora. O mecanismo ou neuroproteção ainda não é completamente conhecido.
[00063] Sem limitar a invenção aos grupos específicos e compostos listados, o seguinte é uma lista de agonistas alfa-2 adrenérgicos representativos úteis nesta invenção: imino- imidazolinas, incluindo clonidina, apraclonidina; imidazolinas, incluindo nafazolina, ximetazolina, tetraidrozolina, e tramazolina; imidazóis, incluindo detomidina, medetomidina, e dexmedetomidina; azepinas, incluindo B-HT 920 (6-alil-2-amino- 5,6,7,8 tetraidro-4H-tiazolo[4,5-d]-azepina e B-HT 933; tiazinas, incluindo xilazina; oxazolinas, incluindo rilmenidina; guanidinas, incluindo guanabenz e guanfacina; catecolaminas; e similares e ésteres, sais e derivados destes.
[00064] Agonistas alfa-2-adrenérgicos particularmente úteis incluem componentes de quinoxalina. Em uma modalidade, os componentes de quinoxalina incluem quinoxalina, derivados destes e misturas destes. Preferivelmente, os derivados de quinoxalina incluem (2-imidozolin-2-ilamino) quinoxalina. Mais preferivelmente, os derivados de quinoxalina incluem 5-haleto- 6-(2-imidozolin-2-ilamino) quinoxalina. O "haleto" de 5- haleto-6-(2-imidozolin-2-ilamino) quinoxalina pode ser um flúor, um cloro, um iodo ou preferivelmente, um bromo, para formar 5-bromo-6-(2-imidozolin-2-ilamino) quinoxalina. Ainda mais preferivelmente, os derivados de quinoxalina a ser empregados de acordo com esta invenção incluem um tartarato de 5-bromo-6-(2-imidozolin-2-ilamino) quinoxalina ou tartarato de brimonidina.
[00065] Outros derivados de quinoxalina úteis são bem conhecidos. Por exemplo, derivados úteis de uma quinoxalina incluem aqueles descritos por Burke e outros, Patente U.S. No 5.703.077. Veja da mesma forma Danielwicz e outros 3.890.319. Cada uma das descrições de Burke e outros e Danielwicz e outros está incorporada em sua totalidade por referência aqui.
[00066] As quinoxalinas e derivados destas, por exemplo, tartarato de brimonidina, que contêm amina e preferivelmente têm pKa's maiores do que 7, preferivelmente cerca de 7,5 a 9.
[00067] Análogos dos compostos anteriores que funcionam como agonistas alfa-2 adrenérgicos da mesma forma são especificamente destinados a ser abrangidos pela invenção.
[00068] Preferivelmente, os agonistas alfa-2- adrenérgicos da presente invenção, são eficazes na ativação de receptores alfa-2A-adrenérgicos, receptores alfa-2B- adrenérgicos e/ou receptores alfa-2C adrenérgicos.
[00069] Em uma modalidade, os componentes de agonista alfa-2-adrenérgico são pelo menos cerca de 30% não carregados nas composições reivindicadas e presentemente descritas, preferivelmente pelo menos cerca de 50% não carregados. Aqueles de experiência na técnica apreciarão que o pKa é o log negativo da ionização constante (ou o pH em que o composto é 50% ionizado), e que uma referência neste pedido a um percentual específico do composto não carregado (tal como, por exemplo, pelo menos 30% ou 50% não carregado) é destinado a se referir ao composto em uma base estequiométrica.
[00070] Preferivelmente, os componentes de agonista alfa-2-adrenérgico solúveis das presentes formulações são pelo menos cerca de 30% não carregados, ou pelo menos cerca de 50% não carregados no ambiente biológico em que as composições são administradas.
[00071] Sem desejar estar limitado por qualquer teoria ou mecanismo de ação, acredita-se que as formas não carregadas dos presentes compostos alfa 2 adrenérgicos facilitam sua permeabilidade através das bicamadas de lipídio de membrana.
[00072] Nessas modalidades envolvendo um SEC, qualquer SEC adequado (ou combinação de SECs) pode ser empregado de acordo com a presente invenção. Em uma modalidade, os SECs incluem SECs não carregados, tal como, sem limitação, componentes de pirrolidona, álcool polivinílico (PVA), derivados de celulose não carregados, Pemulin, carbômeros, Carbopols e similares. Exemplos de componentes de pirrolidona são polivinilpirrolidonas (povidona) e derivados destes. Em uma outra modalidade, os SECs incluem componentes polianiônicos. Os componentes polianiônicos úteis incluem, porém não são limitados aqueles materiais que são eficazes no aumento da solubilidade aparente, preferivelmente solubilidade em água, de componentes de agonista alfa-2-adrenérgico pobremente solúveis e/ou realçam a estabilidade dos componentes de agonista alfa-2-adrenérgico e /ou reduzem os efeitos colaterais não desejados dos componentes de agonista alfa-2-adrenérgico. Além disso, o componente polianiônico é preferivelmente e oftalmicamente aceitável para tratamento tópico nas concentrações empregadas. Adicionalmente, o componente polianiônico preferivelmente inclui três (3) ou mais cargas aniônicas (ou negativas). No evento em que o componente polianiônico é um material polimérico, é preferido que cada uma das unidades de repetição do material polimérico inclua uma carga aniônica discreta. Componentes aniônicos particularmente úteis são aqueles que são solúveis em água, por exemplo, solúveis nas concentrações e valores de pH empregados no meio aquoso líquido presentemente útil, tal como um meio aquoso líquido contendo os componentes alfa-2- adrenérgicos.
[00073] O componente polianiônico é preferivelmente e suficientemente aniônico para formar uma iônica ou outra interação eletrostática com aquelas partes polares ou carregadas do componente de agonista alfa-2-adrenérgico. Tal interação é acreditada ser desejável para solubilizar certas formulações do componente de agonista alfa-2-adrenérgico e/ou para manter tal componente de agonista alfa-2-adrenérgico solúvel no componente de portador, por exemplo um meio líquido.
[00074] Componentes polianiônicos da mesma forma incluem um ou mais materiais poliméricos tendo cargas aniônicas múltiplas. Exemplos incluem: carboximetilamidos de metal carboximetilidroxietilamidos de metal poliacrilonitrilos e poliacrilamidas hidrolisados heparina homopolímeros e copolímeros de um ou mais dentre: ácidos acrílico e metacrílico acrilatos e metacrilatos de metal ácido algínico alginatos de metal ácido vinilsulfônico vinilsulfonato de metal aminoácidos, tal como ácido aspártico, ácido glutâmico e similares sais de metal de aminoácidos ácido p-estirenossulfônico p-estirenossulfonato de metal ácido 2-metacriloiloxietilsulfônico 2-metacriloiloxetilsulfonatos de metal ácidos 3-metacriloilóxi-2-hidroxipropilsulônico 3-metacriloilóxi-2-hidroxipropilsulfonatos de metal ácido 2-acrilamido-2-metilpropanossulfônico 2-acrilamido-2-metilpropanossulfonatos de metal ácido alilsulfônico alilsulfonato de metal e similares.
[00075] Por "metal" é significado metais alcalinos- terrosos e alcalinos tal como Na, K, Ca e similares.
[00076] Em outra modalidade, os componentes polianiônicos incluem polissacarídeos aniônicos que tendem a existir em formas ionizadas em pHs mais altos, por exemplo, pH's de cerca de 7 ou mais altos. Os seguintes são alguns exemplos de polissacarídeos aniônicos que podem ser empregados de acordo com esta invenção.
[00077] Polidextrose é um polímero de condensação aleatoriamente ligado de dextrose que é apenas metabolizada parcialmente por mamíferos. O polímero pode conter uma quantidade menor de sorbitol ligado, ácido cítrico, e glicose. Sulfato de condroitina da mesma forma conhecido como sulfato de condroitina de sódio é um mucopolissacarídeo encontrado em toda parte do tecido humano, especificamente cartilagem, ossos, tendões, ligamentos, e paredes vasculares. Este polissacarídeo foi extraído e purificado a partir da cartilagem de tubarões. Carragenina é um polissacarídeo linear tendo unidades de galactose repetidas e 3,6 unidades de anidrogalactose, ambas das quais podem ser sulfatadas ou não sulfatadas, ligadas alternando-se 1 - 3 e 1 - 4 ligações alfa glicosídicas. Carragenina é um hidrocolóide que é extraído do calor de várias espécies de alga marinha vermelha e musgo irlandês. Maltodextrinas são polímeros de glicose solúveis em água que são formados pela reação de amido com um ácido e/ou enzimas na presença de água.
[00078] Outros polissacarídeos aniônicos constatados úteis na presente invenção são materiais coloidais hidrofílicos e incluem as gomas naturais tais como goma gellan, gomas de alginato, isto é, sais de metal alcalino e amônio de ácido algínico e misturas destes. Além disso, quitosana, que é o nome comum para quitina desacetilada é útil. Quitina é um produto natural compreendendo poli-(N-acetil-D-glicosamina). Goma gellan é produzida a partir da fermentação de Pseudomonas elodea para produzir um heteropolis-sacarídeo extracelular. Os alginatos e quitosana estão disponíveis como pós secos a partir de, por exemplo, Protan, Inc., Commack, N.Y. Goma gellan pode ser comprada a partir de, por exemplo, the Kelco Division of Merk & Co., Inc., San Diego, Calif.
[00079] Geralmente, os alginatos podem ser qualquer dos alginatos solúveis em água incluindo os alginatos de metal alcalino, tal como sais de sódio, potássio, lítio, rubídio e césio de ácido algínico, bem como o sal de amônio, e os alginatos solúveis a partir de uma base orgânica tal como alginatos de mono-, di-, ou trietanolamina, alginatos de anilina, e similares. Geralmente, cerca de 0,2% a cerca de 1% em peso e, preferivelmente, cerca de 0,5% a cerca de 3,0% em peso de gellan, polissacarídeos iônicos de quitosana ou alginato, com base no peso total da composição, é empregado para obter as composições de gel da invenção.
[00080] Em uma modalidade, os polissacarídeos aniônicos são ciclizados. Mais preferivelmente, os polissacarídeos aniônicos ciclizados incluem menos do que dez unidades de monômero. Ainda mais preferivelmente, os polissacarídeos ciclizados incluem menos do que seis unidades de monômero.
[00081] Um grupo particularmente útil de polissacarídeos aniônicos ciclizados inclui as ciclodextrinas. Exemplos do grupo de ciclodextrina incluem, porém não são limitados a: α-ciclodextrina, derivados de α-ciclodextrina, β- ciclodextrina, derivados de β-ciclodextrina, Y—ciclodextrina, derivados de Y—ciclodextrina, carboximetil-β-ciclodextrina, carboximetil-etil-β-ciclodextrina, dietil-β-ciclodextrina, dimetil—β—ciclodextrina, metil—β—ciclodextrina, metil—β— ciclodextrina aleatória, glicosil—β—ciclodextrina, maltosil—β— ciclodextrina, hidroxietil—β—ciclodextrina, hidroxipropil—β— ciclodextrina, sulfobutiléter—e—ciclodextrina, e similares e misturas destes. Sulfobutiléter-p-ciclodextrina é um poliassacarídeo aniônico ciclizado preferido de acordo com a presente invenção. É vantajoso que os SECs empregados nesta invenção, incluindo as ciclodextrinas mencionadas acima, sejam formulados a fim de ser não—tóxicos ao mamífero (incluindo a seres humanos) na concentração empregada.
[00082] Quando aqui empregado, o termo "derivativo(s)", quando relacionado a uma ciclodextrina, significa qualquer composto substituído ou de outra maneira modificado que tem a estrutura química característica de uma ciclodextrina suficientemente para funcionar como um componente de ciclodextrina, por exemplo, para realçar a solubilidade e/ou estabilidade de componentes ativos e/ou reduzir efeitos colaterais indesejados dos componentes ativos e/ou para formar complexos inclusivos com componentes ativos, como descrito aqui.
[00083] Embora ciclodextrinas e/ou seus derivados possam ser empregados como SECs, uma modalidade da invenção pode incluir SECs diferente de ciclodextrinas e/ou seus derivados.
[00084] Uma classe preferida e particularmente útil de componente polianiônico inclui derivados de celulose aniônicos. Derivados de celulose aniônicos incluem carboximetil celuloses de metal, carboximetil hidroxietil celuloses de metal e hidroxipropil metil celuloses e derivados destes.
[00085] Os presentes componentes polianiônicos frequentemente podem existir no estado não carregado, por exemplo no estado sólido, em combinação com um contra-íon; em particular, uma pluralidade de cátions discretos aproximadamente igual no número ao número de cargas aniônicas discretas do SEC de forma que o componente polianiônico seja eletricamente neutro quando possui uma carga.
[00086] Desde que os componentes polianiônicos sejam preferivelmente oftalmicamente aceitáveis, é preferido que o metal associado com o componente polianiônico não ionizado seja oftalmicamente aceitável nas concentrações empregadas. Metais particularmente úteis incluem os metais alcalinos, por exemplo, sódio e potássio, os metais alcalinos-terrosos, por exemplo, cálcio e magnésio, e misturas destes.
[00087] Sódio é um metal muito útil capaz de agir como um contra-íon no componente polianiônico não ionizado. Componentes polianiônicos que, nos estados não ionizados, são combinados com cátions diferentes de H+ e cátions de metal podem ser empregados na presente invenção.
[00088] Nessas modalidades da presente invenção que envolvem o uso do SEC, a quantidade de SEC não é de importância crítica, contanto que a solubilidade no componente de agonista alfa-2-adrenérgico seja pelo menos um pouco aumentada e esteja presente em uma quantidade biologicamente aceitável. Tal quantidade deveria ser eficaz para realizar a função desejada ou funções na presente composição e/ou depois da administração ao ser humano ou animal. Em uma modalidade, a quantidade de SEC, preferivelmente o componente polianiônico, é suficiente para ajudar na solubilização de uma quantidade maior, e mais preferivelmente substancialmente todo, o componente de agonista alfa-2-adrenérgico na presente composição. Em uma modalidade útil, a quantidade de componente polianiônico na presente composição está na faixa de cerca de 0,1% a cerca de 30% (p/v) ou mais da composição. Preferivelmente, a quantidade de componente polianiônico está na faixa de cerca de 0,2% (p/v) a cerca de 10% (p/v). Mais preferivelmente, a quantidade de componente polianiônico está na faixa de cerca de 0,2% (p/v) a cerca de 0,6% (p/v).
[00089] Ainda mais preferivelmente, o componente polianiônico é carboximetilcelulose e está presente na composição na faixa de cerca de 0,2% (p/v) a cerca de 0,6% (p/v). Uma concentração particularmente útil de carboximetilcelulose nas presentes composições é cerca de 0,5%.
[00090] Em uma modalidade, os SECs, por exemplo uma carboximetilcelulose, ajudam na solubilização dos componentes de agonista alfa-2-adrenérgico nas composições. Embora os SECs sejam capazes de ajudar na solubilização de componentes de agonista alfa-2-adrenérgico ionizado, é preferível que SECs empregados neste aspecto da invenção ajudem na solubilização de componentes de agonista alfa-2-adrenérgico em pH neutro ou alcalino. Por exemplo, em uma modalidade, carboximetilcelulose pode ajudar a solubilizar componentes de agonista alfa-2- adrenérgico ionizados. Em outra modalidade, carboximetilcelulose pode ajudar a solubilizar substancialmente a população não carregada de componentes de agonista alfa-2-adrenérgico. Em uma modalidade preferida, a carboxilmetilcelulose ajuda a solubilizar tartarato de brimonidina ionizado nas composições. Mais preferivelmente, a carboxilmetilcelulose ajuda a solubilizar uma população substancialmente não carregada de tartarato de brimonidina nas composições.
[00091] As composições da presente invenção podem da mesma forma incluir componentes conservantes ou componentes que ajudam na preservação da composição. Em uma modalidade preferida, as composições reivindicadas contêm pelo menos um componente conservante selecionado a fim de ser efetivo e eficaz como conservantes nas presentes composições, que está na presença de componentes polianiônicos, e preferivelmente têm toxicidade reduzida e mais preferivelmente substancialmente nenhuma toxicidade quando as composições são administradas a um ser humano ou animal.
[00092] Preferivelmente, os presentes componentes conservantes ou componentes que ajudam na preservação da composição, preferivelmente os componentes de agonista alfa-2- adrenérgico aqui, são eficazes em concentrações menores do que cerca de 1% (p/v) ou cerca de 0,8% (p/v) e podem ser 500 ppm (p/v) ou menores, por exemplo, na faixa de cerca de 10 ppm(p/v) ou menores a cerca de 200 ppm(p/v). Componentes conservantes de acordo com a presente invenção preferivelmente incluem, porém não são limitados àqueles que formam complexos com o componente polianiônico em uma extensão menor do que formam o cloreto de benzalcônio.
[00093] Exemplos muito úteis dos componentes presentes conservantes incluem, porém não são limitados a componentes conservantes oxidativos, por exemplo e sem limitação, conservantes oxidativos tais como componentes de óxi-cloro e óxi-borato, peróxidos, persais, perácidos, e similares, e misturas destes. Exemplos específicos de componentes de óxi- cloro úteis como conservantes de acordo com a presente invenção incluem componentes de hipoclorito, por exemplo hipocloritos; componentes de clorato, por exemplo clorato; componentes de perclorato, por exemplo percloratos; e componentes de clorito. Exemplos de componentes de clorito incluem dióxido de cloro estabilizado (SCD), cloritos de metal, tais como metal alcalino e cloritos de metal alcalino terroso, e similares e misturas destes. Clorito de sódio de grau técnico (ou grau de USP) é um componente conservante muito útil. A composição química exata de muitos componentes de clorito, por exemplo, SCD, não é completamente entendida. A fabricação ou produção de certos componentes de clorito é descrita na Patente U.S. McNicholas 3.278.447, que é incorporada em sua totalidade aqui por referência. Exemplos específicos de produtos de SCD úteis incluem aqueles vendidos sob a marca registrada Dura Klor por Rio Linda Chemical Company, Inc., e aqueles vendidos sob a marca registrada Anthium Dioxide by Internacional Dioxide, Inc. Um SCD especialmente útil é um produto vendido sob a marca registrada PuriteD por Allergan, Inc.
[00094] Outros exemplos de componentes conservantes oxidativos incluem componentes de peróxi. Por exemplo, quantidades de traço de componentes de peróxi estabilizados com um estabilizador de peróxido de hidrogênio, tal como dietileno triamina penta(ácido metilenofosfônico) ou ácido 1- hidroxietilideno-1,1-difosfônico, podem ser utilizadas como um conservante para uso em componentes designados para ser empregados no ambiente ocular. Da mesma forma, virtualmente qualquer componente de peróxi pode ser empregado contanto que seja hidrolisado em água para produzir peróxido de hidrogênio. Exemplos de tais fontes de peróxido de hidrogênio, que fornecem uma quantidade de resultante eficaz de peróxido de hidrogênio, incluem decaidrato de perborato de sódio, peróxido de sódio e peróxido de uréia. Foi constatado que ácido peracético, um composto de peróxi orgânico, pode não ser estabilizado utilizando o presente sistema. Veja, por exemplo, Martin e outros Patente U.S. No 5.725.887, a descrição da qual é incorporada em sua totalidade aqui por referência.
[00095] Conservantes diferentes de componentes conservantes oxidativos podem ser incluídos nas composições. A escolha de conservantes pode depender da rotina de administração. Conservantes adequados para composições a ser administradas por uma rotina podem possuir propriedades prejudiciais que impedem sua administração por outra rotina. Para composições nasais e oftálmicas, conservantes preferidos incluem, sem limitação, compostos de amônio quaternários, em particular a mistura de compostos de alquil benzil dimetil amônio e similares genericamente conhecidos como "cloreto de benzalcônio", a mistura compreendendo brometo de deciltrimetilmônio, brometo de dodeci-ltrimetilmônio e brometo de tetradeciltrimetilmônio denominado "cetrimida", BDB, e o conservante poliquatérnio-1 (comercializado sob o nome comercial Poliquad®), e conservantes de biguanida, tal como biguanida de poliexametileno ("PHMB").
[00096] Para composições a ser administradas por inalação, entretanto, o conservante preferido é clorbutol e similares. Outros conservantes que podem ser empregados, especialmente para composições a ser administradas retalmente, incluem ésteres alcalinos de ácido de p-hidroxibenzóico e misturas destes, tal como a mistura de ésteres metílicos, etílicos, propílicos, butílicos e similares que são vendidos sob o "nome comercial Nipastat."
[00097] Em outro amplo aspecto da presente invenção, composições são fornecidas que compreendem um componente de agonista alfa-2-adrenérgico, um componente conservante em uma quantidade eficaz para pelo menos ajudar na preservação, preferivelmente em uma quantidade eficaz para preservar, as composições e um componente de portador líquido. Preferivelmente, os componentes conservantes incluem componentes de óxi-cloro, ou PHMB. Tais compostos devem ser eficazes na prevenção do crescimento de bactérias gram positivas, bactérias gram-negativas, ou fungos e preferivelmente ser tal que eles (1) não substancialmente ou significativamente prejudicialmente afetem os componentes de agonista alfa-2-adrenérgico nas composições ou os pacientes a quem as composições são administradas, e (2) são substancialmente e biologicamente aceitável e quimicamente estáveis. Tais composições de acordo com a presente invenção compreendem um componente de agonista alfa-2-adrenérgico, um componente de óxi-cloro, um composto de amônio quaternário, ou uma biguanida tal como PHMB, e um componente de portador líquido, e preferivelmente são substancialmente livres de ciclodextrinas.
[00098] Os componentes de portador úteis na presente invenção são selecionados por ser não-tóxicos e não ter efeito prejudicial significativo nas presentes composições, no uso das composições ou no ser humano ou animal a quem são administradas as composições.
[00099] Em uma modalidade, o componente de portador é um portador líquido. Em uma modalidade preferida, o componente de portador é um componente de portador aquoso líquido. Um componente de portador líquido aquoso particularmente útil é aquele derivado a partir de solução salina, por exemplo, uma solução salina convencional ou uma solução salina tamponada convencional. O portador líquido aquoso preferivelmente tem um pH na faixa de cerca de 6 a cerca de 9 ou cerca de 10, mais preferivelmente cerca de 6 a cerca de 8, e ainda mais preferivelmente cerca de 7,5. O meio líquido preferivelmente tem um nível de tonicidade oftalmicamente aceitável, por exemplo, de pelo menos cerca de 200 mOsmol/kg, mais preferivelmente na faixa de cerca de 200 a cerca de 400 mOsmol/kg. Em uma modalidade especialmente útil, a osmolaridade ou tonicidade do componente de portador é substancialmente isotônica com referência à tonicidade dos fluidos da superfície do olho, em particular o olho humano.
[00100] Em uma modalidade, os componentes de portador con-tendo os SECs e os componentes de agonista alfa-2- adrenérgico podem ter viscosidades de mais do que cerca de 0,01 centipoise (cps) a 25oC, preferivelmente mais do que cerca de 1 cps a 25oC, ainda mais preferivelmente mais do que cerca de 10 cps a 25oC. Em uma modalidade preferida, a composição tem uma viscosidade de cerca de 50 cps a 25oC e compreende uma solução salina de tampão convencional, uma carboximetilcelulose e tartarato de brimonidina.
[00101] A fim de assegurar que o pH do componente de portador líquido aquoso, e desse modo o pH da composição, está mantido dentro da faixa desejada, o componente de portador líquido aquoso pode incluir pelo menos um componente de tampão. Embora qualquer componente de tampão adequado possa ser empregado, é preferido selecionar um tampão não capaz de emitir uma quantidade significante de gás, tal como dióxido de cloro ou CO2. É preferido que o componente de tampão seja inorgânico. Componentes de tampão de sal de metal alcalino terroso e metal alcalino são vantajosamente empregados na presente invenção.
[00102] Qualquer componente de ajuste de tonicidade oftalmicamente aceitável adequado pode ser empregado, contanto que tal componente ou componentes seja compatível com os outros ingredientes do componente de portador aquoso líquido e não tenham propriedades danosas ou tóxicas que poderiam prejudicar o ser humano ou animal a quem as presentes composições são administradas. Exemplos de componentes de tonicidade úteis incluem cloreto de sódio, cloreto de potássio, manitol, dextrose, glicerina, propileno glicol e misturas destes. Em uma modalidade, o componente de tonicidade é selecionado a partir de sais inorgânicos e misturas destes.
[00103] As presentes composições podem convenientemente ser apresentadas como soluções ou suspensões em líquidos aquosos ou líquidos não-aquosos, ou como emulsões líquidas de óleo em água ou água em óleo. As presentes composições podem incluir um ou mais ingredientes adicionais tal como diluentes, agentes aromatizantes, agentes tensoativos, espessantes, lubrificantes, e similares, por exemplo, tais ingredientes adicionais que são convencionalmente empregados em composições do mesmo tipo geral.
[00104] As presentes composições, na forma de suspensões aquosas, podem incluir excipientes adequados para a fabricação de suspensões aquosas. Tais excipientes são agentes de suspensão, sem limitação incluindo alginato de sódio, goma tragacanto e goma acácia. Agentes de umectação ou dispersão podem incluir um fosfatídeo de ocorrência natural, por exemplo, lecitina, ou produtos de condensação de óxido de etileno com álcoois alifáticos de cadeia longa, por exemplo, heptadecaetileneoxicetanol, ou produtos de condensação de óxido de etileno com ésteres parciais derivados a partir de ácidos graxos e um hexitol tal como monooleato de sorbitol de polioxietileno, ou produtos de condensação de óxido de etileno com ésteres parciais derivados a partir de ácidos graxos e anidridos de hexitol, por exemplo, monooleato de sorbitano de polioxietileno, e similares e misturas destes. Suspensões aquosas deste aspecto da presente invenção podem da mesma forma conter um ou mais agentes de coloração, um ou mais agentes aromatizantes e um ou mais agentes adoçantes, tal como sacarose, sacarina e similares e misturas destes.
[00105] Se as presentes composições são na forma de suspensões oleosas elas podem ser formuladas em um óleo vegetal, por exemplo, azeite de oliva, óleo de gergelim ou óleo de coco, ou em um óleo mineral tal como parafina líquida. Tais suspensões podem conter um agente espessante, por exemplo cera de abelha, parafina dura ou álcool cetílico. Agentes adoçantes, tais como aqueles mencionados acima, e agentes aromatizantes podem ser adicionados para fornecer uma preparação oral saborosa.
[00106] As presentes composições podem alternativamente ser na forma de emulsões de óleo em água. A fase oleosa pode ser um óleo vegetal, por exemplo, azeite de oliva ou óleo de amendoim, ou um óleo mineral, por exemplo, parafina líquida, e similares e misturas destes. Agentes de emulsificação adequados podem ser gomas de ocorrência natural, por exemplo, goma acácia ou goma tragacanto, fosfatídeos de ocorrência natural, por exemplo, lecitina de soja, e ésteres ou ésteres parciais derivados a partir de ácidos graxos e anidridos de hexitol, por exemplo, monooleato de sorbitano, e produtos de condensação dos referidos ésteres parciais com óxido de etileno, por exemplo, monooleato de sorbitano de polioxietileno. As emulsões podem da mesma forma conter agentes adoçantes e aromatizantes.
[00107] As presentes composições, na forma de xaropes e elixires, podem ser formuladas com agentes adoçantes, por exemplo, como descrito em outro lugar aqui. Tais formulações podem da mesma forma conter um demulcente, e agentes aromatizante e colorante.
[00108] O nível de dose específica para qualquer humano particular ou animal depende de uma variedade de fatores incluindo a atividade do componente ativo empregada, a idade, peso corporal, saúde geral, sexo, dieta, tempo de administração, pH da formulação, rotina de administração, taxa de excreção, combinação de droga e a gravidade da condição particular que passa por terapia. Para 5-bromo-6-(2- imidozolin-2-ilamino) quinoxalina, uma dose terapeuticamente eficaz nas presentes composições é liberada em uma concentração menor do que 0,2% (p/v), tal como cerca de 0,15% (p/v) ou cerca de 0,1% (p/v) ou menor. O pH de tais composições é maior do que 7,0; em um aspecto a dose é cerca de 0,15% e o pH é cerca de 7,2; em outro aspecto a dose é cerca de 0,1% e o pH é cerca de 7,7.
[00109] Em um aspecto da invenção, complexos são formados nas presentes composições. Em uma modalidade, os complexos incluem pelo menos uma unidade de monômero de um componente de quinoxalina. Exemplos de componentes de quinoxalina incluem quinoxalina, (2-imidozolin-2-ilamino) quinoxalina, 5-bromo-6-(2-imidozolin-2-ilamino) quinoxalina, sais destes, ésteres destes, outros derivados destes, e similares e misturas destes. Por exemplo, em uma modalidade, um complexo da presente invenção pode incluir uma conjugação de unidades de monômero de 5-bromo-6-(2-imidozolin-2-ilamino) quinoxalina. Em outra modalidade, o complexo pode incluir uma conjugação de unidades de monômero de 5-bromo-6-(2-imidozolin- 2-ilamino) quinoxalina e unidades de monômero de tartarato de brimonidina.
[00110] Em uma modalidade preferida deste aspecto, os complexos da presente invenção são dímeros. Por exemplo, um dímero de acordo com a presente invenção pode incluir uma quinoxalina e um 5-bromo-6-(2-imi-dozolin-2-ilamino) quinoxalina. Preferivelmente, um dímero de acordo com a presente invenção inclui duas unidades de monômero de tartarato de trimonidina.
[00111] Sem desejar limitar este aspecto da invenção a qualquer teoria ou mecanismo de operação, acredita-se que um agente de formação de peróxido ou agente de oxidação forte tal como os componentes conservantes oxidativos, por exemplo componentes de óxi-cloro, peróxidos, persais, perácidos, e similares, e misturas destes pode facilitar a formação dos complexos, preferivelmente complexos de componentes de agonista alfa-2-adrenér-gico. Por exemplo, dímeros de unidades de monômero de tartarato de brimonidina são acreditados ser formados na presença de cloritos, dióxido de cloro preferivelmente estabilizado.
[00112] Além disso, acredita-se que as interações entre os monômeros que servem para manter os monômeros ou subunidades de monômero juntos para formar um complexo, preferivelmente um oligômero e mais preferivelmente um dímero, possam incluir, porém não limitadas à, ligação covalente, ligação iônica, ligação hidrofóbica, ligação eletrostática, ligação de hidrogênio, outras interações químicas e/ou físicas, e similares e combinações destes. Tais complexos podem desassociar-se em líquido, por exemplo, meio líquido aquoso. Em uma modalidade, os monômeros ou subunidades de monômero são mantidos juntos por ligação covalente diferente. Em uma modalidade, os monômeros ou subunidades de monômero são mantidos juntos por forças ou ligação eletrostática.
[00113] Os seguintes exemplos não limitantes ilustram certos aspectos da presente invenção.
[00114] Tartarato de brimonidina tem um pKa de cerca de 7,78. O perfil de solubilidade de pH de tartarato de brimonidina em uma formulação aquosa (Solução Oftálmica) foi estabelecido na faixa de pH de cerca de 5 a cerca de 8 a 23°C. Tabela 1. Será entendido que concentrações de agonistas adrenérgicos diferentes daquelas mostradas podem ser empregadas nas composições da presente invenção, contanto que elas tenham atividade terapêutica. Da mesma maneira, a temperatura pode ser um pouco variada, por exemplo, curvas de solubilidade podem ser realizadas em temperatura ambiente.
[00115] O veículo de formulação foi preparado primeiro dissolvendo-se álcool polivinílico (PVA) em água. O PVA foi adicionado em aproximadamente 1/3 da quantidade total requerida de água purificada com agitação constante. A suspensão foi agitada durante 20 - 30 minutos e em seguida aquecida a 80 - 95oC com agitação constante. A mistura foi removida a partir da fonte de calor dentro de 1 hora depois de ter alcançado a temperatura de 80 - 90°C e agitada durante um adicional de 10 minutos para garantir a homogeneidade (Parte I). Os outros ingredientes da Solução Oftálmica, exceto para tartarato de brimonidina, foram dissolvidos em um recipiente separado com um adicional de 1/3 da quantidade total requerida de água purificada (Parte II). A mistura de PVA (Parte I) foi em seguida quantitativamente transferida para Parte II empregando vários volumes de enxágue de água purificada. A solução foi ajustada ao volume final com água purificada sem ajuste de pH.
[00116] Tartarato de brimonidina foi pesado e transferido para um tubo teste de 10 mL contendo 5 mL do veículo de formulação descrito acima. O pH de cada amostra foi em seguida ajustado para um valor desejado empregando hidróxido de sódio diluído e/ou ácido clorídrico diluído. As amostras foram colocadas em uma prateleira sobre uma placa de agitação e agitadas em alta velocidade para obter mistura uniforme, durante 2 dias; uma divisão foi colocada entre a prateleira e a placa de agitação para prevenir alguma difusão de calor a partir da placa de agitação às amostras. A temperatura do laboratório foi monitorada através do estudo e foi constatada ser 23±1°C.
[00117] Ao término de dois dias de agitação, o valor do pH de cada amostra foi medido, e em seguida aproximadamente 1 mL de cada amostra foi colocado em um tubo de microcentrífuga (polipropileno) e centrifugado a 4.000 rpm durante 10 minutos. O sobrenadante foi filtrado através de uma unidade de filtro de 1μm (Whatman, 13mm, PTFE) . As primeiras 3 - 4 gotas do filtrado foram descartadas; o resto do filtrado foi recebido e diluído quantitativamente com HPLC de fase móvel. A amostra diluída foi em seguida diretamente injetada na coluna de HPLC (Dupont Zorbax, 250mm x 4,6mm, 5 μm) para ensaio de tartarato de brimonidina a fim de quantificar a quantidade de tartarato de brimonidina. Um controle de tartarato de brimonidina a 0,5% foi preparado no mesmo veículo de formulação em pH 6,3 - 6,5 e ensaiado antes (não tratado) e depois da (tratado) centrifugação e filtração. Isto foi feito para avaliar a perda potencial de tartarato de brimonidina nestas duas etapas da preparação de amostra. Para garantir a reprodutibilidade, o estudo foi repetido em dias consecutivos. Tabela I. Tartarato de brimonidina a 0,5% em Solução Oftálmica.
[00118] Os dados de solubilidade para tartarato de brimonidina nos veículos de formulação são apresentados na Tabela II. O resultados mostram que a solubilidade de tartarato de brimonidina é altamente dependente de pH e transportam mais de duas ordens de magnitude sobre a faixa de pH de 5 - 8. A solubilidade diminui nitidamente quando o pH aumenta. Os resultados para os controles tratados e não tratados são muito fechados, sugerindo que a centrifugação e filtração não cause qualquer perda significante de tartarato de brimonidina. Os dois perfis de solubilidade obtidos em dias consecutivos concordam entre si. Tabela II. Solubilidade De Tartarato de Brimonidina Na Solução Oftálmica Sobre a Faixa de pH De 5 A 8.
a Medido depois de agitar durante dois dias antes da retirada da amostra para centrifugação e filtração. b Representa a concentração teórica com base no peso da amostra. A solução de amostra foi clara indicando que todo o tartarato de brimonidina tinha dissolvido. Concentração de tartarato de brimonidina em controle antes da etapa de centrifugação e filtração. d Concentração de tartarato de brimonidina em controle depois da etapa de centrifugação e filtração. e % p/v.
[00119] O efeito do pH na solubilidade de tartarato de brimonidina em formulações líquidas com e sem SECs foi determinado. Particularmente, o efeito da presença ou ausência de várias concentrações de um SEC exemplar, carboximetilcelulose sódica (CMC), na solubilidade de tartarato de brimonidina em várias condições de pH foi determinado. As várias concentrações de CMC testadas com tartarato de Brimonidina foram 0%, 0,056%, 0,17%, 0,5%, 1,5% (p/v), veja Tabela III.
[00120] As amostras testadas da mesma forma continham componentes isotônicos, componentes de tampão e dióxido de cloro estabilizado (FuriteD), Tabela III. Carboximetilcelulose sódica, cloreto de sódio, cloreto de potássio, diidrato de cloreto de cálcio, e hexaidrato de cloreto de magnésio foram grau de USP. Ácido bórico e decaidrato de borato de sódio foram grau de NF. Tabela III
[00121] Cada amostra (1 a 5) foi trazida em vários pontos dentro de uma faixa de valores de pH de cerca de 7 a cerca de 10. Os frascos contendo as soluções de amostra foram colocados em um rotador de laboratório e deixado equilibrar durante quinze dias a 21oC. As soluções de amostra foram filtradas empregando uma seringa de acetato de celulose de polissulfona de 25 mm de diâmetro tipo filtro com 0,45 Dm de tamanho de poro. As soluções filtradas foram ensaiadas quanto a quantidade de tartarato de brimonidina na solução.
[00122] HPLC convencional e técnicas de detecção foram empregadas para detectar e determinar as concentrações de tartarato de brimonidina solúvel. Veja Tabela IV. A solubilidade é plotada junto ao pH para cada concentração de CMC. Os pontos de dados experimentais foram ajustados em uma equação de Henderson-Hasselbalch modificada empregando uma rotina de quadrados menores não linear (versão de Deltagraph 4,0 DeltaPoint, Inc.), Veja Figura. 1. Os valores de R5 mostram o ajuste estatístico entre os valores experimentais e a equação teórica a ser maior do que 0,991. Tabela IV: Solubilidade de tartarato de Brimonidina (% p/v)
[00123] A figura 1 mostra claramente que a solubilidade de tartarato de brimonidina aumenta em um determinado pH como uma função de concentração de CMC. Por exemplo, em pH 7,5, a amostra com 0% de CMC resultou em 1000 ppm de tartarato de Brimonidina; 0,056% de CMC, 1300 ppm; 0,17% de CMC, 1300 ppm; e 0,5%, 1600 ppm. Em pH 7,5, a amostra com 1,5% de CMC resultou em cerca de 1400 ppm, que é menor do que aquela de uma solução similar com CMC a 0,5%. Não está claro neste ponto qual pode ser a causa desta observação. Entretanto, tartarato de brimonidina é mais solúvel na solução com uma CMC de 1,5% do que nenhuma CMC.
[00124] Entretanto, tartarato de brimonidina é claramente mais solúvel em solução com uma CMC de 1,5% do que nenhuma CMC.
[00125] CMC é da mesma forma eficaz para a solubilizar tartarato de Brimonidina em um ambiente biológico, por exemplo o ambiente biológico da córnea.
[00126] Tartarato de brimonidina é adicionado em um tubo teste contendo uma composição incluindo clorito. O tubo teste foi permitido equilibrar durante dez dias. Amostras obtidas a partir do tubo teste são analisadas por HPLC empregando uma coluna de exclusão de tamanho na presença ou ausência de um chaotrope, tal como uréia. É observado que uma porção das unidades de monômero de tartarato de brimonidina tem conjugado para formar dímeros, como medido pelos pesos moleculares aparentes de brimonidina na solução.
[00127] Tartarato de brimonidina foi formulado para liberação tópica oftálmica em pH 7,2 e uma concentração de 0,15% (p/v) em uma solução aquosa contendo PURITE® como um conservante. A eficácia hipotensiva ocular desta formulação foi determinada em indivíduos clínicos humanos, e comparada à eficácia de ALPHAGAN®, que contém tartarato de brimonidina a 0,2% formulado em solução tópica oftálmica aquosa em pH 6,5 em um tampão de citrato com 0,05% de cloreto de benzalcônio como um conservante. Uma terceira formulação contendo 0,2% (p/v) de tartarato de brimonidina e um conservante de PURITE® foi da mesma forma incluído como um controle.
[00128] 381 indivíduos humanos diagnosticados com glaucoma ou hipertensão ocular foram aleatoriamente ensaiados para tomar uma das três formulações em uma dosagem de uma gota em cada olho afetado três vezes por dia durante 12 meses. A pressão intraocular (IOP) é medida em duas semanas, seis semanas, 3 meses, 6 meses, 9 meses e 12 meses.
[00129] Ao término do período de 12 meses, os resultados indicaram que não houve nenhuma diferença significante na eficácia hipotensiva de uma solução contendo 25% menos do ingrediente ativo (0,15% de brimonidina) quando formulada em pH 7,2, quando comparada ao produto de ALPHAGAN® (brimonidina a 0,2% formulado em pH 6,5). Entretanto, esses indivíduos que receberam brimonidina a 0,15% relataram uma incidência mais baixa de efeitos colaterais, tais como conjuntivite alérgica, secura oral, hiperemia conjuntival, e descarga do olho, quando comparada a concentração mais alta (0,2%) de brimonidina. Estas diferenças não são vistas nas soluções de brimonidina a 0,2% contendo PURITE®, e desse modo não são atribuíveis à diferença em conservantes.
[00130] Uma solução de tartarato de brimonidina a 0,1% em pH 7,7 foi feita como segue: Tabela V: Solução Oftálmica a 0,1% de Brimonidina-Purita
[00131] Uma solução oftálmica aquosa tópica compreendendo 0,1% (p/v) de tartarato de brimonidina formulada em pH 7,7 ("BP 0,1%") como indicado no Exemplo 5, foi feita para testar em indivíduos clínicos humanos sofrendo de IOP alto, e a eficácia desta solução comparada à eficácia de ALPHAGAN®, (tartarato de brimonidina a 0,2% formulado em uma solução tópica oftálmica aquosa tamponada por citrato em pH 6,5 com 0,05% de cloreto de benzalcônio como um conservante).
[00132] 433 indivíduos clínicos humanos foram aleatoriamente escolhidos para receber uma gota de uma das duas soluções no olho afetado três vezes por dia. Pressão intra-ocular é medida em referência (dia 0), três semanas, seis semanas, e 3 meses.
[00133] Os resultados foram como segue:
[00134] A IOP em 0 hora foi idêntica para os dois grupos (24,7 mm Hg), e as IOPs na hora 2 (~ 23 mm Hg) e hora 8 (~ 22 mm Hg) foram similares para os dois grupos.
[00135] Faixas de IOP médias para leituras pós- referência em 0 hora sobre o período de seguimento de 3 meses foram: 20,7 a 21,4 mm Hg (BP 0,1%) 21,0 a 21,7 mm Hg (ALPHAGAN®)
[00136] Os resultados em pontos de tempo pós-referência foram, em geral, similares entre os grupos de tratamento. No mês 3, faixas para as médias de grupo de IOP diurna em horas 0, 2, e 8 foram como segue: 17,2 a 21,4 mm Hg (BP 0,1%) 17,6 a 21,7 mm Hg (ALPHAGAN®)
[00137] Este estudo mostra que, quando entre o BP 0,1% e as formulações de ALPHAGAN®, os indivíduos experimentaram eficácia substancialmente equivalente durante o período do estudo. Estes resultados foram completamente inesperados. Entretanto, provavelmente porque o BP 0,1% continha apenas 50% da quantidade do ingrediente ativo, tartarato de brimonidina, da formulação de ALPHAGAN®, o número de incidentes relatados de efeitos colaterais tais como secura oral, astenia, e prurido de olho foram mais baixos no grupo de BP 0,1% do que no grupo de ALPHAGAN®.
[00138] Outra variação da formulação de tartarato de brimonidina a 0,1% em pH 7,7 pode ser feita de acordo com a seguinte tabela:
[00139] Outra variação da formulação de tartarato de brimonidina a 0,1% em pH 7,7 pode ser feita de acordo com a seguinte tabela:
[00140] Será entendido que sais de sódio podem ser substituídos por sais de outros cátions de metal, tal como potássio ou cálcio. Se presentes, os agentes de tonicidade podem ser sais ou realçadores de tonicidade não-iônicos, tal como glicerina. Tampões podem ser feitos com qualquer agente tendo a capacidade de tamponamento apropriada para o pH escolhido. As concentrações determinadas acima são por meio de exemplo, e não para limitar a invenção em seus aspectos mais amplos.
[00141] Enquanto esta invenção foi descrita com respeito a vários exemplos específicos e modalidades, será entendido que a invenção não está limitada a isso e que ela pode ser praticada com variação considerável dentro do escopo das seguintes reivindicações por aqueles versados na técnica. 1/1
Claims (4)
1. Composição oftálmica aquosa para uso no tratamento de glaucoma ou pressão intraocular elevada caracterizada por compreender uma solução compreendendo 0,1% (p/v) de tartarato de brimonidina e um componente de realce de solubilidade não- iônico (SEC) compreendendo 0,5% (p/v) de carboximetilcelulose, em que a composição tem um pH de 7,7.
2. Composição, de acordo com a reivindicação 1, caracterizada por a composição compreender adicionalmente um conservante selecionado a partir do grupo consistindo em um conservante de amônio quaternário, um conservante oxidativo, e um conservante de biguanida, sendo o conservante de amônio quaternário selecionado a partir de poliquatérnio-1, cloreto de benzalcônio, cetrimida, brometo de benzododecinium (BDB); em que o conservante oxidativo é selecionado a partir do grupo consistindo em um conservante de complexo de óxicloro estabilizado, dióxido de cloro estabilizado (SCD), e perborato de sódio decahidratado; e o conservante de biguanida sendo selecionado a partir de polihexametileno biguanida (PHMB).
3. Composição oftálmica aquosa, de acordo com a reivindicação 1, caracterizada por ser usada para tratar glaucoma ou reduzir a pressão intraocular.
4. Composição oftálmica aquosa, de acordo com a reivindicação 1, caracterizada por compreender uma solução compreendendo 0,10% (p/v) de tartarato de brimonidina, 0,5% (p/v) de carboximetilcelulose e um conservante de amônio quaternário em um pH de 7,7.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US10/928,906 | 2004-08-27 | ||
| US10/928,906 US20050026924A1 (en) | 2000-07-14 | 2004-08-27 | Compositions containing alpha-2-adrenergic agonist components |
| PCT/US2005/029707 WO2006026215A1 (en) | 2004-08-27 | 2005-08-17 | Compositions containing alpha-2-adrenergic agonist components |
Publications (4)
| Publication Number | Publication Date |
|---|---|
| BRPI0514723A BRPI0514723A (pt) | 2008-06-24 |
| BRPI0514723A8 BRPI0514723A8 (pt) | 2018-05-08 |
| BRPI0514723B1 true BRPI0514723B1 (pt) | 2020-12-22 |
| BRPI0514723B8 BRPI0514723B8 (pt) | 2021-05-25 |
Family
ID=35589384
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI0514723A BRPI0514723B8 (pt) | 2004-08-27 | 2005-08-17 | composições contendo componentes de agonista alfa-2-adrenérgico |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US20050026924A1 (pt) |
| JP (2) | JP2008511628A (pt) |
| AU (1) | AU2005280259A1 (pt) |
| BR (1) | BRPI0514723B8 (pt) |
| CA (1) | CA2578784C (pt) |
| MX (1) | MX2007002383A (pt) |
| NZ (1) | NZ599669A (pt) |
| WO (1) | WO2006026215A1 (pt) |
Families Citing this family (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20100203165A1 (en) * | 2008-08-01 | 2010-08-12 | Gerald Horn | Compositions and methods for treatment of disorders or conditions of the eye |
| US12246013B2 (en) | 2008-08-01 | 2025-03-11 | Eye Therapies Llc | Vasoconstriction compositions and methods of use |
| US8338421B2 (en) | 2008-08-01 | 2012-12-25 | Alpha Synergy Development, Inc. | Compositions and methods for reversing rebound hyperemia |
| US8987270B2 (en) | 2009-07-27 | 2015-03-24 | Eye Therapies Llc | Formulations of selective alpha-2 agonists and methods of use thereof |
| EP2555748A2 (en) * | 2010-04-07 | 2013-02-13 | Allergan, Inc. | Combinations of preservatives for ophthalmic compositions |
| JP7217022B2 (ja) | 2017-03-23 | 2023-02-02 | グレイバグ ビジョン インコーポレイテッド | 眼障害の治療のための薬物及び組成物 |
| JP7170436B2 (ja) * | 2017-06-28 | 2022-11-14 | 千寿製薬株式会社 | 水溶性高分子を含む点眼剤 |
| WO2019112030A1 (ja) * | 2017-12-08 | 2019-06-13 | 千寿製薬株式会社 | 水溶性高分子を含む水性液剤 |
| WO2020071297A1 (ja) * | 2018-10-01 | 2020-04-09 | 千寿製薬株式会社 | 水性液剤 |
| JP6901619B2 (ja) * | 2019-09-30 | 2021-07-14 | 千寿製薬株式会社 | 水性液剤 |
| JP6797992B1 (ja) * | 2019-09-30 | 2020-12-09 | 千寿製薬株式会社 | 水性液剤 |
| GR1010024B (el) | 2020-05-06 | 2021-06-01 | Φαρματεν Α.Β.Ε.Ε. | Φαρμακευτικο σκευασμα ελευθερο συντηρητικου για οφθαλμικη χορηγηση που περιλαμβανει βριμονιδινη |
| JP7002692B2 (ja) * | 2020-11-18 | 2022-02-04 | 千寿製薬株式会社 | 水性液剤 |
Family Cites Families (35)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE1154119B (de) * | 1961-11-30 | 1963-09-12 | Boehringer Sohn Ingelheim | Verfahren zur Herstellung von 2-(2', 4', 6'-Trimethylbenzyl)-1, 3-diazacyclopenten-(2) und seinen Salzen |
| US3278447A (en) * | 1963-12-02 | 1966-10-11 | Cloro Bac Products Inc | Process for stabilizing chlorine dioxide solution |
| BE795970A (fr) * | 1972-02-29 | 1973-08-27 | Pfizer | Nouveaux derives de quinoleine, quinoxaline et quinazoline er composition pharmaceutiques les contenant |
| US3994828A (en) * | 1973-06-07 | 1976-11-30 | Dynapol Corporation | Nonabsorbable antioxidant |
| US4499077A (en) * | 1981-02-03 | 1985-02-12 | Stockel Richard F | Anti-microbial compositions and associated methods for preparing the same and for the disinfecting of various objects |
| US4407791A (en) * | 1981-09-28 | 1983-10-04 | Alcon Laboratories, Inc. | Ophthalmic solutions |
| US4530920A (en) * | 1983-11-07 | 1985-07-23 | Syntex (U.S.A.) Inc. | Nonapeptide and decapeptide analogs of LHRH, useful as LHRH agonist |
| US4806556A (en) * | 1985-12-12 | 1989-02-21 | Regents Of The University Of Minnesota | Gut-selective opiates |
| US5719197A (en) * | 1988-03-04 | 1998-02-17 | Noven Pharmaceuticals, Inc. | Compositions and methods for topical administration of pharmaceutically active agents |
| US5607698A (en) * | 1988-08-04 | 1997-03-04 | Ciba-Geigy Corporation | Method of preserving ophthalmic solution and compositions therefor |
| CA2003198C (en) * | 1988-11-29 | 1995-03-21 | Anthony J. Dziabo, Jr. | Aqueous ophthalmic solutions and method for preserving same |
| US5202128A (en) * | 1989-01-06 | 1993-04-13 | F. H. Faulding & Co. Limited | Sustained release pharmaceutical composition |
| US5352796A (en) * | 1989-10-30 | 1994-10-04 | The Salk Institute For Biological Studies | Amino acids useful in making GnRH analogs |
| US5021416A (en) * | 1989-10-31 | 1991-06-04 | Allergan, Inc. | Method for using (2-imidazolin-2-ylamino) quinoxalines to reduce or maintain intraocular pressure |
| US5215991A (en) * | 1990-01-26 | 1993-06-01 | Allergan, Inc. | Combination of selective alpha-adrenergic agonists and Na+ /H+ ex |
| US5091528A (en) * | 1990-09-12 | 1992-02-25 | Allergan, Inc. | 6- or 7- (2-imino-2-imidazolidine)-1,4-benzoxazines as α adrenergic agents |
| US5459133A (en) * | 1992-06-05 | 1995-10-17 | Telor Ophthalmic Pharmaceuticals, Inc. | Methods and products for treating presbyopia |
| JP3527256B2 (ja) * | 1992-12-09 | 2004-05-17 | ロート製薬株式会社 | 抗アレルギー点眼剤 |
| JP3683908B2 (ja) * | 1993-10-13 | 2005-08-17 | アラーガン、インコーポレイテッド | (2−イミダゾリン−2−イルアミノ)キノキサリン誘導体の使用方法 |
| FI962493L (fi) * | 1993-12-17 | 1996-07-26 | Procter & Gamble | Alfa-2-adrenoseptoriagonisteina käyttökelpoisia 6-(2-imidatsolinyyliamino)kinoksaliiniyhdisteitä |
| US5994110A (en) * | 1995-02-10 | 1999-11-30 | Mosbach; Klaus | Methods for direct synthesis of compounds having complementary structure to a desired molecular entity and use thereof |
| IL114193A (en) * | 1994-06-20 | 2000-02-29 | Teva Pharma | Ophthalmic pharmaceutical compositions based on sodium alginate |
| ZA965837B (en) * | 1995-07-11 | 1997-01-31 | Merck & Co Inc | A triazolylmethyl-indole ethylamine bisulfate salt |
| WO1998010758A1 (en) * | 1996-09-13 | 1998-03-19 | The Regents Of The University Of California | Methods for treatment of retinal diseases |
| EP0834308A1 (en) * | 1996-09-30 | 1998-04-08 | LG Chemical Limited | Ophthalmic formulation for treating myopia comprising dopamine agonist and cyclodextrin |
| JP2002523475A (ja) * | 1998-09-02 | 2002-07-30 | アラーガン・セイルズ・インコーポレイテッド | 防腐したシクロデキストリン含有組成物 |
| WO2004073708A1 (en) * | 1998-12-17 | 2004-09-02 | Dean Thomas R | Brinzolamide and brimonidine for treating ocular conditions |
| US6166012A (en) * | 1999-07-30 | 2000-12-26 | Allergan Sales, Inc. | Antibiotic compositions and method for using same |
| RU2311928C2 (ru) * | 2000-07-14 | 2007-12-10 | Аллерган Инк. | Композиции, содержащие альфа-2-адренергические агонисты |
| CA2416169C (en) * | 2000-07-14 | 2008-09-23 | Allergan, Inc. | Compositions containing therapeutically active components having enhanced solubility |
| US20020198210A1 (en) * | 2001-05-03 | 2002-12-26 | Allergan Sales Inc. | Alpha-2-adrenergic agonist/fatty acid compositions |
| US20030165545A1 (en) * | 2002-01-30 | 2003-09-04 | Allergan, Inc. | Ophthalmic compositions including oil-in-water emulsions, and methods for making and using same |
| US7030149B2 (en) * | 2002-04-19 | 2006-04-18 | Allergan, Inc. | Combination of brimonidine timolol for topical ophthalmic use |
| US20040185068A1 (en) * | 2003-03-18 | 2004-09-23 | Zhi-Jian Yu | Self-emulsifying compositions, methods of use and preparation |
| US20040191332A1 (en) * | 2003-03-27 | 2004-09-30 | Allergan, Inc. | Preserved ophthalmic compositions |
-
2004
- 2004-08-27 US US10/928,906 patent/US20050026924A1/en not_active Abandoned
-
2005
- 2005-08-17 CA CA2578784A patent/CA2578784C/en not_active Expired - Lifetime
- 2005-08-17 WO PCT/US2005/029707 patent/WO2006026215A1/en not_active Ceased
- 2005-08-17 AU AU2005280259A patent/AU2005280259A1/en not_active Abandoned
- 2005-08-17 NZ NZ599669A patent/NZ599669A/xx not_active IP Right Cessation
- 2005-08-17 MX MX2007002383A patent/MX2007002383A/es not_active Application Discontinuation
- 2005-08-17 BR BRPI0514723A patent/BRPI0514723B8/pt active IP Right Grant
- 2005-08-19 JP JP2007530000A patent/JP2008511628A/ja active Pending
-
2012
- 2012-08-16 JP JP2012180411A patent/JP2012246304A/ja active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| CA2578784A1 (en) | 2006-03-09 |
| JP2008511628A (ja) | 2008-04-17 |
| WO2006026215A1 (en) | 2006-03-09 |
| BRPI0514723B8 (pt) | 2021-05-25 |
| MX2007002383A (es) | 2007-05-15 |
| US20050026924A1 (en) | 2005-02-03 |
| AU2005280259A1 (en) | 2006-03-09 |
| BRPI0514723A8 (pt) | 2018-05-08 |
| JP2012246304A (ja) | 2012-12-13 |
| BRPI0514723A (pt) | 2008-06-24 |
| CA2578784C (en) | 2015-02-17 |
| NZ599669A (en) | 2013-11-29 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2311928C2 (ru) | Композиции, содержащие альфа-2-адренергические агонисты | |
| RU2291685C2 (ru) | Композиции, содержащие терапевтически активные компоненты, обладающие повышенной растворимостью | |
| AU2001273269A1 (en) | Compositions containing alpha-2-adrenergic agonist components | |
| JP2012246304A (ja) | α−2−アドレナリンアゴニスト成分を含有する組成物 | |
| US20200069576A1 (en) | Compositions containing alpha-2-adrenergic agonist components | |
| US20040214829A1 (en) | Compositions containing alpha-2-adrenergic agonist components | |
| US20040219219A1 (en) | Compositions containing alpha-2-adrenergic agonist components | |
| AU2011250793B2 (en) | Compositions containing alpha-2-adrenergic agonist components | |
| JP2004528369A (ja) | 向上した薬物動態特性を有する組成物 | |
| CA2474280C (en) | Compositions containing alpha-2-adrenergic agonist components | |
| AU2007202599B2 (en) | Compositions containing alpha-2-adrenergic agonist components | |
| AU2005220199B2 (en) | Compositions containing alpha-2-adrenergic agonist components |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B06F | Objections, documents and/or translations needed after an examination request according [chapter 6.6 patent gazette] | ||
| B07D | Technical examination (opinion) related to article 229 of industrial property law [chapter 7.4 patent gazette] | ||
| B07E | Notification of approval relating to section 229 industrial property law [chapter 7.5 patent gazette] | ||
| B07A | Application suspended after technical examination (opinion) [chapter 7.1 patent gazette] | ||
| B09B | Patent application refused [chapter 9.2 patent gazette] | ||
| B12B | Appeal against refusal [chapter 12.2 patent gazette] | ||
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] |
Free format text: PRAZO DE VALIDADE: 10 (DEZ) ANOS CONTADOS A PARTIR DE 22/12/2020, OBSERVADAS AS CONDICOES LEGAIS. |
|
| B16C | Correction of notification of the grant [chapter 16.3 patent gazette] |
Free format text: PRAZO DE VALIDADE: 20 (VINTE) ANOS CONTADOS A PARTIR DE 17/08/2005 OBSERVADAS AS CONDICOES LEGAIS. PATENTE CONCEDIDA CONFORME ADI 5.529/DF |