Waterstofsulfide
Waterstofsulfide (H2S), soms nog zwavelwaterstof genoemd, is een sterk ruikend giftig gas dat vooral bekend is als de oorzaak van de geur van rotte eieren. Het ontstaat bij de rotting van vele zwavelhoudende organische stoffen, zoals eiwitten (die cysteïne en methionine bevatten). Het kan al in zeer lage concentraties door de geur worden waargenomen, maar bij langdurige blootstelling of hoge concentraties gaat de intensiteit van de geurgevoeligheid achteruit. Door de giftigheid ervan is het inademen van ook lage concentraties waterstofsulfide gedurende langere tijd gevaarlijk.
| Waterstofsulfide | ||||||
|---|---|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||||
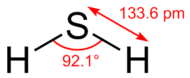
| ||||||
Structuurformule van waterstofsulfide
| ||||||

| ||||||
Molecuulmodel van waterstofsulfide
| ||||||
| Algemeen | ||||||
| Molecuulformule | H2S | |||||
| IUPAC-naam | waterstofsulfide | |||||
| Andere namen | zwavelwaterstof | |||||
| Molmassa | 34,08088 g/mol | |||||
| SMILES | S
| |||||
| InChI | 1S/H2S/h1H2
| |||||
| CAS-nummer | 7783-06-4 | |||||
| EG-nummer | 231-977-3 | |||||
| PubChem | 402 | |||||
| Wikidata | Q170591 | |||||
| Beschrijving | Kleurloos, sterk geurend gas | |||||
| Vergelijkbaar met | dimethylsulfide | |||||
| Waarschuwingen en veiligheidsmaatregelen | ||||||
| ||||||
| H-zinnen | H220 - H280 - H330 - H400 | |||||
| EUH-zinnen | geen | |||||
| P-zinnen | P210 - P260 - P273 - P284 - P310 - P410+P403 | |||||
| MAC-waarde | 2,3 mg/m³ | |||||
| Fysische eigenschappen | ||||||
| Aggregatietoestand | gasvormig | |||||
| Kleur | kleurloos | |||||
| Dichtheid | 1,5392 × 10−3 g/cm³ | |||||
| Smeltpunt | −85,5 °C | |||||
| Kookpunt | −60,33 °C | |||||
| Vlampunt | −82,4 °C | |||||
| Dampdruk | 1,79 × 106 Pa | |||||
| Oplosbaarheid in water | 3,6 g/L | |||||
| Slecht oplosbaar in | water | |||||
| Geometrie en kristalstructuur | ||||||
| Dipoolmoment | 0,97 D | |||||
| Evenwichtsconstante(n) | Kz1 = 8,9 × 10−8 pKz1=7,05 Kz2 = 1,1 × 10−12 pKz2=11,96 [1] | |||||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||||
| ||||||
Waterstofsulfide komt voor opgelost in grondwater, in 'zuur' aardgas en ook in darmgassen, onder meer als afbraakproduct van uien en knoflook.
Het komt in grote hoeveelheden vrij bij het ontzwavelen van aardolieproducten en industriële afvalgassen met behulp van het clausproces.
Synthese
bewerkenWaterstofsulfide kan in het laboratorium bereid worden door het voorzichtig druppelen van een sterk zuur (zoals zwavelzuur of waterstofchloride) op een sulfide, zoals ijzer(II)sulfide:
Vroeger werd hiervoor het toestel van Kipp gebruikt. Tegenwoordig wordt dit gedaan in een drukkolf of wordt het gas in een gascilinder aangekocht.
Eigenschappen
bewerkenWaterstofsulfide is een zwak tweeprotisch anorganisch zuur, dat matig tot slecht oplosbaar is in water. De eerste protische dissociatie, waarvan de pKa 6,9 bedraagt, levert het waterstofsulfide-anion (HS−):
Het sulfide-anion bestaat enkel maar in sterk basische oplossingen. Indien metaalionen in zo'n oplossing aanwezig zijn, ontstaan neerslagen van de overeenkomstige sulfidezouten.
In gasvormige toestand is het iets zwaarder dan lucht. Een mengsel van waterstofsulfide met lucht is een explosief mengsel. Het brandt in zuivere zuurstof met een blauwe vlam, onder vorming van zwaveldioxide en water:
Waterstofsulfide bezit reducerende eigenschappen: het wordt zowel op industriële als laboratoriumschaal gebruikt om organische aziden te reduceren naar de overeenkomstige amines.
Vloeibaar waterstofsulfide
bewerkenHet kookpunt van waterstofsulfide ligt een stuk lager dan dat van water. De oorzaak daarvan is dat de waterstofbrug tussen zwavel en waterstof veel zwakker is dan die met zuurstof. De vloeistof kan gebruikt worden als oplosmiddel, maar dit gedraagt zich erg verschillend van water. De elektrische geleidbaarheid is bijzonder laag omdat er weinig auto-ionisatie optreedt. Zoiets als de autoprotolyse van water is er dus niet of nauwelijks. De stof gedraagt zich daardoor meer als een (polair) organisch oplosmiddel dan als een waterachtig oplosmiddel. Vloeibaar waterstofsulfide lost voornamelijk organische verbindingen op, in plaats van ionogene zoutachtige verbindingen.[2]
Toepassingen
bewerkenHoewel tegenwoordig de giftigheid van de verbinding een beletsel voor het gebruik vormt, is tot het eind van de jaren 60 van de 20e eeuw in de kwalitatieve analyse gebruikgemaakt van het H2S-systeem om vast te stellen met welk metaalion men te doen had.
In 2010 werd in de Verenigde Staten en Groot-Brittannië een stijging waargenomen van het gebruik van waterstofsulfide als zelfmoordgas. Interpol waarschuwde ervoor dat het gas ook gevaarlijk kan zijn voor hulpdiensten.
Uit wetenschappelijk onderzoek is bekend dat waterstofsulfide in kleine hoeveelheden aangemaakt wordt in veel celtypen van het lichaam. Het speelt onder meer een rol in het reguleren van de bloeddruk en het afremmen van ontstekingsprocessen. Bovendien werd duidelijk dat H2S het lichaam kan helpen de zuurstofvraag te verlagen, waardoor het lichaam 90% minder energie nodig heeft. Onderzoek aan de Rijksuniversiteit Groningen wees uit dat waterstofsulfide onder andere beschermt tegen oxidatieve stress, een factor die een belangrijke rol speelt bij ouderdomsziekten. Ook werd geconcludeerd dat H2S bescherming kan bieden bij zuurstofgebrek, zoals bijvoorbeeld tijdens een hart- of niertransplantatie, of in het geval van een hoge bloeddruk.[3]
Toxicologie en veiligheid
bewerkenDe exacte giftige werking van waterstofsulfide is onbekend, maar men vermoedt dat het gas hemoglobine inactiveert. De volgende effecten komen voor wanneer een mens aan opklimmende concentraties wordt blootgesteld:
- 0,0005 ppm: de geurdrempel[bron?]
- < 1,6 ppm: geen negatieve effecten bij een blootstelling van acht uur per dag
- 10–20 ppm: laagste concentratie waarbij oogirritatie kan ontstaan
- 50–100 ppm: schade aan de ogen
- 100–150 ppm: reukorgaan verlamd na een paar keer ademhalen en de geur wordt niet meer waargenomen
- 320–530 ppm: optreden van longembolie met mogelijk fatale consequenties
- 530–1000 ppm: beïnvloedt het centraal zenuwstelsel, vlugge ademhaling
- 800 ppm: dodelijk voor 50% van de mensen bij 5 minuten blootstelling
- > 1000 ppm: onmiddellijke bewusteloosheid en uitval van het ademhalingsapparaat, soms na één keer ademhalen
Zie ook
bewerkenExterne links
bewerken- waterstofsulfide - International Chemical Safety Card
- (en) MSDS van waterstofsulfide
- (en) Gegevens van waterstofsulfide in de GESTIS-stoffendatabank van het IFA
- ↑ NVON-commissie. (2004). Tabel 49: Zuur- en baseconstanten BINAS havo/vwo (5e ed.) – Wolters-Noordhof (Groningen) ISBN 9001893805
- ↑ (en) Moeller, Therald (1952). Inorganic Chemistry. Wiley & Sons, p. 360.
- ↑ Snijder, P.M. Hydrogen sulfide: Protective properties in models of disease (2014)



