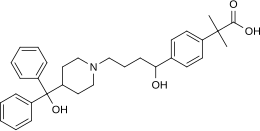
Feksofenadin
| |
|---|---|
| |
| Nama sistematis (IUPAC) | |
| (±)-4-[1-Hidroksi-4-[4-(hidroksidifenilmetil)-1-piperidinil]-butil]-α, α-dimetil asam benzenaasetat | |
| Data klinis | |
| Nama dagang | Allegra, dll |
| AHFS/Drugs.com | monograph |
| MedlinePlus | a697035 |
| Data lisensi | US Daily Med:pranala |
| Kat. kehamilan | B2(AU) |
| Status hukum | Apotek saja (S2) (AU) OTC (CA) P (UK) OTC (US) |
| Rute | Oral |
| Data farmakokinetik | |
| Bioavailabilitas | 30–41%[1] |
| Ikatan protein | 60–70%[2] |
| Metabolisme | Hati (≤5% dari dosis)[2] |
| Waktu paruh | 14,4 jam |
| Ekskresi | Feses (~80%) dan urin (~10%) sebagai obat yang tidak berubah[2] |
| Pengenal | |
| Nomor CAS | 83799-24-0 |
| Kode ATC | R06AX26 |
| PubChem | CID 3348 |
| Ligan IUPHAR | 4819 |
| DrugBank | DB00950 |
| ChemSpider | 3231 |
| UNII | E6582LOH6V |
| KEGG | D07958 |
| ChEBI | CHEBI:5050 |
| ChEMBL | CHEMBL914 |
| Data kimia | |
| Rumus | C32H39NO4 |
| |
Feksofenadin[3] adalah obat antihistamin yang digunakan dalam pengobatan gejala alergi, seperti rinitis alergi dan urtikaria.[4]
Secara terapeutik, feksofenadin adalah penghambat H1 perifer selektif. Obat ini diklasifikasikan sebagai antihistamin generasi kedua karena kurang mampu melewati sawar darah otak dan menyebabkan sedasi, dibandingkan antihistamin generasi pertama.[5][6]
Obat ini dipatenkan pada tahun 1979 dan mulai digunakan secara medis pada tahun 1996.[7] Obat ini ada dalam Daftar Obat Esensial Organisasi Kesehatan Dunia.[8] Feksofenadin telah diproduksi dalam bentuk generik sejak 2011.[9]
Sejarah
[sunting | sunting sumber]Agen antihistamin yang lebih tua, yakni terfenadin ditemukan dimetabolisme menjadi asam karboksilat terkait, yakni feksofenadin. Feksofenadin ditemukan mempertahankan seluruh aktivitas biologis induknya, sekaligus memberikan lebih sedikit efek samping pada pasien, sehingga terfenadin digantikan di pasaran oleh metabolitnya.[10] Feksofenadin awalnya disintesis pada tahun 1993 oleh perusahaan bioteknologi Sepracor yang berbasis di Massachusetts, yang kemudian menjual hak pengembangannya kepada Hoechst Marion Roussel (sekarang bagian dari Sanofi-Aventis), dan kemudian disetujui oleh Badan Pengawas Obat dan Makanan Amerika Serikat (FDA) pada tahun 1996. Albany Molecular Research Inc. (AMRI) memegang hak paten atas zat antara dan produksi feksofenadin HCl, bersama dengan Roussel. Sejak saat itu, obat ini telah mencapai status obat blockbuster dengan penjualan global sebesar US$1,87 miliar pada tahun 2004 (dengan $1,49 miliar berasal dari Amerika Serikat). AMRI menerima pembayaran royalti dari Aventis yang memungkinkan pertumbuhan AMRI.[butuh rujukan]
Pada bulan Januari 2011, FDA menyetujui penjualan feksofenadin yang dijual bebas di Amerika Serikat, dan versi Sanofi Aventis tersedia pada bulan Maret 2011.[11] Pada bulan Desember 2020, MHRA mengklasifikasi ulang feksofenadin dari resep hanya untuk memungkinkan penjualan umum di Britania Raya.[12]
kegunaan dalam Medis
[sunting | sunting sumber]Feksofenadin digunakan untuk meredakan gejala fisik yang berhubungan dengan rinitis alergi musiman dan untuk pengobatan gatal-gatal, termasuk urtikaria kronis.[5] Obat ini tidak menyembuhkan, melainkan mencegah bertambah parahnya rinitis alergi dan urtikaria idiopatik kronis, serta mengurangi keparahan gejala yang terkait dengan kondisi tersebut, meredakan bersin berulang, pilek, mata atau kulit gatal, dan kelelahan tubuh secara umum. Dalam ulasan tahun 2018, feksofenadin bersama dengan levosetirizin, desloratadin, dan setirizin, disebut-sebut sebagai obat yang aman digunakan untuk individu dengan sindrom QT panjang bawaan.[13]
Efikasi
[sunting | sunting sumber]Untuk pengobatan rinitis alergi, feksofenadin sama efektifnya dengan setirizin, namun dikaitkan dengan rasa kantuk yang lebih sedikit dibandingkan setirizin.[14] Feksofenadin juga terbukti menghambat wheal dan flare yang disebabkan oleh histamin hingga tingkat yang jauh lebih besar dibandingkan loratadin atau desloratadin,[15] namun sedikit kurang efektif dibandingkan levosetirizin.[16] Feksofenadin dengan dosis di atas 120 mg sehari tampaknya tidak memberikan kemanjuran tambahan dalam pengobatan rinitis alergi.[17][18]
Efek Samping
[sunting | sunting sumber]Overdosis
[sunting | sunting sumber]Profil keamanan feksofenadin cukup baik, karena tidak ada efek kardiovaskular atau obat penenang yang terbukti terjadi bahkan ketika mengonsumsi 10 kali lipat dosis yang dianjurkan.[19] Penelitian pada manusia berkisar dari dosis tunggal 800 mg, hingga dosis dua kali sehari, 690 mg selama sebulan, tanpa efek samping yang signifikan secara klinis, jika dibandingkan dengan plasebo. Tidak ada kematian yang terjadi dalam pengujian pada tikus, pada dosis 5000 mg/kg berat badan, yang merupakan 110 kali lipat dosis maksimum yang direkomendasikan untuk manusia dewasa. Jika overdosis terjadi, tindakan suportif dianjurkan. Secara teoritis, overdosis dapat muncul sebagai pusing, mulut kering, dan/atau mengantuk, konsisten dengan efek samping yang berlebihan. Hemodialisis tampaknya bukan cara yang efektif untuk menghilangkan feksofenadin dari darah.[20]
Farmakologi
[sunting | sunting sumber]Farmakodinamik
[sunting | sunting sumber]Feksofenadin adalah antagonis reseptor H1 perifer selektif. Penyumbatan mencegah aktivasi reseptor H1 oleh histamin, mencegah terjadinya gejala yang berhubungan dengan alergi. Feksofenadin tidak mudah melewati sawar darah otak, sehingga kecil kemungkinannya menyebabkan kantuk dibandingkan dengan antihistamin lain yang mudah melewati sawar tersebut (yaitu, antihistamin generasi pertama seperti difenhidramin). Secara umum, efek feksofenadin membutuhkan waktu sekitar satu jam, meskipun hal ini mungkin dipengaruhi oleh pilihan bentuk sediaan dan keberadaan makanan tertentu.[20][21]
Feksofenadin juga tidak menunjukkan efek penghambatan reseptor antikolinergik, antidopaminergik, alfa 1-adrenergik, atau beta-adrenergik.[20]
Farmakokinetik[20]
[sunting | sunting sumber]- Penyerapan: Setelah pemberian oral, konsentrasi plasma maksimum tercapai setelah 2-3 jam. Feksofenadin tidak boleh dikonsumsi dengan makanan tinggi lemak, karena konsentrasi rata-rata feksofenadin dalam aliran darah terlihat berkurang dari 20 hingga 60% tergantung pada bentuk pengobatan (tablet, ODT, atau suspensi).
- Distribusi: Feksofenadin 60-70% terikat pada protein plasma, sebagian besar albumin.
- Metabolisme: Feksofenadin adalah substrat CYP3A4, namun hanya sekitar 5% yang dimetabolisme oleh hati, menunjukkan bahwa metabolisme hati relatif kecil dalam pembersihan dari tubuh.
- Eliminasi: Sebagian besar zat dieliminasi tidak berubah melalui feses (80%) dan urin (11-12%).
Interaksi
[sunting | sunting sumber]Mengonsumsi eritromisin atau ketokonazol saat mengonsumsi feksofenadin memang meningkatkan kadar feksofenadin dalam plasma, namun peningkatan ini tidak mempengaruhi interval QT. Alasan terjadinya efek ini kemungkinan besar disebabkan oleh efek yang berhubungan dengan transportasi, khususnya yang melibatkan p-glikoprotein (p-gp).[20] Baik eritromisin dan ketokonazol adalah penghambat p-gp, protein pengangkut yang terlibat dalam mencegah penyerapan feksofenadin di usus. Ketika p-gp dihambat, feksofenadin mungkin diserap lebih baik oleh tubuh, meningkatkan konsentrasi plasma lebih dari yang diharapkan.[butuh rujukan]
Feksofenadin tidak boleh dikonsumsi dengan jus apel, jeruk, atau limau gedang karena dapat menurunkan penyerapan obat. Oleh karena itu, sebaiknya diminum dengan air.[20] Jus limau gedang dapat secara signifikan mengurangi konsentrasi feksofenadin dalam plasma.[22]
Antasida yang mengandung aluminium atau magnesium tidak boleh dikonsumsi dalam waktu 15 menit setelah feksofenadin, karena dapat mengurangi penyerapannya hampir 50%.[20] Hal ini diperkirakan bukan disebabkan oleh perubahan pH (pada kenyataannya, penyerapan sebenarnya dapat meningkat pada pH yang semakin basa), namun lebih disebabkan oleh pembentukan kompleks logam dengan gugus bermuatan/polar pada feksofenadin. Seperti yang dikemukakan oleh Shehnaza dkk (2014), berbagai lokasi molekul dianggap bertanggung jawab atas interaksi ini, termasuk nitrogen piperidin, gugus asam karboksilat (-COOH), dan kedua gugus hidroksil (-OH).[23]
Referensi
[sunting | sunting sumber]- ^ Lappin G, Shishikura Y, Jochemsen R, Weaver RJ, Gesson C, Houston B, Oosterhuis B, Bjerrum OJ, Rowland M, Garner C (May 2010). "Pharmacokinetics of fexofenadine: evaluation of a microdose and assessment of absolute oral bioavailability". European Journal of Pharmaceutical Sciences. 40 (2): 125–131. doi:10.1016/j.ejps.2010.03.009. PMID 20307657.
- ^ a b c Smith SM, Gums JG (July 2009). "Fexofenadine: biochemical, pharmacokinetic and pharmacodynamic properties and its unique role in allergic disorders". Expert Opinion on Drug Metabolism & Toxicology. 5 (7): 813–822. doi:10.1517/17425250903044967. PMID 19545214.
- ^ "Fexofenadine - international brand names". Drugs.com. Diakses tanggal 18 January 2017.
- ^ Bachert C (May 2009). "A review of the efficacy of desloratadine, fexofenadine, and levocetirizine in the treatment of nasal congestion in patients with allergic rhinitis". Clinical Therapeutics. 31 (5): 921–944. doi:10.1016/j.clinthera.2009.05.017. PMID 19539095.
- ^ a b Compalati E, Baena-Cagnani R, Penagos M, Badellino H, Braido F, Gómez RM, Canonica GW, Baena-Cagnani CE (2011). "Systematic review on the efficacy of fexofenadine in seasonal allergic rhinitis: a meta-analysis of randomized, double-blind, placebo-controlled clinical trials". International Archives of Allergy and Immunology. 156 (1): 1–15. doi:10.1159/000321896
 . PMID 21969990.
. PMID 21969990.
- ^ Dicpinigaitis PV, Gayle YE (November 2003). "Effect of the second-generation antihistamine, fexofenadine, on cough reflex sensitivity and pulmonary function". British Journal of Clinical Pharmacology. 56 (5): 501–504. doi:10.1046/j.1365-2125.2003.01902.x. PMC 1884387
 . PMID 14651723.
. PMID 14651723.
- ^ Fischer J, Ganellin CR (2006). Analogue-based Drug Discovery. John Wiley & Sons. hlm. 548. ISBN 9783527607495.
- ^ World Health Organization (2021). World Health Organization model list of essential medicines: 22nd list (2021). Geneva: World Health Organization. hdl:10665/345533
 . WHO/MHP/HPS/EML/2021.02.
. WHO/MHP/HPS/EML/2021.02.
- ^ "Dr. Reddy's announces the launch of Over-the-Counter Fexofenadine HCl and Pseudoephedrine HCl extended release tablets". Dr. Reddy's Laboratories Ltd. 30 August 2011. Diarsipkan dari versi asli tanggal 12 October 2016. Diakses tanggal 27 May 2016.
- ^ Daniel Lednicer (1999). The Organic Chemistry of Drug Synthesis. 6. New York: Wiley Interscience. hlm. 38–40. ISBN 978-0-471-24510-0.
- ^ "Allegra FAQs". Sanofi-Aventis. Diarsipkan dari versi asli tanggal 20 May 2011. Diakses tanggal 5 July 2011.
- ^ "PAR: Reclassification of Allevia 120mg tablets from Prescription Only Medicine (POM) to General Sales List (GSL)". MHRA. 22 December 2020.
- ^ Welzel T, Ziesenitz VC, Seitz S, Donner B, van den Anker JN (November 2018). "Management of anaphylaxis and allergies in patients with long QT syndrome: A review of the current evidence". Annals of Allergy, Asthma & Immunology. 121 (5): 545–551. doi:10.1016/j.anai.2018.07.027
 . PMID 30059791.
. PMID 30059791.
- ^ Hampel F, Ratner P, Mansfield L, Meeves S, Liao Y, Georges G (October 2003). "Fexofenadine hydrochloride, 180 mg, exhibits equivalent efficacy to cetirizine, 10 mg, with less drowsiness in patients with moderate-to-severe seasonal allergic rhinitis". Annals of Allergy, Asthma & Immunology. 91 (4): 354–361. doi:10.1016/S1081-1206(10)61682-1. PMID 14582814.
- ^ Kruszewski J, Kłos K, Sułek K (November 2006). "[Inhibition of histamine-induced wheel after a recommended single dose administration of 10 mg cetirizine, 5 mg desloratadine, 120 i 180 mg fexofenadine, 5 mg levocetirizine and 10 mg loratadine--a randomized, double-blind, placebo controlled trial]". Polski Merkuriusz Lekarski. 21 (125): 443–448. PMID 17345837.
- ^ Grant JA, Riethuisen JM, Moulaert B, DeVos C (February 2002). "A double-blind, randomized, single-dose, crossover comparison of levocetirizine with ebastine, fexofenadine, loratadine, mizolastine, and placebo: suppression of histamine-induced wheal-and-flare response during 24 hours in healthy male subjects". Annals of Allergy, Asthma & Immunology. 88 (2): 190–197. doi:10.1016/S1081-1206(10)61995-3. PMID 11868924.
- ^ Casale TB, Andrade C, Qu R (1999). "Safety and efficacy of once-daily fexofenadine HCl in the treatment of autumn seasonal allergic rhinitis". Allergy and Asthma Proceedings. 20 (3): 193–198. doi:10.2500/108854199778553046. PMID 10389553.
- ^ Howarth PH, Stern MA, Roi L, Reynolds R, Bousquet J (November 1999). "Double-blind, placebo-controlled study comparing the efficacy and safety of fexofenadine hydrochloride (120 and 180 mg once daily) and cetirizine in seasonal allergic rhinitis". The Journal of Allergy and Clinical Immunology. 104 (5): 927–933. doi:10.1016/s0091-6749(99)70070-9
 . PMID 10550734.
. PMID 10550734.
- ^ Philpot EE (Jan–Feb 2000). "Safety of second generation antihistamines". Allergy and Asthma Proceedings. 21 (1): 15–20. doi:10.2500/108854100778249033. PMID 10748947.
- ^ a b c d e f g "Allegra (fexofenadine hydrochloride) tablet, orally disintegrating for oral use Allegra (fexofenadine hydrochloride) tablet, film coated for oral use Allegra (fexofenadine hydrochloride) suspension for oral useInitial U.S. Approval: 1996". DailyMed. 15 December 2008. Diakses tanggal 13 February 2022.
- ^ Stoltz M, Arumugham T, Lippert C, Yu D, Bhargava V, Eller M, Weir S (October 1997). "Effect of food on the bioavailability of fexofenadine hydrochloride (MDL 16455A)". Biopharmaceutics & Drug Disposition. 18 (7): 645–648. doi:10.1002/(SICI)1099-081X(199710)18:7<645::AID-BDD50>3.0.CO;2-3. PMID 9330784.
- ^ Shirasaka Y, Mori T, Murata Y, Nakanishi T, Tamai I (August 2014). "Substrate- and dose-dependent drug interactions with grapefruit juice caused by multiple binding sites on OATP2B1". Pharmaceutical Research. 31 (8): 2035–2043. doi:10.1007/s11095-014-1305-7. PMID 24549825.
- ^ Shehnaz H, Haider A, Arayne MS, Sultana N (Nov 2014). "Carboxyterfenadine antacid interaction monitoring by UV spectrophotometry and RP-HPLC techniques". Arabian Journal of Chemistry. 7 (5): 839–845. doi:10.1016/j.arabjc.2013.01.011
 .
.