Pirazin
| Pirazin | |||
 |

| ||
 |
| ||
| IUPAC-név | pirazin | ||
| Más nevek | 1,4-diazabenzol, p-diazin, 1,4-diazin, paradiazin, piazin, UN 1325 | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 290-37-9 | ||
| PubChem | 9261 | ||
| ChemSpider | 8904 | ||
| EINECS-szám | 206-027-6 | ||
| ChEBI | 30953 | ||
| |||
| |||
| InChIKey | KYQCOXFCLRTKLS-UHFFFAOYSA-N | ||
| ChEMBL | 15797 | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C4H4N2 | ||
| Moláris tömeg | 80,09 g/mol | ||
| Megjelenés | fehér kristályok | ||
| Sűrűség | 1,031 g/cm³ | ||
| Olvadáspont | 52 °C | ||
| Forráspont | 115 °C | ||
| Oldhatóság (vízben) | oldódik | ||
| Savasság (pKa) | 0,37[1] (protonált pirazin) | ||
| Mágneses szuszceptibilitás | −37,6·10−6 cm³/mol | ||
| Veszélyek | |||
| NFPA 704 | |||
| R mondatok | R11, R36/37/38 | ||
| S mondatok | S16, S26, S36 | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
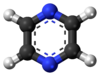
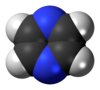
A pirazin heterociklusos aromás szerves vegyület, képlete C4H4N2.
A pirazin szimmetrikus molekula, a pontcsoportja D2h. Kevésbé bázikus, mint a piridin, piridazin vagy a pirimidin.
Az egyes hagyományos kínai medicinák összetevőjeként[2] is előforduló tetrametilpirazin esetében beszámoltak arról, hogy megköti a szuperoxid aniont és csökkenti az emberi polimorfonukleáris leukocitákban a nitrogén-monoxid termelését.[3]
Előállítása
[szerkesztés]Számos módszer ismert a pirazin és származékainak szintézisére, némelyik a legrégebb óta ismert, még ma is használt reakciók közé tartozik.
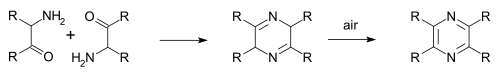
A Staedel–Rugheimer-pirazinszintézis (1876) során 2-klóracetofenon ammóniával reagálva aminoketont képez, majd kondenzációval és oxidációval pirazinná alakul.[4] Ennek egyik változata, a Gutknecht-pirazinszintézis (1879) is ezen az önkondenzáción alapul, de az alfa-aminoketon más úton keletkezik.[5][6]
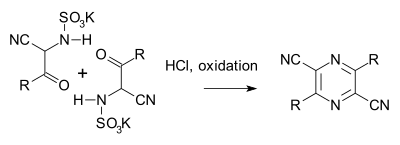
A Gastaldi-szintézis (1921) egy másik változat:[7][8]
Jegyzetek
[szerkesztés]- ↑ Brown, H.C., et al., in Baude, E.A. and Nachod, F.C., Determination of Organic Structures by Physical Methods, Academic Press, New York, 1955.
- ↑ http://www.itmonline.org/arts/ligustrazine.htm
- ↑ Zhang, Zhaohui (2003. november 4.). „Tetramethylpyrazine scavenges superoxide anion and decreases nitric oxide production in human polymorphonuclear leukocytes”. Life Sciences 72 (22), 2465–2472. o. DOI:10.1016/S0024-3205(03)00139-5.
- ↑ Ueber die Einwirkung von Ammoniak auf Chloracetylbenzol (pp. 563–564) W. Staedel, L. Rügheimer doi:10.1002/cber.187600901174 Berichte der deutschen chemischen Gesellschaft Volume 9, Issue 1, pp. 563–564, 1876
- ↑ Mittheilungen Ueber Nitrosoäthylmethylketon H. Gutknecht Berichte der deutschen chemischen Gesellschaft Volume 12, Issue 2 , pp. 2290–2292, 1879 doi:10.1002/cber.187901202284
- ↑ Heterocyclic chemistry T.L. Gilchrist ISBN 0-582-01421-2
- ↑ G. Gastaldi, Gazz. Chim. Ital. 51, (1921) 233
- ↑ Amines: Synthesis, Properties and Applications Stephen A. Lawrence 2004 Cambridge University Press ISBN 0-521-78284-8
Fordítás
[szerkesztés]- Ez a szócikk részben vagy egészben a Pyrazine című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.