Phtalocyanine de cuivre
| Phtalocyanine de cuivre(II) | |
| |
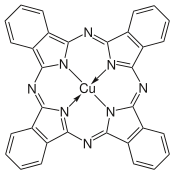
| Structure de la phtalocyanine de cuivre(II) | |
| Identification | |
|---|---|
| Synonymes |
Bleu de phtalocyanine, |
| No CAS | |
| No ECHA | 100.005.169 |
| No CE | 205-685-1 |
| No RTECS | GL8510000 |
| PubChem | 475701 |
| ChEBI | 155903 |
| SMILES | |
| InChI | |
| Apparence | poudre inodore bleu foncé[1] |
| Propriétés chimiques | |
| Formule | C32H16CuN8 |
| Masse molaire[2] | 576,069 ± 0,031 g/mol C 66,72 %, H 2,8 %, Cu 11,03 %, N 19,45 %, |
| Propriétés physiques | |
| T° fusion | 480 °C[1] |
| Solubilité | pratiquement insoluble dans l'eau[1] |
| Masse volumique | 1,61 g/cm3[1] à 20 °C |
| Précautions | |
| NFPA 704[3] | |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
La phtalocyanine de cuivre, notée CuPc, est un complexe de phtalocyanine et de cuivre de formule chimique Cu(C8H4N2)4. Il s'agit d'un solide bleu qui se présente sous la forme de poudre ou d'aiguilles à l'éclat métallique. C'est le pigment bleu le plus connu, dit bleu phtalo, apprécié pour son aspect brillant, son pouvoir colorant et son pouvoir couvrant. Elle est largement utilisée pour les peintures, la teinture des plastiques et les encres d'imprimerie. Les pigments de phtalocyanine de cuivre ont une bonne résistance à haute température et une très bonne solidité à la lumière, aux intempéries et aux altérations chimiques par les acides et les bases. Ils sont très peu solubles dans les solvants usuels, dont l'eau.
-
Poudre de bleu phtalo.
Synthèse
[modifier | modifier le code]Il existe deux procédés de fabrication d'importance commerciale pour la production de phtalocyanine de cuivre :
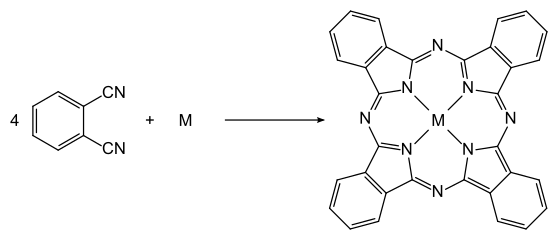
- le procédé au phtalonitrile[4], principalement utilisé en Allemagne ;
- le procédé à l'anhydride phtalique-urée[5], développé au Royaume-Uni et aux États-Unis.
Les deux approches peuvent être réalisées avec ou sans solvant, ce qu'on appelle respectivement les procédés au solvant et les procédés aux micro-ondes (ou au four)[5],[6]. Les premiers permettent d'atteindre les rendements les plus élevés (> 95 %, contre 80 à 90 % pour les procédés aux micro-ondes), de sorte qu'ils ont fait l'objet des premiers développements ; les procédés aux micro-ondes ont bénéficié d'un regain d'intérêt tardif principalement pour des raisons économiques et écologiques car ils sont plus rapides et n'utilisent pas de solvants.
-
Principe du procédé au phtalonitrile.
Procédé au phtalonitrile
[modifier | modifier le code]Cette méthode consiste à chauffer le phtalonitrile avec un sel de cuivre[7], généralement du chlorure de cuivre(I) entre 200 et 240 °C. La réaction complète peut s'écrire comme suit :
Procédé à l'anhydride phtalique-urée
[modifier | modifier le code]La réaction globale entre l'anhydride phtalique et l'urée en présence d'un sel de cuivre peut s'écrire comme suit :
Applications
[modifier | modifier le code]Comme catalyseur
[modifier | modifier le code]Les phtalocyanines de métaux ont longtemps été étudiées comme catalyseurs pour les réactions d'oxydoréduction. Les sujets étudiés sont la réaction de réduction de l'oxygène (en) et l'adoucissement des flux gazeux par élimination du sulfure d'hydrogène H2S.
Comme colorant
[modifier | modifier le code]En raison de sa stabilité, le bleu de phtalocyanine est utilisé dans les encres, les revêtements et de nombreux plastiques. Le pigment est insoluble et n'a pas tendance à migrer dans le matériau. C'est un pigment standard utilisé dans les encres d'imprimerie et pour les emballages. C'est le pigment ayant la plus importante production en volume[8]. Tous les principaux fabricants de pigments artistiques produisent des variantes de phtalocyanine de cuivre, désignées par l'indice de couleur PB15 (bleu)[9] et les indices de couleur PG7 et PG36 (vert)[10].
À l'étude
[modifier | modifier le code]La phtalocyanine de cuivre a souvent été étudiée pour des applications en électronique moléculaire. Elle est potentiellement adaptée aux cellules photovoltaïques organiques en raison de sa grande stabilité chimique et de sa croissance uniforme[11],[12]. CuPc joue généralement le rôle de donneur d'électrons dans les cellules photovoltaïques à matériaux donneurs et accepteurs. L'une des réalisations à hétérojonction les plus courantes est le CuPc/C60 qui est rapidement devenu un système modèle pour l'étude des petites molécules organiques[13],[14]. L'efficacité de conversion de photon en électron dans un tel système atteint environ 5 %.
Le CuPc a également été étudié comme constituant de transistors à effet de champ organiques (en) (OFET)[15]. La phtalocyanine de cuivre a été proposée pour le stockage d'information en calcul quantique, en raison de la durée pendant laquelle ses électrons peuvent rester en superposition[16]. CuPc peut être facilement transformé en un couche mince pour la fabrication de composants, ce qui en fait un matériau candidat pour réaliser des qubits[16],[17].
Notes et références
[modifier | modifier le code]- Entrée « Copper phthalocyanine » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 6 août 2022 (JavaScript nécessaire)
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- « Fiche du composé Copper(II) phthalocyanine », sur Alfa Aesar (consulté le ).
- (en) Suzanne Quillen Lomax, « Phthalocyanine and quinacridone pigments: their history, properties and use », Studies in Conservation, vol. 50, , p. 19-29 (DOI 10.1179/sic.2005.50.Supplement-1.19, lire en ligne)
- (en) Ki Suck Jung, Ji Young Ro, Jong Young Lee et Seong Soo Park, « Conventional versus microwave synthesis of phthalocyanine material », Journal of Materials Science Letters, vol. 20, no 24, , p. 2203-2205 (DOI 10.1023/A:1017932900939, lire en ligne)
- (en) K. S. Jung, J. H. Kwon, S. M. Son, J. S. Shin, G. D. Lee et S. S. Park, « Characteristics of the copper phthalocyanines synthesized at various conditions under the classical and microwave processes », Synthetic Metals, vol. 141, no 3, , p. 259-264 (DOI 10.1016/S0379-6779(03)00414-4, lire en ligne)
- (en) Gerd Löbbert, « Phthalocyanines », Ullmann's Encyclopedia of Industrial Chemistry, (DOI 10.1002/14356007.a20_213, lire en ligne)
- (en) Peter Gregory, « Industrial applications of phthalocyanines », Journal of Porphyrins and Phthalocyanines, vol. 4, no 4, , p. 432-437 (DOI 10.1002/(SICI)1099-1409(200006/07)4:4<432::AID-JPP254>3.0.CO;2-N, lire en ligne)
- (en) « blue », sur handprint.com (consulté le ).
- (en) « green », sur handprint.com (consulté le ).
- (en) M. Szybowicz, T. Runka, M. Drozdowski, W. Bała, A. Grodzicki, P. Piszczek et A. Bratkowski, « High temperature study of FT-IR and Raman scattering spectra of vacuum deposited CuPc thin films », Journal of Molecular Structure, vol. 704, nos 1-3, , p. 107-113 (DOI 10.1016/j.molstruc.2004.01.053, Bibcode 2004JMoSt.704..107S, lire en ligne)
- (en) W. Bała, M. Wojdyła, M. Rebarz, M. szybowic, M. Drozdowski, A. Grodzicki et P. Piszczek, « Influence of central metal atom in MPc (M = Cu, Zn, Mg, Co) on Raman, FT-IR, absorbance, reflectance, and photoluminescence spectra », Journal of Optoelectronics and Advanced Materials, vol. 11, no 3, , p. 264-269 (lire en ligne)
- (en) Askat E. Jailaubekov, Adam P. Willard, John R. Tritsch, Wai-Lun Chan, Na Sai, Raluca Gearba, Loren G. Kaake, Kenrick J. Williams, Kevin Leung, Peter J. Rossky et X-Y. Zhu, « Hot charge-transfer excitons set the time limit for charge separation at donor/acceptor interfaces in organic photovoltaics », Nature Materials, vol. 12, no 1, , p. 66-73 (PMID 23223125, DOI 10.1038/nmat3500, Bibcode 2013NatMa..12...66J, lire en ligne)
- (en) Xin Lia, Yan Chen, Jie Sang, Bao-Xiu Mi, Dan-Hua Mu, Zhi-Gang Li, Hui Zhang, Zhi-Qiang Gao et Wei Huang, « CuPc/C60 bulk heterojunction photovoltaic cells with evidence of phase segregation », Organic Electronics, vol. 14, no 1, , p. 250-254 (DOI 10.1016/j.orgel.2012.10.041, lire en ligne)
- (en) G. Chaidogiannos, F. Petraki, N. Glezos, S. Kennou et S. Nešpůrek, « Low voltage operating OFETs based on solution-processed metal phthalocyanines », Applied Physics A, vol. 96, no 3, , p. 763-767 (DOI 10.1007/s00339-009-5268-1, Bibcode 2009ApPhA..96..763C, S2CID 98694166, lire en ligne)
- (en) Marc Warner, Salahud Din, Igor S. Tupitsyn, Gavin W. Morley, A. Marshall Stoneham, Jules A. Gardener, Zhenlin Wu, Andrew J. Fisher, Sandrine Heutz, Christopher W. M. Kay et Gabriel Aeppli, « Potential for spin-based information processing in a thin-film molecular semiconductor », Nature, vol. 503, no 7477, , p. 504-508 (PMID 24162849, DOI 10.1038/nature12597, Bibcode 2013Natur.503..504W, lire en ligne)
- (en) Marc Warner, Salahud Din, Jules Gardener, Gavin W. Morley, Wei Wu, Marshall Stoneham, Andrew J. Fisher, Sandrine Heutz, Christopher W. M. Kay et Gabriel Aeppli, « Introducing copper phthalocyanine as a qubit. », American Physical Society - APS March Meeting 2012, , article no W13.011 (Bibcode 2012APS..MARW13011W)