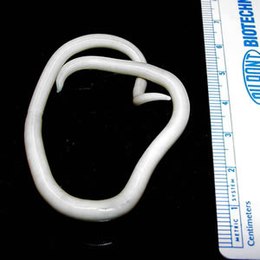
Ascaridiose
| Causes | Ascaris |
|---|---|
| Transmission | Contamination féco-orale |
| Incubation min | 1 semaine |
| Incubation max | 3 semaine |
| Symptômes | Crampe abdominale, vomissement, nausée, douleur abdominale, diarrhée, malaise (en), fièvre légère (d), urticaire et toux |
| Médicament | Mébendazole, ivermectine, embonate de pyrantel (en), pyrantel et albendazole |
|---|---|
| Spécialité | Infectiologie et helminthologiste (d) |
| CIM-10 | B77 |
|---|---|
| CIM-9 | 127.0 |
| OMIM | 000628 |
| DiseasesDB | 934 |
| MedlinePlus | 000628 |
| eMedicine | 212510 |
| MeSH | D001196 |
L'ascaridiose est une parasitose cosmopolite résultant de l'infestation de l'Homme par Ascaris, un nématode de grande taille (de 20 cm de long sur 5 mm de diamètre). Il fait partie des helminthiases ou infections par vers intestinaux, très fréquentes en milieu chaud et là où les conditions d'hygiène restent préoccupantes.
Si la maladie est peu grave par elle-même, elle entraîne un affaiblissement de l'organisme en aggravant la dénutrition et en le rendant moins apte à se défendre contre d'autres maladies. Elle a donc des conséquences socio-économiques importantes.
Épidémiologie
[modifier | modifier le code]
- aucune donnée
- moins de 10
- 10-20
- 20-30
- 30-40
- 40-50
- 50-60
- 60-80
- 80-100
- 100-120
- 120-140
- 140-150
- plus de 150
Parmi les 1 450 millions de personnes infectées par l'Ascaris, 350 millions seraient gravement atteintes de cette verminose cosmopolite occasionnant 60 000 décès annuels, selon l'OMS[1]. La prévalence de l'ascaridiose est très variable selon les régions : si elle tend à disparaître des régions tempérées, où elle fut d'ailleurs habituellement bénigne, elle continue à sévir, à des taux importants, dans les pays chauds du tiers-monde et y pèse lourdement sur le taux de mortalité infantile. En Europe, ce sont les zones rurales qui sont plus particulièrement concernées.
Il s'agit essentiellement d'une maladie de l'enfant ou de l'adulte jeune, sa fréquence baissant avec l'âge.
Cause
[modifier | modifier le code]Transmission
[modifier | modifier le code]La contamination se fait par voie digestive lors de l'ingestion d'eau ou d'aliments contaminés. Les aliments sont souillés par des excréments contenant des œufs, par les mains sales surtout chez les enfants (mains en contact avec du sable contenant des excréments).
Cycle de vie
[modifier | modifier le code]
Les vers adultes vivent dans la lumière (lumen) du gros intestin. Une femelle peut produire environ 200 000 œufs par jour, qui sont dispersés par les selles. Les œufs non fécondés peuvent être ingérés, mais ne sont pas infectieux. Les œufs fécondés évoluent en embryons, et deviennent infectieux après un délai de dix-huit jours à plusieurs semaines, en fonction des conditions de l’environnement (optimum : humidité, chaleur, sol infecté). Après l’ingestion d'œufs infectieux, les larves éclosent, envahissent la muqueuse intestinale, et sont transportées par la veine porte, puis par la circulation systémique jusqu’aux poumons. Les larves poursuivent leur maturation dans les poumons (10 à 14 jours), pénètrent les parois alvéolaires, remontent l’arbre bronchique jusqu’à la gorge, et sont avalées. Après avoir atteint l’intestin grêle, elles s'y développent pour évoluer en vers adultes. Il s’écoule de deux à trois mois entre l’ingestion des œufs infectieux et l’oviposition de la femelle adulte. Les vers adultes peuvent vivre une à deux années.
Le cycle évolutif est direct, à un seul hôte, l'homme ; l'œuf, très résistant, évolue dans le milieu extérieur, s'embryonne en trois semaines au moins, et devient infectieux. Dégluti comme souillure de l'eau, des légumes ou des fruits, il contamine un nouveau sujet.
Deux faits sont à noter :
- l'auto-infestation est impossible, l'œuf n'étant pas embryonné au moment de son expulsion avec les selles ;
- l'œuf embryonné infectieux, efficacement protégé par sa coque épaisse, garde très longtemps son pouvoir pathogène, particulièrement dans l'engrais d'origine humaine.
L'ascaris sécrète au moins deux types de molécules, dont l'une le protège contre le suc gastrique (inhibiteur de pepsine), et l'autre inhibe la prolifération des lymphocytes (phosphorylcholine).
Symptômes
[modifier | modifier le code]Deux tableaux cliniques se succèdent dans l'ascaridiose, le premier traduisant la migration des larves, le second, l'action pathogènes des adultes.
La période d'invasion, pendant les migrations organiques des larves, passe souvent inaperçue, sauf dans les zones de grande endémie ; dans ce cas, infestations massives et réinfestations aboutissent à un tableau clinique d'affection broncho-pulmonaire avec toux sèche quinteuse et syndrome de Löffler[2] typique, simulant trop souvent une tuberculose.
La période d'état est celle du parasitisme intestinal par les vers adultes ou ascaridiose proprement dite.
Dans les régions à bonne hygiène et taux d'infestation faible, le porteur sain est la règle. Chez l'enfant ou le sujet sensible, des troubles divers non spécifiques sont notés : pâleur de la face, troubles nerveux (irritabilité, insomnie), troubles digestifs (ballonnements, pesanteur gastrique, haleine sure, troubles de l'appétit et du transit).
Dans les zones de grande endémie, régions chaudes à mauvaise hygiène et où l'on utilise l'engrais humain, les infestations massives, 200 à 400 vers chez le jeune enfant, 800 à 1 000 chez l'adulte, aboutissent souvent à des manifestations cliniques dramatiques : tableaux de sub-occlusion ou d'occlusion ; hépatites, cholécystites et pancréatites par migrations canaliculaires[3] et surinfections ; péritonites par perforation ; atteintes nerveuses, psychiques, méningées et crises épileptiformes ; atteintes sévères de l'état général par toxi-infections secondaires aboutissant à la cachexie et à la mort.
En dehors de cette morbidité propre, la présence insoupçonnée d'ascaris peut compliquer une intervention chirurgicale abdominale : soit mécaniquement par disjonction des sutures, occlusion ou volvulus, soit par choc toxique lors de la lyse post-mortem des parasites.
La présence du ver ne semble pas provoquer de réaction immunitaire protectrice et les réinfestations sont communes. La présence de plusieurs parasites intestinaux (ankylostome, trichocéphalose) est courante.
La gravité de l'atteinte est corrélée au nombre de parasites retrouvés[4].
Diagnostic
[modifier | modifier le code]Le diagnostic est évident quand le malade rejette un ascaris, habituellement avec les selles, mais parfois aussi par la bouche[5] ou le nez[6], le ver étant migrateur.
Le diagnostic est le plus souvent fait par un laboratoire (découverte d'œufs mamelonnés caractéristiques dans les selles avec un examen parasitologique) ou par la radiographie abdominale après transit baryté (la présence de vers dans l'intestin, opacifié par la baryte déglutie, est alors visible). La recherche des œufs peut être aidée par des techniques de concentration[2] mais ces examens peuvent se révéler être normaux, ou révéler la présence du parasite seulement plusieurs mois après l'infestation[2].
La biologie peut montrer, à la phase d'invasion, une augmentation du taux de polynucléaires éosinophiles[2], non spécifiques. La recherche d'anticorps dirigés contre l'hémoglobine de l'ascaris peut aider à faire un diagnostic plus précoce[7].
Traitement
[modifier | modifier le code]Le traitement antihelminthique est à base d'albendazole ou de mébendazole[8]. L'ivermectine peut constituer une alternative[2].
En cas d'obstruction non grave du tube digestif, l'ingestion d'un soluté de contraste peut aider[9].
Prévention
[modifier | modifier le code]La prévention repose sur la lutte contre le péril fécal : mesures et installations sanitaires, interdiction de l'épandage des engrais humains, hygiène de l'eau, lavage des crudités et des mains, traitement des eaux usées.
Divers
[modifier | modifier le code]Agnès Sorel, favorite du roi de France Charles VII, en était atteinte, comme l'atteste la présence d’œufs d'ascaris dans les restes exhumés. Elle était manifestement traitée pour, des extraits de fougères ayant été retrouvées ainsi qu'une imprégnation en mercure, cause de sa mort et traitement de la maladie à cette époque[10]. Ce fut également le cas des rois d'Angleterre Richard III[11] et Henry VIII[12].
Victor Hugo aurait confondu ver de terre et ascaris en écrivant[13] :
Charles neuf, faible et mou comme un jonc sous le vent, Fut par les vers de terre habité tout vivant.
— Les Quatre Vents de l'esprit, Le Siècle, « Qui que tu sois qui tient un peuple dans ta main ».
Notes et références
[modifier | modifier le code]- (en) Partnership for Parasite Control, Second Meeting Rome, avril 2002
- Jourdan PM, Lamberton PHL, Poppy HL, Fenwick A, Addiss DG, Soil-transmitted helminth infections, lancet, 2018;391:252–265
- Das AK, Hepatic and biliary ascariasis, J Glob Infect Dis, 2014;6:65–72
- de Silva NR, Guyatt HL, Bundy DA, Worm burden in intestinal obstruction caused by Ascaris lumbricoides, Trop Med Int Health, 1997, n°2, p.189–190.
- (en) Margery J, Niang A, « Adult ascaris worm passing from the mouth », Am J Trop Med Hyg, vol. 85, no 3, , p. 395. (PMID 21896792, PMCID PMC3163854, DOI 10.4269/ajtmh.2011.11-0258, lire en ligne [html])
- (en) Kalan A, Tariq M, « Foreign bodies in the nasal cavities: a comprehensive review of the aetiology, diagnostic pointers, and therapeutic measures », Postgrad Med J, vol. 76, no 898, , p. 484-7. (PMID 10908376, PMCID PMC1741675, lire en ligne [html])
- Vlaminck J, Supali T, Geldhof P, Hokke CH, Fischer PU, Weil GJ' Community rates of IgG4 antibodies to Ascaris haemoglobin reflect changes in community egg loads following mass drug administration, PLoS Negl Trop Dis, 2016;10:e0004532
- Levecke B, Montresor A, Albonico M et al. Assessment of anthelmintic efficacy of mebendazole in school children in six countries where soil-transmitted helminths are endemic, PLoS Negl Trop Dis, 2014;8:e3204
- Hamid R, Bhat N, Baba A et al. Use of gastrografin in the management of worm-induced small bowel obstruction in children, Pediatr Surg Int, 2015;31:1171–1176
- Philippe Charlier, Médecin des morts, chapitre « Qui a tué la Dame de Cœur ? », Éditions Pluriel, 2014, p. 17-37
- (en) « DEFINE_ME », sur thelancet.com (consulté le ).
- (en) Douglas Main, « Infected and Hunched : King Richard III Was Crawling With Roundworms », sur livescience.com, (consulté le ).
- V. Gillot, « Ascaridiose », Encyclopédie médico-chirurgicale, maladies infectieuses, , p. 1fascicule 8116