Pralidoxim
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
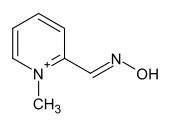
| ||||||||||||||||||||||
| Strukturformel des E-konfigurierten Kations | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Pralidoxim | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C7H9N2O | |||||||||||||||||||||
| Kurzbeschreibung |
gelbe Kristalle[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 137,07 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest (Hydrochlorid)[2] | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||||||||
Pralidoxim (kurz 2-PAM) ist ein Antidot, das bei Vergiftung mit Organophosphaten angewendet werden kann und in verschiedenen chemischen Abwandlungen vorkommt. Eigentlich bezeichnet der Name Pralidoxim lediglich das zugrundeliegende Pyridiniumkation. Prominente Gegenionen sind Chlorid, Iodid und Methylsulfat. Eine bessere Wirkung weist jedoch Trimedoxim auf.
Mögliche Formen
[Bearbeiten | Quelltext bearbeiten]Isomerie
[Bearbeiten | Quelltext bearbeiten]Pralidoxim kann in der E- oder in der Z-Konfiguration vorliegen. Kristallstrukturanalysen zeigten, dass die E-Konfiguration mit linear-ausgestreckter Aldoxim-Gruppe vorherrscht. Allerdings gibt es Hinweise darauf, dass unter physiologischen Bedingungen eine s-cis-Konfiguration der Bindung zwischen dem Ring-Kohlenstoffatom und dem Aldoxim-Kohlenstoffatom entscheidend ist. Auch fand man, dass die Struktur sich durch Deprotonierung stark verändert. Der Pyridinring ist in der protonierten Form deutlich flexibler, als in der deprotonierten Form.[3]
| Diastereomere von Pralidoxim | ||
| Name | (E)-Pralidoxim | (Z)-Pralidoxim |
| Andere Namen | 2-[(E)-(Hydroxyimino)methyl]-1-methylpyridinium | 2-[(Z)-(Hydroxyimino)methyl]-1-methylpyridinium |
| Strukturformel |  |

|
| CAS-Nummer | ||
| 6735-59-7 | 45765-69-3 | |
| PubChem | 135398747 | 135484646 |
| 4884 (unspez.) | ||
| ChemSpider | – | – |
| 5193737 (unspez.) | ||
| DrugBank | – | – |
| DB00733 (unspez.) | ||
| Wikidata | ||
| Q2735334 | Q112768890 | |
Salze
[Bearbeiten | Quelltext bearbeiten]Drei beispielhafte neutrale Verbindungen des Pralidoxims sind in folgender Tabelle aufgeführt:
| Salze von Pralidoxim | |||
| Name | Pralidoximiodid | Pralidoximchlorid | Pralidoximmethylsulfat |
| Strukturformel | 
| ||
| CAS-Nummer | 94-63-3 | 51-15-0 | 1200-55-1 |
| PubChem | 135410029 | 135445761 | 135539491 |
| ChemSpider | 13233097 | 10481993 | 20127125 |
| EG-Nummer | 202-349-6 | 200-080-9 | 214-852-8 |
| ECHA-ID | 100.002.136 | 100.000.074 | 100.013.502 |
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]Die erste Synthese von neutralen Formen des Pralidoxims stammt von Ginsburg und Wilson und wurde 1957 veröffentlicht. Dabei wird das Edukt Picolinaldehyd zuerst mit Hydroxylaminhydrochlorid in einer neutralen, wässrigen Lösung zum Oxim umgesetzt und dann eine Additionsreaktion zum Beispiel mit Methyliodid in Aceton durchgeführt. Das Produkt (hier das Pralidoximiodid) kann aus Wasser rekristallisiert werden.[1]

Ginsburg beschrieb ebenfalls die Synthese des Pralidoximchlorids. Dazu bediente er sich des Pralidoximiodids, welches er bereits hergestellt hatte, und schüttelte es in einer wässrigen Silberchlorid-Lösung. Silberiodid fiel aus und das Pralidoximchlorid blieb in der Lösung.
Das Pralidoximmethylsulfat wird synthetisiert, indem statt Methyliodid im zweiten Schritt das Methylierungsreagenz Dimethylsulfat verwendet wird.[4]
Pharmakologie
[Bearbeiten | Quelltext bearbeiten]Pralidoxim-Salze reaktivieren die durch Organophosphate reversibel inaktivierte Acetylcholinesterase, indem sie den gebildeten Phosphatester zwischen dem Organophosphat und dem Enzym wieder spalten. Somit wird einer Akkumulation des Acetylcholins entgegengewirkt. Die langsame Umwandlung des Enzyms durch das Organophosphat in eine nicht wieder aktivierbare Form wird zudem ebenfalls verhindert. Die Paralyse der Atemwege wird allerdings von Pralidoxim verhältnismäßig schlecht gehindert, weswegen es meist zusammen mit Atropin angewendet wird. Die Anwendung von Pralidoxim muss innerhalb von 24 Stunden nach der Vergiftung erfolgen und ist bei unterschiedlichen Organophosphaten auch unterschiedlich stark wirksam.[5]
Wechselwirkungen
[Bearbeiten | Quelltext bearbeiten]Es sind Wechselwirkungen mit mehreren hundert Arzneimitteln bekannt. Die meisten davon sorgen für eine verlangsamte Exkretion des Pralidoxims und dadurch für eine höhere Konzentration im Blut.[5]
Handelsnamen
[Bearbeiten | Quelltext bearbeiten]Kombination von Pralidoximchlorid mit Atropin: Atnaa, DuoDote[5]
Siehe auch
[Bearbeiten | Quelltext bearbeiten]Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c S. Ginsburg, I. B. Wilson: Oximes of the pyridine series1. In: Journal of the American Chemical Society. Band 79, Nr. 2, 1957, S. 481–485, doi:10.1021/ja01559a067.
- ↑ a b c d Datenblatt Pyridine-2-aldoxime methochloride bei Sigma-Aldrich, abgerufen am 28. Juni 2022 (PDF).
- ↑ A. T. Castro, J. D. Figueroa-Villar: Molecular structure, conformational analysis and charge distribution of pralidoxime: Ab initio and DFT studies. In: International journal of quantum chemistry. Band 89, Nr. 3, 2002, S. 135–146, doi:10.1002/qua.10302.
- ↑ Patent BE641041A: Angemeldet am 10. Juni 1964, veröffentlicht am 10. Dezember 1965.
- ↑ a b c Eintrag zu Pralidoxime in der DrugBank der University of Alberta, abgerufen am 29. Juni 2022.
