Diazodinitrophenol
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
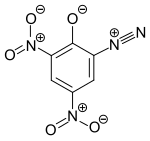
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Diazodinitrophenol | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C6H2N4O5 | ||||||||||||||||||
| Kurzbeschreibung |
gelblich bis rotgelbliches amorphes Pulver, dunkelt im Sonnenlicht aber schnell[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 210,1 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte |
1,63 g·cm−3[1] | ||||||||||||||||||
| Löslichkeit |
wenig löslich in Wasser, etwas löslich in Methanol und Ethanol, löslich in Aceton, Nitroglycerin, Nitrobenzol, Anilin, Pyridin und Essigsäure[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Diazodinitrophenol ist eine chemische Verbindung, die als Initialsprengstoff verwendet wird.
Darstellung
[Bearbeiten | Quelltext bearbeiten]Diazodinitrophenol entsteht durch Diazotierung aus 2-Amino-4,6-dinitrophenol.[3][4] Diese vom Chemiker Peter Grieß im Jahr 1858 erstmals durchgeführte Reaktion gilt als die erste Darstellung einer Diazoniumverbindung. Grieß leitete Salpetrige Säure durch eine alkoholische Lösung von 2-Amino-4,6-dinitrophenol.[5]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Die Verbindung ist im trockenen Zustand durch Schlag, Reibung, Wärme und andere Zündquellen besonders explosionsgefährlich[6] und fällt im Umgang unter das Sprengstoffgesetz.[7]
Tabelle mit wichtigen explosionsrelevanten Eigenschaften: Sauerstoffbilanz −60,9 %[1] Stickstoffgehalt 26,67 %[1] Normalgasvolumen 859 l·kg−1[1] Explosionswärme 3998,8 kJ·kg−1 (H2O (l))
3967,5 kJ·kg−1 (H2O (g))[1]Spezifische Energie 1047,9 kJ·kg−1 (107,0 mt/kg)[1] Bleiblockausbauchung 32,6 cm3·g−1[1] Detonationsgeschwindigkeit 6600 m·s−1[1] Verpuffungspunkt 180–200 °C[1] Schlagempfindlichkeit 1,5 Nm[1] Reibempfindlichkeit 14 N[8]
Die Verbindung ist thermisch instabil und kann sich stark exotherm zersetzen. Eine DSC-Messung zeigt ab 155 °C eine Zersetzungsreaktion mit einer Reaktionsenthalpie von −2075 J·g−1 bzw. −436 kJ·mol−1.[9][10] Thomas M. Klapötke et al. sahen nach einer Vergleichsstudie zwischen Kristallstrukturanalyse und diversen theoretischen Betrachtungen eine Strukturformel mit C=O-Doppelbindung als maßgeblich, wobei die Elektronendichte zwischen der Diazogruppe und dem Ring am besten so verteilt ist, dass sich ein Singulett-Diradikal ergibt mit Lokalisierung der Spindichte in den π-Orbitalen, so dass die Aromatizität erhalten bleibt und die Ladungen minimiert sind. Entsprechend diesem Befund ist Diazonitrophenol eher als Diazoverbindung zu sehen, weniger als Diazoniumsalz. Eine ebenfalls denkbare, neutrale bicyclische Struktur mit N–O-Einfachbindung (Oxadiazol) liegt zumindest im Festkörper sicher nicht vor.[11] Die Diradikalform ist durch viele weitere zwitterionische Grenzformeln, wie z. B. hier in der Infobox gezeigt, stabilisiert.

Verwendung
[Bearbeiten | Quelltext bearbeiten]Die Diazoverbindung findet Verwendung als Initialsprengstoff in den USA. Sie ist kräftiger als Knallquecksilber und etwas schwächer als Bleiazid und wurde als Ersatz für die blei- und quecksilberhaltigen Initialzünder in Zündhütchen eingeführt.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f g h i j k l Köhler, J.; Meyer, R.; Homburg, A.: Explosivstoffe, zehnte, vollständig überarbeitete Auflage, Wiley-VCH, Weinheim 2008, S. 89, ISBN 978-3-527-32009-7.
- ↑ a b Registrierungsdossier zu 6-diazo-2,4-dinitrocyclohexa-2,4-dien-1-one (Abschnitt GHS) bei der Europäischen Chemikalienagentur (ECHA), abgerufen am 15. Januar 2020.
- ↑ L. V. Clark: "Diazodinitrophenol, a Detonating Explosive", in: Ind. Eng. Chem. 1933, 25 (6), S. 663–669; doi:10.1021/ie50282a021.
- ↑ Patent US2408059A: Manufacture of diazodinitrophenol. Angemeldet am 3. Juli 1940, veröffentlicht am 24. September 1946, Anmelder: Olin Industries Inc, Erfinder: Frederick M. Garfield, Herman W. Dreher.
- ↑ Matthias Ducci: Diazotypie – Bildgebung mit Diazoniumsalzen. In: Chemie in unserer Zeit. 28. Februar 2023, doi:10.1002/ciuz.202100029.
- ↑ Roth, L.; Weller, U.: Gefährliche Chemische Reaktionen, 65. Ergänzungslieferung, ecomed-Verlag 2011.
- ↑ Sprengstoffgesetz, Anhang I, Liste der explosionsgefährlichen Stoffe (BGBl. 1975 I S. 853), auf die das Gesetz in vollem Umfang anzuwenden ist.
- ↑ Matyas, R.; Selesovsky, J.; Musil; T.: Sensitivity to friction for primary explosives in J. Hazard. Mat. 213–214 (2012) 236–241, doi:10.1016/j.jhazmat.2012.01.085.
- ↑ Green, S.P.; Wheelhouse, K.M.; Payne, A.D.; Hallett, J.P.; Miller, P.W.; Bull, J.A.: Thermal Stability and Explosive Hazard Assessment of Diazo Compounds and Diazo Transfer Reagents Org. Process Res. Dev. 24 (2020) 67–84, doi:10.1021/acs.oprd.9b00422.
- ↑ Yoshida, T.; Yoshizawa, F.; Itoh, M.; Matsunaga, T.; Watanabe, M.: Prediction of Fire and Explosion Hazard for Reactive Chemicals (I): Estimation of Explosive Properties of Self-Reactive Chemicals from SC-DSC Data in Kogyo Kayaku 48 (1987) 311–316.
- ↑ Gerhard Holl, Thomas M. Klapötke, Kurt Polborn, Claudia Rienäcker: Structure and Bonding in 2‐Diazo‐4,6‐Dinitrophenol (DDNP). In: Propellants, Explosives, Pyrotechnics. Band 28, Nr. 3, 2003, S. 153–156, doi:10.1002/prep.200390022.
Literatur
[Bearbeiten | Quelltext bearbeiten]- Jared Ledgard: The Preparatory Manual of Explosives. Lulu.com, 2007, ISBN 978-0-615-14290-6, S. 141 (eingeschränkte Vorschau in der Google-Buchsuche).
- J. Köhler, Rudolf Meyer, Axel Homburg, Explosivstoffe, ISBN 978-3-527-32009-7, 10. Auflage, S. 89f.
