Métal
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | |
| 1 | H | He | ||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | ||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr |
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe |
| 6 | Cs | Ba | * | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn |
| 7 | Fr | Ra | ** | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |
| 8 | Uue | Ubn | ⁂ | |||||||||||||||
| ↓ | ||||||||||||||||||
| * | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | |||
| ** | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | |||
| ⁂ | Ubu | Ubb | Ubt | Ubq | Ubp | Ubh | Ubs | Ubo | Ube | Utn | Utu | Utb | Utt | Utq | Utp | |||
| Uth | Uts | Uto | Ute | Uqn | Uqu | Uqb | ||||||||||||
| Li | Métaux | B | Métalloïdes | |||||||||||||||
| Mt | Nature chimique inconnue | H | Non-métaux | |||||||||||||||
| Uue | Éléments hypothétiques | |||||||||||||||||
En chimie, les métaux sont des matériaux dont les atomes sont unis par des liaisons métalliques. Il s'agit de corps simples ou d'alliages le plus souvent durs, opaques, brillants, bons conducteurs de la chaleur et de l'électricité. Ils sont généralement malléables, c'est-à-dire qu'ils peuvent être martelés ou pressés pour changer leur forme sans les fissurer, ni les briser. De nombreuses substances qui ne sont pas classées comme métalliques à pression atmosphérique peuvent acquérir des propriétés métalliques lorsqu'elles sont soumises à des pressions élevées. Les métaux possèdent de nombreuses applications courantes, et leur consommation s'est très fortement accrue depuis les années 1980, au point que certains d'entre eux sont devenus des matières premières minérales critiques.
En astrophysique, et notamment en physique stellaire, on appelle métal tout élément chimique autre que l'hydrogène et l'hélium. Ces éléments sont produits par nucléosynthèse stellaire à partir d'hydrogène et d'hélium par fusion nucléaire, processus à l'origine de l'énergie libérée par les étoiles. De ce point de vue, la métallicité d'une étoile est la proportion d'éléments autres que l'hydrogène et l'hélium qui la constituent.

Liaison métallique et structures cristallines des métaux
[modifier | modifier le code]
La densité électronique par niveau d'énergie suit la statistique de Fermi-Dirac et est représentée par un dégradé de noir. Le niveau de Fermi EF des métaux et des semimétaux se trouve dans au moins l'une des bandes, tandis qu'il se trouve loin de toute bande dans les isolants, et suffisamment proche d'une bande dans les semiconducteurs pour peupler la bande de conduction ou la bande de valence d'électrons ou de trous.
Les électrons des matériaux métalliques purs ou alliés se distribuent dans des niveaux d'énergie formant un continuum entre la bande de valence, occupée par les électrons de valence, et la bande de conduction, occupée par les électrons libres injectés thermiquement depuis la bande de valence par-delà le niveau de Fermi. Ces électrons libres forment une liaison métallique délocalisée dans tout le volume du matériau. On peut se représenter un métal comme un réseau tridimensionnel de cations métalliques baignant dans un fluide d'électrons très mobiles. Le modèle de l'électron libre permet de calculer la conductivité électrique ainsi que la contribution des électrons à la capacité thermique et à la conductivité thermique des métaux, bien que ce modèle ne tienne pas compte de la structure du réseau cristallin du métal. Certains matériaux, comme les intermétalliques, présentent des liaisons partiellement métalliques et sont donc à la limite des céramiques.
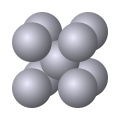
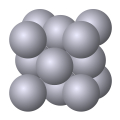
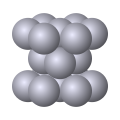
La nature électronique particulière d'une liaison métallique est responsable de plusieurs propriétés macroscopiques des métaux : le fluide d'électrons libres assure à la fois une conductivité électrique et une conductivité thermique élevées en permettant la circulation d'un courant électrique et en favorisant la propagation des phonons dans le matériau ; elle rend compte de la ductilité, de la malléabilité et de la plasticité des métaux en maintenant leur cohésion en cas de déformation brisant les autres liaisons interatomiques ; elle confère aux métaux leur absorbance et leur éclat particulier par son interaction avec les ondes électromagnétiques, ainsi que leur point de fusion et leur point d'ébullition plus élevés que les non-métaux en renforçant les autres types de liaisons interatomiques. Ces dernières, notamment les liaisons covalentes de coordination, sont responsables des différentes structures cristallines formées par les métaux solides : la plus fréquente est la structure cubique centrée, suivie de la structure hexagonale compacte et de la structure cubique à faces centrées.
Dans une structure cubique centrée, chaque atome est situé au centre d'un cube formé par ses huit atomes voisins. Dans les structures cubique à faces centrées et hexagonale compacte, chaque atome est entouré par douze autres atomes, mais l'empilement de ces atomes diffère entre ces deux structures. Certains métaux peuvent adopter des structures cristallines différentes selon la température et la pression auxquels ils sont soumis.
- Principales structures cristallines métalliques
Tous les métaux — notamment les alliages — ne sont cependant pas cristallins, et il peut se former des alliages métalliques amorphes par trempe rapide d'alliages métalliques fondus. On utilise pour ce faire des métaux fondus dont les atomes ont des tailles sensiblement différentes, ce qui limite la cristallisation lors d'un refroidissement rapide. Également appelés verres métalliques, les alliages métalliques amorphes présentent, par rapport aux métaux usuels, une meilleure ténacité, une moindre fragilité, ainsi qu'une plus grande résistance à la déformation et à la corrosion.
La force d'une liaison métallique dépend notamment du nombre d'électrons libres par atome métallique, et atteint un maximum au sein des métaux de transition vers le milieu du bloc d au niveau de la 5e période et au-delà, parmi les métaux réfractaires. Les liaisons métalliques subsistant à l'état liquide, contrairement aux autres liaisons interatomiques, le meilleur indicateur de la force de la liaison métallique d'un métal donné est sa température d'ébullition plutôt que sa température de fusion.
Éléments chimiques métalliques
[modifier | modifier le code]| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||
| 1 | H | He | |||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |
| 6 | Cs | Ba | * |
Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn |
| 7 | Fr | Ra | * * |
Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |
| ↓ | |||||||||||||||||||
* |
La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | |||||
* * |
Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | |||||
| Li | Métaux alcalins | ||||||||||||||||||
| Be | Métaux alcalino-terreux | ||||||||||||||||||
| La | Lanthanides | ||||||||||||||||||
| Ac | Actinides | ||||||||||||||||||
| Sc | Métaux de transition | ||||||||||||||||||
| Al | Métaux pauvres | ||||||||||||||||||
| B | Métalloïdes | ||||||||||||||||||
| C | Non-métaux polyatomiques | ||||||||||||||||||
| O | Non-métaux diatomiques | ||||||||||||||||||
| Ne | Non-métaux monoatomiques | ||||||||||||||||||
| Nh | Nature chimique inconnue | ||||||||||||||||||
Dans le tableau périodique des éléments, les métaux occupent la gauche, le centre et une partie de la droite du tableau, séparés des non-métaux par les métalloïdes. Parmi les 110 éléments dont les propriétés chimiques ont été un tant soit peu caractérisées, on dénombre environ 86 métaux et 7 métalloïdes. La ligne de démarcation entre métaux et non-métaux du tableau ci-contre est conventionnelle : elle est arbitraire et ne marque pas une rupture nette des propriétés macroscopiques entre éléments, dont la transition entre métaux et non-métaux est relativement continue, donnant lieu à la superposition de propriétés métalliques et non métalliques chez certains métalloïdes. De plus, un même élément peut exister selon plusieurs variétés allotropiques aux propriétés davantage métalliques pour les unes et davantage non métalliques pour les autres : un bon exemple est l'étain, qui existe d'une part sous une phase α grise de structure cubique de type diamant, stable aux basses températures, aux propriétés métalloïdes proches d'un non-métal, et, d'autre part, sous une phase β blanche de structure tétragonale, dont les propriétés sont celles d'un métal pauvre.
Les propriétés des métaux eux-mêmes ne sont pas uniformes, et l'on a coutume de les classer en familles plus ou moins informelles qui rendent compte des différences de propriétés entre ces éléments. Du point de vue chimique, le caractère métallique est d'autant plus marqué qu'on se déplace vers la gauche et vers le bas du tableau. Ainsi, les éléments les plus métalliques sont les métaux alcalins, tandis que les moins métalliques sont les non-métaux diatomiques, notamment les halogènes. Entre les deux, d'autres familles d'éléments sont traditionnellement définies, comme les métaux alcalino-terreux, les lanthanides, les actinides, les métaux de transition et les métaux dits « pauvres », ces derniers étant les métaux dont les propriétés métalliques sont les moins affirmées.
Du point de vue pratique, il existe une grande variété de termes désignant des familles d'éléments métalliques et d'alliages. On parle de métaux ferreux et non ferreux selon qu'on considère les alliages contenant ou dépourvus de ferrite, respectivement. On parle de métaux nobles pour désigner les éléments métalliques résistants à la corrosion et à l'oxydation dans l'air humide : ce sont le ruthénium, le rhodium, l'argent, l'osmium, l'iridium, le platine et l'or ; le mercure est parfois également considéré comme un métal noble, tandis que le titane, le niobium et le tantale, qui sont pourtant très résistants à la corrosion, ne sont pas considérés comme des métaux nobles. On parle de métaux précieux pour désigner les métaux les plus rares et dont la valeur marchande est la plus élevée, comme typiquement l'or, l'argent, le platine et le palladium, qui ont chacun un code monétaire ISO 4217 : XAU, XAG, XPT et XPD respectivement ; les platinoïdes sont également considérés comme des métaux précieux. On parle de métaux réfractaires pour désigner les métaux particulièrement résistants aux températures élevées et à l'usure : ce sont typiquement le niobium, le molybdène, le tantale, le tungstène et le rhénium ; le technétium est également réfractaire, mais n'est généralement pas mentionné comme tel car il est synthétique et radioactif.
Propriétés des métaux
[modifier | modifier le code]Propriétés physiques
[modifier | modifier le code]Les métaux purs ont le plus souvent une conductivité électrique, une conductivité thermique et une masse volumique élevées. L'argent est ainsi le meilleur conducteur électrique (6,30 × 107 S/m), suivi par le cuivre (5,96 × 107 S/m), l'or (4,10 × 107 S/m) et l'aluminium (3,50 × 107 S/m). La conductivité électrique du fer est de 107 S/m, tandis que celle de l'acier au carbone 1010 (fer à 0,10 % de carbone) est de seulement 5,9 × 106 S/m, ce qui illustre l'effet des impuretés sur la conductivité des métaux.
Bien que la plupart des métaux aient une masse volumique supérieure à celle de la plupart des non-métaux, celle-ci est très variable selon les matériaux considérés. Parmi les corps simples métalliques, le lithium est le moins dense (0,534 g cm−3 à 25 °C) tandis que l'osmium est le plus dense (22,59 g cm−3). Les métaux alcalins (dont fait partie le lithium) et alcalino-terreux sont les moins denses des métaux ; ils sont également les moins durs, et les métaux alcalins ont un point de fusion particulièrement bas : hormis le lithium, ils sont tous liquides à 100 °C. La densité élevée de la plupart des métaux provient de leur structure cristalline compacte.
Les métaux sont en outre généralement caractérisés par une bonne malléabilité et une grande ductilité qui leur permettent de se déformer sans se briser. Ainsi, le cuivre pur peut être étiré pour former des fils électriques, des tuyaux (plomberie), être mis en plaque et martelé en forme de casseroles ; l'or pur peut également être mis sous forme de feuilles très fines. À l'inverse, certains éléments d'alliage permettent de durcir le métal : c'est par exemple le cas du carbone qui durcit le fer pour donner de l'acier, de l'étain qui durcit le cuivre pour donner le bronze, ou encore de l'argent et du cuivre qui durcissent l'or.
La force des liaisons métalliques est la plus élevée aux environs du centre de la famille des métaux de transition, au niveau des métaux réfractaires, car ces éléments ont un grand nombre d'électrons délocalisés dans leur structure. D'autres facteurs entrent cependant également en ligne de compte, comme le rayon atomique, le numéro atomique, le nombre d'orbitales liantes, la superposition des énergies des orbitales et le type de structure cristalline ; les structures cubiques centrées donnent ainsi des liaisons métalliques moins fortes que les structures cubiques à faces centrées et hexagonales compactes car ces dernières ont une coordinence plus élevée, c'est-à-dire qu'ils lient davantage d'atomes voisins que la première.
Les métaux ont une surface généralement brillante, et sont opaques dès que leur épaisseur dépasse quelques micromètres ; les feuilles d'or transmettent néanmoins une lumière verte.
Propriétés mécaniques
[modifier | modifier le code]
La déformation élastique des métaux peut être modélisée par la loi de Hooke lorsque la déformation est une fonction linéaire de la contrainte. L'application de forces supérieures à la limite d'élasticité ou le chauffage peuvent conduire à une déformation permanente de l'objet, ce qui correspond à une déformation plastique. Cette modification irréversible de la disposition des atomes du matériau peut résulter de l'application :
- d'une force ou d'un travail en tension, en compression, en cisaillement, en flexion ou en torsion ;
- d'un chauffage, ce qui affecte la mobilité des défauts structurels du matériau, comme les joints de grains, les lacunes, les dislocations vis et coin, et les défauts d'empilement (en) des solides cristallins et non cristallins. Le mouvement de tels défauts requiert une énergie d'activation et est donc limité par la vitesse de diffusion atomique.
L'écoulement visqueux autour des joints de grains, par exemple, peut donner lieu au fluage ou la fatigue du métal. Il peut également contribuer à d'importants changements dans la microstructure, comme la croissance des grains et l'accroissement localisé de la densité du matériau par élimination de la porosité intergranulaire. De plus, la nature non directionnelle des liaisons métalliques pourrait contribuer de manière significative à la ductilité des métaux solides.
Propriétés magnétiques
[modifier | modifier le code]Quelques métaux présentent des propriétés magnétiques remarquables comme le ferromagnétisme. Ce sont notamment, à température ambiante, le fer, le cobalt et le nickel. Certaines terres rares (lanthanides dans la classification périodique) sont également ferromagnétiques à basse température. Les propriétés magnétiques varient avec les alliages, ce qui peut être mis à profit pour créer des aimants puissants ou annuler le magnétisme d'un métal comme le fer.
Propriétés des oxydes
[modifier | modifier le code]Les métaux ont tendance à former des cations en perdant des électrons. Le sodium peut ainsi perdre un électron pour former le cation Na+, le calcium deux électrons pour former le cation Ca2+, le fer deux électrons pour former le cation ferreux Fe2+ ou trois électrons pour former le cation ferrique Fe3+. Ces ions métalliques se retrouvent en solution ou dans des sels, comme le chlorure de lithium LiCl ou le sulfure d'argent Ag2S.
Les métaux réagissent avec l'oxygène de l'air pour former des oxydes de façon plus ou moins rapide : le fer forme de la rouille en plusieurs mois, voire années, tandis que le potassium brûle en quelques secondes. Les réactions suivantes sont des exemples d'oxydation de métaux :
Les métaux de transition tels que le fer, le chrome, le cobalt et le nickel s'oxydent plus lentement car leur oxydation forme une couche de passivation qui protège l'intérieur du matériau. Certains forment une couche imperméable qui bloque complètement la progression de l'oxydation et permet de conserver pendant des décennies à la fois leur éclat métallique et leurs bonnes propriétés conductrices de l'électricité : ce sont par exemple l'aluminium, le magnésium, le chrome (utilisé dans l'acier inoxydable) et le titane. Les oxydes métalliques sont généralement basiques, par opposition aux oxydes des non-métaux, qui sont plutôt acides ; les oxydes métalliques acides se rencontrent avec les états d'oxydation très élevés, comme avec le trioxyde de chrome CrO3, l'heptoxyde de dimanganèse Mn2O7 et le tétroxyde d'osmium OsO4, qui présentent des réactions strictement acides. D'autres métaux, tels que le palladium, le platine et l'or ne réagissent pas du tout à l'air libre : pour cette raison, ils sont appelés métaux nobles.
La corrosion des métaux peut être empêchée par leur peinture, leur anodisation ou encore l'apposition d'un revêtement. S'agissant d'une réaction électrochimique, il faut, pour que la protection soit efficace, utiliser un métal plus réducteur que le métal, sinon le revêtement peut favoriser la corrosion, surtout en cas de rayures.
Alliages
[modifier | modifier le code]Un alliage est un mélange de deux éléments chimiques ou davantage dont le principal constituant est un métal. La plupart des métaux purs sont trop mous, trop fragiles ou trop réactifs pour pouvoir être utilisés tels quels. Il est possible de moduler les propriétés des alliages en faisant varier les proportions relatives de leurs différents constituants. Il s'agit généralement de les rendre moins fragiles, plus durs, plus résistants à la corrosion, ou encore de leur donner une couleur et un éclat plus attrayants. De tous les alliages métalliques utilisés de nos jours, ceux du fer — acier, acier allié (en), acier à outils, acier au carbone, acier inoxydable, fonte par exemple — en représentent l'essentiel de la production, aussi bien en valeur qu'en volume. Le fer allié au carbone donne des aciers de moins en moins ductiles et résistants à mesure que le taux de carbone augmente. L'addition de silicium donne du ferrosilicium, souvent allié à la fonte, tandis que l'addition de chrome (à plus de 10 %), éventuellement de nickel et de molybdène, à des aciers au carbone donne de l'acier inoxydable.
Outre les alliages de fer, ceux de cuivre, d'aluminium, de titane et de magnésium sont également importants d'un point de vue économique. Les alliages de cuivre sont connus sous forme de bronze depuis l'âge du bronze. Le billon était un alliage utilisé jusqu'au Moyen Âge pour faire des pièces de monnaie et constitué le plus souvent essentiellement de cuivre avec un peu d'argent et parfois de mercure. De nos jours, le bronze désigne spécifiquement un alliage de cuivre et d'étain, tandis que le laiton est un alliage de cuivre et de zinc, et que le maillechort est un alliage de cuivre, de zinc et de nickel. Ces alliages ont divers usages industriels, notamment dans les installations électriques. Les alliages d'aluminium, de titane et de magnésium ont été développés plus récemment, et sont intéressants en raison de leur grande résistance mécanique pour une masse volumique plutôt faible ; leur coût de revient est cependant élevé, ce qui restreint leur utilisation aux applications de haute technologie pour lesquelles les performances sont plus importantes que le coût. Parmi les différents alliages d'aluminium, on peut citer ceux pour corroyage et pour fonderie. Le zamak est formé de zinc allié à l'aluminium, le magnésium et le cuivre.
Outre des propriétés mécaniques remarquables, les alliages permettent également de faciliter la fusion des métaux, notamment les eutectiques. C'est par exemple le cas du système aluminium-silicium, avec un hypereutectique à environ 78 % d'aluminium, 17 % de silicium, 4 % de cuivre et 1 % de magnésium, utilisé dans l'industrie automobile, et l'alliage étain-plomb Sn63Pb37 qui fond à 183 °C — à comparer aux points de fusion respectifs de l'étain et du plomb, qui sont de 232 °C et 327 °C. L'un des alliages métalliques ayant le plus bas point de fusion est le galinstan, dont la composition massique est typiquement de 68 % de gallium, 22 % d'indium et 10 % d'étain, et qui est liquide à température ambiante. C'est également le cas de l'eutectique NaK, constitué de 77 % de potassium et 23 % de sodium, mais qui est corrosif et très inflammable à l'air libre, surtout en présence d'humidité, ce qui en limite l'usage à des applications très particulières.
Les alliages spéciaux destinés à des applications de pointe, dits superalliages, comme ceux des moteurs à réaction, peuvent contenir plus d'une dizaine d'éléments différents. Les alliages à mémoire de forme sont un autre type d'applications : les alliages Fe-Mn-Si, Cu-Zn-Al et Cu-Al-Ni, par exemple, sont assez bon marché, mais il en existe une très grande variété.
Minerais
[modifier | modifier le code]Les métaux présentent le plus souvent un état d'oxydation positif, c'est-à-dire qu'ils tendent naturellement à former des cations. Il existe cependant des anions métalliques, avec un état d'oxydation négatif, par exemple avec certains complexes carbonyles comme Fe(CO)5− ou avec l'anion de sodium Na−[1].
Étymologiquement, un métal est une substance extraite d'une mine — μέταλλον en grec ancien. En pratique, les métaux sont généralement extraits sous forme de minerais contenant les éléments recherchés. Ces minerais peuvent chimiquement être de nature très diverse. Ce sont souvent des oxydes, comme la bauxite (minerai d'aluminium), l'ilménite (minerai de titane), l'hématite et la magnétite (minerais de fer), ou encore la pechblende (minerai d'uranium). Il peut également s'agir de sulfates, comme la chalcopyrite (minerai de cuivre), la sphalérite (minerai de zinc), la molybdénite (minerai de molybdène) ou encore le cinabre (minerai de mercure). Il existe par ailleurs des silicates, comme le béryl (minerai de béryllium), des carbonates comme la dolomite (minerai de magnésium), et bien d'autres types de composés.
- Quelques exemples de minerais métallifères
-
Chalcopyrite (dorée) sur sphalérite.
Une fois extraits des mines, les minerais sont traités pour isoler le métal recherché, le plus souvent par réduction chimique ou électrolytique. La pyrométallurgie utilise des températures élevées pour convertir les minerais en métaux bruts, tandis que l'hydrométallurgie passe par au moins une étape où le métal est solvaté dans l'eau. Les méthodes employées dépendent des métaux et de leurs impuretés.
Lorsque le minerai est constitué d'un composé ionique du métal avec un non-métal, le minerai doit généralement être fondu, c'est-à-dire chauffé en présence d'un réducteur pour en extraire le métal pur. De nombreux métaux communs comme le fer sont fondus en présence de carbone comme réducteur. D'autres métaux, en revanche, ne peuvent être réduits de cette façon, et sont purifiés par électrolyse : c'est le cas de l'aluminium et du sodium notamment. Les sulfures ne sont pas réduits directement, mais sont d'abord grillés à l'air libre pour être préalablement convertis en oxydes, qui sont ensuite traités de manière classique.
Certains minerais sont des éléments natifs, les plus connus étant le cuivre natif, l'argent natif, l'or natif, voire le fer météorique, mais il en existe bien d'autres, plus rares, comme le fer natif, le nickel natif (dans des roches d'origine météoritique (nickel-fer)), le cadmium natif, l'indium natif, l'étain natif, l'antimoine natif, le tellure natif, le mercure natif, le plomb natif, le bismuth, par exemple. Ces minerais sont solides, à l'exception du mercure, qui se présente à l'état liquide au-dessus de −39 °C dans des poches généralement de petite taille ne dépassant quelques kilogrammes de métal et le plus souvent associées à des métaux nobles, avec lesquels il forme des amalgames. Les platinoïdes existent également sous forme minérale plus ou moins pure, comme le ruthénium natif, le rhodium natif, le palladium natif, l'osmium natif, l'iridium natif et le platine natif.
Applications
[modifier | modifier le code]Certains métaux et alliages possèdent une résistance structurelle élevée par unité de masse, ce qui les rend utiles pour transporter des charges lourdes et résister à des chocs violents. Les alliages métalliques peuvent être conçus pour avoir une résistance élevée aux contraintes de cisaillement, de flexion et de déformation. Le même métal peut cependant être sujet à la fatigue à la suite de contraintes répétées ou d'un dépassement de la contrainte maximum. La résistance et la résilience des métaux a conduit à leur utilisation courante dans la construction des gratte-ciel et des ouvrages d'art ainsi que dans celle de tous types de véhicules, d'appareils et dispositifs, d'outils, de tuyaux, ou encore de voies ferrées.
Les deux métaux les plus utilisés, le fer et l'aluminium, sont également les plus abondants dans l'écorce terrestre. Le fer est le plus utilisé des deux : il est à la base de toutes les grandes constructions métalliques (poutre, rail, coque de navire). L'aluminium est presque toujours utilisé allié à d'autres métaux afin d'en améliorer les propriétés mécaniques, dans des applications tirant profit du fait qu'il est moins dense que le fer (2,70 g cm−3 contre 7,87 g cm−3) et meilleur conducteur électrique (3,50 × 107 S/m contre 107 S/m) ; l'aluminium est par exemple utilisé préférentiellement au cuivre dans les câbles électriques à haute tension aériens.
Le cuivre reste utilisé essentiellement pour ses bonne propriétés de conducteur de l'électricité dans les câbles électriques, et de conducteur thermique dans les ustensiles de cuisine. Les propriétés de conducteur de la chaleur font de certains métaux des matériaux intéressants pour réaliser des dissipateurs thermiques destinés à éviter les surchauffes. Les métaux les moins abondants sont utilisés dans des alliages (chrome, manganèse, titane), et les plus rares interviennent souvent comme catalyseurs (platinoïdes, notamment) et parfois comme placements financiers ou en joaillerie (métaux précieux). La réflectivité élevée de certains métaux, comme l'argent ou l'aluminium, en font des matériaux de choix pour la construction de miroirs, notamment ceux des télescopes. Elle est également à l'origine de l'attrait esthétique de certains métaux utilisés en joaillerie. L'uranium est un métal qui, après séparation isotopique, permet d'alimenter des réacteurs nucléaires pour libérer leur énergie par fission. D'autres métaux, trop réactifs à l'air et/ou à l'eau sont rarement utilisés à l'état métallique (sodium, potassium, calcium).
Dans un certain nombre de cas, les métaux tendent à être remplacés par d'autres matériaux, en général pour des raisons de légèreté (polymères, matériaux composites, céramiques) ou de résistance à la corrosion ou à l'usure (céramiques). Ces matériaux ont toutefois eux aussi leurs limites par rapport aux métaux, en particulier les polymères et composites à matrice polymère ne sont pas utilisables à hautes températures et sont souvent plus souples, tandis que les céramiques résistent mal aux chocs.
Les métaux peuvent être dopés avec des molécules étrangères, qui peuvent être organiques, minérales, biologiques, ou encore des polymères. Ces molécules confèrent au métal des propriétés nouvelles qui peuvent être mises à profit pour des applications aussi variées que les catalyseurs, la médecine, l'électrochimie et la résistance à la corrosion[2].
Spéciation chimique
[modifier | modifier le code]Les différents états d'oxydation, conformations, complexes ou formes transitoires représentent des espèces chimiques distinctes d'un élément et jouent un rôle majeur dans l'élaboration, la corrosion, ainsi que sur leur biodisponibilité et leur toxicité ou écotoxicité. Certaines espèces d'éléments-traces métalliques (ÉTM) sont plus facilement assimilables par les organismes que d'autres, ce qui engendre des effets bénéfiques ou néfastes selon la nature et la concentration du métal (élément essentiel ou non).
Il ne faut pas confondre la spéciation chimique d'un élément avec son fractionnement ou sa partition. La littérature scientifique confond quelquefois ces concepts ce qui complexifie les recherches dans ces domaines.
- spéciation chimique : c'est la distribution d'un élément selon différentes catégories d'espèces chimiques dans un système ;
- fractionnement : c'est la classification d'un élément ou d'un groupe analysé par rapport à ses propriétés physiques et/ou chimiques (grosseur de particules, solubilité, force de liaison, etc.) ;
- partition : répartition d'un composé dans les différentes phases d'un système (solide, liquide, atmosphère, matière organique, etc.) selon des coefficients de partition spécifiques[3].
Cette section décrit donc les principales catégories d'espèces chimiques relatives aux ÉTM et présente des exemples d'espèces chimiques de niveau toxique varié[4].
Oxydation et réduction
[modifier | modifier le code]Comme indiqué précédemment, les métaux se trouvent en général naturellement dans des minerais ; ils sont à l'état oxydé. Par exemple, le fer se trouve à l'état Fe(III) dans l'hématite, à l'état Fe(II) et Fe(III) dans la magnétite, l'aluminium dans l'état Al(III) dans la bauxite… La métallurgie primaire consiste essentiellement en la réduction du minerai pour obtenir un état d'oxydation (0).
À l'inverse, en réagissant avec l'environnement, le métal va s'oxyder et se dissoudre dans l'eau ou bien se lier à d'autres atomes ou ions, en particulier l'oxygène et l'ion hydroxyle. C'est un des mécanismes principaux de la corrosion.
L'état d'oxydation des métaux dans un système influence leurs effets sur les organismes. Par exemple, le chrome(III) est un élément essentiel (c'est-à-dire nécessaire pour le bon fonctionnement de l'organisme) et pénètre difficilement les membranes lipidiques des cellules. En revanche, le Cr(VI), qui s'avère toxique pour certains gènes, est cancérigène et pénètre facilement dans les cellules grâce à des transporteurs spécifiques. Dans d'autres cas, ce sont les formes moins oxydées qui sont toxiques, par exemple avec l'arsenic dont la toxicité est plus importante pour As(III) que pour As(V).
Composition isotopique
[modifier | modifier le code]La composition isotopique de quelques éléments influence leur abondance ou leur toxicité dans l'environnement. Par exemple, le plomb comporte une vingtaine d'isotopes dont quatre sont stables : 204Pb, 206Pb, 207Pb et 208Pb. Les 206Pb et 207Pb proviennent de la désintégration de l'uranium et le 208Pb résulte de la désintégration du thorium, deux éléments radioactifs ; ainsi, l'abondance de ces isotopes s’accroît dans le temps, et la composition isotopique du plomb évolue donc selon les sources d'émission stimulées. Un autre exemple intéressant de variation de la toxicité est lié à la composition isotopique de l'eau (H2O) : remplacer 60 % de l'eau du corps de rongeurs par de l'H218O est sans effet alors qu'une substitution de 30-40 % de cette eau par du D2O[5] engendre la mort de ces animaux.
On peut chercher à trier les isotopes, par exemple pour enrichir la matière en isotopes radioactifs, comme dans le cas de l'enrichissement de l'uranium pour produire du combustible nucléaire. On peut à l'inverse chercher à appauvrir le métal, comme dans le cas des munitions à uranium appauvri.
Les isotopes métalliques sont utilisés comme traceurs pour les phénomènes de diffusion : on élabore un métal contenant une quantité notable d'isotope radioactif, et le profil de radioactivité permet de suivre la progression de ces atomes.
Composés et complexes inorganiques
[modifier | modifier le code]Les métaux s'allient souvent à des ligands inorganiques[6] pour former des composés ou complexes inorganiques possédant des propriétés physico-chimiques différentes. Par exemple, la charge, la solubilité, le coefficient de diffusion ou la force de liaison de ces composés influencent le transport et par conséquent la biodisponibilité et la toxicité des métaux dans les organismes. Par exemple, certains sels de nickel comme les chlorures (NiCl2) et les sulfates (NiSO4) sont solubles dans l'eau et de faible toxicité orale, alors que les sulfures de nickel (Ni3S2) sont pratiquement insolubles dans l'eau mais sont cancérigènes.
Composés organiques
[modifier | modifier le code]Les composés organiques tel les sucres, acides organiques, lipides ou autres composés organiques de faible poids moléculaire ont des affinités plus ou moins importantes avec les métaux. Certains d'entre eux, des acides organiques comme l'acide citrique et l'acide malique, contiennent un groupement fonctionnel (l'hydroxylcarboxyle) qui se lie facilement aux métaux et qui diminuent leur biodisponibilité ; ces composés sont très étudiés en écotoxicologie terrestre car ils sont excrétés par les racines des plantes et les micro-organismes du sol, créant une synergie qui diminue la toxicité des métaux dans le sol[7].
Certains composés organiques particuliers que l'on nomme chélateurs, comme l'EDTA, forment des complexes très stables avec les métaux. Les chélateurs sont des ligands solubles polydentés faiblement acides qui forment des complexes chélateur-métal thermodynamiquement forts ; ils sont quelquefois utilisés pour la restauration des eaux et des sols contaminés aux métaux ou dans les méthodes analytiques chimiques pour extraire les métaux d'une matrice.
Composés organométalliques
[modifier | modifier le code]Les composés organométalliques contiennent une liaison entre le carbone et le métal. Cette liaison peut être de nature covalente ou ionique ; par exemple, les liaisons carbone-sodium et carbone-potassium sont fortement ioniques, les liaisons carbone-étain, carbone-plomb et carbone-mercure sont fortement covalentes et les liens carbone-lithium et carbone-magnésium se situent entre la liaison ionique et la liaison covalente[8].
Par exemple, la bioalkylation, c'est-à-dire la formation d'un alkyle (CHx) avec un métal par des micro-organismes spécifiques, est un processus fréquent dans les sols et les sédiments. Or, bien que la méthylation des métaux (lien CH3-métal) forme des composés plutôt toxiques, certains alkyles métalliques d'arsenic et de sélénium détoxifient le métabolisme de l'humain et d'autres organismes vivants. Néanmoins, la plupart des produits organométalliques résultant d'une bioalkylation sont d'origine anthropogénique, comme certains fongicides ou produits de combustion d'essence, et sont très toxiques pour le système nerveux central de certains organismes (comme les dérivés d'alkyles d'étain, de plomb ou de mercure et d'or).
Composés ou complexes macromoléculaires
[modifier | modifier le code]Les composés ou complexes macromoléculaires sont à la limite de représentation des espèces chimiques. Ils forment malgré tout une catégorie distincte car ils jouent un rôle particulièrement important dans la biodisponibilité des métaux pour les organismes vivants. En effet, les acides humiques et fulviques résultant de la biodégradation de la matière organique sont des anions mobilisant les ÉTM contenus dans les sols et dans les eaux. Les acides humiques et fulviques ont des structures et une composition très variables et complexes mais joueraient un rôle significatif sur la spéciation des métaux.
D'autres particules organiques et inorganiques tels la biomasse et les colloïdes adsorbent les métaux et diminuent ainsi leur toxicité en réduisant leur biodisponibilité. Par contre, d'autres macromolécules anioniques des organismes vivants, comme certains acides nucléiques ou les glycosaminoglycanes, se lient involontairement aux ÉTM et provoquent des mutagenèses dommageables pour l'organisme.
Paramètres influençant la spéciation des métaux
[modifier | modifier le code]La spéciation des métaux dans les phases aqueuses et solides est influencée par plusieurs paramètres (Voir aussi section Environnement de cette page) :
- le pH : en général, un pH acide tend à solubiliser les métaux alors qu'un pH alcalin favorise leur adsorption ;
- la matière organique : la matière organique adsorbe les métaux et est synonyme de stabilité (non biodisponibilité) ;
- la concentration des ligands : plus la concentrations des ligants inorganiques et organiques est élevée, plus le métal se lie à ce ligand et forme une espèce chimique populeuse ;
- la force du lien ionique ou covalent : plus le lien métal-composé est fort, plus l'espèce chimique associée à ce composé sera stable ;
- la stœchiométrie : les principes stœchiométriques doivent évidemment être respectés pour engendrer la formation des composés.
Cette spéciation implique que l'équilibre chimique est atteint. Or, la complexation des métaux avec les ligands inorganiques est très rapide car ils sont nombreux dans la phase aqueuse, mais la complexation des métaux avec les ligands organiques nécessite plus de temps car les sites d'adsorption ou d'attachement sont moins accessibles. Par conséquent, il est préférable d'analyser la spéciation d'une contamination métallique sur une matrice contaminée stable depuis plusieurs années qu'une matrice fraîchement contaminée avec une dynamique chimique évolutive, sans quoi les analyses risquent d'être biaisées.
De plus, la constante d'équilibre relative à la notion d'équilibre chimique peut être illustrée par la réaction :
Métaln+ + Ligandn− → Métal-Ligand
La constante d'équilibre Kéq associée à cette équation varie selon le type de lien :
- Lien ionique : ~ 100 < Kéq < 104
- Complexe : ~ 104 < Kéq < 108
- Chélateur : ~ 108 < Kéq < 1020
Ainsi, puisque Kéq est relativement faible pour les paires ioniques et plus élevée pour les complexes, les métaux préfèrent s'associer à long terme aux complexes stables qu'aux paires ioniques de plus faible énergie de liaison.
Économie et géopolitique
[modifier | modifier le code]Raréfaction des ressources
[modifier | modifier le code]
Le développement de nombreuses industries telles que l'électronique, les technologies de l'information et de la communication, et l'aéronautique, et le pari du « tout technologique » dans la recherche du rendement et de l'efficacité, ont conduit à une augmentation sans précédent de la production et de la consommation de métaux. La période de croissance de 1990 à 2010 a conduit à un doublement de la production des principaux métaux. Alors que dans les années 1970, on utilisait moins de 20 métaux dans la table de Mendeleïev, on en consomme environ 60 depuis les années 2000[10].
Il y a une tendance à la baisse de concentration moyenne des minerais. Par exemple, la concentration moyenne des minerais de cuivre exploités est passée de 1,8 % dans les années 1930 à 0,8 % en 2010[11]. Parallèlement, les réserves, exprimées au niveau de production 2008, se situent pour la plupart des métaux entre 20 et 100 ans de production annuelle[12].
Géopolitique
[modifier | modifier le code]Depuis très longtemps les mines de certains métaux (précieux ou communs mais indispensables à l'industrie), les installations de raffinage, voire certains secrets de fabrication étaient considérés comme d'intérêt stratégique par les États. Les raisons militaires et l'avènement des armes et munitions métalliques puis de l'énergie et de l'arme nucléaire ont accru l'importance de certains métaux. Même pour des métaux géologiquement non rares comme le cuivre, mais faisant l'objet d'un marché fluctuant, de fortes hausses de cuivre se traduisent aussi par l'accroissement de vols de métaux (à titre d'exemple, en France, en 2010, RFF et la SNCF ont subi 2 100 vols de cuivre (quatre fois plus qu'en 2009), qui ont causé des dysfonctionnements et plusieurs dizaines de millions d'euros de préjudice par an pour la seconde[13].
La consommation de certains métaux autrefois sans valeur s'est fortement accrue au XXe siècle, avec par exemple l'uranium (fortement demandé pour des usages militaires et civils), les métaux du groupe du platine (principalement utilisés pour les pots d'échappement catalytiques, comme catalyseur industriel ou pour les chimiothérapies anticancéreuses) la surexploitation des ressources minières les plus accessibles ou les plus « pures » et malgré les économies permises par un recyclage d'une partie des métaux constituant les produits en fin de vie ou les chutes de production, la notion de métaux stratégiques est encore prégnante. Ainsi, la France a créé[14][réf. incomplète] en 2011 un « Comité pour les métaux stratégiques », chargé d'aider le ministère à élaborer et mettre en œuvre une politique rénovée de gestion de ces métaux, via notamment des approvisionnements mieux sécurisés. Le ministre chargé des matières premières en préside les trois collèges (administrations, organismes techniques et fédérations professionnelles et industriels). La FEDEREC (fédération des entreprises du recyclage) et la FEDEM (fédération des minerais, minéraux industriels et métaux non ferreux) y participent.
Environnement
[modifier | modifier le code]Contrairement aux composés organiques, les métaux ne sont pas biodégradables par les micro-organismes. Cette caractéristique engendre certains problèmes de gestion de la contamination métallique. En effet, le sort des métaux dans l’environnement pose de grands défis analytiques ; les métaux se retrouvent sous plusieurs formes dans le sol et dans l'eau (complexe avec la matière organique du sol, avec les minéraux, précipitation, ions libres, etc.) complexifiant les prédictions de toxicité et d'écotoxicité[15],[16].
Toxicité et écotoxicité terrestre
[modifier | modifier le code]La toxicité et l'écotoxicité des métaux dans les sols sont étroitement liées à leurs caractéristiques propres (radioactivité éventuelle et type de radioactivité, métal lourd, toxicité chimique, micro ou nanoparticules, etc.), spéciation chimique et biodisponibilité ; plus l'espèce métallique est libre et mobile, plus elle est biodisponible et plus il y a un risque de toxicité sur les organismes vivants. En général, les ions métalliques libres (en solution) constituent la forme chimique la plus disponible pour les organismes et donc la plus susceptible d'être toxique. Cependant, d'autres espèces ou fractions de métaux peuvent être instables et mobiles (fraction labile ou liée aux oxydes libres par exemple) et engendrer un risque pour les organismes.
Certains métaux (fer, cuivre et zinc notamment) sont des éléments essentiels. Ils sont toxiques au-delà d'une certaine dose, mais une carence entraîne des troubles métaboliques graves.
Ainsi, plusieurs paramètres influencent la toxicité des métaux dans les sols[17],[18] :
- le pH : généralement, un pH acide solubilise les métaux normalement immobiles et augmente donc le risque de toxicité ;
- la composition du sol : les argiles et la matière organique du sol adsorbent les contaminants et les séquestrent sous forme de complexes stables faiblement mobiles, alors que les particules plus grosses comme le sable ou le gravier retiennent moins les métaux du sol ;
- le temps passé après une contamination aiguë, ou le temps durant lequel une contamination chronique a eu lieu : un site fraîchement contaminé ne présente pas nécessairement plus de toxicité qu'un site ayant subi une contamination diffuse mais étalée sur plusieurs années ou décennies ;
- le niveau de saturation des sites d'adsorption : plus les sites sont capables de fixer, les métaux approchent leur niveau de saturation, plus le métal aura tendance à se solubiliser ou se rendre biodisponible.
Empreinte énergétique
[modifier | modifier le code]Pour aller de la mine à un objet façonné, il faut passer par de nombreuses étapes et utiliser beaucoup d'équipements qui consomment de l'énergie. Les métaux étant pratiquement tous sous forme d'oxydes ou de sulfures dans la nature, il faut, pour les obtenir sous forme métallique, fournir l'énergie nécessaire à casser les liaisons chimiques correspondantes.
L'empreinte énergétique d'un métal est la quantité d'énergie nécessaire pour obtenir du métal pur. Dans ce qui suit, la quantité d'énergie est mesurée en tep (tonne équivalent pétrole), pour une tonne de métal pur.
Pour obtenir l'énergie « contenue » dans un métal « neuf », issu de la première transformation du minerai, il faut prendre en compte :
- l'énergie d'extraction du minerai ;
- l'énergie des traitements pré-métallurgiques (minéralurgie) ;
- l'énergie de la métallurgie d'élaboration ;
- l'énergie de la première transformation (fonte et affinage) ;
- l'énergie du transport éventuel entre les différentes étapes[19].
- Énergie des métaux donnée par différentes sources
(en tep — tonne d'équivalent pétrole — par tonne de métal brut)
| Métal | Norgate et Rankine (2002) |
J.C. Prevot (*) (2005) |
ADEME (**) (2006) |
BRGM (2007) |
R.U. Ayres (*) (2002) |
|---|---|---|---|---|---|
| Titane | 10,5-13,6 | 9,9 | |||
| Magnésium | 10,0-10,2 | 8,6 | |||
| Aluminium | 5,0 | 6,4-7,4 | 3,8 | 5,8 | 2,5 (***) |
| Étain | 4,6 | ||||
| Nickel | 2,7-4,6 | 3,3 | |||
| Cuivre | 0,8-1,5 | 2,4-3,6 | 1,0 | 1,9 | 1,1-1,5 (***) |
| Zinc | 0,9-1,1 | 1,7-1,9 | 1,0 | 1,6 | 1,5 (***) |
| Acier | 0,5 | 0,8-1,4 | 0,4 | 0,8 | |
| Plomb | 0,5-0,8 | 0,8-1,1 | 0,8 | 0,5 | 0,7 (***) |
(*) Source en MJ / kg et 1 MJ = 2,38 × 10−5 tep.
(**) Source en tec (tonne équivalent carbone) ; conversion utilisée : 1 tec = 1,3 tep (valeur moyenne européenne).
(***) Énergie injectée dans les procédés uniquement : hors énergie d'extraction, des intrants (acides, solvants, etc.), de transport.
La consommation énergétique totale pour la production de métaux bruts est alors de 730 à 1 070 Mtep, soit 7 à 10 % de l'énergie primaire mondiale. L'acier et l'aluminium en représentent la plus grande part, soit respectivement 544-680 Mtep et 147-288 Mtep[20].
- Impact du recyclage
Les grands métaux sont globalement recyclables, et l'énergie nécessaire au recyclage est bien moindre que l'énergie nécessaire à la fabrication du métal neuf. Par exemple, pour l'acier, l'énergie nécessaire au recyclage représente 25 à 40 % de l'énergie nécessaire à la production du métal primaire. Le recyclage de l'aluminium ne nécessite quant à lui que 4 à 5 % de l'énergie requise pour la production de l'aluminium primaire[21].
Astronomie
[modifier | modifier le code]Planétologie
[modifier | modifier le code]En planétologie, les métaux sont les matériaux les plus denses, comme le fer ou le nickel, qui composent le cœur des planètes rocheuses. Ils constituent la catégorie des matériaux les plus « lourds » à côté des « gaz » (hydrogène, hélium), des « glaces » (composés contenant du carbone, de l'azote et/ou de l'oxygène, comme l'eau, le méthane et l'ammoniac) et des « roches » (silicates).
Cosmologie
[modifier | modifier le code]En astrophysique, notamment en physique stellaire et en cosmologie, on appelle « métal » tout élément chimique autre que l'hydrogène et l'hélium. Ces éléments sont produits par nucléosynthèse stellaire à partir d'hydrogène et d'hélium, c'est-à- dire par fusion nucléaire, processus à l'origine de l'énergie libérée par les étoiles. De ce point de vue, la métallicité d'une étoile est la proportion d'éléments autres que l'hydrogène et l'hélium qui la constituent.Elle est notée Z (X et Y représentant respectivement la proportion d'hydrogène et d'hélium).
Notes et références
[modifier | modifier le code]- (en) James L. Dye, « Alkali metal anions. An unusual oxidation state », J. Chem. Educ., vol. 54, no 6, , p. 332
- (en) David Avnir, « Molecularly Doped Metals », Accounts of Chemical Research, vol. 47, no 2, , p. 579-592 (PMID 24283194, DOI 10.1021/ar4001982, lire en ligne)
- C.H. Walker, S.P. Hopkin et al., Principles of Ecotoxicology, Boca Raton: CRC PRESS, Taylor and Francis Group, , 315 p.
- D.M. Templeton, F. Ariese et al., « Guidelines for Terms related to Chemical Speciation and Fractionation of Elements. Definitions, Structural Aspects, and Methodological Approaches », Pure Applied Chemistry, vol. 72, no 8, , p. 1453-1470
- Le deutérium est un isotope de l'hydrogène
- Sans atome de carbone
- S. Sauvé et D.R. Parker, « 14: Chemical Speciation of Trace Elements in Soil Solution », dans Chemical Process in Soils, vol. 8, Madison, Soil Science Society of America, , p. 655-688
- G. Solomons et C. Fryhle, Chimie organique [« Organic Chemistry (John Wiley & Sons, Inc.) »], Mont-Royal, Modulo Éditeur, , p. 483-484
- Données issues de CES Selector version 4.7.0, par Granta Design.
- BG 2010, p. 24-25
- BG 2010, p. 29
- BG 2010, p. 39
- « Vols de cuivre », sur Environnement-online,
- Décret annoncé par le ministre chargé de l'Énergie le 26 janvier 2011.
- Y. Ge, P. Murray et W.H. Hendershot, « Trace Metal Speciation and Bioavailability in Urban Soils », Environmental Pollution, vol. 107, no 1, , p. 137-144
- B. Cances, M. Ponthieu et al., « Metal Ions Speciation in a Soil and its Solution : Experimental Data and Model Results », Geoderma, vol. 113, nos 3-4, , p. 341-355
- R. Naidu, V.V.S.R. Gupta et al., Bioavailability, Toxicity and Risk Relationships in Ecosystems, Endfield: Science Publishers, Inc., , p. 58-82.
- L. L'Herroux, S. Le Roux et al., « Behavior of Metals following Intensive Pig Slurry Applications to a Natural Field Treatment Process in Brittany », Environmental Pollution, vol. 97, nos 1-2, , p. 119-130.
- BG 2010, p. 81-83.
- BG 2010, p. 84-87
- BG 2010, p. 88-89
Voir aussi
[modifier | modifier le code]Bibliographie
[modifier | modifier le code]![]() : document utilisé comme source pour la rédaction de cet article.
: document utilisé comme source pour la rédaction de cet article.
 Philippe Bihouix et Benoît De Guillebon, Quel futur pour les métaux ? : Raréfaction des ressources : un nouveau défi pour la société, EDP Sciences,
Philippe Bihouix et Benoît De Guillebon, Quel futur pour les métaux ? : Raréfaction des ressources : un nouveau défi pour la société, EDP Sciences, - Claude Birraux et Christian Kert, députés, Rapport sur les enjeux des métaux stratégiques : le cas des terres rares, Compte rendu de l'audition publique du et de la présentation des conclusions, le .
- Christophe Bouillon et M. Michel Havard, Rapport d’information sur la gestion durable des matières premières minérales, Assemblée Nationale, , 146 p.
- Pierre-Noël Giraud et Thimothée Ollivier, Économie des matières premières, La découverte, 2015
- Michel Jebrak, Quels métaux pour demain, Dunod, 2015
- Bernadette Mérenne-Schoumaker et Claire Levasseur, Atlas mondial des matières premières : des besoins croissants, des ressources limitées, Autrement, 2015
- Philippe Chalmin, Cyclope : Les marchés mondiaux 2017, Economica, 2017 (édition annuelle)
- Guillaume Pitron, La guerre des métaux rares : La face cachée de la transition énergétique et numérique, Les liens qui libèrent,
Articles connexes
[modifier | modifier le code]Liens externes
[modifier | modifier le code]
- Ressource relative aux beaux-arts :
- Notices dans des dictionnaires ou encyclopédies généralistes :
- [PDF] Rapport de la Commission européenne au Parlement européen, au Conseil, au Comité économique et social européen et au Comité des régions, sur la mise en œuvre de l’initiative « Matières premières »
- (fr) Minéralinfo, le portail français des matières premières minérales primaires et secondaires non énergétiques
- (fr) Base de données de la Société française de chimie (SFC)
- (fr) ADEME, Étude du potentiel de recyclage de certains métaux rares
- (fr) Animation, applications et recherches liées au point de vue quantique sur les métaux (Université Paris Sud)
- (fr) Les métaux dans la vie quotidienne (Université de Lorraine)
- (en) UNEP (2011) Recycling Rates of Metals - A Status Report, A Report of the Working Group on the Global Metal Flows to the International Resource Panel, Graedel, T.E. ; Allwood, J. ; Birat, J.-P. ; Reck, B.K. ; Sibley, S.F. ; Sonnemann, G. ; Buchert, M. ; Hagelüken, C.